BIOSINTESI DI AMMINOACIDI E NUCLEOTIDI
|
|
|
- Pietro Fedele
- 5 anni fa
- Visualizzazioni
Transcript
1 BIOSINTESI DI AMMINOACIDI E NUCLEOTIDI La biosintesi degli amminoacidi ha molto in comune con quella dei nucleotidi, perché entrambe le classi di composti contengono azoto, ma anche perché le due vie di biosintesi sono strettamente interconnesse e hanno molti intermedi in comune. Infatti, alcuni amminoacidi vengono incorporati nelle strutture puriniche e pirimidiniche. METABOLISMO DELL AZOTO L azoto è l elemento più abbondante dell atmosfera terrestre e gli unici organismi a poterlo fissare sono le piante e i batteri, quindi non l uomo. Ciclo dell azoto I processi metabolici di organismi diversi agiscono in modo indipendente per recuperare e riutilizzare l azoto disponibile per i processi biologici, creando il ciclo dell azoto. Il ciclo dell azoto si suddivide in tre tappe: 1) Fissazione: fase in cui i batteri fissano l azoto per formare ammoniaca, la quale potrebbe essere utilizzata da moltissimi organismi, ma viene ulteriormente modificata dagli stessi batteri. 2) Nitrificazione: fase in cui i batteri ossidano l ammoniaca prima a nitrito e successivamente a nitrato. Il nitrato formatosi può essere utilizzato dalle piante e da batteri grazie all azione della nitrato reduttasi. In questo modo, l ammoniaca formatasi può essere inserita nella molecola degli amminoacidi nelle piante. 3) Denitrificazione: fase in cui un batterio o una pianta muoiono, le proteine si degradano, viene liberata ammoniaca, che si trasforma in nitriti e nitrati. Glutammato e glutammina L azoto ridotto è assimilato e incorporato sotto forma di ione ammonio, dapprima nelle molecole di amminoacidi, e in seguito in altri composti azotati (es. basi azotate). Il punto di ingresso dell azoto in questo processo è rappresentato da due amminoacidi: il glutammato e la glutammina. I gruppi amminici della maggior parte degli amminoacidi derivano dal glutammato attraverso reazioni di transaminazione. Le vie biosintetiche che producono glutammato e glutammina sono simili in tutti gli organismi viventi. La via principale per il legame dell ammoniaca al glutammato richiede due reazioni e la prima reazione è catalizzata dalla glutammina sintetasi, la quale fa reagire lo ione ammonio con il glutammato, generando glutammina. Regolazione del metabolismo dell azoto L attività della glutammina sintetasi è altamente regolata in tutti gli organismi ed è regolata allostericamente e covalentemente. Gli inibitori sono otto (es. AMP, CTP, alanina, carbamil fosfato), ma ogni inibitore promuove solo un inibizione parziale e non completa dell enzima. Per avere un inibizione completa dell enzima c è bisogno che ci sia una combinazione di inibitori. BIOSINTESI DEGLI AMMINOACIDI Tutti gli amminoacidi derivano da intermedi della glicolisi, del ciclo dell acido citrico o della via del pentosio fosfato. L azoto entra nelle vie di biosintesi degli amminoacidi come glutammato o glutammina. Esistono due classi di amminoacidi:
2 - Amminoacidi essenziali: devono essere necessariamente introdotti con la dieta, perché l organismo non è in grado di sintetizzarli da zero. - Amminoacidi non essenziali: possono essere assunti con la dieta oppure possono essere sintetizzati dall organismo. Gli amminoacidi si possono raggruppare in sei famiglie, ognuna delle quali è in grado di produrre un certo tipo di amminoacidi: - α-chetoglutarato (intermedio del ciclo dell acido citrico) Glutammato Glutammina Prolina Arginina - Ossalacetato (intermedio del ciclo dell acido citrico e della gluconeogenesi) Aspartato Aspargina Metionina Treonina Lisina - Piruvato (intermedio della glicolisi e della gluconeogenesi) Alanina Valina Leucina Isoleucina - 3-fosfoglicerato (intermedio della glicolisi e della gluconeogenesi) Serina Glicina Cisteina - Fosfoenolpiruvato ed eritrosio 4-fosfato (PEP: intermedio della glicolisi e della gluconeogenesi; E-4-P: intermedio della via del pentosio fosfato, che si origina dal 3-fosfoglicerato) Triptofano Fenilalanina Tirosina - Ribosio 5-fosfato (intermedio della via del pentosio fosfato) Istidina METABOLISMO DEI NUCLEOTIDI Il meccanismo di sintesi delle basi puriniche è un esempio di collaborazione tra vari enzimi, senza che essi si trovino all interno di un complesso. Infatti la sintesi di basi puriniche è resa possibile tramite l intervento successivo di una serie di meccanismi differenti tra loro, ma fortemente correlati. In questi casi, il primo meccanismo trasforma il primo substrato della reazione in modo tale da renderlo adatto per essere attaccato dal secondo meccanismo, il quale trasforma il substrato precedentemente trasformato in modo tale da renderlo adatto per essere attaccato dal terzo meccanismo e così via. I nucleotidi hanno diverse funzioni nella cellula. Essi sono, per prima cosa, i precursori del DNA e dell RNA. In secondo luogo, l ATP e il GTP sono trasportatori essenziali dell energia chimica. Infine, i nucleotidi sono componenti di cofattori come il NAD, il FAD e il CoA, e di alcuni intermedi biosintetidi attivati come l UDP e il CDP. Altri sono anche secondi messaggeri cellulare (es. cacp e cgmp). I nucleotidi sono costituiti, fondamentalmente, fosfato, zucchero pentoso e base (purinica o pirimidinica). Esistono due meccanismi per la sintesi delle basi: - Basi puriniche: meccanismo raffinato.
3 - Basi pirimidiniche: meccanismo semplice. Le vie di sintesi delle purine e delle pirimidine hanno in comune diversi precursori importanti. Il fosforibosil pirofosfato (PRPP) partecipa a entrambe le vie, e in questo caso la struttura del ribosio compare per intero nel prodotto finale. Un amminoacido è un precursore importante in ciascuna via: la glicina nel caso delle purine e l aspartato nel caso delle pirimidine. La glutammina è sempre la principale fonte di gruppi amminici e viene utilizzata in cinque tappe delle vie biosintetiche. L aspartato ha anche una seconda funzione nella sintesi delle purine, quella di donatore del gruppo amminico. Biosintesi e regolazione della biosintesi delle basi puriniche I due nucleotidi purinici presenti negli acidi nucleici sono l AMP e il GMP. Questi nucleotidi contengono rispettivamente le basi puriniche adenina e guanina. Questa serie di reazione è lineare fino alla formazione dell inosinato, ma si biforca immediatamente dopo per dare origine al GMP o all AMP. 1) Il gruppo amminico di una glutammina si lega al C-1 del PRPP, liberando glutammato e un pirofosfato. 2) Un intera molecola di glicina si lega col carbossile al gruppo amminico aggiunto dalla glutammina in precedenza, mediante l utilizzo di ATP, liberando ADP + P. 3) Il gruppo formilico del formiltetraidrofolato viene legato al gruppo amminico della glicina aggiunta in precedenza, liberando tetraidrofolato. 4) Il gruppo amminico di una glutammina si lega al carbossile della glicina aggiunta in precedenza, mediante l utilizzo di ATP, liberando glutammato, ADP + P. Questo passaggio descrive il fatto che, prima di chiudere l anello a 5, comincia la formazione dell anello a 6. 5) Una molecola di ATP fa in modo che si chiuda l anello a 5 tra il formile, aggiunto dal formiltetraidrofolato, e il primo gruppo amminico, aggiunto dalla glutammina, liberando acqua, ADP +P. 6) Una molecola di bicarbonato si lega al secondo gruppo amminico aggiunto dalla glutammina e legato al carbossile della glicina, mediante l utilizzo di ATP, liberando ADP + P. 7) Il bicarbonato, legato in precedenza al gruppo amminico, si sposta, legandosi al carbonio legato al carbossile della glicina. 8) Un intera molecola di aspartato si lega al carbonio del bicarbonato con il gruppo amminico, mediante l utilizzo di ATP, liberando ADP + P. 9) Si libera fumarato dall aspartato aggiunto in precedenza, lasciando legato al carbonio del bicarbonato solo il gruppo amminico. 10) Il gruppo formilico del formiltetraidrofolato viene legato al secondo gruppo amminici aggiunto in precedenza dalla glutammina, liberando tetraidrofolato. 11) Una molecola d acqua fa in modo che si chiuda l anello a 6 tra il formile, aggiunto dal formiltetraidrofolato, e il gruppo amminico, aggiunto dall aspartato. Si ha la formazione dell inosinato (IMP), un nucleotide precursore dell AMP e del GMP. La conversione dell IMP in AMP richiede l inserimento nella molecola di un gruppo amminico fornito dall aspartato, come avviene per la formazione dell anello a 6, con una successiva liberazione di una molecola di fumarato; la conversione dell IMP in GMP richiede comunque due reazioni: la prima reazione consiste nell utilizzo di acqua e NAD + per ossidare il C-2, mentre la seconda reazione consiste nell utilizzo di ATP e di glutammina, la quale lega un gruppo amminico lì dove era stato ossidato il C-2. Dei meccanismi di controllo retroattivi cooperano per regolare la velocità complessiva della sintesi dei nucleotidi purinici e le velocità di formazione dei due prodotti finali (AMP e GMP). Un primo meccanismo viene esercitato sulla prima reazione, che è peculiare della sintesi delle purine, cioè il trasferimento di un gruppo amminico al PRPP. Questa reazione è catalizzata da un enzima che è inibito allostericamente da IMP, AMP e GMP. Di conseguenza, se questi tre prodotti vengono ad accumularsi, la sintesi di questi prodotti viene parzialmente inibita, non completamente (non
4 succederà mai che sia completamente inibito). Un secondo meccanismo viene esercitato da un eccesso di GMP, che inibisce l enzima che porta alla formazione dell intermedio che porterà alla formazione di GMP, senza alterare la velocità della produzione di AMP (viene inibita la produzione di GMP, ma viene comunque consentita la produzione di AMP); viceversa, un eccesso di AMP inibisce l enzima che porta alla formazione dell intermedio che porterà alla formazione di AMP, senza alterare la velocità della produzione di GMP (viene inibita la produzione di AMP, ma viene comunque consentita la produzione di GMP). Per la formazione di AMP viene utilizzato GTP, mentre per la formazione di GMP viene utilizzato ATP: un controllo reciproco che tende a bilanciare la sintesi dei due ribonucleotidi. Biosintesi e regolazione della biosintesi delle basi pirimdiniche I ribonucleotidi pirimidinici comuni sono la CMP e l UMP, che contengono rispettivamente le basi pirimidiniche citosina e uracile. La biosintesi dei nucleotidi pirimidinici procede in maniera diversa rispetto a quella dei nucleotidi purinici; in questo caso viene costruito prima l anello pirimidinico a 6, che viene poi legato al ribosio 5-fosfato. Questo processo inizia dal carbamil fosfato, composto che partecipa anche alla sintesi dell urea. Negli animali il carbamil fosfato necessario alla sintesi dell urea viene prodotto nei mitocondri da un enzima mitocondriale, la carbamil fosfato sintetasi I, mentre il carbamil fosfato che entra nella sintesi dei nucleotidi pirimidinici è formato nel citosol da un altro enzima, la carbamil fosfato sintetasi II. Questa serie di reazioni è sempre lineare. 1) Il carbamil fosfato reagisce con l aspartato, originando carbamilaspartato. 2) Viene eliminata una molecola d acqua e l anello si chiude, originando diidrorotato. 3) NAD + viene ridotto a NADH, originando orotato. 4) Una molecola di PRPP si lega a un gruppo amminico dell orotato, originando orotidilato. 5) Avviene una decarbossilazione, originando UMP. 6) L intervento di 2ATP trasforma l UMP, originando UTP, liberando 2ADP. 7) La glutammina e l ATP trasformano l UTP, originando CTP. La regolazione della velocità di sintesi dei nucleotidi piriminici è in gran parte dovuta alla modulzione dell aspartato transcarbamilasi, cioè il primo enzima che agisce nel processo, quello che fa reagire l aspartato con il carbamil fosfato. Questo enzima è inibito da un alta concentrazione di CTP, il prodotto finale della sequenza di reazioni. Ribonucleotide reduttasi I desossiribonucleotidi, le unità costitutive del DNA, derivano dai corrispondenti ribonucleotidi per diretta riduzione del C-2 del ribosio, che forma un desossiderivato. La reazione è catalizzata dalla ribonucleotide reduttasi, un enzima che ha come substrati i ribonucleosidi difosfato e l unico enzima ad avere una multispecificità. L enzima esiste in due forme, in base a un particolarità del substrato: - SH liberi di due cisteine del substrato - SH occupati da un ponte disofluro di due cisteine del substrato L enzima forma un ponte disolfuro e i due SH sono utilizzati per catturare l ossigeno legato al C-2 del ribosio per produrre acqua. Il problema è rappresentato dal fatto che poi è necessario riportare l enzima nella forma attiva, cioè con i due SH liberi. La riduzione del ribonucleotide reduttasi può avvenire in due modi: 1) Meccanismo con tioredossina: due protoni vengono trasferiti dal NADPH + H + al FAD, formando NADP + e FADH 2. I due protoni del FADH 2 vengono trasferiti alla tioredissina ossidata (con ponte disolfuro), che diventa ridotta (con due SH liberi). I due protoni della tioredossina ridotta sono trasferiti alla ribonucleotide reduttasi ossidata (con ponte disolfuro), che diventa ridotta (con due SH liberi). Il substrato finale per i protoni è il nucleotide difosfato (NDP); NMP e NTP non funzionerebbero come substrato.
5 2) Meccanismo con glutaredossina (alcuni organismi non possiedono tioredossina): due protoni vengono trasferiti dal NADPH + H + a due molecole di glutatione ossidato (con ponte disolfuro; due molecole perché nel sito attivo hanno un solo SH e per formare un ponte S-S hanno bisogno di due molecole), formando NADP + e due molecole di glutatione ridotto (con due SH liberi). I due protoni delle due molecole di glutatione ridotto vengono trasferiti alla glutredossina ossidata (con ponte disolfuro), che diventa ridotta (con due SH liberi). I due protoni della glutaredossina ridotta sono trasferiti alla ribonucleotide reduttasi ossidata (con ponte disolfuro), che diventa ridotta (con due SH liberi). Il substrato finale per i protoni è il nucleotide difosfato (NDP); NMP e NTP non funzionerebbero come substrato. La ribonucleotide reduttasi è composta da un dimero R1-R2, in cui ciascun monomero è costituito da due unità: 2 subunità R1, uguali tra loro, e 2 subunità R2, uguali tra loro. La regolazione della ribonuceotide reduttasi è peculiare, perché i suoi effettori regolano non solo l attività, ma anche la specificità di substrato dell enzima. Questo problema è risolto facendo variare, a seconda della condizione in cui si trova la cellula, la specificità dell enzima: se servono molti desossiribonucleotidi (es. sintesi del DNA), allora in questo caso l enzima funzionerà privilegiando come substrati ribonucleotidi; se invece è necessario utilizzare i ribonucleotidi, questa attivazione verso la sintesi di desossiribonucleotidi diminuirà. Ciascuna subunità R1 possiede due tipi di diti regolatori: un sito regola l attività enzimatica complessiva e lega sia l ATP, che attiva l enzima, sia il datp, che lo inattiva; un altro sito modifica la specificità di substrato in risposta all effettore (ATP, datp, dttp o dgtp), che si lega. Quando si legano l ATP o il datp, viene stimolata la riduzione dell UDP e del CDP; quando si legano il dttp o il dgtp, viene stimolata la riduzione del GDP o dell ADP. Questo tipo di regolazione mantiene ben bilanciato il pool di precursori della sintesi del DNA (concentrazione di ribonucleotidi e desossiribonucleotidi deve essere mantenuto bilanciato e costante). Nel DNA non è presente UMP (con uracile), ma dtmp (con timina). Per passare da UMP a dtmp si effettua una metilazione, cioè si lega un metile alla base pirimidinica, tramite l enzima timidilato sintetasi. Patologie - Gotta: è una malattia che colpisce le giunture ed è causata da un elevata concentrazione di acido urico nel sangue e nei tessuti. Viene trattata con un farmaco chiamato allopurinolo (forma enolica: ipoxantina), che rallenta la produzione di acido urico. - Cancro: le cellule cancerose crescono più rapidamente rispetto alle cellule dei tessuti normali e di conseguenza le loro richieste di nucleotidi, come precursori per la sintesi di DNA e di RNA, sono notevolmente superiori. Le cellule cancerose sono in genere più sensibili agli inibitori della biosintesi dei nucleotidi rispetto alle cellule normali. Sono ora noti molti agenti chemioterapici per il cancro e per altre malattie, capaci di inibire uno o più enzimi di queste vie. Questi farmaci hanno l effetto collaterale di colpire, anche se in percentuale minore, le cellule sane, dato che anche queste, seppur avendo una velocità di crescita minore, necessitano gli enzimi per produrre DNA e RNA.
METABOLISMO DEI NUCLEOTIDI
 METABOLISMO DEI NUCLEOTIDI SOSTANZE UBIQUITARIE COSTITUISCONO UNITA MONOMERICHE ACIDI NUCLEICI NUCLEOSIDI TRIFOSFATI (ATP) SONO PRODOTTI TERMINALI RICCHI DI ENERGIA MAGGIOR PARTE DELLE VIE METABOLICHE
METABOLISMO DEI NUCLEOTIDI SOSTANZE UBIQUITARIE COSTITUISCONO UNITA MONOMERICHE ACIDI NUCLEICI NUCLEOSIDI TRIFOSFATI (ATP) SONO PRODOTTI TERMINALI RICCHI DI ENERGIA MAGGIOR PARTE DELLE VIE METABOLICHE
Biosintesi degli aminoacidi
 Biosintesi degli aminoacidi Per l uomo la fonte principale di gruppi NH 4 + sono gli AA contenuti nelle proteine della dieta Parte di NH 4 + che si genera dalla degradazione degli AA viene riciclata e
Biosintesi degli aminoacidi Per l uomo la fonte principale di gruppi NH 4 + sono gli AA contenuti nelle proteine della dieta Parte di NH 4 + che si genera dalla degradazione degli AA viene riciclata e
Nucleotidi 24/10/2012. Studenti: Biotec _ Nucleotidi (1) Ribosio Vs. Desossirbosio
 I Nucleotidi Hanno Tre Componenti Nucleotidi Studenti: Biotec _ 2012 Nucleotidi (1) Ribosio Vs. Desossirbosio Un Nucleotide è una molecola costituita da un composto ad anello contenente azoto (N) legato
I Nucleotidi Hanno Tre Componenti Nucleotidi Studenti: Biotec _ 2012 Nucleotidi (1) Ribosio Vs. Desossirbosio Un Nucleotide è una molecola costituita da un composto ad anello contenente azoto (N) legato
Nucleotidi 20/12/2013. Nucleotidi (1) Ribosio Vs. Desossirbosio
 I Nucleotidi Hanno Tre Componenti Nucleotidi https://www2.chemistry.msu.edu/faculty/reusch/virttxtjml/nucacids.htm Nucleotidi (1) Ribosio Vs. Desossirbosio Un Nucleotide è una molecola costituita da un
I Nucleotidi Hanno Tre Componenti Nucleotidi https://www2.chemistry.msu.edu/faculty/reusch/virttxtjml/nucacids.htm Nucleotidi (1) Ribosio Vs. Desossirbosio Un Nucleotide è una molecola costituita da un
Nucleotidi 26/10/2014. Nucleotidi (1)
 I Nucleotidi Hanno Tre Componenti Base azotata Nucleotidi https://www2.chemistry.msu.edu/faculty/reusch/virttxtjml/nucacids.htm Base azotata Qualsiasi composto che manifesta proprietà basiche per via della
I Nucleotidi Hanno Tre Componenti Base azotata Nucleotidi https://www2.chemistry.msu.edu/faculty/reusch/virttxtjml/nucacids.htm Base azotata Qualsiasi composto che manifesta proprietà basiche per via della
Metabolismo degli amminoacidi
 Metabolismo degli amminoacidi Gli amminoacidi derivati in gran parte dalla degradazione delle proteine della dieta o intracellulari possono essere ossidati per generare energia. La quantità di energia
Metabolismo degli amminoacidi Gli amminoacidi derivati in gran parte dalla degradazione delle proteine della dieta o intracellulari possono essere ossidati per generare energia. La quantità di energia
Metabolismo. dei nucleotidi. Citosina Uracile Timina. Adenina Guanina
 Metabolismo dei nucleotidi Adenina Guanina Citosina Uracile Timina 1 I nucleotidi sono esteri fosforici di un pentosio (ribosio o desossiribosio) in cui una base purinica o pirimidinica è legata all atomo
Metabolismo dei nucleotidi Adenina Guanina Citosina Uracile Timina 1 I nucleotidi sono esteri fosforici di un pentosio (ribosio o desossiribosio) in cui una base purinica o pirimidinica è legata all atomo
Nucleotidi e Acidi Nucleici
 Nucleotidi e Acidi Nucleici https://www2.chemistry.msu.edu/faculty/reusch/virttxtjml/nucacids.htm Componenti degli acidi nucleici Collegato al fosfato Collegato alla base azotata Collegato allo zucchero
Nucleotidi e Acidi Nucleici https://www2.chemistry.msu.edu/faculty/reusch/virttxtjml/nucacids.htm Componenti degli acidi nucleici Collegato al fosfato Collegato alla base azotata Collegato allo zucchero
Modulo 14 Il ciclo di Krebs
 Modulo 14 Il ciclo di Krebs Il destino ossidativo del piruvato In condizioni aerobie il piruvato viene decarbossilato ad acetato. L acetato è ossidato ulteriormente nel ciclo dell acido citrico. Una serie
Modulo 14 Il ciclo di Krebs Il destino ossidativo del piruvato In condizioni aerobie il piruvato viene decarbossilato ad acetato. L acetato è ossidato ulteriormente nel ciclo dell acido citrico. Una serie
Sintesi de novo dei ribonucleotidi purinici
 Sintesi de novo dei ribonucleotidi purinici origine metabolica dei nove atomi dell anello purinico: a differenza delle pirimidine, le basi puriniche vengono costruite sull anello di ribosio fosfato: sono
Sintesi de novo dei ribonucleotidi purinici origine metabolica dei nove atomi dell anello purinico: a differenza delle pirimidine, le basi puriniche vengono costruite sull anello di ribosio fosfato: sono
METABOLISMO del GLUCOSIO: GLUCONEOGENESI e VIA DEI PENTOSI
 METABOLISMO del GLUCOSIO: GLUCONEOGENESI e VIA DEI PENTOSI Glicolisi: Glucosio Glucosio Piruvato Piruvato Gluconeogenesi La Glicolisi (dal greco glykys dolce e lysis scissione) E` la via metabolica che
METABOLISMO del GLUCOSIO: GLUCONEOGENESI e VIA DEI PENTOSI Glicolisi: Glucosio Glucosio Piruvato Piruvato Gluconeogenesi La Glicolisi (dal greco glykys dolce e lysis scissione) E` la via metabolica che
La glicolisi non è l unica via catabolica in grado di produrre energia. Se il suo prodotto viene ulteriormente ossidato si ottiene molta più energia.
 La glicolisi non è l unica via catabolica in grado di produrre energia. Se il suo prodotto viene ulteriormente ossidato si ottiene molta più energia. Il ciclo dell acido citrico è una via metabolica centrale
La glicolisi non è l unica via catabolica in grado di produrre energia. Se il suo prodotto viene ulteriormente ossidato si ottiene molta più energia. Il ciclo dell acido citrico è una via metabolica centrale
CICLO DI KREBS (o DELL ACIDO CITRICO)
 CICLO DI KREBS (o DELL ACIDO CITRICO) È un processo ossidativo che ha un ruolo centrale nel metabolismo energetico delle cellule eucariotiche. Avviene nella matrice mitocondriale. È alimentato soprattutto
CICLO DI KREBS (o DELL ACIDO CITRICO) È un processo ossidativo che ha un ruolo centrale nel metabolismo energetico delle cellule eucariotiche. Avviene nella matrice mitocondriale. È alimentato soprattutto
Funzioni dei nucleotidi
 Funzioni dei nucleotidi monomeri degli acidi nucleici esempi di altre funzioni ATP: moneta energetica GTP: fonte di energia nella sintesi proteica camp: secondo messaggero nella trasduzione del segnale
Funzioni dei nucleotidi monomeri degli acidi nucleici esempi di altre funzioni ATP: moneta energetica GTP: fonte di energia nella sintesi proteica camp: secondo messaggero nella trasduzione del segnale
Via finale comune per l ossidazione di tutti i combustibili metabolici che entrano nella via come molecola di acetil CoA
 Via finale comune per l ossidazione di tutti i combustibili metabolici che entrano nella via come molecola di acetil CoA C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O Processi molecolari in cui è coinvolto il consumo
Via finale comune per l ossidazione di tutti i combustibili metabolici che entrano nella via come molecola di acetil CoA C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O Processi molecolari in cui è coinvolto il consumo
CHIMICA BIOLOGICA. Seconda Università degli Studi di Napoli. DiSTABiF. Corso di Laurea in Scienze Biologiche. Insegnamento di. Anno Accademico
 Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Prof. Antimo Di Maro Anno Accademico 2016-17 Lezione 14 Ciclo di Krebs L ossidazione
Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Prof. Antimo Di Maro Anno Accademico 2016-17 Lezione 14 Ciclo di Krebs L ossidazione
Il metabolismo dei lipidi
 Il metabolismo dei lipidi Digestione, assorbimento e trasporto dei lipidi Concetti chiave I triacilgliceroli sono demoliti dalle lipasi e i prodotti derivanti dalla loro scissione sono assorbiti dall intestino.
Il metabolismo dei lipidi Digestione, assorbimento e trasporto dei lipidi Concetti chiave I triacilgliceroli sono demoliti dalle lipasi e i prodotti derivanti dalla loro scissione sono assorbiti dall intestino.
Una panoramica del ciclo dell acido ciclico
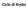 Ciclo di Krebs Una panoramica del ciclo dell acido ciclico Concetti chiave Il ciclo dell acido citrico, o ciclo di Krebs, o ciclo degli acidi tricarbossilici (TCA), è un processo catalitico a 8 tappe che
Ciclo di Krebs Una panoramica del ciclo dell acido ciclico Concetti chiave Il ciclo dell acido citrico, o ciclo di Krebs, o ciclo degli acidi tricarbossilici (TCA), è un processo catalitico a 8 tappe che
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio. GLUCONEOGENESI (sintesi da precursori non glucidici)
 DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) La gluconeogenesi utilizza il piruvato e altri composti a
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) La gluconeogenesi utilizza il piruvato e altri composti a
Metabolismo degli amminoacidi
 Metabolismo degli amminoacidi Bilancio azotato Differenza fra l azoto introdotto e quello eliminato Positivo (gravidanza) Negativo In equilibrio ghiandole salivari bocca amilasi gastrina l (p 1) pepsinogeno
Metabolismo degli amminoacidi Bilancio azotato Differenza fra l azoto introdotto e quello eliminato Positivo (gravidanza) Negativo In equilibrio ghiandole salivari bocca amilasi gastrina l (p 1) pepsinogeno
Gluconeogenesi. Sintesi de-novo di glucosio
 Gluconeogenesi Sintesi de-novo di glucosio La gluconeogenesi garantisce il mantenimento dei livelli di glucosio nel sangue anche per molto tempo dopo l assorbimento e la completa ossidazione del glucosio
Gluconeogenesi Sintesi de-novo di glucosio La gluconeogenesi garantisce il mantenimento dei livelli di glucosio nel sangue anche per molto tempo dopo l assorbimento e la completa ossidazione del glucosio
Biochimica e Biologia per le professioni sanitarie, McGraw-Hill
 Biochimica e Biologia per le professioni sanitarie, McGrawHill Tab. 20.1 Amminoacidi essenziali per l uomo Arginina Istidina Isoleucina Leucina Lisina Metionina Fenilalanina Treonina Triptofano Valina
Biochimica e Biologia per le professioni sanitarie, McGrawHill Tab. 20.1 Amminoacidi essenziali per l uomo Arginina Istidina Isoleucina Leucina Lisina Metionina Fenilalanina Treonina Triptofano Valina
Metabolismo degli Ammino Acidi
 Metabolismo degli Ammino Acidi R 1 C C - R 2 C C - N 3 Transaminasi R 1 C C - R 2 C C - N 3 Transaminasi (amminotransferasi) catalizza il trasferimento reversibile di un ammino gruppo tra due a-cheto acidi.
Metabolismo degli Ammino Acidi R 1 C C - R 2 C C - N 3 Transaminasi R 1 C C - R 2 C C - N 3 Transaminasi (amminotransferasi) catalizza il trasferimento reversibile di un ammino gruppo tra due a-cheto acidi.
Modulo 8: I nucleotidi e gli acidi nucleici
 Modulo 8: I nucleotidi e gli acidi nucleici Modulo 10: Acidi nucleici Filamento di DNA fuoriuscito da una cellula di Escherichia coli Struttura e funzioni dei nucleotidi Funzioni dei nucleotidi: Unità
Modulo 8: I nucleotidi e gli acidi nucleici Modulo 10: Acidi nucleici Filamento di DNA fuoriuscito da una cellula di Escherichia coli Struttura e funzioni dei nucleotidi Funzioni dei nucleotidi: Unità
PROTEINE ed AMMINOACIDI: RUOLO METABOLICO E NUTRIZIONALE (a)
 Università di Roma Tor Vergata - Scienze della Nutrizione Umana Biochimica della Nutrizione Prof.ssa Luciana Avigliano 2011 PROTEINE ed AMMINOACIDI: RUOLO METABOLICO E NUTRIZIONALE (a) amminoacidi proteine
Università di Roma Tor Vergata - Scienze della Nutrizione Umana Biochimica della Nutrizione Prof.ssa Luciana Avigliano 2011 PROTEINE ed AMMINOACIDI: RUOLO METABOLICO E NUTRIZIONALE (a) amminoacidi proteine
METABOLISMO DI BASI AZOTATE E NUCLEOTIDI
 METABOLISMO DI BASI AZOTATE E NUCLEOTIDI Le basi azotate si dividono in purine e pirimidine. Le purine sono l adenina e la guanina. La xantina e la ipoxantina sono considerati due intermedi della sintesi
METABOLISMO DI BASI AZOTATE E NUCLEOTIDI Le basi azotate si dividono in purine e pirimidine. Le purine sono l adenina e la guanina. La xantina e la ipoxantina sono considerati due intermedi della sintesi
Cap.19. Ciclo di Krebs. o Ciclo degli acidi Tricarbossilici o Ciclo dell acido Citrico
 Cap.19 Ciclo di Krebs o Ciclo degli acidi Tricarbossilici o Ciclo dell acido Citrico Acetil-CoA OSSIDAZIONE DEL GLUCOSIO C 6 H 12 O 6 (glucosio) + 6O 2.. 6CO 2 + 6H 2 O I tappa: GLICOLISI 2 + 2 H 2 O II
Cap.19 Ciclo di Krebs o Ciclo degli acidi Tricarbossilici o Ciclo dell acido Citrico Acetil-CoA OSSIDAZIONE DEL GLUCOSIO C 6 H 12 O 6 (glucosio) + 6O 2.. 6CO 2 + 6H 2 O I tappa: GLICOLISI 2 + 2 H 2 O II
ENZIMI. Un enzima è un catalizzatore (acceleratore) di reazioni biologiche.
 ENZIMI ENZIMI Un enzima è un catalizzatore (acceleratore) di reazioni biologiche. Catalizzatore = sostanza in grado di accelerare lo svolgimento di una reazione chimica e quindi di aumentarne la sua velocità,
ENZIMI ENZIMI Un enzima è un catalizzatore (acceleratore) di reazioni biologiche. Catalizzatore = sostanza in grado di accelerare lo svolgimento di una reazione chimica e quindi di aumentarne la sua velocità,
CICLO DI KREBS (o DELL ACIDO CITRICO)
 CICLO DI KREBS (o DELL ACIDO CITRICO) È un processo ossidativo che ha un ruolo centrale nel metabolismo energetico delle cellule eucariotiche. Avviene nella matrice mitocondriale. È alimentato soprattutto
CICLO DI KREBS (o DELL ACIDO CITRICO) È un processo ossidativo che ha un ruolo centrale nel metabolismo energetico delle cellule eucariotiche. Avviene nella matrice mitocondriale. È alimentato soprattutto
Metabolismo degli Ammino Acidi
 Metabolismo degli Ammino Acidi R 1 - R 2 - N 3 Transaminasi R 1 - R 2 - N 3 Transaminasi (amminotransferasi) catalizza il trasferimento reversibile di un ammino gruppo tra due α-cheto acidi. Amminotransferasi
Metabolismo degli Ammino Acidi R 1 - R 2 - N 3 Transaminasi R 1 - R 2 - N 3 Transaminasi (amminotransferasi) catalizza il trasferimento reversibile di un ammino gruppo tra due α-cheto acidi. Amminotransferasi
IL METABOLISMO. Dal carbonio agli OGM Capitolo 2
 IL METABOLISMO Dal carbonio agli OGM Capitolo 2 IL METABOLISMO L'insieme delle trasformazioni chimiche ed energetiche che si verificano nelle cellule di un organismo vivente e ne garantiscono la conservazione,
IL METABOLISMO Dal carbonio agli OGM Capitolo 2 IL METABOLISMO L'insieme delle trasformazioni chimiche ed energetiche che si verificano nelle cellule di un organismo vivente e ne garantiscono la conservazione,
METABOLISMO OSSIDATIVO
 METABOLISMO OSSIDATIVO IDROLISI DEI LIPIDI LIPASI Fosfolipidi Fosfolipasi β ossidazione degli acidi grassi NEL CITOPLASMA: attivazione dell acido grasso Consumo di 2 ATP ΔG idrolisi ATP = -35,9 kj mol
METABOLISMO OSSIDATIVO IDROLISI DEI LIPIDI LIPASI Fosfolipidi Fosfolipasi β ossidazione degli acidi grassi NEL CITOPLASMA: attivazione dell acido grasso Consumo di 2 ATP ΔG idrolisi ATP = -35,9 kj mol
Biosintesi dei carboidrati
 Biosintesi dei carboidrati Gluconeogenesi: sintesi di glucosio da precursori non saccaridici La riserva di glucosio dell organismo (glucosio + glicogeno) è sufficiente per circa 1 giorno. La via gluconeogenetica
Biosintesi dei carboidrati Gluconeogenesi: sintesi di glucosio da precursori non saccaridici La riserva di glucosio dell organismo (glucosio + glicogeno) è sufficiente per circa 1 giorno. La via gluconeogenetica
La fissazione dell azoto
 La fissazione dell azoto Complesso della nitrogenasi N +10H + + 8e + 16ATP N 2 + 10 H + 8e + 16ATP 2NH 4+ + 16ADP + 16P + H2 Metabolismo degli aminoacidi Metabolismo degli aminoacidi Gli aminoacidi
La fissazione dell azoto Complesso della nitrogenasi N +10H + + 8e + 16ATP N 2 + 10 H + 8e + 16ATP 2NH 4+ + 16ADP + 16P + H2 Metabolismo degli aminoacidi Metabolismo degli aminoacidi Gli aminoacidi
La via del gliossilato avviene in parte nei gliossisomi e in parte nei mitocondri. 2 enzimi la isocitrato liasi (ICL) e
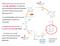 Nelle piante l Acetil CoA può innescare la via del gliossilato che si discosta dal ciclo di Krebs a livello dell isocitrato ed evita le reazioni che provocano liberazione di CO 2 La via del gliossilato
Nelle piante l Acetil CoA può innescare la via del gliossilato che si discosta dal ciclo di Krebs a livello dell isocitrato ed evita le reazioni che provocano liberazione di CO 2 La via del gliossilato
Aerobiosi C A T A B O L I S M O. Lez 4A. Schema generale del metabolismo dei glucidi
 Schema generale del metabolismo dei glucidi -1- Aerobiosi In condizioni aerobiche il piruvato prodotto dalla glicolisi e dalla degradazione di alcuni aminoacidi è ossidato a H 2 O e CO 2 nella respirazione
Schema generale del metabolismo dei glucidi -1- Aerobiosi In condizioni aerobiche il piruvato prodotto dalla glicolisi e dalla degradazione di alcuni aminoacidi è ossidato a H 2 O e CO 2 nella respirazione
NADH e NADPH. ATP = 1 moneta (energetica) della cellula NADH, NADPH = 2 moneta (potere riducente)
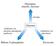 NADH e NADPH ATP = 1 moneta (energetica) della cellula NADH, NADPH = 2 moneta (potere riducente) NADH e NADPH non sono funzionalmente intercambiabili. [NAD + ]/[NADH] ~ 1000 favorisce ossidazione [NADP
NADH e NADPH ATP = 1 moneta (energetica) della cellula NADH, NADPH = 2 moneta (potere riducente) NADH e NADPH non sono funzionalmente intercambiabili. [NAD + ]/[NADH] ~ 1000 favorisce ossidazione [NADP
DESTINI METABOLICI DEL PIRUVATO
 DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Complesso della Piruvato deidrogenasi
DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Complesso della Piruvato deidrogenasi
Capitolo 6 La respirazione cellulare
 Capitolo 6 La respirazione cellulare Introduzione alla respirazione cellulare 6.1 La respirazione polmonare rifornisce le nostre cellule di ossigeno ed elimina diossido di carbonio La respirazione polmonare
Capitolo 6 La respirazione cellulare Introduzione alla respirazione cellulare 6.1 La respirazione polmonare rifornisce le nostre cellule di ossigeno ed elimina diossido di carbonio La respirazione polmonare
Percorsi di chimica organica - Soluzioni degli esercizi del testo
 ercorsi di chimica organica - Soluzioni degli esercizi del testo AITL 14 1. Il prefisso α negli α-amminoacidi sta ad indicare che il gruppo amminico, - 2, si trova sul carbonio alfa (carbonio legato al
ercorsi di chimica organica - Soluzioni degli esercizi del testo AITL 14 1. Il prefisso α negli α-amminoacidi sta ad indicare che il gruppo amminico, - 2, si trova sul carbonio alfa (carbonio legato al
AGISCONO NEL SISTEMA NAVETTA 2 ISOFORME DELL ENZIMA: UNA FORMA MITOCONDRIALE ( MEMBRANA MIT. INTERNA) FAD-dipendente
 METABOLISMO AEROBIO I NADH prodotti durante la glicolisi nel citosol, in condizioni aerobiche (respirazione mitocondriale attiva), possono trasferire elettroni all interno del mitocondrio attraverso i
METABOLISMO AEROBIO I NADH prodotti durante la glicolisi nel citosol, in condizioni aerobiche (respirazione mitocondriale attiva), possono trasferire elettroni all interno del mitocondrio attraverso i
Esercitazione Esempi di domande del 2 test
 Esercitazione Esempi di domande del 2 test Esempio 1. Gli enzimi opposti glicogeno fosforilasi e glicogeno sintasi sono regolati in maniera opposta da una serie di effettori. Quali? Come avviene la regolazione
Esercitazione Esempi di domande del 2 test Esempio 1. Gli enzimi opposti glicogeno fosforilasi e glicogeno sintasi sono regolati in maniera opposta da una serie di effettori. Quali? Come avviene la regolazione
METABOLISMO CELLULARE
 METABOLISMO CELLULARE Struttura dell ATP (Adenosintrifosfato) Adenina (base azotata), Ribosio (zucchero) e un gruppo fosforico ATP Il legame covalente tra i gruppi fosforici si spezza facilmente liberando
METABOLISMO CELLULARE Struttura dell ATP (Adenosintrifosfato) Adenina (base azotata), Ribosio (zucchero) e un gruppo fosforico ATP Il legame covalente tra i gruppi fosforici si spezza facilmente liberando
IL GLUCOSIO PUO ESSERE SINTETIZZATO DA PRECURSORI NON GLUCIDICI
 GLUCONEOGENESI IL GLUCOSIO PUO ESSERE SINTETIZZATO DA PRECURSORI NON GLUCIDICI Quando la quantità di glucosio fornito dagli alimenti o dalle riserve è insufficiente, i diversi organismi sintetizzano glucosio
GLUCONEOGENESI IL GLUCOSIO PUO ESSERE SINTETIZZATO DA PRECURSORI NON GLUCIDICI Quando la quantità di glucosio fornito dagli alimenti o dalle riserve è insufficiente, i diversi organismi sintetizzano glucosio
GLUCOSIO. Vena porta DIGESTIONE DEI DISACCARIDI. Enzimi parete intestinale
 DIGESTIONE DELL AMIDO AMIDO Amilasi salivare DESTRINE Amilasi pancreatica MALTOSIO Enzimi parete intestinale GLUCOSIO Vena porta DIGESTIONE DEI DISACCARIDI DISACCARIDI Enzimi parete intestinale MONOSACCARIDI
DIGESTIONE DELL AMIDO AMIDO Amilasi salivare DESTRINE Amilasi pancreatica MALTOSIO Enzimi parete intestinale GLUCOSIO Vena porta DIGESTIONE DEI DISACCARIDI DISACCARIDI Enzimi parete intestinale MONOSACCARIDI
Metabolismo glucidico
 Metabolismo glucidico Glicogeno glicogenolisi Riboso-5P (NADPH) Colesterolo glicogenosintesi shunt pentoso fosfati Glucoso Glucoso-6P glicolisi Piruvato gluconeogenesi CO 2 -ossidazione Trigliceridi Acidi
Metabolismo glucidico Glicogeno glicogenolisi Riboso-5P (NADPH) Colesterolo glicogenosintesi shunt pentoso fosfati Glucoso Glucoso-6P glicolisi Piruvato gluconeogenesi CO 2 -ossidazione Trigliceridi Acidi
 METABOLISMO DEGLI AMMINOACIDI 1.Quali tra i seguenti sono amminoacidi semiessenziali: -Arginina e istidina -valina e treonina -fenilalanina e metionina -glicina e alanina Cosa si intende per semi essenziali?
METABOLISMO DEGLI AMMINOACIDI 1.Quali tra i seguenti sono amminoacidi semiessenziali: -Arginina e istidina -valina e treonina -fenilalanina e metionina -glicina e alanina Cosa si intende per semi essenziali?
Nella Biosfera viene mantenuto un un equilibrio tra l azoto totale inorganico e quello organico
 Gli a.a. oltre ad essere i costituenti delle proteine giocano numerosi ruoli metabolici: precursori di ormoni, vitamine, coenzimi, porfirine, pigmenti e neurotrasmettitori L esistenza di 20 a.a. nelle
Gli a.a. oltre ad essere i costituenti delle proteine giocano numerosi ruoli metabolici: precursori di ormoni, vitamine, coenzimi, porfirine, pigmenti e neurotrasmettitori L esistenza di 20 a.a. nelle
Fosforilazione a livello del substrato
 10 piruvato chinasi Fosfoenolpiruvato Rib Adenina Piruvato ADP Rib ATP Adenina Fosforilazione a livello del substrato 3 Fosfofruttochinasi-1 (PFK-1) Fruttosio 6-fosfato Fruttosio 1,6-bisfosfato 1 esochinasi
10 piruvato chinasi Fosfoenolpiruvato Rib Adenina Piruvato ADP Rib ATP Adenina Fosforilazione a livello del substrato 3 Fosfofruttochinasi-1 (PFK-1) Fruttosio 6-fosfato Fruttosio 1,6-bisfosfato 1 esochinasi
6 H 2. con G=-686 kcal/mole di H 12 O 6 O + 6 CO O 2. glucosio La respirazione avviene in tre stadi principali; ognuno di questi
 La respirazione La respirazione è un processo di ossidoriduzione nel quale i riducenti sono molecole organiche altamente ridotte e ricche di energia e gli ossidanti sono molecole inorganiche come O 2 Il
La respirazione La respirazione è un processo di ossidoriduzione nel quale i riducenti sono molecole organiche altamente ridotte e ricche di energia e gli ossidanti sono molecole inorganiche come O 2 Il
2 INCONTRO: LA PRODUZIONE DI ENERGIA NELLA CELLULA
 INCONTRO: LA PRODUZIONE DI ENERGIA NELLA CELLULA 1 INTRODUZIONE 1 L energia chimica Esistono diversi tipi di energia e una tra queste è l energia chimica: un tipo di energia che possiedono tutte le molecole
INCONTRO: LA PRODUZIONE DI ENERGIA NELLA CELLULA 1 INTRODUZIONE 1 L energia chimica Esistono diversi tipi di energia e una tra queste è l energia chimica: un tipo di energia che possiedono tutte le molecole
Variazioni di energia libera nella glicolisi
 Variazioni di energia libera nella glicolisi 10 piruvato chinasi Fosfoenolpiruvato Rib Adenina Piruvato ADP Rib ATP Adenina Fosforilazione a livello del substrato 3 Fosfofruttochinasi-1 (PFK-1) Fruttosio
Variazioni di energia libera nella glicolisi 10 piruvato chinasi Fosfoenolpiruvato Rib Adenina Piruvato ADP Rib ATP Adenina Fosforilazione a livello del substrato 3 Fosfofruttochinasi-1 (PFK-1) Fruttosio
Fosforilazione a livello del substrato
 10 piruvato chinasi Fosfoenolpiruvato Rib Adenina Piruvato ADP Rib ATP Adenina Fosforilazione a livello del substrato 3 Fosfofruttochinasi-1 (PFK-1) Fruttosio 6-fosfato Fruttosio 1,6-bisfosfato 1 esochinasi
10 piruvato chinasi Fosfoenolpiruvato Rib Adenina Piruvato ADP Rib ATP Adenina Fosforilazione a livello del substrato 3 Fosfofruttochinasi-1 (PFK-1) Fruttosio 6-fosfato Fruttosio 1,6-bisfosfato 1 esochinasi
Gli acidi nucleici, DNA (acido deossiribonucleico) e RNA (acido. ribonucleico), sono polimeri biologicamente importanti in quanto
 Gli acidi nucleici, DA (acido deossiribonucleico) e RA (acido ribonucleico), sono polimeri biologicamente importanti in quanto svolgono ruoli fondamentali nell ereditarietà e nella sintesi proteica. Sono
Gli acidi nucleici, DA (acido deossiribonucleico) e RA (acido ribonucleico), sono polimeri biologicamente importanti in quanto svolgono ruoli fondamentali nell ereditarietà e nella sintesi proteica. Sono
INTRODUZIONE AL METABOLISMO
 INTRODUZIONE AL METABOLISMO METABOLISMO Il metabolismo (dal greco metabolé = trasformazione) è il complesso delle reazioni chimiche coordinate ed integrate che avvengono in una cellula. Il metabolismo
INTRODUZIONE AL METABOLISMO METABOLISMO Il metabolismo (dal greco metabolé = trasformazione) è il complesso delle reazioni chimiche coordinate ed integrate che avvengono in una cellula. Il metabolismo
FONTI DI AMMINOACIDI: PROTEINE ASSUNTE CON GLI ALIMENTI PROTEINE ENDOGENE (TURNOVER) BIOSINTESI
 FONTI DI AMMINOACIDI: PROTEINE ASSUNTE CON GLI ALIMENTI PROTEINE ENDOGENE (TURNOVER) BIOSINTESI ZIMOGENI ATTIVATI NEL LUME INTESTINALE DURANTE LA DIGESTIONE DELLE PROTEINE ESOGENE Tripsina, chimotripsina,
FONTI DI AMMINOACIDI: PROTEINE ASSUNTE CON GLI ALIMENTI PROTEINE ENDOGENE (TURNOVER) BIOSINTESI ZIMOGENI ATTIVATI NEL LUME INTESTINALE DURANTE LA DIGESTIONE DELLE PROTEINE ESOGENE Tripsina, chimotripsina,
Complesso della piruvato deidrogenasi (1) Stechiometria della reazione finale
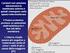 Ciclo di Krebs 1 Complesso della piruvato deidrogenasi (1) Stechiometria della reazione finale 2 Complesso della piruvato deidrogenasi (2) FAD Diidrolipoil deidrogenasi Piruvato decarbossilasi E 3 Diidrolipoil
Ciclo di Krebs 1 Complesso della piruvato deidrogenasi (1) Stechiometria della reazione finale 2 Complesso della piruvato deidrogenasi (2) FAD Diidrolipoil deidrogenasi Piruvato decarbossilasi E 3 Diidrolipoil
1. L'enzima che catalizza la trasformazione della 3-fosfogliceraldeide in acido 1,3 difosfoglicerico è una:
 1. L'enzima che catalizza la trasformazione della 3-fosfogliceraldeide in acido 1,3 difosfoglicerico è una: a) idrolasi b) isomerasi c) aldolasi d) fosfatasi e) deidrogenasi 2. Quale dei sottoelencati
1. L'enzima che catalizza la trasformazione della 3-fosfogliceraldeide in acido 1,3 difosfoglicerico è una: a) idrolasi b) isomerasi c) aldolasi d) fosfatasi e) deidrogenasi 2. Quale dei sottoelencati
DESTINI METABOLICI DEL PIRUVATO
 DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Piruvato Complesso della Piruvato
DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Piruvato Complesso della Piruvato
Nucleotidi e Acidi Nucleici. Struttura di DNA e RNA
 Nucleotidi e Acidi Nucleici Nucleosidi Nucleotidi Funzioni biologiche dei nucleotidi Struttura di DNA e RNA Concatenazione e appaiamento dei nucleotidi Lo scheletro degli acidi nucleici Componenti degli
Nucleotidi e Acidi Nucleici Nucleosidi Nucleotidi Funzioni biologiche dei nucleotidi Struttura di DNA e RNA Concatenazione e appaiamento dei nucleotidi Lo scheletro degli acidi nucleici Componenti degli
07/01/2015. Un esempio semplice... L N-Acetilglucosamina. Cosa mangiano i batteri (oltre al glucosio)?
 Cosa mangiano i batteri (oltre al glucosio)? Altri zuccheri (amino zuccheri, disaccaridi, etc.) Aminoacidi Acidi grassi, altri acidi organici, nucleotidi, etc... I batteri eterotrofi possono crescere utilizzando
Cosa mangiano i batteri (oltre al glucosio)? Altri zuccheri (amino zuccheri, disaccaridi, etc.) Aminoacidi Acidi grassi, altri acidi organici, nucleotidi, etc... I batteri eterotrofi possono crescere utilizzando
Helena Curtis N. Sue Barnes
 Helena Curtis N. Sue Barnes LA FOTOSINTESI INDICE Organismi autotrofi ed eterotrofi Confronto tra fotosintesi e respirazione Reazioni endoergoniche ed esoergoniche Reazioni accoppiate Fase luce-dipendente
Helena Curtis N. Sue Barnes LA FOTOSINTESI INDICE Organismi autotrofi ed eterotrofi Confronto tra fotosintesi e respirazione Reazioni endoergoniche ed esoergoniche Reazioni accoppiate Fase luce-dipendente
INTRODUZIONE AL METABOLISMO. dal gr. metabolè = trasformazione
 INTRODUZIONE AL METABOLISMO dal gr. metabolè = trasformazione IL Metabolismo Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in una cellula o in un organismo. E costituito da
INTRODUZIONE AL METABOLISMO dal gr. metabolè = trasformazione IL Metabolismo Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in una cellula o in un organismo. E costituito da
I MITOCONDRI: LE CENTRALI ENERGETICHE DELLA CELLULA
 I MITOCONDRI: LE CENTRALI ENERGETICHE DELLA CELLULA MITOCONDRIO OSSERVATO AL SEM Localizzazione dei mitocondri SONO IN GENERE PIÙ ABBONDANTI DELLE ZONE DELLA CELLULA CHE RICHIEDONO MAGGIORI QUANTITA DI
I MITOCONDRI: LE CENTRALI ENERGETICHE DELLA CELLULA MITOCONDRIO OSSERVATO AL SEM Localizzazione dei mitocondri SONO IN GENERE PIÙ ABBONDANTI DELLE ZONE DELLA CELLULA CHE RICHIEDONO MAGGIORI QUANTITA DI
fornire energia chimica in vettori attivati ATP e NADH e NADPH e FADH.
 Cibo ed Energia Il glucosio e altre molecole nutritive per esempio i grassi vengono demolite attraverso un ossidazione graduale controllata per fornire energia chimica in una forma utilizzabile dalla cellula,
Cibo ed Energia Il glucosio e altre molecole nutritive per esempio i grassi vengono demolite attraverso un ossidazione graduale controllata per fornire energia chimica in una forma utilizzabile dalla cellula,
DESTINI METABOLICI DEL PIRUVATO
 DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Piruvato Complesso della Piruvato
DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Piruvato Complesso della Piruvato
Svolgono funzioni biologiche di fondamentale importanza e possono essere divise in 7 gruppi principali:
 Svolgono funzioni biologiche di fondamentale importanza e possono essere divise in 7 gruppi principali: proteine strutturali (collagene, cheratine); proteine catalitiche (enzimi); proteine di trasporto
Svolgono funzioni biologiche di fondamentale importanza e possono essere divise in 7 gruppi principali: proteine strutturali (collagene, cheratine); proteine catalitiche (enzimi); proteine di trasporto
Il carbonio è l elemento di base delle biomolecole. Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici.
 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici. 1 Il carbonio deve acquistare quattro elettroni per essere stabile
Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici. 1 Il carbonio deve acquistare quattro elettroni per essere stabile
Il metabolismo cellulare
 Il metabolismo cellulare 1 Il metabolismo cellulare CATABOLISMO Processo esoergonico (per produrre energia) Nutriliti NAD FAD NADP e - +H + ANABOLISMO Processo endoergonico Biopolimeri (x es. proteine)
Il metabolismo cellulare 1 Il metabolismo cellulare CATABOLISMO Processo esoergonico (per produrre energia) Nutriliti NAD FAD NADP e - +H + ANABOLISMO Processo endoergonico Biopolimeri (x es. proteine)
scaricato da www.sunhope.it
 CICLO DEGLI ACIDI TRICARBOSSILICI o CICLO DELL ACIDO CITRICO o CICLO DI KREBS scaricato da www.sunhope.it IL CICLO DI KREBS È LA VIA OSSIDATIVA FINALE DEL CATABOLISMO DI GLUCIDI LIPIDI PROTEINE IL CICLO
CICLO DEGLI ACIDI TRICARBOSSILICI o CICLO DELL ACIDO CITRICO o CICLO DI KREBS scaricato da www.sunhope.it IL CICLO DI KREBS È LA VIA OSSIDATIVA FINALE DEL CATABOLISMO DI GLUCIDI LIPIDI PROTEINE IL CICLO
4. MED Nella respirazione aerobica si ha ossidazione delle molecole di: A) glucosio B) ossigeno C) biossido di carbonio D) acqua E) NAD +
 1. MED 1997 - La tappa di passaggio dalla glicolisi al ciclo di Krebs e' la trasformazione: A) del glucosio in piruvato B) del piruvato in glucosio C) del piruvato in acetil-coa D) del glucosio in acetil-coa
1. MED 1997 - La tappa di passaggio dalla glicolisi al ciclo di Krebs e' la trasformazione: A) del glucosio in piruvato B) del piruvato in glucosio C) del piruvato in acetil-coa D) del glucosio in acetil-coa
riduzione fotosintetica del carbonio, PCR analisi intermedi marcati
 riduzione fotosintetica del carbonio, PCR 14 CO 2 Chlorella analisi intermedi marcati dopo 5 s dopo 30 s l accettore della CO 2 è il ribulosio 1,5 bis-fosfato CICLO C3 3-fosfoglicerato gliceraldeide 3-fosfato
riduzione fotosintetica del carbonio, PCR 14 CO 2 Chlorella analisi intermedi marcati dopo 5 s dopo 30 s l accettore della CO 2 è il ribulosio 1,5 bis-fosfato CICLO C3 3-fosfoglicerato gliceraldeide 3-fosfato
UNIVERSITÀ DI PISA. Facoltà di Farmacia. Corso di Laurea Specialistica in Chimica e Tecnologia Farmaceutiche
 UNIVERSITÀ DI PISA Facoltà di Farmacia Corso di Laurea Specialistica in Chimica e Tecnologia Farmaceutiche Tesi di Laurea: Derivati a struttura 2-fenilftalazinonica: nuovi antagonisti per i recettori A
UNIVERSITÀ DI PISA Facoltà di Farmacia Corso di Laurea Specialistica in Chimica e Tecnologia Farmaceutiche Tesi di Laurea: Derivati a struttura 2-fenilftalazinonica: nuovi antagonisti per i recettori A
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH. ) ed un gruppo carbossilico ( COOH) nella stessa molecola
 Amminoacidi (1) Presentano un gruppo amminico ( NH 2 ) ed un gruppo carbossilico ( COOH) nella stessa molecola CH 3 NH 2 C H α * COOH Acido 2-ammino propanoico (acido α-ammino propionico) 1 Amminoacidi
Amminoacidi (1) Presentano un gruppo amminico ( NH 2 ) ed un gruppo carbossilico ( COOH) nella stessa molecola CH 3 NH 2 C H α * COOH Acido 2-ammino propanoico (acido α-ammino propionico) 1 Amminoacidi
Energia e metabolismi energetici
 Energia e metabolismi energetici L energia è la capacità di produrre lavoro Tutti gli organismi hanno bisogno di energia per vivere. L energia è definita come la capacità di effettuare un lavoro L energia
Energia e metabolismi energetici L energia è la capacità di produrre lavoro Tutti gli organismi hanno bisogno di energia per vivere. L energia è definita come la capacità di effettuare un lavoro L energia
Immagini e concetti della biologia
 Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
Ossidazione degli amminoacidi e produzione dell urea
 Ossidazione degli amminoacidi e produzione dell urea Gli amminoacidi sono, con gli zuccheri ed i lipidi, la terza classe di molecole che, attraverso la degradazione ossidativa, contribuiscono significativamente
Ossidazione degli amminoacidi e produzione dell urea Gli amminoacidi sono, con gli zuccheri ed i lipidi, la terza classe di molecole che, attraverso la degradazione ossidativa, contribuiscono significativamente
Respirazione cellullare
 Respirazione cellullare 1 luce La respirazione è un processo complementare alla fotosintesi e permette di completare il ciclo del Carbonio. fotosintesi CO 2 H 2 O O 2 Carboidrati respirazione Energia utile
Respirazione cellullare 1 luce La respirazione è un processo complementare alla fotosintesi e permette di completare il ciclo del Carbonio. fotosintesi CO 2 H 2 O O 2 Carboidrati respirazione Energia utile
I mammiferi sono privi dell enzima nitrogenasi, in grado di fissare l azoto atmosferico N2 NH3.
 Le proteine della dieta vengono scisse, nello stomaco e nell intestino, da diversi enzimi (pepsina, chimotripsina, carbossipeptidasi, elastasi) e i singoli amminoacidi sono assorbiti dalla parete intestinale.
Le proteine della dieta vengono scisse, nello stomaco e nell intestino, da diversi enzimi (pepsina, chimotripsina, carbossipeptidasi, elastasi) e i singoli amminoacidi sono assorbiti dalla parete intestinale.
Regolazione del Ciclo di Krebs 8 reazioni
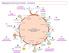 Regolazione del Ciclo di Krebs 8 reazioni Stechiometria del Ciclo Acetil-CoA + 3NAD + + FAD + GDP + Pi + 2H 2 O 2 CO 2 + HS-CoA + 3NADH + 2H + + FADH2 + GTP (GTP ATP) 1 NADH 2,5 ATP 1 FADH 2 1,5 ATP Per
Regolazione del Ciclo di Krebs 8 reazioni Stechiometria del Ciclo Acetil-CoA + 3NAD + + FAD + GDP + Pi + 2H 2 O 2 CO 2 + HS-CoA + 3NADH + 2H + + FADH2 + GTP (GTP ATP) 1 NADH 2,5 ATP 1 FADH 2 1,5 ATP Per
FONTI DI AMMINOACIDI: PROTEINE ASSUNTE CON GLI ALIMENTI PROTEINE ENDOGENE (TURNOVER) BIOSINTESI
 FONTI DI AMMINOACIDI: PROTEINE ASSUNTE CON GLI ALIMENTI PROTEINE ENDOGENE (TURNOVER) BIOSINTESI ZIMOGENI ATTIVATI NEL LUME INTESTINALE DURANTE LA DIGESTIONE DELLE PROTEINE ESOGENE Tripsina, chimotripsina,
FONTI DI AMMINOACIDI: PROTEINE ASSUNTE CON GLI ALIMENTI PROTEINE ENDOGENE (TURNOVER) BIOSINTESI ZIMOGENI ATTIVATI NEL LUME INTESTINALE DURANTE LA DIGESTIONE DELLE PROTEINE ESOGENE Tripsina, chimotripsina,
Composti organici. I composti organici. Atomi e molecole di carbonio. Atomi e molecole di carbonio. Gruppi funzionali. Isomeri
 I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
Le reazioni esoergoniche e quelle endoergoniche del metabolismo cellulare sono legate dalla molecola di ATP.
 1 METABOLISMO CELLULARE Definizione Metabolismo cellulare insieme delle reazioni che producono e necessitano energia nel nostro corpo. Nel metabolismo si distinguono due fasi: Fase catabolica Insieme delle
1 METABOLISMO CELLULARE Definizione Metabolismo cellulare insieme delle reazioni che producono e necessitano energia nel nostro corpo. Nel metabolismo si distinguono due fasi: Fase catabolica Insieme delle
METABOLISMO OSSIDATIVO VIE METABOLICHE CONVERGENTI
 METABOLISMO OSSIDATIVO VIE METABOLICHE CONVERGENTI Nelle piante l ossidazione degli acidi grassi avviene nei perossisomi delle foglie e nei gliossisomi dei semi Nelle cellule animali il sito principale
METABOLISMO OSSIDATIVO VIE METABOLICHE CONVERGENTI Nelle piante l ossidazione degli acidi grassi avviene nei perossisomi delle foglie e nei gliossisomi dei semi Nelle cellule animali il sito principale
prodotto finale della glicolisi
 Piruvato: prodotto finale della glicolisi Può andare incontro a vari destini: -in condizioni anaerobie: il piruvato viene ridotto a lattato (fermentazione lattica) o ad etanolo (fermentazione alcolica)
Piruvato: prodotto finale della glicolisi Può andare incontro a vari destini: -in condizioni anaerobie: il piruvato viene ridotto a lattato (fermentazione lattica) o ad etanolo (fermentazione alcolica)
ACIDI GRASSI INSATURI
 LIPIDI ACIDI GRASSI SATURI ACIDI GRASSI INSATURI TRIGLICERIDI TRIGLICERIDI Grassi neutri o lipidi semplici glicerolo + 1 acido grasso monogliceride glicerolo + 2 acidi grassi digliceride glicerolo + 3
LIPIDI ACIDI GRASSI SATURI ACIDI GRASSI INSATURI TRIGLICERIDI TRIGLICERIDI Grassi neutri o lipidi semplici glicerolo + 1 acido grasso monogliceride glicerolo + 2 acidi grassi digliceride glicerolo + 3
IPOTESI UN GENE-UN ENZIMA
 IPOTESI UN GENE-UN ENZIMA DNA: contiene tutte le informazioni per definire lo sviluppo e la fisiologia della cellula: ma come svolge questa funzione? Beadle e Tatum (1941): studiando mutanti della comune
IPOTESI UN GENE-UN ENZIMA DNA: contiene tutte le informazioni per definire lo sviluppo e la fisiologia della cellula: ma come svolge questa funzione? Beadle e Tatum (1941): studiando mutanti della comune
Metabolismo. Metabolismo. Il complesso di tutte le reazioni organiche di trasformazioni tra energia e materia viene definito come metabolismo.
 Metabolismo Dr. Augusto Innocenti, PhD Biologo Nutrizionista Prof. a contratto Università di Parma Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Metabolismo
Metabolismo Dr. Augusto Innocenti, PhD Biologo Nutrizionista Prof. a contratto Università di Parma Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Metabolismo
Attività cellulare altamente coordinata svolta da sistemi multienzimatici, con i seguenti scopi: ottenere energia chimica dall ambiente attraverso la
 Metabolismo Attività cellulare altamente coordinata svolta da sistemi multienzimatici, con i seguenti scopi: ottenere energia chimica dall ambiente attraverso la degradazione di nutrienti operare la sintesi
Metabolismo Attività cellulare altamente coordinata svolta da sistemi multienzimatici, con i seguenti scopi: ottenere energia chimica dall ambiente attraverso la degradazione di nutrienti operare la sintesi
CELLULA PROCARIOTICA PROCARIOTE
 CELLULA PROCARIOTICA O PROCARIOTE CELLULA EUCARIOTICA O EUCARIOTE Sany0196.jpg IL NUCLEO Provvisto di due membrane (interna ed esterna) che congiungendosi in alcuni punti formano i pori nucleari attraverso
CELLULA PROCARIOTICA O PROCARIOTE CELLULA EUCARIOTICA O EUCARIOTE Sany0196.jpg IL NUCLEO Provvisto di due membrane (interna ed esterna) che congiungendosi in alcuni punti formano i pori nucleari attraverso
Reazione prossima all equilibrio Molto rapida. Trioso-fosfato isomerasi
 5 a reazione Delle 2 molecole prodotte dalla scissione del fruttosio 1,6-bisfosfato solo la gliceraldeide 3-P è il substrato della successiva reazione della glicolisi, perciò il diidrossiacetonefosfato
5 a reazione Delle 2 molecole prodotte dalla scissione del fruttosio 1,6-bisfosfato solo la gliceraldeide 3-P è il substrato della successiva reazione della glicolisi, perciò il diidrossiacetonefosfato
Catabolismo di proteine
 Catabolismo di proteine Digestione di proteine dalla dieta Turn-over di proteine endogene Digiuno prolungato DIGESTIONE DI PROTEINE ESOGENE L organismo ricava la maggior parte degli aminoacidi di cui ha
Catabolismo di proteine Digestione di proteine dalla dieta Turn-over di proteine endogene Digiuno prolungato DIGESTIONE DI PROTEINE ESOGENE L organismo ricava la maggior parte degli aminoacidi di cui ha
Esempi di quiz di biochimica. 1. E un disaccaride: A) galattosio B) lattosio C) cellulosa D) fruttosio
 Esempi di quiz di biochimica 1. E un disaccaride: A) galattosio B) lattosio C) cellulosa D) fruttosio 2. Il glicogeno è un: A) disaccaride B) polisaccaride C) monosaccaride D) amino zucchero 3. E un composto
Esempi di quiz di biochimica 1. E un disaccaride: A) galattosio B) lattosio C) cellulosa D) fruttosio 2. Il glicogeno è un: A) disaccaride B) polisaccaride C) monosaccaride D) amino zucchero 3. E un composto
Nucleotidi e acidi nucleici
 Nucleotidi e acidi nucleici ACIDI NUCLEICI Biomolecole fondamentali per tutti gli organismi viventi Unici nella capacità di autoduplicazione Conservazione e trasmissione da una generazione all altra dell
Nucleotidi e acidi nucleici ACIDI NUCLEICI Biomolecole fondamentali per tutti gli organismi viventi Unici nella capacità di autoduplicazione Conservazione e trasmissione da una generazione all altra dell
