Lezione 2. Atomi, Molecole e Ioni
|
|
|
- Giorgio Crippa
- 5 anni fa
- Visualizzazioni
Transcript
1 2018 Lezione 2. Atomi, Molecole e Ioni
2 Teoria Atomica di Dalton (1808) 1. Gli elementi sono composti da particelle estremamente piccole, gli atomi. 2. Tutti gli atomi di un certo elemento sono identici. Hanno la stessa dimensione, massa e proprietà chimiche. Gli atomi di un elemento differiscono da quelli degli altri elementi. 3. I composti sono costituiti da atomi di differenti elementi. Gli atomi che li costituiscono sono sempre presenti in un rapporto numerico definito. 4. Una reazione chimica comporta una differente associazione/combinazione di atomi, non la loro creazione o distruzione. 2
3 Teoria Atomica di Dalton Legge delle proporzioni multiple 3
4 Legge di Conservazione della Massa 16 X + 8 Y 8 X 2 Y 4
5 Tubo a Raggi Catodici J.J. Thomson, misura il rapporto massa/carica dell elettrone e - (1906 Premio Nobel per la Fisica) 5
6 Tubo a Raggi Catodici 6
7 Esperimento di Millikan Misura la massa di e Premio Nobel per la Fisica Carica dell elettrone e - = x C Rapporto carica/massa dell elettrone = x 10 8 C/g Massa dell elettrone = 9.10 x g 7
8 Radioattività I nuclei di molti isotopi che si trovano in natura decadono spontaneamente emettendo particelle alfa, beta o raggi gamma 8
9 Esperimento di Rutherford 9
10 Esperimento di Rutherford (1908 Premio Nobel per la Chimica) velocità particelle ~ 1.4 x 10 7 m/s (~5% velocità della luce ) 1. La carica positiva è concentrata nel nucleo 2. I protoni (p) hanno carica opposta (+) a quella degli elettroni (-) 3. La massa di p è 1840 volte la massa di un e - (1.67 x g) 10
11 Modello dell atomo di Rutherford Tutta la massa di un atomo è concentrata nel suo centro occupando un volume molto piccolo raggio atomico ~ 100 pm = 1 x m raggio nucleare ~ 5 x 10-3 pm = 5 x m
12 Chadwick s Experiment (1932) (1935 Noble Prize in Physics) H atoms - 1 p; He atoms - 2 p mass He/mass H should = 2 measured mass NO He/mass H = Be 1 n + 12 C + energy neutron (n) is neutral (charge = 0) n mass ~ p mass = 1.67 x g 12
13 Proprietà delle particelle subatomiche massa p massa n 1840 x massa e - 13
14 Numero Atomico, Numero di Massa e Isotopi Numero Atomico (Z) = numero di protoni nel nucleo Numero di Massa (A) = numero di protoni + numero di neutroni = numero atomico (Z) + numero di neutroni Isotopi sono atomi di uno stesso elemento (X) aventi un differente numero di neutroni nei loro nuclei Numero di Massa Numero Atomico A Z X Simbolo dell elemento 1 H 2 1 1H (D) 1H (T) U U
15 Gli Isotopi dell Idrogeno idrogeno deuterio trizio 15
16 esempi Quanti protoni, neutroni, ed elettroni ci sono nel 14 6 C? 6 protoni, 8 (14-6) neutroni, 6 elettroni Quanti protoni, neutroni, ed elettroni ci sono nel 11 6 C? 6 protoni, 5 (11-6) neutroni, 6 elettroni 16
17 La Tavola Periodica degli Elementi Metalli alcalini Metalli alcalino terrosi Periodo Gruppo Alogeni Gas nobili 17
18 Abbondanza naturale degli elementi chimici Nella crosta terrestre Nel corpo umano 18
19 Una molecola è un aggregato di due o più atomi uniti fra loro da legami chimici H 2 H 2 O NH 3 CH 4 Una molecola biatomica è costituita da due atomi H 2, N 2, O 2, Br 2, HCl, CO diatomic elements Una molecola poliatomica è costituita da più di due atomi O 3, H 2 O, NH 3, CH 4 19
20 Uno ione è un atomo, o un gruppo di atomi, che possiede una carica netta positiva, o negativa. Quando un atomo neutro perde uno o più elettroni diventa un catione. Na 11 protoni 11 elettroni Na + 11 protoni 10 elettroni Quando un atomo neutro acquista uno o più elettroni diventa un anione. Cl 17 protoni 17 elettroni Cl - 17 protoni 18 elettroni 20
21 Uno ione monoatomico contiene solo un atomo Na +, Cl -, Ca 2+, O 2-, Al 3+, N 3- Uno ione poliatomico contiene più di un atomo OH -, CN -, NH 4+, NO 3-21
22 Gli Ioni più comuni e loro posizione nella Tavola Periodica 22
23 esempi Quanti protoni ed elettroni sono presenti 27 13Al protoni, 10 elettroni (13 3) Quanti protoni ed elettroni sono presenti Se 34 protoni, 36 (34 + 2) elettroni 23
24 Formule e Rappresentazione delle Molecole 24
25 La formula molecolare indica il numero dei differenti atomi presenti in una molecola La formula empirica è la più semplice formula chimica che si può scrivere per un composto molecolare H 2 O C 6 H 12 O 6 O 3 empirica H 2 O CH 2 O O N 2 H 4 NH 2 25
26 I composti ionici sono formati da cationi ed anioni La formula è la medesima della formula empirica La somma delle cariche dovute ai cationi è pari a quella dovuta agli anioni Il composto ionico NaCl 26
27 NO The most reactive metals (green) and the most reactive nonmetals (blue) combine to form ionic compounds. 27
28 Formula dei Composti Ionici 2 x +3 = +6 3 x -2 = -6 Al 2 O 3 Al 3+ O 2-1 x +2 = +2 2 x -1 = -2 CaBr 2 Ca 2+ Br - 1 x +2 = +2 1 x -2 = -2 Na 2 CO 3 Na + CO
29 Un acido può essere definito come una sostanza che libera ioni (H + ) quando viene disciolta in acqua. Per esempio: HCl gassoso e HCl in acqua Fase gassosa (molecola di HCl) In acqua, (H 3 O + e Cl ) (ioni idronio e cloruro) 29
30 Idracidi 30
31 Un ossoacido è un acido che contiene idrogeno, ossigeno e un non-metallo HNO 3 Acido nitrico H 2 CO 3 Acido carbonico H 3 PO 4 Acido fosforico 31
32 Ossiacidi e relativi anioni che contengono atomi di cloro Acido Anione HClO 4 (acido perclorico) ClO 4 (perclorato) HClO 3 (acido clorico) ClO 3 (clorato) HClO 2 (acido cloroso) ClO 2 (clorito) HClO (acido ipocloroso) ClO (ipoclorito) 32
33 Una base è una sostanza che disciolta in acqua libera ioni idrossido (OH - ). NaOH KOH Ba(OH) 2 Idrossido di sodio Idrossido di potassio Idrossido di bario 33
34 Gli Idrati sono composti che contengono un certo numero di molecole d acqua. BaCl 2 2H 2 O LiCl H 2 O MgSO 4 7H 2 O Sr(NO 3 ) 2 4H 2 O Cloruro di bario diidrato Cloruro di litio monoidrato Solfato di magnesio eptaidrato Nitrato di stronzio tetraidrato CuSO 4 5H 2 O CuSO 4 34
35 Nomenclatura composti inorganici Sono due i principali sistemi di nomenclatura: - IUPAC (International Union of Pure and Applied Chemistry), più razionale mette in evidenza i vari atomi di ciascun composto -TRADIZIONALE che mette in evidenza la distinzione tra metalli e non metalli
36 esempi
37
Atomi, Molecole e Ioni Lezione 2
 2017 Atomi, Molecole e Ioni Lezione 2 Teoria Atomica 1. Gli elementi sono composti da particelle estremamente piccole, gli atomi. 2. Tutti gli atomi di un certo elemento sono identici. Hanno la stessa
2017 Atomi, Molecole e Ioni Lezione 2 Teoria Atomica 1. Gli elementi sono composti da particelle estremamente piccole, gli atomi. 2. Tutti gli atomi di un certo elemento sono identici. Hanno la stessa
Atomi, Molecole e Ioni. Capitolo 2
 Atomi, Molecole e Ioni Capitolo 2 La Teoria Atomica di Dalton (1808) 1. Gli Elementi sono composti da particelle estremamente piccole, denominate atomi. 2. Tutti gli atomi di un dato elemento sono identici
Atomi, Molecole e Ioni Capitolo 2 La Teoria Atomica di Dalton (1808) 1. Gli Elementi sono composti da particelle estremamente piccole, denominate atomi. 2. Tutti gli atomi di un dato elemento sono identici
Scienziati in Erba Chimica
 Scienziati in Erba Chimica Acqua Oro Zucchero L atomo Acqua Oro Zucchero La Teoria Atomica di Dalton (1808) 1. Gli Elementi sono composti da particelle estremamente piccole, denominate atomi. 2. Tutti
Scienziati in Erba Chimica Acqua Oro Zucchero L atomo Acqua Oro Zucchero La Teoria Atomica di Dalton (1808) 1. Gli Elementi sono composti da particelle estremamente piccole, denominate atomi. 2. Tutti
Scienziati in Erba Chimica
 Scienziati in Erba Chimica Acqua Oro Zucchero La Chimica ü ü ü ü ü ü ü ü ü ü Cosa studia la chimica? Classificazione della materia Stati della materia Formule chimiche Atomo Tavola periodica degli elementi
Scienziati in Erba Chimica Acqua Oro Zucchero La Chimica ü ü ü ü ü ü ü ü ü ü Cosa studia la chimica? Classificazione della materia Stati della materia Formule chimiche Atomo Tavola periodica degli elementi
La Vita è una Reazione Chimica
 La Vita è una Reazione Chimica Acqua Oro Zucchero La vita è una reazione chimica ü ü ü ü ü ü ü ü ü ü Cosa studia la chimica? Classificazione della materia Stati della materia Formule chimiche Atomo Tavola
La Vita è una Reazione Chimica Acqua Oro Zucchero La vita è una reazione chimica ü ü ü ü ü ü ü ü ü ü Cosa studia la chimica? Classificazione della materia Stati della materia Formule chimiche Atomo Tavola
Atomi, ioni e molecole. atomo e particelle subatomiche. tavola periodica degli elementi. composti covalenti. nomenclatura & formule
 Atomi, ioni e molecole atomo e particelle subatomiche tavola periodica degli elementi composti ionici composti covalenti nomenclatura & formule Particelle subatomiche particella massa assoluta carica assoluta
Atomi, ioni e molecole atomo e particelle subatomiche tavola periodica degli elementi composti ionici composti covalenti nomenclatura & formule Particelle subatomiche particella massa assoluta carica assoluta
Atomi, molecole e ioni
 Atomi, molecole e ioni anione + - catione Teoria atomica di Dalton 1. Un elemento è composto da particelle minuscole chiamate atomi. 2. In una normale reazione chimica, nessun atomo di nessun elemento
Atomi, molecole e ioni anione + - catione Teoria atomica di Dalton 1. Un elemento è composto da particelle minuscole chiamate atomi. 2. In una normale reazione chimica, nessun atomo di nessun elemento
Il numero di ossidazione
 Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
LA TEORIA ATOMICA E L ATOMO Da pagina 81 a pagina 107
 LA TEORIA ATOMICA E L ATOMO Da pagina 81 a pagina 107 4.1 LA TEORIA ATOMICA La materia è formata da atomi, a loro volta costituiti da particelle subatomiche; Esistono tanti tipi di atomi quanti sono gli
LA TEORIA ATOMICA E L ATOMO Da pagina 81 a pagina 107 4.1 LA TEORIA ATOMICA La materia è formata da atomi, a loro volta costituiti da particelle subatomiche; Esistono tanti tipi di atomi quanti sono gli
CLASSIFICAZIONE E NOMENCLATURA DEI COMPOSTI CHIMICI
 CLASSIFICAZIONE E NOMENCLATURA DEI COMPOSTI CHIMICI Valenza e numero di ossidazione La capacità di combinazione di un elemento è chiamata valenza, e corrisponde al numero di legami che un atomo di quell
CLASSIFICAZIONE E NOMENCLATURA DEI COMPOSTI CHIMICI Valenza e numero di ossidazione La capacità di combinazione di un elemento è chiamata valenza, e corrisponde al numero di legami che un atomo di quell
Corso di CHIMICA LEZIONE 1
 Corso di CHIMICA LEZIONE 1 MATERIA tutto ciò occupa spazio e ha massa si presenta in natura sottoforma di Miscugli: sostanze mescolate insieme in vario modo (rocce, acqua marina, aria, cellule) Sostanze
Corso di CHIMICA LEZIONE 1 MATERIA tutto ciò occupa spazio e ha massa si presenta in natura sottoforma di Miscugli: sostanze mescolate insieme in vario modo (rocce, acqua marina, aria, cellule) Sostanze
Il numero di ossidazione
 Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
Il numero di ossidazione
 Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
Chimica Generale ed Inorganica
 Chimica Generale ed Inorganica Chimica Generale prof. Dario Duca H 2 O, CO, CO 2 MgO legge di conservazione della massa Lavoisier legge della composizione costante Proust teoria atomica di Dalton i) gli
Chimica Generale ed Inorganica Chimica Generale prof. Dario Duca H 2 O, CO, CO 2 MgO legge di conservazione della massa Lavoisier legge della composizione costante Proust teoria atomica di Dalton i) gli
CHIMICA: studio della composizione e della struttura della materia e delle sue trasformazioni
 CHIMICA: studio della composizione e della struttura della materia e delle sue trasformazioni composto materia sostanza pura miscela omogenea elemento eterogenea Elementi, Composti e Miscele Miscela eterogenea
CHIMICA: studio della composizione e della struttura della materia e delle sue trasformazioni composto materia sostanza pura miscela omogenea elemento eterogenea Elementi, Composti e Miscele Miscela eterogenea
Stati di Aggregazione e Composizione - elementi atomo - composti - miscele omo- ed eterogenee L Atomo - particelle subatomiche e proprietà - Numero
 1. La Materia Stati di Aggregazione e Composizione - elementi atomo - composti - miscele omo- ed eterogenee L Atomo - particelle subatomiche e proprietà - Numero Atomico e Numero di Massa Gli Isotopi La
1. La Materia Stati di Aggregazione e Composizione - elementi atomo - composti - miscele omo- ed eterogenee L Atomo - particelle subatomiche e proprietà - Numero Atomico e Numero di Massa Gli Isotopi La
2 HCl. H 2 + Cl 2 ATOMI E MOLECOLE. Ipotesi di Dalton
 Ipotesi di Dalton ATOMI E MOLECOLE 1.! Un elemento è formato da particelle indivisibili chiamate atomi. 2.! Gli atomi di uno specifico elemento hanno proprietà identiche. 3.! Gli atomi si combinano secondo
Ipotesi di Dalton ATOMI E MOLECOLE 1.! Un elemento è formato da particelle indivisibili chiamate atomi. 2.! Gli atomi di uno specifico elemento hanno proprietà identiche. 3.! Gli atomi si combinano secondo
Diametro del nucleo: m. Diametro dell atomo: m
 Diametro del nucleo: 10 15 m Diametro dell atomo: 10 9-10 10 m The nuclear atom Thomson (Premio Nobel per la Fisica nel 1907) scopre l elettrone nel 1897 Rutherford (Premio Nobel per la Chimica nel 1908)
Diametro del nucleo: 10 15 m Diametro dell atomo: 10 9-10 10 m The nuclear atom Thomson (Premio Nobel per la Fisica nel 1907) scopre l elettrone nel 1897 Rutherford (Premio Nobel per la Chimica nel 1908)
Atomi, molecole e ioni
 Atomi, molecole e ioni anione + - catione Teoria atomica di Dalton 1. Un elemento è composto da particelle minuscole chiamate atomi. 2. In una normale reazione chimica, nessun atomo di nessun elemento
Atomi, molecole e ioni anione + - catione Teoria atomica di Dalton 1. Un elemento è composto da particelle minuscole chiamate atomi. 2. In una normale reazione chimica, nessun atomo di nessun elemento
Numero di ossidazione
 Numero di ossidazione Si definisce numero di ossidazione la carica elettrica che l elemento assume in un composto se si pensa di associare gli elettroni di ciascun legame all atomo considerato più elettronegativo
Numero di ossidazione Si definisce numero di ossidazione la carica elettrica che l elemento assume in un composto se si pensa di associare gli elettroni di ciascun legame all atomo considerato più elettronegativo
Classificazione e nomenclatura dei composti
 Classificazione e nomenclatura dei composti I nomi delle sostanze La nomenclatura chimica è regolamentata da un associazione internazionale: la IUPAC (International Union of Pure and Applied Chemistry):
Classificazione e nomenclatura dei composti I nomi delle sostanze La nomenclatura chimica è regolamentata da un associazione internazionale: la IUPAC (International Union of Pure and Applied Chemistry):
NUMERO DI OSSIDAZIONE Es. HCl H + Cl - H = +1 Cl = -1 H 2. O 2 H + O 2- H = +1 O = -2 Es. NaCl Na + Cl - Na = +1 Cl = -1
 NUMERO DI OSSIDAZIONE Es. HCl H + Cl - H = +1 Cl = -1 H 2 O 2 H + O 2- H = +1 O = -2 Es. NaCl Na + Cl - Na = +1 Cl = -1 Es. H-H, O=O, Cu, Fe N OX = 0 H: +1, (tranne che negli idruri metallici es. NaH:
NUMERO DI OSSIDAZIONE Es. HCl H + Cl - H = +1 Cl = -1 H 2 O 2 H + O 2- H = +1 O = -2 Es. NaCl Na + Cl - Na = +1 Cl = -1 Es. H-H, O=O, Cu, Fe N OX = 0 H: +1, (tranne che negli idruri metallici es. NaH:
C Ca Ce Cf Co Cr Cs Cu
 Elementi Composti ionici (forze elettrostatiche, edifici ionici) molecolari (ripetersi periodico di molecole) Simboli C Ca Ce Cf Co Cr Cs Cu Formule Indici H 2 SO 4 CO 2 H 2 O N 2 Na 2 CO 3 O 2 Mg(NO 3
Elementi Composti ionici (forze elettrostatiche, edifici ionici) molecolari (ripetersi periodico di molecole) Simboli C Ca Ce Cf Co Cr Cs Cu Formule Indici H 2 SO 4 CO 2 H 2 O N 2 Na 2 CO 3 O 2 Mg(NO 3
gruppo ELEMENTI periodo
 gruppo ELEMENTI periodo METALLI NON-METALLI Metalli: duttili, malleabili, conducono corrente elettrica e calore, sono lucenti. Se un elemento non possiede nessuna delle proprietà sopra elencate è
gruppo ELEMENTI periodo METALLI NON-METALLI Metalli: duttili, malleabili, conducono corrente elettrica e calore, sono lucenti. Se un elemento non possiede nessuna delle proprietà sopra elencate è
NUMERO DI OSSIDAZIONE E NOMENCLATURA
 NUMERO DI OSSIDAZIONE E NOMENCLATURA NOMENCLATURA Lo scopo della nomenclatura è fornire regole per individuare un composto, attribuendogli in modo univoco e chiaro un nome preciso ed una formula. Nomenclatura
NUMERO DI OSSIDAZIONE E NOMENCLATURA NOMENCLATURA Lo scopo della nomenclatura è fornire regole per individuare un composto, attribuendogli in modo univoco e chiaro un nome preciso ed una formula. Nomenclatura
CHIMICA: studio della composizione e della struttura della materia e delle sue trasformazioni
 CHIMICA: studio della composizione e della struttura della materia e delle sue trasformazioni Lavoisier e la legge di conservazione della massa Lavoisier riconobbe l importanza delle misurazioni accurate
CHIMICA: studio della composizione e della struttura della materia e delle sue trasformazioni Lavoisier e la legge di conservazione della massa Lavoisier riconobbe l importanza delle misurazioni accurate
CLASSIFICAZIONE, NOMENCLATURA E FORMULE DEI COMPOSTI INORGANICI
 CLASSIFICAZIONE, NOMENCLATURA E FORMULE DEI COMPOSTI INORGANICI La VALENZA di un elemento è data dal numero di elettroni che esso deve perdere, o acquistare, o mettere in comune con uno o più atomi in
CLASSIFICAZIONE, NOMENCLATURA E FORMULE DEI COMPOSTI INORGANICI La VALENZA di un elemento è data dal numero di elettroni che esso deve perdere, o acquistare, o mettere in comune con uno o più atomi in
LA NOMENCLATURA LA VALENZA
 LA NOMENCLATURA LA VALENZA La valenza è la tendenza di un elemento a legarsi con uno o più elementi Si prendono come riferimento: l'idrogeno è l'elemento più leggero l'ossigeno riesce a combinarsi con
LA NOMENCLATURA LA VALENZA La valenza è la tendenza di un elemento a legarsi con uno o più elementi Si prendono come riferimento: l'idrogeno è l'elemento più leggero l'ossigeno riesce a combinarsi con
Elementi e composti Pesi atomici e pesi molecolari Mole e massa molare
 Elementi e composti Pesi atomici e pesi molecolari Mole e massa molare 2 a lezione 17 ottobre 2016 Elementi ed atomi Una sostanza viene definita «elemento» quando non è scomponibile in altre sostanze Un
Elementi e composti Pesi atomici e pesi molecolari Mole e massa molare 2 a lezione 17 ottobre 2016 Elementi ed atomi Una sostanza viene definita «elemento» quando non è scomponibile in altre sostanze Un
Loriano Storchi.
 Loriano Storchi loriano@storchi.org http://www.storchi.org/ Metodo scientifico Nessuna quantità di esperimenti potrà dimostrare che ho ragione; un unico esperimento potrà dimostrare che ho sbagliato Il
Loriano Storchi loriano@storchi.org http://www.storchi.org/ Metodo scientifico Nessuna quantità di esperimenti potrà dimostrare che ho ragione; un unico esperimento potrà dimostrare che ho sbagliato Il
Verifica di chimica su: Atomo, tavola periodica, legame chimico Nome cognome data classe
 1 Verifica di chimica su: Atomo, tavola periodica, legame chimico Nome cognome data classe 21) Quanti neutroni, protoni ed elettroni ha l elemento con numero atomico Z = 23 e numero di massa A = 51? P=23,
1 Verifica di chimica su: Atomo, tavola periodica, legame chimico Nome cognome data classe 21) Quanti neutroni, protoni ed elettroni ha l elemento con numero atomico Z = 23 e numero di massa A = 51? P=23,
NUMERO DI OSSIDAZIONE Es. HCl H + Cl - H = +1 Cl = -1 H 2. O 2 H + O 2- H = +1 O = -2 Es. NaCl Na + Cl - Na = +1 Cl = -1
 NUMERO DI OSSIDAZIONE Es. HCl H + Cl - H = +1 Cl = -1 H 2 O 2 H + O 2- H = +1 O = -2 Es. NaCl Na + Cl - Na = +1 Cl = -1 Es. H-H, O=O, Cu, Fe = 0 H: +1, (tranne che negli idruri metallici es. NaH 1) O:
NUMERO DI OSSIDAZIONE Es. HCl H + Cl - H = +1 Cl = -1 H 2 O 2 H + O 2- H = +1 O = -2 Es. NaCl Na + Cl - Na = +1 Cl = -1 Es. H-H, O=O, Cu, Fe = 0 H: +1, (tranne che negli idruri metallici es. NaH 1) O:
NOMENCLATURA. Nomenclatura = Metodo sistematico di assegnazione dei nomi Composti formati da carbonio e idrogeno + ossigeno, azoto = composti organici
 NOMENCLATURA Nomenclatura = Metodo sistematico di assegnazione dei nomi Composti formati da carbonio e idrogeno + ossigeno, azoto = composti organici Nomenclatura dei composti inorganici 1Formule Per rappresentare
NOMENCLATURA Nomenclatura = Metodo sistematico di assegnazione dei nomi Composti formati da carbonio e idrogeno + ossigeno, azoto = composti organici Nomenclatura dei composti inorganici 1Formule Per rappresentare
Corso di chimica generale
 Corso di chimica generale Dr. Riccardo Montioli Email: riccardo.montioli@univr.it Programma - La materia e l energia - Le particelle subatomiche e la misura della massa - L atomo, teorie e struttura -
Corso di chimica generale Dr. Riccardo Montioli Email: riccardo.montioli@univr.it Programma - La materia e l energia - Le particelle subatomiche e la misura della massa - L atomo, teorie e struttura -
NOMENCLATURA E REAZIONI
 NOMENCLATURA E REAZIONI Gli elementi chimici si dividono in: METALLI e NON METALLI I METALLI, perdendo elettroni, originano IONI POSITIVI (o CATIONI) I NON METALLI, acquistando elettroni, originano IONI
NOMENCLATURA E REAZIONI Gli elementi chimici si dividono in: METALLI e NON METALLI I METALLI, perdendo elettroni, originano IONI POSITIVI (o CATIONI) I NON METALLI, acquistando elettroni, originano IONI
NUMERO DI OSSIDAZIONE NOMENCLATURA DEI COMPOSTI INORGANICI
 NOMENCLATURA DEI COMPOSTI INORGANICI Formula chimica: indica la natura degli atomi che costituiscono un composto (mediante i loro simboli) ed il rapporto con cui tali atomi sono combinati tra loro Nome:
NOMENCLATURA DEI COMPOSTI INORGANICI Formula chimica: indica la natura degli atomi che costituiscono un composto (mediante i loro simboli) ed il rapporto con cui tali atomi sono combinati tra loro Nome:
Capitolo 13 Classificazione e nomenclatura dei composti
 Capitolo 13 Classificazione e nomenclatura dei composti 1. I nomi delle sostanze 2. Valenza e numero di ossidazione 3. Leggere e scrivere le formule più semplici 4. La classificazione dei composti inorganici
Capitolo 13 Classificazione e nomenclatura dei composti 1. I nomi delle sostanze 2. Valenza e numero di ossidazione 3. Leggere e scrivere le formule più semplici 4. La classificazione dei composti inorganici
Gli elementi presenti in natura sono 120, di cui:
 Gli elementi presenti in natura sono 120, di cui: 92 naturali 18 prodotti artificialmente 4 incerti poiché non ne è stata provata l'esistenza a causa della loro brevissima vita 3 ipotetici 3 scoperti nel
Gli elementi presenti in natura sono 120, di cui: 92 naturali 18 prodotti artificialmente 4 incerti poiché non ne è stata provata l'esistenza a causa della loro brevissima vita 3 ipotetici 3 scoperti nel
Esercizi di. Stechiometria dei composti. mercoledì 9 dicembre 2015
 Esercizi di Stechiometria dei composti mercoledì 9 dicembre 2015 Il cloro ha due isotopi stabili contenenti rispettivamente 18 e 20 neutroni. Utilizzando la tavola periodica degli elementi, scrivere i
Esercizi di Stechiometria dei composti mercoledì 9 dicembre 2015 Il cloro ha due isotopi stabili contenenti rispettivamente 18 e 20 neutroni. Utilizzando la tavola periodica degli elementi, scrivere i
Legame metallico + + + + + + + + Elettroni di valenza + + + + Ioni Na +, Be 2+, K + etc + + + +
 Legame metallico I metalli presentano elevata conducibilità termica ed elettrica e possono subire deformazioni permanenti più facilmente dei solidi ionici. Tali proprietà fisiche sono spiegate dalla natura
Legame metallico I metalli presentano elevata conducibilità termica ed elettrica e possono subire deformazioni permanenti più facilmente dei solidi ionici. Tali proprietà fisiche sono spiegate dalla natura
CAPITOLO 0 IL LESSICO DELLA CHIMICA
 CAPITOLO 0 IL LESSICO DELLA CHIMICA 0.1 (a) Chimica. (b) Chimica. (c) Fisica. (d) Fisica. (e) Chimica. 0.3 La terra è una miscela eterogenea di minerali e materia organica. L aria è una miscela omogenea
CAPITOLO 0 IL LESSICO DELLA CHIMICA 0.1 (a) Chimica. (b) Chimica. (c) Fisica. (d) Fisica. (e) Chimica. 0.3 La terra è una miscela eterogenea di minerali e materia organica. L aria è una miscela omogenea
Il modello strutturale dell atomo
 Il modello strutturale dell atomo Gli atomi sono costituiti dal nucleo e dagli elettroni Proprietà dell atomo dipendono dal nucleo (fisica nucleare) e dagli elettroni (chimica). Il nucleo contiene protoni
Il modello strutturale dell atomo Gli atomi sono costituiti dal nucleo e dagli elettroni Proprietà dell atomo dipendono dal nucleo (fisica nucleare) e dagli elettroni (chimica). Il nucleo contiene protoni
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 12 Classificazione e nomenclatura dei composti 1. I nomi delle sostanze 2. Valenza e numero
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 12 Classificazione e nomenclatura dei composti 1. I nomi delle sostanze 2. Valenza e numero
Sono gli atomi indivisibili?
 Sono gli atomi indivisibili? L atomo è la particella più piccola di un elemento che possiede tutte le caratteristiche chimiche dell elemento stesso. Sono noti 112 elementi o specie atomiche diverse (90
Sono gli atomi indivisibili? L atomo è la particella più piccola di un elemento che possiede tutte le caratteristiche chimiche dell elemento stesso. Sono noti 112 elementi o specie atomiche diverse (90
Chimica Generale ed Inorganica
 Chimica Generale ed Inorganica Chimica Generale prof. Dario Duca Cristalli blu di solfato di rame CH 3 COOH composti molecolari coefficienti stechiometrici C 2 H 2 - CH C 2 H 4 - CH 2 C 2 H 6 - CH 3 CH
Chimica Generale ed Inorganica Chimica Generale prof. Dario Duca Cristalli blu di solfato di rame CH 3 COOH composti molecolari coefficienti stechiometrici C 2 H 2 - CH C 2 H 4 - CH 2 C 2 H 6 - CH 3 CH
CHIMICA Dagli atomi alla trasformazioni NOMI E FORMULE DEI COMPOSTI
 CHIMICA Dagli atomi alla trasformazioni NOMI E FORMULE DEI COMPOSTI Numero di ossidazione Il numero di ossidazione di un atomo in un composto rappresenta la carica (+ o -) che l atomo assumerebbe se gli
CHIMICA Dagli atomi alla trasformazioni NOMI E FORMULE DEI COMPOSTI Numero di ossidazione Il numero di ossidazione di un atomo in un composto rappresenta la carica (+ o -) che l atomo assumerebbe se gli
Capitolo 3: I Composti Chimici
 Capitolo 3: I Composti Chimici FORMULA CHIMICA E' una notazione che usa i simboli atomici con dei numeri a pedice per indicare le quantità relative degli elementi che costituiscono la sostanza. NaCl 1:1
Capitolo 3: I Composti Chimici FORMULA CHIMICA E' una notazione che usa i simboli atomici con dei numeri a pedice per indicare le quantità relative degli elementi che costituiscono la sostanza. NaCl 1:1
Università degli studi di MILANO Facoltà di AGRARIA. El. di Chimica e Chimica Fisica. Mod. 1 CHIMICA. Mod. 2 CHIMICA FISICA.
 Università degli studi di MILANO Facoltà di AGRARIA El. di Chimica e Chimica Fisica Mod. 1 CHIMICA Mod. 2 CHIMICA FISICA Lezione 4 Anno Accademico 2010-2011 Docente: Dimitrios Fessas Si riconoscono così
Università degli studi di MILANO Facoltà di AGRARIA El. di Chimica e Chimica Fisica Mod. 1 CHIMICA Mod. 2 CHIMICA FISICA Lezione 4 Anno Accademico 2010-2011 Docente: Dimitrios Fessas Si riconoscono così
Precorsi Test AMMISSIONE Medicina e Chirurgia - Professioni Sanitarie Università degli Studi di Perugia. Massa atomica MOLE. a.a.
 Precorsi Test AMMISSIONE Medicina e Chirurgia - Professioni Sanitarie Università degli Studi di Perugia Massa atomica MOLE a.a. 2016-17 MATERIA costituita da ATOMI Miscele OMOGENEE o soluzioni Hanno la
Precorsi Test AMMISSIONE Medicina e Chirurgia - Professioni Sanitarie Università degli Studi di Perugia Massa atomica MOLE a.a. 2016-17 MATERIA costituita da ATOMI Miscele OMOGENEE o soluzioni Hanno la
Esercitazioni di Elementi di Chimica. Modulo 2 Struttura della Materia
 Esercitazioni di Elementi di Chimica Modulo 2 Struttura della Materia Esempi di quiz a risposta multipla e questionari a completamento L esame finale sarà composto da problemi simili Qual è lo stato fisico
Esercitazioni di Elementi di Chimica Modulo 2 Struttura della Materia Esempi di quiz a risposta multipla e questionari a completamento L esame finale sarà composto da problemi simili Qual è lo stato fisico
Simulazioni del Test di Accesso Macroarea Scientifico-Tecnologica - Domande di Chimica -
 Simulazioni del Test di Accesso Macroarea Scientifico-Tecnologica - Domande di Chimica - C1) ll numero atomico di un elemento rappresenta: a) il numero di elettroni b) il numero di protoni c) la somma
Simulazioni del Test di Accesso Macroarea Scientifico-Tecnologica - Domande di Chimica - C1) ll numero atomico di un elemento rappresenta: a) il numero di elettroni b) il numero di protoni c) la somma
Principio dell Aufbau (riempimento)
 LA TABELLA PERIODICA DEGLI ELEMENTI Principio dell Aufbau (riempimento) Schema semplificato dei livelli energetici atomici Distribuzione energetica reale dei livelli energetici atomici 7p Schema empirico
LA TABELLA PERIODICA DEGLI ELEMENTI Principio dell Aufbau (riempimento) Schema semplificato dei livelli energetici atomici Distribuzione energetica reale dei livelli energetici atomici 7p Schema empirico
PRIMO ESONERO DI CHIMICA sessione A - 10/11/2011
 PRIMO ESONERO DI CHIMICA sessione A - 10/11/2011 TRACCIA A1 TRACCIA A2 1. (7 p.ti) Un campione contiene 10 g di Al 2 O 3 e 10 g di CaO. Qual è la percentuale in peso dell O nella miscela? Quale la sua
PRIMO ESONERO DI CHIMICA sessione A - 10/11/2011 TRACCIA A1 TRACCIA A2 1. (7 p.ti) Un campione contiene 10 g di Al 2 O 3 e 10 g di CaO. Qual è la percentuale in peso dell O nella miscela? Quale la sua
Capitolo 13 Classificazione e nomenclatura dei composti
 Capitolo 13 Classificazione e nomenclatura dei composti 1. I nomi delle sostanze 2. Valenza e numero di ossidazione 3. Leggere e scrivere le formule più semplici 4. La classificazione dei composti inorganici
Capitolo 13 Classificazione e nomenclatura dei composti 1. I nomi delle sostanze 2. Valenza e numero di ossidazione 3. Leggere e scrivere le formule più semplici 4. La classificazione dei composti inorganici
Corso di CHIMICA INORGANICA
 Corso di CHIMICA INORGANICA Lezione Seconda La teoria atomica La massa atomica e il concetto di Isotopi Dentro l atomo, le particelle subatomiche La Tavola Periodica degli Elementi 2 Gli atomi di un certo
Corso di CHIMICA INORGANICA Lezione Seconda La teoria atomica La massa atomica e il concetto di Isotopi Dentro l atomo, le particelle subatomiche La Tavola Periodica degli Elementi 2 Gli atomi di un certo
L Atomo Nucleare. Rutherford protoni James Chadwick neutroni 1932
 Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Una formula molecolare mostra l esatto numero degli atomi di ciascun elemento nella più piccola unità di una sostanza
 Formule e Modelli 1 Una formula molecolare mostra l esatto numero degli atomi di ciascun elemento nella più piccola unità di una sostanza Una formula empirica mostra il più piccolo rapporto fra gli atomi
Formule e Modelli 1 Una formula molecolare mostra l esatto numero degli atomi di ciascun elemento nella più piccola unità di una sostanza Una formula empirica mostra il più piccolo rapporto fra gli atomi
Struttura atomica della materia
 Struttura atomica della materia 1 FASE fase 3 fase 1 fase 2 FASE: porzione di materia chimicamente e fisicamente omogenea delimitata da superfici di separazione ben definite 2 Classificazione della materia
Struttura atomica della materia 1 FASE fase 3 fase 1 fase 2 FASE: porzione di materia chimicamente e fisicamente omogenea delimitata da superfici di separazione ben definite 2 Classificazione della materia
Nomenclatura chimica
 Nomenclatura chimica Capitolo 13 Classificazione e nomenclatura dei composti 1. I nomi delle sostanze 2. Valenza e numero di ossidazione 3. Leggere e scrivere le formule più semplici 4. La classificazione
Nomenclatura chimica Capitolo 13 Classificazione e nomenclatura dei composti 1. I nomi delle sostanze 2. Valenza e numero di ossidazione 3. Leggere e scrivere le formule più semplici 4. La classificazione
Capitolo 13 Classificazione e nomenclatura dei composti
 Capitolo 13 Classificazione e nomenclatura dei composti 1. I nomi delle sostanze 2. Valenza e numero di ossidazione 3. Leggere e scrivere le formule più semplici 4. La classificazione dei composti inorganici
Capitolo 13 Classificazione e nomenclatura dei composti 1. I nomi delle sostanze 2. Valenza e numero di ossidazione 3. Leggere e scrivere le formule più semplici 4. La classificazione dei composti inorganici
Esercitazione. Nomenclatura e bilanciamento
 Esercitazione Nomenclatura e bilanciamento Nomenclatura dei composti Lo scopo della nomenclatura è fornire regole per individuare un composto, attribuendogli in modo univoco e chiaro un nome preciso ed
Esercitazione Nomenclatura e bilanciamento Nomenclatura dei composti Lo scopo della nomenclatura è fornire regole per individuare un composto, attribuendogli in modo univoco e chiaro un nome preciso ed
Struttura atomica della materia
 Struttura atomica della materia 1 FASE fase 3 fase 1 fase 2 FASE: porzione di materia chimicamente e fisicamente omogenea delimitata da superfici di separazione ben definite 2 Classificazione della materia
Struttura atomica della materia 1 FASE fase 3 fase 1 fase 2 FASE: porzione di materia chimicamente e fisicamente omogenea delimitata da superfici di separazione ben definite 2 Classificazione della materia
Corso di laurea in Chimica e Tecnologia Farmaceutiche Corso di Chimica Generale e Inorganica CH 3
 Corso di laurea in Chimica e Tecnologia Farmaceutiche Corso di Chimica Generale e Inorganica - LA MATERIA- COOH O O Al(OH) 4 - CH 3 Prof.ssa Ivana Fenoglio I lucidi forniti non sono da utilizzare come
Corso di laurea in Chimica e Tecnologia Farmaceutiche Corso di Chimica Generale e Inorganica - LA MATERIA- COOH O O Al(OH) 4 - CH 3 Prof.ssa Ivana Fenoglio I lucidi forniti non sono da utilizzare come
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 16 Classificazione e nomenclatura dei composti 3 Sommario 1. I nomi delle sostanze 2. Valenza e numero di ossidazione 3. Leggere
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 16 Classificazione e nomenclatura dei composti 3 Sommario 1. I nomi delle sostanze 2. Valenza e numero di ossidazione 3. Leggere
Nomenclatura chimica
 Nomenclatura chimica Capitolo 13 Classificazione e nomenclatura dei composti 1. I nomi delle sostanze 2. Valenza e numero di ossidazione 3. Leggere e scrivere le formule più semplici 4. La classificazione
Nomenclatura chimica Capitolo 13 Classificazione e nomenclatura dei composti 1. I nomi delle sostanze 2. Valenza e numero di ossidazione 3. Leggere e scrivere le formule più semplici 4. La classificazione
NOMENCLATURA DEI COMPOSTI INORGANICI
 QUESTA E UNA SCHEDA DI RECUPERO DEL CORSO DI CHIMICA Per andare avanti usa il mouse OGGI PARLEREMO DI NOMENCLATURA DEI COMPOSTI INORGANICI COME SAI GLI ELEMENTI CHIMICI SONO SUDDIVISI IN DUE CATEGORIE
QUESTA E UNA SCHEDA DI RECUPERO DEL CORSO DI CHIMICA Per andare avanti usa il mouse OGGI PARLEREMO DI NOMENCLATURA DEI COMPOSTI INORGANICI COME SAI GLI ELEMENTI CHIMICI SONO SUDDIVISI IN DUE CATEGORIE
Chimica. Lezione 09/11/2010
 Chimica Lezione 09/11/2010 Se la differenza di elettronegatività ( x) è 1,9 il legame è IONICO Se 0,5 x < 1,9 il legame è covalente polare Se x < 0,5 il legame è covalente puro Massa atomica.. Massa
Chimica Lezione 09/11/2010 Se la differenza di elettronegatività ( x) è 1,9 il legame è IONICO Se 0,5 x < 1,9 il legame è covalente polare Se x < 0,5 il legame è covalente puro Massa atomica.. Massa
Corso propedeutico a chimica generale 2009
 Corso propedeutico a chimica generale 2009 Luigi Cerruti luigi.cerruti@unito.it www.minerva.unito.it Lezioni di chimica 3-4 Unità di misura SI Unità fondamentali Unità di misura SI Unità derivate Gli oggetti
Corso propedeutico a chimica generale 2009 Luigi Cerruti luigi.cerruti@unito.it www.minerva.unito.it Lezioni di chimica 3-4 Unità di misura SI Unità fondamentali Unità di misura SI Unità derivate Gli oggetti
METALLO + OSSIGENO = OSSIDO
 Composti binari I composti inorganici binari possono essere di due tipi: 1. Composti binari con ossigeno (ossidi basici e ossidi acidi o anidridi) 2. Composti binari senza ossigeno Composti binari con
Composti binari I composti inorganici binari possono essere di due tipi: 1. Composti binari con ossigeno (ossidi basici e ossidi acidi o anidridi) 2. Composti binari senza ossigeno Composti binari con
Capitolo 2 Gli atomi, le molecole e gli ioni
 John C. Kotz Paul M. Treichel John Townsend http://academic.cengage.com/kotz Atomi, Molecole, & Ioni 2 Capitolo 2 Gli atomi, le molecole e gli ioni Versione italiana a cura di Giaime Marongiu e Guido Ennas
John C. Kotz Paul M. Treichel John Townsend http://academic.cengage.com/kotz Atomi, Molecole, & Ioni 2 Capitolo 2 Gli atomi, le molecole e gli ioni Versione italiana a cura di Giaime Marongiu e Guido Ennas
Argomenti 2 lezione. Bilanciamento delle reazioni chimiche. Resa teorica e resa effettiva. Esercitazioni di Chimica Generale ed Inorganica 2
 Un composto contenente sodio, cloro e ossigeno ha una percentuale in massa di sodio del 25.42. Se 3.25 g di tale composto forniscono 4.33 x 10 22 atomi di ossigeno, calcolare la formula minima. Na: 25.42
Un composto contenente sodio, cloro e ossigeno ha una percentuale in massa di sodio del 25.42. Se 3.25 g di tale composto forniscono 4.33 x 10 22 atomi di ossigeno, calcolare la formula minima. Na: 25.42
Sommario della lezione 2. Materia e definizioni. Struttura dell atomo
 Sommario della lezione 2 Materia e definizioni Struttura dell atomo La materia è qualsiasi cosa abbia una massa e occupi uno spazio. Esiste in tre stati: Solido Forma e volume determinati Liquido Volume
Sommario della lezione 2 Materia e definizioni Struttura dell atomo La materia è qualsiasi cosa abbia una massa e occupi uno spazio. Esiste in tre stati: Solido Forma e volume determinati Liquido Volume
NUMERO DI OSSIDAZIONE NOMENCLATURA CHIMICA
 NUMERO DI OSSIDAZIONE Il numero di ossidazione di un atomo corrisponde al numero di valenza preceduto da un segno + oppure -. Il segno negativo si assegna all atomo più elettronegativo e il segno + si
NUMERO DI OSSIDAZIONE Il numero di ossidazione di un atomo corrisponde al numero di valenza preceduto da un segno + oppure -. Il segno negativo si assegna all atomo più elettronegativo e il segno + si
VERIFICA FINALE ISTITUTO D ISTRUZIONE SUPERIORE VIRGILIO. Scienziati in erba. Durata della prova: 100 minuti
 VERIFICA FINALE Nome Cognome Classe Sez ISTITUTO D ISTRUZIONE SUPERIORE VIRGILIO SAN GIORGIO DEL SANNIO (BN) Scienziati in erba La prova deve essere consegnata allo scadere del tempo previsto per la sua
VERIFICA FINALE Nome Cognome Classe Sez ISTITUTO D ISTRUZIONE SUPERIORE VIRGILIO SAN GIORGIO DEL SANNIO (BN) Scienziati in erba La prova deve essere consegnata allo scadere del tempo previsto per la sua
Classificazione della materia 3 STATI DI AGGREGAZIONE
 Classificazione della materia MATERIA spazio massa Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (Volume e forma propri) LIQUIDO (Volume definito e forma indefinita) GASSOSO
Classificazione della materia MATERIA spazio massa Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (Volume e forma propri) LIQUIDO (Volume definito e forma indefinita) GASSOSO
Le sostanze chimiche prof. Matteo Scapellato
 1. Fenomeni fisici e fenomeni chimici a) Fenomeno fisico: è una trasformazione che non cambia la natura delle sostanze 1 b) Fenomeno chimico o reazione chimica: è una trasformazione che cambia la natura
1. Fenomeni fisici e fenomeni chimici a) Fenomeno fisico: è una trasformazione che non cambia la natura delle sostanze 1 b) Fenomeno chimico o reazione chimica: è una trasformazione che cambia la natura
Li + O 2 a) Si scrive il composto mettendo prima il metallo e poi l ossigeno
 NOMENCLATURA dei COMPOSTI I composti presenti in natura sono moltissimi perché risultano dalla combinazione dei numerosi elementi riportati dalla Tavola Periodica, ma sono comunque tutti classificabili
NOMENCLATURA dei COMPOSTI I composti presenti in natura sono moltissimi perché risultano dalla combinazione dei numerosi elementi riportati dalla Tavola Periodica, ma sono comunque tutti classificabili
Regole e convenzioni della nomenclatura IUPAC e tradizionale
 Regole e convenzioni della nomenclatura IUPAC e tradizionale Ø Ogni specie chimica viene rappresentata univocamente con una formula e indicata con un nome mediante simboli ed indici numerici che indicano
Regole e convenzioni della nomenclatura IUPAC e tradizionale Ø Ogni specie chimica viene rappresentata univocamente con una formula e indicata con un nome mediante simboli ed indici numerici che indicano
400 a.c. atomismo dei filosofi greci: osservazione continua trasformazione degli oggetti naturali fede nella permanenza delle cose reali
 Teoria atomica 400 a.c. atomismo dei filosofi greci: osservazione continua trasformazione degli oggetti naturali fede nella permanenza delle cose reali IPOTESI: Atomi invisibili costituenti l universo
Teoria atomica 400 a.c. atomismo dei filosofi greci: osservazione continua trasformazione degli oggetti naturali fede nella permanenza delle cose reali IPOTESI: Atomi invisibili costituenti l universo
Chimica. La scienza che studia le trasformazioni della materia. Acqua (ghiaccio) Acqua (Liquido) Trasformazione Fisica
 Nozioni di Base Chimica La scienza che studia le trasformazioni della materia Acqua (ghiaccio) ----- Acqua (Liquido) Trasformazione Fisica Metano + Ossigeno -- Anidride Carbonica + Acqua Trasformazione
Nozioni di Base Chimica La scienza che studia le trasformazioni della materia Acqua (ghiaccio) ----- Acqua (Liquido) Trasformazione Fisica Metano + Ossigeno -- Anidride Carbonica + Acqua Trasformazione
Struttura atomica della materia
 Struttura atomica della materia 1 FASE fase 3 fase 1 fase 2 FASE: porzione di materia chimicamente e fisicamente omogenea delimitata da superfici di separazione ben definite 2 Classificazione della materia
Struttura atomica della materia 1 FASE fase 3 fase 1 fase 2 FASE: porzione di materia chimicamente e fisicamente omogenea delimitata da superfici di separazione ben definite 2 Classificazione della materia
Il legame chimico. Gli atomi sia nelle sostanze elementari che nei composti sono tenuti insieme dai legami chimici
 Il legame chimico Gli atomi sia nelle sostanze elementari che nei composti sono tenuti insieme dai legami chimici Fra due atomi o fra due gruppi di atomi è presente un legame chimico quando l entità che
Il legame chimico Gli atomi sia nelle sostanze elementari che nei composti sono tenuti insieme dai legami chimici Fra due atomi o fra due gruppi di atomi è presente un legame chimico quando l entità che
Reazioni di ossido-riduzione
 Reazioni di ossido-riduzione Secondo la teoria di Bronsted-Lowry le reazioni acido-base possono essere considerate processi di scambio protonico HCl + H 2 O Cl - + H 3 O + Cl H O H H Cl H O H H In questi
Reazioni di ossido-riduzione Secondo la teoria di Bronsted-Lowry le reazioni acido-base possono essere considerate processi di scambio protonico HCl + H 2 O Cl - + H 3 O + Cl H O H H Cl H O H H In questi
STRUTTURA ATOMICA LE PARTICELLE SUBATOMICHE E I PRIMI MODELLI ATOMICI
 STRUTTURA ATOMICA LE PARTICELLE SUBATOMICHE E I PRIMI MODELLI ATOMICI STRUTTURA DELL'ATOMO Vari esperimenti condotti fra la fine del 1800 e l inizio del 1900 dimostrarono che gli atomi non sono indivisibili,
STRUTTURA ATOMICA LE PARTICELLE SUBATOMICHE E I PRIMI MODELLI ATOMICI STRUTTURA DELL'ATOMO Vari esperimenti condotti fra la fine del 1800 e l inizio del 1900 dimostrarono che gli atomi non sono indivisibili,
Gli argomenti trattati
 LEZIONE 1 Struttura della materia e Gli argomenti trattati Composizione della materia materia, sostanze e miscele, elementi e composti Fondamenti di struttura atomica Molecole: formula empirica, formula
LEZIONE 1 Struttura della materia e Gli argomenti trattati Composizione della materia materia, sostanze e miscele, elementi e composti Fondamenti di struttura atomica Molecole: formula empirica, formula
Capitolo 2 ATOMI, MOLECOLE, E IONI
 2.7 Innanzi tutto, converti 1 cm in picometri. Capitolo 2 ATOMI, MOLECOLE, E IONI? atomi di He = = 1 10 8 atomi di He 2.8 Nota che stai calcolando il fattore di conversione da metri a miglia. r atomo =
2.7 Innanzi tutto, converti 1 cm in picometri. Capitolo 2 ATOMI, MOLECOLE, E IONI? atomi di He = = 1 10 8 atomi di He 2.8 Nota che stai calcolando il fattore di conversione da metri a miglia. r atomo =
Classe4:chimicaStrutturaAtomica1. Controlla se sai definire i seguenti termini: teoria atomica di Dalton (atomo di Dalton),
 Classe4:chimicaStrutturaAtomica1. Controlla se sai definire i seguenti termini: teoria atomica di Dalton (atomo di Dalton), particelle subatomiche, protone, neutrone, elettronie, nucleo. 2. Decidi se tra
Classe4:chimicaStrutturaAtomica1. Controlla se sai definire i seguenti termini: teoria atomica di Dalton (atomo di Dalton), particelle subatomiche, protone, neutrone, elettronie, nucleo. 2. Decidi se tra
Atomo La più piccola particella di un elemento che resta inalterata nelle trasformazioni chimiche.
 Atomo La più piccola particella di un elemento che resta inalterata nelle trasformazioni chimiche. Molecola La più piccola particella di un individuo chimico (elemento o composto) capace di una propria
Atomo La più piccola particella di un elemento che resta inalterata nelle trasformazioni chimiche. Molecola La più piccola particella di un individuo chimico (elemento o composto) capace di una propria
CHIMICA E BIOCHIMICA
 CHIMICA E BIOCHIMICA CHIMICA: studia la materia Materia= ogni cosa che ha massa Proprietà Struttura Trasformazioni (Reazioni) BIOCHIMICA: studia la chimica degli organismi viventi Di cosa è composta la
CHIMICA E BIOCHIMICA CHIMICA: studia la materia Materia= ogni cosa che ha massa Proprietà Struttura Trasformazioni (Reazioni) BIOCHIMICA: studia la chimica degli organismi viventi Di cosa è composta la
L Atomo e le Molecole
 L Atomo e le Molecole L atomo L'atomo, la particella che come un mattone costituisce tutta la materia, non è un corpicciolo semplice. Esso è a sua volta composto da particelle elementari piccolissime:
L Atomo e le Molecole L atomo L'atomo, la particella che come un mattone costituisce tutta la materia, non è un corpicciolo semplice. Esso è a sua volta composto da particelle elementari piccolissime:
Chimica generale e inorganica
 Corso di: Chimica generale e inorganica Prof. Roberta Spadaccini rspadacc@unisannio.it Orario di ricevimento: lunedi 16-17 Libri di testo consigliati: Brown-Lemay Fondamenti di chimica EDISES Giannoccaro
Corso di: Chimica generale e inorganica Prof. Roberta Spadaccini rspadacc@unisannio.it Orario di ricevimento: lunedi 16-17 Libri di testo consigliati: Brown-Lemay Fondamenti di chimica EDISES Giannoccaro
Atomo: modello microscopico
 Atomo: modello microscopico 1 Modello atomico di Dalton (1808) Materia è composta di atomi indivisibili e indistruttibili Atomi uguali hanno identica massa e identiche proprietà chimiche Gli atomi non
Atomo: modello microscopico 1 Modello atomico di Dalton (1808) Materia è composta di atomi indivisibili e indistruttibili Atomi uguali hanno identica massa e identiche proprietà chimiche Gli atomi non
struttura atomica della materia La chimica
 Struttura atomica della materia 1 La chimica La chimica è la scienza che si occupa dello studio della composizione e delle proprietà delle varie forme della materia 2 bbvbsxbfxbfx 1 Classificazione della
Struttura atomica della materia 1 La chimica La chimica è la scienza che si occupa dello studio della composizione e delle proprietà delle varie forme della materia 2 bbvbsxbfxbfx 1 Classificazione della
Nomenclatura e aspetti quali-quantitativi unità 1, modulo B del libro unità 1, modulo E del libro
 Nomenclatura e aspetti quali-quantitativi unità 1, modulo B del libro unità 1, modulo E del libro È indispensabile conoscere i nomi dei composti dei primi 30 elementi (da H a Zn), oltre a Ba, Cd, Pb e
Nomenclatura e aspetti quali-quantitativi unità 1, modulo B del libro unità 1, modulo E del libro È indispensabile conoscere i nomi dei composti dei primi 30 elementi (da H a Zn), oltre a Ba, Cd, Pb e
PRINCIPALI CLASSI DI COMPOSTI INORGANICI
 PRINCIPALI CLASSI DI COMPOSTI INORGANICI Idruri Idracidi Ossidi Perossidi Idrossidi Ossoacidi Sali Idruri Sono composti binari dell idrogeno con gli elementi più elettropositivi (metalli) IDRURI Metalli
PRINCIPALI CLASSI DI COMPOSTI INORGANICI Idruri Idracidi Ossidi Perossidi Idrossidi Ossoacidi Sali Idruri Sono composti binari dell idrogeno con gli elementi più elettropositivi (metalli) IDRURI Metalli
CHIMICA GENERALE CON LABORATORIO ED ELEMENTI DI ORGANICA (12 CFU) STRUTTURA DEL CORSO
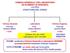 CHIMICA GENERALE CON LABORATORIO ED ELEMENTI DI ORGANICA (12 CFU) STRUTTURA DEL CORSO Chimica Generale Laboratorio Chimica Organica Prof.ssa Barbara Milani 7 CFU Prof. Tiziano Montini 2 CFU Lezione: 8/11
CHIMICA GENERALE CON LABORATORIO ED ELEMENTI DI ORGANICA (12 CFU) STRUTTURA DEL CORSO Chimica Generale Laboratorio Chimica Organica Prof.ssa Barbara Milani 7 CFU Prof. Tiziano Montini 2 CFU Lezione: 8/11
