Sequenza di Kozak Inizio della TRADUZIONE Nucleotidi in blod 100% conservati, sequenza consensus (GCC) G(-6) CC A/G(-3) CC ATG G(+4)
|
|
|
- Giuseppe Valle
- 5 anni fa
- Visualizzazioni
Transcript
1 Sequenza di Kozak Inizio della TRADUZIONE Nucleotidi in blod 100% conservati, sequenza consensus (GCC) G(-6) CC A/G(-3) CC ATG G(+4)
2 Proteine
3 maggior parte della massa cellulare esclusa l acqua
4
5 ATP utilizzato per processi di sintesi ATP ATP ATP
6 Aggiungendo all ATP una molecola di acqua si ottiene ADP e fosfato inorganico (idrolisi del fosfato terminale kcal/mole di energia, delta G negativo) Reazione sfavorita energeticamente Reazione favorita energeticamente IDROLISI si accoppia con altre reazioni sfavorite per es. Fosforilazioni oppure reazioni di condensazione, legami tra due molecole
7 Struttura e funzione delle proteine Le cellule viventi contengono un corredo estremamente diversificato di molecole proteiche, ciascuna costituita da una catena lineare di aminoacidi uniti da legami covalenti. Ogni tipo di proteina ha una sequenza aminoacidica unica che determina sia la sua forma tridimensionale che la sua attività biologica. A seconda della funzione: ENZIMI STRUTTURALI----TRASPORTO MOTRICI--- ACCUMULO---SEGNALE CELLULARE---RECETTORI---- REGOLATRICI DI GENI--
8 La lunghezza varia da 30 a aminoacidi ma per lo più sta tra 50 e 2000
9 Le proteine si dispongono nella conformazione di energia libera minima E questa conformazione è STABILE rimuove le interazioni non covalenti che sono alla base del ripiegamento La forma tridimensionale è specificata nella sequenza amminoacidica. Esistono proteine dette CHAPERONI MOLECOLARI che assistono le proteine nel loro FOLDING o ripiegamento.
10 Le proteine si dispongono nella conformazione di energia libera minima E questa conformazione è STABILE: eccezione proteine aggreganti Proteina prionica Alfa sinucleina APP
11 La struttura delle proteine Struttura primaria = sequenza aminoacidica Struttura secondaria = elica a, piano b Struttura terziaria = elica a, piano b, avvolgimenti caotici, anse o pieghe tra l N- e il C- terminale formazione di DOMINI Struttura quaternaria = più catene polipetidiche
12
13 Le strutture secondarie, terziarie, quaternarie si realizzano mediante una specifica conformazione che le proteine possono assumere attraverso legami deboli non covalenti (van der Waals, ponti idrogeno, attrazioni elettrostatiche legami ionici ecc) Amminoacidi apolari e idrofobici saranno interni alla struttura mentre quelli polari sono esterni esposti al mezzo acquoso per formare legami idrogeno per es. Altri amminoacidi polari all interno della molecola creano legami con altri all interno
14 Struttura e funzione delle proteine STRUTTURA PRIMARIA à SECONDARIA La struttura di una proteina ripiegata su se stessa si stabilizza tramite interazioni non covalenti che si instaurano tra parti diverse della catena polipeptidica. Legami idrogeno tra regioni contigue dell'ossatura polipeptidica possono dare origine a disposizioni regolari e ripetitive, note come elica a e piano b. Nella struttura di molte proteine sono individuabili regioni limitate di forma globulare compatta, note come domini proteici.
15
16
17 Struttura e funzione delle proteine La struttura di una proteina ripiegata su se stessa si stabilizza tramite interazioni non covalenti che si instaurano tra parti diverse della catena polipeptidica. Legami idrogeno tra regioni contigue dell'ossatura polipeptidica possono dare origine a disposizioni regolari e ripetitive, note come elica a e piano b. Nella struttura di molte proteine sono individuabili regioni limitate di forma globulare compatta, note come domini proteici.
18 a-elica L N-H di ogni legame peptidico stabilisce un legame idrogeno con il C=O di un legame peptidico vicino piano-b I singoli tratti delle catene polipeptidiche della struttura sono tenuti insieme da legami idrogeno che si stabiliscono tra legami peptidici dei vari tratti
19 La spirale è una forma diffusa nelle strutture biologiche
20 Esempio proteine TRANSMEMBRANA= parte idrofobica ESTERNA La spirale è un elemento frequente che ricorre (un giro completo della spirale è composto da 3,6 aminoacidi) Il lato idrofobico delle catene aminoacidiche ESTERNO APOLARE che formano l elica-a va a contatto con le molecole fosfolipidiche mentre le parti idrofiliche della molecola formano legami idrogeno all interno della spirale
21 Esempio proteine CITOPLASMA= parte idrofilica ESTERNA Spirale ritorta: aminoacidi non polari in a e d Le due eliche possono avvolgersi un una elica STRUTTURA SUPERAVVOLTA Catene apolari che interagiscono lasciando le catene laterali idrofiliche esterne per reagire con l acqua
22 La freccia punta verso il C terminale Anti-parallelo Parallelo
23
24 Struttura e funzione delle proteine La struttura di una proteina ripiegata su se stessa si stabilizza tramite interazioni non covalenti che si instaurano tra parti diverse della catena polipeptidica. Legami idrogeno tra regioni contigue dell'ossatura polipeptidica possono dare origine a disposizioni regolari e ripetitive, note come elica a e piano b. Nella struttura di molte proteine sono individuabili regioni limitate di forma globulare compatta, note come domini proteici.
25 STRUTTURA SECONDARIA à TERZIARIA Elementi di struttura secondaria come le elica a, piano b, si compattano in strutture terziarie di forma globulare stabili ed indipendenti denominate domini, le proteine hanno solitamente uno o più domini Due domini tenuti insieme da parti non strutturate della proteina, flessibili
26 Per un peptide lungo n aminoacidi sono possibili 20 n combinazioni diverse Con 300 aminoacidi (lunghezza proteina tipica) si potrebbe fare teoricamente ( ) catene polipetidiche strutturalmente diverse ma solo una piccola frazione assume una conformazione stabile
27 STRUTTURA TERZIARIA à QUATERNARIA Molte proteine contengono copie multiple della stessa subunità
28 STRUTTURA TERZIARIA à QUATERNARIA Alcune proteine si formano per aggregazione simmetrica di subunità di due tipi Emoglobina: due coppie di globina a e due coppie di globina b In rosso molecola di eme che lega O ogni molecola trasporta 4 molecole di O
29 STRUTTURA TERZIARIA à QUATERNARIA Le proteine possono aggregarsi in filamenti, strati o globuli
30 STRUTTURA TERZIARIA à QUATERNARIA POLIMERI Un filamento di actina è composto di subunità proteiche identiche
31
32 Collagene Elastina
33 Molte proteine sono attaccate all esterno della membrana cellulare o vengono secrete e vanno a fare parte della matrice extracellulare; tutte queste molecole sono esposte direttamente a condizioni ambientali extracellulari Per meglio mantenere la loro struttura le catene polipeptidiche di queste proteine spesso si stabilizzano attraverso ponti disolfuro (legami covalenti Z-Z) I legami covalenti Z-Z non si formano nel citosol perchè verrebbero idrolizzati in gruppi SH della cisteina dagli agenti riducenti
34 IL FUNZIONAMENTO DELLE PROTEINE LEGANO UN LIGANDO Tutte le proteine legano altre molecole (ligando) Molti legami determinano la specificità (il igando deve combaciare bene con la la proteina legante così aumentano i legami)
35 IL FUNZIONAMENTO DELLE PROTEINE LEGANO UN LIGANDO A sito di legame ogni proteina interagisce con un legame specifico Il sito di legame consta spesso di una cavità superficiale su cui gli aminoacidi (appartenenti a tratti della catena polipetidica distanti) si affacciano in una conformazione particolare
36 IL FUNZIONAMENTO DELLE PROTEINE LEGANO UN LIGANDO, ANTICORPI In azzurro parti variabili di catene pesante e leggera che legano antigene
37 Struttura e funzione delle proteine La funzione biologica di una proteina dipende dalle proprietà chimiche di zone particolari della sua superficie e dalle modalità di interazione con molecole specifiche, dette ligandi (es. enzimi). Gli enzimi sono proteine che, dopo aver legato strettamente molecole specifiche, dette substrati, catalizzano in esse la formazione e la rottura di legami covalenti. Al sito attivo di un enzima le catene aminoacidiche laterali della proteina avvolta su se stessa sono posizionati in maniera da favorire il passaggio dei substrati a uno stato di transizione ad alta energia, necessario perché si convertano in prodotti. La struttura tridimensionale di molte proteine si è evoluta in modo che l'associazione di un ligando anche piccolo può indurre una variazione significativa nella forma della molecola.
38 Classi funzionali degli enzimi Idrolasi Nucleasi Proteasi Sintetasi Isomerasi Polimerasi Chinasi Fosfatasi Ossido-reduttasi ATPasi Scissione idrolitica Degradazione acidinucleici Degradazione proteine Condensano due molecole Redistribuzione legami molecola Polimerizzaizone sintesi DNA/RNA Aggiunta gruppi fosfato Rimozione idrolitica gruppo fosfato Ossidasi, reduttasi, deidrogenasi Idrolisi ATP
39 Il lisozima catalizzando un idrolisi recede una catena polisaccaridica (E = enzima; S = substrato; P = prodotto) Antibiotico naturale contenuto in albume uovo, lacrime, saliva Scinde polisaccaridi di parete batterica e quindi patogeni Catalizzano cioè accelerano REAZIONI CHIMICHE basate su rottura di legami covalenti senza che la propria struttura sia alterata. Hanno una specificità di reazione. Diversi enzimi cooperano generando substrati per altri che intervengono in seguito nelle vie metaboliche
40 La reazione non avviene spontaneamente in mezzo acquoso e deve essere catalizzata cioè facilitata da enzima lisozima: energia libera della catena interrotta è minore di quella integra. In teoria la reazione sarebbe favorita. Però affinché una molecola d acqua urti lo zucchero e lo rompa, esso deve essere presente in conformazione distorta La distorsione richiede una dose notevole di energia che non viene erogata dalla sola collisione dell acqua con lo zucchero. Il lisozima catalizzatore ha un sito attivo che lega in modo specifico il ligando zucchero substrato tramite legami multipli non covalenti.
41
42 Funzione e regolazione delle proteine Quasi tutti gli enzimi sono proteine allosteriche che esistono in due conformazioni diverse quanto ad attività catalitica. L'enzima può essere acceso o spento da ligandi che gli si associano a un sito di regolazione distinto, stabilizzandone la conformazione attiva o inattiva. L attività di quasi tutti gli enzimi cellulari è rigorosamente controllata.
43
44 Altre proteine non legano substrati per modificarli in qualità di enzimi Esse legano altre molecole per acquisire funzioni specifiche Emoglobina lega con legami NON covalenti 4 molecole di eme Molecole ad anello con al centro uno atomo di ferro Lega OSSIGENO NEI POLMONI e rilascia IN TESSUTI
45 Funzione e regolazione dell attività delle proteine Diversi livelli di controllo: espressione genica regolazione della degradazione compartimentalizzazione in membrane organelli, per es lisosomi regolazione più rapida data da modifica della proteina stessa-feedback negativi e positivi o modificazioni chimiche
46 L inibizione retroattiva regola il flusso della via biosintetica Il prodotto Z inibisce il primo enzima esclusivo della via biosintetica Z si lega all enzima in rosso in un sito di regolazione modificando la velocità con cui l enzima trasforma I substrati in prodotti (inibizione)
47 L inibizione retroattiva a siti multipli regola reazioni metaboliche interconnesse Ogni aminoacido regola il primo enzima specifico per la propria sintesi Feedback negativi: lisina si lega all enzima rosso che cambia conformazione. Il suo sito attivo non è più favorevole ad accogliere il substrato. Enzima rosso ha due conformazioni allosteriche: una attiva-lega il substrato una inattiva-lega il regolatore negativo Feedback positivi
48 Funzione e regolazione dell attività delle proteine Diversi livelli di controllo: espressione genica regolazione della degradazione compartimentalizzazione in membrane organelli, per es lisosomi regolazione più rapida data da modifica della proteina stessa-feedback negativi e positivi o modificazioni chimiche Fosforilazione-Acetilazione-Ubiquitilazione Legame con molecola di GTP
49 Guanosin trifosfato (GTP) è un nucleotide Le proteine associate al GTP si trovano in conformazione attiva quando hanno il GTP legato Poi la proteina stessa idrolizza il GTP a GDP, libera un fosfato e passa alla conformazione inattiva Le proteine associate al GTP sono interruttori molecolari La dissociazione del GDP e la sua sostituzione con GTP pone l interruttore su acceso, questo avviene spesso in risposta ad un segnale ricevuto dalla cellula (proteine GTP legate fungono da segnale per attivare a loro volta altre proteine (trasmissione del segnale)
50 Struttura e funzione delle proteine In una cellula eucariotica tipica molte migliaia di proteine sono regolate tramite fosforilazione e defosforilazione ciclica o tramite il legame con il GTP e la sua idrolisi ad opera di una apposita proteina associata al GTP. Le proteine motrici idrolizzano l'atp ad ADP per produrre movimenti direzionali nella cellula. Gli agglomerati di proteine allosteriche capaci di fare cambiamenti di conformazione coordinati sono macchine proteiche efficientissime per svolgere funzioni cellulari complesse.
51 1. Il nucleoside è una molecola formata da due elementi, un composto con anello azotato (base) ed uno zucchero a cinque atomi di carbonio (ribosio o deossiribosio). 2. Un nucleoside dotato di uno o più gruppi fosfato legati allo zucchero si chiama nucleotide. 3. Adenosintrifosfato (ATP) è un nucleotide (subunità d DNA e RNA) la cui reattività dipende dai gruppi fosfato laterali 4. Partecipa al trasferimento di energia di centinaia di reazioni cellulari 5. Viene sintetizzato per mezzo di reazioni alimentari dall energia che si libera nella degradazione ossidativa delle sostanze nutritive 6. I suoi tre fosfati sono legati mediante due legami fosfoanidride la cui rottura libera grandi quantità di energia utilizzabile
52
53 L idrolisi fa fare ampi movimenti alle proteine motrici, senza idrolisi la proteina vibra ma si muove finalisticamente
54 La fosforilazione è un meccanismo diffuso per regolare le proteine Trasferimento di un P (gamma) da ATP a catena laterale proteina di aa che portano -OH Ser, Thr, Tyr Le proteine che legano covalentemente un gruppo fosfato si modificano Le protein chinasi (fosforilazione) e fosfatasi (defosforilazione) sono gli enzimi che regolano il legame dei gruppi fosfato Ad ogni istante, un terzo delle proteine presenti in una cellula eucariotica è fosforilata
55
56
57
58
59
60
Struttura e funzione delle proteine
 Proteine Struttura e funzione delle proteine Le cellule viventi contengono un corredo estremamente diversificato di molecole proteiche, ciascuna costituita da una catena lineare di aminoacidi uniti da
Proteine Struttura e funzione delle proteine Le cellule viventi contengono un corredo estremamente diversificato di molecole proteiche, ciascuna costituita da una catena lineare di aminoacidi uniti da
BIOMOLECOLE (PROTEINE)
 BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
a) un movimento contro gradiente di concentrazione che utilizza fonti primarie di energia
 1. Quale considerazione sulla struttura primaria di una proteina è vera? a) è caratteristica delle proteine insolubili b) i ponti S-S la stabilizzano c) i ponti H la stabilizzano d) la proteina assume
1. Quale considerazione sulla struttura primaria di una proteina è vera? a) è caratteristica delle proteine insolubili b) i ponti S-S la stabilizzano c) i ponti H la stabilizzano d) la proteina assume
Funzioni dei nucleotidi
 Funzioni dei nucleotidi monomeri degli acidi nucleici esempi di altre funzioni ATP: moneta energetica GTP: fonte di energia nella sintesi proteica camp: secondo messaggero nella trasduzione del segnale
Funzioni dei nucleotidi monomeri degli acidi nucleici esempi di altre funzioni ATP: moneta energetica GTP: fonte di energia nella sintesi proteica camp: secondo messaggero nella trasduzione del segnale
Le proteine. Sono polimeri di amminoacidi dispos$ in sequenza. Due amminoacidi si legano tra loro formando un legame pep-dico.
 Le proteine Sono polimeri di amminoacidi dispos$ in sequenza. Due amminoacidi si legano tra loro formando un legame pep-dico. Cur$s et al. Invito alla biologia.blu Zanichelli editore 2011 1 Struttura e
Le proteine Sono polimeri di amminoacidi dispos$ in sequenza. Due amminoacidi si legano tra loro formando un legame pep-dico. Cur$s et al. Invito alla biologia.blu Zanichelli editore 2011 1 Struttura e
Dall RNA alle proteine. La traduzione nei procarioti e negli eucarioti
 Dall RNA alle proteine La traduzione nei procarioti e negli eucarioti Codice genetico La sequenza dell mrna viene decodificata a gruppi di tre nucleotidi, e tradotta in una sequenza di amminoacidi 4 x
Dall RNA alle proteine La traduzione nei procarioti e negli eucarioti Codice genetico La sequenza dell mrna viene decodificata a gruppi di tre nucleotidi, e tradotta in una sequenza di amminoacidi 4 x
Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi. Possono assumere forme diverse a seconda della funzione
 Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi Hanno elevato PM Possono assumere forme diverse a seconda della funzione svolgono molteplici funzioni Tra le proteine
Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi Hanno elevato PM Possono assumere forme diverse a seconda della funzione svolgono molteplici funzioni Tra le proteine
Esempi di funzioni svolte dalle proteine
 Esempi di funzioni svolte dalle proteine Trasporto di sostanze Esempi di funzioni svolte dalle proteine Trasporto di sostanze Funzioni strutturali Esempi di funzioni svolte dalle proteine Trasporto di
Esempi di funzioni svolte dalle proteine Trasporto di sostanze Esempi di funzioni svolte dalle proteine Trasporto di sostanze Funzioni strutturali Esempi di funzioni svolte dalle proteine Trasporto di
Le biomolecole si trovano negli organismi viventi
 Le biomolecole si trovano negli organismi viventi I viventi sono formati per la maggior parte da acqua e molecole, chiamate biomolecole. Le biomolecole sono sostanze contenenti carbonio. I composti del
Le biomolecole si trovano negli organismi viventi I viventi sono formati per la maggior parte da acqua e molecole, chiamate biomolecole. Le biomolecole sono sostanze contenenti carbonio. I composti del
Proteine. Enzimi Fattori di Trascrizione Proteine di Membrana (trasportatori, canale, recettori di membrana)
 Proteine Enzimi Fattori di Trascrizione Proteine di Membrana (trasportatori, canale, recettori di membrana) Ormoni e Fattori di crescita Anticorpi Trasporto Trasporto (emoglobina, LDL, HDL.) Fenotipo Proteine
Proteine Enzimi Fattori di Trascrizione Proteine di Membrana (trasportatori, canale, recettori di membrana) Ormoni e Fattori di crescita Anticorpi Trasporto Trasporto (emoglobina, LDL, HDL.) Fenotipo Proteine
Le Biomolecole II parte. Lezioni d'autore di Giorgio Benedetti
 Le Biomolecole II parte Lezioni d'autore di Giorgio Benedetti LA STRUTTURA TERZIARIA DI UNA PROTEINA La struttura tridimensionale adottata da una proteina è detta struttura terziaria. Essa prende in considerazione
Le Biomolecole II parte Lezioni d'autore di Giorgio Benedetti LA STRUTTURA TERZIARIA DI UNA PROTEINA La struttura tridimensionale adottata da una proteina è detta struttura terziaria. Essa prende in considerazione
Formula generale di un amminoacido
 Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
LE PROTEINE -struttura tridimensionale-
 LE PROTEINE -struttura tridimensionale- Struttura generale di una proteina Ceruloplasmina Cosa sono??? Sono biopolimeri con forme ben definite. composti da molteplici amminoacidi, legati con legami peptidici
LE PROTEINE -struttura tridimensionale- Struttura generale di una proteina Ceruloplasmina Cosa sono??? Sono biopolimeri con forme ben definite. composti da molteplici amminoacidi, legati con legami peptidici
Il carbonio è l elemento di base delle biomolecole. Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici.
 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici. 1 Il carbonio deve acquistare quattro elettroni per essere stabile
Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici. 1 Il carbonio deve acquistare quattro elettroni per essere stabile
30/10/2015. Molte proteine sono. intrinsecamente disordinate. o destrutturate (IDP/IUP), cioè non hanno una struttura
 Molte proteine sono intrinsecamente disordinate o destrutturate (IDP/IUP), cioè non hanno una struttura terziaria e/o secondaria stabile. Le IUP sono caratterizzate da - scarso contenuto in aa apolari,
Molte proteine sono intrinsecamente disordinate o destrutturate (IDP/IUP), cioè non hanno una struttura terziaria e/o secondaria stabile. Le IUP sono caratterizzate da - scarso contenuto in aa apolari,
Immagini e concetti della biologia
 Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
Funzioni delle proteine
 Funzioni delle proteine ENZIMI Proteine di trasporto Proteine di riserva Proteine contrattili o motili Proteine strutturali Proteine di difesa Proteine regolatrici Proteine di trasporto Emoglobina Lipoproteine
Funzioni delle proteine ENZIMI Proteine di trasporto Proteine di riserva Proteine contrattili o motili Proteine strutturali Proteine di difesa Proteine regolatrici Proteine di trasporto Emoglobina Lipoproteine
STRUTTURA E FUNZIONE DELLE PROTEINE
 STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
Le macromolecole dei tessuti - 1
 Le macromolecole dei tessuti - 1 Che cosa sono le proteine? Sono macromolecole complesse ad alta informazione Sono costituite da una o più catene polipeptidiche Ogni catena peptidica è composta da centinaia
Le macromolecole dei tessuti - 1 Che cosa sono le proteine? Sono macromolecole complesse ad alta informazione Sono costituite da una o più catene polipeptidiche Ogni catena peptidica è composta da centinaia
ACIDI GRASSI INSATURI
 LIPIDI ACIDI GRASSI SATURI ACIDI GRASSI INSATURI TRIGLICERIDI TRIGLICERIDI Grassi neutri o lipidi semplici glicerolo + 1 acido grasso monogliceride glicerolo + 2 acidi grassi digliceride glicerolo + 3
LIPIDI ACIDI GRASSI SATURI ACIDI GRASSI INSATURI TRIGLICERIDI TRIGLICERIDI Grassi neutri o lipidi semplici glicerolo + 1 acido grasso monogliceride glicerolo + 2 acidi grassi digliceride glicerolo + 3
COMPOSTI AZOTATI. derivanti dall ammoniaca AMMINE. desinenza -INA AMMIDE
 COMPOSTI AZOTATI derivanti dall ammoniaca AMMINE desinenza -INA AMMIDE ANCORA AMMIDI RISONANZA A M M I D I Il legame ammidico ha parziale carattere di doppio legame per la seguente risonanza: Ammidi H
COMPOSTI AZOTATI derivanti dall ammoniaca AMMINE desinenza -INA AMMIDE ANCORA AMMIDI RISONANZA A M M I D I Il legame ammidico ha parziale carattere di doppio legame per la seguente risonanza: Ammidi H
LE PROTEINE. SONO Polimeri formati dall unione di AMMINOACIDI (AA) Rende diversi i 20 AA l uno dall altro UN ATOMO DI C AL CENTRO
 LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
PROTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi
 POTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (,, O, N) macromolecole organiche, molecole informazionali, polimeri
POTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (,, O, N) macromolecole organiche, molecole informazionali, polimeri
- utilizzano esclusivamente le reattività chimiche di alcuni residui AA
 Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Biologia. Lezione 09/11/2010
 Biologia Lezione 09/11/2010 Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono macromolecole formate da unità (MONOMERI)
Biologia Lezione 09/11/2010 Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono macromolecole formate da unità (MONOMERI)
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
Legami chimici. Covalente. Legami deboli
 Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici STRUTTURA TERZIARIA La struttura tridimensionale
Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici STRUTTURA TERZIARIA La struttura tridimensionale
Regolazione enzimatica Isoenzimi
 Regolazione enzimatica Isoenzimi Gli enzimi regolatori nel metabolismo gruppi di enzimi lavorano insieme per produrre una via metabolica in cui il prodotto del primo enzima diventa il substrato del secondo
Regolazione enzimatica Isoenzimi Gli enzimi regolatori nel metabolismo gruppi di enzimi lavorano insieme per produrre una via metabolica in cui il prodotto del primo enzima diventa il substrato del secondo
Proteine: struttura e funzione
 Proteine: struttura e funzione Prof.ssa Flavia Frabetti PROTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (C, H, O,
Proteine: struttura e funzione Prof.ssa Flavia Frabetti PROTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (C, H, O,
STRUTTURA E FUNZIONE DELLE PROTEINE
 STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
Composti organici. I composti organici. Atomi e molecole di carbonio. Atomi e molecole di carbonio. Gruppi funzionali. Isomeri
 I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
Le molecole biologiche. Sylvia S. Mader Immagini e concetti della biologia Zanichelli editore, 2012
 Le molecole biologiche 1 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici. 2 Il carbonio deve acquistare quattro elettroni
Le molecole biologiche 1 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici. 2 Il carbonio deve acquistare quattro elettroni
le porzioni con strutture secondarie sono avvicinate e impaccate mediante anse e curve della catena. STRUTTURA TERZIARIA
 STRUTTURA TERZIARIA le porzioni con strutture secondarie sono avvicinate e impaccate mediante anse e curve della catena. Le proteine globulari dopo aver organizzato il proprio scheletro polipeptidico con
STRUTTURA TERZIARIA le porzioni con strutture secondarie sono avvicinate e impaccate mediante anse e curve della catena. Le proteine globulari dopo aver organizzato il proprio scheletro polipeptidico con
La Chimica della Vita
 La Chimica della Vita I componenti chimici delle cellule Nell atomo il numero di elettroni è uguale al numero di protoni del suo nucleo. Il nucleo dei diversi isotopi di uno stesso elemento contiene lo
La Chimica della Vita I componenti chimici delle cellule Nell atomo il numero di elettroni è uguale al numero di protoni del suo nucleo. Il nucleo dei diversi isotopi di uno stesso elemento contiene lo
Strategie catalitiche
 Strategie catalitiche catalisi acido-base catalisi covalente catalisi da metalli Dati molecolari di alcune proteine Citocromo C (umano) Ribonucleasi A (pancreas di bue) Lisozima (bianco dell uovo) Mioglobina
Strategie catalitiche catalisi acido-base catalisi covalente catalisi da metalli Dati molecolari di alcune proteine Citocromo C (umano) Ribonucleasi A (pancreas di bue) Lisozima (bianco dell uovo) Mioglobina
PROTEINE: STRUTTURA, ESEMPI E FUNZIONAMENTO TUTORATO 1 GIULIANO F. PATANÈ COLLEGIO A. VOLTA
 PROTEINE: STRUTTURA, ESEMPI E FUNZIONAMENTO TUTORATO 1 GIULIANO F. PATANÈ COLLEGIO A. VOLTA PROTEINE Una proteina è basilarmente una catena polipeptidica (che in termini chimici può anche essere definita
PROTEINE: STRUTTURA, ESEMPI E FUNZIONAMENTO TUTORATO 1 GIULIANO F. PATANÈ COLLEGIO A. VOLTA PROTEINE Una proteina è basilarmente una catena polipeptidica (che in termini chimici può anche essere definita
STRUTTURA TRIDIMENSIONALE DELLE PROTEINE
 STRUTTURA TRIDIMENSIONALE DELLE PROTEINE Biologia della Cellula Animale 2016 1 STRUTTURA PROTEINE Cooper: The Cell, a Molecular Approach, 2 nd ed. http://en.wikipedia.org/wiki/protein_structure STRUTTURA
STRUTTURA TRIDIMENSIONALE DELLE PROTEINE Biologia della Cellula Animale 2016 1 STRUTTURA PROTEINE Cooper: The Cell, a Molecular Approach, 2 nd ed. http://en.wikipedia.org/wiki/protein_structure STRUTTURA
Di cosa è fatta una cellula?
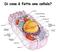 Di cosa è fatta una cellula? Composizione delle cellule - L acqua (H 2 O) rappresenta il 70% del massa della cellula - C,H,N,O,P,S rappresentano il 99% della massa della cellula - Altri elementi più rari
Di cosa è fatta una cellula? Composizione delle cellule - L acqua (H 2 O) rappresenta il 70% del massa della cellula - C,H,N,O,P,S rappresentano il 99% della massa della cellula - Altri elementi più rari
Di cosa è fatta una cellula?
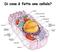 Di cosa è fatta una cellula? Composizione delle cellule - L acqua (H 2 O) rappresenta il 70% del massa della cellula - C,H,N,O rappresentano il 96% della massa della cellula - Altri component frequenti
Di cosa è fatta una cellula? Composizione delle cellule - L acqua (H 2 O) rappresenta il 70% del massa della cellula - C,H,N,O rappresentano il 96% della massa della cellula - Altri component frequenti
Introduzione alla biologia della cellula. Lezione 2 Le biomolecole
 Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
Alcol + alcol etere R-OH + R -OH R-O-R + H 2 O Aldeide + alcol emiacetale R-CHO + R -OH R-CHOH-O-R Acido + Acido anidride R-COOH + R -COOH
 Nomenclatura AMIDI Alcol + alcol etere R-OH + R -OH R-O-R + H 2 O Aldeide + alcol emiacetale R-CHO + R -OH R-CHOH-O-R Acido + Acido anidride R-COOH + R -COOH R-CO-O-CO-R + H 2 O Alcol + Acido estere R-COOH
Nomenclatura AMIDI Alcol + alcol etere R-OH + R -OH R-O-R + H 2 O Aldeide + alcol emiacetale R-CHO + R -OH R-CHOH-O-R Acido + Acido anidride R-COOH + R -COOH R-CO-O-CO-R + H 2 O Alcol + Acido estere R-COOH
Mediatore chimico. Recettore. Trasduzione del segnale. Risposta della cellula
 Mediatore chimico Recettore Trasduzione del segnale Risposta della cellula I mediatori chimici sono prodotti da cellule specializzate e sono diffusi nell organismo da apparati di distribuzione Sistemi
Mediatore chimico Recettore Trasduzione del segnale Risposta della cellula I mediatori chimici sono prodotti da cellule specializzate e sono diffusi nell organismo da apparati di distribuzione Sistemi
Regolazione dell attività enzimatica. Allosteria Modificazioni covalenti Isoenzimi
 Regolazione dell attività enzimatica Allosteria Modificazioni covalenti Isoenzimi Regolazione della attività enzimatica L attività enzimatica deve potere essere regolata in base alle specifiche richieste
Regolazione dell attività enzimatica Allosteria Modificazioni covalenti Isoenzimi Regolazione della attività enzimatica L attività enzimatica deve potere essere regolata in base alle specifiche richieste
Aminoacidi. Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α
 Aminoacidi Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α 1 Isomeria ottica Tutti gli AA, esclusa la glicina, presentano almeno un atomo di carbonio asimmetrico, il
Aminoacidi Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α 1 Isomeria ottica Tutti gli AA, esclusa la glicina, presentano almeno un atomo di carbonio asimmetrico, il
Capitolo 3 Le biomolecole
 apitolo 3 Le biomolecole I composti organici e i loro polimeri 3.1 La diversità molecolare della vita è basata sulle proprietà del carbonio Un atomo di carbonio può formare quattro legami covalenti. Questi
apitolo 3 Le biomolecole I composti organici e i loro polimeri 3.1 La diversità molecolare della vita è basata sulle proprietà del carbonio Un atomo di carbonio può formare quattro legami covalenti. Questi
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 11
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 11 Funzioni delle proteine Concetti chiave: La varietà strutturale delle proteine consente loro di svolgere un enorme quantità
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 11 Funzioni delle proteine Concetti chiave: La varietà strutturale delle proteine consente loro di svolgere un enorme quantità
SOLUZIONI DEGLI ESERCIZI
 Dal carbonio agli OGM Biochimica e biotecnologie SOLUZIONI DEGLI ESERCIZI Capitolo 0 Il mondo del carbonio 1. b, e 2. d 3. 7 4. 5. 6. 7. a) Isomeria di posizione; b) i due composti non sono isomeri; c)
Dal carbonio agli OGM Biochimica e biotecnologie SOLUZIONI DEGLI ESERCIZI Capitolo 0 Il mondo del carbonio 1. b, e 2. d 3. 7 4. 5. 6. 7. a) Isomeria di posizione; b) i due composti non sono isomeri; c)
BIOLOGIA GENERALE 19 dicembre 2006
 Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE 19 dicembre 2006 Facoltà di Psicologia Corso di Laurea in Scienze e Tecniche di Psicologia Generale e Sperimentale
Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE 19 dicembre 2006 Facoltà di Psicologia Corso di Laurea in Scienze e Tecniche di Psicologia Generale e Sperimentale
Formazione del legame peptidico:
 Formazione del legame peptidico: Planare, ha una forza intermedia tra il legame semplice ed il legame doppio. 2^ lezione N R C C O O O + R N R C O C O O N R C C N C C O Ogni piano delle unità peptidiche
Formazione del legame peptidico: Planare, ha una forza intermedia tra il legame semplice ed il legame doppio. 2^ lezione N R C C O O O + R N R C O C O O N R C C N C C O Ogni piano delle unità peptidiche
L ACQUA E LE SUE PROPRIETÀ
 L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
Nucleotidi e Acidi Nucleici. Struttura di DNA e RNA
 Nucleotidi e Acidi Nucleici Nucleosidi Nucleotidi Funzioni biologiche dei nucleotidi Struttura di DNA e RNA Concatenazione e appaiamento dei nucleotidi Lo scheletro degli acidi nucleici Componenti degli
Nucleotidi e Acidi Nucleici Nucleosidi Nucleotidi Funzioni biologiche dei nucleotidi Struttura di DNA e RNA Concatenazione e appaiamento dei nucleotidi Lo scheletro degli acidi nucleici Componenti degli
ENZIMI. Durante la reazione l enzima può essere temporaneamente modificato ma alla fine del processo ritorna nel suo stato originario, un enzima viene
 ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari, e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari, e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
sono le unità monomeriche che costituiscono le proteine hanno tutti una struttura comune
 AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
CARBOIDRATI C H O ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO
 CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
lati esterni altamente Idrofilici
 I due filamenti complementari del DNA sono antiparalleli: uno è in direzione 5-3 e l altro in direzione 3-5. parte interna idrofobica lati esterni altamente Idrofilici APPAIAMENTO DELLE BASI AZOTATE: 2
I due filamenti complementari del DNA sono antiparalleli: uno è in direzione 5-3 e l altro in direzione 3-5. parte interna idrofobica lati esterni altamente Idrofilici APPAIAMENTO DELLE BASI AZOTATE: 2
TRASDUZIONE DEL SEGNALE CELLULARE
 TRASDUZIONE DEL SEGNALE CELLULARE RECETTORI I recettori ormonali sono proteine (spesso glicoproteine) capaci di riconoscere e legare l ormone L interazione tra ormone e recettore è estremamente specifica
TRASDUZIONE DEL SEGNALE CELLULARE RECETTORI I recettori ormonali sono proteine (spesso glicoproteine) capaci di riconoscere e legare l ormone L interazione tra ormone e recettore è estremamente specifica
I materiali della vita
 I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
La chimica della vita
 La chimica della vita La materia presente nell universo è formata da 92 elementi Gli elementi si legano tra loro per formare le molecole che costituiscono i composti Legame covalente O H H Molecola Composto
La chimica della vita La materia presente nell universo è formata da 92 elementi Gli elementi si legano tra loro per formare le molecole che costituiscono i composti Legame covalente O H H Molecola Composto
I componenti chimici delle cellule
 I componenti chimici delle cellule Piccole molecole Macromolecole Piccole molecole C, H, N ed O costituiscono quasi il 99% del peso di una cellula Il 70 % della massa di una cellula è costituito da acqua
I componenti chimici delle cellule Piccole molecole Macromolecole Piccole molecole C, H, N ed O costituiscono quasi il 99% del peso di una cellula Il 70 % della massa di una cellula è costituito da acqua
I PROTIDI ASPETTI GENERALI
 I PROTIDI ASPETTI GENERALI I PROTIDI O PROTEINE SONO SOSTANZE ORGANICHE AZOTATE, DI STRUTTURA MOLTO COMPLESSA, PRESENTI IN OGNI FORMA DI VITA. LE PROTEINE SONO COMPOSTI QUATERNARI, OSSIA SONO FORMATE DA
I PROTIDI ASPETTI GENERALI I PROTIDI O PROTEINE SONO SOSTANZE ORGANICHE AZOTATE, DI STRUTTURA MOLTO COMPLESSA, PRESENTI IN OGNI FORMA DI VITA. LE PROTEINE SONO COMPOSTI QUATERNARI, OSSIA SONO FORMATE DA
scaricato da www.sunhope.it Proteine semplici costituite dai soli amminoacidi
 Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
LE PROTEINE SINTESI PROTEICA. funzione delle proteine nel nostro organismo
 LE PTEIE Le proteine sono sostanze organiche presenti in tutte le cellule di tutti gli organismi viventi Le proteine sono costituite da,,,, (S) Struttura delle proteine Le proteine sono macromolecole (
LE PTEIE Le proteine sono sostanze organiche presenti in tutte le cellule di tutti gli organismi viventi Le proteine sono costituite da,,,, (S) Struttura delle proteine Le proteine sono macromolecole (
REGOLAZIONE DELL ATTIVITA ENZIMATICA 1) MODULAZIONE ALLOSTERICA NON-COVALENTE (REVERSIBILE)
 REGOLAZIONE DELL ATTIVITA ENZIMATICA - Regolazione a lungo termine: la quantità di enzima può essere controllata regolando la velocità della sua sintesi o degradazione (minuti o ore) - Regolazione a breve
REGOLAZIONE DELL ATTIVITA ENZIMATICA - Regolazione a lungo termine: la quantità di enzima può essere controllata regolando la velocità della sua sintesi o degradazione (minuti o ore) - Regolazione a breve
CROMATINA ISTONI. Proteine relativamente piccole, con forte carica positiva per la presenza degli aminoacidi lisina e arginina
 CROMATINA Complesso molecolare formato da DNA, istoni e proteine non istoniche ISTONI Proteine relativamente piccole, con forte carica positiva per la presenza degli aminoacidi lisina e arginina Si conoscono
CROMATINA Complesso molecolare formato da DNA, istoni e proteine non istoniche ISTONI Proteine relativamente piccole, con forte carica positiva per la presenza degli aminoacidi lisina e arginina Si conoscono
Alessandra Bolino. Capo Unità della ricerca Unità di Neuropatie Ereditarie Umane Ospedale San Raffaele-Milano
 Alessandra Bolino Capo Unità della ricerca Unità di Neuropatie Ereditarie Umane Ospedale San Raffaele-Milano Cellula introduzione DNA cromatina e replicazione RNA-Trascrizione e regolazione della trascrizione
Alessandra Bolino Capo Unità della ricerca Unità di Neuropatie Ereditarie Umane Ospedale San Raffaele-Milano Cellula introduzione DNA cromatina e replicazione RNA-Trascrizione e regolazione della trascrizione
Nucleotidi e acidi nucleici
 Nucleotidi e acidi nucleici ACIDI NUCLEICI Biomolecole fondamentali per tutti gli organismi viventi Unici nella capacità di autoduplicazione Conservazione e trasmissione da una generazione all altra dell
Nucleotidi e acidi nucleici ACIDI NUCLEICI Biomolecole fondamentali per tutti gli organismi viventi Unici nella capacità di autoduplicazione Conservazione e trasmissione da una generazione all altra dell
scaricato da I peptidi risultano dall unione di due o più aminoacidi mediante un legame COVALENTE
 Legame peptidico I peptidi risultano dall unione di due o più aminoacidi mediante un legame COVALENTE tra il gruppo amminico di un aminoacido ed il gruppo carbossilico di un altro. 1 Catene contenenti
Legame peptidico I peptidi risultano dall unione di due o più aminoacidi mediante un legame COVALENTE tra il gruppo amminico di un aminoacido ed il gruppo carbossilico di un altro. 1 Catene contenenti
I componenti chimici delle cellule
 I componenti chimici delle cellule Piccole molecole Macromolecole Piccole molecole C, H, N ed O costituiscono quasi il 99% del peso di una cellula Il 70 % della massa di una cellula è costituito da acqua
I componenti chimici delle cellule Piccole molecole Macromolecole Piccole molecole C, H, N ed O costituiscono quasi il 99% del peso di una cellula Il 70 % della massa di una cellula è costituito da acqua
La struttura delle proteine
 La struttura delle proteine Funzioni delle proteine Strutturali Contrattili Trasporto Riserva Ormonali Enzimatiche Protezione Struttura della proteina Struttura secondaria: ripiegamento locale della catena
La struttura delle proteine Funzioni delle proteine Strutturali Contrattili Trasporto Riserva Ormonali Enzimatiche Protezione Struttura della proteina Struttura secondaria: ripiegamento locale della catena
Chimica Biologica A.A α-elica foglietto β reverse turn
 Chimica Biologica A.A. 2010-2011 α-elica foglietto β reverse turn Str. Secondaria sperimentalmente osservata: Si distinguono fondamentalmente tre tipi di strutture secondarie: α elica foglietto β reverse
Chimica Biologica A.A. 2010-2011 α-elica foglietto β reverse turn Str. Secondaria sperimentalmente osservata: Si distinguono fondamentalmente tre tipi di strutture secondarie: α elica foglietto β reverse
CORSO DI BIOCHIMICA PER INGEGNERIA BIOMEDICA I ESERCITAZIONE
 CORSO DI BIOCHIMICA PER INGEGNERIA BIOMEDICA I ESERCITAZIONE 1) Che tipo di ibridazione ha il carbonio coinvolto nel doppio legame degli alcheni? Descrivi brevemente. Alcheni Ibridazione sp 2 2s p x p
CORSO DI BIOCHIMICA PER INGEGNERIA BIOMEDICA I ESERCITAZIONE 1) Che tipo di ibridazione ha il carbonio coinvolto nel doppio legame degli alcheni? Descrivi brevemente. Alcheni Ibridazione sp 2 2s p x p
Gli acidi nucleici, DNA (acido deossiribonucleico) e RNA (acido. ribonucleico), sono polimeri biologicamente importanti in quanto
 Gli acidi nucleici, DA (acido deossiribonucleico) e RA (acido ribonucleico), sono polimeri biologicamente importanti in quanto svolgono ruoli fondamentali nell ereditarietà e nella sintesi proteica. Sono
Gli acidi nucleici, DA (acido deossiribonucleico) e RA (acido ribonucleico), sono polimeri biologicamente importanti in quanto svolgono ruoli fondamentali nell ereditarietà e nella sintesi proteica. Sono
FORMAZIONE DEL LEGAME PEPTIDICO
 AMINOACIDI FORMAZIONE DEL LEGAME PEPTIDICO SEQUENZA AMINOACIDICA DELL INSULINA STRUTTURA SECONDARIA DELLE PROTEINE STRUTTURA TERZIARIA DELLE PROTEINE STRUTTURA QUATERNARIA DELLE PROTEINE Definizione Processi
AMINOACIDI FORMAZIONE DEL LEGAME PEPTIDICO SEQUENZA AMINOACIDICA DELL INSULINA STRUTTURA SECONDARIA DELLE PROTEINE STRUTTURA TERZIARIA DELLE PROTEINE STRUTTURA QUATERNARIA DELLE PROTEINE Definizione Processi
Lezione 1: Atomi e molecole:
 Lezione 1: Atomi e molecole: La materia è costituita da elementi chimici in forma pura o in combinazioni dette composti. La vita richiede circa 25 elementi chimici. La struttura atomica determina il comportamento
Lezione 1: Atomi e molecole: La materia è costituita da elementi chimici in forma pura o in combinazioni dette composti. La vita richiede circa 25 elementi chimici. La struttura atomica determina il comportamento
fornire energia chimica in vettori attivati ATP e NADH e NADPH e FADH.
 Cibo ed Energia Il glucosio e altre molecole nutritive per esempio i grassi vengono demolite attraverso un ossidazione graduale controllata per fornire energia chimica in una forma utilizzabile dalla cellula,
Cibo ed Energia Il glucosio e altre molecole nutritive per esempio i grassi vengono demolite attraverso un ossidazione graduale controllata per fornire energia chimica in una forma utilizzabile dalla cellula,
fornire energia chimica in vettori attivati ATP e NADH e NADPH e FADH.
 Cibo ed Energia Il glucosio e altre molecole nutritive per esempio i grassi vengono demolite attraverso un ossidazione graduale controllata per fornire energia chimica in una forma utilizzabile dalla cellula,
Cibo ed Energia Il glucosio e altre molecole nutritive per esempio i grassi vengono demolite attraverso un ossidazione graduale controllata per fornire energia chimica in una forma utilizzabile dalla cellula,
CATALISI COVALENTE. H 2 O Enz-R-OH + P. Enz-R-O S Enz-R-O-S
 CATALISI COVALENTE Comporta la formazione di intermedi in cui il substrato è legato covalentemente con un residuo amminoacidico del sito attivo dell enzima. La catena laterale re dell enzima può comportarsi
CATALISI COVALENTE Comporta la formazione di intermedi in cui il substrato è legato covalentemente con un residuo amminoacidico del sito attivo dell enzima. La catena laterale re dell enzima può comportarsi
Acidi Nucleici: DNA = acido deossiribonucleico
 Acidi Nucleici: DNA = acido deossiribonucleico depositario dell informazione genetica RNA: acido ribonucleico trascrizione e traduzione dell informazione genetica dogma centrale della biologia molecolare
Acidi Nucleici: DNA = acido deossiribonucleico depositario dell informazione genetica RNA: acido ribonucleico trascrizione e traduzione dell informazione genetica dogma centrale della biologia molecolare
30/10/2015 LIVELLI DI ORGANIZZAZIONE STRUTTURALE DELLE PROTEINE
 LIVELLI DI ORGANIZZAZIONE STRUTTURALE DELLE PROTEINE 1 CARATTERISTICHE DEL LEGAME PEPTIDICO lunghezza intermedia tra un legame singolo e uno doppio ibrido di risonanza per il parziale carattere di doppio
LIVELLI DI ORGANIZZAZIONE STRUTTURALE DELLE PROTEINE 1 CARATTERISTICHE DEL LEGAME PEPTIDICO lunghezza intermedia tra un legame singolo e uno doppio ibrido di risonanza per il parziale carattere di doppio
Capitolo 3 Le biomolecole
 apitolo 3 Le biomolecole opyright 2006 Zanichelli editore I composti organici e i loro polimeri 3.1 La diversità molecolare della vita è basata sulle proprietà del carbonio Un atomo di carbonio può formare
apitolo 3 Le biomolecole opyright 2006 Zanichelli editore I composti organici e i loro polimeri 3.1 La diversità molecolare della vita è basata sulle proprietà del carbonio Un atomo di carbonio può formare
DOGMA CENTRALE DELLA BIOLOGIA. Secondo il dogma centrale della biologia, il DNA dirige la. sintesi del RNA che a sua volta guida la sintesi delle
 DOGMA CENTRALE DELLA BIOLOGIA Secondo il dogma centrale della biologia, il DNA dirige la sintesi del RNA che a sua volta guida la sintesi delle proteine. Tuttavia il flusso unidirezionale di informazioni
DOGMA CENTRALE DELLA BIOLOGIA Secondo il dogma centrale della biologia, il DNA dirige la sintesi del RNA che a sua volta guida la sintesi delle proteine. Tuttavia il flusso unidirezionale di informazioni
MACROMOLECOLE. Polimeri (lipidi a parte)
 MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
Alberts et al., L ESSENZIALE DI BIOLOGIA MOLECOLARE DELLA CELLULA, Zanichelli editore S.p.A. Copyright 2005
 La conversione dell informazione da una forma ad un altra è il punto critico della trasmissione e prende il nome di: TRASDUZIONE DEL SEGNALE Nella comunicazione cellulare: Molecola segnale Proteina recettore
La conversione dell informazione da una forma ad un altra è il punto critico della trasmissione e prende il nome di: TRASDUZIONE DEL SEGNALE Nella comunicazione cellulare: Molecola segnale Proteina recettore
Macromolecole Biologiche. La struttura secondaria (III)
 La struttura secondaria (III) Reverse turn Le proteine globulari hanno una forma compatta, dovuta a numerose inversioni della direzione della catena polipeptidica che le compone. Molte di queste inversioni
La struttura secondaria (III) Reverse turn Le proteine globulari hanno una forma compatta, dovuta a numerose inversioni della direzione della catena polipeptidica che le compone. Molte di queste inversioni
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA)
 La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) L atomo del carbonio (C).. C. Atomo tetravalente. C C C C Gli idrocarburi I legami del carbonio 109.5 gradi
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) L atomo del carbonio (C).. C. Atomo tetravalente. C C C C Gli idrocarburi I legami del carbonio 109.5 gradi
La struttura terziaria delle proteine
 La struttura terziaria delle proteine 1 La struttura terziaria L arrangiamento spaziale degli aminoacidi di una singola catena polipeptidica a formare la sua struttura tridimensionale a domini viene chiamata
La struttura terziaria delle proteine 1 La struttura terziaria L arrangiamento spaziale degli aminoacidi di una singola catena polipeptidica a formare la sua struttura tridimensionale a domini viene chiamata
Introduzione al Citoscheletro
 http://zeiss-campus.magnet.fsu.edu/galleries/cells/index.html Le cellule animali sono cellule eucariotiche caratteristiche, racchiuse da una membrana plasmatica e contenenti un nucleo circondato da una
http://zeiss-campus.magnet.fsu.edu/galleries/cells/index.html Le cellule animali sono cellule eucariotiche caratteristiche, racchiuse da una membrana plasmatica e contenenti un nucleo circondato da una
Chimotripsina Una proteina globulare. Glicina Un amminoacido
 Chimotripsina Una proteina globulare Glicina Un amminoacido - In teoria un numero enorme di differenti catene polipeptidiche potrebbe essere sintetizzato con i 20 amminoacidi standard. 20 4 = 160.000 differenti
Chimotripsina Una proteina globulare Glicina Un amminoacido - In teoria un numero enorme di differenti catene polipeptidiche potrebbe essere sintetizzato con i 20 amminoacidi standard. 20 4 = 160.000 differenti
Schemi delle lezioni 1
 Schemi delle lezioni 1 Detti anche proteine sono i composti organici maggiormente presenti nelle cellule, dato che costituiscono circa il 50% del loro peso secco. Nell uomo adulto rappresentano circa
Schemi delle lezioni 1 Detti anche proteine sono i composti organici maggiormente presenti nelle cellule, dato che costituiscono circa il 50% del loro peso secco. Nell uomo adulto rappresentano circa
Dall RNA alle proteine. La traduzione nei procarioti e negli eucarioti
 Dall RNA alle proteine La traduzione nei procarioti e negli eucarioti Codice genetico La sequenza dell mrna viene decodificata a gruppi di tre nucleotidi, e tradotta in una sequenza di amminoacidi 4 x
Dall RNA alle proteine La traduzione nei procarioti e negli eucarioti Codice genetico La sequenza dell mrna viene decodificata a gruppi di tre nucleotidi, e tradotta in una sequenza di amminoacidi 4 x
Proprietà comuni. Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici
 Gli aminoacidi Proprietà comuni Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici paragonabili Il gruppo α-aminico è un acido più forte (o una base più debole
Gli aminoacidi Proprietà comuni Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici paragonabili Il gruppo α-aminico è un acido più forte (o una base più debole
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA)
 La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) POLIMERI Le cellule sintetizzano un enorme numero di grosse molecole a partire da una ristretta serie di
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) POLIMERI Le cellule sintetizzano un enorme numero di grosse molecole a partire da una ristretta serie di
IPOTESI UN GENE-UN ENZIMA
 IPOTESI UN GENE-UN ENZIMA DNA: contiene tutte le informazioni per definire lo sviluppo e la fisiologia della cellula: ma come svolge questa funzione? Beadle e Tatum (1941): studiando mutanti della comune
IPOTESI UN GENE-UN ENZIMA DNA: contiene tutte le informazioni per definire lo sviluppo e la fisiologia della cellula: ma come svolge questa funzione? Beadle e Tatum (1941): studiando mutanti della comune
Amminoacidi Peptidi Proteine
 Amminoacidi Peptidi Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Gli amminoacidi nelle molecole proteiche sono tutti stereoisomeri L IDROFOBOCI IDROFOBOCI IDROFILICI Secondo gruppo
Amminoacidi Peptidi Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Gli amminoacidi nelle molecole proteiche sono tutti stereoisomeri L IDROFOBOCI IDROFOBOCI IDROFILICI Secondo gruppo
BIOMOLECOLE LE BASI DELLA BIOCHIMICA. Capitolo 1 Dal Carbonio agli OGM PLUS
 BIOMOLECOLE LE BASI DELLA BIOCHIMICA Capitolo 1 Dal Carbonio agli OGM PLUS BIOMOLECOLE Carboidrati Lipidi Acidi Nucleici Proteine BIOMOLECOLE Carboidrati Lipidi Acidi Nucleici - monosaccaridi - disaccaridi
BIOMOLECOLE LE BASI DELLA BIOCHIMICA Capitolo 1 Dal Carbonio agli OGM PLUS BIOMOLECOLE Carboidrati Lipidi Acidi Nucleici Proteine BIOMOLECOLE Carboidrati Lipidi Acidi Nucleici - monosaccaridi - disaccaridi
STRUTTURA TERZIARIA. H 3 N + COO - β-foglietto
 STRUTTURA TERZIARIA α-eliche H 3 N + COO - β-foglietto La catena polipeptidica delle proteine GLOBULARI oltre ad organizzarsi in strutture di tipo secondario va incontro ad un ulteriore ripiegamento sino
STRUTTURA TERZIARIA α-eliche H 3 N + COO - β-foglietto La catena polipeptidica delle proteine GLOBULARI oltre ad organizzarsi in strutture di tipo secondario va incontro ad un ulteriore ripiegamento sino
Macromolecole Biologiche. La struttura secondaria (I)
 La struttura secondaria (I) La struttura secondaria Struttura primaria PRPLVALLDGRDETVEMPILKDVATVAFCDAQSTQEIHE Struttura secondaria La struttura secondaria Le strutture secondarie sono disposizioni regolari
La struttura secondaria (I) La struttura secondaria Struttura primaria PRPLVALLDGRDETVEMPILKDVATVAFCDAQSTQEIHE Struttura secondaria La struttura secondaria Le strutture secondarie sono disposizioni regolari
