FENOMENI ELETTRICI. FENOMENI ELETTRICI eq. elettroch.. e soluz.elettr. elio giroletti
|
|
|
- Dario Italo Calabrese
- 5 anni fa
- Visualizzazioni
Transcript
1 elio giroletti UNIVERSITÀ DEGLI STUDI DI PAVIA dip. Fisica nucleare e teorica via bassi 6, 700 pavia, tel girolett@unipv.it - webgiro FENOMENI ELETTRICI eq. elettroch.. e soluz.elettr. FISICA MEDICA e RADIOPROTEZIONE elio giroletti,, 005 Classe Lauree di INFERMIERISTICA e OSTETRICIA corso integrato FISICA, STATISTICA e INFORMATICA disciplina: FISICA MEDICA e RADIOPROTEZIONE FENOMENI ELETTRICI soluzioni eq. elettroch. elettrolitiche. e soluz.elettr. FISICA MEDICA e RADIOPROTEZIONE elio giroletti,, Dissociazione elettrolitica - Mobilità elettrolitica - Soluzioni elettrolitiche - Flussi elettrochimici - Sunto dei meccanismi di trasporto passivo lucidi di Domenico Scannicchio, rivisti da Elio Giroletti
2 DISSOCIAZIONE ELETTROLITICA legame ionico (forza di Coulomb) I :indebolimento del legame esempio: NaCl in acqua Na + Cl F = qq c 4π ε o ε r r ε r (aria) ε r (acqua) 80 costante dielettrica F C (acqua) 80 F C (aria) DISSOCIAZIONE ELETTROLITICA II : rottura del legame da urti per agitazione termica coefficiente dissociazione elettrolitica δ = δ (T) δ = ν + + ν + ν o N δ n percentuale di dissociazione α = α (T) α = ν o N 0 α α rappresenta % di molecole dissociate DISSOCIAZIONE ELETTROLITICA III : mancata ricombinazione da polarità molecola H O Na O H Cl conduttori elettrolitici: acidi, basi, sali in H O δ > sostanze organiche forte legame covalente} δ esempio NaCl in HO δ = molecole NaCl 84 Na + 84 Cl 6 NaCl (non dissociate) 84 particelle +
3 Elettrolisi 3 moto di ioni (q = Ze ) in soluzione ioni + elettrodo negativo + G (catodo, K) A ioni elettrodo positivo (anodo, A ) esempio I + S I nitrato d'argento in acqua AgNO 3 Ag + + NO 3 deposito al catodo di una massa (m) di peso atomico (A) e valenza (V) leggi di Faraday m = k A Z q k = No e anodo E B catodo A/Z = equivalente chimico SOLUZIONI ELETTROLITICHE ioni in soluzione concentrazione osmolare = n moli volume unità di misura soluzioni elettrolitiche g-ione (0 C) litro osmole {A+ A+} g-equivalente ( Eq ) litro l g-equivalente litro = frazione g-ione (q=n o e) litro * g-eq trasporta una carica elettrica q pari alla costante di Faraday Costante di Faraday = F = N o e = C * SOLUZIONI ELETTROLITICHE g-equivalente frazione g-ione q=no e (*) = litro litro (*) che trasporta una carica q pari alla costante di Faraday q=no e = F = 6,0 0 3,6 0 9 = C ione monovalente ione bivalente ione Z-valente g-eq = g-ione g-eq = g-ione g-eq = Z g-ione g Eq C = lt C[ osmole] Z
4 Composizione del plasma soluto C (g/lt) C (moli/lt)0-3 C (eq/lt)0-3 Z Na+ 3,5 4,5 4,5 + K+ 0, 5,5 5,5 + Ca++ 0,,5 5,0 + Mg+ 0,04,0,0 + Elettrolitivari+ 0,0,0,0 + Cl- 3,6 0,0 0,0 - HCO-,65 8,0 8,0 - HPO 4-0,063,0,0 - Proteine 70,0,0 8,0-8 Elettrolitivari- 0, 6,0 6,0 - Urea CO(NH ) Glucosio C H O 0,3 5,0 I sistemi biologici sono 0,8 5,0 costituiti da 6 6 Non elettroliti vari 0, 9,5 soluzioni elettrolitiche: TOTALE 30 solvente H O e una miriade di soluti 4 MOBILITA' ELETTROLITICA moto di ioni (q = Ze ) in soluzione F = Ze E F a = f v v s = F = Ze E = µ E f f µ = Ze µ =mobilità ionica f e + f=coeff. attrito viscoso G A B A anodo a + S b E i = q t K catodo Z a =Z b =Z C a+ {A + } {x+} = concentr.osmolare dello ione x + (g-ione/litro a 0 C) (osmole) = No Ze {a + } S v a + No Ze {b } S v b = MOBILITA' ELETTROLITICA = No Ze S v a {a + } + v b {b } = = Ze No S µ a {a + } + µ b {b } E v s = µ E i = Ze No S µ a {a + }+µ b {b } E J = i = Ze No S µ a {a+ } + µ b {b } E J = σe conducibilità elettrolitica σ legge generalizzata di Ohm in presenza di molti ioni J = ZeN µ {} i 0 i
5 V V C a+ {A + } E= V/ V/ FLUSSI ELETTROCHIMICI J EsM COMPARTIMENTO M COMPARTIMENTO V V soluzione elettrolitica q J EsM mole = J EsM No Ze = J J EsM = J No Ze = σ E No Ze = V V σ No Ze soluzione elettrolitica = Ze No No Ze µ s {s} V V = µ s {s} V V = x σ= No Ze µ s {s} EsM = flusso Soluto prodotto dal campo elettrico, E 5 FLUSSI ELETTROCHIMICI COMPARTIMENTO M COMPARTIMENTO V V E= V/ soluzione elettrolitica J EsM = µ s {s} V V 0 V V J EsM = µ s C M ( φ) V V J EsM = flusso Soluto prodotto dal campo E soluzione elettrolitica x µ s = Ze = f Ze No D R T (formula di Einstein-Stokes f=rt/n 0 D) Tenendo conto della semi- permeabilità della membrana ( φ) = ε FLUSSI ELETTROCHIMICI 3 J EsM = µ s C M ( φ) V V J EsM ( φ) = ε EsM = flusso Soluto prodotto dal campo Elettrico E attraverso la membrana mbrana M J EsM = µ s C M ( φ) grad V = µ s C M ( φ) ) E µ s = Ze No D R T C M = C + C α α=coeff. partizione meccanismo gradiente di potenziale elettrico (campo elettrico)
6 MECCANISMI DI TRASPORTO PASSIVO 6 J sim = P i C C im ( φ i )L p p µ i C im ( φ i ) V diffusione (grad C) filtrazione (grad p) J VM = L p p + i φ i + ε i = φ i (D i )= coeff. riflessione (diffusione libera) soluto i P = α n π r i = ε i D ε i D i i = coeff. permeabilità C M =α conc.. media nella membrana di spess. (C + C ) = coefficiente di filtrazione L p = n 8η π r4 cm/(s.atm) µ i = Ze No D mobilità ionica del soluto-ione i-esimo R T i = i =,,... soluti diversi osmosi (grad π) campo elettrico (grad V) L p φ i π C=C -C FENOMENI ELETTRICI equil. eq. elettroch.. elettrochimico. e soluz.elettr. FISICA MEDICA e RADIOPROTEZIONE elio giroletti,, equilibrio elettrochimico - aspetti biologici e biochimici lucidi di Domenico Scannicchio, rivisti da Elio Giroletti POTENZIALE ELETTROCHIMICO n moli / n gr-ioni = energia potenziale chimica µ = RT ln C + µo energia potenziale elettrica U = q V energia potenziale elettro-chimica µ = RT ln C + q V + µo Ze No carica elettrica di un g-ione µ = RT ln C + Ze NoV + µo potenziale elettrochimico (relativo a n= g-ione)
7 7 potenziale elettrochimico µ = RT ln C + Ze No V + µo stato di equilibrio ai lati della membrana µ µ = 0 RT ln C + Ze NoV RT ln C Ze NoV =0 RT ln C RT ln C + Ze NoV Ze NoV =0 Ze NoV Ze NoV = RT ln C RT ln C ZNo e (V V ) = RT ln C C cost. Faraday= F= No e = 96487C ZNo e (V V ) = RT ln C C V V = RT FZ ln C C equazione di Nernst relazione di equilibrio ai lati della membrana Costante di Faraday = F = No e = 96487C 3 equazione di Nernst V V = RT FZ ln C C membrana permeabile equilibrio: C = C V = V membrana semipermeabile equilibrio: C C V V
8 oppure equilibrio dinamico J EsM + J DsM = J EsM = flusso di Soluto prodotto al campo Elettrico J DsM = flusso di Soluto prodotto dalla Diffusione equazione di Nernst V V = RT FZ ln C C 5 equazione di Nernst V V = RT FZ ln C C conseguenze: fenomeni bioelettrici potenziale di membrana cellulare potenziale d'azione FENOMENI ELETTRICI eq. elettroch.. e soluz.elettr. FISICA MEDICA e RADIOPROTEZIONE elio giroletti,, 005 dispense su internet webgiro elio giroletti. Università degli Studi di Pavia dip. Fisica nucleare e teorica girolett@unipv.it
Dipartimento Scientifico-Tecnologico
 ISTITUTO TECNICO STATALE LUIGI STURZO Castellammare di Stabia - NA Anno scolastico 2012-13 Dipartimento Scientifico-Tecnologico CHIMICA, FISICA, SCIENZE E TECNOLOGIE APPLICATE Settore Economico Indirizzi:
ISTITUTO TECNICO STATALE LUIGI STURZO Castellammare di Stabia - NA Anno scolastico 2012-13 Dipartimento Scientifico-Tecnologico CHIMICA, FISICA, SCIENZE E TECNOLOGIE APPLICATE Settore Economico Indirizzi:
DETERMINAZIONE DEL PUNTO DI FINE TITOLAZIONE MEDIANTE METODI CHIMICO-FISICI
 DETERMINAZIONE DEL PUNTO DI FINE TITOLAZIONE MEDIANTE METODI CHIMICO-FISICI - si sfrutta una proprietà chimico-fisica o fisica che varia nel corso della titolazione - tale proprietà è in genere proporzionale
DETERMINAZIONE DEL PUNTO DI FINE TITOLAZIONE MEDIANTE METODI CHIMICO-FISICI - si sfrutta una proprietà chimico-fisica o fisica che varia nel corso della titolazione - tale proprietà è in genere proporzionale
... corso di chimica elettrochimica 1
 ... corso di chimica elettrochimica 1 CONTENUTI reazioni elettrochimiche pile e celle elettrolitiche potenziale d elettrodo e forza elettromotrice equazione di Nernst elettrolisi leggi di Faraday batterie
... corso di chimica elettrochimica 1 CONTENUTI reazioni elettrochimiche pile e celle elettrolitiche potenziale d elettrodo e forza elettromotrice equazione di Nernst elettrolisi leggi di Faraday batterie
2. Fisiologia Cellulare Diffusione, Trasporto, Osmosi
 2. Fisiologia Cellulare Diffusione, Trasporto, Osmosi Prof. Carlo Capelli Fisiologia Laurea in Scienze delle attività motorie e sportive Università di Verona Obiettivi Diffusione semplice e mediata da
2. Fisiologia Cellulare Diffusione, Trasporto, Osmosi Prof. Carlo Capelli Fisiologia Laurea in Scienze delle attività motorie e sportive Università di Verona Obiettivi Diffusione semplice e mediata da
Università degli Studi di Pavia Facoltà di Medicina e Chirurgia
 Università degli Studi di Pavia Facoltà di Medicina e Chirurgia CORSO DI LAUREA TRIENNALE CLASSE DELLLE LAUREE DELLE PROFESSIONI SANITARIE DELLA RIABILITAZIONE CLASSE 2 Corso Integrato di Fisica, Statistica,
Università degli Studi di Pavia Facoltà di Medicina e Chirurgia CORSO DI LAUREA TRIENNALE CLASSE DELLLE LAUREE DELLE PROFESSIONI SANITARIE DELLA RIABILITAZIONE CLASSE 2 Corso Integrato di Fisica, Statistica,
Potenziale di membrana: Differenza di potenziale elettrico a cavallo della membrana cellulare dovuta ad una diversa distribuzione ionica ai due lati
 Potenziale di membrana: Differenza di potenziale elettrico a cavallo della membrana cellulare dovuta ad una diversa distribuzione ionica ai due lati della membrana. Il potenziale di membrana (negativo
Potenziale di membrana: Differenza di potenziale elettrico a cavallo della membrana cellulare dovuta ad una diversa distribuzione ionica ai due lati della membrana. Il potenziale di membrana (negativo
ELETTROCHIMICA. Uso di reazioni chimiche per produrre corrente elettrica (Pile)
 ELETTROCHIMICA Uso di reazioni chimiche per produrre corrente elettrica (Pile) Uso di forza elettromotrice (fem) esterna per forzare reazioni chimiche non spontanee (Elettrolisi) Coppia redox: Ossidazione
ELETTROCHIMICA Uso di reazioni chimiche per produrre corrente elettrica (Pile) Uso di forza elettromotrice (fem) esterna per forzare reazioni chimiche non spontanee (Elettrolisi) Coppia redox: Ossidazione
La serie elettrochimica dei potenziali standard di riduzione (25 C)
 MIGLIORI RIDUCENTI MIGLIORI OSSIDANTI La serie elettrochimica dei potenziali standard di riduzione (25 C) ELETTROLISI Una cella elettrolitica è una cella nella quale una corrente fa avvenire una reazione
MIGLIORI RIDUCENTI MIGLIORI OSSIDANTI La serie elettrochimica dei potenziali standard di riduzione (25 C) ELETTROLISI Una cella elettrolitica è una cella nella quale una corrente fa avvenire una reazione
CHIMICA e LABORATORIO e SCIENZE E TECNOLOGIA. L attività del lavoro estivo verrà verificato nei primi giorni dopo le vacanze.
 COMPITI PER LE VACANZE E ATTIVITA PER IL RECUPERO a.s. 2014/2015 SECONDA E ITIS CHIMICA e LABORATORIO e SCIENZE E TECNOLOGIA L attività del lavoro estivo verrà verificato nei primi giorni dopo le vacanze.
COMPITI PER LE VACANZE E ATTIVITA PER IL RECUPERO a.s. 2014/2015 SECONDA E ITIS CHIMICA e LABORATORIO e SCIENZE E TECNOLOGIA L attività del lavoro estivo verrà verificato nei primi giorni dopo le vacanze.
Dissociazione elettrolitica
 Dissociazione elettrolitica Le sostanze ioniche si solubilizzano liberando ioni in soluzione. La dissociazione elettrolitica è il processo con cui un solvente separa ioni di carica opposta e si lega ad
Dissociazione elettrolitica Le sostanze ioniche si solubilizzano liberando ioni in soluzione. La dissociazione elettrolitica è il processo con cui un solvente separa ioni di carica opposta e si lega ad
Equilibri di precipitazione
 Equilibri di precipitazione Molte sostanze solide sono caratterizzate da una scarsa solubilità in acqua (ad es. tutti i carbonati e gli idrossidi degli elementi del II gruppo) AgCl (a differenza di NaCl)
Equilibri di precipitazione Molte sostanze solide sono caratterizzate da una scarsa solubilità in acqua (ad es. tutti i carbonati e gli idrossidi degli elementi del II gruppo) AgCl (a differenza di NaCl)
Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I
 Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I BIOFISICA DELLE MEMBRANE BIOFISICA DELLE MEMBRANE Le funzioni biologiche di tutti gli organismi viventi si svolgono mediante
Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I BIOFISICA DELLE MEMBRANE BIOFISICA DELLE MEMBRANE Le funzioni biologiche di tutti gli organismi viventi si svolgono mediante
Elettrolisi del solfato di rame
 Elettrolisi del solfato di rame Calcolo dell equivalente equivalente elettrochimico del rame Calcolo del valore della carica elementare Un po di storia 1800 - Invenzione della pila di Volta 1807 - Davy,,
Elettrolisi del solfato di rame Calcolo dell equivalente equivalente elettrochimico del rame Calcolo del valore della carica elementare Un po di storia 1800 - Invenzione della pila di Volta 1807 - Davy,,
MEMBRANE. MEMBRANE equilibri gas-liquido. elio giroletti
 UNIVERSITÀ DEGLI STUDI DI PAVIA dip. Fisica nucleare e teorica via Bassi 6, 27100 Pavia, Italy tel. 0382/98.7905 - girolett@unipv.it - www.unipv.it/webgiro 1 elio giroletti MEMBRANE equilibri gas- FISICA
UNIVERSITÀ DEGLI STUDI DI PAVIA dip. Fisica nucleare e teorica via Bassi 6, 27100 Pavia, Italy tel. 0382/98.7905 - girolett@unipv.it - www.unipv.it/webgiro 1 elio giroletti MEMBRANE equilibri gas- FISICA
Elettrochimica. 1. Celle elettrolitiche. 2. Celle galvaniche o pile
 Elettrochimica L elettrochimica studia l impiego di energia elettrica per promuovere reazioni non spontanee e l impiego di reazioni spontanee per produrre energia elettrica, entrambi i processi coinvolgono
Elettrochimica L elettrochimica studia l impiego di energia elettrica per promuovere reazioni non spontanee e l impiego di reazioni spontanee per produrre energia elettrica, entrambi i processi coinvolgono
Integrali (transmembrana), si estendono attraverso l intera membrana. Classificate in famiglie a seconda del numero di segmenti transmembrana.
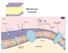 Membrana cellulare Proteine inserite nella membrana cellulare: Integrali (transmembrana), si estendono attraverso l intera membrana. Classificate in famiglie a seconda del numero di segmenti transmembrana.
Membrana cellulare Proteine inserite nella membrana cellulare: Integrali (transmembrana), si estendono attraverso l intera membrana. Classificate in famiglie a seconda del numero di segmenti transmembrana.
Il mantenimento dell omeostasi cellulare dipende dai sistemi che permettono lo scambio di molecole tra citoplasma e liquido
 Il mantenimento dell omeostasi cellulare dipende dai sistemi che permettono lo scambio di molecole tra citoplasma e liquido extracellulare e dalla loro regolazione. Membrana cellulare Ogni cellula presenta
Il mantenimento dell omeostasi cellulare dipende dai sistemi che permettono lo scambio di molecole tra citoplasma e liquido extracellulare e dalla loro regolazione. Membrana cellulare Ogni cellula presenta
Bioingegneria Elettronica I
 Bioingegneria Elettronica I Cenni alla fisiologia delle cellule e dei sistemi biologici A. Bonfiglio La cellula struttura generale La cellula Struttura generale della cellula Composizione dei liquidi intracellulare
Bioingegneria Elettronica I Cenni alla fisiologia delle cellule e dei sistemi biologici A. Bonfiglio La cellula struttura generale La cellula Struttura generale della cellula Composizione dei liquidi intracellulare
REAZIONI ORGANICHE Variazioni di energia e velocità di reazione
 REAZIONI ORGANICHE Variazioni di energia e velocità di reazione Abbiamo visto che i composti organici e le loro reazioni possono essere suddivisi in categorie omogenee. Per ottenere la massima razionalizzazione
REAZIONI ORGANICHE Variazioni di energia e velocità di reazione Abbiamo visto che i composti organici e le loro reazioni possono essere suddivisi in categorie omogenee. Per ottenere la massima razionalizzazione
STATO LIQUIDO. Si definisce tensione superficiale (γ) il lavoro che bisogna fare per aumentare di 1 cm 2 la superficie del liquido.
 STTO LIQUIDO Una sostanza liquida è formata da particelle in continuo movimento casuale, come in un gas, tuttavia le particelle restano a contatto le une alle altre e risentono sempre delle notevoli forze
STTO LIQUIDO Una sostanza liquida è formata da particelle in continuo movimento casuale, come in un gas, tuttavia le particelle restano a contatto le une alle altre e risentono sempre delle notevoli forze
Trattamenti delle acque primarie
 Trattamenti Impianti Meccanici 1 ELIMINAZIONE DELL ANIDRIDE CARBONICA ELIMINAZIONE DELL OSSIGENO AEREAZIONE DELL ACQUA DEFERRITIZZAZIONE DEMANGANIZZAZIONE ADDOLCIMENTO Impianti Meccanici 2 1 Trattamenti
Trattamenti Impianti Meccanici 1 ELIMINAZIONE DELL ANIDRIDE CARBONICA ELIMINAZIONE DELL OSSIGENO AEREAZIONE DELL ACQUA DEFERRITIZZAZIONE DEMANGANIZZAZIONE ADDOLCIMENTO Impianti Meccanici 2 1 Trattamenti
INTERAZIONI DELLE RADIAZIONI CON LA MATERIA
 M. Marengo INTERAZIONI DELLE RADIAZIONI CON LA MATERIA Servizio di Fisica Sanitaria Ospedale Policlinico S.Orsola - Malpighi, Bologna mario.marengo@unibo.it Si definiscono radiazioni ionizzanti tutte le
M. Marengo INTERAZIONI DELLE RADIAZIONI CON LA MATERIA Servizio di Fisica Sanitaria Ospedale Policlinico S.Orsola - Malpighi, Bologna mario.marengo@unibo.it Si definiscono radiazioni ionizzanti tutte le
L H 2 O nelle cellule vegetali e
 L H 2 O nelle cellule vegetali e il suo trasporto nella pianta H 2 O 0.96 Å H O 105 H 2s 2 2p 4 tendenza all ibridizzazione sp 3 H δ+ O δ- δ+ 1.75 Å H legame idrogeno O δ- H H δ+ δ+ energia del legame
L H 2 O nelle cellule vegetali e il suo trasporto nella pianta H 2 O 0.96 Å H O 105 H 2s 2 2p 4 tendenza all ibridizzazione sp 3 H δ+ O δ- δ+ 1.75 Å H legame idrogeno O δ- H H δ+ δ+ energia del legame
Liquidi, Solidi e Forze Intermolecolari
 Liquidi, Solidi e Forze Intermolecolari Distanze tra molecole Stati Fisici (Fase) Comportamento atipico La maggiore differenza tra liquidi e solidi consiste nella libertà di movimento delle loro molecole
Liquidi, Solidi e Forze Intermolecolari Distanze tra molecole Stati Fisici (Fase) Comportamento atipico La maggiore differenza tra liquidi e solidi consiste nella libertà di movimento delle loro molecole
Miscela omogenea monofasica i cui costituenti non è possibile separare meccanicamente
 Miscela omogenea monofasica i cui costituenti non è possibile separare meccanicamente Soluzioni Sistema Omogeneo (presenta le stesse proprietà in qualsiasi sua porzione) Monofasico Nella fase omogenea
Miscela omogenea monofasica i cui costituenti non è possibile separare meccanicamente Soluzioni Sistema Omogeneo (presenta le stesse proprietà in qualsiasi sua porzione) Monofasico Nella fase omogenea
Energia elettrica. L atomo nel suo complesso è neutro perché ha l equilibrio tra protoni ed elettroni presenti nello stesso numero.
 Energia elettrica Si fonda sulla costituzione dell atomo che è costituito da particelle più piccole : neutroni (carica neutra) e protoni (carica +) che costituiscono il nucleo ed elettroni (carica negativa)
Energia elettrica Si fonda sulla costituzione dell atomo che è costituito da particelle più piccole : neutroni (carica neutra) e protoni (carica +) che costituiscono il nucleo ed elettroni (carica negativa)
Fenomeni elettrici (2)
 Roberto irio orso di Laurea in himica e Tecnologia Farmaceutiche Anno accademico 2007 2008 orso di Fisica La lezione di oggi I condensatori e le resistenze ircuiti elettrici con condensatori e resistenze
Roberto irio orso di Laurea in himica e Tecnologia Farmaceutiche Anno accademico 2007 2008 orso di Fisica La lezione di oggi I condensatori e le resistenze ircuiti elettrici con condensatori e resistenze
Indice. 1 La materia e la sua struttura. 2 La radioattività ed i processi nucleari
 Indice PREFAZIONE XIII 1 La materia e la sua struttura 1.1. Le particelle fondamentali e la struttura dell atomo 2 1.2. Il numero atomico, il numero di massa, i nuclidi e gli isotopi 5 1.3. L unità di
Indice PREFAZIONE XIII 1 La materia e la sua struttura 1.1. Le particelle fondamentali e la struttura dell atomo 2 1.2. Il numero atomico, il numero di massa, i nuclidi e gli isotopi 5 1.3. L unità di
ITT BUONARROTI MATERIA: S.I. FISICA E LABORATORIO
 ITT BUONARROTI MATERIA: S.I. FISICA E LABORATORIO Programmazione 2013-2014 Quella che viene qui presentato è la programmazione per moduli disciplinari, nel quale vengono evidenziati: l idea stimolo; i
ITT BUONARROTI MATERIA: S.I. FISICA E LABORATORIO Programmazione 2013-2014 Quella che viene qui presentato è la programmazione per moduli disciplinari, nel quale vengono evidenziati: l idea stimolo; i
Indice. 1 La materia e la sua struttura. 2 La radioattività ed i processi nucleari
 Indice PREFAZIONE ALLA SECONDA EDIZIONE XIII 1 La materia e la sua struttura 1.1. Le particelle fondamentali e la struttura dell atomo 2 1.2. Il numero atomico, il numero di massa, i nuclidi e gli isotopi
Indice PREFAZIONE ALLA SECONDA EDIZIONE XIII 1 La materia e la sua struttura 1.1. Le particelle fondamentali e la struttura dell atomo 2 1.2. Il numero atomico, il numero di massa, i nuclidi e gli isotopi
Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I A.A. 2015-16
 Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I A.A. 2015-16 BIOFISICA DELLE MEMBRANE Negli organismi pluricellulari, a parte i tessuti tegumentari e gli epiteli assorbenti
Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I A.A. 2015-16 BIOFISICA DELLE MEMBRANE Negli organismi pluricellulari, a parte i tessuti tegumentari e gli epiteli assorbenti
Esercizi di Chimica (2 a prova in itinere)
 Esercizi di Chimica (2 a prova in itinere) 3) Calcolare la normalità (N) di una soluzione ottenuta sciogliendo 3,5 g di H 3 PO 4 in 900 ml di acqua [0,119 N] 4) Quanti grammi di soluto sono contenuti in
Esercizi di Chimica (2 a prova in itinere) 3) Calcolare la normalità (N) di una soluzione ottenuta sciogliendo 3,5 g di H 3 PO 4 in 900 ml di acqua [0,119 N] 4) Quanti grammi di soluto sono contenuti in
Chimica Fisica I. a.a. 2012/2013 S. Casassa
 a.a. 2012/2013 S. Casassa 1 Note Tecniche 2 Testi consigliati: G.K. Vemulapalli, Chimica Fisica", EdiSES, Napoli (1995). D.A. Mc Quarrie e J.D. Simon, Chimica Fisica: un approccio molecolare", Zanichelli,
a.a. 2012/2013 S. Casassa 1 Note Tecniche 2 Testi consigliati: G.K. Vemulapalli, Chimica Fisica", EdiSES, Napoli (1995). D.A. Mc Quarrie e J.D. Simon, Chimica Fisica: un approccio molecolare", Zanichelli,
ISTITUTO ISTRUZIONE SUPERIORE "L. EINAUDI" ALBA ANNO SCOLASTICO 2015/2016. CLASSI SECONDE ITI, SEZ. H,G, Disciplina:CHIMICA E LABORATORIO
 ISTITUTO ISTRUZIONE SUPERIORE "L. EINAUDI" ALBA ANNO SCOLASTICO 2015/2016 CLASSI SECONDE ITI, SEZ. H,G, Disciplina:CHIMICA E LABORATORIO PROGETTAZIONE DIDATTICA ANNUALE Elaborata conformemente alle linee
ISTITUTO ISTRUZIONE SUPERIORE "L. EINAUDI" ALBA ANNO SCOLASTICO 2015/2016 CLASSI SECONDE ITI, SEZ. H,G, Disciplina:CHIMICA E LABORATORIO PROGETTAZIONE DIDATTICA ANNUALE Elaborata conformemente alle linee
LA MOLE LA MOLE 2.A PRE-REQUISITI 2.3 FORMULE E COMPOSIZIONE 2.B PRE-TEST
 LA MOLE 2.A PRE-REQUISITI 2.B PRE-TEST 2.C OBIETTIVI 2.1 QUANTO PESA UN ATOMO? 2.1.1 L IDEA DI MASSA RELATIVA 2.1.2 MASSA ATOMICA RELATIVA 2.2.4 ESERCIZI SVOLTI 2.3 FORMULE E COMPOSIZIONE 2.4 DETERMINAZIONE
LA MOLE 2.A PRE-REQUISITI 2.B PRE-TEST 2.C OBIETTIVI 2.1 QUANTO PESA UN ATOMO? 2.1.1 L IDEA DI MASSA RELATIVA 2.1.2 MASSA ATOMICA RELATIVA 2.2.4 ESERCIZI SVOLTI 2.3 FORMULE E COMPOSIZIONE 2.4 DETERMINAZIONE
I segnali elettrici generati nei neuroni sono modificazioni del potenziale di riposo determinate dall apertura o chiusura di canali ionici:
 I segnali elettrici generati nei neuroni sono modificazioni del potenziale di riposo determinate dall apertura o chiusura di canali ionici: Potenziali graduati (risposte passive): modulabili in ampiezza,
I segnali elettrici generati nei neuroni sono modificazioni del potenziale di riposo determinate dall apertura o chiusura di canali ionici: Potenziali graduati (risposte passive): modulabili in ampiezza,
Biosensori Sensori Chimici. nicola.carbonaro@centropiaggio.unipi.it
 Biosensori Sensori Chimici nicola.carbonaro@centropiaggio.unipi.it Principali applicazioni dei Sensori chimici Ruolo fondamentale degli ioni nella maggior parte dei processi biologici Sensori elettrochimici
Biosensori Sensori Chimici nicola.carbonaro@centropiaggio.unipi.it Principali applicazioni dei Sensori chimici Ruolo fondamentale degli ioni nella maggior parte dei processi biologici Sensori elettrochimici
LA CELLULA ED I TRASPORTI ATTRAVERSO LA MEMBRANA PLASMATICA
 LA CELLULA ED I TRASPORTI ATTRAVERSO LA MEMBRANA PLASMATICA LA FUNZIONE E IL PROCESSO La funzione di un sistema o evento fisiologico è il perché il sistema esiste. Il processo indica la modalità attraverso
LA CELLULA ED I TRASPORTI ATTRAVERSO LA MEMBRANA PLASMATICA LA FUNZIONE E IL PROCESSO La funzione di un sistema o evento fisiologico è il perché il sistema esiste. Il processo indica la modalità attraverso
Galvanostegia. Obiettivi: - Descrivere come placcare un oggetto - Essere in grado di scegliere l elettrolita da usare, l'anodo ed il catodo
 Galvanostegia Obiettivi: - Descrivere come placcare un oggetto - Essere in grado di scegliere l elettrolita da usare, l'anodo ed il catodo Che cos è la Galvanostegia? Un processo elettrochimico in cui
Galvanostegia Obiettivi: - Descrivere come placcare un oggetto - Essere in grado di scegliere l elettrolita da usare, l'anodo ed il catodo Che cos è la Galvanostegia? Un processo elettrochimico in cui
Corso vapore Riassunto Acque. L acqua per punti. Chimica, effetti, trattamenti, analisi.
 L acqua per punti. Chimica, effetti, trattamenti, analisi. Indice 1) L acqua.. 1 a. Richiami di chimica: sali, ioni, ph & Co... 1 b. Non solo H 2 O... 2 c. Effetti sugli impianti delle sostanze contenute
L acqua per punti. Chimica, effetti, trattamenti, analisi. Indice 1) L acqua.. 1 a. Richiami di chimica: sali, ioni, ph & Co... 1 b. Non solo H 2 O... 2 c. Effetti sugli impianti delle sostanze contenute
PROGRAMMAZIONE ANNUALE A.S. 2015/2016 DISCIPLINA: CHIMICA CLASSE: 2^A - INDIRIZZO: CHIMICA, MATERIALI E BIOTECNOLOGIE
 RE P U B B L I C A I T A L I A N A ISTITUTO DI ISTRUZIONE SECONDARIA SUPERIORE MINERARIO G. ASPRONI E. FERMI DI IGLESIAS PROGRAMMAZIONE ANNUALE A.S. 2015/2016 DISCIPLINA: CHIMICA CLASSE: 2^A - INDIRIZZO:
RE P U B B L I C A I T A L I A N A ISTITUTO DI ISTRUZIONE SECONDARIA SUPERIORE MINERARIO G. ASPRONI E. FERMI DI IGLESIAS PROGRAMMAZIONE ANNUALE A.S. 2015/2016 DISCIPLINA: CHIMICA CLASSE: 2^A - INDIRIZZO:
Elettroforesi. Elettroforesi: processo per cui molecole cariche si separano in un campo elettrico a causa della loro diversa mobilita.
 Elettroforesi Elettroforesi: processo per cui molecole cariche si separano in un campo elettrico a causa della loro diversa mobilita. A qualunque ph diverso dal pi le proteine hanno una carica netta quindi,
Elettroforesi Elettroforesi: processo per cui molecole cariche si separano in un campo elettrico a causa della loro diversa mobilita. A qualunque ph diverso dal pi le proteine hanno una carica netta quindi,
Elettrolita forte = specie chimica che in soluzione si dissocia completamente (l equilibrio di dissociazione è completamente spostato verso destra)
 A.A. 2005/2006 Laurea triennale in Chimica Esercitazioni di stechiometria - Corso di Chimica Generale ed inorganica C ARGOMENTO 6: Equilibri in soluzione: equilibri acido/base, idrolisi e tamponi (6 h)
A.A. 2005/2006 Laurea triennale in Chimica Esercitazioni di stechiometria - Corso di Chimica Generale ed inorganica C ARGOMENTO 6: Equilibri in soluzione: equilibri acido/base, idrolisi e tamponi (6 h)
La membrana cellulare racchiude il protoplasma, la sostanza vivente che costituisce la cellula, e lo separa dall ambiente esterno, extracellulare.
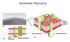 Membrana Plasmatica La membrana cellulare racchiude il protoplasma, la sostanza vivente che costituisce la cellula, e lo separa dall ambiente esterno, extracellulare. La sua funzione principale è quella
Membrana Plasmatica La membrana cellulare racchiude il protoplasma, la sostanza vivente che costituisce la cellula, e lo separa dall ambiente esterno, extracellulare. La sua funzione principale è quella
La conducibilità elettrica nelle soluzioni di elettroliti forti.
 La conducibilità elettrica nelle soluzioni di elettroliti forti. Salvatore Regalbuto e Sonia Formica 8 Istituto Statale di Istruzione Secondaria Superiore Quintiliano Siracusa Misurazione della conducibilità
La conducibilità elettrica nelle soluzioni di elettroliti forti. Salvatore Regalbuto e Sonia Formica 8 Istituto Statale di Istruzione Secondaria Superiore Quintiliano Siracusa Misurazione della conducibilità
PRECIPITAZIONE FRAZIONATA DI PROTEINE Obiettivo: separare proteine sfruttando differenze di solubilità
 PRECIPITAZIONE FRAZIONATA DI PROTEINE Obiettivo: separare proteine sfruttando differenze di solubilità SOLUBILITA DELLE PROTEINE ph FORZA IONICA SOLVENTI POLIMERI ORGANICI TEMPERATURA Effetto del ph Precipitazione
PRECIPITAZIONE FRAZIONATA DI PROTEINE Obiettivo: separare proteine sfruttando differenze di solubilità SOLUBILITA DELLE PROTEINE ph FORZA IONICA SOLVENTI POLIMERI ORGANICI TEMPERATURA Effetto del ph Precipitazione
Capitolo n. 4 - Metodi elettrochimici
 Capitolo n. 4 - Metodi elettrochimici 4.3.1 - Conducibilità elettrica delle soluzioni La conduttimetria è una tecnica analitica basata sulla misura della conducibilità elettrica delle soluzioni elettrolitiche
Capitolo n. 4 - Metodi elettrochimici 4.3.1 - Conducibilità elettrica delle soluzioni La conduttimetria è una tecnica analitica basata sulla misura della conducibilità elettrica delle soluzioni elettrolitiche
gli stati inusuali della materia: il PLASMA e i COLLOIDI Pietro Favia, Gerardo Palazzo
 gli stati inusuali della materia: il PLASMA e i COLLOIDI Pietro Favia, Gerardo Palazzo Dipartimento di Chimica, Università di Bari Aldo Moro CAMPUS, via Orabona 4, 70126 Bari pietro.favia@uniba.it, gerardo.palazzo@uniba.it
gli stati inusuali della materia: il PLASMA e i COLLOIDI Pietro Favia, Gerardo Palazzo Dipartimento di Chimica, Università di Bari Aldo Moro CAMPUS, via Orabona 4, 70126 Bari pietro.favia@uniba.it, gerardo.palazzo@uniba.it
CORRENTE ELETTRICA Intensità e densità di corrente sistema formato da due conduttori carichi a potenziali V 1 e V 2 isolati tra loro V 2 > V 1 V 2
 COENTE ELETTICA Intensità e densità di corrente sistema formato da due conduttori carichi a potenziali V 1 e V isolati tra loro V > V 1 V V 1 Li colleghiamo mediante un conduttore Fase transitoria: sotto
COENTE ELETTICA Intensità e densità di corrente sistema formato da due conduttori carichi a potenziali V 1 e V isolati tra loro V > V 1 V V 1 Li colleghiamo mediante un conduttore Fase transitoria: sotto
quale agisce una forza e viceversa. situazioni. applicate a due corpi che interagiscono. Determinare la forza centripeta di un
 CLASSE Seconda DISCIPLINA Fisica ORE SETTIMANALI 3 TIPO DI PROVA PER GIUDIZIO SOSPESO Test a risposta multipla MODULO U.D Conoscenze Abilità Competenze Enunciato del primo principio della Calcolare l accelerazione
CLASSE Seconda DISCIPLINA Fisica ORE SETTIMANALI 3 TIPO DI PROVA PER GIUDIZIO SOSPESO Test a risposta multipla MODULO U.D Conoscenze Abilità Competenze Enunciato del primo principio della Calcolare l accelerazione
MASSE ATOMICHE. 1,000 g di idrogeno reagiscono con 7,9367 g di ossigeno massa atomica ossigeno=2 x 7,9367=15,873 g (relativa all'idrogeno)
 MASSE ATOMICHE Sono a volte impropriamente chiamate pesi atomici. All'epoca di Dalton non era possibile pesare i singoli atomi ma solo trovare la massa di un atomo relativa a quella di un altro acqua di
MASSE ATOMICHE Sono a volte impropriamente chiamate pesi atomici. All'epoca di Dalton non era possibile pesare i singoli atomi ma solo trovare la massa di un atomo relativa a quella di un altro acqua di
Lezione del 24 Ottobre 2014
 MECCANISMI MOLECOLARI DEGLI STATI PATOLOGICI MECCANISMI MOLECOLARI DELLE MALATTIE METABOLICHE Lezione del 24 Ottobre 2014 EZIOLOGIA Studia le cause che inducono un turbamento persistente dell omeostasi
MECCANISMI MOLECOLARI DEGLI STATI PATOLOGICI MECCANISMI MOLECOLARI DELLE MALATTIE METABOLICHE Lezione del 24 Ottobre 2014 EZIOLOGIA Studia le cause che inducono un turbamento persistente dell omeostasi
Gli scambi tra cellula ed ambiente
 Gli scambi tra cellula ed ambiente Equilibrio osmotico Squilibrio chimico Squilibrio elettrico Equilibrio dinamico Lo scopo dell omeostasi è mantenere l equilibrio dinamico dei compartimenti corporei.
Gli scambi tra cellula ed ambiente Equilibrio osmotico Squilibrio chimico Squilibrio elettrico Equilibrio dinamico Lo scopo dell omeostasi è mantenere l equilibrio dinamico dei compartimenti corporei.
L ACQUA : STRUTTURA E PROPRIETA
 L ACQUA : STRUTTURA E PROPRIETA 1. Sostanza più abbondante in tutti gli esseri viventi 2. Più del 70% del peso di tutti gli esseri viventi 3. Influenza la struttura e la proprietà di tutte le molecole
L ACQUA : STRUTTURA E PROPRIETA 1. Sostanza più abbondante in tutti gli esseri viventi 2. Più del 70% del peso di tutti gli esseri viventi 3. Influenza la struttura e la proprietà di tutte le molecole
LICEO STATALE A.VOLTA COLLE DI VAL D ELSA PROGRAMMA DI FISICA SVOLTO NELLA CLASSE VA ANNO SCOLASTICO 2014/2015
 LICEO STATALE A.VOLTA COLLE DI VAL D ELSA PROGRAMMA DI FISICA SVOLTO NELLA CLASSE VA ANNO SCOLASTICO 2014/2015 Insegnante: LUCIA CERVELLI Testo in uso: Claudio Romeni FISICA E REALTA Zanichelli Su alcuni
LICEO STATALE A.VOLTA COLLE DI VAL D ELSA PROGRAMMA DI FISICA SVOLTO NELLA CLASSE VA ANNO SCOLASTICO 2014/2015 Insegnante: LUCIA CERVELLI Testo in uso: Claudio Romeni FISICA E REALTA Zanichelli Su alcuni
GAS IDEALI E MACCHINE TERMICHE. G. Pugliese 1
 GAS IDEALI E MACCHINE TERMICHE G. Pugliese 1 Proprietà dei gas 1. Non hanno forma né volume proprio 2. Sono facilmente comprimibili 3. Le variabili termodinamiche più appropriate a descrivere lo stato
GAS IDEALI E MACCHINE TERMICHE G. Pugliese 1 Proprietà dei gas 1. Non hanno forma né volume proprio 2. Sono facilmente comprimibili 3. Le variabili termodinamiche più appropriate a descrivere lo stato
Correnti e circuiti a corrente continua. La corrente elettrica
 Correnti e circuiti a corrente continua La corrente elettrica Corrente elettrica: carica che fluisce attraverso la sezione di un conduttore in una unità di tempo Q t Q lim t 0 t ntensità di corrente media
Correnti e circuiti a corrente continua La corrente elettrica Corrente elettrica: carica che fluisce attraverso la sezione di un conduttore in una unità di tempo Q t Q lim t 0 t ntensità di corrente media
Prova in itinere di Chimica Generale 1 Giugno 2011
 Prova in itinere di Chimica Generale 1 Giugno 2011 A COGNOME NOME. MATRICOLA 1 2 3 4 5 6 7 8 Indicazioni per lo svolgimento del compito. Scrivete il vostro Nome e Cognome in STAMPATELLO su ciascuno di
Prova in itinere di Chimica Generale 1 Giugno 2011 A COGNOME NOME. MATRICOLA 1 2 3 4 5 6 7 8 Indicazioni per lo svolgimento del compito. Scrivete il vostro Nome e Cognome in STAMPATELLO su ciascuno di
Cu 2+ ) + Zn(s) potere ossidante. potere ossidante. Cu 2+ Cu. Zn 2+ Consideriamo le due reazioni di ossido-riduzione:
 Elettrochimica Consideriamo le due reazioni di ossido-riduzione: Cu(s) ) + Zn 2+ 2+ (aq aq) Cu Cu 2+ 2+ (aq) + ) + Zn(s) Cu 2+ 2+ (aq) + ) + Zn(s) Cu(s) ) + Zn 2+ 2+ (aq) Cu Zn Zn 2+ Cu 2+ Cu potere ossidante
Elettrochimica Consideriamo le due reazioni di ossido-riduzione: Cu(s) ) + Zn 2+ 2+ (aq aq) Cu Cu 2+ 2+ (aq) + ) + Zn(s) Cu 2+ 2+ (aq) + ) + Zn(s) Cu(s) ) + Zn 2+ 2+ (aq) Cu Zn Zn 2+ Cu 2+ Cu potere ossidante
SCALA DEI PESI ATOMICI RELATIVI E MEDI
 SCALA DEI PESI ATOMICI RELATIVI E MEDI La massa dei singoli atomi ha un ordine di grandezza compreso tra 10-22 e 10-24 g. Per evitare di utilizzare numeri così piccoli, essa è espressa relativamente a
SCALA DEI PESI ATOMICI RELATIVI E MEDI La massa dei singoli atomi ha un ordine di grandezza compreso tra 10-22 e 10-24 g. Per evitare di utilizzare numeri così piccoli, essa è espressa relativamente a
Le reazioni di ossido-riduzione o reazioni redox rivestono grande importanza, non solo in chimica, ma anche nei fenomeni biologici.
 LE REAZIONI DI OSSIDO-RIDUZIONE Le reazioni di ossido-riduzione o reazioni redox rivestono grande importanza, non solo in chimica, ma anche nei fenomeni biologici. La vita dipende dalle reazioni redox.
LE REAZIONI DI OSSIDO-RIDUZIONE Le reazioni di ossido-riduzione o reazioni redox rivestono grande importanza, non solo in chimica, ma anche nei fenomeni biologici. La vita dipende dalle reazioni redox.
in Terminazione Neurone Dendriti Soma Fessura sinaptica sinaptica Nucleo dendrite Segmento iniziale Sinapsi inibitoria Segmento mielinico Assone
 Le funzioni del sistema nervoso si basano sull attività dei neuroni che consiste nel generare, trasmettere ed elaborare informazioni nervose, che dipendono da modificazioni del potenziale di membrana,
Le funzioni del sistema nervoso si basano sull attività dei neuroni che consiste nel generare, trasmettere ed elaborare informazioni nervose, che dipendono da modificazioni del potenziale di membrana,
Chimica. Ingegneria Meccanica, Elettrica e Civile Simulazione d'esame
 Viene qui riportata la prova scritta di simulazione dell'esame di Chimica (per meccanici, elettrici e civili) proposta agli studenti alla fine di ogni tutoraggio di Chimica. Si allega inoltre un estratto
Viene qui riportata la prova scritta di simulazione dell'esame di Chimica (per meccanici, elettrici e civili) proposta agli studenti alla fine di ogni tutoraggio di Chimica. Si allega inoltre un estratto
SOLUZIONI. Una soluzione è una miscela omogenea di più composti chimici. le miscele gassose sono sempre omogenee e quindi formano sempre una soluzione
 SOLUZIONI Una soluzione è una miscela omogenea di più composti chimici SOLUZIONI GASSOSE: SOLUZIONI LIQUIDE: SOLUZIONI SOLIDE: le miscele gassose sono sempre omogenee e quindi formano sempre una soluzione
SOLUZIONI Una soluzione è una miscela omogenea di più composti chimici SOLUZIONI GASSOSE: SOLUZIONI LIQUIDE: SOLUZIONI SOLIDE: le miscele gassose sono sempre omogenee e quindi formano sempre una soluzione
MPT Capitolo 12 Redox. Le ossidoriduzioni. Obiettivo. Definizioni di ossidazione e di riduzione
 1 Le ossidoriduzioni Obiettivo In questo capitolo svilupperemo i concetti fondamentali delle reazioni di ossido-riduzione. Si tratta di conoscenze fondamentali sia per la vita comune, sia, per molti di
1 Le ossidoriduzioni Obiettivo In questo capitolo svilupperemo i concetti fondamentali delle reazioni di ossido-riduzione. Si tratta di conoscenze fondamentali sia per la vita comune, sia, per molti di
ANNO SCOLASTICO 2014/2015 I.I.S. ITCG L. EINAUDI SEZ.ASSOCIATA LICEO SCIENTIFICO G. BRUNO PROGRAMMA DI FISICA. CLASSE: V A Corso Ordinario
 ANNO SCOLASTICO 2014/2015 I.I.S. ITCG L. EINAUDI SEZ.ASSOCIATA LICEO SCIENTIFICO G. BRUNO PROGRAMMA DI FISICA CLASSE: V A Corso Ordinario DOCENTE: STEFANO GARIAZZO ( Paola Frau dal 6/02/2015) La corrente
ANNO SCOLASTICO 2014/2015 I.I.S. ITCG L. EINAUDI SEZ.ASSOCIATA LICEO SCIENTIFICO G. BRUNO PROGRAMMA DI FISICA CLASSE: V A Corso Ordinario DOCENTE: STEFANO GARIAZZO ( Paola Frau dal 6/02/2015) La corrente
L equilibrio dei gas. Lo stato di equilibrio di una data massa di gas è caratterizzato da un volume, una pressione e una temperatura
 Termodinamica 1. L equilibrio dei gas 2. L effetto della temperatura sui gas 3. La teoria cinetica dei gas 4. Lavoro e calore 5. Il rendimento delle macchine termiche 6. Il secondo principio della termodinamica
Termodinamica 1. L equilibrio dei gas 2. L effetto della temperatura sui gas 3. La teoria cinetica dei gas 4. Lavoro e calore 5. Il rendimento delle macchine termiche 6. Il secondo principio della termodinamica
I legami. 1) Rappresenta la struttura della molecola di idrogeno (numero atomico ZH = 1):
 Percorso 3 I legami E S E R C I Z I A Legame covalente omeopolare 1) Rappresenta la struttura della molecola di idrogeno (numero atomico ZH = 1): 2) Rappresenta la struttura della molecola di ossigeno
Percorso 3 I legami E S E R C I Z I A Legame covalente omeopolare 1) Rappresenta la struttura della molecola di idrogeno (numero atomico ZH = 1): 2) Rappresenta la struttura della molecola di ossigeno
RIVELAZIONE DELLE RADIAZIONI IONIZZANTI. Nelle tecniche di rivelazione delle radiazioni ionizzanti le grandezze da rivelare possono essere diverse:
 RIVELAZIONE DELLE RADIAZIONI IONIZZANTI Nelle tecniche di rivelazione delle radiazioni ionizzanti le grandezze da rivelare possono essere diverse: -Fluenza di particelle -Fluenza di energia -Informazioni
RIVELAZIONE DELLE RADIAZIONI IONIZZANTI Nelle tecniche di rivelazione delle radiazioni ionizzanti le grandezze da rivelare possono essere diverse: -Fluenza di particelle -Fluenza di energia -Informazioni
1 atm = 760 mm Hg = 760 torr = 101300 N/m 2 =101300 Pa. Anodo = Polo Positivo Anione = Ione Negativo. Catodo = Polo Negativo Catione = Ione Positivo
 1) Concetti Generali 1. Unità di Misura: A. Pressione 1 atm = 760 mm Hg = 760 torr = 101300 N/m 2 =101300 Pa. B. Calore 1 joule = 10 7 Erg. 1 caloria = 4,185 joule. Anodo = Polo Positivo Anione = Ione
1) Concetti Generali 1. Unità di Misura: A. Pressione 1 atm = 760 mm Hg = 760 torr = 101300 N/m 2 =101300 Pa. B. Calore 1 joule = 10 7 Erg. 1 caloria = 4,185 joule. Anodo = Polo Positivo Anione = Ione
Corso di Laurea in TECNICHE DI RADIOLOGIA MEDICA, PER IMMAGINI E RADIOTERAPIA
 Corso di Laurea in TECNICHE DI RADIOLOGIA MEDICA, PER IMMAGINI E RADIOTERAPIA Anno: 1 Semestre: 1 Corso integrato: MATEMATICA, FISICA, STATISTICA ED INFORMATICA Disciplina: FISICA MEDICA Docente: Prof.
Corso di Laurea in TECNICHE DI RADIOLOGIA MEDICA, PER IMMAGINI E RADIOTERAPIA Anno: 1 Semestre: 1 Corso integrato: MATEMATICA, FISICA, STATISTICA ED INFORMATICA Disciplina: FISICA MEDICA Docente: Prof.
Durante la propagazione di un onda non c è trasporto di materia, ma propagazione di energia.
 ONDE Durante la propagazione di un onda non c è trasporto di materia, ma propagazione di energia. ONDE ELASTICHE Un onda elastica è una perturbazione che si propaga in un mezzo senza movimento di materia
ONDE Durante la propagazione di un onda non c è trasporto di materia, ma propagazione di energia. ONDE ELASTICHE Un onda elastica è una perturbazione che si propaga in un mezzo senza movimento di materia
Never impure protein PURIFICAZIONE DI PROTEINE
 Never waste pure thoughts on an impure protein PURIFICAZIONE DI PROTEINE PURIFICARE Purificare significa ottenere solamente la nostra molecola di interesse. Purificare una proteina per: Determinarne la
Never waste pure thoughts on an impure protein PURIFICAZIONE DI PROTEINE PURIFICARE Purificare significa ottenere solamente la nostra molecola di interesse. Purificare una proteina per: Determinarne la
ISTITUTO TECNICO NAUTICO "L. GIOVANNI LIZZIO PROF. SALVATORE GRASSO PROGRAMMA SVOLTO MODULO 0 : "RICHIAMI RELATIVI AL PRIMO ANNO"
 1 ISTITUTO TECNICO NAUTICO "L. RIZZO" - RIPOSTO ------------------------------------ ANNO SCOLASTICO : 2014-2015 CLASSE : SECONDA SEZIONE : D MATERIA D'INSEGNAMENTO : FISICA E LABORATORIO DOCENTI : PROF.
1 ISTITUTO TECNICO NAUTICO "L. RIZZO" - RIPOSTO ------------------------------------ ANNO SCOLASTICO : 2014-2015 CLASSE : SECONDA SEZIONE : D MATERIA D'INSEGNAMENTO : FISICA E LABORATORIO DOCENTI : PROF.
Proteine integrali di membrana legate sul versante esterno a gruppi di carboidrati. Formati da diverse subunità che circoscrivono un poro acquoso che
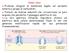 Canali ionici Proteine integrali di membrana legate sul versante esterno a gruppi di carboidrati. Formati da diverse subunità che circoscrivono un poro acquoso che permette il passaggio selettivo di ioni.
Canali ionici Proteine integrali di membrana legate sul versante esterno a gruppi di carboidrati. Formati da diverse subunità che circoscrivono un poro acquoso che permette il passaggio selettivo di ioni.
Fondamenti di chimica Raymond Chang Copyright 2009 The McGraw-Hill Companies srl CAPITOLO 18. Le reazioni redox e l elettrochimica
 CAPITOLO 18 Le reazioni redox e l elettrochimica 18.1 Seguiamo i passaggi descritti in dettaglio nella Sezione 18.1 del testo. (a) sono: Il problema è dato in forma ionica, così combinando lo step 1 co
CAPITOLO 18 Le reazioni redox e l elettrochimica 18.1 Seguiamo i passaggi descritti in dettaglio nella Sezione 18.1 del testo. (a) sono: Il problema è dato in forma ionica, così combinando lo step 1 co
La fisica di Feynmann Termodinamica
 La fisica di Feynmann Termodinamica 3.1 TEORIA CINETICA Teoria cinetica dei gas Pressione Lavoro per comprimere un gas Compressione adiabatica Compressione della radiazione Temperatura Energia cinetica
La fisica di Feynmann Termodinamica 3.1 TEORIA CINETICA Teoria cinetica dei gas Pressione Lavoro per comprimere un gas Compressione adiabatica Compressione della radiazione Temperatura Energia cinetica
Celle a combustibile Fuel cells (FC)
 Celle a combustibile Fuel cells (FC) Celle a combustibile Sono dispositivi di conversione elettrochimica ad alto rendimento energetico. Esse trasformano in potenza elettrica l energia chimica contenuta
Celle a combustibile Fuel cells (FC) Celle a combustibile Sono dispositivi di conversione elettrochimica ad alto rendimento energetico. Esse trasformano in potenza elettrica l energia chimica contenuta
Analisi quantitative
 Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
TENSIONE SUPERFICIALE
 TENSIONE SUPERFICIALE La tensione superficiale è un fenomeno alla cui esistenza possiamo risalire dall'osservazione di molti fatti sperimentali. Ad esempio una goccia d'olio d'oliva, posta in una miscela
TENSIONE SUPERFICIALE La tensione superficiale è un fenomeno alla cui esistenza possiamo risalire dall'osservazione di molti fatti sperimentali. Ad esempio una goccia d'olio d'oliva, posta in una miscela
VIE DI INTRODUZIONE ED ASSORBIMENTO DEI FARMACI
 VIE DI INTRODUZIONE ED ASSORBIMENTO DEI FARMACI I farmaci possono essere introdotti nell organismo per via enterale e per via parenterale.. Con la somministrazione enterale (enteron = intestino), il farmaco
VIE DI INTRODUZIONE ED ASSORBIMENTO DEI FARMACI I farmaci possono essere introdotti nell organismo per via enterale e per via parenterale.. Con la somministrazione enterale (enteron = intestino), il farmaco
Lipidi: funzioni. Strutturale. Riserva energetica. Segnale.
 Lipidi: funzioni. Strutturale. Riserva energetica. Segnale. Lipidi:classificazione. Saponificabili Non saponificabili Semplici Complessi Prostaglandine Steroidi Cere Trigliceridi Fosfogliceridi Sfingolipidi
Lipidi: funzioni. Strutturale. Riserva energetica. Segnale. Lipidi:classificazione. Saponificabili Non saponificabili Semplici Complessi Prostaglandine Steroidi Cere Trigliceridi Fosfogliceridi Sfingolipidi
Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta)
 Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta) E il termine generico che indica una serie di tecniche di separazione di molecole simili in
Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta) E il termine generico che indica una serie di tecniche di separazione di molecole simili in
ANALISI STRUMENTALE: POTENZIOMETRIA
 ANALISI STRUMENTALE: POTENZIOMETRIA POTENZIOMETRIA Misura dell attività di una specie ionica X (a X = g X [X]) in funzione del potenziale elettrodico prodotto dallo stesso ione sulla superficie di un elettrodo
ANALISI STRUMENTALE: POTENZIOMETRIA POTENZIOMETRIA Misura dell attività di una specie ionica X (a X = g X [X]) in funzione del potenziale elettrodico prodotto dallo stesso ione sulla superficie di un elettrodo
Capitolo n. 4 - Metodi elettrochimici
 Capitolo n. 4 - Metodi elettrochimici 4.1 - I metodi elettrochimici Si basano sulle proprietà elettriche della materia, che derivano dalla capacità degli atomi di acquistare o cedere elettroni in particolari
Capitolo n. 4 - Metodi elettrochimici 4.1 - I metodi elettrochimici Si basano sulle proprietà elettriche della materia, che derivano dalla capacità degli atomi di acquistare o cedere elettroni in particolari
CONCENTRAZIONE DELLE SOLUZIONI. Solvente: normalmente liquido in eccesso Soluto: gas, liquido o solido, normalmente in difetto
 CONCENTRAZIONE DELLE SOLUZIONI Solvente: normalmente liquido in eccesso Soluto: gas, liquido o solido, normalmente in difetto Percentuale in peso = g soluto / g soluzione x 100 H 2 O 2 al 3% Percentuale
CONCENTRAZIONE DELLE SOLUZIONI Solvente: normalmente liquido in eccesso Soluto: gas, liquido o solido, normalmente in difetto Percentuale in peso = g soluto / g soluzione x 100 H 2 O 2 al 3% Percentuale
Esercizi sui Motori a Combustione Interna
 Esercizi sui Motori a Combustione Interna 6 MOTORE 4TEMPI AD ACCENSIONE COMANDATA (Appello del 08.0.000, esercizio N ) Un motore ad accensione comandata a 4 tempi di cilindrata V 000 cm 3, funzionante
Esercizi sui Motori a Combustione Interna 6 MOTORE 4TEMPI AD ACCENSIONE COMANDATA (Appello del 08.0.000, esercizio N ) Un motore ad accensione comandata a 4 tempi di cilindrata V 000 cm 3, funzionante
3. METODI CONDUTTIMETRICI
 3. METODI CONDUTTIMETRICI Sono metodi basati sulla misura della conducibilità elettrica delle soluzioni elettrolitiche o delle sue variazioni che si registrano in seguito a reazioni chimiche che modificano
3. METODI CONDUTTIMETRICI Sono metodi basati sulla misura della conducibilità elettrica delle soluzioni elettrolitiche o delle sue variazioni che si registrano in seguito a reazioni chimiche che modificano
PROVA DI AMMISSIONE AL PRIMO ANNO DEL CORSO DI FORMAZIONE A TEMPO PIENO IN OSTEOPATIA PRESSO ACCADEMIA ITALIANA OSTEOPATIA TRADIZIONALE (A.I.O.T.
 PROVA DI AMMISSIONE AL PRIMO ANNO DEL CORSO DI FORMAZIONE A TEMPO PIENO IN OSTEOPATIA PRESSO ACCADEMIA ITALIANA OSTEOPATIA TRADIZIONALE (A.I.O.T.) SCADENZA 20 SETTEMBRE 2014 Presso l'accademia Italiana
PROVA DI AMMISSIONE AL PRIMO ANNO DEL CORSO DI FORMAZIONE A TEMPO PIENO IN OSTEOPATIA PRESSO ACCADEMIA ITALIANA OSTEOPATIA TRADIZIONALE (A.I.O.T.) SCADENZA 20 SETTEMBRE 2014 Presso l'accademia Italiana
ELETTROCHIMICA. Celle Galvaniche o Pile
 ELETTROCHIMICA Le reazioni di ossido-riduzione (redox) ci tengono in vita. Esse, ad esempio, si svolgono nei processi estremamente importanti che catturano l energia solare tramite la fotosintesi o in
ELETTROCHIMICA Le reazioni di ossido-riduzione (redox) ci tengono in vita. Esse, ad esempio, si svolgono nei processi estremamente importanti che catturano l energia solare tramite la fotosintesi o in
Trasporto ionico in soluzione
 Note di Elettrochimica 2009 (corso per studenti di Chimica) j = ke Trasporto ionico in soluzione Luigi Coppola Lab. PC_SM M.Terenzi Dept. of Chemistry, UNICAL lg.coppola@unical.it 1 1. Costanti fondamentali
Note di Elettrochimica 2009 (corso per studenti di Chimica) j = ke Trasporto ionico in soluzione Luigi Coppola Lab. PC_SM M.Terenzi Dept. of Chemistry, UNICAL lg.coppola@unical.it 1 1. Costanti fondamentali
Unità di misura. Perché servono le unità di misura nella pratica di laboratorio e in corsia? Le unità di misura sono molto importanti
 Unità di misura Le unità di misura sono molto importanti 1000 è solo un numero 1000 lire unità di misura monetaria 1000 unità di misura monetaria ma il valore di acquisto è molto diverso 1000/mese unità
Unità di misura Le unità di misura sono molto importanti 1000 è solo un numero 1000 lire unità di misura monetaria 1000 unità di misura monetaria ma il valore di acquisto è molto diverso 1000/mese unità
Contenuti del SYLLABUS per Corsi Integrati Medicina e Chirurgia Corso di Laurea
 Facoltà Contenuti del SYLLABUS per Corsi Integrati Medicina e Chirurgia Corso di Laurea Tecniche di Radiologia Medica, per Immagini e Radioterapia Tipologia Corso di Laurea Triennale Nota per la compilazione:
Facoltà Contenuti del SYLLABUS per Corsi Integrati Medicina e Chirurgia Corso di Laurea Tecniche di Radiologia Medica, per Immagini e Radioterapia Tipologia Corso di Laurea Triennale Nota per la compilazione:
TRASPORTO: qualunque tipo di passaggio di sostanze attraverso la membrana cellulare.
 Membrana citoplasmatica èsedediscambiodi materia, energia e informazione con l ambiente esterno TRASPORTO: qualunque tipo di passaggio di sostanze attraverso la membrana cellulare. Scaricato da www.sunhope.it
Membrana citoplasmatica èsedediscambiodi materia, energia e informazione con l ambiente esterno TRASPORTO: qualunque tipo di passaggio di sostanze attraverso la membrana cellulare. Scaricato da www.sunhope.it
FARMACOCINETICA 1. Farmacologia generale FARMACOCINETICA FARMACOLOGIA FARMACODINAMICA
 FARMACOCINETICA 1 Farmacologia generale FARMACOCINETICA FARMACOLOGIA FARMACODINAMICA 1 ASSORBIMENTO DEI FARMACI cioè il processo per mezzo del quale un farmaco passa dal sito di somministrazione al plasma
FARMACOCINETICA 1 Farmacologia generale FARMACOCINETICA FARMACOLOGIA FARMACODINAMICA 1 ASSORBIMENTO DEI FARMACI cioè il processo per mezzo del quale un farmaco passa dal sito di somministrazione al plasma
Fisica Generale II Facoltà di Ingegneria. a.a. 2013/2014 Prof. Luigi Renna Programma dettagliato
 1 Fisica Generale II Facoltà di Ingegneria. a.a. 2013/2014 Prof. Luigi Renna Programma dettagliato Libro di testo: P. Mazzoldi M. Nigro C. Voci: Elementi di FISICA Elettromagnetismo Onde II edizione (EdiSES,
1 Fisica Generale II Facoltà di Ingegneria. a.a. 2013/2014 Prof. Luigi Renna Programma dettagliato Libro di testo: P. Mazzoldi M. Nigro C. Voci: Elementi di FISICA Elettromagnetismo Onde II edizione (EdiSES,
TERMODINAMICA DI UNA REAZIONE DI CELLA
 TERMODINAMICA DI UNA REAZIONE DI CELLA INTRODUZIONE Lo scopo dell esperienza è ricavare le grandezze termodinamiche per la reazione che avviene in una cella galvanica, attraverso misure di f.e.m. effettuate
TERMODINAMICA DI UNA REAZIONE DI CELLA INTRODUZIONE Lo scopo dell esperienza è ricavare le grandezze termodinamiche per la reazione che avviene in una cella galvanica, attraverso misure di f.e.m. effettuate
FISIOLOGIA RENALE. LEZ.Nr 2
 FISIOLOGIA RENALE LEZ.Nr 2 PROCESSI IMPLICATI NELLA FORMAZIONE DELL URINA ESCREZIONE URINARIA ESCREZIONE URINARIA QUANTIFICAZIONE MEDIANTE PARAMETRI QUALI Superficie filtrante ;Barriera di filtrazione
FISIOLOGIA RENALE LEZ.Nr 2 PROCESSI IMPLICATI NELLA FORMAZIONE DELL URINA ESCREZIONE URINARIA ESCREZIONE URINARIA QUANTIFICAZIONE MEDIANTE PARAMETRI QUALI Superficie filtrante ;Barriera di filtrazione
AUTODIFFUSIONE Autodiffusione
 DIFFUSIONE ATOMICA La diffusione è un processo importante che influenza il comportamento di un materiale alle alte temperature (creep, trattamenti termici superficiali, tempra chimica del vetro, ricristallizzazione,
DIFFUSIONE ATOMICA La diffusione è un processo importante che influenza il comportamento di un materiale alle alte temperature (creep, trattamenti termici superficiali, tempra chimica del vetro, ricristallizzazione,
Corso integrato: FISICA, STATISTICA E INFORMATICA Disciplina: FISICA MEDICA Docente: Prof. Massimo MONCIARDINI Recapito: maxmonc@inwind.
 Corso integrato: FISICA, STATISTICA E INFORMATICA Disciplina: FISICA MEDICA Docente: Prof. Massimo MONCIARDINI Recapito: maxmonc@inwind.it Programma: Introduzione Meccanica Cinematica Dinamica Statica
Corso integrato: FISICA, STATISTICA E INFORMATICA Disciplina: FISICA MEDICA Docente: Prof. Massimo MONCIARDINI Recapito: maxmonc@inwind.it Programma: Introduzione Meccanica Cinematica Dinamica Statica
