Trasporto degli elettroni e fosforilazione ossidativa
|
|
|
- Orsola Gasparini
- 8 anni fa
- Visualizzazioni
Transcript
1 Trasporto degli elettroni e fosforilazione ossidativa 1
2 LA RESPIRAZIONE CELLULARE Le cellule respirano? La respirazione cellulare è il meccanismo attraverso cui la cellula, in presenza di ossigeno, è in grado di ricavare energia utilizzabile nei processi vitali dai legami chimici delle molecole assorbite nella digestione. La respirazione cellulare consta di diverse reazioni, in cui i prodotti di un passaggio sono utilizzati come reagenti per il processo successivo. I prodotti di scarto della respirazione cellulare (come CO 2 o H 2 O) vengono eliminati dalla cellula e, negli organismi superiori, escreti attraverso la respirazione polmonare e le urine. 2
3 Gli organismi aerobici durante il processo di ossidazione dei carburanti metabolici consumano ossigeno e producono biossido di carbonio: C6H12O6 + 6O2 6CO2 + 6 H2O Glucosio 3
4 Le 12 coppie di e- rilasciate durante l ossidazione del glucosio non sono trasferite direttamente all O2 ma ai coenzimi NAD+ e FAD tramite i coenzimi, gli e- passano alla catena di trasporto degli e- 4
5 Durante il processo di trasporto degli elettroni accadono i eguenti eventi: 1) NADH e FADH2 sono riossidati a NAD+ e FAD 2) il trasferimento degli e- partecipa all ossidazione-riduzione di 10 centri redox 3) durante il trasferimento degli e-, dal mitocondrio vengono espulsi dei protoni con la generazione di un gradiente protonico attraverso la membrana mitocondriale. 5
6 6
7 Struttura di un mitocondrio 50% lipidi, 50% proteine 80% proteine 7
8 LA RESPIRAZIONE CELLULARE Modello di mitocondrio e schema generale della respirazione cellulare La respirazione aerobica ha luogo nella matrice e nella membrana mitocondriale interna e questo processo è incrementato dalla grande superficie offerta dalle creste. La matrice contiene la maggior parte degli enzimi coinvolti nell ossidazione degli acidi grassi e gli enzimi degli acidi tricarbossilici (ciclo di Krebs); sono inoltre presenti DNA mitocondriale ed RNA. La membrana mitocondriale interna contiene i citocromi, le molecole di trasporto della catena di trasporto degli elettroni e gli enzimi coinvolti nella produzione di ATP. I mitocondri sono considerati organuli semiautonomi, perché riescono a sintetizzare molte delle proteine di cui necessitano; inoltre, vanno incontro ad un autoreplicazione mediante un processo che è analogo alla divisione dei batteri. 8
9 9
10 10
11 La porina ha una struttura a foflietto β antiparallelo che si arrotola a formare un barile. Sono proteine che formano canali nella membrana dei batteri gram-negativi Le porine sono presenti anche negli eucarioti, nella membrana esterna dei mitocondri e dei cloroplasti. 11
12 12
13 13
14 NAD+, NADH, NADP+, NADPH, FAD, FADH2 La membrana mitocondriale interna è priva di una proteina trasportatrice del NADH Nel mitocondrio vengono trasportati soltanto gli elettroni del NADH citosolico mediante ingegnosi sistemi navetta 14
15 Sistemi navetta di substrati: si servono di isoforme citoplasmatiche e mitocondriali dello stesso enzima 15
16 Shuttle malato aspartato (fegato, muscolo cardiaco) GOT cit. reaz. di transamminazione 4 (e-) 1 malato deidrogenasi (citosolica) (reaz. di riduzione) mmi 3 2 reaz. di transamminazione GOT mit. malato deidrogenasi (ciclo di Krebs) (reaz. di ossidazione) 16
17 Il sistema navetta del Glicerofosfato del muscolo alare degli insetti trasferimento di una coppia di e- glicerolo 3-P deidrogenasi isozima FAD dip. 17
18 Meccanismo conformazionale del traslocatore ADP-ATP o adenina nucleotide traslocasi che trasporta l ATP fuori dalla matrice scambiandolo con l ADP (dimero costituito da due subunità identiche di 30 kd) Il Pi che è necessario anche per la sintesi di ATP nella matrice, viene importato dal citosol mediante un sistema di simporto Pi-H +. Il gradiente protonico transmembrana generato dalla catena di trasporto degli elettroni presente sulla membrana mitocondriale interna non fornisce soltanto la forza termodinamica necessaria per la sintesi di ATP ma promuove anche il trasporto dei suoi materiali di partenza, ADP e Pi. 18
19 I due sistemi di trasporto mitocondriale per il Ca 2+ I MT funzionano da tamponi per il calcio citosolico. Importanza della distribuzione intracellulare del calcio: contrazione muscolare trasmissione neuronale secrezione, azione degli ormoni antiporto con ioni Na+ L entrata nella matrice è promossa dal potenziale di membrana negativo che attrae gli ioni positivi. La velocità dipende dalla [Ca ++ ] esterna Se la [Ca++]cit Se la [Ca++] cit = aumenta l entrata = diminuisce l entrata 19
20 Quando la [Ca++] citoplasmatica aumenta per un lavoro muscolare sostenuto la [Ca++] aumenta anche nella matrice mitoc., attivando gli enzimi del ciclo di Krebs che porta a un aumento dei livelli di NADH, la cui riossidazione tramite il sistema di trasporto degli elettroni genera l ATP necessario per la contrazione. 20
21 I trasportatori degli elettroni che portano gli elettroni dal NADH e dal FADH all O2 sono associati alla membrana mitocondriale interna. Alcuni di questi centri redox sono mobili, altri sono invece componenti di complessi di proteine integrali di membrana. La sequenza dei trasportatori degli elettroni riflette grossolanamente i loro potenziali di riduzione relativi, cosicchè il processo di trsporto degli elettroni è complessivamente esoergonico. 21
22 La via più importante per la formazione di ATP, presente sia negli organismi autotrofi che in quelli eterotrofi, è la fosforilazione ossidativa: questo processo è fortemente endoergonico (cioè necessita di una grande quantità di energia, DG > 0) Il meccanismo più rilevante per la sintesi di ATP da ADP e Pi utilizza energia derivante da gradienti elettrochimici. Questa energia viene liberata grazie alla presenza nella cellula (mitocondrio) di catene trasportatrici di elettroni (processo redox fortemente esoergonico, DG < 0) 22
23 La catena respiratoria libera energia grazie alla differenza tra i potenziali di riduzione tra il donatore (NADH + H + ), complessi della catena respiratoria e l accettore l (O 2 ) di elettroni. Gran parte di questa energia viene impiegata dall ATP sintasi per convertire l ADP l in ATP 23
24 Il flusso di elettroni può produrre un lavoro biologico: Nel circuito che potenzia un motore, la fonte di e- può essere una batteria che contiene due specie chimiche che hanno una diversa affinità per gli e-. Il flusso elettronico procederà spontaneamente nel circuito guidato da una forza proporzionale alla differenza tra le due affinità detta forza elettromotrice (fem). La fem può generare un lavoro se al circuito viene collegato un trasduttore energetico. 24
25 In un analogo circuito biologico la fonte di elettroni è un composto ridotto come per es. il glucosio. Quando viene ossidato enzimaticamente sono rilasciati e- che fluiscono spontaneamente attraverso una serie di trasportatori intermedi fino a raggiungere una specie chimica con un elevata affinità per gli e- come l ossigeno. La forza motrice che si genera fornisce energia ad una varietà di trasduttori molecolari (enzimi e proteine) che compiono un lavoro biologico. 25
26 L ossidazione biologica completa di sostanze organiche nutrienti crea c un flusso di elettroni che procede verso l ossigeno l mediante una serie di trasportatori di elettroni intermedi che si comportano come un ponte p a cestelli: reazione redox esoergonica: : gli elettroni passano spontaneamente da un trasportatore a bassa affinità per gli elettroni ad un altro con affinità maggiore e così via. La reazione complessiva è: sostanza organica + O 2 CO 2 + H 2 O + energia 26
27 Il sistema mitocondriale di trasporto degli e-e non è altro che una sequenza di reazioni di ossido riduzione Durante le reazioni redox, gli elettroni trasferiti possono passare are direttamente dai donatori agli accettori: Fe 2+ + Cu 2+ Fe 3+ + Cu + In alternativa, gli elettroni possono essere trasferiti da un donatore a un accettore mediante un trasportatore di elettroni: XH 2 + Y X +Y H 2 NADH + H + + FAD NAD+ + FADH2 27
28 Un atomo di idrogeno neutro è in grado di trasferire un singolo elettrone: H e- + H + Lo ione negativo idruro (H - ) è invece in grado di trasferire due elettroni: H - 2e- + H + 28
29 Le forme ossidate e ridotte dei composti sono dette coppie redox. donatore di e- (agente riducente) accettore di e- (agente ossidante) La facilità con la quale gli e- passano dal riducente all ossidante è espressa quantitativamente dal valore del potenziale di ossido-riduzione del sistema. 29
30 In una coppia redox il riducente con un potenziale di ox-red molto negativo cede facilmente i suoi e- a coppie con potenziali redox meno negativi o più positivi Viceversa un forte ossidante (caratterizzato da un potenziale redox molto positivo) mostra una grande affinità per gli e-. 30
31 Il potenziale di riduzione standard (E 0 ) è una misura quantitativa dell'affinità di un accettore per gli elettroni in una semi-reazione. Per convenzione internazionale, alla semi-reazione H + + e-e 1/2H 2 viene assegnato un potenziale di riduzione standard pari a zero, quando la concentrazione di ioni H + è 1 M e H 2 è presente alla pressione parziale di 101,3 kpa. Questa semi-reazione viene usata come riferimento per la determinazione dei potenziali delle altre semi-reazioni. 31
32 Il più forte agente ossidante cioè ha elevata affinità per gli elettroni e - 32
33 La catena respiratoria comprende 3 complessi proteici inseriti nella membrana mitocondriale interna (complessi I, III e IV) e molecole di trasferimento mobili, quali il coenzima Q e il citocromo-c: complesso I: NADH deidrogenasi complesso III: citocromo-c reduttasi complesso IV: citocromo-c ossidasi II Il complesso II è la succinato deidrogenasi, è l unico enzima presente del ciclo dell acido citrico presente nella membrana interna mitocondriale. Il complesso V, l ATP sintasi, non partecipa al trasferimento di elettroni 33
34 Tutti i complessi della catena respiratoria sono formati da numerose subunità polipeptidiche e contengono una serie di coenzimi redox legati alle proteine: Flavine: FMN e FAD nei complessi I e II Coenzima Q Centri Ferro-Zolfo: complessi I, II e III Gruppi eme: II, III e IV I trasportatori flavinici e il CoQ sono trasportatori misti: : trasportano elettroni e H + I centri Ferro-Zolfo e i gruppi eme dei citocromi sono trasportatori puri: : trasportano elettroni 34
35 Nicotinamide adenina dinucleotide (NAD+) e nicotinamide adenina dinucleotide fosfato (NADP+). R= H nel NAD+ R= PO 3 - nel NADP 35
36 L FMN e il FAD subiscono delle reazioni di ossido-riduzione reversibili. L FMN è saldamente legato al complesso-i I della catena respiratoria e non si comporta come un substrato diffusibile. Il FAD è tenacemente legato al complesso II, o succinato deidrogenasi. Le flavine sono dei derivati della vitavina riboflavina 36
37 Flavina adenina dinucleotide (FAD) Costituita da FMN + AMP 37
38 Il CoQ,, a differenza dei nucleotidi flavinici è diffusibile e può spostarsi, durante il trasporto elettronico, tra molecole donatrici e accettrici. Il coenzima Q è un benzochinone con una catena isoprenoide insatura. Un valore numerico riportato al pedice indica il numero di unità isoprenoidi (CoQ6, CoQ10) 38
39 Forma ossidata I tre stati di ossidazione dell FMN e del CoQ Flavin mononucleotide (FMN) ( forma ossidata o chinonica) Forma radicalica CoenzimaQ (CoQ) o ubichinone (forma ossidata o chinonica) FMNH*(forma radicalica o semichinonica) CoenzimaQH*o ubisemichinone (forma radicalica o semichinonica Forma ridotta FMNH 2 (forma ridotta o idrochinonica) Coenzima QH 2 o ubichinolo (forma ridotta o idrochinonica) 39
40 Flavin mononuleotide (FMN) e Coenzima Q (CoQ( CoQ) ) o ubichinone Stati di ossidazione di Flavin Il FMN (a) e il coenzimaq (b) formano radicali liberi semichinonici stabili. IL FMN e il CoQ (che possono trasferire uno o due elettroni per volta) sono quindi il punto di contatto tra il donatore a due elettroni NADH e i citocromi accettori ad un solo elettrone 40
41 I centri Fe-S,, come i nucleotidi flavinici,, sono strettamente legati alle proteine. Il ferro è legato allo zolfo elementare e ai gruppi tiolici di cisteine messe a disposizione dalla proteina. Benchè in un centro possano essere presenti vari atomi di ferro, i centri ferro-zolfo partecipano a reazioni di trasferimento di un solo elettrone Esempi di centri ferro-zolfo 41 33
42 I citocromi rappresentano l rappresentano l ultima classe di componenti che partecipano al trasporto degli elettroni. I I citocromi sono delle proteine contenenti eme. L eme è la ferro-porfirina che si trova nelle emoglobine e nella mioglobina.. I citocromi del tipo a, b e c sono le principali varianti di queste proteine presenti nelle cellule. Ciascun citocromo è costituito da una catena polipeptidica e da un gruppo eme specifico. Il ferro presente nei citocromi, ma non quello nell emoglobina emoglobina, subisce delle ossido-riduzioni fisiologiche passando dallo stato ferroso (2+) a quello ferrico (3+) e viceversa 42
43 Esempi di gruppi eme I gruppi eme sono composti tetrapirrolici contenenti ferro (Fe-protoporfirina IX) I singoli citocromi differiscono l uno dall altro per la natura del nucleo porfirinico 43
44 Sequenza del trasporto degli elettroni L ossidazione del NADH e del FADH 2 viene compiuta dalla catena di trasporto degli elettroni, un insieme di complessi proteici contenenti centri redox caratterizzati da affinità per gli elettroni progressivamente crescenti. Gli elettroni viaggiano lungo questa catena partendo da potenziali di riduzione standard più bassi verso potenziali più alti. Gli elettroni vengono trasportati dai Complessi I e II al Complesso III mediante il CoQ,, e dal complesso III al Complesso IV attraverso la proteina periferica di membrana citocromo c 4 H + Complesso I Complesso II Succinato deidrogenasi-fad FeS, cit b560 44
45 Il complesso I o NADH-coenzima Q ossidoreduttasi(nadh deidrogenasi) catalizza l ossidazione l del NADH da parte del CoQ.. E E il più grosso, complesso contenente 43 catene polipeptidiche.. Contiene una molecola di FMN e sei o sette centri ferro-zolfo che partecipano al trasporto degli elettroni. NADH + CoQ (ossidato) NAD + + CoQ (ridotto) 4 H + (6-7) Complesso I Complesso II Succinato deidrogenasi-fad FeS, cit b
46 Il NADH può trasferire soltanto due elettroni per volta, mentre i citocromi del Complesso III a cui il CoQ passa i suoi elettroni, sono in grado di accettare solo un elettrone per ogni passaggio. Il FMN e CoQ che possono trasferire uno o due elettroni per volta, sono quindi il punto di contatto tra il donatore a due elettroni NADH e i citocromi accettori a un solo elettrone. 46
47 Modello che rappresenta il trasporto dei protoni (batteriodopsina,una proteina integrale di membrana di Halobacterium halabium) Nel momento in cui gli elettroni vengono trasportati tra i vari centri redox del Complesso I, quattro protoni vengono trasferiti fuori dalla matrice nello spazio inermembrana. Il complesso I potrebbe esistere in due stadi conformazionali: ossidato e ridotto. 47
48 Il complesso II (citocromo c-reduttasi) c catalizza l ossidazione l del FADH 2 da parte del CoQ FADH 2 + CoQ CoQ (ossidato) 4 H + FAD + CoQ CoQ (ridotto) I suoi centri redox comprendono il FAD legato covalentemente alla succinato deidrogenasi, sul quale passano inizialmente gli elettroni, un centro 4Fe-4S, due centri 2Fe-2S e un citocromo b. 560 Complesso I Complesso II Succinato deidrogenasi-fad FeS, cit b560 48
49 Quando il succinato è convertito in fumarato nel ciclo del TCA, nella succinico deidrogenasi avviene una concomitante riduzione del FAD legato a FADH2. Questo FADH2 trasferisce i suoi elettroni immediatamente ai centri Fe-S che li passano al UQ. UQ + 2H+ + 2e = UQH2 49
50 L energia libera per il trasferimento degli elettroni dal succinato al CoQ è insufficiente per promuovere la sintesi di ATP. Il complesso II è però ugualmente importante perché consente ad elettroni con un potenziale relativamente alto di entrare nelle catene di trasporto degli elettroni saltando il Complesso I. Il complesso I e II non operano in serie, anche se entrambi trasferiscono elettroni da substrati ridotti, NADH o Succinato al CoQ. Il CoQ che diffonde nel doppio strato lipidico tra i complessi respiratori, serve come una sorta di punto di raccolta per gli elettroni. Dalla prima tappa dell ossidazione degli acidi grassi si generano gli elettroni che entrano nella catena di trasporto degli elettroni a livello del CoQ. Il CoQ raccoglie anche gli elettroni provenienti dal FADH2 prodotto dalla navetta del glicerolfosfato. 50
51 Il complesso III catalizza l ossidazione l del CoQ (ridotto) da parte del citocromo c. La UQ- citocromo c riduttasi (UQ( UQ-cit c riduttasi, nome con cui è noto questo complesso) Tale complesso funziona per consentire a una molecola di CoQH 2, un trasportatore a due elettroni, di ridurre due molecole di citocromo c, un trasportatore a un elettrone. Questo complesso contiene due citocromi b,un citocromo c 1 e un centro 2Fe-2S (centro di Rieske) al quale è legata la proteina ferro zolfo detta ISP. CoQ (ridotto) + citocromo c (ossidato) 4 H + citocromo c (ridotto) + CoQ (ossidato) Complesso I Complesso II Succinato deidrogenasi-fad FeS, cit b560 51
52 Il Complesso III è un dimero a forma di pera la cui parte più larga è immersa nella matrice mitocondriale. La porzione che attraversa la membrana è costituita da 13 eliche transmembrana per ogni monomero la maggior parte delle quali sono inclinate rispetto al piano della membrana. Otto di queste eliche appartengono alle subunità del citocromo b che lega i gruppi eme di entrambi i citocromi di tipo b, il citocromo b 562 ( detto anche citocromo H a causa del suo alto potenziale e che si trova vicino allo spazio intermembrana ) e b 566 ( chiamato anche b1 per il basso potenziale e che si trova nella matrice ). La proteina ferro-zolfo (ISP) che lega il centro di Rieske, è ancorata nella regione transmembrana mediante due eliche situate alla sua estremità N-terminale e si estende nello spazio intermembrana. Il citicromo c1 è ancorato nella regione transmembrana mediante la sua eleica C- terminale relativamente mobile contenente un gruppo eme di tipo c 52
53 53
54 Esempi di gruppi eme I gruppi eme sono composti tetrapirrolici contenenti ferro I cit a contengono una catena contengono una catena isoprenoide di 15 carbonii uniti a un gruppo vinilico modificato ed un gruppo formile al posto di uno dei metili. I cit b contengono la contengono la ferro-protoporfirina IX lo stesso eme che si trova nell emoglobina e nella mioglobina. I cit c contengono l eme c, derivato dalla ferro-protoporfirina IX ma legata covalentemente a residui di cisteina della apoproteina. 54
55 La membrana mitocondriale interna contiene una grande concentrazione di CoQ e CoQH2 Il ciclo Q inizia quando una molecola di UQH2 diffonde dalla membrana ad un sito catalitico del complesso III il sito QP. L ossidazione di QUH2 ha luogo in due fasi: 1. Un primo elettrone proveniente dal UQH2 è trasferito alla proteina di Rieske e successivamente al cit c1. Questa reazione rilascia due H+ nel citosol e produce UQ.-, un anione semichinonico del UQ nel sito QP. 2. Un secondo elettrone è successivamente trasferito a l eme bl convertendo l UQ.- a UQ. L elettrone sull eme bl vicino al lato citosolico della membrana è quindi trasferito ad una molecola di UQ su un secondo legante chinoni QN convertendo questo UQ a UQ.-. UQ.- rimane saldamente legato al sito QN. Si completa la prima metà del ciclo del CoQ 55
56 La seconda metà del ciclo è simile alla prima. 1. Una seconda molecola di UQH2 viene ossidata al sito QP ed en secondo elettrone è trasferito al cit c1 2. L altro elettrone passa all eme bl e successivamente all eme bh. 3. L elettrone su bh è trasferito sul anione semichinonico UQ.-, al sito QN. 4. Con l apporto di due H+ provenienti dalla matrice mitocondriale questa reazione produce UQH2, che viene rilasciato dal sito QN e torna nella membrana completando il ciclo del CoQ 56
57 L essenza del ciclo Q è che il CoQH2 subisce una riossidazione che avviene in due cicli, in cui il semichinone, CoQ.-, è un intermedio stabile. Questo richiede che vi siano per il coenzima Q due siti di legame indipendenti: 1. QP che si lega a CoQH2 ed è localizzato tra il centro di Rieske [2Fe-2S] e il gruppo eme bl in prossimità dello spazio intermembrana. 2. QN che lega sia CoQ.- sia CoQ ed è localizzato vicino al gruppo eme bh in prossimità della matrice. 57
58 58
59 Il citocromo c è un trasportatore mobile di elettroni Gli elettroni che attraversano il Complesso III sono trasferiti al citocromo C dal cit c1. Il citocromo C è il solo citocromo nella catena di trasporto degli elettroni che sia idrosolubile. Il citocromo C come l UQ è un trasportatore mobile, è associato debolmente alla membrana interna mitocondriale ( nello spazio intermembrana dalla parte citosolica della membrana interna). In questa posizione è in grado di acquisire elettroni dall insieme Fe-S-cit1 del Complesso III e successivamente migrare lungo la superfice della membrana allo stato ridotto, per trasferire gli elettroni alla citocromo c ossidasi, il IV complesso della catena di trasporto degli elettroni. 59
60 IL CITOCROMO C E UN MEDIATORE DELLA APOPTOSI morte cellulare programmata Reagendo a segnali molecolari nel citosol, nella membrana mitocondriale si aprono i canali di trasporto che rilasciano il citocromo c. Il citocromo c a sua volta, attiva le caspasi, una famiglia di proteasi contenenti una cisteina nel loro sito catalitico. L attivazione delle caspasi innesca una serie di reazioni proteolitiche che causano in ultimo la morte della cellula 60
61 Il complesso IV (citocromo c-ossidasi) c catalizza l ossidazione l del citocromo c ridotto da parte dell O 2, l accettore l terminale degli elettroni nel processo di trasporto degli elettroni citocromo c (ridotto) + ½ O 2 citocromo c (ossidato) + H 2 O 4 H + Complesso I Complesso II Succinato deidrogenasi-fad FeS, cit b560 citocromo c ossidasi 61
62 Il complesso IV dei mammiferi è un dimero i cui monomeri hanno un peso molecolare di 200 KD e sono costituiti da 13 subunità. La parte centrale del ComplessoIV è costituita dalle sue tre subunità I,II,III, più grandi e più idrfobiche, che sono codificate dal DNA mitocondriale, le altre sono codificate dal DNA nucleare e devono essere trasportate dentro il mit. Struttura del dimero delle citocromo c ossidasi, l enzima che catalizza le ossidazioni, con l acquisto di un elettrone, di quattro molecole consecutive di citocromo c ridotto e la contemporanea riduzione di una molecola di O 2 utilizzando quattro elettroni. 4 citocromoc (Fe 2+ ) + 4H+ + O 2 4 citocromo c(fe 3+ ) + 2H 2 O 62
63 Il complesso IV Contiene quattro centri redox: il citocromo a, il citocromo a 3, un atomo di rame chiamato Cu B e un paio di atomi di rame chiamato centro Cu A, Sono anche presenti uno ione Mg 2+ e uno ione Zn 2+. Il Fe dell eme a 3 e il Cu B formano un unico complesso binucleare 63
64 RIASSUMENDO Reazione della citocromo c ossidasi e riduzione di O2 ad H2O. Per ridurre una molecola di O2 a 2 di H2O a livello del complesso binucleare citocromo a3-cub è necessario un totale di 4 elettroni, donati dal citocromo c, e di 4 protoni che si originano nella matrice mitocondriale. Oltre ai 4 protoni utilizzati per ridurre l O2, l, 4 protoni provenienti dalla matrice vengono traslocati nello spazio intermembrana (ogni 2 e-e che attraversano il complesso IV, vengono traslocati 2 protoni). 64
65 65
66 Inibitori della catena respiratoria Rotenone Carbossina Antimicina A Cianuro Inibitore e Amital Monossido di carbonio sito/tipo di azione Si lega al complesso I e blocca il trasferimento di elettroni dai gruppi Fe-S all ubichinone (Q) Si lega al complesso II e blocca il trasferimento di elettroni dal FADH2 all ubichinone Si lega al complesso III e blocca il trasferimento dall ubichinolo ai gruppi Fe-S Blocca il flusso elettronico legandosi al Fe 3+ dei citocromi del complesso IV Blocca il flusso elettronico legandosi al Fe 3+ dei citocromi del complesso IV Oligomicina Blocca il flusso di H + attraverso l ATP sintasi 66
67 67
68 Inibitori sito-specifici specifici del trasporto di elettroni 68
69 Inibitori della respirazione cellulare: il cianuro Il cianuro è un anione che deriva dalla dissociazione dall'acido cianidrico (HCN) HCN H + + CN - Una delle proprietà chimiche del cianuro, utile per capire la sua tossicità è la capacità di combinazione con i metalli: Fe, Ag, Au ecc. Una delle molecole indispensabili per questa funzione è il citocromo-c ossidasi, (o complesso IV) che è l'ultimo complesso enzimatico coinvolto nella catena di trasporto degli elettroniche e possiede al centro della sua complessa struttura un atomo di ferro (Fe). Quando il cianuro entra nella cellula si lega al ferro e l'enzima cessa la sua funzione. La conseguenza è che la cellula cessa di respirare e muore. Per tale ragione il cianuro è un veleno, per tutti gli esseri viventi, anche dosi molto piccole. Zyklon B (o Zyclon B) era il nome commerciale dell'acido cianidrico, un pesticida utilizzato come agente tossico nelle camere a gas di alcuni campi di concentramento e sterminio nazisti. Citocromo-c ossidasi Cianuro di potassio 69
70 Modificatori della respirazione cellulare: l etanolo I forti bevitori vanno incontro a gravi e spesso letali malattie al fegato. CH 3 CH 2 OH CH 3 CHO + 2H + Gli enzimi del fegato ossidano inizialmente l etanolo ad acetaldeide eliminando due atomi di idrogeno, come da reazione schematizzata. Sebbene gli effetti intossicanti dell alcol siano dovuti soprattutto all acetaldeide, i responsabili dell insorgenza delle malattie epatiche sono gli atomi di idrogeno (elettroni e protoni) eliminati dall etanolo. Questi atomi di idrogeno in più, trasportati dalle molecole di NADH, seguono due vie principali nella cellula. La maggior parte di essi passa direttamente nella catena di trasporto degli elettroni, così da saturare il processo e rallentare la normale decomposizione di zuccheri, acidi grassi, amminoacidi, che invece di essere scissi vengono convertiti in grassi che si accumulano nel fegato. Gli altri atomi di idrogeno sono utilizzati nella sintesi degli acidi grassi a partire dagli zuccheri e dagli amminoacidi. 70
71 Il trasporto degli elettroni lungo la catena respiratoria determina un passaggio di protoni dalla matrice mitocondriale allo spazio intermembrana Teoria Chemiosmotica di Peter Mitchell L energia libera prodotta durante il trasporto degli elettroni viene conservata pompando p ioni H+ dalla matrice mitocondriale nello spazio intermembrana, per creare attraverso la membrana mitocondriale interna un gradiente elettrochimico di H+. Il potenziale elettrochimico di questo gradiente viene sfruttato per sintetizzare ATP. Il trasporto degli elettroni, promuove il trasferimento dei protoni da parte dei Complessi I, III, e IV dalla matrice una regione contenente una bassa [H+[ H+], attraverso la membrana mitocondriale interna, allo spazio intermembrana ( che è in contatto con il citosol), caratterizzato da un alta [H+ H+]. 71
72 72
73 Nel modello proposto da Mitchell, il ph della matrice si innalza, e la matrice stessa acquista un potenziale elettrico negativo rispetto al citosol come conseguenza dell uscita dei protoni, Il pompaggio dei protoni cioè produce un gradiente di ph ed una differenza di potenziale elettrico attraverso la membrana mitocondriale interna, condizioni che contribuiscono entrambe ad attrarre i protoni di nuovo nella matrice del citoplasma. Il flusso di protoni lungo questo gradiente elettrochimico è un processo favorito energeticamente, e può quindi promuovere la sintesi di ATP. 73
74 Fosforilazione ossidativa l energia libera prodotta durante il trasporto degli e- deve essere conservata in una forma utilizzabile dall ATP sintasi. 74
75 Il trasporto degli elettroni, promuove il trasferimento dei protoni da parte del complesso I, III, e IV dalla matrice una regione contenente una bassa concent. di H +, attraverso la membrana mitocondriale interna, caratterizzata da un alta concent. di H + L energia libera sequestrata dal risultante gradiente elettrochimico (forza motrice protonica ) alimenta la sintesi di ATP. 75
76 Il motore della respirazione cellulare: ATP-sintasi La ATP-sintasi trasportante H+ tra due settori è un complesso enzimatico che catalizza la seguente reazione: ADP + fosfato + H+ esterno ATP + H 2 O + H+ interno Quando la reazione è catalizzata verso destra, l'enzima è comunemente chiamato ATP-sintasi ed è responsabile della sintesi di adenosintrifosfato (ATP) utilizzando come substrati adenosindifosfato (ADP) e fosfato inorganico, sfruttando il gradiente protonico generato dalla catena di trasporto degli elettroni. 76
77 L ATP sintasi (F 1 F o -ATPasi) ATPasi), è una proteina transmembrana costituita da più subunità con un peso complessivo di 450 KD. Fo ( lega l antibiotico l oligomicina B) è costituita nei mammiferi da 6 copie di una proteina che attraversa la membrana che formano un canale polare per il passaggio di H +. F1 è costituita da subunità α 3 β 3 γδε. Le subunità α e β sono disposte in modo alternato. Lo stelo è costituito dalla subunità γ associato alle subunità δ ed ε 77
78 Il meccanismo per la sintesi di ATP può essere suddiviso in tre tappe: 1. Traslocazione di protoni promossa da F0 2. Formazione catalitica del legame fosfoanidrinico dell ATP promossa da F1 3. Accoppiamento della dissipazione del gradiente protonico con la sintesi di ATP, che necessitano dell interazione di F1 con F0 78
79 Interconversione dei tre stati conformazionali 1 - L'ADP e il P i si legano debolmente al sito di legame nella conformazione L. 2. Un cambiamento conformazionale promosso dal rilascio di energia libera converte il sito L in sito di legame T (chiamato b TP ) che catalizza la formazione di ATP. Questa tappa implica anche cambiamenti conformazionali negli n altri due protomeri,, che convertono il sito T a cui è legato l'atp in sito aperto (O) (detto b E ), e che convertono il sito O in sito L. 3. L'ATP viene sintetizzato a livello del sito T di una subunità mentre si dissocia dal sito O di un'altra subunità.. L'energia libera fornita dal flusso dei protoni facilita principalmente il rilascio dall'enzima dell'atp appena sintetizzato; cioè,, promuove la transizione T O, distruggendo così le interazioni ATP-enzima che in precedenza avevano promosso la formazione spontanea di ATP a partire da ADP e P i, quando la subunità era nella conformazione T. 79
80 IL RAPPORTO P/O E possibile esprimere la quantità di ATP sintetizzato in termini di molecole di substrato ossidate. Le ossidazioni di NADH e FADH2 sono associati rispettivamente con la sintesi di 3, 2 molecole di ATP. Questa stechiometria chiamata rapporto P/O mette in relazione la quantità di ATP sintetizzata con la quantità di ossigeno che viene ridotto. 80
81 Disaccoppiamento della fosforilazione ossidativa La presenza nella membrana interna di un agente che ne aumenta la l permeabilità agli ioni H + disaccoppia la fosforilazione ossidativa dal trasporto degli elettroni in quanto fornisce una strada per la dissipazione e del gradiente protonico elettrochimico che non necessita della sintesi di ATP. La dissipazione di un gradiente elettrochimico di H +, che viene generato dal trasporto degli elettroni ed è disaccoppiato dalla sintesi di ATP, produce calore. 81
82 Meccanismo d azione d del 2,4-dinitrofenolo Uno ionoforo trasportatore di protoni, come il DNP, disaccoppia la fosforilazione ossidativa dalla catena di trasporto degli elettroni dissipando il gradiente elettrochimico di protoni generato dal trasporto degli elettroni. 82
83 Nel tessuto adiposo bruno ( grasso bruno ) il disaccoppiamento della fosforilazione ossidativa genera calore. I mitocondri del grasso bruno contengono un canale per i protoni conosciuto con il nome di proteina disaccoppiante ( UCP, chiamata Termogenina ). Il flusso di protoni porta alla dissipazione del gradiente protonico presente attraverso la membrana mitocondriale interna. Questo processo consente all ossidazione del substrato di procedere e di generare calore senza sintesi diatp: 83
84 Controllo coordinato della glicolisi e del ciclo dell acido citrico Le fonti principali degli elettroni che entrano nella catena di trasporto degli elettroni sono: Glicolisi Degradazioni degli ac. grassi Ciclo dell ac. citrico Disegno schematico,la sfera verde indica attivazione, la sfera rossa indica inibizione 84
85 Specie reattive dell ossigeno Nella riduzione di O 2 si cela un pericolo: -il trasferimento di 4 elettroni dà origine a prodotti innocui - il trasferimento di un singolo elettrone forma un anione superossido -il trasferimento di 2 elettroni genera un perossido O 2 e-.- O e- 2 O
86 I derivati tossici dell ossigeno molecolare (ROS) vengono rimossi da enzimi protettivi superossido O H + dismutasi O 2 + H 2 O 2 2H 2 O 2 Catalasi. 2 H 2 O + O2 2 GSH+H 2 O 2 GSSG+ 2 H 2 O glutatione perossidasi Della superossido dismutasi (SOD) esistono due forma: La SOD mitocondriale un tetramero contenente Mn La SOD citosolica un dimero contenente Cu e Zn 86
87 Alcune malattie degenerative sono associate a danni ossidativi del mitocondrio: Morbo di Parkinson La malattia di Alzheimer La Corea di Huntington 87
88 Alcuni individui affetti dalla malattia ereditariasclerosi laterale amiotrofica (ALS; malattia di Lou Gehrig) sono caratterizzati da una Cu,Zn-SOD mutata Negli enzimi la magior parte delle mutazioni porta a una perdita della funzione. Nella ALS il difetto viene ereditato con un tratto dominante, fattore che è compatibile con l acquisizione di una attività tossica. Infatti la SOD si comporta come una perossidasi e si pensa che ossidi i lipidi, causando la degenerazione dei motoneuroni, caratteristica della malattia. 88
89 Anemia da carenza di Ferro Fabbisogno di ferro in un uomo adulto: 1mg/die in una donna in età fertile: 2mg/die in una donna in gravidanza: 3mg/die Il ferro è necessario per il mantenimento di una quantità normale di 1. Hb, 2. di citocromi 3. di centri ferro-zolfo. 89
90 Miopatie mitocondriali -il lattato si accumula nel liquido cerebrospinale -crampi, debolezza muscolare, encefalopatia trattamento con CoQ10 -Carenza di CoQ10: forma rara che colpisce i bambini. 90
91 Malattie mitocondriali -Neuropatia ottica ereditaria di Leber (mutazione del Complesso I) - Miopatie mitocondriali -I mitocondri svolgono un ruolo centrale nell apoptosi 91
92 CITOCROMO P450 Sono enzimi ossidativi detossificanti Idrolizzano le molecole idrofobiche in modo da ottenere prodotti solubili Molti dei substrati sono composti tossici come alcuni idrocarburi aromatici policiclici alcuni dei quali cancerogeni: bifenili policlorurati(pcb) L idrossilazione catalizzata dal cit. 450 converte queste molecole in sostanze più solubili per la successiva escrezione 92
Metabolismo: Introduzione
 Metabolismo: Introduzione METABOLISMO Insieme delle reazioni chimiche coordinate e integrate che hanno luogo in tutte le cellule C A T A B O L I S M O Ossidazioni esoergoniche Alimenti: Carboidrati Lipidi
Metabolismo: Introduzione METABOLISMO Insieme delle reazioni chimiche coordinate e integrate che hanno luogo in tutte le cellule C A T A B O L I S M O Ossidazioni esoergoniche Alimenti: Carboidrati Lipidi
Fosforilazione ossidativa
 Fosforilazione ossidativa La fosforilazione ossidativa rappresenta il culmine del metabolismo energetico negli organismi aerobi E costituita da due fenomeni strettamente accoppiati: 1. I coenzimi ridotti
Fosforilazione ossidativa La fosforilazione ossidativa rappresenta il culmine del metabolismo energetico negli organismi aerobi E costituita da due fenomeni strettamente accoppiati: 1. I coenzimi ridotti
4) PROTEINE FERRO ZOLFO. Contengono Fe e S in quantità equimolecolari; fanno parte dei complessi respiratori. La NADH DH contiene diversi centri Fe-S.
 4) PROTEINE FERRO ZOLFO Contengono Fe e S in quantità equimolecolari; fanno parte dei complessi respiratori. La NADH DH contiene diversi centri Fe-S. Trasportano elettroni attraverso le transizioni Fe
4) PROTEINE FERRO ZOLFO Contengono Fe e S in quantità equimolecolari; fanno parte dei complessi respiratori. La NADH DH contiene diversi centri Fe-S. Trasportano elettroni attraverso le transizioni Fe
Catena di Trasporto degli elettroni
 Chimica Biologica A.A. 2010-2011 Catena di Trasporto degli elettroni Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Respirazione - il catabolismo di tutti i combustibili
Chimica Biologica A.A. 2010-2011 Catena di Trasporto degli elettroni Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Respirazione - il catabolismo di tutti i combustibili
Da dove prendono energia le cellule animali?
 Da dove prendono energia le cellule animali? La cellula trae energia dai legami chimici contenuti nelle molecole nutritive Probabilmente le più importanti sono gli zuccheri, che le piante sintetizzano
Da dove prendono energia le cellule animali? La cellula trae energia dai legami chimici contenuti nelle molecole nutritive Probabilmente le più importanti sono gli zuccheri, che le piante sintetizzano
CATENA RESPIRATORIA (CR) FOSFORILAZIONE OSSIDATIVA (FO) scaricato da www.sunhope.it
 CATENA RESPIRATORIA (CR) FOSFORILAZIONE OSSIDATIVA (FO) - Decarb. ossid. piruvato - β-ossidazione acidi grassi - Vie ossidative aa - Ciclo di Krebs avvengono tutte nella matrice mitocondriale In tutte
CATENA RESPIRATORIA (CR) FOSFORILAZIONE OSSIDATIVA (FO) - Decarb. ossid. piruvato - β-ossidazione acidi grassi - Vie ossidative aa - Ciclo di Krebs avvengono tutte nella matrice mitocondriale In tutte
Helena Curtis N. Sue Barnes
 Helena Curtis N. Sue Barnes LA RESPIRAZIONE CELLULARE INDICE Demolizione del glucosio Glicolisi Fermentazione lattica Fermentazione alcolica Respirazione cellulare Ciclo di Krebs Catena di trasporto degli
Helena Curtis N. Sue Barnes LA RESPIRAZIONE CELLULARE INDICE Demolizione del glucosio Glicolisi Fermentazione lattica Fermentazione alcolica Respirazione cellulare Ciclo di Krebs Catena di trasporto degli
Respirazione cellulare
 Respirazione cellulare L equazione generale della respirazione C 6 H 12 O 6 + 6 O 2! 6 CO 2 + 6 H 2 O + 36 ATP 1 molec zucchero 6 molec ossigeno 6 molec anidride carbonica 6 molec acqua + = + + 36 molecole
Respirazione cellulare L equazione generale della respirazione C 6 H 12 O 6 + 6 O 2! 6 CO 2 + 6 H 2 O + 36 ATP 1 molec zucchero 6 molec ossigeno 6 molec anidride carbonica 6 molec acqua + = + + 36 molecole
Il potenziale di riduzione standard (E 0 ) è una misura (in volt) di questa affinità e viene determinato in un esperimento di questo tipo:
 Nella fosforilazione ossidativa il potenziale di trasferimento degli elettroni del NADH e del FADH 2 viene convertito nel potenziale di trasferimento del gruppo fosforico dell ATP ATP. Quando due coppie
Nella fosforilazione ossidativa il potenziale di trasferimento degli elettroni del NADH e del FADH 2 viene convertito nel potenziale di trasferimento del gruppo fosforico dell ATP ATP. Quando due coppie
CELLULE EUCARIOTICHE
 CELLULE EUCARIOTICHE Le cellule eucariotiche sono di maggiori dimensioni, rispetto a quelle procariotiche (almeno 10 volte più grandi) Oltre a: membrana plasmatica, citoplasma, DNA e ribosomi (comuni a
CELLULE EUCARIOTICHE Le cellule eucariotiche sono di maggiori dimensioni, rispetto a quelle procariotiche (almeno 10 volte più grandi) Oltre a: membrana plasmatica, citoplasma, DNA e ribosomi (comuni a
Nicotinamide adenin dinucleotide (NAD + ) H - NMN R AMP. Nel NADP + questo gruppo ossidrilico è esterificato con un gruppo fosforico
 Nicotinamide adenin dinucleotide (NAD + ) H - NMN R AMP Nel NADP + questo gruppo ossidrilico è esterificato con un gruppo fosforico FMN riboflavina. FADH. (FMNH. ) (semichinone) AMP Flavin adenin dinucleotide
Nicotinamide adenin dinucleotide (NAD + ) H - NMN R AMP Nel NADP + questo gruppo ossidrilico è esterificato con un gruppo fosforico FMN riboflavina. FADH. (FMNH. ) (semichinone) AMP Flavin adenin dinucleotide
NADH FADH 2 (trasportatori ridotti di elettroni) Catena respiratoria (trasferimento degli
 NADH FADH 2 (trasportatori ridotti di elettroni) Fase 3 Trasferimento degli elettroni e fosforilazione ossidativa Catena respiratoria (trasferimento degli elettroni) Nicotinamide adenin dinucleotide (NAD
NADH FADH 2 (trasportatori ridotti di elettroni) Fase 3 Trasferimento degli elettroni e fosforilazione ossidativa Catena respiratoria (trasferimento degli elettroni) Nicotinamide adenin dinucleotide (NAD
FUNZIONI DEI MITOCONDRI
 FUNZIONI DEI MITOCONDRI La funzione principale dei mitocondri è di compiere le trasformazioni energetiche indispensabili per le funzioni cellulari. Metabolismo energetico: insieme delle reazioni chimiche
FUNZIONI DEI MITOCONDRI La funzione principale dei mitocondri è di compiere le trasformazioni energetiche indispensabili per le funzioni cellulari. Metabolismo energetico: insieme delle reazioni chimiche
SISTEMI ENERGETICI. L ATP privato di uno dei suoi 3 radicali fosforici diventa ADP (adenosindifosfato).
 SISTEMI ENERGETICI LE FONTI ENERGETICHE MUSCOLARI I movimenti sono resi possibili, dal punto di vista energetico, grazie alla trasformazione, da parte dei muscoli, dell energia chimica ( trasformazione
SISTEMI ENERGETICI LE FONTI ENERGETICHE MUSCOLARI I movimenti sono resi possibili, dal punto di vista energetico, grazie alla trasformazione, da parte dei muscoli, dell energia chimica ( trasformazione
Infatti il glucosio viene bruciato in presenza di ossigeno e l'energia liberata, immagazzinata sotto forma di ATP
 I mitocondri sono gli organuli responsabili della produzione di energia necessaria alla cellula per crescere e riprodursi. Queste reazioni, che nel loro insieme costituiscono il processo di "respirazione
I mitocondri sono gli organuli responsabili della produzione di energia necessaria alla cellula per crescere e riprodursi. Queste reazioni, che nel loro insieme costituiscono il processo di "respirazione
L ossidazione completa del glucosio da parte dell O 2. può essere suddivisa in due semi-reazioni
 L ossidazione completa del glucosio da parte dell O 2 C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O può essere suddivisa in due semi-reazioni C 6 H 12 O 6 + 6 O 2 6 CO 2 + 24 H + + 24 e - (si ossidano gli atomi
L ossidazione completa del glucosio da parte dell O 2 C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O può essere suddivisa in due semi-reazioni C 6 H 12 O 6 + 6 O 2 6 CO 2 + 24 H + + 24 e - (si ossidano gli atomi
L ossidazione completa del glucosio da parte dell O 2. può essere suddivisa in due semi-reazioni
 L ossidazione completa del glucosio da parte dell O 2 C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O può essere suddivisa in due semi-reazioni C 6 H 12 O 6 + 6 O 2 6 CO 2 + 24 H + + 24 e - (si ossidano gli atomi
L ossidazione completa del glucosio da parte dell O 2 C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O può essere suddivisa in due semi-reazioni C 6 H 12 O 6 + 6 O 2 6 CO 2 + 24 H + + 24 e - (si ossidano gli atomi
Il mantenimento dell omeostasi cellulare dipende dai sistemi che permettono lo scambio di molecole tra citoplasma e liquido
 Il mantenimento dell omeostasi cellulare dipende dai sistemi che permettono lo scambio di molecole tra citoplasma e liquido extracellulare e dalla loro regolazione. Membrana cellulare Ogni cellula presenta
Il mantenimento dell omeostasi cellulare dipende dai sistemi che permettono lo scambio di molecole tra citoplasma e liquido extracellulare e dalla loro regolazione. Membrana cellulare Ogni cellula presenta
PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA
 PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA Svolgono la loro funzione legando reversibilmente l OSSIGENO. Aumentano la solubilità dell ossigeno nel plasma, da 3ml/L a 220 ml/l. La mioglobina
PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA Svolgono la loro funzione legando reversibilmente l OSSIGENO. Aumentano la solubilità dell ossigeno nel plasma, da 3ml/L a 220 ml/l. La mioglobina
Fosforilazione ossidativa
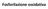 Fosforilazione ossidativa FOSFORILAZIONE OSSIDATIVA La fosforilazione ossidativa è la via finale del metabolismo energetico, in cui gli elettroni (NADH e FADH 2 ) provenienti dalle molecole energetiche
Fosforilazione ossidativa FOSFORILAZIONE OSSIDATIVA La fosforilazione ossidativa è la via finale del metabolismo energetico, in cui gli elettroni (NADH e FADH 2 ) provenienti dalle molecole energetiche
La fotosintesi: energia dal Sole
 La fotosintesi: energia dal Sole Gli organismi fotosintetici usano la luce del Sole, l acqua del suolo e il CO 2 dell atmosfera per produrre composti organici e liberare O 2 grazie alla fotosintesi. Sadava
La fotosintesi: energia dal Sole Gli organismi fotosintetici usano la luce del Sole, l acqua del suolo e il CO 2 dell atmosfera per produrre composti organici e liberare O 2 grazie alla fotosintesi. Sadava
Giovanni Di Bonaventura, Ph.D., B.Sc. Università di Chieti-Pescara
 Giovanni Di Bonaventura, Ph.D., B.Sc. Università di Chieti-Pescara Richieste metaboliche: elementi essenziali In generale, i batteri per la loro crescita hanno bisogno di elementi essenziali. In particolare
Giovanni Di Bonaventura, Ph.D., B.Sc. Università di Chieti-Pescara Richieste metaboliche: elementi essenziali In generale, i batteri per la loro crescita hanno bisogno di elementi essenziali. In particolare
Βeta ossidazione degli acidi grassi BETA OSSIDAZIONE DEGLI ACIDI GRASSI 13/12/2013 SEMINARIO. Acidi grassi (2)
 Acidi grassi (1) Mitocondri SEMINARIO BETA OSSIDAZIONE DEGLI ACIDI GRASSI Sono le principali fonti di energia per alcuni tessuti (es. muscolo cardiaco). Si genera molto più energia dall ossidazione degli
Acidi grassi (1) Mitocondri SEMINARIO BETA OSSIDAZIONE DEGLI ACIDI GRASSI Sono le principali fonti di energia per alcuni tessuti (es. muscolo cardiaco). Si genera molto più energia dall ossidazione degli
Mitocondri e malattie neurodegenerative. metabolismo energetico bilancio redox sopravvivenza cellulare metabolismo del calcio
 Mitocondri e malattie neurodegenerative Mitocondri metabolismo energetico bilancio redox sopravvivenza cellulare metabolismo del calcio Danno mitocondriale: dismetabolismo energetico (necrosi) stress ossidativo
Mitocondri e malattie neurodegenerative Mitocondri metabolismo energetico bilancio redox sopravvivenza cellulare metabolismo del calcio Danno mitocondriale: dismetabolismo energetico (necrosi) stress ossidativo
BIOLOGIA GENERALE 22-24 ottobre 2007
 Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE 22-24 ottobre 2007 Facoltà di Psicologia Tecniche di Psicologia Generale e Sperimentale Alessandro Massolo Dip.
Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE 22-24 ottobre 2007 Facoltà di Psicologia Tecniche di Psicologia Generale e Sperimentale Alessandro Massolo Dip.
Come le cellule traggono energia dal cibo: produzione di ATP
 Come le cellule traggono energia dal cibo: produzione di ATP L energia è contenuta nei legami chimici delle molecole nutritive; la cellula estrae questa energia e la conserva nell ATP: respirazione cellulare
Come le cellule traggono energia dal cibo: produzione di ATP L energia è contenuta nei legami chimici delle molecole nutritive; la cellula estrae questa energia e la conserva nell ATP: respirazione cellulare
N 2, malgrado la sua abbondanza, è un fattore limitante la crescita della maggior parte degli organismi
 Glicina (Gly) Alanina (Ala) N 2, malgrado la sua abbondanza, è un fattore limitante la crescita della maggior parte degli organismi La digestione delle proteine endopeptidasi H O R H O R R H 3+ N -C-C-NH-C-C-NH-C-C-NH-C-C-NH-C-COO
Glicina (Gly) Alanina (Ala) N 2, malgrado la sua abbondanza, è un fattore limitante la crescita della maggior parte degli organismi La digestione delle proteine endopeptidasi H O R H O R R H 3+ N -C-C-NH-C-C-NH-C-C-NH-C-C-NH-C-COO
unità C2. Le trasformazioni energetiche nelle cellule
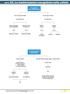 unità 2. Le trasformazioni energetiche nelle cellule Il trasporto nelle cellule avviene senza consumo di energia con consumo di energia trasporto passivo trasporto attivo attraverso il doppio strato fosfolipidico
unità 2. Le trasformazioni energetiche nelle cellule Il trasporto nelle cellule avviene senza consumo di energia con consumo di energia trasporto passivo trasporto attivo attraverso il doppio strato fosfolipidico
FADH ADP + Pi ATP...29 AG ' = -30,5 kj/mol...29 Resa di ATP per l ossidazione completa del glucosio...31
 FOSFORILAZIONE OSSIDATIVA FOSFORILAZIONE OSSIDATIVA...1 Glicolisi e ciclo di Krebs...3 il NADH il NADPH e il FADH2 sono traportatori solubili di elettroni...4 LA FOSFORILAZIONE OSSIDATIVA...5 Il mitocondrio...5
FOSFORILAZIONE OSSIDATIVA FOSFORILAZIONE OSSIDATIVA...1 Glicolisi e ciclo di Krebs...3 il NADH il NADPH e il FADH2 sono traportatori solubili di elettroni...4 LA FOSFORILAZIONE OSSIDATIVA...5 Il mitocondrio...5
Catena di trasporto degli elettroni (catena respiratoria) e Fosforilazione ossidativa
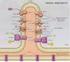 Catena di trasporto degli elettroni (catena respiratoria) e Fosforilazione ossidativa NADH e FADH2 (accettori universali di e-) formati nella glicolisi e nel ciclo di Krebs (e nell ossidazione degli acidi
Catena di trasporto degli elettroni (catena respiratoria) e Fosforilazione ossidativa NADH e FADH2 (accettori universali di e-) formati nella glicolisi e nel ciclo di Krebs (e nell ossidazione degli acidi
I Mitocondri Centrale elettrica cellulare
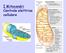 I Mitocondri Centrale elettrica cellulare Potenziale redox standard Fe 2+ D Fe 3+ + e - Fe 2+ + Cu 2+ D Fe 3+ + Cu + Cu 2+ + e - D Cu + Ε = E + RT nf ln [accettore elettroni] [donatore elettroni] n = n
I Mitocondri Centrale elettrica cellulare Potenziale redox standard Fe 2+ D Fe 3+ + e - Fe 2+ + Cu 2+ D Fe 3+ + Cu + Cu 2+ + e - D Cu + Ε = E + RT nf ln [accettore elettroni] [donatore elettroni] n = n
GLUCONEOGENESI. Sintesi (GENESI) di nuove (NEO) molecole di glucosio
 GLUCONEOGENESI Sintesi (GENESI) di nuove (NEO) molecole di glucosio CATABOLISMO ANABOLISMO OSSIDAZIONI Produzione di ATP RIDUZIONI Consumo di ATP La GLUCONEOGENESI è un PROCESSO ANABOLICO La gluconeogenesi
GLUCONEOGENESI Sintesi (GENESI) di nuove (NEO) molecole di glucosio CATABOLISMO ANABOLISMO OSSIDAZIONI Produzione di ATP RIDUZIONI Consumo di ATP La GLUCONEOGENESI è un PROCESSO ANABOLICO La gluconeogenesi
Regolazione del metabolismo del glucosio
 Regolazione del metabolismo del glucosio Regolazione coordinata di glicolisi e gluconeogenesi Glicolisi e gluconeogenesi sono regolate in modo reciproco La regolazione è a livello dei punti di deviazione
Regolazione del metabolismo del glucosio Regolazione coordinata di glicolisi e gluconeogenesi Glicolisi e gluconeogenesi sono regolate in modo reciproco La regolazione è a livello dei punti di deviazione
ENZIMI CINETICA ENZIMATICA
 ENZIMI PERCHE UNA REAZIONE AVVENGA, SI DEVONO SODDISFARE TRE CONDIZIONI I SUBSTRATI DEVONO ENTRARE IN COLLISIONE LA COLLISIONE DEVE AVVENIRE CON ORIENTAMENTO CORRETTO I REAGENTI DEVONO AVERE ENERGIA SUFFICIENTE
ENZIMI PERCHE UNA REAZIONE AVVENGA, SI DEVONO SODDISFARE TRE CONDIZIONI I SUBSTRATI DEVONO ENTRARE IN COLLISIONE LA COLLISIONE DEVE AVVENIRE CON ORIENTAMENTO CORRETTO I REAGENTI DEVONO AVERE ENERGIA SUFFICIENTE
L ossidazione completa del glucosio da parte dell O 2. può essere suddivisa in due semi-reazioni
 L ossidazione completa del glucosio da parte dell O 2 C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O può essere suddivisa in due semi-reazioni C 6 H 12 O 6 + 6 O 2 6 CO 2 + 24 H + + 24 e - (si ossidano gli atomi
L ossidazione completa del glucosio da parte dell O 2 C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O può essere suddivisa in due semi-reazioni C 6 H 12 O 6 + 6 O 2 6 CO 2 + 24 H + + 24 e - (si ossidano gli atomi
Integrali (transmembrana), si estendono attraverso l intera membrana. Classificate in famiglie a seconda del numero di segmenti transmembrana.
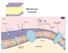 Membrana cellulare Proteine inserite nella membrana cellulare: Integrali (transmembrana), si estendono attraverso l intera membrana. Classificate in famiglie a seconda del numero di segmenti transmembrana.
Membrana cellulare Proteine inserite nella membrana cellulare: Integrali (transmembrana), si estendono attraverso l intera membrana. Classificate in famiglie a seconda del numero di segmenti transmembrana.
Metabolismo degli aminoacidi
 Metabolismo degli aminoacidi Quando gli aminoacidi provenienti dalla digestione gastrica e intestinale, non vengono utilizzati per la costruzione di nuove proteine vengono demoliti Transaminazione Per
Metabolismo degli aminoacidi Quando gli aminoacidi provenienti dalla digestione gastrica e intestinale, non vengono utilizzati per la costruzione di nuove proteine vengono demoliti Transaminazione Per
Le Biomolecole I parte. Lezioni d'autore di Giorgio Benedetti
 Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
FOSFORILAZIONE OSSIDATIVA
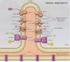 FOSFORILAZIONE OSSIDATIVA Lo scopo ultimo dei processi metabolici ossidativi è quello di canalizzare l energia contenuta nello scheletro carbonioso di zuccheri, ac. grassi e amminoacidi nella sintesi di
FOSFORILAZIONE OSSIDATIVA Lo scopo ultimo dei processi metabolici ossidativi è quello di canalizzare l energia contenuta nello scheletro carbonioso di zuccheri, ac. grassi e amminoacidi nella sintesi di
Il ciclo dell acido citrico
 Il ciclo dell acido citrico Il catabolismo di proteine, grassi e carboidrati avviene nelle tre fasi della respirazione cellulare Il piruvato viene ossidato ad acetil-coa e CO 2 La decarbossilazione
Il ciclo dell acido citrico Il catabolismo di proteine, grassi e carboidrati avviene nelle tre fasi della respirazione cellulare Il piruvato viene ossidato ad acetil-coa e CO 2 La decarbossilazione
in Terminazione Neurone Dendriti Soma Fessura sinaptica sinaptica Nucleo dendrite Segmento iniziale Sinapsi inibitoria Segmento mielinico Assone
 Le funzioni del sistema nervoso si basano sull attività dei neuroni che consiste nel generare, trasmettere ed elaborare informazioni nervose, che dipendono da modificazioni del potenziale di membrana,
Le funzioni del sistema nervoso si basano sull attività dei neuroni che consiste nel generare, trasmettere ed elaborare informazioni nervose, che dipendono da modificazioni del potenziale di membrana,
Ruolo metabolico delle flavine
 Ruolo metabolico delle flavine Deidrogenasi flaviniche che trasferiscono 2 elettroni Acil CoA deidrogenasi (beta ossidazione acidi grassi) Diidrolipoildeidrogenasi (complessi piruvato dh etc.) Glutatione
Ruolo metabolico delle flavine Deidrogenasi flaviniche che trasferiscono 2 elettroni Acil CoA deidrogenasi (beta ossidazione acidi grassi) Diidrolipoildeidrogenasi (complessi piruvato dh etc.) Glutatione
Tipi di reazioni. Reazioni chimiche. Di dissociazione. Di sintesi. Di semplice scambio. Di doppio scambio. Reazioni complesse
 Tipi di reazioni Le reazioni chimiche vengono tradizionalmente classificate a seconda del tipo di trasformazione subita dai reagenti: Reazioni chimiche possono essere Di dissociazione Una sostanza subisce
Tipi di reazioni Le reazioni chimiche vengono tradizionalmente classificate a seconda del tipo di trasformazione subita dai reagenti: Reazioni chimiche possono essere Di dissociazione Una sostanza subisce
Prof. Maria Nicola GADALETA
 Prof. Maria Nicola GADALETA Email: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA Email: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Valitutti, Taddei, Kreuzer, Massey, Sadava, Hills, Heller, Berenbaum
 Dal carbonio agli OGM VERSO L UNIVERSITÀ Le domande sono tratte dalle prove di ammissione emesse annualmente dal Ministero dell Istruzione, dell Università e della Ricerca (MIUR) e le soluzioni sono evidenziate
Dal carbonio agli OGM VERSO L UNIVERSITÀ Le domande sono tratte dalle prove di ammissione emesse annualmente dal Ministero dell Istruzione, dell Università e della Ricerca (MIUR) e le soluzioni sono evidenziate
Trasformazioni materia
 REAZIONI CHIMICHE Trasformazioni materia Trasformazioni fisiche (reversibili) Trasformazioni chimiche (irreversibili) È una trasformazione che non produce nuove sostanze È una trasformazione che produce
REAZIONI CHIMICHE Trasformazioni materia Trasformazioni fisiche (reversibili) Trasformazioni chimiche (irreversibili) È una trasformazione che non produce nuove sostanze È una trasformazione che produce
DNA - RNA. Nucleotide = Gruppo Fosforico + Zucchero Pentoso + Base Azotata. Le unità fondamentali costituenti il DNA e l RNA sono i Nucleotidi.
 DNA - RNA Le unità fondamentali costituenti il DNA e l RNA sono i Nucleotidi. Nucleotide = Gruppo Fosforico + Zucchero Pentoso + Base Azotata. Esistono 4 basi azotate per il DNA e 4 per RNA Differenze
DNA - RNA Le unità fondamentali costituenti il DNA e l RNA sono i Nucleotidi. Nucleotide = Gruppo Fosforico + Zucchero Pentoso + Base Azotata. Esistono 4 basi azotate per il DNA e 4 per RNA Differenze
CATENA RESPIRATORIA (CR) FOSFORILAZIONE OSSIDATIVA (FO)
 CATENA RESPIRATORIA (CR) FOSFORILAZIONE OSSIDATIVA (FO) - Decarb. ossid. piruvato - -Ossidazione acidi grassi - Vie ossidative aa -Ciclo di Krebs avvengono tutte nella matrice mitocondriale In tutte queste
CATENA RESPIRATORIA (CR) FOSFORILAZIONE OSSIDATIVA (FO) - Decarb. ossid. piruvato - -Ossidazione acidi grassi - Vie ossidative aa -Ciclo di Krebs avvengono tutte nella matrice mitocondriale In tutte queste
SOLUZIONI DEGLI ESERCIZI
 Niccolò Taddei - Biochimica Capitolo 9 METABOLISMO TERMINALE E PRODUZIONE DI ENERGIA 1 Il ciclo dell acido citrico è definito anche ciclo di Krebs, dal nome di uno dei suoi scopritori, o ciclo degli acidi
Niccolò Taddei - Biochimica Capitolo 9 METABOLISMO TERMINALE E PRODUZIONE DI ENERGIA 1 Il ciclo dell acido citrico è definito anche ciclo di Krebs, dal nome di uno dei suoi scopritori, o ciclo degli acidi
: : H-Cl + H-N: H-N-H + : Cl : H
 Negli organismi viventi la maggior parte dell energia libera richiesta per promuovere le reazioni biochimiche deriva dall ossidazione dei substrati organici. L ossigeno, l accettore finale degli elettroni
Negli organismi viventi la maggior parte dell energia libera richiesta per promuovere le reazioni biochimiche deriva dall ossidazione dei substrati organici. L ossigeno, l accettore finale degli elettroni
Fosforilazione ossidativa
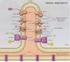 Fosforilazione ossidativa H 2 2H + + 2e - NADH+H + NAD + + 2H + +2e - FADH 2 FAD + 2H + + 2e - ½O 2 + 2H + + 2e - H 2 O + Calore ½ O 2 + 2H + + 2e - H 2 O + ATP 1 La fosforilazione ossidativa avviene nella
Fosforilazione ossidativa H 2 2H + + 2e - NADH+H + NAD + + 2H + +2e - FADH 2 FAD + 2H + + 2e - ½O 2 + 2H + + 2e - H 2 O + Calore ½ O 2 + 2H + + 2e - H 2 O + ATP 1 La fosforilazione ossidativa avviene nella
http://sds.coniliguria.it 1
 Aspetti metabolici dell esercizio fisico Genova 22 gennaio 2011 A cura di Attilio TRAVERSO http://sds.coniliguria.it 1 L allenamento produce modificazioni fisiologiche (adattamenti) in quasi tutti i sistemi
Aspetti metabolici dell esercizio fisico Genova 22 gennaio 2011 A cura di Attilio TRAVERSO http://sds.coniliguria.it 1 L allenamento produce modificazioni fisiologiche (adattamenti) in quasi tutti i sistemi
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 26 La gluconeogenesi Concetti chiave: Il fegato e il rene possono sintetizzare glucosio da lattato, piruvato e amminoacidi.
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 26 La gluconeogenesi Concetti chiave: Il fegato e il rene possono sintetizzare glucosio da lattato, piruvato e amminoacidi.
Niccolò Taddei Biochimica
 Niccolò Taddei Biochimica VERSO L UNIVERSITÀ Le domande sono tratte dalle prove di ammissione emesse annualmente dal Ministero dell Istruzione, dell Università e della Ricerca (MIUR) e le soluzioni sono
Niccolò Taddei Biochimica VERSO L UNIVERSITÀ Le domande sono tratte dalle prove di ammissione emesse annualmente dal Ministero dell Istruzione, dell Università e della Ricerca (MIUR) e le soluzioni sono
ANTIOSSIDANTI Grassi IV LEZIONE
 ANTIOSSIDANTI Grassi IV LEZIONE ANTIOSSIDANTE Sostanza che, pur presente in concentrazione ridotta rispetto al substrato ossidabile, può prevenire o ritardare l ossidazione iniziata da un fattore proossidante.
ANTIOSSIDANTI Grassi IV LEZIONE ANTIOSSIDANTE Sostanza che, pur presente in concentrazione ridotta rispetto al substrato ossidabile, può prevenire o ritardare l ossidazione iniziata da un fattore proossidante.
dieta vengono convertiti in composti dei corpi chetonici.
 Metabolismo degli aminoacidi Metabolismo degli aminoacidi Gli aminoacidi introdotti in eccesso con la dieta vengono convertiti in composti precursori del glucosio, degli acidi grassi e dei corpi chetonici.
Metabolismo degli aminoacidi Metabolismo degli aminoacidi Gli aminoacidi introdotti in eccesso con la dieta vengono convertiti in composti precursori del glucosio, degli acidi grassi e dei corpi chetonici.
La membrana cellulare racchiude il protoplasma, la sostanza vivente che costituisce la cellula, e lo separa dall ambiente esterno, extracellulare.
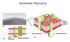 Membrana Plasmatica La membrana cellulare racchiude il protoplasma, la sostanza vivente che costituisce la cellula, e lo separa dall ambiente esterno, extracellulare. La sua funzione principale è quella
Membrana Plasmatica La membrana cellulare racchiude il protoplasma, la sostanza vivente che costituisce la cellula, e lo separa dall ambiente esterno, extracellulare. La sua funzione principale è quella
TIAMINA (vitamina B1, aneurina)
 TIAMINA (vitamina B1, aneurina) Fonti alimentari: cereali integrali (germe e crusca), carne (maiale), lievito di birra, legumi Abbondanza nell organismo umano : 30-100 mg RDA (assunzione giornaliera di
TIAMINA (vitamina B1, aneurina) Fonti alimentari: cereali integrali (germe e crusca), carne (maiale), lievito di birra, legumi Abbondanza nell organismo umano : 30-100 mg RDA (assunzione giornaliera di
METABOLISMO E SISTEMI ENERGETICI
 METABOLISMO E SISTEMI ENERGETICI 1 Obiettivi della lezione 1) Capire come l organismo converta il cibo che ingeriamo in ATP per fornire ai muscoli l energia che essi necessitano per contrarsi. 2) Esaminare
METABOLISMO E SISTEMI ENERGETICI 1 Obiettivi della lezione 1) Capire come l organismo converta il cibo che ingeriamo in ATP per fornire ai muscoli l energia che essi necessitano per contrarsi. 2) Esaminare
ADP + HPO 3, NAD +, NADP +, FAD ATP, NADH, NADPH, FADH 2 ENERGIA CHIMICA
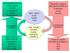 MACROMOLECOLE CELLULARI Proteine Polisaccaridi Lipidi Acidi nucleici ADP + HPO 3 2-, NAD +, NADP +, FAD Metaboliti complessi RICCHI DI ENERGIA Carboidrati Lipidi Proteine ANABOLISMO (biosintesi) MOLECOLE
MACROMOLECOLE CELLULARI Proteine Polisaccaridi Lipidi Acidi nucleici ADP + HPO 3 2-, NAD +, NADP +, FAD Metaboliti complessi RICCHI DI ENERGIA Carboidrati Lipidi Proteine ANABOLISMO (biosintesi) MOLECOLE
Adattamenti del muscolo scheletrico all allenamento aerobico: ruolo dei radicali
 Adattamenti del muscolo scheletrico all allenamento aerobico: ruolo dei radicali Marina Marini Dipartimento di Medicina Specialistica, Diagnostica e Sperimentale Cosa sono i radicali? I radicali liberi
Adattamenti del muscolo scheletrico all allenamento aerobico: ruolo dei radicali Marina Marini Dipartimento di Medicina Specialistica, Diagnostica e Sperimentale Cosa sono i radicali? I radicali liberi
Proteine integrali di membrana legate sul versante esterno a gruppi di carboidrati. Formati da diverse subunità che circoscrivono un poro acquoso che
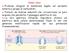 Canali ionici Proteine integrali di membrana legate sul versante esterno a gruppi di carboidrati. Formati da diverse subunità che circoscrivono un poro acquoso che permette il passaggio selettivo di ioni.
Canali ionici Proteine integrali di membrana legate sul versante esterno a gruppi di carboidrati. Formati da diverse subunità che circoscrivono un poro acquoso che permette il passaggio selettivo di ioni.
FOTOSINTESI: LA FASE LUMINOSA
 FOTOSINTESI: LA FASE LUMINOSA Un video : Clic Premessa (I) In questa lezione si esamina in dettaglio la serie di reazioni che trasformano l'energia solare in energia chimica fino alla sintesi di ATP e
FOTOSINTESI: LA FASE LUMINOSA Un video : Clic Premessa (I) In questa lezione si esamina in dettaglio la serie di reazioni che trasformano l'energia solare in energia chimica fino alla sintesi di ATP e
La degradazione ossidativa di zuccheri, ac. grassi, e amminoacidi. livello del substrato) Equivalenti riducenti di NADH e FADH 2
 La degradazione ossidativa di zuccheri, ac. grassi, e amminoacidi produce energia: ATP (fosforilazioni a livello del substrato) Equivalenti riducenti di NADH e FADH 2 Dalla loro ri-ossidazione si può ottenere
La degradazione ossidativa di zuccheri, ac. grassi, e amminoacidi produce energia: ATP (fosforilazioni a livello del substrato) Equivalenti riducenti di NADH e FADH 2 Dalla loro ri-ossidazione si può ottenere
PROTEINE. Amminoacidi
 PROTEINE Le proteine sono le macromolecole alla base delle attività cellulari. Sono oltre diecimila per cellula, dove svolgono differenti funzioni: Sono ad esempio: enzimi: aumentano la velocità delle
PROTEINE Le proteine sono le macromolecole alla base delle attività cellulari. Sono oltre diecimila per cellula, dove svolgono differenti funzioni: Sono ad esempio: enzimi: aumentano la velocità delle
Elettroforesi. Elettroforesi: processo per cui molecole cariche si separano in un campo elettrico a causa della loro diversa mobilita.
 Elettroforesi Elettroforesi: processo per cui molecole cariche si separano in un campo elettrico a causa della loro diversa mobilita. A qualunque ph diverso dal pi le proteine hanno una carica netta quindi,
Elettroforesi Elettroforesi: processo per cui molecole cariche si separano in un campo elettrico a causa della loro diversa mobilita. A qualunque ph diverso dal pi le proteine hanno una carica netta quindi,
Funzioni della membrana plasmatica
 TRASPORTO M.P. -Omeostasi cellulare Funzioni della membrana plasmatica Mantenimento della conc. intracell. di ioni e molecole entro valori corretti Scambi interno - esterno Non c è consumo E Consumo E
TRASPORTO M.P. -Omeostasi cellulare Funzioni della membrana plasmatica Mantenimento della conc. intracell. di ioni e molecole entro valori corretti Scambi interno - esterno Non c è consumo E Consumo E
16/12/2011. Mitocondri. Biotecnologie_2011
 Mitocondri Biotecnologie_2011 1 *l ambiente in assoluto più ossigenato, se sangue arterioso * http://humanphisiology.wikispaces.com/05 Hematology http://thejns.org/na101/home/literatum/publisher/jns/journals/content/jn
Mitocondri Biotecnologie_2011 1 *l ambiente in assoluto più ossigenato, se sangue arterioso * http://humanphisiology.wikispaces.com/05 Hematology http://thejns.org/na101/home/literatum/publisher/jns/journals/content/jn
Prof. Maria Nicola GADALETA
 Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Potenziale di membrana: Differenza di potenziale elettrico a cavallo della membrana cellulare dovuta ad una diversa distribuzione ionica ai due lati
 Potenziale di membrana: Differenza di potenziale elettrico a cavallo della membrana cellulare dovuta ad una diversa distribuzione ionica ai due lati della membrana. Il potenziale di membrana (negativo
Potenziale di membrana: Differenza di potenziale elettrico a cavallo della membrana cellulare dovuta ad una diversa distribuzione ionica ai due lati della membrana. Il potenziale di membrana (negativo
ossigeno e ne facilita la diffusione dai capillari all ambiente intracellulare.
 Ricostituzione e attività pseudoenzimatica della mioglobina modificata Giulia Bertelegni e Carolina Ferrari I.I.S. A.Maserati Facoltà di Scienze MM.FF.NN. Dipartimento di Chimica generale Università degli
Ricostituzione e attività pseudoenzimatica della mioglobina modificata Giulia Bertelegni e Carolina Ferrari I.I.S. A.Maserati Facoltà di Scienze MM.FF.NN. Dipartimento di Chimica generale Università degli
Mediatore chimico. Recettore. Trasduzione del segnale. Risposta della cellula
 Mediatore chimico Recettore Trasduzione del segnale Risposta della cellula I mediatori chimici sono prodotti da cellule specializzate e sono diffusi nell organismo da apparati di distribuzione Sistemi
Mediatore chimico Recettore Trasduzione del segnale Risposta della cellula I mediatori chimici sono prodotti da cellule specializzate e sono diffusi nell organismo da apparati di distribuzione Sistemi
Energia nelle reazioni chimiche. Lezioni d'autore di Giorgio Benedetti
 Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica.
 Concanavalina A Emoglobina subunità Trioso fosfato isomerasi Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica. 1 La conformazione è
Concanavalina A Emoglobina subunità Trioso fosfato isomerasi Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica. 1 La conformazione è
... corso di chimica elettrochimica 1
 ... corso di chimica elettrochimica 1 CONTENUTI reazioni elettrochimiche pile e celle elettrolitiche potenziale d elettrodo e forza elettromotrice equazione di Nernst elettrolisi leggi di Faraday batterie
... corso di chimica elettrochimica 1 CONTENUTI reazioni elettrochimiche pile e celle elettrolitiche potenziale d elettrodo e forza elettromotrice equazione di Nernst elettrolisi leggi di Faraday batterie
Figura 1. Rappresentazione della doppia elica di DNA e struttura delle differenti basi.
 Sommario La molecola di DNA è deputata a conservare le informazioni genetiche necessarie per lo sviluppo ed il funzionamento degli organismi viventi. Poiché contiene le istruzioni per la costruzione delle
Sommario La molecola di DNA è deputata a conservare le informazioni genetiche necessarie per lo sviluppo ed il funzionamento degli organismi viventi. Poiché contiene le istruzioni per la costruzione delle
La pompa Na + /Glucosio: simporto
 MFN0366-A1 (I. Perroteau) - trasportatori e canali La pompa Na + /Glucosio: simporto Il trasportatore oscilla fra due stati alternativi (A e B); nello stato A la proteina è aperta nello spazio extracellulare,
MFN0366-A1 (I. Perroteau) - trasportatori e canali La pompa Na + /Glucosio: simporto Il trasportatore oscilla fra due stati alternativi (A e B); nello stato A la proteina è aperta nello spazio extracellulare,
Equilibri di precipitazione
 Equilibri di precipitazione Molte sostanze solide sono caratterizzate da una scarsa solubilità in acqua (ad es. tutti i carbonati e gli idrossidi degli elementi del II gruppo) AgCl (a differenza di NaCl)
Equilibri di precipitazione Molte sostanze solide sono caratterizzate da una scarsa solubilità in acqua (ad es. tutti i carbonati e gli idrossidi degli elementi del II gruppo) AgCl (a differenza di NaCl)
Legami chimici. Covalente. Legami deboli
 Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
«Macromolecole» Lipidi
 LIPIDI (1) «Macromolecole» Lipidi Biotecnologie Miscellanea di molecole biologiche che condividono la proprietà di non essere solubili in acqua. Molecole idrofobiche. Es: Grassi Oli (grasso liquido a temperatura
LIPIDI (1) «Macromolecole» Lipidi Biotecnologie Miscellanea di molecole biologiche che condividono la proprietà di non essere solubili in acqua. Molecole idrofobiche. Es: Grassi Oli (grasso liquido a temperatura
PROTEINE. sono COMPOSTI ORGANICI QUATERNARI
 PROTEINE sono COMPOSTI ORGANICI QUATERNARI Unione di elementi chimici diversi Il composto chimico principale è il C (carbonio) Sono quattro gli elementi chimici principali che formano le proteine : C (carbonio),
PROTEINE sono COMPOSTI ORGANICI QUATERNARI Unione di elementi chimici diversi Il composto chimico principale è il C (carbonio) Sono quattro gli elementi chimici principali che formano le proteine : C (carbonio),
SINTESI PROTEICA. Replicazione. Trascrizione. Traduzione
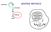 Replicazione SINTESI PROTEICA Trascrizione Traduzione 61 codoni codificanti 3 triplette non senso (STOP) AUG codone di inizio codone per Met Caratteristiche del codice genetico Specificità Il codice genetico
Replicazione SINTESI PROTEICA Trascrizione Traduzione 61 codoni codificanti 3 triplette non senso (STOP) AUG codone di inizio codone per Met Caratteristiche del codice genetico Specificità Il codice genetico
I MITOCONDRI: LE CENTRALI ENERGETICHE DELLA CELLULA
 I MITOCONDRI: LE CENTRALI ENERGETICHE DELLA CELLULA MITOCONDRIO OSSERVATO AL SEM Localizzazione dei mitocondri SONO IN GENERE PIÙ ABBONDANTI DELLE ZONE DELLA CELLULA CHE RICHIEDONO MAGGIORI QUANTITA DI
I MITOCONDRI: LE CENTRALI ENERGETICHE DELLA CELLULA MITOCONDRIO OSSERVATO AL SEM Localizzazione dei mitocondri SONO IN GENERE PIÙ ABBONDANTI DELLE ZONE DELLA CELLULA CHE RICHIEDONO MAGGIORI QUANTITA DI
SINTESI DELL RNA. Replicazione. Trascrizione. Traduzione
 SINTESI DELL RNA Replicazione Trascrizione Traduzione L RNA ha origine da informazioni contenute nel DNA La TRASCRIZIONE permette la conversione di una porzione di DNA in una molecola di RNA con una sequenza
SINTESI DELL RNA Replicazione Trascrizione Traduzione L RNA ha origine da informazioni contenute nel DNA La TRASCRIZIONE permette la conversione di una porzione di DNA in una molecola di RNA con una sequenza
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA
 LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
TEST BIOLOGIA 1 ANNO ABEI Da inviare a connesso@alice.it entro e non oltre il 6 novembre 2015
 1) I batteri sono organismi: a- bicellulari b- monocellulari c- pluricellulari 2) I virus: a- possono riprodursi solo nell acqua b- possono riprodursi solo sulla superficie di una cellula c- possono riprodursi
1) I batteri sono organismi: a- bicellulari b- monocellulari c- pluricellulari 2) I virus: a- possono riprodursi solo nell acqua b- possono riprodursi solo sulla superficie di una cellula c- possono riprodursi
Celle a combustibile Fuel cells (FC)
 Celle a combustibile Fuel cells (FC) Celle a combustibile Sono dispositivi di conversione elettrochimica ad alto rendimento energetico. Esse trasformano in potenza elettrica l energia chimica contenuta
Celle a combustibile Fuel cells (FC) Celle a combustibile Sono dispositivi di conversione elettrochimica ad alto rendimento energetico. Esse trasformano in potenza elettrica l energia chimica contenuta
LA CORRENTE ELETTRICA
 L CORRENTE ELETTRIC H P h Prima che si raggiunga l equilibrio c è un intervallo di tempo dove il livello del fluido non è uguale. Il verso del movimento del fluido va dal vaso a livello maggiore () verso
L CORRENTE ELETTRIC H P h Prima che si raggiunga l equilibrio c è un intervallo di tempo dove il livello del fluido non è uguale. Il verso del movimento del fluido va dal vaso a livello maggiore () verso
scaricato da www.sunhope.it
 Recettori a tirosina chinasi I recettori a tirosina chinasi presentano vari domini Una regione di legame (extracellulare) Una regione transmembrana Una coda intracellulare con numerose tirosine scaricato
Recettori a tirosina chinasi I recettori a tirosina chinasi presentano vari domini Una regione di legame (extracellulare) Una regione transmembrana Una coda intracellulare con numerose tirosine scaricato
Com è fatto l atomo ATOMO. UNA VOLTA si pensava che l atomo fosse indivisibile. OGGI si pensa che l atomo è costituito da tre particelle
 STRUTTURA ATOMO Com è fatto l atomo ATOMO UNA VOLTA si pensava che l atomo fosse indivisibile OGGI si pensa che l atomo è costituito da tre particelle PROTONI particelle con carica elettrica positiva e
STRUTTURA ATOMO Com è fatto l atomo ATOMO UNA VOLTA si pensava che l atomo fosse indivisibile OGGI si pensa che l atomo è costituito da tre particelle PROTONI particelle con carica elettrica positiva e
FOSFORILAZIONE OSSIDATIVA
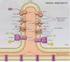 FOSFORILAZIONE OSSIDATIVA Lo scopo ultimo dei processi metabolici ossidativi è quello di canalizzare l energia contenuta nello scheletro carbonioso di zuccheri, ac. grassi e amminoacidi nella sintesi di
FOSFORILAZIONE OSSIDATIVA Lo scopo ultimo dei processi metabolici ossidativi è quello di canalizzare l energia contenuta nello scheletro carbonioso di zuccheri, ac. grassi e amminoacidi nella sintesi di
Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I
 Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I I TRASPORTI ATTRAVERSO MEMBRANE BIOLOGICHE Movimenti di piccoli soluti attraverso le membrane 2 categorie generali Trasporto
Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I I TRASPORTI ATTRAVERSO MEMBRANE BIOLOGICHE Movimenti di piccoli soluti attraverso le membrane 2 categorie generali Trasporto
Monossido d azoto NO (Nitric Oxide) Messaggero del segnale cellulare. Molecola regolatoria nel sistema nervoso centrale e periferico
 Monossido d azoto NO (Nitric Oxide) Ruolo biologico: Messaggero del segnale cellulare Molecola regolatoria nel sistema cardiovascolare Molecola regolatoria nel sistema nervoso centrale e periferico Componente
Monossido d azoto NO (Nitric Oxide) Ruolo biologico: Messaggero del segnale cellulare Molecola regolatoria nel sistema cardiovascolare Molecola regolatoria nel sistema nervoso centrale e periferico Componente
Biosintesi non ribosomiale di metaboliti peptidici bioattivi
 Biosintesi non ribosomiale di metaboliti peptidici bioattivi Principali bersagli degli antibiotici Gli antibiotici derivano per la maggior parte da composti naturali Strutture di alcuni peptidi bioattivi
Biosintesi non ribosomiale di metaboliti peptidici bioattivi Principali bersagli degli antibiotici Gli antibiotici derivano per la maggior parte da composti naturali Strutture di alcuni peptidi bioattivi
REAZIONI ORGANICHE Variazioni di energia e velocità di reazione
 REAZIONI ORGANICHE Variazioni di energia e velocità di reazione Abbiamo visto che i composti organici e le loro reazioni possono essere suddivisi in categorie omogenee. Per ottenere la massima razionalizzazione
REAZIONI ORGANICHE Variazioni di energia e velocità di reazione Abbiamo visto che i composti organici e le loro reazioni possono essere suddivisi in categorie omogenee. Per ottenere la massima razionalizzazione
Trasporto di elettroni e fosforilazione ossidativa
 Prof. Giorgio Sartor Trasporto di elettroni e fosforilazione ossidativa Copyright 2001-2014 by Giorgio Sartor. All rights reserved. B10 v. 2.0 25/03/2014 G v. 2.0 gsartor 2001-2014 Trasporto di elettroni
Prof. Giorgio Sartor Trasporto di elettroni e fosforilazione ossidativa Copyright 2001-2014 by Giorgio Sartor. All rights reserved. B10 v. 2.0 25/03/2014 G v. 2.0 gsartor 2001-2014 Trasporto di elettroni
Metalli in medicina. L utilizzo dei metalli in medicina ha radici ben antiche. Il ferro ed il
 Metalli in medicina L utilizzo dei metalli in medicina ha radici ben antiche. Il ferro ed il rame, per esempio, erano utilizzati nella Grecia antica. Già da secoli il Hg 2+ era utilizzato nel trattamento
Metalli in medicina L utilizzo dei metalli in medicina ha radici ben antiche. Il ferro ed il rame, per esempio, erano utilizzati nella Grecia antica. Già da secoli il Hg 2+ era utilizzato nel trattamento
Continua. Peptidasi H 2 O
 Continua Peptidasi H 2 O Classificazione delle peptidasi 1. Meccanismo catalitico 2. Tipo di reazione catalizzata 3. Struttura molecolare e omologia 1. Meccanismo catalitico (mostrato per la chimotripsina)
Continua Peptidasi H 2 O Classificazione delle peptidasi 1. Meccanismo catalitico 2. Tipo di reazione catalizzata 3. Struttura molecolare e omologia 1. Meccanismo catalitico (mostrato per la chimotripsina)
L adattamento dei batteri. Strategie di adattamento
 L adattamento dei batteri Strategie di adattamento mutazione trasferimento genico orizzontale regolazione dell espressione genica regolazione della trascrizione regolazione della traduzione regolazione
L adattamento dei batteri Strategie di adattamento mutazione trasferimento genico orizzontale regolazione dell espressione genica regolazione della trascrizione regolazione della traduzione regolazione
Capitolo 6 La respirazione cellulare
 Capitolo 6 La respirazione cellulare Introduzione alla respirazione cellulare 6.1 La respirazione polmonare rifornisce le nostre cellule di ossigeno ed elimina diossido di carbonio La respirazione polmonare
Capitolo 6 La respirazione cellulare Introduzione alla respirazione cellulare 6.1 La respirazione polmonare rifornisce le nostre cellule di ossigeno ed elimina diossido di carbonio La respirazione polmonare
