Composti formati esclusivamente dagli elementi Carbonio ed Idrogeno
|
|
|
- Rosalinda Scarpa
- 5 anni fa
- Visualizzazioni
Transcript
1 Alcani
2 Composti formati esclusivamente dagli elementi Carbonio ed Idrogeno
3 Alcani Sono il tipo di idrocarburi che contiene il maggior numero di atomi di per numero di atomi di C Sono anche detti idrocarburi alifatici Tutti gli atomi di C sono ibridati sp 3 ed hanno quindi struttura tetraedrica La loro formula generale è C n 2n+2
4 E molto comune avere a che fare con alcani aventi stessa formula molecolare ma diversa connettività In base a quanto già detto in precedenza, questi sono casi di isomeria costituzionale (stessa formula molecolare ma diversa connettività) Sono anche chiamati isomeri strutturali Esempio: C 7 16 isomeri strutturali (o costituzionali) dell eptano Ricordare: gli isomeri strutturali hanno proprietà fisiche e chimiche diverse!! Il numero di possibili isomeri strutturali cresce velocemente all aumentare del numero di atomi di carbonio: Atomi di carbonio Isomeri strutturali
5 Gli atomi di carbonio di un alcano possono essere distinti in : 1. primari (legati ad 1 solo atomo di C) 2. secondari (legati a 2 atomi di C) 3. terziari (legati a 3 atomi di C) 4. quaternari (legati a 4 atomi di C) Analogamente, idrogeni legati a carboni primari, secondari o terziari sono detti rispettivamente idrogeni primari, secondari o terziari Nomi utilizzati per i raggruppamenti C 3, C 2, C presenti nelle formule condensate: C 3 gruppo metilico C 2 gruppo metilenico C gruppo metinico
6 Tra i diversi isomeri strutturali di un alcano, quello nel quale tutti gli atomi di carbonio sono disposti a formare un unica catena lineare è detto alcano normale e la sua struttura condensata può essere scritta nella seguente forma generale C 3 (C 2 ) n C 3 nella quale sono evidenziabili 2 gruppi metilici e n gruppi metilenici Utilizzando le regole IUPAC (International Union of Pure and Applied Chemistry) il loro nome è ottenuto: = 1. selezionando un prefisso riferito al numero di atomi di carbonio contenuti nell alcano; 2. facendo seguire al prefisso il suffisso -ano butano normale = n-butano n-eptano n-dodecano
7 Tutti gli isomeri strutturali non lineari sono detti ramificati, perché contengono uno o più gruppi atomici (sostituenti) che si protraggono da una catena lineare, come i rami dal tronco di un albero. eptani ramificati Un gruppo sostituente corrispondente ad un alcano privato di 1 atomo di è genericamente detto gruppo alchilico e simboleggiato con R- Il nome di un gruppo alchilico è ottenuto dal nome del corrispondente alcano sostituendo il suffisso ano con ile
8 Nomi comuni (nomenclatura non IUPAC) E utilizzabile nei casi più semplici, per alcani con poche e non complesse ramificazioni. 1. Per gli alcani con più di 3 atomi di carbonio vanno usati i seguenti prefissi per indicare come termina un lato della catena: Iso- Neo- 2. Indipendentemente dalla relativa disposizione, il numero totale di atomi di carbonio determina il nome (i prefissi sono quelli precedentemente elencati in tabella). Formule linea-angolo: ogni vertice e termine di linea corrispondono ad un C, mentre gli atomi di sono sott intesi, in numero tale da completare la tetravalenza degli atomi di C
9 Nomenclatura IUPAC di alcani ramificati 4 C 3 C 2 C 2 CC 2 C 2 C C 2 C 2 C 2 C C 3 C 2 C 2 C 2 CC 2 C 2 C 3 C 3 1. Individuare la catena principale, quella cioè con il maggior numero di atomi di carbonio C 3 C 2 C 2 C 2 CC 2 C 3 C 2 C 2 C Numerare la catena in modo che ai sostituenti sia assegnata la più bassa numerazione
10 3. Ad ogni sostituente viene assegnato un nome e un numero. Il numero indica il C a cui è legato e viene collegato al nome con un trattino 4. Se lo stesso sostituente compare più volte la numerazione deve essere più bassa in corrispondenza del sostituente incontrato per primo. Il numero di volte con il quale il sostituente si ripete è indicato con un prefisso: di- tri- tetra- penta- esa-. I numeri sono separati da virgole ,4-dimetilesano (non 3,5-dimetilesano)
11 5. Due o più sostituenti diversi tra loro sono elencati in ordine alfabetico (ma I prefissi di-, tri-, tetra- ecc. non vanno considerati ai fini di tale ordinamento). Se sono presenti sostituenti diversi in posizioni equivalenti sulla catena, il numero più basso va attribuito al sostituente che viene prima in ordine alfabetico Etil-5metileptano Etil-2,2-dimetilesano (non 2,2-Dimetil-4-etilesano)
12 6. In caso di più catene base di identica lunghezza va scelta come catena principale quella che contiene il maggior numero di sostituenti NO (un sostituente) 3-Etil-2-metilesano (non 3-isopropilesano) SI (due sostituenti) 7. Se un sostituente è a sua volta un alchile ramificato il suo nome andrà ricavato applicando le stesse regole appena riportate metil-4-(1-metiletil)eptano 4-isopropil-2-metileptano
13 Cicloalcani Sono idrocarburi saturi che contengono atomi di carbonio legati a ciclo La loro formula generale è C n 2n Sono comunemente rappresentati con strutture condensate o formule linea- angolo
14 Nomenclatura dei cicloalcani In generale, si attribuisce facendo precedere il prefisso ciclo- al nome del corrispondente alcano a catena aperta ed assegnando nome e numerazione ad ogni sostituente dell anello. 1. In caso di unico sostituente la numerazione non è necessaria 2. In caso di due sostituenti numerare e nominare quest ultimi rispettando l ordine alfabetico
15 3. In caso di più di due sostituenti: numerare l anello in modo da attribuire ai sostituenti la serie più bassa possibile, poi nominare ed elencare I sostituenti seguendo il criterio dell ordine alfabetico. Bicicloalcani Sono alcani contenenti 2 cicli che condividono 2 atomi di carbonio, detti testa di ponte, e una catena alchilica. Le 3 catene alchiliche che uniscono i due atomi testa di ponte sono dette ponti
16 Nomenclatura dei bicicloalcani Si attribuisce facendo precedere il prefisso biciclo- al nome dell alcano a catena aperta avente lo stesso numero di atomi di C ed assegnando nome e numerazione ad ogni sostituente dell anello. Numerazione di un bicicloalcano 1. Deve partire da un atomo testa di ponte e procedere lungo la catena contenente il maggior numero di atomi di carbonio, continuando poi con lo stesso criterio fino alla numerazione completa del biciclo 2. Se ci sono due ponti di uguale lunghezza si procede verso quello che consente di attribuire la più bassa numerazione al primo sostituente incontrato
17 3. Per la scrittura del nome occorre : a) riportare il prefisso Biciclo; b) aprire parentesi quadre dentro le quali devono essere scritte in ordine decrescente le lunghezze dei ponti separate da un punto; c) scrivere il nome base del biciclo considerando il numero di atomi di C contenuti nella struttura
18 Conformazioni di alcani e cicloalcani Rappresentazioni 3D 1. A cunei 2. A cavalletto 3. Proiezione di Newman 3 C 1 C F Cl C 3 F 2 3 C 3 F F C 3 F C 3
19 Conformazione E chiamata in questo modo ogni particolare disposizione tridimensionale (geometria) degli atomi di una molecola che deriva da rotazioni intorno a legami semplici. Tali geometrie sono anche dette rotameri Geometrie associate a conformazioni diverse di una stessa molecola e caratterizzate da un minimo relativo dell energia strutturale sono definite isomeri conformazionali, o semplicemente conformeri, e rappresentano casi particolari di stereoisomeria La diversa stabilità strutturale esistente tra le conformazioni di una molecola può essere interpretata sulla base di 3 differenti contributi: 1. Tensione angolare 2. Tensione di torsione 3. Tensione sterica 1. Tensione angolare È un incremento di energia della molecola collegato all esistenza di angoli di legame più grandi o più piccoli rispetto ai valori ottimali
20 2. Tensione di torsione Torsionale: è un gruppo rappresentato da 4 atomi legati in successione. Intorno al legame semplice esistente tra gli atomi centrali A2 e A3 è possibile la rotazione e pertanto ad ogni torsionale è associato un angolo di torsione (detto anche angolo diedro), che è l angolo esistente tra i due piani definiti A 1 rispettivamente dalle terne di atomi A1-A2-A3 e A2-A3-A4 A 2 A 3 Torsionale A 4 Esempio: rotameri della molecola di etano Una disposizione con angolo diedro di 0, 120 o 240 (o prossimo a questo valore) è detta eclissata Una disposizione con angolo diedro di 60, 180 o 300 (o prossimo a questo valore) è detta sfalsata In particolare, una disposizione con angolo diedro di 0 è anche detta sinperiplanare, una con angolo di 180 è anche detta antiperiplanare e una con un angolo di 60 o 300 è anche detta sinclinale (+ o -, rispettivamente)
21 - sinclinale (-sc) anticlinale (-ac) Sinperiplanare (sp) A A2 A A 1 + sinclinale (+sc) +90 A 2 A 3 A 4 + anticlinale (+ac) A4 Antiperiplanare (ap) (Notazione di Klyne e Prelog) La tensione di torsione (o energia di torsione) è la differenza di energia esistente tra la conformazione considerata e la conformazione sfalsata più vicina da raggiungere per rotazione intorno al legame centrale del torsionale. Ricordare che quest ultima si trova ad un minimo di energia relativa. 3. Tensione sterica Riguarda atomi di una molecola non legati direttamente l uno con l altro e separati da 4 o più legami che risultino costretti dalla particolare geometria a essere più vicini di quanto consenta il loro raggio atomico (parziale sovrapposizione delle sfere di van der Waals).
22 Conformazioni della molecola di etano 3 kcal mol -1 La tensione di torsione può essere imputata: 1. alla repulsione tra i nuclei di idrogeno nella forma eclissata; 2. alla repulsione tra le nuvole di elettroni dei legami C- adiacenti nella forma eclissata; 3. alla stabilizzazione della forma sfalsata dovuta all interazione donatore-accettore tra orbitale di legame e orbitale di antilegame di due C- adiacenti
23 Conformazioni della molecola di butano D Tensione sterica + Tensione angolare Solo poca tensione sterica due tipi di conformazioni sfalsate due tipi di disposizioni eclissate Gauche o sinclinale antiperiplanare anticlinale sinperiplanare
24 La stima delle popolazioni di due specie chimiche in equilibrio può essere ottenuta utilizzando la relazione termodinamica sotto riportata: DG = -RT. ln K eq Che può essere riscritta nella forma -DG K eq = e RT A 25 C RT = kj mol -1 RT = kcal mol -1 A DG =0.9 kcal mol -1 B Per le 2 conformazioni di minima energia della molecola di butano a 25 C sarà [B] K eq = 0.22 [A] = e quindi: %B = K eq K eq x = 17.7% %A = %B = 82.3%
25 Costanti di equilibrio e abbondanze relative di 2 specie chimiche A e B in equilibrio alla temperatura di 25 C in funzione del DG di reazione A B DG (kcal mol -1 ) K eq %B %A
26 Conformazioni di cicloalcani In generale, rispetto agli alcani a struttura aperta è riscontrabile un più alto contenuto energetico riportato con il termine di tensione d anello tensione d anello Ciclopropano Ciclobutano Ciclopentano tensione angolare + tensione di torsione Cicloesano non presente Cicloeptano : : : : : Cicloesadecano tensione di torsione
27 Ciclopropano Forte tensione di torsione (tutti i legami C- sono eclissati) 1. i legami C- sono più corti che negli alcani 2. i legami C-C sono più lunghi che negli alcani 3. Gli angoli di legame -C- sono maggiori di Forte tensione angolare (60 invece di ) tensione d anello: 27.7 kcal mol -1 La reattività del ciclopropano è considerevolmente più elevata rispetto a quella degli altri cicloalcani
28 Ciclobutano Forte tensione angolare (90 invece di ) tensione angolare ulteriormente aggravata (88 invece di ) Conformazioni a farfalla (in veloce interconversione tra di loro) Forte tensione di torsione (tutti i legami C- sono eclissati) tensione di torsione fortemente ridotta tensione d anello: 26.3 kcal mol -1
29 Ciclopentano tensione angolare quasi nulla (108 invece di ) tensione angolare leggermente aumentata (105 invece di ) 5 conformazioni a busta (in veloce interconversione tra di loro) Forte tensione di torsione (tutti i legami C- sono eclissati) tensione di torsione fortemente ridotta tensione d anello: 6.5 kcal mol -1
30 Cicloesano Praticamente non è presente tensione d anello!! La conformazione più stabile assunta dal cicloesano ricorda schematicamente la forma di una sedia tensione angolare quasi nulla (110.9 invece di ) tensione di torsione assente (tutti i legami C- sono sfalsati)
31 Un altra conformazione possibile per il cicloesano è quella a barca-ritorta Le diverse conformazioni possono interconvertire l una nell altra attraverso rotazioni intorno a legami C-C senza la necessità di superare barriere di energia troppo elevate DG =5 kcal mol %
32 Esistono 2 conformazioni di cicloesano a sedia in veloce interconversione tra loro Il passaggio da una conformazione all altra richiede la formazione di una geometria di massima energia, detta a barca a causa della sua forma Nella conformazione a barca 4 gruppi metilenici hanno i rispettivi legami C- eclissati ed è presente una interazione sterica sfavorevole dovuta a due idrogeni legati ai due atomi di carbonio affacciati (idrogeni ad asta di bandiera)
33 Nella conformazione a sedia, che è praticamente l unica ad essere popolata, sono distinguibili due tipi di atomi di idrogeno: Idrogeni equatoriali Idrogeni assiali
34 Come conseguenza dell interconversione tra le due conformazioni a sedia, gli idrogeni equatoriali di una conformazione diventano gli idrogeni assiali dell altra, e viceversa Cicloalcani da 7 a 16 atomi di carbonio Grazie alla elevata mobilità conformazionale non è presente tensione angolare, ma è presente tensione di torsione per l esistenza di almeno una coppia di metileni disposti con i legami C- eclissati
35 A Cicloesani monosostituiti DG = -1,74 kcal mol -1 B a 25 C K eq = 18.9 %B = %A = 5% K eq K eq x = 95% Gli stereoisomeri derivanti dall interconversione delle due conformazioni a sedia di un cicloesano monosostituito hanno certamente una diversa stabilità energetica per l esistenza, solo in una delle due geometrie, di interazioni 1-3 e 1-5 diassiali (cioè forme di tensione sterica)
36 -DG K eq = e RT Solo il gruppo terz-butilico è così ingombrante da determinare, in pratica, l esistenza del solo isomero con il gruppo in equatoriale
37 Isomeria cis-trans nei Cicloalcani di- o poli- sostituiti I cicloalcani con 2 o più sostituenti mostrano un tipo di stereoisomeria denominata cis-trans cis-1,2-dimetilciclopentano C 3 C 3 3 C C 3 C 3 C 3 3 C C 3 trans-1,2-dimetilciclopentano cis : sostituenti dalla stessa parte (rispetto al piano del ciclo) trans : sostituenti da parti opposte (rispetto al piano del ciclo) In questi cicloalcani gli atomi di carbonio portatori dei sostituenti sono detti atomi (o centri) stereogenici perché ogni interscambio di 2 loro ligandi porta alla formazione di uno stereoisomero
38 stereocentri C 3 C 3 stereocentri C 3 C 3
39 Trans-biciclo[4,4,0]decano Trans-decalina Cis-biciclo[4,4,0]decano Cis-decalina
40 Proprietà fisiche di alcani e cicloalcani I punti di fusione, di ebollizione e le densità crescono con le dimensioni delle molecole di alcano, ma, a parità di dimensioni molecolari, sono comunque più piccoli di quelli caratteristici di altre specie molecolari contenenti legami polarizzati Bassi valori dei punti di fusione e di ebollizione sono indicativi di deboli legami intermolecolari
41 Forza delle interazioni legami intermolecolari legami a idrogeno interazioni dipolo dipolo interazioni di van der Waals (forze di dispersione) Uniche interazioni possibili tra molecole di alcano!!
42 Le interazioni di van der Waals diventano più intense all aumentare della superficie esposta dalle molecole (superficie di contatto esistente tra molecola e molecola). C 5 12 p.e. = 36 C C 8 18 p.e. = 126 C All aumentare del peso molecolare aumenta la superficie di contatto intermolecolare e quindi aumentano anche le interazioni di van der Waals
43 A parità di peso molecolare (alcani isomeri) la superficie diminuisce con l aumentare delle ramificazioni
44 Le ramificazioni tendono a globulizzare la molecola, rendendo meno estesi i possibili punti di contatto molecola-molecola n-pentano p.e. = 36 C neopentano p.e. = 9.5 C
45 La stabilità di alcani isomeri aumenta con l aumentare del grado di ramificazione Il calore liberato nella loro reazione di combustione (D di reazione) può essere utilizzato per fare un confronto tra stabilità relative Alcano + O 2 2 O + CO 2
46 Il calore di combustione medio equivalente alla completa ossidazione di un gruppo metilenico (D C2 ) è stato calcolato da misure effettuate su alcani non ramificati (privi quindi di tensione di torsione, tensione sterica e tensione angolare) kcal mol -1 D C 2 = kj mol -1 Utilizzando tale valore possono essere stimati i D di combustione di cicloalcani ipoteticamente privi di tensione d anello. La differenza tra i valori di D sperimentali e quelli calcolati fornisce così una misura quantitativa della tensione d anello presente in ogni determinato cicloalcano
Alcani e Cicloalcani
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alcani e Cicloalcani Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alcani e Cicloalcani Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e
IDROCARBURI: classificazione
 ALCANI 1 IDROCARBURI: classificazione 2 ALCANI Formula bruta: C n H 2n+2 1 C CH 4 2 C C 2 H 6 3 C C 3 H 8 4 C C 4 H 10 3 ALCANI: ibridazione Orbitali s, p e sp 3 z orbitale 2s y x z z z orbitali 2p y x
ALCANI 1 IDROCARBURI: classificazione 2 ALCANI Formula bruta: C n H 2n+2 1 C CH 4 2 C C 2 H 6 3 C C 3 H 8 4 C C 4 H 10 3 ALCANI: ibridazione Orbitali s, p e sp 3 z orbitale 2s y x z z z orbitali 2p y x
Classificazione degli idrocarburi
 Classificazione degli idrocarburi ALCANI Alcani: idrocarburi saturi contenenti solo legami semplici carbonio-carbonio (tutti i carboni sono ibridati sp3). Modelli molecolari di etano, propano e butano.
Classificazione degli idrocarburi ALCANI Alcani: idrocarburi saturi contenenti solo legami semplici carbonio-carbonio (tutti i carboni sono ibridati sp3). Modelli molecolari di etano, propano e butano.
Alcani e cicloalcani. Nomenclatura e nomi comuni Struttura e proprietà Reazioni
 Alcani e cicloalcani Nomenclatura e nomi comuni Struttura e proprietà Reazioni Alcani Gli orbitali atomici hanno forme ben definite. Gli orbitali S sono sferici con gli e - confinati in una regione sferica
Alcani e cicloalcani Nomenclatura e nomi comuni Struttura e proprietà Reazioni Alcani Gli orbitali atomici hanno forme ben definite. Gli orbitali S sono sferici con gli e - confinati in una regione sferica
Stereochimica di alcani e cicloalcani
 di alcani e cicloalcani Conformazioni, conformeri Due conformazioni dell etano. Le conformazioni sono arrangiamenti diversi di atomi che interconvertono per rotazione attorno al legame C-C. Rappresentazione
di alcani e cicloalcani Conformazioni, conformeri Due conformazioni dell etano. Le conformazioni sono arrangiamenti diversi di atomi che interconvertono per rotazione attorno al legame C-C. Rappresentazione
Idrocarburi Saturi. Cicloalcani
 Idrocarburi Saturi Cicloalcani Cicloalcani I cicloalcani sono idrocarburi i cui atomi di carbonio sono uniti per formare un anello In natura sono presenti cicloalcani con dimensioni dell anello che vanno
Idrocarburi Saturi Cicloalcani Cicloalcani I cicloalcani sono idrocarburi i cui atomi di carbonio sono uniti per formare un anello In natura sono presenti cicloalcani con dimensioni dell anello che vanno
Stereochimica di alcani e cicloalcani. Stereochimica. Conformazioni, conformeri
 di alcani e cicloalcani Conformazioni, conformeri Due conformazioni dell etano. I differenti conformeri si interconvertono per rotazione attorno al legame C-C. 1 Rappresentazione a cavalletto e proiezione
di alcani e cicloalcani Conformazioni, conformeri Due conformazioni dell etano. I differenti conformeri si interconvertono per rotazione attorno al legame C-C. 1 Rappresentazione a cavalletto e proiezione
Idrocarburi: composti organici che hanno nella loro struttura solo atomo di C o H
 Idrocarburi: composti organici che hanno nella loro struttura solo atomo di C o H Alifatici: deriva dal greco aleifar cioè unguento; questo perché molti grassi contengono lunghe catene carboniose. GLI
Idrocarburi: composti organici che hanno nella loro struttura solo atomo di C o H Alifatici: deriva dal greco aleifar cioè unguento; questo perché molti grassi contengono lunghe catene carboniose. GLI
Gruppi funzionali. Gruppi funzionali
 Gruppi funzionali Gruppi funzionali La reattività chimica di ogni molecola organica, indipendentemente dalle sue dimensioni o dalla sua complessità, è determinata dai gruppi funzionali che essa contiene
Gruppi funzionali Gruppi funzionali La reattività chimica di ogni molecola organica, indipendentemente dalle sue dimensioni o dalla sua complessità, è determinata dai gruppi funzionali che essa contiene
Gruppi funzionali Un gruppo funzionale è un atomo o un gruppo di atomi con proprietà chimiche e fisiche tipiche. E
 Gruppi funzionali Gruppi funzionali La reattività chimica di ogni molecola organica, indipendentemente dalle sue dimensioni o dalla sua complessità, è determinata dai gruppi funzionali che essa contiene
Gruppi funzionali Gruppi funzionali La reattività chimica di ogni molecola organica, indipendentemente dalle sue dimensioni o dalla sua complessità, è determinata dai gruppi funzionali che essa contiene
IDROCARBURI. Alcani Alcheni Alchini Areni. Tipo di legami carboniocarbonio. Solo legami semplici. Uno o più tripli legami. Uno o più doppi legami
 IMICA ORGANICA La chimica del carbonio, per le proprietà del carbonio di formare un numero grandissimo di composti con proprietà diverse, costituisce una branca della chimica, denominata chimica organica.
IMICA ORGANICA La chimica del carbonio, per le proprietà del carbonio di formare un numero grandissimo di composti con proprietà diverse, costituisce una branca della chimica, denominata chimica organica.
Configurazione. Conformazione
 Configurazione Posizione relativa degli atomi nello spazio che caratterizza un particolare stereoisomero Sono in numero limitato (in genere 2) Conformazione Particolare geometria di una molecola che dipende
Configurazione Posizione relativa degli atomi nello spazio che caratterizza un particolare stereoisomero Sono in numero limitato (in genere 2) Conformazione Particolare geometria di una molecola che dipende
Alcani. Es. CH 3 CH 2 CH 2 CH 3
 Alcani Gli alcani sono i composti organici più semplici costituiti solo da atomi di e di (Idrocarburi); Sono composti saturi poiché ogni atomo di carbonio è legato al numero massimo possibile (4) di altri
Alcani Gli alcani sono i composti organici più semplici costituiti solo da atomi di e di (Idrocarburi); Sono composti saturi poiché ogni atomo di carbonio è legato al numero massimo possibile (4) di altri
Compos. contenen. soltanto C e H IDROCARBURI. alifa.ci. aroma.ci. insaturi. saturi. cicloalcani. alcani alcheni alchini
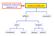 ompos. contenen. soltanto e IDROARBURI alifa.ci aroma.ci saturi insaturi cicloalcani alcani alcheni alchini Alcani Formula: n 2n+2 Nome: prefisso+ano n=1 : 4 metano n=2 : 2 6 etano n=3 : 3 8 propano N=4
ompos. contenen. soltanto e IDROARBURI alifa.ci aroma.ci saturi insaturi cicloalcani alcani alcheni alchini Alcani Formula: n 2n+2 Nome: prefisso+ano n=1 : 4 metano n=2 : 2 6 etano n=3 : 3 8 propano N=4
IDROCARBURI I ALCANI ANALISI CONFORMAZIONALE
 IDROCARBURI I ALCANI NOMENCLATURA ANALISI CONFORMAZIONALE REAZIONI GLI IDROCARBURI CONTENGONO SOLO CARBONIO ED IDROGENO VENGONO DISTINTI IN TRE CLASSI 1. SATURI: SOLO LEGAMI SEMPLICI C-C SE SATURI ED ACICLICI:
IDROCARBURI I ALCANI NOMENCLATURA ANALISI CONFORMAZIONALE REAZIONI GLI IDROCARBURI CONTENGONO SOLO CARBONIO ED IDROGENO VENGONO DISTINTI IN TRE CLASSI 1. SATURI: SOLO LEGAMI SEMPLICI C-C SE SATURI ED ACICLICI:
IBRIDAZIONE DEL CARBONIO NEGLI ALCANI PREMESSA: COSA SONO GLI ORBITALI IBRIDI.
 ALCANI Gli alcani sono composti organici costituiti solamente da carbonio e idrogeno (per questo motivo appartengono alla più ampia classe degli idrocarburi), aventi formula bruta C n H (2n + 2). Gli alcani
ALCANI Gli alcani sono composti organici costituiti solamente da carbonio e idrogeno (per questo motivo appartengono alla più ampia classe degli idrocarburi), aventi formula bruta C n H (2n + 2). Gli alcani
Idrocarburi Saturi. Alcani
 Idrocarburi Saturi Alcani IDROCARBURI I principali componenti del petrolio e del gas naturale, risorse dalle quali proviene la maggior parte dei combustibili per la produzione di energia sono idrocarburi,
Idrocarburi Saturi Alcani IDROCARBURI I principali componenti del petrolio e del gas naturale, risorse dalle quali proviene la maggior parte dei combustibili per la produzione di energia sono idrocarburi,
Capitolo 2 Alcani e Cicloalcani
 himica Organica Informazione Scientifica sul Farmaco apitolo 2 Alcani e icloalcani Organic hemistry, 5 th Edition L. G. Wade, Jr. Prentice all Organic hemistry, 3 rd Edition 1 Paula Y. Bruice, Prentice
himica Organica Informazione Scientifica sul Farmaco apitolo 2 Alcani e icloalcani Organic hemistry, 5 th Edition L. G. Wade, Jr. Prentice all Organic hemistry, 3 rd Edition 1 Paula Y. Bruice, Prentice
3. Cicloalcani. Formula generale: C n H 2n in serie omologa C 9 C 10 C 11 C 12 >C 12. Es.: 1,1-dimetilciclopropano. Anelli. piccoli. Anelli.
 . Cicloalcani Formula generale: C n 2n in serie omologa ciclopropano ciclobutano ciclopentano Anelli piccoli C 9 C 10 C 11 C 12 cicloottano ciclononano ciclodecano cicloundecano ciclododecano Anelli medi
. Cicloalcani Formula generale: C n 2n in serie omologa ciclopropano ciclobutano ciclopentano Anelli piccoli C 9 C 10 C 11 C 12 cicloottano ciclononano ciclodecano cicloundecano ciclododecano Anelli medi
Teoria degli orbitali. Lo spazio intorno al nucleo in cui è possibile trovare con la massima probabilità gli elettroni viene chiamato orbitale.
 Teoria degli orbitali Lo spazio intorno al nucleo in cui è possibile trovare con la massima probabilità gli elettroni viene chiamato orbitale. orbitale nucleo STPA-Chimica Organica 1 L orbitale 1s Gli
Teoria degli orbitali Lo spazio intorno al nucleo in cui è possibile trovare con la massima probabilità gli elettroni viene chiamato orbitale. orbitale nucleo STPA-Chimica Organica 1 L orbitale 1s Gli
Isomeria Costituzionale. Isomeria Conformazionale
 Isomeria ostituzionale Isomeri ostituzionali: omposti con uguale formula molecolare ma con un diverso ordine con cui sono legati gli atomi tra loro. Isomeria onformazionale onformazione: ciascuna disposizione
Isomeria ostituzionale Isomeri ostituzionali: omposti con uguale formula molecolare ma con un diverso ordine con cui sono legati gli atomi tra loro. Isomeria onformazionale onformazione: ciascuna disposizione
Idrocarburi Al A ifatici Ar A oma m tici
 GLI IDROCARBURI Gli idrocarburi sono i più semplici composti del carbonio con l'idrogeno. Sono le molecole di base della chimica organica poiché, oltre ad essere molto numerosi, tutti gli altri composti
GLI IDROCARBURI Gli idrocarburi sono i più semplici composti del carbonio con l'idrogeno. Sono le molecole di base della chimica organica poiché, oltre ad essere molto numerosi, tutti gli altri composti
ALCANI. C n H 2n+2 CH 3 CH 2 CH 2 CH 2 CH 2 CH 3. alcani lineari. alcani ramificati. Cap. 2
 ALANI n 2n+2 2 2 2 2 alcani lineari alcani ramificati ap. 2 1-4 5-10 10-16 15-20 ONFORMAZIONI DEGLI ALANI Ruotando attorno al legame - si individuano alcune posizioni relative dei tetraedri ALTERNATA (SFALSATA)
ALANI n 2n+2 2 2 2 2 alcani lineari alcani ramificati ap. 2 1-4 5-10 10-16 15-20 ONFORMAZIONI DEGLI ALANI Ruotando attorno al legame - si individuano alcune posizioni relative dei tetraedri ALTERNATA (SFALSATA)
CHIMICA ORGANICA CHIMICA DEL CARBONIO
 CHIMICA ORGANICA CHIMICA DEL CARBONIO Fino al 1828 con il termine organico si indicavano le sostanze prodotte dagli organismi viventi, mentre si classificavano come inorganiche tutte le altre Dopo il 1828
CHIMICA ORGANICA CHIMICA DEL CARBONIO Fino al 1828 con il termine organico si indicavano le sostanze prodotte dagli organismi viventi, mentre si classificavano come inorganiche tutte le altre Dopo il 1828
Conformazione degli alcani
 onformazione degli alcani La conformazione di un alcano si riferisce alla disposizione tridimensionale degli atomi che risulta dalla rotazione attorno al legame -. Nonostante in una molecola possano esservi
onformazione degli alcani La conformazione di un alcano si riferisce alla disposizione tridimensionale degli atomi che risulta dalla rotazione attorno al legame -. Nonostante in una molecola possano esservi
Nomenclatura dei CicloAlcani Semplici
 Nomenclatura dei CicloAlcani Semplici Nome Ciclopropano Ciclobutano Ciclopentano Cicloesano Cicloeptano Cicloalcano Formula Molecolare C 3 6 C 4 8 C 5 10 C 6 12 C 7 14 C n 2n Struttura Condensata (C 2
Nomenclatura dei CicloAlcani Semplici Nome Ciclopropano Ciclobutano Ciclopentano Cicloesano Cicloeptano Cicloalcano Formula Molecolare C 3 6 C 4 8 C 5 10 C 6 12 C 7 14 C n 2n Struttura Condensata (C 2
Idrocarburi. Alifatici. Aromatici. Alcani o Idrocarburi saturi: idrocarburi con soli legami singoli. Alcheni o Olefine: idrocarburi con legami doppi.
 IDROCARBURI C x y Alifatici Idrocarburi Alcani o Idrocarburi saturi: idrocarburi con soli legami singoli. Lineari o alcani normali, n-alcani Ramificati Alcheni o Olefine: idrocarburi con legami doppi.
IDROCARBURI C x y Alifatici Idrocarburi Alcani o Idrocarburi saturi: idrocarburi con soli legami singoli. Lineari o alcani normali, n-alcani Ramificati Alcheni o Olefine: idrocarburi con legami doppi.
2. Gli Idrocarburi IDROCARBURI. solo C e H. alcani e cicloalcani (solo C sp 3 ) alcheni e cicloalcheni (almeno 2 C sp 2 ) Alifatici
 2. Gli Idrocarburi IDROCARBURI solo C e H Si classificano in 2 grandi gruppi, a loro volta suddivisi in sottogruppi. Alifatici alcani e cicloalcani (solo C sp 3 ) alcheni e cicloalcheni (almeno 2 C sp
2. Gli Idrocarburi IDROCARBURI solo C e H Si classificano in 2 grandi gruppi, a loro volta suddivisi in sottogruppi. Alifatici alcani e cicloalcani (solo C sp 3 ) alcheni e cicloalcheni (almeno 2 C sp
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 9 Il mondo del carbonio 3 Sommario 1. Esiste un enorme varietà di composti organici 2. Gli idrocarburi saturi: alcani e cicloalcani
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 9 Il mondo del carbonio 3 Sommario 1. Esiste un enorme varietà di composti organici 2. Gli idrocarburi saturi: alcani e cicloalcani
- il DNA, la molecola che contiene l informazione genetica, - le proteine dei nostro organismo ( proteine dei muscoli, della pelle, gli enzimi),
 La chimica organica è la chimica dei composti del carbonio, che sono i mattoni con cui sono costruiti tutti i corpi viventi della terra. Questi composti comprendono ad esempio - il DNA, la molecola che
La chimica organica è la chimica dei composti del carbonio, che sono i mattoni con cui sono costruiti tutti i corpi viventi della terra. Questi composti comprendono ad esempio - il DNA, la molecola che
Gli Alcheni : struttura e nomenclatura
 Gli Alcheni : struttura e nomenclatura Alcheni Gli alcheni sono idrocarburi che contengono un doppio legame carbonio-carbonio sono anche detti olefine o idrocarburi insaturi La formula molecolare è n H
Gli Alcheni : struttura e nomenclatura Alcheni Gli alcheni sono idrocarburi che contengono un doppio legame carbonio-carbonio sono anche detti olefine o idrocarburi insaturi La formula molecolare è n H
Nomenclatura Chimica organica. International Union of Pure and Applied Chemistry (IUPAC).
 Nomi tradizionali e nomi IUPAC Nomenclatura Chimica organica In passato si assegnavano i nomi alle molecole organiche in base alla loro origine o a certe proprietà. Per esempio l acido citrico deriva dal
Nomi tradizionali e nomi IUPAC Nomenclatura Chimica organica In passato si assegnavano i nomi alle molecole organiche in base alla loro origine o a certe proprietà. Per esempio l acido citrico deriva dal
Diagramma di flusso degli idrocarburi
 Glialcanisonoidrocarburi saturi. saturi (solo legami semplici) idrocarburi (solo e ) n 2n+2 Esano 6 14 Diagramma di flusso degli idrocarburi Idrocarburi Saturi Insaturi Alcani Aciclici iclici atena lineare
Glialcanisonoidrocarburi saturi. saturi (solo legami semplici) idrocarburi (solo e ) n 2n+2 Esano 6 14 Diagramma di flusso degli idrocarburi Idrocarburi Saturi Insaturi Alcani Aciclici iclici atena lineare
Tipologie di formule chimiche
 CHIMICA ORGANICA Tipologie di formule chimiche FORMULA RAZIONALE Tipo di formula che utilizza una rappresentazione analoga alla formula bruta per quei gruppi di atomi sulla cui disposizione non vi possono
CHIMICA ORGANICA Tipologie di formule chimiche FORMULA RAZIONALE Tipo di formula che utilizza una rappresentazione analoga alla formula bruta per quei gruppi di atomi sulla cui disposizione non vi possono
02/10/2018. di catena. di posizione. strutturali. di gruppo funzionale. isomeri. geometrici. stereoisomeri. ottici
 Quando due composti organici sono costituiti dagli stessi atomi ma possiedono una struttura differente si definiscono ISOMERI. Esistono diversi tipi di isomeria: di catena strutturali di posizione isomeri
Quando due composti organici sono costituiti dagli stessi atomi ma possiedono una struttura differente si definiscono ISOMERI. Esistono diversi tipi di isomeria: di catena strutturali di posizione isomeri
Alcheni: struttura e proprietà
 Chimica Organica Informazione Scientifica sul Farmaco Alcheni: struttura e proprietà Organic Chemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: struttura degli alcheni nomenclatura proprietà fisiche
Chimica Organica Informazione Scientifica sul Farmaco Alcheni: struttura e proprietà Organic Chemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: struttura degli alcheni nomenclatura proprietà fisiche
CHIMICA delle MACROMOLECOLE BIOLOGICHE
 Progetto Tandem 2016-17 GIOVANNI GOTTE Biochimica/BIO-10, Università degli Studi di Verona CIMICA delle MACROMOLECOLE BIOLOGICE CIMICA ORGANICA CE COS E LA CIMICA ORGANICA? La chimica organica descrive
Progetto Tandem 2016-17 GIOVANNI GOTTE Biochimica/BIO-10, Università degli Studi di Verona CIMICA delle MACROMOLECOLE BIOLOGICE CIMICA ORGANICA CE COS E LA CIMICA ORGANICA? La chimica organica descrive
IDROCARBURI: NOMENCLATURA. Prof.ssa Tiziana Bellini
 IDROCARBURI: NOMENCLATURA Prof.ssa Tiziana Bellini IDROCARBURI LINEARI ALCANI metano IDROCARBURI LINEARI CH 4 CH 4 etano propano butano pentano esano eptano ottano nonano decano ( ) 4 ( ) 5 ( ) 6 ( ) 7
IDROCARBURI: NOMENCLATURA Prof.ssa Tiziana Bellini IDROCARBURI LINEARI ALCANI metano IDROCARBURI LINEARI CH 4 CH 4 etano propano butano pentano esano eptano ottano nonano decano ( ) 4 ( ) 5 ( ) 6 ( ) 7
Sandro Campestrini Dipartimento di Chimica Organica, Via Marzolo 1
 Sandro Campestrini Dipartimento di Chimica Organica, Via Marzolo 1 E-mail: sandro.campestrini@unipd.it Phone: 049-8275289 http://www.chfi.unipd.it/home/s.campestrini Testo consigliato: FONDAMENTI di CHIMICA
Sandro Campestrini Dipartimento di Chimica Organica, Via Marzolo 1 E-mail: sandro.campestrini@unipd.it Phone: 049-8275289 http://www.chfi.unipd.it/home/s.campestrini Testo consigliato: FONDAMENTI di CHIMICA
Chimica Organica. In passato, i composti chimici erano suddivisi in due grandi gruppi,
 Chimica Organica In passato, i composti chimici erano suddivisi in due grandi gruppi, inorganici e organici, in base alla loro origine. La chimica organica diveniva così la chimica dei composti del carbonio.
Chimica Organica In passato, i composti chimici erano suddivisi in due grandi gruppi, inorganici e organici, in base alla loro origine. La chimica organica diveniva così la chimica dei composti del carbonio.
ALCHENI CICLOALCHENI. C n H 2n. C n H 2n-2 C C. Gruppo funzionale degli alcheni (idrocarburi insaturi): doppio legame carbonio-carbonio
 ALCENI C n 2n CICLOALCENI C n 2n-2 C C Gruppo funzionale degli alcheni (idrocarburi insaturi): doppio legame carbonio-carbonio I carboni coinvolti nel doppio legame sono ibridati sp 2 : per cui sono legati
ALCENI C n 2n CICLOALCENI C n 2n-2 C C Gruppo funzionale degli alcheni (idrocarburi insaturi): doppio legame carbonio-carbonio I carboni coinvolti nel doppio legame sono ibridati sp 2 : per cui sono legati
CHIMICA ORGANICA Gli alcani e i cicloalcani
 1 C1-ALCANI E CICLOALCANI CHIMICA ORGANICA Gli alcani e i cicloalcani ALCANI Formula generale C n H 2n+2 Desinenza -ano Gli alcani Gli alcani, detti anche paraffine, appartengono alla classe degli idrocarburi
1 C1-ALCANI E CICLOALCANI CHIMICA ORGANICA Gli alcani e i cicloalcani ALCANI Formula generale C n H 2n+2 Desinenza -ano Gli alcani Gli alcani, detti anche paraffine, appartengono alla classe degli idrocarburi
Alcheni. Francesca Anna Scaramuzzo, PhD
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alcheni Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate per
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alcheni Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate per
3. Indicare quale (o quali) delle seguenti coppie di formule strutturali rappresenta la stessa molecola:
 . Indicare quale (o quali) delle seguenti coppie di formule strutturali rappresenta la stessa molecola: l a) NO b) l l l c) l l 4. Quali tra i seguenti scheletri di atomi di carbonio non rappresentano
. Indicare quale (o quali) delle seguenti coppie di formule strutturali rappresenta la stessa molecola: l a) NO b) l l l c) l l 4. Quali tra i seguenti scheletri di atomi di carbonio non rappresentano
I composti organici. Gli idrocarburi: composti binari, ovvero costituiti solo da due elementi. Carbonio (C) e idrogeno (H)
 I composti organici Gli idrocarburi: composti binari, ovvero costituiti solo da due elementi. Carbonio (C) e idrogeno (H) Gli idrocarburi Gli Alcani Costituiti da uno o più atomi di carbonio legati tra
I composti organici Gli idrocarburi: composti binari, ovvero costituiti solo da due elementi. Carbonio (C) e idrogeno (H) Gli idrocarburi Gli Alcani Costituiti da uno o più atomi di carbonio legati tra
IDROCARBURI. Alcani Alcheni Alchini C-C C=C C C
 IDROCARBURI Alcani Alcheni Alchini C-C C=C C C Nomenclatura Degli idrocarburi saturi (Alcani) CH 4 Metano C 2 H 6 Etano C n H 2n+2 Si dicono alchilici quei gruppi che contengono un idrogeno in meno del
IDROCARBURI Alcani Alcheni Alchini C-C C=C C C Nomenclatura Degli idrocarburi saturi (Alcani) CH 4 Metano C 2 H 6 Etano C n H 2n+2 Si dicono alchilici quei gruppi che contengono un idrogeno in meno del
2. La Struttura dei Composti Organici e le. caratteristiche chimico-fisiche
 Scienze e tecnologie erboristiche e dei prodotti per la salute (STEPS) himica rganica - 2. La Struttura dei omposti rganici e le Prof. Giuseppe Gerardo arbonara caratteristiche chimico-fisiche 5. Geometria
Scienze e tecnologie erboristiche e dei prodotti per la salute (STEPS) himica rganica - 2. La Struttura dei omposti rganici e le Prof. Giuseppe Gerardo arbonara caratteristiche chimico-fisiche 5. Geometria
Esercitazione sulle conformazioni di alcani e cicloesani
 Esercitazione sulle conformazioni di alcani e cicloesani 1. Disegnare la molecola completa del butano, nella conformazione più favorevole per tutti i legami - (usare i legami a cuneo e tratteggiati). 2.
Esercitazione sulle conformazioni di alcani e cicloesani 1. Disegnare la molecola completa del butano, nella conformazione più favorevole per tutti i legami - (usare i legami a cuneo e tratteggiati). 2.
CHIMICA ORGANICA I. Corso di laurea in CHIMICA (L.T.) Esercitazione n. 4 - Esercitazione sulle conformazioni di alcani e cicloesani.
 IMIA ORGANIA I orso di laurea in IMIA (L.T.) Esercitazione n. 4 - Esercitazione sulle conformazioni di alcani e cicloesani. TERMINI ED ARGOMENTI PER LO SVOLGIMENTO DEGLI ESERIZI DI QUESTO FOGLIO: Rotazione
IMIA ORGANIA I orso di laurea in IMIA (L.T.) Esercitazione n. 4 - Esercitazione sulle conformazioni di alcani e cicloesani. TERMINI ED ARGOMENTI PER LO SVOLGIMENTO DEGLI ESERIZI DI QUESTO FOGLIO: Rotazione
b. Disegnate la conformazione piu stabile c. Disegnate le conformazioni eclissate e sfalsate intermedie
 1. Per la seguente molecola a. Disegnate la conformazione meno stabile b. Disegnate la conformazione piu stabile c. Disegnate le conformazioni eclissate e sfalsate intermedie d. Utilizzando le seguenti
1. Per la seguente molecola a. Disegnate la conformazione meno stabile b. Disegnate la conformazione piu stabile c. Disegnate le conformazioni eclissate e sfalsate intermedie d. Utilizzando le seguenti
2. La Struttura dei Composti Organici e le caratteristiche chimico-fisiche
 Università degli Studi di Bari Dipartimento di Farmacia-SdF TENIE EBISTIE 2. La Struttura dei omposti rganici e le caratteristiche chimico-fisiche 5. Geometria molecolare. Stereochimica I Parte onformazione
Università degli Studi di Bari Dipartimento di Farmacia-SdF TENIE EBISTIE 2. La Struttura dei omposti rganici e le caratteristiche chimico-fisiche 5. Geometria molecolare. Stereochimica I Parte onformazione
Nomi e formule dei principali composti organici
 Il numero davvero sterminato dei e la necessità quindi di doverli distinguere ciascuno con la propria formula e il proprio nome, ha costretto i chimici (attraverso un apposito organismo, la IUPAC) a mettere
Il numero davvero sterminato dei e la necessità quindi di doverli distinguere ciascuno con la propria formula e il proprio nome, ha costretto i chimici (attraverso un apposito organismo, la IUPAC) a mettere
Gli idrocarburi sono composti organici, che contengono soltanto atomi di carbonio e di idrogeno. Gli atomi di carbonio (C) sono legati tra loro a
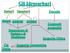 Gli idrocarburi sono composti organici, che contengono soltanto atomi di carbonio e di idrogeno. Gli atomi di carbonio (C) sono legati tra loro a formare lo scheletro della molecola, mentre gli atomi di
Gli idrocarburi sono composti organici, che contengono soltanto atomi di carbonio e di idrogeno. Gli atomi di carbonio (C) sono legati tra loro a formare lo scheletro della molecola, mentre gli atomi di
Introduzione alla Chimica Organica. Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display.
 Introduzione alla Chimica Organica Copyright The McGraw-ill Companies, Inc. Permission required for reproduction or display. 1 Elementi Comuni nei Composti Organici 2 Classificazione degli idrocarburi
Introduzione alla Chimica Organica Copyright The McGraw-ill Companies, Inc. Permission required for reproduction or display. 1 Elementi Comuni nei Composti Organici 2 Classificazione degli idrocarburi
La chimica organica è la chimica dei composti contenenti carbonio
 Chimica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio I carbonati, il biossido di carbonio e i cianuri metallici sono un eccezione in quanto vengono classificati
Chimica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio I carbonati, il biossido di carbonio e i cianuri metallici sono un eccezione in quanto vengono classificati
c. Disegnate le conformazioni eclissate e sfalsate intermedie
 1. Per la seguente molecola a. Disegnate la conformazione meno stabile b. Disegnate la conformazione piu stabile c. Disegnate le conformazioni eclissate e sfalsate intermedie d. Utilizzando le seguenti
1. Per la seguente molecola a. Disegnate la conformazione meno stabile b. Disegnate la conformazione piu stabile c. Disegnate le conformazioni eclissate e sfalsate intermedie d. Utilizzando le seguenti
STEREOCHIMICA ORGANICA
 STEREIMIA RGANIA STEREISMERIA onformazione, configurazione: definizione strutturale e cinetica. Enantiomeria: chiralità centrale, assiale, planare. Stereoisomeria totale e residua. ANALISI NRMAZINALE 01
STEREIMIA RGANIA STEREISMERIA onformazione, configurazione: definizione strutturale e cinetica. Enantiomeria: chiralità centrale, assiale, planare. Stereoisomeria totale e residua. ANALISI NRMAZINALE 01
Chimica del carbonio. 1. Composti contenenti azoto (C,H,N) ammine. Aromatici (derivati del benzene di formula C 6 H 6 )
 himica del carbonio Il carbonio forma con 4 atomi diversi 4 legami covalenti equivalenti posti a 109,5, oppure con 3 atomi diversi 3 legami posti a 120, di cui uno doppio, oppure 2 legami covalenti con
himica del carbonio Il carbonio forma con 4 atomi diversi 4 legami covalenti equivalenti posti a 109,5, oppure con 3 atomi diversi 3 legami posti a 120, di cui uno doppio, oppure 2 legami covalenti con
Nomi e formule dei principali composti organici
 Nomi e formule dei principali composti organici Il numero davvero sterminato dei composti organici e la necessità quindi di doverli distinguere ciascuno con la propria formula e il proprio nome, ha costretto
Nomi e formule dei principali composti organici Il numero davvero sterminato dei composti organici e la necessità quindi di doverli distinguere ciascuno con la propria formula e il proprio nome, ha costretto
CORSO DI CHIMICA E PROPEDEUTICA BIOCHIMICA CORSO DI LAUREA IN TECNICHE DI LABORATORIO BIOMEDICO SAPIENZA UNIVERSITA' DI ROMA CHIMICA ORGANICA
 CORSO DI CHIMICA E PROPEDEUTICA BIOCHIMICA CORSO DI LAUREA IN TECNICHE DI LABORATORIO BIOMEDICO SAPIENZA UNIVERSITA' DI ROMA CHIMICA ORGANICA A causa della sua limitata elettronegativita', il carbonio
CORSO DI CHIMICA E PROPEDEUTICA BIOCHIMICA CORSO DI LAUREA IN TECNICHE DI LABORATORIO BIOMEDICO SAPIENZA UNIVERSITA' DI ROMA CHIMICA ORGANICA A causa della sua limitata elettronegativita', il carbonio
Chimica Organica. Definizione. La chimica organica è la chimica dei composti contenenti carbonio
 Chimica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio I carbonati, il biossido di carbonio e i cianuri metallici sono un eccezione in quanto vengono classificati
Chimica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio I carbonati, il biossido di carbonio e i cianuri metallici sono un eccezione in quanto vengono classificati
Nome degli alcheni a catena lineare
 Gli alcheni sono idrocarboni insaturi. insaturi (almeno un doppio legame) idrocarboni (solo e ) n 2n 1-Esene 6 12 opyright 1999, Michael J. Wovkulich. All rights reserved. Nome degli alcheni a catena lineare
Gli alcheni sono idrocarboni insaturi. insaturi (almeno un doppio legame) idrocarboni (solo e ) n 2n 1-Esene 6 12 opyright 1999, Michael J. Wovkulich. All rights reserved. Nome degli alcheni a catena lineare
Percorsi di chimica organica - Soluzioni degli esercizi del testo
 CAPITOLO 2 C 3 C 3 1. a) c) C 3 CCC 3 C 3 CC 2 CC 3 C 3 C 3 C 3 CC 2 C 2 CC 3 C 3 C 3 C 2 C 3 C 3 C 3 d) C 3 CC 2 CC 2 C 3 e) C3C2C CC2C2C2C3 C 3 C 2 C 3 f) C 3 CC 3 C 3 C 2 C CC 2 C 2 C 3 C 3 2. a) C
CAPITOLO 2 C 3 C 3 1. a) c) C 3 CCC 3 C 3 CC 2 CC 3 C 3 C 3 C 3 CC 2 C 2 CC 3 C 3 C 3 C 2 C 3 C 3 C 3 d) C 3 CC 2 CC 2 C 3 e) C3C2C CC2C2C2C3 C 3 C 2 C 3 f) C 3 CC 3 C 3 C 2 C CC 2 C 2 C 3 C 3 2. a) C
Gli idrocarburi contengono solo atomi di carbonio e di idrogeno. Gli idrocarburi alifatici hanno molecole lineari (talora ramificate) mentre quelli
 Gli idrocarburi contengono solo atomi di carbonio e di idrogeno. Gli idrocarburi alifatici hanno molecole lineari (talora ramificate) mentre quelli ciclici presentano molecole ad anello. Se hanno tutti
Gli idrocarburi contengono solo atomi di carbonio e di idrogeno. Gli idrocarburi alifatici hanno molecole lineari (talora ramificate) mentre quelli ciclici presentano molecole ad anello. Se hanno tutti
Corso di Laurea in Informazione Scientifica sul Farmaco a.a. 2010/2011. Esercitazione per la prima prova parziale di Chimica Organica.
 Corso di Laurea in Informazione Scientifica sul Farmaco a.a. 2010/2011. Esercitazione per la prima prova parziale di Chimica Organica. 1. Scrivere la formula condensata per la molecola seguente: Br e la
Corso di Laurea in Informazione Scientifica sul Farmaco a.a. 2010/2011. Esercitazione per la prima prova parziale di Chimica Organica. 1. Scrivere la formula condensata per la molecola seguente: Br e la
PERCHE STUDIARE LA CHIMICA ORGANICA?
 CIMICA ORGANICA CE COSA E LA CIMICA ORGANICA? La chimica organica è dedicata alla descrizione della struttura, delle proprietà e delle funzioni dei composti del carbonio (C). PERCE STUDIARE LA CIMICA ORGANICA?
CIMICA ORGANICA CE COSA E LA CIMICA ORGANICA? La chimica organica è dedicata alla descrizione della struttura, delle proprietà e delle funzioni dei composti del carbonio (C). PERCE STUDIARE LA CIMICA ORGANICA?
GLI ALCANI. Michele Kodrič
 GLI ALCANI Michee Kodrič DEGLI ALCANI VEDREMO: (CARATTERISTICE (NOMENCLATURA (FORMULAZIONE (COMPOSTI PRINCIPALI (REATTIVITA (OTTENIMENTO (ISOMERIA DI CATENA (GRUPPI ALCILICI 1 CARATTERISTICE DEGLI ALCANI
GLI ALCANI Michee Kodrič DEGLI ALCANI VEDREMO: (CARATTERISTICE (NOMENCLATURA (FORMULAZIONE (COMPOSTI PRINCIPALI (REATTIVITA (OTTENIMENTO (ISOMERIA DI CATENA (GRUPPI ALCILICI 1 CARATTERISTICE DEGLI ALCANI
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA)
 La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) IL CARBONIO E un non metallo, appartiene al IV gruppo ed al II periodo. Possiede 4 elettroni esterni per
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) IL CARBONIO E un non metallo, appartiene al IV gruppo ed al II periodo. Possiede 4 elettroni esterni per
Idrocarburi. Stereoisomeria
 Idrocarburi Stereoisomeria Stereisomeri configurazionali Il fatto che gli atomi di carbonio degli alcani siano tutti ibridati sp 3 rende possibile la formazione anche di altri stereoisomeri (isomeri con
Idrocarburi Stereoisomeria Stereisomeri configurazionali Il fatto che gli atomi di carbonio degli alcani siano tutti ibridati sp 3 rende possibile la formazione anche di altri stereoisomeri (isomeri con
La isomeria in Chimica Organica
 La isomeria in himica Organica isomeri composti differenti con la stessa formula molecolare (bruta) costituzionali isomeri i cui atomi sono connessi in modi diversi stereoisomeri P.es.: butano, 2-metil-propano
La isomeria in himica Organica isomeri composti differenti con la stessa formula molecolare (bruta) costituzionali isomeri i cui atomi sono connessi in modi diversi stereoisomeri P.es.: butano, 2-metil-propano
CHIMICA ORGANICA I - laboratorio AA 2009/10
 CIMICA ORGANICA I - laboratorio AA 2009/10 Esperienza 1 Costtrruziione dii MODELLII MOLECOLARII La conoscenza della struttura tridimensionale delle molecole è un elemento chiave per la comprensione delle
CIMICA ORGANICA I - laboratorio AA 2009/10 Esperienza 1 Costtrruziione dii MODELLII MOLECOLARII La conoscenza della struttura tridimensionale delle molecole è un elemento chiave per la comprensione delle
Gli elettroni della molecola sono quindi descritti da
 IL LEGAME COVALENTE: TEORIA DELL ORBITALE MOLECOLARE La molecola è considerata come un insieme di nuclei ed elettroni e, attraverso la valutazione delle reciproche interazioni, la teoria dell orbitale
IL LEGAME COVALENTE: TEORIA DELL ORBITALE MOLECOLARE La molecola è considerata come un insieme di nuclei ed elettroni e, attraverso la valutazione delle reciproche interazioni, la teoria dell orbitale
Unità didattica 2. Gli alcani sono idrocarburi contenenti solo legami singoli (per cui sono completamente saturi ) formula generale: C n H 2n+2
 Unità didattica 2 Gli alcani sono idrocarburi contenenti solo legami singoli (per cui sono completamente saturi ) fmula generale: C n 2n+2 Gli alcani (o idrocarburi saturi o idrocarburi alifatici o paraffine)
Unità didattica 2 Gli alcani sono idrocarburi contenenti solo legami singoli (per cui sono completamente saturi ) fmula generale: C n 2n+2 Gli alcani (o idrocarburi saturi o idrocarburi alifatici o paraffine)
Riassunto delle lezioni precedenti..
 Riassunto delle lezioni precedenti.. Chimica del Carbonio L atomo di Carbonio può formare legami singoli, legami doppi e legami tripli IDROCARBURI formati solo da carbonio e idrogeno Si dividono in 3 classi:
Riassunto delle lezioni precedenti.. Chimica del Carbonio L atomo di Carbonio può formare legami singoli, legami doppi e legami tripli IDROCARBURI formati solo da carbonio e idrogeno Si dividono in 3 classi:
Capitolo 19 Dal carbonio agli idrocarburi
 apitolo 19 Dal carbonio agli idrocarburi Hai capito? pag. 436 7 H 16 No pag. 437 8 H 16 pag. 438 A La struttura ramificata già descritta in (3) e (4). pag. 438 B l 2, l l, l 2, l l ; isomeria di posizione.
apitolo 19 Dal carbonio agli idrocarburi Hai capito? pag. 436 7 H 16 No pag. 437 8 H 16 pag. 438 A La struttura ramificata già descritta in (3) e (4). pag. 438 B l 2, l l, l 2, l l ; isomeria di posizione.
Alcheni: struttura e reattività
 Alcheni: struttura e reattività Alcheni Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n H 2n Alcheni in biologia ormone delle piante che induce la maturazione dei frutti costituente
Alcheni: struttura e reattività Alcheni Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n H 2n Alcheni in biologia ormone delle piante che induce la maturazione dei frutti costituente
Modulo di Biochimica 3 CFU (30 ore) Orario delle Lezioni: 1 semestre (settembre-dicembre) Lunedì 14-17
 Corso di laurea in ingegneria Biomedica A.A. 2017/2018 Modulo di Biochimica 3 CFU (30 ore) Orario delle Lezioni: 1 semestre (settembre-dicembre) Lunedì 14-17 Dott.ssa Morena Arba PhD. morena.arba@unica.it
Corso di laurea in ingegneria Biomedica A.A. 2017/2018 Modulo di Biochimica 3 CFU (30 ore) Orario delle Lezioni: 1 semestre (settembre-dicembre) Lunedì 14-17 Dott.ssa Morena Arba PhD. morena.arba@unica.it
Chimica Organica. Studio dei composti del CARBONIO
 Chimica Organica Studio dei composti del CARBONIO 1 Contengono C, H e possono contenere N, O, S Carbonio legato covalentemente ad un metallo Tutti gli elementi possibili Composti organici 2 Perché si formano
Chimica Organica Studio dei composti del CARBONIO 1 Contengono C, H e possono contenere N, O, S Carbonio legato covalentemente ad un metallo Tutti gli elementi possibili Composti organici 2 Perché si formano
Idrocarburi alifatici
 Idrocarburi alifatici Gli idrocarburi Gli idrocarburi sono composti organici costituiti esclusivamente da atomi di carbonio e idrogeno. In base alla loro struttura si suddividono in due grandi gruppi:
Idrocarburi alifatici Gli idrocarburi Gli idrocarburi sono composti organici costituiti esclusivamente da atomi di carbonio e idrogeno. In base alla loro struttura si suddividono in due grandi gruppi:
Le proprietà delle sostanze dipendono dal tipo di legame che unisce gli atomi e dalla forma delle molecole.
 4.1 Angolo di legame e forma delle molecole Le proprietà delle sostanze dipendono dal tipo di legame che unisce gli atomi e dalla forma delle molecole. La forma e le dimensioni delle molecole, la disposizione
4.1 Angolo di legame e forma delle molecole Le proprietà delle sostanze dipendono dal tipo di legame che unisce gli atomi e dalla forma delle molecole. La forma e le dimensioni delle molecole, la disposizione
ISOMERIA GEOMETRICA NEI CICLOALCHENI. I cicloalcheni fino a 7 C sono obbligati dalla rigidità dell'anello in configurazione cis H H
 ISOMERIA GEOMETRIA EI ILOALEI I cicloalcheni fino a 7 sono obbligati dalla rigidità dell'anello in configurazione Dal ILOOTTEE in poi l'anello è abbastanza grande da permettere l'esistenza anche dello
ISOMERIA GEOMETRIA EI ILOALEI I cicloalcheni fino a 7 sono obbligati dalla rigidità dell'anello in configurazione Dal ILOOTTEE in poi l'anello è abbastanza grande da permettere l'esistenza anche dello
LA CHIMICA ORGANICA IBRIDAZIONE
 LA CHIMICA ORGANICA Detta anche LA CHIMICA DEL CARBONIO (C) perché Il C gioca un ruolo fondamentale in tutte le molecole organiche (cioè appartenenti o derivanti da esseri viventi). Possiamo spiegarlo
LA CHIMICA ORGANICA Detta anche LA CHIMICA DEL CARBONIO (C) perché Il C gioca un ruolo fondamentale in tutte le molecole organiche (cioè appartenenti o derivanti da esseri viventi). Possiamo spiegarlo
Contenuti della lezione:
 Alcheni e Alchini Contenuti della lezione: Aspetti generali e nomenclatura di alcheni e alchini Uso delle nomenclature cis/trans e E/Z per gli alcheni di-sostituiti e tri- o tetrasostituiti rispetivamente
Alcheni e Alchini Contenuti della lezione: Aspetti generali e nomenclatura di alcheni e alchini Uso delle nomenclature cis/trans e E/Z per gli alcheni di-sostituiti e tri- o tetrasostituiti rispetivamente
LA CHIMICA DEL CARBONIO
 LA CHIMICA DEL CARBONIO E QUELLA PARTE DELLA CHIMICA CHE STUDIA IL CARBONIO E TUTTI I SUOI DERIVATI. I COMPOSTI DEL CARBONIO POSSONO ESSERE NATURALI (PROTEINE, ACIDI NUCLEICI, LIPIDI E CARBOIDRATI) O ESSERE
LA CHIMICA DEL CARBONIO E QUELLA PARTE DELLA CHIMICA CHE STUDIA IL CARBONIO E TUTTI I SUOI DERIVATI. I COMPOSTI DEL CARBONIO POSSONO ESSERE NATURALI (PROTEINE, ACIDI NUCLEICI, LIPIDI E CARBOIDRATI) O ESSERE
Capitolo 23 Dal carbonio agli idrocarburi
 Quesiti e problemi 1 a) sp 3 ; b) sp 2 ; c) sp. 2 B, E 3 Ibridazione Legami Geometria sp 3 4 σ Tetraedrica sp 2 3 σ e 1 π Trigonale planare sp 2 σ e 2 π Lineare 4 5 1 6 7 B 8 a) 1 e 2; b) tutte e tre;
Quesiti e problemi 1 a) sp 3 ; b) sp 2 ; c) sp. 2 B, E 3 Ibridazione Legami Geometria sp 3 4 σ Tetraedrica sp 2 3 σ e 1 π Trigonale planare sp 2 σ e 2 π Lineare 4 5 1 6 7 B 8 a) 1 e 2; b) tutte e tre;
CONTENUTI DELLA LEZIONE:
 Stereochimica CONTENUTI DELLA LEZIONE: 1. La Chiralità: Molecole chirali e achirali 2. Identificare uno stereocentro 3. Enantiomeri 4. Regole per assegnare la configurazione R,S 5. Diastereoisomeri 6.
Stereochimica CONTENUTI DELLA LEZIONE: 1. La Chiralità: Molecole chirali e achirali 2. Identificare uno stereocentro 3. Enantiomeri 4. Regole per assegnare la configurazione R,S 5. Diastereoisomeri 6.
Introduzione alla chimica organica. Daniele Dondi
 Introduzione alla chimica organica Daniele Dondi dondi@unipv.it 1 enni sulla nascita della chimica organica Analisi elementari tramite combustione WÖLER (metà 1800) sintetizza l urea KLBE sintetizza l
Introduzione alla chimica organica Daniele Dondi dondi@unipv.it 1 enni sulla nascita della chimica organica Analisi elementari tramite combustione WÖLER (metà 1800) sintetizza l urea KLBE sintetizza l
Esercizi sulle Forze Intermolecolari
 Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Esercizi sulle Forze Intermolecolari Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio/education/general-chemistry-exercises/
Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Esercizi sulle Forze Intermolecolari Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio/education/general-chemistry-exercises/
Chimica Organica. Breve storia della chimica organica
 Chimica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio I carbonati, il biossido di carbonio e i cianuri metallici sono un eccezione in quanto vengono classificati
Chimica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio I carbonati, il biossido di carbonio e i cianuri metallici sono un eccezione in quanto vengono classificati
L Atomo di Carbonio Tetraedrico e la Rappresentazione di Fischer
 L Atomo di Carbonio Tetraedrico e la Rappresentazione di Fischer Un atomo di carbonio con almeno due sostituenti identici e la sua immagine speculare sono sovrapponibili e quindi eguali atomo1.c3d Un atomo
L Atomo di Carbonio Tetraedrico e la Rappresentazione di Fischer Un atomo di carbonio con almeno due sostituenti identici e la sua immagine speculare sono sovrapponibili e quindi eguali atomo1.c3d Un atomo
Esercizi con i modelli molecolari
 MPLEMENTI Esercizi con i modelli molecolari Gli esercizi riportati in questa appendice sono finalizzati ad agevolare l apprendimento della natura tridimensionale delle molecole. Per eseguirli è necessario
MPLEMENTI Esercizi con i modelli molecolari Gli esercizi riportati in questa appendice sono finalizzati ad agevolare l apprendimento della natura tridimensionale delle molecole. Per eseguirli è necessario
M i n i s t e r o d e l l I s t r u z i o n e, d e l l U n i v e r s i t à e d e l l a R i c e r c a
 PROGRAMMA SVOLTO DOCENTE: Campani Maria Varini Simone A.S: 2018/2019 DISCIPLINA: Chimica organica e biochimica CLASSE: 3^A CHI MAT Per ogni Tema svolto vengono indicati i relativi contenuti. LEGAME CHIMICO
PROGRAMMA SVOLTO DOCENTE: Campani Maria Varini Simone A.S: 2018/2019 DISCIPLINA: Chimica organica e biochimica CLASSE: 3^A CHI MAT Per ogni Tema svolto vengono indicati i relativi contenuti. LEGAME CHIMICO
IL LEGAME CHIMICO. Per descrivere come gli elettroni si distribuiscono nell atomo attorno al nucleo si può far riferimento al MODELLO A GUSCI
 IL LEGAME CIMICO Come dagli atomi si costruiscono le molecole 02/19/08 0959 PM 1 Per descrivere come gli elettroni si distribuiscono nell atomo attorno al nucleo si può far riferimento al MODELLO A GUSCI
IL LEGAME CIMICO Come dagli atomi si costruiscono le molecole 02/19/08 0959 PM 1 Per descrivere come gli elettroni si distribuiscono nell atomo attorno al nucleo si può far riferimento al MODELLO A GUSCI
Gli Alcheni : struttura e nomenclatura
 Gli Alcheni : struttura e nomenclatura Alcheni Gli alcheni sono idrocarburi che contengono un doppio legame carbonio-carbonio sono anche detti olefine o idrocarburi insaturi La formula molecolare è C n
Gli Alcheni : struttura e nomenclatura Alcheni Gli alcheni sono idrocarburi che contengono un doppio legame carbonio-carbonio sono anche detti olefine o idrocarburi insaturi La formula molecolare è C n
Isomeria nelle molecole organiche
 Isomeria nelle molecole organiche 3 Cis/Trans o Z/E 1 4 Regole di priorità negli alcheni: 1. Numero atomico maggiore=maggiore priorità; 2. Maggiore priorità all isotopo più pesante; 3. Se il primo atomo
Isomeria nelle molecole organiche 3 Cis/Trans o Z/E 1 4 Regole di priorità negli alcheni: 1. Numero atomico maggiore=maggiore priorità; 2. Maggiore priorità all isotopo più pesante; 3. Se il primo atomo
Ammine : caratteristiche strutturali
 Ammine : caratteristiche strutturali Le ammine sono composti formalmente derivanti dall ammoniaca in cui uno o più atomi di idrogeno sono stati sostituiti da gruppi alchilici Come per l ammonica l azoto
Ammine : caratteristiche strutturali Le ammine sono composti formalmente derivanti dall ammoniaca in cui uno o più atomi di idrogeno sono stati sostituiti da gruppi alchilici Come per l ammonica l azoto
