Università degli Studi Kore di Enna Facoltà di Scienze Motorie e delbenessere CdL in Scienze delle attività motorie e sportive
|
|
|
- Ilario Cenci
- 5 anni fa
- Visualizzazioni
Transcript
1 Università degli Studi Kore di Enna Facoltà di Scienze Motorie e delbenessere dl in Scienze delle attività motorie e sportive Biochimica - Ph.D. domenico.ciavardelli@unikore.it
2 Esercizi: Soluzioni
3 l N N N Sulla base delle regole proposte, calcolare il numero d ossidazione del carbonio e dell azoto nei seguenti composti organici. Individuare e denominare i principali gruppi funzionali presenti nelle molecole
4 Lezioni 1, 2-Supplemento 2 Le regole per il calcolo dei numeri di ossidazione (carica formale) di un atomo in un sistema poliatomico (ovvero quando quest atomo è legato ad altri atomi) sono le seguenti: Un legame tra atomi uguali non determina separazione di carica (stessa elettronegatività) e quindi non contribuisce alla carica formale dell atomo in esame. Per questo motivo nelle molecole biatomiche omonucleari (2, 2, N2, l2) gli atomi hanno numero di ossidazione nullo. Per lo stesso motivo un atomo di carbonio legato a 4 atomi di carboni avrà carica formale nulla. L idrogeno ha sempre carica formale +1 (tranne che nei composti con metalli alcalini ed alcalino terrosi). Questo implica che un legame con idrogeno determina una carica formale per l atomo a cui è legato. L ossigeno ha sempre carica formale ( tranne che nei perossidi e superossidi).
5 1 + 3 N 2 Il calcolo dei numeri di ossidazione (carica formale) di un atomo in un sistema poliatomico (ovvero quando quest atomo è legato ad altri atomi) deve tenere conto della carica della molecola alla quale l atomo appartiene: la somma algebrica delle cariche formali degli elementi che compongono la molecola deve essere uguale alla carica complessiva della molecola. 3-3 N Gruppo ammidico Legame tra 2 AA Dipeptide Ala-Phe 2 Glucosio, forma ciclica emiacetallica - +1 La molecola è complessivamente neutra (Gruppo amminico di Ala carico positivamente, gruppo carbossilico di Phe carico negativamente +1=) Dalla formula molecolare e dalla carica della molecola è possibile calcolare la carica media di : La formula bruta della molecola è 11143N2 arica della molecola==[(carica formale di )*(numero di atomi )]+[(carica formale di )*(numero di atomi di )]+[(carica formale di )*(numero di atomi di )]+[(carica formale di N)*(numero di atomi di N)]=x+(+1*14)+(*3)+(-3*2)=x =x+2 x=. Dividendo per 11 (numero di atomi di ) si può calcolare il numero di ossidazione medio di nella molecola. ss.: la somma algebrica delle cariche formali degli atomi di calcolate individualmente è (*5)=3-5= e coincide con quella calcolata dalla formula bruta La molecola è neutra Dalla formula molecolare e dalla carica della molecola è possibile calcolare la carica media di : La formula bruta della molecola è 6126 =x+(+1*12)+(*6)=x+122=x+ x=. Dividendo per 6 si ottiene il numero di ossidazione medio di che è ovviamente. ss.: la somma algebrica delle cariche formali degli atomi di calcolate individualmente è +1+(*4)+()= e coincide con quella calcolata dalla formula bruta
6 Ricordare che: P Acido fosforico (oosoacido inorganico) Gruppo estereo dell acetato di etile (ottenuto da acido acetico 3 e etanolo 32) p P - Forma deprotonata dell cido fosforico fosfato A p fisiologico il fosfato è un anione divalente. Questo è il motivo delle cariche negative in biomolecole che contengono gruppi fosfoesterei o fosfoanidridici come ATP. alcolo del numero di ossidazione del fosforo (x) nelle due forme protonata e deprotonata 1. Acido fosforico prima della dissociazione Formula bruta: 3P4; arica nulla (, molecola neutra) =x+(+1*3)+(*4)=x-8 x=+8-3=+5 2. Fosfato dopo la dissociazione a p7 Formula bruta: P4 2- ; carica della molecola= (anione divalente) =x+(+1*1)+(*4)=x+1-8 x=- 1+8=+5 N.B.: il numero di ossidazione di P non cambia quindi la DISSIAZINE AIDA non è una reazione di ossidoriduzione che coinvolge P Gli esteri sono derivati di acidi carbossilici e alcooli (condensazione con perdita di 2 R- + R - = 2 + R-R ) ss.: Il gruppo 3- viene denominato comunemente acetile 22 + P P 2 3 p Gli esteri dell acido fosforico sono derivati dell acido inorganico e alcooli (condensazione con perdita di 2 3P4 + R - = P-R )
7 Ricordare che: Altri importanti gruppi funzionali contenenti P e presenti in varie biomolecole sono le FSFANIDRIDI e le ANIDRIDI MISTE ottenute da acido carbossilico e acido fosforico. In generale le anidridi sono come gli esteri e le ammidi derivati degli acidi carbossilici caratterizzati da reattività maggiore bassa stabilità. Un anidride può essere considerata il prodotto della condensazione con perdita di acqua di 2 molecole di acido carbossilico R R' R R' Gruppo funzionale delle anidridi + 2 Es. anidride acetica 3-3 Acido acetico P P - - R 3 3 Anidride acetica P Le anidridi possono essere ottenute da altri acidi come l acido fosforico che può dare reazioni con un altra molecola di acido fosforico (fosfoanidride) o con una molecola di acido carbossilico (anidride mista). Gruppo funzionale delle fosfoanidridi (Es.: ATP) Gruppo funzionale delle anidridi miste, in figura anidirde dell acido acetico e dell acido fosforico (Es.: 1,3-difosfoglicerato prodotto della reazione 6 della glicolisi )
8 Soluzioni Idrocarburo aromatico (Anello aromatico) Benzene Gruppo arbonilico legato almeno ad Un atomo d idrogeno (aldeide) Formaldeide (aldeide più semplice: R=) +2 Gruppo arbossilico (acido carbossilico) Acido formico (acido carbossilico Più semplice: R=) Idrocarburo Alifatico insaturo (doppio legame) alchene 1-esene (-ene: suffisso usato per gli alcheni; 1-posizione del doppio legame) -3 Idrocarburo Alifatico saturo (atena alifatica satura: legami semplici -, alcano atena alifatica satura: legami semplici -, Alcano R=3: gruppo etilico Gruppo carbonilico Legato a due gruppi Alchilici R hetone R=-3: gruppo metilico 2-butanone (etil-metil chetone): -one: suffisso usato per i chetoni 2-: posizione del gruppo carbonilico (minimo numero possibile) Penten-: prefisso che indica il numero di nella catena principale (5)
9 Idrocarburo Alifatico insaturo (doppio legame) alchene -3-3 Gruppo SSIDRILI ( ledato a un atomo di carbonio legato a gruppi alchilici R o atomi d idrogeno. In tal caso 2 R e 1 ALL SENDARI 2- Propanolo (2-: posizione del gruppo ossidrilico) Gruppo carbossilico (acido carbossilico) Acido propenoico (-ene: suffisso usato per gli alcheni; prop-: prefisso che indica il numero di nella catena principale (3)) Idrocarburo Alifatico saturo (atena alifatica satura: legami semplici -, alcano N più elettronegativo (3.7) di (2.2) e (2.5) Atomo d azoto ledato a a gruppi alchilici R (in tal caso un legame N o atomi d idrogeno Ammina Idrocarburo Alifatico insaturo (triplo legame) Alchino Propino (-ino: suffisso usato per gli alchini; prop-: prefisso che indica il numero di nella catena principale (3)) -3 N -3-3 Questo composto è caratterizzato dalla presenza di un gruppo amminico e di un gruppo carbossilico legati ad un atomo di R=gruppo alchilico=3- =gruppo metilico Gruppo carbossilico Acido carbossilico Idrocarburo Alifatico saturo (atena alifatica satura: legami semplici -, alcano a sua volta legato ad un atomo e ad un gruppo alchilico R. Questo motivo strutturale è tipico di una classe di molecole biologicamente importanti, gli amminoacidi (AA). Per gli amminoacidi per i quali si usa una nomenclatura comune. R=3-=gruppo metilico Alanina
10 -3-3 N Gruppi metilici (3-3 Gruppo Etilico (32 Atomo di azoto legato a 3 Gruppi alchilici gruppo amminico. AMMINA TERZIARIA Etil-dimetil ammina (di-: prefisso usato per indicare la presenza di 2 gruppi) atena alifatica satura: legami semplici -, Alcano R=23: gruppo propilico Gruppo SSIDRILI ( ledato a un atomo di carbonio legato a gruppi alchilici R o atomi d idrogeno. In tal caso 1 R e 2 ALL PRIMARI 1- Propanolo (1-: posizione del gruppo ossidrilico) +1 Gruppo SSIDRILI ( ledato a un atomo di carbonio Appartenente ad un anello romatico ALL ARMATI Idrossibenzene (nome comune: fenolo). atena alifatica satura: legami semplici -, Alcano R=3: gruppo etilico -3 N -3 Atomo di azoto legato a 1 Gruppo alchilico e a due gruppo amminico. AMMINA PRIMARIA Etil-ammina Anello aromatico Idrocarburo aromatico
11 Gruppo alchilico 3- (metile) -3 Idrocarburo Alifatico saturo (atena alifatica satura: legami semplici -, Alcano Esano (prefisso esa-: catena a 6 atomi di ) -3 Idrocarburo aromatico Benzene sostituito (un atomo di idrogeno sostituito da un gruppo Alchilico) metilbenzene (nome comune: toluene). Anello aromatico Idrocarburo aromatico Idrocarburo Alifatico insaturo (doppio legame) Alchene 2-esene (2-: posizione del doppio legame) -3 atena alifatica satura Gruppo alchilico 3- (metile)
12 atena alifatica satura: legami semplici -, Gruppo carbossilico Acido carbossilico Acido propanoico atena alifatica satura: legami semplici -, - Gruppo carbonilico Il carbonile è legato ad un e ad un R Aldeide Aldeide propanoica (o anche propanale; prefisso prop- 3 atomi di ; suffisso ale: tipico delle aldeidi) Aldeide stato ridotto rispetto all acido carbossilico atena alifatica satura: legami semplici -, - -3 l iclo aromatico Due cicli aromatici condensati Sistema policiclico aromatico Legame -alogeno ( in tal caso cloro) Alogenuri alchilici 2-cloropropano
13 Porre in ordine crescente per stato d ossidazione del carbonio i seguenti composti valutando lo stato d ossidazione medio di dalla formula bruta. Ricordare che la formula bruta di una molecola indica la composizione atomica del composto (ad esempio la formula bruta del glucosio è 6126). Nel calcolo del numero di ossidazione medio del carbonio considerare la carica della molecola. Il fosforo nei gruppi fosfato ha numero di ossidazione P 2 P P P P 3 2 P 3
14 Soluzioni Formula molecolare: alcolo della carica formale media di =[x+(+1*3)+(*3)]=x-6 x=6-3=+2 Gli atomi di carbonio sono 3 2/3=numero di ossidazione medio di 3 P Formula molecolare: 341P P 3 alcolo della carica formale media di -4=[x+(+1*4)+(*1)+(+5*2)]=x =x=+2 Gli atomi di sono 3 2/3=numero di ossidazione medio di 2 Formula molecolare: 6126 alcolo della carica formale media di =[x+(+1*12)+(*6)]=x+122 x= (Vedi sopra, slide 5). Numero do ossidazione medio di =
15 4 2 3 P P Formula molecolare: 6112P2( 4- ) arica complessiva della media=-4 alcolo della carica formale complessiva di -4=[x+(+1*1)+(*12)+(+5*2)]= x+14+1=x-4 x=. Numero di ossidazione medio di = P 3 Formula molecolare: 356P- ) arica complessiva della media= alcolo della carica formale complessiva di =[x+(+1*5)+(*6)+(+5*1)]= x+52+5=x x= Numero di ossidazione medio di = P 3 Formula molecolare: 326P( 3- ) arica complessiva della molecola=-3 alcolo della carica formale media di -3=[x+(+1*2)+(*6)+(+5*1)]= x+22+5=x-5 x=+2 Numero di ossidazione medio di =2/3
16 3 2 3 P 2 P = 3 P P 2 3 = < = P = 1 P 3 3 Numero d ossidazione medio del arbonio ommento: molti avranno riconosciuto nei composti mostrati in precedenza gli intermedi della prima fase della respirazione cellulare, la glicolisi. In particolare il composto 2 (1,3-difosfo glicerato) è il prodotto dell ossidazione della gliceraldeide 3-fosfato (composto 5) che richiede la riduzione del coenzima NAD+ a NAD e +. Questa è l unica reazione di ossidoriduzione della glicolisi. Quindi gli intermedi derivati dall 1,3-difosfoglicerato non presenteranno alterazioni della carica formale media di.
17 Indicare quali delle seguenti trasformazioni sono reazioni di ossidoriduzione e specificare se si tratti di una ossidazione o di una riduzione. ( 2 3 P P 3 P 3 P P 2 3 P 2 4 5
18 Soluzioni P 3 3 P 2 P 3 ssidazione (aldeide ossidata a carbossile in un anidride mista) 2 +1 P La carica media del carbonio (+2/3) non cambia: non è una reazione di ossidoriduzione P 2 3 P 2 La carica media del carbonio non cambia: non è una reazione di ossidoriduzione ma un isomerizzazione Stessa formula molecolare 6119P, diversa formula di struttura ISMERI
19 4 +2 ssidazione (il gruppo ossidrilico, eossidato a chetone +2 ) 5 +2 ssidazione (il gruppo ossidrilico, eossidato a chetone +2 )
20 ommento: molti avranno riconosciuto nelle reazioni mostrate alcune reazioni della glicolisi (reazioni 1, 2, 3) e del ciclo di Krebs (reazioni 4, 5, 6). La reazione 1 è l unica reazione di ossidoriduzione della glicolisi (prima fase della respirazione cellulare) che comporta l ossidazione del gruppo aldeidico ad anidride mista ed è associata alla riduzione di nicotinammide adenina dinucleotide (NAD+). Le reazioni 2 e 3 non richiedono ossidazione o riduzione di coenzimi e quindi non sono processi ossidoriduttivi. Le reazioni 4 e 5 sono invece reazioni del ciclo di Krebs e corrispondono alle reazioni 8 e 3 del ciclo di Krebs ovvero alla trasformazione del malato ad ossalacetato (ultima reazione del ciclo) e dell isocitrato ad - chetoglutarato che richiedono la simultanea riduzione di NAD+ a NAD + +. Tali processi sono quindi ossidazioni.
Università degli Studi Kore di Enna Facoltà di Scienze dell Uomo e della Società CdL in Scienze delle attività motorie e sportive
 Università degli Studi Kore di Enna Facoltà di Scienze dell Uomo e della Società dl in Scienze delle attività motorie e sportive Biochimica - Ph.D. email: domenico.ciavardelli@unikore.it Esercizi: Soluzioni
Università degli Studi Kore di Enna Facoltà di Scienze dell Uomo e della Società dl in Scienze delle attività motorie e sportive Biochimica - Ph.D. email: domenico.ciavardelli@unikore.it Esercizi: Soluzioni
Tipologie di formule chimiche
 CHIMICA ORGANICA Tipologie di formule chimiche FORMULA RAZIONALE Tipo di formula che utilizza una rappresentazione analoga alla formula bruta per quei gruppi di atomi sulla cui disposizione non vi possono
CHIMICA ORGANICA Tipologie di formule chimiche FORMULA RAZIONALE Tipo di formula che utilizza una rappresentazione analoga alla formula bruta per quei gruppi di atomi sulla cui disposizione non vi possono
Chimica organica Chimica dei composti del carbonio. Nelle molecole organiche oltre al carbonio sono presenti pochi altri elementi: H, O, N, P,
 himica organica himica dei composti del carbonio. Nelle molecole organiche oltre al carbonio sono presenti pochi altri elementi:,, N, P, S, alogeni. Le molecole organiche presentano particolari raggruppamenti
himica organica himica dei composti del carbonio. Nelle molecole organiche oltre al carbonio sono presenti pochi altri elementi:,, N, P, S, alogeni. Le molecole organiche presentano particolari raggruppamenti
I composti organici. Gli idrocarburi: composti binari, ovvero costituiti solo da due elementi. Carbonio (C) e idrogeno (H)
 I composti organici Gli idrocarburi: composti binari, ovvero costituiti solo da due elementi. Carbonio (C) e idrogeno (H) Gli idrocarburi Gli Alcani Costituiti da uno o più atomi di carbonio legati tra
I composti organici Gli idrocarburi: composti binari, ovvero costituiti solo da due elementi. Carbonio (C) e idrogeno (H) Gli idrocarburi Gli Alcani Costituiti da uno o più atomi di carbonio legati tra
Chimica del carbonio. 1. Composti contenenti azoto (C,H,N) ammine. Aromatici (derivati del benzene di formula C 6 H 6 )
 himica del carbonio Il carbonio forma con 4 atomi diversi 4 legami covalenti equivalenti posti a 109,5, oppure con 3 atomi diversi 3 legami posti a 120, di cui uno doppio, oppure 2 legami covalenti con
himica del carbonio Il carbonio forma con 4 atomi diversi 4 legami covalenti equivalenti posti a 109,5, oppure con 3 atomi diversi 3 legami posti a 120, di cui uno doppio, oppure 2 legami covalenti con
Riassunto delle lezioni precedenti..
 Riassunto delle lezioni precedenti.. Chimica del Carbonio L atomo di Carbonio può formare legami singoli, legami doppi e legami tripli IDROCARBURI formati solo da carbonio e idrogeno Si dividono in 3 classi:
Riassunto delle lezioni precedenti.. Chimica del Carbonio L atomo di Carbonio può formare legami singoli, legami doppi e legami tripli IDROCARBURI formati solo da carbonio e idrogeno Si dividono in 3 classi:
IDROCARBURI. Alcani Alcheni Alchini C-C C=C C C
 IDROCARBURI Alcani Alcheni Alchini C-C C=C C C Nomenclatura Degli idrocarburi saturi (Alcani) CH 4 Metano C 2 H 6 Etano C n H 2n+2 Si dicono alchilici quei gruppi che contengono un idrogeno in meno del
IDROCARBURI Alcani Alcheni Alchini C-C C=C C C Nomenclatura Degli idrocarburi saturi (Alcani) CH 4 Metano C 2 H 6 Etano C n H 2n+2 Si dicono alchilici quei gruppi che contengono un idrogeno in meno del
Gli idrocarburi contengono solo atomi di carbonio e di idrogeno. Gli idrocarburi alifatici hanno molecole lineari (talora ramificate) mentre quelli
 Gli idrocarburi contengono solo atomi di carbonio e di idrogeno. Gli idrocarburi alifatici hanno molecole lineari (talora ramificate) mentre quelli ciclici presentano molecole ad anello. Se hanno tutti
Gli idrocarburi contengono solo atomi di carbonio e di idrogeno. Gli idrocarburi alifatici hanno molecole lineari (talora ramificate) mentre quelli ciclici presentano molecole ad anello. Se hanno tutti
Introduzione alla chimica organica. Daniele Dondi
 Introduzione alla chimica organica Daniele Dondi dondi@unipv.it Il carbonio nelle sue ibridazioni sp 3 sp 2 sp Il carbonio è un elemento fondamentale per la chimica organica. La stabilità del legame -
Introduzione alla chimica organica Daniele Dondi dondi@unipv.it Il carbonio nelle sue ibridazioni sp 3 sp 2 sp Il carbonio è un elemento fondamentale per la chimica organica. La stabilità del legame -
Pillole di... Chimica organica
 sono composti binari che contengono soltanto idrogeno e carbonio. Pillole di... Chimica organica Idrocarburi saturi contengono soltanto legami semplici tra gli atomi di carbonio Alcani (idrocarburi lineari)
sono composti binari che contengono soltanto idrogeno e carbonio. Pillole di... Chimica organica Idrocarburi saturi contengono soltanto legami semplici tra gli atomi di carbonio Alcani (idrocarburi lineari)
Capitolo 8 Alcoli e Fenoli
 Chimica Organica Informazione Scientifica sul Farmaco Capitolo 8 Alcoli e Fenoli Organic Chemistry, 5 th Edition L. G. Wade, Jr. Struttura degli Alcoli Alcoli: Il gruppo funzionale è l ossidrile (), legato
Chimica Organica Informazione Scientifica sul Farmaco Capitolo 8 Alcoli e Fenoli Organic Chemistry, 5 th Edition L. G. Wade, Jr. Struttura degli Alcoli Alcoli: Il gruppo funzionale è l ossidrile (), legato
Isomeria ottica. Un atomo di carbonio presente in un composto organico viene definito asimmetrico quando lega quattro sostituenti diversi.
 Isomeria ottica Un atomo di carbonio presente in un composto organico viene definito asimmetrico quando lega quattro sostituenti diversi. Un atomo di carbonio asimmetrico è un centro chirale, e forma così
Isomeria ottica Un atomo di carbonio presente in un composto organico viene definito asimmetrico quando lega quattro sostituenti diversi. Un atomo di carbonio asimmetrico è un centro chirale, e forma così
H N H R N H R N R R N R H H H
 AMMINE Sono derivati dell ammoniaca (NH 3 ) nei quali uno o più atomi di idrogeno sono sostituiti da altrettanti radicali alchilici (R-, come ad esempio il gruppo -CH 3 ). Come l ammoniaca anche le ammine
AMMINE Sono derivati dell ammoniaca (NH 3 ) nei quali uno o più atomi di idrogeno sono sostituiti da altrettanti radicali alchilici (R-, come ad esempio il gruppo -CH 3 ). Come l ammoniaca anche le ammine
Introduzione alla Chimica Organica. Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display.
 Introduzione alla Chimica Organica Copyright The McGraw-ill Companies, Inc. Permission required for reproduction or display. 1 Elementi Comuni nei Composti Organici 2 Classificazione degli idrocarburi
Introduzione alla Chimica Organica Copyright The McGraw-ill Companies, Inc. Permission required for reproduction or display. 1 Elementi Comuni nei Composti Organici 2 Classificazione degli idrocarburi
Introduzione alla chimica organica. Daniele Dondi
 Introduzione alla chimica organica Daniele Dondi dondi@unipv.it 1 enni sulla nascita della chimica organica Analisi elementari tramite combustione WÖLER (metà 1800) sintetizza l urea KLBE sintetizza l
Introduzione alla chimica organica Daniele Dondi dondi@unipv.it 1 enni sulla nascita della chimica organica Analisi elementari tramite combustione WÖLER (metà 1800) sintetizza l urea KLBE sintetizza l
Alcoli, fenoli ed eteri
 Alcoli, fenoli ed eteri Alcoli e fenoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Fenoli: gruppo ossidrilico legato ad un anello aromatico Metanolo Sintesi industriale Tossico per l uomo
Alcoli, fenoli ed eteri Alcoli e fenoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Fenoli: gruppo ossidrilico legato ad un anello aromatico Metanolo Sintesi industriale Tossico per l uomo
NOMENCLATURA DI MOLECOLE CONTENENTI GRUPPI FUNZIONALI E LEGAMI MULTIPLI
 NOMENCLATURA DI MOLECOLE CONTENENTI GRUPPI FUNZIONALI E LEGAMI MULTIPLI Quando la molecola contiene sia un gruppo funzionale che un legame multiplo la desinenza deve essere doppia, includendo sia il suffisso
NOMENCLATURA DI MOLECOLE CONTENENTI GRUPPI FUNZIONALI E LEGAMI MULTIPLI Quando la molecola contiene sia un gruppo funzionale che un legame multiplo la desinenza deve essere doppia, includendo sia il suffisso
I composti del carbonio
 Elementi di chimica I composti del carbonio Esistono numerosissimi composti del carbonio sono oggetto di studio della chimica organica. Il carbonio tende a formare 4 legami covalenti. Il gruppo funzionale
Elementi di chimica I composti del carbonio Esistono numerosissimi composti del carbonio sono oggetto di studio della chimica organica. Il carbonio tende a formare 4 legami covalenti. Il gruppo funzionale
I gruppi funzionali: GLI ALCOLI, FENOLI E TIOLI
 I gruppi funzionali: GLI ALCOLI, FENOLI E TIOLI La struttura Un alcol può essere considerato come un idrocarburo (alifatico o aromatico) a cui è stato sostituito un gruppo (ossidrile) Il nome deriva dalla
I gruppi funzionali: GLI ALCOLI, FENOLI E TIOLI La struttura Un alcol può essere considerato come un idrocarburo (alifatico o aromatico) a cui è stato sostituito un gruppo (ossidrile) Il nome deriva dalla
DAI GRUPPI FUNZIONALI AI POLIMERI
 DAI GRUPPI FUNZIONALI AI POLIMERI 1. I GRUPPI FUNZIONALI 2. DERIVATI OSSIGENATI DEGLI IDROCARBURI : ALCOLI, FENOLI, ETERI, ALDEIDI E CHETONI, ACIDI CARBOSSILICI E LORO DERIVATI 3. DERIVATI AZOTATI DEGLI
DAI GRUPPI FUNZIONALI AI POLIMERI 1. I GRUPPI FUNZIONALI 2. DERIVATI OSSIGENATI DEGLI IDROCARBURI : ALCOLI, FENOLI, ETERI, ALDEIDI E CHETONI, ACIDI CARBOSSILICI E LORO DERIVATI 3. DERIVATI AZOTATI DEGLI
LA CHIMICA DEL CARBONIO
 LA CHIMICA DEL CARBONIO E QUELLA PARTE DELLA CHIMICA CHE STUDIA IL CARBONIO E TUTTI I SUOI DERIVATI. I COMPOSTI DEL CARBONIO POSSONO ESSERE NATURALI (PROTEINE, ACIDI NUCLEICI, LIPIDI E CARBOIDRATI) O ESSERE
LA CHIMICA DEL CARBONIO E QUELLA PARTE DELLA CHIMICA CHE STUDIA IL CARBONIO E TUTTI I SUOI DERIVATI. I COMPOSTI DEL CARBONIO POSSONO ESSERE NATURALI (PROTEINE, ACIDI NUCLEICI, LIPIDI E CARBOIDRATI) O ESSERE
TAVOLA PERIODICA DEGLI ELEMENTI
 TAVOLA PERIODIA DEGLI ELEMENTI Idrogeno = 1 legame Ossigeno = 2 legami O Azoto = 3 legami N arbonio = 4 legami Questi sono gli atomi che intervengono maggiormente nelle reazioni che tratteremo nella
TAVOLA PERIODIA DEGLI ELEMENTI Idrogeno = 1 legame Ossigeno = 2 legami O Azoto = 3 legami N arbonio = 4 legami Questi sono gli atomi che intervengono maggiormente nelle reazioni che tratteremo nella
Capitolo 24 Dai gruppi funzionali ai polimeri
 Capitolo 24 Dai gruppi funzionali ai polimeri 1. I gruppi funzionali 2. Alcoli, fenoli ed eteri 3. Le reazioni di alcoli e fenoli 4. Alcoli e fenoli di particolare interesse 5. Aldeidi e chetoni 6. Gli
Capitolo 24 Dai gruppi funzionali ai polimeri 1. I gruppi funzionali 2. Alcoli, fenoli ed eteri 3. Le reazioni di alcoli e fenoli 4. Alcoli e fenoli di particolare interesse 5. Aldeidi e chetoni 6. Gli
Alcoli, fenoli ed eteri
 Alcoli, fenoli ed eteri Alcoli e fenoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Fenoli: gruppo ossidrilico legato ad un anello aromatico Metanolo Sintesi industriale Tossico per l uomo
Alcoli, fenoli ed eteri Alcoli e fenoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Fenoli: gruppo ossidrilico legato ad un anello aromatico Metanolo Sintesi industriale Tossico per l uomo
La chimica organica è la chimica dei composti contenenti carbonio
 Chimica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio I carbonati, il biossido di carbonio e i cianuri metallici sono un eccezione in quanto vengono classificati
Chimica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio I carbonati, il biossido di carbonio e i cianuri metallici sono un eccezione in quanto vengono classificati
L acqua e il legame idrogeno
 Elementi di chimica L acqua e il legame idrogeno La molecola di acqua è polare formazione di legami idrogeno. Da questi legami derivano le peculiarità dell acqua (ad es. «solvente universale»). Le reazioni
Elementi di chimica L acqua e il legame idrogeno La molecola di acqua è polare formazione di legami idrogeno. Da questi legami derivano le peculiarità dell acqua (ad es. «solvente universale»). Le reazioni
Chimica Organica. Studio dei composti del CARBONIO
 Chimica Organica Studio dei composti del CARBONIO 1 Contengono C, H e possono contenere N, O, S Carbonio legato covalentemente ad un metallo Tutti gli elementi possibili Composti organici 2 Perché si formano
Chimica Organica Studio dei composti del CARBONIO 1 Contengono C, H e possono contenere N, O, S Carbonio legato covalentemente ad un metallo Tutti gli elementi possibili Composti organici 2 Perché si formano
Chimica Organica. Definizione. La chimica organica è la chimica dei composti contenenti carbonio
 himica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio Il carbonio è l unico elemento capace di legarsi fortemente con se stesso e formare lunghe catene o anelli
himica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio Il carbonio è l unico elemento capace di legarsi fortemente con se stesso e formare lunghe catene o anelli
Capitolo A1 Chimica organica: un introduzione
 Quesiti e problemi 1 C 2 B 3 B 4 B 5 The ability to form covalent bonds. 6 Gli idrocarburi si suddividono in saturi e insaturi. Gli idrocarburi saturi contengono solo legami semplici C-C; fa parte di questo
Quesiti e problemi 1 C 2 B 3 B 4 B 5 The ability to form covalent bonds. 6 Gli idrocarburi si suddividono in saturi e insaturi. Gli idrocarburi saturi contengono solo legami semplici C-C; fa parte di questo
Nomi e formule dei principali composti organici
 Nomi e formule dei principali composti organici Il numero davvero sterminato dei composti organici e la necessità quindi di doverli distinguere ciascuno con la propria formula e il proprio nome, ha costretto
Nomi e formule dei principali composti organici Il numero davvero sterminato dei composti organici e la necessità quindi di doverli distinguere ciascuno con la propria formula e il proprio nome, ha costretto
Problemi 1 PROPEDEUTICITÀ
 Problemi 1 PROPEDEUTICITÀ Da manifesto degli studi del corso per sostenere l esame di Chimica Biologica bisogna aver superato: Citologia e Istologia Chimica Organica (Chimica generale) Non vale questa
Problemi 1 PROPEDEUTICITÀ Da manifesto degli studi del corso per sostenere l esame di Chimica Biologica bisogna aver superato: Citologia e Istologia Chimica Organica (Chimica generale) Non vale questa
Lezione: aldeidi e chetoni
 Lezione: aldeidi e chetoni Il gruppo funzionale carbonilico Nomenclatura Proprietà fisiche Principali reazioni eazioni con N eazioni con alcoli eazioni con tioli eazioni con ammine Tautomeria cheto-enolica
Lezione: aldeidi e chetoni Il gruppo funzionale carbonilico Nomenclatura Proprietà fisiche Principali reazioni eazioni con N eazioni con alcoli eazioni con tioli eazioni con ammine Tautomeria cheto-enolica
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 9 Il mondo del carbonio 3 Sommario 1. Esiste un enorme varietà di composti organici 2. Gli idrocarburi saturi: alcani e cicloalcani
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 9 Il mondo del carbonio 3 Sommario 1. Esiste un enorme varietà di composti organici 2. Gli idrocarburi saturi: alcani e cicloalcani
GRUPPI FUNZIONALI GLI ALCOLI
 GRUPPI FUNZIONALI In chimica organica è detto gruppo funzionale una parte della struttura di una molecola caratterizzata da specifici elementi (atomi) e da una struttura ben definita e precisa, che conferisce
GRUPPI FUNZIONALI In chimica organica è detto gruppo funzionale una parte della struttura di una molecola caratterizzata da specifici elementi (atomi) e da una struttura ben definita e precisa, che conferisce
Alchini. Francesca Anna Scaramuzzo, PhD
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alchini Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate per
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alchini Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate per
R = GRUPPO FUNZIONALE Atomo o raggruppamento atomico
 GRUPPI FUNZIONALI GRUPPO FUNZIONALE Atomo o raggruppamento atomico presente in un composto organico, che conferisce adesso particolari proprietà fisiche e chimiche E il punto più reattivo della molecola
GRUPPI FUNZIONALI GRUPPO FUNZIONALE Atomo o raggruppamento atomico presente in un composto organico, che conferisce adesso particolari proprietà fisiche e chimiche E il punto più reattivo della molecola
Verifiche dei Capitoli - Tomo C
 Soluzioni Verifiche dei Capitoli - Tomo C Per ogni Capitolo sono presentate le soluzioni delle Verifiche, delle Autoverifiche, delle Competenze e dei quesiti proposti nelle schede di Laboratorio. VERIFICHE
Soluzioni Verifiche dei Capitoli - Tomo C Per ogni Capitolo sono presentate le soluzioni delle Verifiche, delle Autoverifiche, delle Competenze e dei quesiti proposti nelle schede di Laboratorio. VERIFICHE
Stampa Preventivo. A.S Pagina 1 di 8
 Stampa Preventivo A.S. 2009-2010 Pagina 1 di 8 Insegnante POLESEL Classe 4LTS ART Materia chimica organica e biochimica preventivo consuntivo 106 0 titolo modulo 1. Idrocarburi 2. Composti ossigenati 3.
Stampa Preventivo A.S. 2009-2010 Pagina 1 di 8 Insegnante POLESEL Classe 4LTS ART Materia chimica organica e biochimica preventivo consuntivo 106 0 titolo modulo 1. Idrocarburi 2. Composti ossigenati 3.
Composti carbonilici. Chimica Organica II
 Composti carbonilici Il gruppo carbonilico è formato da un carbonio legato tramite un doppio legame ad un ossigeno. Probabilmente è il gruppo funzionale più importante. Le proprietà del gruppo carbonilico
Composti carbonilici Il gruppo carbonilico è formato da un carbonio legato tramite un doppio legame ad un ossigeno. Probabilmente è il gruppo funzionale più importante. Le proprietà del gruppo carbonilico
Nomi e formule dei principali composti organici
 Il numero davvero sterminato dei e la necessità quindi di doverli distinguere ciascuno con la propria formula e il proprio nome, ha costretto i chimici (attraverso un apposito organismo, la IUPAC) a mettere
Il numero davvero sterminato dei e la necessità quindi di doverli distinguere ciascuno con la propria formula e il proprio nome, ha costretto i chimici (attraverso un apposito organismo, la IUPAC) a mettere
Ammine N R N R R R-NH 2. Gruppo funzionale: NH 2. Gruppo amminico. Ammine terziarie. Ammine primarie. Ammine secondarie
 Ammine Gruppo funzionale: N 2 Gruppo amminico -N 2 Ammine primarie N N Ammine terziarie Ammine secondarie Ammine Nomi comuni Le ammine semplici vengono generalmente designate con nomi comuni, accettati
Ammine Gruppo funzionale: N 2 Gruppo amminico -N 2 Ammine primarie N N Ammine terziarie Ammine secondarie Ammine Nomi comuni Le ammine semplici vengono generalmente designate con nomi comuni, accettati
Corso di orientamento e preparazione ai Corsi di Laurea della Scuola di Medicina ad accesso programmato a.a. 2019/2020 CHIMICA
 Corso di orientamento e preparazione ai Corsi di Laurea della Scuola di Medicina ad accesso programmato a.a. 2019/2020 CHIMICA «Nulla si crea, nulla si distrugge, ma tutto si trasforma.» (Antoine-Laurent
Corso di orientamento e preparazione ai Corsi di Laurea della Scuola di Medicina ad accesso programmato a.a. 2019/2020 CHIMICA «Nulla si crea, nulla si distrugge, ma tutto si trasforma.» (Antoine-Laurent
ETOILEPEDIA IL LEGAME CHIMICO
 IL LEGAME CHIMICO La teoria quantistica ha introdotto il concetto di valenza, cioè della capacità di un atomo di formare un determinato numero di legami a seconda della propria configurazione elettronica;
IL LEGAME CHIMICO La teoria quantistica ha introdotto il concetto di valenza, cioè della capacità di un atomo di formare un determinato numero di legami a seconda della propria configurazione elettronica;
Domanda 1 La reazione di formazione di emiacetali ed acetali è una reazione di:
 Domanda 1 La reazione di formazione di emiacetali ed acetali è una reazione di: 1. riduzione del gruppo carbonilico (-1) 2. sostituzione elettrofila aromatica (-1) 3. eliminazione (-1) 4. addizione al
Domanda 1 La reazione di formazione di emiacetali ed acetali è una reazione di: 1. riduzione del gruppo carbonilico (-1) 2. sostituzione elettrofila aromatica (-1) 3. eliminazione (-1) 4. addizione al
AMMINE R'' H H C 2 H 5 C H C H C H NH 2 H H. azoto. alifatici o aliciclici. ammina primaria ammina secondaria ammina terziaria N CH 3
 AMMIE Si chiamano primarie le ammine che hanno un solo gruppo alchilico o aromatico legato all azoto azoto. Sono secondarie e terziarie le ammine al cui atomo di azoto sono legate, rispettivamente,, due
AMMIE Si chiamano primarie le ammine che hanno un solo gruppo alchilico o aromatico legato all azoto azoto. Sono secondarie e terziarie le ammine al cui atomo di azoto sono legate, rispettivamente,, due
Gruppo carbonilico. Il gruppo carbonilico è caratterizzato dalla presenza C=O ed i composti che lo contengono vengono definiti composti carbonilici.
 Gruppo carbonilico Il gruppo carbonilico è caratterizzato dalla presenza C= ed i composti che lo contengono vengono definiti composti carbonilici. H R R R R H R R aldeidi chetoni acidi carbossilici ac.
Gruppo carbonilico Il gruppo carbonilico è caratterizzato dalla presenza C= ed i composti che lo contengono vengono definiti composti carbonilici. H R R R R H R R aldeidi chetoni acidi carbossilici ac.
Acidi carbossilici e derivati Composti organici che contengono legami doppi C=O e legami singoli C-eteroatomo (oppure il gruppo CN)
 himica rganica Acidi carbossilici e derivati omposti organici che contengono legami doppi = e legami singoli -eteroatomo (oppure il gruppo N) H Acido carbossilico X Alogenuro acilico Anidride ' N Estere
himica rganica Acidi carbossilici e derivati omposti organici che contengono legami doppi = e legami singoli -eteroatomo (oppure il gruppo N) H Acido carbossilico X Alogenuro acilico Anidride ' N Estere
Appunti di Chimica Organica Elementi per CdL Ostetricia CHIMICA ORGANICA. Appunti di Lezione. Elementi per il corso di Laurea In Ostetricia
 Appunti di himica Organica Elementi per dl Ostetricia IMIA ORGANIA Appunti di Lezione Elementi per il corso di Laurea In Ostetricia Autore: Roberto Zanrè A.A. 2009/2010 1 Appunti di himica Organica Elementi
Appunti di himica Organica Elementi per dl Ostetricia IMIA ORGANIA Appunti di Lezione Elementi per il corso di Laurea In Ostetricia Autore: Roberto Zanrè A.A. 2009/2010 1 Appunti di himica Organica Elementi
Lezione 5. Alogenuri, alcoli, fenoli ed eteri
 Lezione 5 Alogenuri, alcoli, fenoli ed eteri 1 I gruppi funzionali Un gruppo funzionale è un atomo o un gruppo di atomi che determina le proprietà chimiche di un composto organico, permettendone la classificazione.
Lezione 5 Alogenuri, alcoli, fenoli ed eteri 1 I gruppi funzionali Un gruppo funzionale è un atomo o un gruppo di atomi che determina le proprietà chimiche di un composto organico, permettendone la classificazione.
Sandro Campestrini Dipartimento di Chimica Organica, Via Marzolo 1
 Sandro Campestrini Dipartimento di Chimica Organica, Via Marzolo 1 E-mail: sandro.campestrini@unipd.it Phone: 049-8275289 http://www.chfi.unipd.it/home/s.campestrini Testo consigliato: FONDAMENTI di CHIMICA
Sandro Campestrini Dipartimento di Chimica Organica, Via Marzolo 1 E-mail: sandro.campestrini@unipd.it Phone: 049-8275289 http://www.chfi.unipd.it/home/s.campestrini Testo consigliato: FONDAMENTI di CHIMICA
Alcoli, eteri, tioli, solfuri
 Alcoli, eteri, tioli, solfuri Alcoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Metanolo Sintesi industriale Tossico per l uomo (
Alcoli, eteri, tioli, solfuri Alcoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Metanolo Sintesi industriale Tossico per l uomo (
Alcoli ed eteri Composti organici che contengono legami singoli C-O
 Alcoli ed eteri Composti organici che contengono legami singoli C-O Chimica Organica CH 3 CH 2 CH 3 CH 2 O CH 2 CH 3 Alcol etilico etanolo Etere etilico dietiletere Fenolo idrossibenzene Nomenclatura degli
Alcoli ed eteri Composti organici che contengono legami singoli C-O Chimica Organica CH 3 CH 2 CH 3 CH 2 O CH 2 CH 3 Alcol etilico etanolo Etere etilico dietiletere Fenolo idrossibenzene Nomenclatura degli
FENOLI: nomenclatura IUPAC
 FENOLI, AMMINE ed ENAMMINE FENOLI: nomenclatura IUPAC I fenoli sono composti la cui caratteristica strutturale è quella di possedere un gruppo idrossile ( OH) legato a un anello benzenico. Il sistema it
FENOLI, AMMINE ed ENAMMINE FENOLI: nomenclatura IUPAC I fenoli sono composti la cui caratteristica strutturale è quella di possedere un gruppo idrossile ( OH) legato a un anello benzenico. Il sistema it
14/11/2018. Aldeidi e chetoni sono composti caratterizzati dalla presenza del gruppo funzionale carbonile.
 Aldeidi e chetoni sono composti caratterizzati dalla presenza del gruppo funzionale carbonile. L atomo di carbonio ibridato sp 2 è legato a un atomo di ossigeno da un doppio legame. L ossigeno è più elettronegativo
Aldeidi e chetoni sono composti caratterizzati dalla presenza del gruppo funzionale carbonile. L atomo di carbonio ibridato sp 2 è legato a un atomo di ossigeno da un doppio legame. L ossigeno è più elettronegativo
23 Le diverse classi di composti organici
 23 Le diverse classi di composti organici 23.1 I gruppi funzionali I gruppi funzionali sono atomi o gruppi di atomi che determinano le proprietà dei composti organici a cui sono legati, facendo assumere
23 Le diverse classi di composti organici 23.1 I gruppi funzionali I gruppi funzionali sono atomi o gruppi di atomi che determinano le proprietà dei composti organici a cui sono legati, facendo assumere
Derivati degli idrocarburi Gruppi funzionali
 Derivati degli idrocarburi Gruppi funzionali La maggior parte delle molecole organiche contiene altri elementi oltre a C e H. L introduzione di un atomo di un elemento diverso come l ossigeno e l azoto
Derivati degli idrocarburi Gruppi funzionali La maggior parte delle molecole organiche contiene altri elementi oltre a C e H. L introduzione di un atomo di un elemento diverso come l ossigeno e l azoto
Composti carbonilici Acidi carbossilici
 Composti carbonilici Acidi carbossilici Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli
Composti carbonilici Acidi carbossilici Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli
La chimica organica. La chimica organica è la chimica dei composti del carbonio.
 La chimica organica La chimica organica è la chimica dei composti del carbonio. Gli Idrocarburi sono composti organici contenenti solo carbonio (C) e idrogeno (H). Ci sono composti organici che contengono
La chimica organica La chimica organica è la chimica dei composti del carbonio. Gli Idrocarburi sono composti organici contenenti solo carbonio (C) e idrogeno (H). Ci sono composti organici che contengono
Idrocarburi. Idrocarburi
 Idrocarburi 1 Molecole costituite solo da atomi di carbonio e idrogeno Idrocarburi alifatici Idrocarburi saturi, solo legami singoli. Idrocarburi aromatici Idrocarburi insaturi, almeno un legame multiplo
Idrocarburi 1 Molecole costituite solo da atomi di carbonio e idrogeno Idrocarburi alifatici Idrocarburi saturi, solo legami singoli. Idrocarburi aromatici Idrocarburi insaturi, almeno un legame multiplo
Aldeidi e chetoni. Struttura e proprietà Nomenclatura e nomi comuni Fonti Reazioni Principali aldeidi e chetoni
 Aldeidi e chetoni Struttura e proprietà Nomenclatura e nomi comuni Fonti Reazioni Principali aldeidi e chetoni Aldeidi e chetoni Aldeidi e chetoni Aldeidi e chetoni Il legame = è costituito da un legame
Aldeidi e chetoni Struttura e proprietà Nomenclatura e nomi comuni Fonti Reazioni Principali aldeidi e chetoni Aldeidi e chetoni Aldeidi e chetoni Aldeidi e chetoni Il legame = è costituito da un legame
ESERCIZI SPETTROMETRIA DI MASSA
 ESERCIZI SPETTROMETRIA DI MASSA A SPUNTI DI RIFLESSIONE 1. In cosa differiscono le tecniche soft da quelle strong? 2. Con quali tecniche si hanno maggiori probabilità di ottenere ioni molecolari? 3. Per
ESERCIZI SPETTROMETRIA DI MASSA A SPUNTI DI RIFLESSIONE 1. In cosa differiscono le tecniche soft da quelle strong? 2. Con quali tecniche si hanno maggiori probabilità di ottenere ioni molecolari? 3. Per
p p s sp sp sp s p p 1
 p p s sp p sp sp p s 1 alcheni 63 kcal/mol alchini 2 nd 54 kcal/mol 2 Come per gli alcheni, gli alchini interni sostituiti sono più stabili di quelli esterni More stable Etino (acetilene) C 2 H 2 +O 2
p p s sp p sp sp p s 1 alcheni 63 kcal/mol alchini 2 nd 54 kcal/mol 2 Come per gli alcheni, gli alchini interni sostituiti sono più stabili di quelli esterni More stable Etino (acetilene) C 2 H 2 +O 2
CHIMICA ORGANICA. PON C1 di SCIENZE. Esperto prof. C. Formica
 CHIMICA ORGANICA PON C1 di SCIENZE Esperto prof. C. Formica Immagini e testi tratti dai website di: genome.wellcome.ac.uk, dnaftb.org, unipv.it, unimi.it, wikipedia.it, unibs.it, unisi.it, unina.it, uniroma2.it,
CHIMICA ORGANICA PON C1 di SCIENZE Esperto prof. C. Formica Immagini e testi tratti dai website di: genome.wellcome.ac.uk, dnaftb.org, unipv.it, unimi.it, wikipedia.it, unibs.it, unisi.it, unina.it, uniroma2.it,
Una reazione chimica può avvenire in uno o più stadi; l insieme degli stadi costituisce il MECCANISMO DI REAZIONE.
 Una reazione chimica può avvenire in uno o più stadi; l insieme degli stadi costituisce il MECCANISMO DI REAZIONE. Ogni passaggio del meccanismo è costituito da reagenti e prodotti e deve essere bilanciato
Una reazione chimica può avvenire in uno o più stadi; l insieme degli stadi costituisce il MECCANISMO DI REAZIONE. Ogni passaggio del meccanismo è costituito da reagenti e prodotti e deve essere bilanciato
LA CHIMICA ORGANICA IBRIDAZIONE
 LA CHIMICA ORGANICA Detta anche LA CHIMICA DEL CARBONIO (C) perché Il C gioca un ruolo fondamentale in tutte le molecole organiche (cioè appartenenti o derivanti da esseri viventi). Possiamo spiegarlo
LA CHIMICA ORGANICA Detta anche LA CHIMICA DEL CARBONIO (C) perché Il C gioca un ruolo fondamentale in tutte le molecole organiche (cioè appartenenti o derivanti da esseri viventi). Possiamo spiegarlo
Forze intermolecolari
 Forze intermolecolari Sono le forze che si instaurano tra le molecole di un composto e ne determinano lo stato di aggregazione (gas, liquido, solido) interazioni dipolo-dipolo attrazioni di van der Waals
Forze intermolecolari Sono le forze che si instaurano tra le molecole di un composto e ne determinano lo stato di aggregazione (gas, liquido, solido) interazioni dipolo-dipolo attrazioni di van der Waals
Acidi carbossilici. Francesca Anna Scaramuzzo, PhD
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Acidi carbossilici Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Acidi carbossilici Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate
C Ca Ce Cf Co Cr Cs Cu
 Elementi Composti ionici (forze elettrostatiche, edifici ionici) molecolari (ripetersi periodico di molecole) Simboli C Ca Ce Cf Co Cr Cs Cu Formule Indici H 2 SO 4 CO 2 H 2 O N 2 Na 2 CO 3 O 2 Mg(NO 3
Elementi Composti ionici (forze elettrostatiche, edifici ionici) molecolari (ripetersi periodico di molecole) Simboli C Ca Ce Cf Co Cr Cs Cu Formule Indici H 2 SO 4 CO 2 H 2 O N 2 Na 2 CO 3 O 2 Mg(NO 3
DERIVATI DEGLI ACIDI CARBOSSILICI gruppo acile
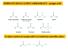 DERIVATI DEGLI ACIDI CARBOSSILICI gruppo acile Acido carbossilico, Alogenuro acilico, Anidride, Estere, Ammide, Tioestere, Fosfato acilico La tipica reazione dei gruppi acilici è la sostituzione nucleofila
DERIVATI DEGLI ACIDI CARBOSSILICI gruppo acile Acido carbossilico, Alogenuro acilico, Anidride, Estere, Ammide, Tioestere, Fosfato acilico La tipica reazione dei gruppi acilici è la sostituzione nucleofila
Alcoli, eteri, tioli, solfuri
 Alcoli, eteri, tioli, solfuri Alcoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Metanolo Sintesi industriale Tossico per l uomo (
Alcoli, eteri, tioli, solfuri Alcoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Metanolo Sintesi industriale Tossico per l uomo (
Idrocarburi Al A ifatici Ar A oma m tici
 GLI IDROCARBURI Gli idrocarburi sono i più semplici composti del carbonio con l'idrogeno. Sono le molecole di base della chimica organica poiché, oltre ad essere molto numerosi, tutti gli altri composti
GLI IDROCARBURI Gli idrocarburi sono i più semplici composti del carbonio con l'idrogeno. Sono le molecole di base della chimica organica poiché, oltre ad essere molto numerosi, tutti gli altri composti
Gruppi funzionali. aldeidi
 Gruppi funzionali alcoli aldeidi chetoni Acidi carbossilici ' eteri ' esteri fenoli In grassetto il gruppo funzionale che definisce il carattere del composto 1 2 Gruppi funzionali: arrangiamento di pochi
Gruppi funzionali alcoli aldeidi chetoni Acidi carbossilici ' eteri ' esteri fenoli In grassetto il gruppo funzionale che definisce il carattere del composto 1 2 Gruppi funzionali: arrangiamento di pochi
Acidi carbossilici: nomenclatura. alcano -> acido alcanoico
 Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli alcoli (OH) Si trovano generalmente come
Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli alcoli (OH) Si trovano generalmente come
Si trovano generalmente come dimeri ciclici a causa dei legami a idrogeno
 Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli alcoli (OH) Si trovano generalmente come
Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli alcoli (OH) Si trovano generalmente come
PERCHE STUDIARE LA CHIMICA ORGANICA?
 CIMICA ORGANICA CE COSA E LA CIMICA ORGANICA? La chimica organica è dedicata alla descrizione della struttura, delle proprietà e delle funzioni dei composti del carbonio (C). PERCE STUDIARE LA CIMICA ORGANICA?
CIMICA ORGANICA CE COSA E LA CIMICA ORGANICA? La chimica organica è dedicata alla descrizione della struttura, delle proprietà e delle funzioni dei composti del carbonio (C). PERCE STUDIARE LA CIMICA ORGANICA?
Unità Didattica 10. I composti carbonilici. Struttura, nomenclatura e reattività
 I composti caratterizzati dal gruppo carbonilico sono le aldeidi ed i chetoni Il gruppo funzionale è il doppio legame C=O Il carbonile ha geometria planare (il carbonio è sp 2 ) Unità Didattica 10 I composti
I composti caratterizzati dal gruppo carbonilico sono le aldeidi ed i chetoni Il gruppo funzionale è il doppio legame C=O Il carbonile ha geometria planare (il carbonio è sp 2 ) Unità Didattica 10 I composti
Capitolo 24 Le famiglie dei composti organici
 Capitolo 24 Le famiglie dei composti organici DOMANDE ED ESERCIZI (versione integrale) 24.1 I composti organici sono raggruppati in famiglie 1. Che cosa si intende per gruppo funzionale? Scrivi le formule
Capitolo 24 Le famiglie dei composti organici DOMANDE ED ESERCIZI (versione integrale) 24.1 I composti organici sono raggruppati in famiglie 1. Che cosa si intende per gruppo funzionale? Scrivi le formule
Valitutti, Taddei, Kreuzer, Massey, Sadava, Hills, Heller, Berenbaum. Dal carbonio agli OGM PLUS Chimica organica, biochimica e biotecnologie
 Dal carbonio agli OGM PLUS Chimica organica, biochimica e biotecnologie VERSO L UNIVERSITÀ Le domande sono tratte dalle prove di ammissione emesse annualmente dal Ministero dell Istruzione, dell Università
Dal carbonio agli OGM PLUS Chimica organica, biochimica e biotecnologie VERSO L UNIVERSITÀ Le domande sono tratte dalle prove di ammissione emesse annualmente dal Ministero dell Istruzione, dell Università
Soluzioni degli esercizi di fine capitolo
 SLUZINI DEGLI ESERIZI DI FINE APITL Soluzioni degli esercizi di fine capitolo David Sadava, David M. illis,. raig eller, May R. Berenbaum, Alfonso 1 Soluzioni degli esercizi per capitolo himica organica:
SLUZINI DEGLI ESERIZI DI FINE APITL Soluzioni degli esercizi di fine capitolo David Sadava, David M. illis,. raig eller, May R. Berenbaum, Alfonso 1 Soluzioni degli esercizi per capitolo himica organica:
Pronti per l Università Liceo Scientifico de Caprariis Atripalda PON F
 Pronti per l Università Liceo Scientifico de Caprariis Atripalda PON F2 2011-14 La chimica del carbonio Il Carbonio Copyright 2008 PresentationFx.com Redistribution Prohibited Image 2008 clix@sxc.hu This
Pronti per l Università Liceo Scientifico de Caprariis Atripalda PON F2 2011-14 La chimica del carbonio Il Carbonio Copyright 2008 PresentationFx.com Redistribution Prohibited Image 2008 clix@sxc.hu This
Ricerca di sottostruttura
 Ricerca di sottostruttura In genere, più che alla ricerca di una molecola esatta, si è interessati alla ricerca di tutti i composti nel database aventi una particolare caratteristica In tale ambito, il
Ricerca di sottostruttura In genere, più che alla ricerca di una molecola esatta, si è interessati alla ricerca di tutti i composti nel database aventi una particolare caratteristica In tale ambito, il
M i n i s t e r o d e l l I s t r u z i o n e, d e l l U n i v e r s i t à e d e l l a R i c e r c a
 PROGRAMMA SVOLTO DOCENTE: Campani Maria Varini Simone A.S: 2018/2019 DISCIPLINA: Chimica organica e biochimica CLASSE: 3^A CHI MAT Per ogni Tema svolto vengono indicati i relativi contenuti. LEGAME CHIMICO
PROGRAMMA SVOLTO DOCENTE: Campani Maria Varini Simone A.S: 2018/2019 DISCIPLINA: Chimica organica e biochimica CLASSE: 3^A CHI MAT Per ogni Tema svolto vengono indicati i relativi contenuti. LEGAME CHIMICO
Alcoli e Tioli. Francesca Anna Scaramuzzo, PhD
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alcoli e Tioli Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alcoli e Tioli Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate
PROGRAMMAZIONE DI SCIENZE INTEGRATE. Materia: Scienze Integrate - Chimica. Classe Seconda D ENO. Anno scolastico Prof.
 PROGRAMMAZIONE DI SCIENZE INTEGRATE Materia: Scienze Integrate - Chimica Classe Seconda D ENO Anno scolastico 2018-2019 Prof. Oberdan Cosimi Libri di testo: Masterchimica. Con e-book e espansione online.
PROGRAMMAZIONE DI SCIENZE INTEGRATE Materia: Scienze Integrate - Chimica Classe Seconda D ENO Anno scolastico 2018-2019 Prof. Oberdan Cosimi Libri di testo: Masterchimica. Con e-book e espansione online.
Domanda 4 Dal punto di vista della reattività, il doppio legame si comporta spesso da:
 Tema svolto Domanda 1 Al punto isoelettrico la solubilità di una amminoacido in acqua è: 1. intermedia (-1) 2. doppia rispetto ad un ph più acido e dimezzata rispetto ad un ph più basico (-1) 3. la più
Tema svolto Domanda 1 Al punto isoelettrico la solubilità di una amminoacido in acqua è: 1. intermedia (-1) 2. doppia rispetto ad un ph più acido e dimezzata rispetto ad un ph più basico (-1) 3. la più
C, H, O, N, P, S Primo composto organico sintetizzato (1928) UREA. Fe, Co, Mg, Zn, Cu, Mn. Applicazioni della Chimica Organica
 IMIA DEL ARBONIO Gli organismi viventi (animali e vegetali) pur nella loro immensa varietà morfologica presentano sempre gli stessi elementi. Tali elementi sono fondamentali per la costruzione di biomolecole
IMIA DEL ARBONIO Gli organismi viventi (animali e vegetali) pur nella loro immensa varietà morfologica presentano sempre gli stessi elementi. Tali elementi sono fondamentali per la costruzione di biomolecole
chiamato i questo modo a causa della presenza del gruppo carbonilico e del gruppo idrossilico. C sp 2 ibrido di risonanza del gruppo carbossilico
 ACIDI CARBOSSILICI ACIDI CARBOSSILICI Gli acidi carbossilici isono caratterizzati idll dalla presenza dl del gruppo carbossilico, chiamato i questo modo a causa della presenza del gruppo carbonilico e
ACIDI CARBOSSILICI ACIDI CARBOSSILICI Gli acidi carbossilici isono caratterizzati idll dalla presenza dl del gruppo carbossilico, chiamato i questo modo a causa della presenza del gruppo carbonilico e
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH
 Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( OO) nella stessa molecola 3 N 2 α * OO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-himica Organica 1 Amminoacidi
Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( OO) nella stessa molecola 3 N 2 α * OO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-himica Organica 1 Amminoacidi
Aldeidi e chetoni. 1) Rottura α 2) Rottura i. Più pronunciate nei chetoni. 3) Rottura β con trasposizione di H in γ (McLafferty)
 Aldeidi e chetoni Hanno potenziale di ionizzazione inferiore a quello degli alcooli dunque lo ione molecolare è più intenso e più facilmente osservabile anche in aldeidi e chetoni superiori. 1) Rottura
Aldeidi e chetoni Hanno potenziale di ionizzazione inferiore a quello degli alcooli dunque lo ione molecolare è più intenso e più facilmente osservabile anche in aldeidi e chetoni superiori. 1) Rottura
Alla attenzione di Busnelli Vera Compiti da svolgere nel periodo estivo per la disciplina CHIMICA. I compiti allegati andranno consegnati a settembre
 Alla attenzione di Busnelli Vera Compiti da svolgere nel periodo estivo per la disciplina CHIMICA. I compiti allegati andranno consegnati a settembre alla prof.savoia Che provvederà alla correzione con
Alla attenzione di Busnelli Vera Compiti da svolgere nel periodo estivo per la disciplina CHIMICA. I compiti allegati andranno consegnati a settembre alla prof.savoia Che provvederà alla correzione con
Addizioni nucleofile. Addizioni a C=O
 Addizioni nucleofile Addizioni a C= Substrato Un composto che possiede un atomo di carbonio elettron-deficiente legato con un legame π (che si possa rompere facilmente) ad un atomo più elettronegativo
Addizioni nucleofile Addizioni a C= Substrato Un composto che possiede un atomo di carbonio elettron-deficiente legato con un legame π (che si possa rompere facilmente) ad un atomo più elettronegativo
Acidi carbossilici. IUPAC catena più lunga contenente il gruppo -COOH al quale si dà il nome dell'alcano in cui la desinenza -o è sostituita con -oico
 Acidi carbossilici caratterizzati dal gruppo carbossilico - R alifatici Ar aromatici IUPA catena più lunga contenente il gruppo - al quale si dà il nome dell'alcano in cui la desinenza -o è sostituita
Acidi carbossilici caratterizzati dal gruppo carbossilico - R alifatici Ar aromatici IUPA catena più lunga contenente il gruppo - al quale si dà il nome dell'alcano in cui la desinenza -o è sostituita
Aldeidi e Chetoni. Francesca Anna Scaramuzzo, PhD
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Aldeidi e Chetoni Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Aldeidi e Chetoni Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate
RELAZIONE FINALE DEL DOCENTE Anno Scolastico 2016/17
 ALLEGATO A Classe V CT RELAZIONE FINALE DEL DOCENTE Anno Scolastico 2016/17 Docente Paganelli Mariangela Materia Scienze Naturali Testo in uso Marinella De Leo, Filippo Giachi Biochimica PLUS. Dalla chimica
ALLEGATO A Classe V CT RELAZIONE FINALE DEL DOCENTE Anno Scolastico 2016/17 Docente Paganelli Mariangela Materia Scienze Naturali Testo in uso Marinella De Leo, Filippo Giachi Biochimica PLUS. Dalla chimica
