LE SOLUZIONI 07/04/2019
|
|
|
- Pio Gianmaria Pugliese
- 5 anni fa
- Visualizzazioni
Transcript
1 LE SOLUZIONI Le sostanze tendono spontaneamente a miscelarsi tra loro; tale fenomeno si deve, soprattutto, all agitazione termica delle particelle che le porta a disperdersi disordinatamente. Si definisce soluzione un sistema fisicamente omogeneo e chimicamente eterogeneo. In una soluzione il componente presente in quantità maggiore viene detto solvente, gli altri componenti sono chiamati soluti. Il solvente e il soluto (o i soluti) sono intimamente mescolati e non più distinguibili tra loro. Non tutte le sostanze si sciolgono in qualunque tipo di solvente. Si dice solubile ciò che riesce a sciogliersi in un determinato solvente, insolubile ciò che non si scioglie. Il processo di mescolamento richiede che le particelle delle sostanze si separino le une dalle altre e, quasi sempre, ciò comporta la rottura di legami. Affinché si formi una soluzione è quindi necessario che si rompano i legami tra le particelle di soluto e quelli tra le particelle di solvente, al loro posto si formeranno nuovi legami tra soluto e solvente. 1
2 Per comprendere i meccanismi che portano alla formazione di una soluzione, osserviamo il mescolamento di due gas dove i legami tra particelle sono praticamente assenti. Immaginiamo di avere un recipiente che contiene due gas separati da un setto mobile. Sollevando il setto, il mescolamento dei gas avviene spontaneamente, causato del movimento delle molecole. Una volta che i gas hanno formato una miscela omogenea non si separano più spontaneamente. Questo perché la rimozione del setto rende lo stato iniziale, ordinato, molto improbabile ed un sistema tende spontaneamente verso lo stato più probabile (più disordinato). Ciò vale anche per i liquidi ed i solidi, ma in essi il mescolamento non è solo questione di ordine e disordine: vi è anche una componente energetica. Qui, infatti, i legami tra le particelle non possono essere trascurati. La rottura di legami richiede energia, mentre la loro formazione libera energia. Poiché ogni sistema tende sempre a raggiungere lo stato di minor energia possibile, il ΔE (E finale E iniziale ) dev essere negativo. Ne consegue che la natura dei legami di partenza e di quelli interazioni che si formano sono importanti. 2
3 Ecco perché tutti i gas sono miscibili tra loro ma non tutti i liquidi e i solidi lo sono! Sostanze polari (o non polari) si mescolano solo con sostanze polari (o non polari) Sostanze polari e non polari non si mescolano mai tra loro. Similia similibus solvuntur, dicevano già gli antichi alchimisti. Vediamo allora il processo di miscelamento tra sostanze non gassose. Esso si compone di due fasi: la dissociazione e la solvatazione. Per dissociazione si intende il meccanismo attraverso il quale le particelle di solido vengono smontate dalla loro struttura cristallina e disperse nella soluzione. Per solvatazione (idratazione nel caso specifico dell acqua), si intende il meccanismo per il quale le particelle di soluto sono impedite ad aggregarsi di nuovo tra loro per ricostituire il solido di partenza. La solubilizzazione avviene a causa dell agitazione delle particelle di solvente. Nel loro disordinato movimento queste urtano le particelle del soluto, spezzano i legami che le tengono unite e le allontanano le une dalle altre. Quando un solido si scioglie, per esempio, non diventa un liquido, ma le sue particelle perdono la loro regolare disposizione e si mescolano intimamente con le molecole di solvente. 3
4 Tutti i composti che in soluzione acquosa formano ioni per dissociazione sono chiamati elettroliti. Le soluzioni di elettroliti conducono la corrente elettrica. Tutti i solidi ionici liberano un gran numero di ioni e formano soluzioni ad elevata conducibilità elettrica; sono per questo chiamati elettroliti forti. Anche alcuni composti polari non ionici, come l acido cloridrico, sono elettroliti forti. La maggior parte di loro, però, si ionizza solo in parte e il numero di ioni in soluzione è, quindi, modesto. Soluti di questo tipo sono chiamati elettroliti deboli. Le soluzioni in cui il soluto forma particelle elettricamente neutre, come lo zucchero o l alcol, non conducono la corrente elettrica. I composti di questo tipo sono chiamati non elettroliti. Una volte che le particelle di soluto si sono disperse, vengono circondate da particelle di solvente che le tengono reciprocamente distanti, impedendo loro di avvicinarsi in maniera sufficiente a riformare i legami che le tenevano unite. La solvatazione pone un limite alla quantità di soluto che è possibile far disciogliere: dipende dalla capacità del solvente a solvatare le particelle di soluto. Si definisce solubilità: la massima quantità di soluto che, ad una data temperatura, si scioglie in 100 grammi di solvente. La solubilità si esprime in percentuale. Per esempio, dire che il sale è solubile al 35% in acqua significa dire che, ad una data temperatura, in 100 g di acqua possono essere disciolti al massimo 35 g di sale. 4
5 Una soluzione che contiene disciolta la massima quantità di soluto viene detta satura, altrimenti si dice insatura. Se ad una soluzione satura si prova ad aggiungere altro soluto, esso rimane indisciolto e tende a depositarsi sul fondo. La solubilità, quindi, si riferisce sempre ad una soluzione satura. Nelle soluzioni sature tra il soluto disciolto e quello indisciolto si instaura un equilibrio dinamico. È importante specificare la temperatura perché essa influisce sulla solubilità: per la stragrande maggioranze dei soluti non gassosi la solubilità è direttamente proporzionale alla temperatura. Se si scalda una soluzione satura questa diventa insatura ed allora vi si potrà sciogliere ancora un altro po di soluto. Al contrario, se si raffredda una soluzione insatura è possibile che divenga satura e parte del soluto possa depositarsi. Se si raffredda una soluzione satura è possibile che il soluto continui a rimanere disciolto, in questa caso la soluzione viene detta sovrassatura. 5
6 La solubilità dei soluti gassosi diminuisce con l aumentare della temperatura. Per esempio, a 20 C l ossigeno ha una solubilità di circa 10 mg per litro di acqua, mentre a 0 C la sua solubilità è quasi doppia. Per mantenere il gas in soluzione, devono instaurarsi legami tra le particelle del solvente e quelle del soluto. Se la temperatura aumenta cresce il movimento delle particelle e questi legami si indeboliscono: le molecole del gas tenderanno così a sfuggire dal solvente. Per i gas, inoltre, la solubilità dipende anche dalla pressione. Ciò accade perché se si aumenta la pressione più molecole di gas sono costrette a passare dalla fase gassosa a quella liquida. Il contrario avviene se la pressione diminuisce. Nel caso di gas che non reagiscono con il solvente, esiste una semplice relazione fra pressione e solubilità, la legge di Henry: A una data temperatura, la concentrazione di un gas in un liquido è direttamente proporzionale alla pressione parziale del gas. La concentrazione di una soluzione è il rapporto tra la quantità di soluto e la quantità di solvente in cui il soluto è disciolto. È possibile esprimere questo rapporto con diverse grandezze. Quelle più usate sono: 1. Percentuale in massa 2. Percentuale in volume 3. Percentuale massa/volume 4. Molarità 5. Molalità 6. Frazione molare 6
7 La concentrazione percentuale in massa (% m/m) indica la quantità in grammi di soluto sciolta in 100 grammi di soluzione. La concentrazione percentuale in volume % V/V) indica il volume in millilitri di soluto in 100 ml di soluzione. La concentrazione percentuale massa su volume (% m/v) indica la quantità in grammi di soluto in 100 ml di soluzione. La concentrazione molare (M) o molarità indica il rapporto fra le moli di soluto e il volume in litri della soluzione. La molarità è particolarmente utile perché ci permette di ricavare il numero di moli di soluto dal volume di soluzione. Per esempio, se abbiamo a disposizione una soluzione 0,1 M e ci servono 0,01 mol di soluto, dovremo semplicemente misurare 100 ml di soluzione. Tutte le volte che un problema richiede calcoli sulla quantità di una certa sostanza e su un volume di soluzione della stessa, il collegamento è dato dalla molarità. Dalla formula si ottengono infatti le seguenti formule inverse: 7
8 La concentrazione molale (m) o molalità è il rapporto tra le moli di soluto e la massa del solvente espressa in kilogrammi. Alcune importanti proprietà fisiche delle soluzioni sono correlate in modo semplice alla loro molalità. Inoltre la molalità di una soluzione non cambia con la temperatura (variando la temperatura cambia infatti il volume ma non la massa). La frazione molare (X) di un componente di una soluzione è il rapporto fra il numero di moli di quel componente e il numero totale delle moli di tutti i componenti. La frazione molare è adimensionale, cioè non ha unità di misura. Nelle miscele di gas si può calcolare la frazione molare dalle pressioni parziali applicando la legge dei gas ideali: In base alla legge di Dalton il denominatore è uguale alla pressione totale della miscela, quindi l equazione si riduce a: Le soluzioni si classificano in tre grandi gruppi a seconda dello stato fisico del solvente: 1. Soluzioni solide 2. Soluzioni liquide 3. Soluzioni gassose Lo stato fisico del soluto non ha importanza perché viene perso nel processo di dissociazione. Normalmente, però, le soluzioni solide si fanno con soluti solidi e quelle gassose con soluti gassosi. 8
9 solide solido + solido leghe soluzioni liquide liquido + gas liquido + solido soluzioni propriamente dette liquido + liquido miscele gassose gas + gas Sono quelle in cui il solvente è solido ed anche i soluti in partenza sono solidi. Poiché i solidi sono costituiti da particelle che non si muovono le une rispetto alle altre, perché si formi una soluzione occorre fonderli e poi lasciarli raffreddare lentamente. Non tutte le combinazioni di solidi possono formare soluzioni. Esempi di soluzioni solide sono le leghe metalliche come l ottone (rame e zinco), il bronzo (rame e stagno), l acciaio o la ghisa (entrambi costituiti da ferro e carbonio). Sono soluzioni solide anche molte pietre preziose: il rubino, per esempio, è una soluzione di ossido di cromo (Cr 2 O 3 ) in corindone (Al 2 O 3 ). Sono le più diffuse, costituite da un solvente liquido in cui sono disciolti uno o più soluti partendo da qualunque stato di aggregazione. Le soluzioni liquide con soluti liquidi prendono il nome di miscele liquide. Quando si parla in generale di soluzioni si intendono le soluzioni liquide (con l esclusione delle miscele liquide). 9
10 Sono quelle costituite da due o più gas. Tutti i gas sono miscibili tra loro, quindi formano sempre una soluzione. Le soluzioni aeriformi vengono chiamate miscele gassose. Un esempio di soluzione aeriforme è l aria. Si definisce miscela un miscuglio omogeneo di due o più gas (miscele gassose) o di due o più liquidi tra loro (miscele liquide). Le miscele sono separate dalle soluzioni perché in esse non ha senso parlare di solvente o di soluti: i loro componenti, se miscibili, lo sono in qualsiasi rapporto quantitativo. Tutti i gas sono miscibili tra loro e il processo di rimescolamento è rapidissimo in quanto le molecole sono già libere di muoversi e non c è bisogno di rompere alcun legame. Per le miscele gassose vale la legge di Dalton: la pressione esercitata da una miscela gassosa è uguale alla somma delle pressioni parziali dei singoli gas che la costituiscono Per pressione parziale si intende la pressione che il singolo gas eserciterebbe se occupasse da solo l intero volume della miscela. 10
11 Al contrario di quel che accade nei gas, non tutti i liquidi sono miscibili tra loro. Sono miscibili due liquidi polari e due liquidi apolari tra loro, ma se proviamo a mescolare un liquido polare con uno apolare non si riesce ad ottenere una miscela omogenea. Si chiamano così le proprietà che emergono quando si forma una soluzione e che dipendono soltanto dal numero di particelle di soluto presenti in soluzione e non dalla loro natura. Le principali proprietà colligative sono: 1. la diminuzione della pressione di vapore 2. l abbassamento crioscopico 3. l innalzamento ebullioscopico 4. l osmosi La tensione di vapore di un liquido è la pressione che esercita il vapore in equilibrio con il liquido in un contenitore chiuso a temperatura costante. All equilibrio, la tendenza del liquido a vaporizzare compensa esattamente la tendenza del vapore a condensare. La tensione di vapore di un liquido aumenta all aumentare della temperatura. La tensione di vapore di una soluzione il cui soluto non è volatile è sempre minore di quella del solvente puro. 11
12 Ciò è dovuto al fatto che le particelle del soluto trattengono quelle del solvente impedendogli di passare nella fase di vapore. In questo modo l equilibrio tra il liquido e il vapore si raggiunge a valori più bassi di pressione di vapore. La diminuzione è direttamente proporzionale alla frazione molare del solvente secondo la legge di Raoult: P soluzione = P solvente X solvente La frazione molare che compare nella legge di Raoult si riferisce al solvente e non al soluto. In realtà, l interesse è volto a conoscere l effetto sulla pressione di vapore della frazione molare del soluto (X soluto ). ma X solvente = 1 X soluto da cui P soluzione = P solvente (1 X soluto ) e quindi riarrangiando e ponendo si ha P soluzione = P solvente P solvente X soluto P solvente P soluzione = P solvente X soluto P solvente P soluzione = ΔP ΔP = P solvente X soluto Il punto di congelamento di una soluzione è sempre minore di quello del solvente puro. Questo perché le particelle di soluto impediscono a quelle del solvente di organizzarsi in cristalli. È il motivo per cui d inverno si sparge il sale sulle strade. La diminuzione di temperatura è direttamente proporzionale alla molalità della soluzione: Δt c = k c m i 12
13 Il punto di ebollizione di una soluzione è sempre maggiore di quello del solvente puro. Questo perché, come si è visto a proposito della pressione di vapore, le particelle di soluto impediscono a quelle del solvente di evaporare. L aumento di temperatura è direttamente proporzionale alla molalità della soluzione: Δt e = k e m i Sia per la crioscopia che per l ebullioscopia, in presenza di elettroliti che per ogni mole liberano più di una mole di particelle, si deve introdurre il coefficiente i che indica le moli totali di ioni liberati da una mole di soluto. L osmosi è il flusso di un solvente che attraversa una membrana semipermeabile per raggiungere una soluzione più concentrata. Una membrana si dice semipermeabile quando può essere attraversata dal solvente ma non dal soluto. L osmosi è quindi il movimento del solvente dalla soluzione più diluita a quella più concentrata. Il fenomeno si può dimostrare attraverso un tubo a U nei cui bracci vi sono due soluzioni a diversa concentrazione separate da una membrana semipermeabile. Le molecole di solvente si muovono attraverso la membrana, ma nella soluzione più diluita (ipotonica) esse sono in maggior numero rispetto alla soluzione più concentrata (ipertonica). Di conseguenza, il flusso del solvente che entra nella soluzione concentrata è maggiore del flusso che ne esce. Ciò determina una variazione dei volumi. 13
14 Il peso della colonna liquida, risultante dalla differenza tra i volumi delle due soluzioni, esercita una pressione idrostatica che ad un certo punto blocca l osmosi impedendo l ulteriore passaggio di solvente. Questa pressione annulla il flusso osmotico e viene quindi chiamata pressione osmotica, indicata con il simbolo π. In altre parole, la pressione osmotica è la pressione che deve essere esercitata sulla soluzione ipertonica per impedire il flusso osmotico. Il termine «pressione» in questo contesto ha un significato particolare: al di fuori dell osmosi, la soluzione non ha una pressione osmotica; è la soluzione che, in virtù di una sua concentrazione può, in particolari condizioni, determinare l osmosi e la conseguente pressione osmotica. La pressione osmotica è proporzionale alla concentrazione delle particelle di soluto nella soluzione ipotonica. Si può dimostrare che la pressione osmotica è proporzionale sia alla temperatura assoluta che alla molarità. Per soluzioni molto diluite, la costante di proporzionalità è la costante dei gas. Si ottiene così l equazione di van t Hoff: = M R T i 14
Capitolo 14 Le proprietà delle soluzioni
 Capitolo 14 Le proprietà delle soluzioni 1. Perché le sostanze si sciolgono 2. Soluzioni acquose ed elettroliti 3. La concentrazione delle soluzioni 4. L effetto del soluto sul solvente: le proprietà colligative
Capitolo 14 Le proprietà delle soluzioni 1. Perché le sostanze si sciolgono 2. Soluzioni acquose ed elettroliti 3. La concentrazione delle soluzioni 4. L effetto del soluto sul solvente: le proprietà colligative
1. Perché le sostanze si sciolgono?
 1. Perché le sostanze si sciolgono? Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore quantità. Il soluto è il
1. Perché le sostanze si sciolgono? Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore quantità. Il soluto è il
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 17 Le proprietà delle soluzioni 3 Sommario (I) 1. Perché le sostanze si sciolgono? 2. Soluzioni acquose ed elettroliti 3. La
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 17 Le proprietà delle soluzioni 3 Sommario (I) 1. Perché le sostanze si sciolgono? 2. Soluzioni acquose ed elettroliti 3. La
1. Perché le sostanze si sciolgono 2. Soluzioni acquose ed elettroliti 3. La concentrazione delle soluzioni 4. L effetto del soluto sul solvente: le
 Unità n 14 Le proprietà delle soluzioni 1. Perché le sostanze si sciolgono 2. Soluzioni acquose ed elettroliti 3. La concentrazione delle soluzioni 4. L effetto del soluto sul solvente: le proprietà colligative
Unità n 14 Le proprietà delle soluzioni 1. Perché le sostanze si sciolgono 2. Soluzioni acquose ed elettroliti 3. La concentrazione delle soluzioni 4. L effetto del soluto sul solvente: le proprietà colligative
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 13 Le proprietà delle soluzioni 1. Perchè le sostanze si sciolgono? 2. La solubilità 3. La concentrazione
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 13 Le proprietà delle soluzioni 1. Perchè le sostanze si sciolgono? 2. La solubilità 3. La concentrazione
Le soluzioni. possono essere. solide (leghe) liquide aeriformi
 Le soluzioni Sono miscele omogenee di due o più sostanze (in forma di molecole, atomi, ioni) di cui quella presente in quantità maggiore è definita solvente, le altre soluti. possono essere solide (leghe)
Le soluzioni Sono miscele omogenee di due o più sostanze (in forma di molecole, atomi, ioni) di cui quella presente in quantità maggiore è definita solvente, le altre soluti. possono essere solide (leghe)
Una miscela ha composizione variabile. Se le proprietà di una miscela nonsono uniformi (fasi diverse), la miscela è eterogenea.
 Le Miscele Una miscela ha composizione variabile. Se le proprietà di una miscela nonsono uniformi (fasi diverse), la miscela è eterogenea. Se le proprietà sono uniformi, la miscela è una miscela omogenea
Le Miscele Una miscela ha composizione variabile. Se le proprietà di una miscela nonsono uniformi (fasi diverse), la miscela è eterogenea. Se le proprietà sono uniformi, la miscela è una miscela omogenea
Soluzioni e miscugli eterogenei. Soluzioni e miscugli eterogenei. Soluzioni e miscugli eterogenei
 Le soluzioni Soluzioni e miscugli eterogenei Un sistema formato da due o più componenti è chiamato miscuglio. I miscugli possono essere : miscugli eterogenei; miscugli omogenei o soluzioni. 2 4 Soluzioni
Le soluzioni Soluzioni e miscugli eterogenei Un sistema formato da due o più componenti è chiamato miscuglio. I miscugli possono essere : miscugli eterogenei; miscugli omogenei o soluzioni. 2 4 Soluzioni
LE PROPRIETÀ DELLE SOLUZIONI
 LE PROPRIETÀ DELLE SOLUZIONI Le Soluzioni o Miscugli omogenei Solvente e soluto Energia sprigionata e acquisita Solvatazione e idratazione Le Soluzioni 3) 1. Composti Ionici (Dissociazione) 2. Composti
LE PROPRIETÀ DELLE SOLUZIONI Le Soluzioni o Miscugli omogenei Solvente e soluto Energia sprigionata e acquisita Solvatazione e idratazione Le Soluzioni 3) 1. Composti Ionici (Dissociazione) 2. Composti
STATO LIQUIDO. Volume proprio Forma non definita Particelle moderatamente ordinate Energia cinetica delle particelle è dello stesso
 STATO LIQUIDO Caratteristiche: Volume proprio Forma non definita Particelle moderatamente ordinate Energia cinetica delle particelle è dello stesso intermolecolare I legami intermolecolari sono responsabili
STATO LIQUIDO Caratteristiche: Volume proprio Forma non definita Particelle moderatamente ordinate Energia cinetica delle particelle è dello stesso intermolecolare I legami intermolecolari sono responsabili
Le soluzioni e la loro concentrazione
 Le soluzioni e la loro concentrazione Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore quantità. Il soluto è il
Le soluzioni e la loro concentrazione Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore quantità. Il soluto è il
SOLUZIONI E CONCENTRAZIONE
 SOLUZIONI E CONCENTRAZIONE Miscela omogenea di due o più sostanze: solvente (presente in maggiore quantità) + soluto In genere il solvente è liquido (es.acqua) mentre il soluto può essere solido, liquido,
SOLUZIONI E CONCENTRAZIONE Miscela omogenea di due o più sostanze: solvente (presente in maggiore quantità) + soluto In genere il solvente è liquido (es.acqua) mentre il soluto può essere solido, liquido,
Esercizi Concentrazioni e diluizioni
 Esercizi Concentrazioni e diluizioni Una soluzione 0.300 m di acido fosforico ha densità 1.010 g/ml. Calcolare la frazione molare, la percentuale in peso, la molarità. Molalità 0.300 m 0.300 moli di acido
Esercizi Concentrazioni e diluizioni Una soluzione 0.300 m di acido fosforico ha densità 1.010 g/ml. Calcolare la frazione molare, la percentuale in peso, la molarità. Molalità 0.300 m 0.300 moli di acido
Proprietà colligative
 Proprietà colligative Le proprietà che dipendono dalla proporzione tra le molecole del soluto e quelle del solvente ma non dall identità chimica del soluto si dicono proprietà colligative. Le proprietà
Proprietà colligative Le proprietà che dipendono dalla proporzione tra le molecole del soluto e quelle del solvente ma non dall identità chimica del soluto si dicono proprietà colligative. Le proprietà
LE SOLUZIONI. Una soluzione è un sistema omogeneo costituito da almeno due componenti
 LE SOLUZIONI Una soluzione è un sistema omogeneo costituito da almeno due componenti Il componente maggioritario e solitamente chiamato solvente mentre i componenti in quantita minore sono chiamati soluti
LE SOLUZIONI Una soluzione è un sistema omogeneo costituito da almeno due componenti Il componente maggioritario e solitamente chiamato solvente mentre i componenti in quantita minore sono chiamati soluti
Si definisce soluzione un sistema omogeneo (costituito da una sola fase) con più di un componente
 Lezione 14 1.Soluzioni 2.Concentrazione 3.Proprietà colligative 1.Legge di Raoult 2.Abbassamento crioscopico 3.Innalzamento ebullioscopico 4.Pressione osmotica Le Soluzioni Si definisce soluzione un sistema
Lezione 14 1.Soluzioni 2.Concentrazione 3.Proprietà colligative 1.Legge di Raoult 2.Abbassamento crioscopico 3.Innalzamento ebullioscopico 4.Pressione osmotica Le Soluzioni Si definisce soluzione un sistema
Lo stato liquido. i liquidi molecolari con legami a idrogeno: le interazioni tra le molecole si stabiliscono soprattutto attraverso legami a idrogeno
 Lo stato liquido Le particelle sono in continuo movimento, anche se questo risulta più limitato rispetto al caso dei gas. Il movimento caratteristico a zig-zag delle particelle è chiamato moto Browniano.
Lo stato liquido Le particelle sono in continuo movimento, anche se questo risulta più limitato rispetto al caso dei gas. Il movimento caratteristico a zig-zag delle particelle è chiamato moto Browniano.
LA FORMAZIONE DELLE SOLUZIONI.
 LA FORMAZIONE DELLE SOLUZIONI. Perché le sostanze si sciolgono? Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore
LA FORMAZIONE DELLE SOLUZIONI. Perché le sostanze si sciolgono? Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore
Soluzioni. Un miscuglio eterogeneo è costituito da materia presente in stati omogenei diversi, definiti fasi del sistema eterogeneo.
 Le soluzioni Soluzioni Una soluzione è una miscela omogenea di due o più componenti. Il componente in quantità maggiore viene in genere indicato come solvente, gli altri con il nome di soluto. I componenti
Le soluzioni Soluzioni Una soluzione è una miscela omogenea di due o più componenti. Il componente in quantità maggiore viene in genere indicato come solvente, gli altri con il nome di soluto. I componenti
solvente soluto concentrazione
 Le soluzioni Una soluzione viene definita come un sistema omogeneo costituito da due o più componenti Il componente presente in maggiore quantità viene detto solvente, quello/i in minore quantità soluto/i
Le soluzioni Una soluzione viene definita come un sistema omogeneo costituito da due o più componenti Il componente presente in maggiore quantità viene detto solvente, quello/i in minore quantità soluto/i
LEZIONE 4. Le soluzioni
 LEZIONE 4 Le soluzioni Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore quantità. Il soluto è il componente delle
LEZIONE 4 Le soluzioni Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore quantità. Il soluto è il componente delle
Le proprietà colligative delle soluzioni
 1 Approfondimento 1.3 Le proprietà colligative delle soluzioni In un solvente puro, cioè senza soluti disciolti in esso, le molecole sono libere di interagire tra loro, attraendosi. L aggiunta di un soluto
1 Approfondimento 1.3 Le proprietà colligative delle soluzioni In un solvente puro, cioè senza soluti disciolti in esso, le molecole sono libere di interagire tra loro, attraendosi. L aggiunta di un soluto
Soluzioni. Miscele: (gas in gas) Leghe: (solidi in solidi) Soluzioni p.d: (solventi liquidi)
 Soluzioni Sono miscele omogenee in cui si riconoscono 2 componenti o fasi: il soluto, presente in quantità minore il solvente presente in quantità maggiore. Tipi di soluzioni: Miscele: (gas in gas) Leghe:
Soluzioni Sono miscele omogenee in cui si riconoscono 2 componenti o fasi: il soluto, presente in quantità minore il solvente presente in quantità maggiore. Tipi di soluzioni: Miscele: (gas in gas) Leghe:
Soluzioni semplici. Soluzioni liquide
 Soluzioni semplici Definizione di soluzione: dispersione omogenea di due (o più) specie chimiche in proporzioni variabili ma entro un campo finito di valori Soluto Solvente G. Sotgiu 1 Soluzioni liquide
Soluzioni semplici Definizione di soluzione: dispersione omogenea di due (o più) specie chimiche in proporzioni variabili ma entro un campo finito di valori Soluto Solvente G. Sotgiu 1 Soluzioni liquide
Sommario della lezione 18. Proprietà colligative
 Sommario della lezione 18 Proprietà colligative Interazioni soluto-solvente Interazioni soluto-solvente La solubilità di un soluto in un particolare solvente dipende da: la natura delle particelle di solvente
Sommario della lezione 18 Proprietà colligative Interazioni soluto-solvente Interazioni soluto-solvente La solubilità di un soluto in un particolare solvente dipende da: la natura delle particelle di solvente
 positiva, endotermico (la soluzione si raffredda) negativa, esotermico (la soluzione si scalda). DH sol = E ret + E solv concentrazione Molare Esempio: Preparare mezzo litro (0,5 l) di soluzione acquosa
positiva, endotermico (la soluzione si raffredda) negativa, esotermico (la soluzione si scalda). DH sol = E ret + E solv concentrazione Molare Esempio: Preparare mezzo litro (0,5 l) di soluzione acquosa
LE SOLUZIONI Soluzione: sistema omogeneo di due o più componenti
 LE SOLUZIONI Soluzione: sistema omogeneo di due o più componenti Il processo di solubilizzazione è una trasformazione fisica, pertanto le proprietà chimiche dei componenti si conservano Le soluzioni possono
LE SOLUZIONI Soluzione: sistema omogeneo di due o più componenti Il processo di solubilizzazione è una trasformazione fisica, pertanto le proprietà chimiche dei componenti si conservano Le soluzioni possono
Bagatti, Corradi, Desco, Ropa. Chimica. seconda edizione
 Bagatti, Corradi, Desco, Ropa Chimica seconda edizione Bagatti, Corradi, Desco, Ropa, Chimica seconda edizione Capitolo 9. L unità di misura dei chimici: la mole SEGUI LA MAPPA La concentrazione delle
Bagatti, Corradi, Desco, Ropa Chimica seconda edizione Bagatti, Corradi, Desco, Ropa, Chimica seconda edizione Capitolo 9. L unità di misura dei chimici: la mole SEGUI LA MAPPA La concentrazione delle
Le soluzioni e il loro comportamento
 A. A. 2016 2017 1 CCS Scienze geologiche CCS Biologia Le soluzioni e il loro comportamento PERCENTUALE IN peso (% p/p) PERCENTUALE IN volume (% v/v) PERCENTUALE IN peso/volume (% p/v) MOLARITA (M) moli
A. A. 2016 2017 1 CCS Scienze geologiche CCS Biologia Le soluzioni e il loro comportamento PERCENTUALE IN peso (% p/p) PERCENTUALE IN volume (% v/v) PERCENTUALE IN peso/volume (% p/v) MOLARITA (M) moli
Soluzioni unità 3, modulo D del libro
 Soluzioni unità 3, modulo D del libro SOLUZIONE: miscela omogenea di 2 o più sostanze Particelle dei componenti di dimensioni molecolari Componenti distribuiti in maniera caotica Se manca uno di questi
Soluzioni unità 3, modulo D del libro SOLUZIONE: miscela omogenea di 2 o più sostanze Particelle dei componenti di dimensioni molecolari Componenti distribuiti in maniera caotica Se manca uno di questi
Le soluzioni e il loro comportamento
 2017 Le soluzioni e il loro comportamento PERCENTUALE IN peso (% p/p) PERCENTUALE IN volume (% v/v) PERCENTUALE IN peso/volume (% p/v) MOLARITA (M) moli soluto / volume soluzione MOLALITA (m) moli soluto
2017 Le soluzioni e il loro comportamento PERCENTUALE IN peso (% p/p) PERCENTUALE IN volume (% v/v) PERCENTUALE IN peso/volume (% p/v) MOLARITA (M) moli soluto / volume soluzione MOLALITA (m) moli soluto
Termodinamica Chimica
 Universita degli Studi dell Insubria Corsi di Laurea in Scienze Chimiche e Chimica Industriale Termodinamica Chimica Miscele e Soluzioni dario.bressanini@uninsubria.it http://scienze-como.uninsubria.it/bressanini
Universita degli Studi dell Insubria Corsi di Laurea in Scienze Chimiche e Chimica Industriale Termodinamica Chimica Miscele e Soluzioni dario.bressanini@uninsubria.it http://scienze-como.uninsubria.it/bressanini
Le soluzioni possono esistere in ognuno dei tre stati della materia: gas, liquido o solido.
 SOLUZIONI Una soluzione è una miscela omogenea (=la sua composizione e le sue proprietà sono uniformi in ogni parte del campione) di due o più sostanze formate da ioni o molecole. Differenza con i colloidi
SOLUZIONI Una soluzione è una miscela omogenea (=la sua composizione e le sue proprietà sono uniformi in ogni parte del campione) di due o più sostanze formate da ioni o molecole. Differenza con i colloidi
Corso di orientamento e preparazione ai Corsi di Laurea della Scuola di Medicina ad accesso programmato a.a. 2019/2020 CHIMICA
 Corso di orientamento e preparazione ai Corsi di Laurea della Scuola di Medicina ad accesso programmato a.a. 2019/2020 CHIMICA «Nulla si crea, nulla si distrugge, ma tutto si trasforma.» (Antoine-Laurent
Corso di orientamento e preparazione ai Corsi di Laurea della Scuola di Medicina ad accesso programmato a.a. 2019/2020 CHIMICA «Nulla si crea, nulla si distrugge, ma tutto si trasforma.» (Antoine-Laurent
PROPRIETA DELLE SOLUZIONI
 1 11 PROPRIETA DELLE SOLUZIONI 2 SOLUZIONI IDEALI H mix = 0 le interazioni fra le molecole di soluto e di solvente puri sono paragonabili a quelle fra soluto e solvente; durante il processo di dissoluzione
1 11 PROPRIETA DELLE SOLUZIONI 2 SOLUZIONI IDEALI H mix = 0 le interazioni fra le molecole di soluto e di solvente puri sono paragonabili a quelle fra soluto e solvente; durante il processo di dissoluzione
PROPRIETA DELLE SOLUZIONI ACQUOSE. Prof.ssa Patrizia Gallucci
 PROPRIETA DELLE SOLUZIONI ACQUOSE Prof.ssa Patrizia Gallucci L'acqua è un composto chimicamente semplice, formato da due atomi di idrogeno e uno di ossigeno (H2O), che riveste fondamentale importanza in
PROPRIETA DELLE SOLUZIONI ACQUOSE Prof.ssa Patrizia Gallucci L'acqua è un composto chimicamente semplice, formato da due atomi di idrogeno e uno di ossigeno (H2O), che riveste fondamentale importanza in
CORSO DI CHIMICA PER L AMBIENTE. Lezione del 12 Aprile 2016
 CORSO DI CHIMICA PER L AMBIENTE Lezione del 12 Aprile 2016 Proprietà dei Metalli Malleabilità: i metalli possono esser facilmente ridotti in lamine sottili per battitura Duttilità: i metalli possono essere
CORSO DI CHIMICA PER L AMBIENTE Lezione del 12 Aprile 2016 Proprietà dei Metalli Malleabilità: i metalli possono esser facilmente ridotti in lamine sottili per battitura Duttilità: i metalli possono essere
LE SOLUZIONI. 7.1 Le soluzioni 7.2 Proprietà solventi dell acqua 7.3 Solubilità 7.4 La concentrazione nelle soluzioni 7.5 Le proprietà colligative
 LE SOLUZIONI 7.1 Le soluzioni 7.2 Proprietà solventi dell acqua 7.3 Solubilità 7.4 La concentrazione nelle soluzioni 7.5 Le proprietà colligative 7.1 Le soluzioni Si definisce soluzione una miscela omogenea
LE SOLUZIONI 7.1 Le soluzioni 7.2 Proprietà solventi dell acqua 7.3 Solubilità 7.4 La concentrazione nelle soluzioni 7.5 Le proprietà colligative 7.1 Le soluzioni Si definisce soluzione una miscela omogenea
solvente soluto concentrazione
 Le soluzioni Una soluzione viene definita come un sistema omogeneo costituito da due o più componenti Il componente presente in maggiore quantità viene detto solvente, quello/i in minore quantità soluto/i
Le soluzioni Una soluzione viene definita come un sistema omogeneo costituito da due o più componenti Il componente presente in maggiore quantità viene detto solvente, quello/i in minore quantità soluto/i
pressione esercitata dalle molecole di gas in equilibrio con Si consideri una soluzione di B in A. Per una soluzione ideale
 PROPRIETA COLLIGATIVE Proprietà che dipendono solo dal numero di particelle presenti in soluzione 1. TENSIONE DI VAPORE 2. INNALZAMENTO EBULLIOSCOPICO 3. ABBASSAMENTO CRIOSCOPICO 4. PRESSIONE OSMOTICA
PROPRIETA COLLIGATIVE Proprietà che dipendono solo dal numero di particelle presenti in soluzione 1. TENSIONE DI VAPORE 2. INNALZAMENTO EBULLIOSCOPICO 3. ABBASSAMENTO CRIOSCOPICO 4. PRESSIONE OSMOTICA
Un elemento è una sostanza pura che non può essere divisa in sostanze più semplici. Le sue molecole sono tutte uguali.
 Elementi, composti, miscugli Un elemento è una sostanza pura che non può essere divisa in sostanze più semplici. Le sue molecole sono tutte uguali. Il composto è formato da sostanze pure scomponibili in
Elementi, composti, miscugli Un elemento è una sostanza pura che non può essere divisa in sostanze più semplici. Le sue molecole sono tutte uguali. Il composto è formato da sostanze pure scomponibili in
LE SOLUZIONI. Una soluzione è un sistema omogeneo costituito da almeno due componenti
 LE SOLUZIONI Una soluzione è un sistema omogeneo costituito da almeno due componenti Il componente maggioritario e solitamente chiamato solvente mentre i componenti in quantita minore sono chiamati soluti
LE SOLUZIONI Una soluzione è un sistema omogeneo costituito da almeno due componenti Il componente maggioritario e solitamente chiamato solvente mentre i componenti in quantita minore sono chiamati soluti
EQUILIBRIO LIQUIDO VAPORE IN SISTEMI FORMATI DA DUE COMPONENTI LIQUIDI COMPLETAMENTE MISCIBILI
 EQUILIBRIO LIQUIDO VAPORE IN SISTEMI FORMATI DA DUE COMPONENTI LIQUIDI COMPLETAMENTE MISCIBILI Consideriamo un sistema formato da due liquidi A e B miscibili in tutte le proporzioni. Per la legge di Raoult
EQUILIBRIO LIQUIDO VAPORE IN SISTEMI FORMATI DA DUE COMPONENTI LIQUIDI COMPLETAMENTE MISCIBILI Consideriamo un sistema formato da due liquidi A e B miscibili in tutte le proporzioni. Per la legge di Raoult
Il binomio di van t Hoff Le proprietà colligative dipendono dal numero di particelle effettivamente presenti nella soluzione. Nel caso in cui il solut
 Proprietà colligative di soluzioni ideali Si definiscono proprietà colligative alcune proprietà delle soluzioni indipendenti dalla natura del soluto ma che dipendono soltanto dal numero delle particelle
Proprietà colligative di soluzioni ideali Si definiscono proprietà colligative alcune proprietà delle soluzioni indipendenti dalla natura del soluto ma che dipendono soltanto dal numero delle particelle
-PROPRIETA COLLIGATIVE-
 -PROPRIETA COLLIGATIVE- Le proprietà colligative sono proprietà delle soluzioni e sono funzioni del numero e non della natura delle particelle di soluto che le compongono. Abbassamento della pressione
-PROPRIETA COLLIGATIVE- Le proprietà colligative sono proprietà delle soluzioni e sono funzioni del numero e non della natura delle particelle di soluto che le compongono. Abbassamento della pressione
SOLUZIONI. Soluzioni gassose, liquide e solide
 LE SOLUZIONI SOLUZIONI Miscela fisicamente omogenea, cioè un insieme di due o più componenti che costituiscono un unica fase. Componente in eccesso: solvente Componente in minore quantità: soluto Soluzioni
LE SOLUZIONI SOLUZIONI Miscela fisicamente omogenea, cioè un insieme di due o più componenti che costituiscono un unica fase. Componente in eccesso: solvente Componente in minore quantità: soluto Soluzioni
Le proprietà colligative delle soluzioni Sappiamo dall esperienza quotidiana che una soluzione ha caratteristiche diverse dal solvente puro.
 Le proprietà colligative delle soluzioni Sappiamo dall esperienza quotidiana che una soluzione ha caratteristiche diverse dal solvente puro. Molte delle sue proprietà, come il sapore, il colore, l odore,
Le proprietà colligative delle soluzioni Sappiamo dall esperienza quotidiana che una soluzione ha caratteristiche diverse dal solvente puro. Molte delle sue proprietà, come il sapore, il colore, l odore,
SOLUZIONI MISCELE FISICAMENTE OMOGENEE SOLIDE, LIQUIDE, GASSOSE
 SOLUZIONI MISCELE FISICAMENTE OMOGENEE SOLIDE, LIQUIDE, GASSOSE SOLUZIONE SOLVENTE (Liquido) POLARE (es. H 2 O) APOLARE (solventi organici) ELETTROLITA (es. NaCl) SOLUTO (Solido, liquido, gas) NON ELETTROLITA
SOLUZIONI MISCELE FISICAMENTE OMOGENEE SOLIDE, LIQUIDE, GASSOSE SOLUZIONE SOLVENTE (Liquido) POLARE (es. H 2 O) APOLARE (solventi organici) ELETTROLITA (es. NaCl) SOLUTO (Solido, liquido, gas) NON ELETTROLITA
Soluzioni, Acidi e Basi
 Soluzioni, Acidi e Basi Mattia Natali 25 luglio 2011 Indice 1 Definizioni: 1 2 Proprietà delle soluzioni 2 2.1 Solubilità............................................ 2 2.2 Prodotto di solubilità.....................................
Soluzioni, Acidi e Basi Mattia Natali 25 luglio 2011 Indice 1 Definizioni: 1 2 Proprietà delle soluzioni 2 2.1 Solubilità............................................ 2 2.2 Prodotto di solubilità.....................................
Le soluzioni. A cura della Prof. ssa Barone Antonina
 Le soluzioni A cura della Prof. ssa Barone Antonina Le soluzioni: caratteri generali Sono sistemi omogenei; In esse, in qualsiasi punto si esegue una misurazione, si ottengono le stesse caratteristiche
Le soluzioni A cura della Prof. ssa Barone Antonina Le soluzioni: caratteri generali Sono sistemi omogenei; In esse, in qualsiasi punto si esegue una misurazione, si ottengono le stesse caratteristiche
CdL Professioni Sanitarie A.A. 2012/2013. Unità 9: Gas e processi di diffusione
 L. Zampieri Fisica per CdL Professioni Sanitarie A.A. 12/13 CdL Professioni Sanitarie A.A. 2012/2013 Gas Unità 9: Gas e processi di diffusione Equazione di stato dei gas perfetti Trasformazioni termodinamiche
L. Zampieri Fisica per CdL Professioni Sanitarie A.A. 12/13 CdL Professioni Sanitarie A.A. 2012/2013 Gas Unità 9: Gas e processi di diffusione Equazione di stato dei gas perfetti Trasformazioni termodinamiche
GLI STATI DELLA MATERIA
 GLI STATI DELLA MATERIA E LE SOLUZIONI Stati di aggregazione della materia Cambiamenti di stato La temperatura del cubetto di ghiaccio aumenta fino a raggiungere un valore detto PUNTO (O TEMPERATURA) DI
GLI STATI DELLA MATERIA E LE SOLUZIONI Stati di aggregazione della materia Cambiamenti di stato La temperatura del cubetto di ghiaccio aumenta fino a raggiungere un valore detto PUNTO (O TEMPERATURA) DI
GLI STATI DI AGGREGAZIONE DELLA MATERIA. Lo stato liquido
 GLI STATI DI AGGREGAZIONE DELLA MATERIA Lo stato liquido Lo stato liquido Liquidi: energia dei moti termici confrontabile con quella delle forze coesive. Limitata libertà di movimento delle molecole, che
GLI STATI DI AGGREGAZIONE DELLA MATERIA Lo stato liquido Lo stato liquido Liquidi: energia dei moti termici confrontabile con quella delle forze coesive. Limitata libertà di movimento delle molecole, che
Le soluzioni possono esistere in ognuno dei tre stati della materia: gas, liquido o solido.
 SOLUZIONI Una soluzione èuna miscela omogenea (=la sua composizione e le sue proprietà sono uniformi in ogni parte del campione) di due o più sostanze formate da ioni o molecole. Differenza con i colloidi
SOLUZIONI Una soluzione èuna miscela omogenea (=la sua composizione e le sue proprietà sono uniformi in ogni parte del campione) di due o più sostanze formate da ioni o molecole. Differenza con i colloidi
SOLUZIONI e DILUIZIONI
 SOLUZIONI e DILUIZIONI Introduzione In chimica viene definita soluzione un sistema in cui due o più sostanze formano un miscuglio omogeneo. Nella maggior parte dei casi una soluzione è costituita da due
SOLUZIONI e DILUIZIONI Introduzione In chimica viene definita soluzione un sistema in cui due o più sostanze formano un miscuglio omogeneo. Nella maggior parte dei casi una soluzione è costituita da due
Soluzione Per una miscela di due liquidi
 Soluzione soluto Si definisce soluto il componente che nel passaggio in soluzione perde il suo stato di aggregazione. Un sale che si scioglie in acqua, o un gas che si scioglie in un liquido Solvente Il
Soluzione soluto Si definisce soluto il componente che nel passaggio in soluzione perde il suo stato di aggregazione. Un sale che si scioglie in acqua, o un gas che si scioglie in un liquido Solvente Il
Miscibilità parziale
 Miscibilità parziale Un generico sistema con composizione C x è costituito da due fasi una è la Soluzione di A satura di B che ha composizione C 1 e l altra è la soluzione B satura di A che ha concentrazione
Miscibilità parziale Un generico sistema con composizione C x è costituito da due fasi una è la Soluzione di A satura di B che ha composizione C 1 e l altra è la soluzione B satura di A che ha concentrazione
Miscela omogenea monofasica i cui costituenti non è possibile separare meccanicamente
 Miscela omogenea monofasica i cui costituenti non è possibile separare meccanicamente Soluzioni Sistema Omogeneo (presenta le stesse proprietà in qualsiasi sua porzione) Monofasico Nella fase omogenea
Miscela omogenea monofasica i cui costituenti non è possibile separare meccanicamente Soluzioni Sistema Omogeneo (presenta le stesse proprietà in qualsiasi sua porzione) Monofasico Nella fase omogenea
Le proprietà colligative delle soluzioni
 Le proprietà colligative delle soluzioni Alcune immagine sono state prese e modificate da Chimica di Kotz, Treichel & Weaver, Edises 2007, III edizione 1 Le proprietà colligative Alcune proprietà delle
Le proprietà colligative delle soluzioni Alcune immagine sono state prese e modificate da Chimica di Kotz, Treichel & Weaver, Edises 2007, III edizione 1 Le proprietà colligative Alcune proprietà delle
Rapporto tra soluto e solvente o soluzione
 Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Le proprietà colligative
 Le proprietà colligative Dr. Gabriella Giulia Pulcini Ph.D. Student, Development of new approaches to teaching and learning Natural and Environmental Sciences University of Camerino, ITALY 1 Abbassamento
Le proprietà colligative Dr. Gabriella Giulia Pulcini Ph.D. Student, Development of new approaches to teaching and learning Natural and Environmental Sciences University of Camerino, ITALY 1 Abbassamento
SOLUZIONI. Soluzioni gassose, liquide e solide
 LE SOLUZIONI SOLUZIONI Miscela fisicamente omogenea, cioè un insieme di due o più componenti che costituiscono un unica fase. Componente in eccesso: solvente Componente in minore quantità: soluto Soluzioni
LE SOLUZIONI SOLUZIONI Miscela fisicamente omogenea, cioè un insieme di due o più componenti che costituiscono un unica fase. Componente in eccesso: solvente Componente in minore quantità: soluto Soluzioni
Undicesima unità didattica. I liquidi e le soluzioni
 Undicesima unità didattica I liquidi e le soluzioni Le soluzioni Sono delle miscele omogenee in cui il solvente è un liquido e il o i soluti possono essere solidi, liquidi o aeriformi Il soluto deve essere
Undicesima unità didattica I liquidi e le soluzioni Le soluzioni Sono delle miscele omogenee in cui il solvente è un liquido e il o i soluti possono essere solidi, liquidi o aeriformi Il soluto deve essere
g esatti di una certa soluzione contengono 10 g di NaCl. La densità della soluzione è di g/ml. Qual'è la molalità e la molarità di NaCl?
 4. 100 g esatti di una certa soluzione contengono 10 g di NaCl. La densità della soluzione è di 1.071 g/ml. Qual'è la molalità e la molarità di NaCl? d = 1,071 g/ml m =? M =? Consideriamo esattamente 100
4. 100 g esatti di una certa soluzione contengono 10 g di NaCl. La densità della soluzione è di 1.071 g/ml. Qual'è la molalità e la molarità di NaCl? d = 1,071 g/ml m =? M =? Consideriamo esattamente 100
Espressioni di concentrazione di una soluzione
 SOLUZIONI Una soluzione è un sistema fisicamente omogeneo costituito da due o più componenti: il solvente e il soluto (o i soluti. Il solvente è il componente presente, in genere ma non di regola, in maggior
SOLUZIONI Una soluzione è un sistema fisicamente omogeneo costituito da due o più componenti: il solvente e il soluto (o i soluti. Il solvente è il componente presente, in genere ma non di regola, in maggior
Proprietà colligative
 roprietà colligative Fra i sistemi reali è utile esaminare il comportamento di soluzioni diluite ottenuti da solidi o liquidi poco volatili rispetto al solvente. Le proprietà di tali soluzioni dipendono
roprietà colligative Fra i sistemi reali è utile esaminare il comportamento di soluzioni diluite ottenuti da solidi o liquidi poco volatili rispetto al solvente. Le proprietà di tali soluzioni dipendono
CONCENTRAZIONE. Le proprietà delle soluzioni di pendono dalle quantità relative delle sostanze che le compongono.
 1 CONCENTRAZIONE Le proprietà delle soluzioni di pendono dalle quantità relative delle sostanze che le compongono. La concentrazione esprime la composizione quantitiva soluzione. di una Unità di concentrazione
1 CONCENTRAZIONE Le proprietà delle soluzioni di pendono dalle quantità relative delle sostanze che le compongono. La concentrazione esprime la composizione quantitiva soluzione. di una Unità di concentrazione
SOLUZIONI. solide (es. leghe)
 SOLUZIONI Definizione: Miscela omogenea (una sola fase) di due o più componenti Soluzioni liquide (es. bevande alcoliche) gassose (es. aria) solide (es. leghe) 1 Unità di misura della concentrazione %
SOLUZIONI Definizione: Miscela omogenea (una sola fase) di due o più componenti Soluzioni liquide (es. bevande alcoliche) gassose (es. aria) solide (es. leghe) 1 Unità di misura della concentrazione %
Capitolo 15 Le proprietà delle soluzioni
 Capitolo 15 Le proprietà delle soluzioni Hai capito? pag. 354 Alle forze di London presenti fra le molecole di soluto se ne sostituiscono di nuove fra le molecole di soluto e solvente. pag. 356 A 0,4%
Capitolo 15 Le proprietà delle soluzioni Hai capito? pag. 354 Alle forze di London presenti fra le molecole di soluto se ne sostituiscono di nuove fra le molecole di soluto e solvente. pag. 356 A 0,4%
Temperatura. Il legame con le grandezze microscopiche è di tipo statistico. Pressione Volume Temperatura
 Temperatura La materia è un sistema fisico a molti corpi Gran numero di molecole (N A =6,02 10 23 ) interagenti tra loro Descrizione mediante grandezze macroscopiche (valori medi su un gran numero di particelle):
Temperatura La materia è un sistema fisico a molti corpi Gran numero di molecole (N A =6,02 10 23 ) interagenti tra loro Descrizione mediante grandezze macroscopiche (valori medi su un gran numero di particelle):
Brady Senese Pignocchino Chimica.blu Zanichelli 2014 Soluzione degli esercizi Capitolo 15
 Brady Senese Pignocchino Chimica.blu Zanichelli 2014 Soluzione degli esercizi Capitolo 15 Esercizio PAG 340 ES 1 PAG 340 ES 2 PAG 340 ES 3 PAG 340 ES 4 PAG 340 ES 5 PAG 340 ES 6 PAG 340 ES 7 Risposta Il
Brady Senese Pignocchino Chimica.blu Zanichelli 2014 Soluzione degli esercizi Capitolo 15 Esercizio PAG 340 ES 1 PAG 340 ES 2 PAG 340 ES 3 PAG 340 ES 4 PAG 340 ES 5 PAG 340 ES 6 PAG 340 ES 7 Risposta Il
PROPRIETÀ TIPICHE DEI LIQUIDI
 STATO LIQUIDO PROPRIETÀ TIPICHE DEI LIQUIDI - hanno volume ma non forma propria - hanno maggiore densità rispetto ai gas - sono incomprimibili - hanno capacità di fluire (forze di Van der Waals) EQUILIBRIO
STATO LIQUIDO PROPRIETÀ TIPICHE DEI LIQUIDI - hanno volume ma non forma propria - hanno maggiore densità rispetto ai gas - sono incomprimibili - hanno capacità di fluire (forze di Van der Waals) EQUILIBRIO
GAS. H 2 N 2 O 2 F 2 Cl 2 CO CO 2 NO 2 SO 2 CH 4
 GAS Non hanno né forma né volume propri. Sono facilmente comprimibili. Sono in genere gassose le sostanze costituite da molecole piccole e di basso peso molecolare. H 2 N 2 O 2 F 2 Cl 2 He Ne Ar CO CO
GAS Non hanno né forma né volume propri. Sono facilmente comprimibili. Sono in genere gassose le sostanze costituite da molecole piccole e di basso peso molecolare. H 2 N 2 O 2 F 2 Cl 2 He Ne Ar CO CO
Fisicaa Applicata, Area Tecnica, M. Ruspa Esercizio. Data una massa m = 8,8 mg di CO 2, calcolare: 1) il numero di moli. 2) il numero di molecole
 Esercizio Data una massa m = 8,8 mg di CO 2, calcolare: 1) il numero di moli 2) il numero di molecole 1 GAS PERFETTO volume occupato dalle molecole è trascurabile; forze di attrazione tra molecole sono
Esercizio Data una massa m = 8,8 mg di CO 2, calcolare: 1) il numero di moli 2) il numero di molecole 1 GAS PERFETTO volume occupato dalle molecole è trascurabile; forze di attrazione tra molecole sono
STATO LIQUIDO. Si definisce tensione superficiale ( ) il lavoro che bisogna fare per aumentare di 1 cm 2 la superficie del liquido.
 STTO LIQUIDO Una sostanza liquida è formata da particelle in continuo movimento casuale, come in un gas, tuttavia le particelle restano a contatto le une alle altre e risentono sempre delle notevoli forze
STTO LIQUIDO Una sostanza liquida è formata da particelle in continuo movimento casuale, come in un gas, tuttavia le particelle restano a contatto le une alle altre e risentono sempre delle notevoli forze
Calcoli stechiometrici in soluzione (Cap. 12)
 Calcoli stechiometrici in soluzione (Cap. 12) Le soluzioni Molarità Gli elettroliti Reazioni in soluzione Reazioni di precipitazione Titolazioni acido-base Le soluzioni Una soluzione è una miscela omogenea
Calcoli stechiometrici in soluzione (Cap. 12) Le soluzioni Molarità Gli elettroliti Reazioni in soluzione Reazioni di precipitazione Titolazioni acido-base Le soluzioni Una soluzione è una miscela omogenea
Gas. Chimica generale ed Inorganica: Chimica Generale. I palloni ad aria calda
 Gas I palloni ad aria calda Gas FIGURA 6-1 Lo stato gassoso di tre alogeni (Gruppo 17) Gas FIGURA 6-1 Lo stato gassoso di tre alogeni (Gruppo 17) Gas FIGURA 6-2 Illustrando la pressione esercitata da un
Gas I palloni ad aria calda Gas FIGURA 6-1 Lo stato gassoso di tre alogeni (Gruppo 17) Gas FIGURA 6-1 Lo stato gassoso di tre alogeni (Gruppo 17) Gas FIGURA 6-2 Illustrando la pressione esercitata da un
-SOLUZIONE- In una soluzione liquida si possono distinguere un solvente (il componente liquido più abbondante) e uno o più soluti.
 -SOLUZIONE- Una soluzione è una miscela omogenea di due o più componenti. In generale una soluzione può essere in fase solida (leghe metalliche), liquida (gas + liquido, liquido + liquido, solido + liquido),
-SOLUZIONE- Una soluzione è una miscela omogenea di due o più componenti. In generale una soluzione può essere in fase solida (leghe metalliche), liquida (gas + liquido, liquido + liquido, solido + liquido),
Classificazione della materia
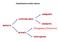 Classificazione della materia composto materia sostanza pura miscela Omogenea (Soluzioni) eterogenea elemento Definizione di Soluzione Una soluzione è il prodotto della dispersione omogenea delle molecole
Classificazione della materia composto materia sostanza pura miscela Omogenea (Soluzioni) eterogenea elemento Definizione di Soluzione Una soluzione è il prodotto della dispersione omogenea delle molecole
Esercitazioni di Elementi di Chimica. Modulo 3 Trasformazioni della Materia
 Esercitazioni di Elementi di Chimica Modulo 3 Trasformazioni della Materia Esempi di quiz a risposta multipla e questionari a completamento L esame finale sarà composto da problemi simili Quale/i dei seguenti
Esercitazioni di Elementi di Chimica Modulo 3 Trasformazioni della Materia Esempi di quiz a risposta multipla e questionari a completamento L esame finale sarà composto da problemi simili Quale/i dei seguenti
Materia La materia è tutto ciò che occupa uno spazio ed ha una massa.
 Materia La materia è tutto ciò che occupa uno spazio ed ha una massa. La più piccola particella della materia è l'atomo Sostanze La sostanza è una porzione di materia che presenta proprietà ben definite.
Materia La materia è tutto ciò che occupa uno spazio ed ha una massa. La più piccola particella della materia è l'atomo Sostanze La sostanza è una porzione di materia che presenta proprietà ben definite.
REGISTRO DELLE LEZIONI 2004/2005. Tipologia. Addì Tipologia. Addì Tipologia
 Cenni della teoria ondulatoria. Duplice comportamento dell'elettrone onda-particella. Tavola periodica di Mendelew, tavola periodica moderna, proprietà generali degli elementi. blocco s, p, d, f. Introduzione
Cenni della teoria ondulatoria. Duplice comportamento dell'elettrone onda-particella. Tavola periodica di Mendelew, tavola periodica moderna, proprietà generali degli elementi. blocco s, p, d, f. Introduzione
Soluzioni, elettroliti e non
 Soluzioni, elettroliti e non Il processo di solubilizzazione è un processo complesso, per interpretarlo occorre conoscere la natura ei legami chimici coinvolti COSA CONSIDERARE? 1) Interazioni soluto -
Soluzioni, elettroliti e non Il processo di solubilizzazione è un processo complesso, per interpretarlo occorre conoscere la natura ei legami chimici coinvolti COSA CONSIDERARE? 1) Interazioni soluto -
DI FASE DISTILLAZIONE
 Chimica Silvia LICOCCIA Professore Ordinario di Fondamenti Chimici per le Tecnologie Dipartimento di Scienze e Tecnologie Chimiche Università di Roma Tor Vergata TRANSIZIONI DI FASE DISTILLAZIONE Le fasi
Chimica Silvia LICOCCIA Professore Ordinario di Fondamenti Chimici per le Tecnologie Dipartimento di Scienze e Tecnologie Chimiche Università di Roma Tor Vergata TRANSIZIONI DI FASE DISTILLAZIONE Le fasi
Diffusione e osmosi. Roberto Cirio. Corso di Laurea in Chimica e Tecnologia Farmaceutiche Anno accademico Corso di Fisica
 Roberto Cirio Corso di Laurea in Chimica e Tecnologia Farmaceutiche Anno accademico 2007 2008 Corso di Fisica La lezione di oggi Sostanze sciolte in liquidi, se utilizzate con membrane, hanno comportamenti
Roberto Cirio Corso di Laurea in Chimica e Tecnologia Farmaceutiche Anno accademico 2007 2008 Corso di Fisica La lezione di oggi Sostanze sciolte in liquidi, se utilizzate con membrane, hanno comportamenti
Vediamo i modi con cui esprimere le concentrazioni delle soluzioni
 Vediamo i modi con cui esprimere le concentrazioni delle soluzioni 1. %m/m = 100 quanti gr di NaCl si devono sciogliere in 500 gr di acqua per ottenere una soluzione al 15%m/m? 15 = 100 (N.B: al denominatore
Vediamo i modi con cui esprimere le concentrazioni delle soluzioni 1. %m/m = 100 quanti gr di NaCl si devono sciogliere in 500 gr di acqua per ottenere una soluzione al 15%m/m? 15 = 100 (N.B: al denominatore
Lezione n. 12. Proprietà colligative Variazione del punto crioscopico. Pressione osmotica. 02/03/2008 Antonino Polimeno 1
 Chimica Fisica - Chimica e Tecnologia Farmaceutiche Lezione n. 12 Proprietà colligative Variazione del punto ebullioscopico Variazione del punto crioscopico Pressione osmotica 02/03/2008 Antonino Polimeno
Chimica Fisica - Chimica e Tecnologia Farmaceutiche Lezione n. 12 Proprietà colligative Variazione del punto ebullioscopico Variazione del punto crioscopico Pressione osmotica 02/03/2008 Antonino Polimeno
2. La concentrazione La quantità di soluto contenuto in una determinata quantità di soluzione (o in alcuni casi di
 LE SOLUZIONI E LA CONCENTRAZIONE 1. Generalità e concetto di solubilità Una soluzione è un sistema omogeneo costituito da due o più componenti. Le soluzioni possono essere solide, liquide o gassose. Sono
LE SOLUZIONI E LA CONCENTRAZIONE 1. Generalità e concetto di solubilità Una soluzione è un sistema omogeneo costituito da due o più componenti. Le soluzioni possono essere solide, liquide o gassose. Sono
Chimica: Studio della materia e delle sue interazioni.
 Chimica: Studio della materia e delle sue interazioni. La descrizione della materia viene affrontata da: punto di vista microscopico: studio di atomi e molecole le loro interazioni e le reazioni chimiche
Chimica: Studio della materia e delle sue interazioni. La descrizione della materia viene affrontata da: punto di vista microscopico: studio di atomi e molecole le loro interazioni e le reazioni chimiche
Gli stati di aggregazione della materia.
 Gli stati di aggregazione della materia. Stati di aggregazione della materia: Solido, liquido, gassoso Passaggi di stato: Solido Liquido (fusione) e liquido solido (solidificazione); Liquido aeriforme
Gli stati di aggregazione della materia. Stati di aggregazione della materia: Solido, liquido, gassoso Passaggi di stato: Solido Liquido (fusione) e liquido solido (solidificazione); Liquido aeriforme
Corso di Studi di Fisica Corso di Chimica
 Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Lezione 34 2009 Programma: a che punto siamo? Definizione di soluzione Una soluzione è una miscela omogenea di due o più sostanze
Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Lezione 34 2009 Programma: a che punto siamo? Definizione di soluzione Una soluzione è una miscela omogenea di due o più sostanze
CORSO DI CHIMICA. Esercitazione del 7 Giugno 2016
 CORSO DI CHIMICA Esercitazione del 7 Giugno 2016 25 ml di una miscela di CO e CO 2 diffondono attraverso un foro in 38 s. Un volume uguale di O 2 diffonde nelle stesse condizioni in 34,3 s. Quale è la
CORSO DI CHIMICA Esercitazione del 7 Giugno 2016 25 ml di una miscela di CO e CO 2 diffondono attraverso un foro in 38 s. Un volume uguale di O 2 diffonde nelle stesse condizioni in 34,3 s. Quale è la
Stato solido. CLASSIFICAZIONE (I) Basata sulla natura delle particelle che costituiscono il solido DEFINIZIONE DA UN PUNTO DI VISTA MACROSCOPICO
 Stato solido DEFINIZIONE DA UN PUNTO DI VISTA MACROSCOPICO Stato dotato di forma propria e volume proprio Le particelle (atomi, ioni, molecole) sono fortemente legate tra loro e non si possono allontanare
Stato solido DEFINIZIONE DA UN PUNTO DI VISTA MACROSCOPICO Stato dotato di forma propria e volume proprio Le particelle (atomi, ioni, molecole) sono fortemente legate tra loro e non si possono allontanare
LE SOLUZIONI LE SOLUZIONI 8.A PRE-REQUISITI 8.B PRE-TEST 8.C OBIETTIVI 8.1 LE SOLUZIONI 8.V VERIFICA SE HAI CAPITO 8.2 CONCENTRAZIONE DELLE SOLUZIONI
 LE SOLUZIONI 8.A PRE-REQUISITI 8.B PRE-TEST 8.C OBIETTIVI 8.1 LE SOLUZIONI 8.2 CONCENTRAZIONE DELLE SOLUZIONI 8.3.2 INNALZAMENTO EBULLIOSCOPICO E ABBASSAMENTO CRIOSCOPICO 8.3.3 PRESSIONE OSMOTICA 8.3.4
LE SOLUZIONI 8.A PRE-REQUISITI 8.B PRE-TEST 8.C OBIETTIVI 8.1 LE SOLUZIONI 8.2 CONCENTRAZIONE DELLE SOLUZIONI 8.3.2 INNALZAMENTO EBULLIOSCOPICO E ABBASSAMENTO CRIOSCOPICO 8.3.3 PRESSIONE OSMOTICA 8.3.4
LIQUIDO LIQUIDO LIQUIDO Alcol in acqua. LIQUIDO LIQUIDO SOLIDO Sale in acqua. SOLIDO SOLIDO GAS Idrogeno nell acciaio
 SOLUZIONI Le soluzioni sono miscele omogenee (= stesse proprietà in qualsiasi sua porzione) di due o più sostanze La sostanza presenta in maggior quantità è detta SOLVENTE mentre quelle in quantità inferiore
SOLUZIONI Le soluzioni sono miscele omogenee (= stesse proprietà in qualsiasi sua porzione) di due o più sostanze La sostanza presenta in maggior quantità è detta SOLVENTE mentre quelle in quantità inferiore
Stechiometria delle soluzioni
 www.matematicamente.it stechiometria delle soluzioni (medicina) 1 Stechiometria delle soluzioni Domande tratte dai test di ammissione a medicina, odontoiatria, veterinaria 1. Se si vuole ottenere una soluzione
www.matematicamente.it stechiometria delle soluzioni (medicina) 1 Stechiometria delle soluzioni Domande tratte dai test di ammissione a medicina, odontoiatria, veterinaria 1. Se si vuole ottenere una soluzione
LA MATERIA NEI SUOI DIVERSI ASPETTI
 LA MATERIA NEI SUOI DIVERSI ASPETTI Materia è tutto ciò che costituisce i corpi e che, assumendo forme diverse nello spazio, si manifesta ai nostri sensi. La materia è ovunque intorno a noi: il nostro
LA MATERIA NEI SUOI DIVERSI ASPETTI Materia è tutto ciò che costituisce i corpi e che, assumendo forme diverse nello spazio, si manifesta ai nostri sensi. La materia è ovunque intorno a noi: il nostro
LE SOLUZIONI. SONO MISCUGLI OMOGENEI I CUI COSTITUENTI CONSERVANO LE LORO PROPRIETÀ
 LE SOLUZIONI LE SOLUZIONI. SONO MISCUGLI OMOGENEI I CUI COSTITUENTI CONSERVANO LE LORO PROPRIETÀ il solvente è il componente in maggiore quantità. Il soluto è il componente delle soluzioni che si trova
LE SOLUZIONI LE SOLUZIONI. SONO MISCUGLI OMOGENEI I CUI COSTITUENTI CONSERVANO LE LORO PROPRIETÀ il solvente è il componente in maggiore quantità. Il soluto è il componente delle soluzioni che si trova
Esercitazioni Infermieristica
 Esercitazioni Infermieristica Novara: Gruppo A 28/1 9-13 29/1 14-18 Gruppo B 28/1 14-18 29/1 9-13 Alba 7/12/2012 11-13 14-17 25/01/2013 15-18 a Novara Alessandria 18/12/2012 10-13 14-16 14/01/2013 10-13
Esercitazioni Infermieristica Novara: Gruppo A 28/1 9-13 29/1 14-18 Gruppo B 28/1 14-18 29/1 9-13 Alba 7/12/2012 11-13 14-17 25/01/2013 15-18 a Novara Alessandria 18/12/2012 10-13 14-16 14/01/2013 10-13
Si definisce soluzione un sistema omogeneo (costituito da una sola fase) con più di un componente
 Le Soluzioni Si definisce soluzione un sistema omogeneo (costituito da una sola fase) con più di un componente - La specie chimica presente nella soluzione in quantità più abbondante viene detta SOLVENTE
Le Soluzioni Si definisce soluzione un sistema omogeneo (costituito da una sola fase) con più di un componente - La specie chimica presente nella soluzione in quantità più abbondante viene detta SOLVENTE
