La isomeria in Chimica Organica
|
|
|
- Beata Venturi
- 4 anni fa
- Visualizzazioni
Transcript
1 La isomeria in himica Organica isomeri composti differenti con la stessa formula molecolare (bruta) costituzionali isomeri i cui atomi sono connessi in modi diversi stereoisomeri P.es.: butano, 2-metil-propano isomeri che a parità di connessione differiscono per come gli atomi sono disposti nello spazio conformazionali stereoisomeri che sono interconvertibili per rotazione intorno a legami singoli (σ) P.es.: conformazione sfalsata ed eclissata dell etano configurazionali stereoisomeri la cui interconversione richiede rottura di legami o comunque una energia tale che non è ottenibile in condizioni ordinarie enantiomeri stereoisomeri che sono l'uno l'immagine speculare dell'altro non sovrapponibile diasteroisomeri stereoisomeri che non sono l'uno l'immagine speculare dell'altro 1
2 Isomeri costituzionali composti con la stessa formula molecolare (bruta) ma che differiscono per l'ordine con cui sono legati gli atomi butano 2-metilpropano 2 6 O 2 alcol etilico O 3 etere dimetilico 3 8 O 3 alcol isopropilico 2 2 alcol n-propilico 2 O 3 etilmetiletere 2
3 conformazionali eclissata etano a b sfalsata a stereoisomeri b diasteroisomeri Z X configurazionali enantiomeri si ha diastereoisomeria cis-trans negli alcheni quando su ciascun carbonio sp 2 ci sono sostituenti diversi (b) y (b) 3 (b) 3 (b) cis-2-butene trans-2-butene Sistemi ciclici 3 3 1,2-cis-dimetilciclopentano 3 1,2-trans-dimetilciclopentano 3
4 Molecole hirali Una molecola, in genere un oggetto, si dice chirale quando non è sovrapponibile alla sua immagine speculare Esempi di oggetti chirali: mano, vite, scala a chiocciola In genere un oggetto achirale possiede un piano di simmetria l l Br l l molecole achirali: il piano del lucido è un piano di simmetria Br chirale l I Un atomo tetraedrico (carbonio) che ha quattro sostituenti (atomi o gruppi) diversi è privo di un piano di simmetria ed è pertanto chirale ed è detto stereocentro ( centro 4 asimmetrico)
5 Enantiomeria L'enantiomeria si ha nelle molecole chirali. La più comune (ma non l'unica) causa di enantiomeria è la presenza di uno stereocentro nella molecola O I II Il 2-butanolo è una molecola chirale: non sovrapponibile alla propria immagine speculare Le due molecole I e II sono due enantiomeri in quanto sono l'una l'immagine speculare dell'altra e non sono sovrapponibili A A B I D D II B specchio 180 A A B I D B D II I e II non sono sovrapponibili 5
6 OGNI MOLEOLA A UN IMMAGINE SPEULARE!!! SOLO SE QUESTE NON SONO SOVRAPPONIBILI SONO DIVERSE, IOE ENANTIOMERI O 3 Identiche Rotazione di
7 Nomenclatura degli stereocentri configurazione assoluta Sistema (R,S ) di ahn, Ingold e Prelog A) Identificare lo stereocentro ed i gruppi ad esso legato B) Assegnare una priorità ai gruppi da 1 (alta priorità) a 4 (bassa priorità) in base al Numero Atomico dell'atomo legato allo stereocentro l ) Orientare la molecola nello spazio in modo che il gruppo a priorità minore (4) sia diretto lontano dall'osservatore, mentre gli altri tre si proiettano verso l'osservatore come i raggi di un volante 4 l 3 3 (S ) 1-cloro-etanolo D) Guardando dalla parte del guidatore dell'auto, cioè opposta alla canna del volante, si vede il verso di rotazione per andare dal gruppo 1 al 3, se questo è orario la configurazione dello stereocentro sarà (R ) se antiorario sarà (S ) 7
8 Regole per assegnare la priorità 1) L atomo con numero atomico maggiore ha priorità sull atomo a numero atomico minore. I > Br > l > F > O > N > > 4 F 1 2 T D 3 2) Nel caso di isotopi la priorità spetta all isotopo con numero di massa maggiore. 3) Se al carbonio chirale (centro stereogenico) sono legati atomi uguali, la priorità si determina sulla base del numero atomico del primo atomo differente (S)-2-metil-3-pentanolo 8
9 4) Gli atomi legati con legami multipli sono considerati come atomi legati con un numero equivalente di legami semplici
10 Descrizione della configurazione dello stereocentro della gliceraldeide Qual é la configurazione di questo enantiomero? O O 2 gliceraldeide 4 O 2 3 gruppo formilico (R )-gliceraldeide Il gruppo formilico precede il - 2 perchè il doppio legame viene considerato come se al formilico fossero legati 2 O, oltre che 1, mentre al gruppo al del gruppo - 2 è legato 1 O, oltre che 2 O O
11 Nomenclatura E-Z per i diastereoisomeri degli alcheni (b) (b) 3 (b) 3 (b) 3 cis-2-butene trans-2-butene Quando l alchene ha 3 o 4 sostituenti la terminologia cis-trans non può essere applicata Br l F Si usano le regole di priorità dei gruppi Priorità più alta l F F l Priorità più alta Priorità più alta Br Priorità più alta Br (Z)-2-Bromo-1-cloro- 1-fluoroetene (E)-2-Bromo-1-cloro- 1-fluoroetene Z= zusammen, insieme E= entgegen, opposto 11
Isomeria Costituzionale. Isomeria Conformazionale
 Isomeria ostituzionale Isomeri ostituzionali: omposti con uguale formula molecolare ma con un diverso ordine con cui sono legati gli atomi tra loro. Isomeria onformazionale onformazione: ciascuna disposizione
Isomeria ostituzionale Isomeri ostituzionali: omposti con uguale formula molecolare ma con un diverso ordine con cui sono legati gli atomi tra loro. Isomeria onformazionale onformazione: ciascuna disposizione
STEREOISOMERIA trans-1,4-dimetilcicloesano cis-1,4-dimetilcicloesano
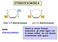 STEREOISOMERIA trans-1,4-dimetilcicloesano cis-1,4-dimetilcicloesano sono stereoisomeri Hanno la stessa formula molecolare, gli atomi legati con lo stesso ordine, ma con diversa orientazione nello spazio
STEREOISOMERIA trans-1,4-dimetilcicloesano cis-1,4-dimetilcicloesano sono stereoisomeri Hanno la stessa formula molecolare, gli atomi legati con lo stesso ordine, ma con diversa orientazione nello spazio
Idrocarburi. Stereoisomeria
 Idrocarburi Stereoisomeria Stereisomeri configurazionali Il fatto che gli atomi di carbonio degli alcani siano tutti ibridati sp 3 rende possibile la formazione anche di altri stereoisomeri (isomeri con
Idrocarburi Stereoisomeria Stereisomeri configurazionali Il fatto che gli atomi di carbonio degli alcani siano tutti ibridati sp 3 rende possibile la formazione anche di altri stereoisomeri (isomeri con
Isomeria nelle molecole organiche
 Isomeria nelle molecole organiche 3 Cis/Trans o Z/E 1 4 Regole di priorità negli alcheni: 1. Numero atomico maggiore=maggiore priorità; 2. Maggiore priorità all isotopo più pesante; 3. Se il primo atomo
Isomeria nelle molecole organiche 3 Cis/Trans o Z/E 1 4 Regole di priorità negli alcheni: 1. Numero atomico maggiore=maggiore priorità; 2. Maggiore priorità all isotopo più pesante; 3. Se il primo atomo
Figura. Stereochimica
 Figura Stereochimica Stereochimica: enantiomeri Differenze apparentemente insignificanti nella struttura 3-D possono causare proprietà molto differenti. Si può osservare questo considerando amido e cellulosa,
Figura Stereochimica Stereochimica: enantiomeri Differenze apparentemente insignificanti nella struttura 3-D possono causare proprietà molto differenti. Si può osservare questo considerando amido e cellulosa,
C 4 H 10 C 4 H 10. Hanno la stessa formula molecolare C 4 H 10.
 Isomeria costituzionale negli alcani Isomeri costituzionali (strutturali): composti con uguale formula molecolare ma diversa formula di struttura (con un diverso ordine con cui sono legati i loro atomi).
Isomeria costituzionale negli alcani Isomeri costituzionali (strutturali): composti con uguale formula molecolare ma diversa formula di struttura (con un diverso ordine con cui sono legati i loro atomi).
CONTENUTI DELLA LEZIONE:
 Stereochimica CONTENUTI DELLA LEZIONE: 1. La Chiralità: Molecole chirali e achirali 2. Identificare uno stereocentro 3. Enantiomeri 4. Regole per assegnare la configurazione R,S 5. Diastereoisomeri 6.
Stereochimica CONTENUTI DELLA LEZIONE: 1. La Chiralità: Molecole chirali e achirali 2. Identificare uno stereocentro 3. Enantiomeri 4. Regole per assegnare la configurazione R,S 5. Diastereoisomeri 6.
Gli isomeri sono composti caratterizzati dalla stessa formula molecolare o bruta. Fino ad ora abbiamo conosciuto tre tipi di isomeria :
 Gli isomeri sono composti caratterizzati dalla stessa formula molecolare o bruta. Fino ad ora abbiamo conosciuto tre tipi di isomeria : ONFORMAZIONALE (eclissata, sfalsata) STRUTTURALE (pentano, 2 metil
Gli isomeri sono composti caratterizzati dalla stessa formula molecolare o bruta. Fino ad ora abbiamo conosciuto tre tipi di isomeria : ONFORMAZIONALE (eclissata, sfalsata) STRUTTURALE (pentano, 2 metil
Isomeri. Unità didattica 5. Isomeri cis-trans. La stereochimica. I composti achirali hanno immagini speculari sovrapponibili
 Isomeri Composti non identici ma che hanno la stessa formula molecolare Unità didattica 5 La stereochimica La disposizione degli atomi nello spazio; La stereochimica delle reazioni di addizione Isomeri
Isomeri Composti non identici ma che hanno la stessa formula molecolare Unità didattica 5 La stereochimica La disposizione degli atomi nello spazio; La stereochimica delle reazioni di addizione Isomeri
ISOMERIA. Isomeri di struttura O OH C 4 H 10 O C 4 H 10
 ISOMERIA O O C 4 10 O C 4 10 Isomeri di struttura Isomeri conformazionali conformazioni rotameri STEREOISOMERIA stereoisomeri o isomeri spaziali o isomeri costituzionali ( in greco vuol dire spazio) si
ISOMERIA O O C 4 10 O C 4 10 Isomeri di struttura Isomeri conformazionali conformazioni rotameri STEREOISOMERIA stereoisomeri o isomeri spaziali o isomeri costituzionali ( in greco vuol dire spazio) si
ISOMERI. composti differenti con la stessa formula molecolare DIASTEREOISOMERI
 ISOMERI composti differenti con la stessa formula molecolare ISOMERI COSTITUZIONALI isomeri i cui atomi hanno una differente connettività STEREOISOMERI isomeri che hanno la stessa connettività ma differiscono
ISOMERI composti differenti con la stessa formula molecolare ISOMERI COSTITUZIONALI isomeri i cui atomi hanno una differente connettività STEREOISOMERI isomeri che hanno la stessa connettività ma differiscono
CHIRALITA' E' una proprietà relativa ad oggetti PRIVI DI UN PIANO DI SIMMETRIA.
 CIRALITA' E' una proprietà relativa ad oggetti PRIVI DI UN PIANO DI SIMMETRIA. non simmetrica rispetto al piano piano di simmetria La mano destra non è sovrapponibile alla mano sinistra: ne è invece l'immagine
CIRALITA' E' una proprietà relativa ad oggetti PRIVI DI UN PIANO DI SIMMETRIA. non simmetrica rispetto al piano piano di simmetria La mano destra non è sovrapponibile alla mano sinistra: ne è invece l'immagine
OPERAZIONI ed ELEMENTI di SIMMETRIA
 OPERAZIONI ed ELEMENTI di SIMMETRIA Una operazione di simmetria è un'azione che lascia immutato l oggetto a cui si applica. A una operazione di simmetria è associato uno o più elementi di simmetria. Le
OPERAZIONI ed ELEMENTI di SIMMETRIA Una operazione di simmetria è un'azione che lascia immutato l oggetto a cui si applica. A una operazione di simmetria è associato uno o più elementi di simmetria. Le
28/03/2013. Stereochimica: enantiomeri
 Figura Stereochimica Stereochimica: enantiomeri Atomi di carbonio tetraedrici e loro immagini speculari. Le molecole del tipo CH 3 X e CH 2 XY sono identiche alle loro immagini speculari, ma una molecola
Figura Stereochimica Stereochimica: enantiomeri Atomi di carbonio tetraedrici e loro immagini speculari. Le molecole del tipo CH 3 X e CH 2 XY sono identiche alle loro immagini speculari, ma una molecola
Idrocarburi Saturi. Cicloalcani
 Idrocarburi Saturi Cicloalcani Cicloalcani I cicloalcani sono idrocarburi i cui atomi di carbonio sono uniti per formare un anello In natura sono presenti cicloalcani con dimensioni dell anello che vanno
Idrocarburi Saturi Cicloalcani Cicloalcani I cicloalcani sono idrocarburi i cui atomi di carbonio sono uniti per formare un anello In natura sono presenti cicloalcani con dimensioni dell anello che vanno
Capitolo 6 stereoisomeria
 himica Organica Informazione Scientifica sul Farmaco apitolo 6 stereoisomeria Organic hemistry, 5 th Edition L. G. Wade, Jr. Louis Pasteur, 1822-1895 In questa lezione: hiralità ed enantiomeri onfigurazione
himica Organica Informazione Scientifica sul Farmaco apitolo 6 stereoisomeria Organic hemistry, 5 th Edition L. G. Wade, Jr. Louis Pasteur, 1822-1895 In questa lezione: hiralità ed enantiomeri onfigurazione
ISOMERIA. Isomeri costituzionali. Stereoisomeri. Nomenclatura. Importanza biologica della chiralità
 ISOMERIA Isomeri costituzionali Stereoisomeri Nomenclatura Importanza biologica della chiralità ISOMERI Si definiscono isomeri composti con identica formula molecolare, ma diversa struttura (concatenazione
ISOMERIA Isomeri costituzionali Stereoisomeri Nomenclatura Importanza biologica della chiralità ISOMERI Si definiscono isomeri composti con identica formula molecolare, ma diversa struttura (concatenazione
L Atomo di Carbonio Tetraedrico e la Rappresentazione di Fischer
 L Atomo di Carbonio Tetraedrico e la Rappresentazione di Fischer Un atomo di carbonio con almeno due sostituenti identici e la sua immagine speculare sono sovrapponibili e quindi eguali atomo1.c3d Un atomo
L Atomo di Carbonio Tetraedrico e la Rappresentazione di Fischer Un atomo di carbonio con almeno due sostituenti identici e la sua immagine speculare sono sovrapponibili e quindi eguali atomo1.c3d Un atomo
Elementi di Stereochimica
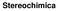 Stereochimica Elementi di Stereochimica Catena Costituzionale Posizione Funzione Isomeria CONFORMAZIONALE Stereoisomeria Diastereoisomeria Enantiomeria CONFIGURAZIONALE CONFORMAZIONALE CONFIGURAZIONALE
Stereochimica Elementi di Stereochimica Catena Costituzionale Posizione Funzione Isomeria CONFORMAZIONALE Stereoisomeria Diastereoisomeria Enantiomeria CONFIGURAZIONALE CONFORMAZIONALE CONFIGURAZIONALE
Corso di Laurea in Informazione Scientifica sul Farmaco a.a. 2010/2011. Esercitazione per la prima prova parziale di Chimica Organica.
 Corso di Laurea in Informazione Scientifica sul Farmaco a.a. 2010/2011. Esercitazione per la prima prova parziale di Chimica Organica. 1. Scrivere la formula condensata per la molecola seguente: Br e la
Corso di Laurea in Informazione Scientifica sul Farmaco a.a. 2010/2011. Esercitazione per la prima prova parziale di Chimica Organica. 1. Scrivere la formula condensata per la molecola seguente: Br e la
CH3CHCH H2C CHCHCH2CH3. 31 L ordine di priorità CIP è riferito ai quattro sostituenti legati allo stereocentro e viene assegnato
 Chimica organica: stereoisomeria ottica Capitolo C4 VERIFICA LE TUE CONOSCENZE 1A 4A 7C 10 D 13 D 2B 5C 8A 11 C 14 B 3D 6C 9B 12 B VERIFICA LE TUE ABILITÀ 15 Un carbonio asimmetrico è un atomo di carbonio
Chimica organica: stereoisomeria ottica Capitolo C4 VERIFICA LE TUE CONOSCENZE 1A 4A 7C 10 D 13 D 2B 5C 8A 11 C 14 B 3D 6C 9B 12 B VERIFICA LE TUE ABILITÀ 15 Un carbonio asimmetrico è un atomo di carbonio
Stereochimica. Atomi di carbonio tetraedrici e loro immagini speculari. Le molecole del tipo CH 3
 Figura Stereochimica Stereochimica: enantiomeri Atomi di carbonio tetraedrici e loro immagini speculari. Le molecole del tipo CH 3 X e CH 2 XY sono identiche alle loro immagini speculari, ma una molecola
Figura Stereochimica Stereochimica: enantiomeri Atomi di carbonio tetraedrici e loro immagini speculari. Le molecole del tipo CH 3 X e CH 2 XY sono identiche alle loro immagini speculari, ma una molecola
Chimica Organica. Stereochimica ISOMERI ISOMERI DI STRUTTURA STEREOISOMERI DIASTEREOMERI ENANTIOMERI ISOMERI CIS-TRANS CONFORMERI ROTAMERI
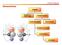 Chimica rganica Stereochimica ISMERI ISMERI DI STRUTTURA STEREISMERI DIASTEREMERI ENANTIMERI ISMERI CIS-TRANS CNFRMERI RTAMERI Stereoisomeri Composti con la stessa connessione tra gli atomi, ma con una
Chimica rganica Stereochimica ISMERI ISMERI DI STRUTTURA STEREISMERI DIASTEREMERI ENANTIMERI ISMERI CIS-TRANS CNFRMERI RTAMERI Stereoisomeri Composti con la stessa connessione tra gli atomi, ma con una
02/10/2018. di catena. di posizione. strutturali. di gruppo funzionale. isomeri. geometrici. stereoisomeri. ottici
 Quando due composti organici sono costituiti dagli stessi atomi ma possiedono una struttura differente si definiscono ISOMERI. Esistono diversi tipi di isomeria: di catena strutturali di posizione isomeri
Quando due composti organici sono costituiti dagli stessi atomi ma possiedono una struttura differente si definiscono ISOMERI. Esistono diversi tipi di isomeria: di catena strutturali di posizione isomeri
Alcani e cicloalcani. Nomenclatura e nomi comuni Struttura e proprietà Reazioni
 Alcani e cicloalcani Nomenclatura e nomi comuni Struttura e proprietà Reazioni Alcani Gli orbitali atomici hanno forme ben definite. Gli orbitali S sono sferici con gli e - confinati in una regione sferica
Alcani e cicloalcani Nomenclatura e nomi comuni Struttura e proprietà Reazioni Alcani Gli orbitali atomici hanno forme ben definite. Gli orbitali S sono sferici con gli e - confinati in una regione sferica
ISOMERIA GEOMETRICA NEGLI ALCHENI
 ISOMERIA GEOMETRIA NEGLI ALENI Negli alcheni, la rotazione è ancora possibile attorno ai legami - semplici, ma non attorno ai legami doppi = propene.. Anche se la rotazione intorno al doppio legame non
ISOMERIA GEOMETRIA NEGLI ALENI Negli alcheni, la rotazione è ancora possibile attorno ai legami - semplici, ma non attorno ai legami doppi = propene.. Anche se la rotazione intorno al doppio legame non
21/03/2011 STEREOCHIMICA. Gli stereoisomeri differiscono unicamente per la disposizione degli atomi nello spazio. Diastereoisomeri.
 L esistenza degli enantiomeri è legata ad una precisa proprietà strutturale delle molecole:le molecole devono essere chirali Una molecola chirale è una molecola che non è sovrapponibile alla sua immagine
L esistenza degli enantiomeri è legata ad una precisa proprietà strutturale delle molecole:le molecole devono essere chirali Una molecola chirale è una molecola che non è sovrapponibile alla sua immagine
Diagramma che riassume i diversi tipi di isomeri. N.B. Gli isomeri costituzionali (o isomeri di struttura: es. n-propile /isopropile non sono
 STEREOCHIMICA La stereochimica studia la struttura molecolare nelle tre dimensioni, cioè nello spazio. Un aspetto della stereochimica è la STEREOISOMERIA. Diagramma che riassume i diversi tipi di isomeri.
STEREOCHIMICA La stereochimica studia la struttura molecolare nelle tre dimensioni, cioè nello spazio. Un aspetto della stereochimica è la STEREOISOMERIA. Diagramma che riassume i diversi tipi di isomeri.
Tipologie di formule chimiche
 CHIMICA ORGANICA Tipologie di formule chimiche FORMULA RAZIONALE Tipo di formula che utilizza una rappresentazione analoga alla formula bruta per quei gruppi di atomi sulla cui disposizione non vi possono
CHIMICA ORGANICA Tipologie di formule chimiche FORMULA RAZIONALE Tipo di formula che utilizza una rappresentazione analoga alla formula bruta per quei gruppi di atomi sulla cui disposizione non vi possono
Gli Alcheni : struttura e nomenclatura
 Gli Alcheni : struttura e nomenclatura Alcheni Gli alcheni sono idrocarburi che contengono un doppio legame carbonio-carbonio sono anche detti olefine o idrocarburi insaturi La formula molecolare è n H
Gli Alcheni : struttura e nomenclatura Alcheni Gli alcheni sono idrocarburi che contengono un doppio legame carbonio-carbonio sono anche detti olefine o idrocarburi insaturi La formula molecolare è n H
CHIMICA ORGANICA. L isomeria
 1 B-ISOMERIA IMIA ORGANIA L isomeria Gli isomeri sono composti diversi (ciascuno con proprietà fisiche e chimiche proprie) che hanno tuttavia la stessa composizione chimica e quindi la stessa formula chimica
1 B-ISOMERIA IMIA ORGANIA L isomeria Gli isomeri sono composti diversi (ciascuno con proprietà fisiche e chimiche proprie) che hanno tuttavia la stessa composizione chimica e quindi la stessa formula chimica
Esercitazione n. 6 Selezione risposte sulla stereoisomeria ottica. 2. Sistemate un piano di simmetria in ciascuna delle seguenti strutture:
 .. Esercitazione n. 6 Selezione risposte sulla stereoisomeria ottica.. Sistemate un piano di simmetria in ciascuna delle seguenti strutture: a) -------------- b) c) d) 5. Indicare con un asterisco gli
.. Esercitazione n. 6 Selezione risposte sulla stereoisomeria ottica.. Sistemate un piano di simmetria in ciascuna delle seguenti strutture: a) -------------- b) c) d) 5. Indicare con un asterisco gli
Chimica Organica. Definizione. La chimica organica è la chimica dei composti contenenti carbonio
 Chimica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio I carbonati, il biossido di carbonio e i cianuri metallici sono un eccezione in quanto vengono classificati
Chimica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio I carbonati, il biossido di carbonio e i cianuri metallici sono un eccezione in quanto vengono classificati
Teoria degli orbitali. Lo spazio intorno al nucleo in cui è possibile trovare con la massima probabilità gli elettroni viene chiamato orbitale.
 Teoria degli orbitali Lo spazio intorno al nucleo in cui è possibile trovare con la massima probabilità gli elettroni viene chiamato orbitale. orbitale nucleo STPA-Chimica Organica 1 L orbitale 1s Gli
Teoria degli orbitali Lo spazio intorno al nucleo in cui è possibile trovare con la massima probabilità gli elettroni viene chiamato orbitale. orbitale nucleo STPA-Chimica Organica 1 L orbitale 1s Gli
Chimica Organica. In passato, i composti chimici erano suddivisi in due grandi gruppi,
 Chimica Organica In passato, i composti chimici erano suddivisi in due grandi gruppi, inorganici e organici, in base alla loro origine. La chimica organica diveniva così la chimica dei composti del carbonio.
Chimica Organica In passato, i composti chimici erano suddivisi in due grandi gruppi, inorganici e organici, in base alla loro origine. La chimica organica diveniva così la chimica dei composti del carbonio.
Conformazione degli alcani
 onformazione degli alcani La conformazione di un alcano si riferisce alla disposizione tridimensionale degli atomi che risulta dalla rotazione attorno al legame -. Nonostante in una molecola possano esservi
onformazione degli alcani La conformazione di un alcano si riferisce alla disposizione tridimensionale degli atomi che risulta dalla rotazione attorno al legame -. Nonostante in una molecola possano esservi
La Glicobiologia è lo studio della struttura, della biosintesi e della biologia degli zuccheri e dei glicani, ampiamente diffusi in natura.
 La Glicobiologia è lo studio della struttura, della biosintesi e della biologia degli zuccheri e dei glicani, ampiamente diffusi in natura. Gli zuccheri sono componenti essenziali di tutti gli organismi
La Glicobiologia è lo studio della struttura, della biosintesi e della biologia degli zuccheri e dei glicani, ampiamente diffusi in natura. Gli zuccheri sono componenti essenziali di tutti gli organismi
Configurazione. Conformazione
 Configurazione (Mislow,, 1965) Posizione relativa degli atomi nello spazio cha caratterizza un particolare stereoisomero Enantiomeri: : configurazione opposta Diastereoisomeri: : configurazione diversa
Configurazione (Mislow,, 1965) Posizione relativa degli atomi nello spazio cha caratterizza un particolare stereoisomero Enantiomeri: : configurazione opposta Diastereoisomeri: : configurazione diversa
Alcheni: struttura e proprietà
 Chimica Organica Informazione Scientifica sul Farmaco Alcheni: struttura e proprietà Organic Chemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: struttura degli alcheni nomenclatura proprietà fisiche
Chimica Organica Informazione Scientifica sul Farmaco Alcheni: struttura e proprietà Organic Chemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: struttura degli alcheni nomenclatura proprietà fisiche
Classificazione degli idrocarburi
 Classificazione degli idrocarburi ALCANI Alcani: idrocarburi saturi contenenti solo legami semplici carbonio-carbonio (tutti i carboni sono ibridati sp3). Modelli molecolari di etano, propano e butano.
Classificazione degli idrocarburi ALCANI Alcani: idrocarburi saturi contenenti solo legami semplici carbonio-carbonio (tutti i carboni sono ibridati sp3). Modelli molecolari di etano, propano e butano.
- il DNA, la molecola che contiene l informazione genetica, - le proteine dei nostro organismo ( proteine dei muscoli, della pelle, gli enzimi),
 La chimica organica è la chimica dei composti del carbonio, che sono i mattoni con cui sono costruiti tutti i corpi viventi della terra. Questi composti comprendono ad esempio - il DNA, la molecola che
La chimica organica è la chimica dei composti del carbonio, che sono i mattoni con cui sono costruiti tutti i corpi viventi della terra. Questi composti comprendono ad esempio - il DNA, la molecola che
Un oggetto si definisce chirale se non è sovrapponibile alla. propria immagine speculare (mano destra e mano sinistra). Non
 Illustrate la chiralità delle molecole: Chiralità Un oggetto si definisce chirale se non è sovrapponibile alla propria immagine speculare (mano destra e mano sinistra). Non c è un piano di simmetria La
Illustrate la chiralità delle molecole: Chiralità Un oggetto si definisce chirale se non è sovrapponibile alla propria immagine speculare (mano destra e mano sinistra). Non c è un piano di simmetria La
CHIMICA ORGANICA CHIMICA DEL CARBONIO
 CHIMICA ORGANICA CHIMICA DEL CARBONIO Fino al 1828 con il termine organico si indicavano le sostanze prodotte dagli organismi viventi, mentre si classificavano come inorganiche tutte le altre Dopo il 1828
CHIMICA ORGANICA CHIMICA DEL CARBONIO Fino al 1828 con il termine organico si indicavano le sostanze prodotte dagli organismi viventi, mentre si classificavano come inorganiche tutte le altre Dopo il 1828
Gli idrocarburi contengono solo atomi di carbonio e di idrogeno. Gli idrocarburi alifatici hanno molecole lineari (talora ramificate) mentre quelli
 Gli idrocarburi contengono solo atomi di carbonio e di idrogeno. Gli idrocarburi alifatici hanno molecole lineari (talora ramificate) mentre quelli ciclici presentano molecole ad anello. Se hanno tutti
Gli idrocarburi contengono solo atomi di carbonio e di idrogeno. Gli idrocarburi alifatici hanno molecole lineari (talora ramificate) mentre quelli ciclici presentano molecole ad anello. Se hanno tutti
isomeria di struttura isomeria di posizione isomeria di catena stereoisomeria isomeria di conformazione isomeria di configurazione 'isomeria ottica
 ISOMERIA L'isomeria di struttura è connessa al diverso modo in cui gli atomi di due o più composti si legano tra loro in sequenza. Ci sono due forme: isomeria di posizione e isomeria di catena. La stereoisomeria
ISOMERIA L'isomeria di struttura è connessa al diverso modo in cui gli atomi di due o più composti si legano tra loro in sequenza. Ci sono due forme: isomeria di posizione e isomeria di catena. La stereoisomeria
Alcheni: struttura e reattività
 Alcheni: struttura e reattività Alcheni Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n 2n Alcheni in biologia ormone delle piante che induce la maturazione dei frutti costituente
Alcheni: struttura e reattività Alcheni Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n 2n Alcheni in biologia ormone delle piante che induce la maturazione dei frutti costituente
Alcheni: struttura e reattività
 Alcheni: struttura e reattività Alcheni Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n 2n Alcheni in biologia ormone delle piante che induce la maturazione dei frutti costituente
Alcheni: struttura e reattività Alcheni Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n 2n Alcheni in biologia ormone delle piante che induce la maturazione dei frutti costituente
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA)
 La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) IL CARBONIO E un non metallo, appartiene al IV gruppo ed al II periodo. Possiede 4 elettroni esterni per
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) IL CARBONIO E un non metallo, appartiene al IV gruppo ed al II periodo. Possiede 4 elettroni esterni per
Stereochimica. Molecole nello spazio
 Stereochimica Molecole nello spazio Stereoisomeri: definizioni Stereoisomeri: isomeri che hanno la medesima connettività tra gli atomi ma differente orientazione 3D degli atomi nello spazio. Stereoisomeri
Stereochimica Molecole nello spazio Stereoisomeri: definizioni Stereoisomeri: isomeri che hanno la medesima connettività tra gli atomi ma differente orientazione 3D degli atomi nello spazio. Stereoisomeri
Alcheni: struttura e reattività
 Alcheni: struttura e reattività Alcheni Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n H 2n Alcheni in biologia ormone delle piante che induce la maturazione dei frutti costituente
Alcheni: struttura e reattività Alcheni Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n H 2n Alcheni in biologia ormone delle piante che induce la maturazione dei frutti costituente
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 9 Il mondo del carbonio 3 Sommario 1. Esiste un enorme varietà di composti organici 2. Gli idrocarburi saturi: alcani e cicloalcani
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 9 Il mondo del carbonio 3 Sommario 1. Esiste un enorme varietà di composti organici 2. Gli idrocarburi saturi: alcani e cicloalcani
Stereochimica di alcani e cicloalcani. Stereochimica. Conformazioni, conformeri
 di alcani e cicloalcani Conformazioni, conformeri Due conformazioni dell etano. I differenti conformeri si interconvertono per rotazione attorno al legame C-C. 1 Rappresentazione a cavalletto e proiezione
di alcani e cicloalcani Conformazioni, conformeri Due conformazioni dell etano. I differenti conformeri si interconvertono per rotazione attorno al legame C-C. 1 Rappresentazione a cavalletto e proiezione
Idrocarburi Saturi. Alcani
 Idrocarburi Saturi Alcani IDROCARBURI I principali componenti del petrolio e del gas naturale, risorse dalle quali proviene la maggior parte dei combustibili per la produzione di energia sono idrocarburi,
Idrocarburi Saturi Alcani IDROCARBURI I principali componenti del petrolio e del gas naturale, risorse dalle quali proviene la maggior parte dei combustibili per la produzione di energia sono idrocarburi,
Contenuti della lezione:
 Alcheni e Alchini Contenuti della lezione: Aspetti generali e nomenclatura di alcheni e alchini Uso delle nomenclature cis/trans e E/Z per gli alcheni di-sostituiti e tri- o tetrasostituiti rispetivamente
Alcheni e Alchini Contenuti della lezione: Aspetti generali e nomenclatura di alcheni e alchini Uso delle nomenclature cis/trans e E/Z per gli alcheni di-sostituiti e tri- o tetrasostituiti rispetivamente
Alcheni: : struttura e reattività. Alcheni. Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n. H 2n. Alcheni in biologia
 Alcheni: : struttura e reattività Alcheni Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n H 2n Alcheni in biologia ormone delle piante che induce la maturazione dei frutti costituente
Alcheni: : struttura e reattività Alcheni Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n H 2n Alcheni in biologia ormone delle piante che induce la maturazione dei frutti costituente
Reazioni Stereospecifiche e Stereoselettive
 Reazioni Stereospecifiche e Stereoselettive La stereospecificità in chimica è la proprietà di una stessa reazione di generare stereoisomeri diversi partendo da stereoisomeri diversi. Si differenzia dalla
Reazioni Stereospecifiche e Stereoselettive La stereospecificità in chimica è la proprietà di una stessa reazione di generare stereoisomeri diversi partendo da stereoisomeri diversi. Si differenzia dalla
Configurazione. Conformazione
 Configurazione Posizione relativa degli atomi nello spazio che caratterizza un particolare stereoisomero Sono in numero limitato (in genere 2) Conformazione Particolare geometria di una molecola che dipende
Configurazione Posizione relativa degli atomi nello spazio che caratterizza un particolare stereoisomero Sono in numero limitato (in genere 2) Conformazione Particolare geometria di una molecola che dipende
Nome degli alcheni a catena lineare
 Gli alcheni sono idrocarboni insaturi. insaturi (almeno un doppio legame) idrocarboni (solo e ) n 2n 1-Esene 6 12 opyright 1999, Michael J. Wovkulich. All rights reserved. Nome degli alcheni a catena lineare
Gli alcheni sono idrocarboni insaturi. insaturi (almeno un doppio legame) idrocarboni (solo e ) n 2n 1-Esene 6 12 opyright 1999, Michael J. Wovkulich. All rights reserved. Nome degli alcheni a catena lineare
Idrocarburi insaturi. Alcheni
 Idrocarburi insaturi Alcheni Idrocarburi insaturi Un idrocarburo si dice insaturo quando possiede un numero di atomi di idrogeno minore al numero massimo possibile per un dato numero di atomi di carbonio.
Idrocarburi insaturi Alcheni Idrocarburi insaturi Un idrocarburo si dice insaturo quando possiede un numero di atomi di idrogeno minore al numero massimo possibile per un dato numero di atomi di carbonio.
Stereochimica di alcani e cicloalcani
 di alcani e cicloalcani Conformazioni, conformeri Due conformazioni dell etano. Le conformazioni sono arrangiamenti diversi di atomi che interconvertono per rotazione attorno al legame C-C. Rappresentazione
di alcani e cicloalcani Conformazioni, conformeri Due conformazioni dell etano. Le conformazioni sono arrangiamenti diversi di atomi che interconvertono per rotazione attorno al legame C-C. Rappresentazione
Chimica Organica. Studio dei composti del CARBONIO
 Chimica Organica Studio dei composti del CARBONIO 1 Contengono C, H e possono contenere N, O, S Carbonio legato covalentemente ad un metallo Tutti gli elementi possibili Composti organici 2 Perché si formano
Chimica Organica Studio dei composti del CARBONIO 1 Contengono C, H e possono contenere N, O, S Carbonio legato covalentemente ad un metallo Tutti gli elementi possibili Composti organici 2 Perché si formano
IBRIDAZIONE DEL CARBONIO NEGLI ALCANI PREMESSA: COSA SONO GLI ORBITALI IBRIDI.
 ALCANI Gli alcani sono composti organici costituiti solamente da carbonio e idrogeno (per questo motivo appartengono alla più ampia classe degli idrocarburi), aventi formula bruta C n H (2n + 2). Gli alcani
ALCANI Gli alcani sono composti organici costituiti solamente da carbonio e idrogeno (per questo motivo appartengono alla più ampia classe degli idrocarburi), aventi formula bruta C n H (2n + 2). Gli alcani
G. Licini, Università di Padova. La riproduzione a fini commerciali è vietata
 CIALITA Una molecola è chirale quando non è sovrapponibile alla sua immagine speculare Immagine speculare = entità distinta Chiralità: proprietà PSEUSCALAE esta invariata con un operazione di simmetria
CIALITA Una molecola è chirale quando non è sovrapponibile alla sua immagine speculare Immagine speculare = entità distinta Chiralità: proprietà PSEUSCALAE esta invariata con un operazione di simmetria
Gli elettroni della molecola sono quindi descritti da
 IL LEGAME COVALENTE: TEORIA DELL ORBITALE MOLECOLARE La molecola è considerata come un insieme di nuclei ed elettroni e, attraverso la valutazione delle reciproche interazioni, la teoria dell orbitale
IL LEGAME COVALENTE: TEORIA DELL ORBITALE MOLECOLARE La molecola è considerata come un insieme di nuclei ed elettroni e, attraverso la valutazione delle reciproche interazioni, la teoria dell orbitale
Alcani e Cicloalcani
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alcani e Cicloalcani Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alcani e Cicloalcani Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e
IDROCARBURI INSATURI: GLI ALCHENI HANNO ALMENO UN DOPPIO LEGAME NELLA STRUTTURA NOMENCLATURA: RADICE COME NEGLI IDROCARBURI, DESINENZA -ENE
 IDRCARBURI INSATURI: GLI ALCENI ANN ALMEN UN DPPI LEGAME NELLA STRUTTURA NMENCLATURA: RADICE CME NEGLI IDRCARBURI, DESINENZA -ENE butano 2-butene o but-2-ene Esempi di nomenclatura degli alcheni Esempi
IDRCARBURI INSATURI: GLI ALCENI ANN ALMEN UN DPPI LEGAME NELLA STRUTTURA NMENCLATURA: RADICE CME NEGLI IDRCARBURI, DESINENZA -ENE butano 2-butene o but-2-ene Esempi di nomenclatura degli alcheni Esempi
Introduzione alla Chimica Organica. Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display.
 Introduzione alla Chimica Organica Copyright The McGraw-ill Companies, Inc. Permission required for reproduction or display. 1 Elementi Comuni nei Composti Organici 2 Classificazione degli idrocarburi
Introduzione alla Chimica Organica Copyright The McGraw-ill Companies, Inc. Permission required for reproduction or display. 1 Elementi Comuni nei Composti Organici 2 Classificazione degli idrocarburi
Gruppi funzionali. Gruppi funzionali
 Gruppi funzionali Gruppi funzionali La reattività chimica di ogni molecola organica, indipendentemente dalle sue dimensioni o dalla sua complessità, è determinata dai gruppi funzionali che essa contiene
Gruppi funzionali Gruppi funzionali La reattività chimica di ogni molecola organica, indipendentemente dalle sue dimensioni o dalla sua complessità, è determinata dai gruppi funzionali che essa contiene
IDROCARBURI: classificazione
 ALCANI 1 IDROCARBURI: classificazione 2 ALCANI Formula bruta: C n H 2n+2 1 C CH 4 2 C C 2 H 6 3 C C 3 H 8 4 C C 4 H 10 3 ALCANI: ibridazione Orbitali s, p e sp 3 z orbitale 2s y x z z z orbitali 2p y x
ALCANI 1 IDROCARBURI: classificazione 2 ALCANI Formula bruta: C n H 2n+2 1 C CH 4 2 C C 2 H 6 3 C C 3 H 8 4 C C 4 H 10 3 ALCANI: ibridazione Orbitali s, p e sp 3 z orbitale 2s y x z z z orbitali 2p y x
. C ISOMERIA GEOMETRICA C H C H H C H C C C H C H
 ISOMRIA GOMTRIA egli alcheni, la rotazione è ancora possibile attorno ai legami - semplici, ma non attorno ai legami doppi = propene.. Anche se la rotazione intorno al doppio legame non è possibile, esiste
ISOMRIA GOMTRIA egli alcheni, la rotazione è ancora possibile attorno ai legami - semplici, ma non attorno ai legami doppi = propene.. Anche se la rotazione intorno al doppio legame non è possibile, esiste
ALCHENI CICLOALCHENI. C n H 2n. C n H 2n-2 C C. Gruppo funzionale degli alcheni (idrocarburi insaturi): doppio legame carbonio-carbonio
 ALCENI C n 2n CICLOALCENI C n 2n-2 C C Gruppo funzionale degli alcheni (idrocarburi insaturi): doppio legame carbonio-carbonio I carboni coinvolti nel doppio legame sono ibridati sp 2 : per cui sono legati
ALCENI C n 2n CICLOALCENI C n 2n-2 C C Gruppo funzionale degli alcheni (idrocarburi insaturi): doppio legame carbonio-carbonio I carboni coinvolti nel doppio legame sono ibridati sp 2 : per cui sono legati
Riassunto delle lezioni precedenti..
 Riassunto delle lezioni precedenti.. Chimica del Carbonio L atomo di Carbonio può formare legami singoli, legami doppi e legami tripli IDROCARBURI formati solo da carbonio e idrogeno Si dividono in 3 classi:
Riassunto delle lezioni precedenti.. Chimica del Carbonio L atomo di Carbonio può formare legami singoli, legami doppi e legami tripli IDROCARBURI formati solo da carbonio e idrogeno Si dividono in 3 classi:
IDROCARBURI. Alcani Alcheni Alchini Areni. Tipo di legami carboniocarbonio. Solo legami semplici. Uno o più tripli legami. Uno o più doppi legami
 IMICA ORGANICA La chimica del carbonio, per le proprietà del carbonio di formare un numero grandissimo di composti con proprietà diverse, costituisce una branca della chimica, denominata chimica organica.
IMICA ORGANICA La chimica del carbonio, per le proprietà del carbonio di formare un numero grandissimo di composti con proprietà diverse, costituisce una branca della chimica, denominata chimica organica.
Gli idrocarburi sono composti organici, che contengono soltanto atomi di carbonio e di idrogeno. Gli atomi di carbonio (C) sono legati tra loro a
 Gli idrocarburi sono composti organici, che contengono soltanto atomi di carbonio e di idrogeno. Gli atomi di carbonio (C) sono legati tra loro a formare lo scheletro della molecola, mentre gli atomi di
Gli idrocarburi sono composti organici, che contengono soltanto atomi di carbonio e di idrogeno. Gli atomi di carbonio (C) sono legati tra loro a formare lo scheletro della molecola, mentre gli atomi di
2. La Struttura dei Composti Organici e le caratteristiche chimico-fisiche
 Università degli Studi di Bari Dipartimento di Farmacia-SdF TENIE EBISTIE 2. La Struttura dei omposti rganici e le caratteristiche chimico-fisiche 5. Geometria molecolare. Stereochimica I Parte onformazione
Università degli Studi di Bari Dipartimento di Farmacia-SdF TENIE EBISTIE 2. La Struttura dei omposti rganici e le caratteristiche chimico-fisiche 5. Geometria molecolare. Stereochimica I Parte onformazione
2. La Struttura dei Composti Organici e le. caratteristiche chimico-fisiche
 Scienze e tecnologie erboristiche e dei prodotti per la salute (STEPS) himica rganica - 2. La Struttura dei omposti rganici e le Prof. Giuseppe Gerardo arbonara caratteristiche chimico-fisiche 5. Geometria
Scienze e tecnologie erboristiche e dei prodotti per la salute (STEPS) himica rganica - 2. La Struttura dei omposti rganici e le Prof. Giuseppe Gerardo arbonara caratteristiche chimico-fisiche 5. Geometria
Alcani. Es. CH 3 CH 2 CH 2 CH 3
 Alcani Gli alcani sono i composti organici più semplici costituiti solo da atomi di e di (Idrocarburi); Sono composti saturi poiché ogni atomo di carbonio è legato al numero massimo possibile (4) di altri
Alcani Gli alcani sono i composti organici più semplici costituiti solo da atomi di e di (Idrocarburi); Sono composti saturi poiché ogni atomo di carbonio è legato al numero massimo possibile (4) di altri
2) Scrivere il nome sistematico per i composti elencati di seguito:
 Chimica Organica Alcheni 1) Disegnare la struttura per le molecole elencate: a. 3,3- dimetilciclopentene c. etil vinil etere b. 6- bromo- 2,3- dimetil- 2- esene d. allil alcol 2) Scrivere il nome sistematico
Chimica Organica Alcheni 1) Disegnare la struttura per le molecole elencate: a. 3,3- dimetilciclopentene c. etil vinil etere b. 6- bromo- 2,3- dimetil- 2- esene d. allil alcol 2) Scrivere il nome sistematico
CONTENUTI DELLA LEZIONE DI OGGI:
 CONTENUTI DELLA LEZIONE DI OGGI: 1. Isomeria (chiralità, enantiomeri, configurazione assoluta, nomenclatura R, S) 2. Analisi miscela di enantiomeri - polarimetria - cromatografia chirale - NMR 3. Risoluzione
CONTENUTI DELLA LEZIONE DI OGGI: 1. Isomeria (chiralità, enantiomeri, configurazione assoluta, nomenclatura R, S) 2. Analisi miscela di enantiomeri - polarimetria - cromatografia chirale - NMR 3. Risoluzione
Come scrivere correttamente le rappresentazioni tridimensionali (formalismo dei cunei pieni e cunei tratteggiati) e le proiezioni di Fischer
 ome scrivere correttamente le rappresentazioni tridimensionali (formalismo dei cunei pieni e cunei tratteggiati) e le proiezioni di Fischer Supponiamo di dover disegnare, usando la rappresentazione tridimensionale
ome scrivere correttamente le rappresentazioni tridimensionali (formalismo dei cunei pieni e cunei tratteggiati) e le proiezioni di Fischer Supponiamo di dover disegnare, usando la rappresentazione tridimensionale
ISOMERI. Stereoisomeri. Isomeri Cos/tuzionali. Conformeri. Geometrici. configurazionali. Enan/omeri. Diastereoisomeri
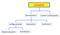 ISOMEI Stereoisomeri Isomeri Cos/tuzionali configurazionali Geometrici Conformeri Diastereoisomeri Enan/omeri Chiralità Dato un Piano di iflessione ( specchio ) è possibile o=enere per qualunque ogge=o
ISOMEI Stereoisomeri Isomeri Cos/tuzionali configurazionali Geometrici Conformeri Diastereoisomeri Enan/omeri Chiralità Dato un Piano di iflessione ( specchio ) è possibile o=enere per qualunque ogge=o
4. Stereoisomeria ottica o enantiomeria
 . Stereoisomeria ottica o enantiomeria Fenomeno per cui due (o più) stereoisomeri sono distinguibili solo per via ottica o enzimatica. Nel 1850 Biot scopre l esistenza, in alcuni composti organici, dell
. Stereoisomeria ottica o enantiomeria Fenomeno per cui due (o più) stereoisomeri sono distinguibili solo per via ottica o enzimatica. Nel 1850 Biot scopre l esistenza, in alcuni composti organici, dell
Esercizi con i modelli molecolari
 MPLEMENTI Esercizi con i modelli molecolari Gli esercizi riportati in questa appendice sono finalizzati ad agevolare l apprendimento della natura tridimensionale delle molecole. Per eseguirli è necessario
MPLEMENTI Esercizi con i modelli molecolari Gli esercizi riportati in questa appendice sono finalizzati ad agevolare l apprendimento della natura tridimensionale delle molecole. Per eseguirli è necessario
Idrocarburi: composti organici che hanno nella loro struttura solo atomo di C o H
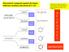 Idrocarburi: composti organici che hanno nella loro struttura solo atomo di C o H Alifatici: deriva dal greco aleifar cioè unguento; questo perché molti grassi contengono lunghe catene carboniose. GLI
Idrocarburi: composti organici che hanno nella loro struttura solo atomo di C o H Alifatici: deriva dal greco aleifar cioè unguento; questo perché molti grassi contengono lunghe catene carboniose. GLI
Esercitazione sulle conformazioni di alcani e cicloesani
 Esercitazione sulle conformazioni di alcani e cicloesani 1. Disegnare la molecola completa del butano, nella conformazione più favorevole per tutti i legami - (usare i legami a cuneo e tratteggiati). 2.
Esercitazione sulle conformazioni di alcani e cicloesani 1. Disegnare la molecola completa del butano, nella conformazione più favorevole per tutti i legami - (usare i legami a cuneo e tratteggiati). 2.
Gli Alcheni : struttura e nomenclatura
 Gli Alcheni : struttura e nomenclatura Alcheni Gli alcheni sono idrocarburi che contengono un doppio legame carbonio-carbonio sono anche detti olefine o idrocarburi insaturi La formula molecolare è C n
Gli Alcheni : struttura e nomenclatura Alcheni Gli alcheni sono idrocarburi che contengono un doppio legame carbonio-carbonio sono anche detti olefine o idrocarburi insaturi La formula molecolare è C n
CHIMICA delle MACROMOLECOLE BIOLOGICHE
 Progetto Tandem 2016-17 GIOVANNI GOTTE Biochimica/BIO-10, Università degli Studi di Verona CIMICA delle MACROMOLECOLE BIOLOGICE CIMICA ORGANICA CE COS E LA CIMICA ORGANICA? La chimica organica descrive
Progetto Tandem 2016-17 GIOVANNI GOTTE Biochimica/BIO-10, Università degli Studi di Verona CIMICA delle MACROMOLECOLE BIOLOGICE CIMICA ORGANICA CE COS E LA CIMICA ORGANICA? La chimica organica descrive
Gruppi funzionali Un gruppo funzionale è un atomo o un gruppo di atomi con proprietà chimiche e fisiche tipiche. E
 Gruppi funzionali Gruppi funzionali La reattività chimica di ogni molecola organica, indipendentemente dalle sue dimensioni o dalla sua complessità, è determinata dai gruppi funzionali che essa contiene
Gruppi funzionali Gruppi funzionali La reattività chimica di ogni molecola organica, indipendentemente dalle sue dimensioni o dalla sua complessità, è determinata dai gruppi funzionali che essa contiene
Idrocarburi Al A ifatici Ar A oma m tici
 GLI IDROCARBURI Gli idrocarburi sono i più semplici composti del carbonio con l'idrogeno. Sono le molecole di base della chimica organica poiché, oltre ad essere molto numerosi, tutti gli altri composti
GLI IDROCARBURI Gli idrocarburi sono i più semplici composti del carbonio con l'idrogeno. Sono le molecole di base della chimica organica poiché, oltre ad essere molto numerosi, tutti gli altri composti
ALIFATICI AROMATICI (Areni) POLIENI BENZENE e derivati CICLOALCHENI CICLOALCANI ALCHINI
 CIMICA ORGANICA IDROCARBURI Gli idrocarburi sono composti che contengono solo atomi di e C e, a seconda del tipo di legami chimici presenti nella molecola, possono essere suddivisi secondo il seguente
CIMICA ORGANICA IDROCARBURI Gli idrocarburi sono composti che contengono solo atomi di e C e, a seconda del tipo di legami chimici presenti nella molecola, possono essere suddivisi secondo il seguente
IDROCARBURI. Alcani Alcheni Alchini C-C C=C C C
 IDROCARBURI Alcani Alcheni Alchini C-C C=C C C Nomenclatura Degli idrocarburi saturi (Alcani) CH 4 Metano C 2 H 6 Etano C n H 2n+2 Si dicono alchilici quei gruppi che contengono un idrogeno in meno del
IDROCARBURI Alcani Alcheni Alchini C-C C=C C C Nomenclatura Degli idrocarburi saturi (Alcani) CH 4 Metano C 2 H 6 Etano C n H 2n+2 Si dicono alchilici quei gruppi che contengono un idrogeno in meno del
Idrocarburi Alifatici
 Idrocarburi Alifatici Alcano R-C 2 -C 2 -R C n 2n+2 Questo è il massimo rapporto /C per un dato numero di atomi di carbonio. Alchene R-C=C-R C n 2n Ogni doppio legame riduce il numero di atomi di idrogeno
Idrocarburi Alifatici Alcano R-C 2 -C 2 -R C n 2n+2 Questo è il massimo rapporto /C per un dato numero di atomi di carbonio. Alchene R-C=C-R C n 2n Ogni doppio legame riduce il numero di atomi di idrogeno
c. Disegnate le conformazioni eclissate e sfalsate intermedie
 1. Per la seguente molecola a. Disegnate la conformazione meno stabile b. Disegnate la conformazione piu stabile c. Disegnate le conformazioni eclissate e sfalsate intermedie d. Utilizzando le seguenti
1. Per la seguente molecola a. Disegnate la conformazione meno stabile b. Disegnate la conformazione piu stabile c. Disegnate le conformazioni eclissate e sfalsate intermedie d. Utilizzando le seguenti
Capitolo A1 Dal carbonio agli idrocarburi
 Quesiti e problemi 1 a) sp 3 ; b) sp 2 ; c) sp. 2 B, E 3 Ibridazione Legami Geometria sp 3 4 σ Tetraedrica sp 2 3 σ e 1 π Trigonale planare sp 2 σ e 2 π Lineare 4 5 6 7 8 C-1: sp 3 ; C-2: sp 2 ; C-3: sp
Quesiti e problemi 1 a) sp 3 ; b) sp 2 ; c) sp. 2 B, E 3 Ibridazione Legami Geometria sp 3 4 σ Tetraedrica sp 2 3 σ e 1 π Trigonale planare sp 2 σ e 2 π Lineare 4 5 6 7 8 C-1: sp 3 ; C-2: sp 2 ; C-3: sp
Composti formati esclusivamente dagli elementi Carbonio ed Idrogeno
 Alcani Composti formati esclusivamente dagli elementi Carbonio ed Idrogeno Alcani Sono il tipo di idrocarburi che contiene il maggior numero di atomi di per numero di atomi di C Sono anche detti idrocarburi
Alcani Composti formati esclusivamente dagli elementi Carbonio ed Idrogeno Alcani Sono il tipo di idrocarburi che contiene il maggior numero di atomi di per numero di atomi di C Sono anche detti idrocarburi
Capitolo 23 Dal carbonio agli idrocarburi
 Quesiti e problemi 1 a) sp 3 ; b) sp 2 ; c) sp. 2 B, E 3 Ibridazione Legami Geometria sp 3 4 σ Tetraedrica sp 2 3 σ e 1 π Trigonale planare sp 2 σ e 2 π Lineare 4 5 1 6 7 B 8 a) 1 e 2; b) tutte e tre;
Quesiti e problemi 1 a) sp 3 ; b) sp 2 ; c) sp. 2 B, E 3 Ibridazione Legami Geometria sp 3 4 σ Tetraedrica sp 2 3 σ e 1 π Trigonale planare sp 2 σ e 2 π Lineare 4 5 1 6 7 B 8 a) 1 e 2; b) tutte e tre;
