PERCORSO DIAGNOSTICO TERAPEUTICO CONDIVISO PER LA PRESCRIZIONE/UTILIZZO DI FATTORI STIMOLANTI LE COLONIE GRANULOCITARIE (G-CSF) A BREVETTO SCADUTO
|
|
|
- Bartolommeo Lombardo
- 8 anni fa
- Visualizzazioni
Transcript
1 PERCORSO DIAGNOSTICO TERAPEUTICO CONDIVISO PER LA PRESCRIZIONE/UTILIZZO DI FATTORI STIMOLANTI LE COLONIE GRANULOCITARIE (G-CSF) A BREVETTO SCADUTO Obiettivo: Luglio 2014 Il presente documento, condiviso e sottoscritto dalle Direzioni sanitarie delle Strutture di ricovero e cura del territorio dell ASL di Brescia, recepito dall ASL di Brescia con Decreto n. 435 del , individua i criteri di riferimento condivisi dai referenti specialisti delle strutture di ricovero e cura del territorio dell ASL di Brescia per la promozione della prescrizione e utilizzo di fattori stimolanti le colonie granulocitarie (G-CSF) a brevetto scaduto. Destinatari: L attuale posizione di EMA e AIFA esclude la sostituibilità terapeutica automatica e l intercambiabilità fra medicinali biologici di riferimento ( originators ) e prodotti biosimilari, riservando la scelta fra queste due opzioni terapeutiche alla decisione clinica del medico specialista prescrittore. In particolare per i pazienti già in trattamento con prodotti biotecnologici è necessario garantire la continuità di cura della terapia farmacologica senza sostituzione automatica del farmaco. Sono pertanto destinatari elettivi del presente documento i malati per i quali deve essere avviata una nuova terapia con fattori stimolanti la crescita granulocitaria (pazienti naive ), per i quali il ricorso a farmaci biosimilari diventa la scelta più appropriata per garantire la sostenibilità di un sistema che deve far fronte alla continua introduzione di nuove terapie ad alto costo. stimolanti le colonie granulocitarie (G-CSF) a brevetto scaduto Pag. 1
2 Quadro regolatorio: Con il termine biosimilare viene indicato un medicinale simile ad un prodotto biologico di riferimento già autorizzato nell Unione Europea e per il quale sia scaduta la copertura brevettuale I medicinali biosimilari differiscono dai farmaci generici che hanno strutture chimiche più semplici e che sono identici ai loro medicinali di riferimento. Il principio attivo di un biosimilare e quello del suo medicinale di riferimento sono la stessa sostanza biologica ma possono essere presenti differenze dovute alla loro natura complessa ed alle tecniche di produzione. Un biosimilare viene approvato quando è dimostrato che tale variabilità ed eventuali differenze non influiscano sulla sicurezza ed efficacia (EMA/837805/2011 del settembre 2012). Secondo gli attuali orientamenti regolatori in UE, un biosimilare e il suo prodotto di riferimento essendo ottenuti mediante modalità differenti, non sono identici, ma essenzialmente simili in termini di qualità, sicurezza ed efficacia. Le linee guida EMA richiedono che il programma di ricerca e sviluppo sia volto a dimostrare la biosimilarità intesa come la comparabilità tra un biosimilare ed il suo prodotto di riferimento attraverso l esercizio di comparabilità ovvero l insieme di una serie di procedure di confronto graduale che inizia con studi di qualità (comparabilità fisico-chimiche e biologiche) e prosegue con la valutazione della comparabilità non clinica (studi clinici non comparativi) e clinica (studi clinici comparativi). Tutti i farmaci autorizzati devono essere chiaramente identificabili attraverso una denominazione commerciale approvata ed attraverso un numero di lotto, al fine di garantirne la tracciabilità. I produttori di farmaci biologici e biosimilari sono tenuti ad istituire un sistema di farmacovigilanza per il monitoraggio della sicurezza del prodotto. Ogni azienda è tenuta a presentare un piano di gestione del rischio (EU-RMP), dove esplicita il profilo di sicurezza del farmaco, delinea le modalità con cui continuerà a stimolanti le colonie granulocitarie (G-CSF) a brevetto scaduto Pag. 2
3 monitorare la sicurezza e l efficacia del medicinale e le misure che intende introdurre per prevenire o minimizzare gli eventuali rischi durante l uso del medicinale, ivi compresa la misurazione dell efficacia nella pratica clinica. Ogni farmaco biosimilare sul mercato ha un EU-RMP in corso. L autorizzazione all immissione in commercio è comunque subordinata alla condizione di eseguire studi post-autorizzazione di sicurezza (PASS) e di efficacia (PAES). I farmaci biologici rappresentano una risorsa terapeutica essenziale per il trattamento di una varietà di malattie. Per motivi di sviluppo e di produzione del farmaco questi medicinali sono gravati da costi particolarmente onerosi per il SSN. La commercializzazione dei farmaci biosimilari può contribuire a migliorare l accesso ai farmaci biologici in due modi: 1) possono rendere farmaci biologici poco accessibili, perchè ad alto costo, più sostenibili e fruibili innescando meccanismi di competitività dei mercati che determinano la riduzione dei prezzi; 2) i risparmi generati dall utilizzo dei biosimilari possono contribuire al finanziamento di nuovi farmaci, rendendo più accessibile l innovazione terapeutica. Nel caso dei biosimilari per consuetudine ed analogia con i farmaci equivalenti la negoziazione del prezzo ha come riferimento una riduzione obbligatoria del prezzo pari ad almeno il 20% rispetto al prezzo del farmaco di riferimento. In Italia la posizione dell AIFA chiarisce che i medicinali biologici e biosimilari non possono essere considerati alla stregua dei farmaci equivalenti escludendo quindi la sostituibilità terapeutica automatica (cioè la pratica per cui il farmacista ha la facoltà, conformemente a norme nazionali e locali, di dispensare al posto del medicinale prescritto un farmaco equivalente senza consultare il medico prescrittore). Di conseguenza la scelta di trattamento con un farmaco biologico di riferimento o con un biosimilare rimane decisione clinica affidata al medico specialista prescrittore. stimolanti le colonie granulocitarie (G-CSF) a brevetto scaduto Pag. 3
4 Criteri di riferimento condivisi: - Area Oncologica I fattori di crescita della linea granulocitaria sono un supporto fondamentale per l oncologo medico impegnato nel trattamento della citopenia da chemioterapia. Il corretto utilizzo di tali farmaci sia a scopo profilattico che terapeutico ha un ruolo di primaria importanza nella riduzione della morbidità e mortalità da chemioterapia. I fattori di crescita granulocitaria sono raccomandati nella profilassi primaria di pazienti che ricevono regimi chemioterapici ad alto rischio di neutropenia (20%). La prescrizione di questi farmaci a scopo preventivo in caso di rischio moderato di neutropenia (10-20%) deve essere effettuata valutando la presenza di fattori di rischio indipendenti (età, comorbidità etc). L eleggibilità del paziente al trattamento profilattico deve essere rivalutata ad ogni ciclo di terapia. Situazioni aggiuntive in cui può essere presa in considerazione la profilassi secondaria sono: 1) una riduzione della riserva midollare dovuta a precedente radioterapia su >20% del midollo osseo, 2) infezione HIV La profilassi primaria deve iniziare ore dal termine della chemioterapia e la somministrazione quotidiana deve continuare sino al raggiungimento di una quota di neutrofili >1000/mL dopo il nadir. Nel caso si impieghi una formulazione peghilata, questa andrà somministrata in monosomministrazione tra le 24 e le 72 ore dopo il termine della chemioterapia. La somministrazione dei fattori di crescita granulocitari è controindicata 48 ore prima la somministrazione del ciclo successivo di chemioterapia. L impiego di questi farmaci nella profilassi secondaria in pazienti che hanno avuto un episodio di neutropenia febbrile va effettuata nei casi in cui il mantenimento della dose (dose dei farmaci e cicli) può influenzare la prognosi dei pazienti. L utilizzo dei fattori di crescita granulocitari non è raccomandato in caso di granulocitopenia febbrile di grado 4 in associazione alla terapia antibiotica. stimolanti le colonie granulocitarie (G-CSF) a brevetto scaduto Pag. 4
5 L uso può essere considerato in pazienti a maggior rischio di morbilità/mortalità allo scopo di ridurre la durata della neutropenia, il rischio infettivo, l ospedalizzazione. In questo contesto terapeutico l attività di farmacovigilanza assume particolare rilevanza, in quanto risulta necessario rilevare nel real world setting l efficacia e la sicurezza del biosimilare riportando attentamente gli eventi avversi, in particolare distinguendo tra quelli che si verificano nei pazienti in trattamento adiuvante e quelli che si presentano nei pazienti affetti da malattia metastatica. - Area Ematologica Due sono gli ambiti ematologici principali di impiego dei fattori di crescita granulocitaria (G-CSF) (indicazione d uso): - la terapia e la profilassi della neutropenia in corso di trattamento chemioradioterapico - la mobilizzazione di cellule staminali, autologhe o da donatore volontario, per il trapianto L uso di Filgrastim nella terapia della neutropenia da chemioterapia o post-trapianto è consolidato e di efficacia documentata. Secondo le raccomandazioni prodotte nel 2007 dall EMA, l efficacia clinica del GCSF (Granulocyte-Colony Stimulating Factors) biosimilare deve essere documentata attraverso la comparabilità con il G-CSF branded per l indicazione riduzione della durata della neutropenia da chemioterapia. La riduzione della durata rappresenta l obiettivo primario, mentre l incidenza di neutropenia febbrile, di infezioni e la dose cumulativa di G-CSF sono secondari. Numerose evidenze scientifiche di efficacia e sicurezza d impiego del filgrastim biosimilare in questo ambito si sono rese disponibili negli ultimi anni. Considerando il breve periodo di osservazione dalla commercializzazione del prodotto biosimilare e le stimolanti le colonie granulocitarie (G-CSF) a brevetto scaduto Pag. 5
6 potenziali differenze in termini di immunogenicità, pur in presenza di dimostrati noninferiorità terapeutica e vantaggio economico, si ribadisce la necessità di prevedere un piano di risk management e farmacovigilanza, allo scopo di catturare gli eventi avversi seri rari (rottura splenica, anafilassi, capillary leak syndrome ) ed i casi di mancata efficacia, come raccomandato dall EMA. Secondo le indicazioni dell EMA, il filgrastim biosimilare ha mantenuto l indicazione della molecola originator nella mobilizzazione di cellule staminali, autologhe o da donatore, in virtù dell esercizio di comparabilità richiesto dall EMA per estrapolazione dell indicazione riduzione della durata della neutropenia da chemioterapia : dal momento che il meccanismo d azione per tutte le indicazioni licenziate si presume sovrapponibile, l EMA prevede l estrapolazione di efficacia una volta documentata la non-inferiorità per l indicazione sopracitata. Numerosi studi prodotti negli ultimi anni, hanno confermato l efficacia e la sicurezza del Filgrastim biosimilare come agente mobilizzante, sia in associazione alla chemioterapia che nel donatore sano, oltrechè nell attecchimento post-trapianto. Tuttavia diversi organismi scientifici hanno sollevato perplessità nell impiego di Filgrastim biosimilare nella mobilizzazione di cellule staminali nel donatore sano; pertanto, prudenzialmente al momento e sino a che non siano disponibili ulteriori evidenze, può essere preferibile l utilizzo dell originator nel donatore sano. stimolanti le colonie granulocitarie (G-CSF) a brevetto scaduto Pag. 6
7 Farmacovigilanza e gestione del rischio Il programma di ricerca e sviluppo dei farmaci biosimilari è incentrato sulla dimostrazione della comparabilità rispetto al prodotto di riferimento (originator), attraverso un continuo e graduale esercizio di comparabilità, che inizia con gli studi di qualità (comparabilità fisico-chimica e biofarmaceutica) e prosegue con la valutazione della comparabilità non-clinica (studi non clinici comparativi) e clinica (studi clinici comparativi). Tuttavia gli studi clinici pre-marketing sono tipicamente disegnati e dimensionati per valutare il grado di comparabilità del biosimilare rispetto ad endpoints di efficacia, mentre la valutazione del grado di comparabilità da un punto di vista della sicurezza, in particolare per quanto concerne le reazioni avverse rare non dose-dipendenti, necessita di ulteriore approfondimento a livello post-marketing nella reale pratica clinica. La nuova normativa europea di farmacovigilanza (Direttiva 2012/84/EC, Regolamento 1235/2010, Regolamento di esecuzione 520/2012) stabilisce che l autorizzazione all'immissione in commercio (AIC) possa essere subordinata alla condizione di eseguire studi post-autorizzazione di sicurezza (PASS) e ogni azienda è tenuta a presentare, unitamente alla domanda di autorizzazione all'immissione in commercio, un piano di gestione del rischio ( Risk Management Plan, RMP). L RMP deve esplicitare in dettaglio il sistema di gestione del rischio, descrivendo il profilo di sicurezza del biosimilare, tenendo conto anche del profilo di sicurezza noto del corrispondente medicinale di riferimento, e delineare le modalità con cui il produttore continuerà a monitorare la sicurezza del medicinale e le misure che i titolari dell autorizzazione intendono introdurre per prevenire o minimizzare gli eventuali rischi durante l'uso del medicinale. Gli RMPs dei fattori stimolanti le colonie granulocitarie (G-CSF) biosimilari sono focalizzati in particolare sulle strategie di minimizzazione del rischio di sindrome da aumentata permeabilità capillare (CLS) in pazienti con tumore e in donatori sani, visti stimolanti le colonie granulocitarie (G-CSF) a brevetto scaduto Pag. 7
8 i recenti casi di reazione avverse ad esito fatale. Inoltre sono previste misure per la gestione del rischio di leucocitosi, polmonite interstiziale e di altre reazioni avverse più comuni. In questo scenario di massima attenzione alla rilevazione di nuovi segnali riguardanti possibili evoluzioni del profilo rischio/efficacia dei prodotti biosimilari, risulta di fondamentale importanza rafforzare i processi di segnalazione di sospette reazioni avverse, coinvolgendo a diversi livelli tutta la comunità: pazienti, prescrittori, operatori sanitari, aziende farmaceutiche, istituzioni. Le singole segnalazioni spontanee di reazioni avverse sono da interpretare come possibili associazioni tra evento avverso e farmaco e non rappresentano una valutazione definitiva di correlazione, ma sono utili in quanto contribuiscono ad alimentare la banca dati europea Eudravigilance, a livello della quale sono implementati algoritmi di analisi su dati aggregati in grado di rilevare segnali di allarme emergenti che necessitano approfondimento e indagini scientifiche formali attraverso studi di sicurezza post-marketing (PASS). Lo studio delle reazioni avverse associate ad un farmaco è infatti un processo continuo che, a partire dalle prime segnalazioni, porta agli studi di farmacoepidemiologia e alla valutazione quantitativa del rischio. Qualora questi segnali dovessero essere confermati, essi potrebbero portare a richiedere l implementazione di tutta una serie di misure regolatorie che possono andare dall aggiornamento delle informazioni di sicurezza del prodotto biosimilare fino al ritiro effettivo dal mercato. In conclusione, la segnalazione di sospette reazioni avverse rimane uno strumento indispensabile per confermare il rapporto beneficio/rischio favorevole dei fattori stimolanti le colonie granulocitarie (G-CSF) biosimilari nelle reali condizioni di impiego. Sul sito nella sezione Operatori > Farmacovigilanza è disponibile la documentazione utile per facilitare il processo di segnalazione delle sospette reazioni avverse. stimolanti le colonie granulocitarie (G-CSF) a brevetto scaduto Pag. 8
9 Riferimenti bibliografici - Agenzia Italiana del Farmaco Position Paper sui Farmaci Biosimilari - EMA Concept Paper Revision of the guideline on similar biological medicinal product (CHMP/BMWP/572643/2011). - EMEA/CHMP/BMWP/42832/2005) EMA Guideline Similar biological medicinal products containing biotechnology-derived proteins as active substance: quality issues (EMEA/CHMP/BWP/49348/2005). - European Medicines Agency (2006) - Annex to guideline on similar biological medicinal products containing biotechnology-derived proteins as active substance: non-clinical and clinical issues guidance on similar medicinal products containing recombinant granulocyte-colony stimulating factor (EMEA/CHMP/BMWP/31329/2005). - Guideline on evaluation of similar biotherapeutic products (SBPs), WHO Aapro M et al update of EORTC guidelines for the use of granulocyte-colony stimulating factor to reduce the incidence of chemotherapy-induced febrile neutropenia in adult patients withlymphoproliferative disorders and solid tumors. Eur J Cancer 2011; 47:8 - Shaw BE et al. Concerns about the use of biosimilar granulocyte colony-stimulating factors for the mobilization of stem cells in normal donors: position of the World Marrow Donor Association. Haemathol 2011; 96 (7): Liumbruno GM et al. Ethical issues and concerns about the use of biosimilar granulcyte colony-stimulating factors for mobilization of stem cells in normal donors. Blood Trnaf 2012; 10:550 - Aapro M et al. Comparative cost-efficiency across the European G5 countries of various regimens of filgrastim, biosimilar filgrastim, and pegfilgrastim to reduce the incidence of chemotherapy-induce febrile neutropenia. J Oncol Pharm Practice 2011; 18 (2): 171 stimolanti le colonie granulocitarie (G-CSF) a brevetto scaduto Pag. 9
I farmaci biosimilari: uso sicurezza e sostenibilità
 I farmaci biosimilari: uso sicurezza e sostenibilità ISS, 25 Giugno 2015 Uso dei biosimilari e sostenibilità: il punto di vista delle aziende biotech Riccardo Palmisano Vice Presidente Assobiotec 1 Scenario
I farmaci biosimilari: uso sicurezza e sostenibilità ISS, 25 Giugno 2015 Uso dei biosimilari e sostenibilità: il punto di vista delle aziende biotech Riccardo Palmisano Vice Presidente Assobiotec 1 Scenario
Dal 2000, con la perdita dei brevetti di importanti principi attivi, abbiamo assistito ad un controllo della spesa territoriale italiana.
 Dal 2000, con la perdita dei brevetti di importanti principi attivi, abbiamo assistito ad un controllo della spesa territoriale italiana. Le scadenze brevettuali sono aumentate dal 2000 ad 2008 ma dopo
Dal 2000, con la perdita dei brevetti di importanti principi attivi, abbiamo assistito ad un controllo della spesa territoriale italiana. Le scadenze brevettuali sono aumentate dal 2000 ad 2008 ma dopo
La prescrizione dei biosimilari: il punto di vista dell oncologo
 La prescrizione dei biosimilari: il punto di vista dell oncologo Prof. Giuseppe Nastasi Direttore U.O.C Oncologia Medica A.O. Bolognini - Seriate (BG) Cosa si aspetta il paziente? Sicurezza ed efficacia
La prescrizione dei biosimilari: il punto di vista dell oncologo Prof. Giuseppe Nastasi Direttore U.O.C Oncologia Medica A.O. Bolognini - Seriate (BG) Cosa si aspetta il paziente? Sicurezza ed efficacia
16/05/2012. La Legge 648/96: una risorsa tutta italiana, da perfezionare e mutare. Carlo Tomino. Roma, 10 Maggio 2012
 La Legge 648/96: una risorsa tutta italiana, da perfezionare e mutare. Carlo Tomino Roma, 10 Maggio 2012 1 Dichiarazione di trasparenza/interessi: Carlo Tomino, dirigente Le opinioni espresse in questa
La Legge 648/96: una risorsa tutta italiana, da perfezionare e mutare. Carlo Tomino Roma, 10 Maggio 2012 1 Dichiarazione di trasparenza/interessi: Carlo Tomino, dirigente Le opinioni espresse in questa
FARMACI BIOLOGICI E BIOSIMILARI
 FARMACI BIOLOGICI E BIOSIMILARI il punto di vista di AMICI Onlus cosa sono i farmaci biosimilari Alla luce delle scadenze brevettuali sono già in commercio, e presto ne arriveranno altri, farmaci biologici
FARMACI BIOLOGICI E BIOSIMILARI il punto di vista di AMICI Onlus cosa sono i farmaci biosimilari Alla luce delle scadenze brevettuali sono già in commercio, e presto ne arriveranno altri, farmaci biologici
La neutropenia è definita in gradi a seconda del valore raggiunta dai neutrofili al Nadir ( tabella 1)
 TRATTAMENTO DELLA NEUTROPENIA CON G-CSF Introduzione La neutropenia e le complicanze ad essa correlate rappresentano la principale tossicità dose limitante della chemioterapia, per il rischio di infezioni
TRATTAMENTO DELLA NEUTROPENIA CON G-CSF Introduzione La neutropenia e le complicanze ad essa correlate rappresentano la principale tossicità dose limitante della chemioterapia, per il rischio di infezioni
Il ruolo di AIFA nella Ricerca Clinica. Luca Pani DG@aifa.gov.it
 Il ruolo di AIFA nella Ricerca Clinica Luca Pani DG@aifa.gov.it Dichiarazione di trasparenza/interessi* Le opinioni espresse in questa presentazione sono personali e non possono essere considerate o citate
Il ruolo di AIFA nella Ricerca Clinica Luca Pani DG@aifa.gov.it Dichiarazione di trasparenza/interessi* Le opinioni espresse in questa presentazione sono personali e non possono essere considerate o citate
Piano di investimento dei fondi per la Farmacovigilanza 2008-2009. Regione Lazio
 Piano di investimento dei fondi per la Farmacovigilanza 2008-2009 Regione Lazio Premessa L attuazione delle linee di indirizzo elaborate dalla Regione Lazio per l impegno dei fondi 2007 della farmacovigilanza
Piano di investimento dei fondi per la Farmacovigilanza 2008-2009 Regione Lazio Premessa L attuazione delle linee di indirizzo elaborate dalla Regione Lazio per l impegno dei fondi 2007 della farmacovigilanza
PASQUALE FREGA Assobiotec
 ITALIAN ORPHAN DRUGS DAY Venerdì 13 febbraio 2015 Sala conferenze Digital for Business - Sesto San Giovanni (MI) PASQUALE FREGA Assobiotec www.digitalforacademy.com Italian Orphan Drug Day Malattie Rare
ITALIAN ORPHAN DRUGS DAY Venerdì 13 febbraio 2015 Sala conferenze Digital for Business - Sesto San Giovanni (MI) PASQUALE FREGA Assobiotec www.digitalforacademy.com Italian Orphan Drug Day Malattie Rare
Il Direttore della Direzione Regionale Programmazione Sanitaria -Risorse Umane e Sanitarie
 Oggetto: Aggiornamento della determinazione 1875 del Modalità di erogazione dei farmaci classificati in regime di rimborsabilità in fascia H e in regime di fornitura OSP2, così come modificata dalla determinazione
Oggetto: Aggiornamento della determinazione 1875 del Modalità di erogazione dei farmaci classificati in regime di rimborsabilità in fascia H e in regime di fornitura OSP2, così come modificata dalla determinazione
AIFA Agenzia Italiana del Farmaco Valproato
 AIFA - Valproato 18/12/2009 (Livello 2) AIFA Agenzia Italiana del Farmaco Valproato Rivalutazione CHMP file:///c /documenti/val9510.htm [18/12/2009 12.44.38] Domande e risposte sulla rivalutazione dei
AIFA - Valproato 18/12/2009 (Livello 2) AIFA Agenzia Italiana del Farmaco Valproato Rivalutazione CHMP file:///c /documenti/val9510.htm [18/12/2009 12.44.38] Domande e risposte sulla rivalutazione dei
PERCORSO DIAGNOSTICO TERAPEUTICO CONDIVISO PER LA PRESCRIZIONE/UTILIZZO DI ERITOPOIETINE A BREVETTO SCADUTO
 PERCORSO DIAGNOSTICO TERAPEUTICO CONDIVISO PER LA PRESCRIZIONE/UTILIZZO DI ERITOPOIETINE A BREVETTO SCADUTO Luglio 2014 Obiettivo: Il presente documento, condiviso e sottoscritto dalle Direzioni sanitarie
PERCORSO DIAGNOSTICO TERAPEUTICO CONDIVISO PER LA PRESCRIZIONE/UTILIZZO DI ERITOPOIETINE A BREVETTO SCADUTO Luglio 2014 Obiettivo: Il presente documento, condiviso e sottoscritto dalle Direzioni sanitarie
ISO/IEC 2700:2013. Principali modifiche e piano di transizione alla nuova edizione. DNV Business Assurance. All rights reserved.
 ISO/IEC 2700:2013 Principali modifiche e piano di transizione alla nuova edizione ISO/IEC 27001 La norma ISO/IEC 27001, Information technology - Security techniques - Information security management systems
ISO/IEC 2700:2013 Principali modifiche e piano di transizione alla nuova edizione ISO/IEC 27001 La norma ISO/IEC 27001, Information technology - Security techniques - Information security management systems
MANUALE D USO DI VIGIFARMACO
 MANUALE D USO DI VIGIFARMACO 1. Perché vanno segnalate le reazioni indesiderate di medicinali? Al momento della commercializzazione di un nuovo farmaco il suo profilo rischio/beneficio è noto solo in parte
MANUALE D USO DI VIGIFARMACO 1. Perché vanno segnalate le reazioni indesiderate di medicinali? Al momento della commercializzazione di un nuovo farmaco il suo profilo rischio/beneficio è noto solo in parte
AIFA Agenzia Italiana del Farmaco Sirolimus (Rapamune)
 AIFA - Sirolimus (Rapamune) 08/02/2010 (Livello 2) AIFA Agenzia Italiana del Farmaco Sirolimus (Rapamune) Nota Informativa Importante (08 Febbraio 2010) file:///c /documenti/sir653.htm [08/02/2010 10.47.36]
AIFA - Sirolimus (Rapamune) 08/02/2010 (Livello 2) AIFA Agenzia Italiana del Farmaco Sirolimus (Rapamune) Nota Informativa Importante (08 Febbraio 2010) file:///c /documenti/sir653.htm [08/02/2010 10.47.36]
CARTA INTESTATA DEL CENTRO CLINICO
 CARTA INTESTATA DEL CENTRO CLINICO CERLiguria_Mod.10_Uso_Compassionevole RICHIESTA DI PARERE AL COMITATO ETICO PER USO TERAPEUTICO DI MEDICINALE SOTTOPOSTO A SPERIMENTAZIONE CLINICA Si applica solo se
CARTA INTESTATA DEL CENTRO CLINICO CERLiguria_Mod.10_Uso_Compassionevole RICHIESTA DI PARERE AL COMITATO ETICO PER USO TERAPEUTICO DI MEDICINALE SOTTOPOSTO A SPERIMENTAZIONE CLINICA Si applica solo se
L ESPERIENZA DELLA DISTRIBUZIONE DIRETTA NELL ASL2 SAVONESE
 Genova, 24 maggio 2013 L ESPERIENZA DELLA DISTRIBUZIONE DIRETTA NELL ASL2 SAVONESE Dott.ssa Simona Genta FATTORI CHE INFLUISCONO SULLA SPESA FARMACEUTICA ANALISI DEI CONSUMI FATTORI CHE RIDUCONO LA SPESA
Genova, 24 maggio 2013 L ESPERIENZA DELLA DISTRIBUZIONE DIRETTA NELL ASL2 SAVONESE Dott.ssa Simona Genta FATTORI CHE INFLUISCONO SULLA SPESA FARMACEUTICA ANALISI DEI CONSUMI FATTORI CHE RIDUCONO LA SPESA
LA GESTIONE DELLE FORNITURE DEL FARMACO OSSIGENO IN AMBITO DOMICILIARE E DEI SERVIZI CONNESSI ALL OSSIGENOTERAPIA DOMICILIARE
 LA GESTIONE DELLE FORNITURE DEL FARMACO OSSIGENO IN AMBITO DOMICILIARE E DEI SERVIZI CONNESSI ALL OSSIGENOTERAPIA DOMICILIARE La proposta di Assogastecnici Gruppo Gas Medicinali OTTOBRE 2010 PREMESSA Con
LA GESTIONE DELLE FORNITURE DEL FARMACO OSSIGENO IN AMBITO DOMICILIARE E DEI SERVIZI CONNESSI ALL OSSIGENOTERAPIA DOMICILIARE La proposta di Assogastecnici Gruppo Gas Medicinali OTTOBRE 2010 PREMESSA Con
Non tutto è scritto sulla pietra!
 VI CORSO DI AGGIORNAMENTO SUI FARMACI: gli scenari che cambiano Cosa sta cambiando nella Farmacovigilanza? - esperienze in casa madre Nadia Canova (Alfa Wassermann SpA) GdL Farmacovigilanza SSFA Non tutto
VI CORSO DI AGGIORNAMENTO SUI FARMACI: gli scenari che cambiano Cosa sta cambiando nella Farmacovigilanza? - esperienze in casa madre Nadia Canova (Alfa Wassermann SpA) GdL Farmacovigilanza SSFA Non tutto
MANUALE DELLA QUALITÀ Pag. 1 di 6
 MANUALE DELLA QUALITÀ Pag. 1 di 6 INDICE GESTIONE DELLE RISORSE Messa a disposizione delle risorse Competenza, consapevolezza, addestramento Infrastrutture Ambiente di lavoro MANUALE DELLA QUALITÀ Pag.
MANUALE DELLA QUALITÀ Pag. 1 di 6 INDICE GESTIONE DELLE RISORSE Messa a disposizione delle risorse Competenza, consapevolezza, addestramento Infrastrutture Ambiente di lavoro MANUALE DELLA QUALITÀ Pag.
La tutela dei pazienti affetti da malattie rare
 La tutela dei pazienti affetti da malattie rare Isabella Quinti Responsabile Centro di Riferimento Immunodeficienze Primitive Sapienza Università di Roma La tutela Sociale: Non sentirsi solo Legislativa
La tutela dei pazienti affetti da malattie rare Isabella Quinti Responsabile Centro di Riferimento Immunodeficienze Primitive Sapienza Università di Roma La tutela Sociale: Non sentirsi solo Legislativa
IL REGISTRO ONCOLOGICO COME STRUMENTO DI IMPLEMENTAZIONE DELLE DECISIONI: QUALE RUOLO NELL HTA
 IL REGISTRO ONCOLOGICO COME STRUMENTO DI IMPLEMENTAZIONE DELLE DECISIONI: QUALE RUOLO NELL HTA Francesca Caprari Direttore Affari Istituzionali e Relazioni Esterne Celgene srl L inizio Il Registro AIFA
IL REGISTRO ONCOLOGICO COME STRUMENTO DI IMPLEMENTAZIONE DELLE DECISIONI: QUALE RUOLO NELL HTA Francesca Caprari Direttore Affari Istituzionali e Relazioni Esterne Celgene srl L inizio Il Registro AIFA
Biosimilari: una chiave di lettura economica
 Biosimilari: una chiave di lettura economica FARMAGOOD L. Garattini (CESAV) 1 1. Il fallimento del mercato in sanità 2. Biosimilare Generico/Equivalente? 3. Le4Pdelmarketingmix Product Place Indice Promotion
Biosimilari: una chiave di lettura economica FARMAGOOD L. Garattini (CESAV) 1 1. Il fallimento del mercato in sanità 2. Biosimilare Generico/Equivalente? 3. Le4Pdelmarketingmix Product Place Indice Promotion
REQUISITI MINIMI PER LA PARTECIPAZIONE AL PROGETTO AIFA PER LA QUALITÀ NELLE SPERIMENTAZIONI A FINI NON INDUSTRIALI (NON-PROFIT)
 DOC AIFA CTQT APRILE 2008 (ALL. 2) REQUISITI MINIMI PER LA PARTECIPAZIONE AL PROGETTO AIFA PER LA QUALITÀ NELLE SPERIMENTAZIONI A FINI NON INDUSTRIALI (NON-PROFIT) Introduzione La finalità del presente
DOC AIFA CTQT APRILE 2008 (ALL. 2) REQUISITI MINIMI PER LA PARTECIPAZIONE AL PROGETTO AIFA PER LA QUALITÀ NELLE SPERIMENTAZIONI A FINI NON INDUSTRIALI (NON-PROFIT) Introduzione La finalità del presente
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITÀ REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA)
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITÀ REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Marzo 2009 Nuove modalità di prescrizione per i medicinali contenenti isotretinoina ad
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITÀ REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Marzo 2009 Nuove modalità di prescrizione per i medicinali contenenti isotretinoina ad
DELIBERAZIONE N. 33/32. Istituzione della rete di cure palliative della d
 32 Oggetto: Istituzione della rete di cure palliative della d Regione Sardegna. L Assessore dell'igiene e Sanità e dell'assistenza Sociale ricorda che la legge 15 marzo 2010, n. 38, tutela il diritto del
32 Oggetto: Istituzione della rete di cure palliative della d Regione Sardegna. L Assessore dell'igiene e Sanità e dell'assistenza Sociale ricorda che la legge 15 marzo 2010, n. 38, tutela il diritto del
1 Cittadinanzattiva Tribunale per i diritti del malato Coordinamento nazionale Associazioni Malati Cronici
 1 Cittadinanzattiva Tribunale per i diritti del malato Coordinamento nazionale Associazioni Malati Cronici 2 Parere per la consultazione pubblica avviata dalla Direzione Generale Impresa e Industria (Commissione
1 Cittadinanzattiva Tribunale per i diritti del malato Coordinamento nazionale Associazioni Malati Cronici 2 Parere per la consultazione pubblica avviata dalla Direzione Generale Impresa e Industria (Commissione
Le novità degli ultimi 12 mesi
 Farmacovigilanza Le novità degli ultimi 12 mesi Maria Nicotra Il sistema di Farmacovigilanza sta attraversando da qualche tempo in Italia una fase di progressivo sviluppo dovuto probabilmente al cambiamento
Farmacovigilanza Le novità degli ultimi 12 mesi Maria Nicotra Il sistema di Farmacovigilanza sta attraversando da qualche tempo in Italia una fase di progressivo sviluppo dovuto probabilmente al cambiamento
Metodologia di calcolo del pay-back 5% - 2013
 Metodologia di calcolo del pay-back 5% - 2013 Vista la proroga al 31 dicembre 2013 emanata ai sensi del D.P.C.M. 26 giugno 2013, dei termini previsti all art.9, comma 1, del D.L. 31 dicembre 2007, n.248,
Metodologia di calcolo del pay-back 5% - 2013 Vista la proroga al 31 dicembre 2013 emanata ai sensi del D.P.C.M. 26 giugno 2013, dei termini previsti all art.9, comma 1, del D.L. 31 dicembre 2007, n.248,
Considerazioni sulla organizzazione del servizio di manutenzione Giuseppe IOTTI, ANACAM
 Technical Convention QUALITY IN MAINTENANCE: FULL SAFETY, FULL ACCESSIBILTY Augsburg, 18 October 2007 Considerazioni sulla organizzazione del servizio di manutenzione Giuseppe IOTTI, ANACAM Ascensori esistenti
Technical Convention QUALITY IN MAINTENANCE: FULL SAFETY, FULL ACCESSIBILTY Augsburg, 18 October 2007 Considerazioni sulla organizzazione del servizio di manutenzione Giuseppe IOTTI, ANACAM Ascensori esistenti
Biosimilari: una chiave di lettura economica
 Biosimilari: una chiave di lettura economica FARMAGOOD L. Garattini (CESAV) 1 1. Il fallimento del mercato in sanità 2. Biosimilare Generico/Equivalente? 3. Le4Pdelmarketingmix Product Place Indice Promotion
Biosimilari: una chiave di lettura economica FARMAGOOD L. Garattini (CESAV) 1 1. Il fallimento del mercato in sanità 2. Biosimilare Generico/Equivalente? 3. Le4Pdelmarketingmix Product Place Indice Promotion
CERTIFICATI BIANCHI - TEE (Titoli di Efficienza Energetica)
 Energia: istruzioni per l uso Mezzacorona (TN), 13 dicembre 2005 Certificati bianchi, verdi e neri Polo Tecnologico per l Energia l srl - Trento CERTIFICATI BIANCHI - TEE (Titoli di Efficienza Energetica)
Energia: istruzioni per l uso Mezzacorona (TN), 13 dicembre 2005 Certificati bianchi, verdi e neri Polo Tecnologico per l Energia l srl - Trento CERTIFICATI BIANCHI - TEE (Titoli di Efficienza Energetica)
Comitato Etico ASL Napoli 2 Nord (istituito con delibera n. 161 del 22/02/2010) STATUTO COMITATO ETICO ASL NAPOLI 2 NORD
 STATUTO COMITATO ETICO ASL NAPOLI 2 NORD ART.1 Finalità del Comitato Etico ART.2 Funzioni ART.3 Composizione e durata ART.4 Regolamento ART.5 Presidente ART 6 Segretario ART.7 Segreteria ART.8 Disposizioni
STATUTO COMITATO ETICO ASL NAPOLI 2 NORD ART.1 Finalità del Comitato Etico ART.2 Funzioni ART.3 Composizione e durata ART.4 Regolamento ART.5 Presidente ART 6 Segretario ART.7 Segreteria ART.8 Disposizioni
QUALITÀ E SICUREZZA PER I NOSTRI PAZIENTI
 QUALITÀ E SICUREZZA PER I NOSTRI PAZIENTI L ACCREDITAMENTO INTERNAZIONALE ALL ECCELLENZA Fondazione Poliambulanza ha ricevuto nel dicembre 2013 l accreditamento internazionale all eccellenza da parte di
QUALITÀ E SICUREZZA PER I NOSTRI PAZIENTI L ACCREDITAMENTO INTERNAZIONALE ALL ECCELLENZA Fondazione Poliambulanza ha ricevuto nel dicembre 2013 l accreditamento internazionale all eccellenza da parte di
Italian Biosimilars Group
 Italian Biosimilars Group gruppo appartenente ad Assogenerici Aderente a I BIOSIMILARI: PARITA DI EFFICACIA E SICUREZZA, MINORI COSTI, MAGGIOR ACCESSO ALLE TERAPIE Le biotecnologie: una rivoluzione, ad
Italian Biosimilars Group gruppo appartenente ad Assogenerici Aderente a I BIOSIMILARI: PARITA DI EFFICACIA E SICUREZZA, MINORI COSTI, MAGGIOR ACCESSO ALLE TERAPIE Le biotecnologie: una rivoluzione, ad
LA COMMISSIONE UNICA DEL FARMACO. Viste le proprie deliberazioni assunte nelle sedute del 25 gennaio 2000 e 7 giugno 2000; Dispone: Art. l.
 PROVVEDIMENTO 20 luglio 2000. Istituzione dell'elenco delle specialità medicinali erogabili a totale carico del Servizio sanitario nazionale ai sensi della legge 648/96. LA COMMISSIONE UNICA DEL FARMACO
PROVVEDIMENTO 20 luglio 2000. Istituzione dell'elenco delle specialità medicinali erogabili a totale carico del Servizio sanitario nazionale ai sensi della legge 648/96. LA COMMISSIONE UNICA DEL FARMACO
II.11 LA BANCA D ITALIA
 Provvedimento del 24 marzo 2010. Regolamento recante la disciplina dell adozione degli atti di natura normativa o di contenuto generale della Banca d Italia nell esercizio delle funzioni di vigilanza bancaria
Provvedimento del 24 marzo 2010. Regolamento recante la disciplina dell adozione degli atti di natura normativa o di contenuto generale della Banca d Italia nell esercizio delle funzioni di vigilanza bancaria
Parte I (punti 3-9): Misure sanitarie obbligatorie per il controllo della Paratubercolosi bovina
 LINEE GUIDA PER L ADOZIONE DI PIANI DI CONTROLLO E PER L ASSEGNAZIONE DELLA QUALIFICA SANITARIA DEGLI ALLEVAMENTI NEI CONFRONTI DELLA PARATUBERCOLOSI BOVINA 1. Definizioni Ai sensi delle presenti linee
LINEE GUIDA PER L ADOZIONE DI PIANI DI CONTROLLO E PER L ASSEGNAZIONE DELLA QUALIFICA SANITARIA DEGLI ALLEVAMENTI NEI CONFRONTI DELLA PARATUBERCOLOSI BOVINA 1. Definizioni Ai sensi delle presenti linee
Il ruolo dell ISF: dall informazione al marketing Raffaella Michieli
 Il ruolo dell ISF: dall informazione al marketing Raffaella Michieli Metodi di cura Per i Medici il Farmaco è il pane quotidiano 85% dei contatti in MG esita in una prescrizione farmacologica Fonte H.S.
Il ruolo dell ISF: dall informazione al marketing Raffaella Michieli Metodi di cura Per i Medici il Farmaco è il pane quotidiano 85% dei contatti in MG esita in una prescrizione farmacologica Fonte H.S.
Manuale di Gestione Integrata POLITICA AZIENDALE. 4.2 Politica Aziendale 2. Verifica RSGI Approvazione Direzione Emissione RSGI
 Pag.1 di 5 SOMMARIO 4.2 Politica Aziendale 2 Verifica RSGI Approvazione Direzione Emissione RSGI. Pag.2 di 5 4.2 Politica Aziendale La Direzione della FOMET SpA adotta e diffonde ad ogni livello della
Pag.1 di 5 SOMMARIO 4.2 Politica Aziendale 2 Verifica RSGI Approvazione Direzione Emissione RSGI. Pag.2 di 5 4.2 Politica Aziendale La Direzione della FOMET SpA adotta e diffonde ad ogni livello della
della manutenzione, includa i requisiti relativi ai sottosistemi strutturali all interno del loro contesto operativo.
 L 320/8 Gazzetta ufficiale dell Unione europea IT 17.11.2012 REGOLAMENTO (UE) N. 1078/2012 DELLA COMMISSIONE del 16 novembre 2012 relativo a un metodo di sicurezza comune per il monitoraggio che devono
L 320/8 Gazzetta ufficiale dell Unione europea IT 17.11.2012 REGOLAMENTO (UE) N. 1078/2012 DELLA COMMISSIONE del 16 novembre 2012 relativo a un metodo di sicurezza comune per il monitoraggio che devono
SISTEMI DI MISURAZIONE DELLA PERFORMANCE
 SISTEMI DI MISURAZIONE DELLA PERFORMANCE Dicembre, 2014 Il Sistema di misurazione e valutazione della performance... 3 Il Ciclo di gestione della performance... 5 Il Sistema di misurazione e valutazione
SISTEMI DI MISURAZIONE DELLA PERFORMANCE Dicembre, 2014 Il Sistema di misurazione e valutazione della performance... 3 Il Ciclo di gestione della performance... 5 Il Sistema di misurazione e valutazione
REGOLAMENTO PER LA PROMOZIONE DELLA SOLIDARIETA INTERNAZIONALE E DEI DIRITTI UMANI. Art. 1 Finalità
 REGOLAMENTO PER LA PROMOZIONE DELLA SOLIDARIETA INTERNAZIONALE E DEI DIRITTI UMANI Art. 1 Finalità La Provincia di Genova, in attuazione di quanto previsto dal proprio Statuto, promuove la cultura della
REGOLAMENTO PER LA PROMOZIONE DELLA SOLIDARIETA INTERNAZIONALE E DEI DIRITTI UMANI Art. 1 Finalità La Provincia di Genova, in attuazione di quanto previsto dal proprio Statuto, promuove la cultura della
DELIBERAZIONE N. 5/31 DEL 11.2.2014. Istituzione della rete per la terapia del dolore della Regione Sardegna.
 Oggetto: Istituzione della rete per la terapia del dolore della Regione Sardegna. L Assessore dell'igiene e Sanità e dell'assistenza Sociale ricorda che la legge 15 marzo 2010, n. 38, tutela il diritto
Oggetto: Istituzione della rete per la terapia del dolore della Regione Sardegna. L Assessore dell'igiene e Sanità e dell'assistenza Sociale ricorda che la legge 15 marzo 2010, n. 38, tutela il diritto
Disclosure Code. Roma, 16 giugno 2016
 Disclosure Code Roma, 16 giugno 2016 Una collaborazione positiva, ben regolata e sempre più trasparente. Un «trasferimento di valori» bilaterale a beneficio della ricerca e dei pazienti La scienza medica
Disclosure Code Roma, 16 giugno 2016 Una collaborazione positiva, ben regolata e sempre più trasparente. Un «trasferimento di valori» bilaterale a beneficio della ricerca e dei pazienti La scienza medica
I SISTEMI DI GESTIONE DELLA SALUTE E SICUREZZA SUL LAVORO: OHSAS 18001 AV2/07/11 ARTEMIDE.
 I SISTEMI DI GESTIONE DELLA SALUTE E SICUREZZA SUL LAVORO: OHSAS 18001 AV2/07/11 ARTEMIDE. 1 Nel panorama legislativo italiano la Salute e la Sicurezza sul Lavoro sono regolamentate da un gran numero di
I SISTEMI DI GESTIONE DELLA SALUTE E SICUREZZA SUL LAVORO: OHSAS 18001 AV2/07/11 ARTEMIDE. 1 Nel panorama legislativo italiano la Salute e la Sicurezza sul Lavoro sono regolamentate da un gran numero di
LEGGE 29 NOVEMBRE 2007 N. 222 ART. 5 COMMA 1 E 2. NOTA SULLA METODOLOGIA APPLICATIVA
 LEGGE 29 NOVEMBRE 2007 N. 222 ART. 5 COMMA 1 E 2. NOTA SULLA METODOLOGIA APPLICATIVA PREMESSA L articolo 5 della legge 29 novembre 2007, n. 222 prevede al comma 1 che: l onere a carico del SSN per l assistenza
LEGGE 29 NOVEMBRE 2007 N. 222 ART. 5 COMMA 1 E 2. NOTA SULLA METODOLOGIA APPLICATIVA PREMESSA L articolo 5 della legge 29 novembre 2007, n. 222 prevede al comma 1 che: l onere a carico del SSN per l assistenza
Farmacosorveglianza. Davide Poli Davide Poli Istituto di Ricerche Farmacologiche Mario Negri davide.poli@marionegri.it
 Farmacosorveglianza Davide Poli Davide Poli Istituto di Ricerche Farmacologiche Mario Negri davide.poli@marionegri.it Good Clinical Practice La Buona Pratica Clinica è uno standard internazionale di etica
Farmacosorveglianza Davide Poli Davide Poli Istituto di Ricerche Farmacologiche Mario Negri davide.poli@marionegri.it Good Clinical Practice La Buona Pratica Clinica è uno standard internazionale di etica
Biosimilari: scelta informata
 Executive summary Biosimilari: scelta informata Position paper sui farmaci biotecnologici e biosimilari A cura del Sottogruppo Biosimilari del Gruppo di Lavoro Farmaco Biotech 1. L innovazione farmaceutica
Executive summary Biosimilari: scelta informata Position paper sui farmaci biotecnologici e biosimilari A cura del Sottogruppo Biosimilari del Gruppo di Lavoro Farmaco Biotech 1. L innovazione farmaceutica
Buone pratiche di sperimentazione clinica negli animali dei medicinali veterinari
 negli animali dei medicinali veterinari Modelli innovativi di lotta alla varroa: l acido formico in gel. Dr. Salvatore Macrì Dirigente Veterinario Ministero della Salute Roma Istituto Zooprofilattico Sperimentale
negli animali dei medicinali veterinari Modelli innovativi di lotta alla varroa: l acido formico in gel. Dr. Salvatore Macrì Dirigente Veterinario Ministero della Salute Roma Istituto Zooprofilattico Sperimentale
Dronedarone e insufficienza renale acuta: analisi delle segnalazioni della Rete Nazionale di Farmacovigilanza
 Dronedarone e insufficienza renale acuta: analisi delle segnalazioni della Rete Nazionale di Farmacovigilanza Domenico Motola Dipartimento di Scienze Mediche e Chirurgiche Unità di farmacologia Università
Dronedarone e insufficienza renale acuta: analisi delle segnalazioni della Rete Nazionale di Farmacovigilanza Domenico Motola Dipartimento di Scienze Mediche e Chirurgiche Unità di farmacologia Università
STUDI CLINICI 1. Che cosa è uno studio clinico e a cosa serve? 2. Come nasce la sperimentazione clinica e che tipi di studi esistono?
 STUDI CLINICI 1. Che cosa è uno studio clinico e a cosa serve? Si definisce sperimentazione clinica, o studio clinico controllato, (in inglese: clinical trial), un esperimento scientifico che genera dati
STUDI CLINICI 1. Che cosa è uno studio clinico e a cosa serve? Si definisce sperimentazione clinica, o studio clinico controllato, (in inglese: clinical trial), un esperimento scientifico che genera dati
ISO 14001:2015 Le nuove prospettive dei Sistemi di Gestione ambientali. Roma 22/10/15 Bollate 05/11/15
 ISO 14001:2015 Le nuove prospettive dei Sistemi di Gestione ambientali Roma 22/10/15 Bollate 05/11/15 EVOLUZIONE DELLA NORMA ISO 14001 Prima pubblicazione: 1996 Prima revisione: 2004 (introdotti cambiamenti
ISO 14001:2015 Le nuove prospettive dei Sistemi di Gestione ambientali Roma 22/10/15 Bollate 05/11/15 EVOLUZIONE DELLA NORMA ISO 14001 Prima pubblicazione: 1996 Prima revisione: 2004 (introdotti cambiamenti
OrisLAB X3 Nuova Dir. 2007/47/CE
 PREMESSE: A partire dal 21 Marzo 2010 è entrata in vigore la Nuova Direttiva 2007/47/CE ad integrazione della ormai nota dir. 93/42/CEE. La nuova normativa è stata pubblicata sulla Gazzetta Ufficiale Serie
PREMESSE: A partire dal 21 Marzo 2010 è entrata in vigore la Nuova Direttiva 2007/47/CE ad integrazione della ormai nota dir. 93/42/CEE. La nuova normativa è stata pubblicata sulla Gazzetta Ufficiale Serie
STUDI SU MATERIALE GENETICO
 Istituto Oncologico Veneto Istituto di Ricovero e Cura a Carattere Scientifico Ospedale Busonera I.O.V. ISTITUTO ONCOLOGICO VENETO I.R.C.C.S. STUDI SU MATERIALE GENETICO Comitato Etico Istituto Oncologico
Istituto Oncologico Veneto Istituto di Ricovero e Cura a Carattere Scientifico Ospedale Busonera I.O.V. ISTITUTO ONCOLOGICO VENETO I.R.C.C.S. STUDI SU MATERIALE GENETICO Comitato Etico Istituto Oncologico
Servizio. Carta dei Servizi rev. 2 del 7 marzo 2012. Farmaceutico
 Carta dei Servizi rev. 2 del 7 marzo 2012 Azienda ULSS n. 22 Bussolengo VR Servizio Territoriale Domegliara, via A. De Gasperi, 72 Direttore: dott.ssa Antonella Ferrari Apertura al pubblico: dal lunedì
Carta dei Servizi rev. 2 del 7 marzo 2012 Azienda ULSS n. 22 Bussolengo VR Servizio Territoriale Domegliara, via A. De Gasperi, 72 Direttore: dott.ssa Antonella Ferrari Apertura al pubblico: dal lunedì
INTESA TRA COMUNE DI MILANO E AZIENDA SANITARIA LOCALE CITTA DI MILANO PER LA SOMMINISTRAZIONE DI FARMACI NEI SERVIZI ALL INFANZIA (0-6 ANNI)
 INTESA TRA COMUNE DI MILANO E AZIENDA SANITARIA LOCALE CITTA DI MILANO PER LA SOMMINISTRAZIONE DI FARMACI NEI SERVIZI ALL INFANZIA (0-6 ANNI) Al fine di garantire un approccio coordinato alla gestione
INTESA TRA COMUNE DI MILANO E AZIENDA SANITARIA LOCALE CITTA DI MILANO PER LA SOMMINISTRAZIONE DI FARMACI NEI SERVIZI ALL INFANZIA (0-6 ANNI) Al fine di garantire un approccio coordinato alla gestione
Revisione della posizione sui farmaci biosimilari da parte della Società Italiana di Farmacologia: working paper 2014
 Revisione della posizione sui farmaci biosimilari da parte della Società Italiana di Farmacologia: working paper 2014 Approvata dal Consiglio Direttivo della SIF I farmaci biosimilari, negli ultimi 5 anni,
Revisione della posizione sui farmaci biosimilari da parte della Società Italiana di Farmacologia: working paper 2014 Approvata dal Consiglio Direttivo della SIF I farmaci biosimilari, negli ultimi 5 anni,
Biosimilari Infliximab in gastroenterologia
 Promozione d uso dei farmaci a brevetto scaduto in particolare nel campo dei farmaci biotecnologici Biosimilari Infliximab in gastroenterologia Guido Basilisco Stefania Orlando, Flavio Caprioli UO di Gastroenterologia
Promozione d uso dei farmaci a brevetto scaduto in particolare nel campo dei farmaci biotecnologici Biosimilari Infliximab in gastroenterologia Guido Basilisco Stefania Orlando, Flavio Caprioli UO di Gastroenterologia
UTILIZZATORI A VALLE: COME RENDERE NOTI GLI USI AI FORNITORI
 UTILIZZATORI A VALLE: COME RENDERE NOTI GLI USI AI FORNITORI Un utilizzatore a valle di sostanze chimiche dovrebbe informare i propri fornitori riguardo al suo utilizzo delle sostanze (come tali o all
UTILIZZATORI A VALLE: COME RENDERE NOTI GLI USI AI FORNITORI Un utilizzatore a valle di sostanze chimiche dovrebbe informare i propri fornitori riguardo al suo utilizzo delle sostanze (come tali o all
Orientamenti sul sottomodulo del rischio di catastrofe per l assicurazione malattia
 EIOPA-BoS-14/176 IT Orientamenti sul sottomodulo del rischio di catastrofe per l assicurazione malattia EIOPA Westhafen Tower, Westhafenplatz 1-60327 Frankfurt Germany - Tel. + 49 69-951119-20; Fax. +
EIOPA-BoS-14/176 IT Orientamenti sul sottomodulo del rischio di catastrofe per l assicurazione malattia EIOPA Westhafen Tower, Westhafenplatz 1-60327 Frankfurt Germany - Tel. + 49 69-951119-20; Fax. +
Il sistema di gestione del rischio clinico
 Il sistema di gestione del rischio clinico Prevenzione dei rischi Riprogettazione organizzativa Valutazione e feedback Analisi dei rischi Audit M&M review RCA Identificazione dei rischi Incident reporting
Il sistema di gestione del rischio clinico Prevenzione dei rischi Riprogettazione organizzativa Valutazione e feedback Analisi dei rischi Audit M&M review RCA Identificazione dei rischi Incident reporting
Fabrizio Galliccia. giovedì 17 maggio 2012 DISCLAIMER
 ATTIVITA DELL ISPETTORATO GCP SVILUPPI RECENTI E NUOVI ORIENTAMENTI IN MATERIA Fabrizio Galliccia giovedì 17 maggio 2012 DISCLAIMER I dati e i commenti contenuti in questa presentazione rappresentano il
ATTIVITA DELL ISPETTORATO GCP SVILUPPI RECENTI E NUOVI ORIENTAMENTI IN MATERIA Fabrizio Galliccia giovedì 17 maggio 2012 DISCLAIMER I dati e i commenti contenuti in questa presentazione rappresentano il
 Le regole del parlamento europeo per garantire qualità e sicurezza nel trattamento di cellule e tessuti umani (Direttiva 2004/23/CE) E stata recentemente recepita anche dall Italia, la direttiva europea
Le regole del parlamento europeo per garantire qualità e sicurezza nel trattamento di cellule e tessuti umani (Direttiva 2004/23/CE) E stata recentemente recepita anche dall Italia, la direttiva europea
GESTIONE DELLA FORMAZIONE E
 08/02/2011 Pag. 1 di 7 GESTIONE DELLA FORMAZIONE E DELL ADDESTRAMENTO DEL PERSONALE 1. SCOPO... 2 2. APPLICABILITÀ... 2 3. DOCUMENTI DI RIFERIMENTO... 2 3.1. Norme... 2 3.2. Moduli / Istruzioni... 2 4.
08/02/2011 Pag. 1 di 7 GESTIONE DELLA FORMAZIONE E DELL ADDESTRAMENTO DEL PERSONALE 1. SCOPO... 2 2. APPLICABILITÀ... 2 3. DOCUMENTI DI RIFERIMENTO... 2 3.1. Norme... 2 3.2. Moduli / Istruzioni... 2 4.
*Perché parliamo di. genere e salute. augusta.angelucci@alice.it
 *Perché parliamo di genere e salute augusta.angelucci@alice.it La conferenza di PechIno 1995 ha a introdotto i principi di : EMPOWERMENT E GENDER MAINSTREAMING 28/10/15 La Conferenza ha adottato la Piattaforma
*Perché parliamo di genere e salute augusta.angelucci@alice.it La conferenza di PechIno 1995 ha a introdotto i principi di : EMPOWERMENT E GENDER MAINSTREAMING 28/10/15 La Conferenza ha adottato la Piattaforma
Accesso ai farmaci innovativi e controllo della spesa a livello regionale
 FARMACI INNOVATIVI Qualità efficacia appropriatezza 9 ottobre 2009 Camera dei Deputati Palazzo Marini (Roma) Accesso ai farmaci innovativi e controllo della spesa a livello regionale Stefania Melena Direzione
FARMACI INNOVATIVI Qualità efficacia appropriatezza 9 ottobre 2009 Camera dei Deputati Palazzo Marini (Roma) Accesso ai farmaci innovativi e controllo della spesa a livello regionale Stefania Melena Direzione
XX CONGRESSO NAZIONALE AMD 2015 Genova, 13/16 maggio 2015 Centro Congressi Magazzini Del Cotone
 XX CONGRESSO NAZIONALE AMD 2015 Genova, 13/16 maggio 2015 Centro Congressi Magazzini Del Cotone L EVOLUZIONE DELLA DIABETOLOGIA ALLA LUCE DEL PIANO NAZIONALE DIABETE EQUIVALENZA ED EFFICACIA COMPARATIVA
XX CONGRESSO NAZIONALE AMD 2015 Genova, 13/16 maggio 2015 Centro Congressi Magazzini Del Cotone L EVOLUZIONE DELLA DIABETOLOGIA ALLA LUCE DEL PIANO NAZIONALE DIABETE EQUIVALENZA ED EFFICACIA COMPARATIVA
I registri per le protesi mammarie e i registri dei dispositivi impiantabili
 I registri per le protesi mammarie e i registri dei dispositivi impiantabili Dott.ssa Rossana Ugenti Direttore Generale del Sistema Informativo e Statistico Sanitario Ministero della salute 6 dicembre
I registri per le protesi mammarie e i registri dei dispositivi impiantabili Dott.ssa Rossana Ugenti Direttore Generale del Sistema Informativo e Statistico Sanitario Ministero della salute 6 dicembre
Situazione a livello regionale
 Situazione a livello regionale Ignota la prevalenza complessiva delle malattie rare, la distribuzione per patologia e l impatto di utilizzo delle risorse fisiche e finanziarie Studio Regione Lombardia,
Situazione a livello regionale Ignota la prevalenza complessiva delle malattie rare, la distribuzione per patologia e l impatto di utilizzo delle risorse fisiche e finanziarie Studio Regione Lombardia,
Corso di formazione sul campo a cura della sezione regionale SIFO Liguria I REGISTRI AIFA
 Corso di formazione sul campo a cura della sezione regionale SIFO Liguria I REGISTRI AIFA FARMACI ONCOLOGICI Genova, Palazzo della Regione Liguria 4 Dicembre 2014 Dr.ssa Alida Rota farmacista Ospedale
Corso di formazione sul campo a cura della sezione regionale SIFO Liguria I REGISTRI AIFA FARMACI ONCOLOGICI Genova, Palazzo della Regione Liguria 4 Dicembre 2014 Dr.ssa Alida Rota farmacista Ospedale
4.5) ISTITUZIONE DEL CENTRO INTERDIPARTIMENTALE DI RICERCA SULLE FIBROSI POLMONARI E MALATTIE RARE DEL POLMONE. ESPRIME
 I DIVISIONE 4.5) ISTITUZIONE DEL CENTRO INTERDIPARTIMENTALE DI RICERCA SULLE FIBROSI POLMONARI E MALATTIE RARE DEL POLMONE. OMISSIS ESPRIME parere favorevole alla istituzione del Centro Interdipartimentale
I DIVISIONE 4.5) ISTITUZIONE DEL CENTRO INTERDIPARTIMENTALE DI RICERCA SULLE FIBROSI POLMONARI E MALATTIE RARE DEL POLMONE. OMISSIS ESPRIME parere favorevole alla istituzione del Centro Interdipartimentale
Originator e biosimilari: interscambiabilità, sostituibilità e aspetti normativi
 Originator e biosimilari: interscambiabilità, sostituibilità e aspetti normativi Giambattista Bonanno Sezione di Farmacologia e Tossicologia Dipartimento di Farmacia Scuola di Scienze Mediche e Farmaceutiche
Originator e biosimilari: interscambiabilità, sostituibilità e aspetti normativi Giambattista Bonanno Sezione di Farmacologia e Tossicologia Dipartimento di Farmacia Scuola di Scienze Mediche e Farmaceutiche
A cura di Giorgio Mezzasalma
 GUIDA METODOLOGICA PER IL MONITORAGGIO E VALUTAZIONE DEL PIANO DI COMUNICAZIONE E INFORMAZIONE FSE P.O.R. 2007-2013 E DEI RELATIVI PIANI OPERATIVI DI COMUNICAZIONE ANNUALI A cura di Giorgio Mezzasalma
GUIDA METODOLOGICA PER IL MONITORAGGIO E VALUTAZIONE DEL PIANO DI COMUNICAZIONE E INFORMAZIONE FSE P.O.R. 2007-2013 E DEI RELATIVI PIANI OPERATIVI DI COMUNICAZIONE ANNUALI A cura di Giorgio Mezzasalma
L USO DEGLI ANTIPSICOTICI
 L USO DEGLI ANTIPSICOTICI NELLA REGIONE VENETO Valentina Fantelli Settore Farmaceutico Regionale Mestre - Venezia, 22 ottobre 2014 Area Sanità e Sociale Sezione Attuazione Programmazione Sanitaria Governance
L USO DEGLI ANTIPSICOTICI NELLA REGIONE VENETO Valentina Fantelli Settore Farmaceutico Regionale Mestre - Venezia, 22 ottobre 2014 Area Sanità e Sociale Sezione Attuazione Programmazione Sanitaria Governance
CRONICITÀ E APPROPRIATEZZA NEI SETTING DI CURA FIBROSI CISTICA DALL OSPEDALE AL TERRITORIO
 CRONICITÀ E APPROPRIATEZZA NEI SETTING DI CURA FIBROSI CISTICA DALL OSPEDALE AL TERRITORIO Cammi Emilio Reggio Emilia, 25 settembre 2015 Fibrosi cistica Malattia genetica rara Patologia multiorgano che
CRONICITÀ E APPROPRIATEZZA NEI SETTING DI CURA FIBROSI CISTICA DALL OSPEDALE AL TERRITORIO Cammi Emilio Reggio Emilia, 25 settembre 2015 Fibrosi cistica Malattia genetica rara Patologia multiorgano che
Ministero della Salute Agenzia Italiana del Farmaco
 Ministero della Salute Agenzia Italiana del Farmaco Linee guida per la classificazione e conduzione degli studi osservazionali sui farmaci IL DIRETTORE GENERALE VISTO il Decreto del Ministero della Salute
Ministero della Salute Agenzia Italiana del Farmaco Linee guida per la classificazione e conduzione degli studi osservazionali sui farmaci IL DIRETTORE GENERALE VISTO il Decreto del Ministero della Salute
STATUTO DELL AZIENDA OSPEDALIERO-UNIVERSITARIA MEYER INDICE SEZIONE
 STATUTO DELL AZIENDA OSPEDALIERO-UNIVERSITARIA MEYER INDICE SEZIONE Titolo 3 - PROGRAMMAZIONE E SVILUPPO DELLA RETE PEDIATRICA REGIONALE Art. 20 - Art. 21 - Art. 22 - Art. 23 - Art. 24 - Art. 25 - Verso
STATUTO DELL AZIENDA OSPEDALIERO-UNIVERSITARIA MEYER INDICE SEZIONE Titolo 3 - PROGRAMMAZIONE E SVILUPPO DELLA RETE PEDIATRICA REGIONALE Art. 20 - Art. 21 - Art. 22 - Art. 23 - Art. 24 - Art. 25 - Verso
Assistenza transfrontaliera
 Centro di Riferimento Regionale per le Malattie Rare II Clinica Pediatrica Ospedale Pediatrico Microcitemico Assistenza transfrontaliera Dott.ssa Francesca Meloni Dott.ssa Paola Pilia, Dott. Matteo Manca
Centro di Riferimento Regionale per le Malattie Rare II Clinica Pediatrica Ospedale Pediatrico Microcitemico Assistenza transfrontaliera Dott.ssa Francesca Meloni Dott.ssa Paola Pilia, Dott. Matteo Manca
Un anno di Open AIFA
 Il dialogo con i pazienti. Bilancio dell Agenzia Un anno di Open AIFA Un anno di Open AIFA. 85 colloqui, 250 persone incontrate, oltre un centinaio tra documenti e dossier presentati e consultati in undici
Il dialogo con i pazienti. Bilancio dell Agenzia Un anno di Open AIFA Un anno di Open AIFA. 85 colloqui, 250 persone incontrate, oltre un centinaio tra documenti e dossier presentati e consultati in undici
REGIONE DEL VENETO AZIENDA UNITA LOCALE SOCIO-SANITARIA N. 6 VICENZA DELIBERAZIONE. n. 749 del 26-10-2015 O G G E T T O
 REGIONE DEL VENETO AZIENDA UNITA LOCALE SOCIO-SANITARIA N. 6 VICENZA DELIBERAZIONE n. 749 del 26-10-2015 O G G E T T O Istituzione Commissione per la valutazione della richiesta di farmaci non erogabili
REGIONE DEL VENETO AZIENDA UNITA LOCALE SOCIO-SANITARIA N. 6 VICENZA DELIBERAZIONE n. 749 del 26-10-2015 O G G E T T O Istituzione Commissione per la valutazione della richiesta di farmaci non erogabili
Piano delle Performance
 Comune di Pavullo nel Frignano Provincia di Modena Bilancio di Previsione 2011 Bilancio Pluriennale 2011 / 2013 Piano delle Performance *** Documento sulla compatibilità del sistema di programmazione,
Comune di Pavullo nel Frignano Provincia di Modena Bilancio di Previsione 2011 Bilancio Pluriennale 2011 / 2013 Piano delle Performance *** Documento sulla compatibilità del sistema di programmazione,
Salute e Sicurezza dei Lavoratori nella filiera del riciclo della carta: il punto di vista dell ente di certificazione. Milano 18 novembre 2008
 Elementi salienti e criticità di un Sistema di Gestione della Salute e Sicurezza dei Lavoratori nella filiera del riciclo della carta: il punto di vista dell ente di certificazione. Milano 18 novembre
Elementi salienti e criticità di un Sistema di Gestione della Salute e Sicurezza dei Lavoratori nella filiera del riciclo della carta: il punto di vista dell ente di certificazione. Milano 18 novembre
Piano d azione per l allineamento schede ADR Registri Farmaci sottoposti a Monitoraggio Rete Nazionale Farmacovigilanza
 Piano d azione per l allineamento schede ADR Registri Farmaci sottoposti a Monitoraggio Rete Nazionale Farmacovigilanza Ufficio Ricerca e Sperimentazione Clinica Coordinamento Registri Farmaci sottoposti
Piano d azione per l allineamento schede ADR Registri Farmaci sottoposti a Monitoraggio Rete Nazionale Farmacovigilanza Ufficio Ricerca e Sperimentazione Clinica Coordinamento Registri Farmaci sottoposti
LA RESEZIONE DELLE METASTASI EPATICHE NEL TUMORE METASTATICO DEL COLON RETTO
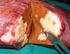 LA RESEZIONE DELLE METASTASI EPATICHE NEL TUMORE METASTATICO DEL COLON RETTO Cetuximab può ridurre la massa tumorale per permettere la resezione delle metastasi, anche, in pazienti inizialmente non resecabili,
LA RESEZIONE DELLE METASTASI EPATICHE NEL TUMORE METASTATICO DEL COLON RETTO Cetuximab può ridurre la massa tumorale per permettere la resezione delle metastasi, anche, in pazienti inizialmente non resecabili,
HTA: FATTORE DI CFESCITA O OSTACOLO ALL INNOVAZIONE?
 Dott. GEORGES PAIZIS Health Policy Director sanofi - aventis HTA: FATTORE DI CFESCITA O OSTACOLO ALL INNOVAZIONE? L Health Technology Assessment (HTA) è un processo multidisciplinare con ben documentate
Dott. GEORGES PAIZIS Health Policy Director sanofi - aventis HTA: FATTORE DI CFESCITA O OSTACOLO ALL INNOVAZIONE? L Health Technology Assessment (HTA) è un processo multidisciplinare con ben documentate
I SISTEMI DI GESTIONE DELLA SICUREZZA
 I SISTEMI DI GESTIONE DELLA SICUREZZA ing. Davide Musiani Modena- Mercoledì 8 Ottobre 2008 L art. 30 del D.Lgs 81/08 suggerisce due modelli organizzativi e di controllo considerati idonei ad avere efficacia
I SISTEMI DI GESTIONE DELLA SICUREZZA ing. Davide Musiani Modena- Mercoledì 8 Ottobre 2008 L art. 30 del D.Lgs 81/08 suggerisce due modelli organizzativi e di controllo considerati idonei ad avere efficacia
2) Esperienza lavorativa: - avere maturato un esperienza lavorativa in ambito sanitario di almeno 3 anni.
 Allegato B). Modello per le visite di verifica dei servizi trasfusionali e delle unità di raccolta del sangue e degli emocomponenti ai sensi dell articolo 5 del decreto legislativo 20 dicembre 2007, n.
Allegato B). Modello per le visite di verifica dei servizi trasfusionali e delle unità di raccolta del sangue e degli emocomponenti ai sensi dell articolo 5 del decreto legislativo 20 dicembre 2007, n.
UN SERVIZIO SANITARIO NAZIONALE MODERNO, EQUO, SOSTENIBILE E UNIVERSALE
 UN SERVIZIO SANITARIO NAZIONALE MODERNO, EQUO, SOSTENIBILE E UNIVERSALE - 1 - Il SSN è un valore per tutti gli italiani. Concorrere a migliorarlo continuamente è un impegno di tutti: Medici, Pazienti,
UN SERVIZIO SANITARIO NAZIONALE MODERNO, EQUO, SOSTENIBILE E UNIVERSALE - 1 - Il SSN è un valore per tutti gli italiani. Concorrere a migliorarlo continuamente è un impegno di tutti: Medici, Pazienti,
INTEGRAZIONE E CONFRONTO DELLE LINEE GUIDA UNI-INAIL CON NORME E STANDARD (Ohsas 18001, ISO, ecc.) Dott.ssa Monica Bianco Edizione: 1 Data: 03.12.
 Learning Center Engineering Management INTEGRAZIONE E CONFRONTO DELLE LINEE GUIDA UNI-INAIL CON NORME E STANDARD (Ohsas 18001, ISO, ecc.) Autore: Dott.ssa Monica Bianco Edizione: 1 Data: 03.12.2007 VIA
Learning Center Engineering Management INTEGRAZIONE E CONFRONTO DELLE LINEE GUIDA UNI-INAIL CON NORME E STANDARD (Ohsas 18001, ISO, ecc.) Autore: Dott.ssa Monica Bianco Edizione: 1 Data: 03.12.2007 VIA
Diagnosi precoce delle neoplasie del collo dell utero
 Diagnosi precoce delle neoplasie del collo dell utero La neoplasia del collo dell utero a livello mondiale rappresenta ancora il secondo tumore maligno della donna, con circa 500.000 nuovi casi stimati
Diagnosi precoce delle neoplasie del collo dell utero La neoplasia del collo dell utero a livello mondiale rappresenta ancora il secondo tumore maligno della donna, con circa 500.000 nuovi casi stimati
Il futuro della normazione tecnica tra legislazione, condivisione e mercato. Gian Luca Salerio Responsabile Area Normazione UNI
 Il futuro della normazione tecnica tra legislazione, condivisione e mercato Gian Luca Salerio Responsabile Area Normazione UNI Il settore dei dispositivi medici e più in generale della medicina è in forte
Il futuro della normazione tecnica tra legislazione, condivisione e mercato Gian Luca Salerio Responsabile Area Normazione UNI Il settore dei dispositivi medici e più in generale della medicina è in forte
Outsourcing del Controllo Qualità dei farmaci per la Sperimentazione Clinica
 Outsourcing del Controllo Qualità dei farmaci per la Sperimentazione Clinica Il ruolo del contratto nell allestimento ed aggiornamento del Product Specification File Rimini 10 Giugno 2009 Dr.ssa F. Iapicca
Outsourcing del Controllo Qualità dei farmaci per la Sperimentazione Clinica Il ruolo del contratto nell allestimento ed aggiornamento del Product Specification File Rimini 10 Giugno 2009 Dr.ssa F. Iapicca
PARTE III PROGRAMMA DI SPESA E.F. 2007 RELATIVO A SPESE CONDOMINIALI, ONERI ACCESSORI, ONERI DI PARTECIPAZIONE A CONSORZI E COMUNIONI
 28-3-2007 - BOLLETTINO UFFICIALE DELLA REGIONE EMILIA-ROMAGNA - PARTE SECONDA - N. 42 7 UPB 1.2.1.1.620 Spese generali di funzionamento Cap. 04350 Manutenzione ordinaria sul patrimonio disponibile e indisponibile
28-3-2007 - BOLLETTINO UFFICIALE DELLA REGIONE EMILIA-ROMAGNA - PARTE SECONDA - N. 42 7 UPB 1.2.1.1.620 Spese generali di funzionamento Cap. 04350 Manutenzione ordinaria sul patrimonio disponibile e indisponibile
Linee guida per il Comitato Tecnico Operativo 1
 Linee guida per il Comitato Tecnico Operativo 1 Introduzione Questo documento intende costituire una guida per i membri del Comitato Tecnico Operativo (CTO) del CIBER nello svolgimento delle loro attività.
Linee guida per il Comitato Tecnico Operativo 1 Introduzione Questo documento intende costituire una guida per i membri del Comitato Tecnico Operativo (CTO) del CIBER nello svolgimento delle loro attività.
UNITÁ OPERATIVA DI PSICOLOGIA OSPEDALIERA DIPARTIMENTO ONCOLOGICO
 UNITÁ OPERATIVA DI PSICOLOGIA OSPEDALIERA DIPARTIMENTO ONCOLOGICO 1/7 Attività L unità operativa di Psicologia Ospedaliera assicura interventi psicologici per: 1. Garantire, quando richiesto, il supporto
UNITÁ OPERATIVA DI PSICOLOGIA OSPEDALIERA DIPARTIMENTO ONCOLOGICO 1/7 Attività L unità operativa di Psicologia Ospedaliera assicura interventi psicologici per: 1. Garantire, quando richiesto, il supporto
MOBILITA SANITARIA IN AMBITO COMUNITARIO
 MOBILITA SANITARIA IN AMBITO COMUNITARIO Decreto Legislativo di recepimento della Direttiva 2011/24/UE Dipartimento della Programmazione e del Servizio Sanitario Nazionale Direzione Generale della Programmazione
MOBILITA SANITARIA IN AMBITO COMUNITARIO Decreto Legislativo di recepimento della Direttiva 2011/24/UE Dipartimento della Programmazione e del Servizio Sanitario Nazionale Direzione Generale della Programmazione
CONVENZIONE SUI SERVIZI SANITARI SUL LAVORO 1
 Convenzione 161 CONVENZIONE SUI SERVIZI SANITARI SUL LAVORO 1 La Conferenza generale dell Organizzazione Internazionale del Lavoro, Convocata a Ginevra dal Consiglio di Amministrazione dell Ufficio Internazionale
Convenzione 161 CONVENZIONE SUI SERVIZI SANITARI SUL LAVORO 1 La Conferenza generale dell Organizzazione Internazionale del Lavoro, Convocata a Ginevra dal Consiglio di Amministrazione dell Ufficio Internazionale
Appendice III. Competenza e definizione della competenza
 Appendice III. Competenza e definizione della competenza Competenze degli psicologi Lo scopo complessivo dell esercizio della professione di psicologo è di sviluppare e applicare i principi, le conoscenze,
Appendice III. Competenza e definizione della competenza Competenze degli psicologi Lo scopo complessivo dell esercizio della professione di psicologo è di sviluppare e applicare i principi, le conoscenze,
SOMMINISTRAZIONE DEI FARMACI A SCUOLA
 ISTITUTO TECNICO INDUSTRIALE STATALE Galileo Galilei Via D. Menci, 1-52100 Arezzo - Tel. 05753131 - Fax 0575313206 E-mail: galilei@itis.arezzo.it; Sito Internet: http://www.itis.arezzo.it C.F.: 80002160515
ISTITUTO TECNICO INDUSTRIALE STATALE Galileo Galilei Via D. Menci, 1-52100 Arezzo - Tel. 05753131 - Fax 0575313206 E-mail: galilei@itis.arezzo.it; Sito Internet: http://www.itis.arezzo.it C.F.: 80002160515
