Bianca Sistema di cristallizzazione:
|
|
|
- Gustavo Fusco
- 8 anni fa
- Visualizzazioni
Transcript
1 Museo del Liceo scientifico A. Avogadro MINERALI a cura del Gruppo Mineralogico Basso Canavese Scheda anagrafica n : 129 Reperto: 177 Nome: Colemanite Etimologia: Dal nome del commerciante americano W.T. Coleman ( )(Evans,1884) Formula chimica: Ca(B(3)B 2 (4)O 4 (OH) 3). H 2 O Durezza: 4,5 Striscia: Bianca Sistema di cristallizzazione: Monoclino I tre assi cristallografici sono tutti di differente lunghezza. Due giacciono su di un piano e sono tra loro perpendicolari; il terzo asse forma sempre un angolo diverso da 90 col piano dei primi due.campione n 177 proveniente dalla Turchia In questo sistema il massimo grado di simmetria è rappresentato dalla presenza di un asse binario, un piano e un centro di simmetria mentre il minimo si ha in cristalli con solo un asse di simmetria binario. Aspetto La colemanite è probabilmente il borato più comune, e in genere si presenta in splendidi cristalli. Splendidi cristalli pseudoromboedrici bipiramidati o prismatici equidimensionali, bianchi, limpidi e ricchi di facce,in cristalli incolori o bianchi più raramente colorati di rosa o di rosso da impurezze del diametro di due e più cm.; anche in masse granulari e spatiche, ricorda vagamente la calcite. Classe: Borati. I borati sono i sali dell'acido borico. Di aspetto non metallico, essi sono in generale teneri. In natura appaiono dappertutto dove si trova una forte concentrazione di boro, nella crosta terrestre, nell'acqua del mare, nei sedimenti, nelle esalazioni di magmi di composizioni varie. I borati si trovano pertanto nelle pegmatiti (borati anidri), nei giacimenti di rocce di contatto e metamorfiche, nei giacimenti salini, nei depositi dei corsi d'acqua e dei laghi mineralizzati, nei depositi creati dalle fumarole (esalazioni di vapore caldo e gas di vulcani in attività). Si distinguono i borati anidri dai borati idrati. Sono minerali poco abbondanti benchè formino talvolta localmente dei giacimenti interessanti dal punto di vista tecnico. Trasparenza: Trasparente translucida Lucentezza: Vitrea Sfaldatura: Perfetta secondo (010), imperfetta secondo (001) Frattura: Irregolare, subconcoide Peso specifico: 2,4
2 Colore: Bianco, grigio Composizione chimica teorica: CaO 27,28%, B 2 O 3 50,81%, H 2 O 21,91 % Luminescenza: Forte fosforescenza gialo-bianca e verde-bianca Proprietà Semidura, leggera, perfettamente sfaldabile; trasparente o traslucida, chimiche e con lucentezza vitrea subadamantina; polvere bianca. fisiche : Insolubile in acqua, è solubile in acido cloridrico a caldo (raffreddandosi la soluzione, precipitano aghi di acido borico fonde facilmente, decrepitando e colorando la fiamma di verde (boro). Trattamenti: Pulire con acqua distillata Minerali simili: Ulexite, inyoite, priceite, datolite Differenze: Durezza, densità Genesi: Sedimentaria (laghi borati). In bacini evaporatici continentali, probabilmente alimentati da sorgenti termali. Paragenesi: Ulexite, gesso, calcite, celestina Località: Molti degli esemplari in commercio provengono dall'enorme miniera a cielo aperto di Boron, in California; tuttavia, i cristalli più belli sono quelli, molto grandi, tozzi e spesso geminati, che provenivano dalla Valle della Morte(Death Valley )(Gower Gulch, Creek, Ryan). Altri ottimi campioni sono quelli delle miniere turche: (Bigadig Eskisehir), (campione n 177 scheda n 129 del museo del Liceo scientifico A.Avogadro) alcuni contengono anche realgar, in minuti aghetti, e formano magnifici contrasti di colore, di particolare suggestivo effetto. In Cile, nel Kazakhstan (URSS) Argentina (Jujuy), Usi: E uno dei principali minerali per l'estrazione dei boro e dei suoi sali, utilizzati nell'industria chimica, in quella farmaceutica e dei cosmetici, nella preparazione degli smalti per acciai, di vetri resistenti al calore (pyrex) particolarmente resistenti agli sbalzi termici di fondenti per saldatura. Attualmente è aumentato l'interesse per i; boro come combustibile per razzi e come parte di leghe ad altissima resistenza. Il materiale con realgar e altri solfuri di arsenico è alquanto meno pregiato per gli usi industriali e costituisce partite di grado inferiore, ma è il preferito dai collezionisti, i quali vi ricavano spesso dei buoni campioni Provenienza: Gruppo Mineralogico Basso Canavese Data: 26/05/ /01/2007 Il boro: Quando si parla di un elemento che si trova in natura, la prima domanda che ci si pone è: qual è la sua abbondanza? Si tratta cioè di un elemento abbondante come ferro, alluminio e carbonio, oppure raro come oro, radio e tallio? Una prima risposta a questa domanda viene data dalla tabella nella quale sono riportate le abbondanze degli elementi nell'universo. Questa tavola contiene, infatti, in forma sintetica, l'abbondanza di tutti gli elementi e mostra che i più leggeri sono anche quelli più abbondanti, mentre i più pesanti sono i più rari. Vi sono, però, alcune eccezioni e il boro è una di queste. Ciò è dovuto al fatto che il boro è un elemento dotato di particolari proprietà nucleari: infatti è in grado di assorbire molto efficacemente i neutroni che colpiscono il suo nucleo. Quando gli elementi si formarono mediante reazioni termonucleari nelle stelle, la materia era continuamente bombardata da neutroni, protoni e altre particelle; gli elementi, i cui nuclei non erano sufficientemente stabili, venivano trasmutati in altri,
3 Il boro in natura: La scoperta e le proprietà: divenendo così sempre più rari. Per questo motivo, litio, berillio e boro sono molto più rari nell'universo di quanto non lo siano gli elementi vicini nel sistema periodico, che seguono invece la regola generale. Sulla Terra il boro, essendo un elemento poco volatile, ha avuto modo di resistere al processo di fuga degli elementi e ora non è tra i più rari. Se diamo un' occhiata al sistema periodico degli elementi, vediamo che le proprietà chimiche del boro sono simili a quelle dell'alluminio, gallio, indio e tallio. Tuttavia, essendo il primo elemento del suo gruppo, ha proprietà particolari che lo fanno assomigliare al secondo elemento del gruppo successivo, cioè al silicio. Il boro, data la sua posizione nel terzo gruppo, ha proprietà caratteristiche rispetto agli altri elementi del suo stesso gruppo e cioè ha peso specifico minimo (2,34) e punto di fusione e di ebollizione molto più elevato. I minerali nei quali si trova il boro sono circa una settantina; tuttavia pochi hanno importanza per lo sfruttamento e l'estrazione dell' elemento. Le forme sotto le quali il boro compare con maggiore frequenza sono il borace, o tinkal, di formula Na 2 B 4 O 7 loh 2 O; l'acido borico naturale o sassolite, H 3 BO 3 ; la colemanite, Ca 2 B 6 O 11 5H 2 O. L'acido borico si trova misto a vapor d'acqua in molte emanazioni vulcaniche. In molti altri minerali la presenza del boro costituisce solo un'interessante curiosità e un motivo di studio per il suo comportamento geochimico. Il boro è presente, per esempio, nella tormalina e si trova in una certa quantità disciolto nell'acqua di mare. In Italia il boro si ricava, convenientemente, dai vapori delle emanazioni vulcaniche nella zona di Larderello, in Toscana. Nel 1808, Sir Humpry Davy e, indipendentemente, Gay-Lussac e Thénard isolarono l'elemento. Erano anni in cui si erano compiute molte scoperte scientifiche, tra cui anche scoperte di elementi. Il boro fu isolato in entrambi i casi facendo reagire l'anidride borica (B203) con il potassio. Le applicazioni del boro allo stato elementare sono praticamente inesistenti, dato che questo elemento possiede un'elevata affinità per l'ossigeno. Fonde alla temperatura di 2300 ; riscaldandolo ulteriormente non entra in ebollizione, se tenuto a pressione ordinaria, perché molto prima sublima. A 2550 la velocità di sublimazione è tale da consumarlo rapidamente. Il boro possiede due isotopi stabili che hanno la proprietà di assorbire i neutroni in maniera diversa, in particolare l'isotopo di massa 10 è quello che li assorbe in maggiore quantità. Infatti la presenza del boro nei materiali che costituiscono i reattori nucleari ne impedisce il funzionamento; la grafite usata come moderatore di neutroni, per esempio, ne deve contenere meno di una parte per dieci milioni. Nella grafìte il boro è presente sotto forma di carburo, che fonde molto sopra i 2400 e sublima solo a più di Perciò, non si può eliminare il boro col riscaldamento, che fa volatilizzare la maggior parte delle impurezze, ma si deve sfruttare la sua affinità per gli alogeni.
4 Il boro allo stato elementare si prepara per riscaldamento del cloruro BCl 3 a C in presenza di idrogeno che separa il cloro dalla molecola. Si prepara anche dall'anidride mediante. elementi avidi di ossigeno (riduttori), come magnesio e alluminio, con un processo simile all'alluminoterrnia o alla calciotermia Il boro si comporta quasi esclusivamente da trivalente; forma diversi composti con l'idrogeno, col carbonio, con l'ossigeno e con altri elementi. Per gli alogeni il boro mostra un' affinità spiccata e con essi forma composti costituiti da molecole a struttura planare nelle quali il piccolissimo ione B+++ è circondato dalle tre grosse sfere ioniche dell' alogeno. Nel caso del cloruro di boro lo ione B³+, che ha raggio ionico 0,20 A, è circondato dalle tre sfere di Clil cui raggio ionico è ben nove volte maggiore (1,81 A). La combinazione del boro con gli alogeni avviene spontaneamente con un fenomeno di combustione molto viva. Il fluoruro è gassoso, catalizza varie reazioni organiche, fra cui le reazioni di alchilazione e polimerizzazione. Insieme all'idruro di boro e litio subisce una reazione di doppio scambio che porta alla formazione di un composto ciclico puro, il diborano. La reazione è la seguente BF LiBH 4 3 LiF + 2 B 2 H 6 Un composto del boro che possiede una durezza molto vicina a quella del diamante è l'azoturo di boro BN, che si forma a temperatura elevata per combinazione diretta degli elementi. Tale composto ha punto di fusione elevatissimo ed è un ottimo isolante termico ed elettrico. Mentre a temperatura ordinaria l'azoturo di boro possiede una struttura esagonale simile a quella della grafite, a temperatura molto elevata e sotto forti pressioni si trasforma in una modificazione cubica nella quale gli atomi stanno più vicini e che presenta, quindi, una maggiore densità. È per questa modificazione che 1'azoturo di boro presenta una durezza almeno uguale a quella del. diamante; esso è stabile anche a bassa pressione e a bassa temperatura; il diamante, Invece, non presenta un così vasto campo di stabilità in quanto con l'aumentare della temperatura si trasforma in grafite. Il boro ha un'elevata affinità anche per l'acqua; a temperatura elevata, infatti, l'elemento scompone l'acqua e si unisce all'ossigeno. Il composto ossigenato fondamentale è l'anidride borica, B 2 O 3, sostanza igroscopica di aspetto vetroso; da questa derivano acidi diversi. Il più noto è l'acido ortoborico H3B03, detto comunemente acido borico, che cristallizza in lamelle bianche molto splendenti dotate di una bassa solubilità in acqua, circa il 3 % a 20 C. È un acido molto debole dotato di una leggera proprietà disinfettante; per questo motivo, la soluzione di acido borico viene impiegata come disinfettante per gli occhi. L'acido borico distilla con il vapor d'acqua ed è per questa sua proprietà che si trova nei vapori surriscaldati dei soffioni toscani da cui si estrae. A 100 C l'acido ortoborico perde una molecola d'acqua dando l'acido metaborico; a 140 C, invece, si trasforma in acido tetraborico secondo le seguenti
5 I composti ciclici: 100 reazioni H 2 _BO 3 H 2 O + HBO 2 ; 140 4H 3 BO 3 5H 2 O + H 2 B 4 O 7 Il borace è il sale di sodio dell'acido tetraborico che possiede la formula Na 2 B 4 O 7. La notevole quantità di acqua di cristallizzazione viene perduta facilmente per riscaldamento: a 80 essa si riduce a 5 molecole di acqua soltanto e a temperature ancora superiori diminuisce a 0. Il sale si scioglie in quest'acqua di cristallizzazione e quando questa, con l'aumentare della temperatura, è evaporata completamente, esso fonde scindendosi in 2 NaBO 2 e B 2 O 3 ; l'anidride borica così formatasi scioglie gli ossidi metallici: perciò il borace viene usato per pulire le superfici metalliche nella saldatura autogena o a lega di argento. Il borace fuso, se puro, è bianco trasparente, ma si colora intensamente se viene inquinato da ioni di altri elementi. Queste colorazioni sono così intense che permettono di riconoscere con sicurezza le sostanze sciolte dal borace. Il borace viene estesamente impiegato nell'industria vetraria. La sua funzione è quella di fondente del quarzo; i vetri, infatti, sono costituiti principalmente da biossido di silicio (il qùarzo), la cui temperatura di fusione è però elevatissima, circa L'aggiunta di borace abbassa questa temperatura di fusione trasformando l'impasto in una sostanza che rammollisce sopra la temperatura di , mentre sotto tale temperatura la sua viscosità è tanto elevata che si comporta quasi come un solido. La sua proprietà di mescolarsi facilmente al vetro e a sostanze ceramiche, abbassandone del grado voluto il punto di fusione, lo rende anche utile per la preparazione degli smalti a fuoco, vetri a basso punto di fusione, opacizzati con sostanze ceramiche, che si usano per ricoprire i metalli e proteggerli dalla corrosione. Affinché queste sostanze aderiscano al metallo anche dopo il raffreddamento, metallo e smalto devono possedere lo stesso coefficiente di dilatazione. Ciò si ottiene dosando la percentuale di borace contenuto nello smalto. Un importante composto ossigenato del boro è il metaperborato di sodio, la cui formula è NaBO 2 H 2 O 2.3H 2 O. Tale composto è stabile quando è solido, ma se viene sciolto in acqua e debolmente riscaldato, libera l'acqua ossigenata. della molecola e svolge ossigeno. Per questa sua proprietà viene usato come sbiancante in molti preparati e soprattutto nei detersivi per biancheria. Il boro forma una serie di composti combinati con l'idrogeno, che vengono detti borani o idruri di boro. Fra i borani, il più importante è il diborano, il primo termine, che ha formula B 2 H 6. A mano a mano che nella serie cresce il numero di atomi di boro, aumentano il punto di fusione e di ebollizione analogamente a quanto accade per gli idrocarburi. Riscaldando il composto solido BH 3 NH 3 si ottiene un liquido B 3 N 3 H 6 detto borazolo, la cui struttura è analoga a quella del benzolo, come mostra la figura 7; analogamente all'idrocarburo aromatico simile, anche questo composto del boro possiede la proprietà di sciogliere facilmente i grassi. 17 dicembre 2006
6
7
GEOLOGIA (studio della litosfera) Essa si divide in MINERALOGIA (studio dei minerali) e PETROGRAFIA ( studio delle rocce)
 GEOLOGIA (studio della litosfera) Essa si divide in MINERALOGIA (studio dei minerali) e PETROGRAFIA ( studio delle rocce) I MINERALI I minerali sono sostanze solide omogenee, inorganiche, esprimibili mediante
GEOLOGIA (studio della litosfera) Essa si divide in MINERALOGIA (studio dei minerali) e PETROGRAFIA ( studio delle rocce) I MINERALI I minerali sono sostanze solide omogenee, inorganiche, esprimibili mediante
Acidi e basi. HCl H + + Cl - (acido cloridrico) NaOH Na + + OH - (idrossido di sodio; soda caustica)
 Acidi e basi Per capire che cosa sono un acido e una base dal punto di vista chimico, bisogna riferirsi ad alcune proprietà chimiche dell'acqua. L'acqua, sia solida (ghiaccio), liquida o gassosa (vapore
Acidi e basi Per capire che cosa sono un acido e una base dal punto di vista chimico, bisogna riferirsi ad alcune proprietà chimiche dell'acqua. L'acqua, sia solida (ghiaccio), liquida o gassosa (vapore
Che cosa sono? Che forma hanno?
 Che cosa sono? Parti solide della crosta terrestre formate da Atomi - Ioni Molecole che sono disposti secondo un ordine Che forma hanno? Possono presentarsi in masse informi o sotto l aspetto di Poliedri
Che cosa sono? Parti solide della crosta terrestre formate da Atomi - Ioni Molecole che sono disposti secondo un ordine Che forma hanno? Possono presentarsi in masse informi o sotto l aspetto di Poliedri
Trasformazioni materia
 REAZIONI CHIMICHE Trasformazioni materia Trasformazioni fisiche (reversibili) Trasformazioni chimiche (irreversibili) È una trasformazione che non produce nuove sostanze È una trasformazione che produce
REAZIONI CHIMICHE Trasformazioni materia Trasformazioni fisiche (reversibili) Trasformazioni chimiche (irreversibili) È una trasformazione che non produce nuove sostanze È una trasformazione che produce
Le Rocce. Le rocce sono corpi solidi naturali costituiti da un aggregazione di più sostanze dette minerali.
 Minerali e Rocce Le Rocce Le rocce sono corpi solidi naturali costituiti da un aggregazione di più sostanze dette minerali. Origine delle rocce Le Rocce La roccia è tutto ciò che forma la crosta terrestre,
Minerali e Rocce Le Rocce Le rocce sono corpi solidi naturali costituiti da un aggregazione di più sostanze dette minerali. Origine delle rocce Le Rocce La roccia è tutto ciò che forma la crosta terrestre,
CO 2 aq l anidride carbonica disciolta, reagendo con l'acqua, forma acido carbonico secondo la reazione:
 DUREZZA DELLE ACQUE. Quando si parla di durezza di un acqua ci si riferisce fondamentalmente alla quantità di ioni calcio e di ioni magnesio disciolti in un certo volume di tale acqua. Ad eccezione delle
DUREZZA DELLE ACQUE. Quando si parla di durezza di un acqua ci si riferisce fondamentalmente alla quantità di ioni calcio e di ioni magnesio disciolti in un certo volume di tale acqua. Ad eccezione delle
La scuola integra culture. Scheda3c
 Scheda3c Gli ELEMENTI DEL CLIMA che caratterizzano le condizioni meteorologiche di una regione sono: la temperatura, la pressione atmosferica, i venti, l umidità e le precipitazioni. La temperatura è data
Scheda3c Gli ELEMENTI DEL CLIMA che caratterizzano le condizioni meteorologiche di una regione sono: la temperatura, la pressione atmosferica, i venti, l umidità e le precipitazioni. La temperatura è data
Le argille sono costituite da silice + allumina + acqua, ovviamente solo in termini di sostanze chimiche e non di struttura. Non sempre (o, meglio,
 Le argille sono costituite da silice + allumina + acqua, ovviamente solo in termini di sostanze chimiche e non di struttura. Non sempre (o, meglio, quasi mai) si può parlare di H 2 O molecolare; piuttosto
Le argille sono costituite da silice + allumina + acqua, ovviamente solo in termini di sostanze chimiche e non di struttura. Non sempre (o, meglio, quasi mai) si può parlare di H 2 O molecolare; piuttosto
Classificazione della materia: Sostanze pure e miscugli
 Classificazione della materia: Sostanze pure e miscugli la composizione e quindi le proprietà intensive sono le stesse in ogni parte del sistema La composizione e le proprietà intensive variano da una
Classificazione della materia: Sostanze pure e miscugli la composizione e quindi le proprietà intensive sono le stesse in ogni parte del sistema La composizione e le proprietà intensive variano da una
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA
 LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
Acqua azzurra, acqua chiara. Istituto Comprensivo della Galilla Scuola Media Dessì - Ballao
 Acqua azzurra, acqua chiara Istituto Comprensivo della Galilla Scuola Media Dessì - Ballao Proprietà fisiche Ecosistemi acquatici Origine della vita Ciclo dell acqua Acqua Scoperte Sensazioni Leggi La
Acqua azzurra, acqua chiara Istituto Comprensivo della Galilla Scuola Media Dessì - Ballao Proprietà fisiche Ecosistemi acquatici Origine della vita Ciclo dell acqua Acqua Scoperte Sensazioni Leggi La
Minerali e rocce. La Terra solida è formata da minerali.
 1.4 Minerali e rocce La Terra solida è formata da minerali. Un minerale è un corpo solido cristallino naturale omogeneo, costituito da un elemento o da un composto chimico inorganico e caratterizzato da
1.4 Minerali e rocce La Terra solida è formata da minerali. Un minerale è un corpo solido cristallino naturale omogeneo, costituito da un elemento o da un composto chimico inorganico e caratterizzato da
MISCUGLI E TECNICHE DI SEPARAZIONE
 MISCUGLI E TECNICHE DI SEPARAZIONE Classe 1^A Grafico Questo documento è solo una presentazione e non deve ritenersi completo se non è accompagnato dalla lezione in classe. Prof. Zarini Marta CLASSIFICAZIONE
MISCUGLI E TECNICHE DI SEPARAZIONE Classe 1^A Grafico Questo documento è solo una presentazione e non deve ritenersi completo se non è accompagnato dalla lezione in classe. Prof. Zarini Marta CLASSIFICAZIONE
PREPARAZIONE E CARATTERIZZAZIONE DEI VETRI COLORATI
 PREPARAZIONE E CARATTERIZZAZIONE DEI VETRI COLORATI DEFINIZIONE DI VETRO LO STATO VETROSO È QUELLO DI UN SOLIDO BLOCCATO NELLA STRUTTURA DISORDINATA DI UN LIQUIDO (FASE AMORFA) SOLIDO:ORDINE A LUNGO RAGGIO
PREPARAZIONE E CARATTERIZZAZIONE DEI VETRI COLORATI DEFINIZIONE DI VETRO LO STATO VETROSO È QUELLO DI UN SOLIDO BLOCCATO NELLA STRUTTURA DISORDINATA DI UN LIQUIDO (FASE AMORFA) SOLIDO:ORDINE A LUNGO RAGGIO
LA TERRA E LA CHIMICA: LA TAVOLA PERIODICA DEGLI ELEMENTI ELEMENTI E COMPOSTI
 I.I.S. A. PACINOTTI IST. TECNICO STATALE INDUSTRIALE Antonio PACINOTTI IST. TECNICO STATALE per GEOMETRI "Giorgio MASSARI" http://www.iispacinottive.it/ Via Caneve, n. 93 30173 - Mestre (VE) tel. 041 5350355
I.I.S. A. PACINOTTI IST. TECNICO STATALE INDUSTRIALE Antonio PACINOTTI IST. TECNICO STATALE per GEOMETRI "Giorgio MASSARI" http://www.iispacinottive.it/ Via Caneve, n. 93 30173 - Mestre (VE) tel. 041 5350355
Capitolo 7. Le soluzioni
 Capitolo 7 Le soluzioni Come visto prima, mescolando tra loro sostanze pure esse danno origine a miscele di sostanze o semplicemente miscele. Una miscela può essere omogenea ( detta anche soluzione) o
Capitolo 7 Le soluzioni Come visto prima, mescolando tra loro sostanze pure esse danno origine a miscele di sostanze o semplicemente miscele. Una miscela può essere omogenea ( detta anche soluzione) o
Determinazione della composizione elementare dello ione molecolare. Metodo dell abbondanza isotopica. Misure di massa esatta
 Determinazione della composizione elementare dello ione molecolare Metodo dell abbondanza isotopica Misure di massa esatta PREMESSA: ISOTOPI PICCHI ISOTOPICI Il picco dello ione molecolare è spesso accompagnato
Determinazione della composizione elementare dello ione molecolare Metodo dell abbondanza isotopica Misure di massa esatta PREMESSA: ISOTOPI PICCHI ISOTOPICI Il picco dello ione molecolare è spesso accompagnato
Durezza è la resistenza che ha un minerale nell'opporsi alla scalfittura. utilizzata la scala di Mohs.
 PROPRIETA FISICHE DEI MINERALI Densità g/cm 3 Durezza è la resistenza che ha un minerale nell'opporsi alla scalfittura. utilizzata la scala di Mohs. Sfaldatura: proprietà di rompersi più facilmente lungo
PROPRIETA FISICHE DEI MINERALI Densità g/cm 3 Durezza è la resistenza che ha un minerale nell'opporsi alla scalfittura. utilizzata la scala di Mohs. Sfaldatura: proprietà di rompersi più facilmente lungo
Tipi di reazioni. Reazioni chimiche. Di dissociazione. Di sintesi. Di semplice scambio. Di doppio scambio. Reazioni complesse
 Tipi di reazioni Le reazioni chimiche vengono tradizionalmente classificate a seconda del tipo di trasformazione subita dai reagenti: Reazioni chimiche possono essere Di dissociazione Una sostanza subisce
Tipi di reazioni Le reazioni chimiche vengono tradizionalmente classificate a seconda del tipo di trasformazione subita dai reagenti: Reazioni chimiche possono essere Di dissociazione Una sostanza subisce
1)Quale tra i seguenti elementi è un gas nobile? a. Si b. Mo c. Ge d. He. 2) L'acqua è:
 1)Quale tra i seguenti elementi è un gas nobile? a. Si b. Mo c. Ge d. He 2) L'acqua è: a. una sostanza elementare b. un composto chimico c. una miscela omogenea d. una soluzione 3) Quale dei seguenti elementi
1)Quale tra i seguenti elementi è un gas nobile? a. Si b. Mo c. Ge d. He 2) L'acqua è: a. una sostanza elementare b. un composto chimico c. una miscela omogenea d. una soluzione 3) Quale dei seguenti elementi
Università di Pisa Facoltà di Ingegneria. Leghe non ferrose. Chimica Applicata. Prof. Cristiano Nicolella
 Università di Pisa Facoltà di Ingegneria Leghe non ferrose Chimica Applicata Prof. Cristiano Nicolella Leghe non ferrose Minerali di alluminio L alluminio è uno degli elementi più abbondanti sulla crosta
Università di Pisa Facoltà di Ingegneria Leghe non ferrose Chimica Applicata Prof. Cristiano Nicolella Leghe non ferrose Minerali di alluminio L alluminio è uno degli elementi più abbondanti sulla crosta
'RPDQGHFRQFHWWXDOL Alcuni interrogativi su fenomeni fisici e chimici
 ,OPDWHULDOHGLGDWWLFRFKHVHJXHqVWDWRVFHOWRWUDGRWWRHDGDWWDWRGDO*UXSSRGLFKLPLFD GHOO,7,60DMRUDQDGL*UXJOLDVFR7RULQR0DUFR)DODVFD$QJHOR&LPHQLV3DROD&RVFLD /RUHGDQD$QJHOHUL$QWRQHOOD0DUWLQL'DULR*D]]ROD*UD]LD5L]]R*LXVL'L'LR
,OPDWHULDOHGLGDWWLFRFKHVHJXHqVWDWRVFHOWRWUDGRWWRHDGDWWDWRGDO*UXSSRGLFKLPLFD GHOO,7,60DMRUDQDGL*UXJOLDVFR7RULQR0DUFR)DODVFD$QJHOR&LPHQLV3DROD&RVFLD /RUHGDQD$QJHOHUL$QWRQHOOD0DUWLQL'DULR*D]]ROD*UD]LD5L]]R*LXVL'L'LR
LABORATORIO DI CHIMICA GENERALE E INORGANICA
 UNIVERSITA DEGLI STUDI DI MILANO Facoltà di Scienze Matematiche, Fisiche e Naturali Corso di Laurea Triennale in Chimica CORSO DI: LABORATORIO DI CHIMICA GENERALE E INORGANICA Docente: Dr. Alessandro Caselli
UNIVERSITA DEGLI STUDI DI MILANO Facoltà di Scienze Matematiche, Fisiche e Naturali Corso di Laurea Triennale in Chimica CORSO DI: LABORATORIO DI CHIMICA GENERALE E INORGANICA Docente: Dr. Alessandro Caselli
Analisi delle acque dell isola di Favignana
 Analisi delle acque dell isola di Favignana Durante le attività svolte al campo scuola nell ambito del progetto Un mare di.. risorse, il nostro gruppo si è occupato di analizzare le acque del mare in diversi
Analisi delle acque dell isola di Favignana Durante le attività svolte al campo scuola nell ambito del progetto Un mare di.. risorse, il nostro gruppo si è occupato di analizzare le acque del mare in diversi
1. Un elemento Ä formato da particelle indivisibili chiamate atomi. 2. Gli atomi di uno specifico elemento hanno proprietå identiche. 3.
 Atomi e molecole Ipotesi di Dalton (primi dell 800) 1. Un elemento Ä formato da particelle indivisibili chiamate atomi. 2. Gli atomi di uno specifico elemento hanno proprietå identiche. 3. Gli atomi dei
Atomi e molecole Ipotesi di Dalton (primi dell 800) 1. Un elemento Ä formato da particelle indivisibili chiamate atomi. 2. Gli atomi di uno specifico elemento hanno proprietå identiche. 3. Gli atomi dei
Esperimenti Informazioni per il PD
 Informazioni per il PD 1/7 Compito Gli alunni conducono degli esperimenti con il sale avendo così la possibilità di studiarlo in quanto composto chimico. Grazie ai vari esperimenti imparano anche quali
Informazioni per il PD 1/7 Compito Gli alunni conducono degli esperimenti con il sale avendo così la possibilità di studiarlo in quanto composto chimico. Grazie ai vari esperimenti imparano anche quali
LA CORRENTE ELETTRICA Prof. Erasmo Modica erasmo@galois.it
 LA CORRENTE ELETTRICA Prof. Erasmo Modica erasmo@galois.it L INTENSITÀ DELLA CORRENTE ELETTRICA Consideriamo una lampadina inserita in un circuito elettrico costituito da fili metallici ed un interruttore.
LA CORRENTE ELETTRICA Prof. Erasmo Modica erasmo@galois.it L INTENSITÀ DELLA CORRENTE ELETTRICA Consideriamo una lampadina inserita in un circuito elettrico costituito da fili metallici ed un interruttore.
Laura Beata Classe 4 B Concorso Sperimento Anch io Silvia Valesano Classe 4 B
 Laura Beata Classe 4 B Concorso Sperimento Anch io Silvia Valesano Classe 4 B RELAZINI DI LABRATRI (Italiano) Titolo: : Cosa mangiamo veramente? Scopo: 1. Scoprire in quali alimenti ci sono o non ci sono
Laura Beata Classe 4 B Concorso Sperimento Anch io Silvia Valesano Classe 4 B RELAZINI DI LABRATRI (Italiano) Titolo: : Cosa mangiamo veramente? Scopo: 1. Scoprire in quali alimenti ci sono o non ci sono
Energia nelle reazioni chimiche. Lezioni d'autore di Giorgio Benedetti
 Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
ENERGIA E CENTRALI SOLARI
 ENERGIA E CENTRALI SOLARI Si dice solare l energia raggiante sprigionata dal Sole per effetto di reazioni nucleari (fusione dell idrogeno) e trasmessa alla Terra sotto forma di radiazione elettromagnetica.
ENERGIA E CENTRALI SOLARI Si dice solare l energia raggiante sprigionata dal Sole per effetto di reazioni nucleari (fusione dell idrogeno) e trasmessa alla Terra sotto forma di radiazione elettromagnetica.
Elettricità e magnetismo
 E1 Cos'è l'elettricità La carica elettrica è una proprietà delle particelle elementari (protoni e elettroni) che formano l'atomo. I protoni hanno carica elettrica positiva. Gli elettroni hanno carica elettrica
E1 Cos'è l'elettricità La carica elettrica è una proprietà delle particelle elementari (protoni e elettroni) che formano l'atomo. I protoni hanno carica elettrica positiva. Gli elettroni hanno carica elettrica
MISURE DI POTERE CALORIFICO E COMPOSIZIONE
 MISURE DI POTERE CALORIFICO E COMPOSIZIONE Potere calorifico dei combustibili: bomba calorimetrica e calorimetro di Junkers Composizione: gascromatografia Composizione dei gas combusti: o Sonda λ o Strumenti
MISURE DI POTERE CALORIFICO E COMPOSIZIONE Potere calorifico dei combustibili: bomba calorimetrica e calorimetro di Junkers Composizione: gascromatografia Composizione dei gas combusti: o Sonda λ o Strumenti
UNIVERSITA' DEGLI STUDI DI CASSINO E DEL LAZIO MERIDIONALE. Energia Geotermica
 UNIVERSITA' DEGLI STUDI DI CASSINO E DEL LAZIO MERIDIONALE Energia Geotermica La struttura della Terra Il calore geotermico si genera per decadimento di sostanze radioattive e si propaga verso la superficie
UNIVERSITA' DEGLI STUDI DI CASSINO E DEL LAZIO MERIDIONALE Energia Geotermica La struttura della Terra Il calore geotermico si genera per decadimento di sostanze radioattive e si propaga verso la superficie
LA MATERIA Suggerimenti didattici e schede
 LA MATERIA Suggerimenti didattici e schede Iniziamo il percorso chiedendo a un bambino di consegnarci alcune cose: una gomma, una penna, un capello. Domandiamo a un altro di consegnarci una gioia, una
LA MATERIA Suggerimenti didattici e schede Iniziamo il percorso chiedendo a un bambino di consegnarci alcune cose: una gomma, una penna, un capello. Domandiamo a un altro di consegnarci una gioia, una
La combustione. Docente: prof.ssa Lobello Carmela
 La combustione Percorso didattico realizzato dalla classe II D Istituto d Istruzione secondaria di I grado S Francesco d Assisi Francavilla Fontana (Br) Docente: prof.ssa Lobello Carmela Perché la combustione?
La combustione Percorso didattico realizzato dalla classe II D Istituto d Istruzione secondaria di I grado S Francesco d Assisi Francavilla Fontana (Br) Docente: prof.ssa Lobello Carmela Perché la combustione?
Che cos è un detersivo?
 Che cos è un detersivo? Miscela di sostanze chimiche che mischiate all acqua sono in grado di rimuovere lo sporco Agiscono sulle sostanze che non si sciolgono facilmente in acqua (idrofobe) I principali
Che cos è un detersivo? Miscela di sostanze chimiche che mischiate all acqua sono in grado di rimuovere lo sporco Agiscono sulle sostanze che non si sciolgono facilmente in acqua (idrofobe) I principali
CALORE. Compie lavoro. Il calore è energia. Temperatura e calore. L energia è la capacità di un corpo di compiere un lavoro
 Cos è il calore? Per rispondere si osservino le seguenti immagini Temperatura e calore Il calore del termosifone fa girare una girandola Il calore del termosifone fa scoppiare un palloncino Il calore del
Cos è il calore? Per rispondere si osservino le seguenti immagini Temperatura e calore Il calore del termosifone fa girare una girandola Il calore del termosifone fa scoppiare un palloncino Il calore del
Nascita e morte delle stelle
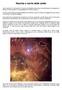 Nascita e morte delle stelle Se la materia che componeva l universo primordiale fosse stata tutta perfettamente omogenea e diffusa in modo uguale, non esisterebbero né stelle né pianeti. C erano invece
Nascita e morte delle stelle Se la materia che componeva l universo primordiale fosse stata tutta perfettamente omogenea e diffusa in modo uguale, non esisterebbero né stelle né pianeti. C erano invece
Dalla roccia al metallo: metallurgia estrattiva
 Dalla roccia al metallo: metallurgia estrattiva http://www.tavolaperiodica.it/metallurgia_estrattiva.html Immaginando in maniera assolutamente fantasiosa e personale che così si sia avuta l intuizione
Dalla roccia al metallo: metallurgia estrattiva http://www.tavolaperiodica.it/metallurgia_estrattiva.html Immaginando in maniera assolutamente fantasiosa e personale che così si sia avuta l intuizione
CICLO DELL ACQUA. Marco Carozzi
 CICLO DELL ACQUA Marco Carozzi Sommario Ciclo biogeochimico La molecola d acqua: breve introduzione Ciclo dell acqua ed elementi del ciclo evaporazione, evapotraspirazione, condensazione, precipitazioni,
CICLO DELL ACQUA Marco Carozzi Sommario Ciclo biogeochimico La molecola d acqua: breve introduzione Ciclo dell acqua ed elementi del ciclo evaporazione, evapotraspirazione, condensazione, precipitazioni,
METALLI FERROSI GHISA ACCIAIO
 METALLI FERROSI I metalli ferrosi sono i metalli e le leghe metalliche che contengono ferro. Le leghe ferrose più importanti sono l acciaio e la ghisa. ACCIAIO: lega metallica costituita da ferro e carbonio,
METALLI FERROSI I metalli ferrosi sono i metalli e le leghe metalliche che contengono ferro. Le leghe ferrose più importanti sono l acciaio e la ghisa. ACCIAIO: lega metallica costituita da ferro e carbonio,
Cosa misura il ph: la concentrazione di ioni H +, che si scrive [H + ]. La definizione di ph è: ph = -log 10 [H + ]
![Cosa misura il ph: la concentrazione di ioni H +, che si scrive [H + ]. La definizione di ph è: ph = -log 10 [H + ] Cosa misura il ph: la concentrazione di ioni H +, che si scrive [H + ]. La definizione di ph è: ph = -log 10 [H + ]](/thumbs/34/16945364.jpg) La molecola d acqua è un dipolo perché l atomo di ossigeno è molto elettronegativo ed attira più vicini a sé gli elettroni di legame. Questo, unito alla forma della molecola, produce un accumulo di carica
La molecola d acqua è un dipolo perché l atomo di ossigeno è molto elettronegativo ed attira più vicini a sé gli elettroni di legame. Questo, unito alla forma della molecola, produce un accumulo di carica
ENERGIA NELLE REAZIONI CHIMICHE
 ENERGIA NELLE REAZIONI CHIMICHE Nelle trasformazioni chimiche e fisiche della materia avvengono modifiche nelle interazioni tra le particelle che comportano sempre variazioni di energia "C è un fatto,
ENERGIA NELLE REAZIONI CHIMICHE Nelle trasformazioni chimiche e fisiche della materia avvengono modifiche nelle interazioni tra le particelle che comportano sempre variazioni di energia "C è un fatto,
INTERVENTO DI CLAUDIA RICCARDI PLASMAPROMETEO - Dipartimento di Fisica Università degli Studi di Milano - Bicocca
 INTERVENTO DI CLAUDIA RICCARDI PLASMAPROMETEO - Dipartimento di Fisica Università degli Studi di Milano - Bicocca La ricerca come strumento per lo sviluppo aziendale: sinergia tra università e industria
INTERVENTO DI CLAUDIA RICCARDI PLASMAPROMETEO - Dipartimento di Fisica Università degli Studi di Milano - Bicocca La ricerca come strumento per lo sviluppo aziendale: sinergia tra università e industria
Perché il logaritmo è così importante?
 Esempio 1. Perché il logaritmo è così importante? (concentrazione di ioni di idrogeno in una soluzione, il ph) Un sistema solido o liquido, costituito da due o più componenti, (sale disciolto nell'acqua),
Esempio 1. Perché il logaritmo è così importante? (concentrazione di ioni di idrogeno in una soluzione, il ph) Un sistema solido o liquido, costituito da due o più componenti, (sale disciolto nell'acqua),
tecnologia PROPRIETÀ DEI METALLI Scuola secondaria primo grado. classi prime Autore: Giuseppe FRANZÈ
 tecnologia PROPRIETÀ DEI METALLI Scuola secondaria primo grado. classi prime Autore: Giuseppe FRANZÈ LE PROPRIETÀ DEI MATERIALI DA COSTRUZIONE Si possono considerare come l'insieme delle caratteristiche
tecnologia PROPRIETÀ DEI METALLI Scuola secondaria primo grado. classi prime Autore: Giuseppe FRANZÈ LE PROPRIETÀ DEI MATERIALI DA COSTRUZIONE Si possono considerare come l'insieme delle caratteristiche
DISTILLAZIONE: PREMESSE
 DISTILLAZIONE: PREMESSE PROCESSO DI ELEZIONE NELLA PREPARAZIONE DI ACQUA PER PREPARAZIONI INIETTABILI PROCESSO GENERALMENTE APPLICATO COME STADIO FINALE DI PURIFICAZIONE AD UN ACQUA GIA TRATTATA IL TIPO
DISTILLAZIONE: PREMESSE PROCESSO DI ELEZIONE NELLA PREPARAZIONE DI ACQUA PER PREPARAZIONI INIETTABILI PROCESSO GENERALMENTE APPLICATO COME STADIO FINALE DI PURIFICAZIONE AD UN ACQUA GIA TRATTATA IL TIPO
MODULO 3 - LA MATERIA: COMPOSIZIONE E TRASFORMAZIONI
 MODULO 3 - LA MATERIA: COMPOSIZIONE E TRASFORMAZIONI La materia è tutto ciò che ha una massa, energia e occupa spazio, cioè ha un volume; essa si classifica in base alla sua composizione chimica ed in
MODULO 3 - LA MATERIA: COMPOSIZIONE E TRASFORMAZIONI La materia è tutto ciò che ha una massa, energia e occupa spazio, cioè ha un volume; essa si classifica in base alla sua composizione chimica ed in
I materiali di rivestimento. di Maximillian Vegetti, Federico Maffioli e Davide Biganzoli
 I materiali di rivestimento di Maximillian Vegetti, Federico Maffioli e Davide Biganzoli Porosità della ceramica -Le ceramiche hanno la caratteristica di essere porose, un fattore che non le ha rese utilizzabili
I materiali di rivestimento di Maximillian Vegetti, Federico Maffioli e Davide Biganzoli Porosità della ceramica -Le ceramiche hanno la caratteristica di essere porose, un fattore che non le ha rese utilizzabili
TEORIA CINETICA DEI GAS
 TEORIA CINETICA DEI GAS La teoria cinetica dei gas è corrispondente con, e infatti prevede, le proprietà dei gas. Nella materia gassosa, gli atomi o le molecole sono separati da grandi distanze e sono
TEORIA CINETICA DEI GAS La teoria cinetica dei gas è corrispondente con, e infatti prevede, le proprietà dei gas. Nella materia gassosa, gli atomi o le molecole sono separati da grandi distanze e sono
13 La temperatura - 8. Il gas perfetto
 La mole e l equazione del gas perfetto Tutto ciò che vediamo intorno a noi è composto di piccolissimi grani, che chiamiamo «molecole». Per esempio, il ghiaccio, l acqua liquida e il vapore acqueo sono
La mole e l equazione del gas perfetto Tutto ciò che vediamo intorno a noi è composto di piccolissimi grani, che chiamiamo «molecole». Per esempio, il ghiaccio, l acqua liquida e il vapore acqueo sono
materia atomi miscugli omogenei e eterogenei sostanze elementari composti
 Elementi e Composti materia miscugli omogenei e eterogenei sostanze elementari composti atomi Gli atomi sono, per convenzione, le unità costituenti le sostanze Le sostanze possono essere costituite da
Elementi e Composti materia miscugli omogenei e eterogenei sostanze elementari composti atomi Gli atomi sono, per convenzione, le unità costituenti le sostanze Le sostanze possono essere costituite da
TERMOMETRIA E PROCESSI TERMICI
 TERMOMETRIA E PROCESSI TERMICI SISTEMA parte di materia e/o spazio, idealmente isolata, su cui si concentra ntra l attenzione dell osservatore AMBIENTE ESTERNO tutto ciò che sta al di fuori, ma pur sempre
TERMOMETRIA E PROCESSI TERMICI SISTEMA parte di materia e/o spazio, idealmente isolata, su cui si concentra ntra l attenzione dell osservatore AMBIENTE ESTERNO tutto ciò che sta al di fuori, ma pur sempre
Capacità di assorbire una deformazione plastica senza rompersi: alta=duttile (es. oro) bassa=fragile (es. vetro)
 Capacità di assorbire una deformazione plastica senza rompersi: alta=duttile (es. oro) bassa=fragile (es. vetro) E dipendente dalla temperatura:capacità di riposizionamento di difetti ed atomi (diffusione
Capacità di assorbire una deformazione plastica senza rompersi: alta=duttile (es. oro) bassa=fragile (es. vetro) E dipendente dalla temperatura:capacità di riposizionamento di difetti ed atomi (diffusione
INTRODUZIONE: PERDITE IN FIBRA OTTICA
 INTRODUZIONE: PERDITE IN FIBRA OTTICA Il nucleo (o core ) di una fibra ottica è costituito da vetro ad elevatissima purezza, dal momento che la luce deve attraversare migliaia di metri di vetro del nucleo.
INTRODUZIONE: PERDITE IN FIBRA OTTICA Il nucleo (o core ) di una fibra ottica è costituito da vetro ad elevatissima purezza, dal momento che la luce deve attraversare migliaia di metri di vetro del nucleo.
Corso di aggiornamento su rocce, minerali e fossili della Regione Marche
 Corso di aggiornamento su rocce, minerali e fossili della Regione Marche Progetto ISS Fermo, 23 Maggio 2011 Prof Pierluigi Stroppa Oro nativo Malachite Rosa del deserto Un minerale è una sostanza naturale
Corso di aggiornamento su rocce, minerali e fossili della Regione Marche Progetto ISS Fermo, 23 Maggio 2011 Prof Pierluigi Stroppa Oro nativo Malachite Rosa del deserto Un minerale è una sostanza naturale
La raffinazione del petrolio
 La raffinazione del petrolio Approfondimento sulla distillazione per la I^ Itis Prof. Maurizi Franco Itis Einstein Roma ( foto ed immagini reperiti da internet, eventuali detentori di diritti sono pregati
La raffinazione del petrolio Approfondimento sulla distillazione per la I^ Itis Prof. Maurizi Franco Itis Einstein Roma ( foto ed immagini reperiti da internet, eventuali detentori di diritti sono pregati
Le proprietà periodiche degli elementi LA LEZIONE
 Le proprietà periodiche degli elementi LA LEZIONE Le proprietà degli elementi mostrano delle tendenze che possono essere predette usando il sistema periodico ed essere spiegate e comprese analizzando la
Le proprietà periodiche degli elementi LA LEZIONE Le proprietà degli elementi mostrano delle tendenze che possono essere predette usando il sistema periodico ed essere spiegate e comprese analizzando la
Campione sciolto in un solvente (deuterato) e. posto in un tubo. di vetro a pareti sottili di diametro di 5 mm e lungo circa 20 cm
 posto in un tubo Campione sciolto in un solvente (deuterato) e di vetro a pareti sottili di diametro di 5 mm e lungo circa 20 cm o spettrometro NMR è formato da alcuni mponenti fondamentali: un magnete,
posto in un tubo Campione sciolto in un solvente (deuterato) e di vetro a pareti sottili di diametro di 5 mm e lungo circa 20 cm o spettrometro NMR è formato da alcuni mponenti fondamentali: un magnete,
GAS NATURALE O METANO
 Composto prevalentemente da un idrocarburo: metano da da cui prende il nome. GAS NATURALE O METANO Alto potere calorifico. Mancanza di tossicità e impurità. È un'ottima risorsa energetica. È l'energia
Composto prevalentemente da un idrocarburo: metano da da cui prende il nome. GAS NATURALE O METANO Alto potere calorifico. Mancanza di tossicità e impurità. È un'ottima risorsa energetica. È l'energia
I MINERALI DELLA CROSTA TERRESTRE
 I MINERALI DELLA CROSTA TERRESTRE Sono solidi cristallini, di origine inorganica, caratterizzati da una precisa formula chimica. Una sostanza è un minerale se: si presenta come solido cristallino, cioè
I MINERALI DELLA CROSTA TERRESTRE Sono solidi cristallini, di origine inorganica, caratterizzati da una precisa formula chimica. Una sostanza è un minerale se: si presenta come solido cristallino, cioè
QUALITÀ E TRATTAMENTO DELL ACQUA DEL CIRCUITO CHIUSO
 QUALITÀ E TRATTAMENTO DELL ACQUA DEL CIRCUITO CHIUSO (PARTE 1) FOCUS TECNICO Gli impianti di riscaldamento sono spesso soggetti a inconvenienti quali depositi e incrostazioni, perdita di efficienza nello
QUALITÀ E TRATTAMENTO DELL ACQUA DEL CIRCUITO CHIUSO (PARTE 1) FOCUS TECNICO Gli impianti di riscaldamento sono spesso soggetti a inconvenienti quali depositi e incrostazioni, perdita di efficienza nello
GIOCHI DELLA CHIMICA
 GIOCHI DELLA CHIMICA FASE D ISTITUTO (TRIENNIO) 21 marzo 2016 La prova è costituita da 50 quesiti. ALUNNO CLASSE Scrivi la risposta a ciascuna domanda nel foglio risposte allegato. 1. Quale dei seguenti
GIOCHI DELLA CHIMICA FASE D ISTITUTO (TRIENNIO) 21 marzo 2016 La prova è costituita da 50 quesiti. ALUNNO CLASSE Scrivi la risposta a ciascuna domanda nel foglio risposte allegato. 1. Quale dei seguenti
LEZIONE 1. Materia: Proprietà e Misura
 LEZIONE 1 Materia: Proprietà e Misura MISCELE, COMPOSTI, ELEMENTI SOSTANZE PURE E MISCUGLI La materia può essere suddivisa in sostanze pure e miscugli. Un sistema è puro solo se è formato da una singola
LEZIONE 1 Materia: Proprietà e Misura MISCELE, COMPOSTI, ELEMENTI SOSTANZE PURE E MISCUGLI La materia può essere suddivisa in sostanze pure e miscugli. Un sistema è puro solo se è formato da una singola
I METALLI. I metalli sono materiali strutturali costituiti ciascuno da un singolo elemento. Hanno tra loro proprietà molto simili.
 M et 1 all I METALLI I metalli sono materiali strutturali costituiti ciascuno da un singolo elemento. Hanno tra loro proprietà molto simili. Proprietà Le principali proprietà dei metalli sono le seguenti:
M et 1 all I METALLI I metalli sono materiali strutturali costituiti ciascuno da un singolo elemento. Hanno tra loro proprietà molto simili. Proprietà Le principali proprietà dei metalli sono le seguenti:
Lezione 15 metodi di analisi termici legati alla separazione di fase. Separazione di fase. Fasi della materia: solido, liquido, gas
 Lezione 15 metodi di analisi termici legati alla separazione di fase Separazione di fase Fasi della materia: solido, liquido, gas SOLIDO Scioglimento solidificazione LIQUIDO evaporazione condensazione
Lezione 15 metodi di analisi termici legati alla separazione di fase Separazione di fase Fasi della materia: solido, liquido, gas SOLIDO Scioglimento solidificazione LIQUIDO evaporazione condensazione
Breve compendio delle ceramiche esistenti e delle loro qualità.
 Breve compendio delle ceramiche esistenti e delle loro qualità. Materiale sintetico parzialmente o totalmente cristallino solido, inorganico, non metallico, formato a freddo e consolidato per trattamento
Breve compendio delle ceramiche esistenti e delle loro qualità. Materiale sintetico parzialmente o totalmente cristallino solido, inorganico, non metallico, formato a freddo e consolidato per trattamento
I TEST DI CHIMICA - INGEGNERIA DELL INFORMAZIONE AA 04/05
 I TEST DI CHIMICA - INGEGNERIA DELL INFORMAZIONE AA 04/05 COGNOME E NOME: 1. Br 1 si è trasformato in Br +3 in una reazione in cui lo ione bromuro: A) ha acquistato 3 elettroni B) ha ceduto 4 elettroni
I TEST DI CHIMICA - INGEGNERIA DELL INFORMAZIONE AA 04/05 COGNOME E NOME: 1. Br 1 si è trasformato in Br +3 in una reazione in cui lo ione bromuro: A) ha acquistato 3 elettroni B) ha ceduto 4 elettroni
È importante quindi conoscere le proprietà chimiche dell acqua. Le reazioni acido base sono particolari esempi di equilibrio chimico in fase acquosa
 Premessa Le nozioni di acido e di base non sono concetti assoluti ma sono relativi al mezzo in cui tale sostanze sono sciolte. L acqua è il solvente per eccellenza, scelto per studiare le caratteristiche
Premessa Le nozioni di acido e di base non sono concetti assoluti ma sono relativi al mezzo in cui tale sostanze sono sciolte. L acqua è il solvente per eccellenza, scelto per studiare le caratteristiche
PREVENZIONE INCENDI. Celsino Govoni
 PREVENZIONE INCENDI Celsino Govoni Che cos è un ESPLOSIONE? Cosa c era dentro a quell ambulatorio? Cosa è rimasto di quel centro medico posto in quel paesino!! La causa, a volte, è di piccole dimensioni
PREVENZIONE INCENDI Celsino Govoni Che cos è un ESPLOSIONE? Cosa c era dentro a quell ambulatorio? Cosa è rimasto di quel centro medico posto in quel paesino!! La causa, a volte, è di piccole dimensioni
352&(662',&20%867,21(
 352&(662',&20%867,21( Il calore utilizzato come fonte energetica convertibile in lavoro nella maggior parte dei casi, è prodotto dalla combustione di sostanze (es. carbone, metano, gasolio) chiamate combustibili.
352&(662',&20%867,21( Il calore utilizzato come fonte energetica convertibile in lavoro nella maggior parte dei casi, è prodotto dalla combustione di sostanze (es. carbone, metano, gasolio) chiamate combustibili.
Ciao, il mio nome è Sheppy e aiuterò il professore nella sua lezione! Salve, io sono il prof KinderCovi e oggi vi accompagnerò nel mondo dellʼacqua
 L acqua è la sostanza che rende possibile la vita degli uomini, degli animali e delle piante sulla terra. Non a caso le prime forme di vita si sono sviluppate nell acqua. Anche se la terra è ricoperta
L acqua è la sostanza che rende possibile la vita degli uomini, degli animali e delle piante sulla terra. Non a caso le prime forme di vita si sono sviluppate nell acqua. Anche se la terra è ricoperta
Conclusione e domande Informazioni per il PD
 Informazioni per il PD 1/6 Compito Gli alunni concludono le lezioni sul tema del sale vicino all esposizione e rispondono a una serie di domande. Obiettivi Gli alunni sono in grado di rispondere alle domande
Informazioni per il PD 1/6 Compito Gli alunni concludono le lezioni sul tema del sale vicino all esposizione e rispondono a una serie di domande. Obiettivi Gli alunni sono in grado di rispondere alle domande
10) Se ad una soluzione aumentiamo la temperatura cosa succede? Dire quale delle seguenti affermazioni è corretta.
 Associazione di Promozione Sociale Lesina (FG) Cognome e Nome Sede: Via Principe di Piemonte, 93-71010 - Lesina (FG) - C.F. 93034730718 Tel. 0882.992808 E-mail: mail@antoniotucci.net - www.agora.lesina.org
Associazione di Promozione Sociale Lesina (FG) Cognome e Nome Sede: Via Principe di Piemonte, 93-71010 - Lesina (FG) - C.F. 93034730718 Tel. 0882.992808 E-mail: mail@antoniotucci.net - www.agora.lesina.org
CHIMICA ORGANICA. Gli alcoli
 1 E1-ALCOLI CIMICA OGANICA ALCOLI Formula generale Desinenza -olo Gli alcoli Gli alcoli sono, dopo gli idrocarburi, i composti organici più comuni, che è possibile considerare come derivati dagli alcani
1 E1-ALCOLI CIMICA OGANICA ALCOLI Formula generale Desinenza -olo Gli alcoli Gli alcoli sono, dopo gli idrocarburi, i composti organici più comuni, che è possibile considerare come derivati dagli alcani
I minerali. Alunno: Astarita Vittorio - Classe: 1 a E. Durezza (scala di Mohs) 7,5-8 Verde, azzurro, giallo, rosa, rosso, arancio, incolore, blu
 I minerali Alunno: Astarita Vittorio - Classe: 1 a E N. Nome minerale 1 Classe mineralogica Quarzo Silicati SiO 2 Composizione chimica Abito cristallino Prismatico esagonale Durezza (scala di Mohs) Colore
I minerali Alunno: Astarita Vittorio - Classe: 1 a E N. Nome minerale 1 Classe mineralogica Quarzo Silicati SiO 2 Composizione chimica Abito cristallino Prismatico esagonale Durezza (scala di Mohs) Colore
Gli elementi di transizione
 Gli elementi di transizione A partire dal quarto periodo del Sistema Periodico, nella costruzione della configurazione elettronica degli elementi, dopo il riempimento degli orbitali s del guscio di valenza
Gli elementi di transizione A partire dal quarto periodo del Sistema Periodico, nella costruzione della configurazione elettronica degli elementi, dopo il riempimento degli orbitali s del guscio di valenza
Ke = ] = Kw = 10 = 10-7 moli/litro, ed in base a quanto avevamo affermato in precedenza: [H + ] = [OH - ] = 10-7 moli/litro.
![Ke = ] = Kw = 10 = 10-7 moli/litro, ed in base a quanto avevamo affermato in precedenza: [H + ] = [OH - ] = 10-7 moli/litro. Ke = ] = Kw = 10 = 10-7 moli/litro, ed in base a quanto avevamo affermato in precedenza: [H + ] = [OH - ] = 10-7 moli/litro.](/thumbs/27/12374782.jpg) Prodotto ionico dell acqua e ph Prodotto ionico dell acqua L acqua è un elettrolita debolissimo e si dissocia secondo la reazione: H 2 O H + + OH - La costante di equilibrio dell acqua è molto piccola
Prodotto ionico dell acqua e ph Prodotto ionico dell acqua L acqua è un elettrolita debolissimo e si dissocia secondo la reazione: H 2 O H + + OH - La costante di equilibrio dell acqua è molto piccola
Materiali per alte temperature
 Materiali per alte temperature Prof. Barbara Rivolta Dipartimento di Meccanica Politecnico di Milano 14 Novembre 2013, Lecco Fenomeni metallurgici ad alta temperatura 2 Fenomeni meccanici: sovrasollecitazioni
Materiali per alte temperature Prof. Barbara Rivolta Dipartimento di Meccanica Politecnico di Milano 14 Novembre 2013, Lecco Fenomeni metallurgici ad alta temperatura 2 Fenomeni meccanici: sovrasollecitazioni
I METALLI NOBILI PROPRIETA
 I METALLI NOBILI Sono metalli preziosi non tanto per le loro proprietà meccaniche (cioè di resistenza alle sollecitazioni) ma per le loro proprietà tecnologiche e fisiche ed anche perché non sono abbondanti
I METALLI NOBILI Sono metalli preziosi non tanto per le loro proprietà meccaniche (cioè di resistenza alle sollecitazioni) ma per le loro proprietà tecnologiche e fisiche ed anche perché non sono abbondanti
SCALA DEI PESI ATOMICI RELATIVI E MEDI
 SCALA DEI PESI ATOMICI RELATIVI E MEDI La massa dei singoli atomi ha un ordine di grandezza compreso tra 10-22 e 10-24 g. Per evitare di utilizzare numeri così piccoli, essa è espressa relativamente a
SCALA DEI PESI ATOMICI RELATIVI E MEDI La massa dei singoli atomi ha un ordine di grandezza compreso tra 10-22 e 10-24 g. Per evitare di utilizzare numeri così piccoli, essa è espressa relativamente a
La percentuale massa/volume (%m/v) indica la quantità di soluto espressa in grammi presente in 100 ml di soluzione.
 La concentrazione delle soluzioni Le soluzioni sono costituite da quantità molto variabili dei loro componenti: se vogliamo fornire una indicazione precisa circa la loro composizione, è importante conoscere
La concentrazione delle soluzioni Le soluzioni sono costituite da quantità molto variabili dei loro componenti: se vogliamo fornire una indicazione precisa circa la loro composizione, è importante conoscere
SISTEMA BINARIO DI DUE LIQUIDI VOLATILI TOTALMENTE MISCIBILI che seguono Raoult
 SISTEM INRIO DI DUE IQUIDI OTII MENTE MISCIII che seguono Raoult Consideriamo due liquidi e totalmente miscibili di composizione χ e χ presenti in un contenitore ad una certa temperatura T=T 1. o strato
SISTEM INRIO DI DUE IQUIDI OTII MENTE MISCIII che seguono Raoult Consideriamo due liquidi e totalmente miscibili di composizione χ e χ presenti in un contenitore ad una certa temperatura T=T 1. o strato
Termologia. Introduzione Scale Termometriche Espansione termica Capacità termica e calori specifici Cambiamenti di fase e calori latenti
 Termologia Introduzione Scale Termometriche Espansione termica Capacità termica e calori specifici Cambiamenti di fase e calori latenti Trasmissione del calore Legge di Wien Legge di Stefan-Boltzmann Gas
Termologia Introduzione Scale Termometriche Espansione termica Capacità termica e calori specifici Cambiamenti di fase e calori latenti Trasmissione del calore Legge di Wien Legge di Stefan-Boltzmann Gas
LABORATORIO DI CHIMICA GENERALE E INORGANICA
 UNIVERSITA DEGLI STUDI DI MILANO Facoltà di Scienze Matematiche, Fisiche e Naturali Corso di Laurea Triennale in Chimica CORSO DI: LABORATORIO DI CHIMICA GENERALE E INORGANICA Docente: Dr. Alessandro Caselli
UNIVERSITA DEGLI STUDI DI MILANO Facoltà di Scienze Matematiche, Fisiche e Naturali Corso di Laurea Triennale in Chimica CORSO DI: LABORATORIO DI CHIMICA GENERALE E INORGANICA Docente: Dr. Alessandro Caselli
Antincendio. Corso per Volontari Operativi Generici di Protezione Civile
 Antincendio Corso per Volontari Operativi Generici di Protezione Civile realizzato secondo gli Standard Regionali in materia di Formazione per la Protezione Civile D.G.R. 4036/2007 - Scuola Superiore di
Antincendio Corso per Volontari Operativi Generici di Protezione Civile realizzato secondo gli Standard Regionali in materia di Formazione per la Protezione Civile D.G.R. 4036/2007 - Scuola Superiore di
Com è fatto l atomo ATOMO. UNA VOLTA si pensava che l atomo fosse indivisibile. OGGI si pensa che l atomo è costituito da tre particelle
 STRUTTURA ATOMO Com è fatto l atomo ATOMO UNA VOLTA si pensava che l atomo fosse indivisibile OGGI si pensa che l atomo è costituito da tre particelle PROTONI particelle con carica elettrica positiva e
STRUTTURA ATOMO Com è fatto l atomo ATOMO UNA VOLTA si pensava che l atomo fosse indivisibile OGGI si pensa che l atomo è costituito da tre particelle PROTONI particelle con carica elettrica positiva e
LA MATERIA MATERIA. COMPOSIZIONE (struttura) Atomi che la compongono
 LA MATERIA 1 MATERIA PROPRIETÀ (caratteristiche) COMPOSIZIONE (struttura) FENOMENI (trasformazioni) Stati di aggregazione Solido Liquido Aeriforme Atomi che la compongono CHIMICI Dopo la trasformazione
LA MATERIA 1 MATERIA PROPRIETÀ (caratteristiche) COMPOSIZIONE (struttura) FENOMENI (trasformazioni) Stati di aggregazione Solido Liquido Aeriforme Atomi che la compongono CHIMICI Dopo la trasformazione
IDROGENO IN PRATICA. del gruppo degli allievi del Volta. Laboratorio di chimica I.T. I. Volta
 IDROGENO IN PRATICA Pratiche di laboratorio su iniziative del gruppo degli allievi del Volta Laboratorio di chimica I.T. I. Volta da: L Isola Misteriosa Giulio Verne 1874 Senza il carbone non ci sarebbero
IDROGENO IN PRATICA Pratiche di laboratorio su iniziative del gruppo degli allievi del Volta Laboratorio di chimica I.T. I. Volta da: L Isola Misteriosa Giulio Verne 1874 Senza il carbone non ci sarebbero
Analisi di Controllo di un Acqua Minerale Naturale
 Analisi di Controllo di un Acqua Minerale aturale ITODUZIOE Le acque potabili possono essere in diverse tipologie: si definiscono acque destinate al consumo umano, quelle acque rese potabili dopo aver
Analisi di Controllo di un Acqua Minerale aturale ITODUZIOE Le acque potabili possono essere in diverse tipologie: si definiscono acque destinate al consumo umano, quelle acque rese potabili dopo aver
Affinché un incendio si sviluppi, è necessario che si verifichino tre condizioni indicate nel "cerchio del fuoco".
 Via Tatti, 5 20029 Turbigo (MI) Ing. Marco Cagelli Teoria della combustione Nozioni base Il cerchio del fuoco Affinché un incendio si sviluppi, è necessario che si verifichino tre condizioni indicate nel
Via Tatti, 5 20029 Turbigo (MI) Ing. Marco Cagelli Teoria della combustione Nozioni base Il cerchio del fuoco Affinché un incendio si sviluppi, è necessario che si verifichino tre condizioni indicate nel
LEGHE FERRO - CARBONIO
 LEGHE FERRO - CARBONIO Le leghe binarie ferro-carbonio comprendono gli acciai ordinari e le ghise. Come già studiato gli acciai hanno percentuale di carbonio tra 0,008 e 2,06, le ghise tra 2,06 e 6,67.
LEGHE FERRO - CARBONIO Le leghe binarie ferro-carbonio comprendono gli acciai ordinari e le ghise. Come già studiato gli acciai hanno percentuale di carbonio tra 0,008 e 2,06, le ghise tra 2,06 e 6,67.
La Vita è una Reazione Chimica
 La Vita è una Reazione Chimica Acqua Oro Zucchero Il numero atomico, il numero di massa e gli isotopi numero atomico (Z) = numero di protoni nel nucleo numero di massa (A) = numero di protoni + numero
La Vita è una Reazione Chimica Acqua Oro Zucchero Il numero atomico, il numero di massa e gli isotopi numero atomico (Z) = numero di protoni nel nucleo numero di massa (A) = numero di protoni + numero
ATTREZZATURA DI LABORATORIO
 ATTREZZATURA DI LABORATORIO IN GENERALE RICORDIAMO CHE 1) il vetro pyrex non reagisce chimicamente con altre sostanze tranne che con l acido fluoridrico se riscaldato non si spacca 2) gli strumenti in
ATTREZZATURA DI LABORATORIO IN GENERALE RICORDIAMO CHE 1) il vetro pyrex non reagisce chimicamente con altre sostanze tranne che con l acido fluoridrico se riscaldato non si spacca 2) gli strumenti in
Quando un composto ionico viene immesso in acqua si dissocia formando uno ione negativo ed uno positivo.
 I composti chimici Il legame chimico Un atomo raggiunge la stabilità quando i suoi livelli energetici sono completi. Solamente i gas nobili hanno questa caratteristica mentre gli altri atomi no, per cui
I composti chimici Il legame chimico Un atomo raggiunge la stabilità quando i suoi livelli energetici sono completi. Solamente i gas nobili hanno questa caratteristica mentre gli altri atomi no, per cui
Progetto L età di Leonardo per i curricoli del biennio unitari finalizzati all innalzamento dell istruzione a 16 anni dall a.s.
 Progetto L età di Leonardo per i curricoli del biennio unitari finalizzati all innalzamento dell istruzione a 16 anni dall a.s. 2007/08 [Eleonora Aquilini] Le sostanze basiche Preparate una soluzione di
Progetto L età di Leonardo per i curricoli del biennio unitari finalizzati all innalzamento dell istruzione a 16 anni dall a.s. 2007/08 [Eleonora Aquilini] Le sostanze basiche Preparate una soluzione di
CAPITOLO 11 Materiali ceramici ESERCIZI CON SOLUZIONE SVOLTA. Problemi di conoscenza e comprensione
 CAPITOLO 11 Materiali ceramici ESERCIZI CON SOLUZIONE SVOLTA Problemi di conoscenza e comprensione 11.10 (a) Le strutture a isola dei silicati si formano quando ioni positivi, come Mg 2+ e Fe 2+, si legano
CAPITOLO 11 Materiali ceramici ESERCIZI CON SOLUZIONE SVOLTA Problemi di conoscenza e comprensione 11.10 (a) Le strutture a isola dei silicati si formano quando ioni positivi, come Mg 2+ e Fe 2+, si legano
Quando si parla di inquinamento dell'acqua, si intende sia l'inquinamento dell'acqua superficiale (fiumi, laghi, mare) sia dell'acqua presente sotto
 L'acqua inquinata Quando si parla di inquinamento dell'acqua, si intende sia l'inquinamento dell'acqua superficiale (fiumi, laghi, mare) sia dell'acqua presente sotto il suolo (falde acquifere). Va tenuto
L'acqua inquinata Quando si parla di inquinamento dell'acqua, si intende sia l'inquinamento dell'acqua superficiale (fiumi, laghi, mare) sia dell'acqua presente sotto il suolo (falde acquifere). Va tenuto
EMISSIONE E ASSORBIMENTO DI LUCE DA PARTE DELLA MATERIA
 EMISSIONE E ASSORBIMENTO DI LUCE DA PARTE DELLA MATERIA Poiché la luce è energia trasportata da oscillazioni del campo elettrico (fotoni) e la materia è fatta di particelle elettricamente cariche (atomi
EMISSIONE E ASSORBIMENTO DI LUCE DA PARTE DELLA MATERIA Poiché la luce è energia trasportata da oscillazioni del campo elettrico (fotoni) e la materia è fatta di particelle elettricamente cariche (atomi
Lezione IX - 19/03/2003 ora 8:30-10:30 - Ciclo di Carnot, Otto, Diesel - Originale di Spinosa Alessandro.
 Lezione IX - 9/03/003 ora 8:30-0:30 - Ciclo di Carnot, Otto, Diesel - Originale di Spinosa Alessandro. Ciclo di Carnot Si consideri una macchina termica semplice che compie trasformazioni reversibili,
Lezione IX - 9/03/003 ora 8:30-0:30 - Ciclo di Carnot, Otto, Diesel - Originale di Spinosa Alessandro. Ciclo di Carnot Si consideri una macchina termica semplice che compie trasformazioni reversibili,
