Le terapie ad oggi disponibili per il trattamento dei tumori del polmone, soprattutto in fase avanzata di malattia, offrono scarso beneficio eccetto
|
|
|
- Lucia Verde
- 8 anni fa
- Visualizzazioni
Transcript
1 indice generale introduzione 524 immunoterapia NSCLC - prima linea 528 l immunoterapia ha un ruolo nel trattamento di prima linea dei pazienti con nsclc avanzato? NSCLC - seconda linea 534 l immunoterapia ha un ruolo nel trattamento di seconda linea dei pazienti con nsclc avanzato? SCLC 543 l immunoterapia ha un ruolo nel trattamento dei pazienti affetti da sclc?
2 immunoterapia Le terapie ad oggi disponibili per il trattamento dei tumori del polmone, soprattutto in fase avanzata di malattia, offrono scarso beneficio eccetto nel sottogruppo di pazienti con neoplasia oncogene-driven, che rappresenta il 15-20% dell intera popolazione, per cui sono già disponibili nella pratica clinica agenti a bersaglio molecolare [1]. La nuova frontiera nel trattamento dei tumori del polmone è rappresentata dall immunoterapia. Questo è accaduto grazie ai significativi progressi ottenuti nella comprensione del sistema immunitario che hanno portato allo sviluppo di nuove molecole in grado di potenziare la risposta immunitaria dei pazienti. Pertanto, tutti i malati oncologici, indipendentemente dalle anormalità genetiche o metaboliche, possono trarre potenziale beneficio dal trattamento perché il target è proprio la risposta immunitaria del paziente e non la cellula tumorale. Gli immuno-checkpoints si riferiscono ad una serie di vie inibitorie nel sistema immunitario che sono cruciali per il mantenimento dell auto-tolleranza e la prevenzione dell eccessiva, prolungata, e potenziale attività deleteria delle cellule T nei tessuti periferici [2]. È sempre più evidente che il cancro del polmone può utilizzare questi immuno-checkpoints per eludere la risposta immunitaria anti-tumorale, ad esempio attraverso la perdita di espressione di antigeni associati al tumore (tumor-associated antigens, TAA) e/o antigeni del sistema maggiore di istocompatibilità (major histocompatibility complex, MHC), o attraverso la produzione di citochine e l espressione di nuove molecole di membrana ad attività inibitoria. Questo fenomeno di continuo rimodellamento molecolare è definito come cancer immunoediting che consta di tre fasi principali e sequenziali tra loro: eliminazione (completa distruzione delle cellule tumorali da parte del sistema immunitario dell ospite), equilibrio (le cellule tumorali, attraverso una selezione operata dalle cellule T, diventano resistenti al sistema immunitario), ed evasione (le cellule tumorali originano lesioni clinicamente rilevabili) [3]. Al momento gli immuno-checkpoints noti per essere coinvolti nell evoluzione del cancro del polmone sono il recettore del cytotoxic T-lymphocyte antigen-4 (CTLA-4) e l asse programmed cell death-1 (PD- 1)/programmed cell death-ligand 1 (PD-L1). Il CTLA-4, noto anche come CD152, è un recettore appartenente alla superfamiglia delle immunoglobuline (Ig) espresso sui linfociti T citotossici. A seguito del 524
3 introduzione legame con uno dei suoi ligandi, B7-1 oppure B7-2 espressi sull antigen-presenting cell (APC), trasmette all'interno del linfocita un segnale di tipo inibitorio, contribuendo così alla regolazione omeostatica della risposta immunitaria [4]. L ipilimumab ed il tremelimumab, anticorpi monoclonali anti-ctla-4, sono attualmente in sviluppo clinico nel carcinoma del polmone. Anche il PD-1 è un recettore di superficie appartenente alla superfamiglia delle Ig ed è espresso sulle cellule T e pro-b e riconosce come ligandi il PD-L1 e il PD-L2. Il PD-L1 è una proteina transmembrana il cui legame ai suoi recettori, PD-1 e B7.1, sulla superficie delle cellule T ne determina la loro disattivazione [4]. Il nivolumab e il pembrolizumab, sono anticorpi monoclonali anti-pd-1, mentre l atezolizumab e il durvalumab, sono anticorpi monoclonali anti-pd- L1. Questi farmaci sono in fase avanzata di sviluppo clinico nelle neoplasie polmonari. L immunoterapia ha determinato un cambiamento delle modalità con cui dovrebbero essere misurate le risposte obiettive, sia negli studi clinici che nella pratica clinica. Dagli studi condotti nel trattamento immunoterapico del melanoma, si è visto che la risposta antitumorale si rende evidente non prima di settimane o mesi rispetto all inizio del trattamento, con un guadagno in sopravvivenza che si manifesta dopo diversi mesi. Questo perché i farmaci immunoterapici attivano il sistema immunitario che a sua volta determina una risposta cellulo-mediata. La valutazione della risposta al trattamento è basata sull impiego dei criteri RECIST o WHO. In corso di immunoterapia questi criteri convenzionali non sono adeguati per la presenza di infiltrato infiammatorio peritumorale che può mimare una pseudo-progressione e che è fenomeno tipico durante questo tipo di trattamento. Per ovviare a questa problematica sono stati creati i criteri per la valutazione della risposta immunocorrelata (ircr), secondo cui una iniziale progressione radiologica, intesa come comparsa di nuove lesioni e/o incremento delle dimensioni di lesioni pre-esistenti, in assenza di progressione clinica, deve essere confermata ad una valutazione successiva [5]. L impiego corretto della ircr può permettere l identificazione di un gruppo di pazienti lungo-sopravviventi tra quelli che potrebbero essere considerati in progressione con i criteri convenzionali e che quindi non potrebbero continuare a beneficiare del trattamento specifico. Altro aspetto che l immunoterapia ha evidenziato è la necessità di capire se questo trattamento è per tutti o è importante selezionare i pazienti che maggiormente possano beneficiare della terapia immunologica 525
4 ottimizzando i risultati ed i costi per la sostenibilità da parte del sistema nazionale. Purtroppo, ad oggi abbiamo pochi dati disponibili, il target individuato è l espressione di PD-L1 ma non è chiaro quale cutoff e metodologia impiegare per definire il gruppo di pazienti da trattare. Altra considerazione che complica ulteriormente questo aspetto è che l assetto immunitario tende a cambiare nel tempo pertanto anche l espressione di PD-L1 può essere diversa a seconda di quando il prelievo di tessuto tumorale sia stato fatto, alla diagnosi, o alla progressione. Questo va considerato nella lettura dei risultati degli studi ad oggi disponibili. Studi clinici con ampia casistica attualmente in corso nel trattamento delle neoplasie polmonari stanno ulteriormente valutando questo aspetto. La presente linea guida vuole rivedere i dati clinici al momento disponibili (Ottobre 2015) nel trattamento delle neoplasie polmonari per definire l attuale ruolo dell immunoterapia nella gestione della patologia polmonare (Appendice 1) [6]. APPENDICE 1. Metodo di classificazione delle evidenze e delle raccomandazioni Livello di Le informazioni sono Grado di Evidenza Raccomandazione Ia Ib derivate da revisioni sistematiche o meta-analisi di TCR derivate da almeno un TCR ben condotto A IIa derivate da almeno uno studio clinico prospettico di buona qualità IIb derivate da altri tipi di studi prospettici di minor qualità B III derivate da studi retrospettivi di buona qualità IV basate unicamente su opinione di esperti C TCR: trial clinico randomizzato 526
5 introduzione bibliografia 1. Associazione Italiana Oncologia Toracica. Linee guida per la gestione del paziente con tumore polmonare. ht tp:// (accesso il 15 Ottobre 2015). 2. Pardoll DM. The blockade of immune checkpoints in cancer immunotherapy. Nat Rev Cancer 2012; 12: Dun GP, Old LJ, Schreiber RD. The three Es of cancer immunoediting. Annu Rev Immunol 2004; 22: Reck M, Paz-Ares L. Immunologic checkpoint blockade in lung cancer. Semin Oncol 2015; 42: Wolchok JD, Hoos A, O Day S et al. Guidelines for the evaluation of immune therapy activity in solid tumors: immune-related response criteria. Clin Cancer Res 2009; 15: McCormick KA, Fleming B. Clinical practice guidelines. The Agency for Health Care Policy and Research fosters the development of evidence-based guidelines. Health Progress 1992; 73:
6 NSCLC - prima linea l immunoterapia ha un ruolo nel trattamento di prima linea dei pazienti con nsclc avanzato? Alla classe degli anti-ctla-4 (cytotoxic T-lymphocyte antigen-4) appartiene l ipilimumab, anticorpo monoclonale IgG1 interamente umano, già registrato in Italia per il trattamento del melanoma avanzato (non resecabile o metastatico) alla dose di 3 mg/kg somministrati ogni 3 settimane, per un totale di 4 dosi. L ipilimumab è stato testato nel trattamento di prima linea del carcinoma del polmone non a piccole cellule (NSCLC) avanzato nell ambito di uno studio di fase II randomizzato a tre bracci. Nei due bracci sperimentali, l ipilimumab è stato somministrato alla dose di 10 mg/kg, in combinazione con carboplatino (area sotto la curva [AUC] 6), e paclitaxel (175 mg/m 2 ), secondo la schedula phased (2 cicli di chemioterapia in associazione a placebo seguiti da altri 4 cicli di chemioterapia con ipilimumab) o concomitante (4 cicli di chemioterapia in associazione con ipilimumab seguiti da altri 2 cicli di chemioterapia con placebo). Il braccio di controllo consisteva nella sola chemioterapia in associazione a placebo. Erano previsti un massimo 6 cicli somministrati ogni 3 settimane. Dopo i 6 cicli di chemioterapia, l ipilimumab, o il placebo nel braccio di controllo, è stato somministrato ogni 12 settimane fino a progressione. Lo studio ha randomizzato 204 pazienti con obiettivo primario la sopravvivenza libera da progressione immuno-relata (irpfs); gli obiettivi secondari comprendevano la PFS, la risposta obiettiva (ORR), la ORR immuno-relata, la sopravvivenza (OS) e la tossicità. La irpfs è risultata migliore nel braccio con ipilimumab somministrato secondo la schedula phased rispetto alla sola chemioterapia (5.7 versus 4.6 mesi: hazard ratio [HR] 0.72; p = 0.05). Anche la OS è stata migliore con 12.2 versus 8.3 mesi (HR 0.87; p = 0.23) e una ORR del 32% versus 14%, rispettivamente. La schedula di ipilimumab concomitante ha riportato risultati simili al braccio di controllo. La tossicità immuno-relata di grado 3-4, in particolare rash cutaneo, diarrea, colite, ipertransaminasemia, ipofisite e ipopituitarismo, è stata del 6% per il braccio di controllo, il 20% per il braccio concomitante, e il 15% per il braccio phased [4]. Possibili spiegazioni relative al vantaggio riportato solo con la schedula phased potrebbero essere sia l effetto sinergico tra la chemioterapia e gli 528
7 NSCLC - prima linea immunoterapici, ma anche l attività immunosoppressiva della chemioterapia con l associazione ottimale di questi farmaci ancora da definire. Interessante è l analisi di sottogruppo per istologia, i pazienti affetti da NSCLC squamoso ed arruolati nella schedula phased hanno riportato una migliore irpfs nei confronti del braccio di controllo (HR 0.55) e rispetto al vantaggio riportato dai pazienti con istologia nonsquamosa (HR 0.82). In questo braccio di trattamento anche la OS è risultata essere migliore per i pazienti con istologia squamosa (HR 0.48) rispetto a quella riportata per i pazienti con istologia non-squamosa (HR 1.17). Non ci sono state differenze tra le due istologie nel braccio di terapia concomitante [1]. Il nivolumab, anticorpo monoclonale IgG4 anti-pd-1 (programmed cell death-1), completamente umano, è stato somministrato come agente singolo alla dose di 3 mg/kg ogni 2 settimane fino a progressione o tossicità inaccettabile a 52 pazienti con NSCLC avanzato. La ORR era l obiettivo primario ed è stata del 21% con una OS di 98.3 settimane. La ORR nei 39 pazienti con istologia non-squamosa è stata del 23% e nei 13 pazienti con istologia squamosa del 15%. Nei 26 pazienti con PD-L1 (programmed cell death-ligand 1) 5% la ORR è stata del 31% nei 21 pazienti con PD-L1 negativo del 10%. La tossicità di grado 3-4 è stata riportata nel 15% dei pazienti ed è stata prevalentemente rash cutaneo, ipertransaminasemia, polmoniti [2]. Nel trattamento di prima linea, è in valutazione anche la combinazione di ipilimumab alla dose di 1 o 3 mg/kg con nivolumab alla dose di 1 o 3 mg/kg. I dati preliminari relativi a 148 pazienti hanno riportato una ORR del 13-39% e una stabilità di malattia del 21-42%, nei 4 bracci di associazione alle diverse dosi, indipendentemente dall istologia e dall espressione di PD-L1. La PFS è stata tra 4.9 e 10.6 mesi. La tossicità di grado 3-4 è stata riportata nel 28-35% dei pazienti e costituita prevalentemente da polmoniti, endocrinopatie, rash cutaneo, e disturbi gastrointestinali [3]. Il pembrolizumab è un anticorpo monoclonale IgG4 anti-pd-1 completamente umano già registrato in Italia per il trattamento del melanoma avanzato. Lo studio KEYNOTE-001 ha arruolato 495 pazienti affetti da NSCLC avanzato, sia in prima che in linee successive di trattamento, a ricevere il pembrolizumab alla dose di 2 mg/kg ogni 3 settimane oppure 10 mg/kg ogni 2 o 3 settimane. In totale sono stati arruolati 101 pazienti con NSCLC non pretrattato in cui è stata riportata una ORR del 24.8% della durata mediana di 23.3 mesi. La PFS mediana è stata di 6 529
8 530 mesi e la OS di 16.2 mesi. La tossicità di grado 3-4 è stata riportata nel 9.5% dei casi e rappresentata prevalentemente da prurito e polmoniti. Una stretta correlazione è stata individuata fra i risultati della terapia con pembrolizumab e l espressione di PD-L1 50%. Infatti, in questo sottogruppo di pazienti la ORR è stata del 50%, la PFS mediana di 12.5 mesi e la OS mediana non è stata raggiunta [4]. Sono stati recentemente presentati i dati preliminari della coorte A e C dello studio KEYNO- TE-021, ancora in corso, in cui il pembrolizumab alla dose di 2 o 10 mg/kg e stato associato alla combinazione di carboplatino + paclitaxel, per tutte le istologie, o carboplatino + pemetrexed, per il NSCLC nonsquamoso. Nei 20 e 24 pazienti arruolati nella coorte A e C la ORR è stata del 30% e del 58%, rispettivamente. La tossicità di grado 3-4 è stata complessivamente del 27% [5]. L atezolizumab, è un anticorpo monoclonale IgG1 anti-pd-l1 completamente umano, somministrato alla dose di 1200 mg, endovena ogni 3 settimane, nell ambito di uno studio di fase II, a 3 coorti di pazienti con obiettivo primario la ORR. Nella coorte 1 sono stati arruolati 31 pazienti non pretrattati e la ORR è stata del 29%. L espressione immunoistochimica di PD-L1 è stata valutata sia sulle cellule immunitarie infiltranti il tumore (IC) che sulle cellule tumorali (TC) ed in presenza di TC3 o IC3 si sono riportate ORR migliori [6]. In base a questo dato, lo studio di fase II BIRCH ha arruolato pazienti affetti da NSCLC avanzato PD-L1 positivi (solo TC/IC 2-3) a ricevere atezolizumab 1200 mg endovena ogni 3 settimane. Nella coorte 1 sono stati arruolati 139 pazienti non pretrattati. L obiettivo primario era la ORR che è stata del 19% ed in particolare nel sottogruppo di pazienti TC3 o IC3 la ORR è stata del 26%. La PFS mediana è stata di 5.5 mesi. La OS mediana è stata di 14 mesi e non ancora raggiunta nel gruppo di pazienti TC3 o IC3. La tossicità di grado 3-4 è stata del 9%, maggiormente astenia, nausea e polmoniti [7]. Nell ambito di uno studio di fase Ib, l atezolizumab, alla dose di 15 mg/kg, è stato somministrato in combinazione con carboplatino (AUC 6) e paclitaxel (200 mg/m 2 ) oppure nab-paclitaxel (100 mg/m 2, settimanale) oppure pemetrexed (500 mg/m 2, solo istologia non squamosa). Sono stati trattati 41 pazienti (8 con il paclitaxel, 16 con il nabpaclitaxel e 17 con il pemetrexed) riportando una ORR del 63.4% (50% con il paclitaxel, 56.3% con il nab-paclitaxel e 76,5% con il pemetrexed). Questi dati ipotizzano un potenziale effetto sinergico tra atezolizumab e chemioterapia senza un peggioramento del profilo di
9 NSCLC - prima linea tossicità dei farmaci [8]. La Tabella 1 riassume i risultati dei principali studi di prima linea condotti con gli immunoterapici nel NSCLC. Questi risultati derivano da piccoli studi o sono dati retrospettivi da sottogruppi di pazienti e pertanto devono essere valutati con cautela. Nel complesso, i dati sono stati sufficientemente interessanti per iniziare studi di fase III in pazienti affetti da NSCLC avanzato nelle diverse istologie in cui gli immunoterapici sono somministrati sia come agente singolo che in combinazione con altri immunoterapici o chemioterapia. Negli studi in corso ci si propone anche di definire in maniera più adeguata il ruolo predittivo e/o prognostico di PD-L1, il cutoff più opportuno da considerare oltre che la metodologia da impiegare per la sua determinazione. Infatti, sono in corso studi di prima linea in cui i pazienti sono selezionati in base all espressione di PD-L1 [9]. TAbELLA 1. Risultati dei principali studi clinici di prima linea con anti-ctla-4, anti-pd-1 e anti-pd-l1 nel NSCLC avanzato Autore Tipo Trattamento N.pz ORR irorr PFS irpfs OS Tossicità di (%) (%) (mesi) (mesi) (mesi) Grado 3 studio (%) Lynch [1] IIR CBDCA + PAC + Placebo vs CBDCA + PAC + IPI phased vs CBDCA + PAC + IPI concomitante Gettinger [2] I Nivolumab NR NR NR 98.3* 15 Rizvi [3] I Nivolumab + IPI NR NR NR NR 48 KEYNOTE-001 I Pembrolizumab NR 6 NR [4] BIRCH [7] II Atezolizumab NR 5.5 NR *Settimane; NSCLC: carcinoma del polmone non a piccole cellule; CTLA-4: cytotoxic T-lymphocyte antigen-4; PD1: programmed cell death 1; PD-L1: programmed cell death-ligand 1; N.pz: numero di pazienti; irorr: risposta obiettiva immuno-relata; irpfs: sopravvivenza libera da progressione immunorelata; OS: sopravvivenza mediana; IIR: studio di fase II randomizzato; CBDCA: carboplatino; PAC: paclitaxel; IPI: ipilimumab; NR: non riportato 531
10 raccomandazioni Per i pazienti affetti da NSCLC avanzato, il trattamento di prima linea con farmaco immunoterapico, sia come agente singolo che in combinazione con altri immunoterapici o con la chemioterapia, non è raccomandato in quanto ancora in fase di sperimentazione livello di evidenza iib grado di raccomandazione B 532
11 NSCLC - prima linea bibliografia 1. Lynch TJ, Bondarenko I, Luft A et al. Ipilimumab in combination with paclitaxel and carboplatin as first-line treatment in stage IIIB/IV non-small-cell lung cancer: Results from a randomized, doubleblind, multicenter phase II study. J Clin Oncol 2012; 30: Gettinger SN, Hellmann MD, Shepherd Fa et al. First-line monotherapy with nivolumab (NIVO; anti-programmed death-1 [PD-1]) in advanced non-small cell lung cancer (NSCLC): Safety, efficacy and correlation of outcomes with PD-1 ligand (PD-L1) expression. J Clin Oncol 2015; 33(S5):8025 (abstract). 3. Rizvi N, Gettinger SN, Goldman J et al. Safety and efficacy of first-line nivolumab (anti-programmed death-1 [PD-1]) and ipilimumab in non-small cell lung cancer (NSCLC). J Thorac Oncol 2015; 10 (Supplement 2):S176 (abstract O02.05). 4. Garon EB, Rizvi NA, Hui R et al. Pembrolizumab for the treatment of non-small-cell lung cancer. N Engl J Med 2015; 372: Papadimitrakopoulou V, Patnaik A, Borghaei H et al. Pembrolizumab (pembro; MK-3475) plus platinum doublet chemotherapy (PDC) as front-line therapy for advanced non-small cell lung cancer (NSCLC): KEYNOTE-021 Cohorts A and C. J Clin Oncol 2015; 33(S5):8031 (abstract). 6. Spigel DR, Chaft JE, Gettinger SN et al. Clinical activity and safety from a phase II study (FIR) of MPDL3280A (anti-pdl1) in PD-L1 selected patients with non-small cell lung cancer (NSCLC). J Clin Oncol 2015; 33(S5):8028 (abstract). 7. Besse B, Johnson M, Janne PA et al. Phase II, single-arm trial (BIRCH) of atezolizumab as firstline or subsequent therapy for locally advanced or metastatic PD-L1-selected non-small cell lung cancer (NSCLC). European Cancer Congress Vienna Settembbre 2015, 16LBA (abstract). 8. Camidge R, Liu SV, Powderly J et al. Atezolizumab (MPDL3280A) combined with platinum-based chemotherapy in non-small cell lung cancer (NSCLC): a phase Ib safety and efficacy update. J Thorac Oncol 2015; 10 (Supplement 2):S176-S177 (abstract O02.07). 9. National Cancer Institute Clinical Trials Database. (accesso il 15 Ottobre 2015). 533
12 NSCLC - seconda linea l immunoterapia ha un ruolo nel trattamento di seconda linea dei pazienti con nsclc avanzato? Alla classe degli anti-ctla-4 (cytotoxic T-lymphocyte antigen-4) appartiene l ipilimumab, anticorpo monoclonale IgG1 interamente umano, già registrato in Italia per il trattamento del melanoma avanzato (non resecabile o metastatico) alla dose di 3 mg/kg somministrati ogni 3 settimane, per un totale di 4 dosi. La coorte D dello studio di fase I KEYNOTE-021 sta valutando in pazienti affetti da carcinoma del polmone non a piccole cellule (NSCLC) già pretrattati con 2 linee di terapia l associazione di ipilimumab e pembrolizumab, altro anticorpo monoclonale IgG4 anti-pd-1 (programmed cell death-1) completamente umano già registrato in Italia per il trattamento del melanoma avanzato. Sono stati arruolati 17 pazienti a ricevere ipilimumab alla dose di 1 o 3 mg/kg in associazione a pembrolizumab alla dose di 2 o 10 mg/kg. L obiettivo primario comprende la tollerabilità e la tossicità dose limitante (DLT) nelle prime 3 settimane di trattamento. Non è stata registrata alcuna DLT con rash e diarrea di grado 2 le tossicità più frequenti. Negli 11 pazienti valutabili per la risposta si è registrata una ORR del 55% [1]. Il nivolumab, anticorpo monoclonale IgG4 anti-pd-1 completamente umano, è stato somministrato alla dose di 1, 3 o 10 mg/kg endovena ogni 2 settimane per un massimo di 96 settimane, in 129 pazienti affetti da NSCLC avanzato di cui il 54% trattati con 3 linee di terapia. La OS mediana è stata di 9.9 mesi, la ORR del 17% con la durata della risposta di 17 mesi e con risultato analogo in tutte le istologie. Tossicità di grado 3-4 è stata riportata nel 14% dei pazienti con 3 morti tossiche (2%) dovute a polmoniti. La dose di 3 mg/kg è stata selezionata per gli studi successivi [2]. Lo studio di fase II, CheckMate-063, ha arruolato 117 pazienti con NSCLC ad istologia squamosa che avessero ricevuto almeno 2 linee di terapia. L obiettivo primario era la ORR che è risultata del 14.5% con una SD del 26%. La tossicità di grado 3-4 è stata del 17% con 2 morti tossiche per polmonite ed infarto miocardico. In questo studio è stata condotta un analisi esplorativa sull espressione di PD-L1 con cutoff del 5% su 76 pazienti di cui era disponibile in archivio il tessuto neoplastico. La ORR è stata raggiunta indipendentemen- 534
13 NSCLC - seconda linea te dall espressione di PD-L1 (< 5%: ORR 14%; 5%: ORR 24%; non disponibile: ORR 30%), ma è importante sottolineare che i campioni tissutali non erano relativi al pretrattamento con nivolumab ma erano stati prelevati in momenti diversi della storia della neoplasia di ogni singolo paziente [3]. Da qui sono partiti due studi randomizzati di fase III, con obiettivo primario la OS, che hanno valutato in seconda linea il nivolumab (3 mk/kg ogni 2 settimane) versus il docetaxel (75 mg/m 2 ogni 3 settimane) in pazienti con NSCLC ad istologia squamosa (CheckMate- 017) o non-squamosa (CheckMate-057). Lo studio CheckMate-017, in cui sono stati randomizzati 272 pazienti con istologia squamosa, ha riportato una OS statisticamente e clinicamente significativa a favore di nivolumab con 9.2 versus 6 mesi (HR 0.59; p < 0.001). La sopravvivenza ad 1 anno è stata del 42% e 24% ed una ORR del 20% versus 9% (p = 0.008), rispettivamente. La PFS è stata di 3.5 e 2.8 mesi (HR 0.62; p < 0.001), rispettivamente. Gli eventi avversi di grado 3-4 sono stati riportati nel 7% e nel 54% dei pazienti trattati con nivolumab e docetaxel, rispettivamente. La valutazione dell espressione di PD-L1 (programmed cell death-ligand 1), condotta sia su tessuto archiviato oppure ottenuto al momento della randomizzazione, non è risultato né prognostico né predittivo a prescindere del cutoff considerato (1%, 5% o 10%) [4]. Nello studio CheckMate-057 sono stati randomizzati 582 pazienti con istologia non-squamosa con un vantaggio statisticamente significativo in OS a favore di nivolumab rispetto al docetaxel (12.2 versus 9.4; HR 0.73; p = 0.002). In questo studio potevano essere arruolati pazienti in seconda o in terza linea di trattamento nel caso fossero EGFR (epidermal growth factor receptor) mutati o ALK (anaplastic lymphoma kinase) traslocati e avessero ricevuto anche l inibitore specifico. Anche in questo caso la sopravvivenza ad 1 anno è stata migliore per il nivolumab con 51% versus 39%, e a 18 mesi del 39% e 23%, rispettivamente. La PFS è stata di 2.9 versus 4.2 mesi (HR 4.2: p = 0.39), con iniziale incrocio delle curve, ma la PFS ad 1 anno è stata del 19% e 8%, rispettivamente. Anche in questo studio il profilo di tossicità ha favorito il nivolumab con gli eventi avversi di grado 3-4 riportati nel 10% e nel 54% dei pazienti trattati con nivolumab e docetaxel, rispettivamente. Al contrario del precedente, in questo studio è stata riscontrata una forte correlazione tra espressione di PD-L1, a qualsiasi cutoff (1%, 5%, o 10%), con la OS ( 1%: HR 0.59; 5%: HR 0.43; 10%: HR 0.40), e la PFS ( 1%: HR 0.70; 5%: HR 0.54; 10%: HR 0.52) [5]. I risultati riportati da questi due studi con l impiego del 535
14 536 nivolumab sono considerati practice-changing portando alla rapida registrazione del farmaco, alla dose di 3 mg/kg ogni 2 settimane, per il trattamento di seconda linea nella sola istologia squamosa del NSCLC sia negli Stati Uniti che in Europa, e che FDA, l 8 Ottobre 2015, ha esteso anche all istologia non-squamosa [6]. In Italia, il nivolumab è utilizzabile nel trattamento di seconda linea del solo NSCLC squamoso, grazie alla richiesta di AIOT, con inserimento nell ambito della legge 648 con determina del 17 Settembre 2015 (GU Serie Generale n.220 del ). La Tabella 1 riassume i risultati degli studi CheckMate-017 e CheckMate-057 e la Figura 1 riporta l algoritmo di trattamento suggerito per la seconda linea di trattamento del NSCLC squamoso in pazienti con performance status 0-1. Il pembrolizumab, anticorpo monoclonale IgG4 anti-pd-1 completamente umano già registrato in Italia per il trattamento del melanoma avanzato, è stato somministrato, nell ambito dello studio di fase I, KEY- NOTE-001, alla dose di 2 mg/kg ogni 3 settimane oppure 10 mg/kg ogni 2 o 3 settimane a 495 pazienti affetti da NSCLC avanzato, sia in prima che in linee successive di trattamento. La ORR dei 394 pazienti già pretrattati è stata del 18% della durata mediana di 10.4 mesi. La PFS mediana è stata di 3 mesi e la OS di 9.3 mesi. La tossicità di grado 3-4 è stata riportata nel 9.5% dei casi e rappresentata prevalentemente da prurito e polmoniti. Una stretta correlazione è stata individuata fra i risultati della terapia con pembrolizumab e l espressione di PD-L1 50%. Infatti, in questo sottogruppo di pazienti la ORR è stata del 43.9%, la PFS mediana di 6.1 mesi e la OS mediana non è stata raggiunta [7]. In base a questi risultati, il 2 Ottobre 2015, FDA ha registrato il pembrolizumab, alla dose di 2 mg/kg ogni 3 settimane, per il trattamento di seconda linea dei pazienti affetti da NSCLC a prescindere dal tipo istologico e dal trattamento ricevuto (sia chemioterapia con regimi a base di platino, sia inibitori di EGFR o di ALK in pazienti con mutazione di EGFR o traslocazione di ALK, rispettivamente), con espressione di PD-L1 50%. FDA ha registrato anche il test per la determinazione di PD-L1 (PD-L1 IHC 22C3 pharmd) [6]. L atezolizumab, anticorpo monoclonale IgG1 completamente umano anti-pd-l1, è stato somministrato alla dose 20 mg/kg, ogni 3 settimane, a 88 pazienti affetti da NSCLC avanzato e pesantemente pretrattati. L obiettivo primario di questo studio di fase Ia era la ORR che è stata del 21% con una PFS a 24 settimane del 42% e la OS ad 1 anno
15 NSCLC - seconda linea TAbELLA 1. Risultati degli studi CheckMate-017 e CheckMate-057 CheckMate-017 [4] CheckMate-057 [5] Nivolumab Docetaxel Nivolumab Docetaxel Tipo di Studio Fase III Fase III Linea Obiettivo primario OS OS Istologia NSCLC Squamosa Non-Squamosa Performance status Metastasi cerebrali Si Si ORR (%) ORR (p-value) SD (%) Durata della risposta (mesi) NR PFS (mesi) PFS (HR; p-value) 0.62; < ; 0.39 PFS ad 1 anno (%) OS (mesi) OS (HR; p-value) 0.59; < ; OS ad 1 anno (%) PFS HR (espressione di PD-L1) 1% < 1% % < 5% % < 10% Non quantificabile OS HR (espressione di PD-L1) 1% < 1% % < 5% % < 10% Non quantificabile Tossicità (%) Qualsiasi grado Grado NSCLC: carcinoma del polmone non a piccole cellule; ORR: risposta obiettiva; PFS: sopravvivenza libera da progressione; OS: sopravvivenza mediana; HR: hazard ratio; NR: non raggiunta; PD-L1: programmed cell death-ligand 1 537
16 FIGURA 1. Algoritmo suggerito per il trattamento di seconda linea del carcinoma squamoso del polmone con farmaci rimborsabili in Italia NSCLC Squamoso Platino/Gemcitabina Platino/Vinorelbina Platino/Docetaxel Platino/Paclitaxel Prima Linea Nivolumab Seconda Linea Docetaxel Erlotinib Terza Linea dell 82%. L 11% dei pazienti ha riportato tossicità di grado 3-4 rappresentata da dispnea, astenia e iposodiemia. L espressione immunoistochimica di PD-L1 è stata valutata sia sulle cellule immunitarie infiltranti il tumore (IC) che sulle cellule tumorali (TC). Nei 20 pazienti con massima espressione di PD-L1 (TC3 o IC3) la ORR è stata del 45%, la PFS a 24 settimane del 45% e la OS ad 1 anno dell 89% [8]. Lo studio di fase II randomizzato POPLAR ha arruolato 287 pazienti con NSCLC pretrattato a ricevere atezolizumab alla dose di 1200 mg versus docetaxel a 75 mg/m 2, ogni 3 settimane. L obiettivo primario dello studio era la OS che è stata di 11.4 mesi per atezolizumab e di 9.5 mesi per il docetaxel (HR 0.77; p = 0.11). La PFS è stata di 2.8 e 3.4 mesi (HR 0.96), rispettivamente, con ORR del 15% in entrambi i bracci di tratta- 538
17 NSCLC - seconda linea mento. L incremento dell espressione di PD-L1 sia TC che IC favoriva l atezolizumab. Infatti, in presenza di TC/IC 1-3 (n = 195) la OS non è stata raggiunta con atezolizumab ed è stata di 9.1 mesi con docetaxel (HR 0.63; p = 0.024), la PFS è stata di 3.3 e 3.0 mesi (HR 0.87), rispettivamente con la ORR del 18% in entrambi i bracci. Nei 92 pazienti in cui non vi è espressione di PD-L1 (TC/IC 0) la OS è stata di 9.7 mesi in entrambi i bracci (HR 1.22) con la PFS di 1.9 e 4.1 mesi (HR 1.15) e la ORR di 8% e 10% per il braccio atezolizumab versus docetaxel. Nei 105 pazienti con elevata espressione di PD-L1 (TC/IC 3) la OS non è stata raggiunta per l atezolizumab mentre è stata di 11.1 mesi per il docetaxel (HR 0.46), la PFS è stata di 7.8 e 3.9 mesi (HR 0.56) con la ORR del 38% e 13%, rispettivamente. Tossicità di grado 3-4 sono state riportate nel 43% e 56% dei pazienti nel braccio atezolizumab versus docetaxel [9]. Lo studio di fase II BIRCH ha arruolato 659 pazienti, di cui 139 in prima linea, 267 in seconda linea e 253 trattati con tre o più linee, affetti da NSCLC avanzato PD-L1 positivi (solo TC/IC 2-3) a ricevere l atezolizumab alla dose di 1200 mg ogni 3 settimane. L obiettivo primario era la ORR che è stata del 17% in entrambe le coorti di pazienti pretrattati. Nei sottogruppi di pazienti TC3 o IC3 la ORR è stata, considerando solo le 2 coorti che hanno arruolato pazienti pretrattati, del 24% e 27%, rispettivamente. La PFS mediana è stata di 2.8 mesi in entrambe le coorti. La OS ad 1 anno è stata del 76% e 71%, rispettivamente. La tossicità di grado 3-4 è stata del 12% e dell 11%, rispettivamente e maggiormente astenia, nausea e polmoniti [10]. Il durvalumab è un anticorpo monoclonale umanizzato IgG1 con alta affinità per PD-L1. Uno studio di fase I/II ha arruolato 198 pazienti affetti da NSCLC avanzato già pretrattati a ricevere durvalumab alla dose di 10 mg/kg ogni 2 settimane fino a progressione o tossicità inaccettabile. L obiettivo primario dello studio era la ORR che è risultata essere del 14% nei 149 pazienti valutabili con maggiore attività nell istologia squamosa (ORR del 20%) rispetto alla non-squamosa (ORR del 10%) e nei pazienti PD-L1 positivi (ORR del 23%). La tossicità di grado 3-4, prevalentemente astenia e nausea, è stata del 6% [11]. La Tabella 2 riassume i risultati dei principali studi di seconda linea condotti con gli immunoterapici. Nel trattamento di seconda linea del NSCLC, i risultati dell immunoterapia sono più consistenti, rispetto a quelli riportati per la terapia di prima linea, portando alla registrazione del nivolumab e del pembroli- 539
18 zumab. Attualmente sono in corso numerosi studi di fase III in seconda linea di trattamento di pazienti affetti da NSCLC avanzato nelle diverse istologie in cui ci si propone di definire in maniera più adeguata il ruolo predittivo e/o prognostico di PD-L1, il cutoff più opportuno da considerare oltre che la metodologia da impiegare per la sua determinazione [12], eccetto per il pembrolizumab in cui si è già determinato il cutoff (PD-L1 50%) ed il corrispondente test. TAbELLA 2. Risultati dei principali studi clinici di seconda linea con anti-ctla-4, anti-pd-1 e anti-pd-l1 nel NSCLC avanzato Autore Tipo Istotipo Linea Trattamento N.pz ORR PFS OS Tossicità di (%) (mesi) (mesi) Grado 3 studio (%) KEYNOTE-021 I NSCLC 2 Ipilimumab + Pembrolizumab NR NR 18 (coorte D) [1] Gettinger [2] I NSCLC > 1 Nivolumab CheckMate 063 II Squamoso 2 Nivolumab [3] KEYNOTE-001 I NSCLC 2 Pembrolizumab [7] Horn [8] Ia NSCLC > 1 Atezolizumab %* 82% 11 POPLAR [9] IIR NSCLC 2 Atezolizumab vs Docetaxel BIRCH [10] II NSCLC 2 Atezolizumab Rizvi [11] I/II NSCLC 1 Durvalumab NR NR 6 *PFS a 4 settimane; OS ad 1 anno; OS a 6 mesi; NSCLC: carcinoma del polmone non a piccole cellule; CTLA-4: cytotoxic T-lymphocyte antigen-4; PD1: programmed cell death 1; PD-L1: programmed cell death-ligand 1; N.pz: numero di pazienti; ORR: risposta obiettiva; PFS: sopravvivenza libera da progressione; OS: sopravvivenza mediana; IIR: fase II randomizzato; NR: non riportato 540
19 NSCLC - seconda linea raccomandazioni Per i pazienti affetti da NSCLC avanzato ad istologia squamosa, il trattamento di seconda linea con nivolumab come agente singolo è raccomandato livello di evidenza ib grado di raccomandazione a Per i pazienti affetti da NSCLC avanzato ad istologia non-squamosa, il trattamento di seconda linea con nivolumab come agente singolo è raccomandato. Al momento della stesura delle presenti linee guida, il nivolumab non è ancora registrato in Italia nei pazienti con istologia non-squamosa livello di evidenza ib grado di raccomandazione a Per i pazienti affetti da NSCLC avanzato, il trattamento di seconda-linea con pembrolizumab come agente singolo è raccomandato solo in presenza di espressione di PD-L1 50% determinata con il test PD-L1 IHC 22C3 pharmdx. Al momento della stesura delle presenti linee guida pembrolizumab non è ancora registrato in Italia livello di evidenza iia grado di raccomandazione b 541
20 542 bibliografia 1. Patnaik A, Socinski MA, Gubens MA et al. Phase 1 study of pembrolizumab (pembro; MK-3475) plus ipilimumab (IPI) as second-line therapy for advanced non-small cell lung cancer (NSCLC): KEYNOTE-021 cohort D. J Clin Oncol 2015; 33 (S5):8011 (abstract). 2. Gettinger SN, Horn L, Gandhi L et al. Overall survival and long-term safety of nivolumab (anti-programmed death 1 antibody, BMS , ONO-4538) in patients with previously treated advanced non-small-cell lung cancer. J Clin Oncol 2015; 33: Rizvi NA, Mazières J, Planchard D et al. Activity and safety of nivolumab, an anti-pd-1 immune checkpoint inhibitor, for patients with advanced, refractory squamous non-small-cell lung cancer (CheckMate 063): a phase 2, single-arm trial. Lancet Oncol 2015; 16: Brahmer J, Reckamp KL, Baas P et al. Nivolumab versus docetaxel in advanced squamous-cell non-small-cell lung cancer. N Engl J Med 2015; 373: Borghaei H, Paz-Ares L, Horn L et al. Nivolumab versus docetaxel in advanced nonsquamous non-small-cell lung cancer. N Engl J Med 2015; [Epub ahead of print]. 6. FDA approves Keytruda for advanced non-small cell lung cancer. (accesso il 15 Ottobre 2015). 7. Garon EB, Rizvi NA, Hui R et al. Pembrolizumab for the treatment of non-small-cell lung cancer. N Engl J Med 2015; 372: Horn L, Spigel DR, Gettinger SN et al. Clinical activity, safety and predictive biomarkers of the engineered antibody MPDL3280A (anti-pdl1) in non-small cell lung cancer (NSCLC): update from a phase Ia study. J Clin Oncol 2015; 33(S5):8029 (abstract). 9. Spira AI, Park K, Mazieres J et al. Efficacy, safety and predictive biomarker results from a randomized phase II study comparing MPDL3280A vs docetaxel in 2L/3L NSCLC (POPLAR). J Clin Oncol 2015; 33(S5):8010 (abstract). 10. Besse B, Johnson M, Janne PA et al. Phase II, single-arm trial (BIRCH) of atezolizumab as firstline or subsequent therapy for locally advanced or metastatic PD-L1-selected non-small cell lung cancer (NSCLC). European Cancer Congress Vienna Settembbre 2015, 16LBA (abstract). 11. Rizvi NA, Brahmer JR, Ou S-HI et al. Safety and clinical activity of MEDI4736, an anti-programmed cell death-ligand 1 (PD-L1) antibody, in patients with non-small cell lung cancer (NSCLC). J Clin Oncol 2015; 33(S5):8032 (abstract). 12. National Cancer Institute Clinical Trials Database. (accesso il 15 Ottobre 2015).
21 SCLC SCLC l immunoterapia ha un ruolo nel trattamento dei pazienti affetti da sclc? Il ruolo dell immunoterapia è attualmente valutata anche per il trattamento del carcinoma del polmone a piccole cellule (SCLC). In uno studio di fase Ib, KEYNOTE-028, 147 pazienti con SCLC e già pretrattati sono stati testati per l espressione di PD-L1 (programmed cell death-ligand 1) che è risultata essere 1% in 42 casi (28.6%) e pertanto arruolabili a trattamento con pembrolizumab, anticorpo monoclonale IgG4 anti-pd-1 completamente umano già registrato in Italia per il trattamento del melanoma avanzato. I dati preliminari disponibili su 24 pazienti trattati con pembrolizumab, alla dose di 10 mg/kg ogni 2 settimane, hanno evidenziato una risposta obiettiva (ORR), endpoint primario, del 29.2%. La sopravvivenza libera da progressione (PFS) è stata di 1.8 mesi con la PFS a 6 mesi del 32.5%. La tossicità di grado 3 è stata dell 8.3% con una morte tossica per colite [1]. Il nivolumab, anticorpo monoclonale IgG4 anti-pd-1 (programmed cell death 1) completamente umano, già registrato per il trattamento di seconda linea del carcinoma del polmone non a piccole cellule (al momento della stesura delle seguenti linee guida in Italia è registrato solo per l istologia squamosa), e l ipilimumab, anticorpo monoclonale IgG1 anti-ctla-4 (cytotoxic T-lymphocyte antigen-4) interamente umano, già registrato in Italia per il trattamento del melanoma avanzato, sono in fase di sviluppo clinico nel SCLC. Uno studio di fase I/II ha arruolato 75 pazienti con SCLC già pretrattati a ricevere nivolumab come agente singolo alla dose di 3 mg/kg ogni 2 settimane, oppure la combinazione di nivolumab, alle dosi di 1 o 3 mg/kg, ed ipilimumab, alle dosi di 1 o 3 mg/kg ogni 3 settimane per 4 cicli seguiti dal solo nivolumab alla dose di 3 mg/kg ogni 2 settimane. Nei 40 pazienti valutabili e trattati con il solo nivolumab la ORR è stata del 15%, nei 20 pazienti valutabili e trattati con la combinazione la ORR è stata del 25%. La tossicità di grado 3-4 è stata del 6% per entrambi i trattamenti e rappresentata da rash e diarrea [2]. La Tabella 1 riassume i risultati dei principali studi condotti con gli immunoterapici nel SCLC. Nel SCLC i dati sono ancora preliminari ma abbastanza interessanti 543
22 per definire uno sviluppo clinico dei farmaci immunoterapici sia come agenti singoli che in combinazione anche con la chemioterapia sia in prima linea che in quelle successive [3]. La speranza è di riuscire a migliorare la prognosi del SCLC che resta ferma, da diversi decenni, ai risultati ottenuti dalla combinazione platino/etoposide. TAbELLA 1. Risultati dei principali studi clinici con anti-ctla-4 e anti-pd-1 nel SCLC Autore Tipo Linea Target Trattamento N.pz ORR PFS OS Tossicità di (%) (mesi) (mesi) Grado 3 studio (%) KEYNOTE-028 Ib 2 PD-1 Pembrolizumab NR 8.3 [1] Antonia [2] I/II 2 PD-1 Nivolumab NR NR 6 PD-1 + CTLA-4 Nivolumab + Ipilimumab NR NR 6 SCLC: carcinoma del polmone a piccole cellule; CTLA-4: cytotoxic T-lymphocyte antigen-4; PD1: programmed cell death 1; N.pz: numero di pazienti; ORR: risposta obiettiva; PFS: sopravvivenza libera da progressione; OS: sopravvivenza mediana; NR: non riportato raccomandazioni Per i pazienti affetti da SCLC, il trattamento sia di prima linea che di quelle successive con farmaco immunoterapico, sia come agente singolo che in combinazione con altri immunoterapici o con la chemioterapia, non è raccomandato in quanto ancora in fase di sperimentazione livello di evidenza iib grado di raccomandazione B 544
23 SCLC bibliografia 1. Ott PA, Elez E, Hiret S et al. Pembrolizumab for ED SCLC: Efficacy and Relationship with PD-L1 Expression. J Thorac Oncol 2015; 10 (Supplement 2):S193 (abstract O10.04). 2. Antonia SJ, Bendel J, Taylor M et al. Phase I/II study of nivolumab with or without ipilimumab for treatment of recurrent small cell lung cancer (SCLC): CA J Clin Oncol 2015; 33(S5):7503 (abstract). 3. National Cancer Institute Clinical Trials Database. (accesso il 15 Ottobre 2015). 545
24 Stesura a cura di Antonio Rossi Revisione a cura di Filippo de Marinis & Cesare Gridelli Copyrights AIOT Tutti i diritti sono riservati. E vietata la riproduzione parziale o totale dei contenuti attraverso qualsiasi mezzo, elettronico o meccanico, incluse le fotocopie, la registrazione, la memorizzazione e il successivo utilizzo dei dati, senza l esplicito consenso scritto di AIOT. Stampato nel mese di ottobre 2015 presso Tipografia Riccieri - Roma Progetto grafico a cura di Fabrizio Piersanti e Carmela Caristia
25
26
Le terapie ad oggi disponibili per il trattamento dei tumori del polmone, soprattutto in fase avanzata di malattia, offrono scarso beneficio eccetto
 IMMUNOTERAPIA IMMUNOTERAPIA 230 NSCLC - PRIMA LINEA 234 NSCLC - SECONdA LINEA 239 SCLC 250 immunoterapia Le terapie ad oggi disponibili per il trattamento dei tumori del polmone, soprattutto in fase avanzata
IMMUNOTERAPIA IMMUNOTERAPIA 230 NSCLC - PRIMA LINEA 234 NSCLC - SECONdA LINEA 239 SCLC 250 immunoterapia Le terapie ad oggi disponibili per il trattamento dei tumori del polmone, soprattutto in fase avanzata
16th World Conference on Lung Cancer (WCLC): highlights
 16th World Conference on Lung Cancer (WCLC): highlights RISULTATI PRELIMINARI STUDIO ITACA Lo studio Itaca è uno studio multicentrico italiano di Fase III che confronta un trattamento chemioterapico tailored
16th World Conference on Lung Cancer (WCLC): highlights RISULTATI PRELIMINARI STUDIO ITACA Lo studio Itaca è uno studio multicentrico italiano di Fase III che confronta un trattamento chemioterapico tailored
NSCLC - stadio iiib/iv
 I TUMORI POLMONARI linee guida per la pratica clinica NSCLC - stadio iiib/iv quale trattamento per i pazienti anziani con malattia avanzata? Il carcinoma polmonare è un tumore frequente nell età avanzata.
I TUMORI POLMONARI linee guida per la pratica clinica NSCLC - stadio iiib/iv quale trattamento per i pazienti anziani con malattia avanzata? Il carcinoma polmonare è un tumore frequente nell età avanzata.
SCHEDA FARMACO (a cura di UOS Farmacoeconomia e HTA, Area Centro) Nintedanib (VARGATEF)
 Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta SCHEDA FARMACO (a cura di UOS Farmacoeconomia e HTA, Area Centro) Nintedanib (VARGATEF)
Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta SCHEDA FARMACO (a cura di UOS Farmacoeconomia e HTA, Area Centro) Nintedanib (VARGATEF)
Sinossi di studio clinico Codice: GECP06/01 Pag. 1 di 5
 Codice: GECP06/01 Pag. 1 di 5 Studio aperto randomizzato multicentrico di fase III di confronto tra il trattamento con Erlotinib (Tarceva ) e la chemioterapia nei pazienti affetti da carcinoma non a piccole
Codice: GECP06/01 Pag. 1 di 5 Studio aperto randomizzato multicentrico di fase III di confronto tra il trattamento con Erlotinib (Tarceva ) e la chemioterapia nei pazienti affetti da carcinoma non a piccole
Espressione di geni specifici per un determinato tumore
 Espressione di geni specifici per un determinato tumore Paziente A: Non ha il cancro Espressione dei geni: Nessuna Biopsia Geni associati al cancro allo stomaco Paziente B: Ha un tumore allo stomaco Bassa
Espressione di geni specifici per un determinato tumore Paziente A: Non ha il cancro Espressione dei geni: Nessuna Biopsia Geni associati al cancro allo stomaco Paziente B: Ha un tumore allo stomaco Bassa
Aggiornamento al
 Ca polmone NSCLC- terapia adiuvante APERTI ARRUOLAMENTO IN FASE DI ATTIVAZIONE ESEGUITA solo FEASIBILITY A randomized, phase 3 trial with anti-pd-1 monoclonal antibody pembrolizumab (MK-3475) versus placebo
Ca polmone NSCLC- terapia adiuvante APERTI ARRUOLAMENTO IN FASE DI ATTIVAZIONE ESEGUITA solo FEASIBILITY A randomized, phase 3 trial with anti-pd-1 monoclonal antibody pembrolizumab (MK-3475) versus placebo
SEBASTIANO FILETTI. Dipartimento di Medicina Interna e Specialità Mediche. Università di Roma Sapienza, Roma
 SEBASTIANO FILETTI Dipartimento di Medicina Interna e Specialità Mediche Università di Roma Sapienza, Roma La malattia tiroidea è in aumento negli ultimi anni. Quali le ragioni? Dati epidemiologici provenienti
SEBASTIANO FILETTI Dipartimento di Medicina Interna e Specialità Mediche Università di Roma Sapienza, Roma La malattia tiroidea è in aumento negli ultimi anni. Quali le ragioni? Dati epidemiologici provenienti
Cetuximab e mutazione K-Ras nel tumore del colon-retto
 Università di Pisa Dipartimento di Farmacia Corso di laurea in CTF Corso: Basi biochimiche dell azione dei farmaci Cetuximab e mutazione K-Ras nel tumore del colon-retto Pisa, 27/03/2014 Samuela Fabiani
Università di Pisa Dipartimento di Farmacia Corso di laurea in CTF Corso: Basi biochimiche dell azione dei farmaci Cetuximab e mutazione K-Ras nel tumore del colon-retto Pisa, 27/03/2014 Samuela Fabiani
Pembrolizumab (Keytruda ) Premio Galeno Italia 2015
 Pembrolizumab (Keytruda ) Premio Galeno Italia 2015 Pembrolizumab ( MK3475) è un anticorpo monoclonale IgG4, umanizzato, ad alta affinità, anti PD-1 Exerts dual ligand blockade of the PD-1 pathway Similar
Pembrolizumab (Keytruda ) Premio Galeno Italia 2015 Pembrolizumab ( MK3475) è un anticorpo monoclonale IgG4, umanizzato, ad alta affinità, anti PD-1 Exerts dual ligand blockade of the PD-1 pathway Similar
Dott. Alessandro Fabbri U.O. Pneumologia ASL 3 PT Direttore ff Dott. Franco Vannucci
 Dott. Alessandro Fabbri U.O. Pneumologia ASL 3 PT Direttore ff Dott. Franco Vannucci Negli ultimi anni c è stato un notevole cambiamento nella gestione diagnosticoterapeutica dei soggetti affetti da neoplasia
Dott. Alessandro Fabbri U.O. Pneumologia ASL 3 PT Direttore ff Dott. Franco Vannucci Negli ultimi anni c è stato un notevole cambiamento nella gestione diagnosticoterapeutica dei soggetti affetti da neoplasia
Anticorpi monoclonali Anti-EGFR. -Ruolo Biologico -Evidenze terapeutiche -Problemi -Sviluppi futuri. Valentina Anrò
 Anticorpi monoclonali Anti-EGFR -Ruolo Biologico -Evidenze terapeutiche -Problemi -Sviluppi futuri Valentina Anrò Ruolo Biologico Epidermal Growth Factor Receptor Extracellular Domain Transmembrane Domain
Anticorpi monoclonali Anti-EGFR -Ruolo Biologico -Evidenze terapeutiche -Problemi -Sviluppi futuri Valentina Anrò Ruolo Biologico Epidermal Growth Factor Receptor Extracellular Domain Transmembrane Domain
Documento PTR n.212 relativo a:
 Direzione Generale Sanità e Politiche Sociali Commissione Regionale del Farmaco (D.G.R. 1540/2006, 2129/2010 e 490/2011) Documento PTR n.212 relativo a: PAZOPANIB Aprile 2014 Pazopanib Indicazioni registrate
Direzione Generale Sanità e Politiche Sociali Commissione Regionale del Farmaco (D.G.R. 1540/2006, 2129/2010 e 490/2011) Documento PTR n.212 relativo a: PAZOPANIB Aprile 2014 Pazopanib Indicazioni registrate
L immunoterapia nel NSCLC: evoluzione delle conoscenze e dei progressi clinici
 186 Rassegna Recenti Prog Med 2016; 107: 186-192 L immunoterapia nel NSCLC: evoluzione delle conoscenze e dei progressi clinici alessia pochesci 1,2, antonio passaro 1, chiara catania 1, cristina noberasco
186 Rassegna Recenti Prog Med 2016; 107: 186-192 L immunoterapia nel NSCLC: evoluzione delle conoscenze e dei progressi clinici alessia pochesci 1,2, antonio passaro 1, chiara catania 1, cristina noberasco
SCHEDA FARMACO. Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta
 Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta Indicazione terapeutica Classificazione: Spesa per paziente trattato (euro, posologia/durata)
Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta Indicazione terapeutica Classificazione: Spesa per paziente trattato (euro, posologia/durata)
La maggior parte dei pazienti con carcinoma del polmone non a piccole cellule (NSCLC) e mutazione di EGFR trattati in prima linea con inibitore
 NSCLC - linee successive QUALE TRATTAMENTO DI II LINEA PER I PAZIENTI 217 PROGRESSIONE AGLI ANTI-EGFR? QUALE TRATTAMENTO DI II LINEA PER I PAZIENTI 220 IN PROGRESSIONE AL CRIZOTINIB? QUALE CHEMIOTERAPIA
NSCLC - linee successive QUALE TRATTAMENTO DI II LINEA PER I PAZIENTI 217 PROGRESSIONE AGLI ANTI-EGFR? QUALE TRATTAMENTO DI II LINEA PER I PAZIENTI 220 IN PROGRESSIONE AL CRIZOTINIB? QUALE CHEMIOTERAPIA
LA RESEZIONE DELLE METASTASI EPATICHE NEL TUMORE METASTATICO DEL COLON RETTO
 LA RESEZIONE DELLE METASTASI EPATICHE NEL TUMORE METASTATICO DEL COLON RETTO Cetuximab può ridurre la massa tumorale per permettere la resezione delle metastasi, anche, in pazienti inizialmente non resecabili,
LA RESEZIONE DELLE METASTASI EPATICHE NEL TUMORE METASTATICO DEL COLON RETTO Cetuximab può ridurre la massa tumorale per permettere la resezione delle metastasi, anche, in pazienti inizialmente non resecabili,
Novità nell immunoterapia del NSCLC. Marcello Tiseo Oncologia Medica Coordinatore PDTA Oncologia Toracica Azienda Ospedaliero-Universitaria di Parma
 Novità nell immunoterapia del NSCLC Marcello Tiseo Oncologia Medica Coordinatore PDTA Oncologia Toracica Azienda Ospedaliero-Universitaria di Parma Agenda Introduzione Anti-CTLA4: ipilimumab Anti-PD1/Anti-PDL1:
Novità nell immunoterapia del NSCLC Marcello Tiseo Oncologia Medica Coordinatore PDTA Oncologia Toracica Azienda Ospedaliero-Universitaria di Parma Agenda Introduzione Anti-CTLA4: ipilimumab Anti-PD1/Anti-PDL1:
E.Molfese, P.Matteucci, A.Iurato, M. Fiore, L.E. Trodella, L. Poggesi, R.M. D Angelillo, E. Iannacone, L.Trodella!
 Il trattamento stereotassico delle lesioni surrenaliche in pazienti oligometastatici affetti da NSCLC: una promettente arma per il controllo locale di malattia?! E.Molfese, P.Matteucci, A.Iurato, M. Fiore,
Il trattamento stereotassico delle lesioni surrenaliche in pazienti oligometastatici affetti da NSCLC: una promettente arma per il controllo locale di malattia?! E.Molfese, P.Matteucci, A.Iurato, M. Fiore,
Trials clinici. Disegni di studio
 Trials Clinici Dott.ssa Pamela Di Giovanni Studi descrittivi Disegni di studio Popolazioni Individui Studi analitici Osservazionali Sperimentali Studi di correlazione o ecologici Case report - Case series
Trials Clinici Dott.ssa Pamela Di Giovanni Studi descrittivi Disegni di studio Popolazioni Individui Studi analitici Osservazionali Sperimentali Studi di correlazione o ecologici Case report - Case series
Tumori: farmaco immunoterapico efficace contro cancro polmone
 1June2015 http://salute.agi.it/farmaci-eterapie/notizie/tumori_farmaco_immunoterapico_efficace_contro_cancro_polmone-201505291356-farrsa1015 Tumori: farmaco immunoterapico efficace contro cancro polmone
1June2015 http://salute.agi.it/farmaci-eterapie/notizie/tumori_farmaco_immunoterapico_efficace_contro_cancro_polmone-201505291356-farrsa1015 Tumori: farmaco immunoterapico efficace contro cancro polmone
BE-Positive: Beyond progression after tki in Egfr-Positive NSCLC patients. Sinossi
 BE-Positive: Beyond progression after tki in Egfr-Positive NSCLC patients Sinossi Principal Investigator e centro promotore dello studio: Dr.ssa Silvia Novello (Divisione di Oncologia Toracica, Università
BE-Positive: Beyond progression after tki in Egfr-Positive NSCLC patients Sinossi Principal Investigator e centro promotore dello studio: Dr.ssa Silvia Novello (Divisione di Oncologia Toracica, Università
Un paziente su cinque con cancro al polmone sopravvive dopo 3 anni
 http://salute24.ilsole24ore.com/articles/17936-un-paziente-su-cinque-con-cancro-al-polmone-sopravvive-dopo-3-anni Un paziente su cinque con cancro al polmone sopravvive dopo 3 anni Un paziente su cinque,
http://salute24.ilsole24ore.com/articles/17936-un-paziente-su-cinque-con-cancro-al-polmone-sopravvive-dopo-3-anni Un paziente su cinque con cancro al polmone sopravvive dopo 3 anni Un paziente su cinque,
IMMUNO-ONCOLOGIA. Immunooncologia. La nuova arma contro il tumore del polmone. Associazione Italiana di Oncologia Medica
 IMMUNO-ONCOLOGIA Immunooncologia La nuova arma contro il tumore del polmone Associazione Italiana di Oncologia Medica Indice 3 Perché questo opuscolo 4 L immuno-oncologia, la nuova frontiera terapeutica
IMMUNO-ONCOLOGIA Immunooncologia La nuova arma contro il tumore del polmone Associazione Italiana di Oncologia Medica Indice 3 Perché questo opuscolo 4 L immuno-oncologia, la nuova frontiera terapeutica
I markers biologici come fattori predittivi di efficacia terapeutica nei tumori solidi: l esperienza di Varese
 I markers biologici come fattori predittivi di efficacia terapeutica nei tumori solidi: l esperienza di Varese Daniela Furlan U.O. Anatomia Patologica, Ospedale di Circolo e Fondazione Macchi, Varese Il
I markers biologici come fattori predittivi di efficacia terapeutica nei tumori solidi: l esperienza di Varese Daniela Furlan U.O. Anatomia Patologica, Ospedale di Circolo e Fondazione Macchi, Varese Il
Aggiornamenti su RAS: mutazioni di KRAS ed NRAS nel carcinoma del colon retto. Carmelo Lupo
 Aggiornamenti su RAS: mutazioni di KRAS ed NRAS nel carcinoma del colon retto Carmelo Lupo RAS-RAF signaling Activation of the RAS-RAF signaling cascade occurs via the following sequential steps 1 : Activation
Aggiornamenti su RAS: mutazioni di KRAS ed NRAS nel carcinoma del colon retto Carmelo Lupo RAS-RAF signaling Activation of the RAS-RAF signaling cascade occurs via the following sequential steps 1 : Activation
Rassegna Stampa. Comunicato stampa. Intermedia s.r.l. per la comunicazione integrata
 Rassegna Stampa Comunicato stampa LA COMMISSIONE EUROPEA APPROVA PEMBROLIZUMAB PER IL TRATTAMENTO IN PRIMA LINEA DI PAZIENTI CON CARCINOMA POLMONARE METASTATICO NON A PICCOLE CELLULE Intermedia s.r.l.
Rassegna Stampa Comunicato stampa LA COMMISSIONE EUROPEA APPROVA PEMBROLIZUMAB PER IL TRATTAMENTO IN PRIMA LINEA DI PAZIENTI CON CARCINOMA POLMONARE METASTATICO NON A PICCOLE CELLULE Intermedia s.r.l.
Lynch TJ, Patel T, Dreisbach L, McCleod M, Heim WJ, Hermann RC, Paschold E, Iannotti NO, Dakhil S, Gorton S, Pautret V, Weber MR, Woytowitz D.
 Lynch TJ, Patel T, Dreisbach L, McCleod M, Heim WJ, Hermann RC, Paschold E, Iannotti NO, Dakhil S, Gorton S, Pautret V, Weber MR, Woytowitz D. Cetuximab and First-Line Taxane/Carboplatin Chemotherapy in
Lynch TJ, Patel T, Dreisbach L, McCleod M, Heim WJ, Hermann RC, Paschold E, Iannotti NO, Dakhil S, Gorton S, Pautret V, Weber MR, Woytowitz D. Cetuximab and First-Line Taxane/Carboplatin Chemotherapy in
Fondazione AIOM Incontra pazienti e cittadini. Immunoterapia in oncologia: risultati e prospettive? Alessandra Fabi
 Fondazione AIOM Incontra pazienti e cittadini Immunoterapia in oncologia: risultati e prospettive? Alessandra Fabi Roma, 25 Maggio 2019 UNA "NUOVA" ARMA IN ONCOLOGIA BASI dell immunologia Michaela Sharpe,
Fondazione AIOM Incontra pazienti e cittadini Immunoterapia in oncologia: risultati e prospettive? Alessandra Fabi Roma, 25 Maggio 2019 UNA "NUOVA" ARMA IN ONCOLOGIA BASI dell immunologia Michaela Sharpe,
SCLC - terapia di ii linea 53 II LINEA - RISULTATI E LIMITII
 SCLC - terapia di ii linea TRATTAMENTO STANDARD IN 53 II LINEA - RISULTATI E LIMITII SCLC - terapia di ii linea trattamento standard in ii linea - risultati e limiti Quasi la totalità dei pazienti affetti
SCLC - terapia di ii linea TRATTAMENTO STANDARD IN 53 II LINEA - RISULTATI E LIMITII SCLC - terapia di ii linea trattamento standard in ii linea - risultati e limiti Quasi la totalità dei pazienti affetti
therapies in ii e iii linea?
 I TUMORI POLMONARI linee guida per la pratica clinica NSCLC - linee successive chemioterapia o targeted therapies in ii e iii linea? Attualmente i farmaci approvati nel trattamento di II linea del carcinoma
I TUMORI POLMONARI linee guida per la pratica clinica NSCLC - linee successive chemioterapia o targeted therapies in ii e iii linea? Attualmente i farmaci approvati nel trattamento di II linea del carcinoma
Sperimentazione Clinica: ruolo e responsabilità dell Infermiere
 Sperimentazione Clinica: ruolo e responsabilità dell Infermiere Fasi dello studio Disegni di ricerca sperimentale Barbara Gorini, Investigator Site Development Lead, Development Operations- Pfizer ITALIA
Sperimentazione Clinica: ruolo e responsabilità dell Infermiere Fasi dello studio Disegni di ricerca sperimentale Barbara Gorini, Investigator Site Development Lead, Development Operations- Pfizer ITALIA
Art 1 Art 2 Art 3 ore 12,00 del 3 agosto '15
 AZIENDA U.S.L. 2 - Lucca Via per S.Alessio- Monte S.Quirico 55100 Lucca BANDO PER L'ISTITUZIONE DI N. 1 BORSA DI STUDIO FINALIZZATA ALLA GESTIONE STATISTICA E ALL ESECUZIONE DELLE PROCEDURE OPERATIVE DELLA
AZIENDA U.S.L. 2 - Lucca Via per S.Alessio- Monte S.Quirico 55100 Lucca BANDO PER L'ISTITUZIONE DI N. 1 BORSA DI STUDIO FINALIZZATA ALLA GESTIONE STATISTICA E ALL ESECUZIONE DELLE PROCEDURE OPERATIVE DELLA
Specialità: Avastin(Roche spa)
 BEVACIZUMAB per l'indicazione: trattamento in prima linea di pazienti con carcinoma polmonare non a piccole cellule, non resecabile, avanzato, metastatico o in ricaduta in aggiunta a chemioterapia a base
BEVACIZUMAB per l'indicazione: trattamento in prima linea di pazienti con carcinoma polmonare non a piccole cellule, non resecabile, avanzato, metastatico o in ricaduta in aggiunta a chemioterapia a base
La terapia medica primaria e adiuvante e il follow-up: le principali novità. a cura di Claudio Zamagni (Bologna) e Antonio Frassoldati (Ferrara)
 Protocollo diagnostico-terapeutico per le Pazienti con carcinoma mammario La terapia medica primaria e adiuvante e il follow-up: le principali novità a cura di Claudio Zamagni (Bologna) e Antonio Frassoldati
Protocollo diagnostico-terapeutico per le Pazienti con carcinoma mammario La terapia medica primaria e adiuvante e il follow-up: le principali novità a cura di Claudio Zamagni (Bologna) e Antonio Frassoldati
Le linee guida evidence based
 Le linee guida evidence based Linee guida: definizione Raccomandazioni di comportamento clinico, prodotte attraverso un processo sistematico, allo scopo di assistere medici e pazienti nel decidere quali
Le linee guida evidence based Linee guida: definizione Raccomandazioni di comportamento clinico, prodotte attraverso un processo sistematico, allo scopo di assistere medici e pazienti nel decidere quali
coin lesion polmonare
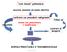 coin lesion polmonare accurata anamnesi ed esame obiettivo impossibile confronto con precedenti radiogrammi lesione non preesistente o modificatasi TC Follow-up caratteri di benignità lesione sospetta
coin lesion polmonare accurata anamnesi ed esame obiettivo impossibile confronto con precedenti radiogrammi lesione non preesistente o modificatasi TC Follow-up caratteri di benignità lesione sospetta
MINI SCHEDA HTA CRIZOTINIB (XALKORI )
 1/7 MINI SCHEDA HTA CRIZOTINIB (XALKORI ) Nome Commerciale XALKORI Principio Attivo Crizotinib Ditta Produttrice Pfizer Italia Srl ATC L01XE16 Formulazione Capsule rigide Dosaggio 200 mg 250 mg Altri antineoplastici
1/7 MINI SCHEDA HTA CRIZOTINIB (XALKORI ) Nome Commerciale XALKORI Principio Attivo Crizotinib Ditta Produttrice Pfizer Italia Srl ATC L01XE16 Formulazione Capsule rigide Dosaggio 200 mg 250 mg Altri antineoplastici
Nuovi regimi terapeutici nel trattamento del mieloma multiplo in pazienti non candidabili a trapianto
 Nuovi regimi terapeutici nel trattamento del mieloma multiplo in pazienti non candidabili a trapianto Antonio Palumbo Divisione di Ematologia Universitaria, Ospedale Molinette, Torino Per più di quattro
Nuovi regimi terapeutici nel trattamento del mieloma multiplo in pazienti non candidabili a trapianto Antonio Palumbo Divisione di Ematologia Universitaria, Ospedale Molinette, Torino Per più di quattro
Dott.ssa Chiara Dell Agnola. MdA Oncologia,AOUI Verona
 Dott.ssa Chiara Dell Agnola MdA Oncologia,AOUI Verona Malattia metastatica La neoplasia del testa-collo si presenta in oltre la metà dei pazienti in stadio avanzato (Stadio III e IV) 40-80% recidiva loco-regionale
Dott.ssa Chiara Dell Agnola MdA Oncologia,AOUI Verona Malattia metastatica La neoplasia del testa-collo si presenta in oltre la metà dei pazienti in stadio avanzato (Stadio III e IV) 40-80% recidiva loco-regionale
NESSUNO STUDIO METODOLOGICAMENTE SCORRETTO PUO ESSERE CONSIDERATO ETICO
 COME E QUANDO GLI ASPETTI TECNICI DEI PROTOCOLLI POSSONO-DEVONO ESSERE OGGETTO-ARGOMENTO DI DECISIONI ETICHE? Fausto Roila Oncologia Medica, Terni NESSUNO STUDIO METODOLOGICAMENTE SCORRETTO PUO ESSERE
COME E QUANDO GLI ASPETTI TECNICI DEI PROTOCOLLI POSSONO-DEVONO ESSERE OGGETTO-ARGOMENTO DI DECISIONI ETICHE? Fausto Roila Oncologia Medica, Terni NESSUNO STUDIO METODOLOGICAMENTE SCORRETTO PUO ESSERE
IL diabetico. Gestione condivisa. Claudio Marengo Marco Comoglio Andrea Pizzini
 IL diabetico anziano Gestione condivisa Claudio Marengo Marco Comoglio Andrea Pizzini SEEd srl C.so Vigevano, 35-10152 Torino Tel. 011.566.02.58 - Fax 011.518.68.92 www.edizioniseed.it info@seed-online.it
IL diabetico anziano Gestione condivisa Claudio Marengo Marco Comoglio Andrea Pizzini SEEd srl C.so Vigevano, 35-10152 Torino Tel. 011.566.02.58 - Fax 011.518.68.92 www.edizioniseed.it info@seed-online.it
Dir. Resp.: Alessandro Sallusti
 Tiratura 04/2015: 148.106 Diffusione 04/2015: 83.049 Lettori I 2015: 484.000 Dir. Resp.: Alessandro Sallusti da pag. 37 13-06-2015 Lettori 38.890 http://www.corriere.it/salute/ CONGRESSO AMERICANO DI ONCOLOGIA
Tiratura 04/2015: 148.106 Diffusione 04/2015: 83.049 Lettori I 2015: 484.000 Dir. Resp.: Alessandro Sallusti da pag. 37 13-06-2015 Lettori 38.890 http://www.corriere.it/salute/ CONGRESSO AMERICANO DI ONCOLOGIA
Informazioni per potenziali partecipanti. Possiamo sciogliere l'amiloidosi AL?
 Informazioni per potenziali partecipanti Possiamo sciogliere l'amiloidosi AL? È ora di affrontare diversamente l amiloidosi AL? L amiloidosi AL è una malattia rara e spesso fatale causata dall accumulo
Informazioni per potenziali partecipanti Possiamo sciogliere l'amiloidosi AL? È ora di affrontare diversamente l amiloidosi AL? L amiloidosi AL è una malattia rara e spesso fatale causata dall accumulo
Il punto di vista del clinico
 Il punto di vista del clinico Giulio Metro S.C. Oncologia Medica Ospedale Santa Maria della Misericordia, Azienda Ospedaliera di Perugia Registri di monitoraggio AIFA: stato dell arte ed esperienze a confronto
Il punto di vista del clinico Giulio Metro S.C. Oncologia Medica Ospedale Santa Maria della Misericordia, Azienda Ospedaliera di Perugia Registri di monitoraggio AIFA: stato dell arte ed esperienze a confronto
Igiene. Dott. Pamela Di Giovanni. Definizione
 Igiene Dott. Pamela Di Giovanni Definizione Disciplina medica che ha come obiettivo la tutela e la promozione della salute umana, intendendo per salute umana un completo stato di benessere psichico, fisico
Igiene Dott. Pamela Di Giovanni Definizione Disciplina medica che ha come obiettivo la tutela e la promozione della salute umana, intendendo per salute umana un completo stato di benessere psichico, fisico
Terapia in fase Avanzata
 IL CARCINOMA DEL COLON-RETTO 14 OTTOBRE 2011, ROMA Terapia in fase Avanzata Maria Sofia Rosati Oncologia A Policlinico Umberto I Roma Numeri.. e persone!! ***Solo il 56% *50% dei pz con CRC è over 70 degli
IL CARCINOMA DEL COLON-RETTO 14 OTTOBRE 2011, ROMA Terapia in fase Avanzata Maria Sofia Rosati Oncologia A Policlinico Umberto I Roma Numeri.. e persone!! ***Solo il 56% *50% dei pz con CRC è over 70 degli
Seconda Parte Specifica di scuola - Statistica sanitaria e Biometria - 31/07/2015
 Domande relative alla specializzazione in: Statistica sanitaria e Biometria Domanda #1 (codice domanda: n.641) : In epidemiologia, una variabile di confondimento è una variabile: A: associata sia alla
Domande relative alla specializzazione in: Statistica sanitaria e Biometria Domanda #1 (codice domanda: n.641) : In epidemiologia, una variabile di confondimento è una variabile: A: associata sia alla
Her2/neu Il ruolo del Pertuzumab
 Università degli Studi di Torino Corso di Laurea Specialistica in Biotecnologie Mediche Her2/neu Il ruolo del Pertuzumab Corso di Immunologia Molecolare Anno Accademico 2007/08 Elisa Migliore Her2 nelle
Università degli Studi di Torino Corso di Laurea Specialistica in Biotecnologie Mediche Her2/neu Il ruolo del Pertuzumab Corso di Immunologia Molecolare Anno Accademico 2007/08 Elisa Migliore Her2 nelle
ANALISI DI IMPATTO DI BUDGET DI UNA NUOVA STRATEGIA VACCINALE PATRIZIA BERTO, NICOLA PRINCIPI
 ANALISI DI IMPATTO DI BUDGET DI UNA NUOVA STRATEGIA VACCINALE PATRIZIA BERTO, NICOLA PRINCIPI INTRODUZIONE Le Infezioni da Pneumococco (PNU) rappresentano un problema sanitario grave, soprattutto a causa
ANALISI DI IMPATTO DI BUDGET DI UNA NUOVA STRATEGIA VACCINALE PATRIZIA BERTO, NICOLA PRINCIPI INTRODUZIONE Le Infezioni da Pneumococco (PNU) rappresentano un problema sanitario grave, soprattutto a causa
L Investigator s Brochure. Marisa Dell Aera Comitato Etico Azienda Ospedaliera Policlinico Bari. Maglie 25 novembre 2004
 L Investigator s Brochure Marisa Dell Aera Comitato Etico Azienda Ospedaliera Policlinico Bari Maglie 25 novembre 2004 Investigator s Brochure Good Clinical Practice DM 15/07/97 Cosa è? L IB è una raccolta
L Investigator s Brochure Marisa Dell Aera Comitato Etico Azienda Ospedaliera Policlinico Bari Maglie 25 novembre 2004 Investigator s Brochure Good Clinical Practice DM 15/07/97 Cosa è? L IB è una raccolta
SINOSSI DELLO STUDIO EUDRACT N. 2012-001028-36 COORDINAMENTO E RESPONSABILE DELLO STUDIO
 SINOSSI DELLO STUDIO TITOLO EUDRACT N. 2012-001028-36 COORDINAMENTO E RESPONSABILE DELLO STUDIO SPONSOR Sequenza ottimale di ormonoterapia in pazienti con carcinoma mammario metastatico ricadute dopo terapia
SINOSSI DELLO STUDIO TITOLO EUDRACT N. 2012-001028-36 COORDINAMENTO E RESPONSABILE DELLO STUDIO SPONSOR Sequenza ottimale di ormonoterapia in pazienti con carcinoma mammario metastatico ricadute dopo terapia
ARTICOLO SCIENTIFICO: ANALISI E VALUTAZIONE CRITICA DELLE INFORMAZIONI. critical appraisal BOSCARO GIANNI 1
 ARTICOLO SCIENTIFICO: ANALISI E VALUTAZIONE CRITICA DELLE INFORMAZIONI critical appraisal BOSCARO GIANNI 1 BOSCARO GIANNI 2 Analisi Statistica analisi descrittiva: descrizione dei dati campionari con grafici,
ARTICOLO SCIENTIFICO: ANALISI E VALUTAZIONE CRITICA DELLE INFORMAZIONI critical appraisal BOSCARO GIANNI 1 BOSCARO GIANNI 2 Analisi Statistica analisi descrittiva: descrizione dei dati campionari con grafici,
Novità dall American Society Of Clinical Oncology Annual Meeting 2014. Mario Scartozzi
 HER2Club in gastric cancer Novità dall American Society Of Clinical Oncology Annual Meeting 2014. Mario Scartozzi Anche quest anno il consueto appuntamento di aggiornamento per gli oncologi di tutto il
HER2Club in gastric cancer Novità dall American Society Of Clinical Oncology Annual Meeting 2014. Mario Scartozzi Anche quest anno il consueto appuntamento di aggiornamento per gli oncologi di tutto il
SCHEDA DI VALUTAZIONE PER L INSERIMENTO DI FARMACI NON PRESENTI NEL PTR ERLOTINIB
 RICHIESTA DI INSERIMENTO IN PTR DI ATC L01XE03 (TARCEVA ) Presentata da Componente Commissione Prontuario Terapeutico Regionale In data 13 Dicembre 2006 Per le seguenti motivazioni (sintesi): Tarceva non
RICHIESTA DI INSERIMENTO IN PTR DI ATC L01XE03 (TARCEVA ) Presentata da Componente Commissione Prontuario Terapeutico Regionale In data 13 Dicembre 2006 Per le seguenti motivazioni (sintesi): Tarceva non
STUDI SU MATERIALE GENETICO
 Istituto Oncologico Veneto Istituto di Ricovero e Cura a Carattere Scientifico Ospedale Busonera I.O.V. ISTITUTO ONCOLOGICO VENETO I.R.C.C.S. STUDI SU MATERIALE GENETICO Comitato Etico Istituto Oncologico
Istituto Oncologico Veneto Istituto di Ricovero e Cura a Carattere Scientifico Ospedale Busonera I.O.V. ISTITUTO ONCOLOGICO VENETO I.R.C.C.S. STUDI SU MATERIALE GENETICO Comitato Etico Istituto Oncologico
SCHEDA DI VALUTAZIONE PER L INSERIMENTO DI FARMACI NON PRESENTI NEL PTR
 RICHIESTA DI INSERIMENTO IN PTR DI GEFITINIB ATC L01XE02 (IRESSA ) Presentata da Dott. A. Contu Direttore Oncologia medica ASL 1 Sassari In data luglio 2010 Per le seguenti motivazioni: Iressa è l unico
RICHIESTA DI INSERIMENTO IN PTR DI GEFITINIB ATC L01XE02 (IRESSA ) Presentata da Dott. A. Contu Direttore Oncologia medica ASL 1 Sassari In data luglio 2010 Per le seguenti motivazioni: Iressa è l unico
Tumore del polmone (Non Small Cell Lung Cancer) Metastatico o non operabile. Erlotinib II linea di terapia. Raccomandazioni d'uso. Documento PTR n.
 Documento PTR n.131 Raccomandazioni d'uso Tumore del polmone (Non Small Cell Lung Cancer) Metastatico o non operabile Erlotinib II linea di terapia A cura del Gruppo Regionale Farmaci Oncologici (GReFO)
Documento PTR n.131 Raccomandazioni d'uso Tumore del polmone (Non Small Cell Lung Cancer) Metastatico o non operabile Erlotinib II linea di terapia A cura del Gruppo Regionale Farmaci Oncologici (GReFO)
Raccomandazioni evidence-based. Farmaci per il tumore polmonare non a piccole cellule (NSCLC), avanzato, seconda linea di terapia
 Raccomandazioni evidence-based Farmaci per il tumore polmonare non a piccole cellule (NSCLC), avanzato, seconda linea di terapia A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d
Raccomandazioni evidence-based Farmaci per il tumore polmonare non a piccole cellule (NSCLC), avanzato, seconda linea di terapia A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d
Università del Piemonte Orientale. Corso di Laurea in Medicina e Chirurgia. Corso di Statistica Medica. I modelli di studio
 Università del Piemonte Orientale Corso di Laurea in Medicina e Chirurgia Corso di Statistica Medica I modelli di studio Corso di laurea in medicina e chirurgia - Statistica Medica Disegno dello studio
Università del Piemonte Orientale Corso di Laurea in Medicina e Chirurgia Corso di Statistica Medica I modelli di studio Corso di laurea in medicina e chirurgia - Statistica Medica Disegno dello studio
 CRITERI RADIOLOGICI DI VALUTAZIONE DELLA RISPOSTA ALLA TERAPIA ONCOLOGICA Radiologia Ferrara CRITERI RECIST Response Evaluation Criteria In Solid Tumor CRITERI RECIST Sono un gruppo di regole atte ad identificare
CRITERI RADIOLOGICI DI VALUTAZIONE DELLA RISPOSTA ALLA TERAPIA ONCOLOGICA Radiologia Ferrara CRITERI RECIST Response Evaluation Criteria In Solid Tumor CRITERI RECIST Sono un gruppo di regole atte ad identificare
Histological subtypes of non small cell lung cancer (NSCLC): benchmark on NSCLC NOS. Are adenocarcinoma decreasing? Our experience on 1636 cases.
 Histological subtypes of non small cell lung cancer (NSCLC): benchmark on NSCLC NOS. Are adenocarcinoma decreasing? Our experience on 1636 cases. De Pellegrin A., De Maglio G., Pizzolitto S. A.O.U. S.
Histological subtypes of non small cell lung cancer (NSCLC): benchmark on NSCLC NOS. Are adenocarcinoma decreasing? Our experience on 1636 cases. De Pellegrin A., De Maglio G., Pizzolitto S. A.O.U. S.
Corso per operatori dei Registri Tumori Reggio Emilia 3-6 dicembre 2007. Tumore del polmone. Adele Caldarella
 Corso per operatori dei Registri Tumori Reggio Emilia 3-6 dicembre 2007 Tumore del polmone Adele Caldarella Frequenza del tumore del polmone in Italia AIRTum AIRTum Mortalità per tumore del polmone AIRTum
Corso per operatori dei Registri Tumori Reggio Emilia 3-6 dicembre 2007 Tumore del polmone Adele Caldarella Frequenza del tumore del polmone in Italia AIRTum AIRTum Mortalità per tumore del polmone AIRTum
Quando il dolore è ancora un problema. XVII CIPOMO Congresso Nazionale Roma, 20-22 giugno 2013
 Quando il dolore è ancora un problema XVII CIPOMO Congresso Nazionale Roma, 20-22 giugno 2013 Marta Gentili vivere senza dolore onlus In Italia, nel 2012, si stimano circa 364 mila nuove diagnosi per tumore
Quando il dolore è ancora un problema XVII CIPOMO Congresso Nazionale Roma, 20-22 giugno 2013 Marta Gentili vivere senza dolore onlus In Italia, nel 2012, si stimano circa 364 mila nuove diagnosi per tumore
Indicatori sulla terapia di oncologia medica
 Indicatori sulla terapia di oncologia medica Michela Donadio Oncologia Medica Senologica Azienda Ospedaliera Città della Salute e della Scienza di Torino Torino, 2 dicembre 20 Terapie mediche neoad/adiuvanti:
Indicatori sulla terapia di oncologia medica Michela Donadio Oncologia Medica Senologica Azienda Ospedaliera Città della Salute e della Scienza di Torino Torino, 2 dicembre 20 Terapie mediche neoad/adiuvanti:
Neoplasie della mammella - 2
 Neoplasie della mammella - 2 Fattori prognostici Numero di N+ : >3 Età e stato menopausale Diametro di T Invasione linfatica e vascolare Tipo istologico Grading Recettore per Estrogeni/Progesterone Amplificazione
Neoplasie della mammella - 2 Fattori prognostici Numero di N+ : >3 Età e stato menopausale Diametro di T Invasione linfatica e vascolare Tipo istologico Grading Recettore per Estrogeni/Progesterone Amplificazione
MINI SCHEDA HTA BEVACIZUMAB (AVASTIN ) INDICAZIONE CARCINOMA OVARICO
 1/7 MINI SCHEDA HTA BEVACIZUMAB (AVASTIN ) INDICAZIONE CARCINOMA OVARICO Nome Commerciale Avastin Principio Attivo Bevacizumab Ditta Produttrice Roche ATC L01XC07 Formulazione Concentrato per soluzione
1/7 MINI SCHEDA HTA BEVACIZUMAB (AVASTIN ) INDICAZIONE CARCINOMA OVARICO Nome Commerciale Avastin Principio Attivo Bevacizumab Ditta Produttrice Roche ATC L01XC07 Formulazione Concentrato per soluzione
LA CHEMIOTERAPIA ORALE IN ASSOCIAZIONE ALLA RADIOTERAPIA
 LA CHEMIOTERAPIA ORALE IN ASSOCIAZIONE ALLA RADIOTERAPIA G.Lazzari, G. Silvano S. C. Radioterapia Oncologica ASL TA/ 1 - Taranto Taranto, 21 gennaio 2005 BACKGROUND Le formulazioni orali di chemioterapia
LA CHEMIOTERAPIA ORALE IN ASSOCIAZIONE ALLA RADIOTERAPIA G.Lazzari, G. Silvano S. C. Radioterapia Oncologica ASL TA/ 1 - Taranto Taranto, 21 gennaio 2005 BACKGROUND Le formulazioni orali di chemioterapia
Anita Andreano e Antonio Russo
 DEFINIZIONE DI UN SET DI INDICATORI DEL PROCESSO DI DIAGNOSI E CURA DEL TUMORE POLMONARE TRAMITE METODO DELPHI-MODIFICATO E PRESENTAZIONE DEGLI INDICATORI CALCOLATI SULLA POPOLAZIONE DI DUE ASL DELLA PROVINCIA
DEFINIZIONE DI UN SET DI INDICATORI DEL PROCESSO DI DIAGNOSI E CURA DEL TUMORE POLMONARE TRAMITE METODO DELPHI-MODIFICATO E PRESENTAZIONE DEGLI INDICATORI CALCOLATI SULLA POPOLAZIONE DI DUE ASL DELLA PROVINCIA
 Indicatori di qualità nei carcinomi genitali femminili: ovaio e utero Serata di presentazione progetto Zonta Club Locarno 13.04.2010 Registro Tumori Canton Ticino Istituto Cantonale di Patologia Via in
Indicatori di qualità nei carcinomi genitali femminili: ovaio e utero Serata di presentazione progetto Zonta Club Locarno 13.04.2010 Registro Tumori Canton Ticino Istituto Cantonale di Patologia Via in
Etica nella ricerca nelle cure oncologiche. Ufficio di Sanità Comitato Etico cantonale
 Etica nella ricerca nelle cure oncologiche Ufficio di Sanità Comitato Etico cantonale Ricerca clinica e etica Autonomia Beneficienza Giustizia Informazione Consenso Volontarietà Libertà d interruzione
Etica nella ricerca nelle cure oncologiche Ufficio di Sanità Comitato Etico cantonale Ricerca clinica e etica Autonomia Beneficienza Giustizia Informazione Consenso Volontarietà Libertà d interruzione
Scritto da Giovanni Creton Domenica 27 Febbraio 2011 17:32 - Ultimo aggiornamento Domenica 27 Marzo 2011 19:43
 E evidente che lo screening per un tumore può diagnosticare la malattia molto precocemente, ma nel caso del tumore alla prostata il ricorso al test del PSA può creare dati incerti e rischi sanitari in
E evidente che lo screening per un tumore può diagnosticare la malattia molto precocemente, ma nel caso del tumore alla prostata il ricorso al test del PSA può creare dati incerti e rischi sanitari in
Algoritmi e percorsi terapeutici dei Carcinomi del Polmone
 Algoritmi e percorsi terapeutici dei Carcinomi del Polmone Standard Individualizzata Sperimentale Stadio Ia/Ib T1-2a N0 M0 radicale) CHIR con resezione sub-lobare, solo stadio Ib CHIR con VATS campionamento
Algoritmi e percorsi terapeutici dei Carcinomi del Polmone Standard Individualizzata Sperimentale Stadio Ia/Ib T1-2a N0 M0 radicale) CHIR con resezione sub-lobare, solo stadio Ib CHIR con VATS campionamento
Lo sviluppo del cancro è un processo complesso che coinvolge parecchi cambiamenti nella stessa cellula staminale. Poiché tutte le cellule staminali
 Tumore Cos è il tumore? Il tumore o neoplasia (dal greco neo,, nuovo, e plasìa,, formazione), o cancro se è maligno, è una classe di malattie caratterizzate da una incontrollata riproduzione di alcune
Tumore Cos è il tumore? Il tumore o neoplasia (dal greco neo,, nuovo, e plasìa,, formazione), o cancro se è maligno, è una classe di malattie caratterizzate da una incontrollata riproduzione di alcune
Commissione Regionale Farmaco LAPATINIB
 Commissione Regionale Farmaco (D.G.R. 1540/2006 e D.G.R. 490 dell 11 aprile 2011) Documento relativo a: LAPATINIB Settembre 2011 Indicazioni registrate Lapatinib Il lapatinib ha ricevuto la seguente estensione
Commissione Regionale Farmaco (D.G.R. 1540/2006 e D.G.R. 490 dell 11 aprile 2011) Documento relativo a: LAPATINIB Settembre 2011 Indicazioni registrate Lapatinib Il lapatinib ha ricevuto la seguente estensione
A.A. 2015/2016. Statistica Medica. Corso di. CdL in Fisioterapia CdL in Podologia
 A.A. 2015/2016 Corso di Statistica Medica CdL in Fisioterapia CdL in Podologia La statistica è la scienza che ha come fine lo studio quantitativo e qualitativo di un "collettivo". Studia i modi in cui
A.A. 2015/2016 Corso di Statistica Medica CdL in Fisioterapia CdL in Podologia La statistica è la scienza che ha come fine lo studio quantitativo e qualitativo di un "collettivo". Studia i modi in cui
Shift work and chronic disease: the epidemiological evidence
 Shift work and chronic disease: the epidemiological evidence X-S. Wang, M. E. G. Armstrong, B. J. Cairns, T. J. Key and R. C. Travis Cancer Epidemiology Unit, University of Oxford, Oxford, UK. Occupational
Shift work and chronic disease: the epidemiological evidence X-S. Wang, M. E. G. Armstrong, B. J. Cairns, T. J. Key and R. C. Travis Cancer Epidemiology Unit, University of Oxford, Oxford, UK. Occupational
Nivolumab nel trattamento della seconda linea del tumore polmonare non a piccole cellule a istologia squamosa
 634 Rassegne Recenti Prog Med 2016; 107: 634-640 Nivolumab nel trattamento della seconda linea del tumore polmonare non a piccole cellule a istologia squamosa FILIPPO DE MARINIS 1, ANTONIO PASSARO 1 1
634 Rassegne Recenti Prog Med 2016; 107: 634-640 Nivolumab nel trattamento della seconda linea del tumore polmonare non a piccole cellule a istologia squamosa FILIPPO DE MARINIS 1, ANTONIO PASSARO 1 1
SCHEDA FARMACO. (a cura di UOS Farmacoeconomia e HTA, Area Centro)
 SCHEDA FARMACO (a cura di UOS Farmacoeconomia e HTA, Area Centro) Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta Dabrafenib (Tafinlar)
SCHEDA FARMACO (a cura di UOS Farmacoeconomia e HTA, Area Centro) Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta Dabrafenib (Tafinlar)
Comparabilità fra le somministrazioni successive effetto di trascinamento ( carry-over ) effetto di periodo
 Metodo epidemiologici per la clinica _efficacia / 2 Gli studi crossover Periodo 1 Periodo 2 R A N D O M A B A B Valutazione Tempo 1 0 1 1 2 0 2 1 Gli studi crossover Metodo epidemiologici per la clinica
Metodo epidemiologici per la clinica _efficacia / 2 Gli studi crossover Periodo 1 Periodo 2 R A N D O M A B A B Valutazione Tempo 1 0 1 1 2 0 2 1 Gli studi crossover Metodo epidemiologici per la clinica
FOLLOW-UP DEL TUMORE POLMONARE
 Linee Guida ITT Istituto Toscano Tumori ORDINE DEI MEDICI CHIRURGHI e degli ODONTOIATRI della PROVINCIA di AREZZO 3 gennaio 2007 Ivano Archinucci UO di Pneumologia ASL 8 STADI DEL CARCINOMA POMONARE STADIO
Linee Guida ITT Istituto Toscano Tumori ORDINE DEI MEDICI CHIRURGHI e degli ODONTOIATRI della PROVINCIA di AREZZO 3 gennaio 2007 Ivano Archinucci UO di Pneumologia ASL 8 STADI DEL CARCINOMA POMONARE STADIO
CAPITOLO 1 indice. Tumore della mammella pag. 27 Tumore della cervice uterina pag. 30 Melanoma pag. 31 Linfomi pag. 31. bibliografia pag.
 CAPITOLO 1 indice le neoplasie nell anziano pag. 5 Valutazione del paziente anziano pag. 7 Aspetti generali del trattamento pag. 10 Tumori del colon-retto pag. 11 Tumori della mammella pag. 13 Tumori del
CAPITOLO 1 indice le neoplasie nell anziano pag. 5 Valutazione del paziente anziano pag. 7 Aspetti generali del trattamento pag. 10 Tumori del colon-retto pag. 11 Tumori della mammella pag. 13 Tumori del
Scritto da RyderItalia Mercoledì 12 Maggio 2010 11:19 - Ultimo aggiornamento Mercoledì 03 Novembre 2010 15:57
 LA TERAPIA METRONOMICA Per oltre mezzo secolo, la terapia sistemica per i tumori è stata caratterizzata dalla somministrazione dei farmaci chemioterapici. La maggior parte di questi farmaci ha lo scopo
LA TERAPIA METRONOMICA Per oltre mezzo secolo, la terapia sistemica per i tumori è stata caratterizzata dalla somministrazione dei farmaci chemioterapici. La maggior parte di questi farmaci ha lo scopo
RIASSUNTO DEL PROTOCOLLO DI SPERIMENTAZIONE CLINICA P.R.O.S.E.
 RIASSUNTO DEL PROTOCOLLO DI SPERIMENTAZIONE CLINICA P.R.O.S.E. pag 1 di 4 Randomized Proteomic Stratified Phase III Study of Second Line Erlotinib versus Chemotherapy in Patients with Inoperable Non Small
RIASSUNTO DEL PROTOCOLLO DI SPERIMENTAZIONE CLINICA P.R.O.S.E. pag 1 di 4 Randomized Proteomic Stratified Phase III Study of Second Line Erlotinib versus Chemotherapy in Patients with Inoperable Non Small
TAILOR AIFA TArceva Italian Lung Optimization trial
 H TAILR AIFA TArceva Italian Lung ptimization trial ttimizzazione dell erlotinib per il trattamento di pazienti con tumore del polmone avanzato non a piccole cellule: uno studio italiano randomizzato SISSI
H TAILR AIFA TArceva Italian Lung ptimization trial ttimizzazione dell erlotinib per il trattamento di pazienti con tumore del polmone avanzato non a piccole cellule: uno studio italiano randomizzato SISSI
MH e imaging cerebrale
 Novità dalla ricerca sulla Malattia di Huntington In un linguaggio semplice. Scritto da ricercatori. Per la comunità mondiale MH. La MH fa si che il cervello si sviluppi in modo diverso Volumi cerebrali
Novità dalla ricerca sulla Malattia di Huntington In un linguaggio semplice. Scritto da ricercatori. Per la comunità mondiale MH. La MH fa si che il cervello si sviluppi in modo diverso Volumi cerebrali
Comunicare l innovazione in oncologia Le basi scientifiche
 Comunicare l innovazione in oncologia Le basi scientifiche Massimo Di Maio SCDU Oncologia, AO Ordine Mauriziano Dipartimento di Oncologia Università degli Studi di Torino massimo.dimaio@unito.it «Appello»
Comunicare l innovazione in oncologia Le basi scientifiche Massimo Di Maio SCDU Oncologia, AO Ordine Mauriziano Dipartimento di Oncologia Università degli Studi di Torino massimo.dimaio@unito.it «Appello»
Domande relative alla specializzazione in: Oncologia medica
 Domande relative alla specializzazione in: Oncologia medica Domanda #1 (codice domanda: n.541) : Cosa caratterizza il grado T2 del colangiocarcinoma? A: Interessamento del connettivo periduttale B: Coinvolgimento
Domande relative alla specializzazione in: Oncologia medica Domanda #1 (codice domanda: n.541) : Cosa caratterizza il grado T2 del colangiocarcinoma? A: Interessamento del connettivo periduttale B: Coinvolgimento
Ruolo prognostico della dual-point 18F-Etil-Tirosina PET/CT cerebrale nella valutazione della sospetta recidiva di glioma cerebrale
 Ruolo prognostico della dual-point 18F-Etil-Tirosina PET/CT cerebrale nella valutazione della sospetta recidiva di glioma cerebrale E.Borsatti, L.Bolidi, T.Baresic, R.Tatta, D.Monte, E.Bidoli*, M.Arcicasa
Ruolo prognostico della dual-point 18F-Etil-Tirosina PET/CT cerebrale nella valutazione della sospetta recidiva di glioma cerebrale E.Borsatti, L.Bolidi, T.Baresic, R.Tatta, D.Monte, E.Bidoli*, M.Arcicasa
Fattori predittivi di risposta all immunoterapia nel carcinoma mammario
 Fattori predittivi di risposta all immunoterapia nel carcinoma mammario Bogina Giuseppe Ospedale Sacro Cuore Negrar giuseppe.bogina@sacrocuore.it IMMUNOTERAPIA E CANCRO Testa-Collo Vescica Rene Melanoma
Fattori predittivi di risposta all immunoterapia nel carcinoma mammario Bogina Giuseppe Ospedale Sacro Cuore Negrar giuseppe.bogina@sacrocuore.it IMMUNOTERAPIA E CANCRO Testa-Collo Vescica Rene Melanoma
REGOLAMENTO DEL COMITATO PRODUZIONE E RICERCA SCIENTIFICA SIAARTI
 REGOLAMENTO DEL COMITATO PRODUZIONE E RICERCA SCIENTIFICA SIAARTI Il Comitato Produzione e Ricerca Scientifica (CPRS) svolge le seguenti funzioni: 1. Stabilisce la metodologia per la produzione di linee
REGOLAMENTO DEL COMITATO PRODUZIONE E RICERCA SCIENTIFICA SIAARTI Il Comitato Produzione e Ricerca Scientifica (CPRS) svolge le seguenti funzioni: 1. Stabilisce la metodologia per la produzione di linee
LA RETE ONCOLOGICA DEL PIEMONTE E VALLE D AOSTA NOVITA E CONTROVERSIE ASCO 2015 TUMORI TESTA-COLLO
 LA RETE ONCOLOGICA DEL PIEMONTE E VALLE D AOSTA NOVITA E CONTROVERSIE ASCO 2015 TUMORI TESTA-COLLO Dott.ssa Marina Schena SC Oncologia Medica I AOU Città della Salute e della Scienza di Torino Head and
LA RETE ONCOLOGICA DEL PIEMONTE E VALLE D AOSTA NOVITA E CONTROVERSIE ASCO 2015 TUMORI TESTA-COLLO Dott.ssa Marina Schena SC Oncologia Medica I AOU Città della Salute e della Scienza di Torino Head and
Stefania Corso 17 ANNI. Una lotta durata una vita
 Stefania Corso 17 ANNI Una lotta durata una vita Stefania Corso, 17 anni Copyright 2015 Edizioni del Faro Gruppo Editoriale Tangram Srl Via Verdi, 9/A 38122 Trento www.edizionidelfaro.it info@edizionidelfaro.it
Stefania Corso 17 ANNI Una lotta durata una vita Stefania Corso, 17 anni Copyright 2015 Edizioni del Faro Gruppo Editoriale Tangram Srl Via Verdi, 9/A 38122 Trento www.edizionidelfaro.it info@edizionidelfaro.it
Tumori polmonari non a piccole cellule con istotipo non squamoso. Nuove prospettive nel trattamento di seconda linea
 641 Recenti Prog Med 2016; 107: 641-646 Tumori polmonari non a piccole cellule con istotipo non squamoso. Nuove prospettive nel trattamento di seconda linea FRANCESCO GROSSI UOS Tumori Polmonari, IRCCS
641 Recenti Prog Med 2016; 107: 641-646 Tumori polmonari non a piccole cellule con istotipo non squamoso. Nuove prospettive nel trattamento di seconda linea FRANCESCO GROSSI UOS Tumori Polmonari, IRCCS
Terapia di II^ linea in pazienti «non oncogene addicted»
 Proposta di PDTA della Rete Oncologica Veneta per i pazienti affetti da tumore del polmone non oncogene addicted. Terapia di II^ linea in pazienti «non oncogene addicted» Dr. Antonio Santo (Responsabile
Proposta di PDTA della Rete Oncologica Veneta per i pazienti affetti da tumore del polmone non oncogene addicted. Terapia di II^ linea in pazienti «non oncogene addicted» Dr. Antonio Santo (Responsabile
LINEE GUIDA ROL - COLON. Stadio I
 Adenoma con displasia alto grado o severa Escissione locale LINEE GUIDA ROL - COLON segmentaria per lesioni non suscettibili di escissione locale Sostituisce carcinoma in situ o adenoma intramucoso. Stadio
Adenoma con displasia alto grado o severa Escissione locale LINEE GUIDA ROL - COLON segmentaria per lesioni non suscettibili di escissione locale Sostituisce carcinoma in situ o adenoma intramucoso. Stadio
Dott. Elena Niccolai, PhD. Dipartimento di Medicina Sperimentale e Clinica Università degli Studi di Firenze
 Dott. Elena Niccolai, PhD Dipartimento di Medicina Sperimentale e Clinica Università degli Studi di Firenze Premio Gianfranco Del Prete per le malattie orfane, Firenze 8 novembre 2014 ADENOCARCINOMA PANCREATICO
Dott. Elena Niccolai, PhD Dipartimento di Medicina Sperimentale e Clinica Università degli Studi di Firenze Premio Gianfranco Del Prete per le malattie orfane, Firenze 8 novembre 2014 ADENOCARCINOMA PANCREATICO
Il futuro della normazione tecnica tra legislazione, condivisione e mercato. Gian Luca Salerio Responsabile Area Normazione UNI
 Il futuro della normazione tecnica tra legislazione, condivisione e mercato Gian Luca Salerio Responsabile Area Normazione UNI Il settore dei dispositivi medici e più in generale della medicina è in forte
Il futuro della normazione tecnica tra legislazione, condivisione e mercato Gian Luca Salerio Responsabile Area Normazione UNI Il settore dei dispositivi medici e più in generale della medicina è in forte
IL MEDICO DI MEDICINA GENERALE E LA NEFROPATIA DIABETICA: studio sui comportamenti prescrittivi diagnosticoterapeutici di un gruppo di medici genovesi
 Università degli Studi di Genova Facoltà di Medicina e Chirurgia IL MEDICO DI MEDICINA GENERALE E LA NEFROPATIA DIABETICA: studio sui comportamenti prescrittivi diagnosticoterapeutici di un gruppo di medici
Università degli Studi di Genova Facoltà di Medicina e Chirurgia IL MEDICO DI MEDICINA GENERALE E LA NEFROPATIA DIABETICA: studio sui comportamenti prescrittivi diagnosticoterapeutici di un gruppo di medici
