Corso di Studi di Fisica Corso di Chimica
|
|
|
- Gilda Pesce
- 4 anni fa
- Visualizzazioni
Transcript
1 Corso di Studi di Fisica Corso di Chimica Luigi Cerruti Lezione
2 Solubilità Diapositiva della prof. Nadia Lotti
3 Solubilità Stabilite le condizioni di equilibrio di una soluzione satura (equilibrio dinamico tra sale indisciolto e sale in soluzione) la concentrazione del sale, che è la massima a quella temperatura, è definita solubilità del sale AgCl (s) + aq Ag + (aq) + Cl - (aq) Si tratta di un equilibrio eterogeneo
4 Solubilità dei sali Sale solubile: concentrazione minima in soluzione 0,1 mol L -1, a temperatura ambiente Sale insolubile: concentrazione minima in soluzione 0,001 mol L -1, a temperatura ambiente I composti ionici coprono un'ampia gamma di solubilità: a un'estremità sta il clorato di litio (LiClO 3 ), che si scioglie fino a 35 moli (3200 g) per litro a 25 C; il solfuro di mercurio(ii) (HgS) è all'estremo opposto, avendo una solubilità a 25 C di mol L-1 Questo significa che 200 litri di soluzione di HgS sono richiesti per contenere un singolo paio di ioni Hg 2+ e S 2-
5 Questioni di solubilità Dipendenza dal solvente. "Il simile scioglie il simile". Benzene e tetracloroetilene sono ottimi solventi per i composti apolari (per esempio, i grassi), e infatti sono usati in lavanderia nel cosiddetto lavaggio a secco; L'acqua è un ottimo solvente per composti ionici e polari. Viceversa lo zucchero o il sale non si sciolgono nel benzene o in olio d'oliva, né la cera si scioglie in acqua. La ragione di questa selettività per i solventi è che, se le forze intermolecolari che agiscono nella soluzione e nel solido sono simili, l'energia che le molecole del soluto hanno in soluzione risulta analoga a quella che possedevano nel solido originale. In caso contrario, il solido tende a mantenere la coesione originaria, in quanto termodinamicamente più favorevole.
6 Preparazione in laboratorio di una soluzione 0,01M di di KMnO 4 0,0025 moli (0,395 g) in 250 ml di acqua Diapositiva della prof. Nadia Lotti
7 Solubilità e temperatura /pubblica/curve_di_solubilit.pdf
8 50 g miscela solida 80% Gly, 20% Ala Gly 40 g, Ala 10 g. sciolte in 100 g acqua Separazione per cristallizzazione Glicina (Gly; (NH 2 )-CH 2 -COOH) ed alanina (Ala; (NH 2 )-CH 2 -CH 2 -COOH) sono due amminoacidi la cui solubilità aumenta con la temperatura secondo i valori riportati in Tabella 1. Il grafico a fianco della Tabella rappresenta come varia la solubilità dei due amminoacidi al variare della temperatura. /pubblica/curve_di_solubilit.pdf
9 Prodotto di solubilità (K ps ) Nelle condizioni di equilibrio della soluzione di un sale poco solubile, l equazione di dissoluzione è: M m X n(solido) mm u+ + nx v- La costante relativa a questo equilibrio è indicata con K ps ed è data da: K ps = [M u+ ] m [X v- ] n La costante è indipendente dalla quantità della fase solida purché essa sia presente Diapositiva della prof. Nadia Lotti
10 Un esercizio: sapendo che K ps del Fe(OH) 2 è 1.6 x 10-14, calcolarne la solubilità espressa in g dm -3 Fe(OH) 2 Fe OH - K ps = [Fe 2+ ] [OH - ] 2 Se x è la concentrazione degli ioni Fe 2+ in soluzione, quella degli ioni OH - risulterà 2x, quindi posso scrivere: K ps = [Fe 2+ ] [ OH - ] 2 = x(2x) 2 = 1.6 x x = 1.6 x 10-5 mol L -1 la solubilità risulterà: 1.6 x 10-5 x 89.87g mol -1 = 1.438x10-3 g dm -3 Diapositiva della prof. Nadia Lotti
11 Un esercizio: Sapendo che la solubilità del CaCO 3 è 9.0 x 10-5 mol/l, determinare il prodotto di solubilità CaCO 3 Ca 2+ + CO 3 2- K ps = [Ca 2+ ] [CO 3 2- ] Dato che da ogni mole di CaCO 3 che si dissocia si formano una mole di ioni Ca 2+ ed una di ioni CO 3 2- avrò: K ps ps = [Ca 2+ ] [CO 2-3 ] = ( ) 2 = Diapositiva della prof. Nadia Lotti
12 Un esercizio: la Kps di Mg(OH) 2 è 1.2 x Calcolare il ph di una soluzione satura di Mg (OH) 2. Mg(OH) 2 Mg OH - K ps = [Mg 2+ ] [OH - ] 2 Per ogni molecola di sostanza disciolta si formano uno ione Mg 2+ e due ioni OH -. Se x è la [OH - ] nella soluzione satura di idrossido di magnesio posso scrivere: K ps ps = (x/2) x 2 = x= mol dm -3 e poh=3.54 ph=10.46 Diapositiva della prof. Nadia Lotti
13 Solubilità dei sali Sono sempre solubili sali di: metalli alcalini e ione NH 4 + nitrati perclorati e acetati Sono per lo più solubili sali di: cloruri, bromuri e ioduri tranne quelli di Ag + e Pb 2+ solfati tranne quelli di Ca 2+, Sr 2+, Ba 2+ e Pb 2+ Sono per lo più insolubili sali di: solfuri e idrossidi tranne che dei gruppi I-II e NH 4 + carbonati e fosfati tranne che del gruppo I e NH 4 +
Solubilità dei sali Prodotto di solubilità
 Solubilità dei sali Prodotto di solubilità Aggiunta di una soluzione di NaCl ad una di AgNO 3 : formazione di un precipitato -AgCl- Solubilità Stabilite le condizioni di equilibrio di una soluzione satura
Solubilità dei sali Prodotto di solubilità Aggiunta di una soluzione di NaCl ad una di AgNO 3 : formazione di un precipitato -AgCl- Solubilità Stabilite le condizioni di equilibrio di una soluzione satura
Solubilità dei sali Prodotto di solubilità
 Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Chimica A.A. 2017/2018
 Chimica A.A. 2017/2018 INGEGNERIA BIOMEDICA Tutorato Lezione 9 Calcolare la solubilità molare del solfato di bario in una soluzione 0.020 M di solfato di sodio. Il prodotto di solubilità del solfato di
Chimica A.A. 2017/2018 INGEGNERIA BIOMEDICA Tutorato Lezione 9 Calcolare la solubilità molare del solfato di bario in una soluzione 0.020 M di solfato di sodio. Il prodotto di solubilità del solfato di
Prodotto di solubilità ed Effetto dello ione comune
 Prodotto di solubilità ed Effetto dello ione comune Dr. Gabriella Giulia Pulcini Ph.D. Student, Development of new approaches to teaching and learning Natural and Environmental Sciences University of Camerino,
Prodotto di solubilità ed Effetto dello ione comune Dr. Gabriella Giulia Pulcini Ph.D. Student, Development of new approaches to teaching and learning Natural and Environmental Sciences University of Camerino,
Solubilità dei sali Prodotto di solubilità
 Solubilità dei sali Prodotto di solubilità Aggiunta di una soluzione di NaCl ad una di AgNO 3 : formazione di un precipitato -AgCl- Solubilità Stabilite le condizioni di equilibrio di una soluzione satura
Solubilità dei sali Prodotto di solubilità Aggiunta di una soluzione di NaCl ad una di AgNO 3 : formazione di un precipitato -AgCl- Solubilità Stabilite le condizioni di equilibrio di una soluzione satura
EQUILIBRI IN SOLUZIONI SATURE DI SALI POCO SOLUBILI. K eq = Ba 2+ SO 4 EQUILIBRIO CHIMICO. A a B b. Equilibri eterogenei: Equilibri omogenei:
 EQUILIBRIO CHIMICO aa + bb cc + dd K eq = C c D d A a B b K eq è una costante che dipende esclusivamente dalla natura delle specie all equilibrio e dalla temperatura Equilibri omogenei: Tutte le specie
EQUILIBRIO CHIMICO aa + bb cc + dd K eq = C c D d A a B b K eq è una costante che dipende esclusivamente dalla natura delle specie all equilibrio e dalla temperatura Equilibri omogenei: Tutte le specie
Prodotto di solubilità (Kps)
 Prodotto di solubilità (Kps) SOLUBILITA Concentrazione massima che si può raggiungere per un soluto in un dato solvente ad una certa temperatura. (Es: g soluto/100g di solvente) Solubiltà di NaCl in acqua
Prodotto di solubilità (Kps) SOLUBILITA Concentrazione massima che si può raggiungere per un soluto in un dato solvente ad una certa temperatura. (Es: g soluto/100g di solvente) Solubiltà di NaCl in acqua
Solubilità. Il fatto che un composto sia un elettrolita forte (cioè si dissoci completamente in acqua) non deve essere confuso con la sua solubilità.
 Solubilità Il fatto che un composto sia un elettrolita forte (cioè si dissoci completamente in acqua) non deve essere confuso con la sua solubilità. La solubilità di un composto in acqua è definita come
Solubilità Il fatto che un composto sia un elettrolita forte (cioè si dissoci completamente in acqua) non deve essere confuso con la sua solubilità. La solubilità di un composto in acqua è definita come
Dissoluzione dei Solidi
 Dissoluzione dei Solidi La capacità di un solvente di sciogliere un certo soluto non è illimitata Un solido si scioglie tanto più in un solvente quanto più gli è affine chimicamente; questo significa che
Dissoluzione dei Solidi La capacità di un solvente di sciogliere un certo soluto non è illimitata Un solido si scioglie tanto più in un solvente quanto più gli è affine chimicamente; questo significa che
Avvisi. Totale: 14 CFU. Il voto finale sarà la media pesata fra: 1. Voto di Chimica Generale ed Inorganica (6/14) 2. Voto di Chimica Organica (8/14)
 Avvisi Chimica (Corso Integrato): Chimica Generale ed Inorganica (6 CFU) Dott. Francesco Musiani Chimica Organica (8 CFU) Modulo 1 (teoria): Prof. Luca Gentilucci Modulo 2 (laboratorio): Dott. Andrea Gualandi
Avvisi Chimica (Corso Integrato): Chimica Generale ed Inorganica (6 CFU) Dott. Francesco Musiani Chimica Organica (8 CFU) Modulo 1 (teoria): Prof. Luca Gentilucci Modulo 2 (laboratorio): Dott. Andrea Gualandi
Chimica Generale. Reazioni Chimiche. Reazioni Chimiche
 Una reazione chimica è un processo in cui avviene un cambiamento chimico di uno o più composti, detti reagenti, che vengono convertiti in una nuova serie di composti detti prodotti. Spesso le reazioni
Una reazione chimica è un processo in cui avviene un cambiamento chimico di uno o più composti, detti reagenti, che vengono convertiti in una nuova serie di composti detti prodotti. Spesso le reazioni
Calcoli stechiometrici in soluzione (Cap. 12)
 Calcoli stechiometrici in soluzione (Cap. 12) Le soluzioni Molarità Gli elettroliti Reazioni in soluzione Reazioni di precipitazione Titolazioni acido-base Le soluzioni Una soluzione è una miscela omogenea
Calcoli stechiometrici in soluzione (Cap. 12) Le soluzioni Molarità Gli elettroliti Reazioni in soluzione Reazioni di precipitazione Titolazioni acido-base Le soluzioni Una soluzione è una miscela omogenea
specie chimiche. in quantità maggiore presente nella soluzione, e tutti gli altri componenti che sono detti soluti. Un componente di una soluzione
 Equilibri di solubilità 1 1 Si definisce SOLUZIONE una miscela omogenea di due o più specie chimiche. In una soluzione si distinguono un solvente, che è il componente in quantità maggiore presente nella
Equilibri di solubilità 1 1 Si definisce SOLUZIONE una miscela omogenea di due o più specie chimiche. In una soluzione si distinguono un solvente, che è il componente in quantità maggiore presente nella
EQUILIBRI DI SOLUBILITA
 EQUILIBRI DI SOLUBILITA Solubilità In generale solo una quantità finita di un solido si scioglie in un dato volume di solvente dando luogo ad una soluzione satura, cioè una soluzione in equilibrio con
EQUILIBRI DI SOLUBILITA Solubilità In generale solo una quantità finita di un solido si scioglie in un dato volume di solvente dando luogo ad una soluzione satura, cioè una soluzione in equilibrio con
EQUILIBRI DI SOLUBILITÀ DI COMPOSTI IONICI POCO SOLUBILI
 EQUILIBRI DI SOLUBILITÀ DI COMPOSTI IONICI POCO SOLUBILI Quando abbiamo a che fare con dei composti ionici molto solubili, per raggiungere la saturazione 1 della soluzione è necessario aggiungere all'acqua
EQUILIBRI DI SOLUBILITÀ DI COMPOSTI IONICI POCO SOLUBILI Quando abbiamo a che fare con dei composti ionici molto solubili, per raggiungere la saturazione 1 della soluzione è necessario aggiungere all'acqua
Evento Crui: il 21 marzo «primavera» delle università italiane
 Evento Crui: il 21 marzo «primavera» delle università italiane Su iniziativa della CRUI, il prossimo 21 marzo in ogni sede Universitaria nazionale si terranno incontri e dibattiti pubblici per sensibilizzare
Evento Crui: il 21 marzo «primavera» delle università italiane Su iniziativa della CRUI, il prossimo 21 marzo in ogni sede Universitaria nazionale si terranno incontri e dibattiti pubblici per sensibilizzare
Soluzioni. Miscele: (gas in gas) Leghe: (solidi in solidi) Soluzioni p.d: (solventi liquidi)
 Soluzioni Sono miscele omogenee in cui si riconoscono 2 componenti o fasi: il soluto, presente in quantità minore il solvente presente in quantità maggiore. Tipi di soluzioni: Miscele: (gas in gas) Leghe:
Soluzioni Sono miscele omogenee in cui si riconoscono 2 componenti o fasi: il soluto, presente in quantità minore il solvente presente in quantità maggiore. Tipi di soluzioni: Miscele: (gas in gas) Leghe:
18.4 Equilibri di solubilità
 Problemi risolti 18. Equilibri di solubilità A) Quanti ml di una soluzione 5. 10 M di acido solforico è necessario aggiungere a 50 ml di una soluzione 3,. 10 M di CaCl affinchè inizi a precipitare CaSO
Problemi risolti 18. Equilibri di solubilità A) Quanti ml di una soluzione 5. 10 M di acido solforico è necessario aggiungere a 50 ml di una soluzione 3,. 10 M di CaCl affinchè inizi a precipitare CaSO
24. PRECIPITAZIONE Prodotto di solubilità (K s )
 24. PRECIPITAZIONE D. In un racconto di Primo Levi, a proposito di un analisi chimica di campioni di roccia, si incontrano queste parole apparentemente prive di senso: «... giù il ferro con ammoniaca,
24. PRECIPITAZIONE D. In un racconto di Primo Levi, a proposito di un analisi chimica di campioni di roccia, si incontrano queste parole apparentemente prive di senso: «... giù il ferro con ammoniaca,
LE SOLUZIONI Soluzione: sistema omogeneo di due o più componenti
 LE SOLUZIONI Soluzione: sistema omogeneo di due o più componenti Il processo di solubilizzazione è una trasformazione fisica, pertanto le proprietà chimiche dei componenti si conservano Le soluzioni possono
LE SOLUZIONI Soluzione: sistema omogeneo di due o più componenti Il processo di solubilizzazione è una trasformazione fisica, pertanto le proprietà chimiche dei componenti si conservano Le soluzioni possono
EQUILIBRI DI SOLUBILITA
 EQUILIBRI DI SOLUBILITA Molti composti ionici sono poco solubili. In soluzione, inizialmente si sciolgono (a), fino a raggiungere un equilibrio dinamico tra ioni che passano in soluzione e ioni che cristallizzano
EQUILIBRI DI SOLUBILITA Molti composti ionici sono poco solubili. In soluzione, inizialmente si sciolgono (a), fino a raggiungere un equilibrio dinamico tra ioni che passano in soluzione e ioni che cristallizzano
Analizziamo i casi più frequenti. Acido forte Base forte Acido debole Base debole Idrolisi Tampone
 Lezione 17 1. Acidi e basi deboli 2. Relazione tra a e b 3. ph di acidi e basi deboli (esempi) 4. Idrolisi salina acida e basica 5. Soluzioni tampone 6. Equilibrio eterogeneo 7. Idrolisi salina acida e
Lezione 17 1. Acidi e basi deboli 2. Relazione tra a e b 3. ph di acidi e basi deboli (esempi) 4. Idrolisi salina acida e basica 5. Soluzioni tampone 6. Equilibrio eterogeneo 7. Idrolisi salina acida e
TUTORAGGIO CHIMICA A.A. 2018/2019 Tutoraggio Chimica (Prof. L. Pilia) Nicola Melis
 TUTORAGGIO CHIMICA 18.12.2018 1 Es. 1: Il fluoruro di calcio si discioglie in piccole quantità in acqua. Calcolare il valore di K ps sapendo che [Ca 2+ ] = 2,3*10-4 CaF 2 (s) Ca 2+ (aq) + 2 F - (aq) Es.
TUTORAGGIO CHIMICA 18.12.2018 1 Es. 1: Il fluoruro di calcio si discioglie in piccole quantità in acqua. Calcolare il valore di K ps sapendo che [Ca 2+ ] = 2,3*10-4 CaF 2 (s) Ca 2+ (aq) + 2 F - (aq) Es.
SOLUZIONE DEL COMPITO A DI CHIMICA DEL
 SOLUZIONE DEL COMPITO A DI CHIMICA DEL 05-07-13 1A) 33.5 g di ioduro di sodio e 33.0 g di iodio vengono sciolti in acqua trattati con 17.9 L (a c.n.) di cloro; si formano iodato di sodio, acido iodico
SOLUZIONE DEL COMPITO A DI CHIMICA DEL 05-07-13 1A) 33.5 g di ioduro di sodio e 33.0 g di iodio vengono sciolti in acqua trattati con 17.9 L (a c.n.) di cloro; si formano iodato di sodio, acido iodico
Le soluzioni possono esistere in ognuno dei tre stati della materia: gas, liquido o solido.
 SOLUZIONI Una soluzione èuna miscela omogenea (=la sua composizione e le sue proprietà sono uniformi in ogni parte del campione) di due o più sostanze formate da ioni o molecole. Differenza con i colloidi
SOLUZIONI Una soluzione èuna miscela omogenea (=la sua composizione e le sue proprietà sono uniformi in ogni parte del campione) di due o più sostanze formate da ioni o molecole. Differenza con i colloidi
Esame (0) - solubilità dei composti e reaz - Codice Prova:
 1) Ci si aspetta la formazione di un precipitato quando una soluzione acquosa di ioduro di potassio è aggiunta ad una soluzione acquosa di: A. idrossido di bario B. perclorato di piombo C. cloruro di ferro(ii)
1) Ci si aspetta la formazione di un precipitato quando una soluzione acquosa di ioduro di potassio è aggiunta ad una soluzione acquosa di: A. idrossido di bario B. perclorato di piombo C. cloruro di ferro(ii)
Acidi Basi e Sali. ChimicaGenerale_lezione19 1
 Acidi Basi e Sali Le soluzioni della maggior parte dei sali sono acide o basiche piuttosto che neutre. Infatti, cationi e anioni possono agire da basi o acidi E possibile prevedere il ph di una soluzione
Acidi Basi e Sali Le soluzioni della maggior parte dei sali sono acide o basiche piuttosto che neutre. Infatti, cationi e anioni possono agire da basi o acidi E possibile prevedere il ph di una soluzione
Equilibri acido-base
 Equilibri acido-base Ione idronio, acidi forti ed acidi deboli in acqua, costante di dissociazione dell acido (Ka) Acido forte: completamente dissociato HA(aq) H + (aq) + A - (aq) HA(aq) + H 2 O(l) H 3
Equilibri acido-base Ione idronio, acidi forti ed acidi deboli in acqua, costante di dissociazione dell acido (Ka) Acido forte: completamente dissociato HA(aq) H + (aq) + A - (aq) HA(aq) + H 2 O(l) H 3
PROPRIETA ACIDO-BASE DELLE SOLUZIONI SALINE
 PROPRIETA ACIDO-BASE DELLE SOLUZIONI SALINE Un sale è un solido ionico contenente un catione diverso da H + e un anione diverso da OH -. I sali sono degli elettroliti forti, cioè in acqua si dissociano
PROPRIETA ACIDO-BASE DELLE SOLUZIONI SALINE Un sale è un solido ionico contenente un catione diverso da H + e un anione diverso da OH -. I sali sono degli elettroliti forti, cioè in acqua si dissociano
Equilibri acido-base
 Equilibri acido-base Ione idronio, acidi forti ed acidi deboli in acqua, costante di dissociazione dell acido (Ka) Acido forte: completamente dissociato HA(aq) H + (aq) + A - (aq) HA(aq) + H 2 O(l) H 3
Equilibri acido-base Ione idronio, acidi forti ed acidi deboli in acqua, costante di dissociazione dell acido (Ka) Acido forte: completamente dissociato HA(aq) H + (aq) + A - (aq) HA(aq) + H 2 O(l) H 3
SOLUBILITA EQUILIBRI ETEROGENEI
 SOLUBILITA EQUILIBRI ETEROGENEI Cosa succede quando si scioglie un sale (NaCl) in acqua Cl - LEGAME IONE DIPOLO Se sciogliamo in un solvente polare (tipo H 2 O) una sostanza ionica(tipo NaCl) questa si
SOLUBILITA EQUILIBRI ETEROGENEI Cosa succede quando si scioglie un sale (NaCl) in acqua Cl - LEGAME IONE DIPOLO Se sciogliamo in un solvente polare (tipo H 2 O) una sostanza ionica(tipo NaCl) questa si
BaSO 4 Ba ++ + SO 4. Co-x x x. Solubilità : moli di composto dissociate per litro. [Ba ++ ] = [SO 4= ] = [BaSO 4 ] o (moli di composto dissociato)
![BaSO 4 Ba ++ + SO 4. Co-x x x. Solubilità : moli di composto dissociate per litro. [Ba ++ ] = [SO 4= ] = [BaSO 4 ] o (moli di composto dissociato) BaSO 4 Ba ++ + SO 4. Co-x x x. Solubilità : moli di composto dissociate per litro. [Ba ++ ] = [SO 4= ] = [BaSO 4 ] o (moli di composto dissociato)](/thumbs/66/54590881.jpg) 1. Da misure di conducibilità elettrica risulta che la solubilità del solfato di bario BaSO 4 in acqua pura è 1.05 10 5 mole/litro a 25 C. Si calcoli il prodotto di solubilità del solfato di bario. BaSO
1. Da misure di conducibilità elettrica risulta che la solubilità del solfato di bario BaSO 4 in acqua pura è 1.05 10 5 mole/litro a 25 C. Si calcoli il prodotto di solubilità del solfato di bario. BaSO
Rapporto tra soluto e solvente o soluzione
 Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
BaSO 4 Ba ++ + SO. Solubilità : moli di composto dissociate per litro. [Ba ++ ] = [SO 4= ] = [BaSO 4 ] o. (moli di composto dissociato)
![BaSO 4 Ba ++ + SO. Solubilità : moli di composto dissociate per litro. [Ba ++ ] = [SO 4= ] = [BaSO 4 ] o. (moli di composto dissociato) BaSO 4 Ba ++ + SO. Solubilità : moli di composto dissociate per litro. [Ba ++ ] = [SO 4= ] = [BaSO 4 ] o. (moli di composto dissociato)](/thumbs/101/151115258.jpg) 1. Da misure di conducibilità elettrica risulta che la solubilità del solfato di bario BaSO 4 in acqua pura è 1.05 10 5 mole/litro a 5 C. Si calcoli il prodotto di solubilità del solfato di bario. BaSO
1. Da misure di conducibilità elettrica risulta che la solubilità del solfato di bario BaSO 4 in acqua pura è 1.05 10 5 mole/litro a 5 C. Si calcoli il prodotto di solubilità del solfato di bario. BaSO
Esperienza n. 1 PREVISIONE E RICONOSCIMENTO DI ALCUNE REAZIONI DI METATESI.
 Corso di Laboratorio di Chimica Generale Esperienza n. 1 PREVISIONE E RICONOSCIMENTO DI ALCUNE REAZIONI DI METATESI. REAZIONI IN SOLUZIONE 1 Alcuni tipi di reazioni ioniche, che non implichino processi
Corso di Laboratorio di Chimica Generale Esperienza n. 1 PREVISIONE E RICONOSCIMENTO DI ALCUNE REAZIONI DI METATESI. REAZIONI IN SOLUZIONE 1 Alcuni tipi di reazioni ioniche, che non implichino processi
ESERCIZI DI RIEPILOGO GENERALE
 ESERCIZI DI RIEPILOGO GENERALE 1) Scrivere le formule brute e le formule di Lewis per: ammoniaca; ione ammonio; ione solfato; ione bicarbonato; acido acetico; anidride solforosa. Dove necessario, indicare
ESERCIZI DI RIEPILOGO GENERALE 1) Scrivere le formule brute e le formule di Lewis per: ammoniaca; ione ammonio; ione solfato; ione bicarbonato; acido acetico; anidride solforosa. Dove necessario, indicare
Equilibri in soluzione acquosa unità 1, modulo G del libro
 Equilibri in soluzione acquosa unità 1, modulo G del libro Si parla di equilibri in soluzione acquosa quando un soluto, solido, viene sciolto in acqua. Cosa accade? La specie solida si dissocia in ioni,
Equilibri in soluzione acquosa unità 1, modulo G del libro Si parla di equilibri in soluzione acquosa quando un soluto, solido, viene sciolto in acqua. Cosa accade? La specie solida si dissocia in ioni,
Concentrazione delle Soluzioni
 Concentrazione delle Soluzioni Si definisce soluzione una miscela omogenea di più sostanze: Soluzione liquido-liquido: alcol etilico-acqua, vino-acqua, rhum-cocacola Soluzione solido-liquido: zucchero-acqua,
Concentrazione delle Soluzioni Si definisce soluzione una miscela omogenea di più sostanze: Soluzione liquido-liquido: alcol etilico-acqua, vino-acqua, rhum-cocacola Soluzione solido-liquido: zucchero-acqua,
Gli equilibri di solubilità
 Gli equilibri di solubilità Abbiamo definito la solubilità come la concentrazione della soluzione satura, che è una soluzione il cui il composto in soluzione è in equilibrio con il composto indisciolto.
Gli equilibri di solubilità Abbiamo definito la solubilità come la concentrazione della soluzione satura, che è una soluzione il cui il composto in soluzione è in equilibrio con il composto indisciolto.
SOLUZIONI COMPITO A DI CHIMICA DEL
 SOLUZIONI COMPITO A DI CHIMICA DEL 18-07-12 1A) 1.3 kg di un campione solido contenente il 40% di permanganato di potassio, il 50% di dicromato di potassio e il 10% di impurezze vengono sciolti in una
SOLUZIONI COMPITO A DI CHIMICA DEL 18-07-12 1A) 1.3 kg di un campione solido contenente il 40% di permanganato di potassio, il 50% di dicromato di potassio e il 10% di impurezze vengono sciolti in una
Classificazione della materia
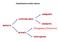 Classificazione della materia composto materia sostanza pura miscela Omogenea (Soluzioni) eterogenea elemento Definizione di Soluzione Una soluzione è il prodotto della dispersione omogenea delle molecole
Classificazione della materia composto materia sostanza pura miscela Omogenea (Soluzioni) eterogenea elemento Definizione di Soluzione Una soluzione è il prodotto della dispersione omogenea delle molecole
Concentrazione delle Soluzioni
 Concentrazione delle Soluzioni Si definisce soluzione una miscela omogenea di più sostanze: Soluzione liquido-liquido: alcol etilico-acqua, vino-acqua, rhum-cocacola Soluzione solido-liquido: zucchero-acqua,
Concentrazione delle Soluzioni Si definisce soluzione una miscela omogenea di più sostanze: Soluzione liquido-liquido: alcol etilico-acqua, vino-acqua, rhum-cocacola Soluzione solido-liquido: zucchero-acqua,
ANALISI SISTEMATICA DEI CATIONI
 ANALISI SISTEMATICA DEI CATIONI Particolare procedura analitica attraverso la quale tutte le specie cationiche presenti in una ipotetica miscela vengono inizialmente separate in gruppi, mediante l uso
ANALISI SISTEMATICA DEI CATIONI Particolare procedura analitica attraverso la quale tutte le specie cationiche presenti in una ipotetica miscela vengono inizialmente separate in gruppi, mediante l uso
Appello Straordinario di Chimica Generale ed Inorganica (29 Aprile 2019) Canale M-Z. Testo A
 Appello Straordinario di Chimica Generale ed Inorganica (29 Aprile 2019) Canale M-Z Testo A 1) Una soluzione è ottenuta miscelando 15,00 ml di una soluzione di HCl (MM36,46) 0,360 M, 10,00 ml di una soluzione
Appello Straordinario di Chimica Generale ed Inorganica (29 Aprile 2019) Canale M-Z Testo A 1) Una soluzione è ottenuta miscelando 15,00 ml di una soluzione di HCl (MM36,46) 0,360 M, 10,00 ml di una soluzione
Sommario della lezione 24. Equilibri di solubilità. Chimica Organica. Elettrochimica
 Sommario della lezione 24 Equilibri di solubilità Chimica Organica Elettrochimica EQUILIBRI DI SOLUBILITA Solubilità È la concentrazione del soluto in una soluzione satura (dove è presente il corpo di
Sommario della lezione 24 Equilibri di solubilità Chimica Organica Elettrochimica EQUILIBRI DI SOLUBILITA Solubilità È la concentrazione del soluto in una soluzione satura (dove è presente il corpo di
Le soluzioni e la loro concentrazione
 Le soluzioni e la loro concentrazione Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore quantità. Il soluto è il
Le soluzioni e la loro concentrazione Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore quantità. Il soluto è il
T.A.R.M Luigi Cerruti Lezioni di chimica 11-12
 T.A.R.M. 2009 www.minerva.unito.it Luigi Cerruti Lezioni di chimica 11-12 La definizione di mole La mole è la quantità di sostanza di un sistema che contiene tante entità elementari quanti sono gli atomi
T.A.R.M. 2009 www.minerva.unito.it Luigi Cerruti Lezioni di chimica 11-12 La definizione di mole La mole è la quantità di sostanza di un sistema che contiene tante entità elementari quanti sono gli atomi
A-PDF Merger DEMO : Purchase from to remove the watermark
 A-PDF Merger DEMO : Purchase from www.a-pdf.com to remove the watermark Corso di Laurea in Farmacia/ISF Esame di Chimica Generale ed Inorganica Prova scritta di Stechiometria 3-0-004 Cognome e Nome Corso
A-PDF Merger DEMO : Purchase from www.a-pdf.com to remove the watermark Corso di Laurea in Farmacia/ISF Esame di Chimica Generale ed Inorganica Prova scritta di Stechiometria 3-0-004 Cognome e Nome Corso
ESAME DI SCIENZE SPERIMENTALI PARTE CHIMICA
 ESAME DI SCIENZE SPERIMENTALI PARTE CHIMICA VALUTAZIONE - Prima parte: scelte multiple (26 punti = 13 domande da 2 punti) (totale: 80 punti) - Seconda parte: domande (30 punti = 5 domande da 6 punti) -
ESAME DI SCIENZE SPERIMENTALI PARTE CHIMICA VALUTAZIONE - Prima parte: scelte multiple (26 punti = 13 domande da 2 punti) (totale: 80 punti) - Seconda parte: domande (30 punti = 5 domande da 6 punti) -
Soluti in acqua. Elettroliti. Non elettroliti
 Soluti in acqua Elettroliti Forti Dissociazione Elettrolitica COMPLETA Soluto Deboli Dissociazione Elettrolitica NON COMPLETA Non elettroliti Dissociazione Elettrolitica NaCl (s) + acqua Na + (aq) + Cl
Soluti in acqua Elettroliti Forti Dissociazione Elettrolitica COMPLETA Soluto Deboli Dissociazione Elettrolitica NON COMPLETA Non elettroliti Dissociazione Elettrolitica NaCl (s) + acqua Na + (aq) + Cl
Corso di Laurea in Chimica e Tecnologia Farmaceutiche Esame di Chimica Analitica e Complementi di Chimica Modulo di Chimica Analitica 8 Novembre 2012
 Modulo di Chimica Analitica 8 Novembre 2012 1. Una soluzione viene preparata sciogliendo1210 mg di K 3 Fe(CN) 6 in 775 ml di acqua. Calcolare: a) la concentrazione analitica di K 3 Fe(CN) 6 b) la concentrazione
Modulo di Chimica Analitica 8 Novembre 2012 1. Una soluzione viene preparata sciogliendo1210 mg di K 3 Fe(CN) 6 in 775 ml di acqua. Calcolare: a) la concentrazione analitica di K 3 Fe(CN) 6 b) la concentrazione
Corso di Laurea in ISF Esame di Chimica Generale ed Inorganica Appello del Cognome e Nome
 Corso di Laurea in ISF Esame di Chimica Generale ed Inorganica Appello del 30-01-2006 Cognome e Nome Anno Immatricolazione n matricola Esercizio 1 Calcolare il ph di una soluzione ottenuta aggiungendo
Corso di Laurea in ISF Esame di Chimica Generale ed Inorganica Appello del 30-01-2006 Cognome e Nome Anno Immatricolazione n matricola Esercizio 1 Calcolare il ph di una soluzione ottenuta aggiungendo
Esercizio 1) n.mol CH n.mol C 4 H 6 3 = Dalla prima equazione: n.mol CH 4 = n.mol C 4 H 6 4 sostituendo nella seconda equazione:
 Esercizio 1 L esercizio è una sorta di analisi indiretta. Le due singole reazioni bilanciate x CH 4 (g + 2.0 O 2(g 1 CO 2 (g + 2 H 2 O (l y C 4 H 6 (g + 5.5 O 2(g 4 CO 2 (g + 3 H 2 O (l Indico con x la
Esercizio 1 L esercizio è una sorta di analisi indiretta. Le due singole reazioni bilanciate x CH 4 (g + 2.0 O 2(g 1 CO 2 (g + 2 H 2 O (l y C 4 H 6 (g + 5.5 O 2(g 4 CO 2 (g + 3 H 2 O (l Indico con x la
BaSO. BaSO 4 è una costante quindi: K ps = prodotto di solubilità
 Gli equilibri di solubilità sono equilibri eterogenei in quanto si stabiliscono tra due fasi: un solido e la soluzione satura dei suoi ioni. Sono gli equilibri che coinvolgono le reazioni di dissoluzione
Gli equilibri di solubilità sono equilibri eterogenei in quanto si stabiliscono tra due fasi: un solido e la soluzione satura dei suoi ioni. Sono gli equilibri che coinvolgono le reazioni di dissoluzione
Effetto del ph sulla solubilità
 Effetto del ph sulla solubilità CH COOAg (s Ag CH COO [Ag ][CH COO ] 0 CH COO H CH COOH 0 Se si aumenta H, aggiungendo un acido forte, il secondo equilibrio si sposta verso destra sottraendo una parte
Effetto del ph sulla solubilità CH COOAg (s Ag CH COO [Ag ][CH COO ] 0 CH COO H CH COOH 0 Se si aumenta H, aggiungendo un acido forte, il secondo equilibrio si sposta verso destra sottraendo una parte
CAPITOLO 12 EQUILIBRI ACIDO-BASE E SOLUBILITA
 CAPITOLO 12 EQUILIBRI ACIDO-BASE E SOLUBILITA 12.1 (a) ph = 2,57 (b) ph = 4,44 12.3 (a) no. (b) no. (c) sì. (d) sì. (e) no. 12.5 ph = 8,88 12.7 0,024 12.9 0,58 12.11 ph = 9,25; ph = 9,18. 12.13 Na 2 A/NaHA.
CAPITOLO 12 EQUILIBRI ACIDO-BASE E SOLUBILITA 12.1 (a) ph = 2,57 (b) ph = 4,44 12.3 (a) no. (b) no. (c) sì. (d) sì. (e) no. 12.5 ph = 8,88 12.7 0,024 12.9 0,58 12.11 ph = 9,25; ph = 9,18. 12.13 Na 2 A/NaHA.
Calcolare la resa teorica di AgCl: 0.640g x 100/98.3 = 0.651g. Calcolare le moli di AgCl: massa molare AgCl: g/mol
 Esercizio 1 Quanti millilitri di una soluzione 2.73x10-1 M di AgNO3 bisogna far reagire con una soluzione di HCl per ottenere 640 mg di AgCl sapendo che la resa della reazione è del 98.3%. Scrivere la
Esercizio 1 Quanti millilitri di una soluzione 2.73x10-1 M di AgNO3 bisogna far reagire con una soluzione di HCl per ottenere 640 mg di AgCl sapendo che la resa della reazione è del 98.3%. Scrivere la
scheda di lavoro relativa all'esperienza di laboratorio: REAZIONI FRA IONI IN SOLUZIONE ACQUOSA Scopo dell'esperienza: verificare la formazione di...
 scheda di lavoro relativa all'esperienza di laboratorio: REAZIONI FRA IONI IN SOLUZIONE ACQUOSA Scopo dell'esperienza: verificare la formaz di... Prerequisiti: :.. composto ionico:.. reazioni di doppio
scheda di lavoro relativa all'esperienza di laboratorio: REAZIONI FRA IONI IN SOLUZIONE ACQUOSA Scopo dell'esperienza: verificare la formaz di... Prerequisiti: :.. composto ionico:.. reazioni di doppio
Soluzioni e Concentrazione
 Scuola di Ingegneria Industriale e dell Informazione Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Soluzioni e Concentrazione Prof. Dipartimento CMIC Giulio Natta https://corsi.chem.polimi.it/citterio/default.htm
Scuola di Ingegneria Industriale e dell Informazione Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Soluzioni e Concentrazione Prof. Dipartimento CMIC Giulio Natta https://corsi.chem.polimi.it/citterio/default.htm
L ANALISI CHIMICA 2 SOSTANZA INCOGNITA. Analisi degli anioni e dei cationi. Riconoscimento della sostanza
 L ANALISI CHIMICA 1 L Analisi Chimica è un insieme di operazioni che si eseguono per separare, riconoscere (Analisi Chimica Qualitativa) e dosare (Analisi Chimica Quantitativa) una sostanza o una miscela
L ANALISI CHIMICA 1 L Analisi Chimica è un insieme di operazioni che si eseguono per separare, riconoscere (Analisi Chimica Qualitativa) e dosare (Analisi Chimica Quantitativa) una sostanza o una miscela
+ 4e - + 16H 3 O + 3S 2- + 36H 2 O 3SO 2-4 + 24e - + 24H 3 O +
 SOLUZIONI COMPITO A DI CHIMICA DEL 22-06-11 1A) 258 g di un minerale contenente il 91% di solfuro di arsenico (III), vengono immessi in 4,0 L di una soluzione acquosa di acido manganico al 10% in peso
SOLUZIONI COMPITO A DI CHIMICA DEL 22-06-11 1A) 258 g di un minerale contenente il 91% di solfuro di arsenico (III), vengono immessi in 4,0 L di una soluzione acquosa di acido manganico al 10% in peso
Soluzioni Acido Base Definizione di Brønsted
 acido + base sale + acqua Soluzioni Acido Base Definizione di Brønsted acido: sostanza capace di donare protoni* HCl + H 2 O Cl + H 3 O + * In soluzione, il protone esiste in forma idratata (H 3 O + )
acido + base sale + acqua Soluzioni Acido Base Definizione di Brønsted acido: sostanza capace di donare protoni* HCl + H 2 O Cl + H 3 O + * In soluzione, il protone esiste in forma idratata (H 3 O + )
Transizioni di fase: Equazione di Clausius-Clapeyron
 Passaggi di stato e diagrammi di stato Come già detto più volte la materia è presente sottoforma di diversi stati di aggregazione: - solido - liquido - gassoso Ed è possibile osservare il passaggio da
Passaggi di stato e diagrammi di stato Come già detto più volte la materia è presente sottoforma di diversi stati di aggregazione: - solido - liquido - gassoso Ed è possibile osservare il passaggio da
Es: consideriamo una soluzione contenente acido K = 1, [CH 3 COOH]
![Es: consideriamo una soluzione contenente acido K = 1, [CH 3 COOH] Es: consideriamo una soluzione contenente acido K = 1, [CH 3 COOH]](/thumbs/103/157927484.jpg) SOLUZIONI TAMPONE Una soluzione tampone è una soluzione che contiene quantità paragonabili (dello stesso ordine di grandezza) di un acido debole e della sua base coniugata o di una base debole e del suo
SOLUZIONI TAMPONE Una soluzione tampone è una soluzione che contiene quantità paragonabili (dello stesso ordine di grandezza) di un acido debole e della sua base coniugata o di una base debole e del suo
dispersioni omogenee di due o più specie chimiche l una nell altra
 Soluzioni : dispersioni omogenee di due o più specie chimiche l una nell altra Solvente : componente che si trova nel medesimo stato fisico della soluzione componente che si trova in quantità maggiore
Soluzioni : dispersioni omogenee di due o più specie chimiche l una nell altra Solvente : componente che si trova nel medesimo stato fisico della soluzione componente che si trova in quantità maggiore
Prodotto di Solubilità
 Prodotto di Solubilità L equilibrio chimico ionico, ionizzazione degli elettroliti L equilibrio chimico ionico si riferisce ad un processo chimico in cui compaiono ioni come unità fondamentali. In talune
Prodotto di Solubilità L equilibrio chimico ionico, ionizzazione degli elettroliti L equilibrio chimico ionico si riferisce ad un processo chimico in cui compaiono ioni come unità fondamentali. In talune
Esercizi - A.A. 2017/2018
 Esercizi - A.A. 2017/2018 Preparazione soluzioni e diluizioni Es. 1 2 ml di piridina (d = 0.892 g/ml) sono disciolti in 80 ml di etanolo (d = 0.79 g/ml). Trovare la % in massa di piridina nella soluzione.
Esercizi - A.A. 2017/2018 Preparazione soluzioni e diluizioni Es. 1 2 ml di piridina (d = 0.892 g/ml) sono disciolti in 80 ml di etanolo (d = 0.79 g/ml). Trovare la % in massa di piridina nella soluzione.
Stechiometria delle soluzioni
 www.matematicamente.it stechiometria delle soluzioni (medicina) 1 Stechiometria delle soluzioni Domande tratte dai test di ammissione a medicina, odontoiatria, veterinaria 1. Se si vuole ottenere una soluzione
www.matematicamente.it stechiometria delle soluzioni (medicina) 1 Stechiometria delle soluzioni Domande tratte dai test di ammissione a medicina, odontoiatria, veterinaria 1. Se si vuole ottenere una soluzione
Esame di Chimica Generale 13 Gennaio 2017
 Esame di Chimica Generale 13 Gennaio 2017 COGNOME NOME. MATRICOLA 1 2 3 4 5 6 7 8 9 10 Indicazioni per lo svolgimento del compito. Scrivete il vostro Nome e Cognome in STAMPATELLO su ciascuno di questi
Esame di Chimica Generale 13 Gennaio 2017 COGNOME NOME. MATRICOLA 1 2 3 4 5 6 7 8 9 10 Indicazioni per lo svolgimento del compito. Scrivete il vostro Nome e Cognome in STAMPATELLO su ciascuno di questi
PROVA SCRITTA DI CHIMICA GENERALE ED INORGANICA Scienze e Tecnologie per l Ambiente 1 Febbraio 2013
 1 Febbraio 2013 1) a) Scrivere le formule di Lewis, l ibridizzazione dell'atomo centrale, la geometria molecolare ed eventuale presenza di momento dipolare per SF 6 e per gli anioni dei sali: fosfato di
1 Febbraio 2013 1) a) Scrivere le formule di Lewis, l ibridizzazione dell'atomo centrale, la geometria molecolare ed eventuale presenza di momento dipolare per SF 6 e per gli anioni dei sali: fosfato di
9065X Chimica. Modello esame svolto. Esempio di compito scritto di Chimica. Politecnico di Torino CeTeM
 svolto Esempio di compito scritto di Chimica 1 - La configurazione elettronica: [Ar]3d 6 4s 0 rappresenta lo ione: 1) Mn 2+ 2) Ni 2+ 3) Fe 3+ 4) Co 3+ 5) Cu 2+ 2 - Un gas reale mantenuto sempre al di sopra
svolto Esempio di compito scritto di Chimica 1 - La configurazione elettronica: [Ar]3d 6 4s 0 rappresenta lo ione: 1) Mn 2+ 2) Ni 2+ 3) Fe 3+ 4) Co 3+ 5) Cu 2+ 2 - Un gas reale mantenuto sempre al di sopra
Le soluzioni. Soluzione = miscela omogenea di due o più specie chimiche
 Le soluzioni 1 Soluzione = miscela omogenea di due o più specie chimiche Possono essere sistemi solidi, liquidi o gas, ma comunemente si parla di soluzioni liquide È il componente che ha lo stesso stato
Le soluzioni 1 Soluzione = miscela omogenea di due o più specie chimiche Possono essere sistemi solidi, liquidi o gas, ma comunemente si parla di soluzioni liquide È il componente che ha lo stesso stato
Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2015/2016 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2015/2016 Dott. Giuseppe La Regina Tu,
1) A che cosa è dovuta la elevata viscosità del mercurio elementare (allo stato liquido)?
 1) A che cosa è dovuta la elevata viscosità del mercurio elementare (allo stato liquido)? A. ai legami ad idrogeno tra gli atomi di mercurio B. alle interazioni tipo London tra gli atomi di mercurio C.
1) A che cosa è dovuta la elevata viscosità del mercurio elementare (allo stato liquido)? A. ai legami ad idrogeno tra gli atomi di mercurio B. alle interazioni tipo London tra gli atomi di mercurio C.
Equilibri di precipitazione
 Equilibri di precipitazione Molte sostanze solide sono caratterizzate da una scarsa solubilità in acqua (ad es. tutti i carbonati e gli idrossidi degli elementi del II gruppo) AgCl (a differenza di NaCl)
Equilibri di precipitazione Molte sostanze solide sono caratterizzate da una scarsa solubilità in acqua (ad es. tutti i carbonati e gli idrossidi degli elementi del II gruppo) AgCl (a differenza di NaCl)
N.B. Indicare i passaggi dei calcoli
 Corso Corso di di Laurea Laurea in in Fisica ca COMPITO N 3 DA CONSEGNARE ENTRO IL 11/12/09 Cognome Nome(*)....N di Matricola (*) scrivere in stampatello N.B. Indicare i passaggi dei calcoli 1. Il cloro
Corso Corso di di Laurea Laurea in in Fisica ca COMPITO N 3 DA CONSEGNARE ENTRO IL 11/12/09 Cognome Nome(*)....N di Matricola (*) scrivere in stampatello N.B. Indicare i passaggi dei calcoli 1. Il cloro
Dipendenza della Solubilità dalla temperatura
 SOLUBILIZZAZIONE Simile scioglie il simile: le molecole di sostanze diverse si mescolano intimamente nelle miscele se possiedono forze intermolecolari simili (soluzioni ideali). Anche se le forze intermolecolari
SOLUBILIZZAZIONE Simile scioglie il simile: le molecole di sostanze diverse si mescolano intimamente nelle miscele se possiedono forze intermolecolari simili (soluzioni ideali). Anche se le forze intermolecolari
Università degli Studi di Torino CORSO DI CHIMICA GENERALE ED INORGANICA C. Schede di valutazione relative alle esercitazioni pratiche in laboratorio
 Università degli Studi di Torino CORSO DI CHIMICA GENERALE ED INORGANICA C Schede di valutazione relative alle esercitazioni pratiche in laboratorio Anno accademico 2006-2007 Dott.ssa Elena Ghibaudi Dott.
Università degli Studi di Torino CORSO DI CHIMICA GENERALE ED INORGANICA C Schede di valutazione relative alle esercitazioni pratiche in laboratorio Anno accademico 2006-2007 Dott.ssa Elena Ghibaudi Dott.
i) 0.10 a = eq) 0 a =
 Università degli Studi di Roma Tor Vergata, Facoltà di Scienze MFN Corso di Laurea Triennale in Chimica Applicata, Insegnamento di Chimica Generale Modulo di Stechiometria. AA 2008/2009 Seconda prova scritta
Università degli Studi di Roma Tor Vergata, Facoltà di Scienze MFN Corso di Laurea Triennale in Chimica Applicata, Insegnamento di Chimica Generale Modulo di Stechiometria. AA 2008/2009 Seconda prova scritta
Corso di Chimica Generale Inorganica Soluzione degli Esercizi del Compito del 6 settembre 2010
 Corso di Chimica Generale Inorganica Soluzione degli Esercizi del Compito del 6 settembre 010 Si avvertono gli studenti che la verbalizzazione dei risultati dell esame è fatta esclusivamente per via elettronica.
Corso di Chimica Generale Inorganica Soluzione degli Esercizi del Compito del 6 settembre 010 Si avvertono gli studenti che la verbalizzazione dei risultati dell esame è fatta esclusivamente per via elettronica.
Lezione 4. Le soluzioni Acidi e Basi Reazioni Chimiche La Concentrazione delle Soluzioni
 2018 Lezione 4. Le soluzioni Acidi e Basi Reazioni Chimiche La Concentrazione delle Soluzioni Una soluzione è una miscela omogenea di 2 o più sostanze Il soluto è la sostanza (o sostanze) presente/i in
2018 Lezione 4. Le soluzioni Acidi e Basi Reazioni Chimiche La Concentrazione delle Soluzioni Una soluzione è una miscela omogenea di 2 o più sostanze Il soluto è la sostanza (o sostanze) presente/i in
Prova scritta CTF del 20- Gen NO 2
 Prova scritta CTF del 20Gen2011 1) Il Legame Covalente 2) Bilanciare in ambiente acido la seguente reazione di ossido riduzione: MnO 4 + NO 2 = Mn 2+ + NO 3 3) Applicando la teoria della repulsione delle
Prova scritta CTF del 20Gen2011 1) Il Legame Covalente 2) Bilanciare in ambiente acido la seguente reazione di ossido riduzione: MnO 4 + NO 2 = Mn 2+ + NO 3 3) Applicando la teoria della repulsione delle
PROVA SCRITTA DI CHIMICA GENERALE ED INORGANICA Scienze e Tecnologie per l Ambiente 3 Febbraio 2010
 3 Febbraio 2010 eventuale presenza di momento dipolare per le molecole: PH 3, BrF 5, ione perclorato. 2) Calcolare il ph a 25 C di una soluzione acquosa 0.10 M di acido cloracetico (indicare con HA) sapendo
3 Febbraio 2010 eventuale presenza di momento dipolare per le molecole: PH 3, BrF 5, ione perclorato. 2) Calcolare il ph a 25 C di una soluzione acquosa 0.10 M di acido cloracetico (indicare con HA) sapendo
 2NH3(g) Pa(Ag)=108 Pa(I)=127 pf(agi)=235 -> S(g/l) =S(m/l) pf = 9.2 10-9 235 =2162 10-9 = 2.16 10-6 (g/l) Effetto del ph Anche il ph può influenzare la solubilità di un sale poco solubile. E ciò
2NH3(g) Pa(Ag)=108 Pa(I)=127 pf(agi)=235 -> S(g/l) =S(m/l) pf = 9.2 10-9 235 =2162 10-9 = 2.16 10-6 (g/l) Effetto del ph Anche il ph può influenzare la solubilità di un sale poco solubile. E ciò
PROVA SCRITTA DI CHIMICA GENERALE ED INORGANICA Scienze e Tecnologie per l Ambiente
 10 Dicembre 2008 eventuale presenza di momento dipolare per I - 3 e per gli anioni dei sali: nitrato di sodio, perclorato di potassio. 2) a) Calcolare il ph di una soluzione di carbonato di sodio 0.10
10 Dicembre 2008 eventuale presenza di momento dipolare per I - 3 e per gli anioni dei sali: nitrato di sodio, perclorato di potassio. 2) a) Calcolare il ph di una soluzione di carbonato di sodio 0.10
1 - Titolazioni acido-base e ph
 1 - Titolazioni acido-base e ph Procedimento (m.m. di NH 3 = 17,03) Moli di NaOH consumate (1,04 x 10-3 ) Moli di HCl iniziali (7,75 x 10-3 ) Moli di NH 3 (6,71 x 10-3 ) Massa di NH 3 (114,3 mg) Concentrazione
1 - Titolazioni acido-base e ph Procedimento (m.m. di NH 3 = 17,03) Moli di NaOH consumate (1,04 x 10-3 ) Moli di HCl iniziali (7,75 x 10-3 ) Moli di NH 3 (6,71 x 10-3 ) Massa di NH 3 (114,3 mg) Concentrazione
Brady Senese Pignocchino Chimica.blu Zanichelli 2014 Soluzione degli esercizi Capitolo 22
 Brady Senese Pignocchino Chimica.blu Zanichelli 014 Soluzione degli esercizi Capitolo Esercizio Risposta PAG 515 ES 1 Basica, a causa dell idrolisi dell anione (base coniugata di un acido debole). PAG
Brady Senese Pignocchino Chimica.blu Zanichelli 014 Soluzione degli esercizi Capitolo Esercizio Risposta PAG 515 ES 1 Basica, a causa dell idrolisi dell anione (base coniugata di un acido debole). PAG
Rapporto tra soluto e solvente o soluzione
 Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
La Vita è una Reazione Chimica
 La Vita è una Reazione Chimica Acqua Oro Zucchero I Legami Chimici F N F F Il legame chimico il legame ionico Polare il legame covalente Dativo Gli elettroni di valenza sono gli elettroni del livello più
La Vita è una Reazione Chimica Acqua Oro Zucchero I Legami Chimici F N F F Il legame chimico il legame ionico Polare il legame covalente Dativo Gli elettroni di valenza sono gli elettroni del livello più
Classificazione chimica della materia
 Classificazione chimica della materia sostanze (o specie chimiche) sistemi ad un componente specie elementari costituite da atomi dello stesso elemento argento, zolfo, ossigeno, idrogeno composti costituiti
Classificazione chimica della materia sostanze (o specie chimiche) sistemi ad un componente specie elementari costituite da atomi dello stesso elemento argento, zolfo, ossigeno, idrogeno composti costituiti
SOLUZIONI COMPITO A CHIMICA
 SOLUZIONI COMPITO A CHIMICA 16-01-2012 1A) Il permanganato di ammonio si può ottenere dalla reazione tra permanganato di bario e solfato di ammonio, filtrando il precipitato di solfato di bario che si
SOLUZIONI COMPITO A CHIMICA 16-01-2012 1A) Il permanganato di ammonio si può ottenere dalla reazione tra permanganato di bario e solfato di ammonio, filtrando il precipitato di solfato di bario che si
Espressioni di concentrazione di una soluzione
 SOLUZIONI Una soluzione è un sistema fisicamente omogeneo costituito da due o più componenti: il solvente e il soluto (o i soluti. Il solvente è il componente presente, in genere ma non di regola, in maggior
SOLUZIONI Una soluzione è un sistema fisicamente omogeneo costituito da due o più componenti: il solvente e il soluto (o i soluti. Il solvente è il componente presente, in genere ma non di regola, in maggior
LA FORMAZIONE DELLE SOLUZIONI.
 LA FORMAZIONE DELLE SOLUZIONI. Perché le sostanze si sciolgono? Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore
LA FORMAZIONE DELLE SOLUZIONI. Perché le sostanze si sciolgono? Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore
Sommario della lezione 18. Proprietà colligative
 Sommario della lezione 18 Proprietà colligative Interazioni soluto-solvente Interazioni soluto-solvente La solubilità di un soluto in un particolare solvente dipende da: la natura delle particelle di solvente
Sommario della lezione 18 Proprietà colligative Interazioni soluto-solvente Interazioni soluto-solvente La solubilità di un soluto in un particolare solvente dipende da: la natura delle particelle di solvente
Soluzioni. 12 a. La soluzione più acida è la soluzione A. b. La soluzione con il ph maggiore è la soluzione B.
 Soluzioni capitolo 21 VERIFICA LE TUE CONOSCENZE IL PRODOTTO IONICO DELL ACQUA 1 Concentrazione degli ioni H 3 O + : a. [H 3 O + ] = 1 $ 10-1 mol/l b. [H 3 O + ] = 1 $ 10 0 mol/l 2 Concentrazione degli
Soluzioni capitolo 21 VERIFICA LE TUE CONOSCENZE IL PRODOTTO IONICO DELL ACQUA 1 Concentrazione degli ioni H 3 O + : a. [H 3 O + ] = 1 $ 10-1 mol/l b. [H 3 O + ] = 1 $ 10 0 mol/l 2 Concentrazione degli
DISSOLUZIONE DEL CLORURO DI SODIO
 DISSOLUZIONE DEL CLORURO DI SODIO Nel processo di dissoluzione del NaCl le molecole di acqua dipolari attraggono gli ioni del sale, indebolendo l attrazione elettrostatica tra Na + e Cl -. Inizialmente
DISSOLUZIONE DEL CLORURO DI SODIO Nel processo di dissoluzione del NaCl le molecole di acqua dipolari attraggono gli ioni del sale, indebolendo l attrazione elettrostatica tra Na + e Cl -. Inizialmente
Facoltà di Agraria. Corso di Chimica Generale Inorganica Soluzione degli esercizi del Compito del 24 giugno 2010
 Facoltà di Agraria Corso di Chimica Generale Inorganica Soluzione degli esercizi del Compito del 24 giugno 2010 Si avvertono gli studenti che la verbalizzazione dei risultati dell esame è fatta esclusivamente
Facoltà di Agraria Corso di Chimica Generale Inorganica Soluzione degli esercizi del Compito del 24 giugno 2010 Si avvertono gli studenti che la verbalizzazione dei risultati dell esame è fatta esclusivamente
SOLUZIONI COMPITO A CHIMICA
 SOLUZIONI COMPITO A CHIMICA 07-07-211 1A) Per combustione di una miscela (0,596 moli totali) di due idrocarburi di formula (C 7 H 16 e C 9 H 20 ) si ottengono 102.420 g di acqua ed anidride carbonica.
SOLUZIONI COMPITO A CHIMICA 07-07-211 1A) Per combustione di una miscela (0,596 moli totali) di due idrocarburi di formula (C 7 H 16 e C 9 H 20 ) si ottengono 102.420 g di acqua ed anidride carbonica.
POLITECNICO DI MILANO ING. ENG AER MEC. Corso di FONDAMENTI DI CHIMICA I PROVA IN ITINERE 28 Gennaio 2010 Compito A
 POLITECNICO DI MILANO ING. ENG AER MEC. Corso di FONDAMENTI DI CHIMICA I PROVA IN ITINERE 28 Gennaio 2010 Compito A Avvertenze: scrivere le soluzioni sull apposito foglio che va completato con tutti i
POLITECNICO DI MILANO ING. ENG AER MEC. Corso di FONDAMENTI DI CHIMICA I PROVA IN ITINERE 28 Gennaio 2010 Compito A Avvertenze: scrivere le soluzioni sull apposito foglio che va completato con tutti i
