LICEO SCIENTIFICO G. BRUNO A.S. 2011/2012
|
|
|
- Gaspare Dolce
- 8 anni fa
- Visualizzazioni
Transcript
1 PROGRAMMA DI LABORATORIO DI CHIMICA SVOLTO NELLA CLASSE 1^ C Di seguito vengono elencate le attività teoriche e pratiche effettuate durante l anno scolastico: chimica. Lettura integrale delle norme di comportamento da osservare in laboratorio, finalizzate all ottenimento di un atteggiamento corretto, responsabile e consapevole sull attività da svolgere, improntata alla massima sicurezza ottenibile, anche attraverso l utilizzo corretto dei dispositivi di protezione individuale. 2. Presentazione della vetreria, della morsetteria e di alcune apparecchiature e strumenti di uso comune (piastre riscaldanti con agitatore magnetico, termometri digitali, cronometri e bilance tecniche). 3. Studio di alcuni parametri che caratterizzano la vetreria EX ed IN : classe, portata, sensibilità e tolleranza. 4. Misure di volume con la vetreria EX ed IN. 5. Letture di volume con la vetreria EX ed IN. 6. Determinazione della densità di una serie di corpi solidi irregolari, attraverso misure dirette della massa e indirette del volume. Raccolta e trasposizione dei dati su grafico cartesiano (indicazioni operative sulla corretta realizzazione dei grafici). 7. Determinazione della densità di una soluzione idroalcolica. Uso del densimetro a galleggiamento (modalità sulla correzione della lettura della densità). 8. Differenza calore/temperatura: uso corretto delle sonde digitali per la misura della temperatura e del cronometro. Raccolta dati e trasposizione degli stessi su grafico cartesiano. 9. Passaggi di stato: fusione e solidificazione di una sostanza pura. Raccolta dati e trasposizione degli stessi su grafico cartesiano. 10. Presentazione di alcune tecniche di separazione (filtrazione, cristallizzazione, centrifugazione, distillazione e cromatografia). 11. Separazione di un miscuglio binario solido-solido. 12. Separazione cromatografia di alcuni inchiostri. Renzo Lazzarini
2 PROGRAMMA DI LABORATORIO DI CHIMICA SVOLTO NELLA CLASSE 1^ D Di seguito vengono elencate le attività teoriche e pratiche effettuate durante l anno scolastico: chimica. Lettura integrale delle norme di comportamento da osservare in laboratorio, finalizzate all ottenimento di un atteggiamento corretto, responsabile e consapevole sull attività da svolgere, improntata alla massima sicurezza ottenibile, anche attraverso l utilizzo corretto dei dispositivi di protezione individuale. 2. Presentazione della vetreria, della morsetteria e di alcune apparecchiature e strumenti di uso comune (piastre riscaldanti con agitatore magnetico, termometri digitali, cronometri e bilance tecniche). 3. Studio di alcuni parametri che caratterizzano la vetreria EX ed IN : classe, portata, sensibilità e tolleranza. 4. Misure di volume con la vetreria EX ed IN. 5. Letture di volume con la vetreria EX ed IN. 6. Determinazione della densità di una serie di corpi solidi irregolari, attraverso misure dirette della massa e indirette del volume. Raccolta e trasposizione dei dati su grafico cartesiano (indicazioni operative sulla corretta realizzazione dei grafici). 7. Determinazione della densità di una soluzione idroalcolica. Uso del densimetro a galleggiamento (modalità sulla correzione della lettura della densità). 8. Differenza calore/temperatura: uso corretto delle sonde digitali per la misura della temperatura e del cronometro. Raccolta dati e trasposizione degli stessi su grafico cartesiano. 9. Passaggi di stato: fusione e solidificazione di una sostanza pura. Raccolta dati e trasposizione degli stessi su grafico cartesiano. 10. Presentazione di alcune tecniche di separazione (filtrazione, cristallizzazione, centrifugazione, distillazione e cromatografia). 11. Separazione di un miscuglio binario solido-solido. 12. Separazione cromatografia di alcuni inchiostri. Renzo Lazzarini
3 PROGRAMMA DI LABORATORIO DI CHIMICA 1^ F Di seguito vengono elencate le attività teoriche e pratiche effettuate durante l anno scolastico: chimica. Lettura integrale delle norme di comportamento da osservare in laboratorio, finalizzate all ottenimento di un atteggiamento corretto, responsabile e consapevole sull attività da svolgere, improntata alla massima sicurezza ottenibile, anche attraverso l utilizzo corretto dei dispositivi di protezione individuale. 2. Presentazione della vetreria e di alcune apparecchiature e strumenti di uso comune (piastre riscaldanti con agitatore magnetico, termometri digitali, cronometri e bilance tecniche). 3. Studio di alcuni parametri che caratterizzano la vetreria EX ed IN : classe, portata, sensibilità e tolleranza. 4. Misure di volume con la vetreria EX ed IN. 5. Letture di volume con la vetreria EX ed IN. 6. Determinazione della densità di una serie di corpi solidi irregolari, attraverso misure dirette della massa e indirette del volume. Raccolta e trasposizione dei dati su grafico cartesiano (indicazioni operative sulla corretta realizzazione dei grafici). 7. Determinazione della densità di una soluzione idroalcolica. Uso del densimetro a galleggiamento (modalità sulla correzione della lettura della densità). 8. Differenza calore/temperatura: uso corretto delle sonde digitali per la misura della temperatura e del cronometro. Raccolta dati e trasposizione degli stessi su grafico cartesiano. 9. Passaggi di stato: fusione e solidificazione di una sostanza pura. Raccolta dati e trasposizione degli stessi su grafico cartesiano. 10. Presentazione di alcune tecniche di separazione (filtrazione, cristallizzazione, centrifugazione, distillazione e cromatografia). 11. Separazione di un miscuglio binario solido-solido.
4 PROGRAMMA DI LABORATORIO DI CHIMICA SVOLTO NELLA CLASSE 2^ C Di seguito vengono elencati gli argomenti e le esercitazioni effettuate durante l anno scolastico: chimica. Lettura integrale delle norme di comportamento da osservare. 2. Consegna dei camici protettivi e dei dispositivi di protezione individuale e loro corretto impiego. 3. Introduzione ai principali macrofenomeni che accompagnano le trasformazioni chimiche. 4. Osservazione e interpretazione dei macrofenomeni che accompagnano alcune reazioni chimiche. 5. Verifica sperimentale della Legge di Lavoisier. Commenti sui risultati ottenuti. 6. Verifica sperimentale della legge di Proust. Commenti sui risultati ottenuti. 7. La concentrazione delle soluzioni. Ripresa delle unità fisiche della concentrazione. 8. Concetto di Molarità. Esempi di calcolo applicativo. 9. Modalità di preparazione delle soluzioni: partendo da soluto solido e per diluizione. 10. Esercizi sulla concentrazione delle soluzioni.
5 PROGRAMMA DI LABORATORIO DI CHIMICA SVOLTO NELLA CLASSE 2^ D Di seguito vengono elencati gli argomenti e le esercitazioni effettuate durante l anno scolastico: chimica. Lettura integrale delle norme di comportamento da osservare. 2. Consegna dei camici protettivi e dei dispositivi di protezione individuale e loro corretto impiego. 3. Introduzione ai principali macrofenomeni che accompagnano le trasformazioni chimiche. 4. Osservazione e interpretazione dei macrofenomeni che accompagnano alcune reazioni chimiche. 5. Verifica sperimentale della Legge di Lavoisier. Commenti sui risultati ottenuti. 6. Verifica sperimentale della legge di Proust. Commenti sui risultati ottenuti. 7. La concentrazione delle soluzioni. Ripresa delle unità fisiche della concentrazione. 8. Concetto di Molarità. Esempi di calcolo applicativo. 9. Modalità di preparazione delle soluzioni: partendo da soluto solido e per diluizione. 10. Esercizi sulla concentrazione delle soluzioni.
6 PROGRAMMA DI LABORATORIO DI CHIMICA SVOLTO NELLA CLASSE 2^ F Di seguito vengono elencati gli argomenti e le esercitazioni effettuate durante l anno scolastico: chimica. Lettura integrale delle norme di comportamento da osservare. 2. Consegna dei camici protettivi e dei dispositivi di protezione individuale e loro corretto impiego. 3. Introduzione ai principali macrofenomeni che accompagnano le trasformazioni chimiche. 4. Osservazione e interpretazione dei macrofenomeni che accompagnano alcune reazioni chimiche. 5. Verifica sperimentale della Legge di Lavoisier. Commenti sui risultati ottenuti. 6. Verifica sperimentale della legge di Proust. Commenti sui risultati ottenuti. 7. La concentrazione delle soluzioni. Ripresa delle unità fisiche della concentrazione. 8. Concetto di Molarità. Esempi di calcolo applicativo. 9. Modalità di preparazione delle soluzioni: partendo da soluto solido e per diluizione. 10. Esercizi sulla concentrazione delle soluzioni.
7 PROGRAMMA DI LABORATORIO DI CHIMICA SVOLTO NELLA CLASSE 3^ B Di seguito vengono elencate gli argomenti svolti e le esercitazioni effettuate durante l anno scolastico: chimica; norme di comportamento da osservare e utilizzo corretto dei dispositivi di protezione individuale. 2. Fattori di rischio e classi di pericolosità dei reagenti chimici: simbologia e pittogrammi. Significato delle frasi di rischio e di sicurezza (frasi H e P). Le schede di sicurezza dei reagenti chimici. 3. Osservazione e studio dei principali macrofenomeni che accompagnano le trasformazioni chimiche. 4. Verifica sperimentale della Legge di Lavoisier. 5. Studio della reattività dei metalli del 1 e 2 gruppo della tavola periodica. 6. Le unità di misura chimiche della concentrazione: Molarità, Normalità e Molalità: concetto di mole, di massa equivalente e definizione dei criteri per la determinazione del n eq/mole per acidi, basi e sali. Esercizi applicativi. 7. Esercizi applicativi sulla concentrazione delle soluzioni. 8. Preparazione di soluzioni partendo da soluto solido. 9. Preparazione di soluzioni per diluizione. 10. Preparazione di soluzioni per mescolamento. 11. Esercizi applicativi sulle tre modalità di preparazione delle soluzioni. 12. Non additività dei volumi in una soluzione e contrazione di volume nelle soluzioni: cause e conseguenze sul piano pratico nella preparazione delle soluzioni; volume reale e virtuale delle soluzioni. Esercizi applicativi. 13. Misure di ph con cartine indicatrici a scala cromatica. 14. Titolazioni di una base forte con un acido forte: costruzione della curva di titolazione con il phmetro; calcolo del ph teorico fino al punto di equivalenza e dopo il punto di equivalenza. 15. Studio della curva di titolazione e scelta degli indicatori per effettuare la titolazione. 16. Determinazione del titolo di una soluzione di NaOH.
8 PROGRAMMA DI LABORATORIO DI CHIMICA SVOLTO NELLA CLASSE 3^ C Di seguito vengono elencate gli argomenti svolti e le esercitazioni effettuate durante l anno scolastico: chimica; norme di comportamento da osservare e utilizzo corretto dei dispositivi di protezione individuale. 2. Fattori di rischio e classi di pericolosità dei reagenti chimici: simbologia e pittogrammi. Significato delle frasi di rischio e di sicurezza (frasi H e P). Le schede di sicurezza dei reagenti chimici. 3. Osservazione e studio dei principali macrofenomeni che accompagnano le trasformazioni chimiche. 4. Studio della reattività dei metalli del 1 e 2 gruppo della tavola periodica. 5. Verifica sperimentale della Legge di Lavoisier. 6. Le unità di misura chimiche della concentrazione: Molarità e Normalità: concetto di mole, di massa equivalente e definizione dei criteri per la determinazione del n eq/mole per acidi, basi e sali. Esercizi applicativi. 7. Esercizi applicativi sulla concentrazione delle soluzioni. 8. Preparazione di soluzioni partendo da soluto solido. 9. Preparazione di soluzioni per diluizione. 10. Preparazione di soluzioni per mescolamento. 11. Esercizi applicativi sulle tre modalità di preparazione delle soluzioni. 12. Non additività dei volumi in una soluzione e contrazione di volume nelle soluzioni: cause e conseguenze sul piano pratico nella preparazione delle soluzioni; volume reale e virtuale delle soluzioni. Esercizi applicativi. 13. Introduzione ai principali fattori che influenzano la velocità di reazione: concentrazione, temperatura. 14. Misure di ph con cartine indicatrici a scala cromatica. 15. Titolazioni di una base forte con un acido forte: costruzione della curva di titolazione con il phmetro; calcolo del ph teorico fino al punto di equivalenza e dopo il punto di equivalenza. 16. Studio della curva di titolazione e scelta degli indicatori per effettuare la titolazione. 17. Determinazione del titolo di una soluzione di NaOH. Mestre 06/06/2012
9 PROGRAMMA DI LABORATORIO DI CHIMICA SVOLTO NELLA CLASSE 3^ F Di seguito vengono elencate gli argomenti svolti e le esercitazioni effettuate durante l anno scolastico: chimica; norme di comportamento da osservare e utilizzo corretto dei dispositivi di protezione individuale. 2. Fattori di rischio e classi di pericolosità dei reagenti chimici: simbologia e pittogrammi. Significato delle frasi di rischio e di sicurezza (frasi H e P). Le schede di sicurezza dei reagenti chimici. 3. Osservazione e studio dei principali macrofenomeni che accompagnano le trasformazioni chimiche. 4. Verifica sperimentale della Legge di Lavoisier. 5. Studio della reattività dei metalli del 1 e 2 gruppo della tavola periodica. 6. Le unità di misura chimiche della concentrazione: Molarità, Normalità e Molalità: concetto di mole, di massa equivalente e definizione dei criteri per la determinazione del n eq/mole per acidi, basi e sali. Esercizi applicativi. 7. Esercizi applicativi sulla concentrazione delle soluzioni. 8. Preparazione di soluzioni partendo da soluto solido. 9. Preparazione di soluzioni per diluizione. 10. Preparazione di soluzioni per mescolamento. 11. Esercizi applicativi sulle tre modalità di preparazione delle soluzioni. 12. Non additività dei volumi in una soluzione e contrazione di volume nelle soluzioni: cause e conseguenze sul piano pratico nella preparazione delle soluzioni; volume reale e virtuale delle soluzioni. Esercizi applicativi. 13. Prove di conducibilità elettrica: conduttori di 1^ e 2^ specie; elettroliti forti e deboli; influenza della concentrazione sulla conducibilità (per legame ionico) 14. Prove di miscibilità liquidi polari e apolari; influenza del campo elettrostatico sui liquidi polari (per legame covalente polare) 15. Studio dei principali fattori che influenzano la velocità di reazione: concentrazione, temperatura. 16. Misure di ph con cartine indicatrici a scala cromatica. 17. Titolazioni di una base forte con un acido forte: costruzione della curva di titolazione con il phmetro; calcolo del ph teorico fino al punto di equivalenza e dopo il punto di equivalenza. 18. Studio della curva di titolazione e scelta degli indicatori per effettuare la titolazione. 19. Determinazione del titolo di una soluzione di NaOH.
10 PROGRAMMA DI LABORATORIO DI CHIMICA SVOLTO NELLA CLASSE 4^ A Di seguito vengono elencate gli argomenti svolti e le esercitazioni effettuate durante l anno scolastico: chimica; norme di comportamento da osservare e utilizzo corretto dei dispositivi di protezione individuale. 2. Fattori di rischio e classi di pericolosità dei reagenti chimici: simbologia e pittogrammi. Significato delle frasi di rischio e di sicurezza ( frasi H e P). Le schede di sicurezza dei reagenti chimici. 3. Presentazione della vetreria, di alcune apparecchiature e strumenti di uso comune. 4. Determinazione della composizione ponderale di un miscuglio binario; 5. Osservazione e studio dei principali macrofenomeni che accompagnano le trasformazioni chimiche. 6. Studio della reattività dei metalli del 1 e 2 gruppo della tavola periodica. 7. Verifica sperimentale della Legge di Lavoisier. 8. Modalità di preparazione delle soluzioni: partendo da soluto solido e per diluizione. 9. Esercizi applicativi sulla concentrazione delle soluzioni. 10. Introduzione allo studio dei principali fattori che influenzano la velocità di reazione: concentrazione e temperatura. 11. Verifica della Legge di Charles. 12. Misure di ph con le cartine tornasole. 13. Curva di titolazione acido forte/base forte. 14. Presentazione titolazione e scelta degli indicatori di ph. 15. Titolazione acido forte/base forte. Mestre 06/06/2012
11 PROGRAMMA DI LABORATORIO DI CHIMICA 4^ B Di seguito vengono elencati gli argomenti e le esercitazioni effettuate durante l anno scolastico: chimica; norme di comportamento da osservare e utilizzo corretto dei dispositivi di protezione individuale. 2. Fattori di rischio e classi di pericolosità dei reagenti chimici: simbologia e pittogrammi. Significato delle frasi di rischio e di sicurezza (frasi H e P). Le schede di sicurezza dei reagenti chimici. 3. Introduzione all analisi volumetrica: termini concettuali e aspetti procedurali. 4. Curva di titolazione acido forte/base forte. 5. Titolazione acido forte/base forte e scelta degli indicatori di ph. 6. Determinazione del titolo di una soluzione di NaOH. 7. Determinazione dell acidità totale di un aceto per uso alimentare. 8. Titolazioni red-ox: determinazione della concentrazione dell acqua ossigenata commerciale. 9. Introduzione all elettrochimica: le reazioni di ossidoriduzione. 10. La Pila Daniell. Realizzazione di un sistema elettrochimico in serie. Funzione del ponte salino; calcolo della f.e.m Elettrolisi dell acqua e funzionamento del voltametro di Hoffman. 12. Introduzione alla calorimetria: determinazione della capacità termica di un calorimetro. 13. Verifica sperimentale della Legge di Hess. 14. Potere riducente dei glucidi. 15. Determinazione volumetrica del glucosio con il reattivo di Fehling.
12 PROGRAMMA DI LABORATORIO DI CHIMICA SVOLTO NELLA CLASSE 4^ C Di seguito vengono elencate gli argomenti svolti e le esercitazioni effettuate durante l anno scolastico: chimica; norme di comportamento da osservare in laboratorio e utilizzo corretto dei dispositivi di protezione individuale. 2. Fattori di rischio e classi di pericolosità dei reagenti chimici: simbologia e pittogrammi. Significato delle frasi di rischio e di sicurezza (frasi H e P). Le schede di sicurezza dei reagenti chimici. 3. Presentazione e modalità di impiego dei dispositivi di protezione individuali (DPI) e consegna dei camici protettivi. 4. Presentazione della vetreria, di alcune apparecchiature e strumenti di uso comune. 5. Parametri e caratteristiche della vetreria: EX e IN. 6. Misure di volume con la vetreria IN ed EX 7. Introduzione alle principali tecniche di separazione. 8. Determinazione della composizione ponderale di un miscuglio binario; 9. Osservazione e interpretazione dei principali macrofenomeni che accompagnano le trasformazioni chimiche. 10. Verifica sperimentale della Legge di Lavoisier. 11. Verifica sperimentale della legge di Proust. 12. Reattività in acqua dei metalli del 1 e del 2 gruppo. 13. Modalità di preparazione delle soluzioni: partendo da soluto solido e per diluizione. Mestre 06/06/2012
13 PROGRAMMA DI LABORATORIO DI CHIMICA SVOLTO NELLA CLASSE 4^ E Di seguito vengono elencate gli argomenti svolti e le esercitazioni effettuate durante l anno scolastico: chimica; norme di comportamento da osservare. Presentazione e modalità di impiego dei Dispositivi di Protezione Individuali e consegna dei camici protettivi. 2. Fattori di rischio e classi di pericolosità dei reagenti chimici: simbologia e pittogrammi. Significato delle frasi di rischio e di sicurezza (frasi H e P). Le schede di sicurezza dei reagenti chimici. 3. Presentazione della vetreria, di alcune apparecchiature e strumenti di uso comune. 4. Parametri e caratteristiche della vetreria: EX e IN. 5. Misure di volume con la vetreria IN ed EX 6. Introduzione alle principali tecniche di separazione. 7. Determinazione della composizione ponderale di un miscuglio binario; 8. Osservazione e interpretazione dei principali macrofenomeni che accompagnano le trasformazioni chimiche. 9. Verifica sperimentale della Legge di Lavoisier. 10. Modalità di preparazione delle soluzioni: partendo da soluto solido e per diluizione. 11. Misure di ph con le cartine tornasole. 12. Introduzione ai principali fattori che influenzano la velocità di reazione: concentrazione e temperatura. 13. Osservazione e studio di alcune reazioni di ossidoriduzione.
14 PROGRAMMA DI LABORATORIO DI CHIMICA 4^ F Di seguito vengono elencate le attività teoriche e pratiche (esercitazioni) effettuate durante l anno scolastico: chimica; norme di comportamento da osservare e utilizzo corretto dei dispositivi di protezione individuale. 2. Fattori di rischio e classi di pericolosità dei reagenti chimici: simbologia e pittogrammi. Significato delle frasi di rischio e di sicurezza (frasi H e P). Le schede di sicurezza dei reagenti chimici. 3. Introduzione all analisi volumetrica: termini concettuali e aspetti procedurali. 4. Curva di titolazione acido forte/base forte. 5. Titolazione acido forte/base forte e scelta degli indicatori di ph. 6. Determinazione del titolo di una soluzione di NaOH. 7. Determinazione dell acidità totale di un aceto per uso alimentare. 8. Titolazioni red-ox: determinazione della concentrazione dell acqua ossigenata commerciale. 9. Introduzione all elettrochimica: le reazioni di ossidoriduzione. 10. La Pila Daniell. Realizzazione di un sistema elettrochimico in serie. Funzione del ponte salino; calcolo della f.e.m Elettrolisi dell acqua e funzionamento del voltametro di Hoffman. 12. Introduzione alla calorimetria: determinazione della capacità termica di un calorimetro. 13. Verifica sperimentale della Legge di Hess. 14. Potere riducente dei glucidi. 15. Determinazione volumetrica del glucosio con il reattivo di Fehling. 16. Introduzione alle analisi delle acque minerali e loro classificazione. 17. Determinazione complessometrica della durezza di un acqua minerale con EDTA. 18. Determinazione dell alcalinità totale di un acqua minerale.
15 PROGRAMMA DI LABORATORIO DI CHIMICA SVOLTO NELLA CLASSE 4^ G Di seguito vengono elencate gli argomenti svolti e le esercitazioni effettuate durante l anno scolastico: chimica; norme di comportamento da osservare in laboratorio e utilizzo corretto dei dispositivi di protezione individuale. 2. Fattori di rischio e classi di pericolosità dei reagenti chimici: simbologia e pittogrammi. Significato delle frasi di rischio e di sicurezza ( frasi H e P). Le schede di sicurezza dei reagenti chimici. 3. Presentazione e modalità di impiego dei dispositivi di protezione individuali (DPI) e consegna dei camici protettivi. 4. Presentazione della vetreria, di alcune apparecchiature e strumenti di uso comune. 5. Parametri e caratteristiche della vetreria: EX e IN. 6. Misure di volume con la vetreria IN ed EX 7. Introduzione alle principali tecniche di separazione. 8. Determinazione della composizione ponderale di un miscuglio binario; 9. Osservazione e interpretazione dei principali macrofenomeni che accompagnano le trasformazioni chimiche. 10. Verifica sperimentale della Legge di Lavoisier. 11. Modalità di preparazione delle soluzioni: partendo da soluto solido, per diluizione e per mescolamento. 12. Esercizi applicativi sulla concentrazione delle soluzioni. 13. Introduzione ai principali fattori che influenzano la velocità di reazione: concentrazione, temperatura. e catalizzatore 14. Misure di ph con le cartine tornasole. 15. Curva di titolazione acido forte/base forte. 16. Presentazione titolazione e scelta degli indicatori di ph. 17. Titolazione acido forte/base forte. Mestre 06/06/2012
TAVOLA DI PROGRAMMAZIONE PER GRUPPI DIDATTICI
 TAVOLA DI PROGRAMMAZIONE PER GRUPPI DIDATTICI MATERIA: CHIMICA CLASSI: PRIME I II QUADRIMESTRE Competenze Abilità/Capacità Conoscenze* Attività didattica Strumenti Tipologia verifiche Osservare, descrivere
TAVOLA DI PROGRAMMAZIONE PER GRUPPI DIDATTICI MATERIA: CHIMICA CLASSI: PRIME I II QUADRIMESTRE Competenze Abilità/Capacità Conoscenze* Attività didattica Strumenti Tipologia verifiche Osservare, descrivere
DIPARTIMENTO DI SCIENZE INTEGRATE CHIMICA FISICA SCIENZE DELLA TERRA - BIOLOGIA
 IISS A. De Pace Lecce A.S. 2012-2013 DIPARTIMENTO DI SCIENZE INTEGRATE FISICA SCIENZE DELLA TERRA - BIOLOGIA PIANI DI STUDIO DELLE DISCIPLINE SECONDO ANNO Piano di studi della disciplina DESCRIZIONE Lo
IISS A. De Pace Lecce A.S. 2012-2013 DIPARTIMENTO DI SCIENZE INTEGRATE FISICA SCIENZE DELLA TERRA - BIOLOGIA PIANI DI STUDIO DELLE DISCIPLINE SECONDO ANNO Piano di studi della disciplina DESCRIZIONE Lo
Programmazione individuale di Laboratorio Materia : Chimica e Laboratorio. Docenti : Giancarlo Cardone Classe : 2 CAT a.s.
 Programmazione individuale di Laboratorio Materia : Chimica e Laboratorio. Docenti : Giancarlo Cardone Classe : 2 CAT a.s. 2015-2016 Mondovi 05/11/2015 Prof. Giancarlo Cardone PROGRAMMAZIONE DELL ATTIVITA
Programmazione individuale di Laboratorio Materia : Chimica e Laboratorio. Docenti : Giancarlo Cardone Classe : 2 CAT a.s. 2015-2016 Mondovi 05/11/2015 Prof. Giancarlo Cardone PROGRAMMAZIONE DELL ATTIVITA
ISTITUTO ISTRUZIONE SUPERIORE "L. EINAUDI" ALBA ANNO SCOLASTICO 2015/2016
 ISTITUTO ISTRUZIONE SUPERIORE "L. EINAUDI" ALBA ANNO SCOLASTICO 2015/2016 Classe II^ D COSTRUZIONI AMBIENTE E TERRITORIO Disciplina : SCIENZE INTEGRATE CHIMICA E LABORATORIO PROGETTAZIONE DIDATTICA ANNUALE
ISTITUTO ISTRUZIONE SUPERIORE "L. EINAUDI" ALBA ANNO SCOLASTICO 2015/2016 Classe II^ D COSTRUZIONI AMBIENTE E TERRITORIO Disciplina : SCIENZE INTEGRATE CHIMICA E LABORATORIO PROGETTAZIONE DIDATTICA ANNUALE
Programmazione annuale docente classi 2^A AM 2^B AM 2^C AM
 Programmazione annuale docente classi 2^A AM 2^B AM 2^C AM Docente : Macaluso Maria Annunziata Classe : 2^ sez.a B - C Indirizzo AM Materia di insegnamento : Scienze Integrate (CHIMICA) Libro di testo
Programmazione annuale docente classi 2^A AM 2^B AM 2^C AM Docente : Macaluso Maria Annunziata Classe : 2^ sez.a B - C Indirizzo AM Materia di insegnamento : Scienze Integrate (CHIMICA) Libro di testo
Esercitazione 8. Gli equilibri acido-base: Ka, Kb. L autoprotolisi dell acqua. Misura del ph Soluzioni tampone 1,0 10-14
 Esercitazione 8 Misura del ph Soluzioni tampone Gli equilibri acido-base: Ka, Kb HA + H 2 O! H 3 O + + A - Ka = [H 3 O+ ][A - ] [HA] A - + H 2 O! OH - + HA Kb = [OH- ][HA] [A - ] Ka Kb = [ H 3 O + ] [
Esercitazione 8 Misura del ph Soluzioni tampone Gli equilibri acido-base: Ka, Kb HA + H 2 O! H 3 O + + A - Ka = [H 3 O+ ][A - ] [HA] A - + H 2 O! OH - + HA Kb = [OH- ][HA] [A - ] Ka Kb = [ H 3 O + ] [
PIANO DI LAVORO ANNUALE
 Docenti Materia Classi Alessandra Cattaneo Erminia Palma Scienze Integrate (Chimica) biennio PIANO DI LAVORO ANNUALE 1. Finalità Promuovere negli allievi lo sviluppo e il perfezionamento delle capacità
Docenti Materia Classi Alessandra Cattaneo Erminia Palma Scienze Integrate (Chimica) biennio PIANO DI LAVORO ANNUALE 1. Finalità Promuovere negli allievi lo sviluppo e il perfezionamento delle capacità
Esperienza A: idrofilicità e idrofobicità
 Esperienza A: idrofilicità e idrofobicità Obiettivo: Fare osservare che alcune sostanze, mescolate all'acqua, danno luogo a soluzioni omogenee mentre altre danno miscele eterogenee. Dalla descrizione delle
Esperienza A: idrofilicità e idrofobicità Obiettivo: Fare osservare che alcune sostanze, mescolate all'acqua, danno luogo a soluzioni omogenee mentre altre danno miscele eterogenee. Dalla descrizione delle
ISTITUTO TECNICO NAUTICO "L. GIOVANNI LIZZIO PROF. SALVATORE GRASSO PROGRAMMA SVOLTO MODULO 0 : "RICHIAMI RELATIVI AL PRIMO ANNO"
 1 ISTITUTO TECNICO NAUTICO "L. RIZZO" - RIPOSTO ------------------------------------ ANNO SCOLASTICO : 2014-2015 CLASSE : SECONDA SEZIONE : D MATERIA D'INSEGNAMENTO : FISICA E LABORATORIO DOCENTI : PROF.
1 ISTITUTO TECNICO NAUTICO "L. RIZZO" - RIPOSTO ------------------------------------ ANNO SCOLASTICO : 2014-2015 CLASSE : SECONDA SEZIONE : D MATERIA D'INSEGNAMENTO : FISICA E LABORATORIO DOCENTI : PROF.
Programma (piano di lavoro) preventivo
 I S T I T U T O T E C N I C O I N D U S T R I A L E S T A T A L E G u g l i e l m o M a r c o n i V e r o n a Programma (piano di lavoro) preventivo Anno Scolastico 2014/2015 Materia SCIENZE INTEGRATE:
I S T I T U T O T E C N I C O I N D U S T R I A L E S T A T A L E G u g l i e l m o M a r c o n i V e r o n a Programma (piano di lavoro) preventivo Anno Scolastico 2014/2015 Materia SCIENZE INTEGRATE:
Progettazione disciplinare:
 PIANO DI LAVORO ANNUALE-PROGETTAZIONE INDIVIDUALE PER SINGOLA DISCIPLINA E PER CLASSE Classe 1A A.S. 2015/2016 Disciplina: CHIMICA Docente: Rosselli Antonino Ore settimanali: 3 (1 di laboratorio) Libro
PIANO DI LAVORO ANNUALE-PROGETTAZIONE INDIVIDUALE PER SINGOLA DISCIPLINA E PER CLASSE Classe 1A A.S. 2015/2016 Disciplina: CHIMICA Docente: Rosselli Antonino Ore settimanali: 3 (1 di laboratorio) Libro
Le reazioni di ossidoriduzione
 I.S. G. TASSINARI PROGRAMMAZIONE di CHIMICA ANALITICA E STUMENTALE Classe 4L - A.S. 2015-16 Docenti: prof.ssa Stefania Comes- prof.ssa Anna Alfano ANALISI INIZIALE DELLA CLASSE: La classe risulta composta
I.S. G. TASSINARI PROGRAMMAZIONE di CHIMICA ANALITICA E STUMENTALE Classe 4L - A.S. 2015-16 Docenti: prof.ssa Stefania Comes- prof.ssa Anna Alfano ANALISI INIZIALE DELLA CLASSE: La classe risulta composta
Programmazione individuale per competenze CLASSE 3^B LSA. Materia: CHIMICA
 Programmazione individuale per competenze CLASSE 3^B LSA Materia: CHIMICA Situazione della classe Accordi con la classe Accordi con le altre discipline Correlazione con i progetti proposti alla classe
Programmazione individuale per competenze CLASSE 3^B LSA Materia: CHIMICA Situazione della classe Accordi con la classe Accordi con le altre discipline Correlazione con i progetti proposti alla classe
Domanda 1 Quesiti preliminari
 Domanda 1 Quesiti preliminari 1.1 A che temperatura bolle l acqua nella vostra aula di scienze? 1.2 Se in una pentola senza coperchio posta su di un fornello ho dell acqua che bolle e continuo a riscaldare,
Domanda 1 Quesiti preliminari 1.1 A che temperatura bolle l acqua nella vostra aula di scienze? 1.2 Se in una pentola senza coperchio posta su di un fornello ho dell acqua che bolle e continuo a riscaldare,
... corso di chimica elettrochimica 1
 ... corso di chimica elettrochimica 1 CONTENUTI reazioni elettrochimiche pile e celle elettrolitiche potenziale d elettrodo e forza elettromotrice equazione di Nernst elettrolisi leggi di Faraday batterie
... corso di chimica elettrochimica 1 CONTENUTI reazioni elettrochimiche pile e celle elettrolitiche potenziale d elettrodo e forza elettromotrice equazione di Nernst elettrolisi leggi di Faraday batterie
PIANO DI STUDIO DELLA DISCIPLINA
 Modulo Gestione Qualità UNI EN ISO 9001 : 2008 Tel. 0331635718 fax 0331679586 info@isisfacchinetti.it www.isisfacchinetti.it PIANO STUDIO DELLA DISCIPLINA PIANO DI STUDIO DELLA DISCIPLINA Chimica Analitica
Modulo Gestione Qualità UNI EN ISO 9001 : 2008 Tel. 0331635718 fax 0331679586 info@isisfacchinetti.it www.isisfacchinetti.it PIANO STUDIO DELLA DISCIPLINA PIANO DI STUDIO DELLA DISCIPLINA Chimica Analitica
Esercizi di Chimica (2 a prova in itinere)
 Esercizi di Chimica (2 a prova in itinere) 3) Calcolare la normalità (N) di una soluzione ottenuta sciogliendo 3,5 g di H 3 PO 4 in 900 ml di acqua [0,119 N] 4) Quanti grammi di soluto sono contenuti in
Esercizi di Chimica (2 a prova in itinere) 3) Calcolare la normalità (N) di una soluzione ottenuta sciogliendo 3,5 g di H 3 PO 4 in 900 ml di acqua [0,119 N] 4) Quanti grammi di soluto sono contenuti in
I.S.I.S. Zenale e Butinone di Treviglio Dipartimento di Scienze integrate anno scolastico 2013/14
 I.S.I.S. Zenale e Butinone di Treviglio Dipartimento di Scienze integrate anno scolastico 2013/14 KIT RECUPERO SCIENZE INTEGRATE FISICA CLASSI SECONDE TECNICO GRAFICO SUPPORTO DIDATTICO PER ALUNNI CON
I.S.I.S. Zenale e Butinone di Treviglio Dipartimento di Scienze integrate anno scolastico 2013/14 KIT RECUPERO SCIENZE INTEGRATE FISICA CLASSI SECONDE TECNICO GRAFICO SUPPORTO DIDATTICO PER ALUNNI CON
REAZIONI ESOTERMICHE ED ENDOTERMICHE
 REAZIONI ESOTERMICHE ED ENDOTERMICHE Obiettivo di questo esperimento è confrontare l effetto termico di 0,1 moli di diverse sostanze ioniche solide quando vengono sciolte in una stessa quantità di acqua.
REAZIONI ESOTERMICHE ED ENDOTERMICHE Obiettivo di questo esperimento è confrontare l effetto termico di 0,1 moli di diverse sostanze ioniche solide quando vengono sciolte in una stessa quantità di acqua.
ISTITUTO TECNICO INDUSTRIALE STATALE. B.Pascal Roma
 Ministero dell Istruzione, dell Università e della Ricerca ISTITUTO TECNICO INDUSTRIALE STATALE B.Pascal Roma Anno Scolastico 2012-201 PIANO DI LAVORO DELLE CLASSI PRIME MATERIA: Scienze Integrate CHIMICA
Ministero dell Istruzione, dell Università e della Ricerca ISTITUTO TECNICO INDUSTRIALE STATALE B.Pascal Roma Anno Scolastico 2012-201 PIANO DI LAVORO DELLE CLASSI PRIME MATERIA: Scienze Integrate CHIMICA
Esperimenti per gioco. Progetto realizzato dagli alunni del liceo O.M. Corbino.
 Esperimenti per gioco Progetto realizzato dagli alunni del liceo O.M. Corbino. Il progetto ha lo scopo di avvicinare i ragazzi al mondo della scienza tramite lo svolgimento di semplici esperienze di laboratorio
Esperimenti per gioco Progetto realizzato dagli alunni del liceo O.M. Corbino. Il progetto ha lo scopo di avvicinare i ragazzi al mondo della scienza tramite lo svolgimento di semplici esperienze di laboratorio
PROGRAMMAZIONE DIDATTICA ANNUALE
 PROGRAMMAZIONE DIDATTICA ANNUALE Anno Scolastico: 2013 / 2014 Dipartimento (1) : Scienze - Chimica Coordinatore (1) : Classe: Prof. Giovanni MIRAGLIOTTA 2^B.G, Q Indirizzo: Economico aziendale; servizi
PROGRAMMAZIONE DIDATTICA ANNUALE Anno Scolastico: 2013 / 2014 Dipartimento (1) : Scienze - Chimica Coordinatore (1) : Classe: Prof. Giovanni MIRAGLIOTTA 2^B.G, Q Indirizzo: Economico aziendale; servizi
Dissociazione elettrolitica
 Dissociazione elettrolitica Le sostanze ioniche si solubilizzano liberando ioni in soluzione. La dissociazione elettrolitica è il processo con cui un solvente separa ioni di carica opposta e si lega ad
Dissociazione elettrolitica Le sostanze ioniche si solubilizzano liberando ioni in soluzione. La dissociazione elettrolitica è il processo con cui un solvente separa ioni di carica opposta e si lega ad
Laboratori classi prime (in rosso le variazioni in corso d anno)
 Laboratori classi prime (in rosso le variazioni in corso d anno) Argomenti Obiettivi Metodi Verifiche 1) Norme di sicurezza Conoscere il luogo di lavoro ( laboratorio di chimica) Conoscere e applicare
Laboratori classi prime (in rosso le variazioni in corso d anno) Argomenti Obiettivi Metodi Verifiche 1) Norme di sicurezza Conoscere il luogo di lavoro ( laboratorio di chimica) Conoscere e applicare
Prova in itinere di Chimica Generale 1 Giugno 2011
 Prova in itinere di Chimica Generale 1 Giugno 2011 A COGNOME NOME. MATRICOLA 1 2 3 4 5 6 7 8 Indicazioni per lo svolgimento del compito. Scrivete il vostro Nome e Cognome in STAMPATELLO su ciascuno di
Prova in itinere di Chimica Generale 1 Giugno 2011 A COGNOME NOME. MATRICOLA 1 2 3 4 5 6 7 8 Indicazioni per lo svolgimento del compito. Scrivete il vostro Nome e Cognome in STAMPATELLO su ciascuno di
La corrente elettrica La resistenza elettrica La seconda legge di Ohm Resistività e temperatura L effetto termico della corrente
 Unità G16 - La corrente elettrica continua La corrente elettrica La resistenza elettrica La seconda legge di Ohm Resistività e temperatura L effetto termico della corrente 1 Lezione 1 - La corrente elettrica
Unità G16 - La corrente elettrica continua La corrente elettrica La resistenza elettrica La seconda legge di Ohm Resistività e temperatura L effetto termico della corrente 1 Lezione 1 - La corrente elettrica
Metodo III.1. Determinazione dell umidità. 1. Determinazione dell umidità nei fertilizzanti che non contengono sostanze volatili diverse dall acqua
 METODI III METODI DI DETERMINAZIONE DELL UMIDITA, GRANULOMETRIA, ph e SALINITA Metodo III.1 Determinazione dell umidità 1. Determinazione dell umidità nei fertilizzanti che non contengono sostanze volatili
METODI III METODI DI DETERMINAZIONE DELL UMIDITA, GRANULOMETRIA, ph e SALINITA Metodo III.1 Determinazione dell umidità 1. Determinazione dell umidità nei fertilizzanti che non contengono sostanze volatili
Determinazione del pka per un acido moderatamente debole per via potenziometrica C.Tavagnacco - versione 02.02.05
 Determinazione del pka per un acido moderatamente debole per via potenziometrica C.Tavagnacco - versione 02.02.05 Dall equazione di Henderson-Hasselbalch (H-H), ph = pka + log ([A - ]/[HA]) si ricava che
Determinazione del pka per un acido moderatamente debole per via potenziometrica C.Tavagnacco - versione 02.02.05 Dall equazione di Henderson-Hasselbalch (H-H), ph = pka + log ([A - ]/[HA]) si ricava che
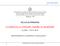
Cosa misura il ph: la concentrazione di ioni H +, che si scrive [H + ]. La definizione di ph è: ph = -log 10 [H + ]
![Cosa misura il ph: la concentrazione di ioni H +, che si scrive [H + ]. La definizione di ph è: ph = -log 10 [H + ] Cosa misura il ph: la concentrazione di ioni H +, che si scrive [H + ]. La definizione di ph è: ph = -log 10 [H + ]](/thumbs/34/16945364.jpg) La molecola d acqua è un dipolo perché l atomo di ossigeno è molto elettronegativo ed attira più vicini a sé gli elettroni di legame. Questo, unito alla forma della molecola, produce un accumulo di carica
La molecola d acqua è un dipolo perché l atomo di ossigeno è molto elettronegativo ed attira più vicini a sé gli elettroni di legame. Questo, unito alla forma della molecola, produce un accumulo di carica
MATRICE DELLE COMPETENZE DI SCIENZE E TECNOLIE APPLICATE INDIRIZZO DI MECCANICA, MECCATRONICA ED ENERGIA
 MATRICE DELLE COMPETENZE DI SCIENZE E TECNOLIE APPLICATE INDIRIZZO DI MECCANICA, MECCATRONICA ED ENERGIA Competenze in esito al quinquennio (dall Allegato C del Regolamento) 1. Individuare le proprietà
MATRICE DELLE COMPETENZE DI SCIENZE E TECNOLIE APPLICATE INDIRIZZO DI MECCANICA, MECCATRONICA ED ENERGIA Competenze in esito al quinquennio (dall Allegato C del Regolamento) 1. Individuare le proprietà
Programmazione esperimenti di laboratorio
 Ministero dell'istruzione Università e Ricerca Liceo Scientifico Statale Niccolò Rodolico sede: via A.Baldovinetti, 5-50142 Firenze tel. 055.70.24.47 Fax. 055.70.24.91 e-mail: info@liceorodolico.it e-mail
Ministero dell'istruzione Università e Ricerca Liceo Scientifico Statale Niccolò Rodolico sede: via A.Baldovinetti, 5-50142 Firenze tel. 055.70.24.47 Fax. 055.70.24.91 e-mail: info@liceorodolico.it e-mail
Esperienza 15: taratura. della termocoppia. Laboratorio di Fisica 1 (II Modulo) A. Baraldi, M. Riccò. Università di Parma. a.a.
 Esperienza 15: taratura Università di Parma della termocoppia a.a. 2011/2012 Laboratorio di Fisica 1 (II Modulo) A. Baraldi, M. Riccò Copyright M.Solzi Obiettivi dell esperienza Scopo dell'esperienza è
Esperienza 15: taratura Università di Parma della termocoppia a.a. 2011/2012 Laboratorio di Fisica 1 (II Modulo) A. Baraldi, M. Riccò Copyright M.Solzi Obiettivi dell esperienza Scopo dell'esperienza è
Corso di Laboratorio di Chimica Generale Esperienza 6: ph, sua misura e applicazioni
 Corso di Laboratorio di Chimica Generale Esperienza 6: ph, sua misura e applicazioni Una delle più importanti proprietà di una soluzione acquosa è la sua concentrazione di ioni idrogeno. Lo ione H + o
Corso di Laboratorio di Chimica Generale Esperienza 6: ph, sua misura e applicazioni Una delle più importanti proprietà di una soluzione acquosa è la sua concentrazione di ioni idrogeno. Lo ione H + o
CURRICOLO DISCIPLINARE DI SCIENZE
 A.S. 2014/2015 MINISTERO DELL ISTRUZIONE DELL UNIVERSITÀ E DELLA RICERCA Istituto Comprensivo Palena-Torricella Peligna Scuola dell Infanzia, Primaria e Secondaria di 1 grado Palena (CH) SCUOLA PRIMARIA
A.S. 2014/2015 MINISTERO DELL ISTRUZIONE DELL UNIVERSITÀ E DELLA RICERCA Istituto Comprensivo Palena-Torricella Peligna Scuola dell Infanzia, Primaria e Secondaria di 1 grado Palena (CH) SCUOLA PRIMARIA
CLASSE: 1^ CAT. E 1^ GRA
 ITS BANDINI - SIENA MATERIA DI INSEGNAMENTO: FISICA e LABORATORIO CLASSE: 1^ CAT. E 1^ GRA In relazione alla programmazione curricolare ci si prefigge di raggiungere i seguenti obiettivi disciplinari:
ITS BANDINI - SIENA MATERIA DI INSEGNAMENTO: FISICA e LABORATORIO CLASSE: 1^ CAT. E 1^ GRA In relazione alla programmazione curricolare ci si prefigge di raggiungere i seguenti obiettivi disciplinari:
LEZIONE 1. Materia: Proprietà e Misura
 LEZIONE 1 Materia: Proprietà e Misura MISCELE, COMPOSTI, ELEMENTI SOSTANZE PURE E MISCUGLI La materia può essere suddivisa in sostanze pure e miscugli. Un sistema è puro solo se è formato da una singola
LEZIONE 1 Materia: Proprietà e Misura MISCELE, COMPOSTI, ELEMENTI SOSTANZE PURE E MISCUGLI La materia può essere suddivisa in sostanze pure e miscugli. Un sistema è puro solo se è formato da una singola
Anno Scolastico 2014-2015. INDIRIZZO: Manutenzione e assistenza tecnica Sez.A. DISCIPLINA: Tecnologie meccaniche e applicazioni
 ISTITUTO PROFESSIONALE PER L INDUSTRIA E L ARTIGIANATO E. BERNARDI PADOVA Anno Scolastico 2014-2015 INDIRIZZO: Manutenzione e assistenza tecnica Sez.A DISCIPLINA: Tecnologie meccaniche e applicazioni CLASSI:
ISTITUTO PROFESSIONALE PER L INDUSTRIA E L ARTIGIANATO E. BERNARDI PADOVA Anno Scolastico 2014-2015 INDIRIZZO: Manutenzione e assistenza tecnica Sez.A DISCIPLINA: Tecnologie meccaniche e applicazioni CLASSI:
QUALITÀ E TRATTAMENTO DELL ACQUA DEL CIRCUITO CHIUSO
 QUALITÀ E TRATTAMENTO DELL ACQUA DEL CIRCUITO CHIUSO (PARTE 1) FOCUS TECNICO Gli impianti di riscaldamento sono spesso soggetti a inconvenienti quali depositi e incrostazioni, perdita di efficienza nello
QUALITÀ E TRATTAMENTO DELL ACQUA DEL CIRCUITO CHIUSO (PARTE 1) FOCUS TECNICO Gli impianti di riscaldamento sono spesso soggetti a inconvenienti quali depositi e incrostazioni, perdita di efficienza nello
CLASSE PRIMA A. I..I.S. via Silvestri,301 Plesso A.Volta Programma di Fisica e Laboratorio Programma Attività Didattiche svolte A.S.
 CLASSE PRIMA A I..I.S. via Silvestri,301 Plesso A.Volta Programma di Fisica e Laboratorio Programma Attività Didattiche svolte Materia A.S.2014/2015 FISICA e Laboratorio di Fisica Unità 2- Strumenti matematici:
CLASSE PRIMA A I..I.S. via Silvestri,301 Plesso A.Volta Programma di Fisica e Laboratorio Programma Attività Didattiche svolte Materia A.S.2014/2015 FISICA e Laboratorio di Fisica Unità 2- Strumenti matematici:
MISURE DI POTERE CALORIFICO E COMPOSIZIONE
 MISURE DI POTERE CALORIFICO E COMPOSIZIONE Potere calorifico dei combustibili: bomba calorimetrica e calorimetro di Junkers Composizione: gascromatografia Composizione dei gas combusti: o Sonda λ o Strumenti
MISURE DI POTERE CALORIFICO E COMPOSIZIONE Potere calorifico dei combustibili: bomba calorimetrica e calorimetro di Junkers Composizione: gascromatografia Composizione dei gas combusti: o Sonda λ o Strumenti
Verifica sperimentale della legge di Proust delle proporzioni costanti
 Verifica sperimentale della legge di Proust delle proporzioni costanti Un lavoro degli studenti della classe 4B del Liceo Scientifico Ernesto Balducci di Pontassieve Gli scienziati francesi Antoine Lavoisier
Verifica sperimentale della legge di Proust delle proporzioni costanti Un lavoro degli studenti della classe 4B del Liceo Scientifico Ernesto Balducci di Pontassieve Gli scienziati francesi Antoine Lavoisier
Analisi di Controllo di un Acqua Minerale Naturale
 Analisi di Controllo di un Acqua Minerale aturale ITODUZIOE Le acque potabili possono essere in diverse tipologie: si definiscono acque destinate al consumo umano, quelle acque rese potabili dopo aver
Analisi di Controllo di un Acqua Minerale aturale ITODUZIOE Le acque potabili possono essere in diverse tipologie: si definiscono acque destinate al consumo umano, quelle acque rese potabili dopo aver
CHIMICA. Una teoria è scientifica solo se è falsificabile (cioè se è possibile sperimentalmente smentire le sue previsioni)
 CHIMICA SCIENZA SPERIMENTALE: cioè si basa sul metodo sperimentale (Galileo è il precursore). Osservazione dei fenomeni (raccolta e interpretazioni dati) Formulazione ipotesi Verifica sperimentale (eventualmente
CHIMICA SCIENZA SPERIMENTALE: cioè si basa sul metodo sperimentale (Galileo è il precursore). Osservazione dei fenomeni (raccolta e interpretazioni dati) Formulazione ipotesi Verifica sperimentale (eventualmente
quale agisce una forza e viceversa. situazioni. applicate a due corpi che interagiscono. Determinare la forza centripeta di un
 CLASSE Seconda DISCIPLINA Fisica ORE SETTIMANALI 3 TIPO DI PROVA PER GIUDIZIO SOSPESO Test a risposta multipla MODULO U.D Conoscenze Abilità Competenze Enunciato del primo principio della Calcolare l accelerazione
CLASSE Seconda DISCIPLINA Fisica ORE SETTIMANALI 3 TIPO DI PROVA PER GIUDIZIO SOSPESO Test a risposta multipla MODULO U.D Conoscenze Abilità Competenze Enunciato del primo principio della Calcolare l accelerazione
Programmazione Modulare
 Indirizzo: BIENNIO Programmazione Modulare Disciplina: FISICA Classe: 2 a D Ore settimanali previste: (2 ore Teoria 1 ora Laboratorio) Prerequisiti per l'accesso alla PARTE D: Effetti delle forze. Scomposizione
Indirizzo: BIENNIO Programmazione Modulare Disciplina: FISICA Classe: 2 a D Ore settimanali previste: (2 ore Teoria 1 ora Laboratorio) Prerequisiti per l'accesso alla PARTE D: Effetti delle forze. Scomposizione
LABORATORIO PLS CHIMICA DEI MATERIALI SINTESI DI NANOGOLD
 PIANO NAZIONALE LAUREE SCIENTIFICHE (PNLS1) la scienza per una migliore qualità della vita LABORATORIO PLS CHIMICA DEI MATERIALI SINTESI DI NANOGOLD Relazione LAB PLS Chimica dei Materiali 01-07-2011 pag.
PIANO NAZIONALE LAUREE SCIENTIFICHE (PNLS1) la scienza per una migliore qualità della vita LABORATORIO PLS CHIMICA DEI MATERIALI SINTESI DI NANOGOLD Relazione LAB PLS Chimica dei Materiali 01-07-2011 pag.
SISTEMI ELETTROCHIMICI
 Università degli studi di Palermo SISTEMI ELETTROCHIMICI Dott. Ing. Serena Randazzo Dipartimento di Ingegneria Chimica, Gestionale, Informatica e Meccanica OUTLINE 1) Introduzione sui sistemi elettrochimici
Università degli studi di Palermo SISTEMI ELETTROCHIMICI Dott. Ing. Serena Randazzo Dipartimento di Ingegneria Chimica, Gestionale, Informatica e Meccanica OUTLINE 1) Introduzione sui sistemi elettrochimici
Acidi e basi. HCl H + + Cl - (acido cloridrico) NaOH Na + + OH - (idrossido di sodio; soda caustica)
 Acidi e basi Per capire che cosa sono un acido e una base dal punto di vista chimico, bisogna riferirsi ad alcune proprietà chimiche dell'acqua. L'acqua, sia solida (ghiaccio), liquida o gassosa (vapore
Acidi e basi Per capire che cosa sono un acido e una base dal punto di vista chimico, bisogna riferirsi ad alcune proprietà chimiche dell'acqua. L'acqua, sia solida (ghiaccio), liquida o gassosa (vapore
Anno scolastico 2014/2015
 I."MAJORANA-MARCONI" PROGRAMMAZIONE DIDATTICA ANNUALE PER LE SECONDE CLASSI AD INDIRIZZO PROFESSIONALE Anno scolastico 2014/2015 MATERIA: SCIENZE INTEGRATE/CHIMICA E LABORATORIO DOCENTI: CASTAGNA ADRIANA,
I."MAJORANA-MARCONI" PROGRAMMAZIONE DIDATTICA ANNUALE PER LE SECONDE CLASSI AD INDIRIZZO PROFESSIONALE Anno scolastico 2014/2015 MATERIA: SCIENZE INTEGRATE/CHIMICA E LABORATORIO DOCENTI: CASTAGNA ADRIANA,
(E4-U18) Gli homework da preparare prima di iniziare la parte sperimentale sono calcoli e simulazioni dei circuiti su cui vengono eseguite le misure.
 Esercitazione 5 (E4-U18) Caratterizzazione e misure su circuiti digitali Scopo dell esercitazione Gli obiettivi di questa esercitazione sono: - Misurare i parametri elettrici di porte logiche, - Verificare
Esercitazione 5 (E4-U18) Caratterizzazione e misure su circuiti digitali Scopo dell esercitazione Gli obiettivi di questa esercitazione sono: - Misurare i parametri elettrici di porte logiche, - Verificare
Le proprietà periodiche degli elementi LA LEZIONE
 Le proprietà periodiche degli elementi LA LEZIONE Le proprietà degli elementi mostrano delle tendenze che possono essere predette usando il sistema periodico ed essere spiegate e comprese analizzando la
Le proprietà periodiche degli elementi LA LEZIONE Le proprietà degli elementi mostrano delle tendenze che possono essere predette usando il sistema periodico ed essere spiegate e comprese analizzando la
I.T.I. A. MALIGNANI UDINE CLASSI 3 e ELT MATERIA: ELETTROTECNICA PROGRAMMA PREVENTIVO
 CORRENTE CONTINUA: FENOMENI FISICI E PRINCIPI FONDAMENTALI - Richiami sulle unità di misura e sui sistemi di unità di misura. - Cenni sulla struttura e sulle proprietà elettriche della materia. - Le cariche
CORRENTE CONTINUA: FENOMENI FISICI E PRINCIPI FONDAMENTALI - Richiami sulle unità di misura e sui sistemi di unità di misura. - Cenni sulla struttura e sulle proprietà elettriche della materia. - Le cariche
SINTESI C1. Materia ed energia
 Le proprietà fisiche della materia Il mondo che ci circonda è formato da un gran numero di oggetti diversi. Siano essi di origine naturale o creati dagli esseri umani questi oggetti in chimica e fisica
Le proprietà fisiche della materia Il mondo che ci circonda è formato da un gran numero di oggetti diversi. Siano essi di origine naturale o creati dagli esseri umani questi oggetti in chimica e fisica
miscela di reazione miscela di reazione
 Alla fine della reazione: miscela di reazione 1.Si tratta con acqua o acqua e ghiaccio 2.Si aggiunge un solvente organico immiscibile e si agita Si lava (estrae) con una base Si lava (estrae) con un acido
Alla fine della reazione: miscela di reazione 1.Si tratta con acqua o acqua e ghiaccio 2.Si aggiunge un solvente organico immiscibile e si agita Si lava (estrae) con una base Si lava (estrae) con un acido
CURRICOLO DI SCIENZE SCUOLA PRIMARIA ISTITUTO COMPRENSIVO PASSIRANO-PADERNO. Revisione Curricolo di Istituto a.s. 2014-2015
 ISTITUTO COMPRENSIVO PASSIRANO-PADERNO CURRICOLO DI SCIENZE SCUOLA PRIMARIA Revisione Curricolo di Istituto a.s. 2014-2015 Curricolo suddiviso in obiettivi didattici, nuclei tematici e anni scolastici
ISTITUTO COMPRENSIVO PASSIRANO-PADERNO CURRICOLO DI SCIENZE SCUOLA PRIMARIA Revisione Curricolo di Istituto a.s. 2014-2015 Curricolo suddiviso in obiettivi didattici, nuclei tematici e anni scolastici
PROGRAMMA DI CHIMICA
 PROGRAMMA DI CHIMICA Plesso Volta - Classe 1A Indirizzo ITIS A.S. 2018-19 ARGOMENTO 1 Dai miscugli alle sostanze 1.1 Osservando la materia 1.2 Grandezze e strumenti di misura: portata e sensibilità, massa
PROGRAMMA DI CHIMICA Plesso Volta - Classe 1A Indirizzo ITIS A.S. 2018-19 ARGOMENTO 1 Dai miscugli alle sostanze 1.1 Osservando la materia 1.2 Grandezze e strumenti di misura: portata e sensibilità, massa
Istituto di Istruzione Secondaria Superiore Statale «IIS Via Silvestri 301»
 Istituto di Istruzione Secondaria Superiore Statale «IIS Via Silvestri 301» Classe 1 a A Indirizzo ELETTRONICA ED ELETTROTECNICA ARGOMENTO 1 Dai miscugli alle sostanze 1.1 Osservando la materia 1.2 Grandezze
Istituto di Istruzione Secondaria Superiore Statale «IIS Via Silvestri 301» Classe 1 a A Indirizzo ELETTRONICA ED ELETTROTECNICA ARGOMENTO 1 Dai miscugli alle sostanze 1.1 Osservando la materia 1.2 Grandezze
PROGRAMMAZIONE DISCIPLINARE ISTITUTO TECNICO PER IL TURISMO SCIENZE INTEGRATE FISICA CLASSE PRIMA
 PROGRAMMAZIONE DISCIPLINARE PROGRAMMAZIONE DISCIPLINARE ISTITUTO TECNICO PER IL TURISMO SCIENZE INTEGRATE FISICA CLASSE PRIMA 1. Competenze: le specifiche competenze di base disciplinari previste dalla
PROGRAMMAZIONE DISCIPLINARE PROGRAMMAZIONE DISCIPLINARE ISTITUTO TECNICO PER IL TURISMO SCIENZE INTEGRATE FISICA CLASSE PRIMA 1. Competenze: le specifiche competenze di base disciplinari previste dalla
SCIENZE INTEGRATE FISICA
 CLASSE DISCIPLINA ORE SETTIMANALI TIPO DI PROVA PER GIUDIZIO SOSPESO MODULO 1: Il moto e l energia I concetti di sistema di riferimento e le grandezze cinematiche. I diversi tipi di rappresentazione del
CLASSE DISCIPLINA ORE SETTIMANALI TIPO DI PROVA PER GIUDIZIO SOSPESO MODULO 1: Il moto e l energia I concetti di sistema di riferimento e le grandezze cinematiche. I diversi tipi di rappresentazione del
LA SICUREZZA IN LABORATORIO. di F. Luca
 LA SICUREZZA IN LABORATORIO di F. Luca IN LABORATORIO NORME DI COMPORTAMENTO X. NON correre. NON ingombrare con gli zaini lo spazio intorno ai banconi di lavoro o in prossimità delle uscite X. NON mangiare
LA SICUREZZA IN LABORATORIO di F. Luca IN LABORATORIO NORME DI COMPORTAMENTO X. NON correre. NON ingombrare con gli zaini lo spazio intorno ai banconi di lavoro o in prossimità delle uscite X. NON mangiare
Il test di cessione: modalità di esecuzione e criticità dei limiti
 Il test di cessione: modalità di esecuzione e criticità dei limiti Nicola Mondini Convegno sul tema: La qualità degli aggregati riciclati: i controlli ambientali ed i controlli prestazionali Ferrara, 18
Il test di cessione: modalità di esecuzione e criticità dei limiti Nicola Mondini Convegno sul tema: La qualità degli aggregati riciclati: i controlli ambientali ed i controlli prestazionali Ferrara, 18
ISTITUTO ISTRUZIONE SECONDARIA SUPERIORE Carlo e Nello ROSSELLI di Aprilia Programmazione didattica
 percentuale alunni ISTITUTO ISTRUZIONE SECONDARIA SUPERIORE Carlo e Nello ROSSELLI di Aprilia Programmazione didattica CLASSE 1 A GEOMETRA Anno Scolastico 2009/2010 Classe sperimentale. Anticipazione della
percentuale alunni ISTITUTO ISTRUZIONE SECONDARIA SUPERIORE Carlo e Nello ROSSELLI di Aprilia Programmazione didattica CLASSE 1 A GEOMETRA Anno Scolastico 2009/2010 Classe sperimentale. Anticipazione della
ANALISI CHIMICA compiti delle vacanze. a.s. 2014/2015 IV E chimici
 ANALISI CHIMICA compiti delle vacanze a.s. 2014/2015 IV E chimici I libri di testo non devono essere venduti in quanto si lavorerà ancora su di esso nel corso del prossimo anno scolastico Rubino, Venzaghi,
ANALISI CHIMICA compiti delle vacanze a.s. 2014/2015 IV E chimici I libri di testo non devono essere venduti in quanto si lavorerà ancora su di esso nel corso del prossimo anno scolastico Rubino, Venzaghi,
DETERMINAZIONE DEL PUNTO DI FINE TITOLAZIONE MEDIANTE METODI CHIMICO-FISICI
 DETERMINAZIONE DEL PUNTO DI FINE TITOLAZIONE MEDIANTE METODI CHIMICO-FISICI - si sfrutta una proprietà chimico-fisica o fisica che varia nel corso della titolazione - tale proprietà è in genere proporzionale
DETERMINAZIONE DEL PUNTO DI FINE TITOLAZIONE MEDIANTE METODI CHIMICO-FISICI - si sfrutta una proprietà chimico-fisica o fisica che varia nel corso della titolazione - tale proprietà è in genere proporzionale
SCUOLA PRIMARIA CURRICOLO DI SCIENZE CLASSE PRIMA. INDICATORI COMPETENZE ABILITA CONOSCENZE 1. Esplorare e descrivere oggetti e materiali
 SCUOLA PRIMARIA CURRICOLO DI SCIENZE CLASSE PRIMA INDICATORI 1. Esplorare e descrivere oggetti e materiali 2. Osservare e sperimentare sul campo Sviluppa atteggiamenti di curiosità verso il mondo circostante
SCUOLA PRIMARIA CURRICOLO DI SCIENZE CLASSE PRIMA INDICATORI 1. Esplorare e descrivere oggetti e materiali 2. Osservare e sperimentare sul campo Sviluppa atteggiamenti di curiosità verso il mondo circostante
LEZIONE 12. Idrolisi salina Indicatori di ph Soluzioni tampone Titolazioni acido-base IDROLISI SALINA. Scaricato da Sunhope.it
 LEZIONE 12 Idrolisi salina Indicatori di ph Soluzioni tampone Titolazioni acido-base IDROLISI SALINA Idrolisi salina Per IDROLISI SALINA si intende il fenomeno per il quale la dissoluzione in acqua di
LEZIONE 12 Idrolisi salina Indicatori di ph Soluzioni tampone Titolazioni acido-base IDROLISI SALINA Idrolisi salina Per IDROLISI SALINA si intende il fenomeno per il quale la dissoluzione in acqua di
ACIDI E BASI IN CASA. Scheda studente n.1
 Scheda studente n.1 Come interagisce ciascun liquido con la polvere di marmo? Seguite le istruzioni, osservate con attenzione ciò che accade e completate la tabella. polvere di marmo e le seguenti sostanze:
Scheda studente n.1 Come interagisce ciascun liquido con la polvere di marmo? Seguite le istruzioni, osservate con attenzione ciò che accade e completate la tabella. polvere di marmo e le seguenti sostanze:
2) Calcolare la molarità di una soluzione di acido solforico al 17%,d = 1.12 g/ml
 Bari,11 gennaio 1999 Compito di analisi dei farmaci I 1) 1 ml di H 2 O 2 viene titolato con KMnO 4. Sono necessari 18.1 ml. La soluzione di KMnO 4 è 0.1023 N e la densità dell acqua ossigenata è 1.01 g/ml.
Bari,11 gennaio 1999 Compito di analisi dei farmaci I 1) 1 ml di H 2 O 2 viene titolato con KMnO 4. Sono necessari 18.1 ml. La soluzione di KMnO 4 è 0.1023 N e la densità dell acqua ossigenata è 1.01 g/ml.
ASSE SCIENTIFICO TECNOLOGICO COMPETENZE DI SCIENZE INTEGRATE (SCIENZE DELLA TERRA) 1 ANNO
 ASSE SCIENTIFICO TECNOLOGICO COMPETENZE DI SCIENZE INTEGRATE (SCIENZE DELLA TERRA) 1 ANNO Competenze in esito al quinquennio (dall Allegato C del Regolamento) Macro Competenza A: Utilizzare gli strumenti
ASSE SCIENTIFICO TECNOLOGICO COMPETENZE DI SCIENZE INTEGRATE (SCIENZE DELLA TERRA) 1 ANNO Competenze in esito al quinquennio (dall Allegato C del Regolamento) Macro Competenza A: Utilizzare gli strumenti
DAI MISCUGLI ALLE SOSTANZE PURE
 Come si presenta la materia? DAI MISCUGLI ALLE SOSTANZE PURE Il criterio per distinguere i materiali è la presenza di una o più FASI porzioni di materia fisicamente distinte tra loro delimitate da nette
Come si presenta la materia? DAI MISCUGLI ALLE SOSTANZE PURE Il criterio per distinguere i materiali è la presenza di una o più FASI porzioni di materia fisicamente distinte tra loro delimitate da nette
Liquidi, Solidi e Forze Intermolecolari
 Liquidi, Solidi e Forze Intermolecolari Distanze tra molecole Stati Fisici (Fase) Comportamento atipico La maggiore differenza tra liquidi e solidi consiste nella libertà di movimento delle loro molecole
Liquidi, Solidi e Forze Intermolecolari Distanze tra molecole Stati Fisici (Fase) Comportamento atipico La maggiore differenza tra liquidi e solidi consiste nella libertà di movimento delle loro molecole
ISTITUTO COMPRENSIVO MONTEGROTTO TERME SCUOLA PRIMARIA DISCIPLINA: SCIENZE - CLASSE PRIMA OBIETTIVI DI APPRENDIMENTO
 PRIMA DELLA DISCIPLINA: SCIENZE - CLASSE PRIMA L alunno sviluppa atteggiamenti di curiosità e modi di guardare il mondo che lo stimolano a cercare spiegazioni di quello che vede succedere. Esplora i fenomeni
PRIMA DELLA DISCIPLINA: SCIENZE - CLASSE PRIMA L alunno sviluppa atteggiamenti di curiosità e modi di guardare il mondo che lo stimolano a cercare spiegazioni di quello che vede succedere. Esplora i fenomeni
Cognome. Nome Classe 1^ VERIFICA DI CHIMICA Recupero trimestre Data NB troverai le soluzioni nel testo in grassetto o sottolineato
 Cognome. Nome Classe 1^ ERIICA DI CHIMICA Recupero trimestre Data NB troverai le soluzioni nel testo in grassetto o sottolineato 1. Quale dei seguenti enunciati non descrive lo stato liquido? a) le particelle
Cognome. Nome Classe 1^ ERIICA DI CHIMICA Recupero trimestre Data NB troverai le soluzioni nel testo in grassetto o sottolineato 1. Quale dei seguenti enunciati non descrive lo stato liquido? a) le particelle
MISCUGLI E TECNICHE DI SEPARAZIONE
 MISCUGLI E TECNICHE DI SEPARAZIONE Classe 1^A Grafico Questo documento è solo una presentazione e non deve ritenersi completo se non è accompagnato dalla lezione in classe. Prof. Zarini Marta CLASSIFICAZIONE
MISCUGLI E TECNICHE DI SEPARAZIONE Classe 1^A Grafico Questo documento è solo una presentazione e non deve ritenersi completo se non è accompagnato dalla lezione in classe. Prof. Zarini Marta CLASSIFICAZIONE
Programmazione modulare. Moduli Titolo del modulo Ore
 Ministero dell Istruzione, dell Università e della Ricerca Ufficio Scolastico Regionale per il Lazio ISTITUTO DI ISTRUZIONE SUPERIORE Via Domizia Lucilla Programmazione annuale A.S. 2015-2016 Mod. 7.1.A
Ministero dell Istruzione, dell Università e della Ricerca Ufficio Scolastico Regionale per il Lazio ISTITUTO DI ISTRUZIONE SUPERIORE Via Domizia Lucilla Programmazione annuale A.S. 2015-2016 Mod. 7.1.A
DENSITA La densità è una grandezza fisica che indica la massa, di una sostanza o di un corpo, contenuta nell unità di volume; è data dal rapporto:
 Richiami di Chimica DENSITA La densità è una grandezza fisica che indica la massa, di una sostanza o di un corpo, contenuta nell unità di volume; è data dal rapporto: d = massa / volume unità di misura
Richiami di Chimica DENSITA La densità è una grandezza fisica che indica la massa, di una sostanza o di un corpo, contenuta nell unità di volume; è data dal rapporto: d = massa / volume unità di misura
PROGRAMMAZIONE DIDATTICA ANNUALE DOCENTI
 ISS IPSIA SILVIO CECCATO di MONTECCHIO MAGGIORE ( VI ) classe QUINTA A e B PROGRAMMAZIONE DIDATTICA ANNUALE DOCENTI Anno scolastico 2015/16 Materia: LABORATORI TECNOLOGICI ED ESERCITAZIONI Indirizzo :
ISS IPSIA SILVIO CECCATO di MONTECCHIO MAGGIORE ( VI ) classe QUINTA A e B PROGRAMMAZIONE DIDATTICA ANNUALE DOCENTI Anno scolastico 2015/16 Materia: LABORATORI TECNOLOGICI ED ESERCITAZIONI Indirizzo :
Banco Prova Caldaie. per generatori di energia termica avente una potenza nominale inferiore a 100kW
 Banco Prova Caldaie per generatori di energia termica avente una potenza nominale inferiore a 100kW 1 Generalità Il banco prova caldaie attualmente disponibile presso il nostro Laboratorio è stato realizzato
Banco Prova Caldaie per generatori di energia termica avente una potenza nominale inferiore a 100kW 1 Generalità Il banco prova caldaie attualmente disponibile presso il nostro Laboratorio è stato realizzato
Quando un composto ionico viene immesso in acqua si dissocia formando uno ione negativo ed uno positivo.
 I composti chimici Il legame chimico Un atomo raggiunge la stabilità quando i suoi livelli energetici sono completi. Solamente i gas nobili hanno questa caratteristica mentre gli altri atomi no, per cui
I composti chimici Il legame chimico Un atomo raggiunge la stabilità quando i suoi livelli energetici sono completi. Solamente i gas nobili hanno questa caratteristica mentre gli altri atomi no, per cui
Specializzazione Elettronica ed Elettrotecnica Articolazione Elettrotecnica. Elettronica ed Elettrotecnica - Classe 3^
 Specializzazione Elettronica ed Elettrotecnica Articolazione Elettrotecnica Elettronica ed Elettrotecnica - Classe 3^ 1- Reti elettriche in corrente continua Grandezze elettriche fondamentali e loro legami,
Specializzazione Elettronica ed Elettrotecnica Articolazione Elettrotecnica Elettronica ed Elettrotecnica - Classe 3^ 1- Reti elettriche in corrente continua Grandezze elettriche fondamentali e loro legami,
ISTITUTO DI ISTRUZIONE SUPERIORE VIA SILVESTRI, 301 ROMA Sez. associata: I.T.C.G. "Alberto Ceccherelli" - Via di Bravetta, 383
 ISTITUTO DI ISTRUZIONE SUPERIORE VIA SILVESTRI, 301 ROMA Sez. associata: I.T.C.G. "Alberto Ceccherelli" - Via di Bravetta, 383 Materia: Scienze Integrate - CHIMICA Docente: Rosmarini Diana Classe: I Sez.:
ISTITUTO DI ISTRUZIONE SUPERIORE VIA SILVESTRI, 301 ROMA Sez. associata: I.T.C.G. "Alberto Ceccherelli" - Via di Bravetta, 383 Materia: Scienze Integrate - CHIMICA Docente: Rosmarini Diana Classe: I Sez.:
LA CORRENTE ELETTRICA Prof. Erasmo Modica erasmo@galois.it
 LA CORRENTE ELETTRICA Prof. Erasmo Modica erasmo@galois.it L INTENSITÀ DELLA CORRENTE ELETTRICA Consideriamo una lampadina inserita in un circuito elettrico costituito da fili metallici ed un interruttore.
LA CORRENTE ELETTRICA Prof. Erasmo Modica erasmo@galois.it L INTENSITÀ DELLA CORRENTE ELETTRICA Consideriamo una lampadina inserita in un circuito elettrico costituito da fili metallici ed un interruttore.
Istituto S. Giuliana Falconieri Classe IIIB Liceo Linguistico-Europeo Programmazione di Scienze A.S. 2013-2014
 Istituto S. Giuliana Falconieri Classe IIIB Liceo Linguistico-Europeo Le trasformazioni fisiche della materia Gli stati fisici della materia I sistemi omogenei ed eterogenei Le sostanze pure ed i miscugli
Istituto S. Giuliana Falconieri Classe IIIB Liceo Linguistico-Europeo Le trasformazioni fisiche della materia Gli stati fisici della materia I sistemi omogenei ed eterogenei Le sostanze pure ed i miscugli
Sistemi elettrici secondo la tensione ed il loro modo di collegamento a terra. Sistemi elettrici e messa a terra -- Programma LEONARDO
 Sistemi elettrici secondo la tensione ed il loro modo di collegamento a terra Classificazione dei sistemi in categorie secondo la loro tensione nominale In relazione alla loro tensione nominale i sistemi
Sistemi elettrici secondo la tensione ed il loro modo di collegamento a terra Classificazione dei sistemi in categorie secondo la loro tensione nominale In relazione alla loro tensione nominale i sistemi
I rifiuti: un possibile tema per affrontare in modo globale e sistemico gli argomenti previsti per la II. media
 I rifiuti: un possibile tema per affrontare in modo globale e sistemico gli argomenti previsti per la II. media Esperti di scienze naturali Docenti delle Sm di Cadenazzo e Lugano-Besso 1. Introduzione
I rifiuti: un possibile tema per affrontare in modo globale e sistemico gli argomenti previsti per la II. media Esperti di scienze naturali Docenti delle Sm di Cadenazzo e Lugano-Besso 1. Introduzione
LICEO SCIENTIFICO LEONARDO da VINCI REGGIO CALABRIA PROGRAMMA DI SCIENZE NATURALI CLASSE 2 a SEZ. Q A.S. 2012/2013
 LICEO SCIENTIFICO LEONARDO da VINCI REGGIO CALABRIA PROGRAMMA DI SCIENZE NATURALI CLASSE 2 a SEZ. Q A.S. 2012/2013 CHIMICA NUCLEO FONDANTE A : MISURE E GRANDEZZE TRASFORMAZIONI CHIMICO-FISICHE DELLA MATERIA
LICEO SCIENTIFICO LEONARDO da VINCI REGGIO CALABRIA PROGRAMMA DI SCIENZE NATURALI CLASSE 2 a SEZ. Q A.S. 2012/2013 CHIMICA NUCLEO FONDANTE A : MISURE E GRANDEZZE TRASFORMAZIONI CHIMICO-FISICHE DELLA MATERIA
DETERMINAZIONE DEL GRADO DI ACIDITÀ DI UN ACETO COMMERCIALE
 DETERMINAZIONE DEL GRADO DI ACIDITÀ DI UN ACETO COMMERCIALE L esperienza consiste nel misurare il grado di acidità di un aceto, acquistando i concetti di titolazione acido-base, punto di equivalenza, indicatore
DETERMINAZIONE DEL GRADO DI ACIDITÀ DI UN ACETO COMMERCIALE L esperienza consiste nel misurare il grado di acidità di un aceto, acquistando i concetti di titolazione acido-base, punto di equivalenza, indicatore
PIANO DI LAVOR A. S. 2013/ 2014. III E sezione tecnica CHIMICI. Testo in adozione. Dispense
 Pagina 1 di 5 Nome docenti BENEDETTO LUIGINA Materia insegnata Analisi Chimica e laboratorio Classe III E sezione tecnica CHIMICI Nome Ins. Tecn. Pratico Romagnollo Lidia Rubino,Venzaghi,Cozzi Le basi
Pagina 1 di 5 Nome docenti BENEDETTO LUIGINA Materia insegnata Analisi Chimica e laboratorio Classe III E sezione tecnica CHIMICI Nome Ins. Tecn. Pratico Romagnollo Lidia Rubino,Venzaghi,Cozzi Le basi
PIANO di LAVORO A. S. 2013/ 2014
 Nome docente DAGHERO LUIGI Materia insegnata Classe Testo in adozione TECNICA PROFESSIONALE ELETTROTECNICA 4G TECNOLOGIE ELETTRICO ELETTRONICHE E APPLICAZIONI/1-2 ED. Mondadori 1 PIANO di LAVORO Punti
Nome docente DAGHERO LUIGI Materia insegnata Classe Testo in adozione TECNICA PROFESSIONALE ELETTROTECNICA 4G TECNOLOGIE ELETTRICO ELETTRONICHE E APPLICAZIONI/1-2 ED. Mondadori 1 PIANO di LAVORO Punti
REGOLE PER L'ATTRIBUZIONE DEI COEFFICIENTI STECHIOMETRICI DI UNA REAZIONE
 REGOLE PER L'ATTRIBUZIONE DEI COEFFICIENTI STECHIOMETRICI DI UNA REAZIONE OSSIDORIDUTTIVA SECONDO IL METODO DELLO IONE-ELETTRIONE. 1) Si individuano le coppie di atomi il cui numero di ossidazione cambia
REGOLE PER L'ATTRIBUZIONE DEI COEFFICIENTI STECHIOMETRICI DI UNA REAZIONE OSSIDORIDUTTIVA SECONDO IL METODO DELLO IONE-ELETTRIONE. 1) Si individuano le coppie di atomi il cui numero di ossidazione cambia
I.T.I.S. E. FERMI _ MODENA
 I.T.I.S. E. FERMI _ MODENA Programma svolto del corso di Chimica Analitica e Strumentale Classe 3^C a.s. 2013-14 Docenti: Giorgia Messori, Claudia Tacconi Il libro di testo utilizzato è stato: Rubino,
I.T.I.S. E. FERMI _ MODENA Programma svolto del corso di Chimica Analitica e Strumentale Classe 3^C a.s. 2013-14 Docenti: Giorgia Messori, Claudia Tacconi Il libro di testo utilizzato è stato: Rubino,
Riepilogo programma di Chimica Ginnasio Anno scolastico 2011/2012
 Riepilogo programma di Chimica Ginnasio Anno scolastico 2011/2012 Misure e grandezze Grandezze fondamentali Grandezza fisica Simbolo della grandezza Unità di misura Simbolo dell unità di misura lunghezza
Riepilogo programma di Chimica Ginnasio Anno scolastico 2011/2012 Misure e grandezze Grandezze fondamentali Grandezza fisica Simbolo della grandezza Unità di misura Simbolo dell unità di misura lunghezza
4001 Trans-esterificazione dell olio di ricino a estere metilico dell acido ricinoleico
 4001 Trans-esterificazione dell olio di ricino a estere metilico dell acido ricinoleico lio di ricino + MeH NaMe H Me CH 4 (32.0) C 19 H 36 3 (312.5) Classificazione Tipo di reazione e classi di sostanze
4001 Trans-esterificazione dell olio di ricino a estere metilico dell acido ricinoleico lio di ricino + MeH NaMe H Me CH 4 (32.0) C 19 H 36 3 (312.5) Classificazione Tipo di reazione e classi di sostanze
PROGRAMMAZIONE GENERALE SCIENZA DEI MATERIALI DENTALI CLASSE IVE ODONTOTECNICA anno scolastico 2014/2015
 PROGRAMMAZIONE GENERALE SCIENZA DEI MATERIALI DENTALI CLASSE IVE ODONTOTECNICA anno scolastico 2014/2015 Competenze da conseguire al termine del quinto anno: applicare le metodologie e le tecniche della
PROGRAMMAZIONE GENERALE SCIENZA DEI MATERIALI DENTALI CLASSE IVE ODONTOTECNICA anno scolastico 2014/2015 Competenze da conseguire al termine del quinto anno: applicare le metodologie e le tecniche della
a 25 C da cui si ricava che:
 Equilibrio di autoionizzazione dell acqua Come già osservato l acqua presenta caratteristiche anfotere, potendosi comportare tanto da acido (con una sostanza meno acida che si comporta da base) quanto
Equilibrio di autoionizzazione dell acqua Come già osservato l acqua presenta caratteristiche anfotere, potendosi comportare tanto da acido (con una sostanza meno acida che si comporta da base) quanto
 ET CONTROLLO CORRENTI INDOTTE CORSO PER OPERATORI DI II LIVELLO TOTALE ORE : 88 PARTE 1 - PRINCIPI DEL CONTROLLO CON CORRENTI INDOTTE 1.1) Scopo e limitazioni del metodo di controllo con correnti indotte
ET CONTROLLO CORRENTI INDOTTE CORSO PER OPERATORI DI II LIVELLO TOTALE ORE : 88 PARTE 1 - PRINCIPI DEL CONTROLLO CON CORRENTI INDOTTE 1.1) Scopo e limitazioni del metodo di controllo con correnti indotte
SECONDO BIENNIO ISTITUTO TECNICO
 SETTORE DOCUMENTI PER LA DISCUSSIONE ISTITUTO TECNICO INDIRIZZO ARTICOLAZIONE ELETTROTECNICA TECNOLOGICO ELETTRONICA ED ELETTROTECNICA ESITI DI APPRENDIMENTO (competenze, abilità, conoscenze) Regolamento,
SETTORE DOCUMENTI PER LA DISCUSSIONE ISTITUTO TECNICO INDIRIZZO ARTICOLAZIONE ELETTROTECNICA TECNOLOGICO ELETTRONICA ED ELETTROTECNICA ESITI DI APPRENDIMENTO (competenze, abilità, conoscenze) Regolamento,
SENSORI E TRASDUTTORI
 SENSORI E TRASDUTTORI Il controllo di processo moderno utilizza tecnologie sempre più sofisticate, per minimizzare i costi e contenere le dimensioni dei dispositivi utilizzati. Qualsiasi controllo di processo
SENSORI E TRASDUTTORI Il controllo di processo moderno utilizza tecnologie sempre più sofisticate, per minimizzare i costi e contenere le dimensioni dei dispositivi utilizzati. Qualsiasi controllo di processo
Storia dei generatori di tensione e della corrente elettrica
 Storia dei generatori di tensione e della corrente elettrica Prof. Daniele Ippolito Liceo Scientifico Amedeo di Savoia di Pistoia 1778 Alessandro Volta, in analogia al potenziale gravitazionale definito
Storia dei generatori di tensione e della corrente elettrica Prof. Daniele Ippolito Liceo Scientifico Amedeo di Savoia di Pistoia 1778 Alessandro Volta, in analogia al potenziale gravitazionale definito
ISTITUTO D ISTRUZIONE SUPERIORE ISTITUTO TECNICO ECONOMICO STATALE. Roberto Valturio RELAZIONE FINALE E PROGRAMMA SVOLTO. a.s.
 ISTITUTO D ISTRUZIONE SUPERIORE ISTITUTO TECNICO ECONOMICO STATALE Roberto Valturio RELAZIONE FINALE E PROGRAMMA SVOLTO a.s. 2O13-2014 Materia : Chimica e Biologia Classe : II sez. B Rimini,05/06/2014
ISTITUTO D ISTRUZIONE SUPERIORE ISTITUTO TECNICO ECONOMICO STATALE Roberto Valturio RELAZIONE FINALE E PROGRAMMA SVOLTO a.s. 2O13-2014 Materia : Chimica e Biologia Classe : II sez. B Rimini,05/06/2014
