Corso di formazione. I requisiti specifici per l Autorizzazione e l Accreditamento dei ST e delle UdR del sangue e degli emocomponenti
|
|
|
- Renato Cirillo
- 8 anni fa
- Visualizzazioni
Transcript
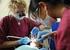
1 Corso di formazione I requisiti specifici per l Autorizzazione e l Accreditamento dei ST e delle UdR del sangue e degli emocomponenti I processi di erogazione del servizio: selezione del donatore; raccolta, lavorazione, etichettatura, confezionamento, conservazione e trasporto del sangue e degli emocomponenti Roma, 16 luglio 2013 Relatrice: Ivana Menichini
2 I REQUISITI STRUTTURALI REQUISITI STRUTTURALI COMUNI ST E UdR FISSE (S.1-US.1) Il ST/ L UdR fissa dispone di locali atti a garantire l idoneità all uso previsto, con specifico riferimento alla esigenza di consentire lo svolgimento delle diverse attività in ordine logico, al fine di contenere il rischio di errori, nonché operazioni di pulizia e manutenzione atte a minimizzare il rischio di contaminazioni. (S.1.1-US.1.1) Deve essere garantita l idoneità dei locali prima dell utilizzo, ad intervalli regolari e a seguito di modifiche rilevanti. (S.2-US.2) I locali e gli spazi delle UdR devono essere commisurati alle tipologie ed ai volumi delle prestazioni erogate.
3 I REQUISITI STRUTTURALI REQUISITI STRUTTURALI UdR MOBILI (US.4) Le Unità di Raccolta mobili (autoemoteche) devono avere dimensioni adeguate ed essere atte a garantire l idoneità all uso previsto, con specifico riferimento alla esigenza di consentire lo svolgimento delle attività in ordine logico (US.5) Nelle Unità di Raccolta mobili, deve essere garantita l idoneità dei locali prima dell utilizzo, verificata ad intervalli regolari e a seguito di modifiche rilevanti. (US.5.1) Nelle Unità di Raccolta mobili devono essere garantiti almeno: unospazioperlostoccaggiodelmaterialeedeidispositivida impiegare; uno spazio per il deposito temporaneo sicuro dei residui, dei materiali e dispositivi utilizzati ;
4 I REQUISITI STRUTTURALI Area per attesa e accettazione; Locale destinato al colloquio e alla valutazione delle condizioni generali di salute del donatore; Locale (ST-UdR fisse) /area (UdR mobili) destinato/a alla raccolta di sangue intero ed emocomponenti; Area destinata al riposo/ristoro post-donazione; Area destinata esclusivamente alla lavorazione del sangue e degli emocomponenti in circuito chiuso(st); Area adibita alla conservazione del sangue e degli emocomponenti (ST); Area per lo stoccaggio dei materiali, dispositivi e reagenti da impiegare; Area destinata esclusivamente alle attività diagnostiche di laboratorio(st).
5 I REQUISITI STRUTTURALI Requisiti strutturali EVIDENZE Documentazione tecnica comprovante l idoneità dei locali all uso previsto. Piani per la verifica periodica di idoneità dei locali(responsabilità, periodicità, criteri di verifica, registrazioni da produrre). Registrazioni inerenti alle verifiche di idoneità effettuate. Locali/aree/spazi previsti dai Requisiti. Planimetria. Compatibilità locali con il flusso operativo e con le attività svolte. Idoneità locali, arredi e apparecchiature all esecuzione delle operazioni di pulizia e manutenzione previste. Adeguatezza locali con volumi e tipologie di prodotti/prestazioni documentati.
6 MAPPA SISTEMA DI GESTIONE PER LA QUALITÁ Pianificazione prodotti-processi Piano Indicatori qualità Processo di indirizzo e pianificazione Missione, Politica Piano annuale attività - budget Piano Audit interni qualità Piano Formazione Piano Obiettivi qualità Organizzazione Organigramma e Responsabilità Gestione documenti e registrazioni Sistema Informativo Processo di valutazione e miglioramento della qualità Valutazione Gestione azioni correttive e preventive Monitoraggio indicatori processo Monitoraggio Indicatori prodotto Selezione Donatore e Raccolta Processi erogazione prodotti-servizi Lavorazione SI ed emocompon. Qualific. biol. e validaz. SI ed emocomp. Interazione con altre Strutture Assegnaz., consegna e distribuzione Gestione non conformità Gestione degli Audit Conservazione trasporto Rintracciabilità Attività di supporto a erogazione prodotti-servizi Processi di gestione delle risorse Gestione emergenze cliniche, organ. e tecnol. Pulizia, disinfezione, ambienti e disp. medici Sicurezza Operatori e Utenti Gestione dei rifiuti
7 MAPPA SISTEMA DI GESTIONE PER LA QUALITÁ Pianificazione prodotti-processi Piano Indicatori qualità Processo di indirizzo e pianificazione Missione, Politica Piano annuale attività - budget Piano Audit interni qualità Piano Formazione Piano Obiettivi qualità Organizzazione Organigramma e Responsabilità Gestione documenti e registrazioni Sistema Informativo Processo di valutazione e miglioramento della qualità Valutazione Gestione azioni correttive e preventive Monitoraggio indicatori processo Monitoraggio Indicatori prodotto Selezione Donatore e Raccolta Processi erogazione prodotti-servizi Lavorazione SI ed emocompon. Qualific. biol. e validaz. SI ed emocomp. Interazione con altre Strutture Assegnaz., consegna e distribuzione Gestione non conformità Gestione degli Audit Conservazione trasporto Rintracciabilità Attività di supporto a erogazione prodotti-servizi Processi di gestione delle risorse Gestione emergenze cliniche, organ. e tecnol. Pulizia, disinfezione, ambienti e disp. medici Sicurezza Operatori e Utenti Gestione dei rifiuti
8 LA SELEZIONE DEL DONATORE E LA RACCOLTA DI SANGUE INTERO ED EMOCOMPONENTI
9 LA SELEZIONE DEL DONATORE E LA RACCOLTA DI S.I. ED EMOCOMP. Le attività relative a RACCOLTA E CONTROLLO DEL SANGUE UMANO E DEGLI EMC a qualunque uso siano destinati LAVORAZIONE, CONSERVAZIONE, DISTRIBUZIONE E ASSEGNAZIONE, ove siano destinati alla trasfusione sono effettuate unicamente dai SERVIZI TRASFUSIONALI (art. 2, com.1, lett.e) e, limitatamente alle attività di RACCOLTA DEL SANGUE E DEGLI EMC, dalleunitá DI RACCOLTA che abbiano entrambi ottenuto, ai sensi della normativa vigente, (art. 2, com.1, lett.f) l'autorizzazione e l'accreditamento secondo le modalità previste dalla regioni e dalle province autonome (D.Lgs. 20 dicembre 2007, n. 261, art. 4 comma 1)
10 LA SELEZIONE DEL DONATORE E LA RACCOLTA DI S.I. ED EMOCOMP. I SERVIZI TRASFUSIONALI LE STRUTTURE E LE RELATIVE ARTICOLAZIONI ORGANIZZATIVE, comprese quelle per le attività di raccolta, previste dalla normativa vigente secondo i modelli organizzativi regionali, che sono RESPONSABILI SOTTO QUALSIASI ASPETTO della RACCOLTA e del CONTROLLOdelsangueumanoedeisuoicomponenti,qualenesiala destinazione, nonché della LAVORAZIONE, CONSERVAZIONE, DISTRIBUZIONE E ASSEGNAZIONE quando gli stessi sono destinati alla trasfusione. (D.Lgs. 20 dicembre 2007, n. 261, art. 2, comma 1, lettera e)
11 LA SELEZIONE DEL DONATORE E LA RACCOLTA DI S.I. ED EMOCOMP. LE UNITÁ DI RACCOLTA DEL SANGUE E DEGLI EMOCOMPONENTI Le STRUTTURE INCARICATE della RACCOLTA, previa autorizzazione delle regioni o province autonome competenti, gestite dalle Associazioni e Federazioni dei donatori di sangue convenzionate e costituite ai sensi della normativa vigente; le unità di raccolta, gestite singolarmente o in forma aggregata dalle predette Associazioni/Federazioni, OPERANO SOTTO LA RESPONSABILITÀ TECNICA DEL SERVIZIO TRASFUSIONALE DI RIFERIMENTO. (D.Lgs. 20 dicembre 2007, n. 261, art. 2, comma 1, lettera f)
12 LA SELEZIONE DEL DONATORE E LA RACCOLTA DI S.I. ED EMOCOMP. LA REGOLAMENTAZIONE DEI RAPPORTI TRA I ST E LE UdR GESTITE DA ASSOCIAZIONI E FEDERAZIONI DONATORI SANGUE (O.53) Le convenzioni/atti contrattuali che regolamentano i rapporti fra il ST e le UdR ad esso collegate devono specificamente prevedere l affidamento al Servizio Trasfusionale della responsabilità tecnica delle Unità di Raccolta stesse. (O.54) Sono disponibili protocolli/accordi scritti che regolamentanoirapportifrailsteleudradessocollegate,che definiscono: qualifiche e competenze professionali necessarie per le attività di raccolta del sangue intero e degli emocomponenti presso le UdR; livello di informazione ed educazione da fornire ai donatori; modalità operative per la gestione e selezione dei donatori e per la raccolta di sangue intero ed emocomponenti;...
13 LA SELEZIONE DEL DONATORE E LA RACCOLTA DI S.I. ED EMOCOMP. LA REGOLAMENTAZIONE DEI RAPPORTI TRA I ST E LE UdR GESTITE DA ASSOCIAZIONI E FEDERAZIONI DONATORI SANGUE (O.54) modalità operative per la conservazione, il confezionamento e il trasporto al Servizio Trasfusionale delle unità raccolte; attività di controllo/monitoraggio della qualità dei prodotti e delle attività da garantire; modalità operative per la gestione delle apparecchiature e dei materiali da impiegare per la raccolta e la conservazione temporanea del sangue e degli emocomponenti; flussi informativi previsti. (O.55) Sono disponibili procedure scritte per il controllo ed il monitoraggio, da parte del ST, delle attività svolte dalle UdR ad esso collegate e del sangue intero e degli emocomponenti raccolti dalle stesse, nonché per l avvio di eventuali azioni correttive e preventive.
14 LA SELEZIONE DEL DONATORE Arrivo del donatore al ST o alla UdR Accertamento identità del donatore Donatore alla prima donazione Consegna materiale informativo Donatore periodico IL PROCESSO DI SELEZIONE DEL DONATORE Accettazione/Registrazione del donatore Raccolta dati anamnestici (questionario anamnestico)
15 LA SELEZIONE DEL DONATORE DONATORE ALLA PRIMA DONAZIONE NON DIFFERITA E DONATORE PERIODICO DONATORE ALLA PRIMA DONAZIONE DIFFERITA Determinazione della concentrazione di Hb Identificazione donatore ed etichettatura provette esami Colloquio, visita medica e valutazione stato di salute donatore Prelievo venoso per esami di QB e di controllo del donatore Accertamento dell idoneità del donatore Registrazioni secondo normativa vigente e congedo Prescrizione accertamenti Registrazioni secondo normativa vigente
16 LA SELEZIONE DEL DONATORE Valutazione idoneità alla donazione Giudizio di idoneità alla donazione Donatore idoneo? NO Gestione donatore non idoneo SÍ Acquisizione consenso informato alla donazione Generazione identificativo unità di sangue ed etichette
17 LA SELEZIONE DEL DONATORE Arrivo del donatore al ST o alla UdR Accoglienza/ Accertamento identità del donatore Identificazione/ Registrazione del donatore Presentazione/consegna materiale informativo (prima donazione) ISTeleUdRdevonogarantire: l identificazione anagrafica del donatore e la sua identificazione univoca(docum. di riconoscimento con foto, Tesserino associativo con foto e Codice Univoco di Identif.); la registrazione di tutti gli elementi utili alla sua rintracciabilità; la riservatezza e la sicurezza dei dati del donatore.
18 LA SELEZIONE DEL DONATORE Arrivo del donatore al ST o alla UdR Accoglienza/ Accertamento identità del donatore (O.5.1-UO.5.1) Per ogni donatore di sangue ed emocomponenti deve essere predisposta una cartella del donatore, compilata, conservata ed archiviata secondo i criteri definiti dalla normativa vigente. Identificazione/ Registrazione del donatore Presentazione/consegna materiale informativo (prima donazione) RISERVATEZZA E SICUREZZA DEI DATI DEL DONATORE
19 LA SELEZIONE DEL DONATORE (DMS , art. 2) Arrivo del donatore al ST o alla UdR Accoglienza/ Accertamento identità del donatore Identificazione/ Registrazione del donatore Presentazione/consegna materiale informativo (prima donazione) (O.35-UO.31) Viene garantito ai donatori, in collaborazione con il ST di riferimento e secondo le indicazioni dello stesso, adeguato materiale informativo in merito alle caratteristiche essenziali del sangue, degli emocomponenti e dei prodotti emoderivati, ai benefici che i pazienti possono ricavare dalla donazione, nonché alle malattie infettive trasmissibili ed ai comportamenti e stili di vita che possono pregiudicare la sicurezza del ricevente e del donatore. PROCEDURE/ACCORDI FORMALIZZATI TRA ST E UDR
20 LA SELEZIONE DEL DONATORE DONATORE PRIMA DONAZIONE NON DIFFERITA E DONATORE PERIODICO DONATORE ALLA PRIMA DONAZIONE DIFFERITA Compilazione questionario anamnestico Determinazione della concentrazione di Hb Colloquio, visita medica e valutazione stato di salute sonatore Valutazione idoneità del donatore Prescrizione accertamenti Registrazioni secondo normativa vigente Presentazione e consegna questionario anamnestico Compilazione questionario anamnestico Identificazione donatore ed etichettatura provette esami Prelievo venoso per esami di QB e di controllo del donatore Registrazioni secondo normativa vigente e congedo Il donatore deve compilare il questionario anamnestico ad ogni donazione da solo o con l assistenza di personale infermieristico adeguatamente formato, in condizioni atte ad assicurare la tutela della sua privacy e la necessaria riservatezza
21 LA SELEZIONE DEL DONATORE DONATORE ALLA PRIMA DONAZIONE DIFFERITA Presentazione e consegna questionario anamnestico Compilazione questionario anamnestico Identificazione donatore ed etichettatura provette esami Prelievo venoso per esami di QB e di controllo del donatore Registrazioni secondo normativa vigente e congedo Modalità definite per identificazione donatore ed etichettatura provette esami Identificazione del donatore (doc. di identificazione) ed inserimento nel Sistema Gestionale Informatico (SGI) della richiesta degli esami previsti (esami di qualificazione biologica e di controllo del donatore). Generazione delle etichette identificative per i campioni ematici (con il SGI o con altre modalità che garantiscono l univoca identificazione del campione). Etichettatura dei campioni prima della venipuntura.
22 LA SELEZIONE DEL DONATORE DONATORE ALLA PRIMA DONAZIONE DIFFERITA Presentazione e consegna questionario anamnestico Compilazione questionario anamnestico Identificazione donatore ed etichettatura provette esami Prelievo venoso per esami di QB e di controllo del donatore Registrazioni secondo normativa vigente e congedo Prelievo venoso per esami di QB e di controllo del donatore Regole formalizzate per l'effettuazione del prelievo e per la conservazione dei campioni biologici in relazione alla tipologia di esami da effettuare. Registrazioni secondo normativa vigente e congedo Richiesta prodotta e registrata secondo modalità che ne garantiscano il collegamento univoco al donatore e ai risultati analitici e la sua tracciabilità. Al termine del prelievo, controllo dell emostasi nella sede della venipuntura, valutazione dello stato di salute del donatore e congedo da parte dell infermiere.
23 LA SELEZIONE DEL DONATORE DONATORE PRIMA DONAZIONE NON DIFFERITA E DONATORE PERIODICO Compilazione questionario anamnestico Determinazione della concentrazione di Hb Colloquio, visita medica e valutazione stato di salute donatore Valutazione idoneità del donatore Prescrizione accertamenti Registrazioni secondo normativa vigente Determinazione della concentrazione di Hb Disponibilità di un numero di apparecchi per la determinazione della concentrazione emoglobinica predonazione atto a garantire il back-up. Colloquio, visita medica e valutazione stato di salute donatore (normativa vigente) Disponibilità Linee guida/protocolli su: criteri e modalità per accertamento idoneità donatoreadonazionedisangue,emcecse; modalità di svolgimento procedure di selezione; accertamenti diagnostici per ogni donazione e per i controlli periodici del donatore. Procedure scritte per comunicazione al donatore degli esiti degli accertamenti effettuati in occasione della donazione.
24 LA SELEZIONE DEL DONATORE Giudizio di idoneità alla donazione Valutazione idoneità alla donazione Giudizio di idoneità alla donazione Identificabilità del medico responsabile della selezione che ha effettuato la valutazione finale di idoneità. Registrazioni nella Cartella donatore. SÍ Donatore idoneo? NO Gestione donatore non idoneo Acquisizione consenso informato alla donazione Generazione identificativo unità di sangue ed etichette Gestione donatore non idoneo Procedure scritte per la gestione del donatore non idoneo e per l effettuazione di indagini retrospettive.
25 LA SELEZIONE DEL DONATORE Acquisizione consenso informato Valutazione idoneità alla donazione Modulo conforme alla normativa vigente, prima della donazione. Giudizio di idoneità alla donazione Generazione identificativo unità di sangue ed etichette SÍ Donatore idoneo? Acquisizione consenso informato alla donazione Generazione identificativo unità di sangue ed etichette Identificazione del ST-UdR (e di ogni loro ev. articolazione organizzativa) con un codice univoco correlato ad ogni unità di sangue, emocomponenti o CSE raccolta e ad ogni unità lavorata, conformemente alla normativa vigente. Norma UNI per identificazione univoca unità di S.I. ed emc Etichette generate esclusivamente dai SGI (LG CNS 01 Rev.1, )
26 LA RACCOLTA DI SANGUE INTERO, EMOCOMPONENTI E CSE Programmazione della raccolta del sangue e degli emocomponenti Programma di autosufficienza nazionale del sangue e dei suoi prodotti Programmazione regionale annuale Documenti di programmazione della raccolta annuale di sangue intero ed emocomponenti, definiti in collaborazione con le Associazioni e Federazioni dei donatori di sangue / con il Servizio Trasfusionale di riferimento in relazione ai bisogni locali e agli obiettivi regionali e nazionali. Accordi/atti contrattuali di pianificazione della cessione/ acquisizione verso l esterno.
27 LA RACCOLTA DI SANGUE INTERO, EMOCOMPONENTI E CSE IL PROCESSO DI RACCOLTA DI SANGUE INTERO E DI AFERESI Accoglienza e accertamento dell identità del donatore Registrazione della donazione di sangue o di emocomponenti Ispezione dei dispositivi impiegati per la raccolta Etichettatura dei dispositivi di prelievo e dei campioni Controllo apparecchiature e montaggio circuiti di raccolta emocomponenti Accertamento identità donatore prima della venipuntura
28 LA RACCOLTA DI SANGUE INTERO, EMOCOMPONENTI E CSE Verifica corrispondenza donazione, donatore, dispositivi di prelievo e campioni Detersione e disinfezione della cute sede venipuntura Raccolta di sangue intero, emocomponenti o CSE Raccolta campioni per indagini di laboratorio Osservazione donatore e progressione/andamento raccolta Gestione eventuali reazione avverse del donatore Saldatura raccordi sistemi di prelievo a fine procedura
29 LA RACCOLTA DI SANGUE INTERO, EMOCOMPONENTI E CSE Ispezione e controllo unità a fine procedura Registrazione dati relativi alla raccolta Conservazione e trasporto delle unità di sangue, emocomponenti e CSE raccolti Invio al laboratorio di processazione informazioni su raccolta CSE Conservazione ed invio dei campioni per le indagini di laboratorio Informazione sui comportamenti post donazione Riposo/ristoro e congedo del donatore
30 LA RACCOLTA DI SANGUE INTERO, EMOCOMPONENTI E CSE Accoglienza e accertamento identità del donatore Registrazione della donazione di sangue o di emocomponenti Ispezione dei dispositivi impiegati per la raccolta Etichettatura dei dispositivi di prelievo e dei campioni Procedure scritte che definiscono le modalità per: la verifica sicura della identità del donatore e la sua corretta registrazione; l ispezione dei dispositivi impiegati per la raccolta, prima e dopo il prelievo; la reidentificazione positiva del donatore immediatamente prima della venipuntura; la detersione e disinfezione della cute precedenti la venipuntura; l esecuzione di una seconda venipuntura, se necessaria; l effettuazione della raccolta. Sistema di identificazione ed etichettatura atto ad assicurare: l univoca identificazione di ogni donatore, unità di sangue, emc, sacca satellite dei sistemi di prelievo (prima della raccolta), frazione di emc, unità di CSE, emc assemblato e campione biologico associato alla donazione; il loro collegamento univoco alle registrazioni relative al donatore.
31 LA RACCOLTA DI SANGUE INTERO, EMOCOMPONENTI E CSE Controllo apparecchiature e montaggio circuiti di raccolta emocomponenti Accertamento identità donatore prima della venipuntura Verifica corrispondenza donazione, donatore, dispositivi di prelievo e campioni Prima della venipuntura deve essere accuratamente controllata la corrispondenza tra i dati identificativi dell unità di sangue o di emocomponenti e i campioni biologici associati ed il loro collegamento univoco al donatore. Detersione e disinfezione della cute sede venipuntura
32 LA RACCOLTA DI SANGUE INTERO, EMOCOMPONENTI E CSE REQUISITI TECNOLOGICI Raccolta di sangue intero, emocomponenti o CSE Raccolta campioni per indagini di laboratorio Osservazione donatore e progressione/ andamento raccolta Gestione eventuali reazione avverse del donatore Dispositivi di prelievo conformi a normativa vigente, che garantiscano la prevenzione del rischio di contaminazione microbica, come la deviazione del primo volume di sangue raccolto. Raccolta S.I.: bilance automatizzate basculanti (1 per ogni postazione attiva) che garantiscano la corretta miscelazione del sangue con l anticoagulante e almeno la rilevazione del volume del sangue prelevato ed il tempo di prelievo. Aferesi produttiva: separatori cellulari atti a garantire il massimo grado di sicurezza per il donatore. Aferesi terapeutica e raccolta di CSE: apparecchiature atte a garantire elevati livelli di sicurezza per donatori e pazienti, nonché, per le CSE, conformi agli standard trapiantologici definiti con Unità di trap. emopoietico. Lettini o poltrone da prelievo atti a garantire le basilari manovre di primo soccorso. Dotazione per la gestione delle emergenze cliniche prevista dalla normativa vigente.
33 LA RACCOLTA DI SANGUE INTERO, EMOCOMPONENTI E CSE Raccolta di sangue intero, emocomponenti o CSE Raccolta campioni per indagini di laboratorio Presenza di almeno un infermiere e disponibilità di un medico del ST (Per UdR: un medico in possesso delle qualifiche e delle competenze richieste) Osservazione donatore e progressione/ andamento raccolta Gestione eventuali reazione avverse del donatore (UO.23) Tutte le reazioni indesiderate gravi e gli incidenti gravi correlati alle attività di raccolta di sangue intero ed emocomponenti devono essere documentati, gestiti e notificati al Servizio Trasfusionale di riferimento secondo le indicazioni ricevute dal Servizio stesso.
34 LA RACCOLTA DI SANGUE INTERO, EMOCOMPONENTI E CSE Saldatura raccordi sistemi di prelievo Saldatura raccordi sistemi di prelievo a fine procedura Sistemi di saldatura idonei a prevenire il rischio di contaminazione microbica in fase di raccolta e, per i ST, in fase di produzione degli emocomponenti. Ispezione e controllo unità a fine procedura Ispezione e controllo unità a fine proced. Procedureperilcontrollodelleunitàafine procedura e criteri di valutazione della loro utilizzabilità in caso di interruzioni o nel caso di superamento dei tempi max di prelievo previsti dalle norme.
35 LA RACCOLTA DI SANGUE INTERO, EMOCOMPONENTI E CSE Registrazione dati relativi alla raccolta Conservazione e trasporto delle unità di sangue, emocomponenti e CSE raccolti Invio al laboratorio di processazione di informazioni su raccolta CSE Conservazione ed invio dei campioni per le indagini di laboratorio Procedure scritte per: l identificazione del personale che ha effettuato le operazioni di raccolta; la registrazione dei dati relativi ad ogni procedura di prelievo, comprese quelle non completate; l invio al laboratorio di processazione, da parte del personale che ha effettuato la raccolta di CSE periferiche, di una relazione contenente le informazioni relative al prelievo definite dalla normativa vigente; la conservazione ed invio dei campioni per le indagini di laboratorio prelevati al momento della raccolta.
36 LA RACCOLTA DI SANGUE INTERO, EMOCOMPONENTI E CSE Al termine della donazione: Informazione sui comportamenti post donazione Riposo/ristoro e congedo del donatore il donatore riposa sul lettino di prelievo; l infermiere ricorda al donatore i comportamenti da tenere nel postdonazione; l infermiere congeda il donatore solo dopo averne accertato lo stato di completo benessere; ilmedico,cheèintervenutoin presenza di reazione indesiderata o di malessere del donatore, ha la responsabilità di congedare il donatore; ildonatore,dopoilcongedo,sirecanel locale/spazio di ristoro per consumare un adeguato ristoro.
37 LA PRODUZIONE DI EMOCOMPONENTI
38 LA PRODUZIONE DI EMOCOMPONENTI I ST, pur nelle diverse condizioni operative, devono garantire una produzione di emc conforme agli standard di sicurezza e qualità previsti dalla normativa vigente. Tale conformità deve essere riscontrabile alle ispezioni delle Autorità Competenti. Il quadro normativo europeo per gli emoderivati FARMACI DERIVATI DAL PLASMA Trasposizione Direttiva 2003/63/CE D.M Trasposizione Direttiva 2001/83/CE e. mod. D.Lgs. 219/2006 Disposizioni su documentazioni da presentare a corredo delle domande di autorizzazione all'immissione in commercio di medicinali ad uso umano in attuazione della direttiva 2003/63/CE della Commissione del Attuazione della direttiva 2001/83/CE (e successive direttive di modifica) relativa ad un codice comunitario concernente i medicinali per uso umano, nonché della direttiva 2003/94/CE EMA Guidelines su PMF, Infezioni trasmissibili, Plasmaderivati EU Farmacopea EU Annex 14 GMPs
39 LA PRODUZIONE DI EMOCOMPONENTI Il quadro normativo europeo che interessa il sistema sangue Trasposizione Direttiva 2004/23/CE D.Lgs. 191/2007 Norme di qualità e di sicurezza per la donazione, l'approvvigionamento, il controllo, la lavorazione, la conservazione, lo stoccaggio e la distribuzione di tessuti e cellule umani CELLULE E TESSUTI Trasposizione Direttiva 2006/17/CE Direttiva 2006/86/CE D.Lgs. 16/2010 Prescrizioni tecniche per la donazione, l'approvvigionamento e il controllo di tessuti e cellule umani, nonché, per quanto riguarda la rintracciabilità, la notifica di reazioni ed eventi avversi gravi e prescrizioni tecniche per la codifica, la lavorazione, la conservazione, lo stoccaggio e la distribuzione di tessuti e cellule umani «Requisiti organizzativi, strutturali e tecnologici minimi per l esercizio delle attività sanitarie delle Banche di sangue da cordone ombelicale». (Rep. Atti n. 184/CSR del ) «LG per l'accreditamento delle Banche di sangue da cordone ombelicale».(rep. Atti n. 75/CSR del )
40 LA PRODUZIONE DI EMOCOMPONENTI Il Consiglio d Europa ha reso disponibile per gli Stati membri una appendice tecnica alla Raccomandazione n. R(95)15 del Comitato dei Ministri, predisposta sulla base della Farmacopea EU e delle Direttive Europee e periodicamente aggiornata. Set di PRINCIPI e di STANDARD minimi che dovrebbero formare la base per la definizione di un operatività orientata a sicurezza, efficacia e qualità dei componenti del sangue e dei processi trasfusionali. Trattato di Amsterdam (art. 152, 4, 1999) Adottare misure che fissino elevati standard di qualità e sicurezza degli organi e delle sostanze di origine umana, sangue ed emoderivati
41 LA PRODUZIONE DI EMOCOMPONENTI Linee Guida per l accreditamento dei ST e delle UdR Rep. Atti n. 149/CSR Ulteriori requisiti organizzativi per l'accreditamento istituzionale. Settore di esclusiva pertinenza dei Servizi Trasfusionali. Competenza professionale di Medici e Infermieri addetti alla raccolta del sangue/emocomponenti(all. A; A2). Qualificazione ed efficienza del processo attraverso la concentrazione delle attività: volume minimo lavorazione = Unità di sangue intero/anno( All.A/C).
42 LA PRODUZIONE DI EMOCOMPONENTI Appropriato livello di controllo IGIENE AMBIENTALE Accesso controllato. Pareti e pavimenti integri, lavabili e disinfettabili. Ambienti, strumenti, superfici puliti e sanificati. Controllo di temperatura, umidità, ventilazione. Misure per il pest control. Gestione rifiuti. Norme comportamentali per il personale. Sorveglianza della carica microbica: Pianificazione (metodi di campionamento e di analisi, frequenza, punti critici, ) Controlli Registrazione risultati e valutazione Certificazioni finali
43 LA PRODUZIONE DI EMOCOMPONENTI Ricevimento unità di S.I. Ispezione unità Bilanciamento unità Centrifugazione unità e controllo unità centrifugate IL PROCESSO DI PRODUZIONE Separazione S.I.: produzione emocomponenti di I e II livello Collocazione emocomponenti nei siti di conservazione in attesa di validazione Controllo qualità emocomponenti
44 LA PRODUZIONE DI EMOCOMPONENTI Ricevimento unità di S.I. REQUISITI TECNOLOGICI Ispezione unità Bilanciamento unità Centrifugazione unità e controllo unità centrifugate Separazione S.I.: produzione emocomponenti di I e II livello Collocazione emocomponenti nei siti di conservazione in attesa di validazione Controllo qualità emocomponenti Sistemi di saldatura dei circuiti di raccordo dei sistemi di prelievo idonei a prevenire il rischio di contaminazione microbica in fase di raccolta e di produzione emocomponenti. Per le attività di frazionamento del sangue intero in circuito chiuso con mezzi fisici semplici: almeno una centrifuga refrigerata per sacche con funzionalità di gestione e controllo di accelerazione e velocità di centrifugazione; sistemi automatizzati per la scomposizione del sangue intero, atti almeno a rilevare i volumi dei singoli emocomponenti prodotti.
45 LA PRODUZIONE DI EMOCOMPONENTI CENTRIFUGHE PER LE UNITÁ DI SANGUE Possibilità di impostare i profili di lavoro (rpm, accelerazione e decelerazione, tempo, temperatura,...). Tracciabilità delle sedute. SCOMPOSITORI Automatizzati e programmabili. Compatibili con i dispositivi di prelievo. Adeguati al repertorio emocomponenti. Testine saldanti, sensori di livello e di regolazione del flusso. Pesatura netta degli emocomponenti. Trasferimento informatico dei dati al gestionale e tracciabilità.
46 LA PRODUZIONE DI EMOCOMPONENTI Ricevimento unità di S.I. Ispezione unità Bilanciamento unità REQUISITI TECNOLOGICI Sistema di connessione sterile convalidato per l assemblaggio di emocomponenti con interruzione del circuito chiuso. Centrifugazione unità e controllo unità centrifugate Separazione S.I.: produzione emocomponenti di I e II livello Almeno un apparecchio per il congelamento del plasma prodotto atto a garantire la conformità alle specifiche definite dalle normative vigenti. Collocazione emocomponenti nei siti di conservazione in attesa di validazione Almeno un apparecchio per lo scongelamento del plasma, atto a garantire lo scongelamento a temperatura controllata. Controllo qualità emocomponenti
47 LA PRODUZIONE DI EMOCOMPONENTI SISTEMA DI CONNESSIONE STERILE Connessione e allineamento Un sistema validato e utilizzato correttamente consente di equiparare le procedure al sistema chiuso Controllo tenuta Pulizia e controllo APPARECCHIO CONGELAMENTO PLASMA Minuti Strumento che consenta il congelamento rapido e completo in 1 hat<-30 Cnelcoredellasacca Temperatura - 30 (DM ; Guida EDQM; Farmacopea) APPARECCHIO SCONGELAMENTO PLASMA "Deve avvenire tra 30 e 37, in strumento che consenta il controllo della Temperatura"(DM )
48 LA PRODUZIONE DI EMOCOMPONENTI (O.56) Tutto il sangue intero allogenico raccolto viene sottoposto a separazione in emocomponenti. Eventuali deviazioni sono documentate e motivate. REPERTORIO EMOCOMPONENTI FORMALIZZATO E COERENTE CON LA PROGRAMMAZIONE SANITARIA EMOCOMPONENTE METODO PREPARAZIONE SOLUZIONE CONSERVANTE CONTENUTO MEDIO TEMPERATURA CONSERVAZIONE VALIDITÁ ALTRE SPECFICHE (O.57) Sono disponibili procedure scritte, conformi alla normativa vigente, preventivamente convalidate e riconvalidate ad intervalli periodici e a seguito di modifiche rilevanti introdotte nel processo, per lo svolgimento delle attività di lavorazione del sangue e degli emocomponenti destinati ad uso trasfusionale.
49 LA PRODUZIONE DI EMOCOMPONENTI Ricevimento unità di S.I. Ispezione unità Bilanciamento unità Centrifugazione unità e controllo unità centrifugate Separazione S.I.: produzione emocomponenti di I e II livello Collocazione emocomponenti nei siti di conservazione in attesa di validazione Controllo qualità emocomponenti Ricevimento e ispezione unità Conformità trasporto(tempi, contenitori, confezionamento, temperatura) e documenti di accompagnamento. Verifica stato di conservazione unità e rilevazione di eventuali anomalie (saldature, etichettature, volumi, coaguli,...) e gestione non conformità. Lavorazione unità Definizione metodi di lavorazione: Tempi limite e conservazione preseparazione. Piano di lavoro coerente con sistemi di prelievo/lavorazione e necessità terapeutiche. Registrazione attività, inconvenienti, operatori.
50 LA PRODUZIONE DI EMOCOMPONENTI Ricevimento unità di S.I. Ispezione unità Bilanciamento unità In caso di preparazione di emocomponenti in sistema aperto, applicazione di modalità operative atte a prevenire il rischio di contaminazione microbica. Centrifugazione unità e controllo unità centrifugate Separazione S.I.: produzione emocomponenti di I e II livello Collocazione emocomponenti nei siti di conservazione in attesa di validazione Controllo qualità emocomponenti Procedure convalidate. Competenza operatori. Igiene (ambiente, personale, DPI, strumenti). Identificazione dei livelli di pulizia dell aria (at rest in operation). Filtrazione aria. Separazione aree per fasi di lavoro. Monitoraggio microbiologico pianificato e valutato(aria, strumenti e superfici).
51 LA PRODUZIONE DI EMOCOMPONENTI Ricevimento unità di S.I. Ispezione unità Bilanciamento unità Centrifugazione unità e controllo unità centrifugate (O.57.2) La produzione di plasma da inviare alla lavorazione farmaceutica viene effettuata in conformità alla normativa nazionale vigente, nonché ai requisiti stabiliti dalle norme comunitarie inerenti al plasma come materia prima per la produzione di farmaci plasmaderivati. Separazione S.I.: produzione emocomponenti di I e II livello Collocazione emocomponenti nei siti di conservazione in attesa di validazione Controllo qualità emocomponenti Nel ST devono essere applicate sia le Buone Pratiche (Good Practices) sia le Buone Norme di Fabbricazione (Good Manufacturing Practices). I requisiti di cui all Accordo Stato-Regioni prevedono già tale integrazione.
52 LA PRODUZIONE DI EMOCOMPONENTI Ricevimento unità di S.I. Ispezione unità Bilanciamento unità Centrifugazione unità e controllo unità centrifugate Separazione S.I.: produzione emocomponenti di I e II livello Collocazione emocomponenti nei siti di conservazione in attesa di validazione Procedure scritte per lo svolgimento delle attività di produzione di emocomponenti per uso non trasfusionale(es. gel piastrinico, colla di fibrina, etc.). Procedure scritte e convalidate per il congelamento del plasma prodotto, per la sua conservazione successiva al congelamento e per il suo scongelamento. Procedure scritte e convalidate per le attività di congelamento e scongelamento dei globuli rossi e delle piastrine per uso trasfusionale. Controllo qualità emocomponenti
53 LA PRODUZIONE DI EMOCOMPONENTI Ricevimento unità di S.I. Ispezione unità Bilanciamento unità Centrifugazione unità e controllo unità centrifugate Separazione S.I.: produzione emocomponenti di I e II livello PIANO CONTROLLI QUALITÁ FORMALIZZATO Parametri, N unità da controllare, frequenza Sedi di esecuzione Metodi di analisi appropriati, affidabili e sotto controllo Valori attesi e soglie di criticità Metodi di campionamento Registrazioni, archiviazione Responsabilità (esecuzione, valutazione, sorveglianza) Riesame periodico e valutazioni statistiche Collocazione emocomponenti nei siti di conservazione in attesa di validazione Controllo qualità emocomponenti Riferimenti DMS , All.2 Preparazione emc e conservazione. Guida EDQM, Monografie emc. Raccomandazioni SIMTI. Convenzione per la lavorazione industriale.
54 LA PRODUZIONE DI EMOCOMPONENTI PLASMA FRESCO CONGELATO DA SANGUE INTERO Parametri Standard richiesti Frequenza Metodo Volume Valori stabiliti Tutte Peso bilance tarate FVIII 70% Pool di 6 Uogni 2 mesi Gruppi ABO diversi 1 e ultimo mese di conservazione Lab. Coagulazione Proteine Totali > 50g/L Campione Lab. Chimica Clinica Cellule residue GR: <6.0x10 9 /L GB: <0.1x10 9 /L PLT: <50 x10 9 /L 1% delle unità min. 4/mese GR e PLT: Contaglobuli GB: Citofluorimetro Integrità Nessuna rotturain qualsiasi parte della sacca Tutte dopo estrazione, congelamento, scongelamento Ispezione visiva Aspetto Nessun colore anomalo Nessun precipitato visibile Tutte Ispezione visiva Ab irregolari Assenza di anticorpi clinicamente significativi Tutte Lab. Immunoematologia Sterilità Negativa Campione Fine conservazione Lab. Microbiologia
55 LA PRODUZIONE DI EMOCOMPONENTI CONTROLLO STATISTICO DI PROCESSO Utilizzo di tecniche statistiche al fine di determinare se un processo è in grado di fornire output che soddisfino gli standard predefiniti e se è stabile nel tempo CONVALIDA DEI PROCESSI - MISURA DELLA CAPABILITY "Disegno sperimentale" valutazione strutturata dell'incidenza dei fattori critici del processo identificati sulla variabilità del processo stesso. Determinazione del numero di prove. MONITORAGGIO DEL PROCESSO - CONTROLLO DELLA STABILITÁ Tecniche statistiche applicabili alla produzione/controllo degli emocomponenti, modalità di campionamento e di raccolta, elaborazione e presentazione dei dati.
56 L ETICHETTATURA, IL CONFEZIONAMENTO, LA CONSERVAZIONE E IL TRASPORTO DEL SANGUE E DEGLI EMOCOMPONENTI
57 ETICHETTATURA, CONFEZIONAMENTO, CONSERVAZIONE E TRASPORTO DEL SANGUE E DEGLI EMOCOMPONENTI (O.80-UO.42) Sono disponibili procedure scritte, conformi alla normativa vigente(per UdR: e alle indicazioni del responsabile del ST di riferimento), preventivamente convalidate e riconvalidate ad intervalli periodici e a seguito di modifiche rilevanti, per la conservazione, il confezionamento ed il trasporto del sangue e degli emocomponenti a qualunque uso siano destinati, atte a garantire il mantenimento delle caratteristiche biologiche e qualitative degli stessi, nonché la tutela della sicurezza degli operatori e dell ambiente. (O.74) Sono disponibili documenti, destinati alle strutture di diagnosi e cura, approvati dal CoBUS, che, definiscono le modalità e/o i criteri per il ritiro e trasporto delle unità di emocomponenti. L unità restituita deve essere accompagnata da una documentazione attestante la sua integrità e l osservanza delle istruzioni definite dal ST relativamente alla sua conservazione e trasporto
58 CONFEZIONAMENTO E TRASPORTO DEL SANGUE E DEGLI EMC CATENA DEL TRASPORTO DM , Art Le strutture trasfusionali predispongono procedure atte a garantire che il trasporto di sangue ed emc ad ogni stadio della catena trasfusionale avvenga in condizioni che consentono di mantenere l integrità del prodotto. 2. Le sacche contenenti unità di sangue e di emc devono essere ispezionate immediatamente prima del trasporto ed in caso di riscontro di eventuali anomalie dell aspetto e del colore devono essere eliminate. L esame ispettivo delle sacche deve essere ripetuto da chi riceve i preparati inviati. Trasporto: movimentazione di sangue o emocomponenti al di fuori del ST
59 CONFEZIONAMENTO E TRASPORTO DEL SANGUE E DEGLI EMC CONFEZIONAMENTO PER TRASPORTO SU STRADA Accordi internaz., in conformità a norme EU per trasporto merci pericolose su strada(adr- Agreement dangerous road) Ministero infrast. e trasporti, DM Regolamentazione autoveicoli destinati a trasporto plasma e organi CMS n Raccomandazioni per sicurezza trasporto materiali potenzialmente infettivi o biologici deperibili e di campioni diagnostici: Involucri primario, secondario, esterno Etichettatura Documenti di accompagnamento(ddt, BL, etc.) Istruzioni di sicurezza e trattamento emergenze Trasportatori formati APPARECCHIATURE PER TRASPORTO Contenitore esterno rigido con chiusura ermetica, tale da evitare danni fisici al contenuto(rottura sacca e dispersione sangue). Dotazione di un sistema per garantire una temperatura adeguata per ciascun tipo di unità/ successiva lavorazione. Cautela nel posizionamento e trattamento del contenitore durante i trasferimenti. Mezzo di trasporto dotato di presa elettrica.
60 CONFEZIONAMENTO E TRASPORTO DEL SANGUE E DEGLI EMC DISPOSITIVI PER LA RILEVAZIONE DELLA TEMPERATURA DI TRASPORTO Data logger: Dispositivo elettronico da impostare con apposito SW. Rileva e registra temperatura e umidità a intervalli stabiliti. Con lo scarico su PC i dati possono essere rappresentati graficamente, valutati e archiviati. BTT-Blood Temperature Tag: Dispositivo RFID per la rilevazione e registrazione della temperatura. La visualizzazione dei dati su PC ne consente stampa, valutazione ed archiviazione. E' comunque ammessa anche la registrazione delle temperature con termometri di minima e di massima. Valutazioni su registrazioni manuali. Orari partenza e arrivo presa in carico TRACCIABILITÁ TRASPORTI Monitoraggio temperatura (almeno min e max) REGOLE STABILITE E REGISTRAZIONI Operatori Inconvenienti, non conformità
61 ETICHETTATURA DEL SANGUE E DEGLI EMOCOMPONENTI ETICHETTATURA (O.67) Il sistema di etichettatura delle unità di sangue, di emocomponenti e di CSE periferiche raccolte, degli emocomponenti intermedi e di quelli finali deve identificare, senza possibilità di errore, il tipo di contenuto e riportare tutte le informazioni prescritte dalla normativa vigente. (UO.39) Viene garantito l utilizzo di un sistema di identificazione ed etichettatura, secondo le indicazioni fornite dal Servizio Trasfusionale di riferimento, atto ad assicurare: l univoca identificazione di ogni donatore, unità di sangue ed emocomponente, sacca satellite dei sistemi di prelievo(prima della raccolta) e campione biologico associato alla donazione; il loro collegamento univoco alle registrazioni relative al donatore. DM Art Sui contenitori di unità di sangue e di emocomponenti devono essere apposte apposite etichette conformi a quanto indicato nell Allegato n. 3 del presente decreto, "Etichettatura".
62 ETICHETTATURA DEL SANGUE E DEGLI EMOCOMPONENTI (O.68) Le etichette devono essere generate dai sistemi gestionali informatici con garanzia di associazione univoca tra donatore, unità e risultati analitici e, in fase di assegnazione e consegna, tra donatore e ricevente. LG CNS 01 Rev. 1 del ETICHETTATURA INFORMATICA IN OGNI FASE Selezione Controllo prima della raccolta Campioni Sacca di raccolta IDENTIFICATIVO UNICO Corretta identificazione(unità, campioni, bleeding list). Piena tracciabilità del processo. Lettura automatica delle informazioni critiche. Doppia possibilità di lettura(a vista e automatica) per i dati rilevanti. Istruzioni per la corretta etichettatura.
63 ETICHETTATURA DEL SANGUE E DEGLI EMOCOMPONENTI ATTRIBUTI DELL ETICHETTA CONCENTRATO ERITROCITARIO BCD, IN SOLUZIONE ADDITIVA Nome ed indirizzo della struttura di prelievo Numero identificativo della donazione; Nome dell'emocomponente; Volume o peso netto dell'emocomponente GruppoAB0 e tipo Rh (D); Eventuali altri fenotipi gruppo ematici (se ricercati) Elenco ed esito negativo controlli infettivologici obbligatori; Composizione e volume della soluzione anticoagulante-conservante; Composizione e volume delle eventuali soluzioni additive; Data di donazione e di scadenza; Temperatura di conservazione; Eventuali lavorazioni ulteriori: leucodeplezione, irradiazione, Le diciture: «Non utilizzabile a scopo trasfusionale se presenta emolisi o altre anomalie evidenti» e «Per la trasfusione utilizzare un adatto dispositivo munito di un filtro da μm». LG CNS 01 Rev. 1 del Tutti i Servizi Trasfusionali Italiani adottano la norma UNI per la identificazione univoca delle unità di sangue intero e di emocomponenti (entro il )
64 ETICHETTATURA DEL SANGUE E DEGLI EMOCOMPONENTI (O.69) Al fine di garantire un elevato livello di sicurezza trasfusionale per quanto concerne la univoca tracciabilità e identificazione di ogni singolo emocomponente, devono essere predisposte e applicate specifiche procedure che prevedano: l obbligo di verifica informatizzata della corrispondenza tra etichetta di prelievo ed etichetta di validazione quale prerequisito per qualsivoglia utilizzo delle unità ed il blocco delle unità che non superano tale controllo; l assegnazione della funzione della duplicazione delle etichette di validazione a personale all uopo specificamente autorizzato, la documentazione del motivo per cui si effettua tale duplicazione, nonchè l obbligo di ripetere la verifica informatizzata della corrispondenza tra etichetta di prelievo ed etichetta di validazione ed il blocco delle unità che non superano tale controllo; la gestione delle unità provenienti da altra struttura mediante l esclusivo utilizzo del codice identificativo originario, al fine di evitare la rietichettatura delle unità. ETICHETTA DI PRELIEVO Validazione biologica : valutazione finale dell insieme degli elementi di qualificazione biologica della donazione e dei relativi prodotti, che consente di dichiararne l idoneità alla trasfusione (previo accertamento della compatibilità immunologica) e di effettuarne l etichettatura definitiva. ETICHETTA DI VALIDAZIONE
65 ETICHETTATURA DEL SANGUE E DEGLI EMOCOMPONENTI (O.70) L etichettatura delle unità autologhe di sangue, emocomponenti e CSE deve essere conforme alle prescrizioni della normativa vigente. (O.71) L etichettatura dei campioni biologici per i test analitici sui donatori deve essere effettuata in modo da garantire l univoca associazione con i donatori e le donazioni cui i campioni stessi sono associati. (O.72) Le etichette utilizzate devono essere idonee allo specifico impiego secondo la normativa vigente. (O.73) L etichettatura viene effettuata con modalità ed in ambienti atti a minimizzare il rischio di scambi ed errori. CONTROLLO ETICHETTATURA Identificazione aree dedicate e separazione effettiva durante l attività. Definizione modalità per garantire: il controllo in ogni fase di esattezza, integrità e leggibilità dell etichetta; l eliminazione di tutte le etichette di un donatore/una donazione non utilizzate.
66 CONSERVAZIONE DEL SANGUE E DEGLI EMOCOMPONENTI CONSERVAZIONE AREA DEDICATA Locali idonei all uso, tali da consentire le operazioni di pulizia e manutenzione per minimizzare il rischio di contaminazioni. Accesso controllato. Temperatura ambiente controllata. Impianto elettrico adeguato. Disposizione ordinata al fine di prevenire: contaminazioni cross contaminazioni mescolanza di prodotti diversi TECNOLOGIE UdR: Disponibilità di una apparecchiatura per la conservazione a temperatura controllata del sangue e degli emc raccolti, in relazione alle indicazioni del ST. ST: Disponibilità di almeno 2 congelatori per la conservazione del plasma alla temperatura di-25 C o inferiore.
67 CONSERVAZIONE DEL SANGUE E DEGLI EMOCOMPONENTI REQUISITI TECNOLOGICI ST e UdR (T.9-UT.8.1) Le apparecchiature destinate alla conservazione del sangue e degli emocomponenti devono essere dotate: di un sistema di controllo e di registrazione della temperatura, nonché di allarme acustico e visivo in caso di escursioni anomale rispetto alle temperature di esercizio definite; di dispositivi di allarme remotizzato sia acustici che visivi o di equivalenti strumenti di allerta qualora esse siano ubicate in locali o zone non costantemente presidiate da personale del Servizio o da altro personale a ciò deputato. Apparecchiature Adeguate per numero, capacità, struttura Possibilità di ispezioni, pulizie, collocazione ordinata unità Materiali resistenti a detergenti energici Uniformità della Temperatura Registrazione continua della temperatura Sistemi di allarmi acustici e visivi Predisposizione allarme remoto Conformità alle norme di sicurezza Garanzia di alimentazione elettrica Istruzioni Modalità di utilizzo e controllo Principali precauzioni d uso Uso specifico in relazione agli emocomponenti da conservare Misure igieniche e di sicurezza Manutenzioni(anchesuallarmiinsedeeadistanza)
68 CONSERVAZIONE DEL SANGUE E DEGLI EMOCOMPONENTI RILEVAZIONE E CONTROLLO TEMPERATURA DI CONSERVAZIONE SISTEMI DI RILEVAZIONE Registrazione continua della temperatura interna mediante sistemi: adiscocartaceo digitali (anche per umidità relativa) mediante sonde termiche collegate in rete ad un PC su cui è possibile raccogliere ed elaborare i dati di conservazione producendo report, istogrammi, etc. EVIDENZE OGGETTIVE Temperature impostate (esercizio ±) Temperatura in corso Registrazioni archiviate (DM , Art 15) Data, ora, firma di sostituzione/ valutazione del disco Piani e registrazione dei controlli e delle manutenzioni(allarmi compresi)
69 CONSERVAZIONE DEL SANGUE E DEGLI EMOCOMPONENTI REQUISITI ORGANIZZATIVI ST: Unità autologhe e unità raccolte e preparate per scopi specifici conservate separatamente Gestione delle unità scadute e delle unità a carico delle quali, durante la conservazione ed il trasporto, siano rilevate anomalie che ne compromettono l utilizzabilità Procedure per la gestione delle unità non utilizzabili Registrazioni informatiche Segregazione (collocazione fisica)
Torino 2012 Relatrice: Francesca Pollis
 Il trasporto, la conservazione e l etichettatura degli Emocomponenti Torino 2012 Relatrice: Francesca Pollis L ETICHETTATURA, IL CONFEZIONAMENTO, LA CONSERVAZIONE E IL TRASPORTO DEL SANGUE E DEGLI EMOCOMPONENTI
Il trasporto, la conservazione e l etichettatura degli Emocomponenti Torino 2012 Relatrice: Francesca Pollis L ETICHETTATURA, IL CONFEZIONAMENTO, LA CONSERVAZIONE E IL TRASPORTO DEL SANGUE E DEGLI EMOCOMPONENTI
Il sistema qualità in una Unità di Raccolta
 Il sistema qualità in una Unità di Raccolta Bologna, 22 dicembre 2012 Relatrice: Ivana Menichini (UO.1) L Unità di Raccolta deve istituire e mantenere un Sistema di gestione per la qualità, in raccordo
Il sistema qualità in una Unità di Raccolta Bologna, 22 dicembre 2012 Relatrice: Ivana Menichini (UO.1) L Unità di Raccolta deve istituire e mantenere un Sistema di gestione per la qualità, in raccordo
Corso di formazione PLASMA MASTER FILE Autosufficienza dei prodotti emoderivati Nuove modalità di prelievo e donazione
 Corso di formazione PLASMA MASTER FILE Autosufficienza dei prodotti emoderivati Nuove modalità di prelievo e donazione 2015: una realtà. I nuovi requisiti minimi per l autorizzazione e l accreditamento
Corso di formazione PLASMA MASTER FILE Autosufficienza dei prodotti emoderivati Nuove modalità di prelievo e donazione 2015: una realtà. I nuovi requisiti minimi per l autorizzazione e l accreditamento
Provinciale Roma. Relatori: dr. Michele Ciuffreda dr. Maurizio Cari Luciano Rutigliano
 UNITA DI RACCOLTA SANGUE Requisiti Minimi Relatori: dr. Michele Ciuffreda dr. Maurizio Cari Luciano Rutigliano UNITA DI RACCOLTA Decreto Legislativo 20 dicembre 2007, n. 261, articolo 2, comma 1, lettera
UNITA DI RACCOLTA SANGUE Requisiti Minimi Relatori: dr. Michele Ciuffreda dr. Maurizio Cari Luciano Rutigliano UNITA DI RACCOLTA Decreto Legislativo 20 dicembre 2007, n. 261, articolo 2, comma 1, lettera
Il ruolo dei Valutatori: l'importanza della formazione
 Il ruolo dei Valutatori: l'importanza della formazione Mantova, 10 marzo 2012 Relatrice: Ivana Menichini I requisiti specifici per l Autorizzazione e l Accreditamento delle UdR (UO.1) L Unità di Raccolta
Il ruolo dei Valutatori: l'importanza della formazione Mantova, 10 marzo 2012 Relatrice: Ivana Menichini I requisiti specifici per l Autorizzazione e l Accreditamento delle UdR (UO.1) L Unità di Raccolta
I requisiti di accreditamento dei Servizi trasfusionali
 I requisiti di accreditamento dei Servizi trasfusionali Dr.ssa Lucia Cretti Azienda Spedali Civili di Brescia Servizio di Immunoematologia e Medicina Trasfusionale LA NUOVA ORGANIZZAZIONE DEL SERVIZIO
I requisiti di accreditamento dei Servizi trasfusionali Dr.ssa Lucia Cretti Azienda Spedali Civili di Brescia Servizio di Immunoematologia e Medicina Trasfusionale LA NUOVA ORGANIZZAZIONE DEL SERVIZIO
2) Esperienza lavorativa: - avere maturato un esperienza lavorativa in ambito sanitario di almeno 3 anni.
 Allegato B). Modello per le visite di verifica dei servizi trasfusionali e delle unità di raccolta del sangue e degli emocomponenti ai sensi dell articolo 5 del decreto legislativo 20 dicembre 2007, n.
Allegato B). Modello per le visite di verifica dei servizi trasfusionali e delle unità di raccolta del sangue e degli emocomponenti ai sensi dell articolo 5 del decreto legislativo 20 dicembre 2007, n.
MEDICINA TRASFUSIONALE SERVIZI TRASFUSIONALI
 Servizi Trasfusionali Aziendali (STA). Si intendono le strutture e le relative articolazioni organizzative, comprese quelle per le attività di raccolta, previste dalla normativa vigente, secondo il modello
Servizi Trasfusionali Aziendali (STA). Si intendono le strutture e le relative articolazioni organizzative, comprese quelle per le attività di raccolta, previste dalla normativa vigente, secondo il modello
L INFORMATIZZAZIONE. Agostino Rossi SIMT di Piacenza
 Percorso regionale di formazione per il personale operante nelle attività di raccolta del sangue e degli emocomponenti (ai sensi delle LG per l ccreditamento del CNS) L INFRMTIINE gostino Rossi SIMT di
Percorso regionale di formazione per il personale operante nelle attività di raccolta del sangue e degli emocomponenti (ai sensi delle LG per l ccreditamento del CNS) L INFRMTIINE gostino Rossi SIMT di
SERVIZI TRASFUSIONALI REQUISITI MINIMI STRUTTURALI TECNOLOGICI E ORGANIZZATIVI SPECIFICI
 Allegato A). Requisiti strutturali, tecnologici e organizzativi minimi per l esercizio delle attività sanitarie dei servizi trasfusionali e delle unità di raccolta del sangue e degli emocomponenti, ai
Allegato A). Requisiti strutturali, tecnologici e organizzativi minimi per l esercizio delle attività sanitarie dei servizi trasfusionali e delle unità di raccolta del sangue e degli emocomponenti, ai
Le ri cadut e sul si st ema di raccol t a associ at i vo. Bernardi no Spal i vi ero
 Le ri cadut e sul si st ema di raccol t a associ at i vo Bernardi no Spal i vi ero Unità di Raccolta le strutture incaricate della raccolta, previa autorizzazione delle regioni o province autonome competenti,
Le ri cadut e sul si st ema di raccol t a associ at i vo Bernardi no Spal i vi ero Unità di Raccolta le strutture incaricate della raccolta, previa autorizzazione delle regioni o province autonome competenti,
LA CONFERENZA PERMANENTE PER I RAPPORTI TRA LO STATO, LE REGIONI E LE PROVINCE AUTONOME DI TRENTO E BOLZANO
 Testo aggiornato al 18 luglio 2012 Accordo 16 dicembre 2010, n. 242/Csr Gazzetta Ufficiale 17 maggio 2011, n. 113, S. O. Accordo, ai sensi dell articolo 4 del decreto legislativo 28 agosto 1997, n. 281,
Testo aggiornato al 18 luglio 2012 Accordo 16 dicembre 2010, n. 242/Csr Gazzetta Ufficiale 17 maggio 2011, n. 113, S. O. Accordo, ai sensi dell articolo 4 del decreto legislativo 28 agosto 1997, n. 281,
INDICE E STATO DELLE REVISIONI
 Dipartimento Interaziendale Regionale di Direttore Dott. Mario Piani RIF. NORMA UNI EN ISO 9001:2008 sviluppato dal Responsabile Assicurazione Qualità Dipartimentale Dott.ssa G. SIRACUSA e dal Gruppo di
Dipartimento Interaziendale Regionale di Direttore Dott. Mario Piani RIF. NORMA UNI EN ISO 9001:2008 sviluppato dal Responsabile Assicurazione Qualità Dipartimentale Dott.ssa G. SIRACUSA e dal Gruppo di
DM 2 novembre 2015 Disposizioni relative ai requisiti di qualità e sicurezza del sangue e degli emocomponenti Allegati V, VI, VII, VIII
 DM 2 novembre 2015 Disposizioni relative ai requisiti di qualità e sicurezza del sangue e degli emocomponenti Allegati V, VI, VII, VIII Giancarlo Maria Liumbruno Direttore Centro Nazionale Sangue Istituto
DM 2 novembre 2015 Disposizioni relative ai requisiti di qualità e sicurezza del sangue e degli emocomponenti Allegati V, VI, VII, VIII Giancarlo Maria Liumbruno Direttore Centro Nazionale Sangue Istituto
I requisiti specifici per l Autorizzazione e l Accreditamento dei ST e delle UdR
 Relazione Dr.ssa Menichini I requisiti specifici per l Autorizzazione e l Accreditamento dei ST e delle UdR a cura dello studio necstep MAPPA SISTEMA DI GESTIONE PER LA QUALITÁ Processo di indirizzo
Relazione Dr.ssa Menichini I requisiti specifici per l Autorizzazione e l Accreditamento dei ST e delle UdR a cura dello studio necstep MAPPA SISTEMA DI GESTIONE PER LA QUALITÁ Processo di indirizzo
l Allegato II Sala Cesari Casa del Donatore Bologna, sabato 16 gennaio 2016
 Decreto Ministero della Salute 2.11.2015 pubblicato su GURI SG n.300 del 28.12.2015 "Disposizioni relative ai requisiti di qualità e sicurezza del sangue e degli emocomponenti" Coordinatore del Comitato
Decreto Ministero della Salute 2.11.2015 pubblicato su GURI SG n.300 del 28.12.2015 "Disposizioni relative ai requisiti di qualità e sicurezza del sangue e degli emocomponenti" Coordinatore del Comitato
REGIONE VENETO / Segreteria regionale Sanità e Sociale- ARSS Agenzia Regionale Sanitaria e Sociosanitaria
 BSC.XX.1.0 SELEZIONE BSC.AC.1.1 La BSC, sentite le AS afferenti, definisce POS conformi alla normativa e a criteri regionali condivisi, in merito a: selezione dei donatori, esami di laboratorio di idoneità
BSC.XX.1.0 SELEZIONE BSC.AC.1.1 La BSC, sentite le AS afferenti, definisce POS conformi alla normativa e a criteri regionali condivisi, in merito a: selezione dei donatori, esami di laboratorio di idoneità
Ministero della Salute
 Ministero della Salute Guida all interpretazione dei requisiti specifici strutturali, tecnologici e organizzativi nelle Unità di Raccolta del sangue e degli emocomponenti - Aprile 2012 Guida elaborata
Ministero della Salute Guida all interpretazione dei requisiti specifici strutturali, tecnologici e organizzativi nelle Unità di Raccolta del sangue e degli emocomponenti - Aprile 2012 Guida elaborata
 Le regole del parlamento europeo per garantire qualità e sicurezza nel trattamento di cellule e tessuti umani (Direttiva 2004/23/CE) E stata recentemente recepita anche dall Italia, la direttiva europea
Le regole del parlamento europeo per garantire qualità e sicurezza nel trattamento di cellule e tessuti umani (Direttiva 2004/23/CE) E stata recentemente recepita anche dall Italia, la direttiva europea
Effettuare gli audit interni
 Scopo Definire le modalità per la gestione delle verifiche ispettive interne Fornitore del Processo Input Cliente del Processo Qualità (centrale) e Referenti Qualità delle sedi territoriali Direzione Qualità
Scopo Definire le modalità per la gestione delle verifiche ispettive interne Fornitore del Processo Input Cliente del Processo Qualità (centrale) e Referenti Qualità delle sedi territoriali Direzione Qualità
Identificazione del paziente all atto della richiesta di determinazione del gruppo sanguigno e prelievo di campioni di sangue INDICE
 Pag. 1 di 5 INDICE 1. SCOPO 2. CAMPO DI APPLICAZIONE 3. RIFERIMENTI 4. DEFINIZIONI 5. RESPONSABILITÀ 6. DIAGRAMMA DI FLUSSO 7. DESCRIZIONE ATTIVITA' Data Descrizione Redatto Verificato Approvato 11-12-2012
Pag. 1 di 5 INDICE 1. SCOPO 2. CAMPO DI APPLICAZIONE 3. RIFERIMENTI 4. DEFINIZIONI 5. RESPONSABILITÀ 6. DIAGRAMMA DI FLUSSO 7. DESCRIZIONE ATTIVITA' Data Descrizione Redatto Verificato Approvato 11-12-2012
MANUALE DELLA QUALITA Revisione: Sezione 4 SISTEMA DI GESTIONE PER LA QUALITA
 Pagina: 1 di 5 SISTEMA DI GESTIONE PER LA QUALITA 4.0 SCOPO DELLA SEZIONE Illustrare la struttura del Sistema di Gestione Qualità SGQ dell Istituto. Per gli aspetti di dettaglio, la Procedura di riferimento
Pagina: 1 di 5 SISTEMA DI GESTIONE PER LA QUALITA 4.0 SCOPO DELLA SEZIONE Illustrare la struttura del Sistema di Gestione Qualità SGQ dell Istituto. Per gli aspetti di dettaglio, la Procedura di riferimento
PROGETTO TECNICO SISTEMA DI GESTIONE QUALITA IN CONFORMITÀ ALLA NORMA. UNI EN ISO 9001 (ed. 2008) n. 03 del 31/01/09 Salvatore Ragusa
 PROGETTO TECNICO SISTEMA DI GESTIONE QUALITA IN CONFORMITÀ ALLA NORMA UNI EN ISO 9001 (ed. 2008) Revisione Approvazione n. 03 del 31/01/09 Salvatore Ragusa PROGETTO TECNICO SISTEMA QUALITA Il nostro progetto
PROGETTO TECNICO SISTEMA DI GESTIONE QUALITA IN CONFORMITÀ ALLA NORMA UNI EN ISO 9001 (ed. 2008) Revisione Approvazione n. 03 del 31/01/09 Salvatore Ragusa PROGETTO TECNICO SISTEMA QUALITA Il nostro progetto
PROVINCIA AUTONOMA DI TRENTO
 Bollettino Ufficiale n. 23/I-II del 05/06/2012 / Amtsblatt Nr. 23/I-II vom 05/06/2012 127 PROVINCIA AUTONOMA DI TRENTO Reg.delib.n. 1078 Prot. n. VERBALE DI DELIBERAZIONE DELLA GIUNTA PROVINCIALE O G G
Bollettino Ufficiale n. 23/I-II del 05/06/2012 / Amtsblatt Nr. 23/I-II vom 05/06/2012 127 PROVINCIA AUTONOMA DI TRENTO Reg.delib.n. 1078 Prot. n. VERBALE DI DELIBERAZIONE DELLA GIUNTA PROVINCIALE O G G
MANUALE DELLA QUALITÀ Pag. 1 di 6
 MANUALE DELLA QUALITÀ Pag. 1 di 6 INDICE GESTIONE DELLE RISORSE Messa a disposizione delle risorse Competenza, consapevolezza, addestramento Infrastrutture Ambiente di lavoro MANUALE DELLA QUALITÀ Pag.
MANUALE DELLA QUALITÀ Pag. 1 di 6 INDICE GESTIONE DELLE RISORSE Messa a disposizione delle risorse Competenza, consapevolezza, addestramento Infrastrutture Ambiente di lavoro MANUALE DELLA QUALITÀ Pag.
Ministero della Salute
 Ministero della Salute Guida alla conduzione di Audit della Qualità - Giugno 2011 Guida elaborata a cura del Centro Nazionale Sangue Centro Nazionale Sangue Via Giano della Bella, 27 00162 Roma Tel: 06
Ministero della Salute Guida alla conduzione di Audit della Qualità - Giugno 2011 Guida elaborata a cura del Centro Nazionale Sangue Centro Nazionale Sangue Via Giano della Bella, 27 00162 Roma Tel: 06
Direttore Dr.ssa Tiziana Riscaldati. SIMT-POS 033 Look Back. Data: 20-01-2014
 1 Prima Stesura Redattori: Cosenza Data: 20-01-2014 1 2 1 SCOPO Lo scopo della presente procedura è specificare i criteri da adottare per l effettuazione di indagini e valutazioni retrospettive relative
1 Prima Stesura Redattori: Cosenza Data: 20-01-2014 1 2 1 SCOPO Lo scopo della presente procedura è specificare i criteri da adottare per l effettuazione di indagini e valutazioni retrospettive relative
CONFERENZA PERMANENTE PER I RAPPORTI TRA LO STATO LE REGIONI E LE PROVINCE AUTONOME DI TRENTO E BOLZANO
 CONFERENZA PERMANENTE PER I RAPPORTI TRA LO STATO LE REGIONI E LE PROVINCE AUTONOME DI TRENTO E BOLZANO ACCORDO 16 dicembre 2010 Accordo, ai sensi dell'articolo 4 del decreto legislativo 28 agosto 1997,
CONFERENZA PERMANENTE PER I RAPPORTI TRA LO STATO LE REGIONI E LE PROVINCE AUTONOME DI TRENTO E BOLZANO ACCORDO 16 dicembre 2010 Accordo, ai sensi dell'articolo 4 del decreto legislativo 28 agosto 1997,
PRESCRIZIONI PARTICOLARI DIRETTIVA 2006/42/CE RELATIVA ALLE MACCHINE Allegato X Garanzia Qualità Totale
 Titolo PRESCRIZIONI PARTICOLARI DIRETTIVA 2006/42/CE RELATIVA ALLE MACCHINE Allegato X Garanzia Qualità Totale Riferimento Data entrata in vigore Approvato da PR PART ON/MACC/X Rev. 0 del 01/06/2016 IMQ
Titolo PRESCRIZIONI PARTICOLARI DIRETTIVA 2006/42/CE RELATIVA ALLE MACCHINE Allegato X Garanzia Qualità Totale Riferimento Data entrata in vigore Approvato da PR PART ON/MACC/X Rev. 0 del 01/06/2016 IMQ
STUDIO PROFESSIONALE MEDICO
 Gli Studi Professionali Medici (SPM) sono strutture nelle quali è esercitata un attività sanitaria in cui il profilo professionale prevale su quello organizzativo. Tale profilo è riscontrabile non solo
Gli Studi Professionali Medici (SPM) sono strutture nelle quali è esercitata un attività sanitaria in cui il profilo professionale prevale su quello organizzativo. Tale profilo è riscontrabile non solo
PO 01 Rev. 0. Azienda S.p.A.
 INDICE 1 GENERALITA... 2 2 RESPONSABILITA... 2 3 MODALITA DI GESTIONE DELLA... 2 3.1 DEI NEOASSUNTI... 3 3.2 MANSIONI SPECIFICHE... 4 3.3 PREPOSTI... 4 3.4 ALTRI INTERVENTI FORMATIVI... 4 3.5 DOCUMENTAZIONE
INDICE 1 GENERALITA... 2 2 RESPONSABILITA... 2 3 MODALITA DI GESTIONE DELLA... 2 3.1 DEI NEOASSUNTI... 3 3.2 MANSIONI SPECIFICHE... 4 3.3 PREPOSTI... 4 3.4 ALTRI INTERVENTI FORMATIVI... 4 3.5 DOCUMENTAZIONE
SISTEMA DI GESTIONE INTEGRATO. Audit
 Rev. 00 del 11.11.08 1. DISTRIBUZIONE A tutti i membri dell organizzazione ING. TOMMASO 2. SCOPO Gestione degli audit interni ambientali e di salute e sicurezza sul lavoro 3. APPLICABILITÀ La presente
Rev. 00 del 11.11.08 1. DISTRIBUZIONE A tutti i membri dell organizzazione ING. TOMMASO 2. SCOPO Gestione degli audit interni ambientali e di salute e sicurezza sul lavoro 3. APPLICABILITÀ La presente
San Pancrazio, 29 06 2013
 San Pancrazio, 29 06 2013 Garanzia del Cittadino L istituto dell Accreditamento, nel suo complesso, è un sistema di garanzia del cittadino e della comunità. Accreditamento vuol dire Assicurare la sicurezza
San Pancrazio, 29 06 2013 Garanzia del Cittadino L istituto dell Accreditamento, nel suo complesso, è un sistema di garanzia del cittadino e della comunità. Accreditamento vuol dire Assicurare la sicurezza
REGIONE VENETO / Segreteria regionale Sanità e Sociale- ARSS Agenzia Regionale Sanitaria e Sociosanitaria
 Lista di verifica REQUITI MINIMI SPECIFICI E DI QUALITA' PER L'AUTORIZZAZIONE 1 - REQUITI ORGANIZZATIVI BSC.AU.1.0 STRUTTURA ORGANIZZATIVA BSC.AU.1.1 La BSC definisce l'organigramma e le responsabilità
Lista di verifica REQUITI MINIMI SPECIFICI E DI QUALITA' PER L'AUTORIZZAZIONE 1 - REQUITI ORGANIZZATIVI BSC.AU.1.0 STRUTTURA ORGANIZZATIVA BSC.AU.1.1 La BSC definisce l'organigramma e le responsabilità
CHECK LIST ANALISI INIZIALE ORGANIZZAZIONE E GESTIONE DELLA SALUTE E SICUREZZA SUL LAVORO
 CHECK LIST ANALISI INIZIALE ORGANIZZAZIONE E GESTIONE DELLA SALUTE E SICUREZZA SUL LAVORO QUESITO RISCONTRO* Documentazione di P N NA riscontro 1. ANALISI INIZIALE Il DVR /autocertificazione e gli allegati
CHECK LIST ANALISI INIZIALE ORGANIZZAZIONE E GESTIONE DELLA SALUTE E SICUREZZA SUL LAVORO QUESITO RISCONTRO* Documentazione di P N NA riscontro 1. ANALISI INIZIALE Il DVR /autocertificazione e gli allegati
Conferenza Stato Regioni
 Pagina 1 di 5 Conferenza Stato Regioni Accordo tra il Governo, le Regioni e le Province autonome di Trento e Bolzano sul documento recante Linee guida per l accreditamento delle Banche di sangue da cordone
Pagina 1 di 5 Conferenza Stato Regioni Accordo tra il Governo, le Regioni e le Province autonome di Trento e Bolzano sul documento recante Linee guida per l accreditamento delle Banche di sangue da cordone
DM.9 agosto 2000 LINEE GUIDA PER L ATTUAZIONE DEL SISTEMA DI GESTIONE DELLA SICUREZZA TITOLO I POLITICA DI PREVENZIONE DEGLI INCIDENTI RILEVANTI
 DM.9 agosto 2000 LINEE GUIDA PER L ATTUAZIONE DEL SISTEMA DI GESTIONE DELLA SICUREZZA TITOLO I POLITICA DI PREVENZIONE DEGLI INCIDENTI RILEVANTI Articolo 1 (Campo di applicazione) Il presente decreto si
DM.9 agosto 2000 LINEE GUIDA PER L ATTUAZIONE DEL SISTEMA DI GESTIONE DELLA SICUREZZA TITOLO I POLITICA DI PREVENZIONE DEGLI INCIDENTI RILEVANTI Articolo 1 (Campo di applicazione) Il presente decreto si
Lista di controllo n. 1.1 STUDIO ODONTOIATRICO
 Lista di controllo n. 1.1 STUDIO ODONTOIATRICO IL/LA SOTTOSCRITTO/A nato/a a prov. di il titolare/legale rappresentante della Società/Ente/Azienda ai sensi dell art. 5 c. 3 lett. e) del D.P.G.P. 27 novembre
Lista di controllo n. 1.1 STUDIO ODONTOIATRICO IL/LA SOTTOSCRITTO/A nato/a a prov. di il titolare/legale rappresentante della Società/Ente/Azienda ai sensi dell art. 5 c. 3 lett. e) del D.P.G.P. 27 novembre
TENUTA SOTTO CONTROLLO DELLE REGISTRAZIONI
 Rev.0 Data 10.10.2002 TENUTA SOTTO CONTROLLO DELLE REGISTRAZIONI Indice: 1.0 SCOPO 2.0 CAMPO DI APPLICAZIONE 3.0 RIFERIMENTI E DEFINIZIONI 4.0 RESPONSABILITÀ 5.0 MODALITÀ ESECUTIVE 6.0 ARCHIVIAZIONE 7.0
Rev.0 Data 10.10.2002 TENUTA SOTTO CONTROLLO DELLE REGISTRAZIONI Indice: 1.0 SCOPO 2.0 CAMPO DI APPLICAZIONE 3.0 RIFERIMENTI E DEFINIZIONI 4.0 RESPONSABILITÀ 5.0 MODALITÀ ESECUTIVE 6.0 ARCHIVIAZIONE 7.0
Il Sistema Qualità in una Unità di Raccolta. a cura dello studio necstep
 Il Sistema Qualità in una Unità di Raccolta a cura dello studio necstep MAPPA SISTEMA DI GESTIONE PER LA QUALITÁ Processo di indirizzo e pianificazione DOC Pianificazione prodotti-processi Piano Indicatori
Il Sistema Qualità in una Unità di Raccolta a cura dello studio necstep MAPPA SISTEMA DI GESTIONE PER LA QUALITÁ Processo di indirizzo e pianificazione DOC Pianificazione prodotti-processi Piano Indicatori
SGSL UN SISTEMA PER LA GESTIONE DELLA SICUREZZA SUL LAVORO NELLA SCUOLA
 SGSL UN SISTEMA PER LA GESTIONE DELLA SICUREZZA SUL LAVORO NELLA SCUOLA COSA È IN PRATICA UN SISTEMA DI GESTIONE? L insieme delle regole e dei processi di funzionamento di un organizzazione. Comprende:
SGSL UN SISTEMA PER LA GESTIONE DELLA SICUREZZA SUL LAVORO NELLA SCUOLA COSA È IN PRATICA UN SISTEMA DI GESTIONE? L insieme delle regole e dei processi di funzionamento di un organizzazione. Comprende:
AUDIT. 2. Processo di valutazione
 AUDIT 2. Processo di valutazione FASE ATTIVITA DESCRIZIONE Inizio dell'audit Inizio dell attività Costituzione del gruppo di valutazione sulla base delle competenze generali e specifiche e dei differenti
AUDIT 2. Processo di valutazione FASE ATTIVITA DESCRIZIONE Inizio dell'audit Inizio dell attività Costituzione del gruppo di valutazione sulla base delle competenze generali e specifiche e dei differenti
PUNTO DI RACCOLTA SANGUE CORDONALE
 Il Punto di Raccolta del Sangue Cordonale (PRSC) è la struttura del Percorso Nascita in rete, inteso come UO di Ostetricia e Ginecologia pubblica o privata, in cui è attivata la donazione e l invio del
Il Punto di Raccolta del Sangue Cordonale (PRSC) è la struttura del Percorso Nascita in rete, inteso come UO di Ostetricia e Ginecologia pubblica o privata, in cui è attivata la donazione e l invio del
MODALITÀ ORGANIZZATIVE E PIANIFICAZIONE DELLE VERIFICHE SUGLI IMPIANTI
 Pagina:1 di 6 MODALITÀ ORGANIZZATIVE E PIANIFICAZIONE DELLE VERIFICHE SUGLI IMPIANTI INDICE 1. INTRODUZIONE...1 2. ATTIVITÀ PRELIMINARI ALL INIZIO DELLE VERIFICHE...2 3. PIANO OPERATIVO DELLE ATTIVITÀ...2
Pagina:1 di 6 MODALITÀ ORGANIZZATIVE E PIANIFICAZIONE DELLE VERIFICHE SUGLI IMPIANTI INDICE 1. INTRODUZIONE...1 2. ATTIVITÀ PRELIMINARI ALL INIZIO DELLE VERIFICHE...2 3. PIANO OPERATIVO DELLE ATTIVITÀ...2
Direttore Dr.ssa Tiziana Riscaldati. SIMT-POS 051 Gestione del Campione di Sangue
 1 1 2 1 SCOPO. Descrivere le caratteristiche e le modalità di invio dei campioni inviati da soli, in associazione alle richieste trasfusionali o allo scopo di eseguire esami immunoematologici anche sulla
1 1 2 1 SCOPO. Descrivere le caratteristiche e le modalità di invio dei campioni inviati da soli, in associazione alle richieste trasfusionali o allo scopo di eseguire esami immunoematologici anche sulla
LA CONFERENZA PERMANENTE PER I RAPPORTI TRA LO STATO, LE REGIONI E LE PROVINCE AUTONOME DI TRENTO E BOLZANO
 Testo aggiornato al 2 ottobre 2013 Accordo 25 luglio 2012, n. 149/Csr Gazzetta Ufficiale 9 maggio 2013, n. 107 Accordo, ai sensi dell articolo 4 del decreto legislativo 26 agosto 1997, n. 281, tra il Governo,
Testo aggiornato al 2 ottobre 2013 Accordo 25 luglio 2012, n. 149/Csr Gazzetta Ufficiale 9 maggio 2013, n. 107 Accordo, ai sensi dell articolo 4 del decreto legislativo 26 agosto 1997, n. 281, tra il Governo,
QUESTIONARIO QUALIFICAZIONE FORNITORE
 Data: Spett.le Società vi informiamo che (inserire nome azienda) ha attivato un sistema di valutazione, qualificazione e monitoraggio dei propri fornitori. Nell ambito del nostro Sistema di Gestione della
Data: Spett.le Società vi informiamo che (inserire nome azienda) ha attivato un sistema di valutazione, qualificazione e monitoraggio dei propri fornitori. Nell ambito del nostro Sistema di Gestione della
COSTITUZIONE DELL ARCHIVIO BIOLOGICO NAZIONALE PER LA SICUREZZA DELLA RETE TRAPIANTOLOGICA ED ALLEGATO TECNICO.
 COSTITUZIONE DELL ARCHIVIO BIOLOGICO NAZIONALE PER LA SICUREZZA DELLA RETE TRAPIANTOLOGICA ED ALLEGATO TECNICO. (Consulta Nazionale per i Trapianti - 31 agosto 2004) 1. E costituito l Archivio Biologico
COSTITUZIONE DELL ARCHIVIO BIOLOGICO NAZIONALE PER LA SICUREZZA DELLA RETE TRAPIANTOLOGICA ED ALLEGATO TECNICO. (Consulta Nazionale per i Trapianti - 31 agosto 2004) 1. E costituito l Archivio Biologico
Doc Des PVD. Doc Proc PVD. Doc Proc PVD. Doc Proc PVD. Doc PVD. Doc PVD. V a camp. Doc. Des PVD. Des. Des
 Codice Requisiti per accreditamento O.1 Il Servizio Trasfusionale deve istituire e mantenere un Sistema di gestione per la qualità. Evi Mod MT STEMA DI GESTIONE PER LA QUALITÀ (Funzione di Garanzia della
Codice Requisiti per accreditamento O.1 Il Servizio Trasfusionale deve istituire e mantenere un Sistema di gestione per la qualità. Evi Mod MT STEMA DI GESTIONE PER LA QUALITÀ (Funzione di Garanzia della
SISTEMI DI GESTIONE PER LA QUALITÀ E R.S. DELLE STRUTTURE TRASFUSIONALI
 SISTEMI DI GESTIONE QUALITÀ E REQUISITI SPECIFICI DELLE STRUTTURE TRASFUSIONALI E DELLE UdR Dr. Pilade Cortellazzi Valutatore Regionale ER per il Sistema Sangue 5 Corso Regionale di formazione ed acquisizione
SISTEMI DI GESTIONE QUALITÀ E REQUISITI SPECIFICI DELLE STRUTTURE TRASFUSIONALI E DELLE UdR Dr. Pilade Cortellazzi Valutatore Regionale ER per il Sistema Sangue 5 Corso Regionale di formazione ed acquisizione
Documento in attesa di approvazione definitiva Nota per la Commissione Consultiva Permanente
 Commissione Consultiva Permanente Comitato n. 4 Modelli di Organizzazione e di Gestione (MOG) Documento in attesa di approvazione definitiva Nota per la Commissione Consultiva Permanente Prima di procedere
Commissione Consultiva Permanente Comitato n. 4 Modelli di Organizzazione e di Gestione (MOG) Documento in attesa di approvazione definitiva Nota per la Commissione Consultiva Permanente Prima di procedere
1 SCOPO E CAMPO DI APPLICAZIONE...2 2 RIFERIMENTI... 2 3 SIGLE E DEFINIZIONI... 2 4 RESPONSABILITA...3 5 PROCEDURA...3
 del 13 11 2012 Pagina 1 di 6 INDICE 1 SCOPO E CAMPO DI APPLICAZIONE...2 2 RIFERIMENTI... 2 3 SIGLE E DEFINIZIONI... 2 4 RESPONSABILITA...3 5 PROCEDURA...3 5.1 Programmazione delle attività...3 5.2 Documentazione...
del 13 11 2012 Pagina 1 di 6 INDICE 1 SCOPO E CAMPO DI APPLICAZIONE...2 2 RIFERIMENTI... 2 3 SIGLE E DEFINIZIONI... 2 4 RESPONSABILITA...3 5 PROCEDURA...3 5.1 Programmazione delle attività...3 5.2 Documentazione...
IL MINISTRO DEL LAVORO E DELLE POLITICHE SOCIALI di concerto con IL MINISTRO DELLA SALUTE
 Decreto del Ministero dell interno 4 febbraio 2011 Definizione dei criteri per il rilascio delle autorizzazioni di cui all art. 82, comma 2, del D.Lgs. 09/04/2008, n. 81, e successive modifiche ed integrazioni.
Decreto del Ministero dell interno 4 febbraio 2011 Definizione dei criteri per il rilascio delle autorizzazioni di cui all art. 82, comma 2, del D.Lgs. 09/04/2008, n. 81, e successive modifiche ed integrazioni.
Corso di formazione. Il Sistema Qualità dei Servizi Trasfusionali e delle Unità di Raccolta del sangue e degli emocomponenti
 Corso di formazione Il Sistema Qualità dei Servizi Trasfusionali e delle Unità di Raccolta del sangue e degli emocomponenti La progettazione e la gestione dei documenti per la qualità Roma, 13 settembre
Corso di formazione Il Sistema Qualità dei Servizi Trasfusionali e delle Unità di Raccolta del sangue e degli emocomponenti La progettazione e la gestione dei documenti per la qualità Roma, 13 settembre
REGOLAMENTO PER LE ISPEZIONI DI SORVEGLIANZA PERIODICA
 REGOLAMENTO PER LE ISPEZIONI DI SORVEGLIANZA PERIODICA (Art. 13 D.P.R. 162/99) INDICE 1. SCOPO E CAMPO DI APPLICAZIONE 2. RIFERIMENTI LEGISLATIVI 3. NORME TECNICHE 4. GENERALITÀ 5. PERSONALE IMPIEGATO
REGOLAMENTO PER LE ISPEZIONI DI SORVEGLIANZA PERIODICA (Art. 13 D.P.R. 162/99) INDICE 1. SCOPO E CAMPO DI APPLICAZIONE 2. RIFERIMENTI LEGISLATIVI 3. NORME TECNICHE 4. GENERALITÀ 5. PERSONALE IMPIEGATO
SCHEDA REQUISITI PER LA QUALIFICAZIONE DEL CORSO PER ESPERTI IN MARKETING & COMUNICAZIONE
 Viale di Val Fiorita, 90-00144 Roma Tel. 065915373 - Fax: 065915374 E-mail: corsi@cepas.it Sito internet: www.cepas.it Pag. 1 di 5 SCHEDA REQUISITI PER LA QUALIFICAZIONE DEL 1 22.03.2002 Rev. Generale
Viale di Val Fiorita, 90-00144 Roma Tel. 065915373 - Fax: 065915374 E-mail: corsi@cepas.it Sito internet: www.cepas.it Pag. 1 di 5 SCHEDA REQUISITI PER LA QUALIFICAZIONE DEL 1 22.03.2002 Rev. Generale
PROTOCOLLO PER LA RICHIESTA TRASFUSIONALE URGENTISSIMA
 INDICE Pag. 1 di 5 1. SCOPO E CAMPO DI APPLICAZIONE... 2 2. PAROLE CHIAVE... 2 3. PERSONALE INTERESSATO... 2 4. MODALITA OPERATIVA... 2 4.1 PREMESSA... 2 4.2 ATTIVAZIONE DELLA PROCEDURA... 3 4.2.1 Richiesta
INDICE Pag. 1 di 5 1. SCOPO E CAMPO DI APPLICAZIONE... 2 2. PAROLE CHIAVE... 2 3. PERSONALE INTERESSATO... 2 4. MODALITA OPERATIVA... 2 4.1 PREMESSA... 2 4.2 ATTIVAZIONE DELLA PROCEDURA... 3 4.2.1 Richiesta
LA CERTIFICAZIONE. Dr.ssa Eletta Cavedoni Responsabile Qualità Cosmolab srl Tortona
 LA CERTIFICAZIONE Dr.ssa Eletta Cavedoni Responsabile Qualità Cosmolab srl Tortona Qualità Grado in cui un insieme di caratteristiche intrinseche soddisfa i requisiti (UNI EN ISO 9000/00) Requisito Esigenza
LA CERTIFICAZIONE Dr.ssa Eletta Cavedoni Responsabile Qualità Cosmolab srl Tortona Qualità Grado in cui un insieme di caratteristiche intrinseche soddisfa i requisiti (UNI EN ISO 9000/00) Requisito Esigenza
DECRETO DIREZIONE GENERALE SANITA' N. 11685 DEL 20/10/2006 Identificativo Atto n. 992
 DECRETO DIREZIONE GENERALE SANITA' N. 11685 DEL 20/10/2006 Identificativo Atto n. 992 Oggetto: APPROVAZIONE DI UNO SCHEMA-TIPO DI CONVENZIONE PER IL SERVIZIO DI MEDICINA TRASFUSIONALE TRA LA STRUTTURA
DECRETO DIREZIONE GENERALE SANITA' N. 11685 DEL 20/10/2006 Identificativo Atto n. 992 Oggetto: APPROVAZIONE DI UNO SCHEMA-TIPO DI CONVENZIONE PER IL SERVIZIO DI MEDICINA TRASFUSIONALE TRA LA STRUTTURA
SCHEMA 0 STORIA. Schema certificativo CP004 0.1 DOCUMENTI ESTERNI DI RIFERIMENTO
 SCHEMA per la certificazione del controllo della produzione in fabbrica ai fini della marcatura CE dei profilati cavi di acciai non legati e a grano fine per impieghi strutturali di cui alle norme UNI
SCHEMA per la certificazione del controllo della produzione in fabbrica ai fini della marcatura CE dei profilati cavi di acciai non legati e a grano fine per impieghi strutturali di cui alle norme UNI
3. APPLICABILITÀ La presente procedura si applica nell organizzazione dell attività di Alac SpA.
 Acquedotto Langhe e Alpi Cuneesi SpA Sede legale in Cuneo, Corso Nizza 9 acquedotto.langhe@acquambiente.it www.acquambiente.it SGSL Audit P11 Rev 00 del 16/09/09 1. DISTRIBUZIONE Direzione RSPP 2. SCOPO
Acquedotto Langhe e Alpi Cuneesi SpA Sede legale in Cuneo, Corso Nizza 9 acquedotto.langhe@acquambiente.it www.acquambiente.it SGSL Audit P11 Rev 00 del 16/09/09 1. DISTRIBUZIONE Direzione RSPP 2. SCOPO
Manuale del Sistema di Gestione Integrato per la Qualità e l Ambiente INDICE
 Pag. 1 di 5 RESPONSABILITÀ DELLA DIREZIONE INDICE 1. Scopo... 2 2. Principi guida... 2 3. Politica per la qualità e l Ambiente... 2 4. Pianificazione... 2 5. Responsabilità, autorità e comunicazione...
Pag. 1 di 5 RESPONSABILITÀ DELLA DIREZIONE INDICE 1. Scopo... 2 2. Principi guida... 2 3. Politica per la qualità e l Ambiente... 2 4. Pianificazione... 2 5. Responsabilità, autorità e comunicazione...
Parte I (punti 3-9): Misure sanitarie obbligatorie per il controllo della Paratubercolosi bovina
 LINEE GUIDA PER L ADOZIONE DI PIANI DI CONTROLLO E PER L ASSEGNAZIONE DELLA QUALIFICA SANITARIA DEGLI ALLEVAMENTI NEI CONFRONTI DELLA PARATUBERCOLOSI BOVINA 1. Definizioni Ai sensi delle presenti linee
LINEE GUIDA PER L ADOZIONE DI PIANI DI CONTROLLO E PER L ASSEGNAZIONE DELLA QUALIFICA SANITARIA DEGLI ALLEVAMENTI NEI CONFRONTI DELLA PARATUBERCOLOSI BOVINA 1. Definizioni Ai sensi delle presenti linee
Dott. Fenoil. Dott. Iannaccone. Dott.ssa Amore. Approvato dal Direttore Sanitario Aziendale dott.ssa Chianale
 DI URINA E PER LA RICERCA DEI METABOLITI LAVORATORI ADDETTI A MANSIONI CHE COMPORTANO PARTICOLARI RISCHI PER LA SICUREZZA PER ACCERTAMENTO DELLO STATO DI TOSSICODIPENDENZA AI SENSI DELLA DGR 13-10928 del
DI URINA E PER LA RICERCA DEI METABOLITI LAVORATORI ADDETTI A MANSIONI CHE COMPORTANO PARTICOLARI RISCHI PER LA SICUREZZA PER ACCERTAMENTO DELLO STATO DI TOSSICODIPENDENZA AI SENSI DELLA DGR 13-10928 del
CORSO FORMATIVO RIVOLTO AI GIOVANI DIRIGENTI AVISINI
 CORSO FORMATIVO RIVOLTO AI GIOVANI DIRIGENTI AVISINI CONOSCERE IL SISTEMA SANGUE PER CRESCERE NELLA NUOVA REALTA AVISINA TITOLO INTERVENTO «Cenni sulla normativa europea ed italiana in ambito trasfusionale:
CORSO FORMATIVO RIVOLTO AI GIOVANI DIRIGENTI AVISINI CONOSCERE IL SISTEMA SANGUE PER CRESCERE NELLA NUOVA REALTA AVISINA TITOLO INTERVENTO «Cenni sulla normativa europea ed italiana in ambito trasfusionale:
ASSEMBLEA NAZIONALE 2010 MONTESILVANO
 ASSEMBLEA NAZIONALE 2010 MONTESILVANO Legge 21 ottobre 2005, n. 219 a) il raggiungimento dell'autosufficienza regionale e nazionale di sangue, emocomponenti e farmaci emoderivati; b) una più efficace tutela
ASSEMBLEA NAZIONALE 2010 MONTESILVANO Legge 21 ottobre 2005, n. 219 a) il raggiungimento dell'autosufficienza regionale e nazionale di sangue, emocomponenti e farmaci emoderivati; b) una più efficace tutela
UNI EN ISO 9001:2008 Sistemi di Gestione per la Qualità: requisiti e guida per l uso
 SORVEGLIANZA E CERTIFICAZIONI UNI EN ISO 9001:2008 Sistemi di Gestione per la Qualità: requisiti e guida per l uso Pagina 1 di 10 INTRODUZIONE La Norma UNI EN ISO 9001:2008 fa parte delle norme Internazionali
SORVEGLIANZA E CERTIFICAZIONI UNI EN ISO 9001:2008 Sistemi di Gestione per la Qualità: requisiti e guida per l uso Pagina 1 di 10 INTRODUZIONE La Norma UNI EN ISO 9001:2008 fa parte delle norme Internazionali
INTRODUZIONE AL MANUALE DELLA QUALITA
 INTRODUZIONE AL MANUALE DELLA QUALITA Elaborazione Verifica Approvazione Il Responsabile Qualità Il Rappresentante della Direzione Il Dirigente Scolastico (.. ) (. ) ( ) Data Data Data Rev Causale (emis./revis.)
INTRODUZIONE AL MANUALE DELLA QUALITA Elaborazione Verifica Approvazione Il Responsabile Qualità Il Rappresentante della Direzione Il Dirigente Scolastico (.. ) (. ) ( ) Data Data Data Rev Causale (emis./revis.)
A.O. MELLINO MELLINI CHIARI (BS) GESTIONE DELLE RISORSE 1. MESSA A DISPOSIZIONE DELLE RISORSE...2 2. RISORSE UMANE...2 3. INFRASTRUTTURE...
 Pagina 1 di 6 INDICE 1. MESSA A DISPOSIZIONE DELLE RISORSE...2 2. RISORSE UMANE...2 2.1. GENERALITÀ... 2 2.2. COMPETENZA, CONSAPEVOLEZZA E ADDESTRAMENTO... 2 3. INFRASTRUTTURE...3 4. AMBIENTE DI LAVORO...6
Pagina 1 di 6 INDICE 1. MESSA A DISPOSIZIONE DELLE RISORSE...2 2. RISORSE UMANE...2 2.1. GENERALITÀ... 2 2.2. COMPETENZA, CONSAPEVOLEZZA E ADDESTRAMENTO... 2 3. INFRASTRUTTURE...3 4. AMBIENTE DI LAVORO...6
CHECK LIST - STUDI DI ANDROLOGIA Certificazione di II livello Diagnosi e terapia disfunzioni sessuali maschili
 1-RISORSE UMANE 1.1-Medico 1.1.1 Il medico che opera all interno dello studio verificato è uno specialista Andrologo / Urologo / Endocrinologo o risulta essere in possesso di un diploma di master di 2
1-RISORSE UMANE 1.1-Medico 1.1.1 Il medico che opera all interno dello studio verificato è uno specialista Andrologo / Urologo / Endocrinologo o risulta essere in possesso di un diploma di master di 2
MANUALE DELLA QUALITÀ SEZIONE 5.1: FUNZIONAMENTO DEL SISTEMA DI GESTIONE PER LA QUALITÀ
 REV. 00 pagina 1/4 MANUALE DELLA QUALITÀ Rif.to: UNI EN ISO 9001:2008 PARTE 5: RESPONSABILITÀ DELLA DIREZIONE SEZIONE 5.1: FUNZIONAMENTO DEL SISTEMA DI GESTIONE PER LA QUALITÀ SOMMARIO A Impegno della
REV. 00 pagina 1/4 MANUALE DELLA QUALITÀ Rif.to: UNI EN ISO 9001:2008 PARTE 5: RESPONSABILITÀ DELLA DIREZIONE SEZIONE 5.1: FUNZIONAMENTO DEL SISTEMA DI GESTIONE PER LA QUALITÀ SOMMARIO A Impegno della
SVILUPPO, CERTIFICAZIONE E MIGLIORAMENTO DEL SISTEMA DI GESTIONE PER LA SICUREZZA SECONDO LA NORMA BS OHSAS 18001:2007
 Progettazione ed erogazione di servizi di consulenza e formazione M&IT Consulting s.r.l. Via Longhi 14/a 40128 Bologna tel. 051 6313773 - fax. 051 4154298 www.mitconsulting.it info@mitconsulting.it SVILUPPO,
Progettazione ed erogazione di servizi di consulenza e formazione M&IT Consulting s.r.l. Via Longhi 14/a 40128 Bologna tel. 051 6313773 - fax. 051 4154298 www.mitconsulting.it info@mitconsulting.it SVILUPPO,
SIMT-POS 043 GESTIONE DELLE NON CONFORMITA ED AZIONI CORRETTIVE
 1 Prima Stesura Data:15-02-2014 Redattori: Gasbarri - Rizzo SIMT-POS 043 GESTIONE DELLE NON CONFORMITA ED AZIONI CORRETTIVE Indice 1 SCOPO... 2 2 CAMPO D APPLICAZIONE... 2 3 DOCUMENTI DI RIFERIMENTO...
1 Prima Stesura Data:15-02-2014 Redattori: Gasbarri - Rizzo SIMT-POS 043 GESTIONE DELLE NON CONFORMITA ED AZIONI CORRETTIVE Indice 1 SCOPO... 2 2 CAMPO D APPLICAZIONE... 2 3 DOCUMENTI DI RIFERIMENTO...
Domanda di Certificazione CE Insiemi/Attrezzature Direttiva PED
 Sezione 1: Dati del Richiedente Spett.le: ECO Certificazioni S.p.A. European Certifying Organization Via Mengolina, 33 Int. 5 48018 Faenza (RA) ITALY Organismo notificato n. 0714 Tel 0546-624911; Fax 0546-624922
Sezione 1: Dati del Richiedente Spett.le: ECO Certificazioni S.p.A. European Certifying Organization Via Mengolina, 33 Int. 5 48018 Faenza (RA) ITALY Organismo notificato n. 0714 Tel 0546-624911; Fax 0546-624922
REGOLAMENTO SUL TRATTAMENTO DEI DATI PERSONALI
 COMUNE DI VIANO PROVINCIA DI REGGIO EMILIA REGOLAMENTO SUL TRATTAMENTO DEI DATI PERSONALI Approvato con deliberazione di G.C. n. 73 del 28.11.2000 INDICE TITOLO 1 ART. 1 ART. 2 ART. 3 ART. 4 ART. 5 ART.
COMUNE DI VIANO PROVINCIA DI REGGIO EMILIA REGOLAMENTO SUL TRATTAMENTO DEI DATI PERSONALI Approvato con deliberazione di G.C. n. 73 del 28.11.2000 INDICE TITOLO 1 ART. 1 ART. 2 ART. 3 ART. 4 ART. 5 ART.
MANUALE DI CONSERVAZIONE
 AZIENDA DI SERVIZI ALLA PERSONA DI SPILIMBERGO Azienda pubblica di servizi alla persona ex L.r. 19/2003 Viale Barbacane, 19-33097 Spilimbergo PN Tel. 0427 2134 Fax 0427 41268 ----------------------------------------------------------------------------------------------------------------------------------
AZIENDA DI SERVIZI ALLA PERSONA DI SPILIMBERGO Azienda pubblica di servizi alla persona ex L.r. 19/2003 Viale Barbacane, 19-33097 Spilimbergo PN Tel. 0427 2134 Fax 0427 41268 ----------------------------------------------------------------------------------------------------------------------------------
DECRETI, DELIBERE E ORDINANZE MINISTERIALI
 d) relazioni bilaterali con la Turchia, i Paesi del Caucaso, le Repubbliche centrasiatiche e la Russia; e) temi trattati nell ambito delle Nazioni Unite e delle Agenzie Specializzate; f) temi relativi
d) relazioni bilaterali con la Turchia, i Paesi del Caucaso, le Repubbliche centrasiatiche e la Russia; e) temi trattati nell ambito delle Nazioni Unite e delle Agenzie Specializzate; f) temi relativi
IL CENTRO NAZIONALE SANGUE
 IL CENTRO NAZIONALE SANGUE Vista la legge 21 ottobre 2005, n. 219, recante: Nuova disciplina delle attività trasfusionali e della produzione nazionale degli emoderivati ed in particolare l articolo 15
IL CENTRO NAZIONALE SANGUE Vista la legge 21 ottobre 2005, n. 219, recante: Nuova disciplina delle attività trasfusionali e della produzione nazionale degli emoderivati ed in particolare l articolo 15
Centro Tecnico per la Rete Unitaria della Pubblica Amministrazione
 Centro Tecnico per la Rete Unitaria della Pubblica Amministrazione Area Rete Unitaria - Sezione Interoperabilità Linee guida del servizio di trasmissione di documenti informatici mediante posta elettronica
Centro Tecnico per la Rete Unitaria della Pubblica Amministrazione Area Rete Unitaria - Sezione Interoperabilità Linee guida del servizio di trasmissione di documenti informatici mediante posta elettronica
ISO 15189 2007: Laboratori Medici particolari requisiti per la qualità e la competenza
 ISO 15189 2007: Laboratori Medici particolari requisiti per la qualità e la competenza Dr.ssa Eletta Cavedoni Cosmolab srl Tortona Corso di Controllo e Gestione Qualità Università degli Studi di Pavia
ISO 15189 2007: Laboratori Medici particolari requisiti per la qualità e la competenza Dr.ssa Eletta Cavedoni Cosmolab srl Tortona Corso di Controllo e Gestione Qualità Università degli Studi di Pavia
Autorizzazione e Accreditamento dei Servizi Trasfusionali e delle Unità di Raccolta: il percorso normativo
 Autorizzazione e Accreditamento dei Servizi Trasfusionali e delle Unità di Raccolta: il percorso normativo Bologna, 22 dicembre 2012 Relatrice: Ivana Menichini D.Lgs. 502/1992 Riordino della disciplina
Autorizzazione e Accreditamento dei Servizi Trasfusionali e delle Unità di Raccolta: il percorso normativo Bologna, 22 dicembre 2012 Relatrice: Ivana Menichini D.Lgs. 502/1992 Riordino della disciplina
Manuale Sicurezza Duemilauno Agenzia Sociale
 Sorveglianza e misurazioni del SG S&SL Indice: 1.0 Scopo e Generalità 2.0 Identificazione delle aree/attività soggette al monitoraggio 3.0 Pianificazione ed esecuzione dei monitoraggi e delle misurazioni
Sorveglianza e misurazioni del SG S&SL Indice: 1.0 Scopo e Generalità 2.0 Identificazione delle aree/attività soggette al monitoraggio 3.0 Pianificazione ed esecuzione dei monitoraggi e delle misurazioni
Gestione dei Documenti di registrazione della Qualità
 In vigore dal 27.9.4 Pagina 1 di 1 ANNULLA E SOSTITUISCE: Rev. 1 REDAZIONE Firma Data 13.9.4 VERIFICA Firma Data 13.9.4 APPROVAZIONE D.I. Firma Data 2.9.4 Rev. Data Descrizione revisione Redatta Verificata
In vigore dal 27.9.4 Pagina 1 di 1 ANNULLA E SOSTITUISCE: Rev. 1 REDAZIONE Firma Data 13.9.4 VERIFICA Firma Data 13.9.4 APPROVAZIONE D.I. Firma Data 2.9.4 Rev. Data Descrizione revisione Redatta Verificata
Le Raccomandazioni ministeriali per la prevenzione dei rischi in chirurgia: linee di indirizzo regionali di implementazione a livello aziendale
 Le Raccomandazioni ministeriali per la prevenzione dei rischi in chirurgia: linee di indirizzo regionali di implementazione a livello aziendale PREMESSA Il Ministero del Lavoro, della Salute e delle Politiche
Le Raccomandazioni ministeriali per la prevenzione dei rischi in chirurgia: linee di indirizzo regionali di implementazione a livello aziendale PREMESSA Il Ministero del Lavoro, della Salute e delle Politiche
COPIA TRATTA DAL SITO WEB ASLBAT.IT
 DIREZIONE SANITARIA AZIENDALE Procedura Operativa APPROVVIGIONAMENTO E GESTIONE MAGAZZINO REVISIONE DATA REDATTO VERIFICATO APPROVATO 00 OTTOBRE 2015 INDICE Farmacista Specializzando Dott. Cataldo Procacci
DIREZIONE SANITARIA AZIENDALE Procedura Operativa APPROVVIGIONAMENTO E GESTIONE MAGAZZINO REVISIONE DATA REDATTO VERIFICATO APPROVATO 00 OTTOBRE 2015 INDICE Farmacista Specializzando Dott. Cataldo Procacci
Firenze 26 Settembre 2014. Antonella Leto Presidente Associazione Nazionale Infermieri Neuroscienze (ANIN)
 Firenze 26 Settembre 2014 Antonella Leto Presidente Associazione Nazionale Infermieri Neuroscienze (ANIN) Regolamento (UE) n. 536/2014 del Parlamento europeo e del Consiglio, del 16 aprile 2014, sulla
Firenze 26 Settembre 2014 Antonella Leto Presidente Associazione Nazionale Infermieri Neuroscienze (ANIN) Regolamento (UE) n. 536/2014 del Parlamento europeo e del Consiglio, del 16 aprile 2014, sulla
Il glossario della Posta Elettronica Certificata (PEC) Diamo una definizione ai termini tecnici relativi al mondo della PEC.
 Il glossario della Posta Elettronica Certificata (PEC) Diamo una definizione ai termini tecnici relativi al mondo della PEC. Avviso di mancata consegna L avviso, emesso dal sistema, per indicare l anomalia
Il glossario della Posta Elettronica Certificata (PEC) Diamo una definizione ai termini tecnici relativi al mondo della PEC. Avviso di mancata consegna L avviso, emesso dal sistema, per indicare l anomalia
Luogo di nascita: Comune Provincia Stato
 Allo Sportello Unico per le Attività Produttive (SUAP) del Comune di OSTRA NOTIFICA INIZIO ATTIVITÀ SETTORE ALIMENTARE AI FINI DELLA REGISTRAZIONE (ART. 6 DEL REGOLAMENTO CE N. 852/2004 E DELLA D.G.R.
Allo Sportello Unico per le Attività Produttive (SUAP) del Comune di OSTRA NOTIFICA INIZIO ATTIVITÀ SETTORE ALIMENTARE AI FINI DELLA REGISTRAZIONE (ART. 6 DEL REGOLAMENTO CE N. 852/2004 E DELLA D.G.R.
IL SISTEMA DI GESTIONE AMBIENTALE PER UN COMUNE
 IL SISTEMA DI GESTIONE AMBIENTALE PER UN COMUNE Relatore: LIFE 04 ENV/IT/494 AGEMAS Obiettivi del sistema di gestione ambientale Prevenzione, riduzione dell inquinamento Eco-efficienza nella gestione delle
IL SISTEMA DI GESTIONE AMBIENTALE PER UN COMUNE Relatore: LIFE 04 ENV/IT/494 AGEMAS Obiettivi del sistema di gestione ambientale Prevenzione, riduzione dell inquinamento Eco-efficienza nella gestione delle
MONITORAGGIO E MISURAZIONE DEL PRODOTTO
 25/02/2011 Pag. 1 di 6 MONITORAGGIO E MISURAZIONE DEL PRODOTTO 1. SCOPO... 2 2. APPLICABILITÀ... 2 3. DOCUMENTI DI RIFERIMENTO... 2 3.1. Norme... 2 3.2. Moduli... 2 4. RESPONSABILITÀ... 2 5. DEFINIZIONI...
25/02/2011 Pag. 1 di 6 MONITORAGGIO E MISURAZIONE DEL PRODOTTO 1. SCOPO... 2 2. APPLICABILITÀ... 2 3. DOCUMENTI DI RIFERIMENTO... 2 3.1. Norme... 2 3.2. Moduli... 2 4. RESPONSABILITÀ... 2 5. DEFINIZIONI...
TENUTA SOTTO CONTROLLO DEI DOCUMENTI
 Pagina 1 di 5 INDICE 1. SCOPO 2. CAMPO DI APPLICAZIONE 3. RESPONSABILITA 4. DESCRIZIONE DELLE ATTIVITÀ 5. INDICATORI DI PROCESSO 6. RIFERIMENTI 7. ARCHIVIAZIONI 8. TERMINOLOGIA ED ABBREVIAZIONI 9. DOCUMENTI
Pagina 1 di 5 INDICE 1. SCOPO 2. CAMPO DI APPLICAZIONE 3. RESPONSABILITA 4. DESCRIZIONE DELLE ATTIVITÀ 5. INDICATORI DI PROCESSO 6. RIFERIMENTI 7. ARCHIVIAZIONI 8. TERMINOLOGIA ED ABBREVIAZIONI 9. DOCUMENTI
MANUALE DELLA QUALITÀ SEZIONE 5.1: FUNZIONAMENTO DEL SISTEMA DI GESTIONE PER LA QUALITÀ
 MANUALE GESTIONE QUALITÀ SEZ. 5.1 REV. 02 pagina 1/5 MANUALE DELLA QUALITÀ Rif.to: UNI EN ISO 9001:2008 PARTE 5: RESPONSABILITÀ DELLA DIREZIONE SEZIONE 5.1: FUNZIONAMENTO DEL SISTEMA DI GESTIONE PER LA
MANUALE GESTIONE QUALITÀ SEZ. 5.1 REV. 02 pagina 1/5 MANUALE DELLA QUALITÀ Rif.to: UNI EN ISO 9001:2008 PARTE 5: RESPONSABILITÀ DELLA DIREZIONE SEZIONE 5.1: FUNZIONAMENTO DEL SISTEMA DI GESTIONE PER LA
Direttore Dr.ssa Tiziana Riscaldati. SIMT-POS 028 Controlli Qualità
 1 1 2 1 SCOPO Scopo della presente Procedura è fornire indicazioni circa le modalità di esecuzione e gestione del Controllo di Qualità (C.Q.) interno ed esterno nell area di Validazione Biologica. 2 CAMPO
1 1 2 1 SCOPO Scopo della presente Procedura è fornire indicazioni circa le modalità di esecuzione e gestione del Controllo di Qualità (C.Q.) interno ed esterno nell area di Validazione Biologica. 2 CAMPO
Marchio dei prodotti agroalimentari del Parco di Montevecchia e della Valle del Curone
 pag. 1 Marchio dei prodotti agroalimentari del Parco di Montevecchia e della Valle del Curone DISCIPLINARE DI PRODUZIONE PRODUZIONI ORTICOLE DA PRODUZIONE BIOLOGICA Premessa Il Parco Regionale di Montevecchia
pag. 1 Marchio dei prodotti agroalimentari del Parco di Montevecchia e della Valle del Curone DISCIPLINARE DI PRODUZIONE PRODUZIONI ORTICOLE DA PRODUZIONE BIOLOGICA Premessa Il Parco Regionale di Montevecchia
I SISTEMI DI GESTIONE DELLA SICUREZZA
 I SISTEMI DI GESTIONE DELLA SICUREZZA ing. Davide Musiani Modena- Mercoledì 8 Ottobre 2008 L art. 30 del D.Lgs 81/08 suggerisce due modelli organizzativi e di controllo considerati idonei ad avere efficacia
I SISTEMI DI GESTIONE DELLA SICUREZZA ing. Davide Musiani Modena- Mercoledì 8 Ottobre 2008 L art. 30 del D.Lgs 81/08 suggerisce due modelli organizzativi e di controllo considerati idonei ad avere efficacia
PROCEDURE PER GARANTIRE LA SICUREZZA DELLA TRASFUSIONE
 A LLEGATO VII PROCEDURE PER GARANTIRE LA SICUREZZA DELLA TRASFUSIONE A. Prelievi ematici per indagini immunoematologiche e pre-trasfusionali 1 I campioni di sangue destinati alla tipizzazione eritrocitaria,
A LLEGATO VII PROCEDURE PER GARANTIRE LA SICUREZZA DELLA TRASFUSIONE A. Prelievi ematici per indagini immunoematologiche e pre-trasfusionali 1 I campioni di sangue destinati alla tipizzazione eritrocitaria,
DOCUMENTO DI VALUTAZIONE DEI RISCHI (RISK ASSESSMENT)
 CT DOI 23 CENTRO Revisione 0 Pag. 1 a 7 Indice 1 DESCRIZIONE ATTIVITÀ Pag. 1.1 ANALISI DEI RISCHI 1.2 ASSEGNAZIONE IPR 2 ELENCO DEI PROCESSI E IPR OTTENUTI 2.1 Processo di selezione e donazione 2.2 Processo
CT DOI 23 CENTRO Revisione 0 Pag. 1 a 7 Indice 1 DESCRIZIONE ATTIVITÀ Pag. 1.1 ANALISI DEI RISCHI 1.2 ASSEGNAZIONE IPR 2 ELENCO DEI PROCESSI E IPR OTTENUTI 2.1 Processo di selezione e donazione 2.2 Processo
GLI AUDIT GCP. Valentine Sforza Quality Management Associates. XI CONGRESSO NAZIONALE SSFA Roma, 6-7 marzo 2008 ARGOMENTI TRATTATI
 GLI AUDIT GCP Valentine Sforza Quality Management Associates 1 ARGOMENTI TRATTATI Chi lo fa Tipologie di Audit Svolgimento di un Audit Esempio di un Audit Rapporto di un Audit Valore di un Audit 2 1 CHI
GLI AUDIT GCP Valentine Sforza Quality Management Associates 1 ARGOMENTI TRATTATI Chi lo fa Tipologie di Audit Svolgimento di un Audit Esempio di un Audit Rapporto di un Audit Valore di un Audit 2 1 CHI
1. DISTRIBUZIONE Direzione, RSPP, RLS, preposti 2. SCOPO
 Acquedotto Langhe e Alpi Cuneesi SpA Sede legale in Cuneo, Corso Nizza 9 acquedotto.langhe@acquambiente.it www.acquambiente.it SGSL Procedura Monitoraggio salute e del 16/09/09 1. DISTRIBUZIONE, RSPP,
Acquedotto Langhe e Alpi Cuneesi SpA Sede legale in Cuneo, Corso Nizza 9 acquedotto.langhe@acquambiente.it www.acquambiente.it SGSL Procedura Monitoraggio salute e del 16/09/09 1. DISTRIBUZIONE, RSPP,
CERTIFICAZIONE DELLE AZIENDE AI SENSI DEI REGOLAMENTI EUROPEI 303/2008 E 304/2008 I & F BUREAU VERITAS ITALIA
 Emesso da Ufficio: CERTIFICAZIONE DELLE AZIENDE AI SENSI INDICE 1. SCOPO E CAMPO DI APPLICAZIONE... 2 2. RIFERIMENTI... 2 3. GENERALITÀ... 4 4. PROCEDURA DI CERTIFICAZIONE... 5 5. CONTENUTI DEL CERTIFICATO...
Emesso da Ufficio: CERTIFICAZIONE DELLE AZIENDE AI SENSI INDICE 1. SCOPO E CAMPO DI APPLICAZIONE... 2 2. RIFERIMENTI... 2 3. GENERALITÀ... 4 4. PROCEDURA DI CERTIFICAZIONE... 5 5. CONTENUTI DEL CERTIFICATO...
