Appunti dalle lezioni di Biochimica metabolica e della nutrizione PARTE II
|
|
|
- Casimiro Sasso
- 8 anni fa
- Visualizzazioni
Transcript
1 Università degli Studi di Enna Kore Facoltà di Scienze dell Uomo e della Società Corso di Laurea magistrale in Scienze e tecniche dell attività motoria e sportiva per la tutela della salute Insegnamento: Biochimica metabolica e della nutrizione, AA Appunti dalle lezioni di Biochimica metabolica e della nutrizione PARTE II
2 METABOLISMO METABOLISMO: insieme di reazioni (trasformazioni chimiche e fisiche) che avvengono nella cellula e ne permettono l esistenza. ANABOLISMO: insieme dei processi di sintesi di biomolecole a partire da precursori semplici. Tali processi richiedono energia (processi endoergonici). CATABOLISMO: insieme dei processi di trasformazione e degradazione di solito ossidativi a carico dei substrati energetici. Da composti complessi (substrati energetici) si attengono molecole semplici e poco reattive quali CO2, H2O, NH2 con produzione di energia chimica (processi esoergonici) sotto forma di adenosina 5 -trifosfato (ATP). I processi anabolici e catabolici sono strettamente correlati e regolati vicendevolmente: l'energia prodotta nei processi catabolici (esoergonici) viene utilizzata per rendere possibili i processi anabolici (endoergonici). ATP è un composto ad alta energia che viene utilizzata dalle cellule come riserva di energia. Infatti la trasformazione di alcuni suoi gruppi funzionali (idrolisi del gruppo fosfo-anidridico) è fortemente esoergonica (produce energia). E costituita da una base azotata adenina, uno zucchero semplice, il ribosio e 3 gruppi fosfato (Pi). Il ribosio è fosforilato in posizione 5 mediante la formazione di un legame fosfoestereo. Tale gruppo fosfato (alfa) è a sua volta legato ad altri due gruppi fosfato (beta e gamma) tramite un legame fosfo-anidridico. Rispetto al gruppo fosfoestereo, i due legami fosfoanidridici di ATP possono essere idrolizzati generando energia (processo esoergonico). Pi=ortofosfato (PO 3 2- ) PPi=pirofosfato (P 2 O 7 4- ) Biochimica-Lezione ATP può essere sintetizzata per Fosforilazione a livello del substrato: trasferimento di un gruppo fosfato da una molecola ad alta energia all'adenosina 5'-difosfato (ADP); Fosforilazione ossidativa: durante l ossidazione di composti ridotti (coenzimi ridotti) prodotti dal catabolismo ossidativo dei substrati energetici viene generato un potenziale elettrochimico di membrana mitocondriale interna (forza proton-motrice). La separazione di carica genera una differenza di potenziale proporzionale alla separazione di carica stessa. La differenza di potenziale elettrochimico è una forma di energia utilizzabile nella sintesi di ATP. Altre molecole ad alto contenuto energetico sono l acetil-coa, in cui è presente un legame tioestereo energeticamente confrontabile con un legame fosfo-anidridico o la fosfo-creatina che può fosforilare ADP con produzione di ATP in un processo catalizzato dalla creatina chinasi. La fosfocreatina può essere considerata una sorta di tampone per ATP intracellulare, ovvero si oppone alle diminuzioni di ATP generandola da ADP. Le molecole ad alta energia possono essere utilizzate nel cosiddetto accoppiamento di reazioni: la cellula utilizza l energia ottenuta dalla trasformazione di una molecola ad alta energia ( G 20 kj mol -1 ) per rendere termodinamicamente favorita una reazione endoergonica. TRASPORTO La membrana ha lo scopo di compartimentalizzare la cellula e regola l ingresso e l uscita di nutrienti e prodotti catabolici di scarto. La membrana permette di stabilire un gradiente di concentrazione, separando soluzioni a differente concentrazione ed un gradiente elettrico, generato da concentrazioni intra ed extracellulari di cariche diverse. Gradiente chimico e gradiente elettrico generano il cosiddetto potenziale elettrochimico di membrana.
3 TRASPORTO PASSIVO: non richiede consumo di energia e avviene quando il gradiente di concentrazione è favorevole. Il trasporto Passivo può avvenire per: diffusione semplice; trasporto attraverso canali (proteine) di membrana diffusione facilitata. Le molecole che possono diffondere passivamente sfruttando il gradiente di concentrazione sono piccole molecole apolari come benzene, O2 (ossigeno),co2 (anidride carbonica) e N2 (azoto) o molecole polari neutre come urea, glicerolo. Molecole polari a peso molecolare elevato non possono diffondere nella membrana e richiedono sempre trasportatori proteici nel processo di diffusione. Un esempio di diffusione passiva facilitata è quello associato ai trasportatori del glucosio (glucose transporters, GluT) che mediano il trasporto del glucosio sulla base del gradiente di concentrazione tra spazio extracellulare e citoplasma. TRASPORTO ATTIVO: associato prevalentemente al trasporto di specie cariche o contro gradiente di concentrazione; l ingresso di una specie molecolare o atomica ionica si ripercuote sul potenziale elettrochimico di membrana che rimane inalterato nelle cellule non eccitabili o deve essere ripristinato nelle cellule eccitabili. Un esempio di tale tipo di trasporto è quello condotto dalle pompe sodio-potassio ATP dipendenti che permettono di mantenere concentrazioni intracellulari di potassio ed extracellulari di sodio contro gradiente di concentrazione. In alcuni casi il trasporto attivo utilizzato anche per molecole neutre. Un esempio è il trasporto attivo del glucosio a livello enterocitario contro gradiente di concentrazione. Trasporto attivo del glucosio: cotrasporto Glucosio-Na + a livello intestinale. Il trasporto intestinale del glucosio si basa sul cotrasporto di glucosio e sodio. Nel lume intestinale la concentrazione di Na + è elevata e maggiore rispetto alla concentrazione intracellulare enterocitaria. Per questo motivo, Na + tende a diffondere negli enterociti. Il trasporto avviene attraverso una trasportatore proteico che media il cotrasporto di glucosio. Il legame tra Na + e trasportatore determina un cambiamento della struttura della proteina inducendone una maggiore affinità per il glucosio, che viene quindi assorbito dalle pareti intestinali. L'aumento del sodio intracellulare determina una diminuzione del gradiente elettrochimico che viene ristabilito attraverso una pompa sodio potassio ATPasica localizzata a livello della parete basale. Tale pompa, associata all'idrolisi di un legame fosfoanidridico di ATP, media l'efflusso di sodio nel sangue e l'influsso di potassio dal sangue all enterocita con ripristino del potenziale elettrochimico di membrana enterocitario. Contemporaneamente, un trasportatore del glucosio di tipo 2 o 5 (GluT2/5), localizzato a livello basale, media il trasporto passivo facilitato del glucosio dall enterocita al flusso ematico.
4 DIGESTIONE E ASSORBIMENTO DEI CARBOIDRATI La digestione dei carboidrati inizia in bocca ad opera della amilasi salivare, che rompe la catena polisaccaridica idrolizzando i legami alfa1-4 glicosidici a ph neutro. Nello stomaco il ph diminuisce rendendo inattivo l'enzima e inibendo l idrolisi dei glucidici legami glicosidici. A livello intestinale viene prodotta l amilasi pancreatica, che permette la formazione di monosaccaridi e disaccaridi per scissione dei legami alfa1-4 glicosidici dei residui polisaccaridici prodotti mediante l'idrolisi catalizzata dall'amilasi salivare. I prodotti ottenuti sono glucosio, maltosio, saccarosio, lattosio. L idrolisi dei disaccaridi è mediata da disaccaridasi specifiche dimeri per specifici disaccaridi. Un esempio è quello della lattasi che idrolizza selettivamente il legame beta 1-4 del disaccaride lattosio con produzione di glucosio e galattosio. La maltasi agisce sul maltosio e scinde il legame alfa1-4 glicosidici per ottenere 2 molecole di glucosio. La saccarasi idrolizza il saccarosio scindendo il legami alfa1-2 glicosidico con produzione di fruttosio e glucosio. Nel lume intestinale, il glucosio è assorbito dai villi mediante il trasporto attivo descritto in precedenza e viene immesso nel flusso ematico. Nei tessuti il glucosio viene assorbito mediante diffusione passiva facilitata. L'assorbimento di glucosio è regolato dagli ormoni insulina e glucagone. Infatti insulina e glucagone attivano o inibiscono, rispettivamente, l espressione genica e la sintesi proteica del trasportatore GLUT4 nei tessuti insulino-dipendenti (muscolare, epatico, adiposo) modulando, quindi, la capacità delle cellule di assorbire glucosio in funzione del glucosio disponibile. Nelle cellule il glucosio può essere degradato aerobicamente o anaerobicamente. La degradazione ossidativa aerobica del glucosio viene definita respirazione cellulare mentre la degradazione anerobica del glucosio viene denominata fermentazione omolattica. PRIMA FASE DELLA RESPIRAZIONE CELLULARE La glicolisi consiste in un serie di reazioni che avvengono nel citoplasma attraverso la quale il glucosio è degradato ed ossidato ad acido piruvico. Nella glicolisi si possono individuare due fasi: una di attivazione, in cui si richiede il consumo di 2 molecole di ATP ed una in cui si producono 4 molecole di ATP. Nella fase di attivazione o investimento, il glucosio (esoso) viene scisso in due triosi (3 atomi di carbonio): una molecola di gliceraldeide 3-fosfato ed una molecola di di-idrossiacetone fosfato. Quest'ultimo può essere convertito in gliceraldeide 3-fosfato. La prima fase del processo determina quindi la formazione di due molecole di gliceraldeide-3-fosfato. Il processo richiede il consumo di 2 molecole di ATP. Le principali reazioni della fase d investimento: 1.GLUCOSIO + ATP GLUCOSIO-6Fosfato + ADP. L enzima che catalizza la reazione è una chinasi (esochinasi). In questa reazione la sintesi del legame fosfoestereo richiede il consumo di una molecola di ATP (accoppiamento di reazioni) e la reazione complessiva è irreversibile. La fosforilazione attiva il glucosio e lo trasforma in una molecola carica negativamente cellula che non può diffondere passivamente dal citoplasma allo spazio extracellulare. 2. FRUTTOSIO-6Fosfato + ATP FRUTTOSIO 1,6-DIFOSFATO + ADP L enzima che catalizza la reazione è una fosfofruttochinasi I. In questa reazione viene consumata la seconda molecola di ATP (accoppiamento di reazioni). Questo processo irreversibile attiva ulteriormente, ovvero rende maggiormente reattivo il fruttosio ottenuto per isomerizzazione del glucosio mediante la sintesi di un secondo legame fosfoestereo.
5 3. FRUTTOSIO 1,6,DIFOSFATO DI-IDROSSIACETONE FOSFATO + GLICERALDEIDE 3- FOSFATO Il diidrossiacetonefosfato viene isomerizzato da trioso fosfato isomerasi (TIM) a gliceraledeide 3- fosfato. La fase di investimento della glicolisi genera due triosi fosfato di precursori di due molecole di piruvato. Il piruvato viene ottenuto mediante una serie di reazioni a partire da gliceraldeide 3-fosfato di 2 molecole di ATP e riduzione di 1 molecola di nicotinammide adenina dinucleotide. Considerando il processo per le 2 molecole di gliceraldeide 3-fosfato prodotte da una molecola di glucosio: 2GLICERALDEIDE 3-FOSFATO + 4ADP + 2NAD + 2 PIRUVATO + 2NADH + 4ATP L ossidazione di GA3P è termodinamicamente favorita poiché E 1,3-DPG/GA3P <E NAD+/NADH. Le molecole di ATP sono ottenute per fosforilazione a livello del substrato dalla lisi del legame anidridico misto di 1,3-DPG (reazione reversibile) e dal legame fosfoestereo di PEP (ricordare l effetto della tautomeria chetoeneolica reazione irreversibile). Entrambe le reazioni rappresentano un esempio di accoppiamento di reazioni ( la trasformazione di un legame ad alta energia viene utilizzata per la sintesi endoergonica di ATP da ADP). Ricordare che esochinasi, fosfofruttochinasi I (PFK1) e piruvato chinasi (PK) catalizzano reazioni fortemente esoergoniche ed irreversibili tappe regolatorie della prima fase. I coenzimi ridotti prodotti nella reazione di ossidoriduzione costituiscono una fonte ulteriore di energia chimica nella terza fase della respirazione cellulare. Le molecole di nicotinammide adenina dinucleotide ridotto possono essere a) ossidate nuovamente a livello citoplasmatico dalla lattato deidrogenasi (LDH) durante la fermentazione omolattica, in modo da alimentare la prima fase della respirazione (ricordare che alcuni lieviti in condizioni di anaerobiosi ripristinano i livelli di NAD + attraverso la fermentazione alcolica e senza produzione di energia chimica; b) trasferite nel mitocondrio mediante sistemi navetta come il sistema navetta del glicerolo 3- fosfato o il sistema navetta malato-aspartato (un eccellente trattazione dei sistemi di trasporto è disponibile ai link: e e ossidate mediante processi redox termodinamicamente favoriti ( E >0 G <0) nella catena di trasporto degli elettroni (electron transport chain, ETC) con successiva conversione di energia elettrochimica in energia chimica durante la fosforilazione ossidativa (sintesi di ATP). BILANCIO ENERGETICO della prima fase della respirazione cellulare ATP NADH OTTENUTE 4 2 CONSUMATE 2 TOT 2 2 Il PIRUVATO prodotto nella prima fase della respirazione può seguire due vie: a) la via anaerobica fermentazione; b) la via aerobica seconda (ciclo di Krebs) e terza fase (catena di trasporto degli elettroni e fosforilazione ossidativa) della respirazione cellulare. FERMENTAZIONE OMOLATTICA
6 piruvato + NADH Acido Lattico + NAD + Lo scopo di tale processo è quello di produrre nuovamente coenzimi ossidati che possano essere utilizzati nella fase precedente (ossidazione di gliceraldeide 3-fosfato a 1,3-difosfoglicerato). Il bilancio energetico rimane invariato ed è di 2 molecole di ATP. Tale destino anaerobico del piruvato si realizza quando sia richiesta energia rapidamente ed in condizioni di carenza di ossigeno. L enzima che catalizza la reazione reversibile è la lattato deidrogenasi (LDH). Alcuni batteri svolgono un metabolismo anaerobico omolattico, altri batteri o lieviti invece fermentano il piruvato producendo l alcol etilco (fermentazione alcolica). SECONDA FASE DELLA RESPIRAZIONE CELLULARE CICLO DI KREBS Il PIRUVATO può superare la membrana mitocondriale interna attraverso un simporto piruvato/h+ e generare acetil-coa, molecola chiave dell'intero metabolismo. Il piruvato subisce una decarbossilazione ossidativa irreversibile con produzione di CO2 (massimo stato di ossidazione del carbonio). L ossidazione è associata alla riduzione del coenzima NAD + ed è catalizzata dall enzima piruvato deidrogenasi Nella matrice mitocondriale, l'acetil-coa condensa con l'ossalacetato generando citrato, dando via al ciclo di Krebs, seconda fase della respirazione cellulare. Le principali reazioni sono: Reazione 1: condensazione dell'acetil-coa con l'ossalacetato (4C) e produzione di citrato (6C). Reazioni 3-4 catalizzate rispettivamente da isocitrato deidrogenasi e alfa-chetoglutarato deidrogenasi: isocitrato (6C) + NAD + alfa-chetoglutarato (5C) + NADH + CO2; alfachetoglutarato (5C) + NAD + succinil-coa + NADH + CO2 Le reazioni 3 e 4 sono decarbossilazioni irreversibili (produzione di CO2) associate alla riduzione di NAD + a NADH. Tutti gli atomi del glucosio sono stati a questo punto ossidati ad anidride carbonica che viene trasformata rapidamente in bicarbonato dall'enzima anidrasi carbonica ed immessa in tal forma nel flusso ematico (ricordare l effetto Bohr e la regolazione dell affinità di Hb per O2). Reazione 5: succinil CoA + GDP succinato (4C) + GTP Il succinil-coa è una molecola ad elevata energia come tutti gli acil-coa in virtù del gruppo tioestere la cui idrolisi è esoergonica e viene utilizzata in un processo che richiede un accoppiamento di reazioni. La molecola di guanosina 5 -trifosfato (GTP) è una molecola ad alta energia ed è un nucleoside trifosfato come ATP. GTP sarà utilizzato nelle prime tappe della gluconeogenesi o per la sintesi di ATP mediante la reazione: GTP + ADP GDP + ATP. Reazione 6-8: ripristino dell ossalacetato succinato (4C) + NAD + + FAD ossalacetato (4C) + NADH + FADH2 Il succinato viene convertito in ossalacetato, primo intermedio del ciclo mediante un processo di ossidazione che perevede la formazione di NADH e riduzione del coenzima flavinadenina dinucleotide (FAD).
7 BILANCIO ENERGETICO A PARTIRE DA UNA MOLECOLA DI GLUCOSIO
8 ATP NADH FADH2 PRIMA FASE DELLA RESPIRAZIONE DECARBOSSILAZIONE OSSIDATIVA DEL PIRUVATO CICLO DI KREBS 2 (GTP) 6 2 TOT CATENA DI TRASPORTO DEGLI ELETTRONI E FOSFORILAZIONE OSSIDATIVA I coenzimi ridotti NADH e FADH2 che sono stati generati dalla glicolisi e dal ciclo di Krebs vengono nuovamente ossidati per alimentare la prima e la seconda fase della respirazione (ricordare che NAD + può essere nuovamente ottenuto anche mediante la fermentazione). Gli elettroni, provenienti dall'ossidazione del glucosio avvenuta nelle fasi I e II ed immagazzinati nei coenzimi ridotti (equivalenti riducenti), vengono ceduti da questi ultimi all'ossigeno con formazione di acqua (prodotto di riduzione dell'ossigeno molecolare immesso nell'organismo attraverso la respirazione) mediante una serie di molecole trasportatrici di elettroni (ubichinone e citocromo c) che fanno parte della catena di trasporto degli elettroni (electron transport chain, ETC). Il trasferimento di elettroni è catalizzato da quattro complessi proteici (complessi mitocondriali). Gli elettroni passano vengono trasferiti dai coenzimi ridotti NADH e FADH2 al coenzima Q, da quest'ultimo al citocromo c ed infine dal citocromo c all'ossigeno mediante processi redox termodinamicamente favoriti grazie a valori di potenziale normale di riduzione progressivamente crescenti. Tanto più negativo è il potenziale di ossido-riduzione di una data specie tanto maggiore sarà la sua tendenza a cedere elettroni. L ossigeno ha un potenziale normale di riduzione positivo ed accetta indirettamente gli elettroni dai coenzimi ridotti che, al contrario, presentano potenziali normali di riduzione negativi. L energia liberata da tali processi redox viene utilizzata dai complessi I, III e IV che sono pompe protoniche, in grado di espellere gli ioni H + nello spazio intermembrana e generare un gradiente elettrochimico che verrà utilizzato nella sintesi di ATP mediante la fosforilazione ossidativa (ipotesi chemio-osmotica). Complesso I Il complesso I è denominato NADH-CoQ (ubichinone) ossidoreduttasi, 1) trasferisce 2e - da NADH al coenzima Q; NADH+H + + CoQ NAD + + CoQH2 2) espelle 2H + dalla matrice allo spazio intermembrana. Complesso II Il complesso II è chiamato succinato-coq(ubichinone) deidrogenasi e trasferisce gli elettroni da FADH2 al CoQ. Il complesso 2 è un punto di integrazione tra ciclo di Krebs e catena di trasporto degli elettroni. Infatti coincide con l'enzima succinato deidrogenasi che catalizza l ossidazione dell'acido succinico ad acido fumarico riducendo il FAD a FADH2 nel ciclo di Krebs. Tale reazione è reversibile. Nella catena di trasporto degli elettroni viene condotto il processo inverso all ossidazione del succinato (riduzione del fumarato a succinato con ossidazione di FADH2). Il complesso 2 non è una pompa protonica, cioè non è in grado di trasferire protoni dalla matrice allo spazio intermembrana (proteina di membrana estrinseca). Complesso III Il complesso III è chiamato CoQ-citocromo c ossidoreduttasi, è la seconda delle tre pompe protoniche della catena respiratoria e trasferisce gli elettroni dal CoQ al citocromo c; CoQH2 + 2cit c(oss.) CoQ + 2cit c(rid.)
9 Espelle 2H + nello spazio intermembrana. Il complesso 3 contiene il citocromo b e c che possiedono gruppi eme. A differenza dell ubichinone capace di trasportare 2 elettroni, i citocromi possono accettare solo 1 elettrone. Il citocromo c1 è una proteina che diffonde liberamente nella membrana mitocondriale interna (lipofila), che accetta un elettrone dall ubichinone e lo cede mediante il complesso IV all ossigeno. Complesso IV Il complesso IV è chiamato citocromo c ossidasi, è la terza ed ultima pompa di protoni della catena di trasporto degli elettroni e trasferisce gli elettroni dal citocromo c a O2 che si riduce ad H2O.
10 Fosforilazione ossidativa L ossidazione di NADH e FADH2 è necessaria al ripristino di coenzimi in forma ossidata indispensabili alla prima e alla seconda fase della respirazione cellulare. Il trasporto degli elettroni attraverso i complessi I-IV è un processo termodinamicamente favorito (esoergonico). L energia liberata mediante il trasferimento esoergonico degli elettroni dai coenzimi ridotti all'ossigeno viene utilizzata per trasferire idrogenioni (H + ) dalla matrice mitocondriale allo spazio intermembrana. Si crea, in tal modo, un gradiente elettrochimico a livello della membrana mitocondriale interna: nella matrice la concentrazione di ioni H + è minore (ph maggiore) rispetto alla concentrazione di ioni H + nello spazio intermembrana (ph minore). Gli ioni H + accumulati nello spazio intermembrana, non possono tornare liberamente nella matrice nonostante il gradiente di concentrazione favorevole poichè la membrana interna è impermeabile a questi ioni. Il trasporto di ioni H + dallo spazio intermembrana alla matrice mitocondriale è mediato dal complesso dell ATPsintasi (complesso V). Il passaggio H + all interno della matrice mitocondriale dissipa l energia elettrica associata al potenziale elettrochimico di membrana che viene convertita in energia chimica mediante produzione di ATP da ADP + Pi. Questo meccanismo è alla base della cosiddetta teoria chemiosmotica. L ossidazione di NADH produce 3 molecole di ATP, mentre l ossidazione di FADH2 ne produce 2. Questa differenza dipende dalla produzione di un gradiente protonico inferiore nell ossidazione di FADH2 (trasporto di 4H + anziché 6H + ). BILANCIO ENERGETICO DELLA RESPIRAZIONE CELLULARE: a) la prima fase della respirazione cellulare porta alla produzione netta di 2 molecole di ATP. Vengono inoltre prodotte 2 molecole di NADH che saranno riossidate nella catena di trasporto degli elettroni con produzione di 3x2=6 molecole di ATP. b) la decarbossilazione ossidativa delle due molecole di piruvato ottenute da una molecola del glucosio porta alla formazione di due molecole di NADH. Tali molecole verranno ossidate con produzione di 3x2=6 molecole di ATP c) la seconda fase della respirazione determina la produzione di una molecola di GTP che può essere convertita in ATP. Vengono inoltre prodotte 3 molecole di NADH e 1 di FADH2. Da una molecola di glucosio si ottengono 2 molecole di acetil-coa. Quindi mediante l'ossidazione dei due gruppi acetilici (2 cicli di Krebs) vengono prodotte 2 molecole di GTP (2xATP), 3x2=6 molecole di NADH e 2x1=2 molecole di FADH2. d) la terza fase della respirazione (catena di trasporto degli elettroni e fosforilazione ossidativa) porta alla produzione di 6x3=18 molecole di ATP dalla ossidazione di NADH e 2x2=4 molecole di ATP dall'ossidazione di FADH2. Complessivamente quindi vengono ottenute = 38 molecole di ATP GLICOGENO Il glicogeno è una riserva di glucosio che viene accumulato negli organismi animali principalmente nel fegato e nel muscolo scheletrico. Il glicogeno è un polisaccaride le cui unità monomeriche sono molecole di glucosio. Tali unità sono unite tra di loro mediante un legame alfa-1,4-glucosidico. Sono inoltre presenti ramificazioni generate mediante legami alfa-1,6-glucosidici. La biosintesi del glicogeno prende il nome di GLICOGENOSINTESI e, come tutti i processi anabolici, richiede energia. La prima reazione prevede l'isomerizzazione del glucosio 6-fosfato: GLUCOSIO 6-P GLUCOSIO 1-P Enzima= fosfoglucomutasi (isomerasi) Il glucosio 6P è un intermedio della glicolisi ed è ottenuto mediante fosforilazione catalizzata dall'esochinasi del glucosio assorbito dalla cellula (ricordare il motivo dell isomerizzazione).
11 La seconda reazione prevede l'attivazione del glucosio 1-P mediante uridina 5'-trifosfato (UTP) molecola ad alta energia analoga a ATP: GLUCOSIO1-P + UTP UDP-GLUCOSIO + (PPi) Enzima= UDP-GLUCOSIO pirofosforilasi G1-P reagisce con l uridina 5'-trifosfato (UTP) e si formano l uridina 5'-difosfato (UDP)-glucosio (UDP-glucosio) e pirofosfato (PPi) (ricordare il ruolo di PPi). La terza reazione prevede la formazione del legame tra UDP-glucosio e la catena di glicogeno in crescita: UDP-GLUCOSIO + Glicogeno (n) Glicogeno (n+1) + UDP Enzima= Glicogeno sintetasi In tal modo, è stata aggiunta una molecola di glucosio all estremità della catena di glicogeno (n+1), con l eliminazione di UDP. n=numero di unità monosaccaridiche costituenti il glicogeno in crescita. Le ramificazioni vengono ottenute mediante la catalisi condotta da un enzima ramificante, la Glicosiltransferasi. 5 Il processo di GLICOGENOLISI genera glucosio dal glicogeno mediante la scissione dei legami glicosidici alfa-1,4 e alfa-1,6. Il glucosio ottenuto può essere immesso dal fegato ma non dal muscolo nel flusso ematico ed alimentari i tessuti che richiedono costantemente glucosio. Prima reazione: GLIGOGENO (n) + Pi GLUCOSIO1-P + GLICOGENO (n-1) Enzima = Glicogeno fosforilasi La glicogeno fosforilasi scinde il legame α-1,4 glicosidico del glicogeno (n) con l intervento del fosfato inorganico (Pi), producendo una molecola di glicogeno che presenta un residuo monosaccaridico in meno (n-1) e glucosio 1-fosfato. Seconda reazione: GLUCOSIO1-P GLUCOSIO6-P Enzima = Fosfoglucomutasi Il glucosio 1 fosfato viene isomerizzato a glucosio 6-fosfato Terza reazione: GLUCOSIO6-P GLUCOSIO Enzima = Glucosio 6-fosfato fosfatasi Il glucosio 6-fosfato può essere defosforilato e immesso in circolo. Tale reazione può avvenire solo nel fegato. Infatti solo gli epatociti esprimono la glucosio 6-fosfato fosfatasi. Il fegato, quindi può rilasciare il glucosio nel sangue per rifornire gli altri tessuti in condizioni di ipoglicemia. Regolazione di glicogenolisi e glicogenosintesi La regolazione di glicogenolisi e glicogenosintesi è fondamentale per il mantenimento di: OSMOLARITA CELLULARE (la concentrazione di glucosio e quindi la pressione osmotica nello spazio extracellulare deve essere equivalente a quella del citoplasma). GLICEMIA (concentrazione ematica di glucosio). La glicogeno sintasi e la glicogeno fosforilasi sono due enzimi che possono esistere in due forme: la forma (a) attiva: la forma (b) inattiva La glicogeno sintasi è nella forma attiva (a) quando defosforilata, mentre la glicogeno fosforilasi risulta attiva (a) quando viene fosforilata. L attività dei due enzimi è quindi regolata mediante fosforilazione reversibile di solito a carico di residui di serina. Specifici residui di serina possono essere fosforilati ad opera di una fosforilasi chinasi e defosforilati da una fosforilasi fosfatasi regolazione dell attività enzimatica per modificazione covalente. Gli enzimi che catalizzano la fosforilazione sono le Chinasi (proteina chinasi A, fosforilasi b chinasi e glicogeno sintasi chinasi attivano la glicogeno fosforilasi, inibiscono la glicogeno sintasi ed attivano la glicogenolisi) mentre le Fosfatasi catalizzano la defosforilazione (la fosforilasi a fosfatasi attiva la glicogeno sintasi ed inibisce la glicogeno fosforilasi, attivando quindi la sintesi del glicogeno).
12 La regolazione delle attività dei due enzimi è ormonale e dipende da insulina e glucagone/adrenalina: Adrenalina e glucagone promuovono la fosforilazione inibendo la fosforilasi a fosfatasi attivazione della glicogeno fosforilasi ed inibizione della glicogeno sintasi attivazione della glicogeno lisi ed inibizione della glicogenosintesi. L insulina inibisce la fosforilazione inibendo le chinasi come glicogeno sintasi chinasi attivazione della glicogeno sintasi e inibizione della glicogeno fosforilasi attivazione della glicogenosintesi ed inibizione della glicogenolisi. Il glucagone attiva la glicogenolisi epatica per ristabilire i livelli di glicemia, stimolando anche la lipolisi nel tessuto adiposo e mobilizzando in tal modo substrati energetici alternativi al glucosio (acidi grassi) in condizioni di digiuno o di elevato fabbisogno energetico. Il mantenimento di valori costanti di glicemia durante il digiuno è di particolare importanza per il sistema nervoso, che in condizioni normali, utilizza il glucosio come fonte energetica predominante. L'insulina ha invece un effetto opposto e riduce i livelli di glicemia inibendo simultaneamente la lipolisi. GLUCONEOGENESI La cellula può ottenere glucosio anche mediante il processo alternativo di GLUCONEOGENESI ovvero mediante la biosintesi di glucosio da molecole non glucidiche come: 1) l acido alfa-chetopropanoico (piruvato), ottenuto da amminoacidi come l alanina o dall acido alfaidrossipropanoico (lattato), prodotto della fermentazione omolattica 2) il glicerolo, ottenuto dalla scissione dei trigliceridi a livello adipocitario 3) alcuni amminoacidi gluconeogenici come aspartato e glutammato che possono generare intermedi del ciclo di Krebs come l ossalacetato coinvolto nella via gluconeogenica. E importante sottolineare che il piruvato e, di conseguenza, il glucosio non possono essere ottenuti dall acetil-coa, prodotto ad esempio dalla beta-ossidazione dei grassi, a causa dell irreversibilità della decarbossilazione ossidativa del piruvato catalizzata dalla piruvato deidrogenasi. La gluconeogenesi (processo anabolico) avviene nel fegato e nella corteccia surrenale quando le scorte di glucosio o di glicogeno sono insufficienti al mantenimento di livelli normali di glicemia. La gluconeogenesi non è il processo inverso della glicolisi, perché la prima fase della respirazione cellulare prevede 3 reazioni irreversibili: 1. Glucosio + ATP Glucosio 6-fosfato +ADP Enzima: Esochinasi 3. Fruttosio 6-fosfato + ATP Fruttosio-1,6-bisfosfato +ADP Enzima: Fosfofruttochinasi 10. Fosfoenolpiruvato produzione di Piruvato Enzima: Piruvato chinasi Tali reazioni sono fortemente esoergoniche ed il processo indiretto non avviene. Nella gluconeogenesi vengono quindi realizzate le seguenti reazioni per aggirare la barriera energetica corrispondente alle tappe irreversibili della prima fase della respirazione: Piruvato+CO2+ATP+H2O Ossalacetato+ADP+Pi+2H+ Enzima: Piruvato Carbossilasi Ossalacetato+GTP Fosfoenolpiruvato+GDP+CO2 Enzima:Fosfoenolpiruvato carbossichinasi La conversione del piruvato in fosfoenolpiruvato viene ottenuta mediante la sintesi intermedia di ossalacetato a livello mitocondriale. Nella prima fase la reazione richiede energia, fornita da ATP; nella seconda fase l ossalacetato viene trasportato nel citoplasma attraverso il sistema navetta del malato/aspartato e decarbossilato a fosfoenolpiruvato. Anche in questa seconda fase il processo richiede energia fornita però da GTP.
13 Le altre due tappe irreversibili della prima fase della respirazione vengono realizzate mediante l azione di enzimi definiti fosfatasi: Fruttosio -1,6-bisfosfato + H2O Fruttosio 6-fosfato + Pi 1.Glucosio 6-fosfato + H2O Glucosio + Pi Enzima: Fruttosio 1,6-bisfosfatasi Enzima: Glucosio 6-fosfatasi (epatica) La gluconeogenesi è energeticamente dispendiosa. Infatti, per ogni sintetizzata da piruvato vengono utilizzate 4 molecole di ATP e 2 di GTP. molecola di glucosio Regolazione concertata di glicolisi e gluconeogenesi Come per glicogenolisi e glicogenosintesi, glicolisi e gluconeogenesi non possono avvenire contemporaneamente e devono essere regolate simultaneamente. Gli enzimi che vengono regolati allostericamente mediante un meccanismo spesso di retroinibizione sono quelli che catalizzano i processi irreversibili descritti precedentemente. Ad esempio, ATP e AMP inibiscono e attivano, rispettivamente, la glicolisi mentre hanno un effetto opposto sulla gluconeogenesi (ricordare la reazione catalizzata da adenilato chinasi per interpretare il ruolo regolatori di AMP). Un particolare meccanismo regolatorio delle due vie si basa sulla sintesi di un isomero del fruttosio 1,6-difosfato a partire dal fruttosio 6-fosfato. Il fruttosio 2,6-difosfato è un effettore allosterico positivo della fosfofruttochinasi (PFK-1) che attiva la via glicolitica. Lo stesso composto disattiva la fruttosio 1,6-bifosfatasi, inibendo la gluconeogenesi. La sintesi del fruttosio 2,6- bisfosfato è promossa dalla fosfofruttochinasi-2 (PFK-2) anche denominata fruttosio bi fosfatasi 2 (FBPase2), enzima bi-funzionale (enzima dimerico contenente simultaneamente un dominio chinasico e uno fosfatasico) regolato da glucagone e insulina (regolazione ormonale). Tali ormoni quindi regolano in modo opposto entrambe le vie metaboliche. Controllo ormonale Insulina attivazione di PFK-2 aumento di fruttosio 2,6-difosfato citoplasmatico attivazione di PFK-1 attivazione della GLICOLISI Glucagone inibizione di PFK-2 riduzione dei livelli citoplasmatici di fruttosio 2,6-difosfato attivazione di fruttosio 1,6-bifosfatasi attivazione della GLUCONEOGENESI Ricordare anche il ruolo del citrato e del protone nella regolazione di PFK-1 e dell alanina e di Acetil-CoA nella regolazione di PK. REGOLAZIONE DEL CICLO DI KREBS 1. Non ormonale. 2. Regolazione allosterica in base al fabbisogno energetico. a) Un aumento di NADH inibisce le 3 reazioni irreversibili. Inoltre inibisce anche piruvato deidrogenasi (inibita anche da aumenti di ATP e acetil-coa). b) Un aumento di ATP inibisce citrato sintasi e isocitrato deidrogenasi (IDH). Il citrato inibisce la citrato sintasi. c) Succinil CoA e citrato inibiscono alfa-chetoglutarato deidrogenasi ( KGDH). d) ADP attiva (ricordare che è prodotto di ATP nella contrazione) citrato sintasi e isocitrato deidrogenasi. e) Ca 2+ attiva IDH e KGDH (la contrazione richiede influsso di calcio attivazione di Krebs). 3. Disponibilità dei substrati (reazioni anaplerotiche possono accelerare/attivare il ciclo).
14 La gluconeogenesi epatica è parte integrante di due processi che integrano il metabolismo glucidico di muscolo e fegato: 1) Il CICLO DI CORI Il lattato, prodotto dal muscolo quando il fabbisogno energetico deve essere soddisfatto in tempi brevi o in condizioni di carenza d'ossigeno, viene trasportato tramite il flusso ematico al fegato. Nel fegato il lattato viene ossidato dalla lattato deidrogenasi (ricordare le diverse isoforme di LDH) a piruvato (processo inverso della fermentazione) che, a sua volta, viene convertito, mediante gluconeogenesi, in glucosio. 2) Il CICLO GLUCOSIO ALANINA L'alanina, ottenuta per transaminazione dal piruvato nel muscolo in condizioni di elevato fabbisogno energetico passa nel circolo sanguigno e raggiunge il fegato, nel quale subisce una nuova transaminazione (reazione inversa della precedente) rigenerando piruvato. Il piruvato può, quindi essere convertito in glucosio tramite la gluconeogenesi.
15 METABOLISMO DEI LIPIDI DIGESTIONE I lipidi alimentari sono un'importante fonte di energia. Essi sono rappresentati in prevalenza da trigliceridi. La digestione dei lipidi avviene nell intestino. I sali biliari emulsionano le molecole lipidiche poco solubili in acqua in micelle facilitando l azione della lipasi pancreatica, l enzima che scinde i trigliceridi in 2 molecole di acidi grassi liberi e una molecola di monoacilglicerolo (molecola di glicerolo esterificata con una molecola di acido grasso di solito in posizione 2 fattori sterici). Gli acidi grassi a catena corta (meno di 12 atomi di carbonio) diffondono liberamente attraverso la parete intestinale nel flusso ematico. Al contrario, gli acidi grassi a catena lunga e i monogliceridi vengono assorbiti dagli enterociti dove vengono nuovamente convertiti in trigliceridi a livello del reticolo endoplasmatico liscio. I trigliceridi ottenuti in tal modo interagiscono con particolari proteine lipofile definite lipoproteine generando dei complessi lipoproteici a bassa densità definiti chilomicroni. I chilomicromni vengono immessi nel flusso linfatico e poi nel flusso ematico per esocitosi e trasportati ai tessuti. A livello muscolare ed adipocitario, i chilomicroni vengono deprivati di trigliceridi generando i cosiddetti chilomicroni remnant che nel fegato vengono trasformati in lipoproteine a bassissima densità (VLDL), utilizzate per trasportare lipidi ai tessuti capaci di utilizzarli (muscolo scheletrico e tessuto adiposo). Tali lipidi possono essere utilizzati per produrre energia (muscolo) o per costituire delle scorte energetiche (tessuto adiposo) da utilizzare in caso di necessità. Le VLDL vengono progressivamente depauperate di trigliceridi trasformandosi in lipoproteine a densità bassa (LDL) che tornano al fegato dove possono nuovamente arricchirsi di trigliceridi introdotti con la dieta. Un caso particolare di lipoproteine è quello delle lipoproteine ad alta densità (HDL) sintetizzate a livello epatico indipendentemente dai chilomicroni. Tali proteine hanno la capacità di interagire con il colesterolo e di mediare il suo trasporto dai tessuti al fegato dove verrà utilizzato per la sintesi degli acidi biliari. Tali lipoproteine hanno, quindi, una funzione protettiva. Infatti, un eccesso di lipidi e colesterolo circolanti possono favorire la formazione di placche ateromasiche dando inizio all aterosclerosi, patologia favorita dall'elevata e progressiva assunzione di grassi animali e correlata ad un aumento del rischio di sviluppare patologie cardiovascolari. MOBILIZZAZIONE DEI TRIGLICERIDI NEL TESSUTO ADIPOSO Seppur utilizzati direttamente come substrati energetici da alcuni tessuti come il muscolo, buona parte dei trigliceridi viene conservata a livello del tessuto adipocitario. E' importante sottolineare che sia il muscolo che il tessuto adiposo sono insulino sensibili. L'accumulo di trigliceridi nel tessuto adiposo avviene in condizioni di limitato fabbisogno energetico e di iperglicemia che stimola la secrezione pancreatica di insulina. Tale ormone attiva il processo. I chilomicroni e le VLDL trasportate al tessuto adiposo subiscono l'azione della lipoproteina lipasi che scinde i trigliceridi in acidi grassi e glicerolo. Gli acidi grassi possono essere assorbiti dagli adipociti mediante un meccanismo indotto dall'insulina che stimola la contemporanea espressione di GluT4, esaltando la capacità di assorbimento di glucosio di tali cellule. Nell'adipocita, gli acidi grassi condensano con glicerolo proveniente dal di-idrossiacetone fosfato, ottenuto dalla prima fase della respirazione e precursore del glicerolo grazie all azione dell enzima glicerolo 3-fosfato deidrogenasi, per formare nuovamente trigliceridi. In condizioni di elevato fabbisogno energetico e di ipoglicemia, il pancreas produce glucagone che ha un'azione opposta all'insulina ed attiva la lipolisi. Infatti il glucagone attiva la cosiddetta lipasi ormone sensibile, inibita al contrario dall insulina, che catalizza l'idrolisi dei trigliceridi localizzati nell'adipocita ad acidi grassi e glicerolo. Gli acidi grassi liberi possono essere veicolati ai tessuti dall'albumina attraverso il flusso sanguigno. Il glicerolo può essere trasportato al fegato per entrare nella gluconeogenesi, via attivata nelle stesse condizioni fisiologiche.
16 CATABOLISMO: BETA-OSSIDAZIONE La degradazione degli acidi grassi avviene nei mitocondri e viene denominata beta-ossidazione. Gli acidi grassi, assorbiti dalle cellule e trasportati nello spazio intermembrana mitocondriale, vengono attivati mediante condensazione con CoA e formazione di acil-coa, molecole analoghe all'acetil-coa e quindi ad alta energia (gruppo tioestereo). La reazione è fortemente endoergonica e richiede consumo di 2 molecole di ATP. Gli acil-coa non possono attraversare la membrana mitocondriale interna e sono trasformati dalla carnitina acil transferasi I in acilcarnitine per reazione con la carnitina. Le acilcarnitine attraversano la membrana tramite translocasi e giunte nella matrice mitocondriale sono riconverite nuovamente in acil-coa dalla carnitina aciltransferasi II. L acil-coa subisce nella matrice mitocondriale una serie di 4 reazioni che costituiscono un ciclo di beta-ossidazione: una deidrogenazione FAD dipendente (sintesi di enoil-coa), una idratazione (sintesi di beta-idrossi acil-coa), una ossidazione dell ossidrile in posizione beta a chetone NAD+ dipendente (sintesi di beta-cheto Acil-CoA) e una reazione di tiolisi (sintesi di Acetil-CoA e di.una molecola di Acil-CoA contenente 2 atomi di carbonio in meno rispetto all Acetil-CoA originario). I coenzimi FAD e NAD ridotti sono convogliati direttamente nella catena di trasporto degli elettroni. Complessivamente, la degradazione ossidativa degli acidi grassi a catena diversamente lunga converte le molecole di acido grasso in un numero variabile di molecole di acetil-coa che possono essere ossidate nel ciclo di Krebs con produzione di energia. Ad esempio, da una molecola di acido palmitico (16 atomi di carbonio) si ottengono, mediante 7 cicli di beta ossidazione, 8 molecole di acetil-coa. L'ossidazione di tali molecole mediante 8 ripetizioni del ciclo di Krebs produce 12x8=96 molecole di ATP. Inoltre, ogni ciclo di betaossidazione comporta la produzione di 1 molecola di FADH2 e 1 molecola di NADH. Mediante 7 cicli di beta-ossidazione vengono quindi prodotte 7 molecole di FADH2 e 7 molecole di NADH che generano rispettivamente 7x2=14 e 7x3=21 molecole di ATP attraverso la terza fase della respirazione cellulare. Il numero di molecole di ATP prodotte è quindi: =131 molecole di ATP. Ricordando però che l'attivazione dell'acido grasso, in tal caso acido palmitico, richiede il consumo di due molecole di ATP la resa complessiva del processo può essere valutata in 131-2=129 molecole di ATP. Ricordare che gli acidi grassi a catena dispari producono nell ultimo ciclo di beta ossidazione una molecola di propionil-coa che può essere convertita in succinil-coa alimentando il ciclo di Krebs. E' importante sottolineare che i lipidi non possono essere usati per produrre glucosio mediante il processo gluconeogenico. Infatti la trasformazione dell'acetil-coa prodotto nella beta-ossidazione in piruvato, primo intermedio della gluconeogenesi, è impossibile poiché a decarbossilazione ossidativa del piruvato ad acetil-coa è altamente esoergonica ed irreversibile. Inoltre, la produzione di energia dagli acidi grassi e dalla sintesi di acetil-coa mediante la betaossidazione può avvenire solo in presenza di adeguate quantità di ossalacetato, intermedio del ciclo di Krebs. Le eventuali carenze di ossalacetato nel ciclo possono essere colmate grazie all'azione dell'enzima piruvato carbossilasi o dell enzima malico che catalizzano la trasformazione anaplerotica del piruvato in ossalacetato (ricordare anche la reazione anaplerotica catalizzata da PEPCK). Quindi l'ossalacetato, indispensabile al ciclo di Krebs, proviene principalmente dal glucosio, precursore del piruvato. Quindi, in assenza di glucosio il ciclo di Krebs, non può avvenire. Ecco perchè si suol dire che i grassi bruciano nel fuoco degli zuccheri. In condizioni di ipoglicemia e bassi livelli di ossalacetato, l acetil-coa prodotto dalla beta ossidazione si accumula, inibisce le fasi I e II della respirazione e condensa generando acetoacetato, beta-idrossibutirrato e acetone definiti corpi chetonici. I corpi chetonici sono prodotti nel fegato e sono importanti substrati energetici per il muscolo cardiaco ed il cervello in condizioni di elevato fabbisogno energetico.
17 BIOSINTESI DEGLI ACIDI GRASSI La beta-ossidazione avviene nella matrice mitocondriale mentre la biosintesi degli acidi grassi avviene a livello citoplasmatico. Utilizza per i processi riduttivi molecole di nicotinammide adenina di nucleotide fosfato ridotto (NADPH), la forma fosforilata del coenzima NAD e come molecola precursore l acetil-coa prodotto principalmente dal catabolismo dei carboidrati o dell etanolo. Quindi i carboidrati possono essere precursori dei lipidi generando acetil-coa mediante la decarbossilazione ossidativa del piruvato catalizzata dalla piruvato deidrogenasi. Ricordare che la reazione è irreversibile e che, per questo motivo, la conversione degli acidi grassi in zuccheri non è possibile,. Nella biosintesi citoplasmatica degli acidi grassi l acetil-coa (molecola a due atomi di carbonio), prodotto a livello mitocondriale, non può attraversare la membrana mitocondriale interna per raggiungere il citoplasma. Viene quindi convertito in citrato dalla citrato sintasi. Il citrato può essere trasportato nel citoplasma attraverso un sistema di trasporto specifico (antiporto citrato-malato; un eccellente trattazione dei sistemi di trasporto mitocondriali è disponibile al link: e nuovamente trasformato in acetil-coa dalla ATP-citrato liasi citoplasmatica (processo endoergonico che richiede ATP). L acetil-coa è ulteriormente attivato mediante una reazione endoergonica di carbossilazione a malonil-coa (molecola a tre atomi di carbonio). Il complesso multienzimatico dell acido grasso sintasi catalizza la sintesi di acidi grassi saturi a non più di 16 atomi di carbonio a partire da acetil-coa e malonil-coa legati simultaneamente a siti tiolici della proteina trasportatrice di acili (ACP), componente della acido grasso sintasi, mediante legami tioesterei. Questo favorisce stericamente la reazione di condensazione. Le unità di acetile contengono due atomi di carbonio. Quindi negli organismi superiori è possibile solo la sintesi di acidi grassi a catena pari. Nell uomo, diversi cicli biosintetici permettono di sintetizzare acidi grassi a catena 16C. L acido palmitico (C16:0) può generare acidi grassi a catena più lunga ed alcuni acidi grassi insaturi per azione di enzimi chiamati rispettivamente elongasi e desaturasi. Il doppio legame non può essere prodotto mai nel nostro organismo oltre l atomo di carbonio in posizione 9. Per questo motivo, l organismo non può sintetizzare acidi grassi insaturi come l acido linoleico (n-6) e linolenico (n-3), che contengono doppi legami oltre il C9 (acidi grassi essenziali), sono assunti solo tramite dieta e sono precursori di importanti molecole che si comportano come ormoni (prostaglandine, leucotrieni e tromboxani) e sono fondamentalmente coinvolte nella regolazione dei processi infiammatori. REGOLAZIONE CONCERTATA DI BETA-OSSIDAZIONE E BIOSINTESI. a) regolazione ormonale di acetil-coa carbossilasi (inibita da glucagone ed attivata da insulina). b) Regolazione allosterica della acetil-coa carbossilasi da citrato e palmitato. c) Regolazione allosterica della carnitina aciltransferasi I dal malonil-coa e acido malonico.
18 CATABOLISMO DELLE PROTEINE E DEGLI AMMINOACIDI La digestione delle proteine ha inizio nello stomaco dove il ph estremamente acido denatura le proteine favorendo l azione dell'enzima pepsina. Tale proteasi è generata da una forma inattiva, il pepsinogeno che viene attivato e trasformato nell'enzima corrispondente mediante una modificazione post-traduzionale che consiste nella rimozione di alcuni residui amminoacidici dalla sequenza primaria. La pepsina idrolizza i legami ammidici (peptidici) tra specifici amminoacidi (AA) dando luogo a polipeptidi di vario peso molecolare. Il ph ottimale delle pepsine è compreso tra 1.6 e 3.2, intervallo che comprende il valore di ph gastrico. La pepsina è quindi inattiva a livello intestinale dove i valori di ph sono maggiori. Nell intestino tenue i peptidi ottenuti dall'azione della pepsina vengono ulteriormente degradati per azione della tripsina e della chimotripsina, potenti enzimi proteolitici funzionali ad un ph neutro. Come la pepsina, anche tripsina e chimotripsina vengono ottenute da un processo di maturazione proteine dei precursori tripsinogeno e chimotrispinogeno, rispettivamente. La digestione porta alla produzione di AA e dipeptidi. Il trasporto degli AA dall intestino tenue ai tessuti avviene in maniera simile al trasporto del glucosio a livello enterocitario. Si tratta quindi di un trasporto attivo che ottimizza l'assorbimento degli AA a livello intestinale. Gli AA assunti tramite la dieta a) sono utilizzati senza che subiscano modifiche strutturali per la sintesi di proteine codificate dal genoma della specifica cellula o tessuto in condizioni di limitato fabbisogno di energia b) come substrati catabolici in condizioni di elevato fabbisogno energetico. La degradazione degli AA prevede formazione di ammoniaca ottenuta dalla rimozione del gruppo alfa-amminico dell AA. La reazione che sposta il gruppo amminico da un generico AA ad un alfachetoacido (piruvato, ossalacetato, alfa-chetoglutarato) accettore di tale gruppo prende il nome di transaminazione. L'AA transaminato si trasforma in un alfa-chetoacido diverso da quello accettore. Quest ultimo accetta il gruppo amminico diventando un AA: alfa-aa (1) + alfa-chetoacido (2) : alfa-chetoacido (1) + alfa-aa(2) Gli enzimi che catalizzano tali reazioni di ossidoriduzione reversibili prendono il nome di transaminasi o amminotransferasi. Molti alfa-chetoacidi (1) ottenuti in tal modo sono intermedi del ciclo di Krebs (dall'aspartato si ottiene ad esempio l'ossalacetato) o piruvato nel caso dell'aa alanina. Gli AA che generano tali alfa-chetoacidi vengono definiti gluconeogenici, poiché precursori dell ossalacetato e quindi del glucosio e possono alimentare il ciclo di Krebs in condizioni di elevato fabbisogno energetico (anaplerosi). Lo scheletro carbonioso dell'aa può anche generare acetil-coa. In tal caso gli AA vengono definiti chetogenici in quanto poteniali precursori di corpi chetonici. Di particolare importanza è la transaminazione che coinvolge un amminoacido generico e l'alfachetoacido alfa-chetoglutarato (un intermedio del ciclo di Krebs). alfa-aa+ alfa-chetoglutarato alfa-chetoacido + glutammato Mediante tale reazione l' alfa-chetoglutarato viene convertito nell'amminoacido glutammato che è l'unico amminoacido dal quale possa essere ottenuta ammoniaca, prodotto finale del catabolismo proteico, mediante una reazione di deaminazione ossidativa catalizzata dall enzima glutammato deidrogenasi. Quindi, l'alfa-chetoglutarato può essere considerato accettore finale di tutti i gruppi amminici derivanti da AA perchè unico precursore di glutammato.
19 L ammoniaca prodotta da tale reazione viene attivata mediante una reazione endoergonica con il bicarbonato e trasformata in carbamilfosfato. Il carbamilfosfato viene quindi trasformato in urea mediante il ciclo omonimo, che avviene a livello epatico e coinvolge sia citoplasma che mitocondri dell'epatocita (ricordare l integrazione di ciclo dell urea e ciclo di Krebs sintesi di fumarato nella conversione di arginosuccinato a arginina). L'urea viene infine eliminata con le urine. Il catabolismo proteico e le transaminazioni che avvengono nel muscolo in condizioni di elevato fabbisogno energetico e per alimentare il ciclo di Krebs (anaplerosi) richiedono un sistema di trasporto dell'ammoniaca al fegato in cui avviene il ciclo dell urea. A livello muscolare, un alfachetoacido accettore del gruppo amminico di amminoacici è il piruvato che si trasforma in alanina. L'alanina trasportata al fegato attraverso il flusso ematico viene nuovamente transaminata per reazione con alfa-chetoglutarato generando piruvato che può entrare nella gluconeogenesi (ciclo glucosio-alanina) e glutammato che procede invece verso la deamminazione ossidativa ed il ciclo dell'urea. L alanina ha quindi sia un ruolo gluconegenico che detossificante, rimuovendo ammoniaca dal muscolo. Un altro importante trasportatore di gruppi amminici dal muscolo al fegato è la glutammina, ottenuta dal glutammato mediante la reazione endoergonica catalizzata dalla glutammina sintetasi. Tale reazione richiede il consumo di una molecola di ATP (accoppiamento di reazioni) e trasforma il gruppo carbossilico gamma del glutammato in gruppo ammidico mediante la condensazione con ammonio dell intermedio acil-fosfato (molecola ad alta energia). La glutammina viene trasportata dal muscolo al fegato o al rene dove viene convertita nuovamente in glutammato ed NH4 + mediante la reazione catalizzata dall enzima glutaminasi. Nel fegato l ammonio entra nel ciclo dell urea mentre nel rene viene escreto attraverso le urine.
GLUCONEOGENESI. Sintesi (GENESI) di nuove (NEO) molecole di glucosio
 GLUCONEOGENESI Sintesi (GENESI) di nuove (NEO) molecole di glucosio CATABOLISMO ANABOLISMO OSSIDAZIONI Produzione di ATP RIDUZIONI Consumo di ATP La GLUCONEOGENESI è un PROCESSO ANABOLICO La gluconeogenesi
GLUCONEOGENESI Sintesi (GENESI) di nuove (NEO) molecole di glucosio CATABOLISMO ANABOLISMO OSSIDAZIONI Produzione di ATP RIDUZIONI Consumo di ATP La GLUCONEOGENESI è un PROCESSO ANABOLICO La gluconeogenesi
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 26 La gluconeogenesi Concetti chiave: Il fegato e il rene possono sintetizzare glucosio da lattato, piruvato e amminoacidi.
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 26 La gluconeogenesi Concetti chiave: Il fegato e il rene possono sintetizzare glucosio da lattato, piruvato e amminoacidi.
Metabolismo: Introduzione
 Metabolismo: Introduzione METABOLISMO Insieme delle reazioni chimiche coordinate e integrate che hanno luogo in tutte le cellule C A T A B O L I S M O Ossidazioni esoergoniche Alimenti: Carboidrati Lipidi
Metabolismo: Introduzione METABOLISMO Insieme delle reazioni chimiche coordinate e integrate che hanno luogo in tutte le cellule C A T A B O L I S M O Ossidazioni esoergoniche Alimenti: Carboidrati Lipidi
GLICOGENOLISI & GLICOGENOSINTESI
 GLICOGENOLISI & GLICOGENOSINTESI ALIMENTARE Glucosio GLUCONEOGENESI GLICOGENOLISI (epatica) Glicemia: 70-90 mg/100ml ~ 5 mm GLICOGENO Nel fegato fino al 6-10% della massa epatica (~100 grammi) Nel muscolo
GLICOGENOLISI & GLICOGENOSINTESI ALIMENTARE Glucosio GLUCONEOGENESI GLICOGENOLISI (epatica) Glicemia: 70-90 mg/100ml ~ 5 mm GLICOGENO Nel fegato fino al 6-10% della massa epatica (~100 grammi) Nel muscolo
GLUCONEOGENESI SINTESI DI NUOVO GLUCOSIO A PARTIRE DA FONTI NON GLUCIDICHE. L UOMO CONSUMA QUASI 160 g DI GLUCOSIO AL GIORNO
 GLUCONEOGENESI SINTESI DI NUOVO GLUCOSIO A PARTIRE DA FONTI NON GLUCIDICHE L UOMO CONSUMA QUASI 160 g DI GLUCOSIO AL GIORNO 75% DI TALE GLUCOSIO E NEL CERVELLO I FLUIDI CORPOREI CONTENGONO SOLO 20 g DI
GLUCONEOGENESI SINTESI DI NUOVO GLUCOSIO A PARTIRE DA FONTI NON GLUCIDICHE L UOMO CONSUMA QUASI 160 g DI GLUCOSIO AL GIORNO 75% DI TALE GLUCOSIO E NEL CERVELLO I FLUIDI CORPOREI CONTENGONO SOLO 20 g DI
Metabolismo degli amminoacidi. Ciclo dell urea
 Metabolismo degli amminoacidi Ciclo dell urea Biosintesi di amminoacidiporfirine, creatina, carnitina, ormoni, nucleotidi Gli amminoacidi possono subire una degradazione ossidativa in 3 diverse situazioni
Metabolismo degli amminoacidi Ciclo dell urea Biosintesi di amminoacidiporfirine, creatina, carnitina, ormoni, nucleotidi Gli amminoacidi possono subire una degradazione ossidativa in 3 diverse situazioni
METABOLISMO DEL Glucosio
 METABLISM DEL Glucosio Il metabolismo del glucosio può essere suddiviso nelle seguenti vie metaboliche: Glicolisi ssidazione del glucosio in acido piruvico e acido lattico. Via del pentoso fosfato Via
METABLISM DEL Glucosio Il metabolismo del glucosio può essere suddiviso nelle seguenti vie metaboliche: Glicolisi ssidazione del glucosio in acido piruvico e acido lattico. Via del pentoso fosfato Via
CONTROLLO ORMONALE DEL METABOLISMO GLUCIDICO DA PARTE DI GLUCAGONE, ADRENALINA E INSULINA
 CONTROLLO ORMONALE DEL METABOLISMO GLUCIDICO DA PARTE DI GLUCAGONE, ADRENALINA E INSULINA QUESTI ORMONI REGOLANO IL FLUSSO DEI METABOLITI NELLA GLICOLISI, NELLA GLICOGENO-SINTESI, NELLA GLIGENO-LISI E
CONTROLLO ORMONALE DEL METABOLISMO GLUCIDICO DA PARTE DI GLUCAGONE, ADRENALINA E INSULINA QUESTI ORMONI REGOLANO IL FLUSSO DEI METABOLITI NELLA GLICOLISI, NELLA GLICOGENO-SINTESI, NELLA GLIGENO-LISI E
Regolazione del metabolismo del glucosio
 Regolazione del metabolismo del glucosio Regolazione coordinata di glicolisi e gluconeogenesi Glicolisi e gluconeogenesi sono regolate in modo reciproco La regolazione è a livello dei punti di deviazione
Regolazione del metabolismo del glucosio Regolazione coordinata di glicolisi e gluconeogenesi Glicolisi e gluconeogenesi sono regolate in modo reciproco La regolazione è a livello dei punti di deviazione
Helena Curtis N. Sue Barnes
 Helena Curtis N. Sue Barnes LA RESPIRAZIONE CELLULARE INDICE Demolizione del glucosio Glicolisi Fermentazione lattica Fermentazione alcolica Respirazione cellulare Ciclo di Krebs Catena di trasporto degli
Helena Curtis N. Sue Barnes LA RESPIRAZIONE CELLULARE INDICE Demolizione del glucosio Glicolisi Fermentazione lattica Fermentazione alcolica Respirazione cellulare Ciclo di Krebs Catena di trasporto degli
Metabolismo degli aminoacidi
 Metabolismo degli aminoacidi Quando gli aminoacidi provenienti dalla digestione gastrica e intestinale, non vengono utilizzati per la costruzione di nuove proteine vengono demoliti Transaminazione Per
Metabolismo degli aminoacidi Quando gli aminoacidi provenienti dalla digestione gastrica e intestinale, non vengono utilizzati per la costruzione di nuove proteine vengono demoliti Transaminazione Per
Respirazione cellulare
 Respirazione cellulare L equazione generale della respirazione C 6 H 12 O 6 + 6 O 2! 6 CO 2 + 6 H 2 O + 36 ATP 1 molec zucchero 6 molec ossigeno 6 molec anidride carbonica 6 molec acqua + = + + 36 molecole
Respirazione cellulare L equazione generale della respirazione C 6 H 12 O 6 + 6 O 2! 6 CO 2 + 6 H 2 O + 36 ATP 1 molec zucchero 6 molec ossigeno 6 molec anidride carbonica 6 molec acqua + = + + 36 molecole
Mais, riso, patate, granozucchero di canna o barbabietola Latte da zucchero Polisaccaride Amido - - Disaccaride Maltosio Saccarosio Lattosio
 Abbiamo visto che i carboidrati sono la principale fonte di energia nell'alimentazione umana. Nella nostra dieta, sono sopratutto presenti nella forma di amido, ma anche il saccarosio è presente in una
Abbiamo visto che i carboidrati sono la principale fonte di energia nell'alimentazione umana. Nella nostra dieta, sono sopratutto presenti nella forma di amido, ma anche il saccarosio è presente in una
METABOLISMO DEL GLICOGENO
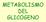 METABOLISMO DEL GLICOGENO Struttura del glicogeno DEMOLIZIONE DEL GLICOGENO: GLICOGENOLISI 1) distacco progressivo di unità glucosidiche con formazione di glucosio-1- fosfato: enzima: glicogeno fosforilasi
METABOLISMO DEL GLICOGENO Struttura del glicogeno DEMOLIZIONE DEL GLICOGENO: GLICOGENOLISI 1) distacco progressivo di unità glucosidiche con formazione di glucosio-1- fosfato: enzima: glicogeno fosforilasi
SISTEMI ENERGETICI. L ATP privato di uno dei suoi 3 radicali fosforici diventa ADP (adenosindifosfato).
 SISTEMI ENERGETICI LE FONTI ENERGETICHE MUSCOLARI I movimenti sono resi possibili, dal punto di vista energetico, grazie alla trasformazione, da parte dei muscoli, dell energia chimica ( trasformazione
SISTEMI ENERGETICI LE FONTI ENERGETICHE MUSCOLARI I movimenti sono resi possibili, dal punto di vista energetico, grazie alla trasformazione, da parte dei muscoli, dell energia chimica ( trasformazione
N 2, malgrado la sua abbondanza, è un fattore limitante la crescita della maggior parte degli organismi
 Glicina (Gly) Alanina (Ala) N 2, malgrado la sua abbondanza, è un fattore limitante la crescita della maggior parte degli organismi La digestione delle proteine endopeptidasi H O R H O R R H 3+ N -C-C-NH-C-C-NH-C-C-NH-C-C-NH-C-COO
Glicina (Gly) Alanina (Ala) N 2, malgrado la sua abbondanza, è un fattore limitante la crescita della maggior parte degli organismi La digestione delle proteine endopeptidasi H O R H O R R H 3+ N -C-C-NH-C-C-NH-C-C-NH-C-C-NH-C-COO
Il metabolismo del glicogeno e la gluconeogenesi. Copyright 2013 Zanichelli editore S.p.A.
 Il metabolismo del glicogeno e la gluconeogenesi Copyright 2013 Zanichelli editore S.p.A. Capitolo 16 La demolizione del glicogeno Concetti chiave 16.1 Il glicogeno, la forma di immagazzinamento del glucosio,
Il metabolismo del glicogeno e la gluconeogenesi Copyright 2013 Zanichelli editore S.p.A. Capitolo 16 La demolizione del glicogeno Concetti chiave 16.1 Il glicogeno, la forma di immagazzinamento del glucosio,
Da dove prendono energia le cellule animali?
 Da dove prendono energia le cellule animali? La cellula trae energia dai legami chimici contenuti nelle molecole nutritive Probabilmente le più importanti sono gli zuccheri, che le piante sintetizzano
Da dove prendono energia le cellule animali? La cellula trae energia dai legami chimici contenuti nelle molecole nutritive Probabilmente le più importanti sono gli zuccheri, che le piante sintetizzano
Metabolismo degli amminoacidi
 Metabolismo degli amminoacidi Gli amminoacidi derivati in gran parte dalla degradazione delle proteine della dieta o intracellulari possono essere ossidati per generare e energia. La quantità di energia
Metabolismo degli amminoacidi Gli amminoacidi derivati in gran parte dalla degradazione delle proteine della dieta o intracellulari possono essere ossidati per generare e energia. La quantità di energia
GLICOLISI e CATABOLISMO degli ESOSI
 GLICOLISI e CATABOLISMO degli ESOSI 1 ph= 7.0 2 Digestione dei polisaccaridi Amilasi salivare e pancreatica = endoglucosidasi 3 Digestione degli oligosaccaridi maltosio, maltotriosio, destrine, Saccarosio,
GLICOLISI e CATABOLISMO degli ESOSI 1 ph= 7.0 2 Digestione dei polisaccaridi Amilasi salivare e pancreatica = endoglucosidasi 3 Digestione degli oligosaccaridi maltosio, maltotriosio, destrine, Saccarosio,
FUNZIONI DEI MITOCONDRI
 FUNZIONI DEI MITOCONDRI La funzione principale dei mitocondri è di compiere le trasformazioni energetiche indispensabili per le funzioni cellulari. Metabolismo energetico: insieme delle reazioni chimiche
FUNZIONI DEI MITOCONDRI La funzione principale dei mitocondri è di compiere le trasformazioni energetiche indispensabili per le funzioni cellulari. Metabolismo energetico: insieme delle reazioni chimiche
Attenzione : lunedì 29 aprile NON ci sarà lezione
 Attenzione : lunedì 29 aprile NON ci sarà lezione Metabolismo dei lipidi a) Ossidazione degli acidi grassi Triacilgliceroli (90% del totale) Gruppi metilenici o metilici Richiedono molto O 2 per essere
Attenzione : lunedì 29 aprile NON ci sarà lezione Metabolismo dei lipidi a) Ossidazione degli acidi grassi Triacilgliceroli (90% del totale) Gruppi metilenici o metilici Richiedono molto O 2 per essere
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio. GLUCONEOGENESI (sintesi da precursori non glucidici)
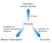 DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) Metabolismo del glucosio La gluconeogenesi epatica è regolata
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) Metabolismo del glucosio La gluconeogenesi epatica è regolata
glicogeno Glucosio 6-P Piruvato Acetil CoA Intermedi del ciclo di Krebs
 PIRUVAT glicogeno Glicogeno sintesi glicogenolisi Glucosio Glucosio 6-P Ribosio 5-P glicolisi Gluconeogenesi Amino acidi Piruvato Acetil CoA lattato Intermedi del ciclo di Krebs Concentrazione di glicogeno
PIRUVAT glicogeno Glicogeno sintesi glicogenolisi Glucosio Glucosio 6-P Ribosio 5-P glicolisi Gluconeogenesi Amino acidi Piruvato Acetil CoA lattato Intermedi del ciclo di Krebs Concentrazione di glicogeno
dieta vengono convertiti in composti dei corpi chetonici.
 Metabolismo degli aminoacidi Metabolismo degli aminoacidi Gli aminoacidi introdotti in eccesso con la dieta vengono convertiti in composti precursori del glucosio, degli acidi grassi e dei corpi chetonici.
Metabolismo degli aminoacidi Metabolismo degli aminoacidi Gli aminoacidi introdotti in eccesso con la dieta vengono convertiti in composti precursori del glucosio, degli acidi grassi e dei corpi chetonici.
Si possono suddividere in:
 Si possono suddividere in: LIPIDI DI DEPOSITO: si accumulano nelle cellule del tessuto adiposo, sono una riserva energetica, mantengono costante la temperatura del corpo (termogenesi) LIPIDI STRUTTURALI:
Si possono suddividere in: LIPIDI DI DEPOSITO: si accumulano nelle cellule del tessuto adiposo, sono una riserva energetica, mantengono costante la temperatura del corpo (termogenesi) LIPIDI STRUTTURALI:
Il ciclo dell acido citrico
 Il ciclo dell acido citrico Il catabolismo di proteine, grassi e carboidrati avviene nelle tre fasi della respirazione cellulare Il piruvato viene ossidato ad acetil-coa e CO 2 La decarbossilazione
Il ciclo dell acido citrico Il catabolismo di proteine, grassi e carboidrati avviene nelle tre fasi della respirazione cellulare Il piruvato viene ossidato ad acetil-coa e CO 2 La decarbossilazione
GLUCOSIO GLUCOSIO-6-FOSFATO ISOMERASI FRUTTOSIO-6-FOSFATO ATP FRUTTOSIO-1,6-DIFOSFATO ALDOLASI ISOMERASI
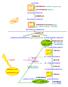 GLUCOSIO ESOCHINASI (costitutivo) inibizione feed-back GLUCOCHINASI (induttivo) GLUCOSIO-6-FOSFATO ISOMERASI - 2 FRUTTOSIO-6-FOSFATO FOSFOFRUTTOCINASI allosterico reg +: e Fr-2,6-dP reg -:, citrato FRUTTOSIO-1,6-DIFOSFATO
GLUCOSIO ESOCHINASI (costitutivo) inibizione feed-back GLUCOCHINASI (induttivo) GLUCOSIO-6-FOSFATO ISOMERASI - 2 FRUTTOSIO-6-FOSFATO FOSFOFRUTTOCINASI allosterico reg +: e Fr-2,6-dP reg -:, citrato FRUTTOSIO-1,6-DIFOSFATO
Giovanni Di Bonaventura, Ph.D., B.Sc. Università di Chieti-Pescara
 Giovanni Di Bonaventura, Ph.D., B.Sc. Università di Chieti-Pescara Richieste metaboliche: elementi essenziali In generale, i batteri per la loro crescita hanno bisogno di elementi essenziali. In particolare
Giovanni Di Bonaventura, Ph.D., B.Sc. Università di Chieti-Pescara Richieste metaboliche: elementi essenziali In generale, i batteri per la loro crescita hanno bisogno di elementi essenziali. In particolare
Esempio di domande possibili alla prova orale di Biochimica AA 2011-12 Farmacia1 - FERIOTTO
 Esempio di domande possibili alla prova orale di Biochimica AA 2011-12 Farmacia1 - FERIOTTO Lo studente spieghi: - Geometria dei legami del carbonio. - Principali gruppi funzionali delle biomolecole. -
Esempio di domande possibili alla prova orale di Biochimica AA 2011-12 Farmacia1 - FERIOTTO Lo studente spieghi: - Geometria dei legami del carbonio. - Principali gruppi funzionali delle biomolecole. -
Il glicogeno (riserva di glucosio) è immagazzinato nel fegato e nei muscoli (con finalità diverse )
 Glicogeno Glicogeno...1 Glicogenolisi...3 Glicogenosintesi...7 Regolazione ormonale della glicogenolisi e delle glicogenosintesi...13 Il recettore del glucagone e quello dell adrenalina sono 2 GPCR (G-Protein
Glicogeno Glicogeno...1 Glicogenolisi...3 Glicogenosintesi...7 Regolazione ormonale della glicogenolisi e delle glicogenosintesi...13 Il recettore del glucagone e quello dell adrenalina sono 2 GPCR (G-Protein
Niccolò Taddei Biochimica
 Niccolò Taddei Biochimica VERSO L UNIVERSITÀ Le domande sono tratte dalle prove di ammissione emesse annualmente dal Ministero dell Istruzione, dell Università e della Ricerca (MIUR) e le soluzioni sono
Niccolò Taddei Biochimica VERSO L UNIVERSITÀ Le domande sono tratte dalle prove di ammissione emesse annualmente dal Ministero dell Istruzione, dell Università e della Ricerca (MIUR) e le soluzioni sono
La nutrizione e il metabolismo
 La nutrizione e il metabolismo 1. Le sostanze nutritive, o nutrienti 2. Definizione di metabolismo 3. Il metabolismo dei carboidrati 4. Il metabolismo dei lipidi 1 L apparato respiratorio 5. Il metabolismo
La nutrizione e il metabolismo 1. Le sostanze nutritive, o nutrienti 2. Definizione di metabolismo 3. Il metabolismo dei carboidrati 4. Il metabolismo dei lipidi 1 L apparato respiratorio 5. Il metabolismo
LIPIDI e METABOLISMO DEGLI ACIDI GRASSI
 LIPIDI e METABOLISMO DEGLI ACIDI GRASSI Lipidi I lipidi sono i principali costituenti delle membrane biologiche. Sono biomolecole insolubile in acqua ma solubili in solventi organici. La loro idrofobicità
LIPIDI e METABOLISMO DEGLI ACIDI GRASSI Lipidi I lipidi sono i principali costituenti delle membrane biologiche. Sono biomolecole insolubile in acqua ma solubili in solventi organici. La loro idrofobicità
digestione dei lipidi alimentari duodeno digiuno sali biliari fosfolipidi bile specifiche idrolasi pancreatiche colecistochinina
 La digestione dei lipidi alimentari, in prevalenza trigliceridi, avviene nel duodeno e nel digiuno per azione combinata dei sali biliari e dei fosfolipidi della bile e delle specifiche idrolasi pancreatiche
La digestione dei lipidi alimentari, in prevalenza trigliceridi, avviene nel duodeno e nel digiuno per azione combinata dei sali biliari e dei fosfolipidi della bile e delle specifiche idrolasi pancreatiche
Degradazione delle proteine della dieta. Catabolismo degli aminoacidi
 Degradazione delle proteine della dieta Catabolismo degli aminoacidi LE PROTEINE DELLA DIETA SONO DEGRADATE ENZIMATICAMENTE AD AMINOACIDI LIBERI L ingresso di una proteina nello stomaco stimola la mucosa
Degradazione delle proteine della dieta Catabolismo degli aminoacidi LE PROTEINE DELLA DIETA SONO DEGRADATE ENZIMATICAMENTE AD AMINOACIDI LIBERI L ingresso di una proteina nello stomaco stimola la mucosa
dotto di Wirsung che si riversa nella papilla maggiore del duodeno;
 Metabolismo dei lipidi Abbiamo già visto che il metabolismo energetico con produzione di ATP, avviene in seguito alla demolizione di zuccheri (glicolisi), lipidi, e in piccolissima percentuale delle proteine.
Metabolismo dei lipidi Abbiamo già visto che il metabolismo energetico con produzione di ATP, avviene in seguito alla demolizione di zuccheri (glicolisi), lipidi, e in piccolissima percentuale delle proteine.
di glucosio da parte di tutte le cellule, facilitandone il trasporto transmembranario 2. aumenta l utilizzazione
 non c Ormone ipoglicemizzante, causa un forte abbassamento della glicemia (70-100 mg/100 ml) perché esalta i processi responsabili della sottrazione di glucosio dal sangue e inibisce i processi responsabili
non c Ormone ipoglicemizzante, causa un forte abbassamento della glicemia (70-100 mg/100 ml) perché esalta i processi responsabili della sottrazione di glucosio dal sangue e inibisce i processi responsabili
Il ciclo nutrizione / digiuno
 Il ciclo nutrizione / digiuno Aspetti generali La fase di assorbimento è il periodo che va dalle 2 alle 4 ore successive all assunzione di un pasto. Durante questo intervallo si verifica un transitorio
Il ciclo nutrizione / digiuno Aspetti generali La fase di assorbimento è il periodo che va dalle 2 alle 4 ore successive all assunzione di un pasto. Durante questo intervallo si verifica un transitorio
Esempio di domande possibili alla prova orale di Biochimica Generale ed Applicata AA 2009-10 Farmacia - FERIOTTO
 Esempio di domande possibili alla prova orale di Biochimica Generale ed Applicata AA 2009-10 Farmacia - FERIOTTO Lo studente spieghi: - Geometria dei legami del carbonio. - Principali gruppi funzionali
Esempio di domande possibili alla prova orale di Biochimica Generale ed Applicata AA 2009-10 Farmacia - FERIOTTO Lo studente spieghi: - Geometria dei legami del carbonio. - Principali gruppi funzionali
METABOLISMO E SISTEMI ENERGETICI
 METABOLISMO E SISTEMI ENERGETICI 1 Obiettivi della lezione 1) Capire come l organismo converta il cibo che ingeriamo in ATP per fornire ai muscoli l energia che essi necessitano per contrarsi. 2) Esaminare
METABOLISMO E SISTEMI ENERGETICI 1 Obiettivi della lezione 1) Capire come l organismo converta il cibo che ingeriamo in ATP per fornire ai muscoli l energia che essi necessitano per contrarsi. 2) Esaminare
BIOLOGIA GENERALE 22-24 ottobre 2007
 Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE 22-24 ottobre 2007 Facoltà di Psicologia Tecniche di Psicologia Generale e Sperimentale Alessandro Massolo Dip.
Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE 22-24 ottobre 2007 Facoltà di Psicologia Tecniche di Psicologia Generale e Sperimentale Alessandro Massolo Dip.
Il mantenimento dell omeostasi cellulare dipende dai sistemi che permettono lo scambio di molecole tra citoplasma e liquido
 Il mantenimento dell omeostasi cellulare dipende dai sistemi che permettono lo scambio di molecole tra citoplasma e liquido extracellulare e dalla loro regolazione. Membrana cellulare Ogni cellula presenta
Il mantenimento dell omeostasi cellulare dipende dai sistemi che permettono lo scambio di molecole tra citoplasma e liquido extracellulare e dalla loro regolazione. Membrana cellulare Ogni cellula presenta
GENERALITA SUL METABOLISMO. DIGESTIONE e ASSORBIMENTO dei CARBOIDRATI GLICOLISI
 GENERALITA SUL METABOLISMO DIGESTIONE e ASSORBIMENTO dei CARBOIDRATI GLICOLISI ENERGIA per Ø gradiente elettrochimico (Na + /K + ATPasi) Ø processi biosintetici (es. sintesi proteica) Ø trasporto transmembrana
GENERALITA SUL METABOLISMO DIGESTIONE e ASSORBIMENTO dei CARBOIDRATI GLICOLISI ENERGIA per Ø gradiente elettrochimico (Na + /K + ATPasi) Ø processi biosintetici (es. sintesi proteica) Ø trasporto transmembrana
Nota dell editore Presentazione
 00PrPag 3-08-2007 11:42 Pagina V Autori Nota dell editore Presentazione XI XIII XV Parte I Chimica 1 Struttura dell atomo 3 Teorie atomiche 3 Costituenti dell atomo 4 Numeri quantici 5 Tipi di orbitali
00PrPag 3-08-2007 11:42 Pagina V Autori Nota dell editore Presentazione XI XIII XV Parte I Chimica 1 Struttura dell atomo 3 Teorie atomiche 3 Costituenti dell atomo 4 Numeri quantici 5 Tipi di orbitali
METABOLISMO DEI LIPIDI
 METABOLISMO DEI LIPIDI Generalità I lipidi alimentari, per poter essere assorbiti dall organismo umano, devono essere preventivamente digeriti (ad eccezione del colesterolo), cioè, trasformati in molecole
METABOLISMO DEI LIPIDI Generalità I lipidi alimentari, per poter essere assorbiti dall organismo umano, devono essere preventivamente digeriti (ad eccezione del colesterolo), cioè, trasformati in molecole
SECREZIONE DI INSULINA:
 SECREZIONE DI INSULINA: O Ca ++ VGCC K-ATP GLUT2 Ca ++ K + O Ca ++ HK I P GK ATP O ADP piruvato acidi grassi corpi chetonici aminoacidi secretina glucagone incretine: colecistochinina (CCK) peptide inibitore
SECREZIONE DI INSULINA: O Ca ++ VGCC K-ATP GLUT2 Ca ++ K + O Ca ++ HK I P GK ATP O ADP piruvato acidi grassi corpi chetonici aminoacidi secretina glucagone incretine: colecistochinina (CCK) peptide inibitore
unità C2. Le trasformazioni energetiche nelle cellule
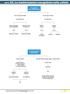 unità 2. Le trasformazioni energetiche nelle cellule Il trasporto nelle cellule avviene senza consumo di energia con consumo di energia trasporto passivo trasporto attivo attraverso il doppio strato fosfolipidico
unità 2. Le trasformazioni energetiche nelle cellule Il trasporto nelle cellule avviene senza consumo di energia con consumo di energia trasporto passivo trasporto attivo attraverso il doppio strato fosfolipidico
Metabolismo dei composti azotati: aminoacidi e nucleotidi
 Metabolismo dei composti azotati: aminoacidi e nucleotidi Metabolismo degli aminoacidi I composti azotati L azoto contenuto nella cellula è presente soprattutto negli AMINOACIDI delle proteine e nelle
Metabolismo dei composti azotati: aminoacidi e nucleotidi Metabolismo degli aminoacidi I composti azotati L azoto contenuto nella cellula è presente soprattutto negli AMINOACIDI delle proteine e nelle
Βeta ossidazione degli acidi grassi BETA OSSIDAZIONE DEGLI ACIDI GRASSI 13/12/2013 SEMINARIO. Acidi grassi (2)
 Acidi grassi (1) Mitocondri SEMINARIO BETA OSSIDAZIONE DEGLI ACIDI GRASSI Sono le principali fonti di energia per alcuni tessuti (es. muscolo cardiaco). Si genera molto più energia dall ossidazione degli
Acidi grassi (1) Mitocondri SEMINARIO BETA OSSIDAZIONE DEGLI ACIDI GRASSI Sono le principali fonti di energia per alcuni tessuti (es. muscolo cardiaco). Si genera molto più energia dall ossidazione degli
Mediatore chimico. Recettore. Trasduzione del segnale. Risposta della cellula
 Mediatore chimico Recettore Trasduzione del segnale Risposta della cellula I mediatori chimici sono prodotti da cellule specializzate e sono diffusi nell organismo da apparati di distribuzione Sistemi
Mediatore chimico Recettore Trasduzione del segnale Risposta della cellula I mediatori chimici sono prodotti da cellule specializzate e sono diffusi nell organismo da apparati di distribuzione Sistemi
ESERCITAZIONI DI BIOCHIMICA
 ESERCITAZIONI DI BIOCHIMICA La denaturazione delle proteine riguarda la struttura terziaria. La proteina attiva di solito è in forma globulare. La sequenza amminoacidica è responsabile dell assetto tridimensionale
ESERCITAZIONI DI BIOCHIMICA La denaturazione delle proteine riguarda la struttura terziaria. La proteina attiva di solito è in forma globulare. La sequenza amminoacidica è responsabile dell assetto tridimensionale
CELLULE EUCARIOTICHE
 CELLULE EUCARIOTICHE Le cellule eucariotiche sono di maggiori dimensioni, rispetto a quelle procariotiche (almeno 10 volte più grandi) Oltre a: membrana plasmatica, citoplasma, DNA e ribosomi (comuni a
CELLULE EUCARIOTICHE Le cellule eucariotiche sono di maggiori dimensioni, rispetto a quelle procariotiche (almeno 10 volte più grandi) Oltre a: membrana plasmatica, citoplasma, DNA e ribosomi (comuni a
A livello della loro struttura chimica, come i grassi, anche i carboidrati sono composti ternari, formati cioè da tre molecole:
 I carboidrati costituiscono la fonte di energia principale per lo svolgimento di tutte le funzioni organiche (mantenimento della temperatura corporea, battito cardiaco, funzioni cerebrali, digestione,
I carboidrati costituiscono la fonte di energia principale per lo svolgimento di tutte le funzioni organiche (mantenimento della temperatura corporea, battito cardiaco, funzioni cerebrali, digestione,
La digestione degli alimenti
 La digestione degli alimenti Le sostanze alimentari complesse (lipidi, glucidi, protidi) che vengono introdotte nell organismo, devono subire delle profonde modificazioni che le trasformano in sostanze
La digestione degli alimenti Le sostanze alimentari complesse (lipidi, glucidi, protidi) che vengono introdotte nell organismo, devono subire delle profonde modificazioni che le trasformano in sostanze
Valitutti, Taddei, Kreuzer, Massey, Sadava, Hills, Heller, Berenbaum
 Dal carbonio agli OGM VERSO L UNIVERSITÀ Le domande sono tratte dalle prove di ammissione emesse annualmente dal Ministero dell Istruzione, dell Università e della Ricerca (MIUR) e le soluzioni sono evidenziate
Dal carbonio agli OGM VERSO L UNIVERSITÀ Le domande sono tratte dalle prove di ammissione emesse annualmente dal Ministero dell Istruzione, dell Università e della Ricerca (MIUR) e le soluzioni sono evidenziate
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 24
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 24 Una panoramica del metabolismo Concetti chiave: Organismi diversi utilizzano strategie differenti per catturare l'energia
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 24 Una panoramica del metabolismo Concetti chiave: Organismi diversi utilizzano strategie differenti per catturare l'energia
I carboidrati La maggior parte dei carboidrati, detti anche saccaridi o glucidi, è riconducibile alla formula chimica generale C n (H 2 O) n.
 MODULO 3 IL METABOLISMO GLUCIDICO RICHIAMI SULLA CHIMICA DEI CARBOIDRATI Introduzione I carboidrati sono macromolecole organiche molto abbondanti in natura. Essi svolgono funzioni metaboliche e strutturali
MODULO 3 IL METABOLISMO GLUCIDICO RICHIAMI SULLA CHIMICA DEI CARBOIDRATI Introduzione I carboidrati sono macromolecole organiche molto abbondanti in natura. Essi svolgono funzioni metaboliche e strutturali
ENZIMI CINETICA ENZIMATICA
 ENZIMI PERCHE UNA REAZIONE AVVENGA, SI DEVONO SODDISFARE TRE CONDIZIONI I SUBSTRATI DEVONO ENTRARE IN COLLISIONE LA COLLISIONE DEVE AVVENIRE CON ORIENTAMENTO CORRETTO I REAGENTI DEVONO AVERE ENERGIA SUFFICIENTE
ENZIMI PERCHE UNA REAZIONE AVVENGA, SI DEVONO SODDISFARE TRE CONDIZIONI I SUBSTRATI DEVONO ENTRARE IN COLLISIONE LA COLLISIONE DEVE AVVENIRE CON ORIENTAMENTO CORRETTO I REAGENTI DEVONO AVERE ENERGIA SUFFICIENTE
scaricato da www.sunhope.it
 Recettori a tirosina chinasi I recettori a tirosina chinasi presentano vari domini Una regione di legame (extracellulare) Una regione transmembrana Una coda intracellulare con numerose tirosine scaricato
Recettori a tirosina chinasi I recettori a tirosina chinasi presentano vari domini Una regione di legame (extracellulare) Una regione transmembrana Una coda intracellulare con numerose tirosine scaricato
 forme diabetiche Diabete di tipo I o magro o giovanile (IDDM): carenza primaria di insulina, più frequente nei giovani e nei bambini. Il deficit insulinico consegue (per predisposizione ereditaria o per
forme diabetiche Diabete di tipo I o magro o giovanile (IDDM): carenza primaria di insulina, più frequente nei giovani e nei bambini. Il deficit insulinico consegue (per predisposizione ereditaria o per
Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I
 Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I I TRASPORTI ATTRAVERSO MEMBRANE BIOLOGICHE Movimenti di piccoli soluti attraverso le membrane 2 categorie generali Trasporto
Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I I TRASPORTI ATTRAVERSO MEMBRANE BIOLOGICHE Movimenti di piccoli soluti attraverso le membrane 2 categorie generali Trasporto
CATENA RESPIRATORIA (CR) FOSFORILAZIONE OSSIDATIVA (FO) scaricato da www.sunhope.it
 CATENA RESPIRATORIA (CR) FOSFORILAZIONE OSSIDATIVA (FO) - Decarb. ossid. piruvato - β-ossidazione acidi grassi - Vie ossidative aa - Ciclo di Krebs avvengono tutte nella matrice mitocondriale In tutte
CATENA RESPIRATORIA (CR) FOSFORILAZIONE OSSIDATIVA (FO) - Decarb. ossid. piruvato - β-ossidazione acidi grassi - Vie ossidative aa - Ciclo di Krebs avvengono tutte nella matrice mitocondriale In tutte
http://sds.coniliguria.it 1
 Aspetti metabolici dell esercizio fisico Genova 22 gennaio 2011 A cura di Attilio TRAVERSO http://sds.coniliguria.it 1 L allenamento produce modificazioni fisiologiche (adattamenti) in quasi tutti i sistemi
Aspetti metabolici dell esercizio fisico Genova 22 gennaio 2011 A cura di Attilio TRAVERSO http://sds.coniliguria.it 1 L allenamento produce modificazioni fisiologiche (adattamenti) in quasi tutti i sistemi
STOMACO. A livello dello stomaco si verifica un limitato assorbimento di alimenti, soprattutto di acqua, di alcuni sali, di alcool e di alcuni farmaci
 STOMACO Nel loro insieme i secreti delle ghiandole formano il succo gastrico, fortemente acido (ph circa 1). Nella mucosa gastrica sono disposte tra le ghiandole cellule mucose, che producono un muco che
STOMACO Nel loro insieme i secreti delle ghiandole formano il succo gastrico, fortemente acido (ph circa 1). Nella mucosa gastrica sono disposte tra le ghiandole cellule mucose, che producono un muco che
Biosintesi dei triacilgliceroli
 Biosintesi dei triacilgliceroli Destino della maggior parte degli acidi grassi sintetizzati o ingeriti: Ø triacilgliceroli (riserva) Ø fosfolipidi (membrane) in base alle necessità metaboliche I triacilgliceroli
Biosintesi dei triacilgliceroli Destino della maggior parte degli acidi grassi sintetizzati o ingeriti: Ø triacilgliceroli (riserva) Ø fosfolipidi (membrane) in base alle necessità metaboliche I triacilgliceroli
Legami chimici. Covalente. Legami deboli
 Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
Integrali (transmembrana), si estendono attraverso l intera membrana. Classificate in famiglie a seconda del numero di segmenti transmembrana.
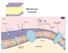 Membrana cellulare Proteine inserite nella membrana cellulare: Integrali (transmembrana), si estendono attraverso l intera membrana. Classificate in famiglie a seconda del numero di segmenti transmembrana.
Membrana cellulare Proteine inserite nella membrana cellulare: Integrali (transmembrana), si estendono attraverso l intera membrana. Classificate in famiglie a seconda del numero di segmenti transmembrana.
METABOLISMO LIPIDICO. Gli ac. grassi sono ossidati o incorporati in trigliceridi di riserva. Lipidi introdotti con gli alimenti.
 METABOLISMO LIPIDICO cistifellea Lipidi introdotti con gli alimenti Gli ac. grassi sono ossidati o incorporati in trigliceridi di riserva inestino I lipidi sono emulsionati dai sali biliari e resi accessibili
METABOLISMO LIPIDICO cistifellea Lipidi introdotti con gli alimenti Gli ac. grassi sono ossidati o incorporati in trigliceridi di riserva inestino I lipidi sono emulsionati dai sali biliari e resi accessibili
LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI PROTEINE. sono ACIDI NUCLEICI. molecole complesse = POLIMERI. formate dall'unione di
 LE BIOMOLECOLE LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI LE BIOMOLECOLE sono LIPIDI PROTEINE ACIDI NUCLEICI molecole complesse = POLIMERI formate dall'unione di molecole semplici = MONOMERI
LE BIOMOLECOLE LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI LE BIOMOLECOLE sono LIPIDI PROTEINE ACIDI NUCLEICI molecole complesse = POLIMERI formate dall'unione di molecole semplici = MONOMERI
Ruolo metabolico delle flavine
 Ruolo metabolico delle flavine Deidrogenasi flaviniche che trasferiscono 2 elettroni Acil CoA deidrogenasi (beta ossidazione acidi grassi) Diidrolipoildeidrogenasi (complessi piruvato dh etc.) Glutatione
Ruolo metabolico delle flavine Deidrogenasi flaviniche che trasferiscono 2 elettroni Acil CoA deidrogenasi (beta ossidazione acidi grassi) Diidrolipoildeidrogenasi (complessi piruvato dh etc.) Glutatione
METABOLISMO DEL GLICOGENO
 METABOLISMO DEL GLICOGENO 1 2 DESTINI DEL GLUCOSIO 6-FOSFATO 3 RAPPRESENTAZIONE SCHEMATICA DEL METABOLISMO DEL GLUCOSIO 4 Glucosio-6-fosfatasi Omeostasi del glicogeno Nell'organismo animale, il glicogeno
METABOLISMO DEL GLICOGENO 1 2 DESTINI DEL GLUCOSIO 6-FOSFATO 3 RAPPRESENTAZIONE SCHEMATICA DEL METABOLISMO DEL GLUCOSIO 4 Glucosio-6-fosfatasi Omeostasi del glicogeno Nell'organismo animale, il glicogeno
Prof. Maria Nicola GADALETA
 Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Fosforilazione ossidativa
 Fosforilazione ossidativa La fosforilazione ossidativa rappresenta il culmine del metabolismo energetico negli organismi aerobi E costituita da due fenomeni strettamente accoppiati: 1. I coenzimi ridotti
Fosforilazione ossidativa La fosforilazione ossidativa rappresenta il culmine del metabolismo energetico negli organismi aerobi E costituita da due fenomeni strettamente accoppiati: 1. I coenzimi ridotti
Bioenergetica & metabolismo (1)
 Bioenergetica & metabolismo (1) Tutte le vie metaboliche sono interconnesse (come le linee di una grande metropolitana) La maggior parte degli organismi viventi hanno vie metaboliche molto simili 1 Vie
Bioenergetica & metabolismo (1) Tutte le vie metaboliche sono interconnesse (come le linee di una grande metropolitana) La maggior parte degli organismi viventi hanno vie metaboliche molto simili 1 Vie
1. Omogenizzazione meccanica del cibo 2. Secrezione di elettroliti 3. Secrezione di enzimi digestivi
 La dieta deve contenere, oltre all acqua, combustibile metabolico, proteine per la crescita e il ricambio delle proteine tissutali, fibre per far massa nel lume intestinale, minerali essenziali per specifiche
La dieta deve contenere, oltre all acqua, combustibile metabolico, proteine per la crescita e il ricambio delle proteine tissutali, fibre per far massa nel lume intestinale, minerali essenziali per specifiche
Le Biomolecole I parte. Lezioni d'autore di Giorgio Benedetti
 Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
PROTEINE E TRASPORTO TRANSMEMBRANALE
 PROTEINE E TRASPORTO TRANSMEMBRANALE Il glucoso ed il galattoso, gli aminoacidi e gli ioni utilizzano apposite proteine per attraversare la MP. L'H 2 O può attraversare con difficoltà lo strato lipidico
PROTEINE E TRASPORTO TRANSMEMBRANALE Il glucoso ed il galattoso, gli aminoacidi e gli ioni utilizzano apposite proteine per attraversare la MP. L'H 2 O può attraversare con difficoltà lo strato lipidico
I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici
 I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici La seta della tela di ragno è un insieme di macromolecole, dette proteine. Sono le caratteristiche fisico-chimiche di queste
I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici La seta della tela di ragno è un insieme di macromolecole, dette proteine. Sono le caratteristiche fisico-chimiche di queste
Biologia Molecolare della Cellula 08 7: Regolazione ormonale del metabolismo del glicogeno e della glicolisi Desensitizzazione
 Biologia Molecolare della Cellula 08 7: Regolazione ormonale del metabolismo del glicogeno e della glicolisi Desensitizzazione camp Proteina-CHINASI camp DIPENDENTE (PKA) Proteine target : ε metabolici
Biologia Molecolare della Cellula 08 7: Regolazione ormonale del metabolismo del glicogeno e della glicolisi Desensitizzazione camp Proteina-CHINASI camp DIPENDENTE (PKA) Proteine target : ε metabolici
Indice. Prefazione. PARTE I - Biochimica propedeutica. Capitolo 1 Concetti generali di chimica di Veronica Carnicelli 1
 Indice Prefazione V PARTE I - Biochimica propedeutica Capitolo 1 Concetti generali di chimica di Veronica Carnicelli 1 1.1 L atomo e gli elementi 1 1.1.1 L atomo 1 1.1.2 Gli elementi e la tavola periodica
Indice Prefazione V PARTE I - Biochimica propedeutica Capitolo 1 Concetti generali di chimica di Veronica Carnicelli 1 1.1 L atomo e gli elementi 1 1.1.1 L atomo 1 1.1.2 Gli elementi e la tavola periodica
Catena di Trasporto degli elettroni
 Chimica Biologica A.A. 2010-2011 Catena di Trasporto degli elettroni Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Respirazione - il catabolismo di tutti i combustibili
Chimica Biologica A.A. 2010-2011 Catena di Trasporto degli elettroni Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Respirazione - il catabolismo di tutti i combustibili
Carboidrati puri : zucchero e amido nei cibi, cellulosa nel legno, carta e cotone = C 6 O 6 (H 2 O) 6
 Carboidrati Carboidrati puri : zucchero e amido nei cibi, cellulosa nel legno, carta e cotone Glucosio Carboidrati modificati: membrane cellulari, acidi nucleici, Da carbonio idrato: glucosio= C 6 H 12
Carboidrati Carboidrati puri : zucchero e amido nei cibi, cellulosa nel legno, carta e cotone Glucosio Carboidrati modificati: membrane cellulari, acidi nucleici, Da carbonio idrato: glucosio= C 6 H 12
Il Metabolismo Energetico 1. Bilancio Quantitativo tra Apporto di Energia e Dispendio Energetico
 Il Metabolismo Energetico 1. Bilancio Quantitativo tra Apporto di Energia e Dispendio Energetico Prof. Carlo Capelli Fisiologia Facoltà di Scienze Motorie, Università degli Studi Verona Obiettivi Energia
Il Metabolismo Energetico 1. Bilancio Quantitativo tra Apporto di Energia e Dispendio Energetico Prof. Carlo Capelli Fisiologia Facoltà di Scienze Motorie, Università degli Studi Verona Obiettivi Energia
Le due porzioni del pancreas, esocrino ed endocrino, sono anatomicamente e funzionalmente diverse.
 ENDOCRINOLOGIA E NUTRIZIONE UMANA LEZIONE 7 PANCREAS Le due porzioni del pancreas, esocrino ed endocrino, sono anatomicamente e funzionalmente diverse. Isole del Langherans Contengono da poche centinaia
ENDOCRINOLOGIA E NUTRIZIONE UMANA LEZIONE 7 PANCREAS Le due porzioni del pancreas, esocrino ed endocrino, sono anatomicamente e funzionalmente diverse. Isole del Langherans Contengono da poche centinaia
ALIMENTAZIONE NELL UOMO
 ALIMENTAZIONE NELL UOMO Alimentazione e Nutrizione Corpo umano come macchina chimica che utilizza l energia chimica degli alimenti (quando si spezzano i legami chimici tra gli atomi che formano le macromolecole
ALIMENTAZIONE NELL UOMO Alimentazione e Nutrizione Corpo umano come macchina chimica che utilizza l energia chimica degli alimenti (quando si spezzano i legami chimici tra gli atomi che formano le macromolecole
IL DESTINO METABOLICO DEL GLUCOSIO E LA SUA RILEVANZA NEL DIABETE MELLITO DI TIPO 2
 IL DESTINO METABOLICO DEL GLUCOSIO E LA SUA RILEVANZA NEL DIABETE MELLITO DI TIPO 2 Ambulatorio Malattie Dismetaboliche 2142 soggetti OGTT Ambulatorio Malattie Dismetaboliche 2142 soggetti OGTT 1069 NGT
IL DESTINO METABOLICO DEL GLUCOSIO E LA SUA RILEVANZA NEL DIABETE MELLITO DI TIPO 2 Ambulatorio Malattie Dismetaboliche 2142 soggetti OGTT Ambulatorio Malattie Dismetaboliche 2142 soggetti OGTT 1069 NGT
TIAMINA (vitamina B1, aneurina)
 TIAMINA (vitamina B1, aneurina) Fonti alimentari: cereali integrali (germe e crusca), carne (maiale), lievito di birra, legumi Abbondanza nell organismo umano : 30-100 mg RDA (assunzione giornaliera di
TIAMINA (vitamina B1, aneurina) Fonti alimentari: cereali integrali (germe e crusca), carne (maiale), lievito di birra, legumi Abbondanza nell organismo umano : 30-100 mg RDA (assunzione giornaliera di
SOLUZIONI DEGLI ESERCIZI
 Niccolò Taddei - Biochimica Capitolo 9 METABOLISMO TERMINALE E PRODUZIONE DI ENERGIA 1 Il ciclo dell acido citrico è definito anche ciclo di Krebs, dal nome di uno dei suoi scopritori, o ciclo degli acidi
Niccolò Taddei - Biochimica Capitolo 9 METABOLISMO TERMINALE E PRODUZIONE DI ENERGIA 1 Il ciclo dell acido citrico è definito anche ciclo di Krebs, dal nome di uno dei suoi scopritori, o ciclo degli acidi
La fotosintesi: energia dal Sole
 La fotosintesi: energia dal Sole Gli organismi fotosintetici usano la luce del Sole, l acqua del suolo e il CO 2 dell atmosfera per produrre composti organici e liberare O 2 grazie alla fotosintesi. Sadava
La fotosintesi: energia dal Sole Gli organismi fotosintetici usano la luce del Sole, l acqua del suolo e il CO 2 dell atmosfera per produrre composti organici e liberare O 2 grazie alla fotosintesi. Sadava
a-amilasi salivare e pancreatica destrine lattasi maltasi oligosaccaridasi saccarasi superficie luminale degli enterociti
 Metabolismo glucidico Digestione degli zuccheri a-amilasi salivare e pancreatica maltotrioso destrina maltosio glucosio lattosio amido saccarosio maltosio maltotrioso destrine lattasi maltasi oligosaccaridasi
Metabolismo glucidico Digestione degli zuccheri a-amilasi salivare e pancreatica maltotrioso destrina maltosio glucosio lattosio amido saccarosio maltosio maltotrioso destrine lattasi maltasi oligosaccaridasi
TRASPORTO: qualunque tipo di passaggio di sostanze attraverso la membrana cellulare.
 Membrana citoplasmatica èsedediscambiodi materia, energia e informazione con l ambiente esterno TRASPORTO: qualunque tipo di passaggio di sostanze attraverso la membrana cellulare. Scaricato da www.sunhope.it
Membrana citoplasmatica èsedediscambiodi materia, energia e informazione con l ambiente esterno TRASPORTO: qualunque tipo di passaggio di sostanze attraverso la membrana cellulare. Scaricato da www.sunhope.it
Funzioni della membrana plasmatica
 TRASPORTO M.P. -Omeostasi cellulare Funzioni della membrana plasmatica Mantenimento della conc. intracell. di ioni e molecole entro valori corretti Scambi interno - esterno Non c è consumo E Consumo E
TRASPORTO M.P. -Omeostasi cellulare Funzioni della membrana plasmatica Mantenimento della conc. intracell. di ioni e molecole entro valori corretti Scambi interno - esterno Non c è consumo E Consumo E
2. Fisiologia Cellulare Diffusione, Trasporto, Osmosi
 2. Fisiologia Cellulare Diffusione, Trasporto, Osmosi Prof. Carlo Capelli Fisiologia Laurea in Scienze delle attività motorie e sportive Università di Verona Obiettivi Diffusione semplice e mediata da
2. Fisiologia Cellulare Diffusione, Trasporto, Osmosi Prof. Carlo Capelli Fisiologia Laurea in Scienze delle attività motorie e sportive Università di Verona Obiettivi Diffusione semplice e mediata da
I L I P I D I. Lipidi complessi: fosfolipidi e glicolipidi; sono formati da CHO e altre sostanze.
 I L I P I D I ASPETTI GENERALI I Lipidi o grassi sono la riserva energetica del nostro organismo; nel corpo umano costituiscono mediamente il 17% del peso corporeo dove formano il tessuto adiposo. In generale
I L I P I D I ASPETTI GENERALI I Lipidi o grassi sono la riserva energetica del nostro organismo; nel corpo umano costituiscono mediamente il 17% del peso corporeo dove formano il tessuto adiposo. In generale
Digestione delle proteine: 6 fasi
 orletto a spazzola Digestione delle proteine: 6 fasi 1. Idrolisi gastrica del legame peptidico 2. Digestione a peptidi più piccoli da parte delle proteasi pancreatiche nel lume dell intestino tenue 3.
orletto a spazzola Digestione delle proteine: 6 fasi 1. Idrolisi gastrica del legame peptidico 2. Digestione a peptidi più piccoli da parte delle proteasi pancreatiche nel lume dell intestino tenue 3.
Pur rappresentando il 60-65% delle calorie della dieta sono contenuti nel corpo solo per l 1% 60-65% 1%
 CARBOIDRATI 1 GLUCIDI Il termine deriva dal greco, dolce, dato che i più semplici hanno sapore dolce; vengono anche chiamati carboidrati Sono i costituenti più importanti dei vegetali che li sintetizzano
CARBOIDRATI 1 GLUCIDI Il termine deriva dal greco, dolce, dato che i più semplici hanno sapore dolce; vengono anche chiamati carboidrati Sono i costituenti più importanti dei vegetali che li sintetizzano
Metabolismo degli Ammino Acidi
 Metabolismo degli Ammino Acidi (La proteina stimola la secrezione della gastrina che stimola la secrezione di l e pepsinogeno) R 1 - R 2 - N 3 Transaminasi R 1 - R 2 - N 3 Transaminasi (amminotransferasi)
Metabolismo degli Ammino Acidi (La proteina stimola la secrezione della gastrina che stimola la secrezione di l e pepsinogeno) R 1 - R 2 - N 3 Transaminasi R 1 - R 2 - N 3 Transaminasi (amminotransferasi)
OBESITA. 11 Aprile 2013
 OBESITA 11 Aprile 2013 L obesità è una patologia cronica caratterizzata dall eccessivo accumulo di tessuto adiposo nell organismo ed è causata da fattori ereditari e non ereditari che determinano un introito
OBESITA 11 Aprile 2013 L obesità è una patologia cronica caratterizzata dall eccessivo accumulo di tessuto adiposo nell organismo ed è causata da fattori ereditari e non ereditari che determinano un introito
OMEOSTASI DELLA TEMPERATURA CORPOREA
 OMEOSTASI DELLA TEMPERATURA CORPOREA Ruolo fisiologico del calcio Omeostasi del calcio ASSORBIMENTO INTESTINALE DEL CALCIO OMEOSTASI GLICEMICA Il livello normale di glicemia? 90 mg/100 ml Pancreas
OMEOSTASI DELLA TEMPERATURA CORPOREA Ruolo fisiologico del calcio Omeostasi del calcio ASSORBIMENTO INTESTINALE DEL CALCIO OMEOSTASI GLICEMICA Il livello normale di glicemia? 90 mg/100 ml Pancreas
