Ruolo biologico degli elementi del I e II gruppo
|
|
|
- Daniella Gina Mantovani
- 8 anni fa
- Visualizzazioni
Transcript
1 Ruolo biologico degli elementi del I e II gruppo 1. Introduzione 2. Trasporto:pompa sodio/potassio 3. Ruolo del potassio: telomeri eacidi nucleici 4. Ruolo biologico del potassio 5. Ruolo del calcio negli esseri viventi
2 Introduzione 4 elementi (Na, K, Mg e Ca) hanno un ruolo importante negli esseri viventi, nei quali si trovano in proporzione relativamente alta. La solubilità dei loro sali, unitamente alla loro abbondanza naturale, sono all origine dell alta biodisponibilità Proprietà Na + K + Mg 2+ Ca 2+ Raggio ionico (Å) Raggio dello ione idratato (Å) Densità di carica/raggio ionico H idrataz. (kj/mol) Numero di coordinazione La diminuzione del potere polarizzante di Ca 2+ rispetto a Mg 2+ conferisce allo ione Ca 2+ un carattere di acido di Lewis più debole rispetto a Mg 2+
3 Esempi di distribuzione intra- ed extracellulare (in mmol/kg) Il ruolo di ognuno dei 4 ioni negli esseri viventi è molto specifico e si basa sulle piccole differenze delle proprietà periodiche Sotto viene riportata la distribuzione e le concentrazioni di equilibrio richieste per ogni elemento per un funzionamento biologico corretto in 2 specie molto diverse Localizzazione Na + K + Mg 2+ Ca 2+ Eritrociti umani (intracellulare) Plasma sanguigno (extracellulare) Neuroni di calamaro (intracellulare) Sistema nervoso del calamaro (extracellulare) Na + e K + sono molto più abbondanti; Na + e Ca 2+ sono essenzialmente extracellulari mentre K + e Mg 2+ sono intracellulari
4 Generazione e uso di gradienti di concentrazione di ioni Gradienti di ioni attraverso le membrane vengono usati per immagazzinare energia e informazione. Gli ioni di particolare importanza sono Na +, K +, Ca 2+ e H +, e i loro gradienti di concentrazione sono di fondamentale importanza nella bioenergetica e nelle funzioni dei sistemi nervosi. Due tipi di proteine sono essenziali per il funzionamento di questi sistemi: quelle implicate nelle pompe ioniche e quelle che costituiscono i canali attraverso i quali fluiscono gli ioni. Il meccanismo che la natura impiega per mantenere le concentrazioni relative di Na + e K + all interno e all esterno della membrana cellulare si basa sulla funzione di una proteina di membrana con funzione di ATP-asa L enzima, chiamato ATP-asa scambiatore di Na +,K + (Na +,K + -ATP-asa) necessita di entrambi gli ioni e inoltre Mg 2+ il quale agisce da cofattore nelle reazioni che richiedono ATP. L enzima accoppia l idrolisi di ATP al movimento simultaneo di Na + e K + contro i loro gradienti di concentrazione, catalizzando la reazione: 3 Na + in + 2 K + out + ATP + H 2 O 3 Na Na + out out + 2 K + in in + ADP + P i
5 Rappresentazione schematica della pompa Na + /K + La proteina contiene 2 subunità α (110 kda per una) e 2 subunità β (55 kda per una). Quelle più piccole sono glucoproteine e il complesso ha le caratteristiche di una proteina integrale di membrana Durante il trasporto la subunità più grande è fosforilata e defosforilata ciclicamente Il modello attuale suppone che che l enzima oscilli fra 2 conformazioni: la forma defosforilata (conf. I) che possiede una cavità con una dimensione adeguata per alloggiare Na +, manifesta una maggiore affinità per questo ione rispetto a K +. La forma defosforilata (conf. II) ha la dimensione della cavità tale da generare una maggiore affinità per il K + rispetto a Na + Questo cambiamento strutturale permette all enzima di realizzare un processo di trasporto nel quale Na + si sposta dall interno all esterno mentre K + entra all interno della cellula.
6 Potenziale di membrana Questo meccanismo, noto come pompa Na/K, è quello che rende possibile il mantenimento continuo delle concentrazioni necessarie, dal punto di vista biologico, di entrambi gli ioni. E da notare che per ogni molecola di ATP idrolizzata escono 3 ioni Na + dalla cellula e entrano solo 2 ioni K + e questo determina un aumento delle cariche positive esterne. Questo processo elettrogenico è parte del meccanismo di mantenimento del potenziale di membrana che può essere considerato come la somma dei potenziali dovuti a ogni ione derivanti dalle differenze di concentrazioni ioniche attraverso la membrana. Le differenze di concentrazione determinano i potenziali in accordo con la legge di Nerst: V = (RT/zF)ln(C est. /C int. ) Considerando la composizione ionica esterna e interna alla cellula si possono calcolare i potenziali di equilibrio di ogni singolo ione.
7 L interazione di Na + con la parte interna della membrana facilita la fosforilazione di uno specifico residuo di acido aspartico dell enzima. Questo processo induce un cambiamento conformazionale che determina il trasporto di 3 ioni Na + attraverso la membrana. Successivamente, l interazione di legame fra K + sulla membrana esterna catalizza la defosforilazione dell enzima, seguita da un inverso cambiamento conformazionale che trasporta i due ioni K + nella cellula. Il ciclo si ripete circa 100 volte al secondo. In contrasto, i canali ionici sono proteine che sono capaci di trasportare ioni/sec. Questa elevata velocità di trasporto ionico è essenziale per segnalare rapidamente eventi quali quelli che avvengono nel sistema nervoso.
8 Ruolo biologico del potassio Le principali funzioni biologiche di Na + sono associate ai potenziali di membrana, mentre la sua chimica quale attivatore di enzimi è molto limitata. Il potassio, invece, oltre alla importante funzione di stabilizzatore delle strutture degli acidi nucleici, è anche necessario alla attivazione di un grande numero di enzimi fra i quali: adenilato ciclasi, aspartato chinasi, DNA polimerasi, serina deaminasi, triptofano sintasi, piruvato chinasi, aldeide deidrogenasi, Na + /K + -ATPase. Dei metalli alcalini, solo K + è stato dimostrato agire come cofattore stechiometrico (in particolare, nella piruvato chinasi, discussa più avanti in associazione con lo ione Mg 2+ ). La bassa densità di carica di K + preclude il suo uso come acido di Lewis e così il suo ruolo consiste nell orientare il piruvato nel sito attivo legandosi a ponte fra l enzima e il substrato. Lo ione K + può interagire con l ossigeno dei gruppi fosfato delle catene di nucleotidi e con gli ossigeni esterni delle basi puriniche e pirimidiniche. Per le sue dimensioni può attorniarsi fino ad un massimo di 8 atomi di O situati ai vertici di un cubo. E stata provata l esistenza di ioni K + nei telomeri che sono sequenze di DNA che si osservano agli estremi dei cromosomi e sono essenziali per la loro stabilità. Il DNA telomerico consiste di semplici sequenze ripetute in tandem (es., AGGTT, nell uomo): un filamento è normalmente ricco in G, mentre l altro è ricco in C.
9 In questi segmenti di DNA telomerico è stata identificata la presenza di DNA a filo quadruplo (quartetti) che presenta un appaiamento di basi noto con il nome di quartetto di guanina Questi quartetti di guanina si distribuiscono in piani paralleli (che terminano con timine) e orientano gli ossigeni dei gruppi carbonilici in modo tale che ogni 2 piani di quartetti di guanina si colloca uno ione K +. Questa struttura ha un buco formato dagli atomi di O (in posizione 6) delle otto guanine perfettamente calibrato per ospitare lo ione potassio.
10 Struttura dei telomeri La presenza dello ione K + che compensa la forza repulsiva fra gli ossigeni e contribuisce alla stabilizzazione di un assemblaggio strutturale che sarebbe assolutamente precario in sua assenza Questa funzione non può essere svolta dallo ione Na + date le sue dimensioni più piccole rispetto alla cavità delimitata dagli ossigeni esterni delle 8 guanine [W.I. Sundquist et al. Nature 342 (1989 )825] Analogamente, è stato provato che lo ione idratato [ K(H 2 O) 6 ] + contribuisce alla stabilizzazione degli acidi nucleici (DNA e RNA) minimizzando la repulsione risultante dalla carica negativa dei gruppi fosfato orientati verso l esterno nella catena dei nucleotidi Questa funzione è svolta anche dallo ione [Mg(H 2 O) 6 ] 2+, in particolare per la forma Z del DNA [R.V. Gessner et al., Biochemistry 24 (1985) 237]
11 Ruolo biologico del magnesio Il carattere di acido di Lewis di Mg 2+ e il suo potere polarizzante nei confronti di molecole di acqua o ossigeni di gruppi fosfato o esteri fosforici, unitamente alla sua biodisponibilità, lo rende indispensabile nella catalisi di molti processi biochimici. Un esempio di processo in cui l intervento di Mg 2+ è essenziale è il trasferimento reversibile del gruppo fosfato dal fosfoenolpiruvato all ADP, producendo piruvato e ATP. La reazione è catalizzata dalla piruvato chinasi e richiede oltre a Mg 2+ anche lo ione K +, che in questo caso contribuisce alla stabilizzazione del complesso enzima piruvato.
12 Complessi del magnesio con nucleotidi Una delle più importanti e diffuse molecole nelle cellule è l adenosina trifosfato, ATP. Un certo numero di enzimi che accoppia l idrolisi dell ATP ad altri processi biochimici richiede ioni Mg 2+ per funzionare in modo efficiente. Gli ioni metallici possono legarsi agli atomi di O degli esteri dei gruppi fosfato in posizione α, β, e γ come pure all azoto della nucleobase. Per lo ione Mg 2+ la coordinazione avviene esclusivamente agli atomi di ossigeno, con molecole di H 2 0 nelle rimanenti posizioni intorno al metallo.
13 Complessi Mg-ATP Pur formando complessi relativamente deboli (K f ~ 10 4 M -1 ), Mg 2+ può stabilizzare il substrato in una conformazione adatta per legarsi all enzima. L isomero più comune è il complesso β,γ-chelato in cui il gruppo fosfato in posizione β è reso chirale. Esistono evidenze che dei due isomeri e Λ solo uno venga selettivamente usato dall enzima che usa complessi Mg(ATP) Data la labilità cinetica dei complessi di Mg 2+, è difficile ottenere informazioni strutturali. Sono stati perciò preparati e caratterizzati vari complessi dell ATP con ioni cineticamente inerti (Cr III, Co III ). Questi complessi spesso funzionano come inibitori di enzimi che richiedono nucleotidi di Mg(II) come substrati o cofattori e sono quindi considerati dei buoni modelli per i tipi di struttura che formano con Mg. Gli isomeri Λ e di [Co(NH 3 ) 4 (β,γ-atp] sono stati fatti reagire con l enzima esochinasi, che normalmente usa Mg(ATP) per convertire glucosio in glucosio-6-fosfato, producendo Mg(ADP). L analisi dei prodotti mostrò che l isomero Λ di [Co(NH 3 ) 4 (β,γ-atp] era convertito a [Co(NH 3 ) 4 (β,γ-adp-glucosio-6-fosfato], ma che l isomero era inattivo Oltre alla stabilizzazione degli acidi nucleici Mg 2+ realizza una importante funzione nei sistemi di immagazzinamento e trasmissione dell informazione genetica.
14 Ruolo del calcio negli esseri viventi Si incontra negli esseri viventi in grande quantità (nell uomo 1000 g) e svolge funzioni molto diverse quali: - Strutturali: ossa, denti, gusci, pareti cellulari - sensoriali: contrazione muscolare,sinapsi, secrezione ormonale - catalisi: controllo degli enzimi digestivi (proteasi), coagulazione del sangue e in una grande varietà di attività cellulari quali: fotosintesi ; fosforilazione ossidativa; divisione cellulare, morte cellulare La struttura delle ossa si basa sull unione di una parte interna di natura organica e un tessuto inorganico esterno formato dal minerale idrossiapatite di calcio, Ca 10 (OH) 2 (PO 4 ) 6 e la fluoroidrossiapatite. Ca 2+ si incontra come ossalato idrato CaC 2 O 4 xh 2 O (x= 1 o 2) nelle uova di insetti o come carbonato (in diverse forme cristalline: calcite, aragonite, vaterite) nel guscio dell uovo determinando, secondo la densità della forma cristallina, punti di maggiore resistenza meccanica o maggiore fragilità. Nell uomo, l unico organo nel quale CaCO 3 è preferito al fosfato di calcio è l orecchio interno nel quale opera come sensore di gravità e si trova come calcite.
15 Lo ione Ca 2+ come acido di Lewis I fosfolipidi, anche dopo essere stati inseriti nelle membrane, non sono metabolicamente inerti: le catene aciliche degli acidi grassi possono essere rimodellate mediante la rimozione e la sostituzione delle catene degli acidi grassi sugli atomi di carbonio in posizione 1 e 2. La fosfolipasi A 2 appartiene a una classe di 4 enzimi extracellulari che idrolizzano legami specifici nei fosfolipidi attraverso un meccanismo Ca-dipendente (gli altri sono le fosfolipasi A1, C e D) che si trova in grande quantità nel liquido pancreatico di mammiferi come pure nei veleni delle api e serpenti. Le strutture ai raggi X di fosfolipasi provenienti da svariate fonti mostrano forti analogie strutturali: il Ca si trova in una cavità prossima alla superficie e ha una coordinazione ottaedrica costituita da Tyr-28, Glu-30,Glu-32, Asp-49 e 2 molecole di H 2 O
16 La catalisi implica 2 tappe che sono cineticamente e strutturalmente indipendenti. Nella prima vari residui dell enzima si dispongono in una superficie esposta, praticamente piana (sito di riconoscimento iterfacciale) che è il responsabile dell assorbimento della fosfolipasi A 2 solubile nell interfaccia lipide-acqua. La seconda tappa, la esterolisi, avviene successivamente all unione del substrato al centro attivo, localizzato al fondo di un canale idrofobico Ca 2+ è un cofattore essenziale per l attività catalitica di questo enzima dato che la sua presenza determina un legame effettivo fra il substrato e il centro attivo Inoltre, la coppia Asp-99- His-48 fanno parte del processo catalitico Viene utilizzata una istidina del centro attivo (His-48), assistita da un aspartato, per polarizzare un legame di una molecola di H 2 O che attacca allora il gruppo carbonilico del substrato
17 Meccanismo catalitico della fosfolipasi A 2 Ca 2+ stabilizza lo stato di transizione interagendo attivamente con l ossigeno del carbonio quaternario Il prodotto finale viene infine staccato da 3 molecole di acqua che entrano nel centro attivo, due delle quali sono quelle che fanno parte della sfera di coordinazione di Ca 2+ nell enzima a riposo E probabile che la riacilazione avvenga utilizzando un acil-coa
18 Il Ca come secondo messaggero Probabilmente il ruolo più importante del Ca negli esseri viventi è quello di secondo messaggero. La principale differenza tra un messaggero primario e secondario è dovuta alla localizzazione dell operazione. I messaggeri primari operano come agenti extracellulari effettuando comunicazione tra cellule oppure iniziano una risposta a un cambiamento nell intorno extracellulare. Esempi includono gli ormoni (quali l insulina) e metaboliti (quali il glucosio). I messaggeri secondari, quali i nucleotidi ciclici (camp, cgmp) e lo ione Ca 2+, funzionano dentro la cellula, in risposta ad un segnale extracellulare. Ca 2+ opera, in questo caso, come un trasmettitore di segnali coordinando un ampia gamma di risposte cellulari, fra le quali la contrazione muscolare, il metabolismo energetico, la endocitosi, la secrezione, la fertilizzazione, la divisione cellulare, la trasmissione sinaptica o il movimento cellulare. La peculiarità del Ca come mediatore intracellulare è la sua presenza ubiquitaria, che comprende i batteri fino ai neuroni altamente specializzati. La fondamentale proprietà del Ca che permette di comprendere il suo carattere unico come mediatore di segnali è, paradossalmente, la sua citotossicità: quando i suoi livelli si mantengono alti per periodi prolungati, si ha la precipitazione del fosfato che perturba il sistema di interscambio energetico nella cellula.
19 Trasporto attivo di Ca 2+ attraverso le membrane Per questa ragione la [Ca 2+ ] libero nel citosol di qualsiasi cellula deve mantenersi estremamente bassa (< 10-7 M), molto più bassa rispetto alla concentrazione nei fluidi extracellulari (10-3 M) o nel reticolo endoplasmatico (RE). Questo forte gradiente di [Ca 2+ ] permette alla cellula di utilizzare il Ca 2+ come trasmettitore di segnali: una brusca variazione locale di [Ca 2+ ] attiva meccanismi cellulari sensibili a questo ione. Affinché questo meccanismo di segnalazione funzioni correttamente è necessario un rigido controllo omeostatico del Ca 2+ che mantenga valori costanti delle concentrazioni. Nella membrana di tutte le cellule eucariote è presente una ATP-asa di alta affinità e bassa capacità che pompa Ca 2+ verso l esterno a spese dell energia somministrata dall idrolisi di ATP Una seconda pompa, di bassa affinità ed elevata capacità, attua in determinati tipi di cellule (muscolari e nervose) un interscambio Ca 2+ /Na +, che accoppia l entrata di Na + e l uscita di Ca 2+. In questo caso, dato che la sua affinità per Ca 2+ è relativamente bassa, entra in funzione quando i livelli di Ca 2+ citosolico superano di 10 volte i valori normali.
20 Specificità dello ione Ca 2+ quale ione messaggero L azione di un messaggero secondario consiste in una rapida risposta ad uno stimolo esterno, e così Ca 2+ deve soddisfare a certi fondamentali criteri per assolvere al suo compito: - Devono esserci delle molecole bersaglio (effettori) entro la cellula che legano Ca 2+ e portano ad una risposta cellulare. Un effettore è una molecola (proteina, ormone o altro) che può legare Ca 2+ ed è quindi attivata per effettuare un compito specifico. Questa molecola deve rimanere passiva finché non è necessario. Molecole effettori per Ca 2+ sono normalmente proteine che iniziano una immediata risposta cellulare dopo la coordinazione del Ca (es. il legame di Ca 2+ con la troponina C determina la contrazione muscolare) o attivano una proteina bersaglio (es. la calmodulina) che successivamente inizia ulteriori risposte cellulari. Queste proteine bersaglio nelle cellule dei mammiferi sono localizzate nel citosol e sulla superficie delle membrane a contatto con il citosol. - La [Ca 2+ ] deve rimanere bassa in una cellula non stimolata per evitare interazione con proteine effettori. Queste proteine devono essere altamente selettive per Ca 2+ poiché esse devono individuare questo ione in presenza di alti livelli intracellulari di Mg 2+ (~0.5 mm) e K + (~ 100 mm) - Durante la stimolazione, la [Ca 2+ ] intracellulare deve aumentare rapidamente. Successivamente la concentrazione deve essere ridotta ai livelli iniziali.
21 La calmodulina: calcium modulating protein Molti processi di trasduzione dei segnali cellulari implicano il rilascio di ioni Ca 2+ : un aumento della loro concentrazione intracellulare è segnalata da una famiglia di proteine (un centinaio di membri) capaci di legare Ca 2+ con affinità e specificità adeguate. Il prototipo di queste proteine è la calmodulina la quale accoppia variazioni di [Ca 2+ ] allo stato di attivazione di una varietà di enzimi quali le proteine chinasi (legate alla degradazione del glicogeno), fosfodiesterasi, pompe Ca 2+ -ATPase. La calmodulina è una piccola proteina monomerica (148 aa) capace di legare fino a 4 ioni Ca 2+. La struttura primaria è altamente conservata in specie che vanno dal paramecio (protozoo) all uomo e caratterizzata da 4 sequenze chiamate EF-hand dove le lettere E ed F indicano eliche α. Questa mano-ef è un dominio in cui 2 α-eliche contigue sono interrotte da un nodo formato da aa nel quale Ca 2+ è eptacoordinato legandosi attraverso gli atomi di O di aspartati, glutammati, asparagina, ecc.
22 Struttura della calmodulina umana La natura di questi siti di coordinazione è importante per definire la specificità verso il metallo: proteine sensibili al Ca devono riconoscere Ca 2+ in presenza di relativamente elevate concentrazioni di Mg 2+. Gli alti N.C. prodotti dalla struttura del dominio EF favorisce lo ione Ca 2+ rispetto a Mg 2+ essendo quest ultimo più piccolo. Per l addotto Cacalmodulina le costanti di dissociazione sono dell ordine! M mentre quelle del Mg 2+ sono ca 10-3 M La molecola, a forma di manubrio, è costituita da un coppia di domini EF uniti da una α- elica (che è l estensione dell elica F del dominio 2 e quella E del dominio 3). Alle estremità di questa elica molto esposta al solvente esistono due larghi frammenti idrofobici costituiti per il 50% da residui di metionina (che sono idrofobici, lineari e possono essere molto flessibili). La calmodulina si lega a peptidi che, in seguito alla parziale destrutturazione dell elica centrale, possono interagire simultaneamente con i due domini della calmodulina, come appare dallo schema seguente.
23 a) Rappresentazione schematica dei cambiamenti strutturali nella calmodulina in seguito all interazione con un peptide b) Rappresentazione più dettagliata del fenomeno, ottenuta mediante studi NMR sulla calmodulina uniformemente arricchita in 13 C e 15 N. La coordinazione del Ca 2+ alla calmodulina induce precisi cambi di conformazione La calmodulina amplifica piccoli cambiamenti nella concentrazione intracellulare di Ca 2+. L essenza del processo di decodificazione del segnale è un doppio cambio conformazionale della proteina
24 Il calcio nella contrazione muscolare Gli ioni Ca 2+ hanno un importante ruolo nella contrazione del muscolo Le miofibrille del tessuto muscolare sono formate da 2 tipi di filamenti che scivolano uno rispetto all altro in un processo che consuma energia. Il primo filamento, chiamato sottile, è costituito da molecole di actina che si trovano polimerizzate da un capo all altro formando un elica. Nel solco dell elica si distende una molecola allungata che è la tropomiosina. La troponina è un complesso proteinico formato da 3 proteine: la troponina I, la T e la (C), e si localizza sopra la tropomiosina, ogni 7 molecole di actina. Solo uno dei componenti del complesso proteinico di troponina, la troponina C, è capace di legare il Ca 2+. Questa proteina, strutturalmente simile alla calmodulina è una proteina con dominio mano-ef.
25 Quando il Ca 2+ è legato alla troponina C, si produce un importante cambio strutturale nel dominio in cui si alloggia il metallo. Il cambio conformazionale, controllato da ATP, che si produce nel gruppo di testa della miosina permette il movimento relativo di uno dei filamenti, grosso e sottile, uno rispetto all altro, dando con ciò la contrazione muscolare.
26 Il calcio e la protrombina La coagulazione del sangue avviene attraverso una complicata sequenza di eventi biochimici che richiede la presenza di molti enzimi e pro-enzimi (zimogeni). La fibrina, che è la proteina del coagulo del sangue, si genera mediante proteolisi del fibrinogeno. La proteasi responsabile di questo processo è la trombina che, a sua volta, si forma per mezzo della proteolisi della protrombina. In alcune di queste proteine è stata scoperta la presenza di 2 aminoacidi non comuni: l acido γ-carbossiglutammico (Gla, struttura a) e l acido β-idrossiaspartico (Hya, struttura b), entrambi in grado di legare Ca 2+. All estremo N-terminale della protrombina esistono 10 residui residui Gla, delineando uno degli assi della molecola e creando una regione di alta densità di carica negativa. E stato isolato un piccolo frammento proteolitico di 48 residui che contiene i 10 residui di Gla dimostrando che questo è in grado di legare 7 ioni Ca 2+
27 La coordinazione del metallo provoca un notevole cambio conformazionale. In presenza di ioni calcio, la protrombina (e altre proteine del sistema di coagulazione del sangue), si lega alle membrane cellulari, che sono ricche di fosfatidil serina, favorendo la formazione del coagulo sulla superficie danneggiata [ K. Harlos et al. Nature 330 (1987) 82]
Mediatore chimico. Recettore. Trasduzione del segnale. Risposta della cellula
 Mediatore chimico Recettore Trasduzione del segnale Risposta della cellula I mediatori chimici sono prodotti da cellule specializzate e sono diffusi nell organismo da apparati di distribuzione Sistemi
Mediatore chimico Recettore Trasduzione del segnale Risposta della cellula I mediatori chimici sono prodotti da cellule specializzate e sono diffusi nell organismo da apparati di distribuzione Sistemi
Le Biomolecole I parte. Lezioni d'autore di Giorgio Benedetti
 Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
Il mantenimento dell omeostasi cellulare dipende dai sistemi che permettono lo scambio di molecole tra citoplasma e liquido
 Il mantenimento dell omeostasi cellulare dipende dai sistemi che permettono lo scambio di molecole tra citoplasma e liquido extracellulare e dalla loro regolazione. Membrana cellulare Ogni cellula presenta
Il mantenimento dell omeostasi cellulare dipende dai sistemi che permettono lo scambio di molecole tra citoplasma e liquido extracellulare e dalla loro regolazione. Membrana cellulare Ogni cellula presenta
in Terminazione Neurone Dendriti Soma Fessura sinaptica sinaptica Nucleo dendrite Segmento iniziale Sinapsi inibitoria Segmento mielinico Assone
 Le funzioni del sistema nervoso si basano sull attività dei neuroni che consiste nel generare, trasmettere ed elaborare informazioni nervose, che dipendono da modificazioni del potenziale di membrana,
Le funzioni del sistema nervoso si basano sull attività dei neuroni che consiste nel generare, trasmettere ed elaborare informazioni nervose, che dipendono da modificazioni del potenziale di membrana,
Proteine integrali di membrana legate sul versante esterno a gruppi di carboidrati. Formati da diverse subunità che circoscrivono un poro acquoso che
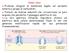 Canali ionici Proteine integrali di membrana legate sul versante esterno a gruppi di carboidrati. Formati da diverse subunità che circoscrivono un poro acquoso che permette il passaggio selettivo di ioni.
Canali ionici Proteine integrali di membrana legate sul versante esterno a gruppi di carboidrati. Formati da diverse subunità che circoscrivono un poro acquoso che permette il passaggio selettivo di ioni.
Potenziale di membrana: Differenza di potenziale elettrico a cavallo della membrana cellulare dovuta ad una diversa distribuzione ionica ai due lati
 Potenziale di membrana: Differenza di potenziale elettrico a cavallo della membrana cellulare dovuta ad una diversa distribuzione ionica ai due lati della membrana. Il potenziale di membrana (negativo
Potenziale di membrana: Differenza di potenziale elettrico a cavallo della membrana cellulare dovuta ad una diversa distribuzione ionica ai due lati della membrana. Il potenziale di membrana (negativo
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 26 La gluconeogenesi Concetti chiave: Il fegato e il rene possono sintetizzare glucosio da lattato, piruvato e amminoacidi.
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 26 La gluconeogenesi Concetti chiave: Il fegato e il rene possono sintetizzare glucosio da lattato, piruvato e amminoacidi.
I RECETTORI ACCOPPIATI A PROTEINE G
 I RECETTORI ACCOPPIATI A PROTEINE G I recettori accoppiati a proteine G sono costituiti da un unica subunità formata da un filamento di aminoacidi che attraversa 7 volte la membrana plasmatica Il sito
I RECETTORI ACCOPPIATI A PROTEINE G I recettori accoppiati a proteine G sono costituiti da un unica subunità formata da un filamento di aminoacidi che attraversa 7 volte la membrana plasmatica Il sito
Integrali (transmembrana), si estendono attraverso l intera membrana. Classificate in famiglie a seconda del numero di segmenti transmembrana.
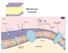 Membrana cellulare Proteine inserite nella membrana cellulare: Integrali (transmembrana), si estendono attraverso l intera membrana. Classificate in famiglie a seconda del numero di segmenti transmembrana.
Membrana cellulare Proteine inserite nella membrana cellulare: Integrali (transmembrana), si estendono attraverso l intera membrana. Classificate in famiglie a seconda del numero di segmenti transmembrana.
Farmaci del sistema nervoso autonomo
 Farmaci del sistema nervoso autonomo Farmaci colinergici Esercitano i loro effetti farmacologici sul sistema nervoso parasimpatico che utilizza Acetilcolina come mediatore chimico L acetilcolina (Ach)
Farmaci del sistema nervoso autonomo Farmaci colinergici Esercitano i loro effetti farmacologici sul sistema nervoso parasimpatico che utilizza Acetilcolina come mediatore chimico L acetilcolina (Ach)
Metalli in medicina. L utilizzo dei metalli in medicina ha radici ben antiche. Il ferro ed il
 Metalli in medicina L utilizzo dei metalli in medicina ha radici ben antiche. Il ferro ed il rame, per esempio, erano utilizzati nella Grecia antica. Già da secoli il Hg 2+ era utilizzato nel trattamento
Metalli in medicina L utilizzo dei metalli in medicina ha radici ben antiche. Il ferro ed il rame, per esempio, erano utilizzati nella Grecia antica. Già da secoli il Hg 2+ era utilizzato nel trattamento
SISTEMI ENERGETICI. L ATP privato di uno dei suoi 3 radicali fosforici diventa ADP (adenosindifosfato).
 SISTEMI ENERGETICI LE FONTI ENERGETICHE MUSCOLARI I movimenti sono resi possibili, dal punto di vista energetico, grazie alla trasformazione, da parte dei muscoli, dell energia chimica ( trasformazione
SISTEMI ENERGETICI LE FONTI ENERGETICHE MUSCOLARI I movimenti sono resi possibili, dal punto di vista energetico, grazie alla trasformazione, da parte dei muscoli, dell energia chimica ( trasformazione
MACROSTRUTTURA DEL MUSCOLO STRIATO SCHELETRICO
 FUNZIONE DEL MUSCOLO SCHELETRICO Ultrastruttura della cellula muscolare. Miofilamenti. Meccanismo della contrazione. Trasmissione neuromuscolare. Scossa semplice e tetano muscolare. Unità motoria. PROPRIETA
FUNZIONE DEL MUSCOLO SCHELETRICO Ultrastruttura della cellula muscolare. Miofilamenti. Meccanismo della contrazione. Trasmissione neuromuscolare. Scossa semplice e tetano muscolare. Unità motoria. PROPRIETA
I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici
 I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici La seta della tela di ragno è un insieme di macromolecole, dette proteine. Sono le caratteristiche fisico-chimiche di queste
I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici La seta della tela di ragno è un insieme di macromolecole, dette proteine. Sono le caratteristiche fisico-chimiche di queste
GLUCONEOGENESI. Sintesi (GENESI) di nuove (NEO) molecole di glucosio
 GLUCONEOGENESI Sintesi (GENESI) di nuove (NEO) molecole di glucosio CATABOLISMO ANABOLISMO OSSIDAZIONI Produzione di ATP RIDUZIONI Consumo di ATP La GLUCONEOGENESI è un PROCESSO ANABOLICO La gluconeogenesi
GLUCONEOGENESI Sintesi (GENESI) di nuove (NEO) molecole di glucosio CATABOLISMO ANABOLISMO OSSIDAZIONI Produzione di ATP RIDUZIONI Consumo di ATP La GLUCONEOGENESI è un PROCESSO ANABOLICO La gluconeogenesi
Regolazione del metabolismo del glucosio
 Regolazione del metabolismo del glucosio Regolazione coordinata di glicolisi e gluconeogenesi Glicolisi e gluconeogenesi sono regolate in modo reciproco La regolazione è a livello dei punti di deviazione
Regolazione del metabolismo del glucosio Regolazione coordinata di glicolisi e gluconeogenesi Glicolisi e gluconeogenesi sono regolate in modo reciproco La regolazione è a livello dei punti di deviazione
La pompa Na + /Glucosio: simporto
 MFN0366-A1 (I. Perroteau) - trasportatori e canali La pompa Na + /Glucosio: simporto Il trasportatore oscilla fra due stati alternativi (A e B); nello stato A la proteina è aperta nello spazio extracellulare,
MFN0366-A1 (I. Perroteau) - trasportatori e canali La pompa Na + /Glucosio: simporto Il trasportatore oscilla fra due stati alternativi (A e B); nello stato A la proteina è aperta nello spazio extracellulare,
scaricato da www.sunhope.it
 Recettori a tirosina chinasi I recettori a tirosina chinasi presentano vari domini Una regione di legame (extracellulare) Una regione transmembrana Una coda intracellulare con numerose tirosine scaricato
Recettori a tirosina chinasi I recettori a tirosina chinasi presentano vari domini Una regione di legame (extracellulare) Una regione transmembrana Una coda intracellulare con numerose tirosine scaricato
Figura 1. Rappresentazione della doppia elica di DNA e struttura delle differenti basi.
 Sommario La molecola di DNA è deputata a conservare le informazioni genetiche necessarie per lo sviluppo ed il funzionamento degli organismi viventi. Poiché contiene le istruzioni per la costruzione delle
Sommario La molecola di DNA è deputata a conservare le informazioni genetiche necessarie per lo sviluppo ed il funzionamento degli organismi viventi. Poiché contiene le istruzioni per la costruzione delle
LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI PROTEINE. sono ACIDI NUCLEICI. molecole complesse = POLIMERI. formate dall'unione di
 LE BIOMOLECOLE LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI LE BIOMOLECOLE sono LIPIDI PROTEINE ACIDI NUCLEICI molecole complesse = POLIMERI formate dall'unione di molecole semplici = MONOMERI
LE BIOMOLECOLE LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI LE BIOMOLECOLE sono LIPIDI PROTEINE ACIDI NUCLEICI molecole complesse = POLIMERI formate dall'unione di molecole semplici = MONOMERI
CONTROLLO ORMONALE DEL METABOLISMO GLUCIDICO DA PARTE DI GLUCAGONE, ADRENALINA E INSULINA
 CONTROLLO ORMONALE DEL METABOLISMO GLUCIDICO DA PARTE DI GLUCAGONE, ADRENALINA E INSULINA QUESTI ORMONI REGOLANO IL FLUSSO DEI METABOLITI NELLA GLICOLISI, NELLA GLICOGENO-SINTESI, NELLA GLIGENO-LISI E
CONTROLLO ORMONALE DEL METABOLISMO GLUCIDICO DA PARTE DI GLUCAGONE, ADRENALINA E INSULINA QUESTI ORMONI REGOLANO IL FLUSSO DEI METABOLITI NELLA GLICOLISI, NELLA GLICOGENO-SINTESI, NELLA GLIGENO-LISI E
NUCLEOTIDI e ACIDI NUCLEICI
 NUCLEOTIDI e ACIDI NUCLEICI Struttura dei nucleotidi Il gruppo fosfato conferisce carica negativa e proprietà acide FUNZIONI DEI NUCLEOTIDI MOLECOLE DI RISERVA DI ENERGIA L idrolisi dei nucleosidi trifosfato
NUCLEOTIDI e ACIDI NUCLEICI Struttura dei nucleotidi Il gruppo fosfato conferisce carica negativa e proprietà acide FUNZIONI DEI NUCLEOTIDI MOLECOLE DI RISERVA DI ENERGIA L idrolisi dei nucleosidi trifosfato
Domande relative alla specializzazione in: Biochimica clinica
 Domande relative alla specializzazione in: Biochimica clinica Domanda #1 (codice domanda: n.403) : Nell'ibridazione fluorescente in situ (Fluorescent in situ hybridization "FISH"), che tipo di sonde fluorescenti
Domande relative alla specializzazione in: Biochimica clinica Domanda #1 (codice domanda: n.403) : Nell'ibridazione fluorescente in situ (Fluorescent in situ hybridization "FISH"), che tipo di sonde fluorescenti
LE MOLECOLE INFORMAZIONALI. Lezioni d'autore Treccani
 LE MOLECOLE INFORMAZIONALI Lezioni d'autore Treccani Introduzione (I) I pionieri della biologia molecolare, scoperta la struttura degli acidi nucleici, pensarono di associare al DNA una sequenza di simboli,
LE MOLECOLE INFORMAZIONALI Lezioni d'autore Treccani Introduzione (I) I pionieri della biologia molecolare, scoperta la struttura degli acidi nucleici, pensarono di associare al DNA una sequenza di simboli,
DNA - RNA. Nucleotide = Gruppo Fosforico + Zucchero Pentoso + Base Azotata. Le unità fondamentali costituenti il DNA e l RNA sono i Nucleotidi.
 DNA - RNA Le unità fondamentali costituenti il DNA e l RNA sono i Nucleotidi. Nucleotide = Gruppo Fosforico + Zucchero Pentoso + Base Azotata. Esistono 4 basi azotate per il DNA e 4 per RNA Differenze
DNA - RNA Le unità fondamentali costituenti il DNA e l RNA sono i Nucleotidi. Nucleotide = Gruppo Fosforico + Zucchero Pentoso + Base Azotata. Esistono 4 basi azotate per il DNA e 4 per RNA Differenze
TEST BIOLOGIA 1 ANNO ABEI Da inviare a connesso@alice.it entro e non oltre il 6 novembre 2015
 1) I batteri sono organismi: a- bicellulari b- monocellulari c- pluricellulari 2) I virus: a- possono riprodursi solo nell acqua b- possono riprodursi solo sulla superficie di una cellula c- possono riprodursi
1) I batteri sono organismi: a- bicellulari b- monocellulari c- pluricellulari 2) I virus: a- possono riprodursi solo nell acqua b- possono riprodursi solo sulla superficie di una cellula c- possono riprodursi
Prof. Maria Nicola GADALETA
 Prof. Maria Nicola GADALETA Email: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA Email: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
la struttura tridimensionale può essere ottenuta solo per Un intero dominio in genere da 50 a 300 residui
 Durante la traduzione l informazione di ripiegamento codificata nella sequenza aminoacidica diventa disponibile in maniera vettoriale la struttura tridimensionale può essere ottenuta solo per Un intero
Durante la traduzione l informazione di ripiegamento codificata nella sequenza aminoacidica diventa disponibile in maniera vettoriale la struttura tridimensionale può essere ottenuta solo per Un intero
Macromolecole Biologiche. I domini (III)
 I domini (III) Domini α/β La cross over connection è l unità costitutiva su cui si basa la topologia di 3 tipi di domini α/β osservati nelle proteine: - α/β barrel - motivi ricchi di Leu (fold a ferro
I domini (III) Domini α/β La cross over connection è l unità costitutiva su cui si basa la topologia di 3 tipi di domini α/β osservati nelle proteine: - α/β barrel - motivi ricchi di Leu (fold a ferro
Biosintesi non ribosomiale di metaboliti peptidici bioattivi
 Biosintesi non ribosomiale di metaboliti peptidici bioattivi Principali bersagli degli antibiotici Gli antibiotici derivano per la maggior parte da composti naturali Strutture di alcuni peptidi bioattivi
Biosintesi non ribosomiale di metaboliti peptidici bioattivi Principali bersagli degli antibiotici Gli antibiotici derivano per la maggior parte da composti naturali Strutture di alcuni peptidi bioattivi
SINTESI PROTEICA. Replicazione. Trascrizione. Traduzione
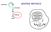 Replicazione SINTESI PROTEICA Trascrizione Traduzione 61 codoni codificanti 3 triplette non senso (STOP) AUG codone di inizio codone per Met Caratteristiche del codice genetico Specificità Il codice genetico
Replicazione SINTESI PROTEICA Trascrizione Traduzione 61 codoni codificanti 3 triplette non senso (STOP) AUG codone di inizio codone per Met Caratteristiche del codice genetico Specificità Il codice genetico
2. Fisiologia Cellulare Diffusione, Trasporto, Osmosi
 2. Fisiologia Cellulare Diffusione, Trasporto, Osmosi Prof. Carlo Capelli Fisiologia Laurea in Scienze delle attività motorie e sportive Università di Verona Obiettivi Diffusione semplice e mediata da
2. Fisiologia Cellulare Diffusione, Trasporto, Osmosi Prof. Carlo Capelli Fisiologia Laurea in Scienze delle attività motorie e sportive Università di Verona Obiettivi Diffusione semplice e mediata da
Tratto dal libro Come vivere 150 anni Dr. Dimitris Tsoukalas
 1 Tratto dal libro Come vivere 150 anni Dr. Dimitris Tsoukalas Capitolo 7 Enzimi, le macchine della vita Piccole macchine regolano la funzione del corpo umano in un orchestrazione perfetta e a velocità
1 Tratto dal libro Come vivere 150 anni Dr. Dimitris Tsoukalas Capitolo 7 Enzimi, le macchine della vita Piccole macchine regolano la funzione del corpo umano in un orchestrazione perfetta e a velocità
Equilibri di precipitazione
 Equilibri di precipitazione Molte sostanze solide sono caratterizzate da una scarsa solubilità in acqua (ad es. tutti i carbonati e gli idrossidi degli elementi del II gruppo) AgCl (a differenza di NaCl)
Equilibri di precipitazione Molte sostanze solide sono caratterizzate da una scarsa solubilità in acqua (ad es. tutti i carbonati e gli idrossidi degli elementi del II gruppo) AgCl (a differenza di NaCl)
Metabolismo: Introduzione
 Metabolismo: Introduzione METABOLISMO Insieme delle reazioni chimiche coordinate e integrate che hanno luogo in tutte le cellule C A T A B O L I S M O Ossidazioni esoergoniche Alimenti: Carboidrati Lipidi
Metabolismo: Introduzione METABOLISMO Insieme delle reazioni chimiche coordinate e integrate che hanno luogo in tutte le cellule C A T A B O L I S M O Ossidazioni esoergoniche Alimenti: Carboidrati Lipidi
Continua. Peptidasi H 2 O
 Continua Peptidasi H 2 O Classificazione delle peptidasi 1. Meccanismo catalitico 2. Tipo di reazione catalizzata 3. Struttura molecolare e omologia 1. Meccanismo catalitico (mostrato per la chimotripsina)
Continua Peptidasi H 2 O Classificazione delle peptidasi 1. Meccanismo catalitico 2. Tipo di reazione catalizzata 3. Struttura molecolare e omologia 1. Meccanismo catalitico (mostrato per la chimotripsina)
La membrana cellulare racchiude il protoplasma, la sostanza vivente che costituisce la cellula, e lo separa dall ambiente esterno, extracellulare.
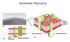 Membrana Plasmatica La membrana cellulare racchiude il protoplasma, la sostanza vivente che costituisce la cellula, e lo separa dall ambiente esterno, extracellulare. La sua funzione principale è quella
Membrana Plasmatica La membrana cellulare racchiude il protoplasma, la sostanza vivente che costituisce la cellula, e lo separa dall ambiente esterno, extracellulare. La sua funzione principale è quella
LA GENETICA: DNA e RNA LA GENETICA. DNA e RNA. Prof. Daniele Verri
 LA GENETICA DNA e RNA Prof. Daniele Verri L'acido desossiribonucleico o deossiribonucleico (DNA) è un acido nucleico che contiene le informazioni necessarie per la formazione di RNA e proteine. LA GENETICA:
LA GENETICA DNA e RNA Prof. Daniele Verri L'acido desossiribonucleico o deossiribonucleico (DNA) è un acido nucleico che contiene le informazioni necessarie per la formazione di RNA e proteine. LA GENETICA:
Helena Curtis N. Sue Barnes
 Helena Curtis N. Sue Barnes LA RESPIRAZIONE CELLULARE INDICE Demolizione del glucosio Glicolisi Fermentazione lattica Fermentazione alcolica Respirazione cellulare Ciclo di Krebs Catena di trasporto degli
Helena Curtis N. Sue Barnes LA RESPIRAZIONE CELLULARE INDICE Demolizione del glucosio Glicolisi Fermentazione lattica Fermentazione alcolica Respirazione cellulare Ciclo di Krebs Catena di trasporto degli
Segnalazione cellulare e trasduzione del segnale. Comunicazione fra le cellule
 Segnalazione cellulare e trasduzione del segnale Comunicazione fra le cellule Le cellule comunicano e interagiscono tra loro tramite il fenomeno della segnalazione cellulare Una cellula segnalatrice produce
Segnalazione cellulare e trasduzione del segnale Comunicazione fra le cellule Le cellule comunicano e interagiscono tra loro tramite il fenomeno della segnalazione cellulare Una cellula segnalatrice produce
BIOLOGIA GENERALE 22-24 ottobre 2007
 Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE 22-24 ottobre 2007 Facoltà di Psicologia Tecniche di Psicologia Generale e Sperimentale Alessandro Massolo Dip.
Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE 22-24 ottobre 2007 Facoltà di Psicologia Tecniche di Psicologia Generale e Sperimentale Alessandro Massolo Dip.
REPLICAZIONE DEL DNA
 REPLICAZIONE DEL DNA La replicazione (o anche duplicazione) è il meccanismo molecolare attraverso cui il DNA produce una copia di sé stesso. Ogni volta che una cellula si divide, infatti, l'intero genoma
REPLICAZIONE DEL DNA La replicazione (o anche duplicazione) è il meccanismo molecolare attraverso cui il DNA produce una copia di sé stesso. Ogni volta che una cellula si divide, infatti, l'intero genoma
CELLULE EUCARIOTICHE
 CELLULE EUCARIOTICHE Le cellule eucariotiche sono di maggiori dimensioni, rispetto a quelle procariotiche (almeno 10 volte più grandi) Oltre a: membrana plasmatica, citoplasma, DNA e ribosomi (comuni a
CELLULE EUCARIOTICHE Le cellule eucariotiche sono di maggiori dimensioni, rispetto a quelle procariotiche (almeno 10 volte più grandi) Oltre a: membrana plasmatica, citoplasma, DNA e ribosomi (comuni a
Le cellule eucariotiche svolgono durante la loro vita una serie ordinata di eventi che costituiscono il Ciclo Cellulare
 Le cellule eucariotiche svolgono durante la loro vita una serie ordinata di eventi che costituiscono il Ciclo Cellulare Interfase comprende le fasi G 1, S, and G 2 Sintesi di macromolecole durante la
Le cellule eucariotiche svolgono durante la loro vita una serie ordinata di eventi che costituiscono il Ciclo Cellulare Interfase comprende le fasi G 1, S, and G 2 Sintesi di macromolecole durante la
Il glicogeno (riserva di glucosio) è immagazzinato nel fegato e nei muscoli (con finalità diverse )
 Glicogeno Glicogeno...1 Glicogenolisi...3 Glicogenosintesi...7 Regolazione ormonale della glicogenolisi e delle glicogenosintesi...13 Il recettore del glucagone e quello dell adrenalina sono 2 GPCR (G-Protein
Glicogeno Glicogeno...1 Glicogenolisi...3 Glicogenosintesi...7 Regolazione ormonale della glicogenolisi e delle glicogenosintesi...13 Il recettore del glucagone e quello dell adrenalina sono 2 GPCR (G-Protein
Dal DNA all RNA. La trascrizione nei procarioti e negli eucarioti
 Dal DNA all RNA La trascrizione nei procarioti e negli eucarioti DOGMA CENTRALE DELLA BIOLOGIA MOLECOLARE Gene Regione di DNA che porta l informazione (= che CODIFICA) per una catena polipeptidica o per
Dal DNA all RNA La trascrizione nei procarioti e negli eucarioti DOGMA CENTRALE DELLA BIOLOGIA MOLECOLARE Gene Regione di DNA che porta l informazione (= che CODIFICA) per una catena polipeptidica o per
Metabolismo degli aminoacidi
 Metabolismo degli aminoacidi Quando gli aminoacidi provenienti dalla digestione gastrica e intestinale, non vengono utilizzati per la costruzione di nuove proteine vengono demoliti Transaminazione Per
Metabolismo degli aminoacidi Quando gli aminoacidi provenienti dalla digestione gastrica e intestinale, non vengono utilizzati per la costruzione di nuove proteine vengono demoliti Transaminazione Per
 forme diabetiche Diabete di tipo I o magro o giovanile (IDDM): carenza primaria di insulina, più frequente nei giovani e nei bambini. Il deficit insulinico consegue (per predisposizione ereditaria o per
forme diabetiche Diabete di tipo I o magro o giovanile (IDDM): carenza primaria di insulina, più frequente nei giovani e nei bambini. Il deficit insulinico consegue (per predisposizione ereditaria o per
Le PROTEINE sono i biopolimeri maggiormente presenti all interno delle cellule, dal momento che costituiscono dal 40 al 70% del peso a secco.
 Le PROTEINE sono i biopolimeri maggiormente presenti all interno delle cellule, dal momento che costituiscono dal 40 al 70% del peso a secco. Svolgono funzioni biologiche di fondamentale importanza e possono
Le PROTEINE sono i biopolimeri maggiormente presenti all interno delle cellule, dal momento che costituiscono dal 40 al 70% del peso a secco. Svolgono funzioni biologiche di fondamentale importanza e possono
Struttura e funzioni della cellula. Corso di Biofisica, Università di Cagliari 1
 Struttura e funzioni della cellula 1 Riferimenti Books and others Biological Physics (updated 1 st ed.), Philip Nelson, Chap. 2 Physical Biology of the Cell, Phillips et al., Chap. 2 Movies Exercise 2
Struttura e funzioni della cellula 1 Riferimenti Books and others Biological Physics (updated 1 st ed.), Philip Nelson, Chap. 2 Physical Biology of the Cell, Phillips et al., Chap. 2 Movies Exercise 2
INTERVENTO DI CLAUDIA RICCARDI PLASMAPROMETEO - Dipartimento di Fisica Università degli Studi di Milano - Bicocca
 INTERVENTO DI CLAUDIA RICCARDI PLASMAPROMETEO - Dipartimento di Fisica Università degli Studi di Milano - Bicocca La ricerca come strumento per lo sviluppo aziendale: sinergia tra università e industria
INTERVENTO DI CLAUDIA RICCARDI PLASMAPROMETEO - Dipartimento di Fisica Università degli Studi di Milano - Bicocca La ricerca come strumento per lo sviluppo aziendale: sinergia tra università e industria
Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica.
 Concanavalina A Emoglobina subunità Trioso fosfato isomerasi Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica. 1 La conformazione è
Concanavalina A Emoglobina subunità Trioso fosfato isomerasi Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica. 1 La conformazione è
Il flusso dell informazione genetica. DNA -->RNA-->Proteine
 Il flusso dell informazione genetica DNA -->RNA-->Proteine Abbiamo visto i principali esperimenti che hanno dimostrato che il DNA è la molecola depositaria dell informazione genetica nella maggior parte
Il flusso dell informazione genetica DNA -->RNA-->Proteine Abbiamo visto i principali esperimenti che hanno dimostrato che il DNA è la molecola depositaria dell informazione genetica nella maggior parte
http://sds.coniliguria.it 1
 Aspetti metabolici dell esercizio fisico Genova 22 gennaio 2011 A cura di Attilio TRAVERSO http://sds.coniliguria.it 1 L allenamento produce modificazioni fisiologiche (adattamenti) in quasi tutti i sistemi
Aspetti metabolici dell esercizio fisico Genova 22 gennaio 2011 A cura di Attilio TRAVERSO http://sds.coniliguria.it 1 L allenamento produce modificazioni fisiologiche (adattamenti) in quasi tutti i sistemi
dieta vengono convertiti in composti dei corpi chetonici.
 Metabolismo degli aminoacidi Metabolismo degli aminoacidi Gli aminoacidi introdotti in eccesso con la dieta vengono convertiti in composti precursori del glucosio, degli acidi grassi e dei corpi chetonici.
Metabolismo degli aminoacidi Metabolismo degli aminoacidi Gli aminoacidi introdotti in eccesso con la dieta vengono convertiti in composti precursori del glucosio, degli acidi grassi e dei corpi chetonici.
Muscolo Scheletrico 1. Anatomia funzionale, eccitazione, contrazione
 Muscolo Scheletrico 1. Anatomia funzionale, eccitazione, contrazione Prof. Carlo Capelli Fisiologia Laurea in Scienze delle attività motorie e sportive Università di Verona Obiettivi Anatomia funzionale
Muscolo Scheletrico 1. Anatomia funzionale, eccitazione, contrazione Prof. Carlo Capelli Fisiologia Laurea in Scienze delle attività motorie e sportive Università di Verona Obiettivi Anatomia funzionale
Prof. Maria Nicola GADALETA
 Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
SINTESI DELL RNA. Replicazione. Trascrizione. Traduzione
 SINTESI DELL RNA Replicazione Trascrizione Traduzione L RNA ha origine da informazioni contenute nel DNA La TRASCRIZIONE permette la conversione di una porzione di DNA in una molecola di RNA con una sequenza
SINTESI DELL RNA Replicazione Trascrizione Traduzione L RNA ha origine da informazioni contenute nel DNA La TRASCRIZIONE permette la conversione di una porzione di DNA in una molecola di RNA con una sequenza
LA CORRENTE ELETTRICA
 L CORRENTE ELETTRIC H P h Prima che si raggiunga l equilibrio c è un intervallo di tempo dove il livello del fluido non è uguale. Il verso del movimento del fluido va dal vaso a livello maggiore () verso
L CORRENTE ELETTRIC H P h Prima che si raggiunga l equilibrio c è un intervallo di tempo dove il livello del fluido non è uguale. Il verso del movimento del fluido va dal vaso a livello maggiore () verso
Elettroforesi. Elettroforesi: processo per cui molecole cariche si separano in un campo elettrico a causa della loro diversa mobilita.
 Elettroforesi Elettroforesi: processo per cui molecole cariche si separano in un campo elettrico a causa della loro diversa mobilita. A qualunque ph diverso dal pi le proteine hanno una carica netta quindi,
Elettroforesi Elettroforesi: processo per cui molecole cariche si separano in un campo elettrico a causa della loro diversa mobilita. A qualunque ph diverso dal pi le proteine hanno una carica netta quindi,
Energia nelle reazioni chimiche. Lezioni d'autore di Giorgio Benedetti
 Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
Meccanismi molecolari di trasduzione del segnale. Le vie di trasduzione del segnale sono molto specifiche ed estremamente sensibili.
 Meccanismi molecolari di trasduzione del segnale. Le vie di trasduzione del segnale sono molto specifiche ed estremamente sensibili. La sensibilita delle vie di trasduzione dipende da 3 fattori: -l affinita
Meccanismi molecolari di trasduzione del segnale. Le vie di trasduzione del segnale sono molto specifiche ed estremamente sensibili. La sensibilita delle vie di trasduzione dipende da 3 fattori: -l affinita
Calcio, fosforo e magnesio
 Calcio, fosforo e magnesio Calcio (Ca 2+) elemento più abbondante del corpo umano (dopo O, C, H, N) 1200 g in totale nell uomo adulto di cui 99% nello scheletro Fosforo (P) 850 g totali nel corpo umano
Calcio, fosforo e magnesio Calcio (Ca 2+) elemento più abbondante del corpo umano (dopo O, C, H, N) 1200 g in totale nell uomo adulto di cui 99% nello scheletro Fosforo (P) 850 g totali nel corpo umano
-assicurare il fabbisogno plastico necessario alla riparazione protezione e ricambio dei tessuti.
 Il principali compiti derivanti dall assunzione periodica di cibo sono: -assicurare il giusto fabbisogno energetico necessario alla vita ed all attività muscolare (tenendo conto che entrate ed uscite devono
Il principali compiti derivanti dall assunzione periodica di cibo sono: -assicurare il giusto fabbisogno energetico necessario alla vita ed all attività muscolare (tenendo conto che entrate ed uscite devono
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio. GLUCONEOGENESI (sintesi da precursori non glucidici)
 DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) Metabolismo del glucosio La gluconeogenesi epatica è regolata
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) Metabolismo del glucosio La gluconeogenesi epatica è regolata
Acidi e basi. HCl H + + Cl - (acido cloridrico) NaOH Na + + OH - (idrossido di sodio; soda caustica)
 Acidi e basi Per capire che cosa sono un acido e una base dal punto di vista chimico, bisogna riferirsi ad alcune proprietà chimiche dell'acqua. L'acqua, sia solida (ghiaccio), liquida o gassosa (vapore
Acidi e basi Per capire che cosa sono un acido e una base dal punto di vista chimico, bisogna riferirsi ad alcune proprietà chimiche dell'acqua. L'acqua, sia solida (ghiaccio), liquida o gassosa (vapore
RNA polimerasi operone. L operatore è il tratto
 La regolazione genica nei procarioti Alcune proteine vengono prodotte dalla cellula ad un ritmo relativamente costante e l attività dei geni che codificano queste proteine non è regolata in modo sofisticato.
La regolazione genica nei procarioti Alcune proteine vengono prodotte dalla cellula ad un ritmo relativamente costante e l attività dei geni che codificano queste proteine non è regolata in modo sofisticato.
Carboidrati puri : zucchero e amido nei cibi, cellulosa nel legno, carta e cotone = C 6 O 6 (H 2 O) 6
 Carboidrati Carboidrati puri : zucchero e amido nei cibi, cellulosa nel legno, carta e cotone Glucosio Carboidrati modificati: membrane cellulari, acidi nucleici, Da carbonio idrato: glucosio= C 6 H 12
Carboidrati Carboidrati puri : zucchero e amido nei cibi, cellulosa nel legno, carta e cotone Glucosio Carboidrati modificati: membrane cellulari, acidi nucleici, Da carbonio idrato: glucosio= C 6 H 12
Il metabolismo dell RNA. Prof. Savino; dispense di Biologia Molecolare, Corso di Laurea in Biotecnologie
 Il metabolismo dell RNA I vari tipi di RNA Il filamento di DNA che dirige la sintesi dello mrna è chiamato filamento stampo o filamento antisenso. L altro filamento che ha sequenza identica a quella dello
Il metabolismo dell RNA I vari tipi di RNA Il filamento di DNA che dirige la sintesi dello mrna è chiamato filamento stampo o filamento antisenso. L altro filamento che ha sequenza identica a quella dello
unità C2. Le trasformazioni energetiche nelle cellule
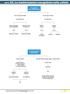 unità 2. Le trasformazioni energetiche nelle cellule Il trasporto nelle cellule avviene senza consumo di energia con consumo di energia trasporto passivo trasporto attivo attraverso il doppio strato fosfolipidico
unità 2. Le trasformazioni energetiche nelle cellule Il trasporto nelle cellule avviene senza consumo di energia con consumo di energia trasporto passivo trasporto attivo attraverso il doppio strato fosfolipidico
Che cos è un detersivo?
 Che cos è un detersivo? Miscela di sostanze chimiche che mischiate all acqua sono in grado di rimuovere lo sporco Agiscono sulle sostanze che non si sciolgono facilmente in acqua (idrofobe) I principali
Che cos è un detersivo? Miscela di sostanze chimiche che mischiate all acqua sono in grado di rimuovere lo sporco Agiscono sulle sostanze che non si sciolgono facilmente in acqua (idrofobe) I principali
COMUNICAZIONE TRA CELLULA ED AMBIENTE FGE AA.2015-16
 COMUNICAZIONE TRA CELLULA ED AMBIENTE FGE AA.2015-16 OMEOSTASI Fisiologia Umana La fisiologia è la scienza che studia i meccanismi di funzionamento degli organismi viventi. E una scienza integrata che
COMUNICAZIONE TRA CELLULA ED AMBIENTE FGE AA.2015-16 OMEOSTASI Fisiologia Umana La fisiologia è la scienza che studia i meccanismi di funzionamento degli organismi viventi. E una scienza integrata che
Respirazione cellulare
 Respirazione cellulare L equazione generale della respirazione C 6 H 12 O 6 + 6 O 2! 6 CO 2 + 6 H 2 O + 36 ATP 1 molec zucchero 6 molec ossigeno 6 molec anidride carbonica 6 molec acqua + = + + 36 molecole
Respirazione cellulare L equazione generale della respirazione C 6 H 12 O 6 + 6 O 2! 6 CO 2 + 6 H 2 O + 36 ATP 1 molec zucchero 6 molec ossigeno 6 molec anidride carbonica 6 molec acqua + = + + 36 molecole
Modello del collasso idrofobico. Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60
 Modello gerarchico Modello del collasso idrofobico Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60 Le Hsp70 si legano ai segmenti idrofobici di
Modello gerarchico Modello del collasso idrofobico Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60 Le Hsp70 si legano ai segmenti idrofobici di
Scuola Media Piancavallo 2
 LA CELLULA Una caratteristica di quasi tutti gli esseri viventi è quella di possedere una struttura più o meno complessa in cui parti diverse, gli organi, sono adatte a svolgere funzioni specifiche. Il
LA CELLULA Una caratteristica di quasi tutti gli esseri viventi è quella di possedere una struttura più o meno complessa in cui parti diverse, gli organi, sono adatte a svolgere funzioni specifiche. Il
La trascrizione nei procarioti. Prof. Savino; dispense di Biologia Molecolare, Corso di Laurea in Biotecnologie
 La trascrizione nei procarioti Concetti base Nucleoside base purinica o pirimidinica legata alla posizione 1 dell anello pentoso Nucleotide base azotata-pentoso-fosfato Concetti base La trascrizione comporta
La trascrizione nei procarioti Concetti base Nucleoside base purinica o pirimidinica legata alla posizione 1 dell anello pentoso Nucleotide base azotata-pentoso-fosfato Concetti base La trascrizione comporta
Monossido d azoto NO (Nitric Oxide) Messaggero del segnale cellulare. Molecola regolatoria nel sistema nervoso centrale e periferico
 Monossido d azoto NO (Nitric Oxide) Ruolo biologico: Messaggero del segnale cellulare Molecola regolatoria nel sistema cardiovascolare Molecola regolatoria nel sistema nervoso centrale e periferico Componente
Monossido d azoto NO (Nitric Oxide) Ruolo biologico: Messaggero del segnale cellulare Molecola regolatoria nel sistema cardiovascolare Molecola regolatoria nel sistema nervoso centrale e periferico Componente
Laura Beata Classe 4 B Concorso Sperimento Anch io Silvia Valesano Classe 4 B
 Laura Beata Classe 4 B Concorso Sperimento Anch io Silvia Valesano Classe 4 B RELAZINI DI LABRATRI (Italiano) Titolo: : Cosa mangiamo veramente? Scopo: 1. Scoprire in quali alimenti ci sono o non ci sono
Laura Beata Classe 4 B Concorso Sperimento Anch io Silvia Valesano Classe 4 B RELAZINI DI LABRATRI (Italiano) Titolo: : Cosa mangiamo veramente? Scopo: 1. Scoprire in quali alimenti ci sono o non ci sono
Βeta ossidazione degli acidi grassi BETA OSSIDAZIONE DEGLI ACIDI GRASSI 13/12/2013 SEMINARIO. Acidi grassi (2)
 Acidi grassi (1) Mitocondri SEMINARIO BETA OSSIDAZIONE DEGLI ACIDI GRASSI Sono le principali fonti di energia per alcuni tessuti (es. muscolo cardiaco). Si genera molto più energia dall ossidazione degli
Acidi grassi (1) Mitocondri SEMINARIO BETA OSSIDAZIONE DEGLI ACIDI GRASSI Sono le principali fonti di energia per alcuni tessuti (es. muscolo cardiaco). Si genera molto più energia dall ossidazione degli
Macromolecole Biologiche. I domini (II)
 I domini (II) Domini β Nonostante l elevato numero di possibili disposizioni di filamenti β (a costituire foglietti β antiparalleli) connessi da tratti di loop, i domini β più frequentemente osservati
I domini (II) Domini β Nonostante l elevato numero di possibili disposizioni di filamenti β (a costituire foglietti β antiparalleli) connessi da tratti di loop, i domini β più frequentemente osservati
PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA
 PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA Svolgono la loro funzione legando reversibilmente l OSSIGENO. Aumentano la solubilità dell ossigeno nel plasma, da 3ml/L a 220 ml/l. La mioglobina
PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA Svolgono la loro funzione legando reversibilmente l OSSIGENO. Aumentano la solubilità dell ossigeno nel plasma, da 3ml/L a 220 ml/l. La mioglobina
Funzioni della membrana plasmatica
 TRASPORTO M.P. -Omeostasi cellulare Funzioni della membrana plasmatica Mantenimento della conc. intracell. di ioni e molecole entro valori corretti Scambi interno - esterno Non c è consumo E Consumo E
TRASPORTO M.P. -Omeostasi cellulare Funzioni della membrana plasmatica Mantenimento della conc. intracell. di ioni e molecole entro valori corretti Scambi interno - esterno Non c è consumo E Consumo E
ENZIMI CINETICA ENZIMATICA
 ENZIMI PERCHE UNA REAZIONE AVVENGA, SI DEVONO SODDISFARE TRE CONDIZIONI I SUBSTRATI DEVONO ENTRARE IN COLLISIONE LA COLLISIONE DEVE AVVENIRE CON ORIENTAMENTO CORRETTO I REAGENTI DEVONO AVERE ENERGIA SUFFICIENTE
ENZIMI PERCHE UNA REAZIONE AVVENGA, SI DEVONO SODDISFARE TRE CONDIZIONI I SUBSTRATI DEVONO ENTRARE IN COLLISIONE LA COLLISIONE DEVE AVVENIRE CON ORIENTAMENTO CORRETTO I REAGENTI DEVONO AVERE ENERGIA SUFFICIENTE
È importante quindi conoscere le proprietà chimiche dell acqua. Le reazioni acido base sono particolari esempi di equilibrio chimico in fase acquosa
 Premessa Le nozioni di acido e di base non sono concetti assoluti ma sono relativi al mezzo in cui tale sostanze sono sciolte. L acqua è il solvente per eccellenza, scelto per studiare le caratteristiche
Premessa Le nozioni di acido e di base non sono concetti assoluti ma sono relativi al mezzo in cui tale sostanze sono sciolte. L acqua è il solvente per eccellenza, scelto per studiare le caratteristiche
Il metabolismo del glicogeno e la gluconeogenesi. Copyright 2013 Zanichelli editore S.p.A.
 Il metabolismo del glicogeno e la gluconeogenesi Copyright 2013 Zanichelli editore S.p.A. Capitolo 16 La demolizione del glicogeno Concetti chiave 16.1 Il glicogeno, la forma di immagazzinamento del glucosio,
Il metabolismo del glicogeno e la gluconeogenesi Copyright 2013 Zanichelli editore S.p.A. Capitolo 16 La demolizione del glicogeno Concetti chiave 16.1 Il glicogeno, la forma di immagazzinamento del glucosio,
C). Quindi, con la spettroscopia NMR, le informazioni sulla struttura molecolare vengono dedotte osservando il comportamento dei nuclei atomici.
 La spettroscopia di Risonanza Magnetica Nucleare (NMR) è una tecnica analitica strumentale che permette di ottenere dettagliate informazioni sulla struttura molecolare dei composti in esame. La spettroscopia
La spettroscopia di Risonanza Magnetica Nucleare (NMR) è una tecnica analitica strumentale che permette di ottenere dettagliate informazioni sulla struttura molecolare dei composti in esame. La spettroscopia
Il DNA e la duplicazione cellulare. Acidi nucleici: DNA, materiale ereditario
 Il DN e la duplicazione cellulare Il DN, materiale ereditario Struttura del DN Replicazione del DN Dal DN alla proteina Il odice genetico iclo cellulare Mitosi Meiosi Da Figura 8-11 ampbell & Reece cidi
Il DN e la duplicazione cellulare Il DN, materiale ereditario Struttura del DN Replicazione del DN Dal DN alla proteina Il odice genetico iclo cellulare Mitosi Meiosi Da Figura 8-11 ampbell & Reece cidi
L APPARATO CIRCOLATORIO
 L APPARATO CIRCOLATORIO Tutte le cellule del nostro corpo hanno bisogno di sostanze nutritive e di ossigeno per svolgere le loro funzioni vitali. Così, esiste il sangue, un tessuto fluido che porta in
L APPARATO CIRCOLATORIO Tutte le cellule del nostro corpo hanno bisogno di sostanze nutritive e di ossigeno per svolgere le loro funzioni vitali. Così, esiste il sangue, un tessuto fluido che porta in
Il magnetismo nella materia
 Le orbite degli elettroni in atomo di idrogeno Forma spaziale degli Orbitali elettronici di atomo di idrogeno Un solido Il magnetismo nella materia ferrimagnetismo Dr. Daniele Di Gioacchino Istituto Nazionale
Le orbite degli elettroni in atomo di idrogeno Forma spaziale degli Orbitali elettronici di atomo di idrogeno Un solido Il magnetismo nella materia ferrimagnetismo Dr. Daniele Di Gioacchino Istituto Nazionale
Legami chimici. Covalente. Legami deboli
 Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
Dal DNA alle proteine: La trascrizione e la traduzione
 Dal DNA alle proteine: La trascrizione e la traduzione DNA RNA Trascrizione RNA PROTEINE Traduzione Dove avvengono? GLI EUCARIOTI I PROCARIOTI Cambell, Reece Biologia ZANICHELLI Trascrizione Sintesi di
Dal DNA alle proteine: La trascrizione e la traduzione DNA RNA Trascrizione RNA PROTEINE Traduzione Dove avvengono? GLI EUCARIOTI I PROCARIOTI Cambell, Reece Biologia ZANICHELLI Trascrizione Sintesi di
Metabolismo degli amminoacidi. Ciclo dell urea
 Metabolismo degli amminoacidi Ciclo dell urea Biosintesi di amminoacidiporfirine, creatina, carnitina, ormoni, nucleotidi Gli amminoacidi possono subire una degradazione ossidativa in 3 diverse situazioni
Metabolismo degli amminoacidi Ciclo dell urea Biosintesi di amminoacidiporfirine, creatina, carnitina, ormoni, nucleotidi Gli amminoacidi possono subire una degradazione ossidativa in 3 diverse situazioni
amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente
 Gli amminoacidi naturali sono α-amminoacidi : il gruppo amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente formula generale: gruppo funzionale carbossilico
Gli amminoacidi naturali sono α-amminoacidi : il gruppo amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente formula generale: gruppo funzionale carbossilico
Si tratta di corpiccioli di natura ribonucleoproteica che nel citoplasma di tutte le cellule presiedono ai processi di sintesi proteica.
 I R I BOSOM I I RIBOSOMI sono organuli citoplasmatici presenti in tutte le cellule, sia procariotiche che eucariotiche. Sono visibili al M.O. solo quando presenti in gran numero, (come capita nelle cellule
I R I BOSOM I I RIBOSOMI sono organuli citoplasmatici presenti in tutte le cellule, sia procariotiche che eucariotiche. Sono visibili al M.O. solo quando presenti in gran numero, (come capita nelle cellule
PROTEINE. Amminoacidi
 PROTEINE Le proteine sono le macromolecole alla base delle attività cellulari. Sono oltre diecimila per cellula, dove svolgono differenti funzioni: Sono ad esempio: enzimi: aumentano la velocità delle
PROTEINE Le proteine sono le macromolecole alla base delle attività cellulari. Sono oltre diecimila per cellula, dove svolgono differenti funzioni: Sono ad esempio: enzimi: aumentano la velocità delle
Valitutti, Taddei, Kreuzer, Massey, Sadava, Hills, Heller, Berenbaum
 Dal carbonio agli OGM VERSO L UNIVERSITÀ Le domande sono tratte dalle prove di ammissione emesse annualmente dal Ministero dell Istruzione, dell Università e della Ricerca (MIUR) e le soluzioni sono evidenziate
Dal carbonio agli OGM VERSO L UNIVERSITÀ Le domande sono tratte dalle prove di ammissione emesse annualmente dal Ministero dell Istruzione, dell Università e della Ricerca (MIUR) e le soluzioni sono evidenziate
Attori principali nei TCRS. Processi biologici in cui sono coinvolti sistemi a due componenti. Numero di TCRS nel genoma batterico
 rocessi biologici in cui sono coinvolti sistemi a due componenti Utilizzazione di elementi necessari alla crescita (azoto); NtrC Virulenza (BvgAS di Bordetella pertussis) Resistenza a metalli pesanti (pco)
rocessi biologici in cui sono coinvolti sistemi a due componenti Utilizzazione di elementi necessari alla crescita (azoto); NtrC Virulenza (BvgAS di Bordetella pertussis) Resistenza a metalli pesanti (pco)
Vettori di espressione
 Vettori di espressione Vengono usati per: 1.Generare sonde di RNA 2.Produrre la proteina codificata Per fare questo viene utilizzato un promotore che risiede sul vettore, modificato per ottimizzare l interazione
Vettori di espressione Vengono usati per: 1.Generare sonde di RNA 2.Produrre la proteina codificata Per fare questo viene utilizzato un promotore che risiede sul vettore, modificato per ottimizzare l interazione
glicogeno Glucosio 6-P Piruvato Acetil CoA Intermedi del ciclo di Krebs
 PIRUVAT glicogeno Glicogeno sintesi glicogenolisi Glucosio Glucosio 6-P Ribosio 5-P glicolisi Gluconeogenesi Amino acidi Piruvato Acetil CoA lattato Intermedi del ciclo di Krebs Concentrazione di glicogeno
PIRUVAT glicogeno Glicogeno sintesi glicogenolisi Glucosio Glucosio 6-P Ribosio 5-P glicolisi Gluconeogenesi Amino acidi Piruvato Acetil CoA lattato Intermedi del ciclo di Krebs Concentrazione di glicogeno
Prof.ssa Gamba Sabrina. Lezione 7: IL DNA. Duplicazione e sintesi delle proteine
 Prof.ssa Gamba Sabrina Lezione 7: IL DNA Duplicazione e sintesi delle proteine concetti chiave della lezione Costituzione fisico-chimica del DNA Basi azotate Duplicazione Concetto di geni Rna Trascrizione
Prof.ssa Gamba Sabrina Lezione 7: IL DNA Duplicazione e sintesi delle proteine concetti chiave della lezione Costituzione fisico-chimica del DNA Basi azotate Duplicazione Concetto di geni Rna Trascrizione
