STRUTTURA. Composti organici costituiti da sequenze di aminoacidi. < 30 aa aa. Aminoacidi aa OLIGOPEPTIDI PROTEINE POLIPEPTIDI
|
|
|
- Costantino Pagani
- 7 anni fa
- Visualizzazioni
Transcript
1 PROTEINE dal greco proteios primario Strutture molecolari più rilevanti sia dal punto di vista funzionale che quantitativo degli esseri viventi costituendo circa il 15 % della massa totale.
2 FUNZIONI Catalisi enzimatica Trasporto (emoglobina, albumina, lipoproteine, proteine di membrana) Protezione (immunoglobuline) Coagulazione (fribinogeno) Contrazione (actina, miosina) Ormonale (insulina, glucagone, vasopressina, testosterone) Trasmissione impulsi nervosi (acetilcolina, noradrenalina) Strutturale (collagene, elastina, cheratina..) Regolazione dell espressione genica (induttori, repressori) Organizzazione del DNA nei cromosomi (nucleoproteine)
3 STRUTTURA Composti organici costituiti da sequenze di aminoacidi < 30 aa Aminoacidi aa OLIGOPEPTIDI + 30 aa PROTEINE POLIPEPTIDI
4 AMINOACIDI unità strutturali delle proteine gruppo aminico R I + NH 3 - C - COO - I H caratteristico di ogni a.a. gruppo carbossilico
5 AMINOACIDI PROTEICI sono circa una ventina, ma legandosi in un elevato numero di combinazioni riescono a formare l enorme varietà di proteine esistenti AMINOACIDI NON PROTEICI Non si trovano mai nella composizione delle proteine. Sono composti intermedi di reazioni metaboliche (es. ornitina dal ciclo dell urea; omocisteina da cui deriva la metionina, etc )
6 AMINOACIDI PROTEICI Gli aminoacidi possono essere classificati in base alla loro carica elettrica e all affinità per l acqua della loro catena laterale. Avremo cosi aminoacidi: - con carica positiva - con carica negativa - neutri polari (senza carica e idrofilici) - neutri apolari (senza carica e idrofobici)
7 AMINOACIDI PROTEICI Neutri apolari Neutri polari Basici(carica-) Acidi(carica+) Alanina Glicina Lisina Aspartato Valina Serina Arginina Glutammato Leucina Treonina Istidina Isoleucina Cisteina Metionina Asparagina Fenilalanina Glutamina Triptofano Tirosina * aminoacidi essenziali * aminoacidi semiessenziali (fanno risparmiare Metionina e Fenilalanina) * aminoacidi condizionatamente essenziali (in condizioni fisiologiche particolari quando non sono sintetizzati a velocità sufficiente; substrato energetico di macrofagi e linfociti responsabili delle difese immunitarie) Valina, Leucina, Isoleucina: a.a. ramificati; substrato energetico a livello muscolare con risparmio delle scorte di glicogeno
8 ingombro sterico dei gruppi R affinità tra i gruppi polari ed apolari attrazione tra gruppi acidi e basici modellano la conformazione delle proteine nello spazio dalle quali dipende in modo essenziale l attività biologica delle proteine stesse
9 Il legame chimico che unisce 2 aminoacidi (monomeri) a formare un polimero (oligopeptide, polipeptide o proteina) è detto legame peptidico e si instaura tra il gruppo aminico ( -NH 3 + ) di un aa ed il gruppo carbossilico (- COO - ) di un altro aa, con liberazione di una molecola d acqua. Le reazioni che producono legami covalenti tra monomeri e che liberano una molecola d acqua per ogni legame covalente formato vengono chiamate reazioni di condensazione. Una singola catena di aa è chiamata polipeptide (oligopeptide se composta da meno di 30 aa). Ogni polipeptide ha un gruppo aminico libero (estremità N- terminale) e un gruppo carbossilico libero all altra (estremità C-terminale).
10 LEGAME PEPTIDICO + NH 3 CHR 1 COO - + NH 3 CHR 2 COO - Legame peptidico H 2 O O II + NH 3 CHR 1 C N CHR 2 COO - I H
11
12 STRUTTURA DELLE PROTEINE La maggior parte delle proteine è costituita da più di una catena polipeptidica. Anche se una proteina potrebbe assumere un grande numero di forme diverse, dette conformazioni, la maggior parte delle catene peptidiche si ripiega in una determinata, (la sua unica) conformazione detta nativa. Uno degli elementi che più incidono sulle modalità di ripiegamento di una proteina è la distribuzione delle catene laterali polari e non polari. Le catene laterali idrofobe tendono a rimanere all interno della proteina, in modo da evitare il contatto con l ambiente acquoso, mentre le catene polari (idrofiliche) stanno all esterno, dove reagiscono con altri gruppi polari o con l acqua.
13 STRUTTURA DELLE PROTEINE Nella struttura delle proteine sono individuabili 4 livelli di organizzazione.
14 1. Struttura primaria : sequenza lineare di aminoacidi
15 2. Struttura secondaria Ripiegamento delle catene 1 ie in strutture regolari (α-elica o foglietto β) a dare una configurazione tridimensionale necessaria per lo svolgimento dell attività biologica della proteina stessa conformazione a spirale α - elica conformazione β foglietto pieghettato legami idrogeno
16 3. Struttura terziaria Ulteriore ripiegamento ed avvolgimento della catena polipeptidica 2 ia (mantenuto da interazioni elettrostatiche, idrofobiche e legami ad idrogeno) in una conformazione più stabile e compatta detta dominio. Proteine globulari (regolatorie) albumine (trasporto acidi grassi) α-globuline (protrombina, VLDL,LDL) β-globuline (transferrina, HDL) γ-globuline (immunoglobuline) istoni (organizzazione del DNA) Proteine fibrose (strutturali) collagene: tendini resistenza alla tensione elastina: vene, arterie e polmoni estensione e deformazione senza danni per i tessuti
17 4. Struttura quaternaria diverse catene polipeptidiche in str. 3 ia tenute insieme da forze elettrostatiche si associano a formare una singola proteina Emoglobina 4 subunità proteiche ognuna associata ad un gruppo EME (anello al cui interno c è lo ione ferroso che lega l ossigeno)
18
19 PROTEINE CONIUGATE Quando la proteina è associata ad altre molecole organiche o gruppi chimici Glicoproteine (responsabili del riconoscimento antigenico e dei rapporti intercellulari, ormoni ipofisari, globuline) Lipoproteine (VLDL, LDL, HDL) Fosfoproteine (dentina e caseina) Cromoproteine (mioglobina, emoglobina)
20 FUNZIONE ENZIMATICA DELLE PROTEINE Gli enzimi catalitici sono proteine in grado di accelerare la velocità di una reazione senza alterarne l equilibrio, senza entrare a far parte dei prodotti della reazione stessa e senza risultare alterate al termine del processo. Viene chiamato substrato la sostanza che subisce una trasformazione durante la reazione catalizzata dall enzima L enzima possiede un sito di legame che riconosce e lega il substrato e un sito catalitico che lo catalizza. Il legame enzima-substrato può avvenire secondo 2 modalità:
21 chiave-serratura : enzima e substrato risultano essere complementari per forma e carica elettrica adesione indotta : il substrato induce l enzima ad un cambio conformazionale che renda possibile il legame e la conseguente reazione catalitica substrato sito attivo L enzima cambia conformazione man mano che il substrato si lega prodotti Ingresso del substrato nel sito attivo dell enzima Complesso enzima-substrato Complesso enzima-prodotti Uscita dei prodotti dal sito attivo dell enzima
22 L attività catalitica degli enzimi non è costante né riguardo il numero né riguardo il tipo di reazioni che avvengono, ma viene regolata in base alle necessità metaboliche della cellula. Spesso un enzima che catalizza una reazione viene inibito o attivato dal prodotto ultimo della reazione mediante un meccanismo di feed-back (retroazione) negativo o positivo. inibitore enzima Inibizione competitiva L enzima lega l inibitore L inibitore compete con il substrato Gli enzimi spesso contengono piccole molecole strettamente legate dette coenzimi, cofattori enzimatici di natura organica, che aiutano gli enzimi ad esplicitare la loro attività catalitica. La maggior parte degli enzimi ha suffisso in asi (ligasi, liasi, etc) e derivano dal nome della sostanza su cui agisce l enzima (substrato) e dal nome della reazione che catalizza (es. malico deidrogenasi).
23 ACIDI NUCLEICI Macromolecole di grande complessità chiamate così perché sono collocate nel nucleo delle cellule. L unità di base è il NUCLEOTIDE radicale fosforico A adenina G guanina C citosina T timina U uracile zucchero pentoso ribosio o desossiribosio
24 DNA Zucchero: desossiribosio Gruppo fosfato Basi: adenina guanina citosina timina RNA Zucchero: ribosio Gruppo fosfato Basi: adenina guanina citosina uracile
25 Basi azotate Sono suddivise in due gruppi a seconda della loro struttura: PURINE Costituite da due anelli appaiati A = adenina G = guanina PIRIMIDINE Costituite da un solo anello C = citosina T = timina (solo nel DNA) U = uracile (solo nel RNA) Nucleoside = base azotata + zucchero pentoso Nucleotide = base azotata + zucchero pentoso + gr. fosfato
26 DNA acido desossiribonucleico Trasmissione dell informazione genetica Non esce mai dal nucleo MODEDLLO A DOPPIA ELICA 2 filamenti nucleotidici paralleli Il collegamento avviene tra le basi complementari dei due filamenti che si abbinano a coppie esclusive A T C G
27 RNA acido ribonucleico Trasporta fuori dal nucleo le informazioni genetiche dopo averle ricopiate dal DNA È responsabile della sintesi delle proteine MODEDLLO A SINGOLA ELICA 1 solo filamento di nucleotidi
28 RNA acido ribonucleico RNA messaggero mrna singolo filamento complementare di DNA trasferisce fuori dal nucleo le informazioni genetiche RNA di trasporto trna trasporta gli aminoacidi nella sintesi proteica RNA ribosomiale rrna insieme a proteine costituisce i ribosomi dove avviene la sintesi proteica
29 I nucleotidi, sono altresì molecole in grado di fornire energia a tutte quelle reazioni di sintesi che lo richiedono (sintesi delle proteine, degli ac.nucleici, dei polisaccaridi, etc ) perciò entrano nella composizione anche di ATP adenosin trifosfato accumulatore di energia NADP nicotinamide-adenindinucleotide fosfato trasporto di ioni H + FAD flavin-adenin-dinucleotide trasporto di ioni H +
30 VITAMINE Composti organici eterogenei necessari in dose minime, ma indispensabili per la sopravvivenza delle cellule no valore energetico ottenibili attraverso una dieta equilibrata bioregolatori (cofattori enzimatici) fattori di crescita (A, D) strutture nervose (B, PP) resistenza ad infezioni e radicali liberi (A, C, E) protezione della pelle prevenzione da tumori suddivise in 2 gruppi a seconda della solubilità in acqua o nei grassi LIPOSOLUBILI IDROSOLUBILI
31 K E tocoferolo D ergocalciferolo A retinolo VITAMINE LIPOSOLUBILI VIT. PRINCIPALI FUNZIONI SINTOMI DA CARENZA PRINCIPALI FONTI ALIMENTARI Interviene nel meccanismo della visione, favorisce il mantenimento degli epiteli, immunostimolante, protegge dal cancro Anemia, diarrea, cecità notturna, depressione del sistema immunitario, lesioni oculari Fegato, uova, burro, spinaci ed altri vegetali a foglie verde scuro, broccoli, meloni, albicocche, carote ed altri frutti color arancio Mineralizzazione delle ossa e corretta utilizzazione del calcio e del fosforo Rachitismo nel bambino e fragilità ossea nell adulto Fegato, uova, pesce azzurro (sardine). Proviene anche dalla sintesi endogena del colesterolo Antiossidante, blocca la formazione dei radicali liberi, protegge le membrane cellulari Anemia, debolezza, crampi Olii vegetali non raffinati, germe di grano, semi, noci, vegetali a foglia verde Interviene nel meccanismo della coagulazione del sangue, antiemorragica Emorragie o ritardato tempo di coagulazione Broccoli, cavoli, vegetali a foglia verde, fegato. Viene anche sintetizzata dai batteri del tratto intestinale.
32 B6 piridossina B5 acido pantotenico B3/PP niacina B2 riboflavina B1 tiamina VITAMINE IDROSULUBILI VIT. PRINCIPALI FUNZIONI SINTOMI DA CARENZA PRINCIPALI FONTI ALIMENTARI Cofattore nel metabolismo energetico dei carboidrati, stimola l appetito e le funzioni del sistema nervoso Problemi cardiaci, inappetenza, debolezza, insonnia, irritabilità degenerazione del sistema nervoso Presente in moltissimi alimenti, soprattutto cereali integrali, legumi, maiale, noci È in molteplici reazioni metaboliche, aiuta la visione e la pelle Lingua magenta, ferite agli angoli della bocca, arrossamento degli occhi Latte e derivati, carne, cereali integrali, vegetali verdi Coenzima nella respirazione cellulare(componente del NADP), aiuta la pelle e i sistemi digerente e nervoso Diarrea, debolezza, alterazioni mentali fino al delirio, glossite, pellagra Olatte, carne, uova,pesce, cereali integrali,frutta secca ed altri alimenti proteici Costituisce il coenzima A utilizzato nel metabolismo energetico Insonnia, vomito, disturbi intestinali Largamente diffuso negli alimenti Ha un ruolo essenziale nella regolazione del metabolismo delle proteine e dei grassi ed è la più importante per il sistema immunitario, regolazione dell umore. Anemia, glossite, irritabilità, convulsioni, deterioramento dell immunità umorale e cellulo-mediata Cereali integrali, vegetali verdi, legumi, carne, pesce
33 C acido ascorbico H biotina B12 cobalamina B9 acido folico VITAMINE IDROSULUBILI VIT. PRINCIPALI FUNZIONI SINTOMI DA CARENZA PRINCIPALI FONTI ALIMENTARI Ha un ruolo importante nella formazione dell emoglobina ed azione stimolante sul sistema immunitario Disturbi intestinali, depressione del sistema immunitario, anemia megaloblastica, confusione mentale, spina bifida nel feto Vegetali a foglia verde, legumi, semi, fegato Fa parte di un coenzima utilizzato nella sintesi di nuove cellule. Interviene nella formazione dei globuli rossi. Anemia, glossite, affaticamento, degenerazione del sistema nervoso, depressione Alimenti di origine animale: carne, pesce, latte, formaggi, uova Fa parte di un coenzima utilizzato nel metabolismo dei grassi e dei carboidrati e coinvolto nella sintesi degli aminoacidi Inappetenza, nausea, depressione, debolezza, perdita di capelli, dermatiti, anomala attività cardiaca Largamente diffusa negli alimenti, in modo particolare in: legumi, uova, fegato, funghi, cacao, mandorle. Antiossidante, interviene nelle sintesi del collagene e della tiroxina, aumenta la resistenza alle infezioni, aiuta l assorbimento del ferro, contrasta lo stress. Frequenti infezioni, anemia, gengive sanguinanti, depressione, fragilità capillare e ossea, scorbuto Agrumi, broccoli, cavoli, melone, fragole, kiwi, pomodori, papaia, mango, peperoni, patate, lattuga.
ACIDI GRASSI INSATURI
 LIPIDI ACIDI GRASSI SATURI ACIDI GRASSI INSATURI TRIGLICERIDI TRIGLICERIDI Grassi neutri o lipidi semplici glicerolo + 1 acido grasso monogliceride glicerolo + 2 acidi grassi digliceride glicerolo + 3
LIPIDI ACIDI GRASSI SATURI ACIDI GRASSI INSATURI TRIGLICERIDI TRIGLICERIDI Grassi neutri o lipidi semplici glicerolo + 1 acido grasso monogliceride glicerolo + 2 acidi grassi digliceride glicerolo + 3
Il carbonio è l elemento di base delle biomolecole. Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici.
 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici. 1 Il carbonio deve acquistare quattro elettroni per essere stabile
Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici. 1 Il carbonio deve acquistare quattro elettroni per essere stabile
Immagini e concetti della biologia
 Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
Vitamine: aspetti generali
 7.4 Le vitamine Vitamine: aspetti generali Le vitamine si caratterizzano perché: - sono composti organici di piccole dimensioni - sono presenti negli alimenti in piccole quantità come vitamine vere e proprie,
7.4 Le vitamine Vitamine: aspetti generali Le vitamine si caratterizzano perché: - sono composti organici di piccole dimensioni - sono presenti negli alimenti in piccole quantità come vitamine vere e proprie,
La massa è la quantità di materia di cui è fatta una qualsiasi cosa
 Dall atomo all organizzazione cellulare Tutti gli organismi viventi sono costituiti da atomi Due o più atoni insieme formano le molecole La materia è tutto ciò che occupa uno spazio, ha un volume e una
Dall atomo all organizzazione cellulare Tutti gli organismi viventi sono costituiti da atomi Due o più atoni insieme formano le molecole La materia è tutto ciò che occupa uno spazio, ha un volume e una
Le molecole biologiche. Sylvia S. Mader Immagini e concetti della biologia Zanichelli editore, 2012
 Le molecole biologiche 1 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici. 2 Il carbonio deve acquistare quattro elettroni
Le molecole biologiche 1 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici. 2 Il carbonio deve acquistare quattro elettroni
Jay Phelan, Maria Cristina Pignocchino. Scopriamo la biologia
 Jay Phelan, Maria Cristina Pignocchino Scopriamo la biologia Capitolo 2 Le molecole della vita 3 1. Le classi delle biomolecole Le biomolecole sono composti organici formati da: catene di atomi di carbonio,
Jay Phelan, Maria Cristina Pignocchino Scopriamo la biologia Capitolo 2 Le molecole della vita 3 1. Le classi delle biomolecole Le biomolecole sono composti organici formati da: catene di atomi di carbonio,
Le biomolecole si trovano negli organismi viventi
 Le biomolecole si trovano negli organismi viventi I viventi sono formati per la maggior parte da acqua e molecole, chiamate biomolecole. Le biomolecole sono sostanze contenenti carbonio. I composti del
Le biomolecole si trovano negli organismi viventi I viventi sono formati per la maggior parte da acqua e molecole, chiamate biomolecole. Le biomolecole sono sostanze contenenti carbonio. I composti del
a) un movimento contro gradiente di concentrazione che utilizza fonti primarie di energia
 1. Quale considerazione sulla struttura primaria di una proteina è vera? a) è caratteristica delle proteine insolubili b) i ponti S-S la stabilizzano c) i ponti H la stabilizzano d) la proteina assume
1. Quale considerazione sulla struttura primaria di una proteina è vera? a) è caratteristica delle proteine insolubili b) i ponti S-S la stabilizzano c) i ponti H la stabilizzano d) la proteina assume
I materiali della vita
 I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
Biologia. Lezione 09/11/2010
 Biologia Lezione 09/11/2010 Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono macromolecole formate da unità (MONOMERI)
Biologia Lezione 09/11/2010 Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono macromolecole formate da unità (MONOMERI)
I PROTIDI ASPETTI GENERALI
 I PROTIDI ASPETTI GENERALI I PROTIDI O PROTEINE SONO SOSTANZE ORGANICHE AZOTATE, DI STRUTTURA MOLTO COMPLESSA, PRESENTI IN OGNI FORMA DI VITA. LE PROTEINE SONO COMPOSTI QUATERNARI, OSSIA SONO FORMATE DA
I PROTIDI ASPETTI GENERALI I PROTIDI O PROTEINE SONO SOSTANZE ORGANICHE AZOTATE, DI STRUTTURA MOLTO COMPLESSA, PRESENTI IN OGNI FORMA DI VITA. LE PROTEINE SONO COMPOSTI QUATERNARI, OSSIA SONO FORMATE DA
Schemi delle lezioni 1
 Schemi delle lezioni 1 Detti anche proteine sono i composti organici maggiormente presenti nelle cellule, dato che costituiscono circa il 50% del loro peso secco. Nell uomo adulto rappresentano circa
Schemi delle lezioni 1 Detti anche proteine sono i composti organici maggiormente presenti nelle cellule, dato che costituiscono circa il 50% del loro peso secco. Nell uomo adulto rappresentano circa
Le molecole della vita
 Le molecole della vita Introduzione: cose da sapere per capire. Gli atomi (es. carbonio, ossigeno, idrogeno) si uniscono a formare molecole Le molecole costituiscono tutta la materia che ci circonda Atomi
Le molecole della vita Introduzione: cose da sapere per capire. Gli atomi (es. carbonio, ossigeno, idrogeno) si uniscono a formare molecole Le molecole costituiscono tutta la materia che ci circonda Atomi
La chimica della vita
 La chimica della vita La materia presente nell universo è formata da 92 elementi Gli elementi si legano tra loro per formare le molecole che costituiscono i composti Legame covalente O H H Molecola Composto
La chimica della vita La materia presente nell universo è formata da 92 elementi Gli elementi si legano tra loro per formare le molecole che costituiscono i composti Legame covalente O H H Molecola Composto
sono le unità monomeriche che costituiscono le proteine hanno tutti una struttura comune
 AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
Alimentazione corretta
 Alimentazione corretta LE VITAMINE LE VITAMINE LE VITAMINE LE VITAMINE I CARBOIDRATI I SALI MINERALI I SALI MINERALI I SALI MINERALI I SALI MINERALI I LIPIDI LE PROTEINE ACQUA VITAMINA ALIMENTI FUNZIONE
Alimentazione corretta LE VITAMINE LE VITAMINE LE VITAMINE LE VITAMINE I CARBOIDRATI I SALI MINERALI I SALI MINERALI I SALI MINERALI I SALI MINERALI I LIPIDI LE PROTEINE ACQUA VITAMINA ALIMENTI FUNZIONE
Composti organici. I composti organici. Atomi e molecole di carbonio. Atomi e molecole di carbonio. Gruppi funzionali. Isomeri
 I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA)
 La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) POLIMERI Le cellule sintetizzano un enorme numero di grosse molecole a partire da una ristretta serie di
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) POLIMERI Le cellule sintetizzano un enorme numero di grosse molecole a partire da una ristretta serie di
Le proteine o protidi
 Le proteine o protidi A differenza di glucidi e lipidi (che di regola non contengono azoto), le proteine sono composti organici quaternari, che possiedono sempre atomi di azoto nella loro molecola (quasi
Le proteine o protidi A differenza di glucidi e lipidi (che di regola non contengono azoto), le proteine sono composti organici quaternari, che possiedono sempre atomi di azoto nella loro molecola (quasi
CARBOIDRATI C H O ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO
 CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
Principi nutritivi. carboidrati, proteine e grassi.
 Principi nutritivi carboidrati, proteine e grassi L organismo umano è simile a un motore e, come questo per funzionare ha bisogno di combustibile ed ossigeno: il combustibile è fornito dagli alimenti,
Principi nutritivi carboidrati, proteine e grassi L organismo umano è simile a un motore e, come questo per funzionare ha bisogno di combustibile ed ossigeno: il combustibile è fornito dagli alimenti,
Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi. Possono assumere forme diverse a seconda della funzione
 Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi Hanno elevato PM Possono assumere forme diverse a seconda della funzione svolgono molteplici funzioni Tra le proteine
Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi Hanno elevato PM Possono assumere forme diverse a seconda della funzione svolgono molteplici funzioni Tra le proteine
Somministrazione o assunzione di alimenti allo scopo di nutrire l organismo
 Definizioni Alimentazione Somministrazione o assunzione di alimenti allo scopo di nutrire l organismo Nutrizione complesso di processi biologici che consentono o condizionano la conservazione, l accrescimento,
Definizioni Alimentazione Somministrazione o assunzione di alimenti allo scopo di nutrire l organismo Nutrizione complesso di processi biologici che consentono o condizionano la conservazione, l accrescimento,
L ACQUA E LE SUE PROPRIETÀ
 L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
Sali minerali negli alimenti
 1 SALI MINERALI Sali minerali elementi inorganici. Sono necessari in piccole quantità (mg o mcg). Non forniscono calorie. Costituiscono circa il 4% in peso del corpo umano. Svolgono sia un azione plastica
1 SALI MINERALI Sali minerali elementi inorganici. Sono necessari in piccole quantità (mg o mcg). Non forniscono calorie. Costituiscono circa il 4% in peso del corpo umano. Svolgono sia un azione plastica
Vittoria Patti MACROMOLECOLE BIOLOGICHE. 4. proteine
 Vittoria Patti MACROMOLECOLE BIOLOGICHE 4. proteine 1 Funzioni principali delle proteine funzione cosa significa esempi ENZIMATICA STRUTTURALE TRASPORTO MOVIMENTO DIFESA IMMUNITARIA ORMONALE catalizzare
Vittoria Patti MACROMOLECOLE BIOLOGICHE 4. proteine 1 Funzioni principali delle proteine funzione cosa significa esempi ENZIMATICA STRUTTURALE TRASPORTO MOVIMENTO DIFESA IMMUNITARIA ORMONALE catalizzare
Introduzione alla biologia della cellula. Lezione 2 Le biomolecole
 Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
Vitamine liposolubili
 Vitamine liposolubili Vitamine liposolubili A Q D F E K Vitamine liposolubili Queste vitamine sono accomunate dal fatto di essere solubili esclusivamente nei grassi e nei solventi dei grassi; il loro assorbimento,
Vitamine liposolubili Vitamine liposolubili A Q D F E K Vitamine liposolubili Queste vitamine sono accomunate dal fatto di essere solubili esclusivamente nei grassi e nei solventi dei grassi; il loro assorbimento,
STRUTTURA E FUNZIONE DELLE PROTEINE
 STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
BIOMOLECOLE (PROTEINE)
 BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
Struttura degli amminoacidi
 AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
 http://digilander.libero.it/glampis64 Idrogeno, ossigeno, carbonio e azoto costituiscono il 99% delle cellule. I composti del carbonio sono chiamati composti organici o molecole organiche. I composti organici
http://digilander.libero.it/glampis64 Idrogeno, ossigeno, carbonio e azoto costituiscono il 99% delle cellule. I composti del carbonio sono chiamati composti organici o molecole organiche. I composti organici
LE BUONE VITAMINE PER I BAMBINI
 LE BUONE VITAMINE PER I BAMBINI Una corretta alimentazione, che sia il più possibile varia, anche per i bambini è un fattore necessario per una crescita sana. Il corpo non è in grado di sintetizzare autonomamente
LE BUONE VITAMINE PER I BAMBINI Una corretta alimentazione, che sia il più possibile varia, anche per i bambini è un fattore necessario per una crescita sana. Il corpo non è in grado di sintetizzare autonomamente
Formula generale di un amminoacido
 Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
CPIA 1 FOGGIA punto di erogazione San Severo. Prof.ssa ANNA LUCIA L. CANCELLIERE
 CPIA 1 FOGGIA punto di erogazione San Severo Prof.ssa ANNA LUCIA L. CANCELLIERE Sono delle grandi molecole che troviamo nel mondo dei viventi sia come molecole costituenti gli organismi viventi che come
CPIA 1 FOGGIA punto di erogazione San Severo Prof.ssa ANNA LUCIA L. CANCELLIERE Sono delle grandi molecole che troviamo nel mondo dei viventi sia come molecole costituenti gli organismi viventi che come
Indice generale 1. Introduzione alla biochimica 2. Acqua, ph, acidi, basi, sali, tamponi
 Indice generale 1. Introduzione alla biochimica 1 Unità di misura 1 Energia e calore 3 Struttura dell atomo 3 Tavola periodica degli elementi 4 Legami chimici 8 Legami covalenti 8 Legami non covalenti
Indice generale 1. Introduzione alla biochimica 1 Unità di misura 1 Energia e calore 3 Struttura dell atomo 3 Tavola periodica degli elementi 4 Legami chimici 8 Legami covalenti 8 Legami non covalenti
Proteine: struttura e funzione
 Proteine: struttura e funzione Prof.ssa Flavia Frabetti PROTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (C, H, O,
Proteine: struttura e funzione Prof.ssa Flavia Frabetti PROTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (C, H, O,
Percorsi di chimica organica - Soluzioni degli esercizi del testo
 ercorsi di chimica organica - Soluzioni degli esercizi del testo AITL 14 1. Il prefisso α negli α-amminoacidi sta ad indicare che il gruppo amminico, - 2, si trova sul carbonio alfa (carbonio legato al
ercorsi di chimica organica - Soluzioni degli esercizi del testo AITL 14 1. Il prefisso α negli α-amminoacidi sta ad indicare che il gruppo amminico, - 2, si trova sul carbonio alfa (carbonio legato al
Gli acidi nucleici, DNA (acido deossiribonucleico) e RNA (acido. ribonucleico), sono polimeri biologicamente importanti in quanto
 Gli acidi nucleici, DA (acido deossiribonucleico) e RA (acido ribonucleico), sono polimeri biologicamente importanti in quanto svolgono ruoli fondamentali nell ereditarietà e nella sintesi proteica. Sono
Gli acidi nucleici, DA (acido deossiribonucleico) e RA (acido ribonucleico), sono polimeri biologicamente importanti in quanto svolgono ruoli fondamentali nell ereditarietà e nella sintesi proteica. Sono
Nucleotidi e acidi nucleici
 Nucleotidi e acidi nucleici ACIDI NUCLEICI Biomolecole fondamentali per tutti gli organismi viventi Unici nella capacità di autoduplicazione Conservazione e trasmissione da una generazione all altra dell
Nucleotidi e acidi nucleici ACIDI NUCLEICI Biomolecole fondamentali per tutti gli organismi viventi Unici nella capacità di autoduplicazione Conservazione e trasmissione da una generazione all altra dell
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
Costituenti chimici della materia vivente
 Costituenti chimici della materia vivente Le macromolecole biologiche Macromolecole (dal greco macros = grande) biologiche. Classi di composti biologici multifunzionali: Polisaccaridi proteine acidi
Costituenti chimici della materia vivente Le macromolecole biologiche Macromolecole (dal greco macros = grande) biologiche. Classi di composti biologici multifunzionali: Polisaccaridi proteine acidi
LE PROTEINE SINTESI PROTEICA. funzione delle proteine nel nostro organismo
 LE PTEIE Le proteine sono sostanze organiche presenti in tutte le cellule di tutti gli organismi viventi Le proteine sono costituite da,,,, (S) Struttura delle proteine Le proteine sono macromolecole (
LE PTEIE Le proteine sono sostanze organiche presenti in tutte le cellule di tutti gli organismi viventi Le proteine sono costituite da,,,, (S) Struttura delle proteine Le proteine sono macromolecole (
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA)
 La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) L atomo del carbonio (C).. C. Atomo tetravalente. C C C C Gli idrocarburi I legami del carbonio 109.5 gradi
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) L atomo del carbonio (C).. C. Atomo tetravalente. C C C C Gli idrocarburi I legami del carbonio 109.5 gradi
Introduzione alla biologia della cellula. Lezione 3 Le biomolecole DNA e RNA
 Introduzione alla biologia della cellula Lezione 3 Le biomolecole DNA e RNA Acidi nucleici DNA (acido desossiribonucleico) RNA (acido ribonucleico) Sono polimeri di monomeri detti NUCLEOTIDI Un nucleotide
Introduzione alla biologia della cellula Lezione 3 Le biomolecole DNA e RNA Acidi nucleici DNA (acido desossiribonucleico) RNA (acido ribonucleico) Sono polimeri di monomeri detti NUCLEOTIDI Un nucleotide
 http://digilander.libero.it/glampis64 I composti organici di interesse biologico sono: Carboidrati Proteine Lipidi Acidi nucleici Le macromolecole sono composti di grandi dimensioni, unione di piccole
http://digilander.libero.it/glampis64 I composti organici di interesse biologico sono: Carboidrati Proteine Lipidi Acidi nucleici Le macromolecole sono composti di grandi dimensioni, unione di piccole
SOLUZIONI DEGLI ESERCIZI
 Dal carbonio agli OGM Biochimica e biotecnologie SOLUZIONI DEGLI ESERCIZI Capitolo 0 Il mondo del carbonio 1. b, e 2. d 3. 7 4. 5. 6. 7. a) Isomeria di posizione; b) i due composti non sono isomeri; c)
Dal carbonio agli OGM Biochimica e biotecnologie SOLUZIONI DEGLI ESERCIZI Capitolo 0 Il mondo del carbonio 1. b, e 2. d 3. 7 4. 5. 6. 7. a) Isomeria di posizione; b) i due composti non sono isomeri; c)
Proteine strutturali Sostegno meccanico Cheratina: costituisce i capelli Collagene: costituisce le cartilagini Proteine di immagazzinamento
 Tipo Funzione Esempi Enzimi Accelerano le reazioni chimiche Saccarasi: posiziona il saccarosio in modo che possa essere scisso nelle due unità di glucosio e fruttosio che lo formano Ormoni Messaggeri chimici
Tipo Funzione Esempi Enzimi Accelerano le reazioni chimiche Saccarasi: posiziona il saccarosio in modo che possa essere scisso nelle due unità di glucosio e fruttosio che lo formano Ormoni Messaggeri chimici
COMPOSTI AZOTATI. derivanti dall ammoniaca AMMINE. desinenza -INA AMMIDE
 COMPOSTI AZOTATI derivanti dall ammoniaca AMMINE desinenza -INA AMMIDE ANCORA AMMIDI RISONANZA A M M I D I Il legame ammidico ha parziale carattere di doppio legame per la seguente risonanza: Ammidi H
COMPOSTI AZOTATI derivanti dall ammoniaca AMMINE desinenza -INA AMMIDE ANCORA AMMIDI RISONANZA A M M I D I Il legame ammidico ha parziale carattere di doppio legame per la seguente risonanza: Ammidi H
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 10 Le basi della biochimica 3 Sommario 1. Le molecole biologiche si dividono in quattro classi 2. I carboidrati sono il «carburante»
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 10 Le basi della biochimica 3 Sommario 1. Le molecole biologiche si dividono in quattro classi 2. I carboidrati sono il «carburante»
Nucleotidi e Acidi Nucleici. Struttura di DNA e RNA
 Nucleotidi e Acidi Nucleici Nucleosidi Nucleotidi Funzioni biologiche dei nucleotidi Struttura di DNA e RNA Concatenazione e appaiamento dei nucleotidi Lo scheletro degli acidi nucleici Componenti degli
Nucleotidi e Acidi Nucleici Nucleosidi Nucleotidi Funzioni biologiche dei nucleotidi Struttura di DNA e RNA Concatenazione e appaiamento dei nucleotidi Lo scheletro degli acidi nucleici Componenti degli
Biochimica. studio della vita a livello molecolare
 Biochimica studio della vita a livello molecolare studio della composizione molecolare dei sistemi viventi studio delle reazioni chimiche cui vanno incontro i sistemi viventi ALCUNI QUESITI DELLA BIOCHIMICA
Biochimica studio della vita a livello molecolare studio della composizione molecolare dei sistemi viventi studio delle reazioni chimiche cui vanno incontro i sistemi viventi ALCUNI QUESITI DELLA BIOCHIMICA
Proteine. Enzimi Fattori di Trascrizione Proteine di Membrana (trasportatori, canale, recettori di membrana)
 Proteine Enzimi Fattori di Trascrizione Proteine di Membrana (trasportatori, canale, recettori di membrana) Ormoni e Fattori di crescita Anticorpi Trasporto Trasporto (emoglobina, LDL, HDL.) Fenotipo Proteine
Proteine Enzimi Fattori di Trascrizione Proteine di Membrana (trasportatori, canale, recettori di membrana) Ormoni e Fattori di crescita Anticorpi Trasporto Trasporto (emoglobina, LDL, HDL.) Fenotipo Proteine
Il carbonio è l elemento più abbondante nelle molecole biologiche
 Le biomolecole Il carbonio è l elemento più abbondante nelle molecole biologiche Le molecole contenenti carbonio sono chiamate biomolecole. Le biomolecole fanno parte di un gruppo molto ampio di composti
Le biomolecole Il carbonio è l elemento più abbondante nelle molecole biologiche Le molecole contenenti carbonio sono chiamate biomolecole. Le biomolecole fanno parte di un gruppo molto ampio di composti
Struttura delle Proteine
 Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
Il metabolismo ATP. concetti di base e disegno generale
 Il metabolismo ATP concetti di base e disegno generale Eg e funzioni cellulari Le cellule necessitano di un costante apporto di Eg per svolgere diverse funzioni: lavoro meccanico lavoro elettrico trasporto
Il metabolismo ATP concetti di base e disegno generale Eg e funzioni cellulari Le cellule necessitano di un costante apporto di Eg per svolgere diverse funzioni: lavoro meccanico lavoro elettrico trasporto
Alcol + alcol etere R-OH + R -OH R-O-R + H 2 O Aldeide + alcol emiacetale R-CHO + R -OH R-CHOH-O-R Acido + Acido anidride R-COOH + R -COOH
 Nomenclatura AMIDI Alcol + alcol etere R-OH + R -OH R-O-R + H 2 O Aldeide + alcol emiacetale R-CHO + R -OH R-CHOH-O-R Acido + Acido anidride R-COOH + R -COOH R-CO-O-CO-R + H 2 O Alcol + Acido estere R-COOH
Nomenclatura AMIDI Alcol + alcol etere R-OH + R -OH R-O-R + H 2 O Aldeide + alcol emiacetale R-CHO + R -OH R-CHOH-O-R Acido + Acido anidride R-COOH + R -COOH R-CO-O-CO-R + H 2 O Alcol + Acido estere R-COOH
STRUTTURA E FUNZIONE DELLE PROTEINE
 STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
lati esterni altamente Idrofilici
 I due filamenti complementari del DNA sono antiparalleli: uno è in direzione 5-3 e l altro in direzione 3-5. parte interna idrofobica lati esterni altamente Idrofilici APPAIAMENTO DELLE BASI AZOTATE: 2
I due filamenti complementari del DNA sono antiparalleli: uno è in direzione 5-3 e l altro in direzione 3-5. parte interna idrofobica lati esterni altamente Idrofilici APPAIAMENTO DELLE BASI AZOTATE: 2
LE PROTEINE -struttura tridimensionale-
 LE PROTEINE -struttura tridimensionale- Struttura generale di una proteina Ceruloplasmina Cosa sono??? Sono biopolimeri con forme ben definite. composti da molteplici amminoacidi, legati con legami peptidici
LE PROTEINE -struttura tridimensionale- Struttura generale di una proteina Ceruloplasmina Cosa sono??? Sono biopolimeri con forme ben definite. composti da molteplici amminoacidi, legati con legami peptidici
COME È FATTO? Ogni filamento corrisponde ad una catena di nucleotidi
 Il DNA Il DNA è una sostanza che si trova in ogni cellula e contiene tutte le informazioni sulla forma e sulle funzioni di ogni essere vivente: eppure è una molecola incredibilmente semplice. COME È FATTO?
Il DNA Il DNA è una sostanza che si trova in ogni cellula e contiene tutte le informazioni sulla forma e sulle funzioni di ogni essere vivente: eppure è una molecola incredibilmente semplice. COME È FATTO?
CELLULA PROCARIOTICA PROCARIOTE
 CELLULA PROCARIOTICA O PROCARIOTE CELLULA EUCARIOTICA O EUCARIOTE Sany0196.jpg IL NUCLEO Provvisto di due membrane (interna ed esterna) che congiungendosi in alcuni punti formano i pori nucleari attraverso
CELLULA PROCARIOTICA O PROCARIOTE CELLULA EUCARIOTICA O EUCARIOTE Sany0196.jpg IL NUCLEO Provvisto di due membrane (interna ed esterna) che congiungendosi in alcuni punti formano i pori nucleari attraverso
IPOTESI UN GENE-UN ENZIMA
 IPOTESI UN GENE-UN ENZIMA DNA: contiene tutte le informazioni per definire lo sviluppo e la fisiologia della cellula: ma come svolge questa funzione? Beadle e Tatum (1941): studiando mutanti della comune
IPOTESI UN GENE-UN ENZIMA DNA: contiene tutte le informazioni per definire lo sviluppo e la fisiologia della cellula: ma come svolge questa funzione? Beadle e Tatum (1941): studiando mutanti della comune
PROTIDI: LE PROTEINE E GLI AMMINOACIDI
 PROTIDI: LE PROTEINE E GLI AMMINOACIDI GLI AMMINOACIDI Struttura generica di un amminoacido. R rappresenta un gruppo laterale specifico di ogni amminoacido. In chimica, gli amminoacidi (impropriamente
PROTIDI: LE PROTEINE E GLI AMMINOACIDI GLI AMMINOACIDI Struttura generica di un amminoacido. R rappresenta un gruppo laterale specifico di ogni amminoacido. In chimica, gli amminoacidi (impropriamente
Nucleotidi 20/12/2013. Nucleotidi (1) Ribosio Vs. Desossirbosio
 I Nucleotidi Hanno Tre Componenti Nucleotidi https://www2.chemistry.msu.edu/faculty/reusch/virttxtjml/nucacids.htm Nucleotidi (1) Ribosio Vs. Desossirbosio Un Nucleotide è una molecola costituita da un
I Nucleotidi Hanno Tre Componenti Nucleotidi https://www2.chemistry.msu.edu/faculty/reusch/virttxtjml/nucacids.htm Nucleotidi (1) Ribosio Vs. Desossirbosio Un Nucleotide è una molecola costituita da un
scaricato da www.sunhope.it Proteine semplici costituite dai soli amminoacidi
 Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
Formula 2 Vitamin & Mineral Complex Donna
 INDICAZIONI CONSENTITE SUL PRODOTTO Formula 2 Vitamin & Mineral Complex Donna INDICAZIONI PRINCIPALI Attività ormonale: Contiene vitamina B6, che contribuisce alla regolazione dell attività ormonale. Metabolismo
INDICAZIONI CONSENTITE SUL PRODOTTO Formula 2 Vitamin & Mineral Complex Donna INDICAZIONI PRINCIPALI Attività ormonale: Contiene vitamina B6, che contribuisce alla regolazione dell attività ormonale. Metabolismo
Biochimica. studio della vita a livello molecolare
 Biochimica studio della vita a livello molecolare studio della composizione molecolare dei sistemi viventi studio delle reazioni chimiche cui vanno incontro i sistemi viventi ALCUNI QUESITI DELLA BIOCHIMICA
Biochimica studio della vita a livello molecolare studio della composizione molecolare dei sistemi viventi studio delle reazioni chimiche cui vanno incontro i sistemi viventi ALCUNI QUESITI DELLA BIOCHIMICA
Funzioni dei nucleotidi
 Funzioni dei nucleotidi monomeri degli acidi nucleici esempi di altre funzioni ATP: moneta energetica GTP: fonte di energia nella sintesi proteica camp: secondo messaggero nella trasduzione del segnale
Funzioni dei nucleotidi monomeri degli acidi nucleici esempi di altre funzioni ATP: moneta energetica GTP: fonte di energia nella sintesi proteica camp: secondo messaggero nella trasduzione del segnale
02/12/2014. Tutti gli esseri viventi sono composti da cellule LA CELLULA E L UNITA STRUTTURALE E FUNZIONALE DEGLI ORGANISMI VIVENTI
 Tutti gli esseri viventi sono composti da cellule Eubatteri Procarioti unicellulari Archebatteri LA CELLULA E L UNITA STRUTTURALE E FUNZIONALE DEGLI ORGANISMI VIVENTI -Autoconservazione mantenimento della
Tutti gli esseri viventi sono composti da cellule Eubatteri Procarioti unicellulari Archebatteri LA CELLULA E L UNITA STRUTTURALE E FUNZIONALE DEGLI ORGANISMI VIVENTI -Autoconservazione mantenimento della
Capitolo 3 Le biomolecole
 apitolo 3 Le biomolecole I composti organici e i loro polimeri 3.1 La diversità molecolare della vita è basata sulle proprietà del carbonio Un atomo di carbonio può formare quattro legami covalenti. Questi
apitolo 3 Le biomolecole I composti organici e i loro polimeri 3.1 La diversità molecolare della vita è basata sulle proprietà del carbonio Un atomo di carbonio può formare quattro legami covalenti. Questi
Legami chimici. Covalente. Legami deboli
 Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici STRUTTURA TERZIARIA La struttura tridimensionale
Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici STRUTTURA TERZIARIA La struttura tridimensionale
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH. ) ed un gruppo carbossilico ( COOH) nella stessa molecola
 Amminoacidi (1) Presentano un gruppo amminico ( NH 2 ) ed un gruppo carbossilico ( COOH) nella stessa molecola CH 3 NH 2 C H α * COOH Acido 2-ammino propanoico (acido α-ammino propionico) 1 Amminoacidi
Amminoacidi (1) Presentano un gruppo amminico ( NH 2 ) ed un gruppo carbossilico ( COOH) nella stessa molecola CH 3 NH 2 C H α * COOH Acido 2-ammino propanoico (acido α-ammino propionico) 1 Amminoacidi
Gli acidi nucleici sono eteropolimeri lineari costituiti da subunità nucleotidiche (monomeri).
 Gli acidi nucleici sono eteropolimeri lineari costituiti da subunità nucleotidiche (monomeri). Un nucleotide è formato da: uno zucchero: (Ribosio o Deossiribosio), a 5 atomi di carbonio in forma ciclica
Gli acidi nucleici sono eteropolimeri lineari costituiti da subunità nucleotidiche (monomeri). Un nucleotide è formato da: uno zucchero: (Ribosio o Deossiribosio), a 5 atomi di carbonio in forma ciclica
Pagine sul libro. da pag. 124 a pag. 133
 Vitamine e Minerali Pagine sul libro da pag. 124 a pag. 133 CHE COSA SONO LE VITAMINE NUTRIENTI ESSENZIALI NON CALORICI VITAMINE Vitamine significa ammine della vita. Sono composti organici. Sono necessarie
Vitamine e Minerali Pagine sul libro da pag. 124 a pag. 133 CHE COSA SONO LE VITAMINE NUTRIENTI ESSENZIALI NON CALORICI VITAMINE Vitamine significa ammine della vita. Sono composti organici. Sono necessarie
BIOMOLECOLE LE BASI DELLA BIOCHIMICA. Capitolo 1 Dal Carbonio agli OGM PLUS
 BIOMOLECOLE LE BASI DELLA BIOCHIMICA Capitolo 1 Dal Carbonio agli OGM PLUS BIOMOLECOLE Carboidrati Lipidi Acidi Nucleici Proteine BIOMOLECOLE Carboidrati Lipidi Acidi Nucleici - monosaccaridi - disaccaridi
BIOMOLECOLE LE BASI DELLA BIOCHIMICA Capitolo 1 Dal Carbonio agli OGM PLUS BIOMOLECOLE Carboidrati Lipidi Acidi Nucleici Proteine BIOMOLECOLE Carboidrati Lipidi Acidi Nucleici - monosaccaridi - disaccaridi
I PROTIDI. Aspetti generali
 I PROTIDI Aspetti generali I protidi o proteine sono sostanze organiche azotate, di struttura molto complessa, presenti in ogni forma di vita. In natura esistono moltissime proteine: si calcola, ad esempio,
I PROTIDI Aspetti generali I protidi o proteine sono sostanze organiche azotate, di struttura molto complessa, presenti in ogni forma di vita. In natura esistono moltissime proteine: si calcola, ad esempio,
Di cosa è fatta una cellula?
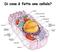 Di cosa è fatta una cellula? Composizione delle cellule - L acqua (H 2 O) rappresenta il 70% del massa della cellula - C,H,N,O rappresentano il 96% della massa della cellula - Altri component frequenti
Di cosa è fatta una cellula? Composizione delle cellule - L acqua (H 2 O) rappresenta il 70% del massa della cellula - C,H,N,O rappresentano il 96% della massa della cellula - Altri component frequenti
Capitolo 3 Le biomolecole
 apitolo 3 Le biomolecole opyright 2006 Zanichelli editore I composti organici e i loro polimeri 3.1 La diversità molecolare della vita è basata sulle proprietà del carbonio Un atomo di carbonio può formare
apitolo 3 Le biomolecole opyright 2006 Zanichelli editore I composti organici e i loro polimeri 3.1 La diversità molecolare della vita è basata sulle proprietà del carbonio Un atomo di carbonio può formare
Caratteristiche generali
 Caratteristiche generali Sono così chiamati perché hanno caratteristiche acide e si trovano prevalentemente nel nucleo delle cellule, dove svolgono la funzione informazionale. Gli acidi nucleici sono infatti
Caratteristiche generali Sono così chiamati perché hanno caratteristiche acide e si trovano prevalentemente nel nucleo delle cellule, dove svolgono la funzione informazionale. Gli acidi nucleici sono infatti
Definizione Composti quaternari: C H O N S P Fe Mg I
 PROTIDI Definizione Composti quaternari: C H O N S P Fe Mg I ORIGINE cellulare ogni cellula sintetizza le sue prote CARATTERISTICHE insolubili in acqua sensibili a variazioni di ph coagulano in presenza
PROTIDI Definizione Composti quaternari: C H O N S P Fe Mg I ORIGINE cellulare ogni cellula sintetizza le sue prote CARATTERISTICHE insolubili in acqua sensibili a variazioni di ph coagulano in presenza
Modulo 8: I nucleotidi e gli acidi nucleici
 Modulo 8: I nucleotidi e gli acidi nucleici Modulo 10: Acidi nucleici Filamento di DNA fuoriuscito da una cellula di Escherichia coli Struttura e funzioni dei nucleotidi Funzioni dei nucleotidi: Unità
Modulo 8: I nucleotidi e gli acidi nucleici Modulo 10: Acidi nucleici Filamento di DNA fuoriuscito da una cellula di Escherichia coli Struttura e funzioni dei nucleotidi Funzioni dei nucleotidi: Unità
Formula 2 Vitamin & Mineral Complex Uomo
 INDICAZIONI CONSENTITE SUL PRODOTTO Formula 2 Vitamin & Mineral Complex Uomo INDICAZIONI PRINCIPALI Sistema immunitario: Contiene le vitamine A e C, che contribuiscono alla normale funzione del Funzione
INDICAZIONI CONSENTITE SUL PRODOTTO Formula 2 Vitamin & Mineral Complex Uomo INDICAZIONI PRINCIPALI Sistema immunitario: Contiene le vitamine A e C, che contribuiscono alla normale funzione del Funzione
Amminoacidi. Struttura base di un a-amminoacido
 Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
VITAMINA D (VITAMINA D3)
 VANIGLIA VITAMINA A - contribuisce al normale metabolismo del ferro - contribuisce al mantenimento di membrane mucose normali - contribuisce al mantenimento della capacità visiva normale - interviene nel
VANIGLIA VITAMINA A - contribuisce al normale metabolismo del ferro - contribuisce al mantenimento di membrane mucose normali - contribuisce al mantenimento della capacità visiva normale - interviene nel
ACIDI NUCLEICI ESPERIMENTI
 ACIDI NUCLEICI ESPERIMENTI 1869 FRIEDRICK MIESCHER Isolò per la prima volta una sostanza zuccherina leggermente acida contenente fosforo Questa sostanza venne chiamata: acido nucleico perché scoperta nel
ACIDI NUCLEICI ESPERIMENTI 1869 FRIEDRICK MIESCHER Isolò per la prima volta una sostanza zuccherina leggermente acida contenente fosforo Questa sostanza venne chiamata: acido nucleico perché scoperta nel
LE MOLECOLE BIOLOGICHE
 LE MOLECOLE BIOLOGICHE Le cellule contengono quattro famiglie principali di molecole organiche Zuccheri (monosaccaridi) - forniscono una fonte di energia - subunità dei polisaccaridi Amminoacidi - subunità
LE MOLECOLE BIOLOGICHE Le cellule contengono quattro famiglie principali di molecole organiche Zuccheri (monosaccaridi) - forniscono una fonte di energia - subunità dei polisaccaridi Amminoacidi - subunità
Nucleotidi 26/10/2014. Nucleotidi (1)
 I Nucleotidi Hanno Tre Componenti Base azotata Nucleotidi https://www2.chemistry.msu.edu/faculty/reusch/virttxtjml/nucacids.htm Base azotata Qualsiasi composto che manifesta proprietà basiche per via della
I Nucleotidi Hanno Tre Componenti Base azotata Nucleotidi https://www2.chemistry.msu.edu/faculty/reusch/virttxtjml/nucacids.htm Base azotata Qualsiasi composto che manifesta proprietà basiche per via della
Nucleotidi 04/11/2015
 Base azotata Nucleotidi Qualsiasi composto che manifesta proprietà basiche per via della presenza di una doppietta di elettroni non condivisi su un atomo di azoto (come nell ammoniaca e nelle ammine).
Base azotata Nucleotidi Qualsiasi composto che manifesta proprietà basiche per via della presenza di una doppietta di elettroni non condivisi su un atomo di azoto (come nell ammoniaca e nelle ammine).
MACROMOLECOLE. Polimeri (lipidi a parte)
 MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
Gerard Tortora, Brian Derrickson. Conosciamo
 1 Gerard Tortora, Brian Derrickson Conosciamo il corpo umano Capitolo 1 L organizzazione del corpo umano 1. Che cosa sono l anatomia e la fisiologia 2. I livelli di organizzazione e gli apparati del corpo
1 Gerard Tortora, Brian Derrickson Conosciamo il corpo umano Capitolo 1 L organizzazione del corpo umano 1. Che cosa sono l anatomia e la fisiologia 2. I livelli di organizzazione e gli apparati del corpo
VITAMINA E - contribuisce alla protezione delle cellule dallo stress ossidativo
 VITAMINA A - contribuisce al normale metabolismo del ferro - contribuisce al mantenimento della capacità visiva normale - interviene nel processo di specializzazione delle cellule VITAMINA E VITAMINA C
VITAMINA A - contribuisce al normale metabolismo del ferro - contribuisce al mantenimento della capacità visiva normale - interviene nel processo di specializzazione delle cellule VITAMINA E VITAMINA C
DNA: Struttura e caratteristiche
 DNA: Struttura e caratteristiche Il DNA è un acido nucleico formato da monomeri detti nucleotidi. Ogni nucleotide è formato da: Zucchero pentoso (desossiribosio) Gruppo fosfato Base azotata Basi azotate:
DNA: Struttura e caratteristiche Il DNA è un acido nucleico formato da monomeri detti nucleotidi. Ogni nucleotide è formato da: Zucchero pentoso (desossiribosio) Gruppo fosfato Base azotata Basi azotate:
Le molecole biologiche. Le proteine
 Le molecole biologiche Le proteine Le proteine sono macromolecole che costituiscono la maggior parte delle strutture cellulari ed extra-cellulari Così come nel caso di lipidi e carboidrati, anch esse
Le molecole biologiche Le proteine Le proteine sono macromolecole che costituiscono la maggior parte delle strutture cellulari ed extra-cellulari Così come nel caso di lipidi e carboidrati, anch esse
Enzimi = catalizzatori di una reazione biochimica Caratteristiche: Specificità: ogni enzima riconosce specificamente il/i substrato/i e non altre
 Enzimi = catalizzatori di una reazione biochimica Caratteristiche: Specificità: ogni enzima riconosce specificamente il/i substrato/i e non altre molecole, anche chimicamente simili al substrato. Saturabilità:
Enzimi = catalizzatori di una reazione biochimica Caratteristiche: Specificità: ogni enzima riconosce specificamente il/i substrato/i e non altre molecole, anche chimicamente simili al substrato. Saturabilità:
PROTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi
 POTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (,, O, N) macromolecole organiche, molecole informazionali, polimeri
POTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (,, O, N) macromolecole organiche, molecole informazionali, polimeri
Nel DNA e nell RNA i nucleotidi sono legati covalentemente da legami fosfodiesterei.
 DNA e RNA Composizione e proprietà Struttura Analisi 1 STRUTTURA DAGLI ACIDI NUCLEICI Nel DNA e nell RNA i nucleotidi sono legati covalentemente da legami fosfodiesterei. I gruppi fosforici hanno pka vicino
DNA e RNA Composizione e proprietà Struttura Analisi 1 STRUTTURA DAGLI ACIDI NUCLEICI Nel DNA e nell RNA i nucleotidi sono legati covalentemente da legami fosfodiesterei. I gruppi fosforici hanno pka vicino
