AA : Corso di Orientamento Elementi di Chimica Domenico Ciavardelli - Ph.D. domenico.ciavardelli@unikore.it
|
|
|
- Rossana Ferrario
- 7 anni fa
- Visualizzazioni
Transcript
1 Università degli Studi Kore di Enna Facoltà di Scienze dell Uomo e della Società CdL in Scienze delle attività motorie e sportive AA : Corso di Orientamento - Ph.D. domenico.ciavardelli@unikore.it
2 Carboidrati Prodotti di Degradazione/Ossidazione Proteine Lipidi
3
4 Numero atomico (Z) Massa Atomica (A, u) Punto di fusione ( C) Punto di ebollizione ( C) Elettronegatività (Scala Pauling) Densità (0 C, 1atm) Numeri di Ossidazione Configurazione elettronica
5 Teoria Atomica modello sviluppato in 2500 anni! Democrito( a.c.):, indivisibile. Epicuro ( a.c.): atomi immutabili Conservazione della materia. Lucrezio: De Rerum Natura John Dalton ( ) Teoria Atomistica Moderna
6 1927 Solvay Conference on Quantum Mechanics
7 A Z X A = numero di massa Z = numero atomico N = numero di neutroni = A-Z Stesso numero atomico, diverso numero di massa ISOTOPI Es.: 12 C, 13 C Stesso numero di massa, diverso numero atomico ISOBARI Es.: 14 C, 14 N Massa di un elettrone: *10-24 g Massa di un protone:1.6723*10-24 g Massa di un neutrone:1.6745*10-24 g Massa Atomica Relativa (uma) 1uma = 1/12 massa (g) 12 C, massa 12 C = 19,925*10-24 g 1uma= 19,925*10-24g/12 = 1,660*10-24 Massa 12 C (uma) = 12 Massa degli elettroni trascurabile.
8 Modello Atomico: evoluzione. Dalton atomi indivisibili Spettroscopia Ottica Transizioni livelli energetici Fisica Quantistica Thomson particelle subatomiche Plank Teoria dei Quanti Einstein Fotoni e Teoria Corpuscolare della Luce Rutherford atomo nucleare Atomo di Bohr r De Broglie Dualismo particella/onda dell elettrone Heisemberg Principio di indeterminazione Schrödinger Numeri Quantici Probabilità Orbitali
9 Orbitale atomico: Orbitali s: n = 1, 2, 3, 4,... l = 0 V=4/3 r 3 Orbitali p: n = 2, 3, 4,... l = 1 Orbitali d: n = 3, 4,..., l = 2 n=numero quantico principale l=numero quantico secondario
10 Ogni funzione d onda ovvero ogni orbitale corrisponde ad uno specifico livello energetico ogni elettrone può avere un energia che varia in modo discreto Livelli energetici per ATOMI POLIELETTRONICI E = f( n, l ) 3d 4s M L 2p 2s 3p 3s K 1s n
11 Costruzione delle configurazioni elettroniche degli elementi Aufbau Costruzione distribuzione degli elettroni in atomi polielettronici nei possibili orbitali atomici con la graduale occupazione degli orbitali di minore energia. Principio di esclusione di Pauli: gli elettroni in un atomo non possono essere caratterizzati dagli stessi numeri quantici. Ogni orbitale può ospitare al massimo due elettroni aventi diverso valore di numero quantico di spin ± ½. Regola di Hund: principio della massima molteplicità. Gli elettroni si dispongono con spin paralleli nel massimo degli orbitali disponibili. n
12 Es. Costruzione della configurazione elettronica per l azoto: N: 1s 2 2s 2 2p 3 numeriamo arbitrariamente i 7 elettroni (e - ) dell azoto: e - 1, e- 2, e- 3, e- 4, e- 5, e- 6, e- 7. Il primo elettrone e - 1 avrà l energia più bassa possibile maggiore stabilità favorita in pratica questo si traduce nell iniziare a riempire l orbitale a minore energia 1s Ogni orbitale può descrivere il moto di due elettroni a spin antiparallelo l orbitale 1s che abbiamo iniziato a riempire è semivuoto ovvero può descrivere il moto di un altro elettrone ed è l orbitale, seppur parzialmente riempito, a minore energia e - 2 occuperà la lacuna elettronica nell orbitale 1s è avrà spin antiparallelo rispetto a e - 1 (moto di rotazione sul proprio asse opposto a quello dell orbitale e - 1 ). Con la stessa logica gli elettroni e - 3 e e- 4 riempiranno l orbitale 2s che corrisponde al livello energetico immediatamente superiore rispetto ad 1s che ormai è pieno. Gli elettroni e - 5, e- 6, e- 7 non potranno che essere descritti dai 3 orbitali degeneri (stessa energia) 2p che corrispondono al livello energetico immediatamente superiore al livello corrispondente all orbitale 2s. Questi 3 elettroni hanno a disposizione 3 orbitali vuoti come si disporranno?
13 1) Prima possibilità: 2e - (e - 5 ed e - 6 ) occuperanno il primo orbitale p e avranno spin antiparallelo mentre l ultimo elettrone (e - 7 ) occuperà uno degli orbitali p vuoti E = f( n, l ) 2) Seconda possibilità: I tre elettroni e - 5, e- 6, e- 7 occupernno singolarmente i 3 orbitali 2p vuoti E = f( n, l ) M L 2p 2s e5 e6 e7 e3 e4 M L 2p 2s e3 e5 e6 e7 e4 K 1s e1 e2 K 1s e1 e2 1 2 n 1 2 La seconda possibilità corrisponde alla maggiore stabilità in quanto si riducono notevolmente le forze di repulsione tra i due elettroni entrambi carichi negativamente minore repulsione maggiore stabilità configurazione favorita! n
14 Primo e Secondo periodo. He: 1s 2 Li: [He]2s 1 Be: [He]2s 2 B: [He]2s 2 2p 1 C: [He]2s 2 2p 2 N: [He]2s 2 2p 3 O: [He]2s 2 2p 4 F: [He]2s 2 2p 5 Ne: [He]2s 2 2p 6 E = f (n, l ) M L K 1s 2p 2s Elio [He] 3d 3p s 4s 4 n
15 Configurazione elettronica Legame Chimico Interazione attrattiva sufficientemente intensa da permettere la formazione di un sistema poli-atomico stabile ed individuabile come entità distinta MOLECOLA VALENZA: numero di legami che un atomo può formare TEORIA VB. REGOLA DELL OTTETTO: gli elementi tendono alla configurazione elettronica esterna ad 8 elettroni dei gas nobili. Tale tendenza determina la valenza di una specie atomica. Ogni atomo può formare un numero di legami pari al numero dei propri elettroni spaiati (Es: nel caso dell azoto descritto prima si ha la possibilità di formare tre legami per messa in compartecipazione dei tre elettroni spaiati) Ogni atomo può raggiungere l ottetto per: 1. Condivisione di elettroni tra atomi diversi configurazione dell ottetto LEGAME COVALENTE 2. Condivisione di elettroni provenienti da UNO DEI 2 ATOMI coinvolti nell interazione LEGAME DATIVO 3. TRASFERIMENTO di elettroni da un atomo donatore ad un atomo accettore, che acquista che acquista una carica negativa formazione di IONI LEGAME ETEROPOLARE o IONICO
16 Legame Covalente Es: Molecola di idrogeno I due elettroni originariamente spaiati sono accoppiati in un orbitale molecolare e condivisi dai due nuclei. Legame covalente Orbitale Molecolare (Legame minimo di energia) DIAGRAMMA DELL ENERGIA: La formazione del legame porta il sistema costituito dai due atomi ad uno stato corrispondente ad un livello energetico minore. Infatti i due atomi di idrogeno (H: 1s) mettendo in compartecipazione gli elettroni nella formazione del legame covalente assumeranno la configurazione stabile dell Elio (He: 1s 2 ) corrispondente al riempimento del livello K. Aumentando la distanza tra i due atomi rispetto alla lunghezza di legame (r ) il sistema molecola viene meno e la sua energia tende a zero. Per valori della distanza tra i due atomi <r prevalgono le forze repulsive tra i nuclei e l energia del sistema tende a +. Gli elettroni di legame occupano orbitali molecolari generati dalla sovrapposizione di orbitali atomici tanto più efficace in termini di stabilizzazione del legame quanto più la direzionalità degli orbitali atomici di partenza è simile. Lo stesso tipo di legame si instaura tra atomi che formano altre molecole biatomiche omonucleari: N2, O2, F2 LEGAME COVALENTE PURO. Tali composti si presentano in natura come molecole biatomiche omonucleari in virtù della stabilizzazione di tale sistema rispetto ai relativi sistemi atomici.
17 Un LEGAME potrà essere definito COVALENTE PURO solo nel caso di legami tra atomi uguali. Solo in tal caso, infatti, la differenza di elettronegatività tra gli atomi è nulla e gli elettroni di legame sarà ugualmente attratti dai due nuclei. LEGAMI COVALENTE POLARIZZATO attrazione degli elettroni di legame da parte dell atomo più elettronegativo Atomi X e Y tali che χ(x) < χ(y) X ----Y χ= elettronegatività = parziale carica positiva di X, = parziale carica negativa di Y Polarità del Legame
18 Proprietà periodiche Gli elementi di uno stesso gruppo presentano caratteristiche chimiche e fisiche simili. Nell ambito di un gruppo le proprietà variano REGOLARMENTE al variare del numero atomico. 1. Potenziale di prima ionizzazione. 2. Affinità elettronica. 3. Raggio Atomico.
19 1. Potenziale di ionizzazione: energia E necessaria al processo M + E (M + ) + (e-) (Ossidazione) Cosa si intende per periodicita? Il processo di ionizzazione è quindi ENDOERGONICO. Diminuisce nei gruppi poichè gli elettroni più esterni sono schermati da quelli interni e cresce da sinistra a destra lungo i periodi poiche l aumento del numero di elettroni corrisponde all aumento della carica nucleare con l aumento dell energia richiesta per l estrazione dell elettrone Es: Metalli alcalini e alcalino terrosi tendono a dare ioni mono e bivalenti positivi rispettivamente Es: valore massimo per i gas nobili: REGOLA dell OTTETTO.
20 2 Affinità elettronica: energia E sviluppata nella formazione di uno ione negativo gassoso X + (e-) (PROCESSO ESOERGONICO) (X-) + E o, considerando il processo inverso, l energia necessaria a strappare un elettrone all anione. Es.: Il cloro tende ad acquistare un elettrone il processo è favorito ed esotermico elevata affinità elettronica. Il sodio, al contrario, ha un comportamento opposto: tende a perdere un elettrone non ad acquistarlo. il processo di formazione dello ione Na - è sfavorito e la sua affinità elettronica è molto bassa Aumenta da sinistra a destra lungo i periodi (aumenta Z e la carica nucleare a parità di n l elemento acquista più facilmente l elettrone, il processo è più favorito e l energia sviluppata è maggiore) e diminuisce lungo i gruppi (aumentano Z ma anche n. Benchè aumenti la carica nucleare, cresce anche il livello energetico degli orbitali capaci di ospitare l elettrone per dare l anione gassoso. L elettrone acquistato sarà meno vincolato, l anione sarà meno stabile e il processo complessivamente meno favorito). 3 Raggio atomico: distanza dal nucleo dell regione in cui è massima la probabilità di trovare gli elettroni più esterni. Tale distanza è direttamente proporzionale al numero quantico principale n. Diminuisce lungo i periodi (n=cost, Z crescente contrazione) Cresce nell ambito dei gruppi (n cresce, Z cresce ma prevale l effetto di n).
21 =elettrone spaiato (possibilità di formare un legame) =nucleo =orbitale atomico (zona dello spazio in cui è più probabile trovare un elettrone) Atomi uguali (stessa ELETTRONEGATIVITA ) Atomi differenti (diversa ELETTRONEGATIVITA ) Legame covalente puro (Nessuna polarità di legame; elettroni ugualmente condivisi dai due nuclei) Legame covalente polare (L atomo più elettronegativo attrae gli elettroni di legame; Polarità)
22 Orbitali atomici (ψ n, l, ml ) e configurazione elettronica Legame chimico 1. I A (1) H Li Na K Rb II A (2) Be Mg Ca Sr Covalente puro 2. Covalente polarizzato Differenza di Elettronegatività 3. Legame ionico Elettronegatività χ III B (13) B Al Ga In IV B (14) C Si Ge Sn V B (15) N P As Sb VI B (16) O S Se Te VII B (17) F Cl Br I Cs Ba Tl Pb Bi Po At Aumentando la differenza di elettronegatività tra gli atomi coinvolti nel legame aumenta il carattere polare del legame covalente. Per valori di χ>1.7 (Scala Pauling) il legame potrà essere definito ionico. Differenza di elettronegatività 0,00 0,65 0,94 1,19 1,43 1,67 1,91 2,19 2,54 3,03 Percentuale di carattere ionico 0% 10% 20% 30% 40% 50% 60% 70% 80% 90%
23 Es.: Come possiamo prevedere sia un legame C-H? χ C =2,50; χc=2,20 χ=0,3 il legame sarà leggermente polarizzato verso il carbonio ma la differenza di elettronegatività è così bassa da poter considerare il legame covalente. Es.: Come possiamo prevedere sia il legame C-O? χc=2,50; χc=3,50 χ=1,0 il legame covalente χ<1,7) ma di sicuro più polarizzato rispetto al precedente parziali cariche + e - su C e O rispettivamente Es.: Come possiamo prevedere sia il legame Na-Cl? χna=1,01; χcl=2,83 χ=1,81>1,7 il legame non sarà covalente polare ma sarà di tipo ionico completa separazione di cariche interazione elettrostatica attrattiva tra anione Cl - e catione Na +.
24 Legame ionico Repulsione r<2,4 Å Equilibrio r=2,4 Å Energia potenziale (ev) Attrazione r>2,4 Å Energia di legame=4,2 ev Na + Cl - Distanza interatomica, r (Angstroms, Å=1*10-10 m) Na 0 + Cl 0 Legame ionico χ è tale che l atomo più elettronegativo acquista l elettrone dall atomo più elettropositivo COMPLETA SEPARAZIONE DI CARICA) Interazione puramente elettrostatica: Legge di Coulomb F=k*(q 1 *q 2 )/r 2 Distanza tra gli ioni (r, lunghezza del legame) corrispondente al minimo di energia per il sistema poliatomico
25 Differenza di elettronegatività NUMERO DI OSSIDAZIONE: carica formale che può essere assegnata ad un elemento (atomo) coinvolto in un legame chimico. L elemento più elettronegativo attrae gli elettroni di legame e assume una carica formale negativa. L elemento meno elettronegativo tende a cedere l elettrone di legame assumendo una carica formale positiva H Cl H 0 H 0 C 0 H 0 C + H 0 H è uno degli elementi meno elettronegativi: carica formale +1 O è uno degli elementi più elettronegativi: carica formale -2 Elementi e composti nello stato di riferimento legami tra atomi uguali χ=0 carica formale nulla O - O -
26 Il numero di ossidazione del Carbonio aumenta CH4 CH3OH H2CO HCOOH CO2
27 Variazione del numero di ossidazione reazioni di ossidoriduzione Ossidazione e riduzione Riduzione B ossidato A ridotto Ossidazione Aumento della carica positiva Diminuzione della carica positiva
28 Per approfondimenti: Capitoli 1, 2, 3 del testo Chimica, Bichimica e Biologia Applicata di Massimo Stefani e Niccolò Taddei, seconda edizione (Zanichelli 2008). E possibile inoltre utilizzare qualsiasi testo in uso presso le scuole secondarie di secondo grado.
combinazione di atomi tenuti insieme da forze più o meno un insieme caratteristico di proprietà
 IL LEGAME CHIMICO La regola dell ottetto sebbene una semplificazione rende conto del perchè gli atomi reagiscono. In natura, solo i gas nobili sono presenti come specie monoatomiche. Anche le sostanze
IL LEGAME CHIMICO La regola dell ottetto sebbene una semplificazione rende conto del perchè gli atomi reagiscono. In natura, solo i gas nobili sono presenti come specie monoatomiche. Anche le sostanze
Struttura dell atomo e Sistema Periodico degli elementi unità 1, 2 e 3, modulo C del libro
 Struttura dell atomo e Sistema Periodico degli elementi unità 1, 2 e 3, modulo C del libro Gli atomi di tutti gli elementi sono formati da tre tipi di particelle elementari: elettrone, protone e neutrone.
Struttura dell atomo e Sistema Periodico degli elementi unità 1, 2 e 3, modulo C del libro Gli atomi di tutti gli elementi sono formati da tre tipi di particelle elementari: elettrone, protone e neutrone.
La tavola periodica. 1- Introduzione
 La tavola periodica 1- Introduzione La legge periodica (1869, Mendeleiev in Russia e Meyer in Germania) stabilisce che gli elementi, quando vengono disposti in ordine di massa atomica, mostrano una periodicità
La tavola periodica 1- Introduzione La legge periodica (1869, Mendeleiev in Russia e Meyer in Germania) stabilisce che gli elementi, quando vengono disposti in ordine di massa atomica, mostrano una periodicità
Forma e proprietà dell orbitale 1s
 Riassumendo Forma e proprietà dell orbitale 1s Proprietà degli orbitali 2s Forma e proprietà degli orbitali 2p Forma e proprieta degli orbitali d Orbitali di tipo f Comportamento degli elettroni in un
Riassumendo Forma e proprietà dell orbitale 1s Proprietà degli orbitali 2s Forma e proprietà degli orbitali 2p Forma e proprieta degli orbitali d Orbitali di tipo f Comportamento degli elettroni in un
Zolfo (Z = 16) Conf. Elettronica 1s 2 2s 2 2p 6 3s 2 3p 4 Conf. Elettronica esterna 3s 2 3p 4
 TAVOLA PERIODICA DEGLI ELEMENTI Gli elementi sono ordinati nella tavola periodica secondo numero atomico crescente ed in base alle loro proprietà chimico-fisiche che seguono un andamento periodico. Gli
TAVOLA PERIODICA DEGLI ELEMENTI Gli elementi sono ordinati nella tavola periodica secondo numero atomico crescente ed in base alle loro proprietà chimico-fisiche che seguono un andamento periodico. Gli
Struttura dell atomo e Sistema Periodico degli elementi unità 1, 2 e 3, modulo C del libro
 Struttura dell atomo e Sistema Periodico degli elementi unità 1, 2 e 3, modulo C del libro Gli atomi di tutti gli elementi sono formati da tre tipi di particelle elementari: elettrone, protone e neutrone.
Struttura dell atomo e Sistema Periodico degli elementi unità 1, 2 e 3, modulo C del libro Gli atomi di tutti gli elementi sono formati da tre tipi di particelle elementari: elettrone, protone e neutrone.
Struttura elettronica e tavola periodica
 Struttura elettronica e tavola periodica La tavola è suddivisa nei blocchi s, p, d e f Eccezioni: 1) Elio (He) il quale pur appartenendo al blocco s, compare in quello p. Possiede uno strato di valenza
Struttura elettronica e tavola periodica La tavola è suddivisa nei blocchi s, p, d e f Eccezioni: 1) Elio (He) il quale pur appartenendo al blocco s, compare in quello p. Possiede uno strato di valenza
ESERCIZI PREPARATORI PER IL COMPITO DI CHIMICA MODULO 2
 ESERCIZI PREPARATORI PER IL COMPITO DI CHIMICA MODULO 2 69 Il blocco s delle Tavola periodica è costituito dai seguenti elementi a) metalli di transizione b) metalli alcalini c) alogeni d) metalli alcalini
ESERCIZI PREPARATORI PER IL COMPITO DI CHIMICA MODULO 2 69 Il blocco s delle Tavola periodica è costituito dai seguenti elementi a) metalli di transizione b) metalli alcalini c) alogeni d) metalli alcalini
ATOMO POLIELETTRONICO. Numero quantico di spin m s
 ATOMO POLIELETTRONICO La teoria fisico-matematica che ha risolto esattamente il problema dell atomo di idrogeno non è in grado di descrivere con uguale precisione l atomo polielettronico. Problema: interazioni
ATOMO POLIELETTRONICO La teoria fisico-matematica che ha risolto esattamente il problema dell atomo di idrogeno non è in grado di descrivere con uguale precisione l atomo polielettronico. Problema: interazioni
Principio dell Aufbau (riempimento)
 LA TABELLA PERIODICA DEGLI ELEMENTI Principio dell Aufbau (riempimento) Schema semplificato dei livelli energetici atomici Distribuzione energetica reale dei livelli energetici atomici 7p Schema empirico
LA TABELLA PERIODICA DEGLI ELEMENTI Principio dell Aufbau (riempimento) Schema semplificato dei livelli energetici atomici Distribuzione energetica reale dei livelli energetici atomici 7p Schema empirico
Verifica di chimica su: Atomo, tavola periodica, legame chimico Nome cognome data classe
 1 Verifica di chimica su: Atomo, tavola periodica, legame chimico Nome cognome data classe 21) Quanti neutroni, protoni ed elettroni ha l elemento con numero atomico Z = 23 e numero di massa A = 51? P=23,
1 Verifica di chimica su: Atomo, tavola periodica, legame chimico Nome cognome data classe 21) Quanti neutroni, protoni ed elettroni ha l elemento con numero atomico Z = 23 e numero di massa A = 51? P=23,
Il legame chimico ATOMI MOLECOLE
 Il legame chimico Gli atomi tendono a combinarsi con altri atomi per dare un sistema finale più stabile di quello iniziale (a minor contenuto di energia). ATOMI MOLECOLE 1 Stati repulsivi di non legame
Il legame chimico Gli atomi tendono a combinarsi con altri atomi per dare un sistema finale più stabile di quello iniziale (a minor contenuto di energia). ATOMI MOLECOLE 1 Stati repulsivi di non legame
Unbowed, Unbent, Unbroken
 Unbowed, Unbent, Unbroken L ATOMO E LE SUE PROPRIETÀ STRUTTURA DELL ATOMO Carica Massa Protoni = particelle a carica positiva +1,6 x 10-19 C 1,67 x 10-27 Kg Elettroni = particelle a carica negativa -1,6
Unbowed, Unbent, Unbroken L ATOMO E LE SUE PROPRIETÀ STRUTTURA DELL ATOMO Carica Massa Protoni = particelle a carica positiva +1,6 x 10-19 C 1,67 x 10-27 Kg Elettroni = particelle a carica negativa -1,6
Sommario della lezione 4. Proprietà periodiche. Massa atomica e massa molecolare. Concetto di mole. Prime esercitazioni
 Sommario della lezione 4 Proprietà periodiche Massa atomica e massa molecolare Concetto di mole Prime esercitazioni Configurazione elettronica e Tabella Periodica Negli elementi di transizione, il numero
Sommario della lezione 4 Proprietà periodiche Massa atomica e massa molecolare Concetto di mole Prime esercitazioni Configurazione elettronica e Tabella Periodica Negli elementi di transizione, il numero
TAVOLA PERIODICA (Mendeleev, 1869)
 TAVOLA PERIODICA (Mendeleev, 1869) Osservazione e correlazione di proprietà chimiche (reattività, colore, solubilità, acidità, etc.) Li, Na, K, Rb Mg, Ca, Sr, Ba F, Cl, Br, I Ordinamento secondo Peso Atomico
TAVOLA PERIODICA (Mendeleev, 1869) Osservazione e correlazione di proprietà chimiche (reattività, colore, solubilità, acidità, etc.) Li, Na, K, Rb Mg, Ca, Sr, Ba F, Cl, Br, I Ordinamento secondo Peso Atomico
Nel 1926 Erwin Schrödinger propose un equazione celebre e mai abbandonata per il calcolo delle proprietà degli atomi e delle molecole
 Nel 1926 Erwin Schrödinger propose un equazione celebre e mai abbandonata per il calcolo delle proprietà degli atomi e delle molecole Secondo questa teoria l elettrone può essere descritto come fosse un
Nel 1926 Erwin Schrödinger propose un equazione celebre e mai abbandonata per il calcolo delle proprietà degli atomi e delle molecole Secondo questa teoria l elettrone può essere descritto come fosse un
Atomi, molecole e ioni
 Atomi, molecole e ioni anione + - catione Teoria atomica di Dalton 1. Un elemento è composto da particelle minuscole chiamate atomi. 2. In una normale reazione chimica, nessun atomo di nessun elemento
Atomi, molecole e ioni anione + - catione Teoria atomica di Dalton 1. Un elemento è composto da particelle minuscole chiamate atomi. 2. In una normale reazione chimica, nessun atomo di nessun elemento
Classe4:chimicaStrutturaAtomica1. Controlla se sai definire i seguenti termini: teoria atomica di Dalton (atomo di Dalton),
 Classe4:chimicaStrutturaAtomica1. Controlla se sai definire i seguenti termini: teoria atomica di Dalton (atomo di Dalton), particelle subatomiche, protone, neutrone, elettronie, nucleo. 2. Decidi se tra
Classe4:chimicaStrutturaAtomica1. Controlla se sai definire i seguenti termini: teoria atomica di Dalton (atomo di Dalton), particelle subatomiche, protone, neutrone, elettronie, nucleo. 2. Decidi se tra
Legame Chimico. Legame Chimico
 Legame Chimico Fra due atomi o gruppi di atomi esiste un legame chimico se le forze agenti tra essi danno luogo alla formazione di un aggregato di atomi sufficientemente stabile da consentire di svelarne
Legame Chimico Fra due atomi o gruppi di atomi esiste un legame chimico se le forze agenti tra essi danno luogo alla formazione di un aggregato di atomi sufficientemente stabile da consentire di svelarne
I numeri quantici. Numero quantico principale, n: numero intero Caratterizza l energia dell elettrone
 I numeri quantici La regione dello spazio in cui si ha la probabilità massima di trovare un elettrone con una certa energia è detto orbitale Gli orbitali vengono definiti dai numeri quantici Numero quantico
I numeri quantici La regione dello spazio in cui si ha la probabilità massima di trovare un elettrone con una certa energia è detto orbitale Gli orbitali vengono definiti dai numeri quantici Numero quantico
LEZIONE 2. Configurazioni elettroniche e tavola periodica
 LEZIONE 2 Configurazioni elettroniche e tavola periodica COSTRUZIONE DELLA CONFIGURAZIONE ELETTRONICA 1. Principio di Aufbau: gli elettroni occupano gli orbitali in ordine crescente di energia. dipende
LEZIONE 2 Configurazioni elettroniche e tavola periodica COSTRUZIONE DELLA CONFIGURAZIONE ELETTRONICA 1. Principio di Aufbau: gli elettroni occupano gli orbitali in ordine crescente di energia. dipende
I LEGAMI CHIMICI E LA REGOLA DELL OTTETTO
 I LEGAMI CHIMICI E LA REGOLA DELL OTTETTO REGOLA DELL OTTETTO: Tutti gli atomi si legano, cedono, acquistano o condividono elettroni per raggiungere un livello esterno pieno di otto (o due) elettroni.
I LEGAMI CHIMICI E LA REGOLA DELL OTTETTO REGOLA DELL OTTETTO: Tutti gli atomi si legano, cedono, acquistano o condividono elettroni per raggiungere un livello esterno pieno di otto (o due) elettroni.
ATOMO. Legge della conservazione della massa Legge delle proporzioni definite Dalton
 Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti interi
Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti interi
STRUTTURA ATOMICA. tutti gli atomi hanno un nucleo carico positivamente che possiede quasi tutta la massa atomica
 STRUTTURA ATOMICA tutti gli atomi hanno un nucleo carico positivamente che possiede quasi tutta la massa atomica il nucleo è composto da protoni e neutroni che hanno massa = 1 nella scala dei pesi atomici
STRUTTURA ATOMICA tutti gli atomi hanno un nucleo carico positivamente che possiede quasi tutta la massa atomica il nucleo è composto da protoni e neutroni che hanno massa = 1 nella scala dei pesi atomici
GLI ELEMENTI CHIMICI
 I costituenti degli elementi chimici GLI ELEMENTI CHIMICI Gli elementi chimici si differenziano per il numero di protoni nel nucleo. Il numero dei protoni definisce il numero atomico (Z) di un elemento.
I costituenti degli elementi chimici GLI ELEMENTI CHIMICI Gli elementi chimici si differenziano per il numero di protoni nel nucleo. Il numero dei protoni definisce il numero atomico (Z) di un elemento.
Le proprietà degli elementi sono funzioni periodiche dei rispettivi numeri atomici.
 I blocchi s, p, d ed f della Tavola Periodica 1 La tavola periodica La tavola periodica La tavola periodica Le proprietà degli elementi sono funzioni periodiche dei rispettivi numeri atomici. Si possono
I blocchi s, p, d ed f della Tavola Periodica 1 La tavola periodica La tavola periodica La tavola periodica Le proprietà degli elementi sono funzioni periodiche dei rispettivi numeri atomici. Si possono
L atomo. Il neutrone ha una massa 1839 volte superiore a quella dell elettrone. 3. Le particelle fondamentali dell atomo
 L atomo 3. Le particelle fondamentali dell atomo Gli atomi sono formati da tre particelle fondamentali: l elettrone con carica negativa; il protone con carica positiva; il neutrone privo di carica. Il
L atomo 3. Le particelle fondamentali dell atomo Gli atomi sono formati da tre particelle fondamentali: l elettrone con carica negativa; il protone con carica positiva; il neutrone privo di carica. Il
Le proprietà periodiche degli elementi
 Le proprietà periodiche degli elementi 1 Numerazione gruppi IUPAC Numero atomico Simbolo Peso atomico Metallo Semimetallo Non metallo 2 Numerazione gruppi tradizionale, n coincide con gli elettroni esterni
Le proprietà periodiche degli elementi 1 Numerazione gruppi IUPAC Numero atomico Simbolo Peso atomico Metallo Semimetallo Non metallo 2 Numerazione gruppi tradizionale, n coincide con gli elettroni esterni
Numero atomico Z : numero di protoni presenti nell atomo di quell elemento. Numero di massa A : somma dei protoni e dei neutroni in un atomo
 ATOMI E TAVOLA PERIODICA ATOMO: è il più piccolo costituente di un elemento che ne conservi le proprietà chimiche ELEMENTO: sostanza che non può essere scissa in una sostanza più semplice mediante reazione
ATOMI E TAVOLA PERIODICA ATOMO: è il più piccolo costituente di un elemento che ne conservi le proprietà chimiche ELEMENTO: sostanza che non può essere scissa in una sostanza più semplice mediante reazione
Sommario della lezione 4. Proprietà periodiche. Massa atomica e massa molecolare. Concetto di mole. Prime esercitazioni
 Sommario della lezione 4 Proprietà periodiche Massa atomica e massa molecolare Concetto di mole Prime esercitazioni Proprietà periodiche Il raggio atomico è definito come la metà della distanza minima
Sommario della lezione 4 Proprietà periodiche Massa atomica e massa molecolare Concetto di mole Prime esercitazioni Proprietà periodiche Il raggio atomico è definito come la metà della distanza minima
le SOSTANZE Sostanze elementari (ELEMENTI) COMPOSTI Costituiti da due o più atomi DIVERSI tra loro
 Il legame chimico In natura gli atomi sono solitamente legati ad altri in unità più complesse che, se aggregate fra loro costituiscono quello che macroscopicamente percepiamo come materia, le SOSTANZE
Il legame chimico In natura gli atomi sono solitamente legati ad altri in unità più complesse che, se aggregate fra loro costituiscono quello che macroscopicamente percepiamo come materia, le SOSTANZE
Legame covalente Puro Polare Legame dativo o di coordinazione Legame ionico Legame metallico
 I LEGAMI CHIMICI Legami atomici o forti Legami molecolari o deboli Legame covalente Puro Polare Legame dativo o di coordinazione Legame ionico Legame metallico Legame dipolo-dipolo Legame idrogeno Legame
I LEGAMI CHIMICI Legami atomici o forti Legami molecolari o deboli Legame covalente Puro Polare Legame dativo o di coordinazione Legame ionico Legame metallico Legame dipolo-dipolo Legame idrogeno Legame
Tavola periodica e previsione sul comportamento chimico degli elementi (numero di ossidazione)- orbitali ibridi
 Tavola periodica e previsione sul comportamento chimico degli elementi (numero di ossidazione)- orbitali ibridi Gli elementi sono ordinati secondo numero atomico Z ( numero dei protoni ) crescente Il numero
Tavola periodica e previsione sul comportamento chimico degli elementi (numero di ossidazione)- orbitali ibridi Gli elementi sono ordinati secondo numero atomico Z ( numero dei protoni ) crescente Il numero
U.M.A. e le masse ATOMICHE
 U.M.A. e le masse ATOMICHE L unità di massa atomica (u.m.a.) viene definita come 1/12 della massa del 12 C Il peso atomico (massa atomica relativa) di un atomo viene definito come: massa atomo considerato
U.M.A. e le masse ATOMICHE L unità di massa atomica (u.m.a.) viene definita come 1/12 della massa del 12 C Il peso atomico (massa atomica relativa) di un atomo viene definito come: massa atomo considerato
COMPORTAMENTO DUALISTICO della MATERIA
 COMPORTAMENTO DUALISTICO della MATERIA Come la luce anche la materia assume comportamento dualistico. Equazione di De Broglie: λ = h/mv Per oggetti macroscopici la lunghezza d onda è così piccola da non
COMPORTAMENTO DUALISTICO della MATERIA Come la luce anche la materia assume comportamento dualistico. Equazione di De Broglie: λ = h/mv Per oggetti macroscopici la lunghezza d onda è così piccola da non
CHIMICA: studio della struttura e delle trasformazioni della materia
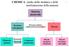 CHIMICA: studio della struttura e delle trasformazioni della materia!1 Materia (materali) Sostanze (omogenee) Processo fisico Miscele Elementi (atomi) Reazioni chimiche Composti (molecole) Miscele omogenee
CHIMICA: studio della struttura e delle trasformazioni della materia!1 Materia (materali) Sostanze (omogenee) Processo fisico Miscele Elementi (atomi) Reazioni chimiche Composti (molecole) Miscele omogenee
ATOMO. Legge della conservazione della massa Legge delle proporzioni definite Dalton
 Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (1808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti
Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (1808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti
PROVA 1. Dati i composti con formula KBr e HClO 2 :
 PROVA 1 Dati i composti con formula KBr e HClO 2 : 1) Individuare a quale categoria di composti appartengono (ossidi,anidridi,idrossidi,acidi,sali) 2) Determinare le valenze o i numeri di ossidazione di
PROVA 1 Dati i composti con formula KBr e HClO 2 : 1) Individuare a quale categoria di composti appartengono (ossidi,anidridi,idrossidi,acidi,sali) 2) Determinare le valenze o i numeri di ossidazione di
Il legame chimico. Lezioni 17-20
 Il legame chimico Lezioni 17-20 1 Il legame chimico Le forze attrattive di natura elettrica che tengono uniti gli atomi in molecole o in composti ionici sono dette legami chimici. Legami atomici: covalente
Il legame chimico Lezioni 17-20 1 Il legame chimico Le forze attrattive di natura elettrica che tengono uniti gli atomi in molecole o in composti ionici sono dette legami chimici. Legami atomici: covalente
Corso di CHIMICA LEZIONE 3
 Corso di CHIMICA LEZIONE 3 1 2 3 4 5 6 7 H Li Na K Fr Be Ma g Ca Ba TAVOLA PERIODICA He I II s 1 s 2 III IV V VI VII VIII p 1 p 2 p 3 p 4 p 5 p 6 blocco s La Ac 6 7 d 1 d 2 d 3 d 4 d 5 d 6 d 7 d 8 d 9
Corso di CHIMICA LEZIONE 3 1 2 3 4 5 6 7 H Li Na K Fr Be Ma g Ca Ba TAVOLA PERIODICA He I II s 1 s 2 III IV V VI VII VIII p 1 p 2 p 3 p 4 p 5 p 6 blocco s La Ac 6 7 d 1 d 2 d 3 d 4 d 5 d 6 d 7 d 8 d 9
n l c = velocità di propagazione nel vuoto = m/s l = lunghezza d onda [cm]
![n l c = velocità di propagazione nel vuoto = m/s l = lunghezza d onda [cm] n l c = velocità di propagazione nel vuoto = m/s l = lunghezza d onda [cm]](/thumbs/92/108343390.jpg) Tavola Mendeleev Quando gli elementi vengono riportati secondo un ordine di peso atomico crescente, le proprietà degli elementi si ripetono ad intervalli regolari c l n n l c = velocità di propagazione
Tavola Mendeleev Quando gli elementi vengono riportati secondo un ordine di peso atomico crescente, le proprietà degli elementi si ripetono ad intervalli regolari c l n n l c = velocità di propagazione
Struttura dell atomo atomo particelle sub-atomiche - protoni positiva - neutroni } nucleoni - elettroni negativa elemento
 Struttura dell atomo L atomo è la più piccola parte dell elemento che conserva le proprietà dell elemento Negli atomi ci sono tre diverse particelle sub-atomiche: - protoni (con carica positiva unitaria)
Struttura dell atomo L atomo è la più piccola parte dell elemento che conserva le proprietà dell elemento Negli atomi ci sono tre diverse particelle sub-atomiche: - protoni (con carica positiva unitaria)
I LEGAMI CHIMICI. Configurazione elettronica stabile: è quella in cui tutti i livelli energetici dell atomo sono pieni di elettroni
 I LEGAMI CIMICI In natura sono pochi gli elementi che presentano atomi allo stato libero. Gli unici elementi che sono costituiti da atomi isolati si chiamano gas nobili o inerti, formano il gruppo VIII
I LEGAMI CIMICI In natura sono pochi gli elementi che presentano atomi allo stato libero. Gli unici elementi che sono costituiti da atomi isolati si chiamano gas nobili o inerti, formano il gruppo VIII
Il legame chimico. Legame metallico
 Il legame chimico Legame ionico: un atomo cede elettroni e un altro li acquista con formazione di ioni di carica opposta che vengono tenuti insieme da forze elettrostatiche. Legame covalente: si realizza
Il legame chimico Legame ionico: un atomo cede elettroni e un altro li acquista con formazione di ioni di carica opposta che vengono tenuti insieme da forze elettrostatiche. Legame covalente: si realizza
ATOMO. Avogadro (1811) Volumi uguali di gas diversi contengono un ugual numero di MOLECOLE (N A =6,022*10 23 )
 ATOMO Democrito IV secolo A.C. (atomos = indivisibile) Lavoisier (1770) Legge della conservazione della massa in una trasf. chimica es. C + O 2 CO 2 Dalton (1808) Teoria atomica E=mc 2 Avogadro (1811)
ATOMO Democrito IV secolo A.C. (atomos = indivisibile) Lavoisier (1770) Legge della conservazione della massa in una trasf. chimica es. C + O 2 CO 2 Dalton (1808) Teoria atomica E=mc 2 Avogadro (1811)
Tavola Periodica degli Elementi: Gruppi e Periodi
 La Tavola Periodica Tavola Periodica degli Elementi: Gruppi e Periodi Periodi: Proprietà variabili con continuità. Periodi Gruppi: Proprietà Chimiche simili Gruppi Proprietà Periodiche e Struttura Elettroniche
La Tavola Periodica Tavola Periodica degli Elementi: Gruppi e Periodi Periodi: Proprietà variabili con continuità. Periodi Gruppi: Proprietà Chimiche simili Gruppi Proprietà Periodiche e Struttura Elettroniche
Configurazione elettronica e Tavola periodica. Lezioni 13-16
 Configurazione elettronica e Tavola periodica Lezioni 13-16 Orbitali possibili Gusci e sottogusci Gli elettroni che occupano orbitali con lo stesso valore di numero quantico principale n si dice che sono
Configurazione elettronica e Tavola periodica Lezioni 13-16 Orbitali possibili Gusci e sottogusci Gli elettroni che occupano orbitali con lo stesso valore di numero quantico principale n si dice che sono
I legami chimici. Perché si formano i legami? Perché si formano i legami? 16/01/2019. Come e perché gli atomi si legano tra loro
 I legami chimici Come e perché gli atomi si legano tra loro Perché si formano i legami? In natura, se non in casi eccezionali, non si trovano atomi liberi. Per separare due atomi legati è necessario fornire
I legami chimici Come e perché gli atomi si legano tra loro Perché si formano i legami? In natura, se non in casi eccezionali, non si trovano atomi liberi. Per separare due atomi legati è necessario fornire
Le proprietà periodiche degli elementi
 Le proprietà periodiche degli elementi 1 2 1 Numerazione gruppi IUPAC Numero atomico Simbolo Peso atomico Metallo Semimetallo Non metallo 1s 2s2p 3s3p 4s3d4p 5s4d5p 6s4f5d6p 7s5f6d7p 3 Numerazione gruppi
Le proprietà periodiche degli elementi 1 2 1 Numerazione gruppi IUPAC Numero atomico Simbolo Peso atomico Metallo Semimetallo Non metallo 1s 2s2p 3s3p 4s3d4p 5s4d5p 6s4f5d6p 7s5f6d7p 3 Numerazione gruppi
Università degli studi di MILANO Facoltà di AGRARIA. El. di Chimica e Chimica Fisica. Mod. 1 CHIMICA. Mod. 2 CHIMICA FISICA.
 Università degli studi di MILANO Facoltà di AGRARIA El. di Chimica e Chimica Fisica Mod. 1 CHIMICA Mod. 2 CHIMICA FISICA Lezione 4 Anno Accademico 2010-2011 Docente: Dimitrios Fessas Si riconoscono così
Università degli studi di MILANO Facoltà di AGRARIA El. di Chimica e Chimica Fisica Mod. 1 CHIMICA Mod. 2 CHIMICA FISICA Lezione 4 Anno Accademico 2010-2011 Docente: Dimitrios Fessas Si riconoscono così
Il sistema periodico degli elementi
 Il sistema periodico degli elementi Cos è il sistema periodico? Che informazioni ne possiamo ricavare? Che predizioni possiamo trarne? 15/10/2012 Meyer: periodicità delle variazioni del volume molare atomico
Il sistema periodico degli elementi Cos è il sistema periodico? Che informazioni ne possiamo ricavare? Che predizioni possiamo trarne? 15/10/2012 Meyer: periodicità delle variazioni del volume molare atomico
RIASSUNTI DI CHIMICA
 Tecla Spelgatti RIASSUNTI DI CHIMICA per il liceo scientifico 2 - LA TAVOLA PERIODICA Questo testo è distribuito con licenza Common Creative: http://creativecommons.org/licenses/ CC BY-NC-ND Attribuzione
Tecla Spelgatti RIASSUNTI DI CHIMICA per il liceo scientifico 2 - LA TAVOLA PERIODICA Questo testo è distribuito con licenza Common Creative: http://creativecommons.org/licenses/ CC BY-NC-ND Attribuzione
Definizioni. Vecchia: derivata da organismi viventi Nuova: la chimica dei composti del carbonio Da inorganico a organico, Wöhler, 1828
 CHIMICA ORGANICA 4 Definizioni Vecchia: derivata da organismi viventi Nuova: la chimica dei composti del carbonio Da inorganico a organico, Wöhler, 828 + - NH 4 OCN ammonio cianato calore O H 2 N C NH
CHIMICA ORGANICA 4 Definizioni Vecchia: derivata da organismi viventi Nuova: la chimica dei composti del carbonio Da inorganico a organico, Wöhler, 828 + - NH 4 OCN ammonio cianato calore O H 2 N C NH
ORBITALE ATOMICO. Forma
 L ATOMO ORBITALE ATOMICO n (numero quantico principale) Energia e Dimensione l (numero quantico azimutale) Forma m l (numero quantico magnetico) Orientazione nello spazio l dipende da n assume n valori:
L ATOMO ORBITALE ATOMICO n (numero quantico principale) Energia e Dimensione l (numero quantico azimutale) Forma m l (numero quantico magnetico) Orientazione nello spazio l dipende da n assume n valori:
Le proprietà periodiche degli elementi
 Le proprietà periodiche degli elementi 1 Numerazione gruppi IUPAC Numero atomico Simbolo Peso atomico Metallo Semimetallo Non metallo 1s 2s2p 3s3p 4s3d4p 5s4d5p 6s4f5d6p 7s5f6d7p 2 Numerazione gruppi tradizionale,
Le proprietà periodiche degli elementi 1 Numerazione gruppi IUPAC Numero atomico Simbolo Peso atomico Metallo Semimetallo Non metallo 1s 2s2p 3s3p 4s3d4p 5s4d5p 6s4f5d6p 7s5f6d7p 2 Numerazione gruppi tradizionale,
TAVOLA PERIODICA. 118 elementi, di cui 92 presenti in natura
 TAVOLA PERIODICA 118 elementi, di cui 92 presenti in natura L ordine della tavola periodica: individuare un criterio per classificare gli elementi! L ordine della tavola periodica: individuare un criterio
TAVOLA PERIODICA 118 elementi, di cui 92 presenti in natura L ordine della tavola periodica: individuare un criterio per classificare gli elementi! L ordine della tavola periodica: individuare un criterio
LEGAMI CHIMICI. Gli elettroni esterni sono implicati nella formazione dei legami chimici
 LEGAMI CHIMICI Gli elettroni esterni sono implicati nella formazione dei legami chimici La VALENZA di un elemento è data dal numero di elettroni che esso deve perdere, o acquistare, o mettere in comune
LEGAMI CHIMICI Gli elettroni esterni sono implicati nella formazione dei legami chimici La VALENZA di un elemento è data dal numero di elettroni che esso deve perdere, o acquistare, o mettere in comune
Molecole e legami. Chimica generale
 Molecole e legami Chimica generale Atomi e molecole È estremamente difficile trovare in natura una sostanza formata solamente da atomi semplici Solo i gas inerti dell ottavo gruppo sono presenti in natura
Molecole e legami Chimica generale Atomi e molecole È estremamente difficile trovare in natura una sostanza formata solamente da atomi semplici Solo i gas inerti dell ottavo gruppo sono presenti in natura
Per comprendere le proprietà delle molecole è molto importante determinare:
 Legame chimico Per comprendere le proprietà delle molecole è molto importante determinare: la STRUTTURA, ovvero il modo in cui gli atomi sono disposti nello spazio la NATURA DEL LEGAME, ovvero il tipo
Legame chimico Per comprendere le proprietà delle molecole è molto importante determinare: la STRUTTURA, ovvero il modo in cui gli atomi sono disposti nello spazio la NATURA DEL LEGAME, ovvero il tipo
METALLI: bassa energia di ionizzazione bassa affinità elettronica. NON METALLI: elevata energia di ionizzazione elevata affinità elettronica
 METALLI: bassa energia di ionizzazione bassa affinità elettronica NON METALLI: elevata energia di ionizzazione elevata affinità elettronica LEGAME CHIMICO La formazione di legami tra atomi per formare
METALLI: bassa energia di ionizzazione bassa affinità elettronica NON METALLI: elevata energia di ionizzazione elevata affinità elettronica LEGAME CHIMICO La formazione di legami tra atomi per formare
Le proprietà periodiche degli elementi
 Le proprietà periodiche degli elementi 1 Numerazione gruppi IUPAC Numero atomico Simbolo Peso atomico Metallo Semimetallo Non metallo 1s 2s2p 3s3p 4s3d4p 5s4d5p 6s4f5d6p 7s5f6d7p 2 Numerazione gruppi tradizionale,
Le proprietà periodiche degli elementi 1 Numerazione gruppi IUPAC Numero atomico Simbolo Peso atomico Metallo Semimetallo Non metallo 1s 2s2p 3s3p 4s3d4p 5s4d5p 6s4f5d6p 7s5f6d7p 2 Numerazione gruppi tradizionale,
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 10 Il sistema periodico 1. L energia di legame 2. I gas nobili e le regole dell ottetto 3. Il
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 10 Il sistema periodico 1. L energia di legame 2. I gas nobili e le regole dell ottetto 3. Il
Chimica. Lezione 2 Il legame chimico Parte I
 Chimica Lezione 2 Il legame chimico Parte I Gli ioni Uno ione è un ATOMO o una MOLECOLA che possiede una CARICA (positiva o negativa) È quindi una specie chimica che ha acquistato o ceduto uno o più elettroni
Chimica Lezione 2 Il legame chimico Parte I Gli ioni Uno ione è un ATOMO o una MOLECOLA che possiede una CARICA (positiva o negativa) È quindi una specie chimica che ha acquistato o ceduto uno o più elettroni
PROPRIETÀ PERIODICHE DEGLI ELEMENTI
 PROPRIETÀ PERIODICHE DEGLI ELEMENTI 1) Energia di ionizzazione E ion Energia necessaria per sottrarre ad un atomo, allo stato di gas monoatomico, un elettrone A (g) d A + (g) + e - E ion processo endotermico
PROPRIETÀ PERIODICHE DEGLI ELEMENTI 1) Energia di ionizzazione E ion Energia necessaria per sottrarre ad un atomo, allo stato di gas monoatomico, un elettrone A (g) d A + (g) + e - E ion processo endotermico
COMPETENZE ABILITÀ CONOSCENZE. descrivere la. Comprendere ed applicare analogie relative ai concetti presi in analisi. struttura.
 ca descrivere la struttura dell atomo, la tavola periodica e le sue caratteristiche per spiegare le differenze tra i vari tipi di legami, descrivendoli e interpretandoli alla luce degli elettroni di valenza
ca descrivere la struttura dell atomo, la tavola periodica e le sue caratteristiche per spiegare le differenze tra i vari tipi di legami, descrivendoli e interpretandoli alla luce degli elettroni di valenza
CHIMICA: studio della struttura e delle trasformazioni della materia
 CHIMICA: studio della struttura e delle trasformazioni della materia 1 Materia (materali) Sostanze (omogenee) Processo fisico Miscele Elementi (atomi) Reazioni chimiche Composti (molecole) Miscele omogenee
CHIMICA: studio della struttura e delle trasformazioni della materia 1 Materia (materali) Sostanze (omogenee) Processo fisico Miscele Elementi (atomi) Reazioni chimiche Composti (molecole) Miscele omogenee
Il Legame Chimico e la Struttura Molecolare
 2017 1 Il Legame Chimico e la Struttura Molecolare LEGAME CIMICO 2 In che modo gli atomi in una molecola o uno ione poliatomico interagiscono?! Perchè alcune molecole sono planari ed altre non lo sono?!
2017 1 Il Legame Chimico e la Struttura Molecolare LEGAME CIMICO 2 In che modo gli atomi in una molecola o uno ione poliatomico interagiscono?! Perchè alcune molecole sono planari ed altre non lo sono?!
Chimica. Lezione 2 Parte II Composti ionici e molecolari
 Chimica Lezione 2 Parte II Composti ionici e molecolari Composti molecolari Gli ELEMENTI chimici (ad eccezione dei gas nobili) vivono in aggregati più o meno complessi Sono aggregati discreti (hanno un
Chimica Lezione 2 Parte II Composti ionici e molecolari Composti molecolari Gli ELEMENTI chimici (ad eccezione dei gas nobili) vivono in aggregati più o meno complessi Sono aggregati discreti (hanno un
APPUNTI DELLE LEZIONI DI. Scienza e Tecnologia dei Materiali (Energetica)
 Corso di Laurea in Ingegneria Energetica APPUNTI DELLE LEZIONI DI Scienza e Tecnologia dei Materiali (Energetica) Anno Accademico 2012/2013 Sito web: http://www.uniroma2.it/didattica/stm_ene Prof. Ing.
Corso di Laurea in Ingegneria Energetica APPUNTI DELLE LEZIONI DI Scienza e Tecnologia dei Materiali (Energetica) Anno Accademico 2012/2013 Sito web: http://www.uniroma2.it/didattica/stm_ene Prof. Ing.
CHIMICA ORGANICA (CANALE M-Z)
 CHIMICA ORGANICA (CANALE M-Z) Durata corso (8 marzo-10 maggio) + settimana recupero Orario lezioni Esercitazioni Modalità d esame Esoneri Libri di testo Ricevimento studenti e-mail/telefono docente: Michela.Salamone@uniroma2.it
CHIMICA ORGANICA (CANALE M-Z) Durata corso (8 marzo-10 maggio) + settimana recupero Orario lezioni Esercitazioni Modalità d esame Esoneri Libri di testo Ricevimento studenti e-mail/telefono docente: Michela.Salamone@uniroma2.it
Scienziati in Erba Chimica
 Scienziati in Erba Chimica Acqua Oro Zucchero L atomo Acqua Oro Zucchero La Teoria Atomica di Dalton (1808) 1. Gli Elementi sono composti da particelle estremamente piccole, denominate atomi. 2. Tutti
Scienziati in Erba Chimica Acqua Oro Zucchero L atomo Acqua Oro Zucchero La Teoria Atomica di Dalton (1808) 1. Gli Elementi sono composti da particelle estremamente piccole, denominate atomi. 2. Tutti
Atomi e molecole. Gli atomi degli elementi si trovano in natura generalmente combinati tra loro in molecole o composti ionici
 IL LEGAME CHIMICO Atomi e molecole È estremamente difficile trovare in natura una sostanza formata da singoli atomi isolati Solo i gas nobili sono presenti in natura come gas monoatomici Gli atomi degli
IL LEGAME CHIMICO Atomi e molecole È estremamente difficile trovare in natura una sostanza formata da singoli atomi isolati Solo i gas nobili sono presenti in natura come gas monoatomici Gli atomi degli
CHIMICA E BIOCHIMICA
 CHIMICA E BIOCHIMICA CHIMICA: studia la materia Materia= ogni cosa che ha massa Proprietà Struttura Trasformazioni (Reazioni) BIOCHIMICA: studia la chimica degli organismi viventi Di cosa è composta la
CHIMICA E BIOCHIMICA CHIMICA: studia la materia Materia= ogni cosa che ha massa Proprietà Struttura Trasformazioni (Reazioni) BIOCHIMICA: studia la chimica degli organismi viventi Di cosa è composta la
Esperto prof. C. Formica
 Esperto prof. C. Formica Immagini e testi tratti dai website di: genome.wellcome.ac.uk, dnaftb.org, unipv.it, unimi.it, wikipedia.it, unibs.it, unina.it, uniroma.it, nih.gov, zanichelli.it, sciencemag.org,
Esperto prof. C. Formica Immagini e testi tratti dai website di: genome.wellcome.ac.uk, dnaftb.org, unipv.it, unimi.it, wikipedia.it, unibs.it, unina.it, uniroma.it, nih.gov, zanichelli.it, sciencemag.org,
Struttura atomica, configurazione elettronica e periodicità chimica
 Struttura atomica, configurazione elettronica e periodicità chimica Dualismo onda-particella (V. de Broglie) Principio di indeterminazione (W. Heisenberg) Equazione di Shrodinger(1925) Modello quantomeccanico
Struttura atomica, configurazione elettronica e periodicità chimica Dualismo onda-particella (V. de Broglie) Principio di indeterminazione (W. Heisenberg) Equazione di Shrodinger(1925) Modello quantomeccanico
Gruppo costituito da elementi con uguale configurazione elettronica esterna.
 SISTEMA PERIODICO Ciascun elemento è caratterizzato dal n atomico Z, che esprime il n di cariche positive (protoni), presenti nel nucleo dell'atomo. La tabella periodica si articola in gruppi e periodi
SISTEMA PERIODICO Ciascun elemento è caratterizzato dal n atomico Z, che esprime il n di cariche positive (protoni), presenti nel nucleo dell'atomo. La tabella periodica si articola in gruppi e periodi
Lavoisier (1770) Legge della conservazione della massa in una trasf. chimica es. C + O 2 CO 2 Dalton (1808) Teoria atomica
 ATOMO Democrito IV secolo A.C. Lavoisier (1770) Legge della conservazione della massa in una trasf. chimica es. C + O 2 CO 2 Dalton (1808) Teoria atomica E=mc 2 Avogadro (1811) Volumi uguali di gas diversi
ATOMO Democrito IV secolo A.C. Lavoisier (1770) Legge della conservazione della massa in una trasf. chimica es. C + O 2 CO 2 Dalton (1808) Teoria atomica E=mc 2 Avogadro (1811) Volumi uguali di gas diversi
Tavola periodica degli elementi
 Tavola periodica degli elementi!1 I chimici Mendeleev (russo) e Meyer (tedesco) scoprirono indipendentemente che ordinando gli elementi secondo peso atomico crescente in file orizzontali sovrapposte, si
Tavola periodica degli elementi!1 I chimici Mendeleev (russo) e Meyer (tedesco) scoprirono indipendentemente che ordinando gli elementi secondo peso atomico crescente in file orizzontali sovrapposte, si
Orbitali nei primi tre livelli
 Orbitali nei primi tre livelli La tavola periodica degli elementi Numeri quantici e tavola Configurazioni elettroniche degli atomi Elenco degli orbitali occupati in un atomo nel suo stato fondamentale
Orbitali nei primi tre livelli La tavola periodica degli elementi Numeri quantici e tavola Configurazioni elettroniche degli atomi Elenco degli orbitali occupati in un atomo nel suo stato fondamentale
La materia. https://www.youtube.com/watch?v=sfvvxv2deaa
 La materia https://www.youtube.com/watch?v=sfvvxv2deaa Un materiale sottoposto a filtrazione, si suddivide in un solido bianco A e in un liquido B. Il liquido B, per mezzo della distillazione, è separato
La materia https://www.youtube.com/watch?v=sfvvxv2deaa Un materiale sottoposto a filtrazione, si suddivide in un solido bianco A e in un liquido B. Il liquido B, per mezzo della distillazione, è separato
IL LEGAME CHIMICO. Per descrivere come gli elettroni si distribuiscono nell atomo attorno al nucleo si può far riferimento al MODELLO A GUSCI
 IL LEGAME CIMICO Come dagli atomi si costruiscono le molecole 02/19/08 0959 PM 1 Per descrivere come gli elettroni si distribuiscono nell atomo attorno al nucleo si può far riferimento al MODELLO A GUSCI
IL LEGAME CIMICO Come dagli atomi si costruiscono le molecole 02/19/08 0959 PM 1 Per descrivere come gli elettroni si distribuiscono nell atomo attorno al nucleo si può far riferimento al MODELLO A GUSCI
Gli orbitali atomici. Il modo più semplice di visualizzare un atomo. TUTTAVIA NON POSSO DIRE CON PRECISIONE DOVE SI TROVA OGNI e -
 Gli orbitali atomici Il modo più semplice di visualizzare un atomo TUTTAVIA NON POSSO DIRE CON PRECISIONE DOVE SI TROVA OGNI e - ORBITALI ATOMICI: regione di spazio (con forma tipica) dove c è una elevata
Gli orbitali atomici Il modo più semplice di visualizzare un atomo TUTTAVIA NON POSSO DIRE CON PRECISIONE DOVE SI TROVA OGNI e - ORBITALI ATOMICI: regione di spazio (con forma tipica) dove c è una elevata
Regola dell'ottetto e suo superamento Legame ionico Covalenza e ordine di legame Carica formale Risonanza ElettronegativitÄ e polaritä del legame
 IL LEGAME CHIMICO Regola dell'ottetto e suo superamento Legame ionico Covalenza e ordine di legame Carica formale Risonanza ElettronegativitÄ e polaritä del legame 1 IL LEGAME CHIMICO Il legame chimico
IL LEGAME CHIMICO Regola dell'ottetto e suo superamento Legame ionico Covalenza e ordine di legame Carica formale Risonanza ElettronegativitÄ e polaritä del legame 1 IL LEGAME CHIMICO Il legame chimico
Corso di CHIMICA LEZIONE 2
 Corso di CHIMICA LEZIONE 2 MODELLO ATOMICO DI THOMSON 1904 L atomo è formato da una sfera carica positivamente in cui gli elettroni con carica negativa, distribuiti uniformemente all interno, neutralizzano
Corso di CHIMICA LEZIONE 2 MODELLO ATOMICO DI THOMSON 1904 L atomo è formato da una sfera carica positivamente in cui gli elettroni con carica negativa, distribuiti uniformemente all interno, neutralizzano
Le idee della chimica
 G. Valitutti A.Tifi A.Gentile Seconda edizione Copyright 2009 Zanichelli editore Capitolo 10 I legami chimici 1. L energia di legame 2. I gas nobili e a regola dell ottetto 3. Il legame covalente 4. Il
G. Valitutti A.Tifi A.Gentile Seconda edizione Copyright 2009 Zanichelli editore Capitolo 10 I legami chimici 1. L energia di legame 2. I gas nobili e a regola dell ottetto 3. Il legame covalente 4. Il
Distribuzione degli elettroni negli orbitali atomici Aufbau
 1s 2s 2p 3s 3p 3d 4s 4p 4d 4f 5s 5p 5d 5f 6s 6p 6d 7s 7p 8s Distribuzione degli elettroni negli orbitali atomici Aufbau Principio di esclusione di Pauli (1925): Due elettroni in un atomo non possono essere
1s 2s 2p 3s 3p 3d 4s 4p 4d 4f 5s 5p 5d 5f 6s 6p 6d 7s 7p 8s Distribuzione degli elettroni negli orbitali atomici Aufbau Principio di esclusione di Pauli (1925): Due elettroni in un atomo non possono essere
Bagatti, Corradi, Desco, Ropa. Chimica. seconda edizione
 Bagatti, Corradi, Desco, Ropa Chimica seconda edizione Bagatti, Corradi, Desco, Ropa, Chimica seconda edizione Capitolo 6. I legami chimici SEGUI LA MAPPA riconoscere valutare dativo puro 1 Gli atomi difficilmente
Bagatti, Corradi, Desco, Ropa Chimica seconda edizione Bagatti, Corradi, Desco, Ropa, Chimica seconda edizione Capitolo 6. I legami chimici SEGUI LA MAPPA riconoscere valutare dativo puro 1 Gli atomi difficilmente
I gas nobili esistono (solo) allo stato di gas monoatomico
 I gas nobili esistono (solo) allo stato di gas monoatomico In condizioni normali non formano composti, dimostrando che i loro atomi non tendono a legarsi (inerzia chimica) Legame chimico G. N. Lewis (1916):
I gas nobili esistono (solo) allo stato di gas monoatomico In condizioni normali non formano composti, dimostrando che i loro atomi non tendono a legarsi (inerzia chimica) Legame chimico G. N. Lewis (1916):
1s 2s 2p 3s 3p 3d 4s 4p 4d 4f 5s 5p 5d 5f... 6s...
 1 - Quanti sono gli orbitali contenenti elettroni in un atomo il cui numero atomico è Z = 16? A 9 B 8 C 7 D 6 energia 5s 4s 4p 3p 3d 3s 2s 2p 2s 2p 3s 3p 3d 4s 4p 4d 4f 5s 5p 5d 5f... 6s... successione
1 - Quanti sono gli orbitali contenenti elettroni in un atomo il cui numero atomico è Z = 16? A 9 B 8 C 7 D 6 energia 5s 4s 4p 3p 3d 3s 2s 2p 2s 2p 3s 3p 3d 4s 4p 4d 4f 5s 5p 5d 5f... 6s... successione
Il Legame Chimico e la Struttura Molecolare
 A.A.2016 2017 CCS-Biologia CCS-Scienze Geologiche 1 Il Legame Chimico e la Struttura Molecolare Energia di interazione di due atomi di idrogeno Cap 8. 1-7, 9, 10(a/b), 17-20, 27-28, 31-33, 37-40, 52, 93-96
A.A.2016 2017 CCS-Biologia CCS-Scienze Geologiche 1 Il Legame Chimico e la Struttura Molecolare Energia di interazione di due atomi di idrogeno Cap 8. 1-7, 9, 10(a/b), 17-20, 27-28, 31-33, 37-40, 52, 93-96
Corso di Studi di Fisica Corso di Chimica
 Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Lezioni 3-4 2009 Schema del funzionamento di uno spettrometro di massa Spettro di massa del mercurio 196 Hg 0,146 % 202 Hg 29,80
Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Lezioni 3-4 2009 Schema del funzionamento di uno spettrometro di massa Spettro di massa del mercurio 196 Hg 0,146 % 202 Hg 29,80
Elementi sistemati nella TAVOLA PERIODICA DEGLI ELEMENTI in base al numero atomico crescente O, H, N, C (+ del 96% della materia vivente)
 OVERVIEW Atomo: più piccola porzione di un elemento che mantiene le proprietà chimiche dello stesso Teoria atomica e tavola periodica Legami e interazioni degli atomi Acqua e le sue proprietà Acidi e basi
OVERVIEW Atomo: più piccola porzione di un elemento che mantiene le proprietà chimiche dello stesso Teoria atomica e tavola periodica Legami e interazioni degli atomi Acqua e le sue proprietà Acidi e basi
1. L energia di legame. 2. I gas nobili e a regola dell ottetto. 3. Il legame covalente. 4. Il legame covalente dativo. 5. Il legame covalente polare
 Capitolo 10 I legami chimici 1. L energia di legame 2. I gas nobili e a regola dell ottetto 3. Il legame covalente 4. Il legame covalente dativo 5. Il legame covalente polare 6. Il legame ionico 7. I composti
Capitolo 10 I legami chimici 1. L energia di legame 2. I gas nobili e a regola dell ottetto 3. Il legame covalente 4. Il legame covalente dativo 5. Il legame covalente polare 6. Il legame ionico 7. I composti
LEGAME CHIMICO In genere gli atomi si trovano combinati fra loro in composti molecolari, ionici o metallici.
 LEGAME CIMICO In genere gli atomi si trovano combinati fra loro in composti molecolari, ionici o metallici. Fra le poche eccezioni notiamo i gas nobili che sono particolarmente stabili e non reattivi.
LEGAME CIMICO In genere gli atomi si trovano combinati fra loro in composti molecolari, ionici o metallici. Fra le poche eccezioni notiamo i gas nobili che sono particolarmente stabili e non reattivi.
Configurazioni elettroniche e periodicità
 Configurazioni elettroniche e periodicità Le configurazioni elettroniche dei vari elementi sono una funzione periodica del numero atomico Z. Gli elementi che appartengono allo stesso gruppo nella tavola
Configurazioni elettroniche e periodicità Le configurazioni elettroniche dei vari elementi sono una funzione periodica del numero atomico Z. Gli elementi che appartengono allo stesso gruppo nella tavola
PROPRIETA PERIODICHE
 PROPRIETA PERIODICHE Sono tutte quelle proprietà il cui andamento lungo un periodo o lungo un gruppo presenta un andamento periodico. Le più rilevanti sono: 1) Raggi atomici (o ionici) 2) Potenziale di
PROPRIETA PERIODICHE Sono tutte quelle proprietà il cui andamento lungo un periodo o lungo un gruppo presenta un andamento periodico. Le più rilevanti sono: 1) Raggi atomici (o ionici) 2) Potenziale di
C Ca Ce Cf Co Cr Cs Cu
 Elementi Composti ionici (forze elettrostatiche, edifici ionici) molecolari (ripetersi periodico di molecole) Simboli C Ca Ce Cf Co Cr Cs Cu Formule Indici H 2 SO 4 CO 2 H 2 O N 2 Na 2 CO 3 O 2 Mg(NO 3
Elementi Composti ionici (forze elettrostatiche, edifici ionici) molecolari (ripetersi periodico di molecole) Simboli C Ca Ce Cf Co Cr Cs Cu Formule Indici H 2 SO 4 CO 2 H 2 O N 2 Na 2 CO 3 O 2 Mg(NO 3
LA TEORIA ATOMICA E L ATOMO Da pagina 81 a pagina 107
 LA TEORIA ATOMICA E L ATOMO Da pagina 81 a pagina 107 4.1 LA TEORIA ATOMICA La materia è formata da atomi, a loro volta costituiti da particelle subatomiche; Esistono tanti tipi di atomi quanti sono gli
LA TEORIA ATOMICA E L ATOMO Da pagina 81 a pagina 107 4.1 LA TEORIA ATOMICA La materia è formata da atomi, a loro volta costituiti da particelle subatomiche; Esistono tanti tipi di atomi quanti sono gli
La rappresentazione degli orbitali Orbitali s ( l = 0 )
 Rappresentazione degli orbitali s dell atomo di idrogeno 2 4 r 2 1s r = a 0 (raggio 1 orbita di Bohr) presenza di (n-1) NODI ( 2 =0) r 0 dp /dr 0 r dp /dr 0 massimi in accordo con Bohr r 4a 0 (raggio 2
Rappresentazione degli orbitali s dell atomo di idrogeno 2 4 r 2 1s r = a 0 (raggio 1 orbita di Bohr) presenza di (n-1) NODI ( 2 =0) r 0 dp /dr 0 r dp /dr 0 massimi in accordo con Bohr r 4a 0 (raggio 2
ESERCIZI W X Y Z. Numero di massa Neutroni nel nucleo Soluzione
 ESERCIZI 1) La massa di un elettrone, rispetto a quella di un protone, è: a. uguale b. 1850 volte più piccola c. 100 volte più piccola d. 18,5 volte più piccola 2) I raggi catodici sono: a. radiazioni
ESERCIZI 1) La massa di un elettrone, rispetto a quella di un protone, è: a. uguale b. 1850 volte più piccola c. 100 volte più piccola d. 18,5 volte più piccola 2) I raggi catodici sono: a. radiazioni
