DOSSIER Manuale chimico. Operazione: URAGANO ROSSO Data: Settembre Pagina 1 di 9. Allegato di: FOXTROT LABORATORIO CHIMICO
|
|
|
- Simone Leoni
- 2 anni fa
- Visualizzazioni
Transcript
1 DOSSIER Manuale chimico Allegato di: FOXTROT LABORATORIO CHIMICO Risorsa Intelligence: TECHINT Da: Comando NATO sez. Europa Pagina 1 di 9
2 Non sappiamo esattamente a cosa andrete in contro una volta entrati nel laboratorio, quindi sarà vostra cura adottare tutte le misure necessarie per svolgere al meglio il compito. Il comando non è disposto a rischiare una squadra di chimici per la neutralizzazione del composto quindi dovrete appuntarvi alcuni concetti utili a capire come annullare il composto attraverso le eventuali indicazioni che troverete in loco. Il team di ricerca chimica ha preparato un allegato per istruirvi al meglio su più argomenti possibili in modo da rendervi autonomi nello svolgimento delle operazioni. La chimica studia le trasformazioni chimiche, ossia le trasformazioni che modificano la natura stessa della materia che le subisce, come la combustione del legno o la trasformazione di prodotti petroliferi in materie plastiche. Tali trasformazioni vengono esaminate anche a livello sub-microscopico, attraverso la composizione e la struttura della materia e il comportamento di atomi e molecole. Nelle trasformazioni fisiche, invece, la natura della materia resta inalterata, come nei passaggi da uno stato di aggregazione a un altro (passaggi di stato), quando un metallo conduce la corrente, ecc. La materia si presenta sotto forma di materiali diversi, soprattutto di miscugli (o miscele) di sostanze pure; tuttavia, in qualunque forma si presenti, è sempre costituita da atomi e molecole. Una sostanza pura, o semplicemente sostanza, è un materiale che presenta una composizione ben definita e omogenea, cioè uguale in tutte le sue parti, e si distingue in: elemento (o sostanza elementare), in quanto non è scindibile in sostanze più semplici; composto (o sostanza composta), in quanto è costituita da elementi diversi ed è scomponibile in tali elementi soltanto attraverso trasformazioni chimiche. Le sostanze pure vengono rappresentate mediante simboli. Il simbolo di un elemento esprime l atomo dell elemento, ma generalmente le sostanze si trovano sotto forma di molecole, più stabili. La molecola è la più piccola parte della materia capace di avere una esistenza stabile, ed è costituita quasi sempre da più atomi legati tra loro, secondo un rapporto numerico definito e costante. In una reazione chimica, viene detto coefficiente stechiometrico il numero che precede il simbolo dell atomo o della molecola della sostanza (il valore 1 si sottintende) e che indica il numero degli atomi o delle molecole della sostanza. Invece, l indice numerico è il numero che si scrive a deponente del simbolo di un elemento e indica il numero di atomi di quell elemento nella molecola. I simboli H2, H2O e CO2 sono detti formule molecolari (o formule brute) rispettivamente dell idrogeno, dell acqua e dell anidride carbonica ed Pagina 2 di 9
3 esprimono il tipo di elementi costitutivi e il numero dei loro atomi legati nella molecola. In qualche caso si definisce la formula minima; ad esempio, la formula molecolare dell acqua ossigenata è H2O2 e la sua formula minima è HO, che rappresenta solo il rapporto in cui si trovano gli atomi che costituiscono la molecola. Gli elementi hanno molecole costituite da atomi uguali che molto spesso sono biatomiche: N2(azoto), O2 (ossigeno), Cl2 (cloro), ecc.; talvolta le molecole sono formate da un singolo atomo e sono dunque monoatomiche come, ad esempio, nel caso dei gas nobili: He (elio), Ne (neon), Ar (argo), Kr (kripto) e Rn (radon). I metalli vengono indicati, per convenzione, con il solo simbolo dell elemento: Fe (ferro), Ag (argento), Hg (mercurio), Zn (zinco), ecc. I composti hanno molecole costituite da almeno 2 elementi diversi e presentano proprietà differenti da quelle degli elementi costitutivi come, ad esempio, nell acqua e nell anidride carbonica. L acqua H2O, infatti, è un composto liquido incolore con caratteristiche ben note, del tutto diverse sia dall idrogeno H2 che dall ossigeno O2 di cui è costituita: gas infiammabile e combustibile il primo, classico comburente il secondo. L anidride carbonica CO2 è un gas prodotto dalle combustioni e quindi dalla respirazione, ben diverso dall ossigeno (caratteristico gas comburente) e dal carbonio (solido nero se è grafitico, come le mine delle matite, oppure solido splendente se sotto forma di diamante). In qualunque forma si presenti, tutta la materia è costituita di atomi. Gli atomi sono particelle piccolissime, il cui centro (nucleo) è costituito di nucleoni, precisamente di protoni (p, con carica positiva) e neutroni (n, privi di carica). Intorno al nucleo, distribuiti a distanze diverse, si muovono gli elettroni (e o e, con carica negativa), in numero uguale a quello dei protoni. Il nucleo è circa volte più piccolo dell intero atomo, perciò un atomo è costituito essenzialmente di spazi vuoti. Un protone e un elettrone hanno la stessa carica elettrica (1, C), positiva il primo, negativa il secondo. Dal momento che in un atomo il loro numero è uguale, l atomo risulta neutro. Il protone è stato scelto come unità elementare della carica elettrica positiva (+1) e viene indicato con il simbolo H+ in quanto corrisponde all atomo di idrogeno H contenente soltanto 1 protone privato del suo elettrone. Il modello atomico a orbitali è il modello più attuale che indaga sulla composizione dell atomo e, al contrario dei modelli precedenti, è un modello probabilistico. Prima di descriverlo, è opportuno però ricordare brevemente i concetti fondamentali del modello atomico di Bohr, in parte superati, ma in parte accettati nel modello ad orbitali. Secondo Bohr: un elettrone si muove intorno al nucleo seguendo precise traiettorie, dette orbite, alle quali corrispondono Pagina 3 di 9
4 altrettanti stati energetici; al crescere del raggio dell orbita, cresce anche l energia dell elettrone; un elettrone che si trovi su una certa orbita, per esempio con energia E1, può passare su quella cui compete una maggiore energia (E2) soltanto se gli viene fornita la quantità di energia sufficiente, cioè E2 E1. Il passaggio inverso avviene con l emissione della stessa quantità di energia. In altre parole, un elettrone può assorbire o emettere energia soltanto attraverso quantità finite, dette quanti di energia. Questo è il principio della quantizzazione dell energia, che fa parte della teoria quantistica dell energia, e rappresentò un caposaldo del modello atomico di Bohr. La conoscenza dei legami e la loro disposizione nelle molecole è il presupposto indispensabile per comprendere le proprietà delle sostanze. La formazione dei legami avviene tra ioni (legame ionico) o tra atomi (legame covalente), comportando la loro stabilizzazione in strutture definite. Nei metalli, invece, la stabilizzazione avviene con modalità diverse e caratteristiche diverse. Il legame ionico è un attrazione di natura elettrostatica che si stabilisce tra ioni di carica opposta (cationi e anioni). Mentre i gas nobili (gruppo VIII) non hanno alcuna tendenza a formare cationi o anioni, e dunque non formano legami chimici, alcuni metalli e alcuni non metalli sono invece coinvolti in tali trasformazioni. Nelle molecole dei composti gli elettroni condivisi possono essere anche 8 (come accade per l atomo di carbonio); i legami possono essere semplici, doppi o tripli. Il concetto di legame covalente permette la comprensione dei termini molecola e formula di struttura. La molecola di un elemento, come O2, o di un composto, come H2O, è un aggregato di atomi tenuti insieme da legami covalenti. La formula di struttura riguarda soltanto una sostanza con legami covalenti ed è quella che viene rappresentata evidenziando i legami. Tale formula, oltre ad indicare il tipo di atomi e il rapporto in cui essi si trovano (come la formula molecolare o bruta), precisa il modo in cui gli atomi sono legati. Nei composti ionici non è possibile distinguere la singola molecola e non esiste una formula di struttura; la loro formula bruta esprime soltanto il rapporto tra il numero dei cationi e quello degli anioni, come se fosse una formula minima. I composti chimici quindi vengono espressi mediante vari tipi di formule. E di queste ne esistono di vario genere. La formula a cui siamo abituati è la formula bruta (o formula grezza) che evidenzia gli elementi chimici e il numero di atomi di ciascun elemento che costituiscono la specie chimica in questione come ad esempio la formula per il glucosio C6H12O6. Questa formula ci indica che la molecola del glucosio è formata da carbonio, idrogeno e ossigeno e in particolare quanti atomi di ciascun elemento. Questo tipo di formula però non ci fornisce alcuna informazione sulla connettività degli atomi, ovvero sul Pagina 4 di 9
5 modo in ci questi sono legati fra loro. A questo scopo sono state introdotte le formule di struttura (o formule di costituzione), grazie alle quali è possibile conoscere come gli atomi sono legati fra loro. La formula del glucosio diventa quindi A differenza della formula bruta la formula di struttura ci dà informazioni sulla connettività degli atomi, ovvero su come gli atomi sono legato fra loro. È importante far notare che ad una formula bruta possono essere associate più formule di struttura perché una molecola può avere gli stessi elementi di un altra ma averli disposti in modo diverso. La formula di struttura di alcune molecole è talmente complessa e lunga da scrivere che si usa per convenzione un sistema per risparmiare tempo in scrittura. Questo sistema prevede l omissione degli atomi di carbonio (C) che vengono rappresentati come intersezioni fra trattini. Anche gli atomi di idrogeno H, legati agli atomi di carbonio, non vengono indicati e non viene neppure riportato il trattino che rappresenta il loro legame. A volte gli atomi carbonio delle terminazioni di una coda vengono espressi come CH3 invece di lasciare il trattino e basta. Pagina 5 di 9
6 Gli atomi su cui si usa la convenzione sono solo carbonio C e idrogeno H legato al carbonio. Tutti gli altri elementi vengono rappresentati con i loro legami al completo. Durante la lettura di una formula di questo tipo può essere utile avere una tabella con in numero di legami che ogni elemento può fare. Quindi, tradotto in formula, quante trattini ogni elemento può avere intorno. Carbonio (C) 4 Azoto (N) 3 Idrogeno (H) 1 Ossigeno (O) 2 Boro (B) 3 Fluoro (F) 1 Fosforo (P) 5 Zolfo (S) 2 Un miscuglio è un insieme di più sostanze, elementi e composti, e può essere sia eterogeneo che omogeneo. È, ad esempio, un miscuglio eterogeneo la sabbia, nella quale i vari componenti (tra cui il quarzo, i feldspati e le miche) sono distinguibili e il rapporto numerico tra le loro masse è del tutto variabile. Le proprietà di un tale miscuglio sono date dalla somma delle proprietà dei singoli componenti. In un miscuglio eterogeneo ciascun componente costituisce una fase, che può essere Pagina 6 di 9
7 definita come l insieme delle parti di un sistema che hanno le medesime proprietà; quindi un miscuglio eterogeneo è un sistema polifasico. Le sospensioni temporanee rappresentano un altro esempio di miscuglio eterogeneo. Si formano, ad esempio, aggiungendo all acqua particelle di argilla finemente suddivise; queste formano una sospensione, che è però temporanea in quanto le particelle dopo un po si raccolgono sul fondo del contenitore e possono essere filtrate. Un miscuglio omogeneo o soluzione è, invece, costituito da componenti che non sono distinguibili e pertanto è un sistema monofasico, come una sostanza pura, anche se è costituito da più sostanze. In natura esistono soluzioni liquide (acqua del rubinetto, benzina, acqua minerale, ecc.), solide (leghe metalliche, come oro, ottone e bronzo), gassose (aria e una qualsiasi miscela di gas). La limpidezza (o trasparenza) è una caratteristica delle soluzioni liquide in quanto ne esprime l omogeneità, indipendentemente dal loro colore, che può variare. In una soluzione si distinguono il solvente e il soluto (anche più soluti). Se un componente è un liquido (spesso è acqua) e l altro è un gas o un solido, il liquido viene definito solvente e l altro componente è il soluto. Negli altri casi il solvente è il componente che è presente nella soluzione in maggiore quantità. Le proprietà di una soluzione dipendono dalla sua composizione, cioè dal rapporto tra la quantità del soluto e quella del solvente, oltre che naturalmente dalla loro natura. Ad esempio, una gradazione alcolica di una birra pari al 6-7% è ben diversa da una gradazione del 40% di un whisky! La concentrazione di una soluzione esprime la quantità di soluto presente in una determinata quantità di soluzione (talvolta di solvente). La composizione di una soluzione non è variabile in maniera illimitata come quella di un miscuglio eterogeneo, fatta eccezione per le soluzioni gassose, in quanto i gas sono miscibili in tutte le proporzioni. Infatti, una sostanza A si scioglie in un dato solvente S solo fino ad un certo punto, formando una soluzione satura; questa cioè contiene la massima quantità di soluto che il solvente è in grado di sciogliere a una determinata temperatura e ha la massima concentrazione possibile. Infatti, aggiungendo ancora A, se A è un solido, la parte eccedente precipita sotto forma di corpo di fondo e il sistema, inizialmente monofasico, diventa bifasico. Nel caso in cui una soluzione contenga una quantità di soluto inferiore a quella massima che il solvente è in grado di sciogliere a una data temperatura, viene detta soluzione insatura. Una caratteristica che comunemente viene usata per distinguere le soluzioni può essere l acidità o la basicità. gli acidi sono sostanze che in acqua producono protoni H + (aq); le basi sono sostanze che in acqua producono ioni idrossido OH (aq). Per indicare il carattere acido, basico o neutro di una soluzione si utilizza una grandezza detta ph, Pagina 7 di 9
8 che è il logaritmo negativo, in base 10, della concentrazione molare dello ione H3O+ (aq) Il ph è una grandezza adoperata per valutare l acidità, la neutralità e la basicità di una soluzione. Il ph di una soluzione neutra è 7. Il ph assume valori tanto più bassi rispetto a 7 quanto maggiore è l acidità della soluzione. Il ph assume valori tanto più alti rispetto a 7 quanto maggiore è la basicità della soluzione. Pagina 8 di 9
9 Operazione: URAGANO ROSSO Data: Settembre 2019 Pagina 9 di 9
Elementi e composti Pesi atomici e pesi molecolari Mole e massa molare
 Elementi e composti Pesi atomici e pesi molecolari Mole e massa molare 2 a lezione 17 ottobre 2016 Elementi ed atomi Una sostanza viene definita «elemento» quando non è scomponibile in altre sostanze Un
Elementi e composti Pesi atomici e pesi molecolari Mole e massa molare 2 a lezione 17 ottobre 2016 Elementi ed atomi Una sostanza viene definita «elemento» quando non è scomponibile in altre sostanze Un
FONDAMENTI DI CHIMICA
 FONDAMENTI DI CHIMICA LA CHIMICA E UNA BRANCA DELLA SCIENZA CHE STUDIA LA COMPOSIZIONE DELLA MATERIA E DELLE SOSTANZE, LE LORO PROPRIETA E LE LORO TRASFORMAZIONI IN ALTRE SOSTANZE ED ELEMENTI E/O IN ENERGIA
FONDAMENTI DI CHIMICA LA CHIMICA E UNA BRANCA DELLA SCIENZA CHE STUDIA LA COMPOSIZIONE DELLA MATERIA E DELLE SOSTANZE, LE LORO PROPRIETA E LE LORO TRASFORMAZIONI IN ALTRE SOSTANZE ED ELEMENTI E/O IN ENERGIA
LA STRUTTURA DELLA MATERIA
 LA STRUTTURA DELLA MATERIA La materia è tutto ciò che ci circonda, che occupa uno spazio e ha una massa La materia si presenta sotto diverse forme, dette sostanze. Sono sostanze: il vetro, il legno, il
LA STRUTTURA DELLA MATERIA La materia è tutto ciò che ci circonda, che occupa uno spazio e ha una massa La materia si presenta sotto diverse forme, dette sostanze. Sono sostanze: il vetro, il legno, il
satura SOLUZIONE concentrata diluita MISCUGLIO ETEROGENEO Sospensione (acqua e polvere di marmo) Miscuglio solido (es. sabbia)
 MISCUGLIO ETEROGENEO: è un insieme di due o più sostanze che, pur essendo mescolate tra loro conservano ciascuna le proprie caratteristiche fisiche e chimiche. MISCUGLIO ETEROGENEO Miscuglio solido (es.
MISCUGLIO ETEROGENEO: è un insieme di due o più sostanze che, pur essendo mescolate tra loro conservano ciascuna le proprie caratteristiche fisiche e chimiche. MISCUGLIO ETEROGENEO Miscuglio solido (es.
Chimica. La scienza che studia le trasformazioni della materia. Acqua (ghiaccio) Acqua (Liquido) Trasformazione Fisica
 Nozioni di Base Chimica La scienza che studia le trasformazioni della materia Acqua (ghiaccio) ----- Acqua (Liquido) Trasformazione Fisica Metano + Ossigeno -- Anidride Carbonica + Acqua Trasformazione
Nozioni di Base Chimica La scienza che studia le trasformazioni della materia Acqua (ghiaccio) ----- Acqua (Liquido) Trasformazione Fisica Metano + Ossigeno -- Anidride Carbonica + Acqua Trasformazione
Corso di CHIMICA LEZIONE 1
 Corso di CHIMICA LEZIONE 1 MATERIA tutto ciò occupa spazio e ha massa si presenta in natura sottoforma di Miscugli: sostanze mescolate insieme in vario modo (rocce, acqua marina, aria, cellule) Sostanze
Corso di CHIMICA LEZIONE 1 MATERIA tutto ciò occupa spazio e ha massa si presenta in natura sottoforma di Miscugli: sostanze mescolate insieme in vario modo (rocce, acqua marina, aria, cellule) Sostanze
*Gli atomi sono tutti uguali tra loro?
 *Gli atomi sono tutti uguali tra loro? *Pur essendo tutti formati dalle stesse particelle, gli atomi non sono tutti uguali tra loro: alcuni sono più piccoli, altri più grandi. La piccolezza o la grandezza
*Gli atomi sono tutti uguali tra loro? *Pur essendo tutti formati dalle stesse particelle, gli atomi non sono tutti uguali tra loro: alcuni sono più piccoli, altri più grandi. La piccolezza o la grandezza
LA TEORIA ATOMICA E L ATOMO Da pagina 81 a pagina 107
 LA TEORIA ATOMICA E L ATOMO Da pagina 81 a pagina 107 4.1 LA TEORIA ATOMICA La materia è formata da atomi, a loro volta costituiti da particelle subatomiche; Esistono tanti tipi di atomi quanti sono gli
LA TEORIA ATOMICA E L ATOMO Da pagina 81 a pagina 107 4.1 LA TEORIA ATOMICA La materia è formata da atomi, a loro volta costituiti da particelle subatomiche; Esistono tanti tipi di atomi quanti sono gli
STRUTTURA DELLA MATERIA. Prof.ssa PATRIZIA GALLUCCI
 STRUTTURA DELLA MATERIA Prof.ssa PATRIZIA GALLUCCI MATERIA Il chimico studia sia l aspetto macroscopico che l aspetto microscopico della materia La MATERIA è tutto ciò che ci circonda, ha una massa ed
STRUTTURA DELLA MATERIA Prof.ssa PATRIZIA GALLUCCI MATERIA Il chimico studia sia l aspetto macroscopico che l aspetto microscopico della materia La MATERIA è tutto ciò che ci circonda, ha una massa ed
2 HCl. H 2 + Cl 2 ATOMI E MOLECOLE. Ipotesi di Dalton
 Ipotesi di Dalton ATOMI E MOLECOLE 1.! Un elemento è formato da particelle indivisibili chiamate atomi. 2.! Gli atomi di uno specifico elemento hanno proprietà identiche. 3.! Gli atomi si combinano secondo
Ipotesi di Dalton ATOMI E MOLECOLE 1.! Un elemento è formato da particelle indivisibili chiamate atomi. 2.! Gli atomi di uno specifico elemento hanno proprietà identiche. 3.! Gli atomi si combinano secondo
Le sostanze chimiche
 Le sostanze chimiche Ingredienti base della materia La materia si presenta con diverse forme. Accade perché esistono moltissimi «ingredienti di base» che mescolandosi tra loro danno innumerevoli combinazioni.
Le sostanze chimiche Ingredienti base della materia La materia si presenta con diverse forme. Accade perché esistono moltissimi «ingredienti di base» che mescolandosi tra loro danno innumerevoli combinazioni.
Cos è un trasformazione chimica?
 Chimica Lezione 1 Cos è un trasformazione chimica? Una reazione chimica è una trasformazione della materia che avviene senza variazioni misurabili di massa, in cui uno o più reagenti iniziali modificano
Chimica Lezione 1 Cos è un trasformazione chimica? Una reazione chimica è una trasformazione della materia che avviene senza variazioni misurabili di massa, in cui uno o più reagenti iniziali modificano
con la sostanza di partenza (fig. 6). Fig. 1 Fig. 2 Fig. 3 Fig. 4 Fig. 5 Fig. 6 Fig. 7
 Cap. 6 Dentro la materia saperi essenziali 6.1 Le caratteristiche della materia La materia è tutto ciò che ha una massa e occupa un volume 6.2 La teoria atomica della materia Se immaginiamo di spezzare
Cap. 6 Dentro la materia saperi essenziali 6.1 Le caratteristiche della materia La materia è tutto ciò che ha una massa e occupa un volume 6.2 La teoria atomica della materia Se immaginiamo di spezzare
CHIMICA E BIOCHIMICA
 CHIMICA E BIOCHIMICA CHIMICA: studia la materia Materia= ogni cosa che ha massa Proprietà Struttura Trasformazioni (Reazioni) BIOCHIMICA: studia la chimica degli organismi viventi Di cosa è composta la
CHIMICA E BIOCHIMICA CHIMICA: studia la materia Materia= ogni cosa che ha massa Proprietà Struttura Trasformazioni (Reazioni) BIOCHIMICA: studia la chimica degli organismi viventi Di cosa è composta la
Le sostanze chimiche prof. Matteo Scapellato
 1. Fenomeni fisici e fenomeni chimici a) Fenomeno fisico: è una trasformazione che non cambia la natura delle sostanze 1 b) Fenomeno chimico o reazione chimica: è una trasformazione che cambia la natura
1. Fenomeni fisici e fenomeni chimici a) Fenomeno fisico: è una trasformazione che non cambia la natura delle sostanze 1 b) Fenomeno chimico o reazione chimica: è una trasformazione che cambia la natura
Lezione 2. Leggi ponderali
 Lezione 2 Leggi ponderali I miscugli eterogenei presentano i componenti distinguibili in due o più fasi, in rapporti di massa altamente variabili e che mantengono le caratteristiche originarie. I miscugli
Lezione 2 Leggi ponderali I miscugli eterogenei presentano i componenti distinguibili in due o più fasi, in rapporti di massa altamente variabili e che mantengono le caratteristiche originarie. I miscugli
L Atomo Nucleare. Rutherford protoni James Chadwick neutroni 1932
 Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
ATOMI E MOLECOLE. Tutte le varie forme di materia esistenti sono costituite da sostanze semplici (elementi) e da sostanze composte (composti).
 1 ATOMI E MOLECOLE Tutte le varie forme di materia esistenti sono costituite da sostanze semplici (elementi) e da sostanze composte (composti). Un elemento (es. il mercurio) è una sostanza che non può
1 ATOMI E MOLECOLE Tutte le varie forme di materia esistenti sono costituite da sostanze semplici (elementi) e da sostanze composte (composti). Un elemento (es. il mercurio) è una sostanza che non può
PERCORSI ABILITANTI SPECIALI CLASSE A033 TEST FINALE DEL CORSO DI CHIMICA
 PERCORSI ABILITANTI SPECIALI 2014 - CLASSE A033 TEST FINALE DEL CORSO DI CHIMICA Cognome Nome Numero progressivo sul registro 1. Viene disciolto zucchero in un certo volume di acqua pura fino a che si
PERCORSI ABILITANTI SPECIALI 2014 - CLASSE A033 TEST FINALE DEL CORSO DI CHIMICA Cognome Nome Numero progressivo sul registro 1. Viene disciolto zucchero in un certo volume di acqua pura fino a che si
I LEGAMI CHIMICI. Configurazione elettronica stabile: è quella in cui tutti i livelli energetici dell atomo sono pieni di elettroni
 I LEGAMI CIMICI In natura sono pochi gli elementi che presentano atomi allo stato libero. Gli unici elementi che sono costituiti da atomi isolati si chiamano gas nobili o inerti, formano il gruppo VIII
I LEGAMI CIMICI In natura sono pochi gli elementi che presentano atomi allo stato libero. Gli unici elementi che sono costituiti da atomi isolati si chiamano gas nobili o inerti, formano il gruppo VIII
Chimica: Studio della materia e delle sue interazioni.
 Chimica: Studio della materia e delle sue interazioni. La descrizione della materia viene affrontata da: punto di vista microscopico: studio di atomi e molecole le loro interazioni e le reazioni chimiche
Chimica: Studio della materia e delle sue interazioni. La descrizione della materia viene affrontata da: punto di vista microscopico: studio di atomi e molecole le loro interazioni e le reazioni chimiche
Corso di Studi in Scienze Naturali Corso di Chimica Generale e Inorganica Dott.ssa Maria Cristina Paganini Prof. Elio Giamello
 Corso di Studi in Scienze Naturali Corso di Chimica Generale e Inorganica Dott.ssa Maria Cristina Paganini Prof. Elio Giamello Avvertenza: Le immagini seguenti, proiettate durante le lezioni sono tratte
Corso di Studi in Scienze Naturali Corso di Chimica Generale e Inorganica Dott.ssa Maria Cristina Paganini Prof. Elio Giamello Avvertenza: Le immagini seguenti, proiettate durante le lezioni sono tratte
L'atomo è la parte più piccola della materia che ne conserva tutte le caratteristiche. Esso è formato da particelle più piccole:
 L'atomo è la parte più piccola della materia che ne conserva tutte le caratteristiche. Esso è formato da particelle più piccole: PROTONI NEUTRONI ELETTRONI I protoni e i neutroni si trovano nella parte
L'atomo è la parte più piccola della materia che ne conserva tutte le caratteristiche. Esso è formato da particelle più piccole: PROTONI NEUTRONI ELETTRONI I protoni e i neutroni si trovano nella parte
Chimica. Lezione 1 La materia
 Chimica Lezione 1 La materia Materia Tutte le sostanze che costituiscono l universo Infinita varietà di forme Classificazione a seconda dello stato FISICO (solido, liquido, gassoso) o della COMPOSIZIONE
Chimica Lezione 1 La materia Materia Tutte le sostanze che costituiscono l universo Infinita varietà di forme Classificazione a seconda dello stato FISICO (solido, liquido, gassoso) o della COMPOSIZIONE
Scienziati in Erba Chimica
 Scienziati in Erba Chimica Acqua Oro Zucchero La Chimica ü ü ü ü ü ü ü ü ü ü Cosa studia la chimica? Classificazione della materia Stati della materia Formule chimiche Atomo Tavola periodica degli elementi
Scienziati in Erba Chimica Acqua Oro Zucchero La Chimica ü ü ü ü ü ü ü ü ü ü Cosa studia la chimica? Classificazione della materia Stati della materia Formule chimiche Atomo Tavola periodica degli elementi
VERIFICA FINALE ISTITUTO D ISTRUZIONE SUPERIORE VIRGILIO. Scienziati in erba. Durata della prova: 100 minuti
 VERIFICA FINALE Nome Cognome Classe Sez ISTITUTO D ISTRUZIONE SUPERIORE VIRGILIO SAN GIORGIO DEL SANNIO (BN) Scienziati in erba La prova deve essere consegnata allo scadere del tempo previsto per la sua
VERIFICA FINALE Nome Cognome Classe Sez ISTITUTO D ISTRUZIONE SUPERIORE VIRGILIO SAN GIORGIO DEL SANNIO (BN) Scienziati in erba La prova deve essere consegnata allo scadere del tempo previsto per la sua
Fenomeno fisico. Le trasformazioni che la materia subisce senza modificare la sua composizione e che sono reversibili si chiamano fenomeni fisici
 Atomi e molecole Fenomeno fisico Le trasformazioni che la materia subisce senza modificare la sua composizione e che sono reversibili si chiamano fenomeni fisici Fenomeno chimico Le trasformazioni che
Atomi e molecole Fenomeno fisico Le trasformazioni che la materia subisce senza modificare la sua composizione e che sono reversibili si chiamano fenomeni fisici Fenomeno chimico Le trasformazioni che
VERIFICA Dalla tavola periodica al modello atomico
 VERIFICA Dalla tavola periodica al modello atomico Cognome Nome Classe Data I/1 Vero o Falso? Scegli per ciascuna risposta l'alternativa corretta V F Nella tavola periodica ogni elemento è contrassegnato
VERIFICA Dalla tavola periodica al modello atomico Cognome Nome Classe Data I/1 Vero o Falso? Scegli per ciascuna risposta l'alternativa corretta V F Nella tavola periodica ogni elemento è contrassegnato
A_Test di valutazione di CHIMICA:
 COGNOME NOME... C.I./Patente n... MATRICOLA NO SI, n:... Prova di accertamento per la determinazione di eventuali debiti formativi A_Test di valutazione di CHIMICA: Cosa studia in generale la chimica A)
COGNOME NOME... C.I./Patente n... MATRICOLA NO SI, n:... Prova di accertamento per la determinazione di eventuali debiti formativi A_Test di valutazione di CHIMICA: Cosa studia in generale la chimica A)
Classificazione della materia 3 STATI DI AGGREGAZIONE
 Classificazione della materia MATERIA spazio massa Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (Volume e forma propri) LIQUIDO (Volume definito e forma indefinita) GASSOSO
Classificazione della materia MATERIA spazio massa Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (Volume e forma propri) LIQUIDO (Volume definito e forma indefinita) GASSOSO
Gli atomi e gli elementi. Enrico Degiuli Classe seconda
 Gli atomi e gli elementi Enrico Degiuli Classe seconda Gli atomi Fin dall antichità i filosofi si sono chiesti se la materia si può dividere in parti sempre più piccole (Aristotele) o se invece esistono
Gli atomi e gli elementi Enrico Degiuli Classe seconda Gli atomi Fin dall antichità i filosofi si sono chiesti se la materia si può dividere in parti sempre più piccole (Aristotele) o se invece esistono
Amministrazione, finanza e marketing - Turismo Ministero dell Istruzione, dell Università e della Ricerca PROGRAMMAZIONE DISCIPLINARE PER U. di A.
 MATERIA CHIMICA CLASSE 2 INDIRIZZO AFM / TUR DESCRIZIONE Unità di Apprendimento UdA n. 1 Titolo: LA MATERIA Aver acquisito la capacità di osservare, descrivere ed analizzare i fenomeni legati alle trasformazioni
MATERIA CHIMICA CLASSE 2 INDIRIZZO AFM / TUR DESCRIZIONE Unità di Apprendimento UdA n. 1 Titolo: LA MATERIA Aver acquisito la capacità di osservare, descrivere ed analizzare i fenomeni legati alle trasformazioni
Corso di CHIMICA INORGANICA
 Corso di CHIMICA INORGANICA Lezione Seconda La teoria atomica La massa atomica e il concetto di Isotopi Dentro l atomo, le particelle subatomiche La Tavola Periodica degli Elementi 2 Gli atomi di un certo
Corso di CHIMICA INORGANICA Lezione Seconda La teoria atomica La massa atomica e il concetto di Isotopi Dentro l atomo, le particelle subatomiche La Tavola Periodica degli Elementi 2 Gli atomi di un certo
Elementi di Chimica. Lezione 03
 Elementi di Chimica Lezione 03 Elementi atomi e molecole Come si è detto tutta la materia esistente in natura è costituita da 92 elementi. Tuttavia ben pochi di questi elementi si trovano in natura sotto
Elementi di Chimica Lezione 03 Elementi atomi e molecole Come si è detto tutta la materia esistente in natura è costituita da 92 elementi. Tuttavia ben pochi di questi elementi si trovano in natura sotto
Molecole e legami. Chimica generale
 Molecole e legami Chimica generale Atomi e molecole È estremamente difficile trovare in natura una sostanza formata solamente da atomi semplici Solo i gas inerti dell ottavo gruppo sono presenti in natura
Molecole e legami Chimica generale Atomi e molecole È estremamente difficile trovare in natura una sostanza formata solamente da atomi semplici Solo i gas inerti dell ottavo gruppo sono presenti in natura
Zolfo (Z = 16) Conf. Elettronica 1s 2 2s 2 2p 6 3s 2 3p 4 Conf. Elettronica esterna 3s 2 3p 4
 TAVOLA PERIODICA DEGLI ELEMENTI Gli elementi sono ordinati nella tavola periodica secondo numero atomico crescente ed in base alle loro proprietà chimico-fisiche che seguono un andamento periodico. Gli
TAVOLA PERIODICA DEGLI ELEMENTI Gli elementi sono ordinati nella tavola periodica secondo numero atomico crescente ed in base alle loro proprietà chimico-fisiche che seguono un andamento periodico. Gli
CHIMICA: studio della struttura e delle trasformazioni della materia
 CHIMICA: studio della struttura e delle trasformazioni della materia 1 Materia (materali) Sostanze (omogenee) Processo fisico Miscele Elementi (atomi) Reazioni chimiche Composti (molecole) Miscele omogenee
CHIMICA: studio della struttura e delle trasformazioni della materia 1 Materia (materali) Sostanze (omogenee) Processo fisico Miscele Elementi (atomi) Reazioni chimiche Composti (molecole) Miscele omogenee
Corso di studi in CHIMICA Corso di Chimica Generale e Inorganica Prof. E. Giamello
 Corso di studi in CHIMICA Corso di Chimica Generale e Inorganica 2009-2010 Prof. E. Giamello Avvertenza Le immagini seguenti sono proiettate durante le lezioni. Esse sono tratte dai seguenti testi: Whitten
Corso di studi in CHIMICA Corso di Chimica Generale e Inorganica 2009-2010 Prof. E. Giamello Avvertenza Le immagini seguenti sono proiettate durante le lezioni. Esse sono tratte dai seguenti testi: Whitten
COMPETENZE ABILITÀ CONOSCENZE. descrivere la. Comprendere ed applicare analogie relative ai concetti presi in analisi. struttura.
 ca descrivere la struttura dell atomo, la tavola periodica e le sue caratteristiche per spiegare le differenze tra i vari tipi di legami, descrivendoli e interpretandoli alla luce degli elettroni di valenza
ca descrivere la struttura dell atomo, la tavola periodica e le sue caratteristiche per spiegare le differenze tra i vari tipi di legami, descrivendoli e interpretandoli alla luce degli elettroni di valenza
Bagatti, Corradi, Desco, Ropa. Chimica. seconda edizione
 Bagatti, Corradi, Desco, Ropa Chimica seconda edizione Bagatti, Corradi, Desco, Ropa, Chimica seconda edizione Capitolo 6. I legami chimici SEGUI LA MAPPA riconoscere valutare dativo puro 1 Gli atomi difficilmente
Bagatti, Corradi, Desco, Ropa Chimica seconda edizione Bagatti, Corradi, Desco, Ropa, Chimica seconda edizione Capitolo 6. I legami chimici SEGUI LA MAPPA riconoscere valutare dativo puro 1 Gli atomi difficilmente
Le Reazioni Chimiche
 Le Reazioni Chimiche Quando gli atomi si uniscono: La Molecola Gli atomi hanno la capacità di unirsi tra loro formando le MOLECOLE. Le Formule Chimiche Per indicare le molecole si usano le FORMULE CHIMICHE
Le Reazioni Chimiche Quando gli atomi si uniscono: La Molecola Gli atomi hanno la capacità di unirsi tra loro formando le MOLECOLE. Le Formule Chimiche Per indicare le molecole si usano le FORMULE CHIMICHE
Esempi di SISTEMI ETEROGENEI. latte Acqua + olio Acqua + sabbia
 MATERIA MISCUGLIO SOSTANZA PURA MISCUGLIO OMOGENEO MISCUGLIO ETEROGENEO COMPOSTO ELEMENTO Elemento: una sostanza pura che non può essere scomposta in sostanze più semplici. Composto: una sostanza pura
MATERIA MISCUGLIO SOSTANZA PURA MISCUGLIO OMOGENEO MISCUGLIO ETEROGENEO COMPOSTO ELEMENTO Elemento: una sostanza pura che non può essere scomposta in sostanze più semplici. Composto: una sostanza pura
La chimica studia la materia e i cambiamenti ai quali essa va soggetta. La materia è tutto ciò che possiede massa e occupa spazio.
 La chimica studia la materia e i cambiamenti ai quali essa va soggetta. La materia è tutto ciò che possiede massa e occupa spazio. Tutto ciò che potete toccare è materia, e materia sono moltissime cose
La chimica studia la materia e i cambiamenti ai quali essa va soggetta. La materia è tutto ciò che possiede massa e occupa spazio. Tutto ciò che potete toccare è materia, e materia sono moltissime cose
combinazione di atomi tenuti insieme da forze più o meno un insieme caratteristico di proprietà
 IL LEGAME CHIMICO La regola dell ottetto sebbene una semplificazione rende conto del perchè gli atomi reagiscono. In natura, solo i gas nobili sono presenti come specie monoatomiche. Anche le sostanze
IL LEGAME CHIMICO La regola dell ottetto sebbene una semplificazione rende conto del perchè gli atomi reagiscono. In natura, solo i gas nobili sono presenti come specie monoatomiche. Anche le sostanze
Un nuclide è un atomo caratterizzato dal numero atomico Z (numero di protoni) e dal numero di massa A (numero di neutroni e di protoni).
 L atomo Il nucleo è costituito da neutroni e protoni (nucleoni). Il neutrone non ha carica e la sua massa è,675 0-27 Kg. Il protone ha una carica positiva di,6022 0-9 C e una massa di,673 0-27 Kg. L'elettrone
L atomo Il nucleo è costituito da neutroni e protoni (nucleoni). Il neutrone non ha carica e la sua massa è,675 0-27 Kg. Il protone ha una carica positiva di,6022 0-9 C e una massa di,673 0-27 Kg. L'elettrone
COMPITI PER IL RIPASSO ESTIVO SCIENZE DELLA TERRA CLASSI PRIME
 COMPITI PER IL RIPASSO ESTIVO SCIENZE DELLA TERRA CLASSI PRIME Con l aiuto degli appunti di lezione, di internet, e del libro di testo ( che puoi richiedere in segreteria) rispondi nella maniera più completa
COMPITI PER IL RIPASSO ESTIVO SCIENZE DELLA TERRA CLASSI PRIME Con l aiuto degli appunti di lezione, di internet, e del libro di testo ( che puoi richiedere in segreteria) rispondi nella maniera più completa
Gli argomenti trattati
 LEZIONE 1 Struttura della materia e Gli argomenti trattati Composizione della materia materia, sostanze e miscele, elementi e composti Fondamenti di struttura atomica Molecole: formula empirica, formula
LEZIONE 1 Struttura della materia e Gli argomenti trattati Composizione della materia materia, sostanze e miscele, elementi e composti Fondamenti di struttura atomica Molecole: formula empirica, formula
L Atomo e le Molecole
 L Atomo e le Molecole L atomo L'atomo, la particella che come un mattone costituisce tutta la materia, non è un corpicciolo semplice. Esso è a sua volta composto da particelle elementari piccolissime:
L Atomo e le Molecole L atomo L'atomo, la particella che come un mattone costituisce tutta la materia, non è un corpicciolo semplice. Esso è a sua volta composto da particelle elementari piccolissime:
COMPITI PER IL RIPASSO ESTIVO SCIENZE DELLA TERRA CLASSI PRIME. (per alunni ammessi alla classe 2 )
 COMPITI PER IL RIPASSO ESTIVO SCIENZE DELLA TERRA CLASSI PRIME (per alunni ammessi alla classe 2 ) Con l aiuto degli appunti di lezione, di internet, e del libro di testo ( che puoi richiedere in segreteria)
COMPITI PER IL RIPASSO ESTIVO SCIENZE DELLA TERRA CLASSI PRIME (per alunni ammessi alla classe 2 ) Con l aiuto degli appunti di lezione, di internet, e del libro di testo ( che puoi richiedere in segreteria)
Gruppo costituito da elementi con uguale configurazione elettronica esterna.
 SISTEMA PERIODICO Ciascun elemento è caratterizzato dal n atomico Z, che esprime il n di cariche positive (protoni), presenti nel nucleo dell'atomo. La tabella periodica si articola in gruppi e periodi
SISTEMA PERIODICO Ciascun elemento è caratterizzato dal n atomico Z, che esprime il n di cariche positive (protoni), presenti nel nucleo dell'atomo. La tabella periodica si articola in gruppi e periodi
OVERVIEW. Teoria atomica e tavola periodica. Legami e interazioni degli atomi
 OVERVIEW Teoria atomica e tavola periodica Legami e interazioni degli atomi Acqua e le sue proprietà Acidi e basi Atomo: più piccola porzione di un elemento che mantiene le proprietà chimiche dello stesso
OVERVIEW Teoria atomica e tavola periodica Legami e interazioni degli atomi Acqua e le sue proprietà Acidi e basi Atomo: più piccola porzione di un elemento che mantiene le proprietà chimiche dello stesso
Un elemento è una sostanza pura che non può essere divisa in sostanze più semplici. Le sue molecole sono tutte uguali.
 Elementi, composti, miscugli Un elemento è una sostanza pura che non può essere divisa in sostanze più semplici. Le sue molecole sono tutte uguali. Il composto è formato da sostanze pure scomponibili in
Elementi, composti, miscugli Un elemento è una sostanza pura che non può essere divisa in sostanze più semplici. Le sue molecole sono tutte uguali. Il composto è formato da sostanze pure scomponibili in
Corso di CHIMICA LEZIONE 3
 Corso di CHIMICA LEZIONE 3 1 2 3 4 5 6 7 H Li Na K Fr Be Ma g Ca Ba TAVOLA PERIODICA He I II s 1 s 2 III IV V VI VII VIII p 1 p 2 p 3 p 4 p 5 p 6 blocco s La Ac 6 7 d 1 d 2 d 3 d 4 d 5 d 6 d 7 d 8 d 9
Corso di CHIMICA LEZIONE 3 1 2 3 4 5 6 7 H Li Na K Fr Be Ma g Ca Ba TAVOLA PERIODICA He I II s 1 s 2 III IV V VI VII VIII p 1 p 2 p 3 p 4 p 5 p 6 blocco s La Ac 6 7 d 1 d 2 d 3 d 4 d 5 d 6 d 7 d 8 d 9
(98,9x12) + (1,1x13) = 12,01 100
 5 GLI ISOTOPI Le proprietà di un elemento non dipendono dal numero di massa, ma dal numero atomico; infatti è sufficiente il numero dei protoni a caratterizzare un atomo, in quanto esso condiziona un uguale
5 GLI ISOTOPI Le proprietà di un elemento non dipendono dal numero di massa, ma dal numero atomico; infatti è sufficiente il numero dei protoni a caratterizzare un atomo, in quanto esso condiziona un uguale
Elementi sistemati nella TAVOLA PERIODICA DEGLI ELEMENTI in base al numero atomico crescente O, H, N, C (+ del 96% della materia vivente)
 OVERVIEW Atomo: più piccola porzione di un elemento che mantiene le proprietà chimiche dello stesso Teoria atomica e tavola periodica Legami e interazioni degli atomi Acqua e le sue proprietà Acidi e basi
OVERVIEW Atomo: più piccola porzione di un elemento che mantiene le proprietà chimiche dello stesso Teoria atomica e tavola periodica Legami e interazioni degli atomi Acqua e le sue proprietà Acidi e basi
L Atomo e le Molecole
 L Atomo e le Molecole La materia Tutti i corpi che ci circondano, (rocce, aria, nubi, sabbia, ) sono fatti di materia. Materia è tutto ciò che occupa uno spazio, cioè ha un volume, e ha una massa, quindi
L Atomo e le Molecole La materia Tutti i corpi che ci circondano, (rocce, aria, nubi, sabbia, ) sono fatti di materia. Materia è tutto ciò che occupa uno spazio, cioè ha un volume, e ha una massa, quindi
L Atomo e le Molecole
 L Atomo e le Molecole L atomo L'atomo, la particella che come un mattone costituisce tutta la materia, non è un corpicciolo semplice. Esso è a sua volta composto da particelle elementari piccolissime:
L Atomo e le Molecole L atomo L'atomo, la particella che come un mattone costituisce tutta la materia, non è un corpicciolo semplice. Esso è a sua volta composto da particelle elementari piccolissime:
Corso di laurea in Chimica e Tecnologia Farmaceutiche Corso di Chimica Generale e Inorganica CH 3
 Corso di laurea in Chimica e Tecnologia Farmaceutiche Corso di Chimica Generale e Inorganica - LA MATERIA- COOH O O Al(OH) 4 - CH 3 Prof.ssa Ivana Fenoglio I lucidi forniti non sono da utilizzare come
Corso di laurea in Chimica e Tecnologia Farmaceutiche Corso di Chimica Generale e Inorganica - LA MATERIA- COOH O O Al(OH) 4 - CH 3 Prof.ssa Ivana Fenoglio I lucidi forniti non sono da utilizzare come
COMPITI PER IL RIPASSO ESTIVO SCIENZE DELLA TERRA CLASSI PRIME
 COMPITI PER IL RIPASSO ESTIVO SCIENZE DELLA TERRA CLASSI PRIME Con l aiuto degli appunti di lezione, di internet, e del libro di testo ( che puoi richiedere in segreteria) rispondi nella maniera più completa
COMPITI PER IL RIPASSO ESTIVO SCIENZE DELLA TERRA CLASSI PRIME Con l aiuto degli appunti di lezione, di internet, e del libro di testo ( che puoi richiedere in segreteria) rispondi nella maniera più completa
La Vita è una Reazione Chimica
 La Vita è una Reazione Chimica Acqua Oro Zucchero La vita è una reazione chimica ü ü ü ü ü ü ü ü ü ü Cosa studia la chimica? Classificazione della materia Stati della materia Formule chimiche Atomo Tavola
La Vita è una Reazione Chimica Acqua Oro Zucchero La vita è una reazione chimica ü ü ü ü ü ü ü ü ü ü Cosa studia la chimica? Classificazione della materia Stati della materia Formule chimiche Atomo Tavola
Precorsi Test AMMISSIONE Medicina e Chirurgia - Professioni Sanitarie Università degli Studi di Perugia. Massa atomica MOLE. a.a.
 Precorsi Test AMMISSIONE Medicina e Chirurgia - Professioni Sanitarie Università degli Studi di Perugia Massa atomica MOLE a.a. 2016-17 MATERIA costituita da ATOMI Miscele OMOGENEE o soluzioni Hanno la
Precorsi Test AMMISSIONE Medicina e Chirurgia - Professioni Sanitarie Università degli Studi di Perugia Massa atomica MOLE a.a. 2016-17 MATERIA costituita da ATOMI Miscele OMOGENEE o soluzioni Hanno la
Atomi, molecole e ioni
 Atomi, molecole e ioni anione + - catione Teoria atomica di Dalton 1. Un elemento è composto da particelle minuscole chiamate atomi. 2. In una normale reazione chimica, nessun atomo di nessun elemento
Atomi, molecole e ioni anione + - catione Teoria atomica di Dalton 1. Un elemento è composto da particelle minuscole chiamate atomi. 2. In una normale reazione chimica, nessun atomo di nessun elemento
Struttura dell'atomo a cura di Petr Ushakov
 Struttura dell'atomo a cura di Petr Ushakov Struttura dell'atomo Gli atomi di tutti gli elementi sono formati da tre tipi di particelle elementari: protone, neutrone e elettrone. particelle elementari
Struttura dell'atomo a cura di Petr Ushakov Struttura dell'atomo Gli atomi di tutti gli elementi sono formati da tre tipi di particelle elementari: protone, neutrone e elettrone. particelle elementari
 ELETTRONEGATIVITA CAPACITA DI UN ATOMO DI ATTIRARE UNA COPPIA DI ELETTRONI DI LEGAME DETERMINANDO COSI IL TIPO DI LEGAME CHE SI VIENE A FORMARE. DERIVA DA ALTRE DUE GRANDEZZE I. Energia di ionizzazione:
ELETTRONEGATIVITA CAPACITA DI UN ATOMO DI ATTIRARE UNA COPPIA DI ELETTRONI DI LEGAME DETERMINANDO COSI IL TIPO DI LEGAME CHE SI VIENE A FORMARE. DERIVA DA ALTRE DUE GRANDEZZE I. Energia di ionizzazione:
VERIFICA La struttura della materia: atomi e molecole
 ERIICA La struttura della materia: atomi e molecole Cognome Nome Classe Data I/1 ero o falso? La massa atomica indica quanti neutroni sono presenti nel nucleo La massa atomica indica la massa in grammi
ERIICA La struttura della materia: atomi e molecole Cognome Nome Classe Data I/1 ero o falso? La massa atomica indica quanti neutroni sono presenti nel nucleo La massa atomica indica la massa in grammi
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 4 Le teorie 1. L atomo e la sua storia 2. La nascita della moderna teoria atomica: da Lavoiser
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 4 Le teorie 1. L atomo e la sua storia 2. La nascita della moderna teoria atomica: da Lavoiser
CONOSCENZE ABILITA' (capacità) TEMPI. Programmazione disciplinare di SCIENZE INTEGRATE (CHIMICA) Classe 2 (servizi sociosanitari)
 Programmazione disciplinare di SCIENZE INTEGRATE (CHIMICA) Classe 2 (servizi sociosanitari) CONTENUTI RISULTATI DI APPRENDIMENTO (competenze) CONOSCENZE ABILITA' (capacità) TEMPI MODULO 0 Richiamo della
Programmazione disciplinare di SCIENZE INTEGRATE (CHIMICA) Classe 2 (servizi sociosanitari) CONTENUTI RISULTATI DI APPRENDIMENTO (competenze) CONOSCENZE ABILITA' (capacità) TEMPI MODULO 0 Richiamo della
Atomi, Molecole e Ioni Lezione 2
 2017 Atomi, Molecole e Ioni Lezione 2 Teoria Atomica 1. Gli elementi sono composti da particelle estremamente piccole, gli atomi. 2. Tutti gli atomi di un certo elemento sono identici. Hanno la stessa
2017 Atomi, Molecole e Ioni Lezione 2 Teoria Atomica 1. Gli elementi sono composti da particelle estremamente piccole, gli atomi. 2. Tutti gli atomi di un certo elemento sono identici. Hanno la stessa
Corso di chimica generale
 Corso di chimica generale Dr. Riccardo Montioli Email: riccardo.montioli@univr.it Programma - La materia e l energia - Le particelle subatomiche e la misura della massa - L atomo, teorie e struttura -
Corso di chimica generale Dr. Riccardo Montioli Email: riccardo.montioli@univr.it Programma - La materia e l energia - Le particelle subatomiche e la misura della massa - L atomo, teorie e struttura -
Esercizi di. Stechiometria dei composti. mercoledì 9 dicembre 2015
 Esercizi di Stechiometria dei composti mercoledì 9 dicembre 2015 Il cloro ha due isotopi stabili contenenti rispettivamente 18 e 20 neutroni. Utilizzando la tavola periodica degli elementi, scrivere i
Esercizi di Stechiometria dei composti mercoledì 9 dicembre 2015 Il cloro ha due isotopi stabili contenenti rispettivamente 18 e 20 neutroni. Utilizzando la tavola periodica degli elementi, scrivere i
SEZIONE D - LE BIOMOLECOLE di Mauro Festa Larel, Patrizia Panunzio, Elisabetta Rusconi, Giovanni Valsecchi
 SEZIONE D - LE BIOMOLECOLE di Mauro Festa Larel, Patrizia Panunzio, Elisabetta Rusconi, Giovanni Valsecchi SEZIONE D - LE BIOMOLECOLE D.1 - PREMESSA: UN PO DI CHIMICA Tutta la materia è formata da atomi
SEZIONE D - LE BIOMOLECOLE di Mauro Festa Larel, Patrizia Panunzio, Elisabetta Rusconi, Giovanni Valsecchi SEZIONE D - LE BIOMOLECOLE D.1 - PREMESSA: UN PO DI CHIMICA Tutta la materia è formata da atomi
Soluzioni. Miscele: (gas in gas) Leghe: (solidi in solidi) Soluzioni p.d: (solventi liquidi)
 Soluzioni Sono miscele omogenee in cui si riconoscono 2 componenti o fasi: il soluto, presente in quantità minore il solvente presente in quantità maggiore. Tipi di soluzioni: Miscele: (gas in gas) Leghe:
Soluzioni Sono miscele omogenee in cui si riconoscono 2 componenti o fasi: il soluto, presente in quantità minore il solvente presente in quantità maggiore. Tipi di soluzioni: Miscele: (gas in gas) Leghe:
Il modello strutturale dell atomo
 Il modello strutturale dell atomo Gli atomi sono costituiti dal nucleo e dagli elettroni Proprietà dell atomo dipendono dal nucleo (fisica nucleare) e dagli elettroni (chimica). Il nucleo contiene protoni
Il modello strutturale dell atomo Gli atomi sono costituiti dal nucleo e dagli elettroni Proprietà dell atomo dipendono dal nucleo (fisica nucleare) e dagli elettroni (chimica). Il nucleo contiene protoni
Sommario della lezione 4. Proprietà periodiche. Massa atomica e massa molecolare. Concetto di mole. Prime esercitazioni
 Sommario della lezione 4 Proprietà periodiche Massa atomica e massa molecolare Concetto di mole Prime esercitazioni Proprietà periodiche Il raggio atomico è definito come la metà della distanza minima
Sommario della lezione 4 Proprietà periodiche Massa atomica e massa molecolare Concetto di mole Prime esercitazioni Proprietà periodiche Il raggio atomico è definito come la metà della distanza minima
Bagatti, Corradi, Desco, Ropa. Chimica. seconda edizione
 Bagatti, Corradi, Desco, Ropa Chimica seconda edizione Bagatti, Corradi, Desco, Ropa, Chimica seconda edizione Capitolo 7. e le proprietà delle sostanze SEGUI LA MAPPA 1 afferma che quando un atomo è legato
Bagatti, Corradi, Desco, Ropa Chimica seconda edizione Bagatti, Corradi, Desco, Ropa, Chimica seconda edizione Capitolo 7. e le proprietà delle sostanze SEGUI LA MAPPA 1 afferma che quando un atomo è legato
Atomo La più piccola particella di un elemento che resta inalterata nelle trasformazioni chimiche.
 Atomo La più piccola particella di un elemento che resta inalterata nelle trasformazioni chimiche. Molecola La più piccola particella di un individuo chimico (elemento o composto) capace di una propria
Atomo La più piccola particella di un elemento che resta inalterata nelle trasformazioni chimiche. Molecola La più piccola particella di un individuo chimico (elemento o composto) capace di una propria
Legame covalente Puro Polare Legame dativo o di coordinazione Legame ionico Legame metallico
 I LEGAMI CHIMICI Legami atomici o forti Legami molecolari o deboli Legame covalente Puro Polare Legame dativo o di coordinazione Legame ionico Legame metallico Legame dipolo-dipolo Legame idrogeno Legame
I LEGAMI CHIMICI Legami atomici o forti Legami molecolari o deboli Legame covalente Puro Polare Legame dativo o di coordinazione Legame ionico Legame metallico Legame dipolo-dipolo Legame idrogeno Legame
Struttura dell atomo e della materia unità 1, modulo C del libro
 Struttura dell atomo e della materia unità 1, modulo C del libro Gli elementi sono costituiti da specie atomiche, dette nuclidi. Tali specie atomiche sono formate da tre tipi di particelle elementari:
Struttura dell atomo e della materia unità 1, modulo C del libro Gli elementi sono costituiti da specie atomiche, dette nuclidi. Tali specie atomiche sono formate da tre tipi di particelle elementari:
C Ca Ce Cf Co Cr Cs Cu
 Elementi Composti ionici (forze elettrostatiche, edifici ionici) molecolari (ripetersi periodico di molecole) Simboli C Ca Ce Cf Co Cr Cs Cu Formule Indici H 2 SO 4 CO 2 H 2 O N 2 Na 2 CO 3 O 2 Mg(NO 3
Elementi Composti ionici (forze elettrostatiche, edifici ionici) molecolari (ripetersi periodico di molecole) Simboli C Ca Ce Cf Co Cr Cs Cu Formule Indici H 2 SO 4 CO 2 H 2 O N 2 Na 2 CO 3 O 2 Mg(NO 3
Le idee della chimica
 G. Valitutti A.Tifi A.Gentile Seconda edizione Copyright 2009 Zanichelli editore Capitolo 4 Le teorie della materia 1. L atomo e la sua storia 2. Le «prove sperimentali» della teoria atomica 3. La teoria
G. Valitutti A.Tifi A.Gentile Seconda edizione Copyright 2009 Zanichelli editore Capitolo 4 Le teorie della materia 1. L atomo e la sua storia 2. Le «prove sperimentali» della teoria atomica 3. La teoria
Simulazioni del Test di Accesso Macroarea Scientifico-Tecnologica - Domande di Chimica -
 Simulazioni del Test di Accesso Macroarea Scientifico-Tecnologica - Domande di Chimica - C1) ll numero atomico di un elemento rappresenta: a) il numero di elettroni b) il numero di protoni c) la somma
Simulazioni del Test di Accesso Macroarea Scientifico-Tecnologica - Domande di Chimica - C1) ll numero atomico di un elemento rappresenta: a) il numero di elettroni b) il numero di protoni c) la somma
Per esempio, possiamo osservare il legame ionico nella molecola di cloruro di sodio. Il cloro e il sodio hanno le seguenti strutture di Lewis:
 IL LEGAME IONICO In natura solo i gas nobili presentano atomi allo stato libero. Tutte le altre sostanze consistono di molecole che sono aggregazioni di atomi. Le forze che tengono uniti gli atomi in una
IL LEGAME IONICO In natura solo i gas nobili presentano atomi allo stato libero. Tutte le altre sostanze consistono di molecole che sono aggregazioni di atomi. Le forze che tengono uniti gli atomi in una
Chimica e laboratorio
 ITIS H.HERTZ Progetto Monoennio Chimica e laboratorio PARTE PRIMA I MODULO: Struttura atomica e molecolare della materia PESO : 70% UNITA ORARIE PREVISTE : 20 h Unità A: ATOMI Descrivere le caratteristiche
ITIS H.HERTZ Progetto Monoennio Chimica e laboratorio PARTE PRIMA I MODULO: Struttura atomica e molecolare della materia PESO : 70% UNITA ORARIE PREVISTE : 20 h Unità A: ATOMI Descrivere le caratteristiche
I MISCUGLI OMOGENEI ED ETEROGENEI
 I MISCUGLI OMOGENEI ED ETEROGENEI SISTEMA: PORZIONE DI SPAZIO CHE VIENE SOTTOPOSTA AD OSSERVAZIONE, SU CUI SI FOCALIZZA L ATTENZIONE Acqua e olio Sono presenti 2 porzioni distinte e ben delimitate di materia,
I MISCUGLI OMOGENEI ED ETEROGENEI SISTEMA: PORZIONE DI SPAZIO CHE VIENE SOTTOPOSTA AD OSSERVAZIONE, SU CUI SI FOCALIZZA L ATTENZIONE Acqua e olio Sono presenti 2 porzioni distinte e ben delimitate di materia,
DEFINIZIONE DI SISTEMA DEFINIZIONE DI FASE SISTEMA OMOGENEO /ETEROGENEO MISCUGLIO OMOGENEO/ETEROGENEO
 DEFINIZIONE DI SISTEMA DEFINIZIONE DI FASE SISTEMA OMOGENEO /ETEROGENEO MISCUGLIO OMOGENEO/ETEROGENEO SISTEMA: PORZIONE DI SPAZIO CHE VIENE SOTTOPOSTA AD OSSERVAZIONE, SU CUI SI FOCALIZZA L ATTENZIONE
DEFINIZIONE DI SISTEMA DEFINIZIONE DI FASE SISTEMA OMOGENEO /ETEROGENEO MISCUGLIO OMOGENEO/ETEROGENEO SISTEMA: PORZIONE DI SPAZIO CHE VIENE SOTTOPOSTA AD OSSERVAZIONE, SU CUI SI FOCALIZZA L ATTENZIONE
ATOMO. Viene considerato Elemento fondamentale della materia (solidi, liquidi e gas)
 http://riccardocavallaro.weebly.com ATOMO Viene considerato Elemento fondamentale della materia (solidi, liquidi e gas) Il tipo di atomi e la loro combinazione determina il tipo di materiale/materia. Struttura
http://riccardocavallaro.weebly.com ATOMO Viene considerato Elemento fondamentale della materia (solidi, liquidi e gas) Il tipo di atomi e la loro combinazione determina il tipo di materiale/materia. Struttura
Struttura dell atomo atomo particelle sub-atomiche - protoni positiva - neutroni } nucleoni - elettroni negativa elemento
 Struttura dell atomo L atomo è la più piccola parte dell elemento che conserva le proprietà dell elemento Negli atomi ci sono tre diverse particelle sub-atomiche: - protoni (con carica positiva unitaria)
Struttura dell atomo L atomo è la più piccola parte dell elemento che conserva le proprietà dell elemento Negli atomi ci sono tre diverse particelle sub-atomiche: - protoni (con carica positiva unitaria)
Le Reazioni Chimiche
 I Legami chimici Quando gli atomi cedono, acquistano o mettono in comune degli elettroni formano un legame chimico. I Legami chimici Gli atomi cercano sempre di completare il loro guscio esterno cedendo,
I Legami chimici Quando gli atomi cedono, acquistano o mettono in comune degli elettroni formano un legame chimico. I Legami chimici Gli atomi cercano sempre di completare il loro guscio esterno cedendo,
CHIMICA: studio della struttura e delle trasformazioni della materia
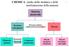 CHIMICA: studio della struttura e delle trasformazioni della materia!1 Materia (materali) Sostanze (omogenee) Processo fisico Miscele Elementi (atomi) Reazioni chimiche Composti (molecole) Miscele omogenee
CHIMICA: studio della struttura e delle trasformazioni della materia!1 Materia (materali) Sostanze (omogenee) Processo fisico Miscele Elementi (atomi) Reazioni chimiche Composti (molecole) Miscele omogenee
ATOMI E MOLECOLE. Psicobiologia Lezione nr. 1. Prof. Lasaponara
 ATOMI E MOLECOLE Psicobiologia Lezione nr. 1 Prof. Lasaponara La struttura dell atomo I legami chimici e le molecole I componenti elementari della materia vivente 20 miliardi di anni fa Caratteristiche
ATOMI E MOLECOLE Psicobiologia Lezione nr. 1 Prof. Lasaponara La struttura dell atomo I legami chimici e le molecole I componenti elementari della materia vivente 20 miliardi di anni fa Caratteristiche
NELLA LEZIONE DI OGGI:
 ABBIAMO VISTO: TEMPERATURA/CALORE SCALE DI TEMPERATURA I PASSAGGI DI STATO NELLA LEZIONE DI OGGI: RIPASSO DELLA DEFINIZIONE DI SISTEMA DEFINIZIONE DI FASE SISTEMA OMOGENEO /ETEROGENEO MISCUGLIO OMOGENEO/ETEROGENEO
ABBIAMO VISTO: TEMPERATURA/CALORE SCALE DI TEMPERATURA I PASSAGGI DI STATO NELLA LEZIONE DI OGGI: RIPASSO DELLA DEFINIZIONE DI SISTEMA DEFINIZIONE DI FASE SISTEMA OMOGENEO /ETEROGENEO MISCUGLIO OMOGENEO/ETEROGENEO
reazioni Sostanze Reazioni di sintesi Reazioni di decomposizione
 Si consumano nelle reazioni Si formano nelle reagenti Si trasformano con prodotti Sostanze Sostanze semplici Sostanze composte Non ottenibili con Non decomponibili con Reazioni di sintesi Reazioni di decomposizione
Si consumano nelle reazioni Si formano nelle reagenti Si trasformano con prodotti Sostanze Sostanze semplici Sostanze composte Non ottenibili con Non decomponibili con Reazioni di sintesi Reazioni di decomposizione
CHIMICA: studio della composizione e della struttura della materia e delle sue trasformazioni
 CHIMICA: studio della composizione e della struttura della materia e delle sue trasformazioni Lavoisier e la legge di conservazione della massa Lavoisier riconobbe l importanza delle misurazioni accurate
CHIMICA: studio della composizione e della struttura della materia e delle sue trasformazioni Lavoisier e la legge di conservazione della massa Lavoisier riconobbe l importanza delle misurazioni accurate
Chimica: Studio della materia e delle sue interazioni.
 Chimica: Studio della materia e delle sue interazioni. La descrizione della materia viene affrontata da: punto di vista microscopico: studio di atomi e molecole le loro interazioni e le reazioni chimiche
Chimica: Studio della materia e delle sue interazioni. La descrizione della materia viene affrontata da: punto di vista microscopico: studio di atomi e molecole le loro interazioni e le reazioni chimiche
Università degli studi di MILANO Facoltà di AGRARIA. El. di Chimica e Chimica Fisica. Mod. 1 CHIMICA. Mod. 2 CHIMICA FISICA.
 Università degli studi di MILANO Facoltà di AGRARIA El. di Chimica e Chimica Fisica Mod. 1 CHIMICA Mod. 2 CHIMICA FISICA Lezione 4 Anno Accademico 2010-2011 Docente: Dimitrios Fessas Si riconoscono così
Università degli studi di MILANO Facoltà di AGRARIA El. di Chimica e Chimica Fisica Mod. 1 CHIMICA Mod. 2 CHIMICA FISICA Lezione 4 Anno Accademico 2010-2011 Docente: Dimitrios Fessas Si riconoscono così
Chimica. Lezione 2 Parte II Composti ionici e molecolari
 Chimica Lezione 2 Parte II Composti ionici e molecolari Composti molecolari Gli ELEMENTI chimici (ad eccezione dei gas nobili) vivono in aggregati più o meno complessi Sono aggregati discreti (hanno un
Chimica Lezione 2 Parte II Composti ionici e molecolari Composti molecolari Gli ELEMENTI chimici (ad eccezione dei gas nobili) vivono in aggregati più o meno complessi Sono aggregati discreti (hanno un
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 4 Le teorie della materia 3 Sommario 1. L atomo e la sua storia 2. Le «prove sperimentali» della teoria atomica 3. La teoria
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 4 Le teorie della materia 3 Sommario 1. L atomo e la sua storia 2. Le «prove sperimentali» della teoria atomica 3. La teoria
I LEGAMI CHIMICI. I legami chimici si formano quando gli atomi cedono, acquistano oppure mettono in comune
 I LEGAMI CHIMICI I legami chimici si formano quando gli atomi cedono, acquistano oppure mettono in comune alcuni elettroni con altri atomi, per completare il guscio elettronico più esterno. 1. LEGAME IONICO
I LEGAMI CHIMICI I legami chimici si formano quando gli atomi cedono, acquistano oppure mettono in comune alcuni elettroni con altri atomi, per completare il guscio elettronico più esterno. 1. LEGAME IONICO
Programma svolto nell a.s
 ISTITUTO DI ISTRUZIONE SUPERIORE VIA SILVESTRI, 301 ROMA Sez. associata: I.T.C.G. "Alberto Ceccherelli" - Via di Bravetta, 383 Materia: Scienze Integrate - CHIMICA Docente: De Rosa Giovanna Classe: I Sez.:
ISTITUTO DI ISTRUZIONE SUPERIORE VIA SILVESTRI, 301 ROMA Sez. associata: I.T.C.G. "Alberto Ceccherelli" - Via di Bravetta, 383 Materia: Scienze Integrate - CHIMICA Docente: De Rosa Giovanna Classe: I Sez.:
Stati di Aggregazione e Composizione - elementi atomo - composti - miscele omo- ed eterogenee L Atomo - particelle subatomiche e proprietà - Numero
 1. La Materia Stati di Aggregazione e Composizione - elementi atomo - composti - miscele omo- ed eterogenee L Atomo - particelle subatomiche e proprietà - Numero Atomico e Numero di Massa Gli Isotopi La
1. La Materia Stati di Aggregazione e Composizione - elementi atomo - composti - miscele omo- ed eterogenee L Atomo - particelle subatomiche e proprietà - Numero Atomico e Numero di Massa Gli Isotopi La
