ANALISI CHIMICA ANALISI QUANTITATIVA ANALISI QUALITATIVA ANALISI ORGANICA. Riconoscimento di sostanze organiche. ANALISI INORGANICA
|
|
|
- Alfredo Venturi
- 7 anni fa
- Visualizzazioni
Transcript
1 ANALISI CHIMICA ANALISI QUANTITATIVA ANALISI QUALITATIVA ANALISI ORGANICA Riconoscimento di sostanze organiche. ANALISI INORGANICA Riconoscimento di sostanze ioniche e solubili in acqua (cationi ed anioni). Reazioni di identificazione: introduzione 1
2 REAZIONE: qualsiasi processo che porta alla formazione di una nuova sostanza chimica. REAGENTE: una sostanza usata per fare avvenire una reazione. PRECIPITATO: qualsiasi sostanza insolubile che si forma in seguito ad una reazione. Ag Cl AgCl Reazioni di identificazione: introduzione 2
3 RESIDUO: è quella parte di solido che rimane dopo parziale dissoluzione per mezzo di un solvente. Una SOLUZIONE è una miscela omogenea di due o più sostanze. La sostanza che si trova in maggiore quantità si chiama SOLVENTE, le sostanze disciolte si chiamano SOLUTI. Una soluzione si definisce LIMPIDA se non presenta particelle solide in sospensione. Una soluzione limpida può essere sia INCOLORE sia COLORATA. Reazioni di identificazione: introduzione 3
4 PROVA (saggio): operazione di laboratorio (reazione) che viene eseguita allo scopo di confermare, o meno, la presenza di una determinata sostanza che nell analisi qualitativa inorganica è generalmente una specie ionica. Una prova può avere esito POSITIVO o NEGATIVO. Se una prova è dubbia occorre fare: PROVA IN BIANCO: si esegue in assenza del campione usando gli stessi reattivi della prova dubbia, utilizzando la stessa procedura. Deve dare esito negativo. PROVA DI CONTROLLO: si esegue su una quantità nota dello ione che si sta cercando usando gli stessi reattivi della prova dubbia, utilizzando la stessa procedura. Deve dare esito positivo. SENSIBILITA : la più piccola quantità di sostanza che per quella prova dà esito positivo. PROVA SPECIFICA: prova che risulta positiva solo per un dato ione e che quindi può essere effettuata anche in presenza di altri ioni senza che questi interferiscano. Reazioni di identificazione: introduzione 4
5 INTERFERENZE: sono definiti interferenti quelle specie la cui presenza altera la risposta della reazione analitica. Interferenze POSITIVE: forniscono lo stesso segnale dell analita (falsi positivi). Interferenze NEGATIVE: causano la diminuzione o anche la soppressione del segnale. Interferenze MASCHERANTI: producono un segnale che modifica e confonde quello che fornisce la reazione analitica. In alcuni casi si aggiunge una specie interferente per bloccare una certa risposta, generalmente si utilizzano interferenti negativi. In alcuni casi per evitare le interferenze bisogna isolare opportunamente l analita dalla miscela in cui si trova. Normalmente si procedere facendo precipitare l anione o il catione selettivamente con un opportuno reattivo precipitante, il precipitato viene poi isolato per centrifugazione. Per essere sicuri di eliminare completamente dal precipitato qualunque traccia degli ioni rimasti nel surnatante bisogna procedere asportando con una pipetta il surnatante, quindi si risospende con acqua deionizzata il precipitato aiutandosi con una bacchetta di vetro, quindi si ricentrifuga e si asporta il nuovo surnatante. Questa operazione andrebbe ripetuta due-tre volte, così da essere sicuri di eliminare completamente gli ioni solubili in acqua. Reazioni di identificazione: introduzione 5
6 L ANALISI QUALITATIVA è un insieme di operazioni chimiche che si eseguono per separare e riconoscere i costituenti di una sostanza o di una miscela di sostanze. ANALISI PER VIA SECCA (senza solvente) analisi di emissione (saggio alla fiamma), reazioni allo stato fuso, comportamento al riscaldamento con e senza reattivi. ANALISI PER VIA UMIDA (analisi in soluzione acquosa) solubilizzazione equilibrio ionico spostamento dell equilibrio attraverso: - variazione del ph, - formazione di complessi, - reazioni redox, - idrolisi, - ione comune. Reazioni di identificazione: introduzione 6
7 Prima di analizzare una sostanza si può fare un esame organolettico valutandone l aspetto, il colore (e l odore). Se la sostanza è solida può essere in polvere, va quindi mescolata per ottenere un campione il più possibile omogeneo; o può essere in granuli ed in questo caso va finemente triturata e polverizzata. Il campione così ottenuto va poi utilizzato per: saggi preliminari; ricerca dei cationi; ricerca degli anioni. I saggi preliminari vengono chiamati saggi per via secca ; si eseguono sulla sostanza secca, senza portarla in soluzione: riscaldamento del campione; riscaldamento del campione in presenza di reattivi; formazione di perle mediante fusione con fondenti speciali; emissione alla fiamma. Reazioni di identificazione: analisi per via secca 7
8 Analisi di emissione alla fiamma Permette di accertare la presenza della maggior parte dei metalli alcalini (e dello ione ammonio). Consente di identificare e/o confermare la presenza di metalli alcalino-terrosi e di qualche metallo di transizione. La base del metodo è l eccitazione termica degli elettroni atomici più esterni, con successivo ripristino dello stato iniziale mediante emissione di energia luminosa: Vi sono più transizione possibili, quindi il ritorno allo stato fondamentale può avvenire in più stadi. Non tutte le transizioni tra livelli elettronici sono permesse. Affinché l emissione sia osservabile la lunghezza d onda della radiazione emessa deve cadere nel campo visibile: 380 nm < < 700 nm Reazioni di identificazione: analisi per via secca 8
9 Reazioni di identificazione: analisi per via secca 9
10 Nella fiamma del bunsen esistono diverse zone distinte per luminosità e temperatura; una zona centrale detta cono freddo costituita da gas incombusto, una zona intermedia molto luminosa detta zona riducente, in cui avviene una combustione parziale ed una zona esterna molto calda e poco luminosa detta zona ossidante, in cui si completa la combustione. Reazioni di identificazione: analisi per via secca 10
11 Questi saggi si basano sul fatto che i composti di alcuni metalli, quando vengono volatilizzati in una fiamma, emettono vapori che impartiscono alla fiamma colorazioni caratteristiche. Queste colorazioni appaiono tanto più facilmente quanto più volatili sono i sali: i cloruri, essendo i sali più volatili, sono i più adatti a colorare la fiamma. Il campione viene introdotto solido, con l uso di un filo di platino, dopo averlo bagnato in HCl per favorire la formazione di cloruri. DH ev DH v DH dis Ecc BaCl 2(aq) BaCl 2(s) BaCl 2(g) Cl + Ba hn Ba* L intensità dell emissione dipende dalla popolazione dello stato eccitato emittente. L osservazione strumentale delle linee di emissione degli elementi indica che tali righe sono in generale composte da più componenti. Ciò implica la presenza di livelli elettronici diversi all interno di uno stesso stato eccitato, di energia molto prossima tra di loro. Reazioni di identificazione: analisi per via secca 11
12 Dal punto di vista pratico si procede utilizzando una piastra di porcellana munita di incavi ed un filo metallico (un pezzetto di filo di ferro, di circa 5-10 cm, che taglierete sul momento e che poi butterete nell opportuno cestino). In un incavo della piastra di porcellana si mettono alcune gocce di HCl 2M, mentre in un incavo asciutto di mette una piccola quantità della sostanza solida di cui si vuole fare il saggio alla fiamma. Si bagna prima il filo metallico in HCl 2M e poi si tocca la polvere, in questo modo alcuni cristalli della sostanza aderiranno al filo bagnato. In seguito alla reazione vista precedentemente si formerà un cloruro volatile del metallo che si vuole analizzare e quindi ponendo il filo nella fiamma questo volatilizzerà e la fiamma assumerà un colore caratteristico. State attenti però a non pensare sempre di avere il catione sodio, perché il filo di ferro che voi usate per fare il saggio con HCl 2M in parte si corrode e quindi si colora di giallo-arancio se voi lo ponete nella zona calda della fiamma, se avete il dubbio fate il confronto con uno standard che sapete contenere il catione sodio. Piastra di porcellana Reazioni di identificazione: analisi per via secca 12
13 Reazioni di identificazione: analisi per via secca 13
14 Nel caso di miscele si ottengono varie colorazioni che si sovrappongono mascherandosi. In questo caso si può sfruttare la diversa volatilità dei sali e le diverse temperature delle varie zone della fiamma. Si immerge il filo di platino prima verso la base della fiamma, quella meno calda, dove volatilizzano facilmente solo i sali dei metalli alcalini; poi si sposta il filo nella zona di fusione dove la temperatura più elevata fa volatilizzare i sali dei metalli alcalinoterrosi, meno volatili. Per poter vedere le colorazioni mascherate si può osservare la fiamma attraverso appositi vetri colorati che funzionano da filtri per la luce. Questi vetri sono in grado di assorbire certi raggi luminosi lasciandone passare altri. La colorazione gialla del sodio maschera quella violetta del potassio, ma se si osserva la fiamma attraverso un vetro al cobalto (blu), si vede la colorazione rossa del potassio perché quella del sodio viene assorbita. Reazioni di identificazione: analisi per via secca 14
15 Reazioni di identificazione: analisi per via secca 15
16 Ione Colore della fiamma Attraverso vetro blu Litio Rosso porpora - Sodio Giallo Invisibile Potassio Violetto Rosso paonazzo Calcio Rosso mattone Grigio verde Bario Verde pallido - Rame Verde-azzurro - Boro Verde mela - Reazioni di identificazione: analisi per via secca 16
17 Calcio Potassio Sodio Bario uola.zanichelli.it /chimicainlabor atorio Boro Rame Litio Reazioni di identificazione: analisi per via secca 17
RICONOSCIMENTO degli ELEMENTI PRESENTI in un CAMPIONE INCOGNITO
 RICONOSCIMENTO degli ELEMENTI PRESENTI in un CAMPIONE INCOGNITO OBIETTIVO: individuare gli elementi presenti in un campione solido inorganico di composizione incognita. Approccio al problema: l analisi
RICONOSCIMENTO degli ELEMENTI PRESENTI in un CAMPIONE INCOGNITO OBIETTIVO: individuare gli elementi presenti in un campione solido inorganico di composizione incognita. Approccio al problema: l analisi
 ANALISI QUALITATIVA INORGANICA Analisi per via secca (senza solvente) analisi di emissione (saggi alla fiamma) - reazioni allo stato fuso (saggi alla perla) comportamento al riscaldamento (senza e con
ANALISI QUALITATIVA INORGANICA Analisi per via secca (senza solvente) analisi di emissione (saggi alla fiamma) - reazioni allo stato fuso (saggi alla perla) comportamento al riscaldamento (senza e con
L ANALISI CHIMICA si occupa:
 L ANALISI CHIMICA si occupa: della scomposizione di miscugli e composti nei loro componenti del riconoscimento e del dosaggio di tali componenti Settori di applicazione: Nel campo alimentare: i costituenti
L ANALISI CHIMICA si occupa: della scomposizione di miscugli e composti nei loro componenti del riconoscimento e del dosaggio di tali componenti Settori di applicazione: Nel campo alimentare: i costituenti
L ANALISI CHIMICA si occupa:
 L ANALISI CHIMICA si occupa: La chimica analitica è l arte di separare, riconoscere sostanze differenti e determinare i costituenti di un campione (Whilelm Ostwald, 1894) della scomposizione di miscugli
L ANALISI CHIMICA si occupa: La chimica analitica è l arte di separare, riconoscere sostanze differenti e determinare i costituenti di un campione (Whilelm Ostwald, 1894) della scomposizione di miscugli
L ANALISI CHIMICA si occupa:
 L ANALISI CHIMICA si occupa: La chimica analitica è l arte di separare, riconoscere sostanze differenti e determinare i costituenti di un campione (Whilelm Ostwald, 1894) della scomposizione di miscugli
L ANALISI CHIMICA si occupa: La chimica analitica è l arte di separare, riconoscere sostanze differenti e determinare i costituenti di un campione (Whilelm Ostwald, 1894) della scomposizione di miscugli
specie chimiche. in quantità maggiore presente nella soluzione, e tutti gli altri componenti che sono detti soluti. Un componente di una soluzione
 Equilibri di solubilità 1 1 Si definisce SOLUZIONE una miscela omogenea di due o più specie chimiche. In una soluzione si distinguono un solvente, che è il componente in quantità maggiore presente nella
Equilibri di solubilità 1 1 Si definisce SOLUZIONE una miscela omogenea di due o più specie chimiche. In una soluzione si distinguono un solvente, che è il componente in quantità maggiore presente nella
Influenza della concentrazione dei reagenti e dei prodotti sull equilibrio chimico. Influenza della temperatura sull equilibrio chimico.
 Esperienza n. 5 Influenza della concentrazione dei reagenti e dei prodotti sull equilibrio chimico. Influenza della temperatura sull equilibrio chimico. una provetta da saggio, porta provette, spruzzetta
Esperienza n. 5 Influenza della concentrazione dei reagenti e dei prodotti sull equilibrio chimico. Influenza della temperatura sull equilibrio chimico. una provetta da saggio, porta provette, spruzzetta
ESAME DI ANALISI DELLE SOSTANZE INORGANICHE DI IMPIEGO FARMACEUTICO + LABORATORIO DI ANALISI QUALITATIVA. Nome e cognome: Numero di matricola:..
 ESAME DI ANALISI DELLE SOSTANZE INORGANICHE DI IMPIEGO FARMACEUTICO + LABORATORIO DI ANALISI QUALITATIVA Nome e cognome: Numero di matricola:.. 1) Indicare, motivando la risposta, il ph di una soluzione
ESAME DI ANALISI DELLE SOSTANZE INORGANICHE DI IMPIEGO FARMACEUTICO + LABORATORIO DI ANALISI QUALITATIVA Nome e cognome: Numero di matricola:.. 1) Indicare, motivando la risposta, il ph di una soluzione
(appunti di Daniela Discalzi e Serena Fortino) Con l'analisi quantitativa si determina la quantità di componenti presenti in un miscuglio.
 ANALISI QUALITATIVA INRGANICA (appunti di Daniela Discalzi e Serena Fortino) Con l'analisi quantitativa si determina la quantità di componenti presenti in un miscuglio. L'analisi qualitativa indica quali
ANALISI QUALITATIVA INRGANICA (appunti di Daniela Discalzi e Serena Fortino) Con l'analisi quantitativa si determina la quantità di componenti presenti in un miscuglio. L'analisi qualitativa indica quali
STECHIOMETRIA 1) Nella sintesi del Bianco S.Giovanni (CaCO 3 ) secondo la reazione CaCl 2 + Na 2 CO 3 = 2NaCl + CaCO 3 partendo da 8,3g (0,038 mol)
 STECHIOMETRIA 1) Nella sintesi del Bianco S.Giovanni (CaCO 3 ) secondo la reazione CaCl 2 + Na 2 CO 3 = 2NaCl + CaCO 3 partendo da 8,3g (0,038 mol) di cloruro di Calcio biidrato e 14,3g (0,050 mol) di
STECHIOMETRIA 1) Nella sintesi del Bianco S.Giovanni (CaCO 3 ) secondo la reazione CaCl 2 + Na 2 CO 3 = 2NaCl + CaCO 3 partendo da 8,3g (0,038 mol) di cloruro di Calcio biidrato e 14,3g (0,050 mol) di
RICERCA DEI CATIONI NELLE SOSTANZE INORGANICHE O ORGANO-METALLICHE RICERCA DEGLI ANIONI NEI SALI DI AMMINE O DI AMMONIO QUATERNARIO
 RICERCA DEI CATIONI NELLE SOSTANZE INORGANICHE O ORGANO-METALLICHE RICERCA DEGLI ANIONI NEI SALI DI AMMINE O DI AMMONIO QUATERNARIO Prof. Antonio Lavecchia Ricerca dei Cationi nelle Sostanze Inorganiche
RICERCA DEI CATIONI NELLE SOSTANZE INORGANICHE O ORGANO-METALLICHE RICERCA DEGLI ANIONI NEI SALI DI AMMINE O DI AMMONIO QUATERNARIO Prof. Antonio Lavecchia Ricerca dei Cationi nelle Sostanze Inorganiche
Circuiti in Serie / Parallelo
 Circuiti in Serie / Parallelo Utilizzatori in serie Più utilizzatori sono collegati in serie quando sono montati uno dopo l altro in modo che la stessa corrente li attraversi in successione. In tal modo
Circuiti in Serie / Parallelo Utilizzatori in serie Più utilizzatori sono collegati in serie quando sono montati uno dopo l altro in modo che la stessa corrente li attraversi in successione. In tal modo
ANALISI CHIMICA QUALITATIVA
 ANALISI CHIMICA QUALITATIVA Analisi per via secca: Saggi alla fiamma Scopo dell esperimento: Riconoscimento della presenza di alcuni elementi per via secca Premessa teorica: I saggi per via secca, così
ANALISI CHIMICA QUALITATIVA Analisi per via secca: Saggi alla fiamma Scopo dell esperimento: Riconoscimento della presenza di alcuni elementi per via secca Premessa teorica: I saggi per via secca, così
(Si identificano Ag +, Hg 2. , Pb 2+ ) - 1 GRUPPO - Reattivo Generale: HCl 2N. Soluzione. Precipitato. Soluzione. Residuo. Soluzione.
 Reattivo Generale: HCl 2N - 1 GRUPPO - (Si identificano Ag +, Hg 2 2+, Pb 2+ ) Esame Sistematico: Nella provetta da centrifuga contenente la soluzione in esame (preparata sciogliendo la sostanza in H 2
Reattivo Generale: HCl 2N - 1 GRUPPO - (Si identificano Ag +, Hg 2 2+, Pb 2+ ) Esame Sistematico: Nella provetta da centrifuga contenente la soluzione in esame (preparata sciogliendo la sostanza in H 2
ANALISI SISTEMATICA DEI CATIONI
 ANALISI SISTEMATICA DEI CATIONI Particolare procedura analitica attraverso la quale tutte le specie cationiche presenti in una ipotetica miscela vengono inizialmente separate in gruppi, mediante l uso
ANALISI SISTEMATICA DEI CATIONI Particolare procedura analitica attraverso la quale tutte le specie cationiche presenti in una ipotetica miscela vengono inizialmente separate in gruppi, mediante l uso
 Analisi dei gas di scarico dei mezzi di trasporto allo scopo di determinare l efficacia dei dispositivi per il controllo delle emissioni inquinanti. Le misure quantitative del calcio ionizzato nel siero
Analisi dei gas di scarico dei mezzi di trasporto allo scopo di determinare l efficacia dei dispositivi per il controllo delle emissioni inquinanti. Le misure quantitative del calcio ionizzato nel siero
Analisi Chimico-Farmaceutiche e Tossicologiche 1
 Analisi Chimico-Farmaceutiche e Tossicologiche 1 Corso A (A H) Prof.ssa Alessia Carocci E-mail: alessia.carocci@uniba.it Studio: stanza 429, III Piano Tel: 080/5442745 Ricevimento studenti: lunedì, mercoledì,
Analisi Chimico-Farmaceutiche e Tossicologiche 1 Corso A (A H) Prof.ssa Alessia Carocci E-mail: alessia.carocci@uniba.it Studio: stanza 429, III Piano Tel: 080/5442745 Ricevimento studenti: lunedì, mercoledì,
Analisi dei gas di scarico dei mezzi di trasporto allo scopo di determinare l efficacia dei dispositivi per il controllo delle emissioni inquinanti.
 1 Analisi dei gas di scarico dei mezzi di trasporto allo scopo di determinare l efficacia dei dispositivi per il controllo delle emissioni inquinanti. Le misure quantitative del calcio ionizzato nel siero
1 Analisi dei gas di scarico dei mezzi di trasporto allo scopo di determinare l efficacia dei dispositivi per il controllo delle emissioni inquinanti. Le misure quantitative del calcio ionizzato nel siero
Sostanze inorganiche: determinazioni qualitative
 Carbonati e Bicarbonati Indicare il tipo di sostanza basandosi sulle caratteristiche alla calcinazione e le prove di solubilità e il ph. Sodio carbonato anidro Na 2 CO 3 (F.U. X Edizione, European Pharmacopeia
Carbonati e Bicarbonati Indicare il tipo di sostanza basandosi sulle caratteristiche alla calcinazione e le prove di solubilità e il ph. Sodio carbonato anidro Na 2 CO 3 (F.U. X Edizione, European Pharmacopeia
IV Gruppo: H 2 S 2 H + + S = I solfuri insolubili nelle predette condizioni sono: ZnS. CoS. bianco. nero. MnS. rosa-salmone. nero.
 IV Gruppo: Comprende quei cationi che precipitano selettivamente come solfuri insolubili a ph = 9 in soluzione tampone: NH 4 OH/NH 4 Cl (esclusi quelli del I, II e III Gruppo). Il reattivo precipitante
IV Gruppo: Comprende quei cationi che precipitano selettivamente come solfuri insolubili a ph = 9 in soluzione tampone: NH 4 OH/NH 4 Cl (esclusi quelli del I, II e III Gruppo). Il reattivo precipitante
IV Gruppo: I solfuri insolubili nelle predette condizioni sono: ZnS. CoS. bianco. nero. MnS. nero. rosa-salmone. NiS
 IV Gruppo: Comprende quei cationi che precipitano selettivamente come solfuri insolubili a ph = 9 in soluzione tampone: NH 4 OH/NH 4 Cl (esclusi quelli del I, II e III Gruppo). Il reattivo precipitante
IV Gruppo: Comprende quei cationi che precipitano selettivamente come solfuri insolubili a ph = 9 in soluzione tampone: NH 4 OH/NH 4 Cl (esclusi quelli del I, II e III Gruppo). Il reattivo precipitante
Saggi preliminari. Esame organolettico Combustione Saggi di solubilità Comportamento chimico
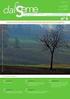 Saggi preliminari Esame organolettico Combustione Saggi di solubilità Comportamento chimico Esame organolettico Stato fisico: legato alle caratteristiche chimico fisiche del composto (solido, liquido o
Saggi preliminari Esame organolettico Combustione Saggi di solubilità Comportamento chimico Esame organolettico Stato fisico: legato alle caratteristiche chimico fisiche del composto (solido, liquido o
PRINCIPALI OPERAZIONI DA EFFETTUARE DURANTE L ANALISI PER VIA UMIDA
 PRINCIPALI OPERAZIONI DA EFFETTUARE DURANTE L ANALISI PER VIA UMIDA 2016 Precipitazione Filtrazione Centrifugazione Lavaggio dei precipitati Evaporazione, ebollizione, calcinazione 1 PRECIPITAZIONE Le
PRINCIPALI OPERAZIONI DA EFFETTUARE DURANTE L ANALISI PER VIA UMIDA 2016 Precipitazione Filtrazione Centrifugazione Lavaggio dei precipitati Evaporazione, ebollizione, calcinazione 1 PRECIPITAZIONE Le
Università degli Studi di Torino CORSO DI CHIMICA GENERALE ED INORGANICA C. Schede di valutazione relative alle esercitazioni pratiche in laboratorio
 Università degli Studi di Torino CORSO DI CHIMICA GENERALE ED INORGANICA C Schede di valutazione relative alle esercitazioni pratiche in laboratorio Anno accademico 2006-2007 Dott.ssa Elena Ghibaudi Dott.
Università degli Studi di Torino CORSO DI CHIMICA GENERALE ED INORGANICA C Schede di valutazione relative alle esercitazioni pratiche in laboratorio Anno accademico 2006-2007 Dott.ssa Elena Ghibaudi Dott.
EQUILIBRI DI SOLUBILITA
 EQUILIBRI DI SOLUBILITA Molti composti ionici sono poco solubili. In soluzione, inizialmente si sciolgono (a), fino a raggiungere un equilibrio dinamico tra ioni che passano in soluzione e ioni che cristallizzano
EQUILIBRI DI SOLUBILITA Molti composti ionici sono poco solubili. In soluzione, inizialmente si sciolgono (a), fino a raggiungere un equilibrio dinamico tra ioni che passano in soluzione e ioni che cristallizzano
bario cloruro biidrato (200 mg; PM ) ferro(iii) cloruro esaidrato (200 mg; PM ) rame(ii) acetato monoidrato (200 mg; PM 181.
 Una delle esercitazioni che effettueremo in laboratorio è la separazione di cationi metallici basata sulla loro precipitazione selettiva. In particolare, seguiremo una metodica che ci consentirà di separare
Una delle esercitazioni che effettueremo in laboratorio è la separazione di cationi metallici basata sulla loro precipitazione selettiva. In particolare, seguiremo una metodica che ci consentirà di separare
Farmacopea Europea (European Pharmacopeia)
 LA FARMACOPEA Le Farmacopea Ufficiale della Repubblica Italiana (XII edizione) era un codice farmaceutico, cioè un insieme di disposizioni tecniche ed amministrative rivolte a permettere il controllo della
LA FARMACOPEA Le Farmacopea Ufficiale della Repubblica Italiana (XII edizione) era un codice farmaceutico, cioè un insieme di disposizioni tecniche ed amministrative rivolte a permettere il controllo della
SAGGI PER VIA SECCA. Fiamma Ossidante. Fiamma Riducente C C
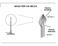 SAGGI PER VIA SECCA Fiamma Ossidante 1350-1500 C Fiamma Riducente 400-500 C Ricerca dei Cationi per Via Secca Gli elementi metallici presenti nei composti organometallici della F.U. sono: Sodio, Potassio,
SAGGI PER VIA SECCA Fiamma Ossidante 1350-1500 C Fiamma Riducente 400-500 C Ricerca dei Cationi per Via Secca Gli elementi metallici presenti nei composti organometallici della F.U. sono: Sodio, Potassio,
Sommario della lezione 24. Equilibri di solubilità. Chimica Organica. Elettrochimica
 Sommario della lezione 24 Equilibri di solubilità Chimica Organica Elettrochimica EQUILIBRI DI SOLUBILITA Solubilità È la concentrazione del soluto in una soluzione satura (dove è presente il corpo di
Sommario della lezione 24 Equilibri di solubilità Chimica Organica Elettrochimica EQUILIBRI DI SOLUBILITA Solubilità È la concentrazione del soluto in una soluzione satura (dove è presente il corpo di
LABORATORIO DI ANALISI DEI FARMACI I A - L
 DIPARTIMENTO DI SCIENZE DEL FARMACO Corso di laurea magistrale in Chimica e tecnologia farmaceutiche Anno accademico 2018/2019-2 anno LABORATORIO DI ANALISI DEI FARMACI I A - L CHIM/08-6 CFU - Insegnamento
DIPARTIMENTO DI SCIENZE DEL FARMACO Corso di laurea magistrale in Chimica e tecnologia farmaceutiche Anno accademico 2018/2019-2 anno LABORATORIO DI ANALISI DEI FARMACI I A - L CHIM/08-6 CFU - Insegnamento
L ANALISI CHIMICA 2 SOSTANZA INCOGNITA. Analisi degli anioni e dei cationi. Riconoscimento della sostanza
 L ANALISI CHIMICA 1 L Analisi Chimica è un insieme di operazioni che si eseguono per separare, riconoscere (Analisi Chimica Qualitativa) e dosare (Analisi Chimica Quantitativa) una sostanza o una miscela
L ANALISI CHIMICA 1 L Analisi Chimica è un insieme di operazioni che si eseguono per separare, riconoscere (Analisi Chimica Qualitativa) e dosare (Analisi Chimica Quantitativa) una sostanza o una miscela
SAGGI PER VIA SECCA. Fiamma Ossidante. Fiamma Riducente C C
 SAGGI PER VIA SECCA Fiamma Ossidante 1350-1500 C Fiamma Riducente 400-500 C Ricerca dei Cationi per Via Secca Gli elementi metallici presenti nei composti organometallici della F.U. sono: Sodio, Potassio,
SAGGI PER VIA SECCA Fiamma Ossidante 1350-1500 C Fiamma Riducente 400-500 C Ricerca dei Cationi per Via Secca Gli elementi metallici presenti nei composti organometallici della F.U. sono: Sodio, Potassio,
EQUILIBRI DI SOLUBILITA
 EQUILIBRI DI SOLUBILITA Solubilità In generale solo una quantità finita di un solido si scioglie in un dato volume di solvente dando luogo ad una soluzione satura, cioè una soluzione in equilibrio con
EQUILIBRI DI SOLUBILITA Solubilità In generale solo una quantità finita di un solido si scioglie in un dato volume di solvente dando luogo ad una soluzione satura, cioè una soluzione in equilibrio con
Esperienza n. 2: Proprietà periodiche di terre alcaline ed alogeni
 Laboratorio di Chimica Inorganica Esperienza n. 2: Proprietà periodiche di terre alcaline ed alogeni A.A. 2014/2015 L esperienza consiste nell osservazione della variazione periodica delle proprietà di
Laboratorio di Chimica Inorganica Esperienza n. 2: Proprietà periodiche di terre alcaline ed alogeni A.A. 2014/2015 L esperienza consiste nell osservazione della variazione periodica delle proprietà di
PRINCIPALI OPERAZIONI DA EFFETTUARE DURANTE L ANALISI:
 PRINCIPALI OPERAZIONI DA EFFETTUARE DURANTE L ANALISI: Precipitazione Filtrazione Centrifugazione Lavaggio dei precipitati Evaporazione, ebollizione, calcinazione PRECIPITAZIONE Le reazioni di precipitazione
PRINCIPALI OPERAZIONI DA EFFETTUARE DURANTE L ANALISI: Precipitazione Filtrazione Centrifugazione Lavaggio dei precipitati Evaporazione, ebollizione, calcinazione PRECIPITAZIONE Le reazioni di precipitazione
RICERCA RICERCA DEGLI ANIONI
 RICERCA DEGLI ANIONI 1 SOSTANZA INIZIALE Na 2 CO 3 Ricerca: ACETATI SOLFITI CARBONATI TARTRATI SOLUZIONE ALCALINA Limpida Incolore RESIDUO Si scarta Ricerca: SOLFATI OSSALATI ARSENIATI NITRITI NITRATI
RICERCA DEGLI ANIONI 1 SOSTANZA INIZIALE Na 2 CO 3 Ricerca: ACETATI SOLFITI CARBONATI TARTRATI SOLUZIONE ALCALINA Limpida Incolore RESIDUO Si scarta Ricerca: SOLFATI OSSALATI ARSENIATI NITRITI NITRATI
Analisi chimico-farmaceutiche e tossicologiche I
 Analisi chimico-farmaceutiche e tossicologiche I Corso I Z Prof.ssa Alessia Catalano E-mail: alessia.catalano@uniba.it Tel: 080/5442745 Stanza 429 - III piano Ricevimento studenti: lunedì, mercoledì, venerdì
Analisi chimico-farmaceutiche e tossicologiche I Corso I Z Prof.ssa Alessia Catalano E-mail: alessia.catalano@uniba.it Tel: 080/5442745 Stanza 429 - III piano Ricevimento studenti: lunedì, mercoledì, venerdì
LABORATORIO DI ANALISI DEI FARMACI I A - L
 DIPARTIMENTO DI SCIENZE DEL FARMACO Corso di laurea magistrale in Chimica e tecnologia farmaceutiche Anno accademico 2016/2017-2 anno LABORATORIO DI ANALISI DEI FARMACI I A - L CHIM/08-6 CFU - 2 semestre
DIPARTIMENTO DI SCIENZE DEL FARMACO Corso di laurea magistrale in Chimica e tecnologia farmaceutiche Anno accademico 2016/2017-2 anno LABORATORIO DI ANALISI DEI FARMACI I A - L CHIM/08-6 CFU - 2 semestre
ASSORBIMENTO UV-VIS. Atomo
 ASSRBIMET UV-VIS 1 Atomo Molecola E 3 E 2 Livelli elettronici (interazioni UV) A Tipi di vibrazione molecolare: E 1 E 0 sottolivelli vibrazionali (interazioni IR) sottolivelli rotazionali (interazioni
ASSRBIMET UV-VIS 1 Atomo Molecola E 3 E 2 Livelli elettronici (interazioni UV) A Tipi di vibrazione molecolare: E 1 E 0 sottolivelli vibrazionali (interazioni IR) sottolivelli rotazionali (interazioni
01. Le basi della meccanica quantistica. 01 j-k. Gli atomi con più elettroni
 01. 01 j-k. Gli atomi con più elettroni 01. Contenuti 1.j Gli atomi con più elettroni: il modello a elettroni indipendenti, il Principio di esclusione di Pauli, la struttura elettronica, la tavola di Mendeleev.
01. 01 j-k. Gli atomi con più elettroni 01. Contenuti 1.j Gli atomi con più elettroni: il modello a elettroni indipendenti, il Principio di esclusione di Pauli, la struttura elettronica, la tavola di Mendeleev.
*M I03* 3/20. perforiran list
 *M15143112I* 2/20 *M15143112I02* *M15143112I03* 3/20 P perforiran list 4/20 *M15143112I04* Pagina vuota *M15143112I05* 5/20 1. L'atomo di un certo elemento contiene 20 neutroni e 17 protoni. 1.1. Scrivete
*M15143112I* 2/20 *M15143112I02* *M15143112I03* 3/20 P perforiran list 4/20 *M15143112I04* Pagina vuota *M15143112I05* 5/20 1. L'atomo di un certo elemento contiene 20 neutroni e 17 protoni. 1.1. Scrivete
Sapienza Università di Roma Facoltà di Farmacia e Medicina Anno Accademico 2014/2015
 Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Corso di Laurea in Chimica e Tecnologie Farmaceutiche Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Dott. Giuseppe La Regina Programma
Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Corso di Laurea in Chimica e Tecnologie Farmaceutiche Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Dott. Giuseppe La Regina Programma
Sapienza Università di Roma Facoltà di Farmacia e Medicina Anno Accademico 2016/2017
 Facoltà di Farmacia e Medicina Anno Accademico 2016/2017 Corso di Laurea in Chimica e Tecnologie Farmaceutiche Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Dott. Giuseppe La Regina Programma
Facoltà di Farmacia e Medicina Anno Accademico 2016/2017 Corso di Laurea in Chimica e Tecnologie Farmaceutiche Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Dott. Giuseppe La Regina Programma
Avvisi. Totale: 14 CFU. Il voto finale sarà la media pesata fra: 1. Voto di Chimica Generale ed Inorganica (6/14) 2. Voto di Chimica Organica (8/14)
 Avvisi Chimica (Corso Integrato): Chimica Generale ed Inorganica (6 CFU) Dott. Francesco Musiani Chimica Organica (8 CFU) Modulo 1 (teoria): Prof. Luca Gentilucci Modulo 2 (laboratorio): Dott. Andrea Gualandi
Avvisi Chimica (Corso Integrato): Chimica Generale ed Inorganica (6 CFU) Dott. Francesco Musiani Chimica Organica (8 CFU) Modulo 1 (teoria): Prof. Luca Gentilucci Modulo 2 (laboratorio): Dott. Andrea Gualandi
2.1 Iodimetria-iodometria
 .1 Iodimetria-iodometria Sono metodi analitici basati su reazioni di ossidoriduzione in cui una delle due coppie redox è I / I - Equazione della semireazione di riduzione dello iodio I + e - I - E = 0,535
.1 Iodimetria-iodometria Sono metodi analitici basati su reazioni di ossidoriduzione in cui una delle due coppie redox è I / I - Equazione della semireazione di riduzione dello iodio I + e - I - E = 0,535
Titolazioni di Precipitazione
 Titolazioni di Precipitazione Le titolazioni di precipitazione si basano su reazioni che generano composti poco solubili L agente titolante è anche detto agente precipitante La velocità di formazione di
Titolazioni di Precipitazione Le titolazioni di precipitazione si basano su reazioni che generano composti poco solubili L agente titolante è anche detto agente precipitante La velocità di formazione di
Fe(OH) 3. Mn(OH) 2. bianco. MnO 2 2H 2 O
 III Gruppo: Comprende quei cationi che precipitano selettivamente come idrossidi insolubili a ph = 9 (esclusi quelli del I e II Gruppo). Il reattivo precipitante è NH 4 OH/NH 4 Cl (soluzione tampone a
III Gruppo: Comprende quei cationi che precipitano selettivamente come idrossidi insolubili a ph = 9 (esclusi quelli del I e II Gruppo). Il reattivo precipitante è NH 4 OH/NH 4 Cl (soluzione tampone a
EQUILIBRI SOLUBILITA. AgNO 3 + H 2 O. Ag + + NO 3- + H 2 O. Provetta 1 : Ag + + NO 3- + H 2 O NaCl + H 2 O Na + + Cl - + H 2 O
 a) Mettere in due provette ca. 2 ml della soluzione di AgNO 3, poi aggiungere in una 34 gocce di NaCl e nell altra 3 4 gocce di K 2 CrO 4 AgNO 3, NaCl, K 2 CrO 4 sono solubili in acqua. In soluzione avremo:
a) Mettere in due provette ca. 2 ml della soluzione di AgNO 3, poi aggiungere in una 34 gocce di NaCl e nell altra 3 4 gocce di K 2 CrO 4 AgNO 3, NaCl, K 2 CrO 4 sono solubili in acqua. In soluzione avremo:
scheda di lavoro relativa all'esperienza di laboratorio: REAZIONI FRA IONI IN SOLUZIONE ACQUOSA Scopo dell'esperienza: verificare la formazione di...
 scheda di lavoro relativa all'esperienza di laboratorio: REAZIONI FRA IONI IN SOLUZIONE ACQUOSA Scopo dell'esperienza: verificare la formaz di... Prerequisiti: :.. composto ionico:.. reazioni di doppio
scheda di lavoro relativa all'esperienza di laboratorio: REAZIONI FRA IONI IN SOLUZIONE ACQUOSA Scopo dell'esperienza: verificare la formaz di... Prerequisiti: :.. composto ionico:.. reazioni di doppio
Chimica Inorganica e Laboratorio
 Chimica Inorganica e Laboratorio Esperienza n. 2: Proprietà periodiche di terre alcaline ed alogeni L esperienza 2 consiste nell osservazione della variazione periodica delle proprietà di due gruppi, le
Chimica Inorganica e Laboratorio Esperienza n. 2: Proprietà periodiche di terre alcaline ed alogeni L esperienza 2 consiste nell osservazione della variazione periodica delle proprietà di due gruppi, le
PROPRIETA ACIDO-BASE DELLE SOLUZIONI SALINE
 PROPRIETA ACIDO-BASE DELLE SOLUZIONI SALINE Un sale è un solido ionico contenente un catione diverso da H + e un anione diverso da OH -. I sali sono degli elettroliti forti, cioè in acqua si dissociano
PROPRIETA ACIDO-BASE DELLE SOLUZIONI SALINE Un sale è un solido ionico contenente un catione diverso da H + e un anione diverso da OH -. I sali sono degli elettroliti forti, cioè in acqua si dissociano
Fe(OH) 3. Mn(OH) 2 2H 2 O
 III Gruppo: Comprende quei cationi che precipitano selettivamente come idrossidi insolubili a ph = 9 (esclusi quelli del I e II Gruppo). Il reattivo precipitante è NH 4 OH/NH 4 Cl (soluzione tampone a
III Gruppo: Comprende quei cationi che precipitano selettivamente come idrossidi insolubili a ph = 9 (esclusi quelli del I e II Gruppo). Il reattivo precipitante è NH 4 OH/NH 4 Cl (soluzione tampone a
Prodotto di solubilità (Kps)
 Prodotto di solubilità (Kps) SOLUBILITA Concentrazione massima che si può raggiungere per un soluto in un dato solvente ad una certa temperatura. (Es: g soluto/100g di solvente) Solubiltà di NaCl in acqua
Prodotto di solubilità (Kps) SOLUBILITA Concentrazione massima che si può raggiungere per un soluto in un dato solvente ad una certa temperatura. (Es: g soluto/100g di solvente) Solubiltà di NaCl in acqua
ALOGENURI (Cl -, Br -, I - ) 1
 ALOGENURI (Cl -, Br -, I - ) 1 Cloruri, bromuri e ioduri di tutti i metalli, eccetto quelli di Pb +,Ag + e Hg + (I), sono solubili in H O. Cloruri, bromuri e ioduri di Pb +,Ag + e Hg + (I) sono inoltre
ALOGENURI (Cl -, Br -, I - ) 1 Cloruri, bromuri e ioduri di tutti i metalli, eccetto quelli di Pb +,Ag + e Hg + (I), sono solubili in H O. Cloruri, bromuri e ioduri di Pb +,Ag + e Hg + (I) sono inoltre
ANALISI dei MEDICINALI II Corso di Laurea in Farmacia (matricole dispari) a.a Prof. Antonio Lavecchia
 ANALISI dei MEDICINALI II Corso di Laurea in Farmacia (matricole dispari) a.a. 2017-2018 Prof. Antonio Lavecchia Testi Consigliati Guida all analisi di composti d'interesse farmaceutico, F. Savelli, Ed.
ANALISI dei MEDICINALI II Corso di Laurea in Farmacia (matricole dispari) a.a. 2017-2018 Prof. Antonio Lavecchia Testi Consigliati Guida all analisi di composti d'interesse farmaceutico, F. Savelli, Ed.
Parte Prima. La Materia e le sue Trasformazioni. 1) Quale delle seguenti affermazioni NON definisce una sostanza pura dal punto di vista chimico?
 Parte Prima La Materia e le sue Trasformazioni 1) Quale delle seguenti affermazioni NON definisce una sostanza pura dal punto di vista chimico? L'acqua pura: a. ha una definita temperatura di ebollizione
Parte Prima La Materia e le sue Trasformazioni 1) Quale delle seguenti affermazioni NON definisce una sostanza pura dal punto di vista chimico? L'acqua pura: a. ha una definita temperatura di ebollizione
La titolazione è un metodo di analisi chimica per la misura della concentrazione di una data sostanza in soluzione.
 Tecniche di analisi chimica Prof. Marcello Romagnoli Titolazione La titolazione è un metodo di analisi chimica per la misura della concentrazione di una data sostanza in soluzione. Una quantità nota del
Tecniche di analisi chimica Prof. Marcello Romagnoli Titolazione La titolazione è un metodo di analisi chimica per la misura della concentrazione di una data sostanza in soluzione. Una quantità nota del
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
PRIMA ESPERIENZA DI LABORATORIO. Prof. Antonio Lavecchia
 PRIMA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Prima Esperienza di Laboratorio Analisi Qualitativa Elementare di Sostanze Inorganiche (Via Umida) Ricerca dei Cationi Calcio, magnesio Ricerca degli
PRIMA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Prima Esperienza di Laboratorio Analisi Qualitativa Elementare di Sostanze Inorganiche (Via Umida) Ricerca dei Cationi Calcio, magnesio Ricerca degli
24. PRECIPITAZIONE Prodotto di solubilità (K s )
 24. PRECIPITAZIONE D. In un racconto di Primo Levi, a proposito di un analisi chimica di campioni di roccia, si incontrano queste parole apparentemente prive di senso: «... giù il ferro con ammoniaca,
24. PRECIPITAZIONE D. In un racconto di Primo Levi, a proposito di un analisi chimica di campioni di roccia, si incontrano queste parole apparentemente prive di senso: «... giù il ferro con ammoniaca,
RICERCA DEGLI ANIONI
 RICERCA DEGLI ANIONI RICERCA DEGLI ANIONI SOSTANZA INIZIALE via secca via umida (soluzione alcalina) Ricerca: ACETATI CARBONATI TARTRATI SOLFITI SOLUZIONE Limpida Incolore RESIDUO Si scarta Ricerca: CLORURI
RICERCA DEGLI ANIONI RICERCA DEGLI ANIONI SOSTANZA INIZIALE via secca via umida (soluzione alcalina) Ricerca: ACETATI CARBONATI TARTRATI SOLFITI SOLUZIONE Limpida Incolore RESIDUO Si scarta Ricerca: CLORURI
PRIMA ESPERIENZA DI LABORATORIO. Prof. Antonio Lavecchia
 PRIMA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Prima Esperienza di Laboratorio Analisi Qualitativa Elementare di Sostanze Inorganiche (Via Umida e Via Secca) Ricerca dei Cationi Calcio, Magnesio,
PRIMA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Prima Esperienza di Laboratorio Analisi Qualitativa Elementare di Sostanze Inorganiche (Via Umida e Via Secca) Ricerca dei Cationi Calcio, Magnesio,
SPETTROSCOPIA DI ASSORBIMENTO ATOMICO
 SPETTROSCOPIA DI ASSORBIMENTO ATOMICO L applicazione della spettroscopia UV-Vis ai singoli atomi piuttosto che alle molecole complesse è detta Spettroscopia di Assorbimento Atomico. L assorbimento di un
SPETTROSCOPIA DI ASSORBIMENTO ATOMICO L applicazione della spettroscopia UV-Vis ai singoli atomi piuttosto che alle molecole complesse è detta Spettroscopia di Assorbimento Atomico. L assorbimento di un
ANALISI DELLE SOSTANZE INORGANICHE DI IMPIEGO FARMACEUTICO E BUONE PRASSI IN LABORATORIO M - Z
 DIPARTIMENTO DI SCIENZE DEL FARMACO Corso di laurea magistrale in Farmacia Anno accademico 2018/2019-2 anno ANALISI DELLE SOSTANZE INORGANICHE DI IMPIEGO FARMACEUTICO E BUONE PRASSI IN LABORATORIO M -
DIPARTIMENTO DI SCIENZE DEL FARMACO Corso di laurea magistrale in Farmacia Anno accademico 2018/2019-2 anno ANALISI DELLE SOSTANZE INORGANICHE DI IMPIEGO FARMACEUTICO E BUONE PRASSI IN LABORATORIO M -
SPETTROMETRIA DI ASSORBIMENTO ATOMICO
 SPETTROMETRIA DI ASSORBIMENTO ATOMICO E una metodica spettroscopica atta alla determinazione qualiquantitativa di metalli. E basata sull assorbimento di radiazioni elettromagnetiche da parte di atomi nell
SPETTROMETRIA DI ASSORBIMENTO ATOMICO E una metodica spettroscopica atta alla determinazione qualiquantitativa di metalli. E basata sull assorbimento di radiazioni elettromagnetiche da parte di atomi nell
a. Cromatografia su colonna; b. Cromatografia su lastra sottile (TLC); c. High Pressure Liquid Cromatography (HPLC); d. Gas-Cromatografia (GC).
 Tecniche analitiche per l analisi di matrici ambientali Dr. Chiara Ponzoni Dr. Maria Cannio Tecniche Spettroscopiche: a. Spettrometria UV-Visibile (UV-Vis); b. Spettrometria IR (IR); c. Spettrometria di
Tecniche analitiche per l analisi di matrici ambientali Dr. Chiara Ponzoni Dr. Maria Cannio Tecniche Spettroscopiche: a. Spettrometria UV-Visibile (UV-Vis); b. Spettrometria IR (IR); c. Spettrometria di
FLUIDO MAGNETICO Sintesi del Ferrofluido
 Università degli Studi di Genova Dipartimento di chimica e chimica industriale Progetto Lauree Scientifiche Laboratori Regionali 2009-2010 Scienza dei Materiali FLUIDO MAGNETICO Sintesi del Ferrofluido
Università degli Studi di Genova Dipartimento di chimica e chimica industriale Progetto Lauree Scientifiche Laboratori Regionali 2009-2010 Scienza dei Materiali FLUIDO MAGNETICO Sintesi del Ferrofluido
9065X Chimica. Modello esame svolto. Esempio di compito scritto di Chimica. Politecnico di Torino CeTeM
 svolto Esempio di compito scritto di Chimica 1 - La configurazione elettronica: [Ar]3d 6 4s 0 rappresenta lo ione: 1) Mn 2+ 2) Ni 2+ 3) Fe 3+ 4) Co 3+ 5) Cu 2+ 2 - Un gas reale mantenuto sempre al di sopra
svolto Esempio di compito scritto di Chimica 1 - La configurazione elettronica: [Ar]3d 6 4s 0 rappresenta lo ione: 1) Mn 2+ 2) Ni 2+ 3) Fe 3+ 4) Co 3+ 5) Cu 2+ 2 - Un gas reale mantenuto sempre al di sopra
DAI MISCUGLI ALLE SOSTANZE PURE
 Come si presenta la materia? DAI MISCUGLI ALLE SOSTANZE PURE Il criterio per distinguere i materiali è la presenza di una o più FASI porzioni di materia fisicamente distinte tra loro delimitate da nette
Come si presenta la materia? DAI MISCUGLI ALLE SOSTANZE PURE Il criterio per distinguere i materiali è la presenza di una o più FASI porzioni di materia fisicamente distinte tra loro delimitate da nette
SOLUZIONI e DILUIZIONI
 SOLUZIONI e DILUIZIONI Introduzione In chimica viene definita soluzione un sistema in cui due o più sostanze formano un miscuglio omogeneo. Nella maggior parte dei casi una soluzione è costituita da due
SOLUZIONI e DILUIZIONI Introduzione In chimica viene definita soluzione un sistema in cui due o più sostanze formano un miscuglio omogeneo. Nella maggior parte dei casi una soluzione è costituita da due
Esercitazione 3. Tipi di soluzioni. Cristallizzazione. Ricristallizzazione. Preparazione del nitrato di potassio
 Esercitazione 3 Preparazione del nitrato di potassio Tipi di soluzioni!la sostanza che si scioglie è detta SOLUTO!La sostanza che scioglie è detta SOLVENTE Soluzione non satura: soluzione che contiene
Esercitazione 3 Preparazione del nitrato di potassio Tipi di soluzioni!la sostanza che si scioglie è detta SOLUTO!La sostanza che scioglie è detta SOLVENTE Soluzione non satura: soluzione che contiene
CHIMICA ANALITICA II con LABORATORIO 4. GRAVIMETRIA
 CHIMICA ANALITICA II con LABORATORIO 4. GRAVIMETRIA Federico Marini Dept. Chemistry, University of Rome La Sapienza, Rome, Italy Gravimetria Consiste nell isolare e pesare un elemento o un composto dell
CHIMICA ANALITICA II con LABORATORIO 4. GRAVIMETRIA Federico Marini Dept. Chemistry, University of Rome La Sapienza, Rome, Italy Gravimetria Consiste nell isolare e pesare un elemento o un composto dell
Solubilità dei sali Prodotto di solubilità
 Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
SOLUBILITA EQUILIBRI ETEROGENEI
 SOLUBILITA EQUILIBRI ETEROGENEI Cosa succede quando si scioglie un sale (NaCl) in acqua Cl - LEGAME IONE DIPOLO Se sciogliamo in un solvente polare (tipo H 2 O) una sostanza ionica(tipo NaCl) questa si
SOLUBILITA EQUILIBRI ETEROGENEI Cosa succede quando si scioglie un sale (NaCl) in acqua Cl - LEGAME IONE DIPOLO Se sciogliamo in un solvente polare (tipo H 2 O) una sostanza ionica(tipo NaCl) questa si
Gli equilibri di solubilità
 Gli equilibri di solubilità Abbiamo definito la solubilità come la concentrazione della soluzione satura, che è una soluzione il cui il composto in soluzione è in equilibrio con il composto indisciolto.
Gli equilibri di solubilità Abbiamo definito la solubilità come la concentrazione della soluzione satura, che è una soluzione il cui il composto in soluzione è in equilibrio con il composto indisciolto.
Prima esperienza di Laboratorio. Alcune reazioni del rame
 Prima esperienza di Laboratorio Alcune reazioni del rame Prelevare 20 cm 3 di soluzione di solfato di rame pentaidrato (CuSO 4 5H 2 O) e versarli in una provetta Da questa riserva di rame, preleverete
Prima esperienza di Laboratorio Alcune reazioni del rame Prelevare 20 cm 3 di soluzione di solfato di rame pentaidrato (CuSO 4 5H 2 O) e versarli in una provetta Da questa riserva di rame, preleverete
Progetto ALCHIMIA. Saggi alla fiamma
 Saggi alla fiamma Scaldati sulla fiamma, alcuni elementi chimici emettono luce di colore caratteristico. L energia fornita dalla fiamma viene, infatti, restituita sotto forma di fotoni di lunghezza d onda
Saggi alla fiamma Scaldati sulla fiamma, alcuni elementi chimici emettono luce di colore caratteristico. L energia fornita dalla fiamma viene, infatti, restituita sotto forma di fotoni di lunghezza d onda
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2015/2016 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2015/2016 Dott. Giuseppe La Regina Tu,
Corso di laurea in Chimica e Tecnologia Farmaceutiche Corso di Chimica Generale e Inorganica CH 3
 Corso di laurea in Chimica e Tecnologia Farmaceutiche Corso di Chimica Generale e Inorganica - LA MATERIA- COOH O O Al(OH) 4 - CH 3 Prof.ssa Ivana Fenoglio I lucidi forniti non sono da utilizzare come
Corso di laurea in Chimica e Tecnologia Farmaceutiche Corso di Chimica Generale e Inorganica - LA MATERIA- COOH O O Al(OH) 4 - CH 3 Prof.ssa Ivana Fenoglio I lucidi forniti non sono da utilizzare come
Utilizzeremo un kit analitico per valutare la qualità dell acqua potabile delle nostre case, scuole e fontanelle cittadine.
 Acqua in brocca Ciao! Io sono LABBY e vi farò da guida per l analisi dell acqua del vostro rubinetto! Utilizzeremo un kit analitico per valutare la qualità dell acqua potabile delle nostre case, scuole
Acqua in brocca Ciao! Io sono LABBY e vi farò da guida per l analisi dell acqua del vostro rubinetto! Utilizzeremo un kit analitico per valutare la qualità dell acqua potabile delle nostre case, scuole
Amministrazione, finanza e marketing - Turismo Ministero dell Istruzione, dell Università e della Ricerca PROGRAMMAZIONE DISCIPLINARE PER U. di A.
 MATERIA CHIMICA CLASSE 2 INDIRIZZO AFM / TUR DESCRIZIONE Unità di Apprendimento UdA n. 1 Titolo: LA MATERIA Aver acquisito la capacità di osservare, descrivere ed analizzare i fenomeni legati alle trasformazioni
MATERIA CHIMICA CLASSE 2 INDIRIZZO AFM / TUR DESCRIZIONE Unità di Apprendimento UdA n. 1 Titolo: LA MATERIA Aver acquisito la capacità di osservare, descrivere ed analizzare i fenomeni legati alle trasformazioni
2 Congresso Nazionale Il colore nelle sue sfumature
 2 Congresso Nazionale Il colore nelle sue sfumature Colore e scienza: l uso del colore nella scienza e nella tecnica ing. Luca Derosa Presidente Associazione Culturale Micene Imex.A Consultants POSSIBILI
2 Congresso Nazionale Il colore nelle sue sfumature Colore e scienza: l uso del colore nella scienza e nella tecnica ing. Luca Derosa Presidente Associazione Culturale Micene Imex.A Consultants POSSIBILI
TECNICHE SPETTROSCOPICHE
 TECNICHE SPETTROSCOPICHE L interazione delle radiazioni elettromagnetiche con la materia e essenzialmente un fenomeno quantico, che dipende sia dalle proprieta della radiazione sia dalla natura della materia
TECNICHE SPETTROSCOPICHE L interazione delle radiazioni elettromagnetiche con la materia e essenzialmente un fenomeno quantico, che dipende sia dalle proprieta della radiazione sia dalla natura della materia
Corso di Studi di Fisica Corso di Chimica
 Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Lezione 29-30 2010 Programma: a che punto siamo? Elettrochimica Elettrochimica è lo studio delle reazioni chimiche che producono
Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Lezione 29-30 2010 Programma: a che punto siamo? Elettrochimica Elettrochimica è lo studio delle reazioni chimiche che producono
Analisi chimiche per i beni culturali
 Analisi chimiche per i beni culturali Nicola Ludwig ricevimento: in via Noto giovedì dopo lezione Nicola.Ludwig@unimi.it Istituto di Fisica Generale Applicata, via Celoria 16 Programma L obiettivo del
Analisi chimiche per i beni culturali Nicola Ludwig ricevimento: in via Noto giovedì dopo lezione Nicola.Ludwig@unimi.it Istituto di Fisica Generale Applicata, via Celoria 16 Programma L obiettivo del
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Riconoscimento sostanza incognita FU
 1. Sostanza organica Riconoscimento sostanza incognita FU Determinazione p.f. Seguire procedura determinazione p.f. di una sostanza a p.f. ignoto Determinazione del punto di fusione di una sostanza a p.f.
1. Sostanza organica Riconoscimento sostanza incognita FU Determinazione p.f. Seguire procedura determinazione p.f. di una sostanza a p.f. ignoto Determinazione del punto di fusione di una sostanza a p.f.
Energia elettrica. L atomo nel suo complesso è neutro perché ha l equilibrio tra protoni ed elettroni presenti nello stesso numero.
 Energia elettrica Si fonda sulla costituzione dell atomo che è costituito da particelle più piccole : neutroni (carica neutra) e protoni (carica +) che costituiscono il nucleo ed elettroni (carica negativa)
Energia elettrica Si fonda sulla costituzione dell atomo che è costituito da particelle più piccole : neutroni (carica neutra) e protoni (carica +) che costituiscono il nucleo ed elettroni (carica negativa)
METODI GRAVIMETRICI DI ANALISI
 METODI GRAVIMETRICI DI ANALISI I metodi gravimetrici si basano sulla misura della massa e sono sostanzialmente di due tipi: - nei metodi di precipitazione l analita viene trasformato in un precipitato
METODI GRAVIMETRICI DI ANALISI I metodi gravimetrici si basano sulla misura della massa e sono sostanzialmente di due tipi: - nei metodi di precipitazione l analita viene trasformato in un precipitato
Soluzioni Acido Base Definizione di Brønsted
 acido + base sale + acqua Soluzioni Acido Base Definizione di Brønsted acido: sostanza capace di donare protoni* HCl + H 2 O Cl + H 3 O + * In soluzione, il protone esiste in forma idratata (H 3 O + )
acido + base sale + acqua Soluzioni Acido Base Definizione di Brønsted acido: sostanza capace di donare protoni* HCl + H 2 O Cl + H 3 O + * In soluzione, il protone esiste in forma idratata (H 3 O + )
CAPITOLO 12 EQUILIBRI ACIDO-BASE E SOLUBILITA
 CAPITOLO 12 EQUILIBRI ACIDO-BASE E SOLUBILITA 12.1 (a) ph = 2,57 (b) ph = 4,44 12.3 (a) no. (b) no. (c) sì. (d) sì. (e) no. 12.5 ph = 8,88 12.7 0,024 12.9 0,58 12.11 ph = 9,25; ph = 9,18. 12.13 Na 2 A/NaHA.
CAPITOLO 12 EQUILIBRI ACIDO-BASE E SOLUBILITA 12.1 (a) ph = 2,57 (b) ph = 4,44 12.3 (a) no. (b) no. (c) sì. (d) sì. (e) no. 12.5 ph = 8,88 12.7 0,024 12.9 0,58 12.11 ph = 9,25; ph = 9,18. 12.13 Na 2 A/NaHA.
CORSO DI CHIMICA PER L AMBIENTE. Lezione del 5 Maggio 2016
 CORSO DI CHIMICA PER L AMBIENTE Lezione del 5 Maggio 2016 Sali Acidi o Basici La neutralità acido-base dell acqua può essere alterata anche dal discioglimento di alcuni sali. Prendiamo ad esempio NH 4
CORSO DI CHIMICA PER L AMBIENTE Lezione del 5 Maggio 2016 Sali Acidi o Basici La neutralità acido-base dell acqua può essere alterata anche dal discioglimento di alcuni sali. Prendiamo ad esempio NH 4
Sapienza Università di Roma Facoltà di Farmacia e Medicina Anno Accademico 2015/2016
 Facoltà di Farmacia e Medicina Anno Accademico 2015/2016 Corso di Laurea in Chimica e Tecnologie Farmaceutiche Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Programma d esame PARTE PRIMA
Facoltà di Farmacia e Medicina Anno Accademico 2015/2016 Corso di Laurea in Chimica e Tecnologie Farmaceutiche Corso di Analisi Chimico Farmaceutica e Tossicologica I (M-Z) Programma d esame PARTE PRIMA
Rapporto tra soluto e solvente o soluzione
 Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
Programma Misure ed Unità di misura. Incertezza della misura. Cifre significative. Notazione scientifica. Atomo e peso atomico. Composti, molecole e ioni. Formula molecolare e peso molecolare. Mole e massa
COMPORTAMENTO DI SALI CONTENENTI PARTICOLARI CATIONI IN SEGUITO A TRATTAMENTO CON COMPLESSANTI, BASI ED ACIDI
 COMPORTAMENTO DI SALI CONTENENTI PARTICOLARI CATIONI IN SEGUITO A TRATTAMENTO CON COMPLESSANTI, BASI ED ACIDI Perché le soluzioni dei cationi metallici di partenza sono acide. Una volta sciolto un sale
COMPORTAMENTO DI SALI CONTENENTI PARTICOLARI CATIONI IN SEGUITO A TRATTAMENTO CON COMPLESSANTI, BASI ED ACIDI Perché le soluzioni dei cationi metallici di partenza sono acide. Una volta sciolto un sale
Atomi, Molecole e Ioni. Capitolo 2
 Atomi, Molecole e Ioni Capitolo 2 La Teoria Atomica di Dalton (1808) 1. Gli Elementi sono composti da particelle estremamente piccole, denominate atomi. 2. Tutti gli atomi di un dato elemento sono identici
Atomi, Molecole e Ioni Capitolo 2 La Teoria Atomica di Dalton (1808) 1. Gli Elementi sono composti da particelle estremamente piccole, denominate atomi. 2. Tutti gli atomi di un dato elemento sono identici
