Spettrofotometria e analisi di amminoacidi
|
|
|
- Mariana Murgia
- 7 anni fa
- Visualizzazioni
Transcript
1 Spettrofotometria e analisi di amminoacidi Quantizzazione di proteine e di miscele di amminoacidi Antimo Di Maro Anno Accademico
2 Assorbimento della luce ONDE ELETTROMAGNETICHE La radiazione elettromagnetica è, dal punto di vista dell'elettromagnetismo classico, un fenomeno ondulatorio dovuto alla contemporanea propagazione di perturbazioni periodiche di un campo elettrico e di un campo magnetico, oscillanti in piani tra di loro ortogonali. E = h = h c/ λ h= costante di Plank E= Energia = Frequenza = numero di onde che passano in punto per unità di tempo λ= Lunghezza d onda (A = Angstrom = m = 0,1 nm; nm = 10-9 m; μm = 10-6 m) 1/λ= λ -1 = Numero d onda c = velocità di propagazione (3 x cm /sec 2 )
3 SPETTRO ELETTROMAGNETICO 700 nm 340 nm Bassa energia (.calore) Alta energia (danneggiano le macromolecole
4
5 FOTOMETRIA L. incidente L. trasmessa Tra 0 e 100% Da 0 ad infinito
6
7
8
9
10 La proprietà di assorbimento della luce UV da parte di Triptofano, Tirosina e Fenilalanina è particolarmente utile per il riconoscimento e la determinazione quantitativa delle proteine mediante l utilizzo dello SPETTROFOTOMETRO
11
12
13 Il massimo dell assorbimento dipende dai gruppi funzionali presenti nelle molecole e da lo SPETTRO DI ASSORBIMENTO
14 ASSORBIMENTO DELLA LUCE ULTRAVIOLETTA DA PARTE DEGLI Aa AROMATICI Il triptofano e la tirosina Assorbono la luce ultravioletta, ciò spiega perché la maggior parte delle proteine hanno un caratteristico assorbimento della luce ad una lunghezza d onda di 280 nm
15 Assorbimento di una proteina Assorbimento di un acido nucleico
16
17 Emoglobina
18
19 L assorbimento di luce ad una qualunque lunghezza d onda può essere messo in relazione con la concentrazione della sostanza assorbente mediante la RELAZIONE DI LAMBERT E BEER A = ε c l A = assorbimento ad una determinata lunghezza d onda; c = concentrazione della sostanza espressa in moli per litro di soluzione; l = lunghezza del cammino ottico espressa in cm; ε = coefficiente di estinzione molare (assorbimento di una soluzione 1M del composto in esame, quando questa è attraversata per 1 cm dalla luce incidente). (dipende da ) Da 0 ad infinito
20 Devo sapere epsilon, che è caratteristica per ogni (macro)molecola Se non conosco epson, posso usare per determinare la concentrazione di una proteina la spettrofotometria ma con una proteina di riferimento a quantità nota, da usare come standard
21 Metodo colorimetrico Coloranti che interagiscono con le proteine e danno una risposta immediata
22 Metodo del biureto. Il metodo del biureto si basa sulla capacità degli ioni Cu +2 di interagire con le proteine e formare dei complessi con l azoto del legame peptidico. Tali complessi producono un colore blu che può essere misurato a 550 nm. Il reattivo del biureto consiste di una soluzione alcalina di solfato di rame (CuSO 4 ). La reazione del biureto è data da tutti i composti che contengono almeno due gruppi peptidici (-CO-NH-) legati fra loro o direttamente, o per mezzo di un atomo di carbonio (peptidi, proteine) o per mezzo di un atomo di azoto, come nel caso del biureto (H 2 N-CO-NH-CO-NH 2 ).
23
24 Con tale metodo gli ione Rame in ambiente basico che interagiscono con i gruppi NH dei legami peptidici che vengono successivamente chelanti dal reattivo
25
26
27
28
29 Come si determina la quantità di una proteina? Se la proteina è pura: 1- Metodo diretto Legge di Lambert e Beer Dalla relazione: A= xlxc si ricava: c=a/( xl) Essendo l noto (dimensioni della cella) si deve disporre del valore di ε relativo alla sostanza in esame, ad una certa lunghezza d onda (280 nm). Quindi, se è noto (da precedenti esperienze o perché tabulato in letteratura) è agevole ottrenere la quantità di una proteina. 2- Se non si conosce oppure siamo in presenza di una miscela di proteine, si può a) far riferimento al dato che 1mg/mL di proteine presentano un assorbanza media di 1 a 280 nm. Se quindi si legge l assorbanza della miscela di proteine, si può avere una dato approssimativo della concentrazione.
30
31 b) si può usare un metodo molto preciso che consiste nell idrolizzare con acidi una porzione di campione e quindi effettuare l analisi amminoacidica sull idrolizzato. Questa è una procedura molto lenta. Non essendo, solitamente, necessaria una precisione così elevata, si utilizzano metodi più rapidi, la maggior parte dei quali sfrutta la colorimetria.
32 METODI COLORIMETRICI PER LA QUANTIFICAZIONE DELLE PROTEINE IL PRINCIPIO: Le proteine presenti nella soluzione reagiscono con un reagente dando luogo ad un prodotto colorato. L intensità del colore sviluppato è correlato con la quantità di proteina. Si fa reagire quantità NOTE di una proteina (es. Albumina da siero bovina- BSA) con il colorante e si ottiene una retta di calibrazione. Poi si fa reagire con lo stesso colorante un volume noto di miscela di proteine e si relazione l assorbanza con la quantità sulla retta di calibrazione. C 1 C 2 Cx C 3 C4 Retta di calibrazione
33 Analisi di amminoacidi Composizione in amminoacidi di proteine e/o alimenti
34 Determinazione della composizione amminoacidica -Sistemi con derivatizzazione post-colonna Cromatografia a scambio ionico e colorazione con ninidrina -Sistemi con derivatizzazione pre-colonna Cromatografia a fase inversa ad alta pressione (RP-HPLC) - 1 fluoro-2,4 dinitrobenzene - dansil cloruro - Isotiocianato - ortoftalaldeide
35 Struttura e ph
36
37 punto isoelettrico, pi ph al quale gli aa presentano carica netta uguale a zero dipende per ogni amminoacido dalla catena laterale per gli aa acidi tale valore è ~ 3 per gli amminoacidi basici ~9. per gli aa neutri varia tra ~ 5 e ~ 6.
38 Determinazione della composizione amminoacidica - Sistemi con derivatizzazione post-colonna Cromatografia a scambio ionico e colorazione con ninidrina - Sistemi con derivatizzazione pre-colonna Cromatografia a fase inversa ad alta pressione (RP- HPLC) - 1 fluoro-2,4 dinitrobenzene - dansil cloruro - Isotiocianato - ortoftalaldeide
39 Cromatografia a scambio ionico in generale Sfrutta la forza d attrazione tra molecole di carica opposta. Le colonne sono impaccate con una matrice su cui si blocca una fase stazionaria carica ( o +). Variando il ph dell eluente o la forza ionica si altera l equilibrio ottenuto e si può provocare il distacco degli analiti. In questa tecnica sono importanti quindi il ph, la forza ionica e la carica del campione. Le migliori separazioni si ottengono con eluizioni a gradiente si forza ionica o con step di ph.
40 Il principio della cromatografia a scambio ionico degli amminoacidi -Resina: Polistirene/divinil benzene - Gruppo carico presente sulla resina: gruppo solfonico: -SO 3 -
41 Il principio della cromatografia a scambio ionico L aggiunta si fa a ph acido, 2,2. TUTTI gli amminoacidi hanno carica positiva e si legano. -Aumento di forza ionica; -Aumento di ph; -Aumento di temperatura. Gli amminoacidi vengono eluiti; Colorati con ninidrina; -Lettura dell assorbimento a 570/420 nm; Integrazione dei picchi; Registrazione; Cromatogramma.
42 La resina + In H 2 SO 4
43 Analizzatore di amminoacidi Separa gli amminoacidi in base alla carica (scambio cationico) e presenta in successione rivelazione post colonna con ninidrina nello spettro del visibile
44
45 Analizzatore di amminoacidi Schema a blocchi Sistema tamponi Ninidrina Colonna a scambio ionico Reattore (a 100/130 C) Registratore Sistema di integrazione Fotometro
46 Ninidrina Gli amminoacidi si colorano in violetto (570 nm); Gli imminoacidi si colorano in giallo (440 nm) Composto di Reuman
47 Determinazione della composizione di aa Separazione dell idrolizzato tramite cromotagrafia a scambio cationico su resina di polivinilbenzene solfonato Rivelazione post colonna con ninidrina [colore violetto a 570 nm, colore giallo a 440 nm per gli imminoacidi (es. prolina)] La quantità degli amminoacidi è proporzionata all assorbimento Comparazione dell idrolizzato con una miscela di aa standard Si rivelano microgrammi di amminoacidi
48
49 -Variazione di forza ionica - Variazione di ph - Variazione di temperatura
50 Dansil cloruro 2,4-dinitro-fluorobenzene (reagente di Sanger) Reagenti per il gruppo N-terminale Fenilisotiocianato ortoftalaldeide
51
52 Fenilisotiocianato
53 Determinazione della composizione di aa proteici Estrazione da matrice delle proteine Idrolisi acida in 6M HCl a 110 C per 24 o per 72 ore (idrolisi del legame peptidico) Separazione dell idrolizzato tramite cromotagrafia Rivelazione post colonna con ninidrina Comparazione dell idrolizzato con una miscela di aa standard La quantità degli amminoacidi è proporzionata all assorbimento
54 Considerazioni Vari protocolli di estrazione Vari procedimenti per preservare amminoacidi che nelle condizioni di idrolisi vanno incontro a degradazione (Ser, Thr, Met ecc) Asparagina e Glutammina si trasformano in ambiente acido negli aa acidi corrispondenti Degradazione del Triptofano
55 Tali analisi possono dare informazioni su: 1. Struttura e caratterizzazione di proteine (composizione in aa); 2. Informazioni sulle caratteristiche di determinati alimenti o tessuti; 3. Qualità proteica per stabilire il valore nutrizionale degli alimenti; 4. Informazioni su cosa succede a prodotti alimentari sottoposti a procedimenti termici (furosina.); 5. ecc
56 Amminoacidi essenziali Treonina (Thr) Lisina (Lys) Valina (Val) Fenilalanina (Phe) Triptofano (Trp) Metionina (Met) Leucina (Leu) Isoleucina (Ile) Istidina * (His)
57 Determinazione della composizione di aa liberi Estrazione dalla matrice degli amminoacidi liberi Separazione dell idrolizzato tramite cromotagrafia Rivelazione post colonna con ninidrina Comparazione dell idrolizzato con una miscela di aa standard La quantità degli amminoacidi è proporzionata all assorbimento
58 Profilo cromatografico di una separazione di aa fisiologici utilizzando Litio Citrato
59 Considerazioni Estrazione Non vi è l idrolisi per liberare gli amminoacidi proteici Asparagina e Glutammina e molti amminoacidi rari o non presenti in proteine sono rilevabili Utilizzo di un analizzatore di amminoacidi per separazione di amminoacidi fisiologici (usa Litio Citrato..)
60 Fenilchetonuria Gli alimenti presentano la maggior parte degli amminoacidi, tra cui è presente la fenilalanina. Tale amminoacido viene in parte utilizzato metabolicamente dopo che l organismo la trasforma in tirosina Nei pazienti con tale patologia non vi è questa via metabolica e si ha accumulo di Phe. Vanno eliminate dalla dieta pietanze ricche in Phe
61
62 Tali analisi possono dare informazioni su: 1.Presenza di amminoacidi modificati 2.Problemi di metabolismo alimentare o di vie metaboliche (disfunzioni..) 3.Qualità alimentare 4.Studi di sistematica molecolare 5.ecc
63 Un altro aspetto importante da considerare per la corretta interpretazione delle analisi amminoacidiche è lo standard interno. Standard interno: sostanza (nor-leucina) con caratteristiche chimico-fisiche simili agli analiti (aa) da separare. Viene aggiunto all inizio del processo di estrazione e subisce gli stessi trattamenti degli amminoacidi. Mediante lo Standard interno, in aggiunta alle informazioni qualitative dei campioni si possono fare analisi quantitative corrette, ottenendo informazioni sulla resa del processo di estrazione, idrolisi ecc nor Leucine
64 Valore nutrizionale delle proteine: La qualità proteica Composizione ideale in aa essenziali di una proteina alimenare secondo vari autori (mg/g di proteina) Amminoacido MIT* Millward** FAO/WHO/UNU*** FNB/IOM**** Istidina Isoleucina Leucina Lisina Metionina cisteina Fenilalanina tirosina Treonina Triptofano Valina * Young e Pellet, 1990 ** Millward et al., 1990 *** FAO/WHO/UNU, 1995 **** Food and Nutrition Board, 2002 Analizzando l amminoacido limitante in riferimento ai valori in Tabella si ritrova il Punteggio chimico, sihacento per una proteina ideale contenente la quantità di aa in Tabella
65 Le proteine del grano hanno una qualità piuttosto bassa, sia come profilo aminoacidico che come assimilazione. Questo perché il profilo amminoacidico delle proteine del grano è abbastanza diverso da quello delle proteine umane, in particolare è carente di lisina, l'amminoacido limitante delle proteine di tutti i cereali, frumento incluso. Questo, si badi bene, non significa che le proteine del grano non vengono assimilate, ma semplicemente che su 100 g di proteine, ne vengono utilizzate a scopo plastico solo una parte (circa la metà). Le proteine dei cereali possono essere complementate con quelle dei legumi, in proporzione 1:1, ottenendo una proteina di qualità comparabile a quella della carne. Infatti l'aminoacido limitante delle proteine dei legumi è la metionina, di cui al contrario i cereali sono ricchi; e viceversa i legumi sono ricchi di lisina, che come abbiamo visto è carente nei cereali. Per ottenere un pasto 100% vegetale ma ricco di proteine di elevata qualità, basta associare una quantità di legumi e prodotti a base di grano tale per cui il contenuto di proteine dell'uno e dell'altro alimento siano equivalenti.
CHIMICA BIOLOGICA. Seconda Università degli Studi di Napoli. Metodologie 1. DiSTABiF. Corso di Laurea in SCIENZE BIOLOGICHE.
 Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in SCIENZE BIOLOGICHE Insegnamento di CHIMICA BIOLOGICA Anno Accademico 2016-17 Metodologie 1 Spettrofotometria e analisi di amminoacidi
Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in SCIENZE BIOLOGICHE Insegnamento di CHIMICA BIOLOGICA Anno Accademico 2016-17 Metodologie 1 Spettrofotometria e analisi di amminoacidi
Spettrofotometria e analisi di amminoacidi. Quantizzazione di proteine e di miscele di amminoacidi
 Spettrofotometria e analisi di amminoacidi Quantizzazione di proteine e di miscele di amminoacidi Assorbimento della luce ONDE ELETTROMAGNETICHE La radiazione elettromagnetica è, dal punto di vista dell'elettromagnetismo
Spettrofotometria e analisi di amminoacidi Quantizzazione di proteine e di miscele di amminoacidi Assorbimento della luce ONDE ELETTROMAGNETICHE La radiazione elettromagnetica è, dal punto di vista dell'elettromagnetismo
Analisi quantitative
 Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
CHIMICA BIOLOGICA. Seconda Università degli Studi di Napoli. DiSTABiF. Antimo Di Maro. Lezione 3. Corso di Laurea in Scienze Biologiche
 Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Antimo Di Maro Anno Accademico 2016-2017 Lezione 3 GLI AMMINOACIDI PROTEICI Le
Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Antimo Di Maro Anno Accademico 2016-2017 Lezione 3 GLI AMMINOACIDI PROTEICI Le
Analisi quantitative
 Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Cosa determina l assorbanza di un cromoforo?
 Cosa determina l assorbanza di un cromoforo? I cromofori sono di solito caratterizzati da doppi legami e sistemi di risonanza Lo spettro di assorbimento di un cromoforo è solo parzialmente determinato
Cosa determina l assorbanza di un cromoforo? I cromofori sono di solito caratterizzati da doppi legami e sistemi di risonanza Lo spettro di assorbimento di un cromoforo è solo parzialmente determinato
Struttura degli amminoacidi
 AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
La Spettroscopia in Biologia
 La Spettroscopia in Biologia Linda Avesani Dip. Scientifico e Tecnologico Università di Verona Spettroscopia e Proprietà della luce La spettroscopia in biologia studia la struttura e la dinamica delle
La Spettroscopia in Biologia Linda Avesani Dip. Scientifico e Tecnologico Università di Verona Spettroscopia e Proprietà della luce La spettroscopia in biologia studia la struttura e la dinamica delle
La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa.
 La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa. Le cellule contengono 4 famiglie principali di piccole molecole organiche: Amminoacidi
La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa. Le cellule contengono 4 famiglie principali di piccole molecole organiche: Amminoacidi
PROTIDI: LE PROTEINE E GLI AMMINOACIDI
 PROTIDI: LE PROTEINE E GLI AMMINOACIDI GLI AMMINOACIDI Struttura generica di un amminoacido. R rappresenta un gruppo laterale specifico di ogni amminoacido. In chimica, gli amminoacidi (impropriamente
PROTIDI: LE PROTEINE E GLI AMMINOACIDI GLI AMMINOACIDI Struttura generica di un amminoacido. R rappresenta un gruppo laterale specifico di ogni amminoacido. In chimica, gli amminoacidi (impropriamente
Tra nm Nucleotidi mono-fosfato
 Un estratto proteico può contenere acidi nucleici, nucleotidi Posso verificare la loro presenza mediante la misura di uno spettro di assorbimento. Gli acidi nucleici e i nucleotidi assorbono nell UV, grazie
Un estratto proteico può contenere acidi nucleici, nucleotidi Posso verificare la loro presenza mediante la misura di uno spettro di assorbimento. Gli acidi nucleici e i nucleotidi assorbono nell UV, grazie
Amminoacidi. Struttura base di un a-amminoacido
 Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
BIOCHIMICA e BIOTECNOLOGIE degli ALIMENTI
 Corso di Laurea Magistrale in SCIENZE DEGLI ALIMENTI E DELLA NUTRIZIONE UMANA Insegnamento di BIOCHIMICA e BIOTECNOLOGIE degli ALIMENTI Le proteine dovrebbero fornire circa il 12% delle calorie totali.
Corso di Laurea Magistrale in SCIENZE DEGLI ALIMENTI E DELLA NUTRIZIONE UMANA Insegnamento di BIOCHIMICA e BIOTECNOLOGIE degli ALIMENTI Le proteine dovrebbero fornire circa il 12% delle calorie totali.
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH
 Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( OO) nella stessa molecola 3 N 2 α * OO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-himica Organica 1 Amminoacidi
Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( OO) nella stessa molecola 3 N 2 α * OO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-himica Organica 1 Amminoacidi
BIOCHIMICA e BIOTECNOLOGIE degli ALIMENTI
 Seconda Università degli Studi di Napoli DiSTABiF Anno Accademico 2015-16 Corso di Laurea Magistrale in SCIENZE DEGLI ALIMENTI E DELLA NUTRIZIONE UMANA Insegnamento di BIOCHIMICA e BIOTECNOLOGIE degli
Seconda Università degli Studi di Napoli DiSTABiF Anno Accademico 2015-16 Corso di Laurea Magistrale in SCIENZE DEGLI ALIMENTI E DELLA NUTRIZIONE UMANA Insegnamento di BIOCHIMICA e BIOTECNOLOGIE degli
Amminoacidi. Struttura base di un a-amminoacido
 Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH. ) ed un gruppo carbossilico ( COOH) nella stessa molecola
 Amminoacidi (1) Presentano un gruppo amminico ( NH 2 ) ed un gruppo carbossilico ( COOH) nella stessa molecola CH 3 NH 2 C H α * COOH Acido 2-ammino propanoico (acido α-ammino propionico) 1 Amminoacidi
Amminoacidi (1) Presentano un gruppo amminico ( NH 2 ) ed un gruppo carbossilico ( COOH) nella stessa molecola CH 3 NH 2 C H α * COOH Acido 2-ammino propanoico (acido α-ammino propionico) 1 Amminoacidi
α-amminoacidi O α O α R CH C O - NH 3 forma ionizzata sale interno (zwitterione) OH NH 2 forma non ionizzata (non esistente in realtà)
 Amminoacidi 2 forma non ionizzata (non esistente in realtà) 3 forma ionizzata sale interno (zwitterione) In soluzione acquosa c'è equilibrio tra tre forme 3 forma cationica p molto acidi 3 forma zwitterionica
Amminoacidi 2 forma non ionizzata (non esistente in realtà) 3 forma ionizzata sale interno (zwitterione) In soluzione acquosa c'è equilibrio tra tre forme 3 forma cationica p molto acidi 3 forma zwitterionica
Schema a blocchi di uno spettrofluorimetro
 MONOCROMATORE EMISSIONE EM Schema a blocchi di uno spettrofluorimetro MONOCROMATORE ECCITAZIONE SORGENTE EXC RIVELATORE (TUBO FOTOMOLTIPLICATORE) Anche il DNA assorbe nell UV Cosa determina l assorbanza
MONOCROMATORE EMISSIONE EM Schema a blocchi di uno spettrofluorimetro MONOCROMATORE ECCITAZIONE SORGENTE EXC RIVELATORE (TUBO FOTOMOLTIPLICATORE) Anche il DNA assorbe nell UV Cosa determina l assorbanza
Determinazioni quantitative in farmacologia
 Determinazioni quantitative in farmacologia 1 Dosaggio biologico determinazione quantitativa della concentrazione o della potenza di una sostanza per mezzo della valutazione della risposta biologica che
Determinazioni quantitative in farmacologia 1 Dosaggio biologico determinazione quantitativa della concentrazione o della potenza di una sostanza per mezzo della valutazione della risposta biologica che
Dosaggio delle proteine
 Laboratorio Integrato 4 Lezione n.2 Dosaggio delle proteine Dott.ssa Francesca Zazzeroni METODI PER EFFETTUARE UN DOSAGGIO PROTEICO 1-Metodo del Biureto - il reattivo del biureto consiste in una soluzione
Laboratorio Integrato 4 Lezione n.2 Dosaggio delle proteine Dott.ssa Francesca Zazzeroni METODI PER EFFETTUARE UN DOSAGGIO PROTEICO 1-Metodo del Biureto - il reattivo del biureto consiste in una soluzione
1. Cromatografia per gel-filtrazione
 1. Cromatografia per gel-filtrazione La gel filtrazione è un metodo cromatografico che separa le sostanze in base alle loro dimensioni molecolari. I materiali che costituiscono il supporto per la gel-filtrazione
1. Cromatografia per gel-filtrazione La gel filtrazione è un metodo cromatografico che separa le sostanze in base alle loro dimensioni molecolari. I materiali che costituiscono il supporto per la gel-filtrazione
A = εlc c = A/εl c = 0.2/38000 M -1 cm -1 1 cm c = M = 5 μm
 COME PROCEDO? Ho una soluzione di una proteina purificata Preparo un bianco con lo stesso tampone utilizzato per dissolvere la proteina Effettuo l azzeramento dello spettrofotometro con il bianco e poi
COME PROCEDO? Ho una soluzione di una proteina purificata Preparo un bianco con lo stesso tampone utilizzato per dissolvere la proteina Effettuo l azzeramento dello spettrofotometro con il bianco e poi
Analisi delle Proteine
 Analisi delle Proteine Elementi che costituiscono le proteine: idrogeno, carbonio, azoto, ossigeno e zolfo; tra cui l azoto è l elemento più distintivo nei cibi, l azoto varia da 13,4% a 19,1%. L analisi
Analisi delle Proteine Elementi che costituiscono le proteine: idrogeno, carbonio, azoto, ossigeno e zolfo; tra cui l azoto è l elemento più distintivo nei cibi, l azoto varia da 13,4% a 19,1%. L analisi
La struttura covalente delle proteine (la sequenza amminoacidica)
 La struttura covalente delle proteine (la sequenza amminoacidica) Sequenza amminoacidica dell ormone insulina bovino (Frederick Sanger, 1953) Il primo passo per determinare la sequenza di un peptide è
La struttura covalente delle proteine (la sequenza amminoacidica) Sequenza amminoacidica dell ormone insulina bovino (Frederick Sanger, 1953) Il primo passo per determinare la sequenza di un peptide è
CHIMICA Ven 15 novembre 2013 Lezioni di Chimica Fisica
 Laurea triennale in BIOLOGIA A. A. 2013-14 14 CHIMICA Ven 15 novembre 2013 Lezioni di Chimica Fisica Spettroscopia UltraVioletta-Visibile ibile (UV( UV-vis) 2^ parte Fluorescenza e Fosforescenza Prof.
Laurea triennale in BIOLOGIA A. A. 2013-14 14 CHIMICA Ven 15 novembre 2013 Lezioni di Chimica Fisica Spettroscopia UltraVioletta-Visibile ibile (UV( UV-vis) 2^ parte Fluorescenza e Fosforescenza Prof.
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH
 Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( COO) nella stessa molecola C 3 N 2 C α * COO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-Chimica Organica
Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( COO) nella stessa molecola C 3 N 2 C α * COO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-Chimica Organica
AMINOACIDI Struttura. Funzione. Classificazione. Proprietà
 AMINOACIDI Struttura Funzione Classificazione Proprietà 1 STRUTTURA Composti caratterizzati dalla presenza di un gruppo aminico (NH 2 ) e di un gruppo acido (COOH) legati al medesimo carbonio (C). In soluzione
AMINOACIDI Struttura Funzione Classificazione Proprietà 1 STRUTTURA Composti caratterizzati dalla presenza di un gruppo aminico (NH 2 ) e di un gruppo acido (COOH) legati al medesimo carbonio (C). In soluzione
Spettrofotometria. Foto di Clotilde B. Angelucci
 Spettrofotometria Foto di Clotilde B. Angelucci Le radiazioni elettromagnetiche e lo spettro Una radiazione elettromagnetica è caratterizzata dalla sua frequenza (ν) o dalla sua lunghezza d onda (λ). Queste
Spettrofotometria Foto di Clotilde B. Angelucci Le radiazioni elettromagnetiche e lo spettro Una radiazione elettromagnetica è caratterizzata dalla sua frequenza (ν) o dalla sua lunghezza d onda (λ). Queste
Spettroscopia molecolare: interazioni luce-materia
 Spettroscopia molecolare: interazioni luce-materia Nella spettroscopia molecolare il campione è irradiato con luce avente λ nell UV, nel visibile o nell infrarosso. Le molecole di cui è costituito il campione
Spettroscopia molecolare: interazioni luce-materia Nella spettroscopia molecolare il campione è irradiato con luce avente λ nell UV, nel visibile o nell infrarosso. Le molecole di cui è costituito il campione
Analisi spettrofotometrica dell Albumina di siero bovino: applicazione della legge di Lambert-Beer:
 Analisi spettrofotometrica dell Albumina di siero bovino: applicazione della legge di Lambert-Beer: Introduzione: La spettrofotometria o fotometria è una tecnica analitica che sfrutta il fenomeno dell'assorbimento
Analisi spettrofotometrica dell Albumina di siero bovino: applicazione della legge di Lambert-Beer: Introduzione: La spettrofotometria o fotometria è una tecnica analitica che sfrutta il fenomeno dell'assorbimento
Caratteristiche generali
 AMMINOACIDI Gli amminoacidi sono le unità costruttive (building blocks) delle proteine. Come dice il termine, gli amminoacidi naturali sono costituiti da un gruppo amminico (-NH 2 ) e da un gruppo carbossilico
AMMINOACIDI Gli amminoacidi sono le unità costruttive (building blocks) delle proteine. Come dice il termine, gli amminoacidi naturali sono costituiti da un gruppo amminico (-NH 2 ) e da un gruppo carbossilico
Metodi di studio delle proteine :
 Metodi di studio delle proteine : determinazione della quantità determinazione della struttura primaria (sequenza a.a.) determinazione della struttura 3D determinazione del peso molecolare Spettrofotometro
Metodi di studio delle proteine : determinazione della quantità determinazione della struttura primaria (sequenza a.a.) determinazione della struttura 3D determinazione del peso molecolare Spettrofotometro
AMMINO ACIDI. L equilibrio è regolato dal ph
 AMMINO ACIDI AMMINO ACIDI Amminoacido: un composto difunzionale che contiene nell ambito della stessa molecola una funzione amminica -NH 2 e una funzione carbossilica -COOH α-ammino acido: I due gruppi
AMMINO ACIDI AMMINO ACIDI Amminoacido: un composto difunzionale che contiene nell ambito della stessa molecola una funzione amminica -NH 2 e una funzione carbossilica -COOH α-ammino acido: I due gruppi
O (PM:266,45), resina Dowex AG50W-X2, acido perclorico 65%.
 Parte sperimentale Reagenti CrCl 3 x 6H 2 O (PM:266,45), resina Dowex AG50W-X2, acido perclorico 65%. Procedura sperimentale Preparazione delle soluzioni eluenti Preparare le seguenti soluzioni madre di
Parte sperimentale Reagenti CrCl 3 x 6H 2 O (PM:266,45), resina Dowex AG50W-X2, acido perclorico 65%. Procedura sperimentale Preparazione delle soluzioni eluenti Preparare le seguenti soluzioni madre di
Spettroscopia nell ultravioletto e nel visibile
 Spettroscopia nell ultravioletto e nel visibile Sono le regioni dello spettro elettromagnetico maggiormente utilizzate nelle ricerche in campo biomedico Le radiazioni elettromagnetiche e lo spettro Una
Spettroscopia nell ultravioletto e nel visibile Sono le regioni dello spettro elettromagnetico maggiormente utilizzate nelle ricerche in campo biomedico Le radiazioni elettromagnetiche e lo spettro Una
sono le unità monomeriche che costituiscono le proteine hanno tutti una struttura comune
 AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
Tecniche spettrofotometriche e cromatografiche
 Tecniche spettrofotometriche e cromatografiche Biochimica e biotecnologie degli alimenti Lezione 3 Tecniche spettroscopiche Le radiazioni elettromagnetiche vengono rappresentate sia come un'onda elettromagnetica
Tecniche spettrofotometriche e cromatografiche Biochimica e biotecnologie degli alimenti Lezione 3 Tecniche spettroscopiche Le radiazioni elettromagnetiche vengono rappresentate sia come un'onda elettromagnetica
LEZIONE DEL 16/03/2017 Prosieguo sugli amminoacidi Tre amminoacidi con gruppo laterale basico Lisina (Lys, K) Arginina (Arg, R) Istidina (His, H)
 LEZIONE DEL 16/03/2017 Prosieguo sugli amminoacidi Tre amminoacidi con gruppo laterale basico Lisina (Lys, K) Ovviamente carica nel gruppo carbossile, amminico implicati in eventuali legami peptidici,
LEZIONE DEL 16/03/2017 Prosieguo sugli amminoacidi Tre amminoacidi con gruppo laterale basico Lisina (Lys, K) Ovviamente carica nel gruppo carbossile, amminico implicati in eventuali legami peptidici,
Prof. Fulvio Ursini Dipartimento di Chimica Biologica (Vallisneri IV piano Nord) Viale G. Colombo, Padova. Tel.
 Prof. Fulvio Ursini Dipartimento di Chimica Biologica (Vallisneri IV piano Nord) Viale G. Colombo, 3-35121 Padova. Tel.:+39-049-8276104 Fax.:+39-049-8073310 E-mail: fulvio.ursini@unipd.it Funzioni delle
Prof. Fulvio Ursini Dipartimento di Chimica Biologica (Vallisneri IV piano Nord) Viale G. Colombo, 3-35121 Padova. Tel.:+39-049-8276104 Fax.:+39-049-8073310 E-mail: fulvio.ursini@unipd.it Funzioni delle
SPETTROFOTOMETRIA UV/VIS
 SPETTROFOTOMETRIA UV/VIS TECNICHE SPETTROSCOPICHE Le tecniche spettroscopiche sono tutte quelle tecniche basate sull interazione tra la materia e le radiazioni elettromagnetiche. La luce, il calore ed
SPETTROFOTOMETRIA UV/VIS TECNICHE SPETTROSCOPICHE Le tecniche spettroscopiche sono tutte quelle tecniche basate sull interazione tra la materia e le radiazioni elettromagnetiche. La luce, il calore ed
La spettrofotometria è una tecnica analitica, qualitativa e quantitativa e permette il riconoscimento e la quantizzazione di una sostanza in base al
 SPETTROFOTOMETRIA Tecnica che si basa sulla misura diretta dell intensitàdi colorecioènel potere da parte di una data soluzione di assorbire della luce in una regione specifica dello spettro. La spettrofotometria
SPETTROFOTOMETRIA Tecnica che si basa sulla misura diretta dell intensitàdi colorecioènel potere da parte di una data soluzione di assorbire della luce in una regione specifica dello spettro. La spettrofotometria
IL MATERIALE CONTENUTO IN QUESTE DIAPOSITIVE E AD ESCLUSIVO USO DIDATTICO PER L UNIVERSITA DI TERAMO
 IL MATERIALE CONTENUTO IN QUESTE DIAPOSITIVE E AD ESCLUSIVO USO DIDATTICO PER L UNIVERSITA DI TERAMO LE IMMAGINE CONTENUTE SONO SCARICATE DAI SITI WEB DI CUI SONO RIPORTATI I LINK METODOLOGIE BIOCHIMICHE
IL MATERIALE CONTENUTO IN QUESTE DIAPOSITIVE E AD ESCLUSIVO USO DIDATTICO PER L UNIVERSITA DI TERAMO LE IMMAGINE CONTENUTE SONO SCARICATE DAI SITI WEB DI CUI SONO RIPORTATI I LINK METODOLOGIE BIOCHIMICHE
TECNICHE DI SEPARAZIONE DELLE PROTEINE Le proteine sono purificate con procedure di frazionamento
 TECNICHE DI SEPARAZIONE DELLE PROTEINE Le proteine sono purificate con procedure di frazionamento Eliminazione selettiva di tutti gli altri componenti della miscela alla fine resta soltanto la sostanza
TECNICHE DI SEPARAZIONE DELLE PROTEINE Le proteine sono purificate con procedure di frazionamento Eliminazione selettiva di tutti gli altri componenti della miscela alla fine resta soltanto la sostanza
- determinazione colorimetrica della concentrazione di una miscela proteica
 CORSO DI LAUREA IN BIOLOGIA GENERALE E APPLICATA Anno Accademico 2013/2014 Laboratorio di Chimica Biologica - Cromatografia a scambio ionico - determinazione colorimetrica della concentrazione di una miscela
CORSO DI LAUREA IN BIOLOGIA GENERALE E APPLICATA Anno Accademico 2013/2014 Laboratorio di Chimica Biologica - Cromatografia a scambio ionico - determinazione colorimetrica della concentrazione di una miscela
TECNICHE CROMATOGRAFICHE
 TECNICHE CROMATOGRAFICHE Le tecniche cromatografiche permettono di separare gli analiti presenti in una miscela complessa. Tutti i sistemi cromatografici sono costituiti da una fase stazionaria, che puo
TECNICHE CROMATOGRAFICHE Le tecniche cromatografiche permettono di separare gli analiti presenti in una miscela complessa. Tutti i sistemi cromatografici sono costituiti da una fase stazionaria, che puo
DOSAGGIO ACIDI NUCLEICI
 DOSAGGIO ACIDI NUCLEICI l Cuvetta contenente il campione di proteina a concentrazione C Sorgente I 0 I 1 I 0 Rivelatore Quando si fa passare una luce di una particolare lunghezza d onda d
DOSAGGIO ACIDI NUCLEICI l Cuvetta contenente il campione di proteina a concentrazione C Sorgente I 0 I 1 I 0 Rivelatore Quando si fa passare una luce di una particolare lunghezza d onda d
- determinazione colorimetrica della concentrazione di una miscela proteica. - Determinazione spettrofotometrica dell attività enzimatica
 CORSO DI LAUREA IN BIOLOGIA GENERALE E APPLICATA Anno Accademico 2012/2013 Laboratorio di Chimica Biologica - Cromatografia a scambio ionico - determinazione colorimetrica della concentrazione di una miscela
CORSO DI LAUREA IN BIOLOGIA GENERALE E APPLICATA Anno Accademico 2012/2013 Laboratorio di Chimica Biologica - Cromatografia a scambio ionico - determinazione colorimetrica della concentrazione di una miscela
Vittoria Patti MACROMOLECOLE BIOLOGICHE. 4. proteine
 Vittoria Patti MACROMOLECOLE BIOLOGICHE 4. proteine 1 Funzioni principali delle proteine funzione cosa significa esempi ENZIMATICA STRUTTURALE TRASPORTO MOVIMENTO DIFESA IMMUNITARIA ORMONALE catalizzare
Vittoria Patti MACROMOLECOLE BIOLOGICHE 4. proteine 1 Funzioni principali delle proteine funzione cosa significa esempi ENZIMATICA STRUTTURALE TRASPORTO MOVIMENTO DIFESA IMMUNITARIA ORMONALE catalizzare
Proteine strutturali Sostegno meccanico Cheratina: costituisce i capelli Collagene: costituisce le cartilagini Proteine di immagazzinamento
 Tipo Funzione Esempi Enzimi Accelerano le reazioni chimiche Saccarasi: posiziona il saccarosio in modo che possa essere scisso nelle due unità di glucosio e fruttosio che lo formano Ormoni Messaggeri chimici
Tipo Funzione Esempi Enzimi Accelerano le reazioni chimiche Saccarasi: posiziona il saccarosio in modo che possa essere scisso nelle due unità di glucosio e fruttosio che lo formano Ormoni Messaggeri chimici
Spettroscopia di assorbimento UV-Vis
 Spettroscopia di assorbimento UV-Vis Metodi spettroscopici La spettroscopia studia i fenomeni alla base delle interazioni della radiazione con la materia Le tecniche spettroscopiche sono tutte quelle tecniche
Spettroscopia di assorbimento UV-Vis Metodi spettroscopici La spettroscopia studia i fenomeni alla base delle interazioni della radiazione con la materia Le tecniche spettroscopiche sono tutte quelle tecniche
Fondamenti di spettroscopia. Spettrofotometria UV/Vis (Tecnica analitica)
 Fondamenti di spettroscopia Spettrofotometria UV/Vis (Tecnica analitica) Spettroscopia Definizione: Lo studio della struttura e della dinamica della materia (in biologia delle molecole) attraverso l analisi
Fondamenti di spettroscopia Spettrofotometria UV/Vis (Tecnica analitica) Spettroscopia Definizione: Lo studio della struttura e della dinamica della materia (in biologia delle molecole) attraverso l analisi
S P E T T R O S C O P I A. Dispense di Chimica Fisica per Biotecnologie Dr.ssa Rosa Terracciano
 S P E T T R O S C O P I A SPETTROSCOPIA I PARTE Cenni generali di spettroscopia: La radiazione elettromagnetica e i parametri che la caratterizzano Le regioni dello spettro elettromagnetico Interazioni
S P E T T R O S C O P I A SPETTROSCOPIA I PARTE Cenni generali di spettroscopia: La radiazione elettromagnetica e i parametri che la caratterizzano Le regioni dello spettro elettromagnetico Interazioni
- determinazione colorimetrica della concentrazione di una miscela proteica
 CORSO DI LAUREA IN BIOLOGIA GENERALE E APPLICATA Anno Accademico 2017/2018 Laboratorio di Chimica Biologica - Cromatografia a scambio ionico - determinazione colorimetrica della concentrazione di una miscela
CORSO DI LAUREA IN BIOLOGIA GENERALE E APPLICATA Anno Accademico 2017/2018 Laboratorio di Chimica Biologica - Cromatografia a scambio ionico - determinazione colorimetrica della concentrazione di una miscela
LE PROTEINE. SONO Polimeri formati dall unione di AMMINOACIDI (AA) Rende diversi i 20 AA l uno dall altro UN ATOMO DI C AL CENTRO
 LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
ε 340 nm A 260 nm A 260nm = 1.36 A 340 nm = A 340nm A = c [NADH] = : 6.22 x 10 3 = x 10-6 M
![ε 340 nm A 260 nm A 260nm = 1.36 A 340 nm = A 340nm A = c [NADH] = : 6.22 x 10 3 = x 10-6 M ε 340 nm A 260 nm A 260nm = 1.36 A 340 nm = A 340nm A = c [NADH] = : 6.22 x 10 3 = x 10-6 M](/thumbs/59/43508258.jpg) ESERCIZI 2 Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione molare a 260 nm sono
ESERCIZI 2 Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione molare a 260 nm sono
Leufelis: una nuova strategia per la malnutrizione nel paziente in D. P.
 PRIMO CORSO DI DIALISI PERITONEALE DEL CADORE Pieve di Cadore, 23-24 Ottobre 2015 Leufelis: una nuova strategia per la malnutrizione nel paziente in D. P. dr Ubaldo Gallo Chimico Nutrizione e Vita Leufelis:
PRIMO CORSO DI DIALISI PERITONEALE DEL CADORE Pieve di Cadore, 23-24 Ottobre 2015 Leufelis: una nuova strategia per la malnutrizione nel paziente in D. P. dr Ubaldo Gallo Chimico Nutrizione e Vita Leufelis:
Somministrazione o assunzione di alimenti allo scopo di nutrire l organismo
 Definizioni Alimentazione Somministrazione o assunzione di alimenti allo scopo di nutrire l organismo Nutrizione complesso di processi biologici che consentono o condizionano la conservazione, l accrescimento,
Definizioni Alimentazione Somministrazione o assunzione di alimenti allo scopo di nutrire l organismo Nutrizione complesso di processi biologici che consentono o condizionano la conservazione, l accrescimento,
LE PROTEINE: POLIMERI COSTITUITI DA 20 TIPI DI MONOMERI, I 20 AMINOACIDI
 LE PROTEINE: POLIMERI OSTITUITI DA 20 TIPI DI MONOMERI, I 20 AMINOAIDI OGNI PROTEINA PUO ESSERE FORMATA DA MOLTE DEINE O ENTINAIA DI AMINOAIDI E SI LEGANO A FORMARE UNA ATENA NON RAMIFIATA La catena di
LE PROTEINE: POLIMERI OSTITUITI DA 20 TIPI DI MONOMERI, I 20 AMINOAIDI OGNI PROTEINA PUO ESSERE FORMATA DA MOLTE DEINE O ENTINAIA DI AMINOAIDI E SI LEGANO A FORMARE UNA ATENA NON RAMIFIATA La catena di
Struttura delle Proteine
 Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
Schemi delle lezioni 1
 Schemi delle lezioni 1 Detti anche proteine sono i composti organici maggiormente presenti nelle cellule, dato che costituiscono circa il 50% del loro peso secco. Nell uomo adulto rappresentano circa
Schemi delle lezioni 1 Detti anche proteine sono i composti organici maggiormente presenti nelle cellule, dato che costituiscono circa il 50% del loro peso secco. Nell uomo adulto rappresentano circa
MACROMOLECOLE. Polimeri (lipidi a parte)
 MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
Quantizzazione del DNA con spettrofotometro
 Quantizzazione del DNA ed elettroforesi 1 Quantizzazione del DNA con spettrofotometro Al termine della metodica di estrazione, occorre quantificare il DNA isolato. Un metodo per quantificare in modo preciso
Quantizzazione del DNA ed elettroforesi 1 Quantizzazione del DNA con spettrofotometro Al termine della metodica di estrazione, occorre quantificare il DNA isolato. Un metodo per quantificare in modo preciso
Soluzioni RAGIONAMENTO LOGICO E CULTURA GENERALE. Risposta. Risposta. Risposta. Risposta. Risposta. Risposta. Risposta. Risposta. Risposta.
 Soluzioni 1 A 2 B 3 B 4 E 5 D 6 E 7 B 8 D 9 C 10 B 11 D 12 B 13 E 14 D 15 C 16 C 17 B 18 D 19 A 20 C 21 D 22 C 23 D 24 C 25 E 26 C 27 D 28 C 29 B 30 B 31 D 32 E 33 B 34 C 35 E 36 A 37 D 38 B 39 C 40 D
Soluzioni 1 A 2 B 3 B 4 E 5 D 6 E 7 B 8 D 9 C 10 B 11 D 12 B 13 E 14 D 15 C 16 C 17 B 18 D 19 A 20 C 21 D 22 C 23 D 24 C 25 E 26 C 27 D 28 C 29 B 30 B 31 D 32 E 33 B 34 C 35 E 36 A 37 D 38 B 39 C 40 D
Nutrizione umana. Prof. Edgardo Canducci aa 2017/18
 Nutrizione umana Prof. Edgardo Canducci aa 2017/18 1 Le proteine aa 2017/18 2 Proteine. Generalità Le proteine (dal greco protos) sono i costituenti principali della materia vivente. Le proteine sono molecole
Nutrizione umana Prof. Edgardo Canducci aa 2017/18 1 Le proteine aa 2017/18 2 Proteine. Generalità Le proteine (dal greco protos) sono i costituenti principali della materia vivente. Le proteine sono molecole
Biochimica delle proteine Prof. M. Bolognesi a.a. 2007/2008. Eloise Mastrangelo
 Biochimica delle proteine Prof. M. Bolognesi a.a. 2007/2008 Eloise Mastrangelo Perché è importante determinare la struttura primaria delle proteine? 1. La conoscenza della sequenza amminoacidica delle
Biochimica delle proteine Prof. M. Bolognesi a.a. 2007/2008 Eloise Mastrangelo Perché è importante determinare la struttura primaria delle proteine? 1. La conoscenza della sequenza amminoacidica delle
ESERCIZI 2. Spiegare il principio di.
 ESERCIZI 2 Spiegare il principio di. Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione
ESERCIZI 2 Spiegare il principio di. Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione
Aminoacidi. Struttura generale Sono 20 e formano le
 Aminoacidi Struttura generale Sono 20 e formano le proteine. Oltre a questi ne esistono altri meno comuni Alcuni subiscono modificazioni dopo essere stati inseriti nelle proteine Altri stanno nell organismo
Aminoacidi Struttura generale Sono 20 e formano le proteine. Oltre a questi ne esistono altri meno comuni Alcuni subiscono modificazioni dopo essere stati inseriti nelle proteine Altri stanno nell organismo
ESERCIZI 2. Spiegare il principio di.
 ESERCIZI 2 Spiegare il principio di. Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione
ESERCIZI 2 Spiegare il principio di. Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 14
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 14 Caratterizzazione strutturale delle proteine Concetti chiave: Per poter essere sequenziata, una proteina deve essere separata
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 14 Caratterizzazione strutturale delle proteine Concetti chiave: Per poter essere sequenziata, una proteina deve essere separata
LA SPETTROMETRIA DI MASSA
 LA SPETTROMETRIA DI MASSA Tecnica che consente di caratterizzare e identificare composti sconosciuti e noti in base alla determinazione della loro massa molecolare e alla loro caratterizzazione strutturale
LA SPETTROMETRIA DI MASSA Tecnica che consente di caratterizzare e identificare composti sconosciuti e noti in base alla determinazione della loro massa molecolare e alla loro caratterizzazione strutturale
Chimica Analitica e Laboratorio 2. Modulo di Spettroscopia Analitica
 Chimica Analitica e Laboratorio 2 Modulo di Spettroscopia Analitica Determinazione della costante di dissociazione di un acido debole 2 Metodi di determinazione del pk d Potenziometria K d = + [ H ][ A
Chimica Analitica e Laboratorio 2 Modulo di Spettroscopia Analitica Determinazione della costante di dissociazione di un acido debole 2 Metodi di determinazione del pk d Potenziometria K d = + [ H ][ A
Cromatografia ionica (IC)
 Cromatografia ionica (IC) Il principio di base della cromatografia ionica è lo scambio ionico su resine scambiatrici forti, che costituiscono la fase stazionaria con cui sono impaccate le colonne, in parziale
Cromatografia ionica (IC) Il principio di base della cromatografia ionica è lo scambio ionico su resine scambiatrici forti, che costituiscono la fase stazionaria con cui sono impaccate le colonne, in parziale
V R V t. Proteine ad alto peso molecolare. Proteine a peso molecolare intermedio. Proteine a basso peso molecolare. Kd + piccolo.
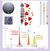 V 0 Proteine ad alto peso molecolare Proteine a peso molecolare intermedio V R V t Proteine a basso peso molecolare Kd elevato Kd piccolo Esclusione molecolare o gelfiltrazione = Volume totale V T = V
V 0 Proteine ad alto peso molecolare Proteine a peso molecolare intermedio V R V t Proteine a basso peso molecolare Kd elevato Kd piccolo Esclusione molecolare o gelfiltrazione = Volume totale V T = V
Modulo 3. Lavorare con le proteine
 Modulo 3 Lavorare con le proteine La purificazione delle proteine Il primo passaggio nello studio delle proprietà di una proteina è la sua purificazione: la sua estrazione dalla matrice biologica in cui
Modulo 3 Lavorare con le proteine La purificazione delle proteine Il primo passaggio nello studio delle proprietà di una proteina è la sua purificazione: la sua estrazione dalla matrice biologica in cui
Test di ingresso LM Scienze Chimiche A. A
 Università degli Studi di Cagliari Test di ingresso LM Scienze Chimiche A. A. 2009-2010 Test di ingresso alla LM in Scienze Chimiche A.A. 2009 2010 1 Chimica Analitica 1) Indicare, tra quelle riportate
Università degli Studi di Cagliari Test di ingresso LM Scienze Chimiche A. A. 2009-2010 Test di ingresso alla LM in Scienze Chimiche A.A. 2009 2010 1 Chimica Analitica 1) Indicare, tra quelle riportate
FORMULARIO DI CHIMICA
 ARGOMENTO Grandezze chimiche fondamentali: 1. Numero di Avogadro 2. Mole 3. Massa Molare 4. Densità 5. Volume molare di un gas Modi di esprimere la concentrazione: 1. Molare M 2. Parti per milione ppm
ARGOMENTO Grandezze chimiche fondamentali: 1. Numero di Avogadro 2. Mole 3. Massa Molare 4. Densità 5. Volume molare di un gas Modi di esprimere la concentrazione: 1. Molare M 2. Parti per milione ppm
Seminario di Cacciatore Rosalia
 Un organismo vivente è un sistema chimico complesso nel quale la materia organica viene sintetizzata, riprodotta, trasformata e decomposta in un incessante ed intenso susseguirsi di reazioni e processi
Un organismo vivente è un sistema chimico complesso nel quale la materia organica viene sintetizzata, riprodotta, trasformata e decomposta in un incessante ed intenso susseguirsi di reazioni e processi
PROTEINE. DEFINIZIONE: Macromolecole formate di AA della serie L uniti tra loro da un legame peptidico.
 LE PROTEINE PROTEINE DEFINIZIONE: Macromolecole formate di AA della serie L uniti tra loro da un legame peptidico. FUNZIONI: Strutturale: costruzione delle strutture cellulari Funzionale: Catalizzatori
LE PROTEINE PROTEINE DEFINIZIONE: Macromolecole formate di AA della serie L uniti tra loro da un legame peptidico. FUNZIONI: Strutturale: costruzione delle strutture cellulari Funzionale: Catalizzatori
TECNICHE ANALITICHE DI RIVELAZIONE PER PROTEINE TECNICHE SPETTROSCOPICHE: Rivelazione in base all interazione fra proteine e radiazione
 TECNICHE ANALITICHE DI RIVELAZIONE PER PROTEINE TECNICHE SPETTROSCOPICHE: Rivelazione in base all interazione fra proteine e radiazione elettromagnetica. Determinazione della concentrazione (quantificazione)
TECNICHE ANALITICHE DI RIVELAZIONE PER PROTEINE TECNICHE SPETTROSCOPICHE: Rivelazione in base all interazione fra proteine e radiazione elettromagnetica. Determinazione della concentrazione (quantificazione)
PROTEINE: funzioni e composizione chimica
 PROTEINE: funzioni e composizione chimica Funzioni strutturali componenti di diversi tessuti Funzioni di regolazione e di trasporto: enzimi, ormoni, carrier, proteine nucleari Contenuto (%) Carbonio 51
PROTEINE: funzioni e composizione chimica Funzioni strutturali componenti di diversi tessuti Funzioni di regolazione e di trasporto: enzimi, ormoni, carrier, proteine nucleari Contenuto (%) Carbonio 51
amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente
 Gli amminoacidi naturali sono α-amminoacidi : il gruppo amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente formula generale: gruppo funzionale carbossilico
Gli amminoacidi naturali sono α-amminoacidi : il gruppo amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente formula generale: gruppo funzionale carbossilico
04/04/2017 CLASSIFICAZIONE METODI SPETTROSCOPICI CHIMICA ANALITICA UNIVERSITÀ DEGLI STUDI DI TERAMO
 UNIVERSITÀ DEGLI STUDI DI TERAMO CL in BIOTECNOLOGIE Anno Accademico 2016/2017 CHIMICA ANALITICA METODI SPETTROSCOPICI I metodi spettroscopici si basano sulla interazione e misura della radiazione elettromagnetica
UNIVERSITÀ DEGLI STUDI DI TERAMO CL in BIOTECNOLOGIE Anno Accademico 2016/2017 CHIMICA ANALITICA METODI SPETTROSCOPICI I metodi spettroscopici si basano sulla interazione e misura della radiazione elettromagnetica
Percorsi di chimica organica - Soluzioni degli esercizi del testo
 ercorsi di chimica organica - Soluzioni degli esercizi del testo AITL 14 1. Il prefisso α negli α-amminoacidi sta ad indicare che il gruppo amminico, - 2, si trova sul carbonio alfa (carbonio legato al
ercorsi di chimica organica - Soluzioni degli esercizi del testo AITL 14 1. Il prefisso α negli α-amminoacidi sta ad indicare che il gruppo amminico, - 2, si trova sul carbonio alfa (carbonio legato al
Spettrofotometria UV-vis
 Spettrofotometria UV-vis Radiazione elettromagnetica: è una forma di trasmissione di energia in cui un campo elettrico e un campo magnetico si propagano attraverso onde nello spazio e nel tempo Interazione
Spettrofotometria UV-vis Radiazione elettromagnetica: è una forma di trasmissione di energia in cui un campo elettrico e un campo magnetico si propagano attraverso onde nello spazio e nel tempo Interazione
L integrazione proteica nelle diverse fisiopatologie
 Università degli Studi di Napoli Federico II Corso di Laurea in Scienze della Nutrizione Umana Corso di: Chimica degli Alimenti L integrazione proteica nelle diverse fisiopatologie Prof. Gian Carlo Tenore
Università degli Studi di Napoli Federico II Corso di Laurea in Scienze della Nutrizione Umana Corso di: Chimica degli Alimenti L integrazione proteica nelle diverse fisiopatologie Prof. Gian Carlo Tenore
9065X Chimica. Modello esame svolto. Esempio di compito scritto di Chimica. Politecnico di Torino CeTeM
 svolto Esempio di compito scritto di Chimica 1 - La configurazione elettronica: [Ar]3d 6 4s 0 rappresenta lo ione: 1) Mn 2+ 2) Ni 2+ 3) Fe 3+ 4) Co 3+ 5) Cu 2+ 2 - Un gas reale mantenuto sempre al di sopra
svolto Esempio di compito scritto di Chimica 1 - La configurazione elettronica: [Ar]3d 6 4s 0 rappresenta lo ione: 1) Mn 2+ 2) Ni 2+ 3) Fe 3+ 4) Co 3+ 5) Cu 2+ 2 - Un gas reale mantenuto sempre al di sopra
LABORATORIO DI CHIMICA FISICA I. Dr Ester Chiessi
 LABORATORIO DI CHIMICA FISICA I. Dr Ester Chiessi STUDIO CINETICO DELLA REAZIONE DI IDROLISI DELL ACETATO DI p- NITROFENILE IN SOLUZIONE ACQUOSA ALCALINA La reazione di idrolisi dell acetato di p-nitrofenile
LABORATORIO DI CHIMICA FISICA I. Dr Ester Chiessi STUDIO CINETICO DELLA REAZIONE DI IDROLISI DELL ACETATO DI p- NITROFENILE IN SOLUZIONE ACQUOSA ALCALINA La reazione di idrolisi dell acetato di p-nitrofenile
Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta)
 Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta) E il termine generico che indica una serie di tecniche di separazione di molecole simili in
Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta) E il termine generico che indica una serie di tecniche di separazione di molecole simili in
differente ripartizione delle sostanze tra due fasi immiscibili
 Cromatografia Dal greco chroma: colore, graphein: scrivere 1903 Mikhail Twsett E il termine generico che indica una serie di tecniche di separazione di molecole (anche molto simili in base alle loro proprietà
Cromatografia Dal greco chroma: colore, graphein: scrivere 1903 Mikhail Twsett E il termine generico che indica una serie di tecniche di separazione di molecole (anche molto simili in base alle loro proprietà
Principi nutritivi calorici
 Principi nutritivi calorici funzione energetica costruttiva regolatrice principi nutritivi glucidi lipidi protidi 1 PROTEINE : cosa sono? Sono molecole organiche costituite da carbonio, ossigeno, idrogeno
Principi nutritivi calorici funzione energetica costruttiva regolatrice principi nutritivi glucidi lipidi protidi 1 PROTEINE : cosa sono? Sono molecole organiche costituite da carbonio, ossigeno, idrogeno
Le reazioni. Sommario. Equazioni chimiche 13/03/2019
 Le reazioni Sommario Scrittura delle equazioni chimiche Bilanciamento delle reazioni Stechiometria delle reazioni Reagente limitante e reagenti in eccesso Resa di una reazione Tipi diversi di reazioni
Le reazioni Sommario Scrittura delle equazioni chimiche Bilanciamento delle reazioni Stechiometria delle reazioni Reagente limitante e reagenti in eccesso Resa di una reazione Tipi diversi di reazioni
Laurea Magistrale in Biologia
 Laurea Magistrale in Biologia Laboratorio del corso di Chimica Fisica Biologica Anno accademico 2009/10 SCOPO Determinazione dei parametri termodinamici associati alla denaturazione termica di una piccola
Laurea Magistrale in Biologia Laboratorio del corso di Chimica Fisica Biologica Anno accademico 2009/10 SCOPO Determinazione dei parametri termodinamici associati alla denaturazione termica di una piccola
Cromatografia a scambio ionico HPLC per la determinazione di cationi ed anioni nelle acque potabili
 Cromatografia a scambio ionico HPLC per la determinazione di cationi ed anioni nelle acque potabili Azienda Sanitaria Provinciale di Catania Team Aziendale HTA LOGO ENTE Il gruppo di lavoro Francesco Barletta
Cromatografia a scambio ionico HPLC per la determinazione di cationi ed anioni nelle acque potabili Azienda Sanitaria Provinciale di Catania Team Aziendale HTA LOGO ENTE Il gruppo di lavoro Francesco Barletta
Le proteine. Sintetizzate nei ribosomi come una sequenza lineare di amminoacidi assumono in seguito una struttura tridimensionale
 Le proteine Elementi funzionali e strutturali di fondamentale importanza per lo svolgimento di funzioni metaboliche, di trasporto, di trasmissione nervosa o contrattile, ormonale o immunitaria Sintetizzate
Le proteine Elementi funzionali e strutturali di fondamentale importanza per lo svolgimento di funzioni metaboliche, di trasporto, di trasmissione nervosa o contrattile, ormonale o immunitaria Sintetizzate
FORMAGGIO - DETERMINAZIONE DEL CONTENUTO DI AMMINOACIDI LIBERI
 Decreto n. 6890 ALLEGATO : METODO DI ANALISI FORMAGGIO - DETERMINAZIONE DEL CONTENUTO DI AMMINOACIDI LIBERI 1. SCOPO E CAMPO DI APPLICAZIONE Questo standard descrive la determinazione del contenuto di
Decreto n. 6890 ALLEGATO : METODO DI ANALISI FORMAGGIO - DETERMINAZIONE DEL CONTENUTO DI AMMINOACIDI LIBERI 1. SCOPO E CAMPO DI APPLICAZIONE Questo standard descrive la determinazione del contenuto di
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA. Angela Chambery Lezione 4
 Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 4 Scoperta degli amminoacidi: gli amminoacidi essenziali Gli amminoacidi essenziali sono quegli amminoacidi che un
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 4 Scoperta degli amminoacidi: gli amminoacidi essenziali Gli amminoacidi essenziali sono quegli amminoacidi che un
