Fattori determinanti il folding proteico
|
|
|
- Ida Federica Costanzo
- 7 anni fa
- Visualizzazioni
Transcript
1 Protein Folding
2 Fattori determinanti il folding proteico α-eliche h e foglietti-β β (60% in media) riempiono il volume proteico efficientemente i Le principali p fasi del folding sono guidate da residui interni (eff. idrofobico) Tolleranza alle mutazioni Le strutture 3D delle proteine sono organizzate gerarchicamente (domini, sottodomini compatti, motivi,...)
3 Fattori determinanti il folding proteico Le proteine si adattano: il fold determina i contatti tra residui; i contatti tra residui NON pre- determinano il fold Esistono molti modi secondo cui i residui interni in una proteina possono adattare il loro impaccamento T4-phage lysozyme: 164 res. >300 mutazioni ingegnerizzate stesso fold
4 La struttura secondaria puo dipendere dalle proprieta dell intorno! dominio GB1 della proteina G di streptococco Residui verde (AATAEKFVFQY) α Residui cyan (EWTYDDATKTF) β sostituiti alternativamente con AWTVEKAFKTF (seq. camaleonte ) Page 280 Le proteine risultanti mantengono il fold, e una denaturazione reversibile Il peptide camaleonte assume due strutture secondarie diverse! AWTVEKAFKTF isolato non e strutturato in soluzione
5 Struttura X-Ray di Rop, una proteina omodimerica composta da motivi αα associati in 4-helix bundle Page 281 Mutazione (guidata sulla base di propensioni dei residui) del 50% dei residui di GB1 (ottenendo un omologia di sequenza del 41% con Rop) converte la proteina nel fold di Rop
6 Paradosso di Levinthal Proteina di 100 residui i Due gradi di liberta torsionali/residuo (phi,psi) 3 conformazioni accessibili per ogni grado di liberta torsionale 3 2x100 possibili conformazioni esplorate/sec Tempo richiesto per esplorare tutte le conformazioni: t = 20 x 10 9 anni! Le proteine si devono ripiegare seguendo un cammino definito, caratterizzato t da conformazioni ni via via piu stabili (diminuizione di G)
7 Strumento per analisi stopped-flow Page 282 Tempo-morto: 50 μs 0.5 ms Uso di T-jump (10-30 C in 100 ns) Segnali spettroscopici: UV, CD Uso di scambio H/D pulsato, abbinato ad NMR
8 Page 283 Spettri di dicroismo circolare (CD) di polipeptidi tipici
9 Page 282 Spettri di assorbimento UV di Phe, Trp, Tyr
10 Scambio pulsato H/D (principio) Usato per seguire il corso del processo di folding di residui individuali nelle proteine Scambio di H + (debolmente acidi) in gruppi NH 2, -NH, -OH, con D 2 O I protoni impegnati in strutture secondarie, o nel cuore della proteina non scambiano con D 2 O
11 Scambio pulsato H/D (applicazione) Proteina denaturata (es. urea) in D 2 O refolding per diluizione (stp.flow) in H 2 O (a ph acido, dove non si ha H/D exchange) Dopo un dato Δt di refolding: aumento di ph, per favorire H/D exchange (scambieranno solo i D + ancora accessibili) Blocco dello scambio H/D (ph acido) Analisi NMR della proteina refolded d per individuare i protoni scambiati nell intervallo Δt.
12 Fasi del folding A) Fase veloce burst iniziale: buona parte delle strutture secondarie sono realizzate entro pochi millisec dall inizio del folding. B) Guidata dal collasso idrofobico, che espelle molecole d acqua dal core della proteina in ripiegamento (misurato con fluorescenza di ANS, CD, maggiore protezione nello scambio H/D). C) Il burst porta al molten globule, contenente buona parte della struttura secondaria attesa, e con raggio di girazione 5-15% maggiore di quello della proteina folded. Catene laterali relativamente libere.
13 Fasi del folding D) Stabilizzazione delle strutture secondarie, e formazione dei proto-domini i ( ms). Strutture ancora in parte fluttuanti; conformeri in interscambio. E) Stabilizzazione della struttura terziaria finale; espulsione definitiva di molecole d acqua; formazione di tutti i legami idrogeno... (richiede diversi secondi; a seconda della complessita della proteina). Il processo di folding e considerato gerarchico, nella sua essenza. ΔG folding caratterizzato da valori bassi ( 5 10 ΔG folding caratterizzato da valori bassi (-5, -10 kcal/mol)
14 Page 285 Folding funnel (a) An idealized funnel landscape.
15 Page 285 Folding funnel (b) The Levinthal golf course landscape.
16 Page 285 Folding funnel (c) Classic folding landscape.
17 Page 285 Folding funnels (d) Rugged energy surface. La rappresentazione considerata piu verosimile
18 Page 286 Scheletro polipeptidico e ponti S-S in BPTI
19 Page 287 Rinaturazione di BPTI attraverso intermedi nonnativi
20 PDI ridotta catalizza il riarrangiamento di ponti S-S non-nativi Page 288 Chapt.9 Anim.Fig.18
21 Page 288 Sintesi di ponti S-S facilitata dalla forma ossidata di PDI.
22 SCRAMBLED RNAse/PDI 2s
23 Struttura 3D della forma ossidata della catena PDI(a) 486 res, 4 domini: a-b-b -a b a Page 289 -Cys-Gly-His-Cys-
24 Struttura 3D della forma ossidata della catena PDI(a) Page 289 Cys36
25 Page 278 Proinsulina porcina. L insulina matura e inibita nella sua attivita dal trattamento con PDI
26
27
28 Prolil-isomerasi isomerasi (rotamasi) Isomerizzazione cis-trans Pro (10% dei residui di Pro) Processo lento nel bilancio del folding Note anche come immunofilline Due famiglie: A) ciclofilline (legano l immunosoppressore ciclosporina A) B) FKBP12 (legano l immunosoppressore di origine fungina FK506)
29 FOLDING ASSISTITO DA CHAPERONINE
30 Diverse classi di Chaperon Heat-shock proteins (Hsp) Hsp70 Hsp40 procariotiche e eucariotiche (in E. coli DnaK DnaJ) ATP-driven refolding processes Chaperonine... Componenti ubiquitari di pro- ed eucarioti (Hsp60-GroEL, Hsp10-GroES) Hsp90 folding di proteine della trasduzione del segnale e di recettori degli ormoni steroidei Nucleoplasmine, refolding/assembly dei nucleosomi Alcune classi di chaperon lavorano in concerto
31 Electron micrograph-derived 3D image of the Hsp60 chaperonin from the photosynthetic bacterium Rhodobacter sphaeroides. Page 291
32 X-Ray structure of GroEL (E.coli). Side view perpendicular to the 7-fold axis D. apicale D. interm. ATPγS D. equat. 7 x 2 x 547 res. Simm. D 7 (72) P age 292
33 X-Ray structure of GroEL. Top view along the 7-fold axis. 45 Angstroem Page 292
34 X-Ray structure of GroES as viewed along its 7-fold axis. 7 x 97 res. C 7 7 Page 293
35 Apical domain of GroEL in complex with a tight-binding 12-residue polypeptide (SWMTTPWGFLHP). Mutations abolishing binding of unfolded polypeptides (and of GroES) map at hydrophobic residues of the rim of the apical domain Page 295
36 X-Ray structure of the GroEL-GroES-(ADP) 7 complex. cis-ring 7 ADP Page 293 trans-ring
37 Page 293 X-Ray structure of the GroEL-Gro-ES-(ADP) 7 complex.
38 Il sistema GroEL/GroEs ha attivita ATPasica essenziale per il refolding delle proteine substrato
39 Domain movements in GroEL. (a) Ribbon diagram of a single subunit of GroEL in the X-ray structure of GroEL alone. Page 294
40 Page 294 Domain movements in GroEL. (b) A GroEL subunit in the X-ray structure of GroEL-GroES-(ADP) 7. ( ) 7
41 X-Ray structure of the GroEL-Gro-ES-(ADP) 7 complex Å 3 Page Å 3
42 Page 294 Domain movements in GroEL. (c) Schematic diagram indicating the conformational changes in GroEL when it binds GroES.
43 Apical domain of GroEL in complex with a tight-binding 12-residue polypeptide (SWMTTPWGFLHP). Mutations abolishing binding of unfolded polypeptides (and of GroES) map at hydrophobic residues of the rim of the apical domain Page 295
44 Movements of the polypeptide-binding helices of GroEL. Page 295 (a) (b)
45 Page 298 Schematic diagram of the mechanism of stretch-induced hydrogen exchange by the GroEL/ES system.
46 Reaction cycle of the GroEL/ES chaperonin system in protein folding. Le pareti della camera centrale (Anfinsen cage) sono idrofiliche (13 secondi) Page 296
47 Rate of hydrogen-tritium exchange of tritiated RuBisCO. Page 297 Nero: curva di scambio T/H in RubisCO in soluzione (misurata in assenza del sistema GroEL-GroES-ATP) Rosso: curva di scambio T/H in RubisCO in soluzione (teorica) Blu: curva di scambio T/H in RubisCO calcolata per un sistema GroEL- GroES-ATP che rilascia RubisCO ad ogni ciclo.
48 Quante proteine si servono di GroEl/GroES ES in E. coli? Circa 300 (rispetto a 2500 proteine citoplasmatiche identificate nell esperimento) Labeling con 35 S-Met Ricerca della radioattivita associata alla chaperonina a tempi diversi Proteine kda, due o piu α/β domains (slow folders: assembly of sheets; easy misfolding) Le proteine che non legano GroEL probabilmente bil raggiungono lo stato folded d rapidamente, e non lasciano patches idrofobici esposti per il legame con GroEL
49 Trends Biochem.Sci (1998) 23, 138.
Denaturazione riduttiva / rinaturazione
 Protein Folding Denaturazione riduttiva / rinaturazione ossidativa di RNase A. Page 277 Meccanismo di scambio di ponti S-S catalizzato t da tioli o da enzimi. i Page 278 Protein Disulfide Isomerase: PDI
Protein Folding Denaturazione riduttiva / rinaturazione ossidativa di RNase A. Page 277 Meccanismo di scambio di ponti S-S catalizzato t da tioli o da enzimi. i Page 278 Protein Disulfide Isomerase: PDI
STRUTTURAZIONE DELLE PROTEINE
 STRUTTURAZIONE DELLE PROTEINE Molti diversi tipi di struttura non avvolta (unfolded states) Un solo tipo di struttura avvolta (folded state) Proteina NATIVA Principi della strutturazione proteica: 1) La
STRUTTURAZIONE DELLE PROTEINE Molti diversi tipi di struttura non avvolta (unfolded states) Un solo tipo di struttura avvolta (folded state) Proteina NATIVA Principi della strutturazione proteica: 1) La
Folding delle Proteine
 Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Folding delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari
Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Folding delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari
LA STRUTTURA DELLE PROTEINE È GERARCHICA
 LA STRUTTURA DELLE PROTEINE È GERARCHICA LA STRUTTURA DETERMINA LA FUNZIONE The Protein Folding Problem Cosa determina la struttura? Energia Cinetica Come si determina la struttura? Metodi Sperimentali
LA STRUTTURA DELLE PROTEINE È GERARCHICA LA STRUTTURA DETERMINA LA FUNZIONE The Protein Folding Problem Cosa determina la struttura? Energia Cinetica Come si determina la struttura? Metodi Sperimentali
Le Biomolecole II parte. Lezioni d'autore di Giorgio Benedetti
 Le Biomolecole II parte Lezioni d'autore di Giorgio Benedetti LA STRUTTURA TERZIARIA DI UNA PROTEINA La struttura tridimensionale adottata da una proteina è detta struttura terziaria. Essa prende in considerazione
Le Biomolecole II parte Lezioni d'autore di Giorgio Benedetti LA STRUTTURA TERZIARIA DI UNA PROTEINA La struttura tridimensionale adottata da una proteina è detta struttura terziaria. Essa prende in considerazione
30/10/2015. Molte proteine sono. intrinsecamente disordinate. o destrutturate (IDP/IUP), cioè non hanno una struttura
 Molte proteine sono intrinsecamente disordinate o destrutturate (IDP/IUP), cioè non hanno una struttura terziaria e/o secondaria stabile. Le IUP sono caratterizzate da - scarso contenuto in aa apolari,
Molte proteine sono intrinsecamente disordinate o destrutturate (IDP/IUP), cioè non hanno una struttura terziaria e/o secondaria stabile. Le IUP sono caratterizzate da - scarso contenuto in aa apolari,
Parametri dell α-elica. residui/giro 3.6. passo dell elica
 GRAFICO DI RAMACHANDRAN Parametri dell α-elica residui/giro 3.6 spazio/residuo passo dell elica 1.5 Å 5.4 Å 1 L α-elica può essere destabilizzata da interazioni tra i gruppi R: repulsione/attrazione elettrostatica
GRAFICO DI RAMACHANDRAN Parametri dell α-elica residui/giro 3.6 spazio/residuo passo dell elica 1.5 Å 5.4 Å 1 L α-elica può essere destabilizzata da interazioni tra i gruppi R: repulsione/attrazione elettrostatica
Proprietà comuni. Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici
 Gli aminoacidi Proprietà comuni Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici paragonabili Il gruppo α-aminico è un acido più forte (o una base più debole
Gli aminoacidi Proprietà comuni Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici paragonabili Il gruppo α-aminico è un acido più forte (o una base più debole
le porzioni con strutture secondarie sono avvicinate e impaccate mediante anse e curve della catena. STRUTTURA TERZIARIA
 STRUTTURA TERZIARIA le porzioni con strutture secondarie sono avvicinate e impaccate mediante anse e curve della catena. Le proteine globulari dopo aver organizzato il proprio scheletro polipeptidico con
STRUTTURA TERZIARIA le porzioni con strutture secondarie sono avvicinate e impaccate mediante anse e curve della catena. Le proteine globulari dopo aver organizzato il proprio scheletro polipeptidico con
Protein folding. (Il ripiegamento delle proteine)
 Protein folding (Il ripiegamento delle proteine) Folding in vitro e in vivo (D.L. Nelson, M.M. Cox, Lehninger Principles of Biochemistry, 4th ed., Worth Publishers, 2005) Il folding delle proteine: perché
Protein folding (Il ripiegamento delle proteine) Folding in vitro e in vivo (D.L. Nelson, M.M. Cox, Lehninger Principles of Biochemistry, 4th ed., Worth Publishers, 2005) Il folding delle proteine: perché
circolare in ambito alimentare Alberto Barbiroli
 Principi ed applicazioni del dicroismo circolare in ambito alimentare Alberto Barbiroli Origine del segnale CD Luce polarizzata planarmente Il vettore campo elettrico oscilla su una linea Sovrapposizione
Principi ed applicazioni del dicroismo circolare in ambito alimentare Alberto Barbiroli Origine del segnale CD Luce polarizzata planarmente Il vettore campo elettrico oscilla su una linea Sovrapposizione
La struttura delle proteine
 La struttura delle proteine Funzioni delle proteine Strutturali Contrattili Trasporto Riserva Ormonali Enzimatiche Protezione Struttura della proteina Struttura secondaria: ripiegamento locale della catena
La struttura delle proteine Funzioni delle proteine Strutturali Contrattili Trasporto Riserva Ormonali Enzimatiche Protezione Struttura della proteina Struttura secondaria: ripiegamento locale della catena
la struttura tridimensionale può essere ottenuta solo per Un intero dominio in genere da 50 a 300 residui
 Durante la traduzione l informazione di ripiegamento codificata nella sequenza aminoacidica diventa disponibile in maniera vettoriale la struttura tridimensionale può essere ottenuta solo per Un intero
Durante la traduzione l informazione di ripiegamento codificata nella sequenza aminoacidica diventa disponibile in maniera vettoriale la struttura tridimensionale può essere ottenuta solo per Un intero
Acquisizione e Stabilità della struttura terziaria delle proteine
 Acquisizione e Stabilità della struttura terziaria delle proteine FORZE CHE STABILIZZANO LA STRUTTURA TERZIARIA DELLE PROTEINE 1. Legame covalente S-S (forte): non è presente in tutte le proteine che,
Acquisizione e Stabilità della struttura terziaria delle proteine FORZE CHE STABILIZZANO LA STRUTTURA TERZIARIA DELLE PROTEINE 1. Legame covalente S-S (forte): non è presente in tutte le proteine che,
Proteine: struttura e funzione
 Proteine: struttura e funzione Prof.ssa Flavia Frabetti PROTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (C, H, O,
Proteine: struttura e funzione Prof.ssa Flavia Frabetti PROTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (C, H, O,
 Hsp90 complessi con recettori per ormoni glucocorticoidi Hsp70 BiP in RE eucarioti, DnaK E. coli Hsp40 DnaJ in E. coli Hsp60 GroEL in E. coli Hsp10 GroES in E. coli H2O Pi C(ADP) Uprot C(ATP) Uprot-C(ADP)
Hsp90 complessi con recettori per ormoni glucocorticoidi Hsp70 BiP in RE eucarioti, DnaK E. coli Hsp40 DnaJ in E. coli Hsp60 GroEL in E. coli Hsp10 GroES in E. coli H2O Pi C(ADP) Uprot C(ATP) Uprot-C(ADP)
Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi. Possono assumere forme diverse a seconda della funzione
 Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi Hanno elevato PM Possono assumere forme diverse a seconda della funzione svolgono molteplici funzioni Tra le proteine
Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi Hanno elevato PM Possono assumere forme diverse a seconda della funzione svolgono molteplici funzioni Tra le proteine
Laurea Magistrale in Biologia
 Laurea Magistrale in Biologia Laboratorio del corso di Chimica Fisica Biologica Anno accademico 2009/10 SCOPO Determinazione dei parametri termodinamici associati alla denaturazione termica di una piccola
Laurea Magistrale in Biologia Laboratorio del corso di Chimica Fisica Biologica Anno accademico 2009/10 SCOPO Determinazione dei parametri termodinamici associati alla denaturazione termica di una piccola
Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica.
 Concanavalina A Emoglobina subunità Trioso fosfato isomerasi Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica. 1 La conformazione è
Concanavalina A Emoglobina subunità Trioso fosfato isomerasi Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica. 1 La conformazione è
PROTEINE: STRUTTURA, ESEMPI E FUNZIONAMENTO TUTORATO 1 GIULIANO F. PATANÈ COLLEGIO A. VOLTA
 PROTEINE: STRUTTURA, ESEMPI E FUNZIONAMENTO TUTORATO 1 GIULIANO F. PATANÈ COLLEGIO A. VOLTA PROTEINE Una proteina è basilarmente una catena polipeptidica (che in termini chimici può anche essere definita
PROTEINE: STRUTTURA, ESEMPI E FUNZIONAMENTO TUTORATO 1 GIULIANO F. PATANÈ COLLEGIO A. VOLTA PROTEINE Una proteina è basilarmente una catena polipeptidica (che in termini chimici può anche essere definita
COMPOSTI AZOTATI. derivanti dall ammoniaca AMMINE. desinenza -INA AMMIDE
 COMPOSTI AZOTATI derivanti dall ammoniaca AMMINE desinenza -INA AMMIDE ANCORA AMMIDI RISONANZA A M M I D I Il legame ammidico ha parziale carattere di doppio legame per la seguente risonanza: Ammidi H
COMPOSTI AZOTATI derivanti dall ammoniaca AMMINE desinenza -INA AMMIDE ANCORA AMMIDI RISONANZA A M M I D I Il legame ammidico ha parziale carattere di doppio legame per la seguente risonanza: Ammidi H
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
- Φ e ψ Presenta 3,6 residui per spira -HB between C=O n residue n and NH n+4. - α-helix
 Structure Basic elements - Φ e ψ -60-50. -Presenta 3,6 residui per spira -HB between C=O n residue n and NH n+4. - α-helix Β-sheet Red oxygen Blu nitrogen white hydrogen black Cα Violet lateral chain -at
Structure Basic elements - Φ e ψ -60-50. -Presenta 3,6 residui per spira -HB between C=O n residue n and NH n+4. - α-helix Β-sheet Red oxygen Blu nitrogen white hydrogen black Cα Violet lateral chain -at
STRUTTURA E FUNZIONE DELLE PROTEINE
 STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
La struttura terziaria di una proteina definisce la disposizione di tutti i suoi atomi nello spazio tridimensionale
 La struttura terziaria di una proteina definisce la disposizione di tutti i suoi atomi nello spazio tridimensionale La struttura secondaria si riferisce a una speciale disposizione spaziale di residui
La struttura terziaria di una proteina definisce la disposizione di tutti i suoi atomi nello spazio tridimensionale La struttura secondaria si riferisce a una speciale disposizione spaziale di residui
PROTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi
 POTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (,, O, N) macromolecole organiche, molecole informazionali, polimeri
POTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (,, O, N) macromolecole organiche, molecole informazionali, polimeri
LE PROTEINE: POLIMERI COSTITUITI DA 20 TIPI DI MONOMERI, I 20 AMINOACIDI
 LE PROTEINE: POLIMERI OSTITUITI DA 20 TIPI DI MONOMERI, I 20 AMINOAIDI OGNI PROTEINA PUO ESSERE FORMATA DA MOLTE DEINE O ENTINAIA DI AMINOAIDI E SI LEGANO A FORMARE UNA ATENA NON RAMIFIATA La catena di
LE PROTEINE: POLIMERI OSTITUITI DA 20 TIPI DI MONOMERI, I 20 AMINOAIDI OGNI PROTEINA PUO ESSERE FORMATA DA MOLTE DEINE O ENTINAIA DI AMINOAIDI E SI LEGANO A FORMARE UNA ATENA NON RAMIFIATA La catena di
Formula generale di un amminoacido
 Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
CARBOIDRATI C H O ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO
 CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
moli OH - /mole amminoacido
 ) ) Di seguito è riportata la curva di titolazione di un amminoacido. Osservando il grafico: a) stabilire il valore dei pka dell aminoacido b) calcolare il valore del pi e individuarlo sul grafico. c)
) ) Di seguito è riportata la curva di titolazione di un amminoacido. Osservando il grafico: a) stabilire il valore dei pka dell aminoacido b) calcolare il valore del pi e individuarlo sul grafico. c)
STRUTTURA E FUNZIONE DELLE PROTEINE
 STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
LE PROTEINE. SONO Polimeri formati dall unione di AMMINOACIDI (AA) Rende diversi i 20 AA l uno dall altro UN ATOMO DI C AL CENTRO
 LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
STRUTTURA TRIDIMENSIONALE DELLE PROTEINE
 STRUTTURA TRIDIMENSIONALE DELLE PROTEINE Biologia della Cellula Animale 2016 1 STRUTTURA PROTEINE Cooper: The Cell, a Molecular Approach, 2 nd ed. http://en.wikipedia.org/wiki/protein_structure STRUTTURA
STRUTTURA TRIDIMENSIONALE DELLE PROTEINE Biologia della Cellula Animale 2016 1 STRUTTURA PROTEINE Cooper: The Cell, a Molecular Approach, 2 nd ed. http://en.wikipedia.org/wiki/protein_structure STRUTTURA
BIOMOLECOLE (PROTEINE)
 BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
Struttura delle Proteine
 Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
Macromolecole Biologiche Interazioni non covalenti
 Interazioni non covalenti D H A δ - δ + δ - Le interazioni non covalenti Interazioni fra atomi che non sono legati da legami covalenti. Le interazioni non covalenti sono molto meno intense rispetto alle
Interazioni non covalenti D H A δ - δ + δ - Le interazioni non covalenti Interazioni fra atomi che non sono legati da legami covalenti. Le interazioni non covalenti sono molto meno intense rispetto alle
La struttura delle proteine e e descritta da quattro livelli di organizzazione
 La struttura delle proteine e e descritta da quattro livelli di organizzazione Struttura Primaria- - la sequenza di aminoacidi Struttura Secondaria - strutture locali stabilizzate da legami H che coinvolgono
La struttura delle proteine e e descritta da quattro livelli di organizzazione Struttura Primaria- - la sequenza di aminoacidi Struttura Secondaria - strutture locali stabilizzate da legami H che coinvolgono
sono le unità monomeriche che costituiscono le proteine hanno tutti una struttura comune
 AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
Fondamentali in ogni organismo, hanno molteplici ruoli:
 Le proteine Fondamentali in ogni organismo, hanno molteplici ruoli: Componenti strutturali (collagene, tessuto connettivo, citoscheletro, pelle) Trasportatori (emoglobina, albumina) Trasmettitori di messaggi
Le proteine Fondamentali in ogni organismo, hanno molteplici ruoli: Componenti strutturali (collagene, tessuto connettivo, citoscheletro, pelle) Trasportatori (emoglobina, albumina) Trasmettitori di messaggi
Le proteine. Sono polimeri di amminoacidi dispos$ in sequenza. Due amminoacidi si legano tra loro formando un legame pep-dico.
 Le proteine Sono polimeri di amminoacidi dispos$ in sequenza. Due amminoacidi si legano tra loro formando un legame pep-dico. Cur$s et al. Invito alla biologia.blu Zanichelli editore 2011 1 Struttura e
Le proteine Sono polimeri di amminoacidi dispos$ in sequenza. Due amminoacidi si legano tra loro formando un legame pep-dico. Cur$s et al. Invito alla biologia.blu Zanichelli editore 2011 1 Struttura e
Mediatore chimico. Recettore. Trasduzione del segnale. Risposta della cellula
 Mediatore chimico Recettore Trasduzione del segnale Risposta della cellula I mediatori chimici sono prodotti da cellule specializzate e sono diffusi nell organismo da apparati di distribuzione Sistemi
Mediatore chimico Recettore Trasduzione del segnale Risposta della cellula I mediatori chimici sono prodotti da cellule specializzate e sono diffusi nell organismo da apparati di distribuzione Sistemi
Proteine. Enzimi Fattori di Trascrizione Proteine di Membrana (trasportatori, canale, recettori di membrana)
 Proteine Enzimi Fattori di Trascrizione Proteine di Membrana (trasportatori, canale, recettori di membrana) Ormoni e Fattori di crescita Anticorpi Trasporto Trasporto (emoglobina, LDL, HDL.) Fenotipo Proteine
Proteine Enzimi Fattori di Trascrizione Proteine di Membrana (trasportatori, canale, recettori di membrana) Ormoni e Fattori di crescita Anticorpi Trasporto Trasporto (emoglobina, LDL, HDL.) Fenotipo Proteine
Formazione delle strutture amiloidi_1
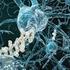 Formazione delle strutture amiloidi_1 Gli aggregati possono essere amorfi AMILOIDOGENESI Formazione delle strutture amiloidi_2 Gli aggregati possono essere strutturati monomero dimero monomero oligomero
Formazione delle strutture amiloidi_1 Gli aggregati possono essere amorfi AMILOIDOGENESI Formazione delle strutture amiloidi_2 Gli aggregati possono essere strutturati monomero dimero monomero oligomero
Proteine strutturali Sostegno meccanico Cheratina: costituisce i capelli Collagene: costituisce le cartilagini Proteine di immagazzinamento
 Tipo Funzione Esempi Enzimi Accelerano le reazioni chimiche Saccarasi: posiziona il saccarosio in modo che possa essere scisso nelle due unità di glucosio e fruttosio che lo formano Ormoni Messaggeri chimici
Tipo Funzione Esempi Enzimi Accelerano le reazioni chimiche Saccarasi: posiziona il saccarosio in modo che possa essere scisso nelle due unità di glucosio e fruttosio che lo formano Ormoni Messaggeri chimici
I ribosomi liberi nel citoplasma sintetizzano le proteine destinate alla via citoplasmatica, cioè quelle destinate a:
 I ribosomi liberi nel citoplasma sintetizzano le proteine destinate alla via citoplasmatica, cioè quelle destinate a: filmato Rimanere nel citoplasma Essere trasportate dal citoplasma al nucleo Essere
I ribosomi liberi nel citoplasma sintetizzano le proteine destinate alla via citoplasmatica, cioè quelle destinate a: filmato Rimanere nel citoplasma Essere trasportate dal citoplasma al nucleo Essere
Amminoacidi e proteine Dagli amminoacidi come building-blocks alla struttura quaternaria
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Amminoacidi e proteine Dagli amminoacidi come building-blocks alla struttura quaternaria
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Amminoacidi e proteine Dagli amminoacidi come building-blocks alla struttura quaternaria
DNA Proteine Cellule. Il DNA contiene l informazione per sintetizzare le proteine. proteine cellule. Essere vivente. geni
 Sintesi Proteica DNA Proteine Cellule Il DNA contiene l informazione per sintetizzare le proteine geni Essere vivente proteine cellule Essere vivente Il DNA si tiene tutta la gloria, Le proteine fanno
Sintesi Proteica DNA Proteine Cellule Il DNA contiene l informazione per sintetizzare le proteine geni Essere vivente proteine cellule Essere vivente Il DNA si tiene tutta la gloria, Le proteine fanno
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA)
 La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) L atomo del carbonio (C).. C. Atomo tetravalente. C C C C Gli idrocarburi I legami del carbonio 109.5 gradi
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) L atomo del carbonio (C).. C. Atomo tetravalente. C C C C Gli idrocarburi I legami del carbonio 109.5 gradi
Funzioni delle proteine
 Funzioni delle proteine ENZIMI Proteine di trasporto Proteine di riserva Proteine contrattili o motili Proteine strutturali Proteine di difesa Proteine regolatrici Proteine di trasporto Emoglobina Lipoproteine
Funzioni delle proteine ENZIMI Proteine di trasporto Proteine di riserva Proteine contrattili o motili Proteine strutturali Proteine di difesa Proteine regolatrici Proteine di trasporto Emoglobina Lipoproteine
LE PROTEINE -struttura tridimensionale-
 LE PROTEINE -struttura tridimensionale- Struttura generale di una proteina Ceruloplasmina Cosa sono??? Sono biopolimeri con forme ben definite. composti da molteplici amminoacidi, legati con legami peptidici
LE PROTEINE -struttura tridimensionale- Struttura generale di una proteina Ceruloplasmina Cosa sono??? Sono biopolimeri con forme ben definite. composti da molteplici amminoacidi, legati con legami peptidici
gruppo amminico Gli aminoacidi polimerizzano durante la sintesi delle proteine mediante la formazione di legami peptidici. gruppo carbossilico
 gruppo amminico Gli aminoacidi polimerizzano durante la sintesi delle proteine mediante la formazione di legami peptidici. gruppo carbossilico Il legame peptidico si ha quando il gruppo carbossilico (-
gruppo amminico Gli aminoacidi polimerizzano durante la sintesi delle proteine mediante la formazione di legami peptidici. gruppo carbossilico Il legame peptidico si ha quando il gruppo carbossilico (-
Classificazione dell Architettura Proteica
 Classificazione dell Architettura Proteica struttura Primaria struttura Secondaria Super-secondaria Domini struttura Terziaria: folding struttura Quaternaria Proteine globulari Il ripiegamento della catena
Classificazione dell Architettura Proteica struttura Primaria struttura Secondaria Super-secondaria Domini struttura Terziaria: folding struttura Quaternaria Proteine globulari Il ripiegamento della catena
Complessi multienzimatici nella biosintesi dei polichetidi: le polichetide sintasi
 Complessi multienzimatici nella biosintesi dei polichetidi: le polichetide sintasi Organizzazione strutturale dei sistemi multienzimatici FAS, PKS e NRPS Analogie tra biosintesi dei polichetidi (PKS)
Complessi multienzimatici nella biosintesi dei polichetidi: le polichetide sintasi Organizzazione strutturale dei sistemi multienzimatici FAS, PKS e NRPS Analogie tra biosintesi dei polichetidi (PKS)
Modificazione selettiva o casuale di una proteina allo scopo di modificare la struttura o la funzione
 Modificazione selettiva o casuale di una proteina allo scopo di modificare la struttura o la funzione PRODURRE CARATTERIZZARE MODULARE ATTIVITA O INTRODURRE NUOVE FUNZIONI Ingegneria proteica PROGETTARE
Modificazione selettiva o casuale di una proteina allo scopo di modificare la struttura o la funzione PRODURRE CARATTERIZZARE MODULARE ATTIVITA O INTRODURRE NUOVE FUNZIONI Ingegneria proteica PROGETTARE
scaricato da www.sunhope.it Proteine semplici costituite dai soli amminoacidi
 Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
Amminoacidi. Struttura base di un a-amminoacido
 Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Alcol + alcol etere R-OH + R -OH R-O-R + H 2 O Aldeide + alcol emiacetale R-CHO + R -OH R-CHOH-O-R Acido + Acido anidride R-COOH + R -COOH
 Nomenclatura AMIDI Alcol + alcol etere R-OH + R -OH R-O-R + H 2 O Aldeide + alcol emiacetale R-CHO + R -OH R-CHOH-O-R Acido + Acido anidride R-COOH + R -COOH R-CO-O-CO-R + H 2 O Alcol + Acido estere R-COOH
Nomenclatura AMIDI Alcol + alcol etere R-OH + R -OH R-O-R + H 2 O Aldeide + alcol emiacetale R-CHO + R -OH R-CHOH-O-R Acido + Acido anidride R-COOH + R -COOH R-CO-O-CO-R + H 2 O Alcol + Acido estere R-COOH
MS e Biomolecole FOLDING PROTEICO. Teoria e applicazioni APPLICAZIONI ESI E MALDI PER LO STUDIO DI PEPTIDI E PROTEINE
 MS e Biomolecole Teoria e applicazioni Spettro ESI-MS della transferrina, una proteina ad alto peso molecolare (circa 80000Da). APPLICAZIONI ESI E MALDI PER LO STUDIO DI PEPTIDI E PROTEINE Determinazione
MS e Biomolecole Teoria e applicazioni Spettro ESI-MS della transferrina, una proteina ad alto peso molecolare (circa 80000Da). APPLICAZIONI ESI E MALDI PER LO STUDIO DI PEPTIDI E PROTEINE Determinazione
STRUTTURA TERZIARIA. H 3 N + COO - β-foglietto
 STRUTTURA TERZIARIA α-eliche H 3 N + COO - β-foglietto La catena polipeptidica delle proteine GLOBULARI oltre ad organizzarsi in strutture di tipo secondario va incontro ad un ulteriore ripiegamento sino
STRUTTURA TERZIARIA α-eliche H 3 N + COO - β-foglietto La catena polipeptidica delle proteine GLOBULARI oltre ad organizzarsi in strutture di tipo secondario va incontro ad un ulteriore ripiegamento sino
Nel DNA e nell RNA i nucleotidi sono legati covalentemente da legami fosfodiesterei.
 DNA e RNA Composizione e proprietà Struttura Analisi 1 STRUTTURA DAGLI ACIDI NUCLEICI Nel DNA e nell RNA i nucleotidi sono legati covalentemente da legami fosfodiesterei. I gruppi fosforici hanno pka vicino
DNA e RNA Composizione e proprietà Struttura Analisi 1 STRUTTURA DAGLI ACIDI NUCLEICI Nel DNA e nell RNA i nucleotidi sono legati covalentemente da legami fosfodiesterei. I gruppi fosforici hanno pka vicino
a) un movimento contro gradiente di concentrazione che utilizza fonti primarie di energia
 1. Quale considerazione sulla struttura primaria di una proteina è vera? a) è caratteristica delle proteine insolubili b) i ponti S-S la stabilizzano c) i ponti H la stabilizzano d) la proteina assume
1. Quale considerazione sulla struttura primaria di una proteina è vera? a) è caratteristica delle proteine insolubili b) i ponti S-S la stabilizzano c) i ponti H la stabilizzano d) la proteina assume
Lezione n. 1. Chimica fisica Micro-macro. & descrizioni multiscala
 Chimica Fisica Biotecnologie sanitarie Lezione n. 1 Chimica fisica Micro-macro & descrizioni multiscala Gli strumenti della chimica fisica Esempio o 1: metodi spettroscopici interazione radiazione / materia
Chimica Fisica Biotecnologie sanitarie Lezione n. 1 Chimica fisica Micro-macro & descrizioni multiscala Gli strumenti della chimica fisica Esempio o 1: metodi spettroscopici interazione radiazione / materia
DNA: Struttura e caratteristiche
 DNA: Struttura e caratteristiche Il DNA è un acido nucleico formato da monomeri detti nucleotidi. Ogni nucleotide è formato da: Zucchero pentoso (desossiribosio) Gruppo fosfato Base azotata Basi azotate:
DNA: Struttura e caratteristiche Il DNA è un acido nucleico formato da monomeri detti nucleotidi. Ogni nucleotide è formato da: Zucchero pentoso (desossiribosio) Gruppo fosfato Base azotata Basi azotate:
Schema generale. Folding e misfolding di proteine: concetti generali e applicazioni con tecniche di singola molecola. Esperimento di Anfinsen
 Schema generale Folding e misfolding di proteine: concetti generali e applicazioni con tecniche di singola molecola Concetti generali di folding delle proteine: cenni storici, meccanismi di folding, modello
Schema generale Folding e misfolding di proteine: concetti generali e applicazioni con tecniche di singola molecola Concetti generali di folding delle proteine: cenni storici, meccanismi di folding, modello
TAPPE PRINCIPALI DELLA SINTESI PROTEICA. FORMAZIONE DEI PRECURSORI ATTIVATI (Aminoacil-tRNA): accoppiamento tra codice nucleotidico ed aminoacidi
 TAPPE PRINCIPALI DELLA SINTESI PROTEICA FORMAZIONE DEI PRECURSORI ATTIVATI (Aminoacil-tRNA): accoppiamento tra codice nucleotidico ed aminoacidi SINTESI DEL POLIPEPTIDE SUI RIBOSOMI 3 fasi Inizio = Riconoscimento
TAPPE PRINCIPALI DELLA SINTESI PROTEICA FORMAZIONE DEI PRECURSORI ATTIVATI (Aminoacil-tRNA): accoppiamento tra codice nucleotidico ed aminoacidi SINTESI DEL POLIPEPTIDE SUI RIBOSOMI 3 fasi Inizio = Riconoscimento
2011 - G. Licini, Università di Padova. La riproduzione a fini commerciali è vietata
 Ammino acidi Composto che contiene una funziome acida e amminica. Usualmente però con amminoacidi si intendono gli alfa- amminoacidi. Tra questi composti ve ne sono 20 che vengono definiti geneticamente
Ammino acidi Composto che contiene una funziome acida e amminica. Usualmente però con amminoacidi si intendono gli alfa- amminoacidi. Tra questi composti ve ne sono 20 che vengono definiti geneticamente
Fosforilazione ossidativa
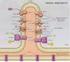 Chimica Biologica A.A. 2010-2011 Fosforilazione ossidativa Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Teoria Chemiosmotica ΔG = 2.3 RT (ph (matrice) -ph (spazio
Chimica Biologica A.A. 2010-2011 Fosforilazione ossidativa Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Teoria Chemiosmotica ΔG = 2.3 RT (ph (matrice) -ph (spazio
lati esterni altamente Idrofilici
 I due filamenti complementari del DNA sono antiparalleli: uno è in direzione 5-3 e l altro in direzione 3-5. parte interna idrofobica lati esterni altamente Idrofilici APPAIAMENTO DELLE BASI AZOTATE: 2
I due filamenti complementari del DNA sono antiparalleli: uno è in direzione 5-3 e l altro in direzione 3-5. parte interna idrofobica lati esterni altamente Idrofilici APPAIAMENTO DELLE BASI AZOTATE: 2
Schemi delle lezioni 1
 Schemi delle lezioni 1 Detti anche proteine sono i composti organici maggiormente presenti nelle cellule, dato che costituiscono circa il 50% del loro peso secco. Nell uomo adulto rappresentano circa
Schemi delle lezioni 1 Detti anche proteine sono i composti organici maggiormente presenti nelle cellule, dato che costituiscono circa il 50% del loro peso secco. Nell uomo adulto rappresentano circa
Struttura secondaria
 Struttura secondaria Struttura localmente ordinata Polimeri lineari ad unità monomeriche asimmetriche elica j = 0,1,2,..., N N = numero di residui z j = h z j + z 0 x j = r cos (j2p h z /P + d 0 ) y j
Struttura secondaria Struttura localmente ordinata Polimeri lineari ad unità monomeriche asimmetriche elica j = 0,1,2,..., N N = numero di residui z j = h z j + z 0 x j = r cos (j2p h z /P + d 0 ) y j
Dicroismo circolare e chiralità. Una molecola si dice chirale se non è sovrapponibile alla sua immagine speculare.
 Dicroismo circolare Dicroismo circolare e chiralità Una molecola si dice chirale se non è sovrapponibile alla sua immagine speculare. Dicroismo circolare e chiralità Le molecole chirali assorbono in
Dicroismo circolare Dicroismo circolare e chiralità Una molecola si dice chirale se non è sovrapponibile alla sua immagine speculare. Dicroismo circolare e chiralità Le molecole chirali assorbono in
MS e Biomolecole FOLDING PROTEICO. Teoria e applicazioni APPLICAZIONI ESI E MALDI PER LO STUDIO DI PEPTIDI E PROTEINE
 MS e Biomolecole Teoria e applicazioni APPLICAZIONI ESI E MALDI PER LO STUDIO DI PEPTIDI E PROTEINE Determinazione del peso molecolare Individuazione di isoforme Mappatura peptidica e conferma della struttura
MS e Biomolecole Teoria e applicazioni APPLICAZIONI ESI E MALDI PER LO STUDIO DI PEPTIDI E PROTEINE Determinazione del peso molecolare Individuazione di isoforme Mappatura peptidica e conferma della struttura
Aminoacidi. Struttura generale Sono 20 e formano le
 Aminoacidi Struttura generale Sono 20 e formano le proteine. Oltre a questi ne esistono altri meno comuni Alcuni subiscono modificazioni dopo essere stati inseriti nelle proteine Altri stanno nell organismo
Aminoacidi Struttura generale Sono 20 e formano le proteine. Oltre a questi ne esistono altri meno comuni Alcuni subiscono modificazioni dopo essere stati inseriti nelle proteine Altri stanno nell organismo
Costituenti chimici della materia vivente
 Costituenti chimici della materia vivente Le macromolecole biologiche Macromolecole (dal greco macros = grande) biologiche. Classi di composti biologici multifunzionali: Polisaccaridi proteine acidi
Costituenti chimici della materia vivente Le macromolecole biologiche Macromolecole (dal greco macros = grande) biologiche. Classi di composti biologici multifunzionali: Polisaccaridi proteine acidi
L ACQUA. Struttura e proprieta dell acqua
 L ACQUA Struttura e proprieta dell acqua (D. Voet, J.G. Voet, Biochemistry, 3 ed., John Wiley & Sons, 2004) Le proprietà del ghiaccio e dell acqua liquida sono in gran parte dovute alla presenza di legami
L ACQUA Struttura e proprieta dell acqua (D. Voet, J.G. Voet, Biochemistry, 3 ed., John Wiley & Sons, 2004) Le proprietà del ghiaccio e dell acqua liquida sono in gran parte dovute alla presenza di legami
Lo studio delle varie conformazioni del DNA
 Lo studio delle varie conformazioni del DNA Separazione dei topoisomeri Molecole di DNA ccc di una uguale lunghezza e composizione in basi, ma diverso Lk, sono dette topoisomeri. I topoisomeri possono
Lo studio delle varie conformazioni del DNA Separazione dei topoisomeri Molecole di DNA ccc di una uguale lunghezza e composizione in basi, ma diverso Lk, sono dette topoisomeri. I topoisomeri possono
Lezione 1: Atomi e molecole:
 Lezione 1: Atomi e molecole: La materia è costituita da elementi chimici in forma pura o in combinazioni dette composti. La vita richiede circa 25 elementi chimici. La struttura atomica determina il comportamento
Lezione 1: Atomi e molecole: La materia è costituita da elementi chimici in forma pura o in combinazioni dette composti. La vita richiede circa 25 elementi chimici. La struttura atomica determina il comportamento
1. Le biomolecole: Struttura e funzione delle proteine
 1. Le biomolecole: Struttura e funzione delle proteine Corso 240/350: Didattica di biochimica e biologia molecolare con laboratorio (2 CFU) 16 ore) Marco Scocchi ( BIO/10-11) Le biomolecole Biomolecola:
1. Le biomolecole: Struttura e funzione delle proteine Corso 240/350: Didattica di biochimica e biologia molecolare con laboratorio (2 CFU) 16 ore) Marco Scocchi ( BIO/10-11) Le biomolecole Biomolecola:
Farmacodinamica. Emilio Russo
 Farmacodinamica Emilio Russo Curve concentrazione-risposta Immediata valutazione dell azione biologica Nessuna informazione sul recettore Interferenza di fenomeni esterni (assorbimento, distribuzione
Farmacodinamica Emilio Russo Curve concentrazione-risposta Immediata valutazione dell azione biologica Nessuna informazione sul recettore Interferenza di fenomeni esterni (assorbimento, distribuzione
Biochimica delle proteine Prof. M. Bolognesi a.a. 2007/2008. Eloise Mastrangelo
 Biochimica delle proteine Prof. M. Bolognesi a.a. 2007/2008 Eloise Mastrangelo Perché è importante determinare la struttura primaria delle proteine? 1. La conoscenza della sequenza amminoacidica delle
Biochimica delle proteine Prof. M. Bolognesi a.a. 2007/2008 Eloise Mastrangelo Perché è importante determinare la struttura primaria delle proteine? 1. La conoscenza della sequenza amminoacidica delle
Aminoacidi e Proteine. Relazione Struttura-funzioni e fonti alimentari
 Aminoacidi e Proteine. Relazione Struttura-funzioni e fonti alimentari Proteine corporee 40% nel muscolo di cui 65% miosina ed actina per locomozione e lavoro muscolare, ma anche come fonte di amminoacidi
Aminoacidi e Proteine. Relazione Struttura-funzioni e fonti alimentari Proteine corporee 40% nel muscolo di cui 65% miosina ed actina per locomozione e lavoro muscolare, ma anche come fonte di amminoacidi
Riepilogo 1^ lezione
 Riepilogo 1^ lezione I 20 amminoacidi che si trovano comunemente nelle proteine sono uniti l uno all altro da legami peptidici. La sequenza lineare degli amminoacidi legati contiene l informazione necessaria
Riepilogo 1^ lezione I 20 amminoacidi che si trovano comunemente nelle proteine sono uniti l uno all altro da legami peptidici. La sequenza lineare degli amminoacidi legati contiene l informazione necessaria
La struttura terziaria delle proteine
 La struttura terziaria delle proteine 1 La struttura terziaria L arrangiamento spaziale degli aminoacidi di una singola catena polipeptidica a formare la sua struttura tridimensionale a domini viene chiamata
La struttura terziaria delle proteine 1 La struttura terziaria L arrangiamento spaziale degli aminoacidi di una singola catena polipeptidica a formare la sua struttura tridimensionale a domini viene chiamata
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA. Angela Chambery Lezione 5
 Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 5 Il legame peptidico Concetti chiave: In un polipeptide gli amminoacidi sono uniti dai legami peptidici. Il legame
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 5 Il legame peptidico Concetti chiave: In un polipeptide gli amminoacidi sono uniti dai legami peptidici. Il legame
CENNI SUL TIPO DI FORZE
 CENNI SUL TIPO DI FORZE Forze deboli che influenzano la struttura delle proteine: le interazioni di van der Waals repulsione attrazione Forze attrattive dovute a interazioni istantanee che si generano
CENNI SUL TIPO DI FORZE Forze deboli che influenzano la struttura delle proteine: le interazioni di van der Waals repulsione attrazione Forze attrattive dovute a interazioni istantanee che si generano
Proteine ed acidi nucleici
 Proteine ed acidi nucleici Prof.ssa Flavia Frabetti aa. 2010-11 PRTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (,,,
Proteine ed acidi nucleici Prof.ssa Flavia Frabetti aa. 2010-11 PRTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (,,,
Caratteristiche generali
 AMMINOACIDI Gli amminoacidi sono le unità costruttive (building blocks) delle proteine. Come dice il termine, gli amminoacidi naturali sono costituiti da un gruppo amminico (-NH 2 ) e da un gruppo carbossilico
AMMINOACIDI Gli amminoacidi sono le unità costruttive (building blocks) delle proteine. Come dice il termine, gli amminoacidi naturali sono costituiti da un gruppo amminico (-NH 2 ) e da un gruppo carbossilico
Nucleotidi e acidi nucleici
 Nucleotidi e acidi nucleici ACIDI NUCLEICI Biomolecole fondamentali per tutti gli organismi viventi Unici nella capacità di autoduplicazione Conservazione e trasmissione da una generazione all altra dell
Nucleotidi e acidi nucleici ACIDI NUCLEICI Biomolecole fondamentali per tutti gli organismi viventi Unici nella capacità di autoduplicazione Conservazione e trasmissione da una generazione all altra dell
Strategie catalitiche
 Strategie catalitiche catalisi acido-base catalisi covalente catalisi da metalli Dati molecolari di alcune proteine Citocromo C (umano) Ribonucleasi A (pancreas di bue) Lisozima (bianco dell uovo) Mioglobina
Strategie catalitiche catalisi acido-base catalisi covalente catalisi da metalli Dati molecolari di alcune proteine Citocromo C (umano) Ribonucleasi A (pancreas di bue) Lisozima (bianco dell uovo) Mioglobina
CONTROLLO E REGOLAZIONE DELLA TRADUZIONE. PROCARIOTI: trascrizione e traduzione avvengono nello stesso compartimento
 CONTROLLO E REGOLAZIONE DELLA TRADUZIONE PROCARIOTI: trascrizione e traduzione avvengono nello stesso compartimento EUCARIOTI:trascrizione e traduzione in compartimenti diversi RISPOSTA STRINGENTE LA SINTESI
CONTROLLO E REGOLAZIONE DELLA TRADUZIONE PROCARIOTI: trascrizione e traduzione avvengono nello stesso compartimento EUCARIOTI:trascrizione e traduzione in compartimenti diversi RISPOSTA STRINGENTE LA SINTESI
MACROMOLECOLE. Polimeri (lipidi a parte)
 MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
Le macromolecole dei tessuti - 1
 Le macromolecole dei tessuti - 1 Che cosa sono le proteine? Sono macromolecole complesse ad alta informazione Sono costituite da una o più catene polipeptidiche Ogni catena peptidica è composta da centinaia
Le macromolecole dei tessuti - 1 Che cosa sono le proteine? Sono macromolecole complesse ad alta informazione Sono costituite da una o più catene polipeptidiche Ogni catena peptidica è composta da centinaia
STRUTTURA E FUNZIONE DELLE
 STRUTTURA E FUNZIONE DELLE PROTEINE Compongono la STRUTTURA della cellula ma hanno anche altre FUNZIONI intelaiatura citoscheletrica strutture cellulari (organelli) impalcatura di sostegno extracellulare
STRUTTURA E FUNZIONE DELLE PROTEINE Compongono la STRUTTURA della cellula ma hanno anche altre FUNZIONI intelaiatura citoscheletrica strutture cellulari (organelli) impalcatura di sostegno extracellulare
materiale didattico disponibile su tozzini/didattica.html
 materiale didattico disponibile su http://homepage.sns.it/ tozzini/didattica.html Sommario Proteine Funzioni principali Legame peptidico Struttura primaria Struttura secondaria Struttura terziaria Struttura
materiale didattico disponibile su http://homepage.sns.it/ tozzini/didattica.html Sommario Proteine Funzioni principali Legame peptidico Struttura primaria Struttura secondaria Struttura terziaria Struttura
Modello del collasso idrofobico. Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60
 Modello gerarchico Modello del collasso idrofobico Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60 Le Hsp70 si legano ai segmenti idrofobici di
Modello gerarchico Modello del collasso idrofobico Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60 Le Hsp70 si legano ai segmenti idrofobici di
Chimica Biologica A.A α-elica foglietto β reverse turn
 Chimica Biologica A.A. 2010-2011 α-elica foglietto β reverse turn Str. Secondaria sperimentalmente osservata: Si distinguono fondamentalmente tre tipi di strutture secondarie: α elica foglietto β reverse
Chimica Biologica A.A. 2010-2011 α-elica foglietto β reverse turn Str. Secondaria sperimentalmente osservata: Si distinguono fondamentalmente tre tipi di strutture secondarie: α elica foglietto β reverse
9) Scrivere un disaccaride formato dal β-d-galattosio e dall α-d-n-acetil-glucosammina legati da un legame glicosidico β(1-4).
 CARBOIDRATI - AMMINOACIDI - PROTEINE 1) Scrivere la proiezione di Fisher del D-ribosio e del D-glucosio. La lettera D a cosa si riferisce? Disegnare inoltre il disaccaride ottenuto dalla condensazione
CARBOIDRATI - AMMINOACIDI - PROTEINE 1) Scrivere la proiezione di Fisher del D-ribosio e del D-glucosio. La lettera D a cosa si riferisce? Disegnare inoltre il disaccaride ottenuto dalla condensazione
20/12/ tipi di amino acidi: parecchie combinazioni
 20 tipi di amino acidi: parecchie combinazioni Le proteine sono polimeri di amino acidi 1 SEMPLICI : costituite solo da amino acidi PROTEINE CONIUGATE Apoproteina = parte proteica Gruppo prostetico = parte
20 tipi di amino acidi: parecchie combinazioni Le proteine sono polimeri di amino acidi 1 SEMPLICI : costituite solo da amino acidi PROTEINE CONIUGATE Apoproteina = parte proteica Gruppo prostetico = parte
