ANALISI CHIMICA QUALITATIVA
|
|
|
- Michele Poli
- 7 anni fa
- Visualizzazioni
Transcript
1 ANALISI CHIMICA QUALITATIVA Analisi per via secca: Saggi alla fiamma Scopo dell esperimento: Riconoscimento della presenza di alcuni elementi per via secca Premessa teorica: I saggi per via secca, così detti perché si eseguono a partire direttamente dalla sostanza iniziale, sono saggi preliminari, e forniscono utili informazioni sulla presenza di alcuni ioni nel campione analizzato. Il saggio alla fiamma è un analisi spettroscopica, il cui mezzo di riscaldamento è appunto la fiamma. Possono essere rivelati con quest analisi solo quegli elementi, le cui radiazioni elettromagnetiche cadono nel campo del visibile. Quando all atomo di un dato elemento viene ceduta energia (calore), gli elettroni di quest atomo, si spostano da un livello energetico più basso, a uno più alto. In seguito, l elettrone ritorna sul livello precedente, liberando l energia accumulata in precedenza, sotto forma di radiazione elettromagnetica. Per esempio, la colorazione gialla del sodio è dovuta alla transizione elettronica dall orbitale 3s al 3p, cui corrisponde l emissione di una lunghezza d onda di 589 nm. Materiale occorrente: Becco Bunsen Filo al Nichel-Cromo Acido cloridrico (HCl) Elementi da analizzare Vetrino al cobalto Descrizione dell esperimento: I saggi si conducono immergendo un filo di Nickel-Cromo, pulito con HCl, nel campione da analizzare, in modo tale da farne aderire uno o due cristalli ed esponendoli alla fiamma del Becco Bunsen. Si osserva così la colorazione assunta dalla fiamma, e dal colore, si può risalire all elemento che ha generato questa colorazione. È bene porre il filo prima nella zona bassa della fiamma del Bunsen, poi pian piano, spostarlo nella zona alta. In certi casi può essere necessario l utilizzo di un vetrino al cobalto, per filtrare la radiazione giallo-arancio, caratteristica soprattutto del Sodio. Questo si rende necessario, perché alcuni Sali, come il Potassio, hanno una colorazione molto debole, che viene, se presente, coperta da quella del sodio. L utilizzo del vetrino al cobalto, permette il riconoscimento degli elementi più deboli, in quanto appunto, elimina la radiazione del sodio. Ione Litio Sodio Potassio Calcio Stronzio Bario Colore Rosso - carminio Giallo intenso Violetto Rosso-Arancio Rosso porpora Verde Questo esperimento non ha recato problemi di esecuzione, ed è stato già da subito positivo. 1
2 Analisi degli Anioni Scopo dell esperimento: Riconoscimento della presenza di alcuni Anioni Premessa teorica: L analisi degli anioni, permette appunto di verificare se in un dato elemento è presente o meno un dato anione. Un anione è un atomo che ha acquistato degli elettroni (Cl -, F -, O -2, N -3 ), quindi, tramite queste prove, si può verificare il tipo di sale (cloruro, solfato, solfito ). Materiale occorrente: Acetato (Na, K) CH 3 COONa, CH 3 COOK Bisolfito di potassio KHSO 4 Carbonato (Na) Na 2 CO 3 Acido cloridrico (2 M) HCl Idrossido di Bario Ba(OH) 2 Acido acetico CH 3 COOH Solfito (Na) Na 2 SO 3 Solfuro (Fe) Fe 2 S 3 Bicromato di potassio K 2 Cr 2 O 7 Acetato di piombo (CH 3 COO) 2 Pb Provette Tubo a squadra Spatola Becco Bunsen Vetrino da orologio Descrizione dell esperimento: 1. Acetato: Con l aiuto di una spatola, si pone in un vetrino da orologio la sostanza iniziale (CH 3 COONa oppure CH 3 COOK), con il doppio di KHSO 4 solido e 1 goccia di acqua. Con il retro della spatola, di schiaccia la miscela così ottenuta; un odore caratteristico di acido acetico, indica la presenza di un acetato. 2 CH 3 COONa + 2 KHSO 4 2 CH 3 COOH + K 2 SO 4 + Na 2 SO 4 CH 3 COOK + KHSO 4 CH 3 COOH + K 2 SO 4 2
3 2. Carbonato: Si pone, con l ausilio di una spatola, una leggera quantità di sostanza da analizzare (Na 2 CO 3 ), in una provetta. Si pongono nella provetta circa 1 o 2 ml di HCl o H 2 SO 4 diluiti. Si chiude ermeticamente con il tubo a squadra, avendo cura di far pescare contemporaneamente l altra estremità del tubo in un altra provetta, contenente qualche ml di una soluzione di Ba(OH) 2. Si scalda leggermente la prima provetta, con il Bunsen in fiamma riducente, in modo da facilitare lo sviluppo di CO 2. La CO 2 sviluppata, viene fatta gorgogliare nell acqua di barite, che, a contatto con essa, reagisce, formando carbonato di bario ( BaCO 3 ), che precipita. A questo punto, si aggiunge qualche goccia di acido acetico, se avviene la completa dissoluzione del precipitato, il campione iniziale, era sicuramente un carbonato. Quest ultima fase, serve perché le due reazioni precedenti, sono positive, anche con i solfiti e i tiosolfati, che però danno un precipitato insolubile in acido acetico. Na 2 CO HCl 2 NaCl + CO 2 + H 2 O CO 2 + Ba(OH) 2 BaCO 3 + H 2 O BACO 3 + CH 3 COOH Ba(CH 3 COO) 2 + CO 2 + H 2 O 3. Solfito: Si pone in una provetta una piccola quantità di sostanza da analizzare (Na 2 SO 3) con 1 ml di HCl. Riscaldando la provetta, si facilità la liberazione di SO 2. Per verificare la presenza di anidride solforosa, si pone sull imboccatura della provetta, una cartina, imbevuta di soluzione di bicromato di potassio. Se avviene una liberazione di SO 2, la cartina, da color arancio, diventerà verde. 4. Solfuro: Na 2 SO HCl 2 NaCl + SO 2 + H 2 O K 2 Cr 2 O SO HCl Cr 2 (SO 4 ) 3 verde + 2 KCl + H 2 O Si pone in una provetta una piccola quantità di sostanza da analizzare (Fe 2 S 3 ), si aggiunge qualche goccia di HCl, e si riscalda il tutto. Da questa reazione si libera H 2 S. la presenza di questo gas, si può verificare in due modi: Semplicemente riconoscendo il classico odore di uova marce, caratteristico di questo gas. Ponendo sull imboccatura della provetta una cartina imbevuta di (CH 3 COO) 2 Pb, che a contatto con l H 2 S, forma solfuro di piombo, di colore nero. Fe 2 S HCl 3 H 2 S + 2 FeCl 3 H 2 S + (CH 3 COO) 2 Pb PbS nero + 2 CH 3 COOH Questi esperimenti, generalmente, non hanno recato alcun problema di esecuzione, essendo positivi al primo tentativo. 3
4 Analisi dei Cationi Scopo dell esperimento: Riconoscimento della presenza di alcuni Cationi Premessa teorica: L analisi dei cationi permette appunto di verificare se in un dato elemento è presente o meno un dato catione. Un catione è un atomo che ha ceduto degli elettroni (Na +, Li +, NH 4 +, Be +2 ), quindi, tramite queste prove, si può verificare la presenza di un elemento in un composto. Queste analisi sono utili, non solo in chimica, ma anche in molte altre discipline, come la geologia, dove sono utilizzate per riconoscere certe rocce o certi minerali. Materiale occorrente: Ammonio (cloruro) NH 4 Cl Acido Nitrico HNO 3 Idrossido d ammonio NH 4 OH Dimetilgliossima 2 (CH 3 CNOH) 2 Idrossido di sodio NaOH Ferro (cloruro) FeCl 3 Solfocianuro (K) KSCN Ferrocianuro di potassio K 4 [Fe(CN) 6 ] Piombo (nitrato) Pb(NO 3 ) 2 Ioduro di potassio KI Provette Cartina al tornasole Pipetta Descrizione dell esperimento: 1. Ammonio: Con l aiuto di una pipetta, si pone in una provetta la sostanza da analizzare (NH 4 Cl). Con un altra pipetta si aggiunge qualche goccia di NaOH diluita. La reazione produce cloruro di sodio, acqua e ammoniaca. Ponendo sull imboccatura della provetta un pezzo di cartina al tornasole, si può notare come l ammoniaca gassosa faccia virare il colore della cartina, verificando la presenza di ammoniaca, e quindi di ammonio. NH 4 Cl + NaOH NaCl + NH 3 + H 2 O 4
5 2. Ferro: Per questo riconoscimento, si possono usare due reattivi: K 4 [Fe(CN) 6 ] oppure KSCN. Si pone, con l ausilio di una pipetta, qualche ml di sostanza da analizzare (FeCl 3 ), in una provetta. Si aggiunge nella provetta qualche goccia di K 4 [Fe(CN) 6 ] oppure KSCN. In caso di presenza di ferro, la soluzione si colorerà o di rosso, se si è utilizzato il KSCN, altrimenti si colorerà di blu, se si è utilizzato il K 4 [Fe(CN) 6 ]. 3. Piombo: FeCl 3 + KSCN Fe(SCN) 3 (rosso) + 3 HCl 4 FeCl K 4 [Fe(CN) 6 ] 12 KCl + Fe 4 [Fe(CN) 6 ] 3 (blu di Prussia) Si pone, con l ausilio di una pipetta, qualche ml di sostanza da analizzare (Pb(NO 3 ) 2 ), in una provetta. Si aggiunge nella provetta qualche goccia di KI. In caso di presenza di piombo, si formerà un precipitato giallo intenso di PbI Nichel: Pb(NO 3 ) KI PbI KNO 3 I Sali del nichel (Ni 2+ ), in questo caso nitrato di nichel, trattati in ambiente ammoniacale con aggiunta del reagente Dimetilgliossima (usato in soluzione alcolica), danno un precipitato rossofragola di un complesso interno Ni-dimetilgliossima: Ni + 4 HNO 3 Ni(NO 3 ) NO H 2 O Ni(NO 3 ) NH 3 OH + 2(CH 3 CNOH) 2 (CH 3 CNOH) 2 Ni(CH 3 CNO) 2 (rosa) + 2 NH 4 NO H 2 O Questi esperimenti, come quelli concernenti gli anioni, generalmente, non hanno recato alcun problema di esecuzione, essendo positivi al primo tentativo. 5
6 Meteorite Meteorite certo 100 % Durante la reazione con HNO 3 si nota una vivace effervescenza. Colorazione della soluzione di giallo, caratteristico del nitrato ferroso Evidente liberazione di vapori di NO 2 Reagisce positivamente sia con il K 4 [Fe(CN) 6 ] che con il KSCN. Meteorite Test Durante la reazione con HNO 3 non si nota un effervescenza. Colorazione della soluzione di ruggine Liberazione di vapori di NO 2 assente Reagisce positivamente sia con il K 4 [Fe(CN) 6 ] che con il KSCN. Fe + 6 HNO 3 Fe(NO 3 ) NO 2 (vapori rossi) + 3 H 2 O FeCl 3 + KSCN Fe(SCN) 3 (rosso) + 3 HCl 4 FeCl K 4 [Fe(CN) 6 ] 12 KCl + Fe 4 [Fe(CN) 6 ] 3 (blu di Prussia) Dopo aver eseguito la reazione per verificare la presenza del ferro e del nickel, si può concludere che il campione analizzato, non sia un meteorite, perché la prova del ferro è risultata leggermente positiva, mentre quella del nichel, totalmente negativa. 6
7 Preparazione del campione Reazione del ferro con ferrocianuro di K Reazione del Nichel in ambiente ammoniacale con dimetilgliossima Campione esaminato: Meteorite 7
PRIMA ESPERIENZA DI LABORATORIO. Prof. Antonio Lavecchia
 PRIMA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Prima Esperienza di Laboratorio Analisi Qualitativa Elementare di Sostanze Inorganiche (Via Umida e Via Secca) Ricerca dei Cationi Calcio, Magnesio,
PRIMA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Prima Esperienza di Laboratorio Analisi Qualitativa Elementare di Sostanze Inorganiche (Via Umida e Via Secca) Ricerca dei Cationi Calcio, Magnesio,
RICONOSCIMENTO degli ELEMENTI PRESENTI in un CAMPIONE INCOGNITO
 RICONOSCIMENTO degli ELEMENTI PRESENTI in un CAMPIONE INCOGNITO OBIETTIVO: individuare gli elementi presenti in un campione solido inorganico di composizione incognita. Approccio al problema: l analisi
RICONOSCIMENTO degli ELEMENTI PRESENTI in un CAMPIONE INCOGNITO OBIETTIVO: individuare gli elementi presenti in un campione solido inorganico di composizione incognita. Approccio al problema: l analisi
RICERCA RICERCA DEGLI ANIONI
 RICERCA DEGLI ANIONI 1 SOSTANZA INIZIALE Na 2 CO 3 Ricerca: ACETATI SOLFITI CARBONATI TARTRATI SOLUZIONE ALCALINA Limpida Incolore RESIDUO Si scarta Ricerca: SOLFATI OSSALATI ARSENIATI NITRITI NITRATI
RICERCA DEGLI ANIONI 1 SOSTANZA INIZIALE Na 2 CO 3 Ricerca: ACETATI SOLFITI CARBONATI TARTRATI SOLUZIONE ALCALINA Limpida Incolore RESIDUO Si scarta Ricerca: SOLFATI OSSALATI ARSENIATI NITRITI NITRATI
ESAME DI ANALISI DELLE SOSTANZE INORGANICHE DI IMPIEGO FARMACEUTICO + LABORATORIO DI ANALISI QUALITATIVA. Nome e cognome: Numero di matricola:..
 ESAME DI ANALISI DELLE SOSTANZE INORGANICHE DI IMPIEGO FARMACEUTICO + LABORATORIO DI ANALISI QUALITATIVA Nome e cognome: Numero di matricola:.. 1) Indicare, motivando la risposta, il ph di una soluzione
ESAME DI ANALISI DELLE SOSTANZE INORGANICHE DI IMPIEGO FARMACEUTICO + LABORATORIO DI ANALISI QUALITATIVA Nome e cognome: Numero di matricola:.. 1) Indicare, motivando la risposta, il ph di una soluzione
RICERCA DEGLI ANIONI
 RICERCA DEGLI ANIONI RICERCA DEGLI ANIONI SOSTANZA INIZIALE via secca via umida (soluzione alcalina) Ricerca: ACETATI CARBONATI TARTRATI SOLFITI SOLUZIONE Limpida Incolore RESIDUO Si scarta Ricerca: CLORURI
RICERCA DEGLI ANIONI RICERCA DEGLI ANIONI SOSTANZA INIZIALE via secca via umida (soluzione alcalina) Ricerca: ACETATI CARBONATI TARTRATI SOLFITI SOLUZIONE Limpida Incolore RESIDUO Si scarta Ricerca: CLORURI
PRIMA ESPERIENZA DI LABORATORIO. Prof. Antonio Lavecchia
 PRIMA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Prima Esperienza di Laboratorio Analisi Qualitativa Elementare di Sostanze Inorganiche (Via Umida) Ricerca dei Cationi Calcio, magnesio Ricerca degli
PRIMA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Prima Esperienza di Laboratorio Analisi Qualitativa Elementare di Sostanze Inorganiche (Via Umida) Ricerca dei Cationi Calcio, magnesio Ricerca degli
RICERCA DEI CATIONI NELLE SOSTANZE INORGANICHE O ORGANO-METALLICHE RICERCA DEGLI ANIONI NEI SALI DI AMMINE O DI AMMONIO QUATERNARIO
 RICERCA DEI CATIONI NELLE SOSTANZE INORGANICHE O ORGANO-METALLICHE RICERCA DEGLI ANIONI NEI SALI DI AMMINE O DI AMMONIO QUATERNARIO Prof. Antonio Lavecchia Ricerca dei Cationi nelle Sostanze Inorganiche
RICERCA DEI CATIONI NELLE SOSTANZE INORGANICHE O ORGANO-METALLICHE RICERCA DEGLI ANIONI NEI SALI DI AMMINE O DI AMMONIO QUATERNARIO Prof. Antonio Lavecchia Ricerca dei Cationi nelle Sostanze Inorganiche
Fe(OH) 3. Mn(OH) 2 2H 2 O
 III Gruppo: Comprende quei cationi che precipitano selettivamente come idrossidi insolubili a ph = 9 (esclusi quelli del I e II Gruppo). Il reattivo precipitante è NH 4 OH/NH 4 Cl (soluzione tampone a
III Gruppo: Comprende quei cationi che precipitano selettivamente come idrossidi insolubili a ph = 9 (esclusi quelli del I e II Gruppo). Il reattivo precipitante è NH 4 OH/NH 4 Cl (soluzione tampone a
Fe(OH) 3. Mn(OH) 2. bianco. MnO 2 2H 2 O
 III Gruppo: Comprende quei cationi che precipitano selettivamente come idrossidi insolubili a ph = 9 (esclusi quelli del I e II Gruppo). Il reattivo precipitante è NH 4 OH/NH 4 Cl (soluzione tampone a
III Gruppo: Comprende quei cationi che precipitano selettivamente come idrossidi insolubili a ph = 9 (esclusi quelli del I e II Gruppo). Il reattivo precipitante è NH 4 OH/NH 4 Cl (soluzione tampone a
Università degli Studi di Torino CORSO DI CHIMICA GENERALE ED INORGANICA C. Schede di valutazione relative alle esercitazioni pratiche in laboratorio
 Università degli Studi di Torino CORSO DI CHIMICA GENERALE ED INORGANICA C Schede di valutazione relative alle esercitazioni pratiche in laboratorio Anno accademico 2006-2007 Dott.ssa Elena Ghibaudi Dott.
Università degli Studi di Torino CORSO DI CHIMICA GENERALE ED INORGANICA C Schede di valutazione relative alle esercitazioni pratiche in laboratorio Anno accademico 2006-2007 Dott.ssa Elena Ghibaudi Dott.
Esame (0) - solubilità dei composti e reaz - Codice Prova:
 1) Ci si aspetta la formazione di un precipitato quando una soluzione acquosa di ioduro di potassio è aggiunta ad una soluzione acquosa di: A. idrossido di bario B. perclorato di piombo C. cloruro di ferro(ii)
1) Ci si aspetta la formazione di un precipitato quando una soluzione acquosa di ioduro di potassio è aggiunta ad una soluzione acquosa di: A. idrossido di bario B. perclorato di piombo C. cloruro di ferro(ii)
Chimica Generale. Reazioni Chimiche. Reazioni Chimiche
 Una reazione chimica è un processo in cui avviene un cambiamento chimico di uno o più composti, detti reagenti, che vengono convertiti in una nuova serie di composti detti prodotti. Spesso le reazioni
Una reazione chimica è un processo in cui avviene un cambiamento chimico di uno o più composti, detti reagenti, che vengono convertiti in una nuova serie di composti detti prodotti. Spesso le reazioni
Reazioni analitiche dello ione acetato
 Reazioni analitiche dello ione acetato Gli acetati trattati con acidi più forti dell acido acetico formano acido acetico, un liquido incolore, volatile che odora di aceto. Il composto generalmente utilizzato
Reazioni analitiche dello ione acetato Gli acetati trattati con acidi più forti dell acido acetico formano acido acetico, un liquido incolore, volatile che odora di aceto. Il composto generalmente utilizzato
ANALISI SISTEMATICA DEI CATIONI
 ANALISI SISTEMATICA DEI CATIONI Particolare procedura analitica attraverso la quale tutte le specie cationiche presenti in una ipotetica miscela vengono inizialmente separate in gruppi, mediante l uso
ANALISI SISTEMATICA DEI CATIONI Particolare procedura analitica attraverso la quale tutte le specie cationiche presenti in una ipotetica miscela vengono inizialmente separate in gruppi, mediante l uso
 ANALISI QUALITATIVA INORGANICA Analisi per via secca (senza solvente) analisi di emissione (saggi alla fiamma) - reazioni allo stato fuso (saggi alla perla) comportamento al riscaldamento (senza e con
ANALISI QUALITATIVA INORGANICA Analisi per via secca (senza solvente) analisi di emissione (saggi alla fiamma) - reazioni allo stato fuso (saggi alla perla) comportamento al riscaldamento (senza e con
IV Gruppo: H 2 S 2 H + + S = I solfuri insolubili nelle predette condizioni sono: ZnS. CoS. bianco. nero. MnS. rosa-salmone. nero.
 IV Gruppo: Comprende quei cationi che precipitano selettivamente come solfuri insolubili a ph = 9 in soluzione tampone: NH 4 OH/NH 4 Cl (esclusi quelli del I, II e III Gruppo). Il reattivo precipitante
IV Gruppo: Comprende quei cationi che precipitano selettivamente come solfuri insolubili a ph = 9 in soluzione tampone: NH 4 OH/NH 4 Cl (esclusi quelli del I, II e III Gruppo). Il reattivo precipitante
IV Gruppo: I solfuri insolubili nelle predette condizioni sono: ZnS. CoS. bianco. nero. MnS. nero. rosa-salmone. NiS
 IV Gruppo: Comprende quei cationi che precipitano selettivamente come solfuri insolubili a ph = 9 in soluzione tampone: NH 4 OH/NH 4 Cl (esclusi quelli del I, II e III Gruppo). Il reattivo precipitante
IV Gruppo: Comprende quei cationi che precipitano selettivamente come solfuri insolubili a ph = 9 in soluzione tampone: NH 4 OH/NH 4 Cl (esclusi quelli del I, II e III Gruppo). Il reattivo precipitante
Reazioni analitiche dello ione alluminio L ammoniaca in soluzione acquosa provoca la precipitazione dell idrossido Al(OH) 3 bianco gelatinoso.
 Reazioni analitiche dello ione alluminio L ammoniaca in soluzione acquosa provoca la precipitazione dell idrossido Al(OH) bianco gelatinoso. Al NHOH Al(OH) NH L idrossido precipitato è quasi insolubile
Reazioni analitiche dello ione alluminio L ammoniaca in soluzione acquosa provoca la precipitazione dell idrossido Al(OH) bianco gelatinoso. Al NHOH Al(OH) NH L idrossido precipitato è quasi insolubile
II Gruppo: CH 3 - C + H 2 O CH 3 - C + H 2 S CH 3 - C + NH 4 OH TAA
 II Gruppo: Comprende quei cationi che precipitano selettivamente come solfuri insolubili nell intervallo di ph = 0 2 per HCl (esclusi quelli del I Gruppo). Il reattivo precipitante è la solfuro d ammonio
II Gruppo: Comprende quei cationi che precipitano selettivamente come solfuri insolubili nell intervallo di ph = 0 2 per HCl (esclusi quelli del I Gruppo). Il reattivo precipitante è la solfuro d ammonio
Reazioni in soluzione acquosa
 Reazioni in soluzione acquosa Soluzioni, solvente e soluto Elettroliti Dissoluzione e solvatazione di elettroliti Equazioni chimiche Equazioni ioniche Concentrazione di soluzioni Reazioni di precipitazione
Reazioni in soluzione acquosa Soluzioni, solvente e soluto Elettroliti Dissoluzione e solvatazione di elettroliti Equazioni chimiche Equazioni ioniche Concentrazione di soluzioni Reazioni di precipitazione
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
COMPORTAMENTO DI SALI CONTENENTI PARTICOLARI CATIONI IN SEGUITO A TRATTAMENTO CON COMPLESSANTI, BASI ED ACIDI
 COMPORTAMENTO DI SALI CONTENENTI PARTICOLARI CATIONI IN SEGUITO A TRATTAMENTO CON COMPLESSANTI, BASI ED ACIDI Perché le soluzioni dei cationi metallici di partenza sono acide. Una volta sciolto un sale
COMPORTAMENTO DI SALI CONTENENTI PARTICOLARI CATIONI IN SEGUITO A TRATTAMENTO CON COMPLESSANTI, BASI ED ACIDI Perché le soluzioni dei cationi metallici di partenza sono acide. Una volta sciolto un sale
Esperienza n. 1 PREVISIONE E RICONOSCIMENTO DI ALCUNE REAZIONI DI METATESI.
 Corso di Laboratorio di Chimica Generale Esperienza n. 1 PREVISIONE E RICONOSCIMENTO DI ALCUNE REAZIONI DI METATESI. REAZIONI IN SOLUZIONE 1 Alcuni tipi di reazioni ioniche, che non implichino processi
Corso di Laboratorio di Chimica Generale Esperienza n. 1 PREVISIONE E RICONOSCIMENTO DI ALCUNE REAZIONI DI METATESI. REAZIONI IN SOLUZIONE 1 Alcuni tipi di reazioni ioniche, che non implichino processi
STECHIOMETRIA 1) Nella sintesi del Bianco S.Giovanni (CaCO 3 ) secondo la reazione CaCl 2 + Na 2 CO 3 = 2NaCl + CaCO 3 partendo da 8,3g (0,038 mol)
 STECHIOMETRIA 1) Nella sintesi del Bianco S.Giovanni (CaCO 3 ) secondo la reazione CaCl 2 + Na 2 CO 3 = 2NaCl + CaCO 3 partendo da 8,3g (0,038 mol) di cloruro di Calcio biidrato e 14,3g (0,050 mol) di
STECHIOMETRIA 1) Nella sintesi del Bianco S.Giovanni (CaCO 3 ) secondo la reazione CaCl 2 + Na 2 CO 3 = 2NaCl + CaCO 3 partendo da 8,3g (0,038 mol) di cloruro di Calcio biidrato e 14,3g (0,050 mol) di
Problema 1 Mg + 2HCl H 2 + MgCl 2. di Mg 1 Mg 1 H 2 quindi 0,823 moli di H 2 di H 2
 REAZIONI CHIMICHE 1. Con riferimento alla seguente reazione (da bilanciare): Mg + HCl H 2 + MgCl 2 calcolare i grammi di H 2 che si ottengono facendo reagire completamente 20 g di magnesio. utilizzando
REAZIONI CHIMICHE 1. Con riferimento alla seguente reazione (da bilanciare): Mg + HCl H 2 + MgCl 2 calcolare i grammi di H 2 che si ottengono facendo reagire completamente 20 g di magnesio. utilizzando
CAPITOLO 12 EQUILIBRI ACIDO-BASE E SOLUBILITA
 CAPITOLO 12 EQUILIBRI ACIDO-BASE E SOLUBILITA 12.1 (a) ph = 2,57 (b) ph = 4,44 12.3 (a) no. (b) no. (c) sì. (d) sì. (e) no. 12.5 ph = 8,88 12.7 0,024 12.9 0,58 12.11 ph = 9,25; ph = 9,18. 12.13 Na 2 A/NaHA.
CAPITOLO 12 EQUILIBRI ACIDO-BASE E SOLUBILITA 12.1 (a) ph = 2,57 (b) ph = 4,44 12.3 (a) no. (b) no. (c) sì. (d) sì. (e) no. 12.5 ph = 8,88 12.7 0,024 12.9 0,58 12.11 ph = 9,25; ph = 9,18. 12.13 Na 2 A/NaHA.
ESERCIZI DI RIEPILOGO GENERALE
 ESERCIZI DI RIEPILOGO GENERALE 1) Scrivere le formule brute e le formule di Lewis per: ammoniaca; ione ammonio; ione solfato; ione bicarbonato; acido acetico; anidride solforosa. Dove necessario, indicare
ESERCIZI DI RIEPILOGO GENERALE 1) Scrivere le formule brute e le formule di Lewis per: ammoniaca; ione ammonio; ione solfato; ione bicarbonato; acido acetico; anidride solforosa. Dove necessario, indicare
Atomi, Molecole e Ioni. Capitolo 2
 Atomi, Molecole e Ioni Capitolo 2 La Teoria Atomica di Dalton (1808) 1. Gli Elementi sono composti da particelle estremamente piccole, denominate atomi. 2. Tutti gli atomi di un dato elemento sono identici
Atomi, Molecole e Ioni Capitolo 2 La Teoria Atomica di Dalton (1808) 1. Gli Elementi sono composti da particelle estremamente piccole, denominate atomi. 2. Tutti gli atomi di un dato elemento sono identici
D Docenti : Giuseppe Pantano e Daniele Bianchi A.S. 2018/19 DISCIPLINA: Scienze Integrate Chimica
 Tel. 0331 635718 fax 0331 679586 info@isisfacchinetti.gov.it https://isisfacchinetti.gov.it ISIS C. Facchinetti Sede: via Azimonti, 5-21053 Castellanza PROGRAMMA SVOLTO E RELAZIONE FINALE DEL DOCENTE Rev.
Tel. 0331 635718 fax 0331 679586 info@isisfacchinetti.gov.it https://isisfacchinetti.gov.it ISIS C. Facchinetti Sede: via Azimonti, 5-21053 Castellanza PROGRAMMA SVOLTO E RELAZIONE FINALE DEL DOCENTE Rev.
I PROVA INCOGNITA. Cognome.. Nome. corso. Pesafiltri n...
 Cognome.. I PROVA INCOGNITA Nome. corso. Pesafiltri n... Cationi Data Anioni Firma 1 MISCELA INCOGNITA PbCO 3 CuCl 2 Co(NO 3 ) 2 SrCO 3 Piombo carbonato Cloruro rameico Cobalto nitrato Stronzio carbonato
Cognome.. I PROVA INCOGNITA Nome. corso. Pesafiltri n... Cationi Data Anioni Firma 1 MISCELA INCOGNITA PbCO 3 CuCl 2 Co(NO 3 ) 2 SrCO 3 Piombo carbonato Cloruro rameico Cobalto nitrato Stronzio carbonato
Sostanze inorganiche: determinazioni qualitative
 Carbonati e Bicarbonati Indicare il tipo di sostanza basandosi sulle caratteristiche alla calcinazione e le prove di solubilità e il ph. Sodio carbonato anidro Na 2 CO 3 (F.U. X Edizione, European Pharmacopeia
Carbonati e Bicarbonati Indicare il tipo di sostanza basandosi sulle caratteristiche alla calcinazione e le prove di solubilità e il ph. Sodio carbonato anidro Na 2 CO 3 (F.U. X Edizione, European Pharmacopeia
I PROVA INCOGNITA. Cognome.. Nome. corso. Pesafiltri n...
 Cognome.. I PROVA INCOGNITA Nome. corso. Pesafiltri n... Cationi Data Anioni Firma MISCELA INCOGNITA 4 cationi e 3 anioni PbCO 3 CuCl 2 Co(NO 3 ) 2 SrCO 3 Piombo carbonato Cloruro rameico Cobalto nitrato
Cognome.. I PROVA INCOGNITA Nome. corso. Pesafiltri n... Cationi Data Anioni Firma MISCELA INCOGNITA 4 cationi e 3 anioni PbCO 3 CuCl 2 Co(NO 3 ) 2 SrCO 3 Piombo carbonato Cloruro rameico Cobalto nitrato
24. PRECIPITAZIONE Prodotto di solubilità (K s )
 24. PRECIPITAZIONE D. In un racconto di Primo Levi, a proposito di un analisi chimica di campioni di roccia, si incontrano queste parole apparentemente prive di senso: «... giù il ferro con ammoniaca,
24. PRECIPITAZIONE D. In un racconto di Primo Levi, a proposito di un analisi chimica di campioni di roccia, si incontrano queste parole apparentemente prive di senso: «... giù il ferro con ammoniaca,
Il numero di ossidazione
 Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
CALCOLO DEL ph. ph = - log [1,0x10-3 ] = 3,00
![CALCOLO DEL ph. ph = - log [1,0x10-3 ] = 3,00 CALCOLO DEL ph. ph = - log [1,0x10-3 ] = 3,00](/thumbs/68/59131328.jpg) CALCOLO DEL ph Calcolare il ph di una soluzione di HCl 1,0x10-3 M HCl acido forte che si dissocia completamente HCl H + + Cl - 1 mol di HCl produce 1 mol di H + ph = - log [1,0x10-3 ] = 3,00 Tipici acidi
CALCOLO DEL ph Calcolare il ph di una soluzione di HCl 1,0x10-3 M HCl acido forte che si dissocia completamente HCl H + + Cl - 1 mol di HCl produce 1 mol di H + ph = - log [1,0x10-3 ] = 3,00 Tipici acidi
LA TERRA E LA CHIMICA: LA TAVOLA PERIODICA DEGLI ELEMENTI ELEMENTI E COMPOSTI
 I.I.S. A. PACINOTTI IST. TECNICO STATALE INDUSTRIALE Antonio PACINOTTI IST. TECNICO STATALE per GEOMETRI "Giorgio MASSARI" http://www.iispacinottive.it/ Via Caneve, n. 93 30173 - Mestre (VE) tel. 041 5350355
I.I.S. A. PACINOTTI IST. TECNICO STATALE INDUSTRIALE Antonio PACINOTTI IST. TECNICO STATALE per GEOMETRI "Giorgio MASSARI" http://www.iispacinottive.it/ Via Caneve, n. 93 30173 - Mestre (VE) tel. 041 5350355
Il numero di ossidazione
 Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
Il numero di ossidazione
 Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
Il numero di ossidazione Il numero di ossidazione è una carica positiva o negativa che viene attribuita formalmente a ciascun elemento in un composto. Esso viene determinato dal numero di elettroni in
scheda di lavoro relativa all'esperienza di laboratorio: REAZIONI FRA IONI IN SOLUZIONE ACQUOSA Scopo dell'esperienza: verificare la formazione di...
 scheda di lavoro relativa all'esperienza di laboratorio: REAZIONI FRA IONI IN SOLUZIONE ACQUOSA Scopo dell'esperienza: verificare la formaz di... Prerequisiti: :.. composto ionico:.. reazioni di doppio
scheda di lavoro relativa all'esperienza di laboratorio: REAZIONI FRA IONI IN SOLUZIONE ACQUOSA Scopo dell'esperienza: verificare la formaz di... Prerequisiti: :.. composto ionico:.. reazioni di doppio
ANALISI ORGANICA Saggi preliminari
 ANALISI ORGANICA Le sostanze ORGANICHE sono per buona parte molecole strutturalmente complesse e a volte abbastanza simili tra di loro. Inoltre, il loro numero è grande per cui eseguire l identificazione
ANALISI ORGANICA Le sostanze ORGANICHE sono per buona parte molecole strutturalmente complesse e a volte abbastanza simili tra di loro. Inoltre, il loro numero è grande per cui eseguire l identificazione
Le reazioni chimiche
 Le reazioni chimiche Gli alunni del laboratorio scientifico: Matilde, Gianmarco, Gloria, Matteo, Alexandru, Cristiano, Simone e Samuele (classe IA) Michele e Simone (classe IIA) a.s. 2011/2012 Scuola Secondaria
Le reazioni chimiche Gli alunni del laboratorio scientifico: Matilde, Gianmarco, Gloria, Matteo, Alexandru, Cristiano, Simone e Samuele (classe IA) Michele e Simone (classe IIA) a.s. 2011/2012 Scuola Secondaria
SOSTANZE INORGANICHE
 SOSTANZE INORGANICHE Na2B4O7 Na2HPO4 H3BO3 La soluzione acquosa, trattata con AgNO3 dà un precipitato solubile in HNO3 conc. Indicazioni Generali La sol. acq. si tratta a freddo con alcune gocce di AgNO3.
SOSTANZE INORGANICHE Na2B4O7 Na2HPO4 H3BO3 La soluzione acquosa, trattata con AgNO3 dà un precipitato solubile in HNO3 conc. Indicazioni Generali La sol. acq. si tratta a freddo con alcune gocce di AgNO3.
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Lezione 4. Le soluzioni Acidi e Basi Reazioni Chimiche La Concentrazione delle Soluzioni
 2018 Lezione 4. Le soluzioni Acidi e Basi Reazioni Chimiche La Concentrazione delle Soluzioni Una soluzione è una miscela omogenea di 2 o più sostanze Il soluto è la sostanza (o sostanze) presente/i in
2018 Lezione 4. Le soluzioni Acidi e Basi Reazioni Chimiche La Concentrazione delle Soluzioni Una soluzione è una miscela omogenea di 2 o più sostanze Il soluto è la sostanza (o sostanze) presente/i in
SAGGI PER IL RICONOSCIMENTO DEI PIGMENTI. Bianco San Giovanni - CaCO 3
 SAGGI PER IL RICONOSCIMENTO DEI PIGMENTI Le prove descritte in questo capitolo riguardano: 1. Analisi qualitativa per via umida per il riconoscimento di anioni e di cationi 2. Saggi alla fiamma per il
SAGGI PER IL RICONOSCIMENTO DEI PIGMENTI Le prove descritte in questo capitolo riguardano: 1. Analisi qualitativa per via umida per il riconoscimento di anioni e di cationi 2. Saggi alla fiamma per il
REAZIONI ACIDO-BASE OSSERVARE, DESCRIVERE E DARE UNA SPIEGAZIONE DEI FENOMENI CHIMICI AVVENUTI
 ESPERIENZA 2 REAZIONI ACIDO-BASE OBIETTIVO. L'esperienza serve a completare la presa di contatto con le attrezzature di laboratorio e i reagenti chimici più comuni, verificando le conoscenze acquisite
ESPERIENZA 2 REAZIONI ACIDO-BASE OBIETTIVO. L'esperienza serve a completare la presa di contatto con le attrezzature di laboratorio e i reagenti chimici più comuni, verificando le conoscenze acquisite
1 - Titolazioni acido-base e ph
 1 - Titolazioni acido-base e ph Procedimento (m.m. di NH 3 = 17,03) Moli di NaOH consumate (1,04 x 10-3 ) Moli di HCl iniziali (7,75 x 10-3 ) Moli di NH 3 (6,71 x 10-3 ) Massa di NH 3 (114,3 mg) Concentrazione
1 - Titolazioni acido-base e ph Procedimento (m.m. di NH 3 = 17,03) Moli di NaOH consumate (1,04 x 10-3 ) Moli di HCl iniziali (7,75 x 10-3 ) Moli di NH 3 (6,71 x 10-3 ) Massa di NH 3 (114,3 mg) Concentrazione
4. In un becker ci sono 50 ml di NaOH 0,10 M. Quale soluzione, se aggiunta alla soluzione nel becker, non provoca variazioni del ph?
 1. Quale tra i seguenti acidi è il più debole? a. CH 3 COOH K a = 1,8*10 5 c. HF K a = 3,5*10 4 b. HCN K a = 4,9*10 10 d. HCNO K a = 1,6*10 4 2. Nell equilibrio: Fe 3+ ( aq ) + SCN ( aq ) Fe(SCN) 2+ (
1. Quale tra i seguenti acidi è il più debole? a. CH 3 COOH K a = 1,8*10 5 c. HF K a = 3,5*10 4 b. HCN K a = 4,9*10 10 d. HCNO K a = 1,6*10 4 2. Nell equilibrio: Fe 3+ ( aq ) + SCN ( aq ) Fe(SCN) 2+ (
DI ANALISI CHIMICA QUALITATIVA NON SISTEMATICA DI ALCUNI IONI
 Schemaconreazioniok.3 PERCORSI DIDATTICI per studenti del 2 anno I.T.A.S. G. Raineri Piacenza NOTE DI ANALISI CHIMICA QUALITATIVA NON SISTEMATICA DI ALCUNI IONI Ernesto Colombani SEQUENZA DELLE OPERAZIONI
Schemaconreazioniok.3 PERCORSI DIDATTICI per studenti del 2 anno I.T.A.S. G. Raineri Piacenza NOTE DI ANALISI CHIMICA QUALITATIVA NON SISTEMATICA DI ALCUNI IONI Ernesto Colombani SEQUENZA DELLE OPERAZIONI
bario cloruro biidrato (200 mg; PM ) ferro(iii) cloruro esaidrato (200 mg; PM ) rame(ii) acetato monoidrato (200 mg; PM 181.
 Una delle esercitazioni che effettueremo in laboratorio è la separazione di cationi metallici basata sulla loro precipitazione selettiva. In particolare, seguiremo una metodica che ci consentirà di separare
Una delle esercitazioni che effettueremo in laboratorio è la separazione di cationi metallici basata sulla loro precipitazione selettiva. In particolare, seguiremo una metodica che ci consentirà di separare
METODO DI VOLHARD. Nel metodo di Volhard gli ioni argento sono titolati con una soluzione standard di ione tiocianato: Ag + + SCN - AgSCN
 METODO DI VOLHARD Il metodo viene impiegato per la determinazione di ioni alogenuro quali I -, Cl -, Br -. Un eccesso noto di soluzione standard di nitrato di argento AgNO 3 viene aggiunto al campione
METODO DI VOLHARD Il metodo viene impiegato per la determinazione di ioni alogenuro quali I -, Cl -, Br -. Un eccesso noto di soluzione standard di nitrato di argento AgNO 3 viene aggiunto al campione
Circuiti in Serie / Parallelo
 Circuiti in Serie / Parallelo Utilizzatori in serie Più utilizzatori sono collegati in serie quando sono montati uno dopo l altro in modo che la stessa corrente li attraversi in successione. In tal modo
Circuiti in Serie / Parallelo Utilizzatori in serie Più utilizzatori sono collegati in serie quando sono montati uno dopo l altro in modo che la stessa corrente li attraversi in successione. In tal modo
Relazione giorno 4 Febbraio 2011
 Relazione giorno 4 Febbraio 2011 Classi IVA e IVB Titolo esperienza Passaggi di stato, innalzamento ebullioscopico e abbassamento crioscopico. Curva di riscaldamento dell acqua. Introduzione al problema
Relazione giorno 4 Febbraio 2011 Classi IVA e IVB Titolo esperienza Passaggi di stato, innalzamento ebullioscopico e abbassamento crioscopico. Curva di riscaldamento dell acqua. Introduzione al problema
(Si identificano Ag +, Hg 2. , Pb 2+ ) - 1 GRUPPO - Reattivo Generale: HCl 2N. Soluzione. Precipitato. Soluzione. Residuo. Soluzione.
 Reattivo Generale: HCl 2N - 1 GRUPPO - (Si identificano Ag +, Hg 2 2+, Pb 2+ ) Esame Sistematico: Nella provetta da centrifuga contenente la soluzione in esame (preparata sciogliendo la sostanza in H 2
Reattivo Generale: HCl 2N - 1 GRUPPO - (Si identificano Ag +, Hg 2 2+, Pb 2+ ) Esame Sistematico: Nella provetta da centrifuga contenente la soluzione in esame (preparata sciogliendo la sostanza in H 2
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
+ NO 2 + 3H 2 O = Ce +3 + NO 3 + 2H 3 O +, b) 0.478 g
 1) Una soluzione di Na 3 PO 4 (PM = 163.94) viene titolata con una soluzione di AgNO 3 (PM = 169.87) a) Scrivere l equazione chimica del processo di titolazione e specificare di quale tecnica si tratta
1) Una soluzione di Na 3 PO 4 (PM = 163.94) viene titolata con una soluzione di AgNO 3 (PM = 169.87) a) Scrivere l equazione chimica del processo di titolazione e specificare di quale tecnica si tratta
(appunti di Daniela Discalzi e Serena Fortino) Con l'analisi quantitativa si determina la quantità di componenti presenti in un miscuglio.
 ANALISI QUALITATIVA INRGANICA (appunti di Daniela Discalzi e Serena Fortino) Con l'analisi quantitativa si determina la quantità di componenti presenti in un miscuglio. L'analisi qualitativa indica quali
ANALISI QUALITATIVA INRGANICA (appunti di Daniela Discalzi e Serena Fortino) Con l'analisi quantitativa si determina la quantità di componenti presenti in un miscuglio. L'analisi qualitativa indica quali
ESERCIZI. 1. Completa le seguenti reazioni e, se necessario, bilanciale: b, K + H 2 O! c. Na + H 2! d. KOH + CO 2! e. K 2 CO 3! calore!
 ESERCIZI 1. Completa le seguenti reazioni e, se necessario, bilanciale: elettrolisi a. LiCl (fuso)!!! " b, K + H 2 O! c. Na + H 2! d. KOH + CO 2! e. K 2 CO 3! calore! " f. Na 2 CO 3 + H 2 SO 4! g. K 2
ESERCIZI 1. Completa le seguenti reazioni e, se necessario, bilanciale: elettrolisi a. LiCl (fuso)!!! " b, K + H 2 O! c. Na + H 2! d. KOH + CO 2! e. K 2 CO 3! calore! " f. Na 2 CO 3 + H 2 SO 4! g. K 2
Corso di Chimica e Propedeutica Biochimica Reazioni in soluzione acquosa
 Corso di Chimica e Propedeutica Biochimica Reazioni in soluzione acquosa Alcune immagini sono state prese e modificate da Chimica di Kotz, Treichel & Weaver, Edises 2007, III edizione 1 Ioni in soluzione
Corso di Chimica e Propedeutica Biochimica Reazioni in soluzione acquosa Alcune immagini sono state prese e modificate da Chimica di Kotz, Treichel & Weaver, Edises 2007, III edizione 1 Ioni in soluzione
Osservazioni su alcuni ossidanti comuni che agiscono in soluzione acquosa
 Osservazioni su alcuni ossidanti comuni che agiscono in soluzione acquosa Esercizio: scrivere la reazione corrispondente ad ogni asterisco e bilanciare. PERMANGANATO Il permanganato di potassio K è un
Osservazioni su alcuni ossidanti comuni che agiscono in soluzione acquosa Esercizio: scrivere la reazione corrispondente ad ogni asterisco e bilanciare. PERMANGANATO Il permanganato di potassio K è un
NUMERO DI OSSIDAZIONE Es. HCl H + Cl - H = +1 Cl = -1 H 2. O 2 H + O 2- H = +1 O = -2 Es. NaCl Na + Cl - Na = +1 Cl = -1
 NUMERO DI OSSIDAZIONE Es. HCl H + Cl - H = +1 Cl = -1 H 2 O 2 H + O 2- H = +1 O = -2 Es. NaCl Na + Cl - Na = +1 Cl = -1 Es. H-H, O=O, Cu, Fe = 0 H: +1, (tranne che negli idruri metallici es. NaH 1) O:
NUMERO DI OSSIDAZIONE Es. HCl H + Cl - H = +1 Cl = -1 H 2 O 2 H + O 2- H = +1 O = -2 Es. NaCl Na + Cl - Na = +1 Cl = -1 Es. H-H, O=O, Cu, Fe = 0 H: +1, (tranne che negli idruri metallici es. NaH 1) O:
Numero di ossidazione
 Numero di ossidazione Si definisce numero di ossidazione la carica elettrica che l elemento assume in un composto se si pensa di associare gli elettroni di ciascun legame all atomo considerato più elettronegativo
Numero di ossidazione Si definisce numero di ossidazione la carica elettrica che l elemento assume in un composto se si pensa di associare gli elettroni di ciascun legame all atomo considerato più elettronegativo
PRIMO ESONERO DI CHIMICA sessione A - 10/11/2011
 PRIMO ESONERO DI CHIMICA sessione A - 10/11/2011 TRACCIA A1 TRACCIA A2 1. (7 p.ti) Un campione contiene 10 g di Al 2 O 3 e 10 g di CaO. Qual è la percentuale in peso dell O nella miscela? Quale la sua
PRIMO ESONERO DI CHIMICA sessione A - 10/11/2011 TRACCIA A1 TRACCIA A2 1. (7 p.ti) Un campione contiene 10 g di Al 2 O 3 e 10 g di CaO. Qual è la percentuale in peso dell O nella miscela? Quale la sua
LABORATORIO PROPEDEUTICO ALL ANALISI DEI MEDICINALI
 LABORATORIO PROPEDEUTICO ALL ANALISI DEI MEDICINALI Prof.ssa Gabbriella Innocenti Studenti:! Francesco Scapin! nº 25! Luca Pegoraro!! nº 27! Chiara Mariotti!! nº 28! Eleonora Sartori! nº 30 Dipartimento
LABORATORIO PROPEDEUTICO ALL ANALISI DEI MEDICINALI Prof.ssa Gabbriella Innocenti Studenti:! Francesco Scapin! nº 25! Luca Pegoraro!! nº 27! Chiara Mariotti!! nº 28! Eleonora Sartori! nº 30 Dipartimento
Esame di Chimica Generale 12 Settembre 2012
 Esame di Chimica Generale 12 Settembre 2012 COGNOME NOME. MATRICOLA 1 2 3 4 5 6 7 8 9 10 Indicazioni per lo svolgimento del compito. Scrivete il vostro Nome e Cognome in STAMPATELLO su ciascuno di questi
Esame di Chimica Generale 12 Settembre 2012 COGNOME NOME. MATRICOLA 1 2 3 4 5 6 7 8 9 10 Indicazioni per lo svolgimento del compito. Scrivete il vostro Nome e Cognome in STAMPATELLO su ciascuno di questi
Corso di Chimica Generale Inorganica Soluzione degli Esercizi del Compito del 28 luglio 2010
 Corso di Chimica Generale Inorganica Soluzione degli Esercizi del Compito del 28 luglio 2010 Si avvertono gli studenti che la verbalizzazione dei risultati dell esame è fatta esclusivamente per via elettronica.
Corso di Chimica Generale Inorganica Soluzione degli Esercizi del Compito del 28 luglio 2010 Si avvertono gli studenti che la verbalizzazione dei risultati dell esame è fatta esclusivamente per via elettronica.
ALOGENURI (Cl -, Br -, I - ) 1
 ALOGENURI (Cl -, Br -, I - ) 1 Cloruri, bromuri e ioduri di tutti i metalli, eccetto quelli di Pb +,Ag + e Hg + (I), sono solubili in H O. Cloruri, bromuri e ioduri di Pb +,Ag + e Hg + (I) sono inoltre
ALOGENURI (Cl -, Br -, I - ) 1 Cloruri, bromuri e ioduri di tutti i metalli, eccetto quelli di Pb +,Ag + e Hg + (I), sono solubili in H O. Cloruri, bromuri e ioduri di Pb +,Ag + e Hg + (I) sono inoltre
ESERCIZI I PARTE. 1 Bilanciamento
 ESERCIZI I PARTE 1 1 Bilanciamento 1. H 3 PO 3 + CuO Cu 3 (PO 3 ) 2 +3H 2 O ) 2. Cs 2 O + H 2 O CsOH 3. P 2 O 5 + H 2 O HPO 3 4. NaCl + H 2 SO 4 Na 2 SO 4 + HCl 5. NaF + Mg(OH) 2 MgF 2 + NaOH 6. Al(OH)
ESERCIZI I PARTE 1 1 Bilanciamento 1. H 3 PO 3 + CuO Cu 3 (PO 3 ) 2 +3H 2 O ) 2. Cs 2 O + H 2 O CsOH 3. P 2 O 5 + H 2 O HPO 3 4. NaCl + H 2 SO 4 Na 2 SO 4 + HCl 5. NaF + Mg(OH) 2 MgF 2 + NaOH 6. Al(OH)
H N. Mn 2+ +.. Fe 3+ +.. H 2 O
 CHIMICA ANALITICA- PROVA SCRITTA 3 FEBBRAIO 2005-1a. Quanti microlitri di 1-nonene (densità 1-nonene = 0.73 g/ml) bisogna prelevare per preparare 50 ml di soluzione di concentrazione 1000 ppm in metanolo
CHIMICA ANALITICA- PROVA SCRITTA 3 FEBBRAIO 2005-1a. Quanti microlitri di 1-nonene (densità 1-nonene = 0.73 g/ml) bisogna prelevare per preparare 50 ml di soluzione di concentrazione 1000 ppm in metanolo
Analizziamo terra e acqua
 Analizziamo terra e acqua L analisi delle acque Per utilizzare al meglio un terreno e capire se è adatto alla coltivazione bisogna analizzare l acqua che viene utilizzata per annaffiare un terreno. Bisogna
Analizziamo terra e acqua L analisi delle acque Per utilizzare al meglio un terreno e capire se è adatto alla coltivazione bisogna analizzare l acqua che viene utilizzata per annaffiare un terreno. Bisogna
See more about
 See more about www.scienzaescuola.it ESERCIZI DI STECHIOMETRIA CON ESEMPI DI SOLUZIONI TIPO. Prof. Gabrielli Luciano (Lic. Scientifico L. da Vinci -Sora FR) P.M : Calcola il P.M. di: Al 2 (SO 4 ) 3 Fe(NO
See more about www.scienzaescuola.it ESERCIZI DI STECHIOMETRIA CON ESEMPI DI SOLUZIONI TIPO. Prof. Gabrielli Luciano (Lic. Scientifico L. da Vinci -Sora FR) P.M : Calcola il P.M. di: Al 2 (SO 4 ) 3 Fe(NO
Esame di Chimica Generale 15 Giugno 2016
 Esame di Chimica Generale 15 Giugno 2016 COGNOME NOME. MATRICOLA 1 2 3 4 5 6 7 8 9 10 Indicazioni per lo svolgimento del compito. Scrivete il vostro Nome e Cognome in STAMPATELLO su ciascuno di questi
Esame di Chimica Generale 15 Giugno 2016 COGNOME NOME. MATRICOLA 1 2 3 4 5 6 7 8 9 10 Indicazioni per lo svolgimento del compito. Scrivete il vostro Nome e Cognome in STAMPATELLO su ciascuno di questi
NOMENCLATURA DEI COMPOSTI CHIMICI
 NOMENCLATURA DEI COMPOSTI CHIMICI Agli albori della chimica non c erano regole di nomenclatura; per individuare i composti si usavano dei nomi comuni che generalmente derivavano da loro proprietà organolettiche
NOMENCLATURA DEI COMPOSTI CHIMICI Agli albori della chimica non c erano regole di nomenclatura; per individuare i composti si usavano dei nomi comuni che generalmente derivavano da loro proprietà organolettiche
Esame di Chimica Generale del 21 Settembre 2017
 Esame di Chimica Generale del 21 Settembre 2017 COGNOME NOME. MATRICOLA 1 2 3 4 5 6 7 8 9 10 Indicazioni per lo svolgimento del compito. Scrivete il vostro Nome e Cognome in STAMPATELLO su ciascuno di
Esame di Chimica Generale del 21 Settembre 2017 COGNOME NOME. MATRICOLA 1 2 3 4 5 6 7 8 9 10 Indicazioni per lo svolgimento del compito. Scrivete il vostro Nome e Cognome in STAMPATELLO su ciascuno di
*M I03* 3/20. perforiran list
 *M15143112I* 2/20 *M15143112I02* *M15143112I03* 3/20 P perforiran list 4/20 *M15143112I04* Pagina vuota *M15143112I05* 5/20 1. L'atomo di un certo elemento contiene 20 neutroni e 17 protoni. 1.1. Scrivete
*M15143112I* 2/20 *M15143112I02* *M15143112I03* 3/20 P perforiran list 4/20 *M15143112I04* Pagina vuota *M15143112I05* 5/20 1. L'atomo di un certo elemento contiene 20 neutroni e 17 protoni. 1.1. Scrivete
NUMERO DI OSSIDAZIONE Es. HCl H + Cl - H = +1 Cl = -1 H 2. O 2 H + O 2- H = +1 O = -2 Es. NaCl Na + Cl - Na = +1 Cl = -1
 NUMERO DI OSSIDAZIONE Es. HCl H + Cl - H = +1 Cl = -1 H 2 O 2 H + O 2- H = +1 O = -2 Es. NaCl Na + Cl - Na = +1 Cl = -1 Es. H-H, O=O, Cu, Fe N OX = 0 H: +1, (tranne che negli idruri metallici es. NaH:
NUMERO DI OSSIDAZIONE Es. HCl H + Cl - H = +1 Cl = -1 H 2 O 2 H + O 2- H = +1 O = -2 Es. NaCl Na + Cl - Na = +1 Cl = -1 Es. H-H, O=O, Cu, Fe N OX = 0 H: +1, (tranne che negli idruri metallici es. NaH:
Esame di Chimica Generale 13 Gennaio 2017
 Esame di Chimica Generale 13 Gennaio 2017 COGNOME NOME. MATRICOLA 1 2 3 4 5 6 7 8 9 10 Indicazioni per lo svolgimento del compito. Scrivete il vostro Nome e Cognome in STAMPATELLO su ciascuno di questi
Esame di Chimica Generale 13 Gennaio 2017 COGNOME NOME. MATRICOLA 1 2 3 4 5 6 7 8 9 10 Indicazioni per lo svolgimento del compito. Scrivete il vostro Nome e Cognome in STAMPATELLO su ciascuno di questi
Nomenclatura delle sostanze chimiche
 Nomenclatura delle sostanze chimiche SOSTANZE CHIMICHE!1 ELEMENTI Metalli Non metalli COMPOSTI Ossidi Anidridi Idrossidi Acidi Sali Idruri - ossiacidi - idracidi METALLI!2 Duttili Malleabili Buoni conduttori
Nomenclatura delle sostanze chimiche SOSTANZE CHIMICHE!1 ELEMENTI Metalli Non metalli COMPOSTI Ossidi Anidridi Idrossidi Acidi Sali Idruri - ossiacidi - idracidi METALLI!2 Duttili Malleabili Buoni conduttori
ISTITUTO DI ISTRUZIONE SUPERIORE M. Montessori L. Da Vinci
 7 ISTITUTO DI ISTRUZIONE SUPERIORE M. Montessori L. Da Vinci Via della Repubblica, 3 40046 Porretta Terme C.F. 80071330379 - Tel. 0534/521211 Fax 0534/23098 bois00100p@istruzione.it www.scuolamontessoridavinci.it
7 ISTITUTO DI ISTRUZIONE SUPERIORE M. Montessori L. Da Vinci Via della Repubblica, 3 40046 Porretta Terme C.F. 80071330379 - Tel. 0534/521211 Fax 0534/23098 bois00100p@istruzione.it www.scuolamontessoridavinci.it
Analisi di farmaci inorganici XI esercitazione di laboratorio
 Analisi di farmaci inorganici XI esercitazione di laboratorio Iodosan Goccemed Principio attivo: Tipo prodotto: Gruppo merceologico: Impiego terapeutico: Forma farmaceutica: I2 (iodio elementare). parafarmaco
Analisi di farmaci inorganici XI esercitazione di laboratorio Iodosan Goccemed Principio attivo: Tipo prodotto: Gruppo merceologico: Impiego terapeutico: Forma farmaceutica: I2 (iodio elementare). parafarmaco
CLASSIFICAZIONE, NOMENCLATURA E FORMULE DEI COMPOSTI INORGANICI
 CLASSIFICAZIONE, NOMENCLATURA E FORMULE DEI COMPOSTI INORGANICI La VALENZA di un elemento è data dal numero di elettroni che esso deve perdere, o acquistare, o mettere in comune con uno o più atomi in
CLASSIFICAZIONE, NOMENCLATURA E FORMULE DEI COMPOSTI INORGANICI La VALENZA di un elemento è data dal numero di elettroni che esso deve perdere, o acquistare, o mettere in comune con uno o più atomi in
Progetto fumo. 2CT - ANNO SCOLASTICO 2015/16 Istituto tecnico industriale statale A.Volta
 Progetto fumo 2CT - ANNO SCOLASTICO 2015/16 Istituto tecnico industriale statale A.Volta 1 Processo di estrazione del monossido di carbonio Principi teorici Per comprendere questo procedimento, e i termini
Progetto fumo 2CT - ANNO SCOLASTICO 2015/16 Istituto tecnico industriale statale A.Volta 1 Processo di estrazione del monossido di carbonio Principi teorici Per comprendere questo procedimento, e i termini
Equilibri in soluzione acquosa unità 1, modulo G del libro
 Equilibri in soluzione acquosa unità 1, modulo G del libro Si parla di equilibri in soluzione acquosa quando un soluto, solido, viene sciolto in acqua. Cosa accade? La specie solida si dissocia in ioni,
Equilibri in soluzione acquosa unità 1, modulo G del libro Si parla di equilibri in soluzione acquosa quando un soluto, solido, viene sciolto in acqua. Cosa accade? La specie solida si dissocia in ioni,
131,3 86 (222) 126,9 85 (210) 127,6 84 (209) 209,0 121, ,2 118, , ,4 200,6 112, , ,0 106, ,1 192,2 102,9 77
 *M16243112I* 2/20 *M16243112I02* *M16243112I03* 3/20 I 1 II 2 1 1,008 2 2 3 4 3 4 5 6 7 8 9 10 11 12 44,96 5 5 6 6 7 3 6,941 11 22,99 19 39,10 37 85,47 55 132,9 87 (223) 4 9,012 12 24,31 20 40,08 38 87,62
*M16243112I* 2/20 *M16243112I02* *M16243112I03* 3/20 I 1 II 2 1 1,008 2 2 3 4 3 4 5 6 7 8 9 10 11 12 44,96 5 5 6 6 7 3 6,941 11 22,99 19 39,10 37 85,47 55 132,9 87 (223) 4 9,012 12 24,31 20 40,08 38 87,62
SAGGI PER VIA SECCA. Fiamma Ossidante. Fiamma Riducente C C
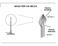 SAGGI PER VIA SECCA Fiamma Ossidante 1350-1500 C Fiamma Riducente 400-500 C Ricerca dei Cationi per Via Secca Gli elementi metallici presenti nei composti organometallici della F.U. sono: Sodio, Potassio,
SAGGI PER VIA SECCA Fiamma Ossidante 1350-1500 C Fiamma Riducente 400-500 C Ricerca dei Cationi per Via Secca Gli elementi metallici presenti nei composti organometallici della F.U. sono: Sodio, Potassio,
CH 3 COOH 100% 20% Acido Acetico Glaciale. Acido Acetico Diluito. Pericolo. Attenzione H226 H314 H315 H319. n. Cas Cod. Ph.Eur.
 Acido Acetico Glaciale n. Cas 64-19-7 Cod. Ph.Eur. 1000400 CH 3 COOH 100% H226 H314 n. Cas 64-19-7 Cod. Ph.Eur. 1000402 Acido Acetico Diluito CH 3 COOH Attenzione 20% H315 H319 SOL n. Cas 7647-01-0 Cod.
Acido Acetico Glaciale n. Cas 64-19-7 Cod. Ph.Eur. 1000400 CH 3 COOH 100% H226 H314 n. Cas 64-19-7 Cod. Ph.Eur. 1000402 Acido Acetico Diluito CH 3 COOH Attenzione 20% H315 H319 SOL n. Cas 7647-01-0 Cod.
Marco Bonechi Allievo dell I.T.S. T. Buzzi - Prato. ESERCIZI SUL ph 3 0,002 0, Completa la seguente tabella relativa a acidi o basi deboli.
 ESERCIZI SUL ph Livello difficoltà 1 (dalla concentrazione, calcolare il valore del ph) 1. Completa la tabella relativa a soluzioni di acidi o basi forti. 1 11 ph poh [H + ] [OH - ] 3 0,002 0,2 13 2 2.
ESERCIZI SUL ph Livello difficoltà 1 (dalla concentrazione, calcolare il valore del ph) 1. Completa la tabella relativa a soluzioni di acidi o basi forti. 1 11 ph poh [H + ] [OH - ] 3 0,002 0,2 13 2 2.
PRINCIPIO TESTATO: reazioni di sintesi, doppio scambio con precipitazione, eso-endotermiche e di ossido-riduzione.
 TITOLO: ALCUNI TIPI DI REAZIONI CHIMICHE - Chimica 13 Alcune esperienze sono puramente dimostrative OBIETTIVI: osservare diversi tipi di reazioni chimiche e comprenderne le basi. PRINCIPIO TESTATO: reazioni
TITOLO: ALCUNI TIPI DI REAZIONI CHIMICHE - Chimica 13 Alcune esperienze sono puramente dimostrative OBIETTIVI: osservare diversi tipi di reazioni chimiche e comprenderne le basi. PRINCIPIO TESTATO: reazioni
CORSO DI LAUREA IN BIOLOGIA ECOLOGICA. Esercitazioni di Laboratorio di Chimica Generale ed Inorganica
 CORSO DI LAUREA IN BIOLOGIA ECOLOGICA Esercitazioni di Laboratorio di Chimica Generale ed Inorganica Anno Accademico 2002-2003 1 ESERCITAZIONE Titolazione di una soluzione di HCl con una soluzione di NaOH
CORSO DI LAUREA IN BIOLOGIA ECOLOGICA Esercitazioni di Laboratorio di Chimica Generale ed Inorganica Anno Accademico 2002-2003 1 ESERCITAZIONE Titolazione di una soluzione di HCl con una soluzione di NaOH
NUMERO DI OSSIDAZIONE NOMENCLATURA CHIMICA
 NUMERO DI OSSIDAZIONE Il numero di ossidazione di un atomo corrisponde al numero di valenza preceduto da un segno + oppure -. Il segno negativo si assegna all atomo più elettronegativo e il segno + si
NUMERO DI OSSIDAZIONE Il numero di ossidazione di un atomo corrisponde al numero di valenza preceduto da un segno + oppure -. Il segno negativo si assegna all atomo più elettronegativo e il segno + si
L ANALISI CHIMICA si occupa:
 L ANALISI CHIMICA si occupa: della scomposizione di miscugli e composti nei loro componenti del riconoscimento e del dosaggio di tali componenti Settori di applicazione: Nel campo alimentare: i costituenti
L ANALISI CHIMICA si occupa: della scomposizione di miscugli e composti nei loro componenti del riconoscimento e del dosaggio di tali componenti Settori di applicazione: Nel campo alimentare: i costituenti
TUTORAGGIO CHIMICA A.A. 2018/2019 Tutoraggio Chimica (Prof. L. Pilia) Nicola Melis
 TUTORAGGIO CHIMICA 20.11.2018 1 Che volume, in ml, di acido cloridrico 2,50 M è necessario per far reagire completamente 11,8 g di Zn? Quale sarà la molarità di ZnCl 2 a seguito della reazione? Zn + HCl
TUTORAGGIO CHIMICA 20.11.2018 1 Che volume, in ml, di acido cloridrico 2,50 M è necessario per far reagire completamente 11,8 g di Zn? Quale sarà la molarità di ZnCl 2 a seguito della reazione? Zn + HCl
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
NUMERO DI OSSIDAZIONE E NOMENCLATURA
 NUMERO DI OSSIDAZIONE E NOMENCLATURA NOMENCLATURA Lo scopo della nomenclatura è fornire regole per individuare un composto, attribuendogli in modo univoco e chiaro un nome preciso ed una formula. Nomenclatura
NUMERO DI OSSIDAZIONE E NOMENCLATURA NOMENCLATURA Lo scopo della nomenclatura è fornire regole per individuare un composto, attribuendogli in modo univoco e chiaro un nome preciso ed una formula. Nomenclatura
Esercitazione 6. Chimica biologica del Fe. Il Ferro ) 2 (SO 4 6H 2. Fe(NH 4
 Esercitazione Preparazione del sale di Mohr Fe(NH 4 ) 2 (SO 4 ) 2 H 2 O Chimica biologica del Fe In un uomo di 75 kg sono presenti 4 g di Fe Nei Paesi occidentali ne assumiamo 15 mg/d Il Ferro Configurazione
Esercitazione Preparazione del sale di Mohr Fe(NH 4 ) 2 (SO 4 ) 2 H 2 O Chimica biologica del Fe In un uomo di 75 kg sono presenti 4 g di Fe Nei Paesi occidentali ne assumiamo 15 mg/d Il Ferro Configurazione
ESERCIZI SUL ph 3 0,002 0,2 13. 2. Completa la seguente tabella relativa a acidi o basi deboli.
 ESERCIZI SUL ph Livello difficoltà 1 1. Completa la tabella relativa a soluzioni di acidi o basi forti. 1 11 ph poh [H + ] [OH - ] 3 0,002 0,2 13 2 2. Completa la seguente tabella relativa a acidi o basi
ESERCIZI SUL ph Livello difficoltà 1 1. Completa la tabella relativa a soluzioni di acidi o basi forti. 1 11 ph poh [H + ] [OH - ] 3 0,002 0,2 13 2 2. Completa la seguente tabella relativa a acidi o basi
L ANALISI CHIMICA 2 SOSTANZA INCOGNITA. Analisi degli anioni e dei cationi. Riconoscimento della sostanza
 L ANALISI CHIMICA 1 L Analisi Chimica è un insieme di operazioni che si eseguono per separare, riconoscere (Analisi Chimica Qualitativa) e dosare (Analisi Chimica Quantitativa) una sostanza o una miscela
L ANALISI CHIMICA 1 L Analisi Chimica è un insieme di operazioni che si eseguono per separare, riconoscere (Analisi Chimica Qualitativa) e dosare (Analisi Chimica Quantitativa) una sostanza o una miscela
