Regolano il metabolismo, sia come enzimi, sia come ormoni (insulina, glucagone, ecc.)
|
|
|
- Rosina Gasparini
- 7 anni fa
- Visualizzazioni
Transcript
1 Grazie alla elevata dinamicità delle strutture proteiche (gli atomi sono in continuo movimento fluttuante) e per la capacità che hanno di legarsi in modo selettivo ad altre molecole, le proteine svolgono un numero elevato di funzioni (classificazione): Regolano il metabolismo, sia come enzimi, sia come ormoni (insulina, glucagone, ecc.) Trasportano diverse molecole; Le funzioni di molte proteine richiedono il legame reversibile di altre molecole. Una molecola che si lega reversibilmente ad una proteina è detta LIGANDO q Il sito a cui si lega il ligando è chiamato SITO DI LEGAME è complementare al ligando per dimensione, forma e carica q le proteine sono flessibili e presentano modificazioni conformazionali più o meno elevate e possono essere essenziali per la funzione della proteina q il legame di un LIGANDO alla proteina è spesso accompagnato da MODIFICAZIONE CONFORMAZIONALE q nella struttura quaternaria la modificazione di una subunità può essere trasmessa alle subunità vicine q le interazioni tra proteine e ligandi possono essere REGOLATE di solito attraverso il legame con altri ligandi 1
2 L ossigeno è poco solubile in acqua e non potrebbe essere trasportato a sufficienza ai tessuti se non fosse trasportato legato ad una proteina : l EMOGLOBINA 2
3 In realtà questo ruolo viene svolto da un metallo di transizione: il FERRO. Il ferro è infatti incorporato in un gruppo legato a queste proteine: il gruppo EME PROTOPORFIRINA costituita da quattro anelli pirrolici Il ferro che è nello stato ferroso (Fe +2 ) può fare 6 legami di coordinazione Quattro legami del ferro sono impegnati con l azoto dell anello porfirinico gli altri due sono perpendicolari all anello. Mentre uno dei due legami di coordinazione perpendicolari all anello lega l ossigeno, l altro è impegnato con un di azoto di un residuo di istidina di una catena laterale della proteina che impedisce l ossidazione del metallo in presenza di ossigeno. 3
4 Due catene laterali idrofobiche dal lato dell eme che lega l ossigeno coadiuvano nel mantenere l eme nella posizione corretta. Mentre il Fe +2 lega reversibilmente l ossigeno il Fe +3 non è in grado di legarlo. Quando l EME non è legato a proteine ma è libero in soluzione la presenza di ossigeno ne determina l ossidazione a Fe +3 La componente proteica della mioglobina impedisce l ossidazione del ferro a Fe (III) In determinate condizioni il ferro II dell emoglobine o della mioglobina si ossida a Fe (III) per dare luogo alla METAMIOGLOBINA e alla METAEMOGLOBINA ; a queste proteine si deve il colore marrone scuro della carne esposta all aria d e del sangue secco 4
5 Quando il ferro emico si lega all ossigeno, le proprietà elettroniche si modificano e ciò spiega il diverso colore che ha il sangue venoso (povero di ossigeno) rispetto a quello arterioso (ricco di ossigeno). Alcune molecole come il monossido di carbonio (CO) e il monossido di azoto (NO) si possono coordinare al ferro con un affinità superiore a quella dell ossigeno. Inoltre il legane del monossido di carbonio è irreversibile. Esistono molte proteine con gruppi eme ( citocromi, clorofilla emoglobine e mioglobina) ma solo due proteine legano e trasportano l ossigeno. Mioglobina una catena polipeptidica Emoglobina quattro catene polipeptidiche 5
6 Singola catena polipeptidica di 153 residui amminoacidici lega l ossigeno soprattutto al livello del cuore e del muscolo scheletrico; sembra avere la funzione di tampone per l ossigeno allo scopo di mantenere costante la concentrazione intracellulare in base al livello del metabolismo aerobico. La mioglobina è particolarmente abbondante nel tessuto scheletrico di quei mammiferi marini che devono immagazzinare ossigeno per le loro prolungate immersioni La funzione della mioglobina così come dell emoglobina è quella di legare l ossigeno ma anche di rilasciarlo al momento opportuno L ossigeno è trasportato nell organismo animale legato all emoglobina degli eritrociti. Gli eritrociti sono vestigia di cellule che hanno la durata, almeno negli uomini, di 120 giorni e derivano da cellule staminali dette emocitoblasti. L emoglobina è una proteina tetramerica che contiene due subunità α e due β ognuna delle quali contiene un centro eme che lega l ossigeno. 6
7 La struttura globale dell emoglobina è α 2 β 2. entrambe le catene sono molto simili così come sono simili alla miogobina. La mioglobina lega una molecola di ossigeno l emoglobina ne lega quattro entrambe legano l o s s i g e n o REVERSIBILMENTE, ma l emoglobina presenta una COOPERATIVITA POSITIVA L emoglobina funziona da trasportatore di ossigeno, la mioglobina da riserva di ossigeno. Questa diversità funzionale è dovuta alla diversa capacità di legare e rilasciare ossigeno La struttura tridimensionale dei due tipi di catene (α e β) dell emoglobina è molto simile alla struttura della mioglobina. Lo stato R (rilasciato) ha un affinità maggiore dello stato T (teso) anche se l ossigeno si lega ad entrambi. L ossigeno che lega T innesca una variazione conformazionale, che converte le subunità nello stato R Nello stato T la forfirina ha una forma a cupola perché il ferro nell eme tende a protrudere verso l istidina prossimale; quando si lega l ossigeno l eme assume una conformazione più planare 7
8 L ossigenazione causa la rotazione di un protomero di 15 rispetto all altro, portando le catene β in stretto contatto reciproco La funzione di queste proteine è quella di legare l ossigeno ma anche di rilasciarlo al momento opportuno. In BIOCHIMICA la funzione delle proteine dipende dalle interazioni LIGANDO-PROTEINA In generale il legame reversibile di un ligando alla proteina può essere descritto da una reazione all equilibrio: P + L PL K a = [PL] [P] [L] Ka = Costante di Associazione La Ka è una misura dell affinità proteina (P) ligando (L) Se la Ka è molto elevata l affinità del ligando per la proteina è molto elevata. 8
9 La costante di dissociazione K d è molto più usata della costante di associazione per esprimere l affinità della proteina per un ligando P L P + L K d = [P] [L] [PL] K a = 1/K d Un valore basso di K d corrisponde ad un elevata affinità Negli esperimenti in cui viene usato ossigeno come ligando è molto più facile misurare la pressione parziale po 2 che non la concentrazione Le curve di dissociazione dell emoglobina e della mioglobina sono diverse ed adeguate ai rispettivi ruoli fisiologici Se riportiamo in un grafico il grado di SATURAZIONE (frazione dei possibili siti a cui è effettivamente legato l ossigeno) rispetto alla pressione di ossigeno otteniamo una curva IPERBOLICA per la mioglobina ed una SIGMOIDE per l emoglobina 9
10 La mioglobina è molto efficiente a richiamare ossigeno dai capillari alle cellule muscolari ALTA AFFINITA PER L OSSIGENO Nell emoglobina occorre più ossigeno per arrivare allo stesso grado di saturazione ( 50%) L emoglobina deve legare in modo efficiente l ossigeno nei polmoni e rilasciarlo nei tessuti : LEGAME COOPERATIVO DELL OSSIGENO CINETICA SIGMOIDE 10
11 Capillari polmonari: 100 mm Hg muscolo in attività: 20 mm Hg Nei tessuti: 40 mm Hg La curva sigmoide c può essere pensata come una curva ibrida che riflette la presenza di forma a bassa affinità e forma ad alta affinità. Il legame cooperativo dell ossigeno rende l emoglobina più sensibile alle variazioni della concentrazione di ossigeno. 11
12 L ossigenazione dell emoglobina innesca cambiamenti conformazionali nella componente proteica Una molecola di ossigeno si lega più facilmente ad una emoglobina che ha legato altro ossigeno (legame cooperativo) COOPERATIVITA Proprietà esclusiva delle proteine multimeriche In qualunque tipo di legame, una curva sigmoide è indicativa di un interazione cooperativa tra i siti di legame Oltre a trasportare l O 2 dai polmoni ai tessuti l emoglobina trasporta la CO 2 dai tessuti ai polmoni. La CO 2 è trasportata come CARBAMMATO legato al gruppo amminico terminale di una catena di emoglobina CO 2 + Hb-NH 3 + 2H + + Hb-N-C-O - I carbammati cambiano la carica delle proteine favorendo la formazione di ponti salini tra le catene α e β. La CO 2 legata all emoglobina è il 15% del totale nel sangue venoso. La restante parte di CO 2 è trasportata come BICARBONATO che si forma negli eritrociti per idratazione dell acido carbonico in presenza di un enzima : l ANIDRASI CARBONICA H O 12
13 Anidrasi carbonica CO 2 + H 2 O H 2 CO 3 HCO H + Per ogni 2 molecole di O 2 rilasciate la deossiemoglobina lega un H + contribuendo in maniera significativa al potere tamponante del sangue. L effetto Bohr costituisce inoltre un meccanismo grazie al quale è possibile rifornire un ulteriore quantità di ossigeno ai muscoli in elevata attività metabolica dove la pressione di ossigeno può essere inferiore a 20 Torr. Questi muscoli generano acido lattico così velocemente che portano ad un abbassamento del ph da 7,4 a 7,2 del sangue che vi passa attraverso. 13
14 L emoglobina purificata mostra un affinità per l ossigeno altamente superiore rispetto a quella nel sangue intero. Il D-2,3-bisfosfoglicerato (BPG) si lega saldamente alla desossiemolobina ma debolmente alla forma ossigenata. La presenza di BPG determina perciò una diminuzione dell affinità dell emoglobina per l O 2, favorendo la conformazione deossigenata I gruppi anionici del BPG sono legati in una tasca della proteina con residui istidinici carichi positivamente ed i gruppi amminici terminali di entrambe le subunità β. Quando non è legato l ossigeno le due eliche tendono ad avvicinarsi restringendo la cavità centrale determinando l espulsione del DPG dalla cavità centrale. 14
15 Quando la concentrazione di H + diventa più alta (ph più basso al livello polmonare) la curva di dissociazione dell emoglobina è più stesa determinando un rilascio maggiore di ossigeno 15
16 L associazione di più catene in un tetramero determina un rilascio di ossigeno molto più elevato di quanto sarebbe possibile con una singola catena la curva spiega sia l efficienza di legame che di rilascio dell ossigeno ma come si può spiegare dal punto di vista MOLECOLARE questa COOPERATIVITA Tutti questi effetti sono il risultato di Gli effetti allosterici, nei quali il legame di un ligando ad un sito modifica il legame di un altro ligando ad un altro sito, richiedono la presenza di interazioni tra le subunità delle proteine oligomeriche Per spiegare il legame cooperativo di un ligando sono stati elaborati due modelli. MODELLI MOLECOLARI DELL ALLOSTERISMO il modello simmetrico dell allosterismo, sviluppato nel 1965 da J. Monod, J. Whyman e J.P. Changeaux, è catatterizzato dalle seguenti regole: 16
17 Una proteina allosterica è un oligomero 1. Ciascun oligomero esiste in due stati conformazionali R ( relaxed) e T (tensed) in equilibrio tra di loro 2. Il ligando può legare una subunità di una o dell altra conformazione 3. il legame del ligando sposta l equilibrio in favore di R 4. Durante la modificazione conformazionale la simmetria molecolare della proteina è conservata. La variazione delle subunità varia quindi in maniera CONCERTATA. E difficile credere che la simmetria oligomerica sia invariabilmente conservata in tutte le proteine a seguito del legame del ligando; 17
18 Koshland, Nemethy e Filmer nel 1966 proposero un secondo modello modello Nel modello sequenziale il legame del substrato induce una modificazione conformazionale in un protomero (subunità); le interazioni cooperative derivano dagli effetti che queste variazioni conformazionali hanno sulle subunità vicine. L affinità dell enzima per il legame del substrato varia con il numero di molecole di substrato legate, passando attraverso una serie di forme intermedie ad affinità diversa 18
19 19
IL GRUPPO EME. PROTOPORFIRINA IX: struttura organica ad anello costituita da 4 anelli pirrolici uniti da ponti metinici.
 IL GRUPPO EME PROTOPORFIRINA IX: struttura organica ad anello costituita da 4 anelli pirrolici uniti da ponti metinici. L inserimento di un atomo di ferro nello stato di ossidazione ferroso (Fe 2+ ) determina
IL GRUPPO EME PROTOPORFIRINA IX: struttura organica ad anello costituita da 4 anelli pirrolici uniti da ponti metinici. L inserimento di un atomo di ferro nello stato di ossidazione ferroso (Fe 2+ ) determina
STRUTTURA E FUNZIONE
 STRUTTURA E FUNZIONE O 2 non solubile in acqua Esistono due proteine che permettono il trasporto di O 2 nel corpo emoglobina (Hb) si trova nei globuli rossi Trasporta anche CO 2 and H + Mioglobina (Mb)
STRUTTURA E FUNZIONE O 2 non solubile in acqua Esistono due proteine che permettono il trasporto di O 2 nel corpo emoglobina (Hb) si trova nei globuli rossi Trasporta anche CO 2 and H + Mioglobina (Mb)
Mioglobina Emoglobina
 Mioglobina Emoglobina RESPIRAZIONE : assunzione di O 2 dall ambiente e rilascio di CO 2 La RESPIRAZIONE CELLULARE è un processo redox attraverso il quale vengono trasferiti atomi di idrogeno da un composto
Mioglobina Emoglobina RESPIRAZIONE : assunzione di O 2 dall ambiente e rilascio di CO 2 La RESPIRAZIONE CELLULARE è un processo redox attraverso il quale vengono trasferiti atomi di idrogeno da un composto
Esempi di proteine: Mioglobina ed Emoglobina
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica Organica e Biochimica Esempi di proteine: Mioglobina ed Emoglobina Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica Organica e Biochimica Esempi di proteine: Mioglobina ed Emoglobina Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base
La struttura di una proteina e ruolo biologico da essa svolto sono strettamente connessi. Alcune funzioni biologiche delle proteine:
 La struttura di una proteina e ruolo biologico da essa svolto sono strettamente connessi. Alcune funzioni biologiche delle proteine: Catalizzatori = Enzimi Accumulo e trasporto di ossigeno = mioglobina
La struttura di una proteina e ruolo biologico da essa svolto sono strettamente connessi. Alcune funzioni biologiche delle proteine: Catalizzatori = Enzimi Accumulo e trasporto di ossigeno = mioglobina
Esempi di proteine: Mioglobina ed Emoglobina
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Esempi di proteine: Mioglobina ed Emoglobina Mioglobina: caratteristiche generali, funzione
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Esempi di proteine: Mioglobina ed Emoglobina Mioglobina: caratteristiche generali, funzione
GLI ENZIMI ALLOSTERICI hanno più subunità che agiscono in maniera cooperativa. La cinetica enzimatica ha un andamento SIGMOIDE (non MM)
 Effetti allosterici - Modelli d azione GLI ENZIMI ALLOSEICI hanno più subunità che agiscono in maniera cooperativa. La cinetica enzimatica ha un andamento SIGMOIDE (non MM) Negli enzimi allosterici le
Effetti allosterici - Modelli d azione GLI ENZIMI ALLOSEICI hanno più subunità che agiscono in maniera cooperativa. La cinetica enzimatica ha un andamento SIGMOIDE (non MM) Negli enzimi allosterici le
FUNZIONI delle PROTEINE
 FUNZIONI delle PROTEINE Ha le dimensioni del reciproco di una concentrazione (M -1 ) Ha le dimensioni di una concentrazione (M) La frazione dei siti occupati rispetto ai siti totali è definita come θ FRAZIONE
FUNZIONI delle PROTEINE Ha le dimensioni del reciproco di una concentrazione (M -1 ) Ha le dimensioni di una concentrazione (M) La frazione dei siti occupati rispetto ai siti totali è definita come θ FRAZIONE
Le proteine che legano l ossigenol
 Le proteine che legano l ossigenol Protoporfirina IX EME (Fe-protoporfirina IX) L atomo di ferro del gruppo eme può formare sei legami Struttura della mioglobina di capodoglio (J. Kendrew, anni 50)
Le proteine che legano l ossigenol Protoporfirina IX EME (Fe-protoporfirina IX) L atomo di ferro del gruppo eme può formare sei legami Struttura della mioglobina di capodoglio (J. Kendrew, anni 50)
Nel corso dell evoluzione, con il passaggio dalla. progressivamente differenziati due meccanismi. un sistema circolatorio adeguato;
 PROTEINE RESPIRATORIE EMOGLOBINA & MIOGLOBINA Nel corso dell evoluzione, con il passaggio dalla vita anaerobia alla vita aerobia si sono progressivamente differenziati due meccanismi che sono in grado
PROTEINE RESPIRATORIE EMOGLOBINA & MIOGLOBINA Nel corso dell evoluzione, con il passaggio dalla vita anaerobia alla vita aerobia si sono progressivamente differenziati due meccanismi che sono in grado
Emoglobina e mioglobina
 Emoglobina e mioglobina Per molti organismi, l O 2 è una molecola di importanza vitale: l'ossigeno è infatti l'accettore finale degli elettroni, che "fluendo" attraverso i complessi della catena respiratoria,
Emoglobina e mioglobina Per molti organismi, l O 2 è una molecola di importanza vitale: l'ossigeno è infatti l'accettore finale degli elettroni, che "fluendo" attraverso i complessi della catena respiratoria,
Modulo 4. Una proteina in azione
 Modulo 4 Una proteina in azione Mioglobina ed emoglobina: un esempio di funzionamento di una proteina La funzione della maggior parte della proteine globulari è mediata dall interazione reversibile con
Modulo 4 Una proteina in azione Mioglobina ed emoglobina: un esempio di funzionamento di una proteina La funzione della maggior parte della proteine globulari è mediata dall interazione reversibile con
Prof. Maria Nicola GADALETA
 Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
LEZIONE 25: EMOGLOBINA L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO
 LEZIONE 25: EMOGLOBINA L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 25_emoglobina 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata
LEZIONE 25: EMOGLOBINA L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 25_emoglobina 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata
PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA
 PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA Legano reversibilmente l OSSIGENO. La mioglobina (monomerica) è presente nelle cellule muscolari. L emoglobina (tetramerica) è presente negli
PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA Legano reversibilmente l OSSIGENO. La mioglobina (monomerica) è presente nelle cellule muscolari. L emoglobina (tetramerica) è presente negli
Mioglobina ed emoglobina
 Mioglobina ed emoglobina α β Muscolo Deposito di O 2 Alta affinità per O 2 β α Globulo rosso Trasporto di O 2 Bassa affinità per O 2 Cooperativa ed allosterica Animali Mb-knockout (2003) : funzionalità
Mioglobina ed emoglobina α β Muscolo Deposito di O 2 Alta affinità per O 2 β α Globulo rosso Trasporto di O 2 Bassa affinità per O 2 Cooperativa ed allosterica Animali Mb-knockout (2003) : funzionalità
Le proteine che legano ossigeno:
 Le proteine che legano ossigeno: . I cristalli si ottengono per precipitazione lenta della molecola da una soluzione, in condizioni che non dovrebbero alterare la sua struttura Un cristallo proteico È
Le proteine che legano ossigeno: . I cristalli si ottengono per precipitazione lenta della molecola da una soluzione, in condizioni che non dovrebbero alterare la sua struttura Un cristallo proteico È
FUNZIONE DELLE PROTEINE RAPPORTO STRUTTURA-FUNZIONE
 FUNZIONE DELLE PROTEINE RAPPORTO STRUTTURA-FUNZIONE Principi basilari: 1.Le funzioni di molte proteine richiedono il legame reversibile con altre molecole (LIGANDO) Un ligando può essere di natura diversa,
FUNZIONE DELLE PROTEINE RAPPORTO STRUTTURA-FUNZIONE Principi basilari: 1.Le funzioni di molte proteine richiedono il legame reversibile con altre molecole (LIGANDO) Un ligando può essere di natura diversa,
L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO
 L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 23 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata all emoglobina: L O 2 totale
L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 23 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata all emoglobina: L O 2 totale
EMOGLOBINA, MIOGLOBINA MIOGLOBINA ED EMOGLOBINA NEL TRASPORTO DELL OSSIGENO
 EMOGLOBINA, MIOGLOBINA MIOGLOBINA ED EMOGLOBINA NEL TRASPORTO DELL OSSIGENO Trasporto dell ossigeno In tutti gli animali superiori, il metabolismo è aerobico L energia che si può estrarre dal glucosio
EMOGLOBINA, MIOGLOBINA MIOGLOBINA ED EMOGLOBINA NEL TRASPORTO DELL OSSIGENO Trasporto dell ossigeno In tutti gli animali superiori, il metabolismo è aerobico L energia che si può estrarre dal glucosio
Ripiegamento e stabilità delle proteine
 Ripiegamento e stabilità delle proteine Ripiegamento e stabilità delle proteine La conformazione nativa di una proteina è quella a cui si associa la sua funzione biologica. Il termine stabilità può essere
Ripiegamento e stabilità delle proteine Ripiegamento e stabilità delle proteine La conformazione nativa di una proteina è quella a cui si associa la sua funzione biologica. Il termine stabilità può essere
Coefficiente di Hill ( n o n H ) = quanto i siti di legame per l O 2 sono cooperativi tra di loro.
 Cos è n? po n 2 Y= n n p50 + po 2 Coefficiente di Hill ( n o n H ) = quanto i siti di legame per l O 2 sono cooperativi tra di loro. Per l Hb non è mai uguale al numero dei siti per l O 2, Le diverse emoproteine
Cos è n? po n 2 Y= n n p50 + po 2 Coefficiente di Hill ( n o n H ) = quanto i siti di legame per l O 2 sono cooperativi tra di loro. Per l Hb non è mai uguale al numero dei siti per l O 2, Le diverse emoproteine
- natura riduttiva - richiede energia
 - natura ossidativa - produce energia - natura riduttiva - richiede energia 1 L O 2 è poco solubile in acqua (10 ml/l a 20 C): se esso fosse semplicemente disciolto, potrebbe diffondere efficacemente solo
- natura ossidativa - produce energia - natura riduttiva - richiede energia 1 L O 2 è poco solubile in acqua (10 ml/l a 20 C): se esso fosse semplicemente disciolto, potrebbe diffondere efficacemente solo
Formula generale di un amminoacido
 Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
EMOGLOBINA (Hb) nei globuli rossi e
 Nel metabolismo aerobio l O 2 è l accettore finale nel mitocondrio degli elettroni liberati dai composti carboniosi Proteine leganti l O 2 sono EMOGLOBINA (Hb) nei globuli rossi e MIOGLOBINA nelle fibre
Nel metabolismo aerobio l O 2 è l accettore finale nel mitocondrio degli elettroni liberati dai composti carboniosi Proteine leganti l O 2 sono EMOGLOBINA (Hb) nei globuli rossi e MIOGLOBINA nelle fibre
Il legame dell O 2 con l eme di una subunità determina un cambio conformazionale che facilita l attacco dell O 2 agli altri gruppi eme.
 1 Forma T Forma R Il legame dell O 2 con l eme di una subunità determina un cambio conformazionale che facilita l attacco dell O 2 agli altri gruppi eme. 2 1 3 La forma sigmoide della curva indica che
1 Forma T Forma R Il legame dell O 2 con l eme di una subunità determina un cambio conformazionale che facilita l attacco dell O 2 agli altri gruppi eme. 2 1 3 La forma sigmoide della curva indica che
Mioglobina Emoglobina
 Mioglobina Emoglobina Eventi successivi i alla comparsa dell O 2 Possibilità di ottenere circa 20 volte più energia dalla combustione del glucosio Sviluppo di un sistema circolatorio per la distribuzione
Mioglobina Emoglobina Eventi successivi i alla comparsa dell O 2 Possibilità di ottenere circa 20 volte più energia dalla combustione del glucosio Sviluppo di un sistema circolatorio per la distribuzione
EMOGLOBINA, MIOGLOBINA MIOGLOBINA ED EMOGLOBINA NEL TRASPORTO DELL OSSIGENO
 EMOGLOBINA, MIOGLOBINA MIOGLOBINA ED EMOGLOBINA NEL TRASPORTO DELL OSSIGENO Trasporto dell ossigeno In tutti gli animali superiori, il metabolismo è aerobico L energia che si può estrarre dal glucosio
EMOGLOBINA, MIOGLOBINA MIOGLOBINA ED EMOGLOBINA NEL TRASPORTO DELL OSSIGENO Trasporto dell ossigeno In tutti gli animali superiori, il metabolismo è aerobico L energia che si può estrarre dal glucosio
Trasporto di CO 2. ed effetto Bohr. . La CO 2. nei tessuti produce CO 2. Il consumo di O 2. deve essere rimossa e portata ai polmoni (o alle branchie)
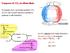 Trasporto di CO 2 ed effetto Bohr Il consumo di O 2 nei tessuti produce CO 2. La CO 2 deve essere rimossa e portata ai polmoni (o alle branchie) Anidrasi carbonica POLMONI La CO 2 abbassa il ph negli eritrociti
Trasporto di CO 2 ed effetto Bohr Il consumo di O 2 nei tessuti produce CO 2. La CO 2 deve essere rimossa e portata ai polmoni (o alle branchie) Anidrasi carbonica POLMONI La CO 2 abbassa il ph negli eritrociti
PROTEINE: STRUTTURA, ESEMPI E FUNZIONAMENTO TUTORATO 1 GIULIANO F. PATANÈ COLLEGIO A. VOLTA
 PROTEINE: STRUTTURA, ESEMPI E FUNZIONAMENTO TUTORATO 1 GIULIANO F. PATANÈ COLLEGIO A. VOLTA PROTEINE Una proteina è basilarmente una catena polipeptidica (che in termini chimici può anche essere definita
PROTEINE: STRUTTURA, ESEMPI E FUNZIONAMENTO TUTORATO 1 GIULIANO F. PATANÈ COLLEGIO A. VOLTA PROTEINE Una proteina è basilarmente una catena polipeptidica (che in termini chimici può anche essere definita
EMOGLOBINA (Hb) nei globuli rossi e
 Nel metabolismo aerobio l O 2 è l accettore finale nel mitocondrio degli elettroni liberati dai composti carboniosi Proteine leganti l O 2 sono EMOGLOBINA (Hb) nei globuli rossi e MIOGLOBINA nelle fibre
Nel metabolismo aerobio l O 2 è l accettore finale nel mitocondrio degli elettroni liberati dai composti carboniosi Proteine leganti l O 2 sono EMOGLOBINA (Hb) nei globuli rossi e MIOGLOBINA nelle fibre
Prof. Maria Nicola GADALETA
 Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Trasporto di O 2 nel sangue
 Trasporto di O 2 nel sangue Il 97% dell O 2 trasportato nel plasma è chimicamente legato all Hb nei globuli rossi, solo il 3% è fisicamente disciolto Trasporto O 2 nel plasma Trasporto O 2 legato ad Hb
Trasporto di O 2 nel sangue Il 97% dell O 2 trasportato nel plasma è chimicamente legato all Hb nei globuli rossi, solo il 3% è fisicamente disciolto Trasporto O 2 nel plasma Trasporto O 2 legato ad Hb
Emoglobina e mioglobina
 Emoglobina e mioglobina Per poter parlare in modo comprensibile dell emoglobina (Hb), è utile occuparsi prima della mioglobina (Mb) che è molto simile all emoglobina ma è molto più semplice. Tra emoglobina
Emoglobina e mioglobina Per poter parlare in modo comprensibile dell emoglobina (Hb), è utile occuparsi prima della mioglobina (Mb) che è molto simile all emoglobina ma è molto più semplice. Tra emoglobina
CLASSIFICAZIONE O.T.I.L.Is. Lig
 GLI ENZIMI CHE COSA SONO? Sono delle proteine altamente specializzate con attività catalitica, accelerano le reazioni chimiche rimanendo inalterati al termine della reazione stessa. CLASSIFICAZIONE O.T.I.L.Is.
GLI ENZIMI CHE COSA SONO? Sono delle proteine altamente specializzate con attività catalitica, accelerano le reazioni chimiche rimanendo inalterati al termine della reazione stessa. CLASSIFICAZIONE O.T.I.L.Is.
Emoglobina e mioglobina
 Emoglobina e mioglobina L emoglobina e la mioglobina proteine centrali per l evoluzione La transizione dalla vita anaerobica a quella aerobica rappresenta un passo fondamentale dell'evoluzione perchè ha
Emoglobina e mioglobina L emoglobina e la mioglobina proteine centrali per l evoluzione La transizione dalla vita anaerobica a quella aerobica rappresenta un passo fondamentale dell'evoluzione perchè ha
Lo scambio gassoso negli animali
 Lo scambio gassoso negli animali Durante la RESPIRAZIONE CELLULARE (mitocondri) le cellule consumano O2 e producono CO2 L approvvigionamento di O2 e la rimozione della CO2 avvengono tramite SCAMBI GASSOSI
Lo scambio gassoso negli animali Durante la RESPIRAZIONE CELLULARE (mitocondri) le cellule consumano O2 e producono CO2 L approvvigionamento di O2 e la rimozione della CO2 avvengono tramite SCAMBI GASSOSI
Regolazione enzimatica Isoenzimi
 Regolazione enzimatica Isoenzimi Gli enzimi regolatori nel metabolismo gruppi di enzimi lavorano insieme per produrre una via metabolica in cui il prodotto del primo enzima diventa il substrato del secondo
Regolazione enzimatica Isoenzimi Gli enzimi regolatori nel metabolismo gruppi di enzimi lavorano insieme per produrre una via metabolica in cui il prodotto del primo enzima diventa il substrato del secondo
Fisiologia della Respirazione 8.Trasporto dei gas nel sangue. Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona
 Fisiologia della Respirazione 8.Trasporto dei gas nel sangue Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona Obiettivi Necessità di un sistema di trasporto chimico ad alta capacità
Fisiologia della Respirazione 8.Trasporto dei gas nel sangue Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona Obiettivi Necessità di un sistema di trasporto chimico ad alta capacità
Il metalloma Struttura e reattività di metalloproteine. Il trasporto dell O 2
 Il metalloma Struttura e reattività di metalloproteine Il trasporto dell O 2 Il trasporto dell ossigeno Nel sangue la solubilità dell O 2 è molto maggiore che in H 2 O In H 2 O la solubilità è 6.59 cm
Il metalloma Struttura e reattività di metalloproteine Il trasporto dell O 2 Il trasporto dell ossigeno Nel sangue la solubilità dell O 2 è molto maggiore che in H 2 O In H 2 O la solubilità è 6.59 cm
Le proteine III. Corso di Biochimica 1. Prof. Giuseppina Pitari
 Le proteine III Corso di Biochimica 1 Prof. Giuseppina Pitari Ossi-mioglobina legame idrogeno lato distale La mioglobina L eme quindi consiste di una struttura organica alla quale è legato un atomo di
Le proteine III Corso di Biochimica 1 Prof. Giuseppina Pitari Ossi-mioglobina legame idrogeno lato distale La mioglobina L eme quindi consiste di una struttura organica alla quale è legato un atomo di
Fisiologia della Respirazione
 Fisiologia della Respirazione 8.Trasporto dei gas nel sangue FGE aa.2016-17 Obiettivi Necessità di un sistema di trasporto chimico ad alta capacità dell O 2 nel sangue: l emoglobina Curva di dissociazione
Fisiologia della Respirazione 8.Trasporto dei gas nel sangue FGE aa.2016-17 Obiettivi Necessità di un sistema di trasporto chimico ad alta capacità dell O 2 nel sangue: l emoglobina Curva di dissociazione
Gli Enzimi. catalizzatori biologici rendono possibile da un punto di vista cinetico le reazioni chimiche
 catalizzatori biologici rendono possibile da un punto di vista cinetico le reazioni chimiche Gli Enzimi Sono le proteine più importanti e più specializzate Presentano un elevato grado di specificità per
catalizzatori biologici rendono possibile da un punto di vista cinetico le reazioni chimiche Gli Enzimi Sono le proteine più importanti e più specializzate Presentano un elevato grado di specificità per
degli eritrociti è una proteina di trasporto indispensabile per veicolare l ossigeno l l anidride carbonica tra i polmoni e i tessuti
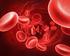 l emoglobina degli eritrociti è una proteina di trasporto indispensabile per veicolare l ossigeno l e l anidride carbonica tra i polmoni e i tessuti Mioglobina, proteina di deposito,, presente nelle fibrocellule
l emoglobina degli eritrociti è una proteina di trasporto indispensabile per veicolare l ossigeno l e l anidride carbonica tra i polmoni e i tessuti Mioglobina, proteina di deposito,, presente nelle fibrocellule
EME (Fe-PROTOPORFIRINA IX)
 EME (Fe-PROTOPORFIRINA IX) 1,3,5,8-tetrametil 2,4-divinil 6,7-dipropionil-porfirina 1 Il ferro può formare sei legami di coordinazione 4 con gli azoti dell anello tetrapirrolico 2 perpendicolari al piano
EME (Fe-PROTOPORFIRINA IX) 1,3,5,8-tetrametil 2,4-divinil 6,7-dipropionil-porfirina 1 Il ferro può formare sei legami di coordinazione 4 con gli azoti dell anello tetrapirrolico 2 perpendicolari al piano
MIOGLOBINA ED EMOGLOBINA
 MIOGLOBINA ED EMOGLOBINA Il passaggio dalla vita anaerobia al metabolismo di tipo aerobico ha rappresentato un vantaggio energetico incredibile. L ossigeno è assolutamente indispensabile per il metabolismo,
MIOGLOBINA ED EMOGLOBINA Il passaggio dalla vita anaerobia al metabolismo di tipo aerobico ha rappresentato un vantaggio energetico incredibile. L ossigeno è assolutamente indispensabile per il metabolismo,
θ = (siti occupati)/(siti disponibili totali) Al numeratore ritrovo solo la mioglobina che ha complessato l'ossigeno, solo l'ossigenata)
 LEZIONE DEL 03/04/2017 Emoglobina - complesso del metallo di transizione (ferro protoporfirina IX) complesso metallorganico. Derivazione della curva di legame iperbolica dell'ossigeno della mioglobina
LEZIONE DEL 03/04/2017 Emoglobina - complesso del metallo di transizione (ferro protoporfirina IX) complesso metallorganico. Derivazione della curva di legame iperbolica dell'ossigeno della mioglobina
REGOLAZIONE ENZIMATICA
 REGOLAZIONE ENZIMATICA Cambio conformazionale In molte molecole proteiche, cambiamenti strutturali possono determinare profondi cambiamenti nella funzione o nell attività. Il cambio conformazionale può
REGOLAZIONE ENZIMATICA Cambio conformazionale In molte molecole proteiche, cambiamenti strutturali possono determinare profondi cambiamenti nella funzione o nell attività. Il cambio conformazionale può
Regolazione dell attività enzimatica. Allosteria Modificazioni covalenti Isoenzimi
 Regolazione dell attività enzimatica Allosteria Modificazioni covalenti Isoenzimi Regolazione della attività enzimatica L attività enzimatica deve potere essere regolata in base alle specifiche richieste
Regolazione dell attività enzimatica Allosteria Modificazioni covalenti Isoenzimi Regolazione della attività enzimatica L attività enzimatica deve potere essere regolata in base alle specifiche richieste
Trasporto gas nel sangue
 Trasporto gas nel sangue Trasporto O2 97% legato all Hb nei globuli rossi 3% fisicamente disciolto, determina il valore di po 2 97% 3% O 2 disciolto nel plasma O 2 legato ad Hb Saturazione Hb 97% 0.3 ml/100ml
Trasporto gas nel sangue Trasporto O2 97% legato all Hb nei globuli rossi 3% fisicamente disciolto, determina il valore di po 2 97% 3% O 2 disciolto nel plasma O 2 legato ad Hb Saturazione Hb 97% 0.3 ml/100ml
Eventi successivi alla comparsa dell O 2
 Eventi successivi alla comparsa dell O 2 Possibilità di ottenere circa 20 volte più energia dalla combustione del glucosio Sviluppo di un sistema circolatorio per la distribuzione dell ossigeno: infatti,
Eventi successivi alla comparsa dell O 2 Possibilità di ottenere circa 20 volte più energia dalla combustione del glucosio Sviluppo di un sistema circolatorio per la distribuzione dell ossigeno: infatti,
Ruolo delle globine nel trasporto e nell immagazzinamento dell ossigeno
 Ruolo delle globine nel trasporto e nell immagazzinamento dell ossigeno Eritrociti umani Ciascun eritrocita contiene circa 300 milioni di molecole di emoglobina Possiedono un motivo strutturale comune.
Ruolo delle globine nel trasporto e nell immagazzinamento dell ossigeno Eritrociti umani Ciascun eritrocita contiene circa 300 milioni di molecole di emoglobina Possiedono un motivo strutturale comune.
Regolazione allosterica
 Macromolecole Biologiche Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Regolazione allosterica Marco Nardini Dipartimento
Macromolecole Biologiche Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Regolazione allosterica Marco Nardini Dipartimento
Trasporto dei gas. Pressioni Volumi
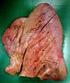 Trasporto dei gas Pressioni Volumi Il 97% dell O 2 trasportato nel plasma si trova chimicamente legato all Hb nei globuli rossi, solo lo 3% è fisicamente disciolto Trasporto O 2 nel plasma Trasporto O
Trasporto dei gas Pressioni Volumi Il 97% dell O 2 trasportato nel plasma si trova chimicamente legato all Hb nei globuli rossi, solo lo 3% è fisicamente disciolto Trasporto O 2 nel plasma Trasporto O
Emoglobina e mioglobina
 Emoglobina e mioglobina L emoglobina e la mioglobina proteine centrali per l evoluzione La transizione dalla vita anaerobica a quella aerobica rappresenta un passo fondamentale dell'evoluzione perchè ha
Emoglobina e mioglobina L emoglobina e la mioglobina proteine centrali per l evoluzione La transizione dalla vita anaerobica a quella aerobica rappresenta un passo fondamentale dell'evoluzione perchè ha
Trasporto O 2 nel sangue
 Trasporto O 2 nel sangue 97% legato all Hb nei globuli rossi 3% fisicamente disciolto (determina il valore di po 2 ) Trasporto O 2 nel plasma Trasporto O 2 legato ad Hb Saturazione Hb 97% 0.3 ml/100ml
Trasporto O 2 nel sangue 97% legato all Hb nei globuli rossi 3% fisicamente disciolto (determina il valore di po 2 ) Trasporto O 2 nel plasma Trasporto O 2 legato ad Hb Saturazione Hb 97% 0.3 ml/100ml
Dopo la ventilazione alveolare, il passaggio successivo del processo respiratorio consiste nella diffusione dell O2 dagli alveoli al sangue e della
 Dopo la ventilazione alveolare, il passaggio successivo del processo respiratorio consiste nella diffusione dell O2 dagli alveoli al sangue e della CO2 in direzione opposta. R = quoziente respiratorio,
Dopo la ventilazione alveolare, il passaggio successivo del processo respiratorio consiste nella diffusione dell O2 dagli alveoli al sangue e della CO2 in direzione opposta. R = quoziente respiratorio,
BIOMOLECOLE (PROTEINE)
 BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
Gli Enzimi. catalizzatori biologici rendono possibile da un punto di vista cinetico le reazioni chimiche
 catalizzatori biologici rendono possibile da un punto di vista cinetico le reazioni chimiche Gli Enzimi Sono le proteine più importanti e più specializzate Presentano un elevato grado di specificità per
catalizzatori biologici rendono possibile da un punto di vista cinetico le reazioni chimiche Gli Enzimi Sono le proteine più importanti e più specializzate Presentano un elevato grado di specificità per
L O 2 nel sangue è trasportato: in piccola parte disciolto nel plasma principalmente legato all Hb. Trasporto dell O 2 nel sangue
 L O 2 nel sangue è trasportato: in piccola parte disciolto nel plasma principalmente legato all Hb Trasporto dell O 2 nel sangue L O 2 è poco solubile in H 2 O per cui nella maggior parte degli organismi
L O 2 nel sangue è trasportato: in piccola parte disciolto nel plasma principalmente legato all Hb Trasporto dell O 2 nel sangue L O 2 è poco solubile in H 2 O per cui nella maggior parte degli organismi
Foto funzioni apparato respiratorio
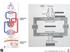 RESPIRAZIONE ESTERNA Foto funzioni apparato respiratorio RESPIRAZIONE INTERNA GLI SCAMBI GASSOSI QUOZIENTE RESPIRATORIO = CO 2 PRODOTTA O 2 CONSUMATO A riposo: Epitelio alveolare 200 ml/min 250 ml/min
RESPIRAZIONE ESTERNA Foto funzioni apparato respiratorio RESPIRAZIONE INTERNA GLI SCAMBI GASSOSI QUOZIENTE RESPIRATORIO = CO 2 PRODOTTA O 2 CONSUMATO A riposo: Epitelio alveolare 200 ml/min 250 ml/min
ACQUISIZIONE SPERIMENTALE DELLA CONOSCENZA NELLE SCIENZE DELLA NATURA.
 CLM C IN MEDICINA E CHIRURGIA C.I. Metodologia medico-scientifica di base II (Scienze umane 2 Epistemologia) A.A. 2013-2014 I anno, 2 semestre ACQUISIZIONE SPERIMENTALE DELLA CONOSCENZA NELLE SCIENZE DELLA
CLM C IN MEDICINA E CHIRURGIA C.I. Metodologia medico-scientifica di base II (Scienze umane 2 Epistemologia) A.A. 2013-2014 I anno, 2 semestre ACQUISIZIONE SPERIMENTALE DELLA CONOSCENZA NELLE SCIENZE DELLA
BIOCHIMICA APPLICATA e CLINICA
 BIOCHIMICA APPLICATA e CLINICA Regolazione Enzimatica Biosegnalazione Regolazione Ormonale Specializzazioni metaboliche (Biochimica d Organo) Integrazione del metabolismo BIOCHIMICA APPLICATA e CLINICA
BIOCHIMICA APPLICATA e CLINICA Regolazione Enzimatica Biosegnalazione Regolazione Ormonale Specializzazioni metaboliche (Biochimica d Organo) Integrazione del metabolismo BIOCHIMICA APPLICATA e CLINICA
IL TRASPORTO DELL O2
 IL TRASPORTO DELL O2 Trasporto dell ossigeno nel sangue Nel sangue arterioso, alla P O2 di 97mmHg: Fisicamente disciolto nel plasma (0,3ml/100ml sangue) Legato all emoglobina dei globuli rossi (20,1 ml/100ml
IL TRASPORTO DELL O2 Trasporto dell ossigeno nel sangue Nel sangue arterioso, alla P O2 di 97mmHg: Fisicamente disciolto nel plasma (0,3ml/100ml sangue) Legato all emoglobina dei globuli rossi (20,1 ml/100ml
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
COMPOSIZIONE DELL ARIA ATMOSFERICA SECCA E PRESSIONI PARZIALI DEI GAS - (760 TORR, 15 C)
 COMPOSIZIONE DELL ARIA ATMOSFERICA SECCA E PRESSIONI PARZIALI DEI GAS - (760 TORR, 15 C) COMPOSIZIONE ARIA NELL ATMOSFERA = COSTANTE A PARTE LE VARIAZIONI DELLA QUANTITA DI VAPORE ACQUEO A 0 C 1 torr =
COMPOSIZIONE DELL ARIA ATMOSFERICA SECCA E PRESSIONI PARZIALI DEI GAS - (760 TORR, 15 C) COMPOSIZIONE ARIA NELL ATMOSFERA = COSTANTE A PARTE LE VARIAZIONI DELLA QUANTITA DI VAPORE ACQUEO A 0 C 1 torr =
Gli elementi corpuscolati del sangue sono vere cellule o derivati cellulari.
 I GLOBULI ROSSI Gli elementi corpuscolati del sangue sono vere cellule o derivati cellulari. I globuli rossi sono i più numerosi (5 milioni per mm 3 nell uomo, 4.5 milioni per mm 3 nella donna) sono detti
I GLOBULI ROSSI Gli elementi corpuscolati del sangue sono vere cellule o derivati cellulari. I globuli rossi sono i più numerosi (5 milioni per mm 3 nell uomo, 4.5 milioni per mm 3 nella donna) sono detti
LE PROTEINE -struttura tridimensionale-
 LE PROTEINE -struttura tridimensionale- Struttura generale di una proteina Ceruloplasmina Cosa sono??? Sono biopolimeri con forme ben definite. composti da molteplici amminoacidi, legati con legami peptidici
LE PROTEINE -struttura tridimensionale- Struttura generale di una proteina Ceruloplasmina Cosa sono??? Sono biopolimeri con forme ben definite. composti da molteplici amminoacidi, legati con legami peptidici
LEZIONE DEL 27/03/2017
 LEZIONE DEL 27/03/2017 Struttura primaria sequenze amminoacidiche --> ponti disolfuro; Strutture secondarie (stabilizzate dai legami idrogeno intercatena): dipendono dal legame peptidico; Strutture terziarie
LEZIONE DEL 27/03/2017 Struttura primaria sequenze amminoacidiche --> ponti disolfuro; Strutture secondarie (stabilizzate dai legami idrogeno intercatena): dipendono dal legame peptidico; Strutture terziarie
I PROTIDI ASPETTI GENERALI
 I PROTIDI ASPETTI GENERALI I PROTIDI O PROTEINE SONO SOSTANZE ORGANICHE AZOTATE, DI STRUTTURA MOLTO COMPLESSA, PRESENTI IN OGNI FORMA DI VITA. LE PROTEINE SONO COMPOSTI QUATERNARI, OSSIA SONO FORMATE DA
I PROTIDI ASPETTI GENERALI I PROTIDI O PROTEINE SONO SOSTANZE ORGANICHE AZOTATE, DI STRUTTURA MOLTO COMPLESSA, PRESENTI IN OGNI FORMA DI VITA. LE PROTEINE SONO COMPOSTI QUATERNARI, OSSIA SONO FORMATE DA
CORSO MONODISCIPLINARE DI BIOCHIMICA (6 CFU)
 UNIVERSITÀ DEGLI STUDI DI TERAMO CORSO DI LAUREA IN BIOTECNOLOGIE CORSO MONODISCIPLINARE DI BIOCHIMICA (6 CFU) Roberto Giacominelli Stuffler IL CORSO MONODISCIPLINARE DI BIOCHIMICA È SUDDIVISO IN DUE UNITÀ
UNIVERSITÀ DEGLI STUDI DI TERAMO CORSO DI LAUREA IN BIOTECNOLOGIE CORSO MONODISCIPLINARE DI BIOCHIMICA (6 CFU) Roberto Giacominelli Stuffler IL CORSO MONODISCIPLINARE DI BIOCHIMICA È SUDDIVISO IN DUE UNITÀ
COMPOSTI AZOTATI. derivanti dall ammoniaca AMMINE. desinenza -INA AMMIDE
 COMPOSTI AZOTATI derivanti dall ammoniaca AMMINE desinenza -INA AMMIDE ANCORA AMMIDI RISONANZA A M M I D I Il legame ammidico ha parziale carattere di doppio legame per la seguente risonanza: Ammidi H
COMPOSTI AZOTATI derivanti dall ammoniaca AMMINE desinenza -INA AMMIDE ANCORA AMMIDI RISONANZA A M M I D I Il legame ammidico ha parziale carattere di doppio legame per la seguente risonanza: Ammidi H
Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi. Possono assumere forme diverse a seconda della funzione
 Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi Hanno elevato PM Possono assumere forme diverse a seconda della funzione svolgono molteplici funzioni Tra le proteine
Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi Hanno elevato PM Possono assumere forme diverse a seconda della funzione svolgono molteplici funzioni Tra le proteine
scaricato da I peptidi risultano dall unione di due o più aminoacidi mediante un legame COVALENTE
 Legame peptidico I peptidi risultano dall unione di due o più aminoacidi mediante un legame COVALENTE tra il gruppo amminico di un aminoacido ed il gruppo carbossilico di un altro. 1 Catene contenenti
Legame peptidico I peptidi risultano dall unione di due o più aminoacidi mediante un legame COVALENTE tra il gruppo amminico di un aminoacido ed il gruppo carbossilico di un altro. 1 Catene contenenti
Proteine: struttura e funzione
 Proteine: struttura e funzione Prof.ssa Flavia Frabetti PROTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (C, H, O,
Proteine: struttura e funzione Prof.ssa Flavia Frabetti PROTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (C, H, O,
end-on (h 1 ) L = NH 3, CN - L Chimica Inorganica Biologica Il diossigeno O 2 Reazioni tra O 2 e metalli: ossidoriduzioni e complessi
 Il diossigeno O 2 Reazioni tra O 2 e metalli: ossidoriduzioni e complessi 4Fe 2+ + O 2 + 2H 2 O + 8 OH - 4(FeOH) 3 2Fe 2 O 3 + H 2 O O 2 interagisce con i metalli ossidandoli e passando allo stato di ox
Il diossigeno O 2 Reazioni tra O 2 e metalli: ossidoriduzioni e complessi 4Fe 2+ + O 2 + 2H 2 O + 8 OH - 4(FeOH) 3 2Fe 2 O 3 + H 2 O O 2 interagisce con i metalli ossidandoli e passando allo stato di ox
AMMINOACIDI. Gli amminoacidi si distinguono in base alla diversità della catena laterale R in ciascuno di essi.
 AMMINOACIDI Gli amminoacidi sono composti polifunzionali, infatti essi presentano sia un gruppo carbossilico, che conferisce loro caratteristiche acide, sia un gruppo amminico, che conferisce loro caratteristiche
AMMINOACIDI Gli amminoacidi sono composti polifunzionali, infatti essi presentano sia un gruppo carbossilico, che conferisce loro caratteristiche acide, sia un gruppo amminico, che conferisce loro caratteristiche
LA MIOGLOBINA e L EMOGLOBINA
 UNITÀ VET. DIDATTICA DI PROPEDEUTICA BIOCHIMICA LA MIOGLOBINA e L EMOGLOBINA Roberto Giacominelli Stuffler LA MIOGLOBINA E L EMOGLOBINAL I vertebrati hanno selezionato due meccanismi principali per rifornire
UNITÀ VET. DIDATTICA DI PROPEDEUTICA BIOCHIMICA LA MIOGLOBINA e L EMOGLOBINA Roberto Giacominelli Stuffler LA MIOGLOBINA E L EMOGLOBINAL I vertebrati hanno selezionato due meccanismi principali per rifornire
Riabilitativa 2015/2016
 Emoglobina e collageno Spina Riabilitativa 2015/2016 WWW.SUNHOPE.IT Alla grande varietà di strutture tridimensionali corrisponde una grande varietà di funzioni Ogni proteina presenta diversi livelli di
Emoglobina e collageno Spina Riabilitativa 2015/2016 WWW.SUNHOPE.IT Alla grande varietà di strutture tridimensionali corrisponde una grande varietà di funzioni Ogni proteina presenta diversi livelli di
Strategie catalitiche
 Strategie catalitiche catalisi acido-base catalisi covalente catalisi da metalli Dati molecolari di alcune proteine Citocromo C (umano) Ribonucleasi A (pancreas di bue) Lisozima (bianco dell uovo) Mioglobina
Strategie catalitiche catalisi acido-base catalisi covalente catalisi da metalli Dati molecolari di alcune proteine Citocromo C (umano) Ribonucleasi A (pancreas di bue) Lisozima (bianco dell uovo) Mioglobina
Scambi gassosi e regolazione del respiro
 Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I Scambi gassosi e regolazione del respiro Ventilazione polmonare Ruolo del Sistema Respiratorio: 1 2 - fornire O 2 - rimuovere
Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I Scambi gassosi e regolazione del respiro Ventilazione polmonare Ruolo del Sistema Respiratorio: 1 2 - fornire O 2 - rimuovere
Il trasporto dell ossigeno
 Prof. Giorgio Sartor Il trasporto dell ossigeno Copyright 2001-2016 by Giorgio Sartor. All rights reserved. Versione 1.9.2 mar 2016 Trasporto dell ossigeno egli organismi aerobi il trasporto dell ossigeno
Prof. Giorgio Sartor Il trasporto dell ossigeno Copyright 2001-2016 by Giorgio Sartor. All rights reserved. Versione 1.9.2 mar 2016 Trasporto dell ossigeno egli organismi aerobi il trasporto dell ossigeno
v = Δ[P] = _ Δ[S] S P
![v = Δ[P] = _ Δ[S] S P v = Δ[P] = _ Δ[S] S P](/thumbs/98/137173050.jpg) CINETICA ENZIMATICA Gli esperimenti di cinetica enzimatica si basano sulla determinazione della velocità di reazione, misurata come variazione della concentrazione del prodotto o del reagente in un dato
CINETICA ENZIMATICA Gli esperimenti di cinetica enzimatica si basano sulla determinazione della velocità di reazione, misurata come variazione della concentrazione del prodotto o del reagente in un dato
GLI ENZIMI: proteine con attività CATALITICA
 Cap. 6 GLI ENZIMI: proteine con attività CATALITICA Catalizzatori biologici: permettono alle reazioni biochimiche di avvenire a temperature e pressioni fisiologiche e a velocità misurabile. Aumentano la
Cap. 6 GLI ENZIMI: proteine con attività CATALITICA Catalizzatori biologici: permettono alle reazioni biochimiche di avvenire a temperature e pressioni fisiologiche e a velocità misurabile. Aumentano la
- utilizzano esclusivamente le reattività chimiche di alcuni residui AA
 Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Scaricato da 1
 A AB B Scaricato da www.sunhope.it 1 1 1 1 2 2 2 3 45 5 5 4 20 20 5 40 40 6 40 20 23 7 5 12 8 35 2 6 9 1 1 Numero di mole ecole 30 25 20 15 10 5 0 0 2 4 6 8 10 Energia Scaricato da www.sunhope.it 2 Scaricato
A AB B Scaricato da www.sunhope.it 1 1 1 1 2 2 2 3 45 5 5 4 20 20 5 40 40 6 40 20 23 7 5 12 8 35 2 6 9 1 1 Numero di mole ecole 30 25 20 15 10 5 0 0 2 4 6 8 10 Energia Scaricato da www.sunhope.it 2 Scaricato
Dipartimento di Biochimica e Biofisica F. Cedrangolo Emoglobina ed introduzione alle emoglobinopatie.
 Dipartimento di Biochimica e Biofisica F. Cedrangolo Emoglobina ed introduzione alle emoglobinopatie. Trasportatori di Ossigeno nei Vertebrati Mioglobina Emoglobina Muscoli Sangue L Emoglobina (Hb) Struttura
Dipartimento di Biochimica e Biofisica F. Cedrangolo Emoglobina ed introduzione alle emoglobinopatie. Trasportatori di Ossigeno nei Vertebrati Mioglobina Emoglobina Muscoli Sangue L Emoglobina (Hb) Struttura
Proteine. Enzimi Fattori di Trascrizione Proteine di Membrana (trasportatori, canale, recettori di membrana)
 Proteine Enzimi Fattori di Trascrizione Proteine di Membrana (trasportatori, canale, recettori di membrana) Ormoni e Fattori di crescita Anticorpi Trasporto Trasporto (emoglobina, LDL, HDL.) Fenotipo Proteine
Proteine Enzimi Fattori di Trascrizione Proteine di Membrana (trasportatori, canale, recettori di membrana) Ormoni e Fattori di crescita Anticorpi Trasporto Trasporto (emoglobina, LDL, HDL.) Fenotipo Proteine
CATENA RESPIRATORIA (CR) FOSFORILAZIONE OSSIDATIVA (FO)
 CATENA RESPIRATORIA (CR) FOSFORILAZIONE OSSIDATIVA (FO) - Decarb. ossid. piruvato - -Ossidazione acidi grassi - Vie ossidative aa -Ciclo di Krebs avvengono tutte nella matrice mitocondriale In tutte queste
CATENA RESPIRATORIA (CR) FOSFORILAZIONE OSSIDATIVA (FO) - Decarb. ossid. piruvato - -Ossidazione acidi grassi - Vie ossidative aa -Ciclo di Krebs avvengono tutte nella matrice mitocondriale In tutte queste
definiscono i confini esterni delle cellule e regolano il traffico di molecole attraverso questi confini. Nelle cellule eucariotiche dividono lo
 definiscono i confini esterni delle cellule e regolano il traffico di molecole attraverso questi confini. Nelle cellule eucariotiche dividono lo spazio interno in compartimenti discreti segregando nel
definiscono i confini esterni delle cellule e regolano il traffico di molecole attraverso questi confini. Nelle cellule eucariotiche dividono lo spazio interno in compartimenti discreti segregando nel
Trasporto dei gas respiratori nel sangue
 Trasporto dei gas respiratori nel sangue La soluzione dei gas nei liquidi C Legge di Henry acq P gas S gas C acq = quantità di gas disciolta nella fase acquosa P gas = pressione parziale del gas nella
Trasporto dei gas respiratori nel sangue La soluzione dei gas nei liquidi C Legge di Henry acq P gas S gas C acq = quantità di gas disciolta nella fase acquosa P gas = pressione parziale del gas nella
Tipi di trasportatori di elettroni nella catena respiratoria
 Tipi di trasportatori di elettroni nella catena respiratoria 1. Flavoproteine 2. Proteine Ferro Zolfo 3. Citocromi 4. Citocromi contenenti Rame 5. Chinone: Coenzima Q All eccezione del coenzima Q, tutti
Tipi di trasportatori di elettroni nella catena respiratoria 1. Flavoproteine 2. Proteine Ferro Zolfo 3. Citocromi 4. Citocromi contenenti Rame 5. Chinone: Coenzima Q All eccezione del coenzima Q, tutti
PROTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi
 POTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (,, O, N) macromolecole organiche, molecole informazionali, polimeri
POTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (,, O, N) macromolecole organiche, molecole informazionali, polimeri
TRASDUZIONE DEL SEGNALE CELLULARE
 TRASDUZIONE DEL SEGNALE CELLULARE RECETTORI I recettori ormonali sono proteine (spesso glicoproteine) capaci di riconoscere e legare l ormone L interazione tra ormone e recettore è estremamente specifica
TRASDUZIONE DEL SEGNALE CELLULARE RECETTORI I recettori ormonali sono proteine (spesso glicoproteine) capaci di riconoscere e legare l ormone L interazione tra ormone e recettore è estremamente specifica
Scambi gassosi e regolazione del respiro
 Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I Scambi gassosi e regolazione del respiro Ruolo del Sistema Respiratorio: - fornire O 2 - rimuovere CO 2 Scaricato da www.sunhope.it
Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I Scambi gassosi e regolazione del respiro Ruolo del Sistema Respiratorio: - fornire O 2 - rimuovere CO 2 Scaricato da www.sunhope.it
STRUTTURA TRIDIMENSIONALE DELLE PROTEINE
 STRUTTURA TRIDIMENSIONALE DELLE PROTEINE Biologia della Cellula Animale 2016 1 STRUTTURA PROTEINE Cooper: The Cell, a Molecular Approach, 2 nd ed. http://en.wikipedia.org/wiki/protein_structure STRUTTURA
STRUTTURA TRIDIMENSIONALE DELLE PROTEINE Biologia della Cellula Animale 2016 1 STRUTTURA PROTEINE Cooper: The Cell, a Molecular Approach, 2 nd ed. http://en.wikipedia.org/wiki/protein_structure STRUTTURA
