Scrivere le molecole
|
|
|
- Evangelina Maggio
- 7 anni fa
- Visualizzazioni
Transcript
1 Scrivere le molecole
2 Scrittura Formula strutturale = = S Acido solforico Etano Formula molecolare 2 S 4 2 6
3 Tipi di scrittura Scrivere tutte le molecole secondo Lewis è spesso lungo e noioso. I chimici hanno sviluppato alcuni tipi di scritture rapide: ondensata Lineare Poligonale
4 Scrittura condensata Sono possibili vari gradi di condensazione Esempi: Alcani lineari e alcani ramificati ( 2 ) Alcuni legami vengono mantenuti ( 3 ) 4 o ( 3 ) 4
5 Sono possibili vari gradi di condensazione Esempi: Alcheni 3 = 3 3 = 3 3 = 3 Alcoli Scrittura condensata ( 3 ) 2 I lone pair di elettroni non si scrivono.
6 Scrittura condensata Anche strutture complesse possono essere scritte su una sola riga, usando le parentesi per racchiudere un gruppo Alcano ramificato 3 ( 3 )( 2 3 ) 2 3
7 Scrittura a scheletro Minima informazione ma non ambigua I carboni non sono mostrati, si assume che siano all intersezione di due o più linee e al termine di ogni linea Gli idrogeni non sono mostrati Tutti gli atomi diversi da e sono mostrati
8 Scrittura a scheletro
9 Notazione per i poligoni Esempi: N
10 Nomi Generici
11 Nome Generico Nomi Identifica un intera classe con caratteristiche simili: Mondo animale: felini, canidi,. Mondo vegetale: solanacee, agrumi,. Farmacologia: antibiotici, antibatterici, himica organica: alcoli, acidi, ammine Nome Specifico Identifica un singolo composto all interno di una classe: Lupo, arancia, aspirina, etanolo,
12 Esempio - Nome generico: ALLI NME SPEIFI FRMULA SPEIFIA metanolo etanolo colesterolo 8 17 R- Formula generica
13 STRUTTURA DELL SELETR determina: parte delle proprietà fisiche INTERA STRUTTURA determina: le proprietà fisiologiche R LEGAME tra il residuo e il gruppo funzionale determina: dettagli di proprietà chimiche parte delle proprietà fisiche GRUPP FUNZINALE determina: le principali proprietà chimiche parte delle proprietà fisiche il nome generico
14 GRUPP è una struttura parziale completa, tranne che per un legame detto valenza libera o legame aperto: Gruppi contenenti solo e si dicono alchili e vengono indicati con R- (R = residuo): Gruppi contenenti anche altri elementi diversi dal carbonio hanno simbolo X- o Y- o Z-: oncetto di Gruppo R- X- Y- Z- N
15 himica dei Gruppi Funzionali 1. Imparare una serie di fatti sperimentali (REAZINI IMIE) e correlarli con la STRUTTURA della molecola. 2. apire e imparare la spiegazione teorica di tale correlazione (quando possibile). 3. Mettere insieme fatti sperimentali e teoria per creare delle regole che servono a predire il comportamento di composti analoghi (con il medesimo gruppo funzionale).
16 Gruppi Funzionali
17 Gruppo Funzionale (GF) 1. Definisce una classe di composti omposti appartenenti ad una stessa classe hanno proprietà simili e simile reattività. 2. È il sito di reazione Determina la chimica della molecola, ossia la sua reattività 3. Fornisce una base per la nomenclatura Ad esempio, tutti i chetoni hanno nei loro nomi il suffisso one:» acetone» ciclopropanone» cortisone
18 omposti senza gruppo funzionale Esiste una classe di composti che contengono soltanto atomi di e legati in vario modo. Sono al 100% scheletro e quasi privi di reattività. Sono gli Idrocarburi Alcani Tuttavia sono importanti perché su di essi si basa la nomenclatura dei composti organici.
19 Gruppi Funzionali Gli alcani sono formati da soli e : Se uno o più idrogeni vengono sostituiti da un atomo diverso dall idrogeno o da un nuovo legame, si crea un Gruppo Funzionale. l
20 omuni Gruppi Funzionali GF.. X:.....Ọ.. S.... Ọ. Ṇ. :: lasse Alogenuri (X = F, l, Br, I) Alcoli Tioli Eteri Ammine Aldeidi GF.... ::.... ::.... : : : : N.. ::.. X.. : :: lasse Acidi carbossilici Esteri carbossilici Anidridi Ammidi Acil alogenuri (X = l, Br) GF :: N.... :.. N.... N Ṅ. : :.. S.. :: lasse Nitro composti Nitroso composti Azo composti Acidi solfonici Alcheni Alchini :: hetoni N: Nitrili Aromatici
21 Notare! Alcuni gruppi funzionali sono strutture parziali con una valenza libera che può essere saturata con un residuo R:.... :: N:.. R R.. :: R N: Altri hanno più valenze libere: :: Ṇ..... R R.. 1 R.. R 1 R 1 N : R.. : R 2 iò comporta la presenza di più residui (R, R 1, R 2, etc.) e quindi di più scheletri.
22 Notare! Il doppio legame =, il triplo legame e l anello aromatico sono considerati gruppi funzionali pur avendo solo carboni e idrogeni perché sono siti di reattività. Una molecola può possedere un solo gruppo funzionale (molecola monofunzionale) o più di uno (molecola polifunzionale).
23 Molecole polifunzionali N ammina nicotina N 3 ammina alcool alchene colesterolo ammide ammide 3 N N 3 ammina 3 N N alchene ammina etere 3 3 etere aromatico 3 etere N 2 ammina caffeina mescalina
24 Scheletro (solo e ) LINEARE (AILI) ILI saturo insaturo saturo insaturo = = =- 2 A L I F A T I I aromatico ARMATII
25 lassificazione di & 1. arbonio saturo sp 3 primario (1 ): Un carbonio legato a un solo altro carbonio 1 : un idrogeno legato a un 1 secondario (2 ): Un carbonio legato a due altri carboni 2 : un idrogeno legato a un 2 terziario (3 ): Un carbonio legato a tre altri carboni 3 : un idrogeno legato a un 3 quaternario (4 ): Un carbonio legato a quattro altri carboni
26 lassificazione di & 1. arbonio saturo sp 3 Y carbonio primario 1 Y carbonio secondario 2 carbonio terziario 3 Quando Y =, alogeno,, N 2, R, anche tali gruppi si definiscono 1, 2, 3 Y carbonio quaternario 4 PERÉ QUESTA DISTINZINE? Perché velocità di reazione e posizione d equilibrio variano, per lo stesso GF Y, in funzione della natura del carbonio cui Y è legato.
27 lassificazione di & primari (1 o ) secondari (2 o ) terziari (3 o ) quaternari (4 o )
28 lassificazione di & 2. arbonio sp 3 adiacente ad un carbonio sp 2 Un carbonio saturo (sp 3 ) adiacente a un carbonio insaturo (sp 2 ) si definisce allilico, se il doppio legame è di un alchene benzilico, se il doppio legame è parte di un anello aromatico vinilici vinilici allilico allilico aromatico aromatici benzilico benzilico
29 lassificazione di 3. Gruppi funzionali insaturi Gruppi funzionali insaturi (=, =, =, N 2,, etc.) possono avere, rispetto ad un altra insaturazione presente nello scheletro, tre posizioni relative. Possono essere: Isolati Almeno 2 legami singoli fra i legami doppi oniugati Alternanza di legami singoli e doppi umulati Nessun legame singolo tra i legami doppi
30 lassificazione di 4. Doppi e tripli legami I doppi legami = si classificano in base al grado di sostituzione dei carboni: 2 R monosostituito R R R 1 2 trisostituito R R 1 disostituito geminale R R 3 R R 1 2 tetrasostituito R R 1 disostituito vicinale trans R terminale R R R 1 disostituito vicinale cis R1 interno
31 Nomenclatura IUPA
32 Nomenclatura IUPA È un sistema nel quale ogni composto ha un suo nome. Seguendo le regole, chiunque assegna a un dato composto il medesimo nome. Viceversa, dato il nome di un composto, ognuno è in grado di disegnare il composto. STRUTTURA IUPA NME
33 Regole di nomenclatura 1. Identificare i GF. 2. Tra questi scegliere il gruppo principale sulla base della tabella di priorità dei gruppi. 3. Scegliere la nomenclatura degli alifatici o degli aromatici sulla base della posizione del gruppo principale. il composto è aromatico se il gruppo principale è legato direttamente all anello
34 Priorità Gruppo lasse Nome del gruppo come sostituente (quando non è principale) 1 () acido alcanoico R carbossi 2 S 3 acido alcansolfonico R S 3 solfo () R 1 () X () N 2 () alchil alcanoato alcanoil alogenuro alcanammide alcanale R R1 R X R N 2 R alcossicarbonil aloformil carbamoil formil il tra parentesi deve portare nella numerazione della catena il numero 1
35 Priorità Gruppo lasse Nome del gruppo come sostituente (quando non è principale) 7 () N alcanonitrile R N ciano 8 alcanone R R 1 osso 9 alcanolo R idrossi 10 N 2 alchilammina R N 2 ammino 11 alchil alchil etere R R 1 alcossi 12 () () alchino R R 1 ino alchene R 1 X alogenoalcano R X N 2 nitroalcano R N 2 R R 2 R 3 ene alo nitro
36 Nomenclatura dei composti alifatici
37 Nomenclatura degli alifatici 1. Identificare la classe di appartenenza (gruppo principale) 2. Identificare la catena principale di atomi di carbonio contigui, seguendo le seguenti regole di priorità: la catena principale deve contenere: a. il gruppo principale b. il massimo numero possibile di legami = e c. il massimo numero possibile di atomi di d. il massimo numero possibile di sostituenti 3. Assegnare il nome alla catena principale in base al numero di carboni da cui è formata.
38 4. Numerare la catena in modo tale che: al gruppo principale spetti il numero più basso possibile ai gruppi secondari spetti il numero più basso possibile (= precede ) 5. Nel nome indicare il numero che spetta al gruppo principale (tranne che per,, N, etc. che hanno il n 1). 6. Includere nel nome il gruppo = (ene) (o, ino). 7. Aggiungere il nome dei sostituenti davanti al nome in ordine alfabetico con la posizione relativa.
39 Procedura 1. Identificare la classe: alcanale, acido alcanoico, alchene 2. Identificare la più lunga catena di atomi di carbonio 3. Assegnare il nome della catena in base al numero di atomi di : 4 1 metano 3 ( 2 ) eptano n tridecano etano 3 ( 2 ) ottano n tetradecano propano 3 ( 2 ) nonano n icosano 3 ( 2 ) butano 3 ( 2 ) decano n triacontano 3 ( 2 ) pentano 3 ( 2 ) undecano n tetracontano 3 ( 2 ) esano 3 ( 2 ) dodecano etc.
40 Se le catene possibili sono due, scegliere quella con il maggior numero di sostituenti sostituenti alchilici ( solo e ) 4. Numerare i carboni Partire dal lato più vicino al primo sostituente. Se vi sono due sostituenti equidistanti cercare il sostituente successivo
41 6. Includere nel nome il gruppo = e/o ambiare il suffisso da alcano in alchene o alchino Assegnare al legame = e un numero di posizione (il più basso possibile) = metil-2-pentene esino Nella numerazione, il doppio legame ha la precedenza sui sostituenti
42 7. Nome dei sostituenti a. Sostituenti alchilici (alcano alchile) 1: 3, metile 2: 3 2, etile 3: 3 2 2, n-propile; 3, isopropile 3 4: , n-butile; 2 3, isobutile , sec-butile; 3, tert-butile etc. 3 3
43 7. Nome dei sostituenti b.sostituenti cicloalchilici, ciclopropile;, ciclobutile;, ciclopentile;, cicloesile c. Sostituenti Alchenilici 2 =, etenile o vinile; 2 =- 2, 2-propenile o allile, fenile; 2, benzile
44 7. Nome dei sostituenti d. Sostituenti diversi da alchili: vedi Tabella dei Gruppi Funzionali. F, fluoro; l, cloro; Br, bromo; I, iodo N 2, nitro; N 2, ammino; N, ciano; S 3, solfo;, oxo, idrossi; R, alcossi;, carbossi etc.
45 Alfabetizzazione I sostituenti vanno fatti precedere al nome in ordine alfabetico. Il corsivo viene ignorato: sec-, tert- Se uno stesso sostituente è presente più volte, usare di-, tri-, tetra-, etc.. Tali prefissi vengono ignorati nella alfabetizzazione.
46 Sostituenti complessi 1. Assegnare il numero 1 al carbonio del sostituente legato alla catena principale. 2. Numerare la catena di atomi di carbonio verso l esterno prendendo la catena più lunga. Dare il nome alla catena alchilica con suffisso ile 3. (Se c è un doppio legame alchile diventa alchenile) 4. Aggiungere i sostituenti con i loro numeri (1-metiletil) I gruppi complessi sono posti in parentesi.
47 Esempi (1,3-dimetilbutil) (2-etil-1,1-dimetilbutil) (1-metilbutil) (1-etilpropil) =-- 3 (4-oxo-2-pentenil)
48 omposti ciclici sostituiti i si può basare o sull anello o sulla catena più lunga isopropilcicloesano 2-cicloesilpropano tert-butilciclopentano 2-ciclopentil-2-metilpropano
49 Nomenclatura delle ammine R-N 2, R 1 -N-R 2 R 1 -N-R 2 ammina ammina ammina primaria secondaria terziaria Trovare la catena più lunga di atomi di. -o dell alcano è sostituito con -ammina. I sostituenti sull azoto hanno N- come prefisso. Br N bromo-1-pentanammina N( 3 ) 2 R N,N-dimetil-3-esanammina Alternativa: considerare -NR 1 R 2 come sostituente
50 Esempi N N,N-dimetil-2-(metilpropil)ammina 3-(N,N-dimetilammino)-4-metilesano N
51 Nomenclatura degli Eteri R 1 --R 2 IUPA: Alcossi alcano metil-2-metossipropano 3 Metossicicloesano omune: R 1 R 2 : alchil 1 alchil 2 etere R 1 = R 2 : dialchil etere dietil etere 3 t-butil metil etere
52 Esempi
53 A. Gruppi funzionali:, B. Priorità: (Gruppo principale) lasse: alcanale. atena principale: 4 Nome parziale: butanale D. Numerazione catena principale: E. Assegnare il numero al gruppo principale (quando serve): non serve F. Includere nel nome il gruppo sussidiario: non c è. G. Aggiungere i sostituenti col loro numero: 3-idrossi. 3-idrossibutanale
54 F atena principale: 5 Nome parziale: acido pentanoico D. Numerazione catena principale 1 A. Gruppi funzionali:, =, F E. Assegnare il numero al gruppo principale (quando serve): non serve B. Priorità: (gruppo principale) lasse: acido alcanoico F. Includere nel nome il gruppo sussidiario con il relativo numero: acido 2-pentenoico G. Aggiungere i sostituenti col loro numero: 5,5,5-trifluoro. acido 5,5,5-trifluoro-2-pentenoico
55 atena principale: 2 Nome parziale: etanolo D. Numerazione catena principale A. Gruppi funzionali:, --, l E. Assegnare il numero al gruppo principale (quando serve): 1-etanolo B. Priorità: (gruppo principale) lasse: alcanolo F. Includere nel nome il gruppo sussidiario con il relativo numero: non c è G. Aggiungere i sostituenti col loro numero: 2-(2-cloroetossi) 2 l 2-(2-cloroetossi)-1-etanolo
56 S A. Gruppi funzionali: S 3, =, N N B. Priorità: S 3 (gruppo principale) lasse: acido alcansolfonico. atena principale: 6 Nome parziale: acido esansolfonico D. Numerazione catena principale E. Assegnare il numero al gruppo principale (quando serve): acido 3-esansolfonico F. Includere nel nome il gruppo sussidiario con il relativo numero: acido 1-esen-3-solfonico G. Aggiungere i sostituenti col loro numero: 6-ciano acido 6-ciano-1-esen-3-solfonico
57 A. Gruppi funzionali: =, B. Priorità: (gruppo principale) lasse: alchino. atena principale: 11 Nome parziale: undecino D. Numerazione catena principale E. Assegnare il numero al gruppo principale (quando serve): 3-undecino F. Includere nel nome il gruppo sussidiario con il relativo numero: 5-undecen-3-ino G. Aggiungere i sostituenti col loro numero: 2,6,10-trimetil 3 2 2,6,10-trimetil- 5-undecen-3-ino 1
58 l A. Gruppi funzionali: =, l, 1 2 B. Priorità: (gruppo principale) lasse: alchil alcanoato. atena principale: 4. atena secondaria: 2 Nome parziale: etil butanoato D. Numerazione catena principale (e secondaria): E. Assegnare il numero al gruppo principale (quando serve): non serve F. Includere nel nome il gruppo sussidiario con il relativo numero: etil 3-butenoato G. Aggiungere i sostituenti col loro numero in ordine alfabetico: 4-cloro- 2,2-dimetil etil 4-cloro-2,2-dimetil-3-butenoato
59 Da ricordare 1. Il nome base usa sempre la catena più lunga 2. Numerare dalla fine più vicina al primo sostituente 3. I gruppi si scrivono in ordine alfabetico: a,b,c.. 4. Nell alfabetizzazione i multipli sono ignorati: dietil= e 5. arboni disostituiti (due gruppi) sono più importanti dei monosostituiti (un gruppo) 6. I numeri sono separati dai numeri da virgole: 2,3 7. I numeri sono separati dalle parole da trattini: 3-etil 8. L ultimo sostituente e la radice non sono separati metilesano
60 Nomenclatura degli aromatici 1. Identificare il composto base (v. tabella) 2. Numerare l'anello a. Il carbonio cui il sostituente è legato porta il numero 1 b. Numerare gli altri carboni nella direzione che permetta il più basso set di numeri c. A parità di numeri, vince il sostituente con iniziale più bassa nell'ordine alfabetico
61 Priorità omposto base Nome base Priorità omposto base Nome base 1 acido benzoico 9 3 cresolo* 2 R alchil benzoato 10 fenolo 3 S 3 acido benzen solfonico 11 3 N 2 toluidina* 4 5 X X = l, Br N 3 benzoil alogenuro acetanilide N 2 3 anilina xilene* 6 N 2 benzammide 14 3 toluene 7 benzaldeide 15 benzene 8 N benzonitrile *o-, m-, p-
62 Esempio l Gruppo principale: Fenolo l gruppo principale 2. Numerazione anello: 3. Sostituente complesso: (2-cloro-1-etilpropil) 4. Assemblaggio: 2-cloro-4-(2-cloro-1-etilpropil)fenolo
63 Dal nome al composto da destra a sinistra 1. Identificare il gruppo principale - suffisso 2. Identificare la catena di atomi di carbonio 3. Identificare la posizione del gruppo principale 4. Identificare i sostituenti e la loro posizione sulla catena 5. Inserire gli idrogeni
64 Dal nome al composto 2-metilesano 5-etil-2-fenil-4-otten-3-one
65 Isomeri costituzionali
66 Isomeria costituzionale o strutturale Isomeri costituzionali sono molecole che hanno lo stesso tipo e numero di atomi (stessa formula) ma legati tra loro in modo diverso. Esempio formula isomeri costituzionali moleculare - stessa formula molecolare - differente struttura
67 Isomeria costituzionale Formula Molecolare Isomeri ostituzionali
68 Numero di Insaturazione formula molecolare AxByzDw A atomi tetravalenti;, Si B atomi monovalenti:, alogeni atomi bivalenti:, S D atomi trivalenti: N, P N.I. = x y/2 + 0z + w/2 + 1 INSATURAZINI: doppi legami, cicli, tripli legami
69 ome trovare gli isomeri costituzionali
70 Isomeri di composti saturi che contengono solo carbonio e atomi monovalenti 1. Formare tutti gli scheletri possibili: i. Disegnare la catena lineare ii. Rimuovere 1 carbonio e legarlo in differentiposizioni della catena così accorciata iii.rimuovere 2 carboni dalla catena originaria, e sistemarli sulla catena, sia individualmente sia insieme sullo stesso carbonio iv. ontinuare così a rimuovere i carboni e legarli alla catena sia individualmente che in gruppi fino a che non è possibile creare nuovi isomeri. 2. Etichettare i carboni, se occorre 3. Aggiungere gli elementi monovalenti
71 Esempi isomeri (1) 3 isomeri (1) 5 isomeri
72 Isomeri di composti saturi che contengono carbonio, atomi mono- e bi- o trivalenti 1. Dividere i in 2 gruppi (se c è o S) in 3 gruppi (se c è N o P) in tutti i modi possibili 2. Formare tutti gli scheletri possibili 3. Etichettare i carboni 4. Legare (o S) a 2 catene di Legare N (o P) a 3 catene di 5. Aggiungere gli elementi monovalenti in tutti i modi possibili, eventualmente etichettando nuovamente lo scheletro
73 Esempi elemento bivalente 1. Tutti i possibili scheletri divisi in 2 gruppi 2. Etichettare i carboni a a b Aggiungere l ossigeno 4. Aggiungere gli idrogeni dove serve 3 isomeri
74 3 7 F 1 elemento bivalente 1. Tutti i possibili scheletri divisi in 2 gruppi a a Etichettare i carboni 3. Aggiugere l ossigeno c b a b a b a b a c 4. Rietichettare i carboni F 5. Aggiungere il fluoro 6. Aggiungere gli idrogeni F F F F F F F 8 isomeri
75 Isomeri di composti insaturi 1. Formare tutti gli scheletri possibili nel modo già visto. 2. Inserire l insaturazione o come legame multiplo o come anello in tutti i modi possibili. 3. Procedere nel modo visto precedentemente.
76 Esempio 3 6 NI = = 1 1 elemento bivalente 1. Tutti i possibili scheletri divisi in 2 gruppi a a b Etichettare. 3. Aggiungere l ossigeno 4. Aggiungere l insaturazione: doppio legame o anello 5. Aggiungere gli idrogeni 6. Eliminare i doppioni 9 isomeri
77 Isomeri costituzionali Sono molecole diverse. anno la stessa formula ma i loro atomi sono legati in modo diverso. Non possono interconvertirsi se non rompendo e riformando legami Tutte le proprietà fisiche degli isomeri costituzionali sono differenti: punti di fusione, punti di ebollizione, densità, solubilità, etc.
78 Isomeri costituzionali negli aromatici
79 1. Benzene 2. Benzene monosostituito 3. Benzene disostituito 4. Benzene trisostituito in modo uguale R orto o- R R R 1 R R R meta m- R R 1 R R R 1 para p- R R R R
80 5. Benzene polisostituito in modo diverso 1) Inserire il 1 sostituente 2) Etichettare b c a b a R 3) Inserire il 2 sostituente 4) Etichettare b c a d R R 1 c d b R 1 a R R 1 b a b R a 3) Inserire il 3 sostituente R 2 R R 2 R R R 4) Etichettare R 1 R 1 R 2 R 1 R 2 R 1 e così via
Chimica del carbonio. 1. Composti contenenti azoto (C,H,N) ammine. Aromatici (derivati del benzene di formula C 6 H 6 )
 himica del carbonio Il carbonio forma con 4 atomi diversi 4 legami covalenti equivalenti posti a 109,5, oppure con 3 atomi diversi 3 legami posti a 120, di cui uno doppio, oppure 2 legami covalenti con
himica del carbonio Il carbonio forma con 4 atomi diversi 4 legami covalenti equivalenti posti a 109,5, oppure con 3 atomi diversi 3 legami posti a 120, di cui uno doppio, oppure 2 legami covalenti con
Diagramma di flusso degli idrocarburi
 Glialcanisonoidrocarburi saturi. saturi (solo legami semplici) idrocarburi (solo e ) n 2n+2 Esano 6 14 Diagramma di flusso degli idrocarburi Idrocarburi Saturi Insaturi Alcani Aciclici iclici atena lineare
Glialcanisonoidrocarburi saturi. saturi (solo legami semplici) idrocarburi (solo e ) n 2n+2 Esano 6 14 Diagramma di flusso degli idrocarburi Idrocarburi Saturi Insaturi Alcani Aciclici iclici atena lineare
Introduzione alla chimica organica. Daniele Dondi
 Introduzione alla chimica organica Daniele Dondi dondi@unipv.it Il carbonio nelle sue ibridazioni sp 3 sp 2 sp Il carbonio è un elemento fondamentale per la chimica organica. La stabilità del legame -
Introduzione alla chimica organica Daniele Dondi dondi@unipv.it Il carbonio nelle sue ibridazioni sp 3 sp 2 sp Il carbonio è un elemento fondamentale per la chimica organica. La stabilità del legame -
Sandro Campestrini Dipartimento di Chimica Organica, Via Marzolo 1
 Sandro Campestrini Dipartimento di Chimica Organica, Via Marzolo 1 E-mail: sandro.campestrini@unipd.it Phone: 049-8275289 http://www.chfi.unipd.it/home/s.campestrini Testo consigliato: FONDAMENTI di CHIMICA
Sandro Campestrini Dipartimento di Chimica Organica, Via Marzolo 1 E-mail: sandro.campestrini@unipd.it Phone: 049-8275289 http://www.chfi.unipd.it/home/s.campestrini Testo consigliato: FONDAMENTI di CHIMICA
IDROCARBURI. Alcani Alcheni Alchini C-C C=C C C
 IDROCARBURI Alcani Alcheni Alchini C-C C=C C C Nomenclatura Degli idrocarburi saturi (Alcani) CH 4 Metano C 2 H 6 Etano C n H 2n+2 Si dicono alchilici quei gruppi che contengono un idrogeno in meno del
IDROCARBURI Alcani Alcheni Alchini C-C C=C C C Nomenclatura Degli idrocarburi saturi (Alcani) CH 4 Metano C 2 H 6 Etano C n H 2n+2 Si dicono alchilici quei gruppi che contengono un idrogeno in meno del
Introduzione alla chimica organica. Daniele Dondi
 Introduzione alla chimica organica Daniele Dondi dondi@unipv.it 1 enni sulla nascita della chimica organica Analisi elementari tramite combustione WÖLER (metà 1800) sintetizza l urea KLBE sintetizza l
Introduzione alla chimica organica Daniele Dondi dondi@unipv.it 1 enni sulla nascita della chimica organica Analisi elementari tramite combustione WÖLER (metà 1800) sintetizza l urea KLBE sintetizza l
Tipologie di formule chimiche
 CHIMICA ORGANICA Tipologie di formule chimiche FORMULA RAZIONALE Tipo di formula che utilizza una rappresentazione analoga alla formula bruta per quei gruppi di atomi sulla cui disposizione non vi possono
CHIMICA ORGANICA Tipologie di formule chimiche FORMULA RAZIONALE Tipo di formula che utilizza una rappresentazione analoga alla formula bruta per quei gruppi di atomi sulla cui disposizione non vi possono
Gruppi funzionali. Gruppi funzionali
 Gruppi funzionali Gruppi funzionali La reattività chimica di ogni molecola organica, indipendentemente dalle sue dimensioni o dalla sua complessità, è determinata dai gruppi funzionali che essa contiene
Gruppi funzionali Gruppi funzionali La reattività chimica di ogni molecola organica, indipendentemente dalle sue dimensioni o dalla sua complessità, è determinata dai gruppi funzionali che essa contiene
Nomenclatura Chimica organica. International Union of Pure and Applied Chemistry (IUPAC).
 Nomi tradizionali e nomi IUPAC Nomenclatura Chimica organica In passato si assegnavano i nomi alle molecole organiche in base alla loro origine o a certe proprietà. Per esempio l acido citrico deriva dal
Nomi tradizionali e nomi IUPAC Nomenclatura Chimica organica In passato si assegnavano i nomi alle molecole organiche in base alla loro origine o a certe proprietà. Per esempio l acido citrico deriva dal
SSPSS Chimica Prime Pioda 1. Nomenclatura. Regola 1. Regola 2. Regola 3
 SSPSS Chimica Prime Pioda 1 Nomenclatura Regola 1 Tabella dei nomi in base al numero di atomi di carbonio N Nome N Nome N Nome 1 metano 11 undecano 21 eneicosano 2 etano 12 dodecano 22 docosano 3 propano
SSPSS Chimica Prime Pioda 1 Nomenclatura Regola 1 Tabella dei nomi in base al numero di atomi di carbonio N Nome N Nome N Nome 1 metano 11 undecano 21 eneicosano 2 etano 12 dodecano 22 docosano 3 propano
Gruppi funzionali Un gruppo funzionale è un atomo o un gruppo di atomi con proprietà chimiche e fisiche tipiche. E
 Gruppi funzionali Gruppi funzionali La reattività chimica di ogni molecola organica, indipendentemente dalle sue dimensioni o dalla sua complessità, è determinata dai gruppi funzionali che essa contiene
Gruppi funzionali Gruppi funzionali La reattività chimica di ogni molecola organica, indipendentemente dalle sue dimensioni o dalla sua complessità, è determinata dai gruppi funzionali che essa contiene
3. Indicare quale (o quali) delle seguenti coppie di formule strutturali rappresenta la stessa molecola:
 . Indicare quale (o quali) delle seguenti coppie di formule strutturali rappresenta la stessa molecola: l a) NO b) l l l c) l l 4. Quali tra i seguenti scheletri di atomi di carbonio non rappresentano
. Indicare quale (o quali) delle seguenti coppie di formule strutturali rappresenta la stessa molecola: l a) NO b) l l l c) l l 4. Quali tra i seguenti scheletri di atomi di carbonio non rappresentano
IDROCARBURI. Alcani Alcheni Alchini Areni. Tipo di legami carboniocarbonio. Solo legami semplici. Uno o più tripli legami. Uno o più doppi legami
 IMICA ORGANICA La chimica del carbonio, per le proprietà del carbonio di formare un numero grandissimo di composti con proprietà diverse, costituisce una branca della chimica, denominata chimica organica.
IMICA ORGANICA La chimica del carbonio, per le proprietà del carbonio di formare un numero grandissimo di composti con proprietà diverse, costituisce una branca della chimica, denominata chimica organica.
Gli idrocarburi contengono solo atomi di carbonio e di idrogeno. Gli idrocarburi alifatici hanno molecole lineari (talora ramificate) mentre quelli
 Gli idrocarburi contengono solo atomi di carbonio e di idrogeno. Gli idrocarburi alifatici hanno molecole lineari (talora ramificate) mentre quelli ciclici presentano molecole ad anello. Se hanno tutti
Gli idrocarburi contengono solo atomi di carbonio e di idrogeno. Gli idrocarburi alifatici hanno molecole lineari (talora ramificate) mentre quelli ciclici presentano molecole ad anello. Se hanno tutti
Ammine N R N R R R-NH 2. Gruppo funzionale: NH 2. Gruppo amminico. Ammine terziarie. Ammine primarie. Ammine secondarie
 Ammine Gruppo funzionale: N 2 Gruppo amminico -N 2 Ammine primarie N N Ammine terziarie Ammine secondarie Ammine Nomi comuni Le ammine semplici vengono generalmente designate con nomi comuni, accettati
Ammine Gruppo funzionale: N 2 Gruppo amminico -N 2 Ammine primarie N N Ammine terziarie Ammine secondarie Ammine Nomi comuni Le ammine semplici vengono generalmente designate con nomi comuni, accettati
Idrocarburi Al A ifatici Ar A oma m tici
 GLI IDROCARBURI Gli idrocarburi sono i più semplici composti del carbonio con l'idrogeno. Sono le molecole di base della chimica organica poiché, oltre ad essere molto numerosi, tutti gli altri composti
GLI IDROCARBURI Gli idrocarburi sono i più semplici composti del carbonio con l'idrogeno. Sono le molecole di base della chimica organica poiché, oltre ad essere molto numerosi, tutti gli altri composti
2. Gli Idrocarburi IDROCARBURI. solo C e H. alcani e cicloalcani (solo C sp 3 ) alcheni e cicloalcheni (almeno 2 C sp 2 ) Alifatici
 2. Gli Idrocarburi IDROCARBURI solo C e H Si classificano in 2 grandi gruppi, a loro volta suddivisi in sottogruppi. Alifatici alcani e cicloalcani (solo C sp 3 ) alcheni e cicloalcheni (almeno 2 C sp
2. Gli Idrocarburi IDROCARBURI solo C e H Si classificano in 2 grandi gruppi, a loro volta suddivisi in sottogruppi. Alifatici alcani e cicloalcani (solo C sp 3 ) alcheni e cicloalcheni (almeno 2 C sp
La chimica organica è la chimica dei composti contenenti carbonio
 Chimica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio I carbonati, il biossido di carbonio e i cianuri metallici sono un eccezione in quanto vengono classificati
Chimica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio I carbonati, il biossido di carbonio e i cianuri metallici sono un eccezione in quanto vengono classificati
Nome degli alcheni a catena lineare
 Gli alcheni sono idrocarboni insaturi. insaturi (almeno un doppio legame) idrocarboni (solo e ) n 2n 1-Esene 6 12 opyright 1999, Michael J. Wovkulich. All rights reserved. Nome degli alcheni a catena lineare
Gli alcheni sono idrocarboni insaturi. insaturi (almeno un doppio legame) idrocarboni (solo e ) n 2n 1-Esene 6 12 opyright 1999, Michael J. Wovkulich. All rights reserved. Nome degli alcheni a catena lineare
Esercitazione n. 3 - Nomenclatura (II)
 Esercitazione n. 3 - omenclatura (II) 1. iascuna delle seguenti strutture è monofunzionale. Indicare in ciascun caso il gruppo funzionale (aggiungendo 1, 2 o 3 quando appropriato), specificandone la desinenza
Esercitazione n. 3 - omenclatura (II) 1. iascuna delle seguenti strutture è monofunzionale. Indicare in ciascun caso il gruppo funzionale (aggiungendo 1, 2 o 3 quando appropriato), specificandone la desinenza
Chimica Organica. Definizione. La chimica organica è la chimica dei composti contenenti carbonio
 himica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio Il carbonio è l unico elemento capace di legarsi fortemente con se stesso e formare lunghe catene o anelli
himica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio Il carbonio è l unico elemento capace di legarsi fortemente con se stesso e formare lunghe catene o anelli
Gli Alcheni : struttura e nomenclatura
 Gli Alcheni : struttura e nomenclatura Alcheni Gli alcheni sono idrocarburi che contengono un doppio legame carbonio-carbonio sono anche detti olefine o idrocarburi insaturi La formula molecolare è n H
Gli Alcheni : struttura e nomenclatura Alcheni Gli alcheni sono idrocarburi che contengono un doppio legame carbonio-carbonio sono anche detti olefine o idrocarburi insaturi La formula molecolare è n H
Idrocarburi Saturi. Alcani
 Idrocarburi Saturi Alcani IDROCARBURI I principali componenti del petrolio e del gas naturale, risorse dalle quali proviene la maggior parte dei combustibili per la produzione di energia sono idrocarburi,
Idrocarburi Saturi Alcani IDROCARBURI I principali componenti del petrolio e del gas naturale, risorse dalle quali proviene la maggior parte dei combustibili per la produzione di energia sono idrocarburi,
Capitolo A1 Chimica organica: un introduzione
 Quesiti e problemi 1 C 2 B 3 B 4 B 5 The ability to form covalent bonds. 6 Gli idrocarburi si suddividono in saturi e insaturi. Gli idrocarburi saturi contengono solo legami semplici C-C; fa parte di questo
Quesiti e problemi 1 C 2 B 3 B 4 B 5 The ability to form covalent bonds. 6 Gli idrocarburi si suddividono in saturi e insaturi. Gli idrocarburi saturi contengono solo legami semplici C-C; fa parte di questo
Introduzione alla Chimica Organica. Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display.
 Introduzione alla Chimica Organica Copyright The McGraw-ill Companies, Inc. Permission required for reproduction or display. 1 Elementi Comuni nei Composti Organici 2 Classificazione degli idrocarburi
Introduzione alla Chimica Organica Copyright The McGraw-ill Companies, Inc. Permission required for reproduction or display. 1 Elementi Comuni nei Composti Organici 2 Classificazione degli idrocarburi
Teoria degli orbitali. Lo spazio intorno al nucleo in cui è possibile trovare con la massima probabilità gli elettroni viene chiamato orbitale.
 Teoria degli orbitali Lo spazio intorno al nucleo in cui è possibile trovare con la massima probabilità gli elettroni viene chiamato orbitale. orbitale nucleo STPA-Chimica Organica 1 L orbitale 1s Gli
Teoria degli orbitali Lo spazio intorno al nucleo in cui è possibile trovare con la massima probabilità gli elettroni viene chiamato orbitale. orbitale nucleo STPA-Chimica Organica 1 L orbitale 1s Gli
IDROCARBURI: NOMENCLATURA. Prof.ssa Tiziana Bellini
 IDROCARBURI: NOMENCLATURA Prof.ssa Tiziana Bellini IDROCARBURI LINEARI ALCANI metano IDROCARBURI LINEARI CH 4 CH 4 etano propano butano pentano esano eptano ottano nonano decano ( ) 4 ( ) 5 ( ) 6 ( ) 7
IDROCARBURI: NOMENCLATURA Prof.ssa Tiziana Bellini IDROCARBURI LINEARI ALCANI metano IDROCARBURI LINEARI CH 4 CH 4 etano propano butano pentano esano eptano ottano nonano decano ( ) 4 ( ) 5 ( ) 6 ( ) 7
I composti organici. Gli idrocarburi: composti binari, ovvero costituiti solo da due elementi. Carbonio (C) e idrogeno (H)
 I composti organici Gli idrocarburi: composti binari, ovvero costituiti solo da due elementi. Carbonio (C) e idrogeno (H) Gli idrocarburi Gli Alcani Costituiti da uno o più atomi di carbonio legati tra
I composti organici Gli idrocarburi: composti binari, ovvero costituiti solo da due elementi. Carbonio (C) e idrogeno (H) Gli idrocarburi Gli Alcani Costituiti da uno o più atomi di carbonio legati tra
Nomi e formule dei principali composti organici
 Nomi e formule dei principali composti organici Il numero davvero sterminato dei composti organici e la necessità quindi di doverli distinguere ciascuno con la propria formula e il proprio nome, ha costretto
Nomi e formule dei principali composti organici Il numero davvero sterminato dei composti organici e la necessità quindi di doverli distinguere ciascuno con la propria formula e il proprio nome, ha costretto
Nomi e formule dei principali composti organici
 Il numero davvero sterminato dei e la necessità quindi di doverli distinguere ciascuno con la propria formula e il proprio nome, ha costretto i chimici (attraverso un apposito organismo, la IUPAC) a mettere
Il numero davvero sterminato dei e la necessità quindi di doverli distinguere ciascuno con la propria formula e il proprio nome, ha costretto i chimici (attraverso un apposito organismo, la IUPAC) a mettere
Chimica organica Chimica dei composti del carbonio. Nelle molecole organiche oltre al carbonio sono presenti pochi altri elementi: H, O, N, P,
 himica organica himica dei composti del carbonio. Nelle molecole organiche oltre al carbonio sono presenti pochi altri elementi:,, N, P, S, alogeni. Le molecole organiche presentano particolari raggruppamenti
himica organica himica dei composti del carbonio. Nelle molecole organiche oltre al carbonio sono presenti pochi altri elementi:,, N, P, S, alogeni. Le molecole organiche presentano particolari raggruppamenti
- il DNA, la molecola che contiene l informazione genetica, - le proteine dei nostro organismo ( proteine dei muscoli, della pelle, gli enzimi),
 La chimica organica è la chimica dei composti del carbonio, che sono i mattoni con cui sono costruiti tutti i corpi viventi della terra. Questi composti comprendono ad esempio - il DNA, la molecola che
La chimica organica è la chimica dei composti del carbonio, che sono i mattoni con cui sono costruiti tutti i corpi viventi della terra. Questi composti comprendono ad esempio - il DNA, la molecola che
NOMENCLATURA DI MOLECOLE CONTENENTI GRUPPI FUNZIONALI E LEGAMI MULTIPLI
 NOMENCLATURA DI MOLECOLE CONTENENTI GRUPPI FUNZIONALI E LEGAMI MULTIPLI Quando la molecola contiene sia un gruppo funzionale che un legame multiplo la desinenza deve essere doppia, includendo sia il suffisso
NOMENCLATURA DI MOLECOLE CONTENENTI GRUPPI FUNZIONALI E LEGAMI MULTIPLI Quando la molecola contiene sia un gruppo funzionale che un legame multiplo la desinenza deve essere doppia, includendo sia il suffisso
DAI GRUPPI FUNZIONALI AI POLIMERI
 DAI GRUPPI FUNZIONALI AI POLIMERI 1. I GRUPPI FUNZIONALI 2. DERIVATI OSSIGENATI DEGLI IDROCARBURI : ALCOLI, FENOLI, ETERI, ALDEIDI E CHETONI, ACIDI CARBOSSILICI E LORO DERIVATI 3. DERIVATI AZOTATI DEGLI
DAI GRUPPI FUNZIONALI AI POLIMERI 1. I GRUPPI FUNZIONALI 2. DERIVATI OSSIGENATI DEGLI IDROCARBURI : ALCOLI, FENOLI, ETERI, ALDEIDI E CHETONI, ACIDI CARBOSSILICI E LORO DERIVATI 3. DERIVATI AZOTATI DEGLI
IDROCARBURI: classificazione
 ALCANI 1 IDROCARBURI: classificazione 2 ALCANI Formula bruta: C n H 2n+2 1 C CH 4 2 C C 2 H 6 3 C C 3 H 8 4 C C 4 H 10 3 ALCANI: ibridazione Orbitali s, p e sp 3 z orbitale 2s y x z z z orbitali 2p y x
ALCANI 1 IDROCARBURI: classificazione 2 ALCANI Formula bruta: C n H 2n+2 1 C CH 4 2 C C 2 H 6 3 C C 3 H 8 4 C C 4 H 10 3 ALCANI: ibridazione Orbitali s, p e sp 3 z orbitale 2s y x z z z orbitali 2p y x
Chimica Organica. Studio dei composti del CARBONIO
 Chimica Organica Studio dei composti del CARBONIO 1 Contengono C, H e possono contenere N, O, S Carbonio legato covalentemente ad un metallo Tutti gli elementi possibili Composti organici 2 Perché si formano
Chimica Organica Studio dei composti del CARBONIO 1 Contengono C, H e possono contenere N, O, S Carbonio legato covalentemente ad un metallo Tutti gli elementi possibili Composti organici 2 Perché si formano
La nomenclatura dei composti organici polifunzionali. Appendice
 Appendice A La nomenclatura dei composti organici polifunzionali on oltre 37 milioni di composti organici già conosciuti e le molte migliaia in più che si creano quotidianamente, assegnare un nome a ciascun
Appendice A La nomenclatura dei composti organici polifunzionali on oltre 37 milioni di composti organici già conosciuti e le molte migliaia in più che si creano quotidianamente, assegnare un nome a ciascun
Capitolo 2 Alcani e Cicloalcani
 himica Organica Informazione Scientifica sul Farmaco apitolo 2 Alcani e icloalcani Organic hemistry, 5 th Edition L. G. Wade, Jr. Prentice all Organic hemistry, 3 rd Edition 1 Paula Y. Bruice, Prentice
himica Organica Informazione Scientifica sul Farmaco apitolo 2 Alcani e icloalcani Organic hemistry, 5 th Edition L. G. Wade, Jr. Prentice all Organic hemistry, 3 rd Edition 1 Paula Y. Bruice, Prentice
M i n i s t e r o d e l l I s t r u z i o n e, d e l l U n i v e r s i t à e d e l l a R i c e r c a
 PROGRAMMA SVOLTO DOCENTE: Campani Maria Varini Simone A.S: 2018/2019 DISCIPLINA: Chimica organica e biochimica CLASSE: 3^A CHI MAT Per ogni Tema svolto vengono indicati i relativi contenuti. LEGAME CHIMICO
PROGRAMMA SVOLTO DOCENTE: Campani Maria Varini Simone A.S: 2018/2019 DISCIPLINA: Chimica organica e biochimica CLASSE: 3^A CHI MAT Per ogni Tema svolto vengono indicati i relativi contenuti. LEGAME CHIMICO
CHIMICA ORGANICA. Gli alcheni
 1 2-ALENI IMIA ORGANIA ALENI Formula generale n 2n Desinenza -ene Gli alcheni La prima classe di idrocarburi insaturi è quella degli alcheni, detti anche olefine, che presentano lungo la catena uno o più
1 2-ALENI IMIA ORGANIA ALENI Formula generale n 2n Desinenza -ene Gli alcheni La prima classe di idrocarburi insaturi è quella degli alcheni, detti anche olefine, che presentano lungo la catena uno o più
Università degli Studi Kore di Enna Facoltà di Scienze dell Uomo e della Società CdL in Scienze delle attività motorie e sportive
 Università degli Studi Kore di Enna Facoltà di Scienze dell Uomo e della Società dl in Scienze delle attività motorie e sportive Biochimica - Ph.D. email: domenico.ciavardelli@unikore.it Esercizi: Soluzioni
Università degli Studi Kore di Enna Facoltà di Scienze dell Uomo e della Società dl in Scienze delle attività motorie e sportive Biochimica - Ph.D. email: domenico.ciavardelli@unikore.it Esercizi: Soluzioni
Università degli Studi Kore di Enna Facoltà di Scienze Motorie e delbenessere CdL in Scienze delle attività motorie e sportive
 Università degli Studi Kore di Enna Facoltà di Scienze Motorie e delbenessere dl in Scienze delle attività motorie e sportive Biochimica - Ph.D. email: domenico.ciavardelli@unikore.it Esercizi: Soluzioni
Università degli Studi Kore di Enna Facoltà di Scienze Motorie e delbenessere dl in Scienze delle attività motorie e sportive Biochimica - Ph.D. email: domenico.ciavardelli@unikore.it Esercizi: Soluzioni
Idrocarburi. Alifatici. Aromatici. Alcani o Idrocarburi saturi: idrocarburi con soli legami singoli. Alcheni o Olefine: idrocarburi con legami doppi.
 IDROCARBURI C x y Alifatici Idrocarburi Alcani o Idrocarburi saturi: idrocarburi con soli legami singoli. Lineari o alcani normali, n-alcani Ramificati Alcheni o Olefine: idrocarburi con legami doppi.
IDROCARBURI C x y Alifatici Idrocarburi Alcani o Idrocarburi saturi: idrocarburi con soli legami singoli. Lineari o alcani normali, n-alcani Ramificati Alcheni o Olefine: idrocarburi con legami doppi.
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 9 Il mondo del carbonio 3 Sommario 1. Esiste un enorme varietà di composti organici 2. Gli idrocarburi saturi: alcani e cicloalcani
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 9 Il mondo del carbonio 3 Sommario 1. Esiste un enorme varietà di composti organici 2. Gli idrocarburi saturi: alcani e cicloalcani
Il termine arene viene impiegato per descrivere gli idrocarburi aromatici, in analogia con gli alcheni. prodotto di sostituzione.
 I Il termine aromatico venne riferito inizialmente all odore caratteristico di questa categoria di idrocarburi. Successivamente, tale nome è stato usato per indicare che questi composti sono altamente
I Il termine aromatico venne riferito inizialmente all odore caratteristico di questa categoria di idrocarburi. Successivamente, tale nome è stato usato per indicare che questi composti sono altamente
Acidi carbossilici e derivati Composti organici che contengono legami doppi C=O e legami singoli C-eteroatomo (oppure il gruppo CN)
 himica rganica Acidi carbossilici e derivati omposti organici che contengono legami doppi = e legami singoli -eteroatomo (oppure il gruppo N) H Acido carbossilico X Alogenuro acilico Anidride ' N Estere
himica rganica Acidi carbossilici e derivati omposti organici che contengono legami doppi = e legami singoli -eteroatomo (oppure il gruppo N) H Acido carbossilico X Alogenuro acilico Anidride ' N Estere
Riassunto delle lezioni precedenti..
 Riassunto delle lezioni precedenti.. Chimica del Carbonio L atomo di Carbonio può formare legami singoli, legami doppi e legami tripli IDROCARBURI formati solo da carbonio e idrogeno Si dividono in 3 classi:
Riassunto delle lezioni precedenti.. Chimica del Carbonio L atomo di Carbonio può formare legami singoli, legami doppi e legami tripli IDROCARBURI formati solo da carbonio e idrogeno Si dividono in 3 classi:
Capitolo 8 Alcoli e Fenoli
 Chimica Organica Informazione Scientifica sul Farmaco Capitolo 8 Alcoli e Fenoli Organic Chemistry, 5 th Edition L. G. Wade, Jr. Struttura degli Alcoli Alcoli: Il gruppo funzionale è l ossidrile (), legato
Chimica Organica Informazione Scientifica sul Farmaco Capitolo 8 Alcoli e Fenoli Organic Chemistry, 5 th Edition L. G. Wade, Jr. Struttura degli Alcoli Alcoli: Il gruppo funzionale è l ossidrile (), legato
Alchini (C n H 2n-2 ) Alcheni: idrocarburi insaturi con uno o più legami carbonio-carbonio doppi.
 himica rganica Alcheni Idrocarburi ( x y ) Alifatici Aromatici Alcani ( n 2n+2 ) Alcheni ( n 2n ) Alchini ( n 2n-2 ) icloalcani ( n 2n ) Alcheni: idrocarburi insaturi con uno o più legami carbonio-carbonio
himica rganica Alcheni Idrocarburi ( x y ) Alifatici Aromatici Alcani ( n 2n+2 ) Alcheni ( n 2n ) Alchini ( n 2n-2 ) icloalcani ( n 2n ) Alcheni: idrocarburi insaturi con uno o più legami carbonio-carbonio
FENOLI: nomenclatura IUPAC
 FENOLI, AMMINE ed ENAMMINE FENOLI: nomenclatura IUPAC I fenoli sono composti la cui caratteristica strutturale è quella di possedere un gruppo idrossile ( OH) legato a un anello benzenico. Il sistema it
FENOLI, AMMINE ed ENAMMINE FENOLI: nomenclatura IUPAC I fenoli sono composti la cui caratteristica strutturale è quella di possedere un gruppo idrossile ( OH) legato a un anello benzenico. Il sistema it
IBRIDAZIONE DEL CARBONIO NEGLI ALCANI PREMESSA: COSA SONO GLI ORBITALI IBRIDI.
 ALCANI Gli alcani sono composti organici costituiti solamente da carbonio e idrogeno (per questo motivo appartengono alla più ampia classe degli idrocarburi), aventi formula bruta C n H (2n + 2). Gli alcani
ALCANI Gli alcani sono composti organici costituiti solamente da carbonio e idrogeno (per questo motivo appartengono alla più ampia classe degli idrocarburi), aventi formula bruta C n H (2n + 2). Gli alcani
Forze intermolecolari
 Forze intermolecolari Sono le forze che si instaurano tra le molecole di un composto e ne determinano lo stato di aggregazione (gas, liquido, solido) interazioni dipolo-dipolo attrazioni di van der Waals
Forze intermolecolari Sono le forze che si instaurano tra le molecole di un composto e ne determinano lo stato di aggregazione (gas, liquido, solido) interazioni dipolo-dipolo attrazioni di van der Waals
APPENDICE I. Proprietà critiche, fattori acentrici e costanti di Rackett di alcune sostanze. ω Z RA. Pc atm. Sostanza Formula Tc C.
 APPENDICE I Proprietà critiche, fattori acentrici e costanti di ackett di alcune sostanze Sostanza Formula Tc C Pc atm Vc cm 3 /mol ω Z A Normal paraffine Metano CH4-82.6 45.30 99 0.011 0.2892 Etano C2H6
APPENDICE I Proprietà critiche, fattori acentrici e costanti di ackett di alcune sostanze Sostanza Formula Tc C Pc atm Vc cm 3 /mol ω Z A Normal paraffine Metano CH4-82.6 45.30 99 0.011 0.2892 Etano C2H6
Pillole di... Chimica organica
 sono composti binari che contengono soltanto idrogeno e carbonio. Pillole di... Chimica organica Idrocarburi saturi contengono soltanto legami semplici tra gli atomi di carbonio Alcani (idrocarburi lineari)
sono composti binari che contengono soltanto idrogeno e carbonio. Pillole di... Chimica organica Idrocarburi saturi contengono soltanto legami semplici tra gli atomi di carbonio Alcani (idrocarburi lineari)
Nomenclatura sos.tu.va IUPAC
 Nomenclatura sos.tu.va IUPAC Chimica organica Prof. Silvia Recchia Nomenclatura sos0tu0va 2 Sommario Introduzione... 3 Costruzione del nome... 4 Legami mul6pli... 6 Gruppo funzionale ripetuto più volte...
Nomenclatura sos.tu.va IUPAC Chimica organica Prof. Silvia Recchia Nomenclatura sos0tu0va 2 Sommario Introduzione... 3 Costruzione del nome... 4 Legami mul6pli... 6 Gruppo funzionale ripetuto più volte...
Isomeria Costituzionale. Isomeria Conformazionale
 Isomeria ostituzionale Isomeri ostituzionali: omposti con uguale formula molecolare ma con un diverso ordine con cui sono legati gli atomi tra loro. Isomeria onformazionale onformazione: ciascuna disposizione
Isomeria ostituzionale Isomeri ostituzionali: omposti con uguale formula molecolare ma con un diverso ordine con cui sono legati gli atomi tra loro. Isomeria onformazionale onformazione: ciascuna disposizione
La Chimica Organica idrogeno carbonio azoto ossigeno composti covalenti catene di atomi di carbonio strutture covalenti e debolmente polarizzate
 LA IMIA ORGANIA La himica Organica I quattro elementi idrogeno, carbonio, azoto e ossigeno rappresentano più del 95% dei costituenti della materia vivente. I composti organici sono composti covalenti che
LA IMIA ORGANIA La himica Organica I quattro elementi idrogeno, carbonio, azoto e ossigeno rappresentano più del 95% dei costituenti della materia vivente. I composti organici sono composti covalenti che
Benzene e Composti Aromatici
 Benzene e Composti Aromatici Contenuti della lezione: Il benzene e i requisiti per l aromaticità Nomenclatura di benzeni mono- e di-sostituiti Composti aromatici diversi dal benzene: IPA e eteroaromatici
Benzene e Composti Aromatici Contenuti della lezione: Il benzene e i requisiti per l aromaticità Nomenclatura di benzeni mono- e di-sostituiti Composti aromatici diversi dal benzene: IPA e eteroaromatici
Soluzioni degli esercizi di fine capitolo
 SLUZINI DEGLI ESERIZI DI FINE APITL Soluzioni degli esercizi di fine capitolo David Sadava, David M. illis,. raig eller, May R. Berenbaum, Alfonso 1 Soluzioni degli esercizi per capitolo himica organica:
SLUZINI DEGLI ESERIZI DI FINE APITL Soluzioni degli esercizi di fine capitolo David Sadava, David M. illis,. raig eller, May R. Berenbaum, Alfonso 1 Soluzioni degli esercizi per capitolo himica organica:
Ammine : caratteristiche strutturali
 Ammine : caratteristiche strutturali Le ammine sono composti formalmente derivanti dall ammoniaca in cui uno o più atomi di idrogeno sono stati sostituiti da gruppi alchilici Come per l ammonica l azoto
Ammine : caratteristiche strutturali Le ammine sono composti formalmente derivanti dall ammoniaca in cui uno o più atomi di idrogeno sono stati sostituiti da gruppi alchilici Come per l ammonica l azoto
LA CHIMICA ORGANICA IBRIDAZIONE
 LA CHIMICA ORGANICA Detta anche LA CHIMICA DEL CARBONIO (C) perché Il C gioca un ruolo fondamentale in tutte le molecole organiche (cioè appartenenti o derivanti da esseri viventi). Possiamo spiegarlo
LA CHIMICA ORGANICA Detta anche LA CHIMICA DEL CARBONIO (C) perché Il C gioca un ruolo fondamentale in tutte le molecole organiche (cioè appartenenti o derivanti da esseri viventi). Possiamo spiegarlo
Nomenclatura IUPAC e struttura di alcheni e alchini
 Imparare la chimica con l aiuto del computer Nomenclatura IUPAC e struttura di alcheni e alchini Con questa esercitazione imparerete a disegnare semplici molecole col computer e ad assegnare la corretta
Imparare la chimica con l aiuto del computer Nomenclatura IUPAC e struttura di alcheni e alchini Con questa esercitazione imparerete a disegnare semplici molecole col computer e ad assegnare la corretta
La chimica organica. La chimica organica è la chimica dei composti del carbonio.
 La chimica organica La chimica organica è la chimica dei composti del carbonio. Gli Idrocarburi sono composti organici contenenti solo carbonio (C) e idrogeno (H). Ci sono composti organici che contengono
La chimica organica La chimica organica è la chimica dei composti del carbonio. Gli Idrocarburi sono composti organici contenenti solo carbonio (C) e idrogeno (H). Ci sono composti organici che contengono
Capitolo 6 Composti Aromatici
 himica Organica Scienze della Terra, dell Ambiente e del Territorio apitolo 6 omposti Aromatici Organic hemistry, 5 th Edition L. G. Wade, Jr. Scoperta del Benzene I composti aromatici sono tra i primi
himica Organica Scienze della Terra, dell Ambiente e del Territorio apitolo 6 omposti Aromatici Organic hemistry, 5 th Edition L. G. Wade, Jr. Scoperta del Benzene I composti aromatici sono tra i primi
Idrocarburi: composti organici che hanno nella loro struttura solo atomo di C o H
 Idrocarburi: composti organici che hanno nella loro struttura solo atomo di C o H Alifatici: deriva dal greco aleifar cioè unguento; questo perché molti grassi contengono lunghe catene carboniose. GLI
Idrocarburi: composti organici che hanno nella loro struttura solo atomo di C o H Alifatici: deriva dal greco aleifar cioè unguento; questo perché molti grassi contengono lunghe catene carboniose. GLI
CORSO DI CHIMICA E PROPEDEUTICA BIOCHIMICA CORSO DI LAUREA IN TECNICHE DI LABORATORIO BIOMEDICO SAPIENZA UNIVERSITA' DI ROMA CHIMICA ORGANICA
 CORSO DI CHIMICA E PROPEDEUTICA BIOCHIMICA CORSO DI LAUREA IN TECNICHE DI LABORATORIO BIOMEDICO SAPIENZA UNIVERSITA' DI ROMA CHIMICA ORGANICA A causa della sua limitata elettronegativita', il carbonio
CORSO DI CHIMICA E PROPEDEUTICA BIOCHIMICA CORSO DI LAUREA IN TECNICHE DI LABORATORIO BIOMEDICO SAPIENZA UNIVERSITA' DI ROMA CHIMICA ORGANICA A causa della sua limitata elettronegativita', il carbonio
CHIMICA ORGANICA - CLASSE 3 - RISPOSTE
 CHIMICA ORGANICA - CLASSE 3 - RISPOSTE Prof: Anna Rosa MASTELLARI. Specializzazione di CHIMICA Testo: CHIMICA ORGANICA, BIORGANICA E LABORATORIO ALCANI E CICLOALCANI (Capitolo 2) 1. Assegnare la nomenclatura
CHIMICA ORGANICA - CLASSE 3 - RISPOSTE Prof: Anna Rosa MASTELLARI. Specializzazione di CHIMICA Testo: CHIMICA ORGANICA, BIORGANICA E LABORATORIO ALCANI E CICLOALCANI (Capitolo 2) 1. Assegnare la nomenclatura
Appunti di Chimica Organica Elementi per CdL Ostetricia CHIMICA ORGANICA. Appunti di Lezione. Elementi per il corso di Laurea In Ostetricia
 Appunti di himica Organica Elementi per dl Ostetricia IMIA ORGANIA Appunti di Lezione Elementi per il corso di Laurea In Ostetricia Autore: Roberto Zanrè A.A. 2009/2010 1 Appunti di himica Organica Elementi
Appunti di himica Organica Elementi per dl Ostetricia IMIA ORGANIA Appunti di Lezione Elementi per il corso di Laurea In Ostetricia Autore: Roberto Zanrè A.A. 2009/2010 1 Appunti di himica Organica Elementi
INTERPRETAZIONE DEGLI SPETTRI IR
 INTERPRETAZIONE DEGLI SPETTRI IR Anche se non esistono gruppi di regole per la interpretazione completa degli spettri infrarossi, si è trovato che possono essere utili alcune linee-guida generali. 1. Cominciare
INTERPRETAZIONE DEGLI SPETTRI IR Anche se non esistono gruppi di regole per la interpretazione completa degli spettri infrarossi, si è trovato che possono essere utili alcune linee-guida generali. 1. Cominciare
Gruppo carbonilico. Il gruppo carbonilico è caratterizzato dalla presenza C=O ed i composti che lo contengono vengono definiti composti carbonilici.
 Gruppo carbonilico Il gruppo carbonilico è caratterizzato dalla presenza C= ed i composti che lo contengono vengono definiti composti carbonilici. H R R R R H R R aldeidi chetoni acidi carbossilici ac.
Gruppo carbonilico Il gruppo carbonilico è caratterizzato dalla presenza C= ed i composti che lo contengono vengono definiti composti carbonilici. H R R R R H R R aldeidi chetoni acidi carbossilici ac.
PERCHE STUDIARE LA CHIMICA ORGANICA?
 CIMICA ORGANICA CE COSA E LA CIMICA ORGANICA? La chimica organica è dedicata alla descrizione della struttura, delle proprietà e delle funzioni dei composti del carbonio (C). PERCE STUDIARE LA CIMICA ORGANICA?
CIMICA ORGANICA CE COSA E LA CIMICA ORGANICA? La chimica organica è dedicata alla descrizione della struttura, delle proprietà e delle funzioni dei composti del carbonio (C). PERCE STUDIARE LA CIMICA ORGANICA?
BENZENE E DERIVATI. Composto aromatico: termine usato per indicare il benzene ed i suoi derivati C 6 H 6. Arene: Idrocarburo aromatico
 BENZENE E DERIVATI Composto aromatico: termine usato per indicare il benzene ed i suoi derivati C 6 H 6 Arene: Idrocarburo aromatico Gruppo arilico: gruppo sostituente che deriva da un arene per rimozione
BENZENE E DERIVATI Composto aromatico: termine usato per indicare il benzene ed i suoi derivati C 6 H 6 Arene: Idrocarburo aromatico Gruppo arilico: gruppo sostituente che deriva da un arene per rimozione
Capitolo 10 Composti Aromatici
 himica Organica Informazione Scientifica sul Farmaco apitolo 10 omposti Aromatici Organic hemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: scoperta del benzene struttura elettronica del benzene
himica Organica Informazione Scientifica sul Farmaco apitolo 10 omposti Aromatici Organic hemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: scoperta del benzene struttura elettronica del benzene
CHIMICA ORGANICA CHIMICA DEL CARBONIO
 CHIMICA ORGANICA CHIMICA DEL CARBONIO Fino al 1828 con il termine organico si indicavano le sostanze prodotte dagli organismi viventi, mentre si classificavano come inorganiche tutte le altre Dopo il 1828
CHIMICA ORGANICA CHIMICA DEL CARBONIO Fino al 1828 con il termine organico si indicavano le sostanze prodotte dagli organismi viventi, mentre si classificavano come inorganiche tutte le altre Dopo il 1828
PROPRIETA FISICHE DEI COMPOSTI ORGANICI
 PRPRIETA FISICE DEI CMPSTI RGAICI I composti organici sono molto numerosi a causa del fatto che il legame σ tra due atomi di carbonio è particolarmente forte, a causa delle piccole dimensioni e del valore
PRPRIETA FISICE DEI CMPSTI RGAICI I composti organici sono molto numerosi a causa del fatto che il legame σ tra due atomi di carbonio è particolarmente forte, a causa delle piccole dimensioni e del valore
Capitolo 19 Dal carbonio agli idrocarburi
 apitolo 19 Dal carbonio agli idrocarburi Hai capito? pag. 436 7 H 16 No pag. 437 8 H 16 pag. 438 A La struttura ramificata già descritta in (3) e (4). pag. 438 B l 2, l l, l 2, l l ; isomeria di posizione.
apitolo 19 Dal carbonio agli idrocarburi Hai capito? pag. 436 7 H 16 No pag. 437 8 H 16 pag. 438 A La struttura ramificata già descritta in (3) e (4). pag. 438 B l 2, l l, l 2, l l ; isomeria di posizione.
Alcani e cicloalcani. Nomenclatura e nomi comuni Struttura e proprietà Reazioni
 Alcani e cicloalcani Nomenclatura e nomi comuni Struttura e proprietà Reazioni Alcani Gli orbitali atomici hanno forme ben definite. Gli orbitali S sono sferici con gli e - confinati in una regione sferica
Alcani e cicloalcani Nomenclatura e nomi comuni Struttura e proprietà Reazioni Alcani Gli orbitali atomici hanno forme ben definite. Gli orbitali S sono sferici con gli e - confinati in una regione sferica
ALCHENI CICLOALCHENI. C n H 2n. C n H 2n-2 C C. Gruppo funzionale degli alcheni (idrocarburi insaturi): doppio legame carbonio-carbonio
 ALCENI C n 2n CICLOALCENI C n 2n-2 C C Gruppo funzionale degli alcheni (idrocarburi insaturi): doppio legame carbonio-carbonio I carboni coinvolti nel doppio legame sono ibridati sp 2 : per cui sono legati
ALCENI C n 2n CICLOALCENI C n 2n-2 C C Gruppo funzionale degli alcheni (idrocarburi insaturi): doppio legame carbonio-carbonio I carboni coinvolti nel doppio legame sono ibridati sp 2 : per cui sono legati
LA CHIMICA DEL CARBONIO
 LA CHIMICA DEL CARBONIO E QUELLA PARTE DELLA CHIMICA CHE STUDIA IL CARBONIO E TUTTI I SUOI DERIVATI. I COMPOSTI DEL CARBONIO POSSONO ESSERE NATURALI (PROTEINE, ACIDI NUCLEICI, LIPIDI E CARBOIDRATI) O ESSERE
LA CHIMICA DEL CARBONIO E QUELLA PARTE DELLA CHIMICA CHE STUDIA IL CARBONIO E TUTTI I SUOI DERIVATI. I COMPOSTI DEL CARBONIO POSSONO ESSERE NATURALI (PROTEINE, ACIDI NUCLEICI, LIPIDI E CARBOIDRATI) O ESSERE
Contenuti della lezione:
 Alcheni e Alchini Contenuti della lezione: Aspetti generali e nomenclatura di alcheni e alchini Uso delle nomenclature cis/trans e E/Z per gli alcheni di-sostituiti e tri- o tetrasostituiti rispetivamente
Alcheni e Alchini Contenuti della lezione: Aspetti generali e nomenclatura di alcheni e alchini Uso delle nomenclature cis/trans e E/Z per gli alcheni di-sostituiti e tri- o tetrasostituiti rispetivamente
Approccio alla CHIMICA ORGANICA. Chimica organica: gli idrocarburi I gruppi funzionali. Paolo Pistarà, Principi di chimica moderna - Tomo A ATLAS
 Approccio alla IMIA ORGANIA himica organica: gli idrocarburi I gruppi funzionali IMIA ORGANIA: GLI IDROARBURI ompetenze Distinguere gli idrocarburi in base al legame covalente (singolo, doppio, triplo)
Approccio alla IMIA ORGANIA himica organica: gli idrocarburi I gruppi funzionali IMIA ORGANIA: GLI IDROARBURI ompetenze Distinguere gli idrocarburi in base al legame covalente (singolo, doppio, triplo)
Lezione 5. Alogenuri, alcoli, fenoli ed eteri
 Lezione 5 Alogenuri, alcoli, fenoli ed eteri 1 I gruppi funzionali Un gruppo funzionale è un atomo o un gruppo di atomi che determina le proprietà chimiche di un composto organico, permettendone la classificazione.
Lezione 5 Alogenuri, alcoli, fenoli ed eteri 1 I gruppi funzionali Un gruppo funzionale è un atomo o un gruppo di atomi che determina le proprietà chimiche di un composto organico, permettendone la classificazione.
Spettri IR. Spettri IR: come si interpretano gli spettri IR. Linee guida per interpretare gli spettri IR
 Spettri IR Spettri IR: come si interpretano gli spettri IR Linee guida per interpretare gli spettri IR Anche se non esistono gruppi di regole per la interpretazione completa degli spettri infrarossi, si
Spettri IR Spettri IR: come si interpretano gli spettri IR Linee guida per interpretare gli spettri IR Anche se non esistono gruppi di regole per la interpretazione completa degli spettri infrarossi, si
Alcani e Cicloalcani
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alcani e Cicloalcani Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alcani e Cicloalcani Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e
p p s sp sp sp s p p 1
 p p s sp p sp sp p s 1 alcheni 63 kcal/mol alchini 2 nd 54 kcal/mol 2 Come per gli alcheni, gli alchini interni sostituiti sono più stabili di quelli esterni More stable Etino (acetilene) C 2 H 2 +O 2
p p s sp p sp sp p s 1 alcheni 63 kcal/mol alchini 2 nd 54 kcal/mol 2 Come per gli alcheni, gli alchini interni sostituiti sono più stabili di quelli esterni More stable Etino (acetilene) C 2 H 2 +O 2
Verifiche dei Capitoli - Tomo C
 Soluzioni Verifiche dei Capitoli - Tomo C Per ogni Capitolo sono presentate le soluzioni delle Verifiche, delle Autoverifiche, delle Competenze e dei quesiti proposti nelle schede di Laboratorio. VERIFICHE
Soluzioni Verifiche dei Capitoli - Tomo C Per ogni Capitolo sono presentate le soluzioni delle Verifiche, delle Autoverifiche, delle Competenze e dei quesiti proposti nelle schede di Laboratorio. VERIFICHE
TAVOLA PERIODICA DEGLI ELEMENTI
 TAVOLA PERIODIA DEGLI ELEMENTI Idrogeno = 1 legame Ossigeno = 2 legami O Azoto = 3 legami N arbonio = 4 legami Questi sono gli atomi che intervengono maggiormente nelle reazioni che tratteremo nella
TAVOLA PERIODIA DEGLI ELEMENTI Idrogeno = 1 legame Ossigeno = 2 legami O Azoto = 3 legami N arbonio = 4 legami Questi sono gli atomi che intervengono maggiormente nelle reazioni che tratteremo nella
Alcheni: struttura e proprietà
 Chimica Organica Informazione Scientifica sul Farmaco Alcheni: struttura e proprietà Organic Chemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: struttura degli alcheni nomenclatura proprietà fisiche
Chimica Organica Informazione Scientifica sul Farmaco Alcheni: struttura e proprietà Organic Chemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: struttura degli alcheni nomenclatura proprietà fisiche
Alcoli, eteri, tioli, solfuri
 Alcoli, eteri, tioli, solfuri Alcoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Metanolo Sintesi industriale Tossico per l uomo (
Alcoli, eteri, tioli, solfuri Alcoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Metanolo Sintesi industriale Tossico per l uomo (
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA)
 La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) IL CARBONIO E un non metallo, appartiene al IV gruppo ed al II periodo. Possiede 4 elettroni esterni per
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) IL CARBONIO E un non metallo, appartiene al IV gruppo ed al II periodo. Possiede 4 elettroni esterni per
Alcoli ed eteri Composti organici che contengono legami singoli C-O
 Alcoli ed eteri Composti organici che contengono legami singoli C-O Chimica Organica CH 3 CH 2 CH 3 CH 2 O CH 2 CH 3 Alcol etilico etanolo Etere etilico dietiletere Fenolo idrossibenzene Nomenclatura degli
Alcoli ed eteri Composti organici che contengono legami singoli C-O Chimica Organica CH 3 CH 2 CH 3 CH 2 O CH 2 CH 3 Alcol etilico etanolo Etere etilico dietiletere Fenolo idrossibenzene Nomenclatura degli
Gruppi funzionali. aldeidi
 Gruppi funzionali alcoli aldeidi chetoni Acidi carbossilici ' eteri ' esteri fenoli In grassetto il gruppo funzionale che definisce il carattere del composto 1 2 Gruppi funzionali: arrangiamento di pochi
Gruppi funzionali alcoli aldeidi chetoni Acidi carbossilici ' eteri ' esteri fenoli In grassetto il gruppo funzionale che definisce il carattere del composto 1 2 Gruppi funzionali: arrangiamento di pochi
Composti carbonilici. Chimica Organica II
 Composti carbonilici Il gruppo carbonilico è formato da un carbonio legato tramite un doppio legame ad un ossigeno. Probabilmente è il gruppo funzionale più importante. Le proprietà del gruppo carbonilico
Composti carbonilici Il gruppo carbonilico è formato da un carbonio legato tramite un doppio legame ad un ossigeno. Probabilmente è il gruppo funzionale più importante. Le proprietà del gruppo carbonilico
Idrocarburi. Idrocarburi
 Idrocarburi 1 Molecole costituite solo da atomi di carbonio e idrogeno Idrocarburi alifatici Idrocarburi saturi, solo legami singoli. Idrocarburi aromatici Idrocarburi insaturi, almeno un legame multiplo
Idrocarburi 1 Molecole costituite solo da atomi di carbonio e idrogeno Idrocarburi alifatici Idrocarburi saturi, solo legami singoli. Idrocarburi aromatici Idrocarburi insaturi, almeno un legame multiplo
Stabilità Relativa dei Carbocationi
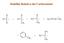 Stabilità elativa dei arbocationi < < 3 = 2 2 3 3 3 < = 3 2 3 Stabilità dei arbocationi Allilico e Benzilico 2 2 2 2 Le Forme Di isonanza egola 1: Le singole forme di risonanza non sono reali ma immaginarie.
Stabilità elativa dei arbocationi < < 3 = 2 2 3 3 3 < = 3 2 3 Stabilità dei arbocationi Allilico e Benzilico 2 2 2 2 Le Forme Di isonanza egola 1: Le singole forme di risonanza non sono reali ma immaginarie.
Alcheni. Francesca Anna Scaramuzzo, PhD
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alcheni Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate per
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alcheni Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate per
