LE PROTEINE, INFATTI, RAPPRESENTANO UN CLASSE DI MOLECOLE MOLTO
|
|
|
- Paolo Adamo
- 7 anni fa
- Visualizzazioni
Transcript
1 STRUTTURA E FUNZIONE DELLE PROTEINE
2 LINK SITO WEB:
3 COSA E UNA PROTEINA? IN REALTA NON SI PUO DEFINIRE UNA SINGOLA PROTEINA. LE PROTEINE, INFATTI, RAPPRESENTANO UN CLASSE DI MOLECOLE MOLTO ETEROGENEA, SIA DA UN PUNTO DI VISTA CHIMICO, SIA DA UN PUNTO DI VISTA FUNZIONALE. COSTITISCONO LA MAGGIOR PARTE DELLA MASSA SECCA DI UNA CELLULA. PER COMPRENDERE COME FUNZIONANO I GENI, COME I MUSCOLI SI CONTRAGGONO, COME I NERVI CONDUCONO ELETTRICITA, COME SI SVILUPPA UN EMBRIONE O COME FUNZIONANO I NOSTRI CORPI, DOBBIAMO RAGGIUNGERE UNA COMPRENSIONE PROFONDA DELLE PROTEINE. L INSIEME DELLE PROTEINE ESPRESSE IN UN BEN DEFINITO MOMENTO TEMPORALE, IN UNO SPECIFICO TIPO CELLULARE O TESSUTO VIENE DEFINITO PROTEOMA.
4 LE PROTEINE SVOLGONO NUMEROSE E SVARIATE FUNZIONI (CLASSE ETEROGENEA DI MACROMOLECOLE ORGANICHE): 1. SOSTEGNO: PROTEINE STRUTTURALI, QUALI COLLAGENO, CHERATINA, ELASTINA, FIBROINA. 2. FATTORI DI TRASCRIZIONE 3. MOVIMENTO: PROTEINE CONTRATTILI, QUALI ACTINA E MIOSINA. 4. TRASPORTO: EMOGLOBINA, MIOGLOBINA, LIPOPROTEINE, ALBUMINA, PROTEINE DI MEMBRANA. 5. CATALISI: TUTTI GLI ENZIMI 6. ORMONI: INSULINA E GLUCAGONE SONO SOLO ALCUNI ESEMPI DI ORMONI DI NATURA PROTEICA. 7. "DIFESA": IMMUNOGLOBULINE (ANTICORPI). 8. "ATTACCO": TOSSINE BATTERICHE, VELENI DEI SERPENTI. 9. RISERVA: NORMALMENTE LE PROTEINE NON HANNO UN RUOLO DI RISERVA DI AMMINOACIDI, MA L'OVOALBUMINA E LA CASEINA SONO ESEMPI DI PROTEINE CON QUESTA FUNZIONE
5 Fenotipo SPECIFICITA DI ALCUNE PROTEINE, PROPRIE DI DETERMINATI FENOTIPI (ES:HB) Proteine costitutive Indispensabili per la sopravvivenza La loro concentrazione deve rimanere costante Proteine adattative Cambiamenti delle condizioni ambientali Produrre risposte metaboliche a specifici segnali Proteine del differenziamento Assunsione ed espressione permanente di nuove funzioni specifiche
6 UNITA DI BASE DELLE PROTEINE L UNITA DI BASE DELLE PROTEINE E L AMINOACIDO (aa.): CARATTERISTICHE PRINCIPALI DI UN aa.: E UNA MOLECOLA CHE PRENDE NOME DAI DUE GRUPPI CHIMICI FUNZIONALI CHE LA CARATTERIZZANO: IL GRUPPO NH2 (AMINICO) ED IL GRUPPO COOH (CARBOSSILICO); IL C (C ALPHA ) E LEGATO A QUATTRO GRUPPI CHIMICI DIVERSI CIA= SCUNO DALL ALTRO, PER TALE MOTIVO QUESTO C E DETTO CHIRALE O STE= REOCENTRO IL GRUPPO R E LA PARTE VARIABILE DELLA MOLECOLA ED E PERTANTO LA PORZIONE PIU CARATTERIZZANTELA (CHIMICAMENTE, STRUTTURALMENTE E FUNZIONALMENTE)
7 QUANTI aa. IN NATURA? IN NATURA CI SONO 20 aa. (+ Pirrolisina e Selenocisteina): Acidi Basici Neutri non polari Neutri polari Il tipo di aminoacidi presenti in una proteina determinerà le caratteristiche chimiche della proteina
8 Aminoacidi essenziali Il nostro organismo non riesce a sintetizzarli e devono essere assunti con la dieta
9 LE PROTEINE POSSONO ESSERE CLASSIFICATE COME: 1. SEMPLICI (SOLO aa.) 2. CONIUGATE (aa. + gruppo prostetico di natura non aminoacidica) CLASSIFICAZIONE DELLE PROTEINE CONIUGATE Classe Glicoproteine Natura chimica del gruppo prostetico Carboidrati LE PROTEINE CONIUGATE PRIVE DI Lipoproteine Nucleoproteine Emoproteine Metalloproteine Lipidi Ac. Nucleici Gruppo eme Ioni metallici GRUPPO PROSTETICO SONO DETTE APOPROTEINE Fosfoproteine Ac. Fosforico Flavoproteine Nucleotidi flavinici
10 LEGAME PEPTIDICO: LA STRUTTURA PRIMARIA DELLE PROTEINE DUE aa. SI LEGANO TRA LORO ATTRAVERSO UNA REAZIONE DI CONDENSA= ZIONE CHE AVVIENE TRA IL GRUPPO COOH DI UN aa. ED IL GRUPPO -NH2 DEL SUCCESSIVO, IN MODO TALE CHE LA MOLECOLA CHE SI GENERA AVRA LE DUE ESTREMITA DIVERSE: UN ESTREMO CARATTERIZZATO DAL GRUPPO CHIMICO -NH2 (N-TERMINALE) E L ESTREMO OPPOSTO CARATTERIZZATO DAL GRUPPO COOH (C-TERMINALE) PIU aa. POSSONO UNIRSI TRA LORO ATTRAVERSO TALI LEGAMI COVALENTI A FORMARE I PEPTIDI (OLIGO-PEPTIDI, SE FORMATI DA 2 A 50 CA. RESIDUI aa. ; POLI-PEPTIDI, SE FORMATI DA PIU DI 50 aa.). UNA PROTEINA PUO ESSERE COSTITUITA DA UN SOLO POLIPEPTIDE (IN TAL CASO,PER CONVENZIONE, SI FANNO COINCIDERE I TERMINI PROT. E PEPTIDE SE QUEST ULTIMO E COSTITUITO DA UN NUM. DI aa. RILEVANTE IN GENERE DA 60 IN SU-, ALTRIMENTI SI USA SEMPLICEMENTE IL TERMINE PEPTIDE) PRO= TEINA MONOMERICA -, OPPURE DA PIU POLIPEPTIDI LEGATI TRA LORO ATTRA= VERSO LEGAMI NON COVALENTI PROTEINA MULTIMERICA -.
11 LEGAME PEPTIDICO: LA STRUTTURA PRIMARIA DELLE PROTEINE (continua) LA SEQUENZA DI PIU aa., IN TAL MODO LEGATI A FORMARE UN SINGOLO PEPTIDE, PER CONVENZIONE, VIENE DETTA STRUTTURA PRIMARIA DELLE PROTEINE: QUESTA STRUTTURA E CARATTERIZZATA, DUNQUE, DALLA PRE= SENZA DI SOLI LEGAMI COVALENTI. SI POSSONO DISTINGUERE UNA: PORZIONE (OSSATURA) COSTANTE, RAPPRESENTATA DALLA MERA SUC= CESSIONE DEI LEGAMI PEPTIDICI; UNA PORZIONE VARIABILE, RAPPRESENTATA DAI GRUPPI R CHE SI ALTER= NANO SOPRA E SOTTO IL PIANO COSTITUITO DALL OSSATURA. I LEGAMI PEPTIDICI IN SENSO STRETTO (LEGAMI N-C) SONO PIUTTOSTO RIGIDI; VICEVERSA I LEGAMI αc N E αc C SONO FLESSIBILI.
12 LEGAME PEPTIDICO: LA STRUTTURA PRIMARIA DELLE PROTEINE (continua) NOTA: PER CONVENZIONE UN PEPTIDE VIENE LETTO DALL ESTREMITA N-TERMINALE ALL ESTREMITA C-TERMINALE (QUESTA CONVENZIONE DERIVA DALLA NATURALE SINTESI DEI PEPTIDI CHE SEGUE L ANDAMENTO N-TERMINALE / C-TERMINALE). La polarità NH 2 -COOH delle proteine corrisponde alla polarità 5 3 dell mrna.
13 LA STRUTTURA SECONDARIA DELLE PROTEINE: L α- ELICA ED IL FOGLIETTO β SPESSO IN UN PEPTIDE SI TROVANO DUE SCHEMI REGOLARI DI RIPIEGA= MENTO: L α-elica E IL FOGLIETTO β. ENTRAMBI DERIVANO DALLA FORMAZIONE DI LEGAMI H FRA I GRUPPI N-H E C=O DELL OSSATURA POLIPEPTIDICA, SENZA COINVOLGERE LE CATENE LA= TERALI DEGLI aa.
14 α-elica SI FORMA QUANDO UNA SIGOLA CATENA POLIPEPTIDICA SI AVVOLGE SU SE STESSA PER FORMARE UN CILINDRO RIGIDO: IN PARTICOLARE SI INSTAURA UN LEGAME H FRA UN LEGAME PEPTIDICO E IL QUARTO SUCCESSIVO; SI GENERA COSI UN ELICA REGOLARE DI PASSO UGUALE A 3,6 aa (CIOE 5,4Å). TIPICAMENTE, BREVI REGIONI AD α-elica SONO ABBONDANTI IN PROTEINE POSTE NELLE MEMBRANE CELLULARI (ES.: PROTEINE DI TRASPORTO E RE= CETTORI); IN ALTRE PROTEINE α-eliche SI AVVOLGONO L UNA INTORNO ALL ALTRA PER FORMARE STRUTTURE STABILI NOTE COME COILED-COIL. (ES.: α-cheratina O MIOSINA). α-elica COILED-COIL
15 FOGLIETTO β (O β-sheet) SI FORMANO PER LEGAMI H TRA GRUPPI PEPTIDICI ADIACENTI APPARTE= NENTI AD UNA STESSA CATENA O A CATENE POLIPETIDICHE DIFFERENTI CHE POSSONO DECORRERE PARALLELE OD ANTI-PARALLELE (PARALLELE SE HANNO LO STESSO ORIENTAMENTO N-TERMINALE / C-TERMINALE; ANTIPARALLELE SE UNA DECORRE N-TERMINALE / C-TERMINALE IN DIREZIONE NORD-SUD O EST-OVEST E L ALTRA N-TERMINALE / C-TERMINAL IN DIREZIONE SUD-NORD O OVEST-EST). I FOGLIETTI BETA COSTITUISCONO IL CORE DI MOLTE STRUTTURE PROTEICHE FOGLIETTO β (O β-sheet)
16 Cys STRUTTURE SUPER SECONDARIE, MOTIVI STRUTTURALI Zinc Finger (ZF) Motif Leucine Zipper (LZ) Motif α-elica Leu β-sheet Zn ++ His Helix-turn-Helix (HTH) Motif Elica di riconoscimento Elica di stabilizzazione
17 LA STRUTTURA TERZIARIA DELLE PROTEINE: I DOMINI PROTEICI LA STRUTTURA 3D CHE UN PEPTIDE ASSUME NELLO SPAZIO A SEGUITO DEL SUO AVVOLGIMENTO (FOLDING) DOVUTO A LEGAMI DI TIPO NON COVALENTE (LEGAMI H; INTERAZIONI DI Van Der Waals; INTERAZIONI IDROFOBICHE E PONTI SALINI) CHE SI INSTAURANO TRA GLI ATOMI O GRUPPI ATOMICI DELLA STESSA MOLECOLA E NOTA COME STRUTTURA TERZIARIA. ALL INTERNO DI UNA SIFFATTA MOLECOLA, SI RITROVANO DELLE SOTTO= STRUTTURE (STRUTTURALMENTE E TALORA FUNZIONALMENTE INDIPEND.) NOTE COME DOMINI PROTEICI. I DOMINI PROTEICI SONO DUNQUE SOTTOSTRUTTURE PRODOTTE DA QUALUNQUE PARTE DELLA CATENA POLIPEPTIDICA IN GRADO DI RIPIEGARSI INDIPENDENTEMENTE IN UNA STRUTTURA COMPATTA STABILE. UN DOMINIO IN GENERE CONSTA DAI 40 AI 350 aa. CARATTESTICI SPESSO DELLE PROTEINE SONO I MODULI, CIOE DEI DOMINI PICCOLI ( aa.) CHE COSTITUISCONO DELLE SIGNATURE NELLE PROTEINE E CHE SPESSO SI RICOMBINANO TRA LORO A FORMARE STRUTTURE NUOVE.
18 LA STRUTTURA TERZIARIA DELLE PROTEINE: I DOMINI PROTEICI (continua) STRUTT. III DOMAINS DOMAIN - SHUFFLING NOTA: MOLTE GRANDI PROTEINE SI SONO EVOLUTE PER UNIONE DI DOMINI PREESISTENTI CHE SI SONO COMBINATI IN MODI DIFFERENTI (RIMESCOLAMENTO DEI DOMINI).
19 I principali tipi di legame che si trovano all interno di una struttura terziaria di una proteina: 1) Legami H 2) Legami ionici 3) Legami covalenti (ponti disolfuro)
20
21 Ponti disolfuro
22
23
24 La posizione di ciascun aminoacido all interno della sequenza ne determina la forma tridimensionale. Quindi la forma che la proteina assume dipende dalla sequenza di aminoacidi che costituiscono la proteina
25 La struttura tridimensionale della proteina è determinata dalla formazione di legami deboli tra le catene laterali dei vari aminoacidi. Legami idrogeno Legami ionici Attrazioni di van derwalls Interazioni idrofobiche
26 Ciascuna proteina si ripiega normalmente in un unica conformazione stabile che in genere è quella in cui è minima l energia libera. Tuttavia la conformazione può cambiare leggermente quando la proteina interagisce con altre molecole della cellula. Questo cambiamento di forma è spesso cruciale per l attività della proteina
27 LA STRUTTURA QUATERNARIA DELLE PROTEINE: LE PROTEINE MULTIMERICHE SPESSO LE PROTEINE CONSTANO DI PIU SUBUNITA PEPTIDICHE (CIASCUNA GIA RIPIEGATA NELLA SUA STRUTTURA 3D) CHE INTERAGISCONO TRA LORO TRAMITE LEGAMI NON COVALENTI (LEGAMI H ED INTERAZIONI IDROFOBICHE PRINCIPALMENTE) A FORMARE UN UNICA STRUTTURA FUNZIONALE: LA PROTEINA AVENTE STRUTTURA QUATERNARIA. Es.:PROTEINA EMOGLOBINA
28
29 RIASSUMENDO: I LIVELLI DI STRUTTURA DELLE PROTEINE
30
31 FOLDING PER POTER SVOLGERE LA PROPRIA FUNZIONE BIOLOGICA, UNA PROTEINA DEVE ESSERE STRUTTURATA NELLA COSIDDETTA CONFORMAZIONE NATIVA. LA CONFORMAZIONE NATIVA È QUELLA STRUTTURA 3D STABILE E FUNZIONALE, CARATTERIZZATA DA UN MINIMO DI ENERGIA POTENZIALE E DA QUELLA PARTICOLARE CONFORMAZIONE, UNICA, CHE CONSENTE ALLA PROTEINA DI SVOLGERE ADEGUATAMENTE LA FUNZIONE A CUI È DEPUTA. IL PROCESSO CHE DALLA BIOSINTESI DEL PEPTIDE, PORTA ALLA PROTEINA STRUTTURATA NELLA FORMA NATIVA, BIOLOGICAMENTE ATTIVA, PRENDE IL NOME DI "FOLDING".
32 IMPORTANZA DEL FOLDING IN BIO-MEDICINA È MOLTO PROBABILE CHE PATOLOGIE QUALI L'ALZHEIMER, LA FIBROSI CISTICA E IL MORBO DELLA MUCCA PAZZA (SINDROME DI CREUTZFELDT-JAKOB NELL'UOMO) ABBIANO UNA ETIOLOGIA COMUNE IN UN DIFETTOSO FOLDING DI ALCUNE PROTEINE, CON CONSEGUENTE AGGREGAZIONE E PRECIPITAZIONE E SUCCESSIVA MORTE CELLULARE.
33 La variazione di un singolo aminoacido può provocare gravi effetti sul fenotipo dell organismo
34 Regolazione dell attività di una proteina Livello trascrizionale Modificazioni chimiche di una proteina
35 01_23.jpg
36 DIAGRAMMA DI FLUSSO DELL ESPRESSIONE GENICA mirna Nuclear phase Choise and Transcription of specific genes RNA Maturation Nucleus-Cytoplasm transfer Cytoplasmatic phase Protein Synthesis Post-translationaltranslational modifications Protein travelling
37 REGOLAZIONE ALLOSTERICA LEGAME CHIMICO DEBOLE (SOPRATTUTTO LEGAMI H) TRA EFFETTORE ALLOSTERICO E PROTEINA ALLOSTERICA E PROPRIA SOPRATTUTTO (MA NON ESCLUSIVAMENTE) DEGLI ENZIMI. IN GENERALE COMUNQUE LE PROTEINE ALLOSTERICHE SONO PROTEINE OLIGOMERICHE (A STRUTTURA QUATERNARIA)
38 REGOLAZIONE PER MODIFICAZIONI POST-TRADUZIONALITRADUZIONALI Type of modification (group added) Target amino acids Comments Phosphorylation (PO 4- ) Tyrosine, serine, threonine Achieved by specific kinases. May be reversed by phosphatases Methylation (CH 3 ) Lysine Achieved by methylases and undone by demethylases Hydroxylation (OH) Proline, lysine, aspartic acid Hydroxyproline and hydroxylysine are particularly common in collagens Acetylation (CH 3 CO) Lysine Achieved by an acetylase and undone by deacetylase Carboxylation (COOH) Glutamate Achieved by γ-carboxylase N-glycosylation (complex carbohydrate) O-glycosylation (complex carbohydrate) Asparagine, usually in the sequence: Asn-X-Ser/Thr Serine, threonine, hydroxylysine Takes place initially in the endoplasmic reticulum; X is any amino acid other than proline Takes place in the Golgi apparatus; less common than N-glycosylation GPI (glycolipid) Aspartate at C terminus Serves to anchor protein to outer layer of plasma membrane Myristoylation (C 14 fatty acyl group) Glycine at N terminus (see text) Serves as membrane anchor Palmitoylation (C 16 fatty acyl group) Cysteine to form S-palmitoyl link. Serves as membrane anchor Farnesylation (C 15 prenyl group) Cysteine at C terminus (see text) Serves as membrane anchor Geranylgeranylation (C 20 prenyl group) Cysteine at C terminus (see text) Serves as membrane anchor
39 ESEMPI DI REGOLAZIONI POST-TRADUZIONALI TRADUZIONALI Solitamente Gli aa. inte= ressati dalla modifica sono Thr; Tyr e Ser
40 NOTA: Chinasi e Fosfatasi sono spesso degli enzimi allosterici, sicchè la loro attività risulta essere regolata da specifici effettori. Ciò evita che la loro attività avvenga contemporaneamente all interno della cellula!
41 ACIDI NUCLEICI
42 Esperimenti preliminari
43 1953: costruzione del modello definitivo del DNA a doppia elica
44 Dogma centrale DNA RNA PROTEINE
45 I nucleotidi
46 I nucleotidi non sono solo componenti essenziali degli ac. Nucleici, ma svolgono numerose funzioni all interno della cellula. Es.: ATP: principale molecola energetica, usata in numerose reazioni cellulari che necessitano di energia; AMP ciclico: coin= volto nei meccanismi i trasduzione del segnale; GTP: lega le proteine G, innescando una cascata di eventi all interno della cellula in risposta a stimoli esterni.
47 Basi azotate DNA Timina Citosina Guanina Adenina RNA Uracile Citosina Guanina Adenina
48 I Polinucleotidi Legame fosfodiestere tra il gruppo ossidrile del C3 del 1 nucleotide ed il gruppo fosfato del C5 del nucleotide successivo NOTA: La sintesi del DNA E dell RNA avviene sempre secondo una polarità 5-3. l energia per la formazione di tali biopolimeri è data dai precursori nucleosidi trifosfato
49 Struttura del DNA Diametro: 2nm Passo elica: 3,4 nm Carica netta: negativa
50 Canonicamete una base pirimidinica si lega ad una base purinica e viceversa. In particolare i legami canonici sono: A::T e G:::C
51
52 Classi di RNAs eucariotici ribosomal RNA (rrna) 18S (small subunit) 28S (large subunit) 5.8S (large subunit) 5S (large subunit) transfer RNA (trna) messenger RNA (mrna) heterogeneous nuclear RNA (hnrna) (precursors of mrna) small nuclear RNA (snrna) U1, U2, U3, U4, U5, U6, U7, U8, U9, U10... small cytoplasmic RNA (scrna) 7SL RNA microrna
SI DEDUCE CHE NELLA CELLULA LE MOLECOLE SONO DISSOLTE A FORMARE UNA SOLUZIONE ACQUOSA PROTEINS RNA DNA 16% 14% 12% 10% 8% 6% 4% 2% 0%
 LINK SITO WEB: WWW.BGBUNICT.IT H 2 O CO 2 - NH 3 CH 4 Aminoacidi, Nucleotidi, Acidi grassi e Glicerolo, Monosaccaridi Proteine, Acidi nucleici, Lipidi, Polisaccaridi LE MACROMOLECOLE CELLULARI IN PESO,
LINK SITO WEB: WWW.BGBUNICT.IT H 2 O CO 2 - NH 3 CH 4 Aminoacidi, Nucleotidi, Acidi grassi e Glicerolo, Monosaccaridi Proteine, Acidi nucleici, Lipidi, Polisaccaridi LE MACROMOLECOLE CELLULARI IN PESO,
Legami chimici. Covalente. Legami deboli
 Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici STRUTTURA TERZIARIA La struttura tridimensionale
Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici STRUTTURA TERZIARIA La struttura tridimensionale
STRUTTURA E FUNZIONE DELLE PROTEINE
 STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
scaricato da www.sunhope.it Proteine semplici costituite dai soli amminoacidi
 Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
sono le unità monomeriche che costituiscono le proteine hanno tutti una struttura comune
 AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
Biologia. Lezione 09/11/2010
 Biologia Lezione 09/11/2010 Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono macromolecole formate da unità (MONOMERI)
Biologia Lezione 09/11/2010 Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono macromolecole formate da unità (MONOMERI)
Funzioni delle proteine
 Funzioni delle proteine ENZIMI Proteine di trasporto Proteine di riserva Proteine contrattili o motili Proteine strutturali Proteine di difesa Proteine regolatrici Proteine di trasporto Emoglobina Lipoproteine
Funzioni delle proteine ENZIMI Proteine di trasporto Proteine di riserva Proteine contrattili o motili Proteine strutturali Proteine di difesa Proteine regolatrici Proteine di trasporto Emoglobina Lipoproteine
Immagini e concetti della biologia
 Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
Legami chimici. Covalente. Legami deboli
 Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
ACIDI GRASSI INSATURI
 LIPIDI ACIDI GRASSI SATURI ACIDI GRASSI INSATURI TRIGLICERIDI TRIGLICERIDI Grassi neutri o lipidi semplici glicerolo + 1 acido grasso monogliceride glicerolo + 2 acidi grassi digliceride glicerolo + 3
LIPIDI ACIDI GRASSI SATURI ACIDI GRASSI INSATURI TRIGLICERIDI TRIGLICERIDI Grassi neutri o lipidi semplici glicerolo + 1 acido grasso monogliceride glicerolo + 2 acidi grassi digliceride glicerolo + 3
Introduzione alla biologia della cellula. Lezione 2 Le biomolecole
 Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
L ACQUA E LE SUE PROPRIETÀ
 L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
Struttura delle Proteine
 Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
I carboidrati sono poli-idrossialdeidiidrossialdeidi o poli-idrossichetoniidrossichetoni o derivati di questi.
 CARBOIDRATI I CARBOIDRATI I carboidrati sono poli-idrossialdeidiidrossialdeidi o poli-idrossichetoniidrossichetoni o derivati di questi. Unità di base dei carboidrati sono i monosaccaridi. Formula bruta
CARBOIDRATI I CARBOIDRATI I carboidrati sono poli-idrossialdeidiidrossialdeidi o poli-idrossichetoniidrossichetoni o derivati di questi. Unità di base dei carboidrati sono i monosaccaridi. Formula bruta
I materiali della vita
 I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
LE PROTEINE SINTESI PROTEICA. funzione delle proteine nel nostro organismo
 LE PTEIE Le proteine sono sostanze organiche presenti in tutte le cellule di tutti gli organismi viventi Le proteine sono costituite da,,,, (S) Struttura delle proteine Le proteine sono macromolecole (
LE PTEIE Le proteine sono sostanze organiche presenti in tutte le cellule di tutti gli organismi viventi Le proteine sono costituite da,,,, (S) Struttura delle proteine Le proteine sono macromolecole (
Proprietà comuni. Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici
 Gli aminoacidi Proprietà comuni Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici paragonabili Il gruppo α-aminico è un acido più forte (o una base più debole
Gli aminoacidi Proprietà comuni Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici paragonabili Il gruppo α-aminico è un acido più forte (o una base più debole
Composti organici. I composti organici. Atomi e molecole di carbonio. Atomi e molecole di carbonio. Gruppi funzionali. Isomeri
 I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
LIVELLI DI STRUTTURA DELLE PROTEINE
 FUNZIONI E STRUTTURA DELLE PROTEINE PROF.SSA AUSILIA ELCE Indice 1 INTRODUZIONE -------------------------------------------------------------------------------------------------------------- 3 2 LIVELLI
FUNZIONI E STRUTTURA DELLE PROTEINE PROF.SSA AUSILIA ELCE Indice 1 INTRODUZIONE -------------------------------------------------------------------------------------------------------------- 3 2 LIVELLI
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 10 Le basi della biochimica 3 Sommario 1. Le molecole biologiche si dividono in quattro classi 2. I carboidrati sono il «carburante»
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 10 Le basi della biochimica 3 Sommario 1. Le molecole biologiche si dividono in quattro classi 2. I carboidrati sono il «carburante»
Struttura degli amminoacidi
 AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA)
 La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) L atomo del carbonio (C).. C. Atomo tetravalente. C C C C Gli idrocarburi I legami del carbonio 109.5 gradi
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) L atomo del carbonio (C).. C. Atomo tetravalente. C C C C Gli idrocarburi I legami del carbonio 109.5 gradi
CARBOIDRATI C H O ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO
 CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
30/10/2015. Molte proteine sono. intrinsecamente disordinate. o destrutturate (IDP/IUP), cioè non hanno una struttura
 Molte proteine sono intrinsecamente disordinate o destrutturate (IDP/IUP), cioè non hanno una struttura terziaria e/o secondaria stabile. Le IUP sono caratterizzate da - scarso contenuto in aa apolari,
Molte proteine sono intrinsecamente disordinate o destrutturate (IDP/IUP), cioè non hanno una struttura terziaria e/o secondaria stabile. Le IUP sono caratterizzate da - scarso contenuto in aa apolari,
Aminoacidi. Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α
 Aminoacidi Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α 1 Isomeria ottica Tutti gli AA, esclusa la glicina, presentano almeno un atomo di carbonio asimmetrico, il
Aminoacidi Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α 1 Isomeria ottica Tutti gli AA, esclusa la glicina, presentano almeno un atomo di carbonio asimmetrico, il
DOGMA CENTRALE DELLA BIOLOGIA. Secondo il dogma centrale della biologia, il DNA dirige la. sintesi del RNA che a sua volta guida la sintesi delle
 DOGMA CENTRALE DELLA BIOLOGIA Secondo il dogma centrale della biologia, il DNA dirige la sintesi del RNA che a sua volta guida la sintesi delle proteine. Tuttavia il flusso unidirezionale di informazioni
DOGMA CENTRALE DELLA BIOLOGIA Secondo il dogma centrale della biologia, il DNA dirige la sintesi del RNA che a sua volta guida la sintesi delle proteine. Tuttavia il flusso unidirezionale di informazioni
Le macromolecole dei tessuti - 1
 Le macromolecole dei tessuti - 1 Che cosa sono le proteine? Sono macromolecole complesse ad alta informazione Sono costituite da una o più catene polipeptidiche Ogni catena peptidica è composta da centinaia
Le macromolecole dei tessuti - 1 Che cosa sono le proteine? Sono macromolecole complesse ad alta informazione Sono costituite da una o più catene polipeptidiche Ogni catena peptidica è composta da centinaia
Nucleotidi e Acidi Nucleici. Struttura di DNA e RNA
 Nucleotidi e Acidi Nucleici Nucleosidi Nucleotidi Funzioni biologiche dei nucleotidi Struttura di DNA e RNA Concatenazione e appaiamento dei nucleotidi Lo scheletro degli acidi nucleici Componenti degli
Nucleotidi e Acidi Nucleici Nucleosidi Nucleotidi Funzioni biologiche dei nucleotidi Struttura di DNA e RNA Concatenazione e appaiamento dei nucleotidi Lo scheletro degli acidi nucleici Componenti degli
LE PROTEINE -struttura tridimensionale-
 LE PROTEINE -struttura tridimensionale- Struttura generale di una proteina Ceruloplasmina Cosa sono??? Sono biopolimeri con forme ben definite. composti da molteplici amminoacidi, legati con legami peptidici
LE PROTEINE -struttura tridimensionale- Struttura generale di una proteina Ceruloplasmina Cosa sono??? Sono biopolimeri con forme ben definite. composti da molteplici amminoacidi, legati con legami peptidici
Amminoacidi - Peptidi - Proteine. Emoglobina
 Amminoacidi - Peptidi - Proteine Emoglobina 1 Emoglobina Gli amminoacidi sono le sostanze di base che costituiscono le proteine. Ogni proteina è caratterizzata da una precisa sequenza di mattoni di amminoacidi.
Amminoacidi - Peptidi - Proteine Emoglobina 1 Emoglobina Gli amminoacidi sono le sostanze di base che costituiscono le proteine. Ogni proteina è caratterizzata da una precisa sequenza di mattoni di amminoacidi.
Definizione Composti quaternari: C H O N S P Fe Mg I
 PROTIDI Definizione Composti quaternari: C H O N S P Fe Mg I ORIGINE cellulare ogni cellula sintetizza le sue prote CARATTERISTICHE insolubili in acqua sensibili a variazioni di ph coagulano in presenza
PROTIDI Definizione Composti quaternari: C H O N S P Fe Mg I ORIGINE cellulare ogni cellula sintetizza le sue prote CARATTERISTICHE insolubili in acqua sensibili a variazioni di ph coagulano in presenza
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA)
 La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) POLIMERI Le cellule sintetizzano un enorme numero di grosse molecole a partire da una ristretta serie di
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) POLIMERI Le cellule sintetizzano un enorme numero di grosse molecole a partire da una ristretta serie di
La chimica della pelle
 La chimica della pelle 1 Gli amminoacidi Queste unità hanno la particolare caratteristica di contenere nella stessa molecola un gruppo acido (- COOH) ed uno basico (- NH 2 ), legati tra loro attraverso
La chimica della pelle 1 Gli amminoacidi Queste unità hanno la particolare caratteristica di contenere nella stessa molecola un gruppo acido (- COOH) ed uno basico (- NH 2 ), legati tra loro attraverso
30/10/2015 LIVELLI DI ORGANIZZAZIONE STRUTTURALE DELLE PROTEINE
 LIVELLI DI ORGANIZZAZIONE STRUTTURALE DELLE PROTEINE 1 CARATTERISTICHE DEL LEGAME PEPTIDICO lunghezza intermedia tra un legame singolo e uno doppio ibrido di risonanza per il parziale carattere di doppio
LIVELLI DI ORGANIZZAZIONE STRUTTURALE DELLE PROTEINE 1 CARATTERISTICHE DEL LEGAME PEPTIDICO lunghezza intermedia tra un legame singolo e uno doppio ibrido di risonanza per il parziale carattere di doppio
Costituenti chimici della materia vivente
 Costituenti chimici della materia vivente Le macromolecole biologiche Macromolecole (dal greco macros = grande) biologiche. Classi di composti biologici multifunzionali: Polisaccaridi proteine acidi
Costituenti chimici della materia vivente Le macromolecole biologiche Macromolecole (dal greco macros = grande) biologiche. Classi di composti biologici multifunzionali: Polisaccaridi proteine acidi
Amminoacidi Peptidi Proteine
 Amminoacidi Peptidi Proteine Amminoacidi-Peptidi-Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Stereoisomeri: composti con la stessa connessione tra gli atomi, ma con una differente
Amminoacidi Peptidi Proteine Amminoacidi-Peptidi-Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Stereoisomeri: composti con la stessa connessione tra gli atomi, ma con una differente
BIOMOLECOLE LE BASI DELLA BIOCHIMICA. Capitolo 1 Dal Carbonio agli OGM PLUS
 BIOMOLECOLE LE BASI DELLA BIOCHIMICA Capitolo 1 Dal Carbonio agli OGM PLUS BIOMOLECOLE Carboidrati Lipidi Acidi Nucleici Proteine BIOMOLECOLE Carboidrati Lipidi Acidi Nucleici - monosaccaridi - disaccaridi
BIOMOLECOLE LE BASI DELLA BIOCHIMICA Capitolo 1 Dal Carbonio agli OGM PLUS BIOMOLECOLE Carboidrati Lipidi Acidi Nucleici Proteine BIOMOLECOLE Carboidrati Lipidi Acidi Nucleici - monosaccaridi - disaccaridi
La struttura delle proteine
 La struttura delle proteine Funzioni delle proteine Strutturali Contrattili Trasporto Riserva Ormonali Enzimatiche Protezione Struttura della proteina Struttura secondaria: ripiegamento locale della catena
La struttura delle proteine Funzioni delle proteine Strutturali Contrattili Trasporto Riserva Ormonali Enzimatiche Protezione Struttura della proteina Struttura secondaria: ripiegamento locale della catena
COMPORTAMENTO ANFOTERO DEGLI AA
 Proprietà acido-basiche degli aminoacidi FORMA NON IONICA Non esiste a nessun valore di ph FORMA ZWITTERIONICA È la forma prevalente a ph 7 COMPORTAMENTO ANFOTERO DEGLI AA CARICA NETTA +1 CARICA NETTA
Proprietà acido-basiche degli aminoacidi FORMA NON IONICA Non esiste a nessun valore di ph FORMA ZWITTERIONICA È la forma prevalente a ph 7 COMPORTAMENTO ANFOTERO DEGLI AA CARICA NETTA +1 CARICA NETTA
LE PROTEINE. SONO Polimeri formati dall unione di AMMINOACIDI (AA) Rende diversi i 20 AA l uno dall altro UN ATOMO DI C AL CENTRO
 LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH. ) ed un gruppo carbossilico ( COOH) nella stessa molecola
 Amminoacidi (1) Presentano un gruppo amminico ( NH 2 ) ed un gruppo carbossilico ( COOH) nella stessa molecola CH 3 NH 2 C H α * COOH Acido 2-ammino propanoico (acido α-ammino propionico) 1 Amminoacidi
Amminoacidi (1) Presentano un gruppo amminico ( NH 2 ) ed un gruppo carbossilico ( COOH) nella stessa molecola CH 3 NH 2 C H α * COOH Acido 2-ammino propanoico (acido α-ammino propionico) 1 Amminoacidi
Capitolo 3 Le biomolecole
 apitolo 3 Le biomolecole opyright 2006 Zanichelli editore I composti organici e i loro polimeri 3.1 La diversità molecolare della vita è basata sulle proprietà del carbonio Un atomo di carbonio può formare
apitolo 3 Le biomolecole opyright 2006 Zanichelli editore I composti organici e i loro polimeri 3.1 La diversità molecolare della vita è basata sulle proprietà del carbonio Un atomo di carbonio può formare
- utilizzano esclusivamente le reattività chimiche di alcuni residui AA
 Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Amminoacidi. Struttura base di un a-amminoacido
 Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Prof. Fulvio Ursini Dipartimento di Chimica Biologica (Vallisneri IV piano Nord) Viale G. Colombo, Padova. Tel.
 Prof. Fulvio Ursini Dipartimento di Chimica Biologica (Vallisneri IV piano Nord) Viale G. Colombo, 3-35121 Padova. Tel.:+39-049-8276104 Fax.:+39-049-8073310 E-mail: fulvio.ursini@unipd.it Funzioni delle
Prof. Fulvio Ursini Dipartimento di Chimica Biologica (Vallisneri IV piano Nord) Viale G. Colombo, 3-35121 Padova. Tel.:+39-049-8276104 Fax.:+39-049-8073310 E-mail: fulvio.ursini@unipd.it Funzioni delle
LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI PROTEINE. sono ACIDI NUCLEICI. molecole complesse = POLIMERI. formate dall'unione di
 LE BIOMOLECOLE LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI LE BIOMOLECOLE sono LIPIDI PROTEINE ACIDI NUCLEICI molecole complesse = POLIMERI formate dall'unione di molecole semplici = MONOMERI
LE BIOMOLECOLE LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI LE BIOMOLECOLE sono LIPIDI PROTEINE ACIDI NUCLEICI molecole complesse = POLIMERI formate dall'unione di molecole semplici = MONOMERI
le porzioni con strutture secondarie sono avvicinate e impaccate mediante anse e curve della catena. STRUTTURA TERZIARIA
 STRUTTURA TERZIARIA le porzioni con strutture secondarie sono avvicinate e impaccate mediante anse e curve della catena. Le proteine globulari dopo aver organizzato il proprio scheletro polipeptidico con
STRUTTURA TERZIARIA le porzioni con strutture secondarie sono avvicinate e impaccate mediante anse e curve della catena. Le proteine globulari dopo aver organizzato il proprio scheletro polipeptidico con
Nucleotidi 26/10/2014. Nucleotidi (1)
 I Nucleotidi Hanno Tre Componenti Base azotata Nucleotidi https://www2.chemistry.msu.edu/faculty/reusch/virttxtjml/nucacids.htm Base azotata Qualsiasi composto che manifesta proprietà basiche per via della
I Nucleotidi Hanno Tre Componenti Base azotata Nucleotidi https://www2.chemistry.msu.edu/faculty/reusch/virttxtjml/nucacids.htm Base azotata Qualsiasi composto che manifesta proprietà basiche per via della
LE BIOMOLECOLE LIPIDI, PROTEINE E ACIDI NUCLEICI GSCATULLO
 LE BIOMOLECOLE LIPIDI, PROTEINE E ACIDI NUCLEICI GSCATULLO ( Le Biomolecole I Lipidi Definizione e classificazione I lipidi rappresentano una vasta classe di composti chimicamente eterogenea per struttura
LE BIOMOLECOLE LIPIDI, PROTEINE E ACIDI NUCLEICI GSCATULLO ( Le Biomolecole I Lipidi Definizione e classificazione I lipidi rappresentano una vasta classe di composti chimicamente eterogenea per struttura
I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici
 I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici La seta della tela di ragno è un insieme di macromolecole, dette proteine. Sono le caratteristiche fisico-chimiche di queste
I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici La seta della tela di ragno è un insieme di macromolecole, dette proteine. Sono le caratteristiche fisico-chimiche di queste
LA SINTESI PROTEICA LE MOLECOLE CHE INTERVENGONO IN TALE PROCESSO SONO:
 LA SINTESI PROTEICA La sintesi proteica è il processo che porta alla formazione delle proteine utilizzando le informazioni contenute nel DNA. Nelle sue linee fondamentali questo processo è identico in
LA SINTESI PROTEICA La sintesi proteica è il processo che porta alla formazione delle proteine utilizzando le informazioni contenute nel DNA. Nelle sue linee fondamentali questo processo è identico in
Vittoria Patti MACROMOLECOLE BIOLOGICHE. 4. proteine
 Vittoria Patti MACROMOLECOLE BIOLOGICHE 4. proteine 1 Funzioni principali delle proteine funzione cosa significa esempi ENZIMATICA STRUTTURALE TRASPORTO MOVIMENTO DIFESA IMMUNITARIA ORMONALE catalizzare
Vittoria Patti MACROMOLECOLE BIOLOGICHE 4. proteine 1 Funzioni principali delle proteine funzione cosa significa esempi ENZIMATICA STRUTTURALE TRASPORTO MOVIMENTO DIFESA IMMUNITARIA ORMONALE catalizzare
SOLUZIONI DEGLI ESERCIZI
 Dal carbonio agli OGM Biochimica e biotecnologie SOLUZIONI DEGLI ESERCIZI Capitolo 0 Il mondo del carbonio 1. b, e 2. d 3. 7 4. 5. 6. 7. a) Isomeria di posizione; b) i due composti non sono isomeri; c)
Dal carbonio agli OGM Biochimica e biotecnologie SOLUZIONI DEGLI ESERCIZI Capitolo 0 Il mondo del carbonio 1. b, e 2. d 3. 7 4. 5. 6. 7. a) Isomeria di posizione; b) i due composti non sono isomeri; c)
IL DOGMA CENTRALE DELLA BIOLOGIA RNA
 La traduzione IL DOGMA CENTRALE DELLA BIOLOGIA Trascrizione DNA Passaggio dell informazione contenuta nel DNA mediante la sintesi di RNA RNA Proteine Duplicazione DNA Traduzione Costruzione della catena
La traduzione IL DOGMA CENTRALE DELLA BIOLOGIA Trascrizione DNA Passaggio dell informazione contenuta nel DNA mediante la sintesi di RNA RNA Proteine Duplicazione DNA Traduzione Costruzione della catena
Chimotripsina Una proteina globulare. Glicina Un amminoacido
 Chimotripsina Una proteina globulare Glicina Un amminoacido - In teoria un numero enorme di differenti catene polipeptidiche potrebbe essere sintetizzato con i 20 amminoacidi standard. 20 4 = 160.000 differenti
Chimotripsina Una proteina globulare Glicina Un amminoacido - In teoria un numero enorme di differenti catene polipeptidiche potrebbe essere sintetizzato con i 20 amminoacidi standard. 20 4 = 160.000 differenti
corta catena (meno di 20 ammino acidi) mancanza di una struttura spaziale organizzata lunga catena di ammino acidi struttura spaziale organizzata
 STRUTTURA DELLE PROTEINE Peptide: corta catena (meno di 20 ammino acidi) mancanza di una struttura spaziale organizzata Polipeptide (proteina): lunga catena di ammino acidi struttura spaziale organizzata
STRUTTURA DELLE PROTEINE Peptide: corta catena (meno di 20 ammino acidi) mancanza di una struttura spaziale organizzata Polipeptide (proteina): lunga catena di ammino acidi struttura spaziale organizzata
Lezione 1: Atomi e molecole:
 Lezione 1: Atomi e molecole: La materia è costituita da elementi chimici in forma pura o in combinazioni dette composti. La vita richiede circa 25 elementi chimici. La struttura atomica determina il comportamento
Lezione 1: Atomi e molecole: La materia è costituita da elementi chimici in forma pura o in combinazioni dette composti. La vita richiede circa 25 elementi chimici. La struttura atomica determina il comportamento
CORSO DI BIOCHIMICA PER INGEGNERIA BIOMEDICA I ESERCITAZIONE
 CORSO DI BIOCHIMICA PER INGEGNERIA BIOMEDICA I ESERCITAZIONE 1) Che tipo di ibridazione ha il carbonio coinvolto nel doppio legame degli alcheni? Descrivi brevemente. Alcheni Ibridazione sp 2 2s p x p
CORSO DI BIOCHIMICA PER INGEGNERIA BIOMEDICA I ESERCITAZIONE 1) Che tipo di ibridazione ha il carbonio coinvolto nel doppio legame degli alcheni? Descrivi brevemente. Alcheni Ibridazione sp 2 2s p x p
NUCLEOTIDI e ACIDI NUCLEICI
 NUCLEOTIDI e ACIDI NUCLEICI Struttura dei nucleotidi Il gruppo fosfato conferisce carica negativa e proprietà acide FUNZIONI DEI NUCLEOTIDI MOLECOLE DI RISERVA DI ENERGIA L idrolisi dei nucleosidi trifosfato
NUCLEOTIDI e ACIDI NUCLEICI Struttura dei nucleotidi Il gruppo fosfato conferisce carica negativa e proprietà acide FUNZIONI DEI NUCLEOTIDI MOLECOLE DI RISERVA DI ENERGIA L idrolisi dei nucleosidi trifosfato
Immunologia e Immunologia Diagnostica MATURAZIONE DEI LINFOCITI
 Immunologia e Immunologia Diagnostica MATURAZIONE DEI LINFOCITI Il percorso di maturazione dei linfociti Sviluppo della specicifità immunologica I linfociti B e T avviano le risposte immunitarie dopo il
Immunologia e Immunologia Diagnostica MATURAZIONE DEI LINFOCITI Il percorso di maturazione dei linfociti Sviluppo della specicifità immunologica I linfociti B e T avviano le risposte immunitarie dopo il
Formazione del legame peptidico:
 Formazione del legame peptidico: Planare, ha una forza intermedia tra il legame semplice ed il legame doppio. 2^ lezione N R C C O O O + R N R C O C O O N R C C N C C O Ogni piano delle unità peptidiche
Formazione del legame peptidico: Planare, ha una forza intermedia tra il legame semplice ed il legame doppio. 2^ lezione N R C C O O O + R N R C O C O O N R C C N C C O Ogni piano delle unità peptidiche
I Composti Organici. Le Biomolecole
 I Composti Organici I composti organici sono molecole tutte contenenti carbonio. Essi comprendono. 1. composti di interesse energetico che sono gli Idrocarburi ( i derivati del petrolio), 2. composti a
I Composti Organici I composti organici sono molecole tutte contenenti carbonio. Essi comprendono. 1. composti di interesse energetico che sono gli Idrocarburi ( i derivati del petrolio), 2. composti a
LE MOLECOLE BIOLOGICHE
 LE MOLECOLE BIOLOGICHE Le cellule contengono quattro famiglie principali di molecole organiche Zuccheri (monosaccaridi) - forniscono una fonte di energia - subunità dei polisaccaridi Amminoacidi - subunità
LE MOLECOLE BIOLOGICHE Le cellule contengono quattro famiglie principali di molecole organiche Zuccheri (monosaccaridi) - forniscono una fonte di energia - subunità dei polisaccaridi Amminoacidi - subunità
amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente
 Gli amminoacidi naturali sono α-amminoacidi : il gruppo amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente formula generale: gruppo funzionale carbossilico
Gli amminoacidi naturali sono α-amminoacidi : il gruppo amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente formula generale: gruppo funzionale carbossilico
IN UN ATOMO SI DISTINGUE UN NUCLEO CARICO POSITIVAMENTE ATTORNO AL QUALE RUOTANO PARTICELLE CARICHE NEGATIVAMENTE: GLI ELETTRONI (e - ) (-)
 LA VITA, LA CHIMICA E L ACQUA PER INIZIARE QUALCHE CENNO DI CHIMICA LA MATERIA E FATTA DI COMBINAZIONI DI ELEMENTI. GLI ELEMENTI SONO COMPOSTI DA SINGOLI ATOMI, LE PIU PICCOLE UNITA CHE MANTENGONO LE PROPRIETA
LA VITA, LA CHIMICA E L ACQUA PER INIZIARE QUALCHE CENNO DI CHIMICA LA MATERIA E FATTA DI COMBINAZIONI DI ELEMENTI. GLI ELEMENTI SONO COMPOSTI DA SINGOLI ATOMI, LE PIU PICCOLE UNITA CHE MANTENGONO LE PROPRIETA
FORMAZIONE DEL LEGAME PEPTIDICO
 AMINOACIDI FORMAZIONE DEL LEGAME PEPTIDICO SEQUENZA AMINOACIDICA DELL INSULINA STRUTTURA SECONDARIA DELLE PROTEINE STRUTTURA TERZIARIA DELLE PROTEINE STRUTTURA QUATERNARIA DELLE PROTEINE Definizione Processi
AMINOACIDI FORMAZIONE DEL LEGAME PEPTIDICO SEQUENZA AMINOACIDICA DELL INSULINA STRUTTURA SECONDARIA DELLE PROTEINE STRUTTURA TERZIARIA DELLE PROTEINE STRUTTURA QUATERNARIA DELLE PROTEINE Definizione Processi
MACROMOLECOLE. Polimeri (lipidi a parte)
 MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
You created this PDF from an application that is not licensed to print to novapdf printer (http://www.novapdf.com)
 LA VITA, LA CHIMICA E L ACQUA PER INIZIARE QUALCHE CENNO DI CHIMICA LA MATERIA E FATTA DI COMBINAZIONI DI ELEMENTI. GLI ELEMENTI SONO COMPOSTI DA SINGOLI ATOMI, LE PIU PICCOLE UNITA CHE MANTENGONO LE PROPRIETA
LA VITA, LA CHIMICA E L ACQUA PER INIZIARE QUALCHE CENNO DI CHIMICA LA MATERIA E FATTA DI COMBINAZIONI DI ELEMENTI. GLI ELEMENTI SONO COMPOSTI DA SINGOLI ATOMI, LE PIU PICCOLE UNITA CHE MANTENGONO LE PROPRIETA
PROTEINE. Amminoacidi
 PROTEINE Le proteine sono le macromolecole alla base delle attività cellulari. Sono oltre diecimila per cellula, dove svolgono differenti funzioni: Sono ad esempio: enzimi: aumentano la velocità delle
PROTEINE Le proteine sono le macromolecole alla base delle attività cellulari. Sono oltre diecimila per cellula, dove svolgono differenti funzioni: Sono ad esempio: enzimi: aumentano la velocità delle
PROTEINE DEFINIZIONE:
 Cap.4 Le PROTEINE DEFINIZIONE: Macromolecole formate di AA della serie L uniti tra loro da un legame peptidico. FUNZIONI DELLE PROTEINE Enzimi Proteine di riconoscimento Proteine di trasporto Proteine
Cap.4 Le PROTEINE DEFINIZIONE: Macromolecole formate di AA della serie L uniti tra loro da un legame peptidico. FUNZIONI DELLE PROTEINE Enzimi Proteine di riconoscimento Proteine di trasporto Proteine
 http://digilander.libero.it/glampis64 Idrogeno, ossigeno, carbonio e azoto costituiscono il 99% delle cellule. I composti del carbonio sono chiamati composti organici o molecole organiche. I composti organici
http://digilander.libero.it/glampis64 Idrogeno, ossigeno, carbonio e azoto costituiscono il 99% delle cellule. I composti del carbonio sono chiamati composti organici o molecole organiche. I composti organici
Una risposta cellulare specifica può essere determinata dalla presenza di mediatori chimici (ormoni o altre molecole), dall interazione con altre
 Una risposta cellulare specifica può essere determinata dalla presenza di mediatori chimici (ormoni o altre molecole), dall interazione con altre cellule (contatto cellula-cellula) o con strutture extracellulari
Una risposta cellulare specifica può essere determinata dalla presenza di mediatori chimici (ormoni o altre molecole), dall interazione con altre cellule (contatto cellula-cellula) o con strutture extracellulari
Biosintesi degli aminoacidi
 Biosintesi degli aminoacidi Per l uomo la fonte principale di gruppi NH 4 + sono gli AA contenuti nelle proteine della dieta Parte di NH 4 + che si genera dalla degradazione degli AA viene riciclata e
Biosintesi degli aminoacidi Per l uomo la fonte principale di gruppi NH 4 + sono gli AA contenuti nelle proteine della dieta Parte di NH 4 + che si genera dalla degradazione degli AA viene riciclata e
9) Scrivere un disaccaride formato dal β-d-galattosio e dall α-d-n-acetil-glucosammina legati da un legame glicosidico β(1-4).
 CARBOIDRATI - AMMINOACIDI - PROTEINE 1) Scrivere la proiezione di Fisher del D-ribosio e del D-glucosio. La lettera D a cosa si riferisce? Disegnare inoltre il disaccaride ottenuto dalla condensazione
CARBOIDRATI - AMMINOACIDI - PROTEINE 1) Scrivere la proiezione di Fisher del D-ribosio e del D-glucosio. La lettera D a cosa si riferisce? Disegnare inoltre il disaccaride ottenuto dalla condensazione
NUCLEOTIDI. Hanno la funzione di conservare, trasmettere e modulare l informazione genetica e di tradurla nella sintesi proteica.
 NUCLEOTIDI a) Forma di energia utilizzata nel metabolismo cellulare (ATP, GTP) b) Entrano a far parte della struttura di cofattori enzimatici (coenzimi) e intermedi metabolici c) Costituiscono gli ACIDI
NUCLEOTIDI a) Forma di energia utilizzata nel metabolismo cellulare (ATP, GTP) b) Entrano a far parte della struttura di cofattori enzimatici (coenzimi) e intermedi metabolici c) Costituiscono gli ACIDI
Gli acidi nucleici sono eteropolimeri lineari costituiti da subunità nucleotidiche (monomeri).
 Gli acidi nucleici sono eteropolimeri lineari costituiti da subunità nucleotidiche (monomeri). Un nucleotide è formato da: uno zucchero: (Ribosio o Deossiribosio), a 5 atomi di carbonio in forma ciclica
Gli acidi nucleici sono eteropolimeri lineari costituiti da subunità nucleotidiche (monomeri). Un nucleotide è formato da: uno zucchero: (Ribosio o Deossiribosio), a 5 atomi di carbonio in forma ciclica
CPIA 1 FOGGIA punto di erogazione San Severo. Prof.ssa ANNA LUCIA L. CANCELLIERE
 CPIA 1 FOGGIA punto di erogazione San Severo Prof.ssa ANNA LUCIA L. CANCELLIERE Sono delle grandi molecole che troviamo nel mondo dei viventi sia come molecole costituenti gli organismi viventi che come
CPIA 1 FOGGIA punto di erogazione San Severo Prof.ssa ANNA LUCIA L. CANCELLIERE Sono delle grandi molecole che troviamo nel mondo dei viventi sia come molecole costituenti gli organismi viventi che come
Il dogma centrale della biologia. molecolare
 Il dogma centrale della biologia Cell molecolare Transcription Translation Ribosome DNA mrna Polypeptide (protein) L informazione per la sintesi delle proteine è contenuta nel DNA. La trascrizione e la
Il dogma centrale della biologia Cell molecolare Transcription Translation Ribosome DNA mrna Polypeptide (protein) L informazione per la sintesi delle proteine è contenuta nel DNA. La trascrizione e la
Amminoacidi Peptidi Proteine
 Amminoacidi Peptidi Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Gli amminoacidi nelle molecole proteiche sono tutti stereoisomeri L IDROFOBOCI IDROFOBOCI IDROFILICI Secondo gruppo
Amminoacidi Peptidi Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Gli amminoacidi nelle molecole proteiche sono tutti stereoisomeri L IDROFOBOCI IDROFOBOCI IDROFILICI Secondo gruppo
Costituzione dei viventi
 Costituzione dei viventi La materia e costituita da elementi chimici in forma pura o in combinazioni dette composti 25 dei 92 elementi naturali sono costituenti essenziali dei viventi 4 (C, O,, N) costituiscono
Costituzione dei viventi La materia e costituita da elementi chimici in forma pura o in combinazioni dette composti 25 dei 92 elementi naturali sono costituenti essenziali dei viventi 4 (C, O,, N) costituiscono
Fondamentali in ogni organismo, hanno molteplici ruoli:
 Le proteine Fondamentali in ogni organismo, hanno molteplici ruoli: Componenti strutturali (collagene, tessuto connettivo, citoscheletro, pelle) Trasportatori (emoglobina, albumina) Trasmettitori di messaggi
Le proteine Fondamentali in ogni organismo, hanno molteplici ruoli: Componenti strutturali (collagene, tessuto connettivo, citoscheletro, pelle) Trasportatori (emoglobina, albumina) Trasmettitori di messaggi
TRASCRIZIONE e TRADUZIONE
 TRASCRIZIONE e TRADUZIONE Trascrizione e traduzione Dogma centrale della biologia molecolare: processo con cui l informazione contenuta nel DNA dirige la sintesi delle proteine. Trascrizione Maturazione
TRASCRIZIONE e TRADUZIONE Trascrizione e traduzione Dogma centrale della biologia molecolare: processo con cui l informazione contenuta nel DNA dirige la sintesi delle proteine. Trascrizione Maturazione
Parametri dell α-elica. residui/giro 3.6. passo dell elica
 GRAFICO DI RAMACHANDRAN Parametri dell α-elica residui/giro 3.6 spazio/residuo passo dell elica 1.5 Å 5.4 Å 1 L α-elica può essere destabilizzata da interazioni tra i gruppi R: repulsione/attrazione elettrostatica
GRAFICO DI RAMACHANDRAN Parametri dell α-elica residui/giro 3.6 spazio/residuo passo dell elica 1.5 Å 5.4 Å 1 L α-elica può essere destabilizzata da interazioni tra i gruppi R: repulsione/attrazione elettrostatica
Gerard Tortora, Brian Derrickson. Conosciamo
 1 Gerard Tortora, Brian Derrickson Conosciamo il corpo umano Capitolo 1 L organizzazione del corpo umano 1. Che cosa sono l anatomia e la fisiologia 2. I livelli di organizzazione e gli apparati del corpo
1 Gerard Tortora, Brian Derrickson Conosciamo il corpo umano Capitolo 1 L organizzazione del corpo umano 1. Che cosa sono l anatomia e la fisiologia 2. I livelli di organizzazione e gli apparati del corpo
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 11
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 11 Funzioni delle proteine Concetti chiave: La varietà strutturale delle proteine consente loro di svolgere un enorme quantità
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 11 Funzioni delle proteine Concetti chiave: La varietà strutturale delle proteine consente loro di svolgere un enorme quantità
Chimica Biologica A.A α-elica foglietto β reverse turn
 Chimica Biologica A.A. 2010-2011 α-elica foglietto β reverse turn Str. Secondaria sperimentalmente osservata: Si distinguono fondamentalmente tre tipi di strutture secondarie: α elica foglietto β reverse
Chimica Biologica A.A. 2010-2011 α-elica foglietto β reverse turn Str. Secondaria sperimentalmente osservata: Si distinguono fondamentalmente tre tipi di strutture secondarie: α elica foglietto β reverse
Diagramma di Ramachandran
 Chimica Biologica A.A. 2010-2011 Diagramma di Ramachandran Diagramma di Ramachandran Catena polipeptidica La formazione in successione di legami peptidici genera la cosiddetta catena principale o scheletro
Chimica Biologica A.A. 2010-2011 Diagramma di Ramachandran Diagramma di Ramachandran Catena polipeptidica La formazione in successione di legami peptidici genera la cosiddetta catena principale o scheletro
Le Biomolecole I parte. Lezioni d'autore di Giorgio Benedetti
 Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
AMINOACIDI - 1 AMINOACIDI - 2
 AMINOAIDI - 1 Proteine (gr. pròtos = primo) 50-80% peso secco cellulare GENE POTEINA EFFETTO proteine calore idrolisi acida o alcalina α-aminoacidi proteasi Struttura generale degli α-aminoacidi primari
AMINOAIDI - 1 Proteine (gr. pròtos = primo) 50-80% peso secco cellulare GENE POTEINA EFFETTO proteine calore idrolisi acida o alcalina α-aminoacidi proteasi Struttura generale degli α-aminoacidi primari
Università Telematica Pegaso. Indice
 LE PROTEINE PROF.SSA AUSILIA ELCE Indice 1 INTRODUZIONE -------------------------------------------------------------------------------------------------------------- 3 2 TRASCRIZIONE--------------------------------------------------------------------------------------------------------------
LE PROTEINE PROF.SSA AUSILIA ELCE Indice 1 INTRODUZIONE -------------------------------------------------------------------------------------------------------------- 3 2 TRASCRIZIONE--------------------------------------------------------------------------------------------------------------
Le idee della chimica
 G. Valitutti A.Tifi A.Gentile Seconda edizione Copyright 2009 Zanichelli editore Capitolo 25 Le basi della biochimica 1. I carboidrati 2. I lipidi 3. Gli amminoacidi, i peptidi e le proteine 4. La struttura
G. Valitutti A.Tifi A.Gentile Seconda edizione Copyright 2009 Zanichelli editore Capitolo 25 Le basi della biochimica 1. I carboidrati 2. I lipidi 3. Gli amminoacidi, i peptidi e le proteine 4. La struttura
Gli amminoacidi Gli amminoacidi sono dei composti polifunzionali che hanno formula generale:
 Gli amminoacidi Gli amminoacidi sono dei composti polifunzionali che hanno formula generale: N 2 Il nome ordinario degli amminoacidi prevale su quello della nomenclatura IUPA. Si possono avere α-amminoacidi,
Gli amminoacidi Gli amminoacidi sono dei composti polifunzionali che hanno formula generale: N 2 Il nome ordinario degli amminoacidi prevale su quello della nomenclatura IUPA. Si possono avere α-amminoacidi,
La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa.
 La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa. Le cellule contengono 4 famiglie principali di piccole molecole organiche: Amminoacidi
La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa. Le cellule contengono 4 famiglie principali di piccole molecole organiche: Amminoacidi
STRUTTURA E FUNZIONE DELLE PROTEINE
 STRUTTURA E FUNZIONE DELLE PROTEINE Le PROTEINE sono i biopolimeri maggiormente presenti all interno delle cellule, dal momento che costituiscono dal 40 al 70% del peso secco. Svolgono funzioni biologiche
STRUTTURA E FUNZIONE DELLE PROTEINE Le PROTEINE sono i biopolimeri maggiormente presenti all interno delle cellule, dal momento che costituiscono dal 40 al 70% del peso secco. Svolgono funzioni biologiche
Livello di organizzazione degli esseri viventi
 Livello di organizzazione degli esseri viventi _Organismo; _Apparato; _Organo; _Tessuti; _Cellule; _Organelli cellulari; _Molecole. Atomo, elemento, molecola, composto, formula, legame, elettronegativita.
Livello di organizzazione degli esseri viventi _Organismo; _Apparato; _Organo; _Tessuti; _Cellule; _Organelli cellulari; _Molecole. Atomo, elemento, molecola, composto, formula, legame, elettronegativita.
CORSO DI LAUREA IN SCIENZE DELLA FORMAZIONE PRIMARIA LEZIONE PRIMA PARTE. Dott.ssa A. Fiarè
 CORSO DI LAUREA IN SCIENZE DELLA FORMAZIONE PRIMARIA LEZIONE PRIMA PARTE Dott.ssa A. Fiarè IL DNA (ACIDO DESOSSIRIBONUCLEICO) E UN ACIDO NUCLEICO DEFINITO POLINUCLEOTIDE, IN QUANTO E UNA MOLECOLA FORMATA
CORSO DI LAUREA IN SCIENZE DELLA FORMAZIONE PRIMARIA LEZIONE PRIMA PARTE Dott.ssa A. Fiarè IL DNA (ACIDO DESOSSIRIBONUCLEICO) E UN ACIDO NUCLEICO DEFINITO POLINUCLEOTIDE, IN QUANTO E UNA MOLECOLA FORMATA
Il DNA conserva l informazione genetica
 Il DNA conserva l informazione genetica Gli esperimenti di Frederick Griffith (1928) Gli esperimenti di Oswald Avery (1944) + Estratti dal ceppo IIIS ucciso al calore di Polisaccaridi Lipidi Proteine Acidi
Il DNA conserva l informazione genetica Gli esperimenti di Frederick Griffith (1928) Gli esperimenti di Oswald Avery (1944) + Estratti dal ceppo IIIS ucciso al calore di Polisaccaridi Lipidi Proteine Acidi
Adenina Adenine H H N N N N N Z
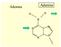 Adenina Adenine Z Guanina O GUAIA Z Citosina CITOSIA Z O Timina Thymine C3 O Z O Siti di attacco elettrofilo 3 Thymine Basi appaiate: Timina-Adenina Adenine C 3 O O 3.ooA Basi appaiate: Citosina-Guanina
Adenina Adenine Z Guanina O GUAIA Z Citosina CITOSIA Z O Timina Thymine C3 O Z O Siti di attacco elettrofilo 3 Thymine Basi appaiate: Timina-Adenina Adenine C 3 O O 3.ooA Basi appaiate: Citosina-Guanina
F. Fogolari Milano, Marzo
 Biomolecole - 1 Federico Fogolari Dipartimento Scientifico e Tecnologico Universita di Verona Ca Vignal 1, Strada Le Grazie 15 37134 Verona, Italy tel. ++39-045-8027906 fax. ++39-045-8027929 email: fogolari@sci.univr.it
Biomolecole - 1 Federico Fogolari Dipartimento Scientifico e Tecnologico Universita di Verona Ca Vignal 1, Strada Le Grazie 15 37134 Verona, Italy tel. ++39-045-8027906 fax. ++39-045-8027929 email: fogolari@sci.univr.it
