Università degli Studi di Roma Tre. Corso di Laurea in Scienze Biologiche NOR. Dispense delle lezioni di Laboratorio di Chimica Organica
|
|
|
- Severino Marino
- 8 anni fa
- Visualizzazioni
Transcript
1 Università degli Studi di Roma Tre Corso di Laurea in Scienze iologiche NOR Dispense delle lezioni di Laboratorio di Chimica Organica I anno II semestre Prof. Giovanna Iucci.. 27/28 1
2 Tecniche di separazione e purificazione dei composti organici I composti organici, sia di origine naturale che prodotti in laboratorio mediante sintesi chimica, si trovano spesso miscelati ad altre sostanze dalle quali devono essere separati. Nel caso, ad esempio, di una sostanza naturale presente in una data matrice biologica, per ottenere il composto allo stato puro, è necessario estrarlo dalla matrice, separarlo e purificarlo dagli altri composti eventualmente presenti. Nel caso di un prodotto ottenuto tramite sintesi chimica, può essere necessario rimuovere il solvente, gli eventuali reagenti in eccesso, il catalizzatore e/o i possibili prodotti collaterali della reazione. I chimici hanno quindi messo a punto una serie di tecniche che consentono di separare un composto (solido o liquido) contenuto in una miscela dagli altri componenti; queste tecniche sfruttano le differenti proprietà chimico-fisiche dei componenti della miscela per separarli. La tabella seguente elenca le più comuni tecniche di separazione e purificazione dei composti organici in funzione dello stato di aggregazione delle sostanze da purificare e della proprietà chimico-fisica utilizzata per separarle dagli altri componenti della miscela. Tabella 1 Tecnica Stato di aggregazione proprietà chimico-fisica Distillazione Liquido Punto di ebollizione Sublimazione Solido Punto di fusione Cristallizzazione Solido Solubilità Estrazione con solventi Liquido/Solido Ripartizione tra fasi Cromatografia Liquido/Solido Ripartizione tra fasi Nelle prossime pagine analizzeremo in dettaglio le diverse tecniche di separazione e purificazione dei composti organici, il loro principio di funzionamento e le loro applicazioni. 2
3 Distillazione La distillazione è una tecnica che permette di separare i diversi componenti di una miscela liquida sfruttando il loro diverso punto di ebollizione; viene utilizzata, ad esempio, nella produzione di bevande alcoliche e nella separazione del petrolio greggio nei suoi componenti. Possono essere separati per distillazione composti liquidi aventi punto di ebollizione diverso. Per la legge di Raoult, il vapore in equilibrio con una miscela di liquidi è più ricco nel componente più volatile (avente punto di ebollizione più basso) rispetto alla miscela di partenza. Consideriamo una miscela liquida di due composti e, aventi diverso punto di ebollizione. La tensione di vapore dei due componenti nella miscela sarà: P = x P P = x P Dove: P, P = tensione di vapore di e nella miscela P, P = tensione di vapore di e allo stato puro x, x = frazione di e nella miscela La tensione di vapore totale della miscela (P) sarà: P = P + P = x P + x P P P =x P P=P +P P =x P P Se definiamo y, y = frazione molare di e nel vapore abbiamo che: P =P. y P =P. y risulta quindi: y y P = P x = x P P x x x =1 x = La composizione della fase vapore risulterà diversa da quella della fase liquida: il vapore sarà più ricco nel componente più volatile, avente cioè allo stato puro punto di ebollizione più basso e tensione di vapore più elevata; nel caso mostrato in figura, il componente. x = x =1 In un tipico apparato per la distillazione, la miscela liquida viene portata all ebollizione in un recipiente; la temperatura del distillato viene controllata tramite un termometro. I vapori, più ricchi nel componente più volatile, vengono condensati in un refrigerante e convogliati in un pallone di raccolta. Non sempre è possibile separare i componenti di una miscela mediante una singola distillazione semplice ma può essere necessario effettuare più distillazioni. 3
4 Sublimazione La sublimazione è il passaggio dallo stato solido direttamente a quello gassoso; questa transizione di fase ha luogo al di sotto di una data pressione, corrispondente al punto triplo del diagramma di fase. ostriamo a titolo di esempio il diagramma di fase della CO 2. La sublimazione può essere usata come metodo per separare un composto solido dalle impurità in esso contenute purché meno volatili del composto da purificare. La figura mostra un apparato per la sublimazione; esso consiste sostanzialmente in un tubo, all interno del quale viene posto il solido da purificare, munito di un refrigerante e collegato ad una sistema di pompaggio che permette di ridurre la pressione (pompa da vuoto). Il solido, riscaldato in condizioni di pressione ridotta, sublima; i suoi vapori, venendo a contatto con il refrigerante, si raffreddano e solidificano nuovamente sul refrigerante. In questo modo è possibile solido dalle impurità in esso contenute che risultino meno volatili. 4
5 Cristallizzazione La cristallizzazione è una metodica utilizzata per purificare ed isolare composti chimici, consistente in una solubilizzazione seguita da una precipitazione. E possibile purificare un composto per cristallizzazione, ad esempio, sciogliendolo a caldo in un solvente, facendolo successivamente precipitare per raffreddamento e filtrandolo. Per effettuare una cristallizzazione è necessario quindi individuare un solvente, detto solvente di cristallizzazione, nel quale il composto da purificare sia solubile a caldo e insolubile a freddo. In questo modo si può separare il composto puro dalle impurezze insolubili nel solvente a caldo e/o da quelle solubili a freddo. Se non è possibile trovare un unico solvente di cristallizzazione, si scioglie il composto da purificare in un solvente (1) in cui esso è solubile e successivamente si aggiunge un solvente (2) in cui è insolubile, ottenendo così la precipitazione; i due solventi (1) e (2) devono ovviamente essere miscibili tra loro. Durante la cristallizzazione, i composti disciolti in un solvente solidificano disponendosi secondo strutture cristalline ordinate, secondo un processo che implica una diminuzione di entropia. La formazione di una singola particella solida, detta il germe di cristallizzazione, costituisce il punto d'inizio del processo di cristallizzazione: tale singola entità funge da agglomerante catalizzando la formazione del solido per accrescimento successivo. pparato per la filtrazione 5
6 Estrazione mediante solventi L estrazione liquido-liquido è una metodica di laboratorio che utilizza il passaggio di un soluto da un solvente ad un altro solvente allo scopo di ottenere composti puri da fonti animali o vegetali o semplicemente per purificare sostanze impure. I due solventi utilizzati non devono essere miscibili fra di loro; generalmente uno dei due solventi è l acqua e l altro è un solvente organico, meno polare. Possono essere utilizzati sia solventi più densi e pesanti dell acqua (es. CH 2 Cl 2, CHCl 3, CCl 4 ) che solventi meno densi e quindi più leggeri dell acqua (etere di petrolio, acetato di etile, il benzene e l etere etilico). L apparecchio più semplice utilizzato per effettuare le estrazioni liquido-liquido è l imbuto separatore, mostrato in figura. Introduciamo nell imbuto separatore i due liquidi non miscibili, che costituiscono quindi due fasi distinte; supponiamo che la fase 1 contenga la sostanza da purificare (soluto) e fase 2 sia il solvente puro con il quale vogliamo estrarla. Se il soluto è solubile nella fase 2, alcune molecole di soluto passeranno spontaneamente dalla fase 1 alla fase 2, e la quantità totale di soluto tenderà a dividersi tra i due solventi (ripartizione tra fasi). gitiamo manualmente l imbuto per aumentare la superficie di contatto e quindi lo scambio di soluto tra le due fasi e raggiungere più velocemente un equilibrio tra la concentrazione del soluto () nella fase 1 nella fase Per questo equilibrio possiamo scrivere la costante termodinamica, detta coefficiente di ripartizione K, data dal rapporto tra le concentrazioni (moli/l) del soluto nei due solventi; più il coefficiente di ripartizione è elevato maggiore sarà l'accuratezza dell'estrazione. [] [] 2 K = = C 1 = concentrazione all equilibrio della sostanza nella fase 1 C 2 = concentrazione all equilibrio della sostanza nella fase 2 In questo modo è possibile separare la sostanza da purificare da altre sostanze presenti in soluzione e aventi una minor affinità per la fase 2, ovvero un valore inferiore di K. llo scopo di estrarre una maggior quantità di soluto può essere opportuno ripetere più volte l operazione; si può dimostrare matematicamente che si estrae più soluto dalla fase 1 alla fase 2 effettuando più estrazioni consecutive con piccole quantità di solvente (fase 2), piuttosto che con una sola estrazione utilizzando una maggior quantità di solvente. 1 C C 1 2 6
7 Cromatografia La cromatografia è un metodo per la separazione dei componenti di una miscela basato sulla ripartizione tra fasi. In una separazione cromatografia i composti contenuti in una miscela vengono separati in funzione della loro differente affinità per due fasi: - una fase fissa, o fase stazionaria, che può essere un solido o un liquido supportato su solido; - una fase mobile, liquida o gassosa, che viene fatta fluire in continuo sulla fase stazionaria. Dobbiamo l invenzione di questa tecnica al botanico russo Tswett che la usò per separare la clorofilla contenuta negli estratti vegetali. Pose la miscela da separare in cima ad una colonna riempita di una polvere di carbonato di calcio, attraverso la quale fece percolare etere di petrolio. ano a mano che l etere di petrolio scorreva lungo la colonna, Tswett osservò la formazione di bande colorate che si muovevano lungo la colonna con velocità diversa (la parola cromatografia deriva dal greco croma =colore), bande dovute ai diversi pigmenti contenuti negli estratti vegetali. Oggi la cromatografia può essere utilizzata, come vedremo, per separare sostanze sia colorate che incolori. In un tipico apparato per la cromatografia, mostrato in figura, la fase stazionaria (consistente in una polvere finemente suddivisa, per aumentare lo sviluppo superficiale) è contenuta all interno di un tubo sottile detto colonna cromatografica. La miscela da separare viene posta in cima alla colonna cromatografica e la fase mobile, detta anche eluente, viene fatta fluire in continuo attraverso la colonna, muovendosi attraverso gli interstizi della fase mobile e riempiendoli. La figura mostra la separazione di una miscela contenente tre diverse sostanze (bianca, nera, grigia) aventi diversa affinità per la fase stazionaria e per la fase mobile. miscela da separare fase stazionaria Flusso del solvente Fig.1 Fig. 2 tempo Le molecole dei vari componenti della miscela tenderanno a ripartirsi fra le due fasi (stazionaria S e mobile ) in funzione del loro diverso coefficiente di ripartizione K: S [] [] S K = = [C, C S = concentrazione di della fase mobile (), stazionaria (S)] Quando le molecole del componente si trovano nella fase mobile esse si muovono seguendo il flusso dell eluente; quando si trovano nella fase stazionaria rimangono ferme. Di conseguenza, tra i componenti della miscela da separare le sostanze che hanno una maggiore affinità per la fase mobile vengono eluite (trasportate dall eluente attraverso la colonna cromatografica) più rapidamente di quelle che hanno maggiore affinità per la fase stazionaria. C C S 7
8 Immaginiamo di porre all uscita della colonna un rivelatore che registra il passaggio di una sostanza eluita ed elabora i dati su di un cromatogramma. Un cromatogramma è un grafico che ha in ascissa il tempo (t) trascorso dall inizio della cromatografia ovvero il volume di eluente (V) corrispondente (supponendo un flusso costante, tempo trascorso e volume di eluente sono tra loro proporzionali) ed in ordinata il segnale del rivelatore, proporzionale alla concentrazione di soluto nella soluzione che fuoriesce dalla colonna. Ogni volta che una sostanza viene rivelata, il cromatogramma registra un picco più o meno alto a seconda della sua concentrazione (vedi figura). cromatogramma Si definisce tempo di ritenzione (t R ) il tempo necessario alla sostanza analizzata per essere eluita dall inizio all uscita della colonna. Il corrispondente volume di ritenzione (V R ) è volume di fase mobile necessario ad eluire l analita. Viene detto tempo morto (t ) il tempo di ritenzione di un composto che non è trattenuto dalla fase stazionaria e che passa attraverso la colonna alla stessa velocità con cui fluisce la fase mobile; è pari quindi al tempo che la fase mobile impiega per attraversare tutta la colonna. Il volume morto (V ) è il volume di ritenzione di un composto che non è trattenuto e corrisponde al volume di fase mobile contenuto all interno della colonna. Il tempo di ritenzione è dato dalla somma del tempo trascorso dalla sostanza analizzata nella fase stazionaria (t S ) e nella fase mobile (t ); poiché quando la sostanza si trova nella fase mobile si muove con alla stessa velocità della fase mobile, il tempo trascorso dalla sostanza analizzata nella fase mobile è pari al tempo morto (t ). Di conseguenza: t R =t +t S Si definisce infine rapporto di ritenzione R di una sostanza eluita il rapporto tra tempo morto ed il suo tempo di ritenzione: t t 1 R = = = t t R t + ts S 1+ t Se una sostanza ha, ad esempio rapporto di ritenzione R=,2, questo significa che essa, attraversano la colonna trascorre il 2% del suo tempo nella fase mobile e il restante 8% nella fase stazionaria. Il tempo trascorso dalla sostanza analizzata in ciascuna delle due fasi è proporzionale numero di moli di sostanza (n) che durante la cromatografia si trovano in quella fase, che possono essere calcolate facendo il prodotto fra la concentrazione della sostanza nella fase ed il volume della fase stessa (n=cv). Ne deriva quindi: ts csvs V 1 S = = K R = t cv V V S 1+ K V V, V S = volume della fase mobile (), stazionaria (S) 8
9 Il rapporto di ritenzione R risulta quindi tanto minore e il tempo di ritenzione t R tanto maggiore quanto più grande è il coefficiente di ripartizione K. Perché la cromatografia possa essere utilizzata efficacemente per separare due sostanze contenute in una miscela (risoluzione) bisogna che esse abbiano coefficiente di ripartizione e quindi rapporto di ritenzione abbastanza diverso da produrre nel cromatogramma due picchi aventi t R molto differente (selettività), che risultino perciò separati tra loro. Per ottenere una buona selettività è necessario soprattutto scegliere opportunamente la fase mobile e la fase stazionaria in modo da ottenere valori di t R molto diversi per le sostanze da separare. vere una buona selettività non è però sufficiente perché, anche se i picchi sono ben distanziati, possono essere tanto larghi da sovrapporsi; è necessario quindi che la separazione cromatografica presenti anche una buona efficienza, ovvero che i picchi nel cromatogramma risultino stretti. Risoluzione scarsa uona risoluzione dovuta a buona selettività uona risoluzione dovuta a buona efficienza L allargamento dei picchi cromato grafici dipende dal fatto che le molecole di un analita non si muovono lungo la colonna tutte con la stessa velocità: la loro dispersione ha generalmente un profilo Gaussiano. Il centro del profilo (banda di eluizione) rappresenta la velocità media. I fattori che possono influenzare l efficienza di una colonna cromatografica sono molteplici. Uno dei fattori che maggiormente contribuisce all allargamento dei picchi è la possibile esistenza di percorsi multipli per le molecole che si muovono attraverso la fase stazionaria, come mostrato in figura. Per ovviare a questo inconveniente è necessario procedere ad un impaccamento della colonna cromatografica, facendo in modo che la fase stazionaria si disponga nel modo più compatto e omogeneo possibile. Un altro fattore che contribuisce all allargamento dei picchi cromatografici è la diffusione longitudinale (in direzione perpendicolare al flusso del solvente) della sostanza da analizzare. 9
10 La cromatografia può essere usata sia a scopo preparativo, per separare e purificare i componenti di una miscela, che come tecnica analitica, per determinare la composizione di un campione; la cromatografia analitica consente di effettuare un analisi sia qualitativa che quantitativa di una miscela. Esistono vari tipi di tecniche cromatografiche, generalmente classificate in funzione della natura delle fasi stazionaria e mobile e del meccanismo di distribuzione. La seguente tabella ne riassume alcune. Tecnica fase meccanismo stazionaria mobile di distribuzione Liquida solido liquido adsorbimento liquido liquido ripartizione HPLC solido liquido adsorbimento (high performance liquido liquido ripartizione liquid chromatography) Gascromatografia solido gas adsorbimento liquido gas ripartizione TLC (Strato sottile) solido liquido adsorbimento Carta liquido liquido ripartizione Scambio Ionico solido liquido scambio ionico GPC (gel permeation solido liquido esclusione chromatography) dimensionale Le varie tecniche possono essere classificate in base alla natura della fase mobile (liquida o gassosa) e della fase stazionaria (solida o liquida); la cromatografia liquida si suddivide in cromatografia liquida classica (utilizzata a scopo preparativo) e cromatografia liquida ad alta pressione o HPLC, che può essere sia preparativa che, soprattutto, analitica. Un altro parametro importante è il tipo di supporto usato per contenere la fase stazionaria: colonna o strato sottile (TLC, cromatografia su carta). Infine vi è un'ulteriore suddivisione basata sul meccanismo di separazione: si distinguono infatti la cromatografia di adsorbimento, di ripartizione, di scambio ionico, e di esclusione dimensionale (vedi pagina seguente). 1
11 dsorbimento: la fase stazionaria è un solido. Le sostanze vengono separate in base alla loro differente tendenza ad adsorbirsi sulla fase stazionaria (solida) o a rimanere disciolte nella fase mobile (generalmente liquida o gassosa). Ripartizione: la fase stazionaria è un liquido. Le sostanze vengono separate in base alla tendenza a ripartirsi tra le due fasi. Scambio ionico: la fase stazionaria è una resina scambiatrice di ioni. Questa tecnica serve per separare molecole cariche. Esclusione dimensionale: la fase stazionaria è un gel poroso. Le sostanze vengono separate in base alle loro dimensioni. E una tecnica usata per separare polimeri o macromolecole biologiche. ndiamo ora ad analizzare le varie tecniche cromatografiche. 11
12 Cromatografia su colonna Si tratta di una tecnica impiegata a scopo esclusivamente preparativo. Si riempie una colonna di vetro con il materiale che funge da fase stazionaria, generalmente un solido (cromatografia di adsorbimento) o, più raramente, un liquido supportato su solido (cromatografia di ripartizione). Per realizzare un buon impiccamento della colonna, il riempimento viene effettuato disperdendo la fase stazionaria nella fase mobile, creando una sospensione che viene inserita nella colonna e lasciando stratificare lentamente la fase stazionaria. Si pone la miscela da separare in cima alla colonna e si fa fluire lungo la colonna la fase mobile (eluente) che, sotto l influenza della gravità, scende trasportando con sé i componenti della miscela. I vari componenti si separano gli uni dagli altri muovendosi a velocità diverse lungo la colonna in funzione della loro differente affinità per la fase stazionaria e la fase mobile. Nel corso dell intero processo di separazione cromatografia, l eluente in uscita viene raccolto in diverse frazioni ed ogni frazione viene analizzata alla ricerca di componenti disciolte mediante, ad esempio, cromatografia analitica (vedi in seguito) oppure analisi spettroscopica. miscela da separare fase stazionaria fase mobile fase stazionaria frazioni Le fasi stazionarie più frequentemente utilizzate nella cromatografia su colonna sono fasi solide polari quali il gel di silice (SiO 2 ) o l allumina (l 2 O 3 ). La fase stazionaria deve essere una polvere finemente suddivisa o un gel, per avere un elevato sviluppo superficiale, poiché il processo di adsorbimento ha luogo sulla superficie del materiale. La fase mobile è un solvente o una miscela di solventi; le fasi mobili vengono classificate in funzione della loro polarità (serie eluotropica). p o l a r i t à idrocarburi alifatici olefine idrocarburi aromatici alogenuri solfuri eteri nitrocomposti esteri, aldeidi e chetoni ammine solfoni solfossidi ammidi ac. carbossilici acqua Influenza della fase mobile: I solventi possono essere distinti a seconda della loro polarità (serie eluotropica). Le sostanze polari avranno maggiore affinità per i solventi più polari, le apolari per i non polari. 12
13 HPLC La cromatografia liquida ad alta prestazione, in inglese High Performance Liquid Cromatography o HPLC, costituisce un evoluzione della classica cromatografia su colonna che permette di ottenere un notevole miglioramento della risoluzione della separazione cromatografica. L HPLC può essere utilizzata come tecnica sia preparativa che analitica per effettuare analisi sia qualitative che quantitative. L aumento dell efficienza della separazione cromatografica è dovuto alle dimensioni estremamente ridotte delle particelle che costituiscono la fase stazionaria (diametro da 3 a 1 µm), permettendo così un migliore impiccamento, ed al diametro sottile della colonna cromatografica, in modo da ridurre la diffusione longitudinale. Per mantenere una ragionevole velocità di flusso dell eluente attraverso la colonna, e quindi un tempo di analisi ragionevole, è necessario applicare elevate pressioni, dell'ordine delle centinaia di atmosfere. cromatografia su colonna HPLC La figura che segue mostra lo schema di un cromatografo HPLC manometro campione serbatoio solvente dati pompa filtro iniettore colonna rivelatore elaboratore flusso dell'eluente L eluente, contenuto in un serbatoio, viene prelevato tramite la pompa, filtrato e sospinto ad alta pressione attraverso la colonna; la pressione viene misurata da un manometro. Il campione da analizzare viene miscelato con l eluente prima di entrare nella colonna tramite un dispositivo detto iniettore. lla fine della colonna è applicato un rivelatore (indice di rifrazione, UV-VIS) che analizza in continuo l eluente che fuoriesce uscita della colonna ed un elaboratore che, elaborando il segnale ricevuto dal rivelatore, traccia il cromatogramma che consente di identificare e quantificare le sostanze iniettate. NH 2 NO 2 NH 2 NO 2 NH 2 Il cromatogramma si presenta come una sequenza di picchi di varia ampiezza ed altezza distribuiti lungo l'asse del tempo. Dal tempo di ritenzione di ogni picco (a parità di condizioni di analisi) è possibile dedurre l'identità del composto eluito; dall'area dei picchi è possibile dedurre la concentrazione delle sostanze eluite. NO 2 t R 13
14 Cromatografia a scambio ionico Nella cromatografia a scambio ionico la fase stazionaria è costituita da una resina scambiatrice, ovvero un materiale polimerico, insolubile in acqua e nei comuni solventi organici, che presenta gruppi funzionali carichi, in grado di interagire con gli ioni presenti nella soluzione. Le resine scambiatrici possono essere divise in due categorie: - resine scambiatrici anioniche, che possiedono gruppi carichi positivamente e sono quindi in grado di interagire con gli ioni negativi. R + Y - + X - R + X - + Y - - resine scambiatrici cationiche, che possiedono gruppi carichi negativamente e sono quindi in grado di interagire con gli ioni positivi. R - Y + + X + R - X + + Y + La cromatografia a scambio ionico trova applicazione nella separazione delle miscele ioniche ed, in particolare, dei composti organici e biologici aventi gruppi acidi o basici, quali, ad esempio, gli aminoacidi. La carica netta di questi composti dipende dal loro pka e dal ph della soluzione in cui sono disciolti; operando in opportune condizioni di ph è possibile separare tra loro gli aminoacidi aventi diverso pka, e quindi diversa carica netta. 14
15 GPC La cromatografia di permeazione sul gel (Gel Permeation Chromatography, GPC), detta anche cromatografia di esclusione dimensionale, è una tecnica cromatografica nella quale le molecole del campione analizzato vengono separate in base alle loro differenti dimensioni o, in termini tecnici, al loro volume idrodinamico. Questa tecnica viene solitamente applicata alle macromolecole, quali i polimeri biologici (ad es. proteine) o sintetici. Nella GPC la fase stazionaria è costituita da un gel di polimero poroso, avente pori di dimensioni diverse. Quando l eluente fluisce attraverso la colonna, le molecole più piccole possono enetrare in tutti nei pori della fase stazionaria, mentre quelle più grandi ne sono escluse. Più grande è la molecola, minore è il numero di pori in cui essa può entrare e quindi minore il percorso che compie attraverso la colonna e più rapida la sua eluizione. Più una molecola è piccola, maggiore il numero di pori in cui entra, più lungo il percorso che compie e maggiore il suo tempo di eluizione. 15
16 Cromatografia su strato sottile (TLC) e su carta La cromatografia su strato sottile (Thin Layer Chromatography TLC) è una tecnica cromatografica di semplice e rapido impiego, utilizzata principalmente come metodologia analitica, per effettuare rapidi test di laboratorio, controllando ad. es. lo svolgimento di una reazione o l efficacia di una separazione. In questa tecnica, la fase stazionaria (gel di silice, allumina, cellulosa) è depositata su una lastrina di vetro sotto forma di strato sottile (circa 1 mm). Nel caso della cromatografia su carta, la fase stazionaria è l acqua adsorbita sulla carta. La TLC è quindi una cromatografia di adsorbimento (solido/liquido) mentre quella su carta è una cromatografia di ripartizione (liquido/liquido). La miscela da separare viene depositata alla base della lastrina, sufficientemente lontano dal bordo, e la lastrina viene successivamente inserita verticalmente in un recipiente che contiene uno strato di eluente alto circa 1 cm; il recipiente viene quindi chiuso per mantenere l'ambiente saturo di vapori di solvente (vedi figura). L eluente tende a salire lungo la lastrina per capillarità, trasportando con sé i vari componenti della miscela e separandoli tra loro in funzione della loro diversa affinità per la fase mobile e la fase stazionaria; prima che il recipiente raggiunga la sommità della lastrina, si pone fine alla separazione estraendo la lastrina del recipiente e lasciando evaporare l eluente. Se le sostanze contenute nel campione sono colorate, a separazione avvenuta è possibile osservarle sulla lastrina come macchie presenti a distanza diversa dalla base. Per l analisi di sostanze incolori, si ricorre all'osservazione sotto luce ultravioletta; in questo caso, la separazione viene effettuata su lastre impregnate di una sostanza fluorescente. Quando la lastrina viene esposta alla radiazione UV, qualsiasi sostanza presente attenuerà la fluorescenza e sarà evidenziata da aloni più scuri. In alternativa si può ricorrere alla reazione con reagenti che sviluppano composti colorati, quali lo iodio e la ninidrina, usata per rivelare gli amminoacidi, evidenziandoli con colori diversi. Per riconoscere con certezza le diverse componenti, a fianco della miscela da separare si possono depositare sulla lastra sostanze note di cui si sospetta l esistenza nella miscela e che servono da riferimento. 16
17 Gascromatografia La gascromatografia (gas-cromatography, GC) è una tecnica usata esclusivamente a scopo analitico che utilizza come fase mobile un gas e può quindi essere utilizzata per analizzare sostanze gassose, ma anche liquide o solide, purché volatili nell intervallo -5 C. Nella GC non vi sono interazioni significative tra le molecole della miscela da analizzare e la fase mobile, essendo questa un gas; i componenti della miscela vengono separati soprattutto in funzione della loro differente volatilità (più un componente è volatile minore sarà il suo tempo di ritenzione) ed, in secondo luogo, in funzione della loro differente affinità per la fase stazionaria (più un componente è affine alla fase stazionaria maggiore sarà il suo tempo di ritenzione). La GC può essere utilizzata per analizzare sostanze gassose, ma anche liquide o solide, purché volatili nell intervallo -5 C. La fase stazionaria utilizzata può essere un solido (cromatografia di adsorbimento) e in tal caso si parla di GSC (gas-solid chromatography) oppure un liquido supportato su di un solido (cromatografia di ripartizione) e in tal caso si parla di GLC (gas-liquid chromatography); può riempire tutto l interno della colonna (colonna impaccata) oppure può essere distribuita come film sottile (circa 1 µm) sulle pareti interne di una colonna estremamente lunga (1 m o più) ed avente un diametro interno inferiore al millimetro (colonna capillare). La fase mobile è un gas inerte (N 2, He, r), detto gas vettore o carrier. In un tipico apparato per la gascromatografia il campione viene immesso tramite l iniettore in testa alla colonna e trasportato attraverso la colonna dal gas vettore. La colonna è inserita in un termostato detto forno che permette di scegliere la temperatura più idonea per una data analisi cromatografica. La scelta della temperatura è molto importante perché al variare della temperatura varia la volatilità dei composti analizzati e quindi variano i loro tempi di ritenzione. Una separazione cromatografica può essere effettuata tenendo la temperatura costante (isoterma) o variandola secondo il gradiente più opportuno. In fondo alla colonna è posto un rivelatore, per monitorare l uscita dalla colonna delle sostanze eluite; il segnale prodotto dal rivelatore viene inviato ad un elaboratore che registra il cromatogramma. 17
TECNICHE DI BASE PER LA SEPARAZIONE DEI COMPONENTI DI UNA MISCELA
 TECNICHE DI BASE PER LA SEPARAZIONE DEI COMPONENTI DI UNA MISCELA CENTRIFUGAZIONE La centrifugazione è un processo che permette di separare una fase solida immiscibile da una fase liquida o due liquidi
TECNICHE DI BASE PER LA SEPARAZIONE DEI COMPONENTI DI UNA MISCELA CENTRIFUGAZIONE La centrifugazione è un processo che permette di separare una fase solida immiscibile da una fase liquida o due liquidi
Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta)
 Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta) E il termine generico che indica una serie di tecniche di separazione di molecole simili in
Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta) E il termine generico che indica una serie di tecniche di separazione di molecole simili in
miscela di reazione miscela di reazione
 Alla fine della reazione: miscela di reazione 1.Si tratta con acqua o acqua e ghiaccio 2.Si aggiunge un solvente organico immiscibile e si agita Si lava (estrae) con una base Si lava (estrae) con un acido
Alla fine della reazione: miscela di reazione 1.Si tratta con acqua o acqua e ghiaccio 2.Si aggiunge un solvente organico immiscibile e si agita Si lava (estrae) con una base Si lava (estrae) con un acido
DAI MISCUGLI ALLE SOSTANZE PURE
 Come si presenta la materia? DAI MISCUGLI ALLE SOSTANZE PURE Il criterio per distinguere i materiali è la presenza di una o più FASI porzioni di materia fisicamente distinte tra loro delimitate da nette
Come si presenta la materia? DAI MISCUGLI ALLE SOSTANZE PURE Il criterio per distinguere i materiali è la presenza di una o più FASI porzioni di materia fisicamente distinte tra loro delimitate da nette
Cromatografia. Foto inedite, cortesia A. Zlatich
 Cromatografia L'invenzione della cromatografia viene attribuita al biochimico russo Mihail Cvet nel 1906, quando riuscì, con questa tecnica, a separare i costituenti da un estratto vegetale. Cvet procedette
Cromatografia L'invenzione della cromatografia viene attribuita al biochimico russo Mihail Cvet nel 1906, quando riuscì, con questa tecnica, a separare i costituenti da un estratto vegetale. Cvet procedette
MODULO 3 - LA MATERIA: COMPOSIZIONE E TRASFORMAZIONI
 MODULO 3 - LA MATERIA: COMPOSIZIONE E TRASFORMAZIONI La materia è tutto ciò che ha una massa, energia e occupa spazio, cioè ha un volume; essa si classifica in base alla sua composizione chimica ed in
MODULO 3 - LA MATERIA: COMPOSIZIONE E TRASFORMAZIONI La materia è tutto ciò che ha una massa, energia e occupa spazio, cioè ha un volume; essa si classifica in base alla sua composizione chimica ed in
POLARITA DI UNA SOSTANZA
 POLARITA DI UNA SOSTANZA Legame intramolecolare: Forze dipolo istantaneo-dipolo istantaneo Forze dipolo-dipolo indotto Forze dipolo-dipolo Legame idrogeno Una sostanza o un solvente è tanto più polare
POLARITA DI UNA SOSTANZA Legame intramolecolare: Forze dipolo istantaneo-dipolo istantaneo Forze dipolo-dipolo indotto Forze dipolo-dipolo Legame idrogeno Una sostanza o un solvente è tanto più polare
Sistemi di separazione di miscele omogenee
 Sistemi di separazione di miscele omogenee Sistemi di separazione di miscele omogenee I sistemi di separazione delle miscele omogenee riguardano la separazione di un soluto da un solvente (come nel caso
Sistemi di separazione di miscele omogenee Sistemi di separazione di miscele omogenee I sistemi di separazione delle miscele omogenee riguardano la separazione di un soluto da un solvente (come nel caso
Cromatografia. Separazione dei componenti di una miscela di Inchiostri con un unico solvente
 CROMATOGRAFIA INCHIOSTRI DIVERSI con UNICO SOLVENTE INCHIOSTRO con SOLVENTI DIVERSI ESTRATTI VEGETALI Cromatografia La cromatografia (letteralmente "scrittura con il colore") è una tecnica di separazione
CROMATOGRAFIA INCHIOSTRI DIVERSI con UNICO SOLVENTE INCHIOSTRO con SOLVENTI DIVERSI ESTRATTI VEGETALI Cromatografia La cromatografia (letteralmente "scrittura con il colore") è una tecnica di separazione
MISCUGLI E TECNICHE DI SEPARAZIONE
 MISCUGLI E TECNICHE DI SEPARAZIONE Classe 1^A Grafico Questo documento è solo una presentazione e non deve ritenersi completo se non è accompagnato dalla lezione in classe. Prof. Zarini Marta CLASSIFICAZIONE
MISCUGLI E TECNICHE DI SEPARAZIONE Classe 1^A Grafico Questo documento è solo una presentazione e non deve ritenersi completo se non è accompagnato dalla lezione in classe. Prof. Zarini Marta CLASSIFICAZIONE
SISTEMA BINARIO DI DUE LIQUIDI VOLATILI TOTALMENTE MISCIBILI che seguono Raoult
 SISTEM INRIO DI DUE IQUIDI OTII MENTE MISCIII che seguono Raoult Consideriamo due liquidi e totalmente miscibili di composizione χ e χ presenti in un contenitore ad una certa temperatura T=T 1. o strato
SISTEM INRIO DI DUE IQUIDI OTII MENTE MISCIII che seguono Raoult Consideriamo due liquidi e totalmente miscibili di composizione χ e χ presenti in un contenitore ad una certa temperatura T=T 1. o strato
Campionamento ed analisi di composti volatili in matrici alimentari
 Campionamento ed analisi di composti volatili in matrici alimentari Lo studio dei composti volatili di un alimento ha l obiettivo di fornirne la caratterizzazione del profilo aromatico, permettendo in
Campionamento ed analisi di composti volatili in matrici alimentari Lo studio dei composti volatili di un alimento ha l obiettivo di fornirne la caratterizzazione del profilo aromatico, permettendo in
Laura Beata Classe 4 B Concorso Sperimento Anch io Silvia Valesano Classe 4 B
 Laura Beata Classe 4 B Concorso Sperimento Anch io Silvia Valesano Classe 4 B RELAZINI DI LABRATRI (Italiano) Titolo: : Cosa mangiamo veramente? Scopo: 1. Scoprire in quali alimenti ci sono o non ci sono
Laura Beata Classe 4 B Concorso Sperimento Anch io Silvia Valesano Classe 4 B RELAZINI DI LABRATRI (Italiano) Titolo: : Cosa mangiamo veramente? Scopo: 1. Scoprire in quali alimenti ci sono o non ci sono
A cura di Elisa, Alessandro e Riccardo 5ACH. IS Fermi Mantova Progetto Scuola 21 AS 2012-2013
 A cura di Elisa, Alessandro e Riccardo 5ACH IS Fermi Mantova Progetto Scuola 21 AS 2012-2013 Cromatografia??? La cromatografia è un metodo chimico-fisico che sfrutta la tendenza delle sostanze a distribuirsi
A cura di Elisa, Alessandro e Riccardo 5ACH IS Fermi Mantova Progetto Scuola 21 AS 2012-2013 Cromatografia??? La cromatografia è un metodo chimico-fisico che sfrutta la tendenza delle sostanze a distribuirsi
Strategie di purificazione di proteine
 Laurea Magistrale in Scienze e Biotecnologie degli Alimenti Strategie di purificazione di proteine Lezione n.xx-2-23 PRINCIPIO - ALIMENTI DA MATRICI SOLIDE E LIQUIDE MATRICI SOLIDE - ROMPERE LA STRUTTURA
Laurea Magistrale in Scienze e Biotecnologie degli Alimenti Strategie di purificazione di proteine Lezione n.xx-2-23 PRINCIPIO - ALIMENTI DA MATRICI SOLIDE E LIQUIDE MATRICI SOLIDE - ROMPERE LA STRUTTURA
MATERIA: tutto ciò che ha una MASSA, occupa un VOLUME e ha ENERGIA
 La materia La materia MATERIA: tutto ciò che ha una MASSA, occupa un VOLUME e ha ENERGIA Il mondo che ci circonda è costituito da materia. La chimica studia le proprietà della materia e i suoi cambiamenti.
La materia La materia MATERIA: tutto ciò che ha una MASSA, occupa un VOLUME e ha ENERGIA Il mondo che ci circonda è costituito da materia. La chimica studia le proprietà della materia e i suoi cambiamenti.
1 a e 2 esperienza di laboratorio: SEPARAZIONE DI UNA MISCELA A TRE COMPONENTI PER ESTRAZIONE
 1 a e 2 esperienza di laboratorio: SEPARAZIONE DI UNA MISCELA A TRE COMPONENTI PER ESTRAZIONE 2014/2015 1 Prima di iniziare ESTRAZIONE: Tecnica utilizzata per separare il prodotto organico desiderato da
1 a e 2 esperienza di laboratorio: SEPARAZIONE DI UNA MISCELA A TRE COMPONENTI PER ESTRAZIONE 2014/2015 1 Prima di iniziare ESTRAZIONE: Tecnica utilizzata per separare il prodotto organico desiderato da
Sistema di filtrazione abbinato ad una pompa del vuoto. Sistema semplice per la filtrazione
 Filtrazione: definizioni La FILTRAZIONE è un comune metodo di separazione basato sul seguente principio: le particelle più piccole di una determinata dimensione passano attraverso i pori di un filtro,
Filtrazione: definizioni La FILTRAZIONE è un comune metodo di separazione basato sul seguente principio: le particelle più piccole di una determinata dimensione passano attraverso i pori di un filtro,
Acidi e basi. HCl H + + Cl - (acido cloridrico) NaOH Na + + OH - (idrossido di sodio; soda caustica)
 Acidi e basi Per capire che cosa sono un acido e una base dal punto di vista chimico, bisogna riferirsi ad alcune proprietà chimiche dell'acqua. L'acqua, sia solida (ghiaccio), liquida o gassosa (vapore
Acidi e basi Per capire che cosa sono un acido e una base dal punto di vista chimico, bisogna riferirsi ad alcune proprietà chimiche dell'acqua. L'acqua, sia solida (ghiaccio), liquida o gassosa (vapore
Termodinamica: legge zero e temperatura
 Termodinamica: legge zero e temperatura Affrontiamo ora lo studio della termodinamica che prende in esame l analisi dell energia termica dei sistemi e di come tale energia possa essere scambiata, assorbita
Termodinamica: legge zero e temperatura Affrontiamo ora lo studio della termodinamica che prende in esame l analisi dell energia termica dei sistemi e di come tale energia possa essere scambiata, assorbita
REAZIONI ORGANICHE Variazioni di energia e velocità di reazione
 REAZIONI ORGANICHE Variazioni di energia e velocità di reazione Abbiamo visto che i composti organici e le loro reazioni possono essere suddivisi in categorie omogenee. Per ottenere la massima razionalizzazione
REAZIONI ORGANICHE Variazioni di energia e velocità di reazione Abbiamo visto che i composti organici e le loro reazioni possono essere suddivisi in categorie omogenee. Per ottenere la massima razionalizzazione
STATO LIQUIDO. Si definisce tensione superficiale (γ) il lavoro che bisogna fare per aumentare di 1 cm 2 la superficie del liquido.
 STTO LIQUIDO Una sostanza liquida è formata da particelle in continuo movimento casuale, come in un gas, tuttavia le particelle restano a contatto le une alle altre e risentono sempre delle notevoli forze
STTO LIQUIDO Una sostanza liquida è formata da particelle in continuo movimento casuale, come in un gas, tuttavia le particelle restano a contatto le une alle altre e risentono sempre delle notevoli forze
Università degli Studi di Catania Dipartimento di Metodologie Fisiche e Chimiche per l Ingegneria
 Università degli Studi di Catania Dipartimento di Metodologie Fisiche e Chimiche per l Ingegneria Corso di laurea in Ingegneria Meccanica Corso di Tecnologie di Chimica Applicata LA CORROSIONE Nei terreni
Università degli Studi di Catania Dipartimento di Metodologie Fisiche e Chimiche per l Ingegneria Corso di laurea in Ingegneria Meccanica Corso di Tecnologie di Chimica Applicata LA CORROSIONE Nei terreni
IL RISPARMIO ENERGETICO E GLI AZIONAMENTI A VELOCITA VARIABILE L utilizzo dell inverter negli impianti frigoriferi.
 IL RISPARMIO ENERGETICO E GLI AZIONAMENTI A VELOCITA VARIABILE L utilizzo dell inverter negli impianti frigoriferi. Negli ultimi anni, il concetto di risparmio energetico sta diventando di fondamentale
IL RISPARMIO ENERGETICO E GLI AZIONAMENTI A VELOCITA VARIABILE L utilizzo dell inverter negli impianti frigoriferi. Negli ultimi anni, il concetto di risparmio energetico sta diventando di fondamentale
Una soluzione è un sistema omogeneo (cioè costituito da una sola fase, che può essere liquida, solida o gassosa) a due o più componenti.
 Una soluzione è un sistema omogeneo (cioè costituito da una sola fase, che può essere liquida, solida o gassosa) a due o più componenti. Solvente (componente presente in maggior quantità) SOLUZIONE Soluti
Una soluzione è un sistema omogeneo (cioè costituito da una sola fase, che può essere liquida, solida o gassosa) a due o più componenti. Solvente (componente presente in maggior quantità) SOLUZIONE Soluti
INTERVENTO DI CLAUDIA RICCARDI PLASMAPROMETEO - Dipartimento di Fisica Università degli Studi di Milano - Bicocca
 INTERVENTO DI CLAUDIA RICCARDI PLASMAPROMETEO - Dipartimento di Fisica Università degli Studi di Milano - Bicocca La ricerca come strumento per lo sviluppo aziendale: sinergia tra università e industria
INTERVENTO DI CLAUDIA RICCARDI PLASMAPROMETEO - Dipartimento di Fisica Università degli Studi di Milano - Bicocca La ricerca come strumento per lo sviluppo aziendale: sinergia tra università e industria
Idrogeologia. Velocità media v (m/s): nel moto permanente è inversamente proporzionale alla superficie della sezione. V = Q [m 3 /s] / A [m 2 ]
![Idrogeologia. Velocità media v (m/s): nel moto permanente è inversamente proporzionale alla superficie della sezione. V = Q [m 3 /s] / A [m 2 ] Idrogeologia. Velocità media v (m/s): nel moto permanente è inversamente proporzionale alla superficie della sezione. V = Q [m 3 /s] / A [m 2 ]](/thumbs/33/15874186.jpg) Idrogeologia Oltre alle proprietà indici del terreno che servono a classificarlo e che costituiscono le basi per utilizzare con facilità l esperienza raccolta nei vari problemi geotecnici, è necessario
Idrogeologia Oltre alle proprietà indici del terreno che servono a classificarlo e che costituiscono le basi per utilizzare con facilità l esperienza raccolta nei vari problemi geotecnici, è necessario
Filtrazione semplice con imbuto.
 Filtrazione semplice con imbuto. Se si dispone di carta da filtro in fogli quadrati di 60 cm di lato, occorre tagliarli in 16 parti. Prendere una quadrato di carta da filtro di 15 cm di lato e piegarlo
Filtrazione semplice con imbuto. Se si dispone di carta da filtro in fogli quadrati di 60 cm di lato, occorre tagliarli in 16 parti. Prendere una quadrato di carta da filtro di 15 cm di lato e piegarlo
Temperatura e Calore
 Temperatura e Calore 1 Temperatura e Calore Stati di Aggregazione Temperatura Scale Termometriche Dilatazione Termica Il Calore L Equilibrio Termico La Propagazione del Calore I Passaggi di Stato 2 Gli
Temperatura e Calore 1 Temperatura e Calore Stati di Aggregazione Temperatura Scale Termometriche Dilatazione Termica Il Calore L Equilibrio Termico La Propagazione del Calore I Passaggi di Stato 2 Gli
4029 Sintesi del dodecil fenil etere da bromododecano e fenolo
 4029 Sintesi del dodecil fenil etere da bromododecano e fenolo OH C 12 H 25 Br (249.2) Br + NaOH (40.0) Adogen 464 C 25 H 54 ClN (404.2) C 6 H 6 O (94.1) C 18 H 30 O (262.4) O + NaBr (102.9) Classificazione
4029 Sintesi del dodecil fenil etere da bromododecano e fenolo OH C 12 H 25 Br (249.2) Br + NaOH (40.0) Adogen 464 C 25 H 54 ClN (404.2) C 6 H 6 O (94.1) C 18 H 30 O (262.4) O + NaBr (102.9) Classificazione
La base di partenza per la maggior parte dei processi produttivi di materiali ceramici sono le sospensioni. Queste si ottengono dalla miscelazione di
 La base di partenza per la maggior parte dei processi produttivi di materiali ceramici sono le sospensioni. Queste si ottengono dalla miscelazione di un solido (polvere) che diverrà il ceramico, con un
La base di partenza per la maggior parte dei processi produttivi di materiali ceramici sono le sospensioni. Queste si ottengono dalla miscelazione di un solido (polvere) che diverrà il ceramico, con un
Acqua azzurra, acqua chiara. Istituto Comprensivo della Galilla Scuola Media Dessì - Ballao
 Acqua azzurra, acqua chiara Istituto Comprensivo della Galilla Scuola Media Dessì - Ballao Proprietà fisiche Ecosistemi acquatici Origine della vita Ciclo dell acqua Acqua Scoperte Sensazioni Leggi La
Acqua azzurra, acqua chiara Istituto Comprensivo della Galilla Scuola Media Dessì - Ballao Proprietà fisiche Ecosistemi acquatici Origine della vita Ciclo dell acqua Acqua Scoperte Sensazioni Leggi La
AUTODIFFUSIONE Autodiffusione
 DIFFUSIONE ATOMICA La diffusione è un processo importante che influenza il comportamento di un materiale alle alte temperature (creep, trattamenti termici superficiali, tempra chimica del vetro, ricristallizzazione,
DIFFUSIONE ATOMICA La diffusione è un processo importante che influenza il comportamento di un materiale alle alte temperature (creep, trattamenti termici superficiali, tempra chimica del vetro, ricristallizzazione,
Università degli Studi di Milano Corso di Laurea in Chimica Industriale. Laboratorio di Processi e Impianti Industriali Chimici I
 Milano, Marzo 2014 Università degli Studi di Milano Corso di Laurea in Chimica Industriale Laboratorio di Processi e Impianti Industriali Chimici I Determinazione dell equilibrio Liquido-Vapore (condizioni
Milano, Marzo 2014 Università degli Studi di Milano Corso di Laurea in Chimica Industriale Laboratorio di Processi e Impianti Industriali Chimici I Determinazione dell equilibrio Liquido-Vapore (condizioni
Liquidi, Solidi e Forze Intermolecolari
 Liquidi, Solidi e Forze Intermolecolari Distanze tra molecole Stati Fisici (Fase) Comportamento atipico La maggiore differenza tra liquidi e solidi consiste nella libertà di movimento delle loro molecole
Liquidi, Solidi e Forze Intermolecolari Distanze tra molecole Stati Fisici (Fase) Comportamento atipico La maggiore differenza tra liquidi e solidi consiste nella libertà di movimento delle loro molecole
CROMATOGRAFIA E GASCROMATOGRAFIA (lezione 3 e lezione 4)
 CROMATOGRAFIA E GASCROMATOGRAFIA (lezione 3 e lezione 4) Il nome cromatografia significa segno colorato e tale nome venne usato poiché le prime analisi venivano eseguite con sostanze pigmentate. Tale tecnica
CROMATOGRAFIA E GASCROMATOGRAFIA (lezione 3 e lezione 4) Il nome cromatografia significa segno colorato e tale nome venne usato poiché le prime analisi venivano eseguite con sostanze pigmentate. Tale tecnica
CAFFE` Il segreto è nel fisico
 CAFFE` Il segreto è nel fisico Preparata la macchina del caffè, e messala sul fuoco: L acqua raggiunge rapidamente la temperatura di ebollizione (100 C). Lo spazio del serbatoio lasciato libero viene occupato
CAFFE` Il segreto è nel fisico Preparata la macchina del caffè, e messala sul fuoco: L acqua raggiunge rapidamente la temperatura di ebollizione (100 C). Lo spazio del serbatoio lasciato libero viene occupato
Estrazione del DNA. 1. Introduzione
 Estrazione del DNA 1. Introduzione L obiettivo di questa esperienza è quello di osservare la molecola degli acidi nucleici, una volta separata dall involucro cellulare in cui è contenuta all interno della
Estrazione del DNA 1. Introduzione L obiettivo di questa esperienza è quello di osservare la molecola degli acidi nucleici, una volta separata dall involucro cellulare in cui è contenuta all interno della
La combustione. Docente: prof.ssa Lobello Carmela
 La combustione Percorso didattico realizzato dalla classe II D Istituto d Istruzione secondaria di I grado S Francesco d Assisi Francavilla Fontana (Br) Docente: prof.ssa Lobello Carmela Perché la combustione?
La combustione Percorso didattico realizzato dalla classe II D Istituto d Istruzione secondaria di I grado S Francesco d Assisi Francavilla Fontana (Br) Docente: prof.ssa Lobello Carmela Perché la combustione?
CHIMICA. Una teoria è scientifica solo se è falsificabile (cioè se è possibile sperimentalmente smentire le sue previsioni)
 CHIMICA SCIENZA SPERIMENTALE: cioè si basa sul metodo sperimentale (Galileo è il precursore). Osservazione dei fenomeni (raccolta e interpretazioni dati) Formulazione ipotesi Verifica sperimentale (eventualmente
CHIMICA SCIENZA SPERIMENTALE: cioè si basa sul metodo sperimentale (Galileo è il precursore). Osservazione dei fenomeni (raccolta e interpretazioni dati) Formulazione ipotesi Verifica sperimentale (eventualmente
GLI STATI DI AGGREGAZIONE DELLA MATERIA. Lo stato gassoso
 GLI STATI DI AGGREGAZIONE DELLA MATERIA Lo stato gassoso Classificazione della materia MATERIA Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (volume e forma propri) LIQUIDO
GLI STATI DI AGGREGAZIONE DELLA MATERIA Lo stato gassoso Classificazione della materia MATERIA Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (volume e forma propri) LIQUIDO
TERMOMETRIA E PROCESSI TERMICI
 TERMOMETRIA E PROCESSI TERMICI SISTEMA parte di materia e/o spazio, idealmente isolata, su cui si concentra ntra l attenzione dell osservatore AMBIENTE ESTERNO tutto ciò che sta al di fuori, ma pur sempre
TERMOMETRIA E PROCESSI TERMICI SISTEMA parte di materia e/o spazio, idealmente isolata, su cui si concentra ntra l attenzione dell osservatore AMBIENTE ESTERNO tutto ciò che sta al di fuori, ma pur sempre
LA MACCHINA FRIGORIFERA E LA POMPA DI
 asdf LA MACCHINA FRIGORIFERA E LA POMPA DI CALORE 12 March 2012 Il ciclo di Carnot... "al contrario" Nell'articolo dedicato alla macchina termica, avevamo visto nel finale la macchina di Carnot e il ciclo
asdf LA MACCHINA FRIGORIFERA E LA POMPA DI CALORE 12 March 2012 Il ciclo di Carnot... "al contrario" Nell'articolo dedicato alla macchina termica, avevamo visto nel finale la macchina di Carnot e il ciclo
352&(662',&20%867,21(
 352&(662',&20%867,21( Il calore utilizzato come fonte energetica convertibile in lavoro nella maggior parte dei casi, è prodotto dalla combustione di sostanze (es. carbone, metano, gasolio) chiamate combustibili.
352&(662',&20%867,21( Il calore utilizzato come fonte energetica convertibile in lavoro nella maggior parte dei casi, è prodotto dalla combustione di sostanze (es. carbone, metano, gasolio) chiamate combustibili.
4001 Trans-esterificazione dell olio di ricino a estere metilico dell acido ricinoleico
 4001 Trans-esterificazione dell olio di ricino a estere metilico dell acido ricinoleico lio di ricino + MeH NaMe H Me CH 4 (32.0) C 19 H 36 3 (312.5) Classificazione Tipo di reazione e classi di sostanze
4001 Trans-esterificazione dell olio di ricino a estere metilico dell acido ricinoleico lio di ricino + MeH NaMe H Me CH 4 (32.0) C 19 H 36 3 (312.5) Classificazione Tipo di reazione e classi di sostanze
Dipendenza della Solubilità dalla temperatura
 SOLUBILIZZAZIONE Simile scioglie il simile: le molecole di sostanze diverse si mescolano intimamente nelle miscele se possiedono forze intermolecolari simili (soluzioni ideali). Anche se le forze intermolecolari
SOLUBILIZZAZIONE Simile scioglie il simile: le molecole di sostanze diverse si mescolano intimamente nelle miscele se possiedono forze intermolecolari simili (soluzioni ideali). Anche se le forze intermolecolari
L H 2 O nelle cellule vegetali e
 L H 2 O nelle cellule vegetali e il suo trasporto nella pianta H 2 O 0.96 Å H O 105 H 2s 2 2p 4 tendenza all ibridizzazione sp 3 H δ+ O δ- δ+ 1.75 Å H legame idrogeno O δ- H H δ+ δ+ energia del legame
L H 2 O nelle cellule vegetali e il suo trasporto nella pianta H 2 O 0.96 Å H O 105 H 2s 2 2p 4 tendenza all ibridizzazione sp 3 H δ+ O δ- δ+ 1.75 Å H legame idrogeno O δ- H H δ+ δ+ energia del legame
Usando il pendolo reversibile di Kater
 Usando il pendolo reversibile di Kater Scopo dell esperienza è la misurazione dell accelerazione di gravità g attraverso il periodo di oscillazione di un pendolo reversibile L accelerazione di gravità
Usando il pendolo reversibile di Kater Scopo dell esperienza è la misurazione dell accelerazione di gravità g attraverso il periodo di oscillazione di un pendolo reversibile L accelerazione di gravità
Università di Pisa Facoltà di Ingegneria. Leghe non ferrose. Chimica Applicata. Prof. Cristiano Nicolella
 Università di Pisa Facoltà di Ingegneria Leghe non ferrose Chimica Applicata Prof. Cristiano Nicolella Leghe non ferrose Minerali di alluminio L alluminio è uno degli elementi più abbondanti sulla crosta
Università di Pisa Facoltà di Ingegneria Leghe non ferrose Chimica Applicata Prof. Cristiano Nicolella Leghe non ferrose Minerali di alluminio L alluminio è uno degli elementi più abbondanti sulla crosta
Piano Lauree Scientifiche 2010 2012 Area Chimica Università di Bologna Facoltà di Chimica Industriale. Laboratori didattici dei Corsi di Laurea
 Chimica Industriale Bologna Faenza Rimini BOLOGNA La Chimica nella vita di tutti i giorni è scienza per il futuro Dr. ELENA STROCCHI elena.strocchi@unibo.it Tel. 051 2093645 FAENZA La Chimica e i Materiali:
Chimica Industriale Bologna Faenza Rimini BOLOGNA La Chimica nella vita di tutti i giorni è scienza per il futuro Dr. ELENA STROCCHI elena.strocchi@unibo.it Tel. 051 2093645 FAENZA La Chimica e i Materiali:
Campione sciolto in un solvente (deuterato) e. posto in un tubo. di vetro a pareti sottili di diametro di 5 mm e lungo circa 20 cm
 posto in un tubo Campione sciolto in un solvente (deuterato) e di vetro a pareti sottili di diametro di 5 mm e lungo circa 20 cm o spettrometro NMR è formato da alcuni mponenti fondamentali: un magnete,
posto in un tubo Campione sciolto in un solvente (deuterato) e di vetro a pareti sottili di diametro di 5 mm e lungo circa 20 cm o spettrometro NMR è formato da alcuni mponenti fondamentali: un magnete,
Introduzione all analisi dei segnali digitali.
 Introduzione all analisi dei segnali digitali. Lezioni per il corso di Laboratorio di Fisica IV Isidoro Ferrante A.A. 2001/2002 1 Segnali analogici Si dice segnale la variazione di una qualsiasi grandezza
Introduzione all analisi dei segnali digitali. Lezioni per il corso di Laboratorio di Fisica IV Isidoro Ferrante A.A. 2001/2002 1 Segnali analogici Si dice segnale la variazione di una qualsiasi grandezza
4.2 CROMATOGRAFIA SU STRATO SOTTILE (TLC)
 1 4.2 CROMATOGRAFIA SU STRATO SOTTILE (TLC) In questa tecnica cromatografica, la fase stazionaria è costituita da materiali diversi (solidi attivi, liquidi supportati su particelle solide inerti, cellulose
1 4.2 CROMATOGRAFIA SU STRATO SOTTILE (TLC) In questa tecnica cromatografica, la fase stazionaria è costituita da materiali diversi (solidi attivi, liquidi supportati su particelle solide inerti, cellulose
TAVOLA DI PROGRAMMAZIONE PER GRUPPI DIDATTICI
 TAVOLA DI PROGRAMMAZIONE PER GRUPPI DIDATTICI MATERIA: CHIMICA CLASSI: PRIME I II QUADRIMESTRE Competenze Abilità/Capacità Conoscenze* Attività didattica Strumenti Tipologia verifiche Osservare, descrivere
TAVOLA DI PROGRAMMAZIONE PER GRUPPI DIDATTICI MATERIA: CHIMICA CLASSI: PRIME I II QUADRIMESTRE Competenze Abilità/Capacità Conoscenze* Attività didattica Strumenti Tipologia verifiche Osservare, descrivere
APPUNTI DI MATEMATICA LE FRAZIONI ALGEBRICHE ALESSANDRO BOCCONI
 APPUNTI DI MATEMATICA LE FRAZIONI ALGEBRICHE ALESSANDRO BOCCONI Indice 1 Le frazioni algebriche 1.1 Il minimo comune multiplo e il Massimo Comun Divisore fra polinomi........ 1. Le frazioni algebriche....................................
APPUNTI DI MATEMATICA LE FRAZIONI ALGEBRICHE ALESSANDRO BOCCONI Indice 1 Le frazioni algebriche 1.1 Il minimo comune multiplo e il Massimo Comun Divisore fra polinomi........ 1. Le frazioni algebriche....................................
LABORATORIO DI CHIMICA GENERALE E INORGANICA
 UNIVERSITA DEGLI STUDI DI MILANO Facoltà di Scienze Matematiche, Fisiche e Naturali Corso di Laurea Triennale in Chimica CORSO DI: LABORATORIO DI CHIMICA GENERALE E INORGANICA Docente: Dr. Alessandro Caselli
UNIVERSITA DEGLI STUDI DI MILANO Facoltà di Scienze Matematiche, Fisiche e Naturali Corso di Laurea Triennale in Chimica CORSO DI: LABORATORIO DI CHIMICA GENERALE E INORGANICA Docente: Dr. Alessandro Caselli
Cromatografia liquida ad alta performance (HPLC)
 Cromatografia liquida ad alta performance (HPLC) La cromatografia in fase liquida viene utilizzata per la separazione di miscele complesse di molecole e/o biomolecole. Riducendo il diametro delle particelle
Cromatografia liquida ad alta performance (HPLC) La cromatografia in fase liquida viene utilizzata per la separazione di miscele complesse di molecole e/o biomolecole. Riducendo il diametro delle particelle
La candela accesa. Descrizione generale. Obiettivi. Sequenza didattica e metodo di lavoro. Esperimenti sulla crescita delle piante
 Esperimenti sulla crescita delle piante unità didattica 1 La candela accesa Durata 60 minuti Materiali per ciascun gruppo - 1 candela - 1 vaso di vetro - 1 cronometro - 1 cannuccia - fiammiferi - 1 pezzo
Esperimenti sulla crescita delle piante unità didattica 1 La candela accesa Durata 60 minuti Materiali per ciascun gruppo - 1 candela - 1 vaso di vetro - 1 cronometro - 1 cannuccia - fiammiferi - 1 pezzo
Tecnologie chimiche industriali
 Tecnologie chimiche industriali INDICAZIONI PER LA PROVA GRAFICA DI TECNOLOGIE CHIMICHE INDUSTRIALI Leggiamo attentamente la traccia e domandiamoci: 1. Quali sono i materiali di processo; 2. In quale stato
Tecnologie chimiche industriali INDICAZIONI PER LA PROVA GRAFICA DI TECNOLOGIE CHIMICHE INDUSTRIALI Leggiamo attentamente la traccia e domandiamoci: 1. Quali sono i materiali di processo; 2. In quale stato
Termologia. Introduzione Scale Termometriche Espansione termica Capacità termica e calori specifici Cambiamenti di fase e calori latenti
 Termologia Introduzione Scale Termometriche Espansione termica Capacità termica e calori specifici Cambiamenti di fase e calori latenti Trasmissione del calore Legge di Wien Legge di Stefan-Boltzmann Gas
Termologia Introduzione Scale Termometriche Espansione termica Capacità termica e calori specifici Cambiamenti di fase e calori latenti Trasmissione del calore Legge di Wien Legge di Stefan-Boltzmann Gas
Capitolo 7. Le soluzioni
 Capitolo 7 Le soluzioni Come visto prima, mescolando tra loro sostanze pure esse danno origine a miscele di sostanze o semplicemente miscele. Una miscela può essere omogenea ( detta anche soluzione) o
Capitolo 7 Le soluzioni Come visto prima, mescolando tra loro sostanze pure esse danno origine a miscele di sostanze o semplicemente miscele. Una miscela può essere omogenea ( detta anche soluzione) o
ATTREZZATURA DI LABORATORIO
 ATTREZZATURA DI LABORATORIO IN GENERALE RICORDIAMO CHE 1) il vetro pyrex non reagisce chimicamente con altre sostanze tranne che con l acido fluoridrico se riscaldato non si spacca 2) gli strumenti in
ATTREZZATURA DI LABORATORIO IN GENERALE RICORDIAMO CHE 1) il vetro pyrex non reagisce chimicamente con altre sostanze tranne che con l acido fluoridrico se riscaldato non si spacca 2) gli strumenti in
Un po di statistica. Christian Ferrari. Laboratorio di Matematica
 Un po di statistica Christian Ferrari Laboratorio di Matematica 1 Introduzione La statistica è una parte della matematica applicata che si occupa della raccolta, dell analisi e dell interpretazione di
Un po di statistica Christian Ferrari Laboratorio di Matematica 1 Introduzione La statistica è una parte della matematica applicata che si occupa della raccolta, dell analisi e dell interpretazione di
Automazione Industriale (scheduling+mms) scheduling+mms. adacher@dia.uniroma3.it
 Automazione Industriale (scheduling+mms) scheduling+mms adacher@dia.uniroma3.it Introduzione Sistemi e Modelli Lo studio e l analisi di sistemi tramite una rappresentazione astratta o una sua formalizzazione
Automazione Industriale (scheduling+mms) scheduling+mms adacher@dia.uniroma3.it Introduzione Sistemi e Modelli Lo studio e l analisi di sistemi tramite una rappresentazione astratta o una sua formalizzazione
Corso di Metodologie Chimiche Dr. ssa Brigida D Abrosca
 Corso di Metodologie Chimiche Dr. ssa Brigida D Abrosca Separazione dei tensioattivi e riconoscimento della classe di appartenenza I formulati di uso domestico a base di tensioattivi sono numerosi almeno
Corso di Metodologie Chimiche Dr. ssa Brigida D Abrosca Separazione dei tensioattivi e riconoscimento della classe di appartenenza I formulati di uso domestico a base di tensioattivi sono numerosi almeno
LA CORRENTE ELETTRICA
 L CORRENTE ELETTRIC H P h Prima che si raggiunga l equilibrio c è un intervallo di tempo dove il livello del fluido non è uguale. Il verso del movimento del fluido va dal vaso a livello maggiore () verso
L CORRENTE ELETTRIC H P h Prima che si raggiunga l equilibrio c è un intervallo di tempo dove il livello del fluido non è uguale. Il verso del movimento del fluido va dal vaso a livello maggiore () verso
Energia nelle reazioni chimiche. Lezioni d'autore di Giorgio Benedetti
 Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
Logica Numerica Approfondimento 1. Minimo Comune Multiplo e Massimo Comun Divisore. Il concetto di multiplo e di divisore. Il Minimo Comune Multiplo
 Logica Numerica Approfondimento E. Barbuto Minimo Comune Multiplo e Massimo Comun Divisore Il concetto di multiplo e di divisore Considerato un numero intero n, se esso viene moltiplicato per un numero
Logica Numerica Approfondimento E. Barbuto Minimo Comune Multiplo e Massimo Comun Divisore Il concetto di multiplo e di divisore Considerato un numero intero n, se esso viene moltiplicato per un numero
Termodinamica. Sistema termodinamico. Piano di Clapeyron. Sistema termodinamico. Esempio. Cosa è la termodinamica? TERMODINAMICA
 Termodinamica TERMODINAMICA Cosa è la termodinamica? La termodinamica studia la conversione del calore in lavoro meccanico Prof Crosetto Silvio 2 Prof Crosetto Silvio Il motore dell automobile trasforma
Termodinamica TERMODINAMICA Cosa è la termodinamica? La termodinamica studia la conversione del calore in lavoro meccanico Prof Crosetto Silvio 2 Prof Crosetto Silvio Il motore dell automobile trasforma
lo 2 2-1 - PERSONALIZZARE LA FINESTRA DI WORD 2000
 Capittol lo 2 Visualizzazione 2-1 - PERSONALIZZARE LA FINESTRA DI WORD 2000 Nel primo capitolo sono state analizzate le diverse componenti della finestra di Word 2000: barra del titolo, barra dei menu,
Capittol lo 2 Visualizzazione 2-1 - PERSONALIZZARE LA FINESTRA DI WORD 2000 Nel primo capitolo sono state analizzate le diverse componenti della finestra di Word 2000: barra del titolo, barra dei menu,
DISTILLAZIONE e ANALISI MERCEOLOGICHE
 DISTILLAZIONE e ANALISI MERCEOLOGICHE ANNA M. DI MARIA Determinazione del grado alcolico del vino (distillazione semplice) pallone di ebollizione da 250 ml tubo adduttore con bolla di sicurezza refrigerante
DISTILLAZIONE e ANALISI MERCEOLOGICHE ANNA M. DI MARIA Determinazione del grado alcolico del vino (distillazione semplice) pallone di ebollizione da 250 ml tubo adduttore con bolla di sicurezza refrigerante
matematica probabilmente
 IS science centre immaginario scientifico Laboratorio dell'immaginario Scientifico - Trieste tel. 040224424 - fax 040224439 - e-mail: lis@lis.trieste.it - www.immaginarioscientifico.it indice Altezze e
IS science centre immaginario scientifico Laboratorio dell'immaginario Scientifico - Trieste tel. 040224424 - fax 040224439 - e-mail: lis@lis.trieste.it - www.immaginarioscientifico.it indice Altezze e
DAF - FLOTTATORI AD ARIA DISCIOLTA
 ECOMACCHINE S.p.A. Via Vandalino 6 10095 Grugliasco (TO) Tel.: +39.0114028611 Fax: +39.0114028627 Email: ecomacchine@ecomacchine.it Web: www.ecomacchine.it DAF - FLOTTATORI AD ARIA DISCIOLTA I distributori
ECOMACCHINE S.p.A. Via Vandalino 6 10095 Grugliasco (TO) Tel.: +39.0114028611 Fax: +39.0114028627 Email: ecomacchine@ecomacchine.it Web: www.ecomacchine.it DAF - FLOTTATORI AD ARIA DISCIOLTA I distributori
LO STATO GASSOSO. Proprietà fisiche dei gas Leggi dei gas Legge dei gas ideali Teoria cinetico-molecolare dei gas Solubilità dei gas nei liquidi
 LO STATO GASSOSO Proprietà fisiche dei gas Leggi dei gas Legge dei gas ideali Teoria cinetico-molecolare dei gas Solubilità dei gas nei liquidi STATO GASSOSO Un sistema gassoso è costituito da molecole
LO STATO GASSOSO Proprietà fisiche dei gas Leggi dei gas Legge dei gas ideali Teoria cinetico-molecolare dei gas Solubilità dei gas nei liquidi STATO GASSOSO Un sistema gassoso è costituito da molecole
LA CORRENTE ELETTRICA CONTINUA
 LA CORRENTE ELETTRICA CONTINUA (Fenomeno, indipendente dal tempo, che si osserva nei corpi conduttori quando le cariche elettriche fluiscono in essi.) Un conduttore metallico è in equilibrio elettrostatico
LA CORRENTE ELETTRICA CONTINUA (Fenomeno, indipendente dal tempo, che si osserva nei corpi conduttori quando le cariche elettriche fluiscono in essi.) Un conduttore metallico è in equilibrio elettrostatico
Elettroforesi. Elettroforesi: processo per cui molecole cariche si separano in un campo elettrico a causa della loro diversa mobilita.
 Elettroforesi Elettroforesi: processo per cui molecole cariche si separano in un campo elettrico a causa della loro diversa mobilita. A qualunque ph diverso dal pi le proteine hanno una carica netta quindi,
Elettroforesi Elettroforesi: processo per cui molecole cariche si separano in un campo elettrico a causa della loro diversa mobilita. A qualunque ph diverso dal pi le proteine hanno una carica netta quindi,
Lavori intelligenti per il risparmio energetico
 Città di San Donà di Piave Assessorato all Ambiente SPORTELLO ENERGIA Lavori intelligenti per il risparmio energetico SOLARE TERMICO Un impianto a collettori solari (anche detto a pannelli solari termici
Città di San Donà di Piave Assessorato all Ambiente SPORTELLO ENERGIA Lavori intelligenti per il risparmio energetico SOLARE TERMICO Un impianto a collettori solari (anche detto a pannelli solari termici
Esercitazione 5 Dinamica del punto materiale
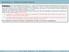 Problema 1 Un corpo puntiforme di massa m = 1.0 kg viene lanciato lungo la superficie di un cuneo avente un inclinazione θ = 40 rispetto all orizzontale e altezza h = 80 cm. Il corpo viene lanciato dal
Problema 1 Un corpo puntiforme di massa m = 1.0 kg viene lanciato lungo la superficie di un cuneo avente un inclinazione θ = 40 rispetto all orizzontale e altezza h = 80 cm. Il corpo viene lanciato dal
METODICHE NEL LABORATORIO CHIMICO-CLINICO
 METODICHE NEL LABORATORIO CHIMICO-CLINICO SPETTROFOTOMETRIA DI ASSORBIMENTO TURBIDIMETRIA/NEFELOMETRIA FLUORIMETRIA SPETTROFOTOMETRIA DI ASSORBIMENTO ATOMICO FOTOMETRIA DI EMISSIONE A FIAMMA RIFLETTANZA
METODICHE NEL LABORATORIO CHIMICO-CLINICO SPETTROFOTOMETRIA DI ASSORBIMENTO TURBIDIMETRIA/NEFELOMETRIA FLUORIMETRIA SPETTROFOTOMETRIA DI ASSORBIMENTO ATOMICO FOTOMETRIA DI EMISSIONE A FIAMMA RIFLETTANZA
Laboratorio in classe: tra forme e numeri Corso organizzato dall USR Lombardia. GRUPPO FRAZIONI SCUOLA SECONDARIA DI I GRADO-CLASSE I a.s.
 Laboratorio in classe: tra forme e numeri Corso organizzato dall USR Lombardia GRUPPO FRAZIONI SCUOLA SECONDARIA DI I GRADO-CLASSE I a.s.009/00 LABORATORIO IN CLASSE TRA FORME E NUMERI - a.s. 009/00 LABORATORIO
Laboratorio in classe: tra forme e numeri Corso organizzato dall USR Lombardia GRUPPO FRAZIONI SCUOLA SECONDARIA DI I GRADO-CLASSE I a.s.009/00 LABORATORIO IN CLASSE TRA FORME E NUMERI - a.s. 009/00 LABORATORIO
IL CALCARE NON SI FORMA PIÙ ED ELIMINA QUELLO ESISTENTE!
 MANUALE TECNICO IL CALCARE NON SI FORMA PIÙ ED ELIMINA QUELLO ESISTENTE! Indice : - Introduzione - Come si forma il calcare? - Processo di nucleazione - Azione dell inibitore sulla formazione del calcare
MANUALE TECNICO IL CALCARE NON SI FORMA PIÙ ED ELIMINA QUELLO ESISTENTE! Indice : - Introduzione - Come si forma il calcare? - Processo di nucleazione - Azione dell inibitore sulla formazione del calcare
Analisi di Controllo di un Acqua Minerale Naturale
 Analisi di Controllo di un Acqua Minerale aturale ITODUZIOE Le acque potabili possono essere in diverse tipologie: si definiscono acque destinate al consumo umano, quelle acque rese potabili dopo aver
Analisi di Controllo di un Acqua Minerale aturale ITODUZIOE Le acque potabili possono essere in diverse tipologie: si definiscono acque destinate al consumo umano, quelle acque rese potabili dopo aver
USO DI EXCEL CLASSE PRIMAI
 USO DI EXCEL CLASSE PRIMAI In queste lezioni impareremo ad usare i fogli di calcolo EXCEL per l elaborazione statistica dei dati, per esempio, di un esperienza di laboratorio. Verrà nel seguito spiegato:
USO DI EXCEL CLASSE PRIMAI In queste lezioni impareremo ad usare i fogli di calcolo EXCEL per l elaborazione statistica dei dati, per esempio, di un esperienza di laboratorio. Verrà nel seguito spiegato:
Appunti sulla Macchina di Turing. Macchina di Turing
 Macchina di Turing Una macchina di Turing è costituita dai seguenti elementi (vedi fig. 1): a) una unità di memoria, detta memoria esterna, consistente in un nastro illimitato in entrambi i sensi e suddiviso
Macchina di Turing Una macchina di Turing è costituita dai seguenti elementi (vedi fig. 1): a) una unità di memoria, detta memoria esterna, consistente in un nastro illimitato in entrambi i sensi e suddiviso
La raffinazione del petrolio
 La raffinazione del petrolio Approfondimento sulla distillazione per la I^ Itis Prof. Maurizi Franco Itis Einstein Roma ( foto ed immagini reperiti da internet, eventuali detentori di diritti sono pregati
La raffinazione del petrolio Approfondimento sulla distillazione per la I^ Itis Prof. Maurizi Franco Itis Einstein Roma ( foto ed immagini reperiti da internet, eventuali detentori di diritti sono pregati
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA
 LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
GC GC/MS. Chiaravalle, 11-12 FEBBRAIO 2010
 GC GC/MS Chiaravalle, 11-12 FEBBRAIO 2010 GAS-CROMATOGRAFO GAS di TRASPORTO (carrier): Gas inerte (azoto,elio..): trasporta componenti della miscela lungo la colonna cromatografica INIETTORE: - Assicura
GC GC/MS Chiaravalle, 11-12 FEBBRAIO 2010 GAS-CROMATOGRAFO GAS di TRASPORTO (carrier): Gas inerte (azoto,elio..): trasporta componenti della miscela lungo la colonna cromatografica INIETTORE: - Assicura
Cos è una. pompa di calore?
 Cos è una pompa di calore? !? La pompa di calore aria/acqua La pompa di calore (PDC) aria-acqua è una macchina in grado di trasferire energia termica (calore) dall aria esterna all acqua dell impianto
Cos è una pompa di calore? !? La pompa di calore aria/acqua La pompa di calore (PDC) aria-acqua è una macchina in grado di trasferire energia termica (calore) dall aria esterna all acqua dell impianto
DISTILLAZIONE: PREMESSE
 DISTILLAZIONE: PREMESSE PROCESSO DI ELEZIONE NELLA PREPARAZIONE DI ACQUA PER PREPARAZIONI INIETTABILI PROCESSO GENERALMENTE APPLICATO COME STADIO FINALE DI PURIFICAZIONE AD UN ACQUA GIA TRATTATA IL TIPO
DISTILLAZIONE: PREMESSE PROCESSO DI ELEZIONE NELLA PREPARAZIONE DI ACQUA PER PREPARAZIONI INIETTABILI PROCESSO GENERALMENTE APPLICATO COME STADIO FINALE DI PURIFICAZIONE AD UN ACQUA GIA TRATTATA IL TIPO
Esperienza A: idrofilicità e idrofobicità
 Esperienza A: idrofilicità e idrofobicità Obiettivo: Fare osservare che alcune sostanze, mescolate all'acqua, danno luogo a soluzioni omogenee mentre altre danno miscele eterogenee. Dalla descrizione delle
Esperienza A: idrofilicità e idrofobicità Obiettivo: Fare osservare che alcune sostanze, mescolate all'acqua, danno luogo a soluzioni omogenee mentre altre danno miscele eterogenee. Dalla descrizione delle
La distribuzione Normale. La distribuzione Normale
 La Distribuzione Normale o Gaussiana è la distribuzione più importante ed utilizzata in tutta la statistica La curva delle frequenze della distribuzione Normale ha una forma caratteristica, simile ad una
La Distribuzione Normale o Gaussiana è la distribuzione più importante ed utilizzata in tutta la statistica La curva delle frequenze della distribuzione Normale ha una forma caratteristica, simile ad una
Genova 15 01 14 TIPOLOGIE DI LAMPADE
 Genova 15 01 14 TIPOLOGIE DI LAMPADE Le lampade a vapori di mercurio sono sicuramente le sorgenti di radiazione UV più utilizzate nella disinfezione delle acque destinate al consumo umano in quanto offrono
Genova 15 01 14 TIPOLOGIE DI LAMPADE Le lampade a vapori di mercurio sono sicuramente le sorgenti di radiazione UV più utilizzate nella disinfezione delle acque destinate al consumo umano in quanto offrono
P.D 4 Acqua come solvente P.D 4A Miscugli e separazione di miscugli Schede esperimenti Scuola secondaria di primo grado
 P.D 4 Acqua come solvente P.D 4A Miscugli e separazione di miscugli Schede esperimenti Scuola secondaria di primo grado ESPERIENZA: LE SOLUZIONI 3 bicchierini di plastica trasparenti sale zucchero Riempiamo
P.D 4 Acqua come solvente P.D 4A Miscugli e separazione di miscugli Schede esperimenti Scuola secondaria di primo grado ESPERIENZA: LE SOLUZIONI 3 bicchierini di plastica trasparenti sale zucchero Riempiamo
Si classifica come una grandezza intensiva
 CAP 13: MISURE DI TEMPERATURA La temperatura È osservata attraverso gli effetti che provoca nelle sostanze e negli oggetti Si classifica come una grandezza intensiva Può essere considerata una stima del
CAP 13: MISURE DI TEMPERATURA La temperatura È osservata attraverso gli effetti che provoca nelle sostanze e negli oggetti Si classifica come una grandezza intensiva Può essere considerata una stima del
Lo spettro IR. Lo spettro IR è un grafico in cui vengono riportate: -Nell Nell asse delle ascisse
 Lo spettro IR Lo spettro IR è un grafico in cui vengono riportate: -Nell Nell asse delle ascisse la frequenza della radiazione IR assorbite espressa in numero d onda (wavenumbers) -In ordinate è riportata
Lo spettro IR Lo spettro IR è un grafico in cui vengono riportate: -Nell Nell asse delle ascisse la frequenza della radiazione IR assorbite espressa in numero d onda (wavenumbers) -In ordinate è riportata
CO 2 aq l anidride carbonica disciolta, reagendo con l'acqua, forma acido carbonico secondo la reazione:
 DUREZZA DELLE ACQUE. Quando si parla di durezza di un acqua ci si riferisce fondamentalmente alla quantità di ioni calcio e di ioni magnesio disciolti in un certo volume di tale acqua. Ad eccezione delle
DUREZZA DELLE ACQUE. Quando si parla di durezza di un acqua ci si riferisce fondamentalmente alla quantità di ioni calcio e di ioni magnesio disciolti in un certo volume di tale acqua. Ad eccezione delle
La percentuale massa/volume (%m/v) indica la quantità di soluto espressa in grammi presente in 100 ml di soluzione.
 La concentrazione delle soluzioni Le soluzioni sono costituite da quantità molto variabili dei loro componenti: se vogliamo fornire una indicazione precisa circa la loro composizione, è importante conoscere
La concentrazione delle soluzioni Le soluzioni sono costituite da quantità molto variabili dei loro componenti: se vogliamo fornire una indicazione precisa circa la loro composizione, è importante conoscere
Circuito di pilotaggio ON OFF con operazionale
 PREMESSA Circuito di pilotaggio ON OFF con operazionale A cura del Prof. Marco Chirizzi www.marcochirizzi.it Si supponga di dovere progettare un circuito di pilotaggio ON OFF in grado di mantenere un fluido
PREMESSA Circuito di pilotaggio ON OFF con operazionale A cura del Prof. Marco Chirizzi www.marcochirizzi.it Si supponga di dovere progettare un circuito di pilotaggio ON OFF in grado di mantenere un fluido
UNIVERSITÀ DEGLI STUDI DI NAPOLI FEDERICO II
 UNIVERSITÀ DEGLI STUDI DI NAPOLI FEDERICO II Scuola Politecnica delle Scienze di Base Dipartimento di Ingegneria Civile, Edile e Ambientale CORSO DI LAUREA MAGISTRALE IN INGEGNERIA PER L AMBIENTE E IL
UNIVERSITÀ DEGLI STUDI DI NAPOLI FEDERICO II Scuola Politecnica delle Scienze di Base Dipartimento di Ingegneria Civile, Edile e Ambientale CORSO DI LAUREA MAGISTRALE IN INGEGNERIA PER L AMBIENTE E IL
4025 Sintesi del 2-iodopropano dal 2-propanolo
 4025 Sintesi del 2-iodopropano dal 2-propanolo OH I + 1/2 I 2 + 1/3 P x + 1/3 P(OH) 3 C 3 H 8 O (60.1) (253.8) (31.0) C 3 H 7 I (170.0) (82.0) Classificazione Tipo di reazione e classi di sostanze Sostituzione
4025 Sintesi del 2-iodopropano dal 2-propanolo OH I + 1/2 I 2 + 1/3 P x + 1/3 P(OH) 3 C 3 H 8 O (60.1) (253.8) (31.0) C 3 H 7 I (170.0) (82.0) Classificazione Tipo di reazione e classi di sostanze Sostituzione
