LA MIOGLOBINA e L EMOGLOBINA
|
|
|
- Cinzia Clemente
- 7 anni fa
- Visualizzazioni
Transcript
1 UNITÀ VET. DIDATTICA DI PROPEDEUTICA BIOCHIMICA LA MIOGLOBINA e L EMOGLOBINA Roberto Giacominelli Stuffler
2 LA MIOGLOBINA E L EMOGLOBINAL I vertebrati hanno selezionato due meccanismi principali per rifornire le loro cellule di ossigeno: 1) il sistema circolatorio 2) le molecole che legano l ossigeno: A) L EMOGLOBINA L (Hb( Hb), B) LA MIOGLOBINA (Mb). 2
3 LA MIOGLOBINA E L EMOGLOBINAL Esse appartengono alla famiglia delle globine, la mioglobina è la proteina di immagazzinamento dell O 2 le specie animali, in tutte l emoglobina emoglobina trasporta l O 2 in tutti i vertebrati ed in alcuni invertebrati; essa rimuove anche la CO 2 dai tessuti. 3
4 LA MIOGLOBINA 4
5 LA STRUTTURA TRIDIMENSIONALE DELLA MIOGLOBINA 5
6 L EMOGLOBINA 6
7 L EMOGLOBINA L emoglobina é una proteina tetramerica, costituita da quattro subunitá, ciascuna delle quali somiglia fortemente alla mioglobina. 7
8 L EMOGLOBINA 8
9 LA MIOGLOBINA E L EMOGLOBINAL Esse devono essere in grado di: 1) legare l O 2, 2) impedire che esso ossidi altre sostanze (che ridurrebbero l O 2 ), 3) rilasciarlo in risposta a specifiche richieste. 9
10 LA MIOGLOBINA E L EMOGLOBINAL Alcuni metalli di transizione, nei loro stati di ossidazione più bassi (es. Fe 2+, Cu + ), hanno la tendenza a legare l ossigeno, l evoluzione ha prodotto una modalità con cui il Fe 2+ (ione ferroso) essere legato alle proteine (Mb e Hb), per creare siti di legame per l O (ione ferroso) può 10
11 LA STRUTTURA TERZIARIA DELLA MIOGLOBINA DI CAPODOGLIO 11
12 LA MIOGLOBINA La struttura della mioglobina e del suo gruppo eme. La mioglobina comprende una parte polipeptidica (globina) ed un gruppo prostetico: il gruppo eme. Il gruppo eme è formato da: una parte organica la protoporfirina IX ed un atomo di ferro. 12
13 IL GRUPPO EME L eme si lega in modo non covalente alla molecola, accomodato in una tasca idrofobica. 13
14 IL GRUPPO EME 14
15 IL GRUPPO EME La protoporfirina IX è formata da 4 anelli pirrolici, legati tra di loro a formare un anello tetrapirrolico, con legati 4 gruppi metilici, 2 gruppi vinilici e 2 gruppi propionici; l atomo di ferro forma 6 legami di coordinazione: i primi 4 con gli atomi di azoto dell anello tetrapirrolico, gli altri 2, addizionali, su ciascun lato del piano dell eme, sono il 5 con l His prossimale (F8), il 6 con l O 2, oppure con altre molecole. 15
16 IL GRUPPO EME DELLA Mb ED Hb 16
17 IL GRUPPO EME L atomo di ferro é di 0.03 nm al di fuori del piano della porfirina, quando la sesta posizione di coordinazione é vuota. 17
18 IL GRUPPO EME É LOCALIZZATO IN UNA CAVITÀ PRESENTE NELLA MOLECOLA DELLA Mb 18
19 IL GRUPPO EME DELLA Mb ED Hb 19
20 I GRUPPI PROPIONICI DELL EME EME SONO ALLA SUPERFICIE DELLA Mb 20
21 LA MIOGLOBINA (4,5 3,5 3,5 2,5nm) Il 75% della catena (globina) é in conformazione ad -elica. Ci sono 8 segmenti elicoidali maggiori (da A ad H) e 5 segmenti non elicoidali (AB, CD, EF, FG, GH) raccordano le varie eliche. 21
22 LE FORME PIÙ IMPORTANTI DELLA MIOGLOBINA Forma Stato di ossidazione del ferro V posizione di coordinazione VI posizione di coordinazione Deossimioglobina 2 + His F8 Vuota Ossimioglobina 2 + His F8 O 2 Ferrimioglobina 3 + His F8 H 2 O Fe Fe 2+ (ione ferroso) Fe3+ (ione ferrico) 22
23 LA DINAMICA DEL RILASCIO DELL OSSIGENO DA PARTE DELLA MIOGLOBINA L ossigeno rilasciato sfugge all esterno, se le fluttuazioni della struttura proteica determinano l apertura di un varco. 23
24 LA MIOGLOBINA Se la Mb (o l Hb) è conservata a contatto con l aria, al di fuori dell ambiente cellulare, il ferro si ossida a formare la metamioglobina (ferrimioglobina) o la metemoglobina, il sito di legame viene inattivato e si lega una molecola d acqua al posto dell O 2. 24
25 LA MIOGLOBINA Un gruppo eme libero lega l O 2 per un periodo molto breve, poiché l O 2 ossida molto rapidamente il Fe 2+ (ione ferroso) a Fe 3+ (ione ferrico), che non é più in grado di legare O 2. In questa reazione si ha l intermedio: eme-o 2 -eme Il gruppo eme presente nella mioglobina è molto meno ossidabile, perché difficilmente due molecole di Mb si potranno avvicinare tanto da permettere la formazione del complesso eme-o 2 -eme. 25
26 LA MIOGLOBINA Quindi, la ragione funzionale dell esistenza della componente proteica della Mb e dell Hb è la protezione del ferro dall ossidazione irreversibile; Mb ed Hb creano ambienti in cui è permesso il primo passaggio di una reazione di ossidazione (il legame dell ossigeno), ma è impedito il passaggio finale (l ossidazione). 26
27 LA MIOGLOBINA Un eme stericamente protetto è essenziale per la funzione biologica della Mb. La vicinanza della valina (E11) e della fenilalanina (CD1) permette che l eme si trovi in una tasca idrofobica stericamente ostruita. Il ferro subisce quindi solo un ossigenazione reversibile e non non una vera e propria ossidazione. 27
28 LA MIOGLOBINA L ossidazione é infatti impossibilitata dall impedimento sterico che presenta l ambiente attorno al complesso ferroporfirinico, l eme libero, invece, può facilmente ossidarsi, perché non esiste in questo caso alcuna protezione sterica. 28
29 I COMPOSTI SINTETICI I fattori sterici sono molto importanti nel complesso ferro-porfirina porfirina, infatti i picchetti (ostacoli) impediscono la formazione del dimero eme-o 2 -eme. 29
30 FORMULA DI STRUTTURA DI UNA FERRO-PORFIRINA CON PICCHETTI DI RECINZIONE Si crea un microambiente che permette l ossigenazione. 30
31 LA TOSSICITA DEL MONOSSIDO DI CARBONIO (CO) La tasca dell eme può accogliere sia l O 2 sia il CO, che ha dimensioni analoghe. Il CO ha un affinità di legame per la Mb (e l Hb) maggiore dell O 2 ed il legame non è facilmente reversibile. Per questo motivo il CO è molto tossico. Nel gruppo eme isolato, l asse dell O 2 presenta un angolo con l asse del legame Fe-O, creando un legame più debole rispetto a quello del CO, in cui gli atomi Fe-C-O sono disposti in modo lineare. 31
32 LA TOSSICITA DEL MONOSSIDO DI CARBONIO (CO) Quando l eme é all interno della tasca della globina, il legame del CO è diminuito dalla presenza dell istidina distale, mentre l O2 si lega allo stesso modo, sia alla Hb, sia alle ferro-porfirine isolate. Questo é un vantaggio per l O2, che é in competizione con il CO per il legame con il ferro. ferro 32
33 LA TOSSICITA DEL MONOSSIDO DI CARBONIO (CO) In conclusione, mentre il gruppo eme isolato forma un legame con il CO volte più forte rispetto a quello con l O 2. Mb e Hb formano un legame con il CO solo 200 volte più forte rispetto a quello con l O 2. In una cellula, il CO blocca l 1% dei siti della Mb ed Hb. 33
34 IL GENE DELLA Mb Il gene della mioglobina è costituito da tre esoni: l esone I codifica gli aminoacidi da 1 a 30, l esone II codifica gli aminoacidi da 31 a 105, l esone III codifica gli aminoacidi da 106 a 153. La minimioglobina, ottenuta con l enzima proteolitico clostripaina, è costituita da 107 aminoacidi (da 32 a 139) ed ha un comportamento simile a quello della mioglobina. 34
35 L EVOLUZIONE DI Mb ED Hb L emoglobina e la mioglobina sono evolute da una stessa proteina ancestrale, probabilmente, un errato appaiamento dei cromosomi omologhi portò alla formazione di un cromosoma contenente i due geni identici, che hanno subito mutazioni ed evoluzioni indipendenti l uno dall altro. 35
36 CONFRONTO TRA Mb ED Hb L Hb ha un organizzazione approssimativamente tetraedrica 36
37 MIOGLOBINA ED EMOGLOBINA 37
38 LE EMOGLOBINE PIU IMPORTANTI Sono stati identificati vari tipi di catene che danno origine ad emoglobine diverse. Hb Gower Hb embrionale Hb Gower Hb Portland 2 2 Hb fetale Hb F 2 2 Ultimi 2-3 mesi della vita fetale Hb adulto Hb A 2 2 Hb A ±2% 38
39 L EMOGLOBINA A (P.M.64500) L emoglobina è una proteina tetramerica, costituita da due subunità e due subunità, ognuna delle quali presenta un gruppo prostetico eme (Fe 2+ ), ed una catena polipeptidica. La globina (la componente proteica) é formata da: 2 catene (141 residui), 2 catene (146 residui). 39
40 LE SEQUENZE AMMINOACIDICHE DELLA MIOGLOBINA DI CAPODOGLIO E DELLE CATENE α E β DELL EMOGLOBINA EMOGLOBINA UMANA La struttura terziaria della Mb e delle 2 subunità α e β della Hb sono molto simili, nonostante solo il 18% dei corrispondenti residui siano identici. 40
41 L AVVOLGIMENTO GLOBINICO (Hb ed Mb) È l intricato ripiegamento della catena polipeptidica, che consente di porre il gruppo eme in un ambiente da permettere il legame reversibile dell ossigeno. 41
42 Esistono due forme di emoglobina: forma T (deossihb( deossihb) ha scarsa affinità per l O 2 forma R (ossihb( ossihb) ha elevata affinità per l O 2 (cooperatività di legame) 42
43 L EMOGLOBINA 43
44 L EMOGLOBINA I residui invarianti sono particolarmente importanti per la funzione dell emoglobina: ecco i principali residui invarianti in più di 60 specie F8 Istidina His prossimale legata all eme E7 Istidina His distale vicina all eme CD1 Fenilalanina Contatti con il gruppo eme F4 Leucina Contatti con il gruppo eme B6 Glicina Permette una stretta vicinanza tra le eliche B ed E C2 Prolina Termine dell elica H2 Tirosina Legami crociati tra le eliche H ed F C4 Treonina Incerto H10 Lisina Incerto 44
45 IL LEGAME DELL OSSIGENO DA PARTE DELLA Mb Nei tessuti (muscolo), la Mb lega l ossigeno l rilasciato dalla Hb presente nel circolo arterioso ed a sua volta lo cede agli organuli cellulari (i mitocondri). Mb + O 2 MbO 2 45
46 LA MIOGLOBINA Il legame di un ligando (O 2 ) ad un sito singolo di una proteina (Mb) può essere descritto da una curva di legame iperbolica. Mb + O 2 MbO 2 46
47 LA CURVA DI LEGAME DELL O 2 ALLA Mb La curva iperbolica è espressa dall equazione: Y = po 2 po 2 +P +P 50 a 100 torr la YO 2 é 0.97 a 20 torr la YO 2 é 0.88 La pressione parziale di O 2 èespressa in torr. L O 2 si lega saldamente alla Mb con una P 50 di soli 2,8 torr. 47
48 SATURAZIONE (Y)( È la frazione di siti occupati dall ossigeno e corrisponde alla percentuale di Mb ossigenata. Il valore di y può variare da 0 a 1. È il termine che esprime la pressione parziale di ossigeno in cui il 50% dei siti sono occupati (y=0,5). Indica l affinità per l ossigeno della Mb. P 50 48
49 TORR È l unità di misura della pressione, equivalente alla pressione esercitata da una colonna di Hg di 1 mm, a 0 C ed a gravità normale. 49
50 IL LEGAME DELL OSSIGENO DA PARTE DELLA Hb 50
51 LE CURVE DI LEGAME RICHIESTE DA UNA PROTEINA DA TRASPORTO 51
52 L EMOGLOBINA L efficienza nel trasporto di ossigeno è ottenuta attraverso il legame cooperativo da parte di proteine dotate di più siti, descritto da una curva di legame sigmoide; nella linea evolutiva che ha portato ai vertebrati, la proteina utilizzata per il trasporto di O 2 é l emoglobina. 52
53 L EMOGLOBINA L Hb è il trasportatore di ossigeno molecolare, una proteina trasportatrice di O 2 ideale dovrebbe essere quasi completamente saturata a 100 mmhg (pressione parziale di O 2 nei polmoni o nelle branchie) e trovarsi quasi totalmente in forma dissociata a circa mmhg (pressione parziale dei tessuti). 53
54 LA CURVA DI SATURAZIONE DELLA Hb CON L OSSIGENO É SIGMOIDE Una curva di legame di tipo sigmoide può essere considerata come una curva ibrida, che riflette la presenza di forme a bassa affinità e ad alta affinità. Per la Hb il valore di P 50 écirca 26 torr, a 100 torr la YO 2 é 0.97, a 20 torr la YO 2 é
55 Le proteine che legano il substrato (ligando) in modo cooperativo danno curve di tipo sigmoide e sono chiamate proteine allosteriche. A basse concentrazioni di [S], la molecola si comporta come se avesse una debole capacità di legame (K 0.5 elevata); all aumentare di [S] viene indotto un aumento della quantità di ligando legato e quindi di efficienza della molecola. Le proprietà cinetiche delle proteine allosteriche non seguono le cinetiche di Michaelis-Menten (che danno le curve di legame iperboliche). 55
56 LE PROTEINE ALLOSTERICHE L emoglobina è una proteina allosterica; il termine allosterico deriva dal greco (állos = altro; stereós = forma). Le proteine così definite possono assumere altre conformazioni indotte dal legame di opportuni modulatori; in una proteina allosterica, il legame di un ligando ad un sito modifica le proprietà di un altro sito sulla stessa molecola, le molecole allosteriche sono proteine oligomeriche, costituite da due o più subunità e con diversi siti attivi, le interazioni allosteriche (cooperative) avvengono quando il legame di un ligando ad un sito specifico viene influenzato dal legame di un altro ligando,, detto effettore o modulatore,, a livello di siti diversi, nella proteina. 56
57 L Hb É UNA PROTEINA ALLOSTERICA Quando più subunità si uniscono, emergono nuove proprietà di fondamentale importanza biologica, l Hb è più complicata e sensibile della Mb, ogni molecola di Hb può legare 4 molecole di O 2, perché sono presenti 4 siti di legame. 57
58 L Hb É UNA PROTEINA ALLOSTERICA Nella Hb esiste una cooperatività di legame, essa è possibile perché lo stato di ossigenazione di un sito può essere comunicato agli altri siti, questo é un esempio di effetto allosterico, dove l occupazione di uno dei siti da parte del ligando (O 2 ) influisce sull affinità di quelli rimasti liberi; le molecole che legano il substrato in modo cooperativo danno curve di tipo sigmoide. 58
59 L Hb É UNA PROTEINA ALLOSTERICA Quando il normale ligando (O 2 nel caso della Hb) di una proteina allosterica è anche un modulatore, l interazione viene detta omotropica, se invece il modulatore è una molecola diversa dal ligando normale, l interazione viene detta eterotropica, questi effetti possono essere sia positivi sia negativi, a seconda che il ligando aumenti o diminuisca l affinità della proteina per il ligando stesso. 59
60 L Hb HA UNA COOPERATIVITA OMOTROPICA POSITIVA La sua cooperatività positiva deriva dalle modificazioni che il legame di un ligando (O 2, effettore omotropico positivo) ad un gruppo eme può indurre sull affinità di legame per il ligando in un altro gruppo eme. 60
61 LA Mb HA UN AFFINIT AFFINITÀ PER L OL 2 MAGGIORE DI QUELLA DELLA Hb Curva iperbolica per la Mb, curva sigmoide per la Hb. La quarta molecola di O 2 si lega all Hb con una affinità 100 volte superiore a quella della prima molecola di O 2 (effetto della globina). 61
62 LE PROPRIETA ALLOSTERICHE DELL EMOGLOBINA EMOGLOBINA 1) Il legame dell O 2 alla Hb favorisce il legame di altro O 2 alla stessa molecola: cooperatività positiva, 2) l affinità della Hb per l O 2 dipende anche dal ph e dalla CO 2, che sono effettori eterotropici negativi, 3) l affinità della Hb per l O 2 é inoltre regolata dal 2,3 bisfosfoglicerato (BPG), uneffettore eterotropico negativo. 62
63 IL COEFFICIENTE DI HILL Il coefficiente di Hill (n) è un parametro correlato al grado di cooperatività tra le subunità di una proteina; in una proteina costituita da subunitá, ognuna in grado di legare una molecola di substrato (ligando), n aumenta con il grado di cooperativitá: se n=1 non c è cooperatività (ramo di iperbole), se n>1 c è cooperatività positiva (curva sigmoide), se n<1 c è cooperatività negativa. 63
64 QUANDO n=1, NON C É COOPERATIVITÀ In questo caso, i siti di legame per l ossigeno sono completamente indipendenti nel loro comportamento, questa situazione é anche di una proteina con un singolo sito di legame (es. la mioglobina). 64
65 QUANDO n>1, C É COOPERATIVITÀ POSITIVA La cooperatività diventa infinita (situazione ipotetica), quando la proteina ha tutti i siti (o nessun sito) di legame per il ligando occupati contemporaneamente, in questo caso, n tende ad essere uguale al n dei siti di legame per il ligande presenti nella proteina e la molecola è completamente cooperativa. 65
66 IL COEFFICIENTE DI HILL Nel caso dell emoglobina n é 2,8. La curva sigmoide dell Hb indica il legame cooperativo dell ossigeno alla proteina, rendendo più efficace il trasporto dell ossigeno. La curva può essere espressa dall equazione: y = (po 2 ) n (po 2 ) n + (P ) n 66
67 LA FUNZIONE DEL COEFFICIENTE DI HILL La saturazione della Hb varia più rapidamente in seguito a variazioni della po 2 di quello che potrebbe, se i siti di legame avessero un comportamento indipendente gli uni dagli altri. 67
68 LA FUNZIONE DEL COEFFICIENTE DI HILL La po 2 alveolare = 100 torr La po 2 dei capillari di muscolo in attività = 20 torr La P 50 Hb = 26 torr Il coefficiente di Hill (n) = 2,8 Y alveoli = 0.97 Y muscolo in attività = 0.32 Valori ottenuti utilizzando la seguente equazione: y = (po 2 ) n (po 2 ) n + (P ) n 68
69 IL COEFFICIENTE DI HILL Il grafico di Hill per il legame dell ossigeno alla mioglobina (blu) ed all emoglobina (rosso). 69
70 L EMOGLOBINA DeossiHb OssiHb (più compatta) 70
71 LE PROPRIETA ALLOSTERICHE DELL EMOGLOBINA EMOGLOBINA Le proprietà allosteriche dell Hb derivano dalle interazioni tra le sue subunità, le catene isolate si comportano come la Mb, le catene isolate formano un tetramero mancante di proprietà allosteriche (HbH). 71
72 LE INTERAZIONI FRA LE SUBUNITA DELL Hb Le subunità sono disposte ai vertici di un tetraedro, esistono notevoli interazioni tra le subunità di tipo diverso: le interfacce 1 1 e 2 2 comprendono 35 residui, le interfacce 1 2 e 2 1 comprendono 19 residui. 72
73 LE INTERAZIONI FRA LE SUBUNITA DELL Hb Esse sono principalmente interazioni di carattere idrofobico, sono presenti anche leg.h ed alcune coppie ioniche, i contatti tra le subunità dello stesso tipo sono pochi e prevalentemente polari; infatti, sono separate da un canale di 20A pieno di solvente. 73
74 LA TRANSIZIONE T RT L Hb possiede due stati di struttura quaternaria: 1) la forma deossi (stato T), 2) la forma ossi (stato R), che ha affinità superiore per l ossigeno, giustificando la cooperatività di legame. 74
75 LO SPETTRO DI ASSORBIMENTO DELLA LUCE VISIBILE DELLA OSSIHb E DEOSSIHb 75
76 LA TRANSIZIONE T RT L ossigenazione determina un cambiamento nella struttura quaternaria, accompagnato ad un cambiamento della struttura terziaria della Hb, una coppia ruota e scivola rispetto all altra. Questo movimento porta le catene più vicine tra loro e restringe la cavità centrale della molecola. 76
77 DEOSSIHb OSSIHb 77
78 LA TRANSIZIONE T R Durante l ossigenazione, la coppia α1 β1 ruota di 15 rispetto all altra coppia. 78
79 LA TRANSIZIONE T RT Durante l ossigenazione, i contatti α 1 β 1 e α 2 β 2 rimangono immodificati, numerose modificazioni strutturali avvengono a livello delle regioni di contatto α 1 β 2 e α 2 β 1. 79
80 LA TRANSIZIONE T R 80
81 LA TRANSIZIONE T RT Il legame dell O 2 ad una subunità determina cambiamenti nella sua struttura terziaria a partire dall eme, che da una forma curvata assume una forma appiattita. Questo provoca una tensione ed un conseguente cambiamento nella struttura circostante, in particolare nelle zone critiche dell interfaccia. 81
82 LA TRANSIZIONE T RT Il legame dell O 2 determina una contrazione di circa 0.1A dei legami Fe-N porfirina ed il conseguente abbassamento della cupola dell eme. 82
83 LA TRANSIZIONE T RT Il legame dell ossigeno attira il ferro all interno del piano dell eme, appiattendolo e provocando tensione, che é attenuata da una variazione nell orientamento della His F8 e ciò é in parte mediato dalla spinta verso destra della val FG5. Il cambiamento di struttura terziaria dell eme viene comunicato all angolo FG. 83
84 IL MOVIMENTO DEL FERRO ALL INTERNO DELL EME, EME, CHE DIVENTA PIÙ PLANARE, VIENE TRASMESSO ALLE ALTRE SUBUNITÀ ATTRAVERSO MODIFICAZIONI CONFORMAZIONALI ALLE LORO INTERFACCE. 84
85 LA TRANSIZIONE T RT Il rimaneggiamento della struttura terziaria di una subunitá porta ad un accumulo di tensione che determina una transizione quaternaria (T R). 85
86 I CONTATTI ALL INTERFACCIA αβ Le regioni di contatto tra due subunità agiscono come un interruttore in grado di innescare due strutture diverse. Le due strutture sono stabilizzate da gruppi diversi di legami H; H in entrambe le conformazioni, le protuberanze di una subunità si adattano esattamente agli incavi presenti nell altra subunità. 86
87 OTTO COPPIE IONICHE (PONTI SALINI) STABILIZZANO LO STATO T DELLA DEOSSIEMOGLOBINA 87
88 IL RETICOLO DI COPPIE IONICHE E LEGAMI IDROGENO NELLA DEOSSIEMOGLOBINA 88
89 GLI OTTO LEGAMI SALINI FRA LE SUBUNITÀ DELLA DEOSSIEMOGLOBINA La transizione T R determina la rottura dei ponti salini. 89
90 UN MODELLO RECENTE PER LA TRANSIZIONE COOPERATIVA DELL EMOGLOBINA. EMOGLOBINA. 90
91 LA TRANSIZIONE T RT A=modello concertato B=modello sequenziale 91
92 IL MOVIMENTO DELL O 2 ATTRAVERSO IL SISTEMA RESPIRATORIO E CIRCOLATORIO 92
93 93
94 L EFFETTO BOHR L effetto della variazione del ph sull Hb. Una caduta del ph nei capillari tessutali ha l effetto di abbassare l affinità dell Hb per l ossigeno, permettendo un rilascio ancora più efficiente delle ultime tracce di ossigeno legato. L effetto reciproco avviene nei capillari dei polmoni. Il ph é un effettore eterotropico negativo. 94
95 L EFFETTO BOHR NELL Hb L efficienza di rilascio dell O 2 aumenta fortemente con la diminuzione del ph. Quando il sangue circola dai polmoni (giallo) ai tessuti (azzurro), il basso valore di ph sposta il legame dell O 2 verso le curve a più bassa affinità. Nel caso della Mb, l effetto Bohr è scarso. 95
96 L EFFETTO BOHR Durante la respirazione, 0,8 molecole di CO 2 sono formate per ogni molecola di O 2 consumata. La CO 2 diffonde dai tessuti ai capillari. Nei globuli rossi: CO 2 +H 2 0 H 2 CO 3 HCO 3- +H + 96
97 L EFFETTO BOHR NEL GLOBULO ROSSO Gli ioni H + vengono assunti dalla Hb che viene indotta a rilasciare l O 2 che ha legato. Al contrario, nei polmoni, dove la po 2 è elevata, il legame dell ossigeno all Hb determina il rilascio dei protoni implicati nell effetto Bohr. 97
98 LA PROTEINA TRASPORTATRICE DEGLI ANIONI NELL ERITROCITA ERITROCITA 98
99 IL RUOLO DEGLI GLI IONI H + ASSUNTI DALL Hb Gli ioni H + permettono l interazione tra l His 146 (cat.β 1 ) e l Asp 94 (cat.β 1 ), stabilizzando lo stato T (deossi) dell Hb. C terminale Protone aggiunto 99
100 RIASSUNTO DELL EFFETTO EFFETTO BOHR NEL GLOBULO ROSSO 100
101 L EFFETTO BOHR La reazione complessiva è: nh + + Hb 4O 2 Hb nh + + 4O 2 dove n ha un valore poco superiore a 2 Nei capillari tessutali, gli ioni H + promuovono il rilascio di O 2, spostando l equilibrio della reazione verso destra. Nei capillari polmonari, l ossigenazione provoca il rilascio di H +,spostando l equazione a sinistra. In seguito al legame dell O 2, l Hb diventa un acido più forte. A sua volta, l H + tende a liberare la CO 2 dal bicarbonato disciolto nel sangue. La CO 2 può così essere espirata. 101
102 L EFFETTO BOHR NEL GLOBULO ROSSO CO 2 CO 2 +H 2 0 H 2 CO 3 HCO 3- H + ossihb H + deossihb + O 2 O 2 Canale per gli anioni Cl - 102
103 IL RUOLO DELLA CO 2 La CO 2 é un effettore eterotropico negativo per il legame dell O 2 all Hb, la CO 2 rilasciata dai tessuti abbassa, infatti, la sua affinità per l O 2 in due modi: 1) con la formazione di bicarbonato (gli H + rilasciati contribuiscono all effetto Bohr), 2) con la formazione di carbamati, le cui interazioni elettrostatiche con gli amminogruppi N-terminali delle catene stabilizzano la deossihb. 103
104 IL TRASPORTO DELLA CO 2 DAI TESSUTI AI POLMONI 1) Esso é fondamentalmente un fenomeno passivo (ione bicarbonato). 2) R-NH 2 +CO 2 R-NH-COO - + H + carbamato Il carbamato forma interazioni elettrostatiche stabilizzanti la deossihb con gli amminogruppi N-terminali delle catene, l equilibrio della reazione dipende dalla [CO 2 ]. 3) CO 2 disciolta (in piccola quantità). 104
105 IL RUOLO DELL Hb E DELLA Mb NEL TRASPORTO DELL O 2 DAI POLMONI AI TESSUTI CHE RESPIRANO E DELLA CO 2 (SOTTO FORMA DI HCO 3- ) DAI TESSUTI AI POLMONI. 105
106 IL RUOLO DEL BPG Il BPG (bisfosfoglicerato) è un effettore eterotropico negativo dell Hb, perché diminuisce la sua affinità per l O
107 IL BISFOSFOGLICERATO (BPG) L effetto del BPG sul legame dell ossigeno all emoglobina. 107
108 IL LEGAME DEL BPG ALLA DEOSSIHb Il BPG si lega alla deossihb (in un rapporto di 1:1) nella cavità tra le catene, formando interazioni elettrostatiche con i gruppi carichi positivamente, presenti attorno a questa apertura. 108
109 IL LEGAME DEL BPG ALLA DEOSSIHb 109
110 IL LEGAME DEL BPG ALLA DEOSSIHb subunità 1 subunità 2 TR 110
111 IL RUOLO DEL BPG Il BPG è stereochimicamente complementare alle sei cariche positive presenti nella cavità centrale, formate da 3 residui di ciascuna catena β. Il BPG stabilizza la deossihb, diminuendo l affinità della deossihb per l ossigeno. I cambiamenti conformazionali che hanno luogo con l ossigenazione rompono il sito di legame. 111
112 IL RUOLO DEL BPG Legame del BPG alla deossiemoglobina A e B = deossihb C = ossihb 112
113 IL RUOLO DEL BPG Il BPG non si adatta alla forma ossihb, infatti, durante l ossigenazione, esso viene rilasciato per il restringimento della cavità centrale, maggiore è il contenuto di BPG negli eritrociti, più stabile è la struttura della deossihb, il BPG regola i cambiamenti a lungo termine nell affinità per l O 2. Un esempio è il suo aumento di concentrazione negli individui che si recano ad alte quote. 113
114 L EMOGLOBINA FETALE (HbF( HbF) Essa ha un ruolo nel passaggio di O 2 dalla madre al feto attraverso la placenta. L Hb fetale (α 2 γ 2 ) lega meno saldamente dell Hb adulta il BPG, perché un residuo di serina (non carico),in ogni catena γ, sostituisce l istidina (con carica positiva), presente in ogni catena β, nel sito di legame con il BPG, ne consegue una minore formazione di legami ionici (da 6 a 4); quindi, l HbF presenta una maggiore affinità per l ossigeno rispetto all HbA. La curva sigmoide é spostata a sinistra. 114
115 LE EMOGLOBINE ANORMALI E PATOLOGICHE Esse possono riguardare: alterazioni sulla superficie della molecola, alterazione del sito attivo, alterazione della struttura terziaria, alterazione della struttura quaternaria. 115
116 LE EMOGLOBINE ANORMALI E PATOLOGICHE La presenza di emoglobine anormali e patologiche è dovuta ad alterazioni della parte proteica della molecola. Sono possibili 1) Modificazioni: A) nelle catene o B) nelle catene o. 116
117 LE EMOGLOBINE ANORMALI E PATOLOGICHE 2) Sostituzione di intere catene dovute a loro difetti di sintesi: i: A) le emoglobine tetramere (HbH), con catene tutte uguali (es. β4) B) le talassemie. 117
118 L ELENCO DI ALCUNE MUTAZIONI NELLE EMOGLOBINE UMANE 118
119 L ANEMIA A CELLULE FALCIFORMI I globuli rossi, in presenza di basse concentrazioni di O 2, assumono una forma allungata a falce, questa deformazione è conseguente alla tendenza dell Hb mutante, nel suo stato deossigenato, ad aggregarsi in lunghe strutture a bastoncino, le cellule allungate formatesi tendono a bloccare i capillari, causando infiammazioni e dolore. 119
120 L ANEMIA A CELLULE FALCIFORMI Confronto tra eritrociti di un soggetto normale (a) e quelli di un paziente affetto da anemia falciforme (b). 120
121 L ANEMIA A CELLULE FALCIFORMI Tali cellule sono fragili e la loro rottura porta ad anemia, rendendo la persona sensibile ad infezioni e malattie; questa é una malattia genetica, gli omozigoti per la mutazione falciforme spesso non sopravvivono fino all età adulta, o la raggiungono gravemente debilitati, gli eterozigoti, che possono produrre l Hb normale, presentano di norma disturbi solo in condizioni di grave carenza di ossigeno. 121
122 L ANEMIA A CELLULE FALCIFORMI Confronto tra gli eritrociti di un soggetto normale e quelli di un paziente affetto da anemia falciforme. 122
123 L ANEMIA A CELLULE FALCIFORMI I soggetti, che sono malati per anemia a C.F., sono omozigoti per un gene autosomico, i soggetti, che presentano il tratto a cellule falciformi, sono eterozigoti per lo stesso gene autosomico e sono di norma asintomatici, la patologia si manifesta nel circolo venoso (quando l Hb é in forma deossi), nella circolazione venosa di un omozigote il 50% dei globuli rossi è a falce, negli eterozigoti solo l 1% 1%. 123
124 L ANEMIA A CELLULE FALCIFORMI L anemia falciforme é trasmessa geneticamente ed è per lo più limitata alla popolazioni tropicali (l incidenza tra le persone nere é circa il 4%o), il tratto a cellule falciformi é presente in 1 nero su 10, éuna patologia cronica ed emolitica, le cellule a falce rimangono intrappolate nei piccoli vasi sanguigni, creando danni agli organi. 124
125 L HbS La solubilità della deossihb nei globuli rossi falciformi è anormalmente bassa (soltanto il 4% della deossihb normale). Si produce un abbondante precipitato fibroso con deformazione dei globuli rossi, che assumono una forma a falce. L Hb delle cellule falciformi é chiamata HbS (sickle = falce). 125
126 L HbS HA UNA DIVERSA MOBILITÀ ELETTROFORETICA RISPETTO ALL HbA P.I. HBA = 6.87 P.I. HBS = 7.09 (Elettroforesi eseguita a ph 8,6). 126
127 IL CONFRONTO TRA HbA (NORMALE) ED HbS (ANEMIA FALCIFORME) L anemia a cellule falciformi é una malattia molecolare. Le piccole differenze di conformazione tra Hb normale ed HbS derivano dalla sostituzione di un solo amminoacido nelle catene β. 127
128 L ANEMIA A CELLULE FALCIFORMI La patologia, infatti, dipende da una singola mutazione di una base azotata nelle catene, che porta alla sostituzione in posizione 6 dell acido glutammico con la valina. 128
129 L ANEMIA A CELLULE FALCIFORMI Per individuare la presenza di tale sostituzione, é stata utilizzata la tecnica del fingerprint, l Hb viene tagliata in singoli frammenti, impiegando la tripsina; il trattamento triptico produce 28 diversi peptidi dal dimero αβ. 129
130 LA TECNICA DEL FINGERPRINT Dal trattamento triptico si ottiene cosí un miscuglio di 28 frammenti sia dalla HbA, sia dalla HbS; si eseguono poi l elettroforesi e la cromatografia, che permettono di evidenziare l amminoacido mutato nell HbS. 130
131 L HbS La valina idrofobica si inserisce in una tasca nell angolo EF della catena di un altra Hb e così Hb adiacenti possono adattarsi l una all altra formando una fibra elicoidale, tale riarrangiamento si ha solo per la deossihb, perché nella forma ossi il riarrangiamento delle subunità rende la tasca inaccessibile. 131
132 L HbS Un sito idrofofico, complementare alla zona appiccicosa (valina), compare in ogni catena β delle HbS e HbA nella loro forma deossigenata. Nelle rispettive forme ossigenate, il sito complementare é nascosto. 132
133 L HbS Il sito complementare di HbS deossigenata può legarsi alla zona appiccicosa di un altra deossi-hbs, con formazione di lunghe fibre, che trasformano i G.R. in cellule a falce, le quali distorcono il vaso sanguigno. 133
134 L HbS Il blocco di un vaso determina una zona a bassa concentrazione di ossigeno, che porta ad una ulteriore deossigenazione dell HbS con produzione prima di altre fibre e conseguentemente di nuove cellule a falce; ha così origine un circolo vizioso. 134
135 IL TRATTO A CELLULE FALCIFORMI Una persona eterozigote è normalmente asintomatica, avendo solo il 50% dell HbS, che é insufficiente per produrre tante fibre da trasformare i G.R. in cellule a falce, la forma a falce é deossi-s. infatti causata da un alta concentrazione di 135
136 LE FASI DI NUCLEAZIONE NELLA FORMAZIONE DELLE FIBRE DI DEOSSI HbS La HbS ha una regione idrofobica sulla superficie, che causa un aggregazione di queste molecole in catene, che si organizzano in fibre insolubili. 136
137 LE FASI DI NUCLEAZIONE NELLA FORMAZIONE DELLE FIBRE DI DEOSSI HbS La forma a falce degli eritrociti è dovuta quindi alla polimerizzazione della deossi HbS sotto forma di fibre rigide, che si estendono per tutta la lunghezza della cellula. 137
138 LE FASI DI NUCLEAZIONE NELLA FORMAZIONE DELLE FIBRE DI DEOSSI HbS 1) Si forma un nucleo di molecole di deossi HbS. 2) Quando la fibra si è formata, essa può nucleare la crescita di altre fibre, di conseguenza, il processo diventa autocatalitico. Se il tempo per la formazione della fibra è superiore al tempo di transito dei globuli rossi dai capillari periferici agli alveoli polmonari, non si formeranno le cellule a falce e non ci sarà alcun blocco del flusso sanguigno. 138
139 SI FORMA UNA FIBRA ELICOIDALE A 14 ELEMENTI 139
140 LE MODIFICAZIONI CHE PORTANO ALLA FORMAZIONE DI AGGREGATI Emoglobina A Emoglobina S 2 1 Glu6 Val6 2 Glu6 1 Val6 Interazione tra molecole Formazione di fibre insolubili 140
141 L ANEMIA FALCIFORME E LA MALARIA La malaria è una malattia parassitaria trasmessa dalla zanzara tropicale anofele, il plasmodium falciparum è un potozoo che sta nei globuli rossi per la maggior parte del ciclo vitale (48 ore), aumentandone l acidità e determinandone l adesione ad una specifica proteina sulla parete dei vasi, esso crea quindi un impedimento del flusso sanguigno nell organo in cui esso é presente (es. malaria cerebrale). 141
142 L ANEMIA FALCIFORME E LA MALARIA L anemia falciforme è limitata alle popolazioni originarie della zone tropicali, con alta incidenza della malaria, gli individui eterozigoti per l HbS presentano una maggiore resistenza alla malaria rispetto agli individui che non portano tale mutazione; perché? in essi, la presenza dell infezione determina un aumento delle cellule a falce dal 2% fino al 40%, poiché la maggiore acidificazone, causata dall infezione, aumenta la formazione di deossihbs, (per l effetto Bohr). 142
143 L ANEMIA FALCIFORME E LA MALARIA Un globulo rosso normale mantiene alta la concentrazione di potassio; l aumentata fragilità delle cellule falciformi porta invece ad un rilascio dello ione, il parassita spesso interrompe il suo ciclo vitale, poiché necessita di alte concentrazioni di potassio, quindi, il tratto per l anemia falciforme risulta essere un adattamento vantaggioso in ambiente malarico. 143
144 L ANEMIA FALCIFORME E LA MALARIA Gli eterozigoti hanno maggiori possibilità di sopravvivenza e quindi maggiore possibilità di trasmettere i propri geni nelle regioni infestate dalla malaria, questo porta anche alla nascita di un gran numero di individui omozigoti per il tratto mutante. 144
145 L Hb DI HAMMERSMITH Essa é un altro esempio di Hb patologica. In posizione CD1 la Phe é sostituita da una serina, con la riduzione del legame dell eme (esso tende a perdersi). 145
146 LE TALASSEMIE Sono difetti genetici, in cui una o più catene non sono prodotte o sono prodotte in piccole quantità. Si distinguono le -talassemie e -talassemie. 146
147 IL FLUSSO DELL INFORMAZIONE GENETICA 147
148 LE TALASSEMIE Le sindromi talassemiche possono insorgere nei seguenti casi: 1) uno o più geni codificanti per le catene dell Hb hanno subito una delezione completa, 2) uno o più geni presentano una mutazione non senso (con conseguente catena polipeptidica accorciata), o della fase di lettura, che produce una catena non funzionale, 3) i geni sono presenti, ma c è una mutazione al di fuori della regione codificante, che determina il blocco della trascrizione, oppure un errato riarrangiamento del pre-mrna. 148
149 L -TALASSEMIA Si ha quando il gene della -globina è stato perduto, o non può essere espresso, il basso livello di -Hb è parzialmente compensato dalla formazione di HbH ( 4) e Hb di Bart ( 4), questi tetrameri trasportano l ossigenol ossigeno, ma non mostrano la transizione allosterica (sono sempre nello stato R) e mancano dell effetto Bohr, la totale assenza di -Hb è incompatibile con la vita. 149
150 LA β-talassemia Si ha quando il gene della -globina è stato perduto, o non può essere espresso, negli omozigoti, è una condizione patologica molto grave che causa la morte del soggetto affetto, prima della maturità, in caso di eterozigosi, il gene della -globina è ancora funzionante, esistono anche talassemie più leggere, in cui la produzione di β- globina é ridotta, ma non completamente soppressa. 150
151 LE TIPOLOGIE DELLA -TALASSEMIA 1) maior essa si manifesta negli omozigoti, nei quali HbF è circa il 90%, é chiamata morbo di Cooley o Anemia Mediterranea 2) minor 3) minima 151
Le proteine che legano l ossigenol
 Le proteine che legano l ossigenol Protoporfirina IX EME (Fe-protoporfirina IX) L atomo di ferro del gruppo eme può formare sei legami Struttura della mioglobina di capodoglio (J. Kendrew, anni 50)
Le proteine che legano l ossigenol Protoporfirina IX EME (Fe-protoporfirina IX) L atomo di ferro del gruppo eme può formare sei legami Struttura della mioglobina di capodoglio (J. Kendrew, anni 50)
FUNZIONI delle PROTEINE
 FUNZIONI delle PROTEINE Ha le dimensioni del reciproco di una concentrazione (M -1 ) Ha le dimensioni di una concentrazione (M) La frazione dei siti occupati rispetto ai siti totali è definita come θ FRAZIONE
FUNZIONI delle PROTEINE Ha le dimensioni del reciproco di una concentrazione (M -1 ) Ha le dimensioni di una concentrazione (M) La frazione dei siti occupati rispetto ai siti totali è definita come θ FRAZIONE
Esempi di proteine: Mioglobina ed Emoglobina
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Esempi di proteine: Mioglobina ed Emoglobina Mioglobina: caratteristiche generali, funzione
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Esempi di proteine: Mioglobina ed Emoglobina Mioglobina: caratteristiche generali, funzione
Emoglobina e mioglobina
 Emoglobina e mioglobina Per molti organismi, l O 2 è una molecola di importanza vitale: l'ossigeno è infatti l'accettore finale degli elettroni, che "fluendo" attraverso i complessi della catena respiratoria,
Emoglobina e mioglobina Per molti organismi, l O 2 è una molecola di importanza vitale: l'ossigeno è infatti l'accettore finale degli elettroni, che "fluendo" attraverso i complessi della catena respiratoria,
Esempi di proteine: Mioglobina ed Emoglobina
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica Organica e Biochimica Esempi di proteine: Mioglobina ed Emoglobina Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica Organica e Biochimica Esempi di proteine: Mioglobina ed Emoglobina Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base
Nel corso dell evoluzione, con il passaggio dalla. progressivamente differenziati due meccanismi. un sistema circolatorio adeguato;
 PROTEINE RESPIRATORIE EMOGLOBINA & MIOGLOBINA Nel corso dell evoluzione, con il passaggio dalla vita anaerobia alla vita aerobia si sono progressivamente differenziati due meccanismi che sono in grado
PROTEINE RESPIRATORIE EMOGLOBINA & MIOGLOBINA Nel corso dell evoluzione, con il passaggio dalla vita anaerobia alla vita aerobia si sono progressivamente differenziati due meccanismi che sono in grado
Mioglobina ed emoglobina
 Mioglobina ed emoglobina α β Muscolo Deposito di O 2 Alta affinità per O 2 β α Globulo rosso Trasporto di O 2 Bassa affinità per O 2 Cooperativa ed allosterica Animali Mb-knockout (2003) : funzionalità
Mioglobina ed emoglobina α β Muscolo Deposito di O 2 Alta affinità per O 2 β α Globulo rosso Trasporto di O 2 Bassa affinità per O 2 Cooperativa ed allosterica Animali Mb-knockout (2003) : funzionalità
Ogni globina ha una tasca in cui lega un gruppo EME, quindi l Hb può legare e trasportare 4 molecole di O 2
 Emoglobina (Hb): tetramero (le globine si associano formando due copie di dimeri αβ (α 1 β 1 e α 2 β 2 ) che si associano a formare un tetramero attraverso interazioni idrofobiche, legami H e ponti salini
Emoglobina (Hb): tetramero (le globine si associano formando due copie di dimeri αβ (α 1 β 1 e α 2 β 2 ) che si associano a formare un tetramero attraverso interazioni idrofobiche, legami H e ponti salini
Regolano il metabolismo, sia come enzimi, sia come ormoni (insulina, glucagone, ecc.)
 Grazie alla elevata dinamicità delle strutture proteiche (gli atomi sono in continuo movimento fluttuante) e per la capacità che hanno di legarsi in modo selettivo ad altre molecole, le proteine svolgono
Grazie alla elevata dinamicità delle strutture proteiche (gli atomi sono in continuo movimento fluttuante) e per la capacità che hanno di legarsi in modo selettivo ad altre molecole, le proteine svolgono
FUNZIONE DELLE PROTEINE RAPPORTO STRUTTURA-FUNZIONE
 FUNZIONE DELLE PROTEINE RAPPORTO STRUTTURA-FUNZIONE Principi basilari: 1.Le funzioni di molte proteine richiedono il legame reversibile con altre molecole (LIGANDO) Un ligando può essere di natura diversa,
FUNZIONE DELLE PROTEINE RAPPORTO STRUTTURA-FUNZIONE Principi basilari: 1.Le funzioni di molte proteine richiedono il legame reversibile con altre molecole (LIGANDO) Un ligando può essere di natura diversa,
Il metalloma Struttura e reattività di metalloproteine. Il trasporto dell O 2
 Il metalloma Struttura e reattività di metalloproteine Il trasporto dell O 2 Il trasporto dell ossigeno Nel sangue la solubilità dell O 2 è molto maggiore che in H 2 O In H 2 O la solubilità è 6.59 cm
Il metalloma Struttura e reattività di metalloproteine Il trasporto dell O 2 Il trasporto dell ossigeno Nel sangue la solubilità dell O 2 è molto maggiore che in H 2 O In H 2 O la solubilità è 6.59 cm
L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO
 L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 23 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata all emoglobina: L O 2 totale
L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 23 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata all emoglobina: L O 2 totale
Emoglobina e mioglobina
 Emoglobina e mioglobina L emoglobina e la mioglobina proteine centrali per l evoluzione La transizione dalla vita anaerobica a quella aerobica rappresenta un passo fondamentale dell'evoluzione perchè ha
Emoglobina e mioglobina L emoglobina e la mioglobina proteine centrali per l evoluzione La transizione dalla vita anaerobica a quella aerobica rappresenta un passo fondamentale dell'evoluzione perchè ha
Trasporto di O 2 nel sangue
 Trasporto di O 2 nel sangue Il 97% dell O 2 trasportato nel plasma è chimicamente legato all Hb nei globuli rossi, solo il 3% è fisicamente disciolto Trasporto O 2 nel plasma Trasporto O 2 legato ad Hb
Trasporto di O 2 nel sangue Il 97% dell O 2 trasportato nel plasma è chimicamente legato all Hb nei globuli rossi, solo il 3% è fisicamente disciolto Trasporto O 2 nel plasma Trasporto O 2 legato ad Hb
Le proteine III. Corso di Biochimica 1. Prof. Giuseppina Pitari
 Le proteine III Corso di Biochimica 1 Prof. Giuseppina Pitari Ossi-mioglobina legame idrogeno lato distale La mioglobina L eme quindi consiste di una struttura organica alla quale è legato un atomo di
Le proteine III Corso di Biochimica 1 Prof. Giuseppina Pitari Ossi-mioglobina legame idrogeno lato distale La mioglobina L eme quindi consiste di una struttura organica alla quale è legato un atomo di
degli eritrociti è una proteina di trasporto indispensabile per veicolare l ossigeno l l anidride carbonica tra i polmoni e i tessuti
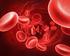 l emoglobina degli eritrociti è una proteina di trasporto indispensabile per veicolare l ossigeno l e l anidride carbonica tra i polmoni e i tessuti Mioglobina, proteina di deposito,, presente nelle fibrocellule
l emoglobina degli eritrociti è una proteina di trasporto indispensabile per veicolare l ossigeno l e l anidride carbonica tra i polmoni e i tessuti Mioglobina, proteina di deposito,, presente nelle fibrocellule
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 10
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 10 Funzioni delle proteine Concetti chiave: La varietà strutturale delle proteine consente loro di svolgere un enorme quantità
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 10 Funzioni delle proteine Concetti chiave: La varietà strutturale delle proteine consente loro di svolgere un enorme quantità
CHIMICA BIOLOGICA. Seconda Università degli Studi di Napoli. Prof. Augusto Parente. Lezione 7. DiSTABiF. Corso di Laurea in SCIENZE BIOLOGICHE
 Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in SCIENZE BIOLOGICHE Insegnamento di CHIMICA BIOLOGICA Prof. Augusto Parente Anno Accademico 2014-15 Lezione 7 Mioglobina Emoglobina po
Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in SCIENZE BIOLOGICHE Insegnamento di CHIMICA BIOLOGICA Prof. Augusto Parente Anno Accademico 2014-15 Lezione 7 Mioglobina Emoglobina po
Trasporto dei gas. Pressioni Volumi
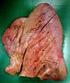 Trasporto dei gas Pressioni Volumi Il 97% dell O 2 trasportato nel plasma si trova chimicamente legato all Hb nei globuli rossi, solo lo 3% è fisicamente disciolto Trasporto O 2 nel plasma Trasporto O
Trasporto dei gas Pressioni Volumi Il 97% dell O 2 trasportato nel plasma si trova chimicamente legato all Hb nei globuli rossi, solo lo 3% è fisicamente disciolto Trasporto O 2 nel plasma Trasporto O
Regolazione allosterica
 Macromolecole Biologiche Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Regolazione allosterica Marco Nardini Dipartimento
Macromolecole Biologiche Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Regolazione allosterica Marco Nardini Dipartimento
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
sono le unità monomeriche che costituiscono le proteine hanno tutti una struttura comune
 AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
- CINETICA ENZIMATICA
 - CINETICA ENZIMATICA ENZIMI: - CATALIZZATORI aumenta la V di una reazione chimica senza subire trasformazioni durante l intero processo - PROTEINE gli enzimi sono proteine di struttura 3 o talora 4 -
- CINETICA ENZIMATICA ENZIMI: - CATALIZZATORI aumenta la V di una reazione chimica senza subire trasformazioni durante l intero processo - PROTEINE gli enzimi sono proteine di struttura 3 o talora 4 -
Gli Enzimi. catalizzatori biologici rendono possibile da un punto di vista cinetico le reazioni chimiche
 catalizzatori biologici rendono possibile da un punto di vista cinetico le reazioni chimiche Gli Enzimi Sono le proteine più importanti e più specializzate Presentano un elevato grado di specificità per
catalizzatori biologici rendono possibile da un punto di vista cinetico le reazioni chimiche Gli Enzimi Sono le proteine più importanti e più specializzate Presentano un elevato grado di specificità per
Dipartimento di Biochimica e Biofisica F. Cedrangolo Emoglobina ed introduzione alle emoglobinopatie.
 Dipartimento di Biochimica e Biofisica F. Cedrangolo Emoglobina ed introduzione alle emoglobinopatie. Trasportatori di Ossigeno nei Vertebrati Mioglobina Emoglobina Muscoli Sangue L Emoglobina (Hb) Struttura
Dipartimento di Biochimica e Biofisica F. Cedrangolo Emoglobina ed introduzione alle emoglobinopatie. Trasportatori di Ossigeno nei Vertebrati Mioglobina Emoglobina Muscoli Sangue L Emoglobina (Hb) Struttura
PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA
 PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA Svolgono la loro funzione legando reversibilmente l OSSIGENO. Aumentano la solubilità dell ossigeno nel plasma, da 3ml/L a 220 ml/l. La mioglobina
PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA Svolgono la loro funzione legando reversibilmente l OSSIGENO. Aumentano la solubilità dell ossigeno nel plasma, da 3ml/L a 220 ml/l. La mioglobina
Fisiologia della Respirazione 8.Trasporto dei gas nel sangue. Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona
 Fisiologia della Respirazione 8.Trasporto dei gas nel sangue Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona Obiettivi Necessità di un sistema di trasporto chimico ad alta capacità
Fisiologia della Respirazione 8.Trasporto dei gas nel sangue Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona Obiettivi Necessità di un sistema di trasporto chimico ad alta capacità
Fisiologia della Respirazione
 Fisiologia della Respirazione 8.Trasporto dei gas nel sangue FGE aa.2016-17 Obiettivi Necessità di un sistema di trasporto chimico ad alta capacità dell O 2 nel sangue: l emoglobina Curva di dissociazione
Fisiologia della Respirazione 8.Trasporto dei gas nel sangue FGE aa.2016-17 Obiettivi Necessità di un sistema di trasporto chimico ad alta capacità dell O 2 nel sangue: l emoglobina Curva di dissociazione
Rapporto Struttura/Funzione delle Proteine
 Macromolecole Biologiche Chimica Biologica A.A. 2010-2011 Rapporto Struttura/Funzione delle Proteine Struttura/Funzione delle Proteine Interazioni proteina-ligando come base della funzione di molte proteine
Macromolecole Biologiche Chimica Biologica A.A. 2010-2011 Rapporto Struttura/Funzione delle Proteine Struttura/Funzione delle Proteine Interazioni proteina-ligando come base della funzione di molte proteine
Amminoacidi Peptidi Proteine
 Amminoacidi Peptidi Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Gli amminoacidi nelle molecole proteiche sono tutti stereoisomeri L IDROFOBOCI IDROFOBOCI IDROFILICI Secondo gruppo
Amminoacidi Peptidi Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Gli amminoacidi nelle molecole proteiche sono tutti stereoisomeri L IDROFOBOCI IDROFOBOCI IDROFILICI Secondo gruppo
- utilizzano esclusivamente le reattività chimiche di alcuni residui AA
 Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Ruolo chiave nella Protein Science Cristallizzata nel 1840 Handbook of Hb crystals 1909 (Reichert & Brown)
 Mb & Hb EMOGLOBINA Ruolo chiave nella Protein Science Cristallizzata nel 1840 Handbook of Hb crystals 1909 (Reichert & Brown) 1 proteina caratterizzata t in ultracentrifuga t 1 proteina a funzione fisiologica
Mb & Hb EMOGLOBINA Ruolo chiave nella Protein Science Cristallizzata nel 1840 Handbook of Hb crystals 1909 (Reichert & Brown) 1 proteina caratterizzata t in ultracentrifuga t 1 proteina a funzione fisiologica
Struttura degli amminoacidi
 AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
 Gruppo EME α β δ ϒ ζ ε A A2 α2β2 97-98 α2δ2 2-3 F Gower1 Gower2 Portland α2 ϒ2 < 1 ζ2ε2 0 α2ε2 0 ζ2ϒ2 0 Periodo fetale Periodo postnatale Varianti strutturali dell emoglobina Emoglobina anomala HbS
Gruppo EME α β δ ϒ ζ ε A A2 α2β2 97-98 α2δ2 2-3 F Gower1 Gower2 Portland α2 ϒ2 < 1 ζ2ε2 0 α2ε2 0 ζ2ϒ2 0 Periodo fetale Periodo postnatale Varianti strutturali dell emoglobina Emoglobina anomala HbS
COMPOSIZIONE DELL ARIA ATMOSFERICA SECCA E PRESSIONI PARZIALI DEI GAS - (760 TORR, 15 C)
 COMPOSIZIONE DELL ARIA ATMOSFERICA SECCA E PRESSIONI PARZIALI DEI GAS - (760 TORR, 15 C) COMPOSIZIONE ARIA NELL ATMOSFERA = COSTANTE A PARTE LE VARIAZIONI DELLA QUANTITA DI VAPORE ACQUEO A 0 C 1 torr =
COMPOSIZIONE DELL ARIA ATMOSFERICA SECCA E PRESSIONI PARZIALI DEI GAS - (760 TORR, 15 C) COMPOSIZIONE ARIA NELL ATMOSFERA = COSTANTE A PARTE LE VARIAZIONI DELLA QUANTITA DI VAPORE ACQUEO A 0 C 1 torr =
Funzioni delle proteine
 Funzioni delle proteine ENZIMI Proteine di trasporto Proteine di riserva Proteine contrattili o motili Proteine strutturali Proteine di difesa Proteine regolatrici Proteine di trasporto Emoglobina Lipoproteine
Funzioni delle proteine ENZIMI Proteine di trasporto Proteine di riserva Proteine contrattili o motili Proteine strutturali Proteine di difesa Proteine regolatrici Proteine di trasporto Emoglobina Lipoproteine
REGOLAZIONE ENZIMATICA
 REGOLAZIONE ENZIMATICA Cambio conformazionale In molte molecole proteiche, cambiamenti strutturali possono determinare profondi cambiamenti nella funzione o nell attività. Il cambio conformazionale può
REGOLAZIONE ENZIMATICA Cambio conformazionale In molte molecole proteiche, cambiamenti strutturali possono determinare profondi cambiamenti nella funzione o nell attività. Il cambio conformazionale può
Proprietà comuni. Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici
 Gli aminoacidi Proprietà comuni Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici paragonabili Il gruppo α-aminico è un acido più forte (o una base più debole
Gli aminoacidi Proprietà comuni Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici paragonabili Il gruppo α-aminico è un acido più forte (o una base più debole
COMPORTAMENTO ANFOTERO DEGLI AA
 Proprietà acido-basiche degli aminoacidi FORMA NON IONICA Non esiste a nessun valore di ph FORMA ZWITTERIONICA È la forma prevalente a ph 7 COMPORTAMENTO ANFOTERO DEGLI AA CARICA NETTA +1 CARICA NETTA
Proprietà acido-basiche degli aminoacidi FORMA NON IONICA Non esiste a nessun valore di ph FORMA ZWITTERIONICA È la forma prevalente a ph 7 COMPORTAMENTO ANFOTERO DEGLI AA CARICA NETTA +1 CARICA NETTA
30/10/2015. Molte proteine sono. intrinsecamente disordinate. o destrutturate (IDP/IUP), cioè non hanno una struttura
 Molte proteine sono intrinsecamente disordinate o destrutturate (IDP/IUP), cioè non hanno una struttura terziaria e/o secondaria stabile. Le IUP sono caratterizzate da - scarso contenuto in aa apolari,
Molte proteine sono intrinsecamente disordinate o destrutturate (IDP/IUP), cioè non hanno una struttura terziaria e/o secondaria stabile. Le IUP sono caratterizzate da - scarso contenuto in aa apolari,
LE PROTEINE -struttura tridimensionale-
 LE PROTEINE -struttura tridimensionale- Struttura generale di una proteina Ceruloplasmina Cosa sono??? Sono biopolimeri con forme ben definite. composti da molteplici amminoacidi, legati con legami peptidici
LE PROTEINE -struttura tridimensionale- Struttura generale di una proteina Ceruloplasmina Cosa sono??? Sono biopolimeri con forme ben definite. composti da molteplici amminoacidi, legati con legami peptidici
possiede una propria struttura, da cui dipende la specifica funzione
 LE PROTEINE SONO DEI POLIMERI LE CUI UNITA RIPETITIVE SONO GLI -AMMINO ACIDI: ogni proteina possiede una propria struttura, da cui dipende la specifica funzione AMMINOACIDI E PROTEINE Le proteine rappresentano
LE PROTEINE SONO DEI POLIMERI LE CUI UNITA RIPETITIVE SONO GLI -AMMINO ACIDI: ogni proteina possiede una propria struttura, da cui dipende la specifica funzione AMMINOACIDI E PROTEINE Le proteine rappresentano
CROMATINA ISTONI. Proteine relativamente piccole, con forte carica positiva per la presenza degli aminoacidi lisina e arginina
 CROMATINA Complesso molecolare formato da DNA, istoni e proteine non istoniche ISTONI Proteine relativamente piccole, con forte carica positiva per la presenza degli aminoacidi lisina e arginina Si conoscono
CROMATINA Complesso molecolare formato da DNA, istoni e proteine non istoniche ISTONI Proteine relativamente piccole, con forte carica positiva per la presenza degli aminoacidi lisina e arginina Si conoscono
Chimica Biologica A.A α-elica foglietto β reverse turn
 Chimica Biologica A.A. 2010-2011 α-elica foglietto β reverse turn Str. Secondaria sperimentalmente osservata: Si distinguono fondamentalmente tre tipi di strutture secondarie: α elica foglietto β reverse
Chimica Biologica A.A. 2010-2011 α-elica foglietto β reverse turn Str. Secondaria sperimentalmente osservata: Si distinguono fondamentalmente tre tipi di strutture secondarie: α elica foglietto β reverse
Prof. Maria Nicola GADALETA
 Prof. Maria Nicola GADALETA Email: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA Email: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Elementi sistemati nella TAVOLA PERIODICA DEGLI ELEMENTI in base al numero atomico crescente O, H, N, C (+ del 96% della materia vivente)
 OVERVIEW Atomo: più piccola porzione di un elemento che mantiene le proprietà chimiche dello stesso Teoria atomica e tavola periodica Legami e interazioni degli atomi Acqua e le sue proprietà Acidi e basi
OVERVIEW Atomo: più piccola porzione di un elemento che mantiene le proprietà chimiche dello stesso Teoria atomica e tavola periodica Legami e interazioni degli atomi Acqua e le sue proprietà Acidi e basi
Ruolo del calcio nella cellula
 Ruolo del calcio nella cellula I meccanismi evolutivi hanno attribuito agli ioni fosfato un importanza fondamentale poiché sono necessari per sintetizzare ATP. Per questo motivo la loro concentrazione
Ruolo del calcio nella cellula I meccanismi evolutivi hanno attribuito agli ioni fosfato un importanza fondamentale poiché sono necessari per sintetizzare ATP. Per questo motivo la loro concentrazione
L equilibrio dell acqua
 L equilibrio dell acqua Il ph e la reazione di autoprotolisi dell acqua Corpaci Ivana La molecola dell acqua H O H! L acqua è un composto molecolare covalente! La sua molecola è polare per la differenza
L equilibrio dell acqua Il ph e la reazione di autoprotolisi dell acqua Corpaci Ivana La molecola dell acqua H O H! L acqua è un composto molecolare covalente! La sua molecola è polare per la differenza
Trasporto O 2 nel sangue
 Trasporto O 2 nel sangue 97% legato all Hb nei globuli rossi 3% fisicamente disciolto, determina il valore di po 2 Trasporto O 2 nel plasma Trasporto O 2 legato ad Hb SaturazioneHb 97% 0.3 ml/100ml 19.4
Trasporto O 2 nel sangue 97% legato all Hb nei globuli rossi 3% fisicamente disciolto, determina il valore di po 2 Trasporto O 2 nel plasma Trasporto O 2 legato ad Hb SaturazioneHb 97% 0.3 ml/100ml 19.4
MACROMOLECOLE. Polimeri (lipidi a parte)
 MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
Appunti di BIOCHIMICA a cura di fabio Zonin 3 PROTEINE GLOBULARI LE EMOPROTEINE GLOBULARI
 Appunti di BIOCHIMICA a cura di fabio Zonin 3 PROTEINE GLOBULARI LE EMOPROTEINE GLOBULARI Sono un gruppo di proteine specializzate che legano a sé un gruppo prostetico chiamato eme. Tale gruppo assume
Appunti di BIOCHIMICA a cura di fabio Zonin 3 PROTEINE GLOBULARI LE EMOPROTEINE GLOBULARI Sono un gruppo di proteine specializzate che legano a sé un gruppo prostetico chiamato eme. Tale gruppo assume
Principi di Biochimica
 Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
PORTA AGLI ORGANI E AI TESSUTI: RIMUOVE: OMEOTERMI INTERVIENE NELLA TERMOREGOLAZIONE FUNZIONI DELLA CIRCOLAZIONE SANGUIGNA IL GLOBULO ROSSO
 FUNZIONI DELLA CIRCOLAZIONE SANGUIGNA IL GLOBULO ROSSO PORTA AGLI ORGANI E AI TESSUTI: a. L OSSIGENO (O 2 ), b. LE SOSTANZE NUTRITIZIE ASSORBITE, c. I SECRETI DELLE GHIANDOLE ENDOCRINE. RIMUOVE: a. L ANIDRIDE
FUNZIONI DELLA CIRCOLAZIONE SANGUIGNA IL GLOBULO ROSSO PORTA AGLI ORGANI E AI TESSUTI: a. L OSSIGENO (O 2 ), b. LE SOSTANZE NUTRITIZIE ASSORBITE, c. I SECRETI DELLE GHIANDOLE ENDOCRINE. RIMUOVE: a. L ANIDRIDE
Formazione. di un peptide.
 Formazione. di un peptide. Quando due aminoacidi si uniscono si forma un legame peptidico. In questo caso il dipeptide glicilalanina (Gly-Ala) viene mostrato come se si stesse formando in seguito a eliminazione
Formazione. di un peptide. Quando due aminoacidi si uniscono si forma un legame peptidico. In questo caso il dipeptide glicilalanina (Gly-Ala) viene mostrato come se si stesse formando in seguito a eliminazione
LE PROTEINE. SONO Polimeri formati dall unione di AMMINOACIDI (AA) Rende diversi i 20 AA l uno dall altro UN ATOMO DI C AL CENTRO
 LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
Scambi gassosi e regolazione del respiro
 Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I Scambi gassosi e regolazione del respiro Ruolo del Sistema Respiratorio: - fornire O 2 - rimuovere CO 2 Scaricato da www.sunhope.it
Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I Scambi gassosi e regolazione del respiro Ruolo del Sistema Respiratorio: - fornire O 2 - rimuovere CO 2 Scaricato da www.sunhope.it
STRUTTURA E FUNZIONE DELLE PROTEINE
 STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH
 Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( OO) nella stessa molecola 3 N 2 α * OO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-himica Organica 1 Amminoacidi
Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( OO) nella stessa molecola 3 N 2 α * OO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-himica Organica 1 Amminoacidi
L ACQUA E LE SUE PROPRIETÀ
 L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
scaricato da www.sunhope.it Proteine semplici costituite dai soli amminoacidi
 Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
La struttura delle proteine
 La struttura delle proteine Funzioni delle proteine Strutturali Contrattili Trasporto Riserva Ormonali Enzimatiche Protezione Struttura della proteina Struttura secondaria: ripiegamento locale della catena
La struttura delle proteine Funzioni delle proteine Strutturali Contrattili Trasporto Riserva Ormonali Enzimatiche Protezione Struttura della proteina Struttura secondaria: ripiegamento locale della catena
DISTRIBUZIONE DELLA PERFUSIONE POLMONARE DISTRIBUZIONE DELLA VENTILAZIONE POLMONARE DEFINIRE LA COMPLIANCE POLMONARE
 VOLUMI POLMONARI DISTRIBUZIONE DELLA PERFUSIONE POLMONARE DISTRIBUZIONE DELLA VENTILAZIONE POLMONARE DEFINIRE LA COMPLIANCE POLMONARE DEFINIRE LE RESISTENZE POLMONARI DEFINIRE IL LAVORO POLMONARE Equazione
VOLUMI POLMONARI DISTRIBUZIONE DELLA PERFUSIONE POLMONARE DISTRIBUZIONE DELLA VENTILAZIONE POLMONARE DEFINIRE LA COMPLIANCE POLMONARE DEFINIRE LE RESISTENZE POLMONARI DEFINIRE IL LAVORO POLMONARE Equazione
Cr Mn Fe Co Ni Cu Zn. Chimica Inorganica Biologica Vita ed Energia
 Vita ed Energia I processi chimici alla base della chimica della vita sono due: Uso dell E solare per produrre materia e O 2 da CO 2 e H 2 O Produzione di E mediante ossidazione di materia con formazione
Vita ed Energia I processi chimici alla base della chimica della vita sono due: Uso dell E solare per produrre materia e O 2 da CO 2 e H 2 O Produzione di E mediante ossidazione di materia con formazione
Le macromolecole dei tessuti - 1
 Le macromolecole dei tessuti - 1 Che cosa sono le proteine? Sono macromolecole complesse ad alta informazione Sono costituite da una o più catene polipeptidiche Ogni catena peptidica è composta da centinaia
Le macromolecole dei tessuti - 1 Che cosa sono le proteine? Sono macromolecole complesse ad alta informazione Sono costituite da una o più catene polipeptidiche Ogni catena peptidica è composta da centinaia
Il trasporto dell ossigeno
 Prof. Giorgio Sartor Il trasporto dell ossigeno Copyright 2001-2016 by Giorgio Sartor. All rights reserved. Versione 1.9.2 mar 2016 Trasporto dell ossigeno egli organismi aerobi il trasporto dell ossigeno
Prof. Giorgio Sartor Il trasporto dell ossigeno Copyright 2001-2016 by Giorgio Sartor. All rights reserved. Versione 1.9.2 mar 2016 Trasporto dell ossigeno egli organismi aerobi il trasporto dell ossigeno
Rapporto Struttura/Funzione delle Proteine
 Macromolecole Biologiche Chimica Biologica A.A. 2010-2011 Rapporto Struttura/Funzione delle Proteine Struttura/Funzione delle Proteine Interazioni proteina-ligando come base della funzione di molte proteine
Macromolecole Biologiche Chimica Biologica A.A. 2010-2011 Rapporto Struttura/Funzione delle Proteine Struttura/Funzione delle Proteine Interazioni proteina-ligando come base della funzione di molte proteine
9) Scrivere un disaccaride formato dal β-d-galattosio e dall α-d-n-acetil-glucosammina legati da un legame glicosidico β(1-4).
 CARBOIDRATI - AMMINOACIDI - PROTEINE 1) Scrivere la proiezione di Fisher del D-ribosio e del D-glucosio. La lettera D a cosa si riferisce? Disegnare inoltre il disaccaride ottenuto dalla condensazione
CARBOIDRATI - AMMINOACIDI - PROTEINE 1) Scrivere la proiezione di Fisher del D-ribosio e del D-glucosio. La lettera D a cosa si riferisce? Disegnare inoltre il disaccaride ottenuto dalla condensazione
Composti organici. I composti organici. Atomi e molecole di carbonio. Atomi e molecole di carbonio. Gruppi funzionali. Isomeri
 I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
Trasporto dei gas respiratori nel sangue
 Trasporto dei gas respiratori nel sangue La soluzione dei gas nei liquidi C Legge di Henry acq P gas S gas C acq = quantità di gas disciolta nella fase acquosa P gas = pressione parziale del gas nella
Trasporto dei gas respiratori nel sangue La soluzione dei gas nei liquidi C Legge di Henry acq P gas S gas C acq = quantità di gas disciolta nella fase acquosa P gas = pressione parziale del gas nella
Struttura delle Proteine
 Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
Mutazioni genetiche 2
 Mutazioni genetiche 2 Cosa sono le mutazioni? Le proteine sono in grado di svolgere la loro funzione solo se la loro sequenza amminoacidica è quella corretta. In caso contrario si possono generare delle
Mutazioni genetiche 2 Cosa sono le mutazioni? Le proteine sono in grado di svolgere la loro funzione solo se la loro sequenza amminoacidica è quella corretta. In caso contrario si possono generare delle
le porzioni con strutture secondarie sono avvicinate e impaccate mediante anse e curve della catena. STRUTTURA TERZIARIA
 STRUTTURA TERZIARIA le porzioni con strutture secondarie sono avvicinate e impaccate mediante anse e curve della catena. Le proteine globulari dopo aver organizzato il proprio scheletro polipeptidico con
STRUTTURA TERZIARIA le porzioni con strutture secondarie sono avvicinate e impaccate mediante anse e curve della catena. Le proteine globulari dopo aver organizzato il proprio scheletro polipeptidico con
Diagramma di Ramachandran
 Chimica Biologica A.A. 2010-2011 Diagramma di Ramachandran Diagramma di Ramachandran Catena polipeptidica La formazione in successione di legami peptidici genera la cosiddetta catena principale o scheletro
Chimica Biologica A.A. 2010-2011 Diagramma di Ramachandran Diagramma di Ramachandran Catena polipeptidica La formazione in successione di legami peptidici genera la cosiddetta catena principale o scheletro
ENZIMI. Un enzima è un catalizzatore (acceleratore) di reazioni biologiche.
 ENZIMI ENZIMI Un enzima è un catalizzatore (acceleratore) di reazioni biologiche. Catalizzatore = sostanza in grado di accelerare lo svolgimento di una reazione chimica e quindi di aumentarne la sua velocità,
ENZIMI ENZIMI Un enzima è un catalizzatore (acceleratore) di reazioni biologiche. Catalizzatore = sostanza in grado di accelerare lo svolgimento di una reazione chimica e quindi di aumentarne la sua velocità,
PROTEINE DEFINIZIONE:
 Cap.4 Le PROTEINE DEFINIZIONE: Macromolecole formate di AA della serie L uniti tra loro da un legame peptidico. FUNZIONI DELLE PROTEINE Enzimi Proteine di riconoscimento Proteine di trasporto Proteine
Cap.4 Le PROTEINE DEFINIZIONE: Macromolecole formate di AA della serie L uniti tra loro da un legame peptidico. FUNZIONI DELLE PROTEINE Enzimi Proteine di riconoscimento Proteine di trasporto Proteine
Amminoacidi. Struttura base di un a-amminoacido
 Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Chimotripsina Una proteina globulare. Glicina Un amminoacido
 Chimotripsina Una proteina globulare Glicina Un amminoacido - In teoria un numero enorme di differenti catene polipeptidiche potrebbe essere sintetizzato con i 20 amminoacidi standard. 20 4 = 160.000 differenti
Chimotripsina Una proteina globulare Glicina Un amminoacido - In teoria un numero enorme di differenti catene polipeptidiche potrebbe essere sintetizzato con i 20 amminoacidi standard. 20 4 = 160.000 differenti
ENZIMI. Durante la reazione l enzima può essere temporaneamente modificato ma alla fine del processo ritorna nel suo stato originario, un enzima viene
 ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari, e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari, e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
CARBOIDRATI C H O ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO
 CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
Organizzazione del genoma umano
 Organizzazione del genoma umano Famiglie di geni o geniche Copie multiple di geni, tutte con sequenza identica o simile. La famiglia multigenica corrisponde a un insieme di geni correlati che si sono evoluti
Organizzazione del genoma umano Famiglie di geni o geniche Copie multiple di geni, tutte con sequenza identica o simile. La famiglia multigenica corrisponde a un insieme di geni correlati che si sono evoluti
Gli elementi corpuscolati del sangue sono vere cellule o derivati cellulari.
 I GLOBULI ROSSI Gli elementi corpuscolati del sangue sono vere cellule o derivati cellulari. I globuli rossi sono i più numerosi (5 milioni per mm 3 nell uomo, 4.5 milioni per mm 3 nella donna) sono detti
I GLOBULI ROSSI Gli elementi corpuscolati del sangue sono vere cellule o derivati cellulari. I globuli rossi sono i più numerosi (5 milioni per mm 3 nell uomo, 4.5 milioni per mm 3 nella donna) sono detti
Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi)
 ENZIMI Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi) Sono in grado di aumentare la velocità dei processi catalizzati fino a
ENZIMI Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi) Sono in grado di aumentare la velocità dei processi catalizzati fino a
Aminoacidi. Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α
 Aminoacidi Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α 1 Isomeria ottica Tutti gli AA, esclusa la glicina, presentano almeno un atomo di carbonio asimmetrico, il
Aminoacidi Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α 1 Isomeria ottica Tutti gli AA, esclusa la glicina, presentano almeno un atomo di carbonio asimmetrico, il
Polimorfismo genetico del collageno
 COLLAGENO È la proteina più abbondante del nostro corpo costituendo il 25% delle proteine totali. È la proteina principale dei tessuti connettivi, la cui matrice extracellulare contiene anche: -proteoglicani
COLLAGENO È la proteina più abbondante del nostro corpo costituendo il 25% delle proteine totali. È la proteina principale dei tessuti connettivi, la cui matrice extracellulare contiene anche: -proteoglicani
Amminoacidi Peptidi Proteine
 Amminoacidi Peptidi Proteine Amminoacidi-Peptidi-Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Stereoisomeri: composti con la stessa connessione tra gli atomi, ma con una differente
Amminoacidi Peptidi Proteine Amminoacidi-Peptidi-Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Stereoisomeri: composti con la stessa connessione tra gli atomi, ma con una differente
IL LEGAME CHIMICO. Per descrivere come gli elettroni si distribuiscono nell atomo attorno al nucleo si può far riferimento al MODELLO A GUSCI
 IL LEGAME CIMICO Come dagli atomi si costruiscono le molecole 02/19/08 0959 PM 1 Per descrivere come gli elettroni si distribuiscono nell atomo attorno al nucleo si può far riferimento al MODELLO A GUSCI
IL LEGAME CIMICO Come dagli atomi si costruiscono le molecole 02/19/08 0959 PM 1 Per descrivere come gli elettroni si distribuiscono nell atomo attorno al nucleo si può far riferimento al MODELLO A GUSCI
L APPARATO CIRCOLATORIO
 L APPARATO CIRCOLATORIO Il sangue Il sangue è un tessuto liquido connettivo (presenza di importante materia extracellulare), formato da una parte liquida, il plasma e una parte corpuscolare formata da
L APPARATO CIRCOLATORIO Il sangue Il sangue è un tessuto liquido connettivo (presenza di importante materia extracellulare), formato da una parte liquida, il plasma e una parte corpuscolare formata da
Trasporto dell ossigeno
 Prof. Giorgio Sartor Trasporto dell ossigeno Copyright 2001-2011 by Giorgio Sartor. All rights reserved. Versione 0.1 oct 2011 Trasporto dell ossigeno egli organismi aerobi il trasporto dell ossigeno avviene
Prof. Giorgio Sartor Trasporto dell ossigeno Copyright 2001-2011 by Giorgio Sartor. All rights reserved. Versione 0.1 oct 2011 Trasporto dell ossigeno egli organismi aerobi il trasporto dell ossigeno avviene
Legame covalente Puro Polare Legame dativo o di coordinazione Legame ionico Legame metallico
 I LEGAMI CHIMICI Legami atomici o forti Legami molecolari o deboli Legame covalente Puro Polare Legame dativo o di coordinazione Legame ionico Legame metallico Legame dipolo-dipolo Legame idrogeno Legame
I LEGAMI CHIMICI Legami atomici o forti Legami molecolari o deboli Legame covalente Puro Polare Legame dativo o di coordinazione Legame ionico Legame metallico Legame dipolo-dipolo Legame idrogeno Legame
La chimica della pelle
 La chimica della pelle 1 Gli amminoacidi Queste unità hanno la particolare caratteristica di contenere nella stessa molecola un gruppo acido (- COOH) ed uno basico (- NH 2 ), legati tra loro attraverso
La chimica della pelle 1 Gli amminoacidi Queste unità hanno la particolare caratteristica di contenere nella stessa molecola un gruppo acido (- COOH) ed uno basico (- NH 2 ), legati tra loro attraverso
ERITROCITI STRUTTURA E METABOLISMO
 ERITROCITI STRUTTURA E METABOLISMO Il globulo rosso maturo ha una struttura molto semplice perché sfornito di nucleo e degli organuli citoplasmatici Dott.ssa M. COPPOLA Dott.ssa C. CRISCUOLO LA MEMBRANA
ERITROCITI STRUTTURA E METABOLISMO Il globulo rosso maturo ha una struttura molto semplice perché sfornito di nucleo e degli organuli citoplasmatici Dott.ssa M. COPPOLA Dott.ssa C. CRISCUOLO LA MEMBRANA
FORMAZIONE DEL LEGAME PEPTIDICO
 AMINOACIDI FORMAZIONE DEL LEGAME PEPTIDICO SEQUENZA AMINOACIDICA DELL INSULINA STRUTTURA SECONDARIA DELLE PROTEINE STRUTTURA TERZIARIA DELLE PROTEINE STRUTTURA QUATERNARIA DELLE PROTEINE Definizione Processi
AMINOACIDI FORMAZIONE DEL LEGAME PEPTIDICO SEQUENZA AMINOACIDICA DELL INSULINA STRUTTURA SECONDARIA DELLE PROTEINE STRUTTURA TERZIARIA DELLE PROTEINE STRUTTURA QUATERNARIA DELLE PROTEINE Definizione Processi
Corso di Chimica e Propedeutica Biochimica Reazioni in soluzione acquosa
 Corso di Chimica e Propedeutica Biochimica Reazioni in soluzione acquosa Alcune immagini sono state prese e modificate da Chimica di Kotz, Treichel & Weaver, Edises 2007, III edizione 1 Ioni in soluzione
Corso di Chimica e Propedeutica Biochimica Reazioni in soluzione acquosa Alcune immagini sono state prese e modificate da Chimica di Kotz, Treichel & Weaver, Edises 2007, III edizione 1 Ioni in soluzione
Cos è un trasformazione chimica?
 Chimica Lezione 1 Cos è un trasformazione chimica? Una reazione chimica è una trasformazione della materia che avviene senza variazioni misurabili di massa, in cui uno o più reagenti iniziali modificano
Chimica Lezione 1 Cos è un trasformazione chimica? Una reazione chimica è una trasformazione della materia che avviene senza variazioni misurabili di massa, in cui uno o più reagenti iniziali modificano
EMOGLOBINA ... www.pianetachimica.it
 EMGLBIA www.pianetachimica.it L'emoglobina è una proteina specializzata nel trasporto di ossigeno, si trova all interno dei globuli rossi del sangue ai quali conferisce il caratteristico colore rosso intenso.
EMGLBIA www.pianetachimica.it L'emoglobina è una proteina specializzata nel trasporto di ossigeno, si trova all interno dei globuli rossi del sangue ai quali conferisce il caratteristico colore rosso intenso.
Le proteine che legano ossigeno: 2) emoglobina. identità di sequenza: 18%
 Le proteine che legano ossigeno: 2) emoglobina identità di sequenza: 18% Il legame dell ossigeno all emoglobina Fisiologicamente (2%) o per effetto di sostanze ossidanti, lo ione Fe2+ si trasforma in
Le proteine che legano ossigeno: 2) emoglobina identità di sequenza: 18% Il legame dell ossigeno all emoglobina Fisiologicamente (2%) o per effetto di sostanze ossidanti, lo ione Fe2+ si trasforma in
Le interazioni deboli:
 Le interazioni deboli: sono legami non covalenti sono da 1 a 3 ordini di grandezza più deboli dei legami covalenti sono alcune volte maggiori della tendenza a dissociare dovuta all agitazione termica delle
Le interazioni deboli: sono legami non covalenti sono da 1 a 3 ordini di grandezza più deboli dei legami covalenti sono alcune volte maggiori della tendenza a dissociare dovuta all agitazione termica delle
Legami chimici. Covalente. Legami deboli
 Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici STRUTTURA TERZIARIA La struttura tridimensionale
Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici STRUTTURA TERZIARIA La struttura tridimensionale
LE PROTEINE SINTESI PROTEICA. funzione delle proteine nel nostro organismo
 LE PTEIE Le proteine sono sostanze organiche presenti in tutte le cellule di tutti gli organismi viventi Le proteine sono costituite da,,,, (S) Struttura delle proteine Le proteine sono macromolecole (
LE PTEIE Le proteine sono sostanze organiche presenti in tutte le cellule di tutti gli organismi viventi Le proteine sono costituite da,,,, (S) Struttura delle proteine Le proteine sono macromolecole (
