Chimica Biologica A.A Cinetica Enzimatica. Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano
|
|
|
- Gianluigi Manfredi
- 7 anni fa
- Visualizzazioni
Transcript
1 Chimica Biologica A.A Cinetica Enzimatica Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano
2 Macromolecole Biologiche Cinetica Chimica Termodinamica: fornisce informazioni sulla spontaneità e sulle condizioni di equilibrio di una reazione (che dipendono dalle caratteristiche di reagenti e prodotti) Cinetica chimica: fornisce informazioni sulla velocità con cui una reazione avviene (questa dipende dalle modalità con cui una reazione avviene, ovvero dal meccanismo di reazione)
3 Macromolecole Biologiche Cinetica Chimica Cinetica chimica reazione con stechiometria totale: A P A reagenti P prodotti A I 1 I 2 P I intermedi di reazione - una qualsiasi reazione, per quanto complessa, può essere scomposta in una serie di reazioni elementari - l insieme di questi passaggi rappresenta il meccanismo di quella reazione - per una reazione elementare la velocità dipende in maniera semplice dalla concentrazione dei reagenti (legge di velocità): aa + bb + zz P v = k[a] a [B] b [Z] z
4 Macromolecole Biologiche Cinetica Chimica Cinetica chimica aa + bb + zz P v = k[a] a [B] b [Z] z v: velocità istantanea di comparsa del prodotto e scomparsa del reagente k: costante di velocità - Ordine di una reazione : grado algebrico della legge di velocità - Molecolarità: numero di molecole che devono collidere per dar luogo alla reazione - per una reazione elementare l ordine corrisponde con la molecolarità
5 Cinetica Chimica Cinetica chimica - reazione del primo ordine: A P velocità della reazione v = d[p]/dt = -d[a]/dt = k[a] T = cost - v (Ms -1 ) k = costante di velocità (primo ordine) (s -1 )
6 Cinetica Chimica Cinetica chimica - reazione del secondo ordine: 2A P velocità della reazione v = d[p]/dt = -d[a]/dt = k[a] 2 T = cost - v (Ms -1 ) k = costante di velocità (secondo ordine) (M -1 s -1 ) - reazione del secondo ordine: A + B P v = d[p]/dt = -d[a]/dt = -d[b]/dt = k[a][b] T = cost - reazione del secondo ordine totale, del primo ordine per [A] e per [B] - le reazioni trimolecolari sono rare
7 Cinetica Chimica Cinetica chimica Equazione di velocità - descrive il progredire di una reazione nel tempo - reazione del primo ordine: v = -d[a]/dt = k[a] [A] t d[a]/[a] = - k dt d ln[a] = -k dt d ln[a] = -k dt [A 0 ] ln[a] - ln[a 0 ] = -kt eq. lineare [A] = [A 0 ] exp (-kt) 0
8 Cinetica Chimica Cinetica chimica - reazione del secondo ordine: v = -d[a]/dt = k[a] 2 [A] -d[a]/[a] 2 = k dt - d [A]/[A] 2 = k dt [A 0 ] 1/[A] = 1/[A 0 ] + kt equazione lineare - costruendo i grafici di ln [A] e di 1/[A] in funzione di t si distinguono le reazioni del primo e secondo ordine (quale delle 2 è lineare) e si determina la costante di velocità - reazione del secondo ordine: A + B P se [B]>>[A] pseudo-reazione del primo ordine rispetto ad A ([B] cost. durante la reazione) analogamente per B t 0
9 Cinetica Chimica Cinetica chimica t 1/2 (emivita o tempo di dimezzamento) tempo necessario affinché metà del reagente si sia trasformato in prodotto - reazione del primo ordine: t 1/2 costante, indipendente da [A 0 ] ln[a] - ln[a 0 ] = -kt ln (1/2) = -k t t 1/2 1/2 = (ln 2)/k = 0.693/k - le sostanze instabili (nuclei radioattivi) si decompongono con reazioni del primo ordine - reazione del secondo ordine: t 1/2 dipende da [A 0 ] 1/[A] = 1/[A 0 ] + kt t 1/2 = 1/k [A 0 ]
10 Reazione catalizzata da enzimi: (reazioni ad 1 substrato) curva di saturazione del substrato Cinetica enzimatica -[S] bassa v proporzionale ad [S] - [S] aumenta v non aumenta proporzionalmente ad [S] - [S] alta v indipendente da [S] effetto di saturazione ogni molecola di enzima ha il sito di legame del substrato occupato da S reazione del primo ordine non catalizzata
11 quindi quando [S] è elevata la v diventa inipendente da [S], cioè è di ordine zero rispetto al substrato la reazione può essere pensata divisa in 2 reazioni elementari: k i = costanti di velocità per le reazioni k 1 k 2 E + S ES E + P Assunzione 1) - l enzima E ed il substrato S si associano reversibilmente a formare il complesso enzima-substrato ES ( complesso di Michaelis ) k -1 - il prodotto P si forma in un secondo momento, quando ES si rompe a dare E + P - se [S] è elevata, tutto l enzima è nella forma ES la seconda tappa limita la velocità di reazione, che sarà insensibile ad aumenti di [S] k -2
12 k 1 k 2 E + S ES E + P k -1 Assunzione 2): la seconda reazione sia irreversibile misure di velocità iniziale v 0 -v 0 si ha fintanto che <10% del substrato è stato trasformato in prodotto (cioè prima che P si accumuli, visto che la velocità inversa è prop. a [P]) si minimizzano gli effetti delle reazioni reversibili (inibizione da parte del prodotto e progressiva inattivazione)
13 Teoria di Michaelis-Menten k 1 k 2 E + S ES E + P k -1 Cinetica Enzimatica - Equazione di Michaelis-Menten velocità di reazione: v = d[p]/dt = k 2 [ES] velocità di formazione del prodotto [ES] = conc. intermedio precedente k 2 = costante di velocità d[es]/dt = k 1 [E][S] k -1 [ES] k 2 [ES] velocità complessiva di produzione di ES Per integrarla occorre fare alcune assunzioni
14 Assunzione dello stato stazionario: se [S]>>[E] (quasi sempre vero in condizioni fisiologiche) d[es]/dt = 0 (la velocità di sintesi e di consumo di ES sono uguali) dopo pochi ms
15 k 1 k 2 E + S ES E + P k -1 (stato stazionario) d[es]/dt = k 1 [E][S] k -1 [ES] k 2 [ES] = 0 k 1 [E][S] = [ES] (k -1 + k 2 ) K M = costante di Michaelis (k -1 + k 2 ) [E][S] K M = = = [ES] k 1 [E T ] - [ES] [ES] [S] dove [E T ] = [E]+[ES] [ES] = [E] T [S] K M + [S]
16 [ES] = [E] T [S] K M + [S] [E T ] facilmente misurabile, [E] ed [ES] non direttamente misurabili v 0 = d[p]/dt t=0 = k 2 [ES] v 0 = k [E] 2 T [S] KM + [S] V MAX = k 2 [E] T velocità massima di una reazione (quando l enzima è totalmente nella forma ES ed [S] è elevata) Eq. di Michaelis-Menten v 0 = V MAX [S] K M + [S] iperbole rettangolare
17 v 0 = V MAX [S] K M + [S] -v 0, in qualsiasi istante, è determinata dal rapporto fra 2 costanti (K M e V MAX ) e la concentrazione del substrato [S] in quell istante - se [S] = K M v 0 = V MAX /2 definizione operativa di K M K M è la conc. del substrato per cui la velocità della reazione è metà di quella massima
18 dalla curva di saturazione del substrato si possono ricavare V MAX e K M ma solo in modo approssimato necessarie [S] troppo elevate (v = 0.99 V MAX se [S] = 99 K M ) [S] >> K M v = V MAX (indipendente da [S] cinetica di ordine 0) [S] < K M v = k [S] con k = V MAX /K M cinetica del primo ordine) -K M unico per ciascuna coppia enzima-substrato -K M diverso per diversi substrati che reagiscono con lo stesso enzima -K M dipende da T e ph
19 k 1 k 2 E + S ES E + P k -1 k -1 (k -1 + k 2 ) k K M = = + 2 k = K S + 2 k 1 k 1 k 1 k 1 k KS = -1 costante di dissociazione del complesso di Michaelis ES k 1 Se K S diminuisce aumenta la affinità dell enzima per il substrato k 2 k 1 Se KS >> cioè k 2 < k -1 K M è anche una misura di affinità dell enzima per il suo substrato (assunzione dell equilibrio, perché la reazione ES P più lenta di ES E+S, cioè prima che la reazione ES P proceda si è creato un equilibrio fra [ES] e [E][S])
20 Riassumendo: K M e V max, una volta noti, definiscono la velocità della reazione enzimatica ammesso che: 1) la reazione coinvolga un solo substrato (in casi multisubstrato varia solo la conc. di un substrato e gli altri sono tenuti costanti) 2) la reazione ES E+P è irreversibile (o esperimento limitato a quando [P]=0) 3) vale l assunzione dello stato stazionario. Vero se [S 0 ]>[E T ] ed [E T ] costante 4) T, ph, forza ionica ecc che possono influenzare la velocità di reazione sono mantenute costanti - l analisi cinetica dello stato stazionario non è in grado di stabilire in modo certo il meccanismo di reazione. - in particolare non è in grado di definire natura e numero di intermedi, che devono essere determinati in altro modo (es: tecniche spettrofotometriche)
21 Numero di turnover ed efficienza catalitica Si definisce la costante catalitica k cat = V MAX [E] T numero di turnover - numero di molecole di substrato convertite in prodotto (numero di processi di reazione) per molecola di enzima per unità di tempo quando l enzima è saturato con il substrato -k cat ha le dimensioni del reciproco di un tempo (s -1 ) ES Ciclo catalitico dell enzima S E P
22 Numero di turnover ed efficienza catalitica numero di turnover k cat = V MAX [E] T - misura della massima attività catalitica - nel modello di reazione di Michaelis-Menten k cat = k 2 essendo V MAX = k 2 [E] T - per [S] saturanti, nota V MAX ed ammesso sia nota la [E T ] nella miscela di reazione si può calcolare k cat, che è una costante, mentre V MAX dipende dalla concentrazione dell enzima (cresce al crescere di [E T ])
23 Numero di turnover ed efficienza catalitica - in condizioni fisiologiche [S] è raramente saturante (in vivo [S]/K M ~ i siti attivi spesso non sono saturati dal substrato) - si usa il rapporto k cat /K M come indice dell efficienza catalitica per enzimi che rispettano la cinetica di Michaelis-Menten ed operano al di sotto della saturazione -se[s]<<k M si formerà poco complesso ES [E] ~ [E] T Cinetica Enzimatica v 0 ~k [E] 2 T [S] KM + [S] k cat v 0 ~ KM [E] [S] k cat /K M costante di velocità del secondo ordine apparente per la reazione di E ed S a formare il prodotto la velocità della reazione varia direttamente in base a quanto spesso l enzima incontra il substrato
24 Numero di turnover ed efficienza catalitica k 1 k 2 E + S ES E + P k -1 K M = (k -1 + k 2 ) k 1 k k cat = 1 k 2 (k + k ) -1 2 K M k1 - la decomposizione di ES in E + P non può avvenire più frequentemente di quanto E ed S si incontrino per formare ES l efficienza catalitica di un enzima non può essere superiore alla velocità (controllata dalla diffusione) con cui E ed S si combinano a dare ES - gli enzimi più efficienti hanno k cat /K M intorno a 10 8 M -1 s -1 (catalizzano una reazione quasi ogni volta che l enzima incontra il substrato Perfezione catalitica )
25 Analisi dei dati Cinetici Cinetica Enzimatica v 0 = V MAX [S] K M + [S] dalla curva di saturazione si ha solo una stima approssimata di V MAX e K M a causa dell andamento asintottico della curva (v 0 = 0.91 V MAX se [S] = 10 K M ) sottostima di V MAX
26 Grafico dei doppi reciproci (Lineweaver-Burk) v 0 = V MAX [S] K M + [S] 1 v 0 K M 1 = + [S] V MAX 1 V MAX - migliori misurazioni ottenute fra 0.5 K M < [S] < 5 K M - importante rappresentazione visiva dati cinetici Es: non-linearità se cinetica Michaelis-Menten (enzimi allosterici) - problemi: per [S] piccoli, piccoli errori in v o risultano in grossi errori in 1/v o punti sper. concentrati (affollamento per [S] grandi)
27 Reazioni a 2 substrati - di solito gli enzimi catalizzano reazioni in cui sono coinvolti 2 o più substrati e portano alla formazione di prodotti multipli - reazioni a 2 substrati (e 2 prodotti): (~60% delle reazioni enzimatiche conosciute) la maggior parte: - reazioni di trasferimento di un gruppo funzionale - reazioni di ossido-riduzione (trasferimento equivalenti riducenti tra i 2 substrati) E A + B P + Q E P-X + B P + B-X - 2 possibili reazioni: (a) Reazioni sequenziali (o a sostituzione singola ) (b) Reazioni a ping-pong (o a doppia sostituzione ) - Reazioni multisubstrato: si scompone la reazione in una serie di stadi ciascuno dei quali obbedisce a meccanismi a singola o doppia sostituzione
28 Reazioni sequenziali - tutti i substrati si devono combinare con l enzima prima che possa avvenire la reazione e che vengano rilasciati i prodotti E + A + B AEB PEQ E + P + Q - sostituzione singola perché il gruppo X verrebbe trasferito direttamente da A (P-X) a B formando P e Q (B-X) - 2 possibili meccanismi: (a) Meccanismo ordinato (b) Meccanismo casuale
29 Reazioni sequenziali (a) Meccanismo ordinato nomenclatura di Cleland addizione rilascio enzima - ordine obbligato di addizione dei substrati all enzima (esiste un substrato primario il cui legame può favorire il legame per il secondo substrato) Esempio: molte deidrogenasi NAD + o NADP + dipendenti usano il coenzima come substrato primario
30 (b) Meccanismo casuale Reazioni sequenziali - entrambi i siti di legame per i substrati sono presenti nell enzima libero e non c e un substrato primario che si deve legare prima Esempio: molte chinasi operano con un meccanismo a 2 substrati casuale (un substrato è l ATP)
31 Reazioni a ping-pong -il substrato A reagisce con l enzima dando il prodotto P ed una forma modificata F dell enzima E -il substrato B interagisce con F dando il prodotto Q rigenerando E E + A AE FP F FB E + Q P B A e B non si incontrano mai sull enzima - doppia sostituzione perché il gruppo X verrebbe trasferito da A (P-X) prima ad E (F = E-X) e poi a B formando Q (B-X) Esempio: la tripsina usa un meccanismo a ping-pong con F = acil-enzima
Chimica Fisica Biologica
 Chimica Fisica Biologica Università degli Studi di Padova Variazione della concentrazione [1] La variazione nel tempo della composizione di un sistema oggetto della cinetica chimica Le concentrazione delle
Chimica Fisica Biologica Università degli Studi di Padova Variazione della concentrazione [1] La variazione nel tempo della composizione di un sistema oggetto della cinetica chimica Le concentrazione delle
Cine%ca enzima%ca. Copyright 2013 Zanichelli editore S.p.A.
 Cine%ca enzima%ca Copyright 2013 Zanichelli editore S.p.A. La cinetica delle reazioni Conce, chiave Le semplici equazioni di velocità descrivono il progredire delle reazioni di primo e di secondo ordine.
Cine%ca enzima%ca Copyright 2013 Zanichelli editore S.p.A. La cinetica delle reazioni Conce, chiave Le semplici equazioni di velocità descrivono il progredire delle reazioni di primo e di secondo ordine.
TEORIA DELLO STATO DI TRANSIZIONE (Henry Eyring anni 30)
 TEORIA DELLO STATO DI TRANSIZIONE (Henry Eyring anni 30) A + B-C A-B + C (A B C) Complesso attivato Stato di transizione Coordinata di reazione H A H B + H C H A + H B H C A+ K B X k' P + Q [ P] d dt =
TEORIA DELLO STATO DI TRANSIZIONE (Henry Eyring anni 30) A + B-C A-B + C (A B C) Complesso attivato Stato di transizione Coordinata di reazione H A H B + H C H A + H B H C A+ K B X k' P + Q [ P] d dt =
Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi)
 ENZIMI Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi) Sono in grado di aumentare la velocità dei processi catalizzati fino a
ENZIMI Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi) Sono in grado di aumentare la velocità dei processi catalizzati fino a
di piccoli gruppi di molecole di RNA catalitico tutti gli enzimi sono proteine Molti enzimi per poter funzionare richiedono la presenza di cofattori.
 Enzimi Con l eccezione l di piccoli gruppi di molecole di RNA catalitico tutti gli enzimi sono proteine Molti enzimi per poter funzionare richiedono la presenza di cofattori. apoenzima + cofattore = oloenzima
Enzimi Con l eccezione l di piccoli gruppi di molecole di RNA catalitico tutti gli enzimi sono proteine Molti enzimi per poter funzionare richiedono la presenza di cofattori. apoenzima + cofattore = oloenzima
costruire un equazione che potesse descrivere in generale il comportamento cinetico degli enzimi e quindi di determinare parametri cinetici più
 Cinetica Enzimatica OBIETTIVO PRINCIPALE: costruire un equazione che potesse descrivere in generale il comportamento cinetico degli enzimi e quindi di determinare parametri cinetici più importanti (K M,
Cinetica Enzimatica OBIETTIVO PRINCIPALE: costruire un equazione che potesse descrivere in generale il comportamento cinetico degli enzimi e quindi di determinare parametri cinetici più importanti (K M,
ENZIMI. Un enzima è un catalizzatore (acceleratore) di reazioni biologiche.
 ENZIMI ENZIMI Un enzima è un catalizzatore (acceleratore) di reazioni biologiche. Catalizzatore = sostanza in grado di accelerare lo svolgimento di una reazione chimica e quindi di aumentarne la sua velocità,
ENZIMI ENZIMI Un enzima è un catalizzatore (acceleratore) di reazioni biologiche. Catalizzatore = sostanza in grado di accelerare lo svolgimento di una reazione chimica e quindi di aumentarne la sua velocità,
Cinetica chimica E lo studio della velocità delle reazioni chimiche, delle leggi di velocità e dei meccanismi di reazione.
 Cinetica chimica E lo studio della velocità delle reazioni chimiche, delle leggi di velocità e dei meccanismi di reazione. Es. 2H 2(g) + O 2(g) d 2H 2 O (l) K eq (25 C)=10 83 (ricavato da lnk=-δg /RT)
Cinetica chimica E lo studio della velocità delle reazioni chimiche, delle leggi di velocità e dei meccanismi di reazione. Es. 2H 2(g) + O 2(g) d 2H 2 O (l) K eq (25 C)=10 83 (ricavato da lnk=-δg /RT)
GLI ENZIMI: proteine con attività CATALITICA
 Cap. 6 GLI ENZIMI: proteine con attività CATALITICA Catalizzatori biologici: permettono alle reazioni biochimiche di avvenire a temperature e pressioni fisiologiche e a velocità misurabile. Aumentano la
Cap. 6 GLI ENZIMI: proteine con attività CATALITICA Catalizzatori biologici: permettono alle reazioni biochimiche di avvenire a temperature e pressioni fisiologiche e a velocità misurabile. Aumentano la
TUTTI GLI ENZIMI POSSONO ESSERE ANALIZZATI IN MODO DA POTER QUANTIFICARE SIA LA VELOCITA DI REAZIONE CHE LA LORO EFFICIENZA ENZIMATICA
 TUTTI GLI ENZIMI POSSONO ESSERE ANALIZZATI IN MODO DA POTER QUANTIFICARE SIA LA VELOCITA DI REAZIONE CHE LA LORO EFFICIENZA ENZIMATICA Lo studio della cinetica enzimatica inizia nel 1909 con ADRIAN BROWN
TUTTI GLI ENZIMI POSSONO ESSERE ANALIZZATI IN MODO DA POTER QUANTIFICARE SIA LA VELOCITA DI REAZIONE CHE LA LORO EFFICIENZA ENZIMATICA Lo studio della cinetica enzimatica inizia nel 1909 con ADRIAN BROWN
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 20 La velocità di reazione 3 Sommario 1. Che cos è la velocità di reazione 2. L equazione cinetica 3. Gli altri fattori che influiscono
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 20 La velocità di reazione 3 Sommario 1. Che cos è la velocità di reazione 2. L equazione cinetica 3. Gli altri fattori che influiscono
REAZIONI CHIMICHE: LEGGI CINETICHE, MECCANISMI DI REAZIONE E BILANCI DI MASSA
 REAZIONI CHIMICHE: LEGGI CINETICHE, MECCANISMI DI REAZIONE E BILANCI DI MASSA Reazione chimica in condizione di equilibrio: concentrazioni costanti che obbediscono al vincolo determinato dalla costante
REAZIONI CHIMICHE: LEGGI CINETICHE, MECCANISMI DI REAZIONE E BILANCI DI MASSA Reazione chimica in condizione di equilibrio: concentrazioni costanti che obbediscono al vincolo determinato dalla costante
Velocità di reazione Una trasformazione chimica modifica completamente la natura delle sostanze iniziali ( i reagenti), formando altre specie (i prodo
 Dinamica chimica (cinetica) Studio della velocità di reazione Bibliografia David W. Oxtoby, Norman H. Nachtrieb, Wade A. Freeman Chimica Edises Mario Nardelli Chimica generale Darrell D. Ebbing, Steven
Dinamica chimica (cinetica) Studio della velocità di reazione Bibliografia David W. Oxtoby, Norman H. Nachtrieb, Wade A. Freeman Chimica Edises Mario Nardelli Chimica generale Darrell D. Ebbing, Steven
Appendice cap. 29: applicazioni
 2 Analisi chimica strumentale Appendice cap. 29: applicazioni Per una reazione del 1 ordine, l equazione differenziale, ovvero la forma differenziale della legge cinetica, assume la forma d[a]/dt = k [A]
2 Analisi chimica strumentale Appendice cap. 29: applicazioni Per una reazione del 1 ordine, l equazione differenziale, ovvero la forma differenziale della legge cinetica, assume la forma d[a]/dt = k [A]
Le reazioni chimiche
 Le reazioni chimiche Reazioni di sintesi Reazioni di sintesi o di combinazione diretta: A + B à AB. Nelle reazioni di sintesi due o più atomi o molecole reagiscono tra loro per dare un unico composto come
Le reazioni chimiche Reazioni di sintesi Reazioni di sintesi o di combinazione diretta: A + B à AB. Nelle reazioni di sintesi due o più atomi o molecole reagiscono tra loro per dare un unico composto come
ENZIMI. Durante la reazione l enzima può essere temporaneamente modificato ma alla fine del processo ritorna nel suo stato originario, un enzima viene
 ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari, e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari, e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
Ioni inorganici (Mg 2+, Zn 2+ ), o molecole organiche o metallorganiche (coenzimi)
 ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
1/v
 1. Nel seguente grafico sono descritti i risultati di cinetica enzimatica ottenuti in 3 esperimenti condotti in assenza di inibitori e in presenza di un inibitore a due diverse concentrazioni. a) Individuare
1. Nel seguente grafico sono descritti i risultati di cinetica enzimatica ottenuti in 3 esperimenti condotti in assenza di inibitori e in presenza di un inibitore a due diverse concentrazioni. a) Individuare
Università degli Studi Mediterranea di Reggio Calabria Facoltà di Agraria Sez. Lamezia Terme A.A
 1 Università degli Studi Mediterranea di Reggio Calabria Facoltà di Agraria Sez. Lamezia Terme A.A. 2006.2007 La cinetica delle reazioni chimiche Studiare una reazione dal punto di vista cinetico significa
1 Università degli Studi Mediterranea di Reggio Calabria Facoltà di Agraria Sez. Lamezia Terme A.A. 2006.2007 La cinetica delle reazioni chimiche Studiare una reazione dal punto di vista cinetico significa
- utilizzano esclusivamente le reattività chimiche di alcuni residui AA
 Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Gli enzimi e l inibizione enzimatica.
 Gli enzimi e l inibizione enzimatica. Catalisi enzimatica La velocità di una reazione è descritta dall equazione di Arrhenius: k = Ae -Ea/RT in cui A è il fattore pre-esponenziale R è la costante dei gas
Gli enzimi e l inibizione enzimatica. Catalisi enzimatica La velocità di una reazione è descritta dall equazione di Arrhenius: k = Ae -Ea/RT in cui A è il fattore pre-esponenziale R è la costante dei gas
Cinetica Chimica. Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display.
 Cinetica Chimica Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. Cinetica Chimica Termodinamica la reaction avrà luogo? Cinetica quanto sarà veloce la reazione?
Cinetica Chimica Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. Cinetica Chimica Termodinamica la reaction avrà luogo? Cinetica quanto sarà veloce la reazione?
Legge dell azione di massa. Misura sperimentale della costante di equilibrio. Corso di Studi di Fisica Corso di Chimica
 Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Legge dell azione di massa Il caso dei gas: utilizziamo le pressioni parziali Lezione 7-8 1 Per definizione le concentrazioni
Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Legge dell azione di massa Il caso dei gas: utilizziamo le pressioni parziali Lezione 7-8 1 Per definizione le concentrazioni
Catalisi. Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A Modulo di Biologia Strutturale
 Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Catalisi Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie
Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Catalisi Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie
IL MODELLO DI MICHAELIS E MENTEN PER LA CINETICA ENZIMATICA.
 CORSO DI CHIMICA E PROPEDEUTICA BIOCHIMICA FACOLTA DI MEDICINA E CHIRURGIA. IL MODELLO DI MICHAELIS E MENTEN PER LA CINETICA ENZIMATICA. Un enzima è una proteina capace di catalizzare una specifica reazione
CORSO DI CHIMICA E PROPEDEUTICA BIOCHIMICA FACOLTA DI MEDICINA E CHIRURGIA. IL MODELLO DI MICHAELIS E MENTEN PER LA CINETICA ENZIMATICA. Un enzima è una proteina capace di catalizzare una specifica reazione
Il metabolismo: concetti di base
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Il metabolismo: concetti di base Caratteristiche generali Strategie Trofiche Il metabolismo:
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Il metabolismo: concetti di base Caratteristiche generali Strategie Trofiche Il metabolismo:
INTRODUZIONE AL METABOLISMO
 INTRODUZIONE AL METABOLISMO METABOLISMO Il metabolismo (dal greco metabolé = trasformazione) è il complesso delle reazioni chimiche coordinate ed integrate che avvengono in una cellula. Il metabolismo
INTRODUZIONE AL METABOLISMO METABOLISMO Il metabolismo (dal greco metabolé = trasformazione) è il complesso delle reazioni chimiche coordinate ed integrate che avvengono in una cellula. Il metabolismo
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 15 La termodinamica e la cinetica 1. Le reazioni producono energia 2. Il primo principio della
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 15 La termodinamica e la cinetica 1. Le reazioni producono energia 2. Il primo principio della
Introduzione al Metabolismo
 Chimica Biologica A.A. 2010-2011 Introduzione al Metabolismo Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Metabolismo Metabolismo l insieme dei processi attraverso
Chimica Biologica A.A. 2010-2011 Introduzione al Metabolismo Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Metabolismo Metabolismo l insieme dei processi attraverso
Le reazioni chimiche. Lezioni d'autore di Giorgio Benedetti
 Le reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO VIDEO Introduzione (I) La cinetica chimica è la branca della chimica che si interessa della velocità delle reazioni chimiche, cioè la variazione
Le reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO VIDEO Introduzione (I) La cinetica chimica è la branca della chimica che si interessa della velocità delle reazioni chimiche, cioè la variazione
FARMACODINAMICA. La farmacodinamica studia gli effetti biochimici e il meccanismo d azione dei farmaci.
 FARMACODINAMICA La farmacodinamica studia gli effetti biochimici e il meccanismo d azione dei farmaci. La farmacodinamica si propone di: * identificare i siti d azione dei farmaci * delineare le interazioni
FARMACODINAMICA La farmacodinamica studia gli effetti biochimici e il meccanismo d azione dei farmaci. La farmacodinamica si propone di: * identificare i siti d azione dei farmaci * delineare le interazioni
Inibizione Enzimatica
 Chimica Biologica A.A. 2010-2011 Inibizione Enzimatica Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Inibizione enzimatica Inibitori: sostanze che riducono l
Chimica Biologica A.A. 2010-2011 Inibizione Enzimatica Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Inibizione enzimatica Inibitori: sostanze che riducono l
ENZIMI. A + B AB (100 Kcal= E. Attiv.) A + B AB (50 Kcal) SUBSTRATO ENZIMA E N E R G I A
 ENZIMI 1) sono catalizzatori di natura biologica e sono proteine 2) gli enzimi abbassano l energia di attivazione di un solo tipo di reazione senza intervenire nella reazione stessa cioè senza esserne
ENZIMI 1) sono catalizzatori di natura biologica e sono proteine 2) gli enzimi abbassano l energia di attivazione di un solo tipo di reazione senza intervenire nella reazione stessa cioè senza esserne
Enzimi come catalizzatori biologici
 Enzimi come catalizzatori biologici Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. La catalisi procede
Enzimi come catalizzatori biologici Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. La catalisi procede
Prof. Maria Nicola GADALETA
 Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Principi di Biochimica
 Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
Prof. Maria Nicola GADALETA FOSFORILAZIONE OSSIDATIVA 4
 Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche FOSFORILAZIONE
Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche FOSFORILAZIONE
La cinetica chimica. Velocità media di reazione
 La cinetica chimica 1. Velocità di reazione. Leggi cinetiche semplici 3. Meccanismi di reazione 4. Effetto della temperatura: legge di Arrhenius e teoria del complesso attivato 5. Catalizzatori Velocità
La cinetica chimica 1. Velocità di reazione. Leggi cinetiche semplici 3. Meccanismi di reazione 4. Effetto della temperatura: legge di Arrhenius e teoria del complesso attivato 5. Catalizzatori Velocità
Amminoacidi Peptidi Proteine
 Amminoacidi Peptidi Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Gli amminoacidi nelle molecole proteiche sono tutti stereoisomeri L IDROFOBOCI IDROFOBOCI IDROFILICI Secondo gruppo
Amminoacidi Peptidi Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Gli amminoacidi nelle molecole proteiche sono tutti stereoisomeri L IDROFOBOCI IDROFOBOCI IDROFILICI Secondo gruppo
FUNZIONI delle PROTEINE
 FUNZIONI delle PROTEINE Ha le dimensioni del reciproco di una concentrazione (M -1 ) Ha le dimensioni di una concentrazione (M) La frazione dei siti occupati rispetto ai siti totali è definita come θ FRAZIONE
FUNZIONI delle PROTEINE Ha le dimensioni del reciproco di una concentrazione (M -1 ) Ha le dimensioni di una concentrazione (M) La frazione dei siti occupati rispetto ai siti totali è definita come θ FRAZIONE
Fondamenti di Chimica Farmaceutica. Recettori come bersagli dei farmaci
 Fondamenti di Chimica Farmaceutica Recettori come bersagli dei farmaci Recettori come bersaglio dei farmaci I farmaci che agiscono sui recettori: a somiglianza dei farmaci che agiscono sugli enzimi vanno
Fondamenti di Chimica Farmaceutica Recettori come bersagli dei farmaci Recettori come bersaglio dei farmaci I farmaci che agiscono sui recettori: a somiglianza dei farmaci che agiscono sugli enzimi vanno
L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO
 L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 23 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata all emoglobina: L O 2 totale
L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 23 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata all emoglobina: L O 2 totale
CONVENZIONE SUI SEGNI
 CONVENZIONE SUI SEGNI Si stabilisce una convenzione sui segni sia per gli scambi di calore che per il lavoro che il sistema compie o subisce L>0: LAVORO COMPIUTO DAL SISTEMA Q>0: CALORE ASSORBITO SISTEMA
CONVENZIONE SUI SEGNI Si stabilisce una convenzione sui segni sia per gli scambi di calore che per il lavoro che il sistema compie o subisce L>0: LAVORO COMPIUTO DAL SISTEMA Q>0: CALORE ASSORBITO SISTEMA
Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi.
 ENZIMI Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. Svolgono il loro ruolo con modalità differenti
ENZIMI Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. Svolgono il loro ruolo con modalità differenti
INTRODUZIONE AL METABOLISMO. dal gr. metabolè = trasformazione
 INTRODUZIONE AL METABOLISMO dal gr. metabolè = trasformazione IL Metabolismo Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in una cellula o in un organismo. E costituito da
INTRODUZIONE AL METABOLISMO dal gr. metabolè = trasformazione IL Metabolismo Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in una cellula o in un organismo. E costituito da
relazioni tra il calore e le altre forme di energia.
 Termodinamica i Termodinamica: ramo della scienza che studia le relazioni tra il calore e le altre forme di energia. Sistema e ambiente sistema: zona dello spazio all interno della quale studiamo i fenomeni
Termodinamica i Termodinamica: ramo della scienza che studia le relazioni tra il calore e le altre forme di energia. Sistema e ambiente sistema: zona dello spazio all interno della quale studiamo i fenomeni
FUNZIONI BIOLOGICHE DELLE PROTEINE
 FUNZIONI BIOLOGICHE DELLE PROTEINE ENZIMI PROTEINE DI TRASPORTO PROTEINE DI RISERVA PROTEINE CONTRATTILI PROTEINE DI DIFESA PROTEINE REGOLATRICI PROTEINE STRUTTURALI ENERGIA LIBERA (G) ΔG = ΔH - TΔS Variazioni
FUNZIONI BIOLOGICHE DELLE PROTEINE ENZIMI PROTEINE DI TRASPORTO PROTEINE DI RISERVA PROTEINE CONTRATTILI PROTEINE DI DIFESA PROTEINE REGOLATRICI PROTEINE STRUTTURALI ENERGIA LIBERA (G) ΔG = ΔH - TΔS Variazioni
CINETICA CHIMICA. Studio della velocità di trasformazione della materia. Reazioni a velocità intermedia Reazioni organiche s in soluzione
 CINETICA CHIMICA Studio della velocità di trasformazione della materia Reazioni velocissime H + + OH - (acido/base) < 10-8 s Esplosioni (TNT, KClO 4, etc..) Reazioni veloci 10-3 s Reazioni tra ioni in
CINETICA CHIMICA Studio della velocità di trasformazione della materia Reazioni velocissime H + + OH - (acido/base) < 10-8 s Esplosioni (TNT, KClO 4, etc..) Reazioni veloci 10-3 s Reazioni tra ioni in
Termodinamica e termochimica
 Termodinamica e termochimica La termodinamica è una scienza che studia proprietà macroscopiche della materia e prevede quali processi chimici e fisici siano possibili, in quali condizioni e con quali energie
Termodinamica e termochimica La termodinamica è una scienza che studia proprietà macroscopiche della materia e prevede quali processi chimici e fisici siano possibili, in quali condizioni e con quali energie
Regolazione allosterica
 Macromolecole Biologiche Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Regolazione allosterica Marco Nardini Dipartimento
Macromolecole Biologiche Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Regolazione allosterica Marco Nardini Dipartimento
ESERCITAZIONI CHIMICA-FISICA I a.a. 2012/2013. Metodo differenziale. Problema
 ESERCITAZIONI CHIMICA-FISICA I a.a. 0/03 Metodo differenziale Problema Per la reazione: A + B P sono stati condotti tre esperimenti cinetici a diverse concentrazioni iniziali dei reagenti. I valori iniziali
ESERCITAZIONI CHIMICA-FISICA I a.a. 0/03 Metodo differenziale Problema Per la reazione: A + B P sono stati condotti tre esperimenti cinetici a diverse concentrazioni iniziali dei reagenti. I valori iniziali
Termodinamica dei sistemi biologici
 Bioenergetica Termodinamica dei sistemi biologici La bioenergetica è lo studio quantitativo delle trasduzioni energetiche, cioè dei cambiamenti di energia da una forma ad un altra Le trasformazioni biologiche
Bioenergetica Termodinamica dei sistemi biologici La bioenergetica è lo studio quantitativo delle trasduzioni energetiche, cioè dei cambiamenti di energia da una forma ad un altra Le trasformazioni biologiche
REGOLAZIONE ENZIMATICA
 REGOLAZIONE ENZIMATICA Cambio conformazionale In molte molecole proteiche, cambiamenti strutturali possono determinare profondi cambiamenti nella funzione o nell attività. Il cambio conformazionale può
REGOLAZIONE ENZIMATICA Cambio conformazionale In molte molecole proteiche, cambiamenti strutturali possono determinare profondi cambiamenti nella funzione o nell attività. Il cambio conformazionale può
Il trasporto del glucosio
 Il trasporto del glucosio Il glucosio non può diffondere direttamente nelle cellule Esso entra nelle cellule mediante due meccanismi di trasporto: a) diffusione facilitata Na + indipendente b) co-trasporto
Il trasporto del glucosio Il glucosio non può diffondere direttamente nelle cellule Esso entra nelle cellule mediante due meccanismi di trasporto: a) diffusione facilitata Na + indipendente b) co-trasporto
Fisica per scienze ed ingegneria
 Serway, Jewett Fisica per scienze ed ingegneria Capitolo 20 Fino a circa il 1850 su riteneva che la meccanica e la termodinamica fossero due scienze completamente distinte. La legge di conservazione dell
Serway, Jewett Fisica per scienze ed ingegneria Capitolo 20 Fino a circa il 1850 su riteneva che la meccanica e la termodinamica fossero due scienze completamente distinte. La legge di conservazione dell
Helena Curtis N. Sue Barnes
 Helena Curtis N. Sue Barnes LA FOTOSINTESI INDICE Organismi autotrofi ed eterotrofi Confronto tra fotosintesi e respirazione Reazioni endoergoniche ed esoergoniche Reazioni accoppiate Fase luce-dipendente
Helena Curtis N. Sue Barnes LA FOTOSINTESI INDICE Organismi autotrofi ed eterotrofi Confronto tra fotosintesi e respirazione Reazioni endoergoniche ed esoergoniche Reazioni accoppiate Fase luce-dipendente
METODOLOGIA ALLENAMENTO MA7 A.A. 2009/20010 Giovedì 28 Gennaio 13:30 15 II metodologico. Luca P. Ardigò
 METODOLOGIA ALLENAMENTO MA7 A.A. 2009/20010 Giovedì 28 Gennaio 13:30 15 II metodologico Luca P. Ardigò L energia metabolica richiesta (nell unità di tempo) in un dato tipo di gara (su una data distanza)
METODOLOGIA ALLENAMENTO MA7 A.A. 2009/20010 Giovedì 28 Gennaio 13:30 15 II metodologico Luca P. Ardigò L energia metabolica richiesta (nell unità di tempo) in un dato tipo di gara (su una data distanza)
Università di Roma Tor Vergata
 Università di Roma Tor Vergata Facoltà di Ingegneria Dipartimento di Ingegneria Industriale Corso di: TERMOTECNICA TRASMISSIONE DEL CALORE: RESISTENZA DI CONTATTO Ing. G. Bovesecchi gianluigi.bovesecchi@gmail.com
Università di Roma Tor Vergata Facoltà di Ingegneria Dipartimento di Ingegneria Industriale Corso di: TERMOTECNICA TRASMISSIONE DEL CALORE: RESISTENZA DI CONTATTO Ing. G. Bovesecchi gianluigi.bovesecchi@gmail.com
Bilancio di energia: il Primo Principio della Termodinamica. Termodinamica dell Ingegneria Chimica
 Bilancio di energia: il Primo Principio della Termodinamica Termodinamica dell Ingegneria Chimica 1 I Sistemi termodinamici Un sistema è definito da una superficie di controllo, reale o immaginaria, che
Bilancio di energia: il Primo Principio della Termodinamica Termodinamica dell Ingegneria Chimica 1 I Sistemi termodinamici Un sistema è definito da una superficie di controllo, reale o immaginaria, che
Affinità ed efficacia
 Affinità ed efficacia Effetto massimo (percentuale) EC50 Parametri delle curve doseeffetto POTENZA: Sensibilità di un organo o di un tessuto al farmaco EFFICACIA: Effetto massimo raggiungibile con quel
Affinità ed efficacia Effetto massimo (percentuale) EC50 Parametri delle curve doseeffetto POTENZA: Sensibilità di un organo o di un tessuto al farmaco EFFICACIA: Effetto massimo raggiungibile con quel
Determinazione di parametri cinetici di una reazione di dissociazione mediante spettroscopia UV-visibile
 Determinazione di parametri cinetici di una reazione di dissociazione mediante spettroscopia UV-visibile Obiettivo dell'esperienza è la determinazione di parametri cinetici per la reazione di decomposizione
Determinazione di parametri cinetici di una reazione di dissociazione mediante spettroscopia UV-visibile Obiettivo dell'esperienza è la determinazione di parametri cinetici per la reazione di decomposizione
SOLUZIONI DEGLI ESERCIZI
 Niccolò Taddei - Biochimica Capitolo 4 GLI ENZIMI 1 Un enzima è un particolare tipo di proteina con funzione di catalizzatore, cioè è in grado di aumentare la velocità di una reazione chimica. Gli enzimi
Niccolò Taddei - Biochimica Capitolo 4 GLI ENZIMI 1 Un enzima è un particolare tipo di proteina con funzione di catalizzatore, cioè è in grado di aumentare la velocità di una reazione chimica. Gli enzimi
Gli enzimi e la catalisi
 Gli enzimi e la catalisi Distribuzione di energia in una popolazione di molecole Normalmente, le molecole stabili sono per lo più presenti ad un livello di energia relativamente basso Solo una piccola
Gli enzimi e la catalisi Distribuzione di energia in una popolazione di molecole Normalmente, le molecole stabili sono per lo più presenti ad un livello di energia relativamente basso Solo una piccola
Transizioni liquido-solido: Aspetti cinetici
 Transizioni liquido-solido: Aspetti cinetici Prof.G.Marletta Chimica Fisica dei Materiali II e Laboratorio Laurea Magistrale in Chimica dei Materiali Università di Catania A.A. 2011/2012 1- Caratteri generali
Transizioni liquido-solido: Aspetti cinetici Prof.G.Marletta Chimica Fisica dei Materiali II e Laboratorio Laurea Magistrale in Chimica dei Materiali Università di Catania A.A. 2011/2012 1- Caratteri generali
Trasformazioni chimiche degli inquinanti Cenni su stratosfera e troposfera Dinamica degli inquinanti A.A
 Università di Roma Tor Vergata Trasformazioni chimiche degli inquinanti Cenni su stratosfera e troposfera Dinamica degli inquinanti A.A. 2012-2013 1 Composizione chimica dell atmosfera Oltre ad O 2 e N
Università di Roma Tor Vergata Trasformazioni chimiche degli inquinanti Cenni su stratosfera e troposfera Dinamica degli inquinanti A.A. 2012-2013 1 Composizione chimica dell atmosfera Oltre ad O 2 e N
La stechiometria di una reazione chimica relaziona le masse di reagenti e prodotti tenendo conto della legge di conservazione della massa.
 La stechiometria di una reazione chimica relaziona le masse di reagenti e prodotti tenendo conto della legge di conservazione della massa. ChimicaGenerale_lezione17 1 L'Equilibrio Chimico Nella chimica
La stechiometria di una reazione chimica relaziona le masse di reagenti e prodotti tenendo conto della legge di conservazione della massa. ChimicaGenerale_lezione17 1 L'Equilibrio Chimico Nella chimica
ENERGIA LIBERA DI GIBBS (G)
 METABOLISMO: Descrive tutte le numerose reazioni con cui le molecole biologiche sono sintetizzate e degradate, e che permettono di ricavare, accumulare e utilizzare energia Ogni reazione metabolica comporta
METABOLISMO: Descrive tutte le numerose reazioni con cui le molecole biologiche sono sintetizzate e degradate, e che permettono di ricavare, accumulare e utilizzare energia Ogni reazione metabolica comporta
Tra nm Nucleotidi mono-fosfato
 Un estratto proteico può contenere acidi nucleici, nucleotidi Posso verificare la loro presenza mediante la misura di uno spettro di assorbimento. Gli acidi nucleici e i nucleotidi assorbono nell UV, grazie
Un estratto proteico può contenere acidi nucleici, nucleotidi Posso verificare la loro presenza mediante la misura di uno spettro di assorbimento. Gli acidi nucleici e i nucleotidi assorbono nell UV, grazie
Complesso della piruvato deidrogenasi (1) Stechiometria della reazione finale
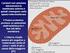 Ciclo di Krebs 1 Complesso della piruvato deidrogenasi (1) Stechiometria della reazione finale 2 Complesso della piruvato deidrogenasi (2) FAD Diidrolipoil deidrogenasi Piruvato decarbossilasi E 3 Diidrolipoil
Ciclo di Krebs 1 Complesso della piruvato deidrogenasi (1) Stechiometria della reazione finale 2 Complesso della piruvato deidrogenasi (2) FAD Diidrolipoil deidrogenasi Piruvato decarbossilasi E 3 Diidrolipoil
CINETICA CHIMICA. ChimicaGenerale_lezione21 1
 CINETICA CHIMICA La cinetica chimica è lo studio della velocità delle reazioni chimiche, cioè della variazione delle concentrazione dei reagenti (o dei prodotti) in funzione del tempo. ChimicaGenerale_lezione21
CINETICA CHIMICA La cinetica chimica è lo studio della velocità delle reazioni chimiche, cioè della variazione delle concentrazione dei reagenti (o dei prodotti) in funzione del tempo. ChimicaGenerale_lezione21
Cap.19. Ciclo di Krebs. o Ciclo degli acidi Tricarbossilici o Ciclo dell acido Citrico
 Cap.19 Ciclo di Krebs o Ciclo degli acidi Tricarbossilici o Ciclo dell acido Citrico Acetil-CoA OSSIDAZIONE DEL GLUCOSIO C 6 H 12 O 6 (glucosio) + 6O 2.. 6CO 2 + 6H 2 O I tappa: GLICOLISI 2 + 2 H 2 O II
Cap.19 Ciclo di Krebs o Ciclo degli acidi Tricarbossilici o Ciclo dell acido Citrico Acetil-CoA OSSIDAZIONE DEL GLUCOSIO C 6 H 12 O 6 (glucosio) + 6O 2.. 6CO 2 + 6H 2 O I tappa: GLICOLISI 2 + 2 H 2 O II
TERMODINAMICA E TERMOCHIMICA
 TERMODINAMICA E TERMOCHIMICA La TERMODINAMICA è una scienza chimico-fisica che studia le trasformazioni dell energia. La TERMOCHIMICA è una particolare branca della termodinamica che valuta quantitativamente
TERMODINAMICA E TERMOCHIMICA La TERMODINAMICA è una scienza chimico-fisica che studia le trasformazioni dell energia. La TERMOCHIMICA è una particolare branca della termodinamica che valuta quantitativamente
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 17
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 17 Enzimi Concetti chiave: Gli enzimi si differenziano dai catalizzatori chimici di uso comune per velocità, condizioni, specificità
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 17 Enzimi Concetti chiave: Gli enzimi si differenziano dai catalizzatori chimici di uso comune per velocità, condizioni, specificità
METABOLISMO CELLULARE
 METABOLISMO CELLULARE Struttura dell ATP (Adenosintrifosfato) Adenina (base azotata), Ribosio (zucchero) e un gruppo fosforico ATP Il legame covalente tra i gruppi fosforici si spezza facilmente liberando
METABOLISMO CELLULARE Struttura dell ATP (Adenosintrifosfato) Adenina (base azotata), Ribosio (zucchero) e un gruppo fosforico ATP Il legame covalente tra i gruppi fosforici si spezza facilmente liberando
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 19 L energia si trasferisce 3 Sommario (I) 1. L «ABC» dei trasferimenti energetici 2. Durante le reazioni varia l energia chimica
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 19 L energia si trasferisce 3 Sommario (I) 1. L «ABC» dei trasferimenti energetici 2. Durante le reazioni varia l energia chimica
Entropia e secondo principio della termodinamica: prevedere la spontaneità di un processo
 1 Entropia e secondo principio della termodinamica: prevedere la spontaneità di un processo Limitazioni della prima legge della termodinamica 2 E = q + w E universo = E sistema + E ambiente E sistema =
1 Entropia e secondo principio della termodinamica: prevedere la spontaneità di un processo Limitazioni della prima legge della termodinamica 2 E = q + w E universo = E sistema + E ambiente E sistema =
U.D. CHIMICA classe 2 a TECN. (CAT) CHIMICA TECNOLOGICO (CAT) PROGRAMMAZIONE ANNUALE: SEQUENZA DI LAVORO
 CHIMICA Classe 2 a TECNOLOGICO (CAT) PROGRAMMAZIONE ANNUALE: SEQUENZA DI LAVORO U.D. Periodo Ore lezione 1. Nomenclatura molecole inorganiche (ripasso) settembre 6 2. Struttura atomica e tavola periodica
CHIMICA Classe 2 a TECNOLOGICO (CAT) PROGRAMMAZIONE ANNUALE: SEQUENZA DI LAVORO U.D. Periodo Ore lezione 1. Nomenclatura molecole inorganiche (ripasso) settembre 6 2. Struttura atomica e tavola periodica
5.1 RUOLO DELLA TERMODINAMICA E DELLA CINETICA 3 5.3 LEGGE DI VELOCITÀ, COSTANTE DI VELOCITÀ E ORDINE DI REAZIONE 7
 Cap. 5 CINETICA E MECCANISMO DELLE REAZIONI DISCONTINUE I N D I C E pag. PREMESSA 3 5.1 RUOLO DELLA TERMODINAMICA E DELLA CINETICA 3 5.2 VELOCITÀ DI REAZIONE E SUA MISURA 4 5.3 LEGGE DI VELOCITÀ, COSTANTE
Cap. 5 CINETICA E MECCANISMO DELLE REAZIONI DISCONTINUE I N D I C E pag. PREMESSA 3 5.1 RUOLO DELLA TERMODINAMICA E DELLA CINETICA 3 5.2 VELOCITÀ DI REAZIONE E SUA MISURA 4 5.3 LEGGE DI VELOCITÀ, COSTANTE
Cos è un trasformazione chimica?
 Chimica Lezione 1 Cos è un trasformazione chimica? Una reazione chimica è una trasformazione della materia che avviene senza variazioni misurabili di massa, in cui uno o più reagenti iniziali modificano
Chimica Lezione 1 Cos è un trasformazione chimica? Una reazione chimica è una trasformazione della materia che avviene senza variazioni misurabili di massa, in cui uno o più reagenti iniziali modificano
DESTINI METABOLICI DEL PIRUVATO
 DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Complesso della Piruvato deidrogenasi
DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Complesso della Piruvato deidrogenasi
Attività elettrica dei neuroni. Neuroni piramidali del SNC che stanno crescendo su una matrice di glia/fibroblasti
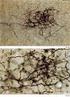 Attività elettrica dei neuroni Neuroni piramidali del SNC che stanno crescendo su una matrice di glia/fibroblasti Un esperimento in current-clamp Si inietta una corrente I di intensità nota nella cellula
Attività elettrica dei neuroni Neuroni piramidali del SNC che stanno crescendo su una matrice di glia/fibroblasti Un esperimento in current-clamp Si inietta una corrente I di intensità nota nella cellula
La pompa sodio-potassio
 a.a. 2005/2006 Laurea Specialistica in Fisica Corso di Fisica Medica 1 La pompa sodio-potassio 14/3/2006 Efficienza del cuore Dipende dall ordinata sequenza di eccitazione e di contrazione che procede
a.a. 2005/2006 Laurea Specialistica in Fisica Corso di Fisica Medica 1 La pompa sodio-potassio 14/3/2006 Efficienza del cuore Dipende dall ordinata sequenza di eccitazione e di contrazione che procede
Molecole e legami. Chimica generale
 Molecole e legami Chimica generale Atomi e molecole È estremamente difficile trovare in natura una sostanza formata solamente da atomi semplici Solo i gas inerti dell ottavo gruppo sono presenti in natura
Molecole e legami Chimica generale Atomi e molecole È estremamente difficile trovare in natura una sostanza formata solamente da atomi semplici Solo i gas inerti dell ottavo gruppo sono presenti in natura
PRINCIPI ELEMENTARI DI ENZIMOLOGIA A. Bellelli, Dipartimento di Scienze Biochimiche A. Rossi Fanelli, Università di Roma Sapienza
 PRINCIPI ELEMENTARI DI ENZIMOLOGIA A. Bellelli, Dipartimento di Scienze Biochimiche A. Rossi Fanelli, Università di Roma Sapienza Come tutti sanno, gli enzimi sono proteine semplici o coniugate capaci
PRINCIPI ELEMENTARI DI ENZIMOLOGIA A. Bellelli, Dipartimento di Scienze Biochimiche A. Rossi Fanelli, Università di Roma Sapienza Come tutti sanno, gli enzimi sono proteine semplici o coniugate capaci
FARMACODINAMICA. La farmacodinamica studia gli effetti biochimici e il meccanismo d azione dei farmaci. identificare i siti d azione dei farmaci
 FARMACODINAMICA La farmacodinamica studia gli effetti biochimici e il meccanismo d azione dei farmaci. La farmacodinamica si propone di: identificare i siti d azione dei farmaci delineare le interazioni
FARMACODINAMICA La farmacodinamica studia gli effetti biochimici e il meccanismo d azione dei farmaci. La farmacodinamica si propone di: identificare i siti d azione dei farmaci delineare le interazioni
DESTINI DEL PIRUVATO
 DESTINI DEL PIRUVATO LA GLICOLISI RILASCIA SOLO UNA PICCOLA PARTE DELL ENERGIA TOTALE DISPONIBILE NELLA MOLECOLA DI GLUCOSIO Le due molecole di piruvato prodotte dalla glicolisi sono ancora relativamente
DESTINI DEL PIRUVATO LA GLICOLISI RILASCIA SOLO UNA PICCOLA PARTE DELL ENERGIA TOTALE DISPONIBILE NELLA MOLECOLA DI GLUCOSIO Le due molecole di piruvato prodotte dalla glicolisi sono ancora relativamente
Capitolo n 5 ELEMENTI DI TERMODINAMICA E DI CINETICA
 Capitolo n 5 ELEMENTI DI TERMODINAMICA E DI CINETICA 5.1 Elementi di Termodinamica chimica 5.1.1 Introduzione alla Termodinamica La Termodinamica è una parte della Fisica che studia i sistemi e le loro
Capitolo n 5 ELEMENTI DI TERMODINAMICA E DI CINETICA 5.1 Elementi di Termodinamica chimica 5.1.1 Introduzione alla Termodinamica La Termodinamica è una parte della Fisica che studia i sistemi e le loro
Cr Mn Fe Co Ni Cu Zn. Chimica Inorganica Biologica Vita ed Energia
 Vita ed Energia I processi chimici alla base della chimica della vita sono due: Uso dell E solare per produrre materia e O 2 da CO 2 e H 2 O Produzione di E mediante ossidazione di materia con formazione
Vita ed Energia I processi chimici alla base della chimica della vita sono due: Uso dell E solare per produrre materia e O 2 da CO 2 e H 2 O Produzione di E mediante ossidazione di materia con formazione
Scritto chimica generale
 Scritto chimica generale 23.01.2012 TESTO A 1. L idrogeno solfuro di ammonio solido si decompone ad ammoniaca gassosa e acido solfidrico gassoso a 25 C. Sapendo che a 25 C la costante per questo equilibrio
Scritto chimica generale 23.01.2012 TESTO A 1. L idrogeno solfuro di ammonio solido si decompone ad ammoniaca gassosa e acido solfidrico gassoso a 25 C. Sapendo che a 25 C la costante per questo equilibrio
Laboratorio Fitness & Wellness
 Laboratorio Fitness & Wellness Anno Accademico 2015/2016 Ewan Thomas, MSc Principi di Bioenergetica e Biomeccanica Metabolismo Catabolismo Processi di degradazione che permettono di liberare energia Anabolismo
Laboratorio Fitness & Wellness Anno Accademico 2015/2016 Ewan Thomas, MSc Principi di Bioenergetica e Biomeccanica Metabolismo Catabolismo Processi di degradazione che permettono di liberare energia Anabolismo
Cinetica chimica. Cinetica chimica
 REAZIONI GLOBALI ED ELEMENTARI: Le reazioni chimiche avvengono quando le molecole di una specie collidono con le molecole di un altra specie e, per effetto di alcune di queste collisioni si formano una
REAZIONI GLOBALI ED ELEMENTARI: Le reazioni chimiche avvengono quando le molecole di una specie collidono con le molecole di un altra specie e, per effetto di alcune di queste collisioni si formano una
L equilibrio chimico
 L equilibrio chimico Vi sono molte reazioni chimiche che non procedono fino a completezza, cioè fino a che uno dei reagenti non si esaurisca, ad esempio la reazione di dimerizzazione del diossido di azoto:
L equilibrio chimico Vi sono molte reazioni chimiche che non procedono fino a completezza, cioè fino a che uno dei reagenti non si esaurisca, ad esempio la reazione di dimerizzazione del diossido di azoto:
Chimica generale Prof. Mario Piccioli
 Chimica generale Prof. Mario Piccioli PROGRAMMA Il modello atomico della materia. Gli individui chimici. Miscele omogenee ed eterogenee. Composti e sostanze elementari. Gli elementi. Le formule delle sostanze.
Chimica generale Prof. Mario Piccioli PROGRAMMA Il modello atomico della materia. Gli individui chimici. Miscele omogenee ed eterogenee. Composti e sostanze elementari. Gli elementi. Le formule delle sostanze.
Chimica e laboratorio
 ITIS H.HERTZ Progetto Monoennio Chimica e laboratorio PARTE PRIMA I MODULO: Struttura atomica e molecolare della materia PESO : 70% UNITA ORARIE PREVISTE : 20 h Unità A: ATOMI Descrivere le caratteristiche
ITIS H.HERTZ Progetto Monoennio Chimica e laboratorio PARTE PRIMA I MODULO: Struttura atomica e molecolare della materia PESO : 70% UNITA ORARIE PREVISTE : 20 h Unità A: ATOMI Descrivere le caratteristiche
CAPITOLO 20 LA CHIMICA NUCLEARE
 CAPITOLO 20 LA CHIMICA NUCLEARE 20.5 (a) La soma dei numeri atomici e la somma dei numeri di massa, da entrambi i lati dell equazione nucleare, deve coincidere. Dalla parte sinistra di questa equazione
CAPITOLO 20 LA CHIMICA NUCLEARE 20.5 (a) La soma dei numeri atomici e la somma dei numeri di massa, da entrambi i lati dell equazione nucleare, deve coincidere. Dalla parte sinistra di questa equazione
Applicazioni biotecnologiche degli enzimi: le lipasi
 Applicazioni biotecnologiche degli enzimi: le lipasi Le lipasi Catalizzano l idrolisi e la sintesi di acilgliceroli Sono stabili in solventi organici Non richiedono cofattori Hanno bassa specificità di
Applicazioni biotecnologiche degli enzimi: le lipasi Le lipasi Catalizzano l idrolisi e la sintesi di acilgliceroli Sono stabili in solventi organici Non richiedono cofattori Hanno bassa specificità di
Sapienza, Università di Roma. Antonella Goggiamani
 Sapienza, Università di Roma CHIMICA ORGANICA Antonella Goggiamani antonella.goggiamani@uniroma1.it Facoltà di Scienze Matematiche, Fisiche e Naturali Corso di Laurea in Scienze Naturali, canale M Z LEZIONI
Sapienza, Università di Roma CHIMICA ORGANICA Antonella Goggiamani antonella.goggiamani@uniroma1.it Facoltà di Scienze Matematiche, Fisiche e Naturali Corso di Laurea in Scienze Naturali, canale M Z LEZIONI
EQUILIBRI DI SOLUBILITA
 EQUILIBRI DI SOLUBILITA Solubilità In generale solo una quantità finita di un solido si scioglie in un dato volume di solvente dando luogo ad una soluzione satura, cioè una soluzione in equilibrio con
EQUILIBRI DI SOLUBILITA Solubilità In generale solo una quantità finita di un solido si scioglie in un dato volume di solvente dando luogo ad una soluzione satura, cioè una soluzione in equilibrio con
Teorie per il calcolo dei coefficienti di trasporto di materia (interfaccia fluido-fluido) Fenomeni di Trasporto
 Teorie per il calcolo dei coefficienti di trasporto di materia (interfaccia fluido-fluido) Fenomeni di Trasporto 1 Teoria del film (Lewis, 1924) Si assume che il trasporto di materia avvenga in uno strato
Teorie per il calcolo dei coefficienti di trasporto di materia (interfaccia fluido-fluido) Fenomeni di Trasporto 1 Teoria del film (Lewis, 1924) Si assume che il trasporto di materia avvenga in uno strato
Introduzione al metabolismo
 Introduzione al metabolismo 1 2 Funzioni del metabolismo 1- Ottenere energia chimica 2- Convertire le molecole 3-Polimerizzare i precursori monomerici 4- Sintetizzare e degradare le biomolecole Il metabolismo
Introduzione al metabolismo 1 2 Funzioni del metabolismo 1- Ottenere energia chimica 2- Convertire le molecole 3-Polimerizzare i precursori monomerici 4- Sintetizzare e degradare le biomolecole Il metabolismo
