Gli Enzimi. catalizzatori biologici rendono possibile da un punto di vista cinetico le reazioni chimiche
|
|
|
- Agnese Giacinta Ceccarelli
- 7 anni fa
- Visualizzazioni
Transcript
1 catalizzatori biologici rendono possibile da un punto di vista cinetico le reazioni chimiche Gli Enzimi Sono le proteine più importanti e più specializzate Presentano un elevato grado di specificità per il substrato Operano in soluzioni acquose con temperature e ph blandi
2 Struttura generale degli enzimi Sono proteine globulari complesse : Addotto enzima-substrato Parte proteica Parte non-proteica Cofattore (ione metallico) Coenzima (natura organica: vitamina o altro) Gruppo Prostetico
3 SITO ATTIVO: specifica porzione dell enzima, deputata al legame con il substrato che porta alla formazione dell addotto ES Addotto ES
4 A(S) B(P) I catalizzatori abbassano l energia di attivazione delle reazioni favoriscono lo stato di transizione formando l addotto ES G prodotti -G substrati ( G ) < 0 Reazione esoergonica
5 Molti catalizzatori non facilitano la formazione dello stato di transizione, ma sostituiscono la reazione difficile con 2 o più reazioni entrambe con uno stato di transizione facile da formare E+S ES EP E+P Risultato: accelerazione della reazione globale. ΔG =energia di attivazione
6 ADDOTTO Enzima-Substrato L energia usata per aumentare la velocità enzimatica deriva dalle interazioni deboli (legami idrogeno, interazioni ioniche e idrofobiche) che si formano tra enzima e substrato ENERGIA di LEGAME
7 Gli enzimi sono caratterizzati da elevata specificità
8 CINETICA ENZIMATICA velocità di una reazione (V): numero di molecole di substrato che si trasformano in prodotto nell unità di tempo. (V) si esprime come mmol/l di prodotto formatosi in un minuto (mm/min). Velocità iniziale V 0 Nelle analisi delle reazioni enzimatiche si utilizzano soltanto le velocità di reazione iniziali (v 0 ), quelle che si misurano non appena si mescolano l enzima ed il substrato. In tal modo la variazione di [S] può essere considerata trascurabile.
9 CINETICA ENZIMATICA: concentrazione del substrato La velocità di una reazione catalizzata da un enzima aumenta all aumentare della concentrazione del substrato fino a raggiungere una velocità massima (V max ). In questa condizione i siti attivi dell enzima sono saturi del substrato Quando tutto l enzima è saturato con il substrato: [ES] = [E tot ] V 0 = Vmax
10 La curva che esprime la relazione tra V 0 e S ha un andamento iperbolico ed è espressa algebricamente dalla equazione di Michaelis-Menten Costante di Michaelis e Menten La Km è quella concentrazione di substrato a cui la V 0 è pari a metà della Vmax
11 L equazione di Michaelis-Menten descrive la variazione della velocità di reazione al variare della concentrazione del substrato. v 0 = velocità iniziale della reazione V max = velocità massima K m = costante di Michaelis-Menten [S] = concentrazione del substrato
12 Caratteristiche della K m La K m è pari alla concentrazione di substrato alla quale la velocità della reazione (V 0 ) è 1/2 della V max. La K m riflette l affinità dell enzima per il substrato: K m piccola = alta affinità dell enzima per il substrato K m grande = bassa affinità dell enzima per il substrato. Ogni enzima ha una K m caratteristica per un dato substrato. La K m non varia al variare della [E].
13 I PARAMETRI CINETICI POSSONO ESSERE USATI PER CONFRONTARE LE ATTIVITA DEGLI ENZIMI
14 Inibizione Enzimatica Inibitori ostacolano o impediscono il funzionamento degli enzimi Inibitore reversibile: Ha un azione temporanea, è possibile allontanare l inibitore dall enzima, consentendo il regolare esplicarsi dell attività catalitica. inibitore irreversibile: la ripresa dell attività enzimatica non è possibile, in quanto non è possibile in nessun modo allontanare l inibitore dall enzima
15 un enzima regolatore è quello che controlla le quantità di sostanze che devono essere trasformate in una via metabolica (catalizza la reazione più lenta, in genere la prima di una serie) tali enzimi non seguono la cinetica di Michaelis Menten e sono responsabili della modulazione della velocità con cui decorre l intero processo metabolico Enzimi regolatori ENZIMI ALLOSTERICI struttura quaternaria (due o più subunità proteiche) in essi esistono più siti chimicamente attivi Effettore o MODULATORE: molecola che interagendo con l enzima in siti lontani dal sito attivo, esercita un effetto positivo o negativo sulla sua attività
16 Modificazione allosterica Enzimi regolatori
17 Enzimi regolatori
18 Enzimi regolatori modificazione covalente reversibile
19 Coenzimi e Cofattori Molti enzimi per poter essere attivi richiedono la presenza di ioni metallici o di altre molecole, talvolta legate con legami covalenti: Coenzimi o cofattori Cofattore: ione o molecola NON PROTEICA la cui presenza è indispensabile perché l enzima possa svolgere la sua attività catalitica. Tra i cofattori hanno rilevante importanza gli ioni di alcuni elementi metallici, in particolare Ca, Mg, Mn, Zn, Cu (p.es. tutti gli enzimi che utilizzano ATP richiedono la presenza di ioni Mg 2+ ).
20 Coenzimi e Cofattori Molti enzimi per poter essere attivi richiedono la presenza di ioni metallici o di altre molecole, talvolta legate con legami covalenti: Coenzimi o cofattori Coenzimi: sono molecole organiche (alcuni di essi derivano da vitamine idrosolubili) prendono parte direttamente all azione catalitica dell enzima spesso si ritrovano modificati chimicamente al termine della reazione (es. NAD + / NADH).
21 Coenzimi I coenzimi da soli sono cataliticamente inattivi ma, unendosi all apoenzima, formano l enzima cataliticamente attivo. Uno stesso coenzima può essere unito a diverse proteine per cui si deduce che la specificità dell azione enzimatica è proprietà dell apoenzima e non del coenzima. La maggior parte dei coenzimi è strettamente legata alle vitamine. Per diventare coenzima, la vitamina subisce delle trasformazioni che vanno dalla semplice fosforilazione (uno dei casi più comuni) a trasformazioni più complesse. La trasformazione della vitamina in coenzima avviene all interno delle cellule ed è di natura enzimatica. I coenzimi possono essere classificati in gruppi diversi, in base al tipo di reazione catalizzata.
22 Coenzimi Coenzimi derivati dalle vitamine idrosolubili Le vitamine sono necessarie per la sintesi di coenzimi e devono essere ottenute con la dieta Piante e microorganismi sono produttori di vitamine La maggior parte delle vitamine deve essere ulteriormente trasformata per generare coenzimi
23 Coenzimi Niacina (Vit. B 3 o PP) NAD + e NADP + La niacina (acido nicotinico) è un precursore di NAD + e NADP + NAD = Nicotinamide Adenina Dinucleotide NADP = Nicotinamide Adenina Dinucleotide Fosfato NAD + e NADP + fungono da coenzimi in molte reazioni di ossidoriduzione
24 Coenzimi I due Coenzimi funzionano come trasportatori di ioni idruro H -
25 Coenzimi
26 Coenzimi Riboflavina (Vit. B 2 ) coenzimi FAD e FMN FAD = Flavin Adenin Dinucleotide FMN = Flavin mono-nucleotide I coenzimi Flavinici sono coinvolti in reazioni di ossido riduzione catalizzate da molti enzimi (flavoenzimi o flavoproteine) Uova, latte, carne, cereali
27 Coenzimi
28 Coenzimi
29 Coenzimi Partecipa alle reazioni di trasferimento di radicali ACILICI, come quelli che avvengono nell ossidazione di carboidrati, acidi grassi e aminoacidi. Acido Pantotenico (Vit B5) Coenzima A (CoA) I gruppi acile sono legati covalentemente al gruppo SH del CoA a formare tioesteri FONTE: Cereali, legumi, carne
30 Coenzimi Partecipa alle reazioni di trasferimento di radicali ACILICI, come quelli che avvengono nell ossidazione di carboidrati, acidi grassi e aminoacidi. I gruppi acile sono legati covalentemente al gruppo SH del CoA a formare tioesteri FONTE: Cereali, legumi, carne
31 PROTEINE RESPIRATORIE EMOGLOBINA & MIOGLOBINA
32 Nel corso dell evoluzione, con il passaggio dalla vita anaerobia alla vita aerobia si sono progressivamente differenziati due meccanismi che sono in grado di garantire alle cellule dei tessuti un flusso di O 2 sufficiente e costante: un sistema circolatorio adeguato; molecole trasportatrici di O 2, che permettono di superare la limitazione imposta dalla bassa solubilità dell ossigeno in acqua.
33 Nei vertebrati le molecole coinvolte nel rifornimento dell ossigeno sono: Emoglobina (Hb) Mioglobina (Mb) si legano reversibilmente con l O 2 e ne rendono possibile il trasporto dai polmoni ai tessuti e l immagazzinamento nel muscolo. L Hb contenuta nei globuli rossi aumenta di 50 volte la quantità di O 2 trasportata da 1 litro di sangue. La Mb si trova nei muscoli e funziona soprattutto come deposito di O 2 ; ha una grande affinità per l O 2 e lo lega quando l Hb delle emazie lo ha già ceduto e, a sua volta lo cede solo quando la pressione parziale del gas (po 2 ) scende a livelli molto bassi.
34 Proteina monomerica (153 AA) Immagazzinamento dell O 2 nella cellula 80% degli AA sono disposti ad α-elica Mioglobina (Mb)
35 Emoglobina (Hb) Eterotetramero costituita da 4 diverse subunità: 2 subunità α 2 subunità β Trasporto dell O 2 dai polmoni alla cellula
36 L Emoglobina trasporta l O 2 dai polmoni ai tessuti La Mioglobina è in grado di legare l ossigeno rilasciato dall Emoglobina nel circolo sanguigno ai tessuti e trasportarlo ai vari organelli cellulari che lo utilizzano (es. mitocondri)
37 EME 4 anelli pirrolici Fe 2+ al centro EME: PROTOPORFIRINA IX Fe 2+
38 EME
39 EME
40 EME
41 EME
42 EME Il Fe 2+ dell eme può legare: O 2 CO H 2 O (metaemoglobina) Fe 2+ Fe 3+
43 EME Il Fe 2+ dell eme può legare: O 2 (ossiemoglobina)
44 EME Il Fe 2+ dell eme può legare: CO (carbossiemoglobina)
45 I derivati carbossi-mioglobina e carbossi-emoglobina presentano CO (non CO 2!!!) legato al gruppo eme. Il legame con il CO è circa 300 volte più stabile di quello con l O 2 ed è irreversibile! Quando nell aria è presente 0.2% di CO in 1 ora si ha perdita di coscienza e in circa 4 ore si ha morte per asfissia (circa 2/3 di Hb sono legati a CO).
46 Protezione dell eme da parte della globina Le globine che circondano l'eme in Mb ed in Hb hanno funzioni di estrema importanza: - impediscono al ferro dell eme di ossidarsi da Fe 2+ ferroso a Fe 3+ ferrico; - creano un sito attivo idrofobico, in cui si lega O 2 che è lipofilo * ; - proteggono l eme da ligandi indesiderabili (esempio CO). * la solubilità di O 2 nel plasma è molto bassa; grazie all'emoglobina nel sangue c'è una concentrazione di O volte superiore a quella del plasma.
47 Mioglobina (Mb)
48 Saturazione frazionale Legame all ossigeno della Mb (MbO 2 ) deposito di O 2 a livello muscolare Muscolo a riposo: mioglobina legata all O 2 Muscolo attivo: consumo di O 2 diminuisce la pressione a livello dei tessuti la mioglobina rilascia l O 2 Pressione tessuti Pressione polmoni Numero di molecole che hanno legato l O 2 rispetto al totale Y Curva iperbolica P 50 Pressione parziale di O 2 alla quale è saturato il 50% delle molecole SEMISATURAZIONE Misura dell affinità per l O 2 Più piccola è la P 50 maggiore è l affinità
49 1. contenuta negli eritrociti 2. trasporto di O 2 dai polmoni ai tessuti (legame reversibile) 3. trasporto reversibile di CO 2. Emoglobina (Hb) struttura quaternaria 4 catene polipetiditiche 4 gruppi eme HbA (α2β2): emoglobina adulta umana 2 catene α 2 catene β HbF (α2 2): emoglobina fetale 2 catene α 2 catene. La sostituzione delle catene β (Hb adulta) con le catene (Hb fetale) comporta differente funzionalità.
50 Emoglobina (Hb)
51
52 L emoglobina esiste in due forme: ossigenata =R; deossigenata =T Il legame di Hb con O 2 induce una modificazione strutturale. La proteina passa da una forma tesa T, mantenuta da interazioni ioniche (ponti salini) fra catene laterali di aminoacidi (es. Asp-His) presenti nelle sub-unità, a una forma rilassata R (ponti salini spezzati). Il fenomeno avviene in direzione opposta quando l emoglobina rilascia l ossigeno.
53 Modificazione conformazionale: Transizione T R
54 Modificazione conformazionale: Transizione T R Stato T (blu) Stato R (rosso)
55
56 Allosterismo (modificazione della struttura quaternaria) proteine con struttura quaternaria possono andare incontro a modificazioni nella disposizione spaziale delle sub-unità costituenti. L emoglobina è una proteina allosterica la cui struttura quaternaria viene modificata dal legame di O 2 alle 4 sub-unità: i 4 siti attivi cooperano positivamente, legando O 2 con affinità crescente e questo causa cambiamento progressivo di struttura quaternaria.
57 Curva di dissociazione dell O 2 per l Emoglobina Hb Hb + 4O 2 = Hb(O 2 ) 4 sigmoidale L emoglobina lega l O 2 quando la pressione parziale del gas (po 2 ) è elevata (polmoni) e lo rilascia quando la pressione è bassa (tessuti).
58 La mioglobina è un ottimo sistema per immagazzinare O 2 : -si lega all O 2 anche a basse po 2 e lo lega strettamente. L emoglobina è un ottimo sistema per trasportare l O 2 : -si carica di O 2 quando po 2 è alta e cede O 2 quando po 2 è bassa.
59 Hb T legame cooperativo EMOGLOBINA lega l O 2 con affinità crescente Hb + 4 O 2 Hb(O 2 ) 4 Hb(O 2 ) 4 R
60 Modello simmetrico Modello sequenziale
61 Fattori che influenzano l affinità dell Hb per O 2 piccole molecole e ioni, presenti negli eritrociti possono regolare il legame di O 2 ad Hb EFFETTORI O MODULATORI ETEROTROPICI: [H + ], CO 2, acido 2,3 bisfosfoglicerico (2,3-BPG) si legano con interazioni deboli in siti diversi da quello di legame dell O 2 diminuiscono l affinità dell emoglobina per l ossigeno. MODULATORI ETEROTOPICI NEGATIVI. L aumento di concentrazione di questi modulatori causa una diminuzione dell affinità di Hb per O 2 e stabilizzano la forma T.
62 EFFETTO BOHR Il legame di Hb con O 2 è fortemente influenzato dal ph e dalla pco 2. Nei tessuti, dove il ph è basso e la pco 2 è alta, l'affinità di Hb per O 2 diminuisce, O 2 viene liberato e H + e CO 2 si legano ad Hb. Il contrario avviene nei capillari polmonari. L'effetto del ph e della CO2 sull'affinità di Hb per O 2 è denominato Hb(O 2 ) 4 + H + = HbH + + 4O 2 Nei tessuti Hb(O 2 ) 4 perde affinità per O 2, lo rilascia a causa delle basse po 2 e, essendo la forma deossigenata più affine per H +, si comporta come un ottimo tampone intracellulare (azione di alcuni residui di istidina). L'azione tampone si accompagna al trasporto dell'anidride carbonica.
63 In aggiunta al trasporto di O 2 dai polmoni ai tessuti, Hb trasporta anche due prodotti della respirazione, H + e CO 2, dai tessuti ai polmoni ed ai reni, organi deputati alla loro escrezione. Trasporto della CO 2 CO 2 liberamente disciolta nel plasma CO 2 trasportata come bicarbonato (HCO 3- ) CO 2 trasportata come carbammati(15-20%) formatosi dalla reazione con i gruppi α aminici terminali non ionizzati dell Hb
64 TESSUTI La maggior parte della CO 2 che diffonde nelle emazie reagisce con l H 2 O formando H 2 CO 3, grazie alla presenza di un enzima, l anidrasi carbonica CO 2 + H 2 O H 2 CO 3 H + + HCO 3 - H + HCO 3 - Legati all Hb passano dal globulo rosso al plasma attraverso una proteina di membrana
65 Gli ioni H + si legano a 3 coppie di siti sull Hb: la più nota è l His 146 delle catene β nei tessuti ad elevato metabolismo, come nei muscoli in attività in cui c è una notevole produzione di composti acidi e di CO 2, l Hb cede più facilmente l O 2 e lega gli H + e la CO 2. Nei polmoni avviene esattamente il contrario.
66 EFFETTO BOHR ph & pco 2 venoso arterioso
67
68 pco 2 pco 2 Influenza della pco 2
69 Influenza del ph tessuti polmoni
70 Influenza del 2,3- BPG
71 Influenza del 2,3- BPG Il 2,3 BPG è una piccola molecola dotata di cariche negative che consentono il legame a una serie di cariche positive delle catene laterali di AA situati sulle due catene β, formando ponti salini e stabilizzando la forma T. Il sito per il 2,3 BPG è presente solo nella forma tesa T.
72 Influenza del 2,3- BPG Nell Hb deossigenata (T) è presente una cavità centrale che si restringe consistentemente in Hb in forma R (ossigenata): tale cavità nella forma T ospita il 2,3 BPG, modulatore allosterico negativo.
73 Influenza del 2,3- BPG Nell Hb deossigenata (T) è presente una cavità centrale che si restringe consistentemente in Hb in forma R (ossigenata): tale cavità nella forma T ospita il 2,3 BPG, modulatore allosterico negativo.
74 EMOGLOBINA FETALE (HbF) Il significato del 2,3 BPG appare chiaro se si confronta la curva di saturazione dell HbA materna e dell Hb e fetale. Gli eritrociti fetali contengono un Hb con struttura quaternaria α2 2. Fra le catene il 2,3-BPG si lega più debolmente rispetto a quello che avviene nell HbA. La curva di saturazione dell Hb fetale è a sinistra rispetto a quella della HbA materna, indicando maggiore affinità per O 2. L'O 2 rilasciato nella circolazione placentare dall Hb materna a certe pressioni parziali, viene assunto dall Hb fetale, più affine, e ciò soddisfa l'esigenza fisiologica di rifornimento di O 2 al feto da parte della madre.
75
76 emoglobinopatie Anemia falciforme
77 emoglobinopatie
78 Le talassemie
79 P. Champe, R. Harvey, D. R. Ferrier, LE BASI DELLA BIOCHIMICA, Zanichelli Editore S.p.A. Copyright 2006
80 P. Champe, R. Harvey, D. R. Ferrier, LE BASI DELLA BIOCHIMICA, Zanichelli Editore S.p.A. Copyright 2006
Nel corso dell evoluzione, con il passaggio dalla. progressivamente differenziati due meccanismi. un sistema circolatorio adeguato;
 PROTEINE RESPIRATORIE EMOGLOBINA & MIOGLOBINA Nel corso dell evoluzione, con il passaggio dalla vita anaerobia alla vita aerobia si sono progressivamente differenziati due meccanismi che sono in grado
PROTEINE RESPIRATORIE EMOGLOBINA & MIOGLOBINA Nel corso dell evoluzione, con il passaggio dalla vita anaerobia alla vita aerobia si sono progressivamente differenziati due meccanismi che sono in grado
FUNZIONI delle PROTEINE
 FUNZIONI delle PROTEINE Ha le dimensioni del reciproco di una concentrazione (M -1 ) Ha le dimensioni di una concentrazione (M) La frazione dei siti occupati rispetto ai siti totali è definita come θ FRAZIONE
FUNZIONI delle PROTEINE Ha le dimensioni del reciproco di una concentrazione (M -1 ) Ha le dimensioni di una concentrazione (M) La frazione dei siti occupati rispetto ai siti totali è definita come θ FRAZIONE
- utilizzano esclusivamente le reattività chimiche di alcuni residui AA
 Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
ENZIMI. Un enzima è un catalizzatore (acceleratore) di reazioni biologiche.
 ENZIMI ENZIMI Un enzima è un catalizzatore (acceleratore) di reazioni biologiche. Catalizzatore = sostanza in grado di accelerare lo svolgimento di una reazione chimica e quindi di aumentarne la sua velocità,
ENZIMI ENZIMI Un enzima è un catalizzatore (acceleratore) di reazioni biologiche. Catalizzatore = sostanza in grado di accelerare lo svolgimento di una reazione chimica e quindi di aumentarne la sua velocità,
Mioglobina ed emoglobina
 Mioglobina ed emoglobina α β Muscolo Deposito di O 2 Alta affinità per O 2 β α Globulo rosso Trasporto di O 2 Bassa affinità per O 2 Cooperativa ed allosterica Animali Mb-knockout (2003) : funzionalità
Mioglobina ed emoglobina α β Muscolo Deposito di O 2 Alta affinità per O 2 β α Globulo rosso Trasporto di O 2 Bassa affinità per O 2 Cooperativa ed allosterica Animali Mb-knockout (2003) : funzionalità
Emoglobina e mioglobina
 Emoglobina e mioglobina Per molti organismi, l O 2 è una molecola di importanza vitale: l'ossigeno è infatti l'accettore finale degli elettroni, che "fluendo" attraverso i complessi della catena respiratoria,
Emoglobina e mioglobina Per molti organismi, l O 2 è una molecola di importanza vitale: l'ossigeno è infatti l'accettore finale degli elettroni, che "fluendo" attraverso i complessi della catena respiratoria,
L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO
 L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 23 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata all emoglobina: L O 2 totale
L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 23 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata all emoglobina: L O 2 totale
Le proteine che legano l ossigenol
 Le proteine che legano l ossigenol Protoporfirina IX EME (Fe-protoporfirina IX) L atomo di ferro del gruppo eme può formare sei legami Struttura della mioglobina di capodoglio (J. Kendrew, anni 50)
Le proteine che legano l ossigenol Protoporfirina IX EME (Fe-protoporfirina IX) L atomo di ferro del gruppo eme può formare sei legami Struttura della mioglobina di capodoglio (J. Kendrew, anni 50)
Amminoacidi Peptidi Proteine
 Amminoacidi Peptidi Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Gli amminoacidi nelle molecole proteiche sono tutti stereoisomeri L IDROFOBOCI IDROFOBOCI IDROFILICI Secondo gruppo
Amminoacidi Peptidi Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Gli amminoacidi nelle molecole proteiche sono tutti stereoisomeri L IDROFOBOCI IDROFOBOCI IDROFILICI Secondo gruppo
Regolano il metabolismo, sia come enzimi, sia come ormoni (insulina, glucagone, ecc.)
 Grazie alla elevata dinamicità delle strutture proteiche (gli atomi sono in continuo movimento fluttuante) e per la capacità che hanno di legarsi in modo selettivo ad altre molecole, le proteine svolgono
Grazie alla elevata dinamicità delle strutture proteiche (gli atomi sono in continuo movimento fluttuante) e per la capacità che hanno di legarsi in modo selettivo ad altre molecole, le proteine svolgono
Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi)
 ENZIMI Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi) Sono in grado di aumentare la velocità dei processi catalizzati fino a
ENZIMI Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi) Sono in grado di aumentare la velocità dei processi catalizzati fino a
Esempi di proteine: Mioglobina ed Emoglobina
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Esempi di proteine: Mioglobina ed Emoglobina Mioglobina: caratteristiche generali, funzione
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Esempi di proteine: Mioglobina ed Emoglobina Mioglobina: caratteristiche generali, funzione
Trasporto di O 2 nel sangue
 Trasporto di O 2 nel sangue Il 97% dell O 2 trasportato nel plasma è chimicamente legato all Hb nei globuli rossi, solo il 3% è fisicamente disciolto Trasporto O 2 nel plasma Trasporto O 2 legato ad Hb
Trasporto di O 2 nel sangue Il 97% dell O 2 trasportato nel plasma è chimicamente legato all Hb nei globuli rossi, solo il 3% è fisicamente disciolto Trasporto O 2 nel plasma Trasporto O 2 legato ad Hb
Esempi di proteine: Mioglobina ed Emoglobina
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica Organica e Biochimica Esempi di proteine: Mioglobina ed Emoglobina Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica Organica e Biochimica Esempi di proteine: Mioglobina ed Emoglobina Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base
Fisiologia della Respirazione
 Fisiologia della Respirazione 8.Trasporto dei gas nel sangue FGE aa.2016-17 Obiettivi Necessità di un sistema di trasporto chimico ad alta capacità dell O 2 nel sangue: l emoglobina Curva di dissociazione
Fisiologia della Respirazione 8.Trasporto dei gas nel sangue FGE aa.2016-17 Obiettivi Necessità di un sistema di trasporto chimico ad alta capacità dell O 2 nel sangue: l emoglobina Curva di dissociazione
Fisiologia della Respirazione 8.Trasporto dei gas nel sangue. Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona
 Fisiologia della Respirazione 8.Trasporto dei gas nel sangue Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona Obiettivi Necessità di un sistema di trasporto chimico ad alta capacità
Fisiologia della Respirazione 8.Trasporto dei gas nel sangue Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona Obiettivi Necessità di un sistema di trasporto chimico ad alta capacità
Trasporto dei gas. Pressioni Volumi
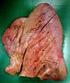 Trasporto dei gas Pressioni Volumi Il 97% dell O 2 trasportato nel plasma si trova chimicamente legato all Hb nei globuli rossi, solo lo 3% è fisicamente disciolto Trasporto O 2 nel plasma Trasporto O
Trasporto dei gas Pressioni Volumi Il 97% dell O 2 trasportato nel plasma si trova chimicamente legato all Hb nei globuli rossi, solo lo 3% è fisicamente disciolto Trasporto O 2 nel plasma Trasporto O
INTRODUZIONE AL METABOLISMO
 INTRODUZIONE AL METABOLISMO METABOLISMO Il metabolismo (dal greco metabolé = trasformazione) è il complesso delle reazioni chimiche coordinate ed integrate che avvengono in una cellula. Il metabolismo
INTRODUZIONE AL METABOLISMO METABOLISMO Il metabolismo (dal greco metabolé = trasformazione) è il complesso delle reazioni chimiche coordinate ed integrate che avvengono in una cellula. Il metabolismo
Helena Curtis N. Sue Barnes
 Helena Curtis N. Sue Barnes LA FOTOSINTESI INDICE Organismi autotrofi ed eterotrofi Confronto tra fotosintesi e respirazione Reazioni endoergoniche ed esoergoniche Reazioni accoppiate Fase luce-dipendente
Helena Curtis N. Sue Barnes LA FOTOSINTESI INDICE Organismi autotrofi ed eterotrofi Confronto tra fotosintesi e respirazione Reazioni endoergoniche ed esoergoniche Reazioni accoppiate Fase luce-dipendente
ENZIMI. Durante la reazione l enzima può essere temporaneamente modificato ma alla fine del processo ritorna nel suo stato originario, un enzima viene
 ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari, e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari, e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
- CINETICA ENZIMATICA
 - CINETICA ENZIMATICA ENZIMI: - CATALIZZATORI aumenta la V di una reazione chimica senza subire trasformazioni durante l intero processo - PROTEINE gli enzimi sono proteine di struttura 3 o talora 4 -
- CINETICA ENZIMATICA ENZIMI: - CATALIZZATORI aumenta la V di una reazione chimica senza subire trasformazioni durante l intero processo - PROTEINE gli enzimi sono proteine di struttura 3 o talora 4 -
CORSO DI BIOCHIMICA PER INGEGNERIA BIOMEDICA 2 ESERCITAZIONE
 CORSO DI BIOCHIMICA PER INGEGNERIA BIOMEDICA 2 ESERCITAZIONE 1) Il collagene è una proteina (globulare / fibrosa). È formata da tre (catene alfa/alfa eliche) con andamento (destrorso/sinistrorso) che vanno
CORSO DI BIOCHIMICA PER INGEGNERIA BIOMEDICA 2 ESERCITAZIONE 1) Il collagene è una proteina (globulare / fibrosa). È formata da tre (catene alfa/alfa eliche) con andamento (destrorso/sinistrorso) che vanno
ENZIMI. A + B AB (100 Kcal= E. Attiv.) A + B AB (50 Kcal) SUBSTRATO ENZIMA E N E R G I A
 ENZIMI 1) sono catalizzatori di natura biologica e sono proteine 2) gli enzimi abbassano l energia di attivazione di un solo tipo di reazione senza intervenire nella reazione stessa cioè senza esserne
ENZIMI 1) sono catalizzatori di natura biologica e sono proteine 2) gli enzimi abbassano l energia di attivazione di un solo tipo di reazione senza intervenire nella reazione stessa cioè senza esserne
METABOLISMO CELLULARE
 METABOLISMO CELLULARE Struttura dell ATP (Adenosintrifosfato) Adenina (base azotata), Ribosio (zucchero) e un gruppo fosforico ATP Il legame covalente tra i gruppi fosforici si spezza facilmente liberando
METABOLISMO CELLULARE Struttura dell ATP (Adenosintrifosfato) Adenina (base azotata), Ribosio (zucchero) e un gruppo fosforico ATP Il legame covalente tra i gruppi fosforici si spezza facilmente liberando
FUNZIONE DELLE PROTEINE RAPPORTO STRUTTURA-FUNZIONE
 FUNZIONE DELLE PROTEINE RAPPORTO STRUTTURA-FUNZIONE Principi basilari: 1.Le funzioni di molte proteine richiedono il legame reversibile con altre molecole (LIGANDO) Un ligando può essere di natura diversa,
FUNZIONE DELLE PROTEINE RAPPORTO STRUTTURA-FUNZIONE Principi basilari: 1.Le funzioni di molte proteine richiedono il legame reversibile con altre molecole (LIGANDO) Un ligando può essere di natura diversa,
GLI ENZIMI: proteine con attività CATALITICA
 Cap. 6 GLI ENZIMI: proteine con attività CATALITICA Catalizzatori biologici: permettono alle reazioni biochimiche di avvenire a temperature e pressioni fisiologiche e a velocità misurabile. Aumentano la
Cap. 6 GLI ENZIMI: proteine con attività CATALITICA Catalizzatori biologici: permettono alle reazioni biochimiche di avvenire a temperature e pressioni fisiologiche e a velocità misurabile. Aumentano la
degli eritrociti è una proteina di trasporto indispensabile per veicolare l ossigeno l l anidride carbonica tra i polmoni e i tessuti
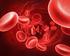 l emoglobina degli eritrociti è una proteina di trasporto indispensabile per veicolare l ossigeno l e l anidride carbonica tra i polmoni e i tessuti Mioglobina, proteina di deposito,, presente nelle fibrocellule
l emoglobina degli eritrociti è una proteina di trasporto indispensabile per veicolare l ossigeno l e l anidride carbonica tra i polmoni e i tessuti Mioglobina, proteina di deposito,, presente nelle fibrocellule
Emoglobina e mioglobina
 Emoglobina e mioglobina L emoglobina e la mioglobina proteine centrali per l evoluzione La transizione dalla vita anaerobica a quella aerobica rappresenta un passo fondamentale dell'evoluzione perchè ha
Emoglobina e mioglobina L emoglobina e la mioglobina proteine centrali per l evoluzione La transizione dalla vita anaerobica a quella aerobica rappresenta un passo fondamentale dell'evoluzione perchè ha
MANTENIMENTO DELLA STRUTTURA CRESCITA SVILUPPO RIPRODUZIONE
 BIOENERGETICA MANTENIMENTO DELLA STRUTTURA CRESCITA SVILUPPO RIPRODUZIONE GLI ORGANISMI VIVENTI POSSONO UTILIZZARE SOLO DUE FORME DI ENERGIA: LUMINOSA (radiazioni di determinate lunghezze d onda) (ORGANISMI
BIOENERGETICA MANTENIMENTO DELLA STRUTTURA CRESCITA SVILUPPO RIPRODUZIONE GLI ORGANISMI VIVENTI POSSONO UTILIZZARE SOLO DUE FORME DI ENERGIA: LUMINOSA (radiazioni di determinate lunghezze d onda) (ORGANISMI
Capitolo 6 La respirazione cellulare
 Capitolo 6 La respirazione cellulare Introduzione alla respirazione cellulare 6.1 La respirazione polmonare rifornisce le nostre cellule di ossigeno ed elimina diossido di carbonio La respirazione polmonare
Capitolo 6 La respirazione cellulare Introduzione alla respirazione cellulare 6.1 La respirazione polmonare rifornisce le nostre cellule di ossigeno ed elimina diossido di carbonio La respirazione polmonare
Il metalloma Struttura e reattività di metalloproteine. Il trasporto dell O 2
 Il metalloma Struttura e reattività di metalloproteine Il trasporto dell O 2 Il trasporto dell ossigeno Nel sangue la solubilità dell O 2 è molto maggiore che in H 2 O In H 2 O la solubilità è 6.59 cm
Il metalloma Struttura e reattività di metalloproteine Il trasporto dell O 2 Il trasporto dell ossigeno Nel sangue la solubilità dell O 2 è molto maggiore che in H 2 O In H 2 O la solubilità è 6.59 cm
INTRODUZIONE AL METABOLISMO. dal gr. metabolè = trasformazione
 INTRODUZIONE AL METABOLISMO dal gr. metabolè = trasformazione IL Metabolismo Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in una cellula o in un organismo. E costituito da
INTRODUZIONE AL METABOLISMO dal gr. metabolè = trasformazione IL Metabolismo Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in una cellula o in un organismo. E costituito da
5. Trasporto di membrana
 5. Trasporto di membrana contiene materiale protetto da copyright, ad esclusivo uso personale; 1 non è consentita diffusione ed utilizzo di tipo commerciale Le membrane biologiche hanno una permeabilità
5. Trasporto di membrana contiene materiale protetto da copyright, ad esclusivo uso personale; 1 non è consentita diffusione ed utilizzo di tipo commerciale Le membrane biologiche hanno una permeabilità
Plasma ph Tamponi: LEC: HCO 3 LIC: Proteine, Emoglobina, Fosfati Urina: Fosfati e ammoniaca
 Equilibrio acidobase Dieta: Acidi grassi Aminoacidi Assunzione H + CO 2, acido lattico, chetoacidi Plasma ph 7.357.42 Tamponi: LEC: HCO 3 LIC: Proteine, Emoglobina, Fosfati Urina: Fosfati e ammoniaca Ventilazione:
Equilibrio acidobase Dieta: Acidi grassi Aminoacidi Assunzione H + CO 2, acido lattico, chetoacidi Plasma ph 7.357.42 Tamponi: LEC: HCO 3 LIC: Proteine, Emoglobina, Fosfati Urina: Fosfati e ammoniaca Ventilazione:
L ossidazione completa del glucosio da parte dell O 2. può essere suddivisa in due semi-reazioni
 L ossidazione completa del glucosio da parte dell O 2 C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O può essere suddivisa in due semi-reazioni C 6 H 12 O 6 + 6 O 2 6 CO 2 + 24 H + + 24 e - (si ossidano gli atomi
L ossidazione completa del glucosio da parte dell O 2 C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O può essere suddivisa in due semi-reazioni C 6 H 12 O 6 + 6 O 2 6 CO 2 + 24 H + + 24 e - (si ossidano gli atomi
Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi.
 ENZIMI Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. Svolgono il loro ruolo con modalità differenti
ENZIMI Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. Svolgono il loro ruolo con modalità differenti
Ogni globina ha una tasca in cui lega un gruppo EME, quindi l Hb può legare e trasportare 4 molecole di O 2
 Emoglobina (Hb): tetramero (le globine si associano formando due copie di dimeri αβ (α 1 β 1 e α 2 β 2 ) che si associano a formare un tetramero attraverso interazioni idrofobiche, legami H e ponti salini
Emoglobina (Hb): tetramero (le globine si associano formando due copie di dimeri αβ (α 1 β 1 e α 2 β 2 ) che si associano a formare un tetramero attraverso interazioni idrofobiche, legami H e ponti salini
FUNZIONI BIOLOGICHE DELLE PROTEINE
 FUNZIONI BIOLOGICHE DELLE PROTEINE ENZIMI PROTEINE DI TRASPORTO PROTEINE DI RISERVA PROTEINE CONTRATTILI PROTEINE DI DIFESA PROTEINE REGOLATRICI PROTEINE STRUTTURALI ENERGIA LIBERA (G) ΔG = ΔH - TΔS Variazioni
FUNZIONI BIOLOGICHE DELLE PROTEINE ENZIMI PROTEINE DI TRASPORTO PROTEINE DI RISERVA PROTEINE CONTRATTILI PROTEINE DI DIFESA PROTEINE REGOLATRICI PROTEINE STRUTTURALI ENERGIA LIBERA (G) ΔG = ΔH - TΔS Variazioni
Indice generale 1. Introduzione alla biochimica 2. Acqua, ph, acidi, basi, sali, tamponi
 Indice generale 1. Introduzione alla biochimica 1 Unità di misura 1 Energia e calore 3 Struttura dell atomo 3 Tavola periodica degli elementi 4 Legami chimici 8 Legami covalenti 8 Legami non covalenti
Indice generale 1. Introduzione alla biochimica 1 Unità di misura 1 Energia e calore 3 Struttura dell atomo 3 Tavola periodica degli elementi 4 Legami chimici 8 Legami covalenti 8 Legami non covalenti
Come le cellule traggono energia dal cibo: produzione di ATP
 Come le cellule traggono energia dal cibo: produzione di ATP L energia è contenuta nei legami chimici delle molecole nutritive; la cellula estrae questa energia e la conserva nell ATP: respirazione cellulare
Come le cellule traggono energia dal cibo: produzione di ATP L energia è contenuta nei legami chimici delle molecole nutritive; la cellula estrae questa energia e la conserva nell ATP: respirazione cellulare
COMPOSIZIONE DELL ARIA ATMOSFERICA SECCA E PRESSIONI PARZIALI DEI GAS - (760 TORR, 15 C)
 COMPOSIZIONE DELL ARIA ATMOSFERICA SECCA E PRESSIONI PARZIALI DEI GAS - (760 TORR, 15 C) COMPOSIZIONE ARIA NELL ATMOSFERA = COSTANTE A PARTE LE VARIAZIONI DELLA QUANTITA DI VAPORE ACQUEO A 0 C 1 torr =
COMPOSIZIONE DELL ARIA ATMOSFERICA SECCA E PRESSIONI PARZIALI DEI GAS - (760 TORR, 15 C) COMPOSIZIONE ARIA NELL ATMOSFERA = COSTANTE A PARTE LE VARIAZIONI DELLA QUANTITA DI VAPORE ACQUEO A 0 C 1 torr =
FOSFORILAZIONE OSSIDATIVA
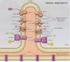 FOSFORILAZIONE OSSIDATIVA Lo scopo ultimo dei processi metabolici ossidativi è quello di canalizzare l energia contenuta nello scheletro carbonioso di zuccheri, ac. grassi e amminoacidi nella sintesi di
FOSFORILAZIONE OSSIDATIVA Lo scopo ultimo dei processi metabolici ossidativi è quello di canalizzare l energia contenuta nello scheletro carbonioso di zuccheri, ac. grassi e amminoacidi nella sintesi di
IL METABOLISMO ENERGETICO
 IL METABOLISMO ENERGETICO IL METABOLISMO L insieme delle reazioni chimiche che riforniscono la cellula e l organismo di energia e materia SI DIVIDE IN: CATABOLISMO produce ENERGIA METABOLISMO ENERGETICO
IL METABOLISMO ENERGETICO IL METABOLISMO L insieme delle reazioni chimiche che riforniscono la cellula e l organismo di energia e materia SI DIVIDE IN: CATABOLISMO produce ENERGIA METABOLISMO ENERGETICO
REGOLAZIONE ENZIMATICA
 REGOLAZIONE ENZIMATICA Cambio conformazionale In molte molecole proteiche, cambiamenti strutturali possono determinare profondi cambiamenti nella funzione o nell attività. Il cambio conformazionale può
REGOLAZIONE ENZIMATICA Cambio conformazionale In molte molecole proteiche, cambiamenti strutturali possono determinare profondi cambiamenti nella funzione o nell attività. Il cambio conformazionale può
DESTINI METABOLICI DEL PIRUVATO
 DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Complesso della Piruvato deidrogenasi
DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Complesso della Piruvato deidrogenasi
Catena di trasporto degli elettroni (catena respiratoria) e Fosforilazione ossidativa
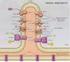 Catena di trasporto degli elettroni (catena respiratoria) e Fosforilazione ossidativa NADH e FADH2 (accettori universali di e-) formati nella glicolisi e nel ciclo di Krebs (e nell ossidazione degli acidi
Catena di trasporto degli elettroni (catena respiratoria) e Fosforilazione ossidativa NADH e FADH2 (accettori universali di e-) formati nella glicolisi e nel ciclo di Krebs (e nell ossidazione degli acidi
Prof. Maria Nicola GADALETA
 Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Gli enzimi e la catalisi
 Gli enzimi e la catalisi Distribuzione di energia in una popolazione di molecole Normalmente, le molecole stabili sono per lo più presenti ad un livello di energia relativamente basso Solo una piccola
Gli enzimi e la catalisi Distribuzione di energia in una popolazione di molecole Normalmente, le molecole stabili sono per lo più presenti ad un livello di energia relativamente basso Solo una piccola
Principi di Biochimica
 Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
Gli elementi corpuscolati del sangue sono vere cellule o derivati cellulari.
 I GLOBULI ROSSI Gli elementi corpuscolati del sangue sono vere cellule o derivati cellulari. I globuli rossi sono i più numerosi (5 milioni per mm 3 nell uomo, 4.5 milioni per mm 3 nella donna) sono detti
I GLOBULI ROSSI Gli elementi corpuscolati del sangue sono vere cellule o derivati cellulari. I globuli rossi sono i più numerosi (5 milioni per mm 3 nell uomo, 4.5 milioni per mm 3 nella donna) sono detti
PORTA AGLI ORGANI E AI TESSUTI: RIMUOVE: OMEOTERMI INTERVIENE NELLA TERMOREGOLAZIONE FUNZIONI DELLA CIRCOLAZIONE SANGUIGNA IL GLOBULO ROSSO
 FUNZIONI DELLA CIRCOLAZIONE SANGUIGNA IL GLOBULO ROSSO PORTA AGLI ORGANI E AI TESSUTI: a. L OSSIGENO (O 2 ), b. LE SOSTANZE NUTRITIZIE ASSORBITE, c. I SECRETI DELLE GHIANDOLE ENDOCRINE. RIMUOVE: a. L ANIDRIDE
FUNZIONI DELLA CIRCOLAZIONE SANGUIGNA IL GLOBULO ROSSO PORTA AGLI ORGANI E AI TESSUTI: a. L OSSIGENO (O 2 ), b. LE SOSTANZE NUTRITIZIE ASSORBITE, c. I SECRETI DELLE GHIANDOLE ENDOCRINE. RIMUOVE: a. L ANIDRIDE
Tamponi biologici per il controllo del ph
 Tamponi biologici per il controllo del ph 1 Si definisce una soluzione tampone una soluzione che si oppone alla variazione del ph per aggiunte moderate di acidi o basi Si tratta generalmente di soluzioni
Tamponi biologici per il controllo del ph 1 Si definisce una soluzione tampone una soluzione che si oppone alla variazione del ph per aggiunte moderate di acidi o basi Si tratta generalmente di soluzioni
Regolazione allosterica
 Macromolecole Biologiche Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Regolazione allosterica Marco Nardini Dipartimento
Macromolecole Biologiche Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Regolazione allosterica Marco Nardini Dipartimento
Trasporto dei gas respiratori nel sangue
 Trasporto dei gas respiratori nel sangue La soluzione dei gas nei liquidi C Legge di Henry acq P gas S gas C acq = quantità di gas disciolta nella fase acquosa P gas = pressione parziale del gas nella
Trasporto dei gas respiratori nel sangue La soluzione dei gas nei liquidi C Legge di Henry acq P gas S gas C acq = quantità di gas disciolta nella fase acquosa P gas = pressione parziale del gas nella
costruire un equazione che potesse descrivere in generale il comportamento cinetico degli enzimi e quindi di determinare parametri cinetici più
 Cinetica Enzimatica OBIETTIVO PRINCIPALE: costruire un equazione che potesse descrivere in generale il comportamento cinetico degli enzimi e quindi di determinare parametri cinetici più importanti (K M,
Cinetica Enzimatica OBIETTIVO PRINCIPALE: costruire un equazione che potesse descrivere in generale il comportamento cinetico degli enzimi e quindi di determinare parametri cinetici più importanti (K M,
fornire energia chimica in vettori attivati ATP e NADH e NADPH e FADH.
 Cibo ed Energia Il glucosio e altre molecole nutritive per esempio i grassi vengono demolite attraverso un ossidazione graduale controllata per fornire energia chimica in una forma utilizzabile dalla cellula,
Cibo ed Energia Il glucosio e altre molecole nutritive per esempio i grassi vengono demolite attraverso un ossidazione graduale controllata per fornire energia chimica in una forma utilizzabile dalla cellula,
Enzimi come catalizzatori biologici
 Enzimi come catalizzatori biologici Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. La catalisi procede
Enzimi come catalizzatori biologici Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. La catalisi procede
TEORIA DELLO STATO DI TRANSIZIONE (Henry Eyring anni 30)
 TEORIA DELLO STATO DI TRANSIZIONE (Henry Eyring anni 30) A + B-C A-B + C (A B C) Complesso attivato Stato di transizione Coordinata di reazione H A H B + H C H A + H B H C A+ K B X k' P + Q [ P] d dt =
TEORIA DELLO STATO DI TRANSIZIONE (Henry Eyring anni 30) A + B-C A-B + C (A B C) Complesso attivato Stato di transizione Coordinata di reazione H A H B + H C H A + H B H C A+ K B X k' P + Q [ P] d dt =
Ioni metallici: Cu 2+, Fe 3+, Zn 2+ Coenzimi : NAD +, FAD + COSUBSTRATI GRUPPI PROSTETICI
 ENZIMI Tutti gli enzimi sono proteine Elevata specificità e senza la formazione di sottoprodotti Non vengono modificati o consumati durante la reazione alla fine si ritrovano inalterati Agiscono in condizioni
ENZIMI Tutti gli enzimi sono proteine Elevata specificità e senza la formazione di sottoprodotti Non vengono modificati o consumati durante la reazione alla fine si ritrovano inalterati Agiscono in condizioni
Il trasporto del glucosio
 Il trasporto del glucosio Il glucosio non può diffondere direttamente nelle cellule Esso entra nelle cellule mediante due meccanismi di trasporto: a) diffusione facilitata Na + indipendente b) co-trasporto
Il trasporto del glucosio Il glucosio non può diffondere direttamente nelle cellule Esso entra nelle cellule mediante due meccanismi di trasporto: a) diffusione facilitata Na + indipendente b) co-trasporto
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
Seminario. Ciclo di Krebs 1. La citrato sintasi forma citrato a partire dall ossaloacetato e dall acetilcoenzima A
 Seminario PASSO PER PASSO 1. La citrato sintasi forma citrato a partire dall ossaloacetato e dall acetilcoenzima A Il ciclo dell acido citrico inizia con la reazione di condensazione di un unità con 4
Seminario PASSO PER PASSO 1. La citrato sintasi forma citrato a partire dall ossaloacetato e dall acetilcoenzima A Il ciclo dell acido citrico inizia con la reazione di condensazione di un unità con 4
Catalisi. Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A Modulo di Biologia Strutturale
 Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Catalisi Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie
Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Catalisi Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie
Scambi gassosi e regolazione del respiro
 Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I Scambi gassosi e regolazione del respiro Ruolo del Sistema Respiratorio: - fornire O 2 - rimuovere CO 2 Scaricato da www.sunhope.it
Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I Scambi gassosi e regolazione del respiro Ruolo del Sistema Respiratorio: - fornire O 2 - rimuovere CO 2 Scaricato da www.sunhope.it
Chimica Biologica A.A Cinetica Enzimatica. Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano
 Chimica Biologica A.A. 2010-2011 Cinetica Enzimatica Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Cinetica Chimica Termodinamica: fornisce
Chimica Biologica A.A. 2010-2011 Cinetica Enzimatica Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Cinetica Chimica Termodinamica: fornisce
FADH ADP + Pi ATP...29 AG ' = -30,5 kj/mol...29 Resa di ATP per l ossidazione completa del glucosio...31
 FOSFORILAZIONE OSSIDATIVA FOSFORILAZIONE OSSIDATIVA...1 Glicolisi e ciclo di Krebs...3 il NADH il NADPH e il FADH2 sono traportatori solubili di elettroni...4 LA FOSFORILAZIONE OSSIDATIVA...5 Il mitocondrio...5
FOSFORILAZIONE OSSIDATIVA FOSFORILAZIONE OSSIDATIVA...1 Glicolisi e ciclo di Krebs...3 il NADH il NADPH e il FADH2 sono traportatori solubili di elettroni...4 LA FOSFORILAZIONE OSSIDATIVA...5 Il mitocondrio...5
Trasporto O 2 nel sangue
 Trasporto O 2 nel sangue 97% legato all Hb nei globuli rossi 3% fisicamente disciolto, determina il valore di po 2 Trasporto O 2 nel plasma Trasporto O 2 legato ad Hb SaturazioneHb 97% 0.3 ml/100ml 19.4
Trasporto O 2 nel sangue 97% legato all Hb nei globuli rossi 3% fisicamente disciolto, determina il valore di po 2 Trasporto O 2 nel plasma Trasporto O 2 legato ad Hb SaturazioneHb 97% 0.3 ml/100ml 19.4
Prof. Maria Nicola GADALETA FOSFORILAZIONE OSSIDATIVA 4
 Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche FOSFORILAZIONE
Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche FOSFORILAZIONE
ENERGIA LIBERA DI GIBBS (G)
 METABOLISMO: Descrive tutte le numerose reazioni con cui le molecole biologiche sono sintetizzate e degradate, e che permettono di ricavare, accumulare e utilizzare energia Ogni reazione metabolica comporta
METABOLISMO: Descrive tutte le numerose reazioni con cui le molecole biologiche sono sintetizzate e degradate, e che permettono di ricavare, accumulare e utilizzare energia Ogni reazione metabolica comporta
Energia di attivazione
 Energia di attivazione La maggior parte delle reazioni chimiche avviene con un apporto iniziale di energia per poter prendere l avvio procedere alla giusta velocità. Questo vale per le reazioni esoergoniche
Energia di attivazione La maggior parte delle reazioni chimiche avviene con un apporto iniziale di energia per poter prendere l avvio procedere alla giusta velocità. Questo vale per le reazioni esoergoniche
di piccoli gruppi di molecole di RNA catalitico tutti gli enzimi sono proteine Molti enzimi per poter funzionare richiedono la presenza di cofattori.
 Enzimi Con l eccezione l di piccoli gruppi di molecole di RNA catalitico tutti gli enzimi sono proteine Molti enzimi per poter funzionare richiedono la presenza di cofattori. apoenzima + cofattore = oloenzima
Enzimi Con l eccezione l di piccoli gruppi di molecole di RNA catalitico tutti gli enzimi sono proteine Molti enzimi per poter funzionare richiedono la presenza di cofattori. apoenzima + cofattore = oloenzima
FISIOLOGIA dell ALLENAMENTO. dai processi fisiologici alle metodiche di allenamento
 FISIOLOGIA dell ALLENAMENTO dai processi fisiologici alle metodiche di allenamento Introduzione alla fisiologia Metabolismo cellulare Il sistema cardiovascolare: funzione cardiaca vasi, flusso, pressione
FISIOLOGIA dell ALLENAMENTO dai processi fisiologici alle metodiche di allenamento Introduzione alla fisiologia Metabolismo cellulare Il sistema cardiovascolare: funzione cardiaca vasi, flusso, pressione
Il ciclo degli acidi tricarbossilici o ciclo dell acido citrico
 Il ciclo degli acidi tricarbossilici o ciclo dell acido citrico Dalla glicolisi alla fosforilazione ossidativa NAD + e NADP + Sono coinvolti nelle reazioni di trasferimento dell idruro H: -. Tutte le reazioni
Il ciclo degli acidi tricarbossilici o ciclo dell acido citrico Dalla glicolisi alla fosforilazione ossidativa NAD + e NADP + Sono coinvolti nelle reazioni di trasferimento dell idruro H: -. Tutte le reazioni
I processi mediante i quali le molecole biologiche vengono scisse e risintetizzate formano una rete di reazioni enzimatiche, complessa e finemente
 I processi mediante i quali le molecole biologiche vengono scisse e risintetizzate formano una rete di reazioni enzimatiche, complessa e finemente regolata, detta metabolismo dell organismo. Questa rete
I processi mediante i quali le molecole biologiche vengono scisse e risintetizzate formano una rete di reazioni enzimatiche, complessa e finemente regolata, detta metabolismo dell organismo. Questa rete
PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA
 PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA Svolgono la loro funzione legando reversibilmente l OSSIGENO. Aumentano la solubilità dell ossigeno nel plasma, da 3ml/L a 220 ml/l. La mioglobina
PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA Svolgono la loro funzione legando reversibilmente l OSSIGENO. Aumentano la solubilità dell ossigeno nel plasma, da 3ml/L a 220 ml/l. La mioglobina
DESTINI DEL PIRUVATO
 DESTINI DEL PIRUVATO LA GLICOLISI RILASCIA SOLO UNA PICCOLA PARTE DELL ENERGIA TOTALE DISPONIBILE NELLA MOLECOLA DI GLUCOSIO Le due molecole di piruvato prodotte dalla glicolisi sono ancora relativamente
DESTINI DEL PIRUVATO LA GLICOLISI RILASCIA SOLO UNA PICCOLA PARTE DELL ENERGIA TOTALE DISPONIBILE NELLA MOLECOLA DI GLUCOSIO Le due molecole di piruvato prodotte dalla glicolisi sono ancora relativamente
Respirazione cellulare
 Respirazione cellulare L equazione generale della respirazione C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O + 36 ATP 1 molec zucchero 6 molec ossigeno 6 molec anidride carbonica 6 molec acqua + = + + 36 molecole
Respirazione cellulare L equazione generale della respirazione C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O + 36 ATP 1 molec zucchero 6 molec ossigeno 6 molec anidride carbonica 6 molec acqua + = + + 36 molecole
Il metabolismo cellulare
 Il metabolismo cellulare L obesità è problema sanitario e sociale Tessuto adiposo bianco e bruno È tutta una questione di energia: Se si assumono più molecole energetiche di quelle che ci servono per costruire
Il metabolismo cellulare L obesità è problema sanitario e sociale Tessuto adiposo bianco e bruno È tutta una questione di energia: Se si assumono più molecole energetiche di quelle che ci servono per costruire
Tamponi Biologici. AO/Febbraio 2016
 Tamponi Biologici AO/Febbraio 2016 Le soluzioni tampone Le soluzioni tampone contengono una coppia acido-base coniugata in cui le concentrazioni di acido e di base, entrambi non forti, sono circa dello
Tamponi Biologici AO/Febbraio 2016 Le soluzioni tampone Le soluzioni tampone contengono una coppia acido-base coniugata in cui le concentrazioni di acido e di base, entrambi non forti, sono circa dello
I materiali della vita
 I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
CHIMICA BIOLOGICA. Seconda Università degli Studi di Napoli. Prof. Augusto Parente. Lezione 7. DiSTABiF. Corso di Laurea in SCIENZE BIOLOGICHE
 Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in SCIENZE BIOLOGICHE Insegnamento di CHIMICA BIOLOGICA Prof. Augusto Parente Anno Accademico 2014-15 Lezione 7 Mioglobina Emoglobina po
Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in SCIENZE BIOLOGICHE Insegnamento di CHIMICA BIOLOGICA Prof. Augusto Parente Anno Accademico 2014-15 Lezione 7 Mioglobina Emoglobina po
prodotto finale della glicolisi
 Piruvato: prodotto finale della glicolisi Può andare incontro a vari destini: -in condizioni anaerobie: il piruvato viene ridotto a lattato (fermentazione lattica) o ad etanolo (fermentazione alcolica)
Piruvato: prodotto finale della glicolisi Può andare incontro a vari destini: -in condizioni anaerobie: il piruvato viene ridotto a lattato (fermentazione lattica) o ad etanolo (fermentazione alcolica)
Il metabolismo: concetti di base
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Il metabolismo: concetti di base Caratteristiche generali Strategie Trofiche Il metabolismo:
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Il metabolismo: concetti di base Caratteristiche generali Strategie Trofiche Il metabolismo:
Fonte diretta di Energia è l ATP.
 Una cellula compie tre tipi di lavoro: -Lavoro meccanico: movimenti muscolari.. -Lavoro di trasporto: trasporto contro gradiente -Lavoro chimico: assemblaggio di polimeri da monomeri Fonte diretta di Energia
Una cellula compie tre tipi di lavoro: -Lavoro meccanico: movimenti muscolari.. -Lavoro di trasporto: trasporto contro gradiente -Lavoro chimico: assemblaggio di polimeri da monomeri Fonte diretta di Energia
Rapporto Struttura/Funzione delle Proteine
 Macromolecole Biologiche Chimica Biologica A.A. 2010-2011 Rapporto Struttura/Funzione delle Proteine Struttura/Funzione delle Proteine Interazioni proteina-ligando come base della funzione di molte proteine
Macromolecole Biologiche Chimica Biologica A.A. 2010-2011 Rapporto Struttura/Funzione delle Proteine Struttura/Funzione delle Proteine Interazioni proteina-ligando come base della funzione di molte proteine
2 INCONTRO: LA PRODUZIONE DI ENERGIA NELLA CELLULA
 INCONTRO: LA PRODUZIONE DI ENERGIA NELLA CELLULA 1 INTRODUZIONE 1 L energia chimica Esistono diversi tipi di energia e una tra queste è l energia chimica: un tipo di energia che possiedono tutte le molecole
INCONTRO: LA PRODUZIONE DI ENERGIA NELLA CELLULA 1 INTRODUZIONE 1 L energia chimica Esistono diversi tipi di energia e una tra queste è l energia chimica: un tipo di energia che possiedono tutte le molecole
L EQUILIBRIO ACIDO-BASE NEL SANGUE
 L EQUILIBRIO ACIDO-BASE NEL SANGUE ph fisiologico: 7.35-7.45 ph < 7.35 acidosi ph > 7.45 alcalosi Lezione 24 1 L equazione di Henderson-Hasselbalch HA H + + A - La costante di equilibrio (K) (o costante
L EQUILIBRIO ACIDO-BASE NEL SANGUE ph fisiologico: 7.35-7.45 ph < 7.35 acidosi ph > 7.45 alcalosi Lezione 24 1 L equazione di Henderson-Hasselbalch HA H + + A - La costante di equilibrio (K) (o costante
Cap.21 CATABOLISMO DEI LIPIDI
 Cap.21 CATABOLISMO DEI LIPIDI Glucosio= forma di energia immediatamente disponibile LIPIDI= Deposito energetico utilizzabile da tutti i tessuti, tranne cervello e globuli rossi Rispetto ai carboidrati,
Cap.21 CATABOLISMO DEI LIPIDI Glucosio= forma di energia immediatamente disponibile LIPIDI= Deposito energetico utilizzabile da tutti i tessuti, tranne cervello e globuli rossi Rispetto ai carboidrati,
TRASDUZIONE DEL SEGNALE CELLULARE
 TRASDUZIONE DEL SEGNALE CELLULARE RECETTORI I recettori ormonali sono proteine (spesso glicoproteine) capaci di riconoscere e legare l ormone L interazione tra ormone e recettore è estremamente specifica
TRASDUZIONE DEL SEGNALE CELLULARE RECETTORI I recettori ormonali sono proteine (spesso glicoproteine) capaci di riconoscere e legare l ormone L interazione tra ormone e recettore è estremamente specifica
Le proteine III. Corso di Biochimica 1. Prof. Giuseppina Pitari
 Le proteine III Corso di Biochimica 1 Prof. Giuseppina Pitari Ossi-mioglobina legame idrogeno lato distale La mioglobina L eme quindi consiste di una struttura organica alla quale è legato un atomo di
Le proteine III Corso di Biochimica 1 Prof. Giuseppina Pitari Ossi-mioglobina legame idrogeno lato distale La mioglobina L eme quindi consiste di una struttura organica alla quale è legato un atomo di
DISTRIBUZIONE DELLA PERFUSIONE POLMONARE DISTRIBUZIONE DELLA VENTILAZIONE POLMONARE DEFINIRE LA COMPLIANCE POLMONARE
 VOLUMI POLMONARI DISTRIBUZIONE DELLA PERFUSIONE POLMONARE DISTRIBUZIONE DELLA VENTILAZIONE POLMONARE DEFINIRE LA COMPLIANCE POLMONARE DEFINIRE LE RESISTENZE POLMONARI DEFINIRE IL LAVORO POLMONARE Equazione
VOLUMI POLMONARI DISTRIBUZIONE DELLA PERFUSIONE POLMONARE DISTRIBUZIONE DELLA VENTILAZIONE POLMONARE DEFINIRE LA COMPLIANCE POLMONARE DEFINIRE LE RESISTENZE POLMONARI DEFINIRE IL LAVORO POLMONARE Equazione
Il trasporto dell ossigeno
 Prof. Giorgio Sartor Il trasporto dell ossigeno Copyright 2001-2016 by Giorgio Sartor. All rights reserved. Versione 1.9.2 mar 2016 Trasporto dell ossigeno egli organismi aerobi il trasporto dell ossigeno
Prof. Giorgio Sartor Il trasporto dell ossigeno Copyright 2001-2016 by Giorgio Sartor. All rights reserved. Versione 1.9.2 mar 2016 Trasporto dell ossigeno egli organismi aerobi il trasporto dell ossigeno
Laboratorio Fitness & Wellness
 Laboratorio Fitness & Wellness Anno Accademico 2015/2016 Ewan Thomas, MSc Principi di Bioenergetica e Biomeccanica Metabolismo Catabolismo Processi di degradazione che permettono di liberare energia Anabolismo
Laboratorio Fitness & Wellness Anno Accademico 2015/2016 Ewan Thomas, MSc Principi di Bioenergetica e Biomeccanica Metabolismo Catabolismo Processi di degradazione che permettono di liberare energia Anabolismo
LA MIOGLOBINA e L EMOGLOBINA
 UNITÀ VET. DIDATTICA DI PROPEDEUTICA BIOCHIMICA LA MIOGLOBINA e L EMOGLOBINA Roberto Giacominelli Stuffler LA MIOGLOBINA E L EMOGLOBINAL I vertebrati hanno selezionato due meccanismi principali per rifornire
UNITÀ VET. DIDATTICA DI PROPEDEUTICA BIOCHIMICA LA MIOGLOBINA e L EMOGLOBINA Roberto Giacominelli Stuffler LA MIOGLOBINA E L EMOGLOBINAL I vertebrati hanno selezionato due meccanismi principali per rifornire
Il metabolismo microbico
 Corso di Microbiologia Generale. A.A. 2015-2016 Il metabolismo microbico Dott.ssa Annalisa Serio Il metabolismo Insieme di reazioni chimiche che avvengono all interno di un organismo vivente: Le reazioni
Corso di Microbiologia Generale. A.A. 2015-2016 Il metabolismo microbico Dott.ssa Annalisa Serio Il metabolismo Insieme di reazioni chimiche che avvengono all interno di un organismo vivente: Le reazioni
ACIDI GRASSI INSATURI
 LIPIDI ACIDI GRASSI SATURI ACIDI GRASSI INSATURI TRIGLICERIDI TRIGLICERIDI Grassi neutri o lipidi semplici glicerolo + 1 acido grasso monogliceride glicerolo + 2 acidi grassi digliceride glicerolo + 3
LIPIDI ACIDI GRASSI SATURI ACIDI GRASSI INSATURI TRIGLICERIDI TRIGLICERIDI Grassi neutri o lipidi semplici glicerolo + 1 acido grasso monogliceride glicerolo + 2 acidi grassi digliceride glicerolo + 3
CICLO DI KREBS (o DELL ACIDO CITRICO)
 CICLO DI KREBS (o DELL ACIDO CITRICO) È un processo ossidativo che ha un ruolo centrale nel metabolismo energetico delle cellule eucariotiche. Avviene nella matrice mitocondriale. È alimentato soprattutto
CICLO DI KREBS (o DELL ACIDO CITRICO) È un processo ossidativo che ha un ruolo centrale nel metabolismo energetico delle cellule eucariotiche. Avviene nella matrice mitocondriale. È alimentato soprattutto
Il livello cellulare di organizzazione: la struttura cellulare. Cattedra di Fisiologia Umana
 Il livello cellulare di organizzazione: la struttura cellulare Cattedra di Fisiologia Umana 1. La diversità delle cellule nel corpo umano Le cellule del corpo hanno molte differenti forme ed una varietà
Il livello cellulare di organizzazione: la struttura cellulare Cattedra di Fisiologia Umana 1. La diversità delle cellule nel corpo umano Le cellule del corpo hanno molte differenti forme ed una varietà
CHIMICA BIOLOGICA. Seconda Università degli Studi di Napoli. DiSTABiF. Corso di Laurea in Scienze Biologiche. Insegnamento di. Anno Accademico
 Seconda Università degli Studi di Napoli DiSTABiF Prof. Antimo Di Maro Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Anno Accademico 2015-16 Lezione 15 Catena di trasporto degli
Seconda Università degli Studi di Napoli DiSTABiF Prof. Antimo Di Maro Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Anno Accademico 2015-16 Lezione 15 Catena di trasporto degli
