Lezione 25: Un approccio macroscopico all equazione dei gas
|
|
|
- Geronima Eloisa Giusti
- 7 anni fa
- Visualizzazioni
Transcript
1 Lezione 25 - pag.1 Lezione 25: Un approccio macroscopico all equazione dei gas Dal micro al macro Nella lezione 22 abbiamo costruito un modello microscopico che spiega bene alcune caratteristiche dei gas rarefatti. Il modello li considera composti da un grandissimo numero di molecole identiche, molto distanti l una dall altra, che si muovono incessantemente in tutto il volume che hanno a disposizione. Proprio la grande distanza fa sì che gli urti tra una molecola e l altra siano in numero trascurabile rispetto agli urti che esse subiscono contro le pareti del recipiente. La pressione sul recipiente è dovuta alla media degli impulsi che ad ogni urto si esercitano contro le sue pareti. Il modello ci aveva permesso di ricavare una previsione interessante, e cioè che il prodotto pressione per volume è proporzionale all energia cinetica media delle molecole: PV = 2/3 N <E C > In questa lezione vogliamo invece spiegare come si possono studiare i gas rarefatti dal punto di vista sperimentale. Naturalmente non è possibile misurare le grandezze microscopiche, come ad esempio la velocità di una singola molecola, o l impulso che essa trasferisce a una parete durante un urto. Dovremo dunque accontentarci di misurare le grandezze che caratterizzano un gas dal punto di vista macroscopico: la sua pressione, il volume che occupa e la temperatura a cui si trova Separare le variabili Lo stato in cui si trova un gas è noto quando si conoscono i valori di pressione, volume e temperatura. Queste tre grandezze si chiamano quindi variabili di stato. Lo stato del gas cambia, quando almeno uno dei tre valori cambia: si chiama trasformazione un processo subito dal gas, nel corso del quale cambia il suo stato. Pensate a quello che succede quando usate una pompa per gonfiare la ruota della bicicletta: ad ogni corsa dello stantuffo il volume dell aria al suo interno diminuisce, aumenta la sua pressione, e aumenta un po la temperatura (infatti dopo qualche corsa tutta la pompa si scalda in modo sensibile). Dunque, in una trasformazione come quella che abbiamo appena descritto, tutte e tre le variabili di stato cambiano simultaneamente: si tratta quindi di un processo difficile da trattare in modo quantitativo. In questa lezione vogliamo descrivere quelle trasformazioni in cui due sole variabili di stato cambiano valore, mentre la terza rimane costante.
2 Lezione 25 - pag Isoterme e legge di Boyle La più semplice trasformazione che possiamo considerare è un isoterma: si chiamano così le trasformazioni in cui la temperatura rimane costante. Quando lo scienziato inglese Robert Boyle, nel diciassettesimo secolo, studiò queste trasformazioni fu necessaria da parte sua una buona dose d ingegno. Oggi possiamo facilmente ripetere le sue osservazioni in modo assai semplice ( fig.25.1) Fig.25.1 Come si studia una trasformazione isoterma Si intrappola una quantità prefissata di aria dentro alla siringa, poi si comprime lentamente lo stantuffo, e si misura come aumenta la pressione quando il volume viene ridotto. L operazione deve essere lenta perché in caso contrario, come già detto, l aria si scalda e la trasformazione non è più isoterma. Boyle scoprì che esiste una semplice relazione tra la pressione a cui si trova un gas e il volume da esso occupato: quando la temperatura rimane costante, le due grandezze sono inversamente proporzionali. La legge di Boyle che abbiamo appena enunciato può essere espressa anche con la formula: PV = costante La costante dipende dalla temperatura: più è alta la temperatura dell aria, più la costante è grande. I risultati degli esperimenti di Boyle possono essere descritti in forma grafica ( fig.25.2) Fig.25.2 Rappresentazione grafica della legge di Boyle. La curva pressione volume, ad una data temperatura, è un ramo di iperbole
3 Lezione 25 - pag Trasformazioni a volume costante Ora consideriamo le trasformazioni a volume costante, delle quali ci interessa studiare come cambia la pressione del gas quando ne cambiamo la temperatura ( fig.25.3). Fig.25.3 Come si studia una trasformazione a volume costante L aria contenuta nella provetta è in equilibrio termico con l acqua contenuta nel becher. Possiamo perciò far variare la sua temperatura da 0 C (quando l acqua nel becher è in equilibrio termico con il ghiaccio) a 100 C (quando l acqua bolle). I risultati di questo esperimento possono essere descritti con un grafico temperatura - pressione ( fig.25.4) Fig.25.4 Il grafico temperatura pressione per un gas il cui volume rimane costante. L andamento è lineare, ma la pendenza dei segmenti di retta è maggiore quando la pressione iniziale del gas è più grande La figura 25.4 mostra i risultati ottenuti in esperimenti con gas differenti, e con volumi iniziali differenti. Questi grafici hanno un aspetto in comune: se li estrapoliamo alle basse temperature, tutti incontrano l asse orizzontale ad una temperatura di -273 C. Se fate questo esperimento nel laboratorio della vostra scuola non aspettatevi di trovare un risultato così preciso: di solito le intersezioni con l asse orizzontale cadono tra 250 C e 300 C.
4 Lezione 25 - pag Trasformazioni a pressione costante Un modo semplice per realizzare una trasformazione a pressione costante consiste nell utilizzare una provetta capillare, nella quale viene inserita, tramite una siringa, una goccia di mercurio. Serve poi una riga millimetrata, da affiancare alla provetta come mostrato in figura ( fig.25.5): Fig.25.5 Come si studia una trasformazione a pressione costante Provetta e riga (è bene che sia metallica!) vengono immerse nell acqua contenuta in un becher: un termometro ne misura la temperatura. Il gas del quale studiamo il comportamento è l aria intrappolata tra il fondo della provetta ed il tappo di mercurio. Accendendo la fiamma sotto al becher la temperatura dell aria sale, la sua pressione non cambia perché il tappo si solleva: in ogni istante, la pressione dell aria è pari alla pressione atmosferica esterna, più la piccola pressione che il tappo di mercurio esercita a causa del suo peso. Conoscendo la sezione della provetta e il livello a cui si trova il tappo di mercurio (che leggiamo sul righello) possiamo così determinare il volume che il gas occupa alle varie temperature. I risultati di questo esperimento possono essere descritti con un grafico temperatura - volume ( fig.25.6).
5 Lezione 25 - pag.5 Fig.25.6 Il grafico temperatura volume per un gas la cui pressione rimane costante. L andamento è lineare, ma la pendenza dei segmenti di retta è maggiore quando il volume iniziale del gas è più grande La figura 25.6 mostra i risultati ottenuti in esperimenti con gas differenti, e con volumi iniziali differenti. Questi grafici hanno in comune lo stesso aspetto che abbiamo visto in precedenza: se li estrapoliamo alle basse temperature, tutti dovrebbero incontrare l asse orizzontale ad una temperatura di -273 C. Come prima, se fate davvero questo esperimento non aspettatevi di trovare un risultato così preciso: anche in questo caso le intersezioni con l asse orizzontale cadono di solito tra 250 C e 300 C La scala Kelvin per la temperatura I risultati dei due esperimenti precedenti si possono descrivere in modo particolarmente semplice se adottiamo una nuova scala per la misura della temperatura, detta scala assoluta o scala kelvin in onore dello scienziato inglese Lord Kelvin. La scala Kelvin, nota anche come scala assoluta della temperatura, ha lo zero a 273 C, non prevede valori negativi, ed è divisa in intervalli uguali al grado della scala Celsius. La temperatura in kelvin è pari al valore della temperatura in gradi Celsius più 273: temperatura in kelvin = temperatura in gradi Celsius L acqua diventa ghiaccio alla temperatura di 273 K, e bolle a 373 K. Il fatto che l ampiezza dei gradi Celsius e dei kelvin sia la stessa, fa sì che le differenze di temperatura siano identiche nelle due scale. Tra la temperatura di fusione del ghiaccio e quella di ebollizione dell acqua c è un intervallo di 100 K, così come c è un intervallo di 100 C Dagli esperimenti alla matematica Vediamo allora che aspetto assumono i grafici che descrivono le trasformazioni di un gas a pressione costante e a volume costante, quando misuriamo le temperature in kelvin ( fig.25.7):
6 Lezione 25 - pag.6 a) b) Fig.25.7 Il grafico temperatura - volume a pressione costante (a) e quello temperatura - pressione a volume costante (b), quando la temperatura è misurata in kelvin I due grafici sono rette che passano per l origine: si tratta insomma di semplici relazioni di proporzionalità diretta! Se indichiamo con T la temperatura assoluta (cioè la temperatura misurata in kelvin), abbiamo quindi: quando V è costante: quando P è costante: P è direttamente proporzionale a T V è direttamente proporzionale a T Studiando le trasformazioni isoterme avevamo invece scoperto che: quando T è costante: P è inversamente proporzionale a V L equazione di stato dei gas Tutte e tre le relazioni che abbiamo visto nel paragrafo precedente possono essere sintetizzate in un unica formula che si chiama equazione di stato dei gas ideali: PV = costante T Essa afferma che il prodotto pressione per volume, nel caso di un gas rarefatto, è proporzionale alla temperatura assoluta a cui si trova il gas. Se dunque raddoppiamo la temperatura mantenendo costante il volume, allora la pressione raddoppia. Se nel raddoppiare la temperatura manteniamo fissa la pressione, allora è il volume a raddoppiare. La costante che compare nell equazione di stato dipende dalla quantità di gas che prendiamo in considerazione: più gas mettiamo in uno stesso volume, più grande sarà la sua pressione, dunque anche il prodotto PV. La quantità di gas si può esprimere in termini microscopici, specificando il numero N di molecole da cui è composto, oppure in termini macroscopici, specificandone la quantità di sostanza n (cioè il numero di moli che contiene). Il legame tra N e n, come sapete, è rappresentato dal numero di Avogadro: N = n N A
7 Lezione 25 - pag.7 Se esprimiamo la quantità di gas in termini del numero n di moli, l equazione si scrive così: PV = nrt Il valore di R, che si chiama costante dei gas, si ricava dagli esperimenti: J R = 8,31. Questo significa che il prodotto pressione per volume vale 8,31 joule mol K per ogni mole di gas considerata, e per ogni kelvin di temperatura assoluta. Se invece vogliamo esprimere la quantità di gas specificandone il numero N di molecole occorre usare una costante molto più piccola, che si indica con k e che si chiama costante di Boltzmann: PV = NkT Dal momento che N è volte più grande di n, la costante di Boltzmann k dovrà per forza essere volte più piccola della costante dei gas R: La sintesi finale k = 1, J K Il modello di gas ideale sviluppato nella lezione 22 ci ha portati a concludere che Ora abbiamo ricavato che PV = 2/3 N <E C > PV = NkT Il confronto delle due equazioni ci permette di concludere che: <E C > = 3/2 kt È un risultato semplice e fantastico: ogni molecola di un gas rarefatto che si trova alla temperatura T, nel suo incessante moto di traslazione da una parete all altra del recipiente, ha in media un energia data da 3/2kT.
1.Pressione di un Gas
 1.Pressione di un Gas Un gas è formato da molecole che si muovono in modo disordinato, urtandosi fra loro e urtando contro le pareti del recipiente che le contiene. Durante gli urti, le molecole esercitano
1.Pressione di un Gas Un gas è formato da molecole che si muovono in modo disordinato, urtandosi fra loro e urtando contro le pareti del recipiente che le contiene. Durante gli urti, le molecole esercitano
1. Lo studio dei gas nella storia 2. I gas ideali e la teoria cinetico-molecolare 3. La pressione dei gas 4. La legge di Boyle o legge isoterma 5.
 Unità n 6 Le leggi dei gas 1. Lo studio dei gas nella storia 2. I gas ideali e la teoria cinetico-molecolare 3. La pressione dei gas 4. La legge di Boyle o legge isoterma 5. La legge di Gay-Lussac o legge
Unità n 6 Le leggi dei gas 1. Lo studio dei gas nella storia 2. I gas ideali e la teoria cinetico-molecolare 3. La pressione dei gas 4. La legge di Boyle o legge isoterma 5. La legge di Gay-Lussac o legge
PRIMI ELEMENTI DI TERMODINAMICA. La termodinamica studia le leggi con cui i sistemi scambiano (cedono e ricevono) energia con l ambiente.
 PRIMI ELEMENTI DI TERMODINAMICA Un sistema è un insieme di corpi che possiamo immaginare avvolti da una superficie chiusa, ma permeabile alla materia e all energia. L ambiente è tutto ciò che si trova
PRIMI ELEMENTI DI TERMODINAMICA Un sistema è un insieme di corpi che possiamo immaginare avvolti da una superficie chiusa, ma permeabile alla materia e all energia. L ambiente è tutto ciò che si trova
Stati della materia. Esempio. Fusione e solidificazione. Esempio. Stati di aggregazione della materia
 Stati della materia STATI DI AGGREGAZIONE DELLA MATERIA E GAS PERFETTI Cosa sono gli stati della materia? Gli stati della materia sono come si presenta la materia nell universo fisico e dipendono dalla
Stati della materia STATI DI AGGREGAZIONE DELLA MATERIA E GAS PERFETTI Cosa sono gli stati della materia? Gli stati della materia sono come si presenta la materia nell universo fisico e dipendono dalla
TERMODINAMICA. Il sistema è il corpo o l insieme dei corpi sotto esame.
 TERMODINAMICA SISTEMI TERMODINAMICI Il sistema è il corpo o l insieme dei corpi sotto esame. L ambiente esterno è l insieme di tutti i corpi che possono interagire con il sistema. Tipi di sistemi termodinamici
TERMODINAMICA SISTEMI TERMODINAMICI Il sistema è il corpo o l insieme dei corpi sotto esame. L ambiente esterno è l insieme di tutti i corpi che possono interagire con il sistema. Tipi di sistemi termodinamici
Unità 1. La temperatura
 Unità 1 La temperatura 1. Il termometro La sensazione di caldo e di freddo è soggettiva: per renderla misurabile si usa il termoscopio. È un recipiente di vetro con tappo forato e tubicino, contenente
Unità 1 La temperatura 1. Il termometro La sensazione di caldo e di freddo è soggettiva: per renderla misurabile si usa il termoscopio. È un recipiente di vetro con tappo forato e tubicino, contenente
L equilibrio dei gas. Lo stato di equilibrio di una data massa di gas è caratterizzato da un volume, una pressione e una temperatura
 Termodinamica 1. L equilibrio dei gas 2. L effetto della temperatura sui gas 3. La teoria cinetica dei gas 4. Lavoro e calore 5. Il rendimento delle macchine termiche 6. Il secondo principio della termodinamica
Termodinamica 1. L equilibrio dei gas 2. L effetto della temperatura sui gas 3. La teoria cinetica dei gas 4. Lavoro e calore 5. Il rendimento delle macchine termiche 6. Il secondo principio della termodinamica
La temperatura e il calore
 La temperatura e il calore Questo simbolo significa che l esperimento si può realizzare con materiali o strumenti presenti nel nostro laboratorio Questo simbolo significa che l esperimento si può realizzare
La temperatura e il calore Questo simbolo significa che l esperimento si può realizzare con materiali o strumenti presenti nel nostro laboratorio Questo simbolo significa che l esperimento si può realizzare
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 6 Le leggi dei gas 1. I gas ideali e la teoria cinetico-molecolare 2. La pressione dei gas 3.
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 6 Le leggi dei gas 1. I gas ideali e la teoria cinetico-molecolare 2. La pressione dei gas 3.
Programma svolto a.s. 2015/2016. Materia: fisica
 Programma svolto a.s. 2015/2016 Classe: 4A Docente: Daniela Fadda Materia: fisica Dettagli programma Cinematica e dinamica: moto circolare uniforme (ripasso); moto armonico (ripasso); moto parabolico (ripasso);
Programma svolto a.s. 2015/2016 Classe: 4A Docente: Daniela Fadda Materia: fisica Dettagli programma Cinematica e dinamica: moto circolare uniforme (ripasso); moto armonico (ripasso); moto parabolico (ripasso);
La temperatura e il calore. Documento riadattato da MyZanichelli.it Isabella Soletta Febbraio 2012 Parte 1/3
 La temperatura e il calore Documento riadattato da MyZanichelli.it Isabella Soletta Febbraio 2012 Parte 1/3 Questo simbolo significa che l esperimento si può realizzare con materiali o strumenti presenti
La temperatura e il calore Documento riadattato da MyZanichelli.it Isabella Soletta Febbraio 2012 Parte 1/3 Questo simbolo significa che l esperimento si può realizzare con materiali o strumenti presenti
GAS IDEALI E REALI. Prendiamo ora in considerazione un sistema particolare termodinamico: il gas. Un gas è un fluido con le seguenti caratteristiche:
 GAS IDEALI E REALI Gas ideale. Prendiamo ora in considerazione un sistema particolare termodinamico: il gas. Un gas è un fluido con le seguenti caratteristiche: - non ha forma, ne volume proprio; - e comprimibile.
GAS IDEALI E REALI Gas ideale. Prendiamo ora in considerazione un sistema particolare termodinamico: il gas. Un gas è un fluido con le seguenti caratteristiche: - non ha forma, ne volume proprio; - e comprimibile.
SCALA TERMOMETRICA CELSIUS
 TERMOLOGIA TEMPERATURA LA TEMPERATURA E UN INDICE DELLA SENSAZIONE FISIOLOGICA DI CALDO/FREDDO. A LIVELLO MICROSCOPICO E INDICE DELLO STATO DI AGITAZIONE TERMICA MOLECOLARE, ESSENDO PROPORZIONALE ALLA
TERMOLOGIA TEMPERATURA LA TEMPERATURA E UN INDICE DELLA SENSAZIONE FISIOLOGICA DI CALDO/FREDDO. A LIVELLO MICROSCOPICO E INDICE DELLO STATO DI AGITAZIONE TERMICA MOLECOLARE, ESSENDO PROPORZIONALE ALLA
Ultima verifica pentamestre. 1)definizione di miscuglio, soluzione, composto, elemento, molecola ( definizione importantissima!!!!!!!!
 Ultima verifica pentamestre 1)definizione di miscuglio, soluzione, composto, elemento, molecola ( definizione importantissima!!!!!!!!) 2) gruppi dal IV al VIII 3) differenza tra massa atomica e massa atomica
Ultima verifica pentamestre 1)definizione di miscuglio, soluzione, composto, elemento, molecola ( definizione importantissima!!!!!!!!) 2) gruppi dal IV al VIII 3) differenza tra massa atomica e massa atomica
Stati di aggregazione della materia
 Stati di aggregazione della materia A seconda della natura dei legami tra gli atomi o delle forze tra le molecole si possono avere diversi stati di aggregazione della materia SOLIDO LIQUIDO GAS PLASMA
Stati di aggregazione della materia A seconda della natura dei legami tra gli atomi o delle forze tra le molecole si possono avere diversi stati di aggregazione della materia SOLIDO LIQUIDO GAS PLASMA
LA 1 a LEGGE DI VOLTA E GAY LUSSAC O DELLE ISOBARICHE
 1 LA 1 a LEGGE DI VOLTA E GAY LUSSAC O DELLE ISOBARICHE L energia si presenta in diverse forme e una delle più importanti è il calore. I fenomeni naturali sono quasi sempre accompagnati da sviluppo o assorbimento
1 LA 1 a LEGGE DI VOLTA E GAY LUSSAC O DELLE ISOBARICHE L energia si presenta in diverse forme e una delle più importanti è il calore. I fenomeni naturali sono quasi sempre accompagnati da sviluppo o assorbimento
TERMODINAMICA Per lo studio scientifico di un problema occorre separare idealmente una regione di spazio limitata ( sistema ) da tutto ciò che la
 ERMODINAMICA Per lo studio scientifico di un problema occorre separare idealmente una regione di spazio limitata ( sistema ) da tutto ciò che la circonda e può influenzarne il comportamento ( ambiente
ERMODINAMICA Per lo studio scientifico di un problema occorre separare idealmente una regione di spazio limitata ( sistema ) da tutto ciò che la circonda e può influenzarne il comportamento ( ambiente
UNITÀ 1 La temperatura. Test
 Test 1 Quale delle seguenti affermazioni è vera? A Il termoscopio è un termometro con una scala graduata. B Il termometro è un termoscopio con la scala graduata. C Il termoscopio visualizza variazioni
Test 1 Quale delle seguenti affermazioni è vera? A Il termoscopio è un termometro con una scala graduata. B Il termometro è un termoscopio con la scala graduata. C Il termoscopio visualizza variazioni
Il Gas Ideale. Il gas ideale é un'astrazione
 Il Gas Ideale a) le particelle sono animate da moto perenne, ed occupano omogeneamente tutto lo spazio a loro disposizione b) il movimento delle particelle è casuale c) le particelle hanno volume proprio
Il Gas Ideale a) le particelle sono animate da moto perenne, ed occupano omogeneamente tutto lo spazio a loro disposizione b) il movimento delle particelle è casuale c) le particelle hanno volume proprio
approfondimento Fasi e cambiamenti di fase
 approfondimento Fasi e cambiamenti di fase Gas ideali e gas reali Teoria cinetica dei gas e conseguenze Cambiamenti di fase e conservazione della energia Gas ideali e gas reali In un gas ideale: l interazione
approfondimento Fasi e cambiamenti di fase Gas ideali e gas reali Teoria cinetica dei gas e conseguenze Cambiamenti di fase e conservazione della energia Gas ideali e gas reali In un gas ideale: l interazione
Lezione 20: Atomi e molecole
 Lezione 20 - pag.1 Lezione 20: Atomi e molecole 20.1. Il punto della situazione Abbiamo visto, nella lezione precedente, come il modello atomico sia in grado di spiegare la grande varietà di sostanze che
Lezione 20 - pag.1 Lezione 20: Atomi e molecole 20.1. Il punto della situazione Abbiamo visto, nella lezione precedente, come il modello atomico sia in grado di spiegare la grande varietà di sostanze che
Stati di aggregazione della materia. GAS Volume e forma indefiniti LIQUIDO Volume definito, forma indefinita SOLIDO Volume e forma definiti
 9. I Gas Farmacia Stati di aggregazione della materia GAS Volume e forma indefiniti LIQUIDO Volume definito, forma indefinita SOLIDO Volume e forma definiti Stato solido Nello stato solido l energia di
9. I Gas Farmacia Stati di aggregazione della materia GAS Volume e forma indefiniti LIQUIDO Volume definito, forma indefinita SOLIDO Volume e forma definiti Stato solido Nello stato solido l energia di
10. LA MISURA DELLA TEMPERATURA
 1. LA MISURA DELLA TEMPERATURA 1.1 L organizzazione della materia Tutte le sostanze sono composte da atomi. Quando due o più atomi si legano assieme formano molecole. Atomi o molecole sono le unità (particelle)
1. LA MISURA DELLA TEMPERATURA 1.1 L organizzazione della materia Tutte le sostanze sono composte da atomi. Quando due o più atomi si legano assieme formano molecole. Atomi o molecole sono le unità (particelle)
Termodinamica: - cenni sui gas perfetti - macchine termiche - secondo principio. 18/12/2013 Macchine termiche e Secondo Principio della Termodinamica
 Termodinamica: - cenni sui gas perfetti - macchine termiche - secondo principio 1 Definizione di Gas Perfetto Un gas perfetto è un gas ideale il cui comportamento approssima quello dei gas reali a densità
Termodinamica: - cenni sui gas perfetti - macchine termiche - secondo principio 1 Definizione di Gas Perfetto Un gas perfetto è un gas ideale il cui comportamento approssima quello dei gas reali a densità
GAS IDEALI (o gas perfetti )
 GAS IDEALI (o gas perfetti ) TEORIA CINETICA DEI GAS (modello di gas ideale ) molecole puntiformi moto rettilineo ed urti elastici forze attrattive - repulsive intermolecolari nulle PARAMETRI DELLO STATO
GAS IDEALI (o gas perfetti ) TEORIA CINETICA DEI GAS (modello di gas ideale ) molecole puntiformi moto rettilineo ed urti elastici forze attrattive - repulsive intermolecolari nulle PARAMETRI DELLO STATO
Un po di storia. Nel 1600 (Galilei muore nel 1642) si capisce che i gas non sono eterei. Si studiano nel contempo i fenomeni termici
 Temperatura 1 Un po di storia Nel 1600 (Galilei muore nel 1642) si capisce che i gas non sono eterei Torricelli (1608-1647) crea il vuoto Newton diceva che non poteva esistere in Natura Si studiano nel
Temperatura 1 Un po di storia Nel 1600 (Galilei muore nel 1642) si capisce che i gas non sono eterei Torricelli (1608-1647) crea il vuoto Newton diceva che non poteva esistere in Natura Si studiano nel
PRESSIONE GAS PERFETTI
 1 PRESSIONE 1. (Da Veterinaria 2002) Il sangue che scorre nelle arterie dell uomo, come noto, ha una certa pressione. Quale tra le seguenti unità di misura (o simboli) potrebbe essere correttamente usata
1 PRESSIONE 1. (Da Veterinaria 2002) Il sangue che scorre nelle arterie dell uomo, come noto, ha una certa pressione. Quale tra le seguenti unità di misura (o simboli) potrebbe essere correttamente usata
delle curve isoterme dell anidride carbonica
 COMPORTAMENTO DEI GAS REALI l andamento delle curve isoterme dell anidride carbonica mostra che: a temperature elevate le isoterme assomigliano a quelle di un gas perfetto Diagramma di Andrews a temperature
COMPORTAMENTO DEI GAS REALI l andamento delle curve isoterme dell anidride carbonica mostra che: a temperature elevate le isoterme assomigliano a quelle di un gas perfetto Diagramma di Andrews a temperature
TERMOLOGIA & TERMODINAMICA I
 TERMOLOGIA & TERMODINAMICA I 1 Meccanica: studia il moto dei corpi e le cause che lo genera Grandezze meccaniche: massa, velocità, accelerazione, forza, energia Struttura atomica dei gas: particelle tutte
TERMOLOGIA & TERMODINAMICA I 1 Meccanica: studia il moto dei corpi e le cause che lo genera Grandezze meccaniche: massa, velocità, accelerazione, forza, energia Struttura atomica dei gas: particelle tutte
Temperatura e calore. Principi della termodinamica Temperatura Calore Gas ideali
 Temperatura e calore Principi della termodinamica Temperatura Calore Gas ideali Termodinamica Termodinamica branca della fisica che descrive le trasformazioni subite da un sistema in seguito a processi
Temperatura e calore Principi della termodinamica Temperatura Calore Gas ideali Termodinamica Termodinamica branca della fisica che descrive le trasformazioni subite da un sistema in seguito a processi
L ENERGIA CINETICA DELLE MOLECOLE DI UN GAS E LA TEMPERATURA Ogni molecola ha in media un'energia cinetica
 Primo principio- 1 - TERMODINAMICA ENERGIA INTERNA DI UN SISTEMA Ad ogni sistema fisico possiamo associare varie forme di energia, l energia cinetica delle molecole di cui è formato, energia potenziale,
Primo principio- 1 - TERMODINAMICA ENERGIA INTERNA DI UN SISTEMA Ad ogni sistema fisico possiamo associare varie forme di energia, l energia cinetica delle molecole di cui è formato, energia potenziale,
FISICA E LABORATORIO INDIRIZZO C.A.T. CLASSE PRIMA. OBIETTIVI U. D. n 1.2: La rappresentazione di dati e fenomeni
 FISICA E LABORATORIO INDIRIZZO C.A.T. CLASSE PRIMA Le competenze di base a conclusione dell obbligo di istruzione sono le seguenti: Osservare, descrivere ed analizzare fenomeni appartenenti alla realtà
FISICA E LABORATORIO INDIRIZZO C.A.T. CLASSE PRIMA Le competenze di base a conclusione dell obbligo di istruzione sono le seguenti: Osservare, descrivere ed analizzare fenomeni appartenenti alla realtà
Termodinamica e termochimica
 Termodinamica e termochimica La termodinamica è una scienza che studia proprietà macroscopiche della materia e prevede quali processi chimici e fisici siano possibili, in quali condizioni e con quali energie
Termodinamica e termochimica La termodinamica è una scienza che studia proprietà macroscopiche della materia e prevede quali processi chimici e fisici siano possibili, in quali condizioni e con quali energie
LA TEORIA CINETICA DEI GAS
 LA TEORIA CINETICA DEI GAS Le teorie microscopiche Le proprietà degli atomi e delle molecole spiegano le proprietà che riscontriamo nei sistemi macroscopici. Grandee microscopiche Massa di una molecola
LA TEORIA CINETICA DEI GAS Le teorie microscopiche Le proprietà degli atomi e delle molecole spiegano le proprietà che riscontriamo nei sistemi macroscopici. Grandee microscopiche Massa di una molecola
INTRODUZIONE ALLA TERMODINAMICA. Supponiamo di voler studiare il comportamento di una determinata quantità di gas contenuta
 INTRODUZIONE ALLA TERMODINAMICA Supponiamo di voler studiare il comportamento di una determinata quantità di gas contenuta in un recipiente, ad esempio 5g di ossigeno. Dato l elevato numero di molecole
INTRODUZIONE ALLA TERMODINAMICA Supponiamo di voler studiare il comportamento di una determinata quantità di gas contenuta in un recipiente, ad esempio 5g di ossigeno. Dato l elevato numero di molecole
LA TEORIA CINETICA DEI GAS.
 LA TEORIA CINETICA DEI GAS. Il comportamento dei gas,contrariamente a quanto accade per i liquidi e per i solidi appare indipendente dalla specie chimica: la bassissima densità,la capacità di espandersi
LA TEORIA CINETICA DEI GAS. Il comportamento dei gas,contrariamente a quanto accade per i liquidi e per i solidi appare indipendente dalla specie chimica: la bassissima densità,la capacità di espandersi
FISICA. Elaborazione dei dati sperimentali. Autore: prof. Pappalardo Vincenzo docente di Matematica e Fisica
 FISICA Elaborazione dei dati sperimentali Autore: prof. Pappalardo Vincenzo docente di Matematica e Fisica LE GRANDEZZE FISICHE Una grandezza fisica è una quantità che può essere misurata con uno strumento
FISICA Elaborazione dei dati sperimentali Autore: prof. Pappalardo Vincenzo docente di Matematica e Fisica LE GRANDEZZE FISICHE Una grandezza fisica è una quantità che può essere misurata con uno strumento
PROBLEMI E QUESITI DI TERMOLOGIA (SOLUZIONI)
 1 PROBLEMI E QUESITI DI TERMOLOGIA (SOLUZIONI) Qui di seguito viene riportata la risoluzione dei problemi presentati nel file Unità omonimo (enunciati). Si raccomanda di prestare molta attenzione ai ragionamenti
1 PROBLEMI E QUESITI DI TERMOLOGIA (SOLUZIONI) Qui di seguito viene riportata la risoluzione dei problemi presentati nel file Unità omonimo (enunciati). Si raccomanda di prestare molta attenzione ai ragionamenti
IL LAVORO E LE ENERGIE Giuseppe Frangiamore con la collaborazione di Carmelo Bastillo
 Il lavoro IL LAVORO E LE ENERGIE Giuseppe Frangiamore con la collaborazione di Carmelo Bastillo Il lavoro è una grandezza scalare, ed è definito dal prodotto di forza per spostamento. L unità di misura
Il lavoro IL LAVORO E LE ENERGIE Giuseppe Frangiamore con la collaborazione di Carmelo Bastillo Il lavoro è una grandezza scalare, ed è definito dal prodotto di forza per spostamento. L unità di misura
Temperatura. Temperatura
 TERMOMETRIA E CALORE Che cos è la? Grandezza che misura l energia accumulata da un corpo come energia 2 La regola molti processi chimico fisici, quali ad esempio la formazione delle calotte polari, le
TERMOMETRIA E CALORE Che cos è la? Grandezza che misura l energia accumulata da un corpo come energia 2 La regola molti processi chimico fisici, quali ad esempio la formazione delle calotte polari, le
La misura della temperatura
 Calore e temperatura 1. La misura della temperatura 2. La dilatazione termica 3. La legge fondamentale della termologia 4. Il calore latente 5. La propagazione del calore La misura della temperatura La
Calore e temperatura 1. La misura della temperatura 2. La dilatazione termica 3. La legge fondamentale della termologia 4. Il calore latente 5. La propagazione del calore La misura della temperatura La
TERMOLOGIA esercizi risolti Classi quarte L.S.
 TERMOLOGIA esercizi risolti Classi quarte L.S. In questa dispensa verrà riportato lo svolgimento di alcuni esercizi inerenti la termologia e le leggi dei gas. Riprendiamo alcuni concetti utili. Temperatura
TERMOLOGIA esercizi risolti Classi quarte L.S. In questa dispensa verrà riportato lo svolgimento di alcuni esercizi inerenti la termologia e le leggi dei gas. Riprendiamo alcuni concetti utili. Temperatura
Il primo principio della termodinamica
 1 Il primo principio della termodinamica Il primo principio della termodinamica Nelle lezioni precedenti abbiamo visto che per far innalzare la temperatura di un sistema vi sono due possibilità: fornendo
1 Il primo principio della termodinamica Il primo principio della termodinamica Nelle lezioni precedenti abbiamo visto che per far innalzare la temperatura di un sistema vi sono due possibilità: fornendo
FISICA CLASSE 4ASU. CAPITOLO 10 Legge di conservazione della : se su un sistema non agiscono forze, la quantità di moto totale del sistema
 FISICA CLASSE 4ASU CAPITOLO 10 Legge di conservazione della : se su un sistema non agiscono forze, la quantità di moto totale del sistema.... Un urto si dice se in esso si conserva l energia totale dei
FISICA CLASSE 4ASU CAPITOLO 10 Legge di conservazione della : se su un sistema non agiscono forze, la quantità di moto totale del sistema.... Un urto si dice se in esso si conserva l energia totale dei
Se due oggetti A e B sono in equilibrio termico con un terzo oggetto C, allora A e B sono in equilibrio termico tra di loro.
 Lezione 7 - pag.1 Lezione 7: Le leggi della termodinamica 7.1. Che cosa è la termodinamica La parola termodinamica significa, alla lettera, dinamica dei fenomeni termici. È un settore della fisica che
Lezione 7 - pag.1 Lezione 7: Le leggi della termodinamica 7.1. Che cosa è la termodinamica La parola termodinamica significa, alla lettera, dinamica dei fenomeni termici. È un settore della fisica che
Protezione Civile - Regione Friuli Venezia Giulia. Protezione Civile - Regione Friuli Venezia Giulia
 1 Principi di idraulica Definizioni MECCANICA DEI FLUIDI È il ramo della fisica che studia le proprietà dei fluidi, cioè liquidi, vapori e gas. Idrostatica Studia i fluidi in quiete Idrodinamica Studia
1 Principi di idraulica Definizioni MECCANICA DEI FLUIDI È il ramo della fisica che studia le proprietà dei fluidi, cioè liquidi, vapori e gas. Idrostatica Studia i fluidi in quiete Idrodinamica Studia
SCHEDA PER LO STUDENTE LA LEGGE DI BOYLE AL LABORATORIO RTL
 SCHEDA PER LO STUDENTE LA LEGGE DI BOYLE AL LABORATORIO RTL I Titolo dell esperienza LA LEGGE DI BOYLE AL LABORATORIO RTL Autori Paola Cattaneo, Savina Ieni, Lorella Liberatori e Marco Litterio Docenti
SCHEDA PER LO STUDENTE LA LEGGE DI BOYLE AL LABORATORIO RTL I Titolo dell esperienza LA LEGGE DI BOYLE AL LABORATORIO RTL Autori Paola Cattaneo, Savina Ieni, Lorella Liberatori e Marco Litterio Docenti
Fisica per scienze ed ingegneria
 Serway, Jewett Fisica per scienze ed ingegneria Capitolo 20 Fino a circa il 1850 su riteneva che la meccanica e la termodinamica fossero due scienze completamente distinte. La legge di conservazione dell
Serway, Jewett Fisica per scienze ed ingegneria Capitolo 20 Fino a circa il 1850 su riteneva che la meccanica e la termodinamica fossero due scienze completamente distinte. La legge di conservazione dell
Determinazione del calore di combustione specifico di un pellet vegetale
 Determinazione del calore di combustione specifico di un pellet vegetale La bomba calorimetrica di Mahler è un apparecchio che consente la determinazione del potere calorifico superiore di un combustibile
Determinazione del calore di combustione specifico di un pellet vegetale La bomba calorimetrica di Mahler è un apparecchio che consente la determinazione del potere calorifico superiore di un combustibile
Capacità termica e calore specifico
 Calori specifici Capacità termica e calore specifico Il calore si trasferisce da un corpo ad un altro fintanto che i corpi sono a temperature differenti. Potremo scrivere quindi: Q = C ΔT = C (T f T i
Calori specifici Capacità termica e calore specifico Il calore si trasferisce da un corpo ad un altro fintanto che i corpi sono a temperature differenti. Potremo scrivere quindi: Q = C ΔT = C (T f T i
RICHIAMI DI TERMOLOGIA
 RICHIAMI DI TERMOLOGIA Introduzione alla Termodicamica Temperatura e calore Misura della temperatura Principio zero della termodinamica Taratura del termometro Scale di temperatura: Celsuis, Fahrenheit,
RICHIAMI DI TERMOLOGIA Introduzione alla Termodicamica Temperatura e calore Misura della temperatura Principio zero della termodinamica Taratura del termometro Scale di temperatura: Celsuis, Fahrenheit,
I GAS La TEMPERATURA
 I GAS La TEMPERATURA Tutti sappiamo che cosa si intende con il termine temperatura, ma darne una definizione rigorosa non è facile: la cosa più corretta che possiamo dire è che la temperatura è quella
I GAS La TEMPERATURA Tutti sappiamo che cosa si intende con il termine temperatura, ma darne una definizione rigorosa non è facile: la cosa più corretta che possiamo dire è che la temperatura è quella
CdL Professioni Sanitarie A.A. 2012/2013. Unità 9: Gas e processi di diffusione
 L. Zampieri Fisica per CdL Professioni Sanitarie A.A. 12/13 CdL Professioni Sanitarie A.A. 2012/2013 Gas Unità 9: Gas e processi di diffusione Equazione di stato dei gas perfetti Trasformazioni termodinamiche
L. Zampieri Fisica per CdL Professioni Sanitarie A.A. 12/13 CdL Professioni Sanitarie A.A. 2012/2013 Gas Unità 9: Gas e processi di diffusione Equazione di stato dei gas perfetti Trasformazioni termodinamiche
LICEO SCIENTIFICO G. GALILEI - Verona Anno Scolastico
 PROGRAMMA PREVISTO Testo di riferimento: "L indagine del mondo fisico Vol. B (Bergamaschini, Marazzini, Mazzoni) Le unità didattiche a fondo chiaro sono irrinunciabili. Le unità didattiche a fondo scuro
PROGRAMMA PREVISTO Testo di riferimento: "L indagine del mondo fisico Vol. B (Bergamaschini, Marazzini, Mazzoni) Le unità didattiche a fondo chiaro sono irrinunciabili. Le unità didattiche a fondo scuro
Grandezze e Misure 1
 Grandezze e Misure 1 Grandezze e Misure Introduzione Il Metodo Sperimentale Unità di Misura Grandezze Fondamentali e Derivate Massa e Densità Misure dirette e indirette Strumenti di misura Errori nelle
Grandezze e Misure 1 Grandezze e Misure Introduzione Il Metodo Sperimentale Unità di Misura Grandezze Fondamentali e Derivate Massa e Densità Misure dirette e indirette Strumenti di misura Errori nelle
[E] l energia occorrente per innalzare di 1 K la temperatura di 1 Mol di sostanza.
![[E] l energia occorrente per innalzare di 1 K la temperatura di 1 Mol di sostanza. [E] l energia occorrente per innalzare di 1 K la temperatura di 1 Mol di sostanza.](/thumbs/54/33206954.jpg) 1. Il calore specifico di una sostanza è: [A] La quantità di calore contenuta nella massa di una determinata sostanza; [B] la massima temperatura che la sostanza può raggiungere; [C] l energia occorrente
1. Il calore specifico di una sostanza è: [A] La quantità di calore contenuta nella massa di una determinata sostanza; [B] la massima temperatura che la sostanza può raggiungere; [C] l energia occorrente
Calore, lavoro e trasformazioni termodinamiche (1)
 Calore, lavoro e trasformazioni termodinamiche (1) Attraverso scambi di calore un sistema scambia energia con l ambiente. Tuttavia si scambia energia anche quando le forze (esterne e interne al sistema)
Calore, lavoro e trasformazioni termodinamiche (1) Attraverso scambi di calore un sistema scambia energia con l ambiente. Tuttavia si scambia energia anche quando le forze (esterne e interne al sistema)
Lezione 23: Un approccio macroscopico alla temperatura
 Lezione 23 - pag.1 Lezione 23: Un approccio macroscopico alla temperatura 23.1. Che cos è la temperatura? Il titolo di questo paragrafo dovrebbe già insospettirvi: ci eravamo posti la stessa domanda a
Lezione 23 - pag.1 Lezione 23: Un approccio macroscopico alla temperatura 23.1. Che cos è la temperatura? Il titolo di questo paragrafo dovrebbe già insospettirvi: ci eravamo posti la stessa domanda a
Università degli Studi di Milano. Facoltà di Scienze Matematiche Fisiche e Naturali
 Università degli Studi di Milano Facoltà di Scienze Matematiche Fisiche e Naturali Corsi di Laurea in: Informatica ed Informatica per le Telecomunicazioni Anno accademico 2010/11, Laurea Triennale, Edizione
Università degli Studi di Milano Facoltà di Scienze Matematiche Fisiche e Naturali Corsi di Laurea in: Informatica ed Informatica per le Telecomunicazioni Anno accademico 2010/11, Laurea Triennale, Edizione
Termometro a liquido
 Termometro a liquido Il principio su cui si basa il "termometro a gas perfetto (termometro campione), richiede una tecnica di uso assai delicato e quindi raramente impiegata nella pratica di laboratorio.
Termometro a liquido Il principio su cui si basa il "termometro a gas perfetto (termometro campione), richiede una tecnica di uso assai delicato e quindi raramente impiegata nella pratica di laboratorio.
Lezione 22: Il modello di gas ideale
 Lezione - pag.1 Lezione : Il modello di gas ideale.1. Che cosa ci proponiamo di fare Abbiamo detto che i gas sono fatti di molecole molto distanti tra di loro, che si muovono incessantemente, occupando
Lezione - pag.1 Lezione : Il modello di gas ideale.1. Che cosa ci proponiamo di fare Abbiamo detto che i gas sono fatti di molecole molto distanti tra di loro, che si muovono incessantemente, occupando
La fisica al Mazzotti. La temperatura
 La fisica al Mazzotti 16 La temperatura 1 2 Gli stati di aggregazione della materia La materia si presenta nei tre stati di aggregazione: Solido ha un volume e una forma propria Liquido ha un volume proprio
La fisica al Mazzotti 16 La temperatura 1 2 Gli stati di aggregazione della materia La materia si presenta nei tre stati di aggregazione: Solido ha un volume e una forma propria Liquido ha un volume proprio
MISURA DELLE FREQUENZE DI RISONANZA DI UN TUBO SONORO
 MISURA DELLE FREQUENZE DI RISONANZA DI UN TUBO SONORO Scopo dell esperienza è lo studio della propagazione delle onde sonore all interno di un tubo, aperto o chiuso, contenete aria o altri gas. Si verificherà
MISURA DELLE FREQUENZE DI RISONANZA DI UN TUBO SONORO Scopo dell esperienza è lo studio della propagazione delle onde sonore all interno di un tubo, aperto o chiuso, contenete aria o altri gas. Si verificherà
6. IL MOTO Come descrivere un moto.
 6. IL MOTO Per definire il movimento di un corpo o il suo stato di quiete deve sempre essere individuato un sistema di riferimento e ogni movimento è relativo al sistema di riferimento in cui esso avviene.
6. IL MOTO Per definire il movimento di un corpo o il suo stato di quiete deve sempre essere individuato un sistema di riferimento e ogni movimento è relativo al sistema di riferimento in cui esso avviene.
Funzioni elementari. Funzioni lineari. 13. Funzioni elementari. Funzioni lineari.
 Funzioni elementari. Funzioni lineari. Funzioni elementari Per potere determinare le proprietà e quindi il grafico di una qualsiasi funzione a partire dalla sua espressione analitica, dobbiamo prima di
Funzioni elementari. Funzioni lineari. Funzioni elementari Per potere determinare le proprietà e quindi il grafico di una qualsiasi funzione a partire dalla sua espressione analitica, dobbiamo prima di
Funzioni elementari: funzioni potenza
 Funzioni elementari: funzioni potenza Lezione per Studenti di Agraria Università di Bologna (Università di Bologna) Funzioni elementari: funzioni potenza 1 / 36 Funzioni lineari Come abbiamo già visto,
Funzioni elementari: funzioni potenza Lezione per Studenti di Agraria Università di Bologna (Università di Bologna) Funzioni elementari: funzioni potenza 1 / 36 Funzioni lineari Come abbiamo già visto,
Misure di velocità con la guidovia a cuscino d aria (1)
 Misure di velocità con la guidovia a cuscino d aria (1) Obiettivo: Riprodurre un moto con velocità costante utilizzando la guidovia a cuscino d aria. Ricavare la tabella oraria e il grafico orario (grafico
Misure di velocità con la guidovia a cuscino d aria (1) Obiettivo: Riprodurre un moto con velocità costante utilizzando la guidovia a cuscino d aria. Ricavare la tabella oraria e il grafico orario (grafico
CALORIMETRO DELLE mescolanze
 CALORIMETRO DELLE mescolanze Scopo dell esperienza è la misurazione del calore specifico di un corpo solido. Il funzionamento del calorimetro si basa sugli scambi di energia, sotto forma di calore, che
CALORIMETRO DELLE mescolanze Scopo dell esperienza è la misurazione del calore specifico di un corpo solido. Il funzionamento del calorimetro si basa sugli scambi di energia, sotto forma di calore, che
Gradi di libertà negli sta/ di aggregazione della materia
 Gradi di libertà negli sta/ di aggregazione della materia I solidi cristallini sono cara-erizza0 da un ordine nelle posizioni e nelle orientazioni. Gradi di libertà negli sta/ di aggregazione della materia
Gradi di libertà negli sta/ di aggregazione della materia I solidi cristallini sono cara-erizza0 da un ordine nelle posizioni e nelle orientazioni. Gradi di libertà negli sta/ di aggregazione della materia
-GAS IDEALI- Le particelle che costituiscono un gas ideale:
 -GAS IDEALI- Le particelle che costituiscono un gas ideale: sono in movimento continuo e casuale hanno un volume trascurabile rispetto al volume totale a disposizione del gas non interagiscono fra loro
-GAS IDEALI- Le particelle che costituiscono un gas ideale: sono in movimento continuo e casuale hanno un volume trascurabile rispetto al volume totale a disposizione del gas non interagiscono fra loro
Prova scritta di Fisica Generale I Corso di studio in Astronomia 16 luglio 2013
 Prova scritta di Fisica Generale I Corso di studio in Astronomia 16 luglio 013 Problema 1 Un cubo di legno di densità ρ = 800 kg/m 3 e lato a = 50 cm è inizialmente in quiete, appoggiato su un piano orizzontale.
Prova scritta di Fisica Generale I Corso di studio in Astronomia 16 luglio 013 Problema 1 Un cubo di legno di densità ρ = 800 kg/m 3 e lato a = 50 cm è inizialmente in quiete, appoggiato su un piano orizzontale.
GAS. Forze di legame intermolecolari ridotte Stato altamente disordinato
 I GAS PERFETTI GAS Forze di legame intermolecolari ridotte Stato altamente disordinato Principali caratteristiche: Bassa viscosità Assenza di volume e forma propri Comprimibilità Miscibilità Pressione:
I GAS PERFETTI GAS Forze di legame intermolecolari ridotte Stato altamente disordinato Principali caratteristiche: Bassa viscosità Assenza di volume e forma propri Comprimibilità Miscibilità Pressione:
Lezione 3. Principi generali della Meccanica Cinematica, Statica e Dinamica
 Lezione 3 Principi generali della Meccanica Cinematica, Statica e Dinamica Premessa L Universo in cui viviamo costituisce un sistema dinamico, cioè un sistema in evoluzione nel tempo secondo opportune
Lezione 3 Principi generali della Meccanica Cinematica, Statica e Dinamica Premessa L Universo in cui viviamo costituisce un sistema dinamico, cioè un sistema in evoluzione nel tempo secondo opportune
L energia potenziale gravitazionale di un oggetto di massa m che si trova ad un altezza h rispetto ad un livello scelto come riferimento è: E PG = mgh
 Lezione 15 - pag.1 Lezione 15: L energia potenziale e l'energia meccanica 15.1. L energia potenziale gravitazionale Consideriamo quello che succede quando solleviamo un oggetto, applicando un forza appena
Lezione 15 - pag.1 Lezione 15: L energia potenziale e l'energia meccanica 15.1. L energia potenziale gravitazionale Consideriamo quello che succede quando solleviamo un oggetto, applicando un forza appena
I gas. ChimicaGenerale_lezione10
 I gas Nel 1630 fu usato per la prima volta il termine gas: Van Helmont che lo inventò, pensava però che non fosse possibile contenere un gas in un recipiente, perché aveva una natura e una composizione
I gas Nel 1630 fu usato per la prima volta il termine gas: Van Helmont che lo inventò, pensava però che non fosse possibile contenere un gas in un recipiente, perché aveva una natura e una composizione
TEMPERATURA E CALORE. Termometri, dilatazione termica, calore specifico. FISICA - Prof. Massimiliano Bacchi
 TEMPERATURA E CALORE Termometri, dilatazione termica, calore specifico 1 Termoscopio Un oggetto può ad alcuni sembrare caldo, ad altri freddo, oppure due oggetti nella stessa stanza sembrano essere uno
TEMPERATURA E CALORE Termometri, dilatazione termica, calore specifico 1 Termoscopio Un oggetto può ad alcuni sembrare caldo, ad altri freddo, oppure due oggetti nella stessa stanza sembrano essere uno
QUANTITA DI MOTO Corso di Fisica per Farmacia, Facoltà di Farmacia, Università G. D Annunzio, Cosimo Del Gratta 2006
 QUANTITA DI MOTO DEFINIZIONE(1) m v Si chiama quantità di moto di un punto materiale il prodotto della sua massa per la sua velocità p = m v La quantità di moto è una grandezza vettoriale La dimensione
QUANTITA DI MOTO DEFINIZIONE(1) m v Si chiama quantità di moto di un punto materiale il prodotto della sua massa per la sua velocità p = m v La quantità di moto è una grandezza vettoriale La dimensione
Lezione 1 (18/09/2014)
 Lezione 1 (18/09/2014) Esercizi svolti a lezione Esercizio 1. Il 15% degli individui di una popolazione è stato colpito da un epidemia. L 8% delle persone colpite è morto. Calcolare la mortalità rispetto
Lezione 1 (18/09/2014) Esercizi svolti a lezione Esercizio 1. Il 15% degli individui di una popolazione è stato colpito da un epidemia. L 8% delle persone colpite è morto. Calcolare la mortalità rispetto
Un modello per il gas ideale
 Un modello per il gas ideale Un gas ideale consiste di particelle (atomi o molecole) che hanno le seguenti proprietà 1. Il volume proprio delle particelle è trascurabile rispetto al volume occupato dal
Un modello per il gas ideale Un gas ideale consiste di particelle (atomi o molecole) che hanno le seguenti proprietà 1. Il volume proprio delle particelle è trascurabile rispetto al volume occupato dal
Premessa: Si continua a studiare il moto degli oggetti in approssimazione di PUNTO MATERIALE
 Leggi della Dinamica Premessa: Si continua a studiare il moto degli oggetti in approssimazione di PUNTO MATERIALE Fisica con Elementi di Matematica 1 Leggi della Dinamica Perché i corpi cambiano il loro
Leggi della Dinamica Premessa: Si continua a studiare il moto degli oggetti in approssimazione di PUNTO MATERIALE Fisica con Elementi di Matematica 1 Leggi della Dinamica Perché i corpi cambiano il loro
Bilancio di energia: il Primo Principio della Termodinamica. Termodinamica dell Ingegneria Chimica
 Bilancio di energia: il Primo Principio della Termodinamica Termodinamica dell Ingegneria Chimica 1 I Sistemi termodinamici Un sistema è definito da una superficie di controllo, reale o immaginaria, che
Bilancio di energia: il Primo Principio della Termodinamica Termodinamica dell Ingegneria Chimica 1 I Sistemi termodinamici Un sistema è definito da una superficie di controllo, reale o immaginaria, che
I GAS POSSONO ESSERE COMPRESSI.
 I GAS Tutti i gas sono accomunati dalle seguenti proprietà: I GAS POSSONO ESSERE COMPRESSI. L aria compressa occupa un volume minore rispetto a quello occupato dall aria non compressa (Es. gomme dell auto
I GAS Tutti i gas sono accomunati dalle seguenti proprietà: I GAS POSSONO ESSERE COMPRESSI. L aria compressa occupa un volume minore rispetto a quello occupato dall aria non compressa (Es. gomme dell auto
STATICA DEI FLUIDI (Giuseppe Frangiamore con la collaborazione di Michele Sorce)
 STATICA DEI FLUIDI (Giuseppe Frangiamore con la collaborazione di Michele Sorce) Definizione Di Pressione In questo capitolo si analizzeranno le caratteristiche meccaniche dei fluidi in condizioni di equilibrio
STATICA DEI FLUIDI (Giuseppe Frangiamore con la collaborazione di Michele Sorce) Definizione Di Pressione In questo capitolo si analizzeranno le caratteristiche meccaniche dei fluidi in condizioni di equilibrio
Onde sonore stazionarie in un tubo risonante
 Onde sonore stazionarie in un tubo risonante Scopo dell esperimento Determinare la velocità del suono analizzando le caratteristiche delle onde sonore stazionarie in un tubo risonante. Richiamo teorico
Onde sonore stazionarie in un tubo risonante Scopo dell esperimento Determinare la velocità del suono analizzando le caratteristiche delle onde sonore stazionarie in un tubo risonante. Richiamo teorico
Capitolo 6. Variabili casuali continue. 6.1 La densità di probabilità
 Capitolo 6 Variabili casuali continue Le definizioni di probabilità che abbiamo finora usato sono adatte solo per una variabile casuale che possa assumere solo valori discreti; vediamo innanzi tutto come
Capitolo 6 Variabili casuali continue Le definizioni di probabilità che abbiamo finora usato sono adatte solo per una variabile casuale che possa assumere solo valori discreti; vediamo innanzi tutto come
CONVENZIONE SUI SEGNI
 CONVENZIONE SUI SEGNI Si stabilisce una convenzione sui segni sia per gli scambi di calore che per il lavoro che il sistema compie o subisce L>0: LAVORO COMPIUTO DAL SISTEMA Q>0: CALORE ASSORBITO SISTEMA
CONVENZIONE SUI SEGNI Si stabilisce una convenzione sui segni sia per gli scambi di calore che per il lavoro che il sistema compie o subisce L>0: LAVORO COMPIUTO DAL SISTEMA Q>0: CALORE ASSORBITO SISTEMA
TERMOLOGIA TERMOMETRIA E CALORIMETRIA
 1 TERMOLOGIA La termologia è il settore della fisica che si interessa dei fenomeni termici, ovvero studia quei fenomeni in cui hanno una grande importanza la temperatura e il calore. Questa branca della
1 TERMOLOGIA La termologia è il settore della fisica che si interessa dei fenomeni termici, ovvero studia quei fenomeni in cui hanno una grande importanza la temperatura e il calore. Questa branca della
FUNZIONI. }, oppure la
 FUNZIONI 1. Definizioni e prime proprietà Il concetto di funzione è di uso comune per esprimere la seguente situazione: due grandezze variano l una al variare dell altra secondo una certa legge. Ad esempio,
FUNZIONI 1. Definizioni e prime proprietà Il concetto di funzione è di uso comune per esprimere la seguente situazione: due grandezze variano l una al variare dell altra secondo una certa legge. Ad esempio,
Gli stati di aggregazione della materia
 Lezione X - 20/03/2003 ora 8:30-10:30 - Stati fisici della materia, strumenti e Legge di Dalton - Originale di Daniele Bolletta e Carlo Chiari Gli stati di aggregazione della materia La materia che ci
Lezione X - 20/03/2003 ora 8:30-10:30 - Stati fisici della materia, strumenti e Legge di Dalton - Originale di Daniele Bolletta e Carlo Chiari Gli stati di aggregazione della materia La materia che ci
Massa degli atomi e delle molecole
 Dallo studio dei volumi di gas nelle reazioni chimiche alle masse degli atomi e delle molecole Lo stato fisico di di un gas è descritto da tre grandezze fisiche: PRESSIONE (p) VOLUME (V) TEMPERATURA (T)
Dallo studio dei volumi di gas nelle reazioni chimiche alle masse degli atomi e delle molecole Lo stato fisico di di un gas è descritto da tre grandezze fisiche: PRESSIONE (p) VOLUME (V) TEMPERATURA (T)
Queste proprietà derivano dalla grande distanza che separa le molecole che compongono un gas.
 Stato Gassoso Lo stato gassoso I gas hanno tre proprietà caratteristiche: 1.sono facilmente comprimibili 2. si espandono per riempire il loro contenitore 3. occupano molto più spazio dei solidi e liquidi
Stato Gassoso Lo stato gassoso I gas hanno tre proprietà caratteristiche: 1.sono facilmente comprimibili 2. si espandono per riempire il loro contenitore 3. occupano molto più spazio dei solidi e liquidi
Ripasso sulla temperatura, i gas perfetti e il calore
 Ripasso sulla temperatura, i gas perfetti e il calore Prof. Daniele Ippolito Liceo Scientifico Amedeo di Savoia di Pistoia La temperatura Fenomeni non interpretabili con le leggi della meccanica Dilatazione
Ripasso sulla temperatura, i gas perfetti e il calore Prof. Daniele Ippolito Liceo Scientifico Amedeo di Savoia di Pistoia La temperatura Fenomeni non interpretabili con le leggi della meccanica Dilatazione
Modulo B Unità 3 Equilibrio dei fluidi Pagina 1. Solidi, liquidi, aeriformi
 Modulo B Unità 3 Equilibrio dei fluidi Pagina Solidi, liquidi, aeriformi I solidi hanno forma e volume propri, i liquidi hanno volume proprio e forma del recipiente che li contiene, gli aeriformi hanno
Modulo B Unità 3 Equilibrio dei fluidi Pagina Solidi, liquidi, aeriformi I solidi hanno forma e volume propri, i liquidi hanno volume proprio e forma del recipiente che li contiene, gli aeriformi hanno
ESERCITAZIONI CHIMICA-FISICA I a.a. 2012/2013. Metodo differenziale. Problema
 ESERCITAZIONI CHIMICA-FISICA I a.a. 0/03 Metodo differenziale Problema Per la reazione: A + B P sono stati condotti tre esperimenti cinetici a diverse concentrazioni iniziali dei reagenti. I valori iniziali
ESERCITAZIONI CHIMICA-FISICA I a.a. 0/03 Metodo differenziale Problema Per la reazione: A + B P sono stati condotti tre esperimenti cinetici a diverse concentrazioni iniziali dei reagenti. I valori iniziali
EQUAZIONE DELLA RETTA
 EQUAZIONE DELLA RETTA EQUAZIONE DEGLI ASSI L equazione dell asse x è 0. L equazione dell asse y è 0. EQUAZIONE DELLE RETTE PARALLELE AGLI ASSI L equazione di una retta r parallela all asse x è cioè è uguale
EQUAZIONE DELLA RETTA EQUAZIONE DEGLI ASSI L equazione dell asse x è 0. L equazione dell asse y è 0. EQUAZIONE DELLE RETTE PARALLELE AGLI ASSI L equazione di una retta r parallela all asse x è cioè è uguale
4. I principi della meccanica
 1 Leggi del moto 4. I principi della meccanica Come si è visto la cinematica studia il moto dal punto di vista descrittivo, ma non si sofferma sulle cause di esso. Ciò è compito della dinamica. Alla base
1 Leggi del moto 4. I principi della meccanica Come si è visto la cinematica studia il moto dal punto di vista descrittivo, ma non si sofferma sulle cause di esso. Ciò è compito della dinamica. Alla base
Capitolo 2 Le misure delle grandezze fisiche
 Capitolo 2 Le misure delle grandezze fisiche Gli strumenti di misura Gli errori di misura Il risultato di una misura Errore relativo ed errore percentuale Propagazione degli errori Rappresentazione di
Capitolo 2 Le misure delle grandezze fisiche Gli strumenti di misura Gli errori di misura Il risultato di una misura Errore relativo ed errore percentuale Propagazione degli errori Rappresentazione di
PIANO CARTESIANO e RETTE classi 2 A/D 2009/2010
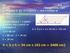 PIANO CARTESIANO e RETTE classi 2 A/D 2009/2010 1) PIANO CARTESIANO serve per indicare, identificare, chiamare... ogni PUNTO del piano (ente geometrico) con una coppia di valori numerici (detti COORDINATE).
PIANO CARTESIANO e RETTE classi 2 A/D 2009/2010 1) PIANO CARTESIANO serve per indicare, identificare, chiamare... ogni PUNTO del piano (ente geometrico) con una coppia di valori numerici (detti COORDINATE).
FUNZIONI LINEARI (Retta, punto di pareggio e relazioni lineari generalizzate)
 FUNZIONI LINEARI (Retta, punto di pareggio e relazioni lineari generalizzate) Copyright SDA Bocconi, Milano La retta Una retta può essere espressa secondo due formulazioni: a. Forma esplicita b. Forma
FUNZIONI LINEARI (Retta, punto di pareggio e relazioni lineari generalizzate) Copyright SDA Bocconi, Milano La retta Una retta può essere espressa secondo due formulazioni: a. Forma esplicita b. Forma
