Gian Giacomo Guilizzoni Dizionario del Chimico Tutti i diritti riservati. Vietata la pubblicazione con ogni mezzo.
|
|
|
- Luigi Adamo
- 8 anni fa
- Visualizzazioni
Transcript
1 V V 1. Volt. 2. Simb. del vanadio, da Vanadis, Venere nella mitologia scandinava. vaccenico, acido Acido trans-11-octadecenoico, CH 3 (CH 2 ) 5 CH=CH(CH 2 ) 9 COOH. vaccini FU Preparazioni contenenti antigeni, destinati a indurre un' immunità attiva specifica contro un agente infettante, o contro una tossina da esso elaborata. vaccinina Benzoilglucosio, C 13 H 16 O 7. vacor Rodenticida, C 13 H 12 N 4 O 3. vacuometri Strumenti per la misura della pressione residua in un recipiente da cui viene evacuato un gas. Con il vacuometro di McLeod a mercurio si possono misurare pressioni da 10-2 a 10-5 torr; con il vacuometro di Pirani, a ionizzazione, da 10-2 a 10-6 torr. vaesite Min., nichelio solfuro, NiS 2. vagli Lastre forate (crivelli) e reti (setacci) usati per la separazione di particelle aventi diversa granulometria. Caratteristiche di un crivello sono lo spessore della lastra, il diametro dei fori e la distanza tra gli assi di due fori. Caratteristiche di un setaccio sono la luce e il numero delle maglie. val ( equivalente). Val Valina. valdivina Glucoside, C 36 H 48 O 20. valentinite Min., ossido di antimonio, Sb 2 O 3. valenza Numero di atomi di idrogeno (per definizione monovalente) che possono unirsi, realmente o virtualmente, con un atomo di un determinato elemento. valerano Terpene, C 15 H 24. valerianica, aldeide 1-pentanale, CH 3 (CH 2 ) 3 CHO. valerianca iso, aldeide 3-metilbutanale, (CH 3 ) 3 CHCH 2 CHO. valerianico, acido Acido 1-pentanoico, CH 3 (CH 2 ) 3 COOH. valerianico iso, acido Acido 3-metilbutanoico, (CH 3 ) 2 CHCH 2 COOH. valerico, acido ( valerianico, acido). valeridina Sedativo, C 13 H 19 NO. valerile Aggruppamento CH 3 (CH 2 ) 3 CO. valerile iso Aggruppamento (CH 3 ) 2 CHCH 2 CO. valerildietilammide iso Sedativo, C 9 H 19 NO. valerilindandione iso Insetticida, C 14 H 14 O 3. valerina ( focenina). valerofenone Fenilbutilchetone, C 6 H 5 CO(CH 2 ) 2 CH 3. valerone 2-pentanone, CH 3 CO(CH 2 ) 2 CH 3. 1
2 valetamato bromuro simpaticolitico, C 19 H 32 BrNO 2. valexon ( phoxim). validamicina Antibiotico, C 20 H 35 NO 13. valina (Val) Acido 2-ammino-3-metilbutanoico, (CH 3 ) 2 CHCH(NH 2 )COOH. valina iso Acido 2-metil-2-amminobutanoico, CH 3 CH 2 C(CH 3 )(NH2)COOH. valium ( diazepam). vallerite Min., solfuro, CuFeS 2. vallosina Alcaloide, C 23 H 28 N 2 O 4. valnoctamide Neurolettico, C 8 H 17 NO. valproico, acido Antiepilettico, C 8 H 16 O 2. VAM Vinile acetato monomero, CH 3 COOCH=CH 2. vamidotion Insetticida, C 8 H 10 NO 4 PS 2. vanadato Anione tetraossovanadato(v), VO 3-4. vanadatometria Metodo di analisi volumetrica basato sull'impiego di soluzioni titolate di vanadio(v). vanadica, anidride Ossido di vanadio(v), V 2 O 5. vanadici, acidi Composti V 2 O 5 nh 2 O. vanadile Aggruppamento VO. vanadinite Min., piombo clorovanadato, Pb 5 Cl(VO 4 ) 3. vanadio Elemento chimico di transizione, gruppo 5d, simb. V, Z = 23; m.a.r. = 50,9415; t.f. = 1900 C; t.e. = 3400 C; n.o. = 2, 3, 5. Il vanadio è diffuso ma in piccole quantità e fu scoperto nel 1870 N.G. Sefstrom. In Italia si estrae dai residui della combustione di oli minerali e si usa per produrre gli acciai rapidi. vandenbrandeite Min., rame uranato, CuUO 4 2H 2 O. van der Waals, costanti di Costanti a (pressione interna) e b (covolume) nell'equazione di van der Waals per i gas reali: (p + a / V 2 ) (V - b) = RT, dove p è la pressione, V il volume molare, T la temperatura assoluta e R la costante universale dei gas. van der Waals, legami di Legami deboli che si stabiliscono tra molecole non polari. vaniglico, acido Acido 4-idrossi-3-metossibenzoico, HO(CH 3 O)C 6 H 3 COOH. vaniglina 4-idrossi-3-metossibenzaldeide, HO(CH 3 O)C 6 H 3 CHO. vaniglina iso 3-idrossi-4-metossibenzaldeide, HO(CH 3 O)C 6 H 3 CHO. vanitiolide Coleretico, C 12 H 15 NO 3 S. vanossite Min., ossido di vanadio idrato, V 6 O 13 5H 2 O. van Slyke, apparecchio di Apparecchio per la determinazione dell' azoto amminico nelle proteine. van't Hoff, coefficiente di (i) Detto anche coefficiente di dissociazione, binomio i = 1 + (ν - 1) α, dove α è il grado di dissociazione e ν il numero di moli più piccole risultanti dalla dissociazione di 1 mol di sostanza. 2
3 van't Hoff, legge di Equazione di stato dei gas ideali applicata alle soluzioni diluite: πv = nrt, dove π è la pressione osmotica, V il volume della soluzione, n il numero di moli del soluto, R la costante universale dei gas e T la temperatura assoluta. Ne deriva che la pressione osmotica delle soluzioni molari di qualsiasi sostanza è all'incirca 22,4 atm alla temeratura di 0 C. van't Hoff, regole di 1 a. Legge di Avogadro applicata alle soluzioni diluite: volumi uguali di soluzioni isotoniche di sostanze diverse, nelle stesse condizioni di temperatura e pressione, contengono ugual numero di particelle disciolte. 2 a. Il numero degli isomeri ottici di un composto organico è 2 n, dove n è il numero degli atomi i carbonio asimmetrici. vanthoffite Min., solfato MgNa 6 (SO 4 ) 4. vapore Sostanza allo stato gassoso che si trova ad una temperatura inferiore alla temperatura critica. vapore non saturo Vapore di una sostanza, sola o in presenza di altri gas e/o vapori, in assenza della fase liquida. vapore saturo Vapore di una sostanza in equilibrio con la fase liquida. vapore saturo secco Vapore saturo riscaldato fino alla temperatura in cui scompare la fase liquida. vapore soprassaturo Vapore saturo surriscaldato raffreddato ad una temperatura inferiore alla temperatura di condensazione, senza che avvenga la condensazione stessa. vapore surriscaldato Vapore saturo secco riscaldato oltre la temperatura in cui scompare la fase liquida, senza che venga raggiunta la tmperatura critica. vaporizzazione Trasformazione endotermica di una sostanza dallo stato liquido allo stato di vapore ( ebollizione) ( evaporazione). varanico, acido Acido biliare, C 27 H 46 O 6. varianza (v) Per una miscela eterogenea, numero di variabili che si possono alterare lasciando invariati il numero ed il tipo delle fasi presenti, secondo la regola delle fasi di Gibbs, v = n f, dove n è il numero dei componenti e f il numero delle fasi in equilibrio. variazione percentuale, coefficiente di (V) Rapporto tra lo scarto tipo di stabilità s e la media aritmetica x di una serie di misurazioni, moltiplicato per 100 (UNI 4723). variscite Min., alluminio fosfato, Al(OH) 2 H 2 PO 4. varon Ossitocico, C 11 H 18 ClNO 3. 3
4 varulite Min., fosfato (Ca,Na)(Fe,Mn) 2 (PO 4 ) 2. vaselina Miscela di alcani superiori, solidi o semisolidi alla temperatura ambiente, con olio minerale viscoso. vashegyite Min., alluminio idrossofosfato, Al 11 (OH) 6 (PO 4 ) 9 38H 2 O. vasicina Alcaloide, C 11 H 12 N 2 O. vasocostrittori Farmaci che restringono i vasi capillari e le piccole arterie. vasodilatatori Farmaci che allargano i vasi capillari e le piccole arterie. vasopressina ( ADH). vat dye Colorante di riduzione. vaterite Min., calcio carbonato, CaCO 3. vauquelinite Min., fosfato CuPb 2 (OH)(CrO 4 )PO 4. vauxite Min., idrossofosfato Al 2 Fe(OH) 2 (PO 4 ) 2 7H 2 O. veatchina Alcaloide, C 22 H 33 NO 2. veatchite Min., stronzio idrossoborato, Sr(OH) 5 B 11 O 16 H 2 O. veenite Min., solfuro (As,Pb,Sb) 2 S 5. vellosina Alcaloide, C 23 H 28 N 2 O 4. velocità (v) Rapporto tra la distanza d percorsa nel tempo t; v = d / t. L' unità SI è il metro al secondo (m/s). velocità angolare (ω) Rapporto tra l angolo α descritto in un moto circolare nel tempo t; ω = α/t; l' unità SI è il radiante al secondo (rad/s); unità fuori SI sono il giro al minuto (1 ag/min 0,105 rad/s) e il giro al secondo (1 ag/s 6,28 rad/s). velocità di un'onda (v) Rapporto tra la lunghezza d'onda λ ed il periodo T; v = λ / T. Ovvero: prodotto della frequenza f per la lunghezza d onda λ; v = f λ. L'unità SI è il metro al secondo (m/s). La velocità della luce, nel vuoto, è c = 2, m/s; si approssima a km/s. velocità periferica (v) Detta anche velocità tangenziale, rapporto tra la distanza d percorsa da un punto su una circonferenza e il tempo t; v = d / t. L'unità SI è il metro al secondo (m/s). velocità di reazione (v) Variazione della concentrazione di un reagente, o di un prodotto, nel tempo. Nel corso di una reazione la concentrazione dei reagenti diminuisce mentre aumenta quella dei prodotti. La velocità di una reazione, nella sua fase iniziale, quando il volume rimane costante, è misurata dalla diminuzione della concentrazione c di un reagente, o dall'aumento della concentrazione c di un prodotto, in un tempo t; v = c / t. Si esprime di solito in moli al litro al secondo (mol/l s). 4
5 velocità di scorrimento (D) Detta anche caduta di taglio, per un liquido è il rapporto D = v / l tra la velocità v di una lastra, posta a distanza l da una seconda, tra le quali sia posto un liquido. L'unità SI è il secondo reciproco (s -1 ). velocità tangenziale ( velocità periferica). ventilazione Separazione delle varie granulometrie di una miscela eterogenea solida mediante getto d'aria o di altro gas compresso. Venturi, tubo di ( venturimetro). venturicidina Antibiotico, C 41 H 67 NO 11. venturimetro Strumento per la misura della velocità di un fluido scorrente in un condotto. veralcamina Alcaloide, C 27 H 43 NO 2. verapamil Vasodilatatore, C 27 H 38 N 2 O 4. verat- Prefisso, da veratro, pianta medicinale. veratrica, aldeide 2,3-dimetossi-benzaldeide, (CH 3 O) 2 C 6 H 3 CHO. veratrico, acido Acido 2,3-dimetossibenzoico, (CH 3 O) 2 C 6 H 3 COOH. veratrico, alcole Alcole 2,3-dimetossibenzilico, (CH 3 O) 2 C 6 H 3 CH 2 OH. veratridina Alcaloide, C 36 H 51 NO 11. veratrina ( cevadina). veratrolo Antisettico, C 8 H 10 O 2. veratrosina Glucoside, C 33 H 49 NO 7. verazide Antitubercolare, C 15 H 15 N 3 O 3. verbacosio Pentasaccaride, C 30 H 52 O 26. verbenalina Glucoside, C 17 H 24 O 10. verbenone Terpene, C 10 H 14 O. verde alizarina ( ceruleina). verde antico Rame idrossocarbonato, Cu 2 (OH) 2 CO 3, pigmento. verde di Arnaudon Cromo fosfato, pigmento. verde di Bindschedler Indicatore chelometrico, C 16 H 21 N 3. verde di Bolley Rame borato, pigmento. verde di Brema Rame idrossido, pigmento. verde brillante ( verde etile). verde bromocresolo Tetrabromocresolsolfonftaleina, C 21 H 14 Br 4 O 5 S, indicatore del ph. verde clorocresolo Indicatore del ph, C 21 H 14 Cl 4 O 5 S. verde di cobalto ( verde di Rinmann). verde di cromo Giallo di cromo + blu di Berlino (o ftalocianine), pigmento. verde diamante B ( verde malachite). verde diazina Colorante (CI 11050). verde etile Indicatore del ph (CI 42040). verde Guinea Colorante (CI 42085). verde di Guignet Ossido di cromo idrato, pigmento. verde imperiale ( verde di Schweinfurt). 5
6 verde indocianina Diagnostico, C 43 H 47 N 2 NaO 6 S 2. verde Janus ( verde diazina). verde di Kassel Bario manganato, pigmento. verde luce ( verde metile). verde malachite Colorante, indicatore del ph (CI 42000). verde manganese ( verde di Kassel). verde Martius ( verde naftolo). verde metile Colorante (CI 42585). verde metilene Colorante (CI 52020). verde naftolo Colorante (CI 10020). verde di Parigi ( verde di Schweinfurt). verde rame Rame idrossoacetato, CH 3 COOCuOH. verde di Rinmann Cobalto zincato, pigmento. verde di Scheele Rame idrogenoarsenito, CuHAsO 3, pigmento. verde di Schweinfurt Rame acetoarsenito, 3Cu(AsO 2 ) 2 (CH 3 COO) 2 Cu, pigmento. verde smeraldo ( verde etile). verde Vittoria ( verde malachite). verde di zinco Giallo zinco + blu di Prussia, pigmento. verecolene ( fencibutirrolo). vergella Semilavorato metallico a sezione circolare, con diametri compresi tra 6 mm e 20 mm, destinata alla produzione del filo. vergenza (D) Detta anche potere diottrico e potere convergente; per una lente, inverso della distanza focale; D = 1 / d. L'unità SI è il metro reciproco o diottria (m -1 ). verghe Barre, profilati e tubi diritti. verina Alcaloide, C 28 H 45 NO 8. vermiculite Min., silicoalluminato (Al,Fe,Mg) 3 (Al,Si) 4 (OH) 2 O 10 4H 2 O, isolante termico e acustico. vermiglione Min., mercurio solfuro, HgS, pigmento. vermiglione antimonio Antimonio solfuro, Sb 2 S 3, pigmento. vernici Prodotti vernicianti non pigmentati; sono liquidi viscosi, non acquosi, costituiti da agenti filmogeni (es. gomme vegetali, oli siccativi, resine alchidiche), solventi (es. ragia, alcoli, esteri), diluenti, plastificanti, antimuffa, antischiuma e altre sostanze. Verniciatura e Decorazione Rivista dell' ANVIDES. vernina ( guanosina). vernonina Glucoside, C 10 H 24 O 7. veronal ( barbitale). versenico, acido ( EDTA). verticillina Antibiotico, C 30 H 28 N 6 O 6 S 4. 6
7 VES Velocità di eritrosedimentazione, cioè velocità di decantazione degli eritrociti del sangue, espressa misurando l altezza del plasma sovrastante in un tubo graduato, dopo 1 h, 2 h, 24 h. vescicanti Aggressivi chimici che provocano infiammazione, ustioni e distruzione dei tessuti. vesuvianite Min., silicato Ca 10 (Fe,Mg) 2 Al 4( OH) 4 Si 9 O 34. vesuvina ( bruno Bismarck). vestzelyite Min., idrossofosfato (Cu,Zn) 3 (OH) 3 PO 4 2H 2 O. vetivano Terpene, C 15 H 24. vetivene Terpene, C 15 H 22. vetiverile Aggruppamento C 13 H 23. vetiverolo Terpene, C 13 H 23 OH. vetivoni Terpeni, C 15 H 22 O. vetri Materiali duri e fragili, trasparenti, traslucidi o opachi, ottenuti per fusione a temperatura elevata di miscele a prevalenza silicea (UNI 5832). I comuni vetri sono soluzioni solide di due silicati (uno alcalino o uno alcalino-terroso, o di zinco, o di piombo) in silice vetrosa; in alcuni la silice è parzialmente sostituita dall'anidride borica. vetri anti-x Vetri che assorbono i raggi X e le radiazioni nucleari. vetri atermici Vetri che assorbono le radiazioni IR. vetri colati e laminati Vetri piani martellati, armati o retinati, rigati, stampati. vetri diffondenti Vetri costituiti da due lastre unite tra loro, con l'intercapedine riempita con fibre di vetro. vetri elaborati in superficie Vetri piani verniciati, smaltati, metallizzati, sabbiati o smerigliati, incisi, satinati. vetri fototropici Vetri in cui sono incorporati alogenuri di argento; per azione dei raggi UV si liberano argento, che rende il vetro più scuro, e l'alogeno; cessata l'esposizione alla luce i due elementi si ricombinano ed il materiale schiarisce. Si usano per occhiali, finestre e contenitori per sostanze fotosensibili. vetri inattinici Vetri che assorbono le radiazioni UV e violette. vetri isolanti Vetri costituiti da due o più lastre saldate ai bordi; nell' l'intercapedine e stato fatto il vuoto. vetri di sicurezza Vetri armati, stratificati o temprati. vetri stratificati Vetri costituiti da due o più lastre incollate con polivinilacetali. vetri tirati Vetri piani classificati, secondo lo spessore nominale in millimetri: sottile 2, normale 3, forte 4, spesso 5, spesso 6, spesso 8, ultraspesso 10, ultraspesso 12, ultraspesso 15, ultraspesso 19 (UNI 5832). Sono da evitare i termini doppio e semidoppio. vetriolo Antico nome dell'acido solforico. vetriolo azzurro Antico nome del rame solfato. vetriolo bianco Antico nome dello zinco solfato. 7
8 vetriolo verde Antico none del ferro(ii) solfato. vetro solubile Soluzione acquosa concentrata di sodio silicato. vetro tessile Tecnofibra costituita da vetro (legge , n. 883). vetroresina Plastici rinforzati con fibre di vetro. vetroso, stato Stato cristallino in cui il reticolo ionico è deformato. I solidi vetrosi hanno comportamento simile a quello dei liquidi; non avendo un punto di fusione definito, riscaldati diventano gradualmente più fluidi (rammollimento) per cui vengono considerati liquidi ad alta viscosità. vettori Grandezze caratterizzate non soltanto da un numero (modulo del vettore) ma anche da una direzione ed un verso (o senso); es. forza, velocità, accelerazione. VHF Very high frequency. vibrazioni atomiche Oscillazione di due parti di una molecola parallelamente al legame (stretching) o trasversale, nel piano della molecola o fuori di esso (bending o scissoring, rocking, wagging, twisting). Vicat, penetrometro di Strumento per la misurazione del tempo di presa dei leganti, costituito da un ago di massa e dimensioni standard che si fa penetrare nell'impasto in tempi successivi. Vichy, sale di Sodio idrogenocarbonato, NaHCO 3. vicianina Glucoside, C 19 H 25 NO 10. vicianosio Glucoside, C 11 H 20 O 10. vicina Glucoside, C 10 H 16 N 4 O 7. vicinale Termine indicante le posizioni 1, 2, 3 di tre sostituenti sull'anello benzenico. Vickers, durezza ( durezza). vidarabina Antibiotico, C 10 H 13 N 5 O 4. Vijis, reattivo di Soluzione di monocloruro di iodio in acido acetico glaciale, per la determinazione del numero di iodio. Villavecchia-Fabris, reattivo di Soluzione di furfurale in etanolo, per individuare la presenza di olio di sesamo in altri oli. villiaumite Min., sodio fluoruro, NaF. viminolo Analgesico, C 21 H 31 ClN 2 O. Vin Vinile. vinacce Parte solida dell'uva fresca o ammostata, con o senza raspi, o dell'uva fermentata, con o senza raspi (DPR , n. 162). vinavil Emulsione acquosa di polivinile acetato. vinbarbitale sodio Ipnotico, C 11 H 15 N 2 NaO 3. vinblastina Antineoplastico, C 46 H 58 N 4 O 9. vincamina Vasodilatatore, C 21 H 26 N 2 O 3. vincristina Antineoplastico, C 46 H 56 N 4 O 10. 8
9 vinello Prodotto ottenuto per fermentazione delle vinacce vergini di uva fresca macerate con acqua, o dell' esaurimento on acqua delle vinacce fermentate; deve contenere 10 g di litio cloruro al quintale (DM ). vinetina ( ossiacantina). vini aromatizzati Vini a cui sono stati addizionati etanolo, saccarosio, aromi naturali e artificiali, aventi gradazione alcolica non inferiore a 21 ; es. vermut, «americani». vini liquorosi Vini con gradazione alcolica non inferiore a 12, addizionati di mistella, acquavite di vino, alcole o mosto concentrato; es. Marsala, Madera. vinilacetico, acido Acido 3-butenoico, CH 2 =CHCH 2 COOH. vinilacetilene Viniletino, CH CCH=CH 2. vinilacrilico, acido Acido 2,4-pentadienoico, CH 2 CH=CH=CHCOOH. vinilal Tecnofibra formata da macromolecole lineari in cui la catena è costituita da alcole polivinilico a tasso di acetilazione variabile (legge , n. 883). vinilammine ( enammine). vinilazione Addizione di acetilene ad acidi carbossilici e ad alcoli. vinile Aggruppamento CH 2 =CH. vinile alogenuri Alogenoeteni, CH 2 =CHX. vinilico, alcole Etenolo, CH 2 =CHOH. vinilico, etere Anestetico, (CH 2 =CH) 2 O. vinilidene Aggruppamento CH 2 =C=. vinilidene alogenuri 1,1-dialogenoeteni, CH 2 =CX 2. vinilmetilglicole Glicole etilenico vinilmetiletere, CH 2 =CHO(CH 2 ) 2 OCH 3. vinilnortestosterone Steroide, C 20 H 28 O 2. vino Prodotto della fermentazione alcolica totale o parziale dell'uva fresca, dell'uva ammostata (uva fresca pigiata, senza raspi) o del mosto d'uva, con gradazione alcolica non inferiore a 6 e gradazione alcolica complessiva naturale non inferiore a 10 (DPR , n. 162). violanina Colorante (CI 45200). violantrolo Colorante naturale, C 34 H 16 O 2. violantroni Coloranti (CI e 60000). violaquercitrina Glucoside, C 27 H 30 O 16. violarite Min., solfuro FeNi 2 S 4. violaxantina Carotenoide, C 40 H 56 O 4. violetto alcali Colorante (CI 42630). violetto di cobalto Cobalto fosfato, Co 3 (PO 4 ) 2, pigmento. violetto cristalli Colorante (CI 42555), indicatore per titolazioni in solventi non acquosi. violetto etile Colorante (CI 42600). violetto genziana ( violetto cristalli). violetto Hoffmann Colorante (CI 42530). violetto Lauth Colorante (CI 52000), indicatore redox e antidoto dell'ossido di carbonio. violetto di manganese Pirofosfato MnNH 4 P 2 O 7, pigmento. 9
10 violetto metile Indicatore del ph (CI 42535). violetto metile 10 B ( violetto cristalli). violetto pirocatecolo Indicatore chelometrico, C 19 H 14 O 7 S. violetto rodulina Colorante (CI 50215). violetto di stagno Stagno cromato, SnCrO 4, pigmento. viologeni Serie di indicatori tedox derivati del dipiridile. violurico, acido Acido isonitrosobarbiturico, C 4 H 3 N 3 O 4. violutina Glucoside, C 19 H 26 O 12. viomicina Antibiotico, C 25 H 43 N 13 O 10. viprinio embonato Antielmintico, C 75 H 79 N 6 O 6. viraggio Cambiamento di colore di un indicatore che si manifesta al punto finale di una titolazione. virgin naphta ( nafta solvente). virginiamicine Antibiotici, C 43 H 49 N 7 O 10 e C 28 H 35 N 3 O 7. virginio Antico nome dell'astato. viriale, equazione del Il prodotto isotermico pv dei gas reali ha per limite RT quando p tende a zero; pv = RT + Bp + Cp 2 +, dove B è il secondo coefficiente del viriale, dipendente dalla natura del gas e dalla temperatura, C il terzo, ecc. viridicatina Antibiotico, C 15 H 11 NO 2. viridina Antibiotico, C 20 H 16 O 6. virus Agenti patogeni costituiti da macromolecole di nucleoproteine, dimensioni nm, possedenti alcune caratteristiche degli organismi viventi; non hanno attività metabolica propria ma si possono adattare e riprodurre in cellule viventi parassitate. VIS Luce visibile. viscosa Tecnofibra di cellulosa rigenerata, ottenuta mediante il procedimento viscosa, per il filamento continuo e per la fibra discontinua (legge , n. 883). viscosina Antibiotico, C 34 H 95 N 9 O 16. viscosità cinematica (ν ) Rapporto tra la viscosità dinamica η di un liquido e la sua densità d;ν = η / d. L'unità SI è il metro quadrato al secondo (m 2 /s); una unità fuori SI è lo stokes (1 St = 10-4 m 2 /s). viscosità dinamica (η) Coefficiente di proporzionalità, che dipende dalla temperatura e dalla natura del liquido, nell' equazione di Poiseuille p = η 8 Q l / π r 4, dove p è la differenza di pressione tra due sezioni di un tubo sottile in cui scorre un liquido con regime laminare, Q è la portata volumica, l la lunghezza e r il raggio. L'unità SI è il pascal per secondo (Pa s); una unità fuori SI è il poise (1P = 10-1 Pa s). 10
11 Tab.V/1. Viscosità dinamica di alcuni liquidi a 20 C. mpa s mpa s etere etilico 0,23 mercurio 1,5 acetone 0,33 cc. solforico 28 benzene 0,7 olio di oliva 84 etanolo 1,2 glicerolo 1500 viscosità, indice di (I.V.) Percentuale di olio P in una miscela di due oli (P + NM ) che presenta una variazione della viscosità con la temperatura uguale a quella dell'olio in esame. All' olio P (da Pennsylvania) la cui viscosità varia poco con la temperatura, si attribuisce I.V. = 100); all'olio NM (da New Mexico), la cui viscosità diminuisce fortemente con la temperatura, si attribuisce I.V. = 0. viscosità intrinseca ([η]) Rapporto tra la viscosità specifica di una soluzione e la concentrazione della soluzione stessa (valore ottenuto per estrapolazione, a concentrazione zero). viscosità relativa (η r ) Viscosità di un liquido espressa in gradi convenzionali ( Engler, grado; Redwood, grado; Saybolt, grado). viscosità specifica (η sp ) Rapporto η sp = η -η 0 / η 0, dove η è la viscosità di una soluzione e η 0 quella del solvente. visnadina Vasodilatatore, C 21 H 24 O 7. vita media (τ ) Per un radioisotopo, tempo nel quale il numero iniziale di particelle si riduce di 1/e, dove e = 2,718, base dei logaritmi naturali. vitaferina Antineoplastico, C 28 H 38 O 6. vitamina A 1 ( retinolo). vitamina A 2 ( deidroretinolo). vitamina A acetato ( axeroftolo). vitamina B 1 ( tiamina). vitamina B 2 ( riboflavina). vitamina B 3 ( pantotenico, acido). vitamina B 4 Diidrovitamina D 2, C 28 H 46 O. vitamina B 5 ( nicotinico, acido). vitamina B 6 ( piridossina). vitamina B 8 ( adenosinmonofosfato). vitamina B 9 ( folico, acido). vitamina B 12 ( cianocobalammina). vitamina B 12c ( nitritocobalamina ). vitamina B 15 ( pangamico, acido). vitamina B t ( carnitina). vitamina B w ( biotina). 11
12 vitamina C ( ascorbico, acido). vitamina D 2 ( ergocalciferolo). vitamina D 3 ( colecalciferolo) vitamina D 4 Diidrovitamina D 2, C 28 H 46 O. vitamina E ( tocoferolo). vitamina E acetato ( tocoferile acetato). vitamina F Acido linoleico + acido linolenico + acido arachidonico. vitamina G ( vitamina B 2 ). vitamina H ( vitamina B w ). vitamina H 1 Acido 4-amminobenzoico, H 2 NC 6 H 4 COOH. vitamina I ( esperidina). vitamina K 1 ( fillochinone). vitamina K 2 ( farnochinone). vitamina K 3 ( menadione). vitamina K 4 ( menadiolo). vitamina K 5 Amminometilnaftolo, C 11 H 11 NO. vitamina L 1 ( antranilico, acido). vitamina M ( vitamina B 9 ). vitamina P ( benzarone). vitamina P 4 ( citrina). vitamina PP (Preventing pellagra) ( nicotammide). vitamina T ( cabagina). vitamine Sostanze di svariata composizione, catalizzatori di molti processi biologici; si classificano in idrosolubili (es. vitamina B 1, vitamina C) e liposolubili (es. vitamina A 1, vitamina K 1 ). vitelllina Fosfoproteina dell' uovo. vitessina Colorante naturale, C 21 H 14 O 6. vitreous-china ( porcellane). vivianite Min., ferro fosfato, Fe 3 (PO 4 ) 2 8H 2 O. vlasovite Min., silicato Na 2 ZrSi 4 O 11. VLF Very low frequency. VMA Acido vanilmandelico, C 9 H 10 O 5. voacangina Alcaloide, C 22 H 28 N 2 O 3. voacamina Alcaloide, C 43 H 52 N 4 O 5. voacristina Alcaloide, C 22 H 28 N 2 O 4. vobasina Alcaloide, C 21 H 24 N 2 O 3. volborthite Min., rame uranato, Cu 3 (UO 4 ) 2 3H 2 O. Vogel-Ossag, viscosimetro di Strumento per la determinazione della viscosità dinamica dei liquidi. volatili, sostanze 1. Sostanze solide e liquide aventi alta tensione di vapore alla temperatura ambiente. 2. Percentuale di gas e vapori emessi da un carbone durante la distillazione. 12
13 volemitolo Pentaidrossieptandiolo, HOCH 2 (CHOH) 5 CH 2 OH. volpinite Calcio solfato, CaSO 4. volt (V) Unità SI della differenza di potenziale elettrico, differenza di potenziale elettrico esistente tra due sezioni di un conduttore che, percorso dalla corrente elettrica costante di 1 A e senza essere sede di altri fenomeni energetici oltre a quello Joule, dissipa, nel tratto compreso tra le due sezioni considerate la potenza di 1 W; 1 V = W/A = J/C = Ω A = C/F. volt termico (K) Unità fuori SI della differenza di potenziale termico. voltaggio ( forza elettromotrice). Volta-Gay-Lussac, leggi di 1. A pressione costante, il volume di un gas ideale aumenta, per l'aumentare di 1 C, di 1/273 del volume posseduto dal gas a 0 C: V t = V 0 (1 + 1/273 t). 2. A volume costante, la pressione di un gas ideale aumenta, per l'aumentare di 1 C, di 1/273 della pressione del gas a 0 C: p t = p 0 (1 + 1/273 t). voltaite Min., solfato Fe 9 K 2 (SO 4 ) 12 18H 2 O. voltametri ( celle elettrolitiche). voltmetri Strumenti per la misura della differenza di potenziale. voltammetria Metodo di analisi basato sulla misura della variazione del potenziale della soluzione in esame, sottoposta a elettrolisi, in funzione della intensità di corrente. voltzite Min., zinco ossisolfuro, Zn 5 OS 5. volucrisporina Colorante naturale, C 18 H 12 O 4. volume (V) Misura dello spazio occupato da un solido, un liquido o un gas. L'unità SI è il metro cubo (m 3 ); una unità fuori SI è il litro (1 l = 1 dm 3 ). volume di un gas in condizioni normali (V n ) Volume occupato da un gas alla temperatura di 273 K ( C) ed alla pressione di 101,325 kpa (1 atm) (c.n., condizioni normali; s.t.p., standard temperature and pressure). L'unità SI è il metro cubo c.n. (o s.t.p.) (m 3 n). Una unità fuori SI è il litro c.n. (o s.t.p.) (l n ). volume equivalente (V e ) Volume occupato da un equivalente di un gas in condizioni normali. volume massico (V m ) Detto anche volume specifico, inverso della massa volumica; V m = 1 / m V. L'unità SI è il metro cubo al kilogrammo (m 3 /kg). volume molare di un gas (V mol ) Volume occupato da una mole di un gas in condizioni normali. L'unità SI è il metro cubo c.n. alla mole 13
14 (m 3 n/mol).; una unità fuori SI è il litro c.n. alla mole (l n /mol). Per i gas ideali, V mol = 22,413 6 dm 3 n/mol ovvero l n /mol. volume molare critico Volume molare di una sostanza alla temperatura e alla pressione critiche. volume specifico ( volume massico). volumenometri Strumenti per la determinazione della massa volumica di cementi, sabbie, scorie. volumetria ( analisi volumetrica). vomicina Alcaloide, C 22 H 24 N 2 O 4. vonsenite Min., borato (Fe,Mg)FeBO 5. VQPRD Vini di qualità prodotti in regioni determinate. VSi Elastomeri siliconici contenenti gruppi metile e vinile. VSO (Distillato) very superior old. VSOP (Distillato) very superior old pale. VTE Evaporatore a tubi verticali. VTIS Vacuum therm instant sterilization, metodo di sterilizzazione del latte. VVSOP (Distillato) very very superior old pale. vulcanite Min., zolfo contenente selenio. vulcanizzazione Reticolazione delle gomme naturali e sintetiche operata mediante riscaldamento in presenza di zolfo o composti dello zolfo, ossidi metallici, acceleranti. Si eseguono anche vulcanizzazioni senza zolfo: perossidica (es. con dicumile perossido) e poliuretanica (es. con diisocianati). vulnerari Farmaci che aiutano a risanare le ferite. vuoto Termine gergale per indicare un gas a bassa pressione: vuoto (~ 10 Pa), medio vuoto ( Pa), alto vuoto ( Pa), ultra alto vuoto (< 10-6 Pa). vuzina Alcaloide, C 27 H 40 N 2 O 2. 14
GLI STATI DI AGGREGAZIONE DELLA MATERIA. Lo stato gassoso
 GLI STATI DI AGGREGAZIONE DELLA MATERIA Lo stato gassoso Classificazione della materia MATERIA Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (volume e forma propri) LIQUIDO
GLI STATI DI AGGREGAZIONE DELLA MATERIA Lo stato gassoso Classificazione della materia MATERIA Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (volume e forma propri) LIQUIDO
Liquidi, Solidi e Forze Intermolecolari
 Liquidi, Solidi e Forze Intermolecolari Distanze tra molecole Stati Fisici (Fase) Comportamento atipico La maggiore differenza tra liquidi e solidi consiste nella libertà di movimento delle loro molecole
Liquidi, Solidi e Forze Intermolecolari Distanze tra molecole Stati Fisici (Fase) Comportamento atipico La maggiore differenza tra liquidi e solidi consiste nella libertà di movimento delle loro molecole
Trasformazioni materia
 REAZIONI CHIMICHE Trasformazioni materia Trasformazioni fisiche (reversibili) Trasformazioni chimiche (irreversibili) È una trasformazione che non produce nuove sostanze È una trasformazione che produce
REAZIONI CHIMICHE Trasformazioni materia Trasformazioni fisiche (reversibili) Trasformazioni chimiche (irreversibili) È una trasformazione che non produce nuove sostanze È una trasformazione che produce
I GAS GAS IDEALI. PV=nRT. Pressione Volume numero di moli Temperatura Costante dei gas. P V n T R. n, T= cost Legge di Boyle
 I GAS Pressione Volume numero di moli Temperatura Costante dei gas GAS IDEALI P V n T R n = 1 Isoterma: pv = cost Isobara: V/T = cost. Isocora: P/t = cost. n, T= cost Legge di Boyle n, P = cost Legge di
I GAS Pressione Volume numero di moli Temperatura Costante dei gas GAS IDEALI P V n T R n = 1 Isoterma: pv = cost Isobara: V/T = cost. Isocora: P/t = cost. n, T= cost Legge di Boyle n, P = cost Legge di
Una soluzione è un sistema omogeneo (cioè costituito da una sola fase, che può essere liquida, solida o gassosa) a due o più componenti.
 Una soluzione è un sistema omogeneo (cioè costituito da una sola fase, che può essere liquida, solida o gassosa) a due o più componenti. Solvente (componente presente in maggior quantità) SOLUZIONE Soluti
Una soluzione è un sistema omogeneo (cioè costituito da una sola fase, che può essere liquida, solida o gassosa) a due o più componenti. Solvente (componente presente in maggior quantità) SOLUZIONE Soluti
PREPARAZIONE E CARATTERIZZAZIONE DEI VETRI COLORATI
 PREPARAZIONE E CARATTERIZZAZIONE DEI VETRI COLORATI DEFINIZIONE DI VETRO LO STATO VETROSO È QUELLO DI UN SOLIDO BLOCCATO NELLA STRUTTURA DISORDINATA DI UN LIQUIDO (FASE AMORFA) SOLIDO:ORDINE A LUNGO RAGGIO
PREPARAZIONE E CARATTERIZZAZIONE DEI VETRI COLORATI DEFINIZIONE DI VETRO LO STATO VETROSO È QUELLO DI UN SOLIDO BLOCCATO NELLA STRUTTURA DISORDINATA DI UN LIQUIDO (FASE AMORFA) SOLIDO:ORDINE A LUNGO RAGGIO
Equilibri di precipitazione
 Equilibri di precipitazione Molte sostanze solide sono caratterizzate da una scarsa solubilità in acqua (ad es. tutti i carbonati e gli idrossidi degli elementi del II gruppo) AgCl (a differenza di NaCl)
Equilibri di precipitazione Molte sostanze solide sono caratterizzate da una scarsa solubilità in acqua (ad es. tutti i carbonati e gli idrossidi degli elementi del II gruppo) AgCl (a differenza di NaCl)
2014 2015 CCS - Biologia CCS - Fisica I gas e loro proprietà. I liquidi e loro proprietà
 2014 2015 CCS - Biologia CCS - Fisica I gas e loro proprietà 1 I liquidi e loro proprietà 2 Proprietà Generali dei Gas I gas possono essere espansi all infinito. I gas occupano i loro contenitori uniformemente
2014 2015 CCS - Biologia CCS - Fisica I gas e loro proprietà 1 I liquidi e loro proprietà 2 Proprietà Generali dei Gas I gas possono essere espansi all infinito. I gas occupano i loro contenitori uniformemente
LO STATO GASSOSO. Proprietà fisiche dei gas Leggi dei gas Legge dei gas ideali Teoria cinetico-molecolare dei gas Solubilità dei gas nei liquidi
 LO STATO GASSOSO Proprietà fisiche dei gas Leggi dei gas Legge dei gas ideali Teoria cinetico-molecolare dei gas Solubilità dei gas nei liquidi STATO GASSOSO Un sistema gassoso è costituito da molecole
LO STATO GASSOSO Proprietà fisiche dei gas Leggi dei gas Legge dei gas ideali Teoria cinetico-molecolare dei gas Solubilità dei gas nei liquidi STATO GASSOSO Un sistema gassoso è costituito da molecole
Ke = ] = Kw = 10 = 10-7 moli/litro, ed in base a quanto avevamo affermato in precedenza: [H + ] = [OH - ] = 10-7 moli/litro.
![Ke = ] = Kw = 10 = 10-7 moli/litro, ed in base a quanto avevamo affermato in precedenza: [H + ] = [OH - ] = 10-7 moli/litro. Ke = ] = Kw = 10 = 10-7 moli/litro, ed in base a quanto avevamo affermato in precedenza: [H + ] = [OH - ] = 10-7 moli/litro.](/thumbs/27/12374782.jpg) Prodotto ionico dell acqua e ph Prodotto ionico dell acqua L acqua è un elettrolita debolissimo e si dissocia secondo la reazione: H 2 O H + + OH - La costante di equilibrio dell acqua è molto piccola
Prodotto ionico dell acqua e ph Prodotto ionico dell acqua L acqua è un elettrolita debolissimo e si dissocia secondo la reazione: H 2 O H + + OH - La costante di equilibrio dell acqua è molto piccola
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA
 LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
Stati di aggregazione della materia unità 2, modulo A del libro
 Stati di aggregazione della materia unità 2, modulo A del libro Gli stati di aggregazione della materia sono tre: solido, liquido e gassoso, e sono caratterizzati dalle seguenti grandezze: Quantità --->
Stati di aggregazione della materia unità 2, modulo A del libro Gli stati di aggregazione della materia sono tre: solido, liquido e gassoso, e sono caratterizzati dalle seguenti grandezze: Quantità --->
PREPARAZIONE E CARATTERIZZAZIONE DEI VETRI COLORATI
 PREPARAZIONE E CARATTERIZZAZIONE DEI VETRI COLORATI Cos è un vetro? COS È UN VETRO? SOLIDO? LIQUIDO? ALTRO? GLI STATI DELLA MATERIA Volume specifico Liquido Vetro Tg CAMBIAMENTO DI VOLUME Tf Tf =TEMPERATURA
PREPARAZIONE E CARATTERIZZAZIONE DEI VETRI COLORATI Cos è un vetro? COS È UN VETRO? SOLIDO? LIQUIDO? ALTRO? GLI STATI DELLA MATERIA Volume specifico Liquido Vetro Tg CAMBIAMENTO DI VOLUME Tf Tf =TEMPERATURA
L H 2 O nelle cellule vegetali e
 L H 2 O nelle cellule vegetali e il suo trasporto nella pianta H 2 O 0.96 Å H O 105 H 2s 2 2p 4 tendenza all ibridizzazione sp 3 H δ+ O δ- δ+ 1.75 Å H legame idrogeno O δ- H H δ+ δ+ energia del legame
L H 2 O nelle cellule vegetali e il suo trasporto nella pianta H 2 O 0.96 Å H O 105 H 2s 2 2p 4 tendenza all ibridizzazione sp 3 H δ+ O δ- δ+ 1.75 Å H legame idrogeno O δ- H H δ+ δ+ energia del legame
CHIMICA ORGANICA. Gli alcoli
 1 E1-ALCOLI CIMICA OGANICA ALCOLI Formula generale Desinenza -olo Gli alcoli Gli alcoli sono, dopo gli idrocarburi, i composti organici più comuni, che è possibile considerare come derivati dagli alcani
1 E1-ALCOLI CIMICA OGANICA ALCOLI Formula generale Desinenza -olo Gli alcoli Gli alcoli sono, dopo gli idrocarburi, i composti organici più comuni, che è possibile considerare come derivati dagli alcani
Esercizi di Chimica (2 a prova in itinere)
 Esercizi di Chimica (2 a prova in itinere) 3) Calcolare la normalità (N) di una soluzione ottenuta sciogliendo 3,5 g di H 3 PO 4 in 900 ml di acqua [0,119 N] 4) Quanti grammi di soluto sono contenuti in
Esercizi di Chimica (2 a prova in itinere) 3) Calcolare la normalità (N) di una soluzione ottenuta sciogliendo 3,5 g di H 3 PO 4 in 900 ml di acqua [0,119 N] 4) Quanti grammi di soluto sono contenuti in
GEOLOGIA (studio della litosfera) Essa si divide in MINERALOGIA (studio dei minerali) e PETROGRAFIA ( studio delle rocce)
 GEOLOGIA (studio della litosfera) Essa si divide in MINERALOGIA (studio dei minerali) e PETROGRAFIA ( studio delle rocce) I MINERALI I minerali sono sostanze solide omogenee, inorganiche, esprimibili mediante
GEOLOGIA (studio della litosfera) Essa si divide in MINERALOGIA (studio dei minerali) e PETROGRAFIA ( studio delle rocce) I MINERALI I minerali sono sostanze solide omogenee, inorganiche, esprimibili mediante
LA CORRENTE ELETTRICA
 L CORRENTE ELETTRIC H P h Prima che si raggiunga l equilibrio c è un intervallo di tempo dove il livello del fluido non è uguale. Il verso del movimento del fluido va dal vaso a livello maggiore () verso
L CORRENTE ELETTRIC H P h Prima che si raggiunga l equilibrio c è un intervallo di tempo dove il livello del fluido non è uguale. Il verso del movimento del fluido va dal vaso a livello maggiore () verso
PROVA STRUTTURATA DI CHIMICA ORGANICA
 1. Una delle seguenti definizioni di gruppo funzionale è errata. Quale? "In chimica organica, i gruppi funzionali sono gruppi di atomi presenti in ogni molecola A. dai quali dipendono le caratteristiche
1. Una delle seguenti definizioni di gruppo funzionale è errata. Quale? "In chimica organica, i gruppi funzionali sono gruppi di atomi presenti in ogni molecola A. dai quali dipendono le caratteristiche
DETERMINAZIONE DEL PUNTO DI FINE TITOLAZIONE MEDIANTE METODI CHIMICO-FISICI
 DETERMINAZIONE DEL PUNTO DI FINE TITOLAZIONE MEDIANTE METODI CHIMICO-FISICI - si sfrutta una proprietà chimico-fisica o fisica che varia nel corso della titolazione - tale proprietà è in genere proporzionale
DETERMINAZIONE DEL PUNTO DI FINE TITOLAZIONE MEDIANTE METODI CHIMICO-FISICI - si sfrutta una proprietà chimico-fisica o fisica che varia nel corso della titolazione - tale proprietà è in genere proporzionale
Gas e gas perfetti. Marina Cobal - Dipt.di Fisica - Universita' di Udine 1
 Gas e gas perfetti 1 Densita Densita - massa per unita di volume Si misura in g/cm 3 ρ = M V Bassa densita Alta densita Definizione di Pressione Pressione = Forza / Area P = F/A unita SI : 1 Nt/m 2 = 1
Gas e gas perfetti 1 Densita Densita - massa per unita di volume Si misura in g/cm 3 ρ = M V Bassa densita Alta densita Definizione di Pressione Pressione = Forza / Area P = F/A unita SI : 1 Nt/m 2 = 1
LEZIONE 1. Materia: Proprietà e Misura
 LEZIONE 1 Materia: Proprietà e Misura MISCELE, COMPOSTI, ELEMENTI SOSTANZE PURE E MISCUGLI La materia può essere suddivisa in sostanze pure e miscugli. Un sistema è puro solo se è formato da una singola
LEZIONE 1 Materia: Proprietà e Misura MISCELE, COMPOSTI, ELEMENTI SOSTANZE PURE E MISCUGLI La materia può essere suddivisa in sostanze pure e miscugli. Un sistema è puro solo se è formato da una singola
DENSITA La densità è una grandezza fisica che indica la massa, di una sostanza o di un corpo, contenuta nell unità di volume; è data dal rapporto:
 Richiami di Chimica DENSITA La densità è una grandezza fisica che indica la massa, di una sostanza o di un corpo, contenuta nell unità di volume; è data dal rapporto: d = massa / volume unità di misura
Richiami di Chimica DENSITA La densità è una grandezza fisica che indica la massa, di una sostanza o di un corpo, contenuta nell unità di volume; è data dal rapporto: d = massa / volume unità di misura
TEORIA CINETICA DEI GAS
 TEORIA CINETICA DEI GAS La teoria cinetica dei gas è corrispondente con, e infatti prevede, le proprietà dei gas. Nella materia gassosa, gli atomi o le molecole sono separati da grandi distanze e sono
TEORIA CINETICA DEI GAS La teoria cinetica dei gas è corrispondente con, e infatti prevede, le proprietà dei gas. Nella materia gassosa, gli atomi o le molecole sono separati da grandi distanze e sono
L E L E G G I D E I G A S P A R T E I
 L E L E G G I D E I G A S P A R T E I Variabili di stato Equazioni di stato Legge di Boyle Pressione, temperatura, scale termometriche Leggi di Charles/Gay-Lussac Dispense di Chimica Fisica per Biotecnologie
L E L E G G I D E I G A S P A R T E I Variabili di stato Equazioni di stato Legge di Boyle Pressione, temperatura, scale termometriche Leggi di Charles/Gay-Lussac Dispense di Chimica Fisica per Biotecnologie
GIOCHI DELLA CHIMICA
 GIOCHI DELLA CHIMICA FASE D ISTITUTO (TRIENNIO) 21 marzo 2016 La prova è costituita da 50 quesiti. ALUNNO CLASSE Scrivi la risposta a ciascuna domanda nel foglio risposte allegato. 1. Quale dei seguenti
GIOCHI DELLA CHIMICA FASE D ISTITUTO (TRIENNIO) 21 marzo 2016 La prova è costituita da 50 quesiti. ALUNNO CLASSE Scrivi la risposta a ciascuna domanda nel foglio risposte allegato. 1. Quale dei seguenti
= 9,3 10-5 M = 1,05 10-5 M
 - Calcolare la solubilità molare di CaCO 3 ( = 8,7 10-9 ). La reazione di solubilizzazione di CaCO 3 (carbonato di calcio) è: CaCO 3 (s) Ca 2+ + CO 3 L espressione della sarà quindi: = [Ca 2+ ] [CO 3 ]
- Calcolare la solubilità molare di CaCO 3 ( = 8,7 10-9 ). La reazione di solubilizzazione di CaCO 3 (carbonato di calcio) è: CaCO 3 (s) Ca 2+ + CO 3 L espressione della sarà quindi: = [Ca 2+ ] [CO 3 ]
1. Un elemento Ä formato da particelle indivisibili chiamate atomi. 2. Gli atomi di uno specifico elemento hanno proprietå identiche. 3.
 Atomi e molecole Ipotesi di Dalton (primi dell 800) 1. Un elemento Ä formato da particelle indivisibili chiamate atomi. 2. Gli atomi di uno specifico elemento hanno proprietå identiche. 3. Gli atomi dei
Atomi e molecole Ipotesi di Dalton (primi dell 800) 1. Un elemento Ä formato da particelle indivisibili chiamate atomi. 2. Gli atomi di uno specifico elemento hanno proprietå identiche. 3. Gli atomi dei
MODULO 3 - LA MATERIA: COMPOSIZIONE E TRASFORMAZIONI
 MODULO 3 - LA MATERIA: COMPOSIZIONE E TRASFORMAZIONI La materia è tutto ciò che ha una massa, energia e occupa spazio, cioè ha un volume; essa si classifica in base alla sua composizione chimica ed in
MODULO 3 - LA MATERIA: COMPOSIZIONE E TRASFORMAZIONI La materia è tutto ciò che ha una massa, energia e occupa spazio, cioè ha un volume; essa si classifica in base alla sua composizione chimica ed in
Classificazione della materia: Sostanze pure e miscugli
 Classificazione della materia: Sostanze pure e miscugli la composizione e quindi le proprietà intensive sono le stesse in ogni parte del sistema La composizione e le proprietà intensive variano da una
Classificazione della materia: Sostanze pure e miscugli la composizione e quindi le proprietà intensive sono le stesse in ogni parte del sistema La composizione e le proprietà intensive variano da una
I TEST DI CHIMICA - INGEGNERIA DELL INFORMAZIONE AA 04/05
 I TEST DI CHIMICA - INGEGNERIA DELL INFORMAZIONE AA 04/05 COGNOME E NOME: 1. Br 1 si è trasformato in Br +3 in una reazione in cui lo ione bromuro: A) ha acquistato 3 elettroni B) ha ceduto 4 elettroni
I TEST DI CHIMICA - INGEGNERIA DELL INFORMAZIONE AA 04/05 COGNOME E NOME: 1. Br 1 si è trasformato in Br +3 in una reazione in cui lo ione bromuro: A) ha acquistato 3 elettroni B) ha ceduto 4 elettroni
SCALA DEI PESI ATOMICI RELATIVI E MEDI
 SCALA DEI PESI ATOMICI RELATIVI E MEDI La massa dei singoli atomi ha un ordine di grandezza compreso tra 10-22 e 10-24 g. Per evitare di utilizzare numeri così piccoli, essa è espressa relativamente a
SCALA DEI PESI ATOMICI RELATIVI E MEDI La massa dei singoli atomi ha un ordine di grandezza compreso tra 10-22 e 10-24 g. Per evitare di utilizzare numeri così piccoli, essa è espressa relativamente a
STATO LIQUIDO. Si definisce tensione superficiale (γ) il lavoro che bisogna fare per aumentare di 1 cm 2 la superficie del liquido.
 STTO LIQUIDO Una sostanza liquida è formata da particelle in continuo movimento casuale, come in un gas, tuttavia le particelle restano a contatto le une alle altre e risentono sempre delle notevoli forze
STTO LIQUIDO Una sostanza liquida è formata da particelle in continuo movimento casuale, come in un gas, tuttavia le particelle restano a contatto le une alle altre e risentono sempre delle notevoli forze
Scritto Chimica generale 13.02.2012 Gruppo A
 Scritto Chimica generale 13.02.2012 Gruppo A 1. Calcolare il ph di una soluzione ottenuta mescolando 12.0 ml di una soluzione 1.00 M di nitrato di calcio, 150 ml di una soluzione 1.00 M di acido cloridrico,
Scritto Chimica generale 13.02.2012 Gruppo A 1. Calcolare il ph di una soluzione ottenuta mescolando 12.0 ml di una soluzione 1.00 M di nitrato di calcio, 150 ml di una soluzione 1.00 M di acido cloridrico,
Acidi e basi. HCl H + + Cl - (acido cloridrico) NaOH Na + + OH - (idrossido di sodio; soda caustica)
 Acidi e basi Per capire che cosa sono un acido e una base dal punto di vista chimico, bisogna riferirsi ad alcune proprietà chimiche dell'acqua. L'acqua, sia solida (ghiaccio), liquida o gassosa (vapore
Acidi e basi Per capire che cosa sono un acido e una base dal punto di vista chimico, bisogna riferirsi ad alcune proprietà chimiche dell'acqua. L'acqua, sia solida (ghiaccio), liquida o gassosa (vapore
LA CORRENTE ELETTRICA Prof. Erasmo Modica erasmo@galois.it
 LA CORRENTE ELETTRICA Prof. Erasmo Modica erasmo@galois.it L INTENSITÀ DELLA CORRENTE ELETTRICA Consideriamo una lampadina inserita in un circuito elettrico costituito da fili metallici ed un interruttore.
LA CORRENTE ELETTRICA Prof. Erasmo Modica erasmo@galois.it L INTENSITÀ DELLA CORRENTE ELETTRICA Consideriamo una lampadina inserita in un circuito elettrico costituito da fili metallici ed un interruttore.
modulo: CHIMICA DEI POLIMERI
 CORSO PON Esperto nella progettazione, caratterizzazione e lavorazione di termoplastici modulo: CHIMICA DEI POLIMERI Vincenzo Venditto influenza delle caratteristiche strutturali, microstrutturali e morfologiche
CORSO PON Esperto nella progettazione, caratterizzazione e lavorazione di termoplastici modulo: CHIMICA DEI POLIMERI Vincenzo Venditto influenza delle caratteristiche strutturali, microstrutturali e morfologiche
13 La temperatura - 8. Il gas perfetto
 La mole e l equazione del gas perfetto Tutto ciò che vediamo intorno a noi è composto di piccolissimi grani, che chiamiamo «molecole». Per esempio, il ghiaccio, l acqua liquida e il vapore acqueo sono
La mole e l equazione del gas perfetto Tutto ciò che vediamo intorno a noi è composto di piccolissimi grani, che chiamiamo «molecole». Per esempio, il ghiaccio, l acqua liquida e il vapore acqueo sono
Capitolo 7. Le soluzioni
 Capitolo 7 Le soluzioni Come visto prima, mescolando tra loro sostanze pure esse danno origine a miscele di sostanze o semplicemente miscele. Una miscela può essere omogenea ( detta anche soluzione) o
Capitolo 7 Le soluzioni Come visto prima, mescolando tra loro sostanze pure esse danno origine a miscele di sostanze o semplicemente miscele. Una miscela può essere omogenea ( detta anche soluzione) o
Tipi di reazioni. Reazioni chimiche. Di dissociazione. Di sintesi. Di semplice scambio. Di doppio scambio. Reazioni complesse
 Tipi di reazioni Le reazioni chimiche vengono tradizionalmente classificate a seconda del tipo di trasformazione subita dai reagenti: Reazioni chimiche possono essere Di dissociazione Una sostanza subisce
Tipi di reazioni Le reazioni chimiche vengono tradizionalmente classificate a seconda del tipo di trasformazione subita dai reagenti: Reazioni chimiche possono essere Di dissociazione Una sostanza subisce
Degrado dei materiali non-metallici 1 materiali polimerici. Contenuto
 Contenuto o legame chimico C C - legame covalente, energia di legame - struttura tetragonale dei quattro legami del carbonio reazioni di polimerizzazione - poliaddizione, esempi - policondensazione, esempi
Contenuto o legame chimico C C - legame covalente, energia di legame - struttura tetragonale dei quattro legami del carbonio reazioni di polimerizzazione - poliaddizione, esempi - policondensazione, esempi
... corso di chimica elettrochimica 1
 ... corso di chimica elettrochimica 1 CONTENUTI reazioni elettrochimiche pile e celle elettrolitiche potenziale d elettrodo e forza elettromotrice equazione di Nernst elettrolisi leggi di Faraday batterie
... corso di chimica elettrochimica 1 CONTENUTI reazioni elettrochimiche pile e celle elettrolitiche potenziale d elettrodo e forza elettromotrice equazione di Nernst elettrolisi leggi di Faraday batterie
Corso di Laurea in Chimica e Tecnologia Farmaceutiche Esame di Chimica Analitica e Complementi di Chimica Modulo di Chimica Analitica 8 Novembre 2012
 Modulo di Chimica Analitica 8 Novembre 2012 1. Una soluzione viene preparata sciogliendo1210 mg di K 3 Fe(CN) 6 in 775 ml di acqua. Calcolare: a) la concentrazione analitica di K 3 Fe(CN) 6 b) la concentrazione
Modulo di Chimica Analitica 8 Novembre 2012 1. Una soluzione viene preparata sciogliendo1210 mg di K 3 Fe(CN) 6 in 775 ml di acqua. Calcolare: a) la concentrazione analitica di K 3 Fe(CN) 6 b) la concentrazione
Chimica. Ingegneria Meccanica, Elettrica e Civile Simulazione d'esame
 Viene qui riportata la prova scritta di simulazione dell'esame di Chimica (per meccanici, elettrici e civili) proposta agli studenti alla fine di ogni tutoraggio di Chimica. Si allega inoltre un estratto
Viene qui riportata la prova scritta di simulazione dell'esame di Chimica (per meccanici, elettrici e civili) proposta agli studenti alla fine di ogni tutoraggio di Chimica. Si allega inoltre un estratto
FILTRO A TESSUTO. Allegato n. Azienda. Punto di emissione n. Temperatura emissione (K) Altezza geometrica di emissione (m)
 REGIONE EMILIA-ROMAGNA Allegato n. Azienda ASSESSORATO AMBIENTE E DIFESA DEL SUOLO FILTRO A TESSUTO Punto di emissione n. Temperatura emissione (K) Altezza geometrica di emissione (m) Portata massima di
REGIONE EMILIA-ROMAGNA Allegato n. Azienda ASSESSORATO AMBIENTE E DIFESA DEL SUOLO FILTRO A TESSUTO Punto di emissione n. Temperatura emissione (K) Altezza geometrica di emissione (m) Portata massima di
MATERIA: tutto ciò che ha una MASSA, occupa un VOLUME e ha ENERGIA
 La materia La materia MATERIA: tutto ciò che ha una MASSA, occupa un VOLUME e ha ENERGIA Il mondo che ci circonda è costituito da materia. La chimica studia le proprietà della materia e i suoi cambiamenti.
La materia La materia MATERIA: tutto ciò che ha una MASSA, occupa un VOLUME e ha ENERGIA Il mondo che ci circonda è costituito da materia. La chimica studia le proprietà della materia e i suoi cambiamenti.
Esame di Chimica Generale (M-Z) A.A. 2011-2012 (25 gennaio 2012)
 CORSO DI LAUREA IN SCIENZE BIOLOGICHE Esame di Chimica Generale (M-Z) A.A. 2011-2012 (25 gennaio 2012) 1) Bilanciare la seguente ossidoriduzione: KMnO 4 + H 2 O 2 + H 2 SO 4 MnSO 4 + K 2 SO 4 + O 2 + H
CORSO DI LAUREA IN SCIENZE BIOLOGICHE Esame di Chimica Generale (M-Z) A.A. 2011-2012 (25 gennaio 2012) 1) Bilanciare la seguente ossidoriduzione: KMnO 4 + H 2 O 2 + H 2 SO 4 MnSO 4 + K 2 SO 4 + O 2 + H
Unità di misura. Perché servono le unità di misura nella pratica di laboratorio e in corsia? Le unità di misura sono molto importanti
 Unità di misura Le unità di misura sono molto importanti 1000 è solo un numero 1000 lire unità di misura monetaria 1000 unità di misura monetaria ma il valore di acquisto è molto diverso 1000/mese unità
Unità di misura Le unità di misura sono molto importanti 1000 è solo un numero 1000 lire unità di misura monetaria 1000 unità di misura monetaria ma il valore di acquisto è molto diverso 1000/mese unità
INDIRIZZO TECNOLOGICO CLASSE A033 n. 2
 INDIRIZZO TECNOLOGICO CLASSE A033 n. 2 1) La tensione di rete domestica è in Italia di 230 V. In una stanza è accesa una lampada di 100W, in un altra stanza una lampada di 200W. L intensità di corrente
INDIRIZZO TECNOLOGICO CLASSE A033 n. 2 1) La tensione di rete domestica è in Italia di 230 V. In una stanza è accesa una lampada di 100W, in un altra stanza una lampada di 200W. L intensità di corrente
LABORATORIO DI CHIMICA GENERALE E INORGANICA
 UNIVERSITA DEGLI STUDI DI MILANO Facoltà di Scienze Matematiche, Fisiche e Naturali Corso di Laurea Triennale in Chimica CORSO DI: LABORATORIO DI CHIMICA GENERALE E INORGANICA Docente: Dr. Alessandro Caselli
UNIVERSITA DEGLI STUDI DI MILANO Facoltà di Scienze Matematiche, Fisiche e Naturali Corso di Laurea Triennale in Chimica CORSO DI: LABORATORIO DI CHIMICA GENERALE E INORGANICA Docente: Dr. Alessandro Caselli
Applicazioni della Termochimica: Combustioni
 CHIMICA APPLICATA Applicazioni della Termochimica: Combustioni Combustioni Il comburente più comune è l ossigeno dell aria Aria secca:! 78% N 2 21% O 2 1% gas rari Combustioni Parametri importanti:! 1.Potere
CHIMICA APPLICATA Applicazioni della Termochimica: Combustioni Combustioni Il comburente più comune è l ossigeno dell aria Aria secca:! 78% N 2 21% O 2 1% gas rari Combustioni Parametri importanti:! 1.Potere
MATERIALI. Introduzione
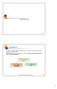 MATERIALI 398 Introduzione Gli acciai sono leghe metalliche costituite da ferro e carbonio, con tenore di carbonio (in massa) non superiore al 2%. Attenzione: la normazione sugli acciai è in fase di armonizzazione
MATERIALI 398 Introduzione Gli acciai sono leghe metalliche costituite da ferro e carbonio, con tenore di carbonio (in massa) non superiore al 2%. Attenzione: la normazione sugli acciai è in fase di armonizzazione
È importante quindi conoscere le proprietà chimiche dell acqua. Le reazioni acido base sono particolari esempi di equilibrio chimico in fase acquosa
 Premessa Le nozioni di acido e di base non sono concetti assoluti ma sono relativi al mezzo in cui tale sostanze sono sciolte. L acqua è il solvente per eccellenza, scelto per studiare le caratteristiche
Premessa Le nozioni di acido e di base non sono concetti assoluti ma sono relativi al mezzo in cui tale sostanze sono sciolte. L acqua è il solvente per eccellenza, scelto per studiare le caratteristiche
Analisi di Controllo di un Acqua Minerale Naturale
 Analisi di Controllo di un Acqua Minerale aturale ITODUZIOE Le acque potabili possono essere in diverse tipologie: si definiscono acque destinate al consumo umano, quelle acque rese potabili dopo aver
Analisi di Controllo di un Acqua Minerale aturale ITODUZIOE Le acque potabili possono essere in diverse tipologie: si definiscono acque destinate al consumo umano, quelle acque rese potabili dopo aver
FILTRO A TESSUTO. Punto di emissione n. Temperatura emissione (K) Altezza geometrica di emissione (m)
 FILTRO A TESSUTO Punto di emissione n. Temperatura emissione (K) Altezza geometrica di emissione (m) Portata massima di progetto (mc/s) Sezione del camino (mq) Percentuale di materiale particolato con
FILTRO A TESSUTO Punto di emissione n. Temperatura emissione (K) Altezza geometrica di emissione (m) Portata massima di progetto (mc/s) Sezione del camino (mq) Percentuale di materiale particolato con
Unità di misura e formule utili
 Unità di misura e formule utili Lezione 7 Unità di misura Il Sistema Internazionale di unità di misura (SI) nasce dall'esigenza di utilizzare comuni unità di misura per la quantificazione e la misura delle
Unità di misura e formule utili Lezione 7 Unità di misura Il Sistema Internazionale di unità di misura (SI) nasce dall'esigenza di utilizzare comuni unità di misura per la quantificazione e la misura delle
BIOLOGIA GENERALE. Alessandro Massolo Dip. Biologia Animale e Genetica c/o Prof. F. Dessì-Fulgheri (Via Romana 17) massolo@unifi.
 Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE Facoltà di Scienze della Formazione Scienze della Formazione Primaria Alessandro Massolo Dip. Biologia Animale
Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE Facoltà di Scienze della Formazione Scienze della Formazione Primaria Alessandro Massolo Dip. Biologia Animale
IL SISTEMA INTERNAZIONALE DI MISURA
 IL SISTEMA INTERNAZIONALE DI MISURA UNITÀ SI Il sistema di misura standard, adottato su scala mondiale, è conosciuto come Système International d Unités. Le unità fondamentali da cui derivano tutte le
IL SISTEMA INTERNAZIONALE DI MISURA UNITÀ SI Il sistema di misura standard, adottato su scala mondiale, è conosciuto come Système International d Unités. Le unità fondamentali da cui derivano tutte le
Genova 15 01 14 TIPOLOGIE DI LAMPADE
 Genova 15 01 14 TIPOLOGIE DI LAMPADE Le lampade a vapori di mercurio sono sicuramente le sorgenti di radiazione UV più utilizzate nella disinfezione delle acque destinate al consumo umano in quanto offrono
Genova 15 01 14 TIPOLOGIE DI LAMPADE Le lampade a vapori di mercurio sono sicuramente le sorgenti di radiazione UV più utilizzate nella disinfezione delle acque destinate al consumo umano in quanto offrono
SENSORI E TRASDUTTORI
 SENSORI E TRASDUTTORI Il controllo di processo moderno utilizza tecnologie sempre più sofisticate, per minimizzare i costi e contenere le dimensioni dei dispositivi utilizzati. Qualsiasi controllo di processo
SENSORI E TRASDUTTORI Il controllo di processo moderno utilizza tecnologie sempre più sofisticate, per minimizzare i costi e contenere le dimensioni dei dispositivi utilizzati. Qualsiasi controllo di processo
Università degli studi di MILANO Facoltà di AGRARIA. El. di Chimica e Chimica Fisica Mod. 2 CHIMICA FISICA. Lezione 2 LO STATO GASSOSO
 Università degli studi di MILANO Facoltà di AGRARIA El. di Chimica e Chimica Fisica Mod. 2 CHIMICA FISICA Lezione 2 Anno Accademico 2010-2011 Docente: Dimitrios Fessas LO STATO GASSOSO Prof. Dimitrios
Università degli studi di MILANO Facoltà di AGRARIA El. di Chimica e Chimica Fisica Mod. 2 CHIMICA FISICA Lezione 2 Anno Accademico 2010-2011 Docente: Dimitrios Fessas LO STATO GASSOSO Prof. Dimitrios
03 - Unità di misura, tabelle di conversione
 0 0 - Unità di misura, tabelle di conversione - Tabella unità di misura sistema internazionale - Tabelle di conversione - Tabelle pesi specifici e temp. di fusione - Tabelle filettature - Tabelle pesi
0 0 - Unità di misura, tabelle di conversione - Tabella unità di misura sistema internazionale - Tabelle di conversione - Tabelle pesi specifici e temp. di fusione - Tabelle filettature - Tabelle pesi
METALLI FERROSI GHISA ACCIAIO
 METALLI FERROSI I metalli ferrosi sono i metalli e le leghe metalliche che contengono ferro. Le leghe ferrose più importanti sono l acciaio e la ghisa. ACCIAIO: lega metallica costituita da ferro e carbonio,
METALLI FERROSI I metalli ferrosi sono i metalli e le leghe metalliche che contengono ferro. Le leghe ferrose più importanti sono l acciaio e la ghisa. ACCIAIO: lega metallica costituita da ferro e carbonio,
Ripasso sulla temperatura, i gas perfetti e il calore
 Ripasso sulla temperatura, i gas perfetti e il calore Prof. Daniele Ippolito Liceo Scientifico Amedeo di Savoia di Pistoia La temperatura Fenomeni non interpretabili con le leggi della meccanica Dilatazione
Ripasso sulla temperatura, i gas perfetti e il calore Prof. Daniele Ippolito Liceo Scientifico Amedeo di Savoia di Pistoia La temperatura Fenomeni non interpretabili con le leggi della meccanica Dilatazione
TAVOLA DI PROGRAMMAZIONE PER GRUPPI DIDATTICI
 TAVOLA DI PROGRAMMAZIONE PER GRUPPI DIDATTICI MATERIA: CHIMICA CLASSI: PRIME I II QUADRIMESTRE Competenze Abilità/Capacità Conoscenze* Attività didattica Strumenti Tipologia verifiche Osservare, descrivere
TAVOLA DI PROGRAMMAZIONE PER GRUPPI DIDATTICI MATERIA: CHIMICA CLASSI: PRIME I II QUADRIMESTRE Competenze Abilità/Capacità Conoscenze* Attività didattica Strumenti Tipologia verifiche Osservare, descrivere
La percentuale massa/volume (%m/v) indica la quantità di soluto espressa in grammi presente in 100 ml di soluzione.
 La concentrazione delle soluzioni Le soluzioni sono costituite da quantità molto variabili dei loro componenti: se vogliamo fornire una indicazione precisa circa la loro composizione, è importante conoscere
La concentrazione delle soluzioni Le soluzioni sono costituite da quantità molto variabili dei loro componenti: se vogliamo fornire una indicazione precisa circa la loro composizione, è importante conoscere
Dissociazione elettrolitica
 Dissociazione elettrolitica Le sostanze ioniche si solubilizzano liberando ioni in soluzione. La dissociazione elettrolitica è il processo con cui un solvente separa ioni di carica opposta e si lega ad
Dissociazione elettrolitica Le sostanze ioniche si solubilizzano liberando ioni in soluzione. La dissociazione elettrolitica è il processo con cui un solvente separa ioni di carica opposta e si lega ad
COMPITO DI CHIMICA DEL 19-04-2013
 COMPITO DI CHIMICA DEL 19-04-2013 1) Una certa quantità di solfato di ferro (II), sciolta in una soluzione acquosa di acido solforico, viene trattata con 1.0 10-3 mol di permanganato di potassio. Si ottengono
COMPITO DI CHIMICA DEL 19-04-2013 1) Una certa quantità di solfato di ferro (II), sciolta in una soluzione acquosa di acido solforico, viene trattata con 1.0 10-3 mol di permanganato di potassio. Si ottengono
L ALIMENTAZIONE ANTINFIAMMATORIA PER IL PODISTA. Dott.ssa Elisa Seghetti Biologa Nutrizionista - Neurobiologa
 L ALIMENTAZIONE ANTINFIAMMATORIA PER IL PODISTA Dott.ssa Elisa Seghetti Biologa Nutrizionista - Neurobiologa L atleta moderno ha bisogno di un maggior numero di adattamenti metabolici all esercizio fisico.
L ALIMENTAZIONE ANTINFIAMMATORIA PER IL PODISTA Dott.ssa Elisa Seghetti Biologa Nutrizionista - Neurobiologa L atleta moderno ha bisogno di un maggior numero di adattamenti metabolici all esercizio fisico.
Si classifica come una grandezza intensiva
 CAP 13: MISURE DI TEMPERATURA La temperatura È osservata attraverso gli effetti che provoca nelle sostanze e negli oggetti Si classifica come una grandezza intensiva Può essere considerata una stima del
CAP 13: MISURE DI TEMPERATURA La temperatura È osservata attraverso gli effetti che provoca nelle sostanze e negli oggetti Si classifica come una grandezza intensiva Può essere considerata una stima del
LA TERRA E LA CHIMICA: LA TAVOLA PERIODICA DEGLI ELEMENTI ELEMENTI E COMPOSTI
 I.I.S. A. PACINOTTI IST. TECNICO STATALE INDUSTRIALE Antonio PACINOTTI IST. TECNICO STATALE per GEOMETRI "Giorgio MASSARI" http://www.iispacinottive.it/ Via Caneve, n. 93 30173 - Mestre (VE) tel. 041 5350355
I.I.S. A. PACINOTTI IST. TECNICO STATALE INDUSTRIALE Antonio PACINOTTI IST. TECNICO STATALE per GEOMETRI "Giorgio MASSARI" http://www.iispacinottive.it/ Via Caneve, n. 93 30173 - Mestre (VE) tel. 041 5350355
Indice. 1 La materia e la sua struttura. 2 La radioattività ed i processi nucleari
 Indice PREFAZIONE XIII 1 La materia e la sua struttura 1.1. Le particelle fondamentali e la struttura dell atomo 2 1.2. Il numero atomico, il numero di massa, i nuclidi e gli isotopi 5 1.3. L unità di
Indice PREFAZIONE XIII 1 La materia e la sua struttura 1.1. Le particelle fondamentali e la struttura dell atomo 2 1.2. Il numero atomico, il numero di massa, i nuclidi e gli isotopi 5 1.3. L unità di
Correnti e circuiti a corrente continua. La corrente elettrica
 Correnti e circuiti a corrente continua La corrente elettrica Corrente elettrica: carica che fluisce attraverso la sezione di un conduttore in una unità di tempo Q t Q lim t 0 t ntensità di corrente media
Correnti e circuiti a corrente continua La corrente elettrica Corrente elettrica: carica che fluisce attraverso la sezione di un conduttore in una unità di tempo Q t Q lim t 0 t ntensità di corrente media
BILANCI DI ENERGIA. Capitolo 2 pag 70
 BILANCI DI ENERGIA Capitolo 2 pag 70 BILANCI DI ENERGIA Le energie in gioco sono di vario tipo: energia associata ai flussi entranti e uscenti (potenziale, cinetica, interna), Calore scambiato con l ambiente,
BILANCI DI ENERGIA Capitolo 2 pag 70 BILANCI DI ENERGIA Le energie in gioco sono di vario tipo: energia associata ai flussi entranti e uscenti (potenziale, cinetica, interna), Calore scambiato con l ambiente,
Corso di Laurea in TECNICHE DI RADIOLOGIA MEDICA, PER IMMAGINI E RADIOTERAPIA
 Corso di Laurea in TECNICHE DI RADIOLOGIA MEDICA, PER IMMAGINI E RADIOTERAPIA Anno: 1 Semestre: 1 Corso integrato: MATEMATICA, FISICA, STATISTICA ED INFORMATICA Disciplina: FISICA MEDICA Docente: Prof.
Corso di Laurea in TECNICHE DI RADIOLOGIA MEDICA, PER IMMAGINI E RADIOTERAPIA Anno: 1 Semestre: 1 Corso integrato: MATEMATICA, FISICA, STATISTICA ED INFORMATICA Disciplina: FISICA MEDICA Docente: Prof.
Acqua azzurra, acqua chiara. Istituto Comprensivo della Galilla Scuola Media Dessì - Ballao
 Acqua azzurra, acqua chiara Istituto Comprensivo della Galilla Scuola Media Dessì - Ballao Proprietà fisiche Ecosistemi acquatici Origine della vita Ciclo dell acqua Acqua Scoperte Sensazioni Leggi La
Acqua azzurra, acqua chiara Istituto Comprensivo della Galilla Scuola Media Dessì - Ballao Proprietà fisiche Ecosistemi acquatici Origine della vita Ciclo dell acqua Acqua Scoperte Sensazioni Leggi La
I L I P I D I. Lipidi complessi: fosfolipidi e glicolipidi; sono formati da CHO e altre sostanze.
 I L I P I D I ASPETTI GENERALI I Lipidi o grassi sono la riserva energetica del nostro organismo; nel corpo umano costituiscono mediamente il 17% del peso corporeo dove formano il tessuto adiposo. In generale
I L I P I D I ASPETTI GENERALI I Lipidi o grassi sono la riserva energetica del nostro organismo; nel corpo umano costituiscono mediamente il 17% del peso corporeo dove formano il tessuto adiposo. In generale
Lo stato gassoso e le caratteristiche dei gas
 Lo stato gassoso e le caratteristiche dei gas 1. I gas si espandono fino a riempire completamente e ad assumere la forma del recipiente che li contiene 2. Igasdiffondonounonell altroesonoingradodimescolarsiintuttiirapporti
Lo stato gassoso e le caratteristiche dei gas 1. I gas si espandono fino a riempire completamente e ad assumere la forma del recipiente che li contiene 2. Igasdiffondonounonell altroesonoingradodimescolarsiintuttiirapporti
Gas. Vapore. Forma e volume del recipiente in cui è contenuto. un gas liquido a temperatura e pressione ambiente. microscopico MACROSCOPICO
 Lo Stato Gassoso Gas Vapore Forma e volume del recipiente in cui è contenuto. un gas liquido a temperatura e pressione ambiente MACROSCOPICO microscopico bassa densità molto comprimibile distribuzione
Lo Stato Gassoso Gas Vapore Forma e volume del recipiente in cui è contenuto. un gas liquido a temperatura e pressione ambiente MACROSCOPICO microscopico bassa densità molto comprimibile distribuzione
C V. gas monoatomici 3 R/2 5 R/2 gas biatomici 5 R/2 7 R/2 gas pluriatomici 6 R/2 8 R/2
 46 Tonzig La fisica del calore o 6 R/2 rispettivamente per i gas a molecola monoatomica, biatomica e pluriatomica. Per un gas perfetto, il calore molare a pressione costante si ottiene dal precedente aggiungendo
46 Tonzig La fisica del calore o 6 R/2 rispettivamente per i gas a molecola monoatomica, biatomica e pluriatomica. Per un gas perfetto, il calore molare a pressione costante si ottiene dal precedente aggiungendo
Temperatura e Calore
 Temperatura e Calore La materia è un sistema fisico a molti corpi Gran numero di molecole (N A =6,02 10 23 ) interagenti tra loro Descrizione mediante grandezze macroscopiche (valori medi su un gran numero
Temperatura e Calore La materia è un sistema fisico a molti corpi Gran numero di molecole (N A =6,02 10 23 ) interagenti tra loro Descrizione mediante grandezze macroscopiche (valori medi su un gran numero
I SISTEMI DI UNITA DI MISURA
 Provincia di Reggio Calabria Assessorato all Ambiente Corso di Energy Manager Maggio - Luglio 2008 I SISTEMI DI UNITA DI MISURA Ilario De Marco Il sistema internazionale di unità di misura Lo studio di
Provincia di Reggio Calabria Assessorato all Ambiente Corso di Energy Manager Maggio - Luglio 2008 I SISTEMI DI UNITA DI MISURA Ilario De Marco Il sistema internazionale di unità di misura Lo studio di
Selezione test GIOCHI DELLA CHIMICA
 Selezione test GIOCHI DELLA CHIMICA CLASSE A Velocità - Equilibrio - Energia Regionali 2010 36. Se il valore della costante di equilibrio di una reazione chimica diminuisce al crescere della temperatura,
Selezione test GIOCHI DELLA CHIMICA CLASSE A Velocità - Equilibrio - Energia Regionali 2010 36. Se il valore della costante di equilibrio di una reazione chimica diminuisce al crescere della temperatura,
Meccanica e Macchine
 Introduzione alle macchine Meccanica e Macchine La statica tratta lo studio dell equilibrio dei corpi, si occupa delle forze, dei baricentri delle leve e delle travi. La cinematica tratta lo studio del
Introduzione alle macchine Meccanica e Macchine La statica tratta lo studio dell equilibrio dei corpi, si occupa delle forze, dei baricentri delle leve e delle travi. La cinematica tratta lo studio del
Termologia. Introduzione Scale Termometriche Espansione termica Capacità termica e calori specifici Cambiamenti di fase e calori latenti
 Termologia Introduzione Scale Termometriche Espansione termica Capacità termica e calori specifici Cambiamenti di fase e calori latenti Trasmissione del calore Legge di Wien Legge di Stefan-Boltzmann Gas
Termologia Introduzione Scale Termometriche Espansione termica Capacità termica e calori specifici Cambiamenti di fase e calori latenti Trasmissione del calore Legge di Wien Legge di Stefan-Boltzmann Gas
K [H 2 O] 2 = K w = [H 3 O + ][OH ]
![K [H 2 O] 2 = K w = [H 3 O + ][OH ] K [H 2 O] 2 = K w = [H 3 O + ][OH ]](/thumbs/27/10717050.jpg) Autoionizzazione dell acqua L acqua pura allo stato liquido è un debole elettrolita anfiprotico. L equilibrio di dissociazione è: 2H 2 O H 3 O + + OH - [H 3 O + ][OH ] K = [H 2 O] 2 Con K
Autoionizzazione dell acqua L acqua pura allo stato liquido è un debole elettrolita anfiprotico. L equilibrio di dissociazione è: 2H 2 O H 3 O + + OH - [H 3 O + ][OH ] K = [H 2 O] 2 Con K
Le materie plastiche Chimica e tecnologie chimiche
 Cosa sono... Le materie plastiche Chimica e tecnologie chimiche materiali artificiali polimerici con STRUTTURA MACROMOLECOLARE Monomeri e polimeri Materiali plastici... si dividono in TERMOPLASTICI ELASTOMERI
Cosa sono... Le materie plastiche Chimica e tecnologie chimiche materiali artificiali polimerici con STRUTTURA MACROMOLECOLARE Monomeri e polimeri Materiali plastici... si dividono in TERMOPLASTICI ELASTOMERI
1)Quale tra i seguenti elementi è un gas nobile? a. Si b. Mo c. Ge d. He. 2) L'acqua è:
 1)Quale tra i seguenti elementi è un gas nobile? a. Si b. Mo c. Ge d. He 2) L'acqua è: a. una sostanza elementare b. un composto chimico c. una miscela omogenea d. una soluzione 3) Quale dei seguenti elementi
1)Quale tra i seguenti elementi è un gas nobile? a. Si b. Mo c. Ge d. He 2) L'acqua è: a. una sostanza elementare b. un composto chimico c. una miscela omogenea d. una soluzione 3) Quale dei seguenti elementi
La raffinazione del petrolio
 La raffinazione del petrolio Approfondimento sulla distillazione per la I^ Itis Prof. Maurizi Franco Itis Einstein Roma ( foto ed immagini reperiti da internet, eventuali detentori di diritti sono pregati
La raffinazione del petrolio Approfondimento sulla distillazione per la I^ Itis Prof. Maurizi Franco Itis Einstein Roma ( foto ed immagini reperiti da internet, eventuali detentori di diritti sono pregati
QUALITÀ E TRATTAMENTO DELL ACQUA DEL CIRCUITO CHIUSO
 QUALITÀ E TRATTAMENTO DELL ACQUA DEL CIRCUITO CHIUSO (PARTE 1) FOCUS TECNICO Gli impianti di riscaldamento sono spesso soggetti a inconvenienti quali depositi e incrostazioni, perdita di efficienza nello
QUALITÀ E TRATTAMENTO DELL ACQUA DEL CIRCUITO CHIUSO (PARTE 1) FOCUS TECNICO Gli impianti di riscaldamento sono spesso soggetti a inconvenienti quali depositi e incrostazioni, perdita di efficienza nello
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA. Angela Chambery Lezione 2
 Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 2 Versatilità del carbonio nel formare legami covalenti La chimica degli organismi viventi è organizzata intorno al
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 2 Versatilità del carbonio nel formare legami covalenti La chimica degli organismi viventi è organizzata intorno al
tecnologia PROPRIETÀ DEI METALLI Scuola secondaria primo grado. classi prime Autore: Giuseppe FRANZÈ
 tecnologia PROPRIETÀ DEI METALLI Scuola secondaria primo grado. classi prime Autore: Giuseppe FRANZÈ LE PROPRIETÀ DEI MATERIALI DA COSTRUZIONE Si possono considerare come l'insieme delle caratteristiche
tecnologia PROPRIETÀ DEI METALLI Scuola secondaria primo grado. classi prime Autore: Giuseppe FRANZÈ LE PROPRIETÀ DEI MATERIALI DA COSTRUZIONE Si possono considerare come l'insieme delle caratteristiche
Energia nelle reazioni chimiche. Lezioni d'autore di Giorgio Benedetti
 Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
Capitolo 03 LA PRESSIONE ATMOSFERICA. 3.1 Esperienza del Torricelli 3.2 Unità di misura delle pressioni
 Capitolo 03 LA PRESSIONE ATMOSFERICA 3.1 Esperienza del Torricelli 3.2 Unità di misura delle pressioni 12 3.1 Peso dell aria I corpi solidi hanno un loro peso, ma anche i corpi gassosi e quindi l aria,
Capitolo 03 LA PRESSIONE ATMOSFERICA 3.1 Esperienza del Torricelli 3.2 Unità di misura delle pressioni 12 3.1 Peso dell aria I corpi solidi hanno un loro peso, ma anche i corpi gassosi e quindi l aria,
MISCUGLI E TECNICHE DI SEPARAZIONE
 MISCUGLI E TECNICHE DI SEPARAZIONE Classe 1^A Grafico Questo documento è solo una presentazione e non deve ritenersi completo se non è accompagnato dalla lezione in classe. Prof. Zarini Marta CLASSIFICAZIONE
MISCUGLI E TECNICHE DI SEPARAZIONE Classe 1^A Grafico Questo documento è solo una presentazione e non deve ritenersi completo se non è accompagnato dalla lezione in classe. Prof. Zarini Marta CLASSIFICAZIONE
) e 200 ml di NaOH 0.1 M. I volumi si considerano additivi.[ph = 4.085]
![) e 200 ml di NaOH 0.1 M. I volumi si considerano additivi.[ph = 4.085] ) e 200 ml di NaOH 0.1 M. I volumi si considerano additivi.[ph = 4.085]](/thumbs/26/9134725.jpg) Chimica Analitica Prova scritta del 19 Gennaio 2004 1) 375 ml di soluzione acquosa contengono 21.2 µg di un principio attivo. Esprimere la concentrazione della soluzione in parti per milione (ppm) [0.056
Chimica Analitica Prova scritta del 19 Gennaio 2004 1) 375 ml di soluzione acquosa contengono 21.2 µg di un principio attivo. Esprimere la concentrazione della soluzione in parti per milione (ppm) [0.056
Indice. 1 La materia e la sua struttura. 2 La radioattività ed i processi nucleari
 Indice PREFAZIONE ALLA SECONDA EDIZIONE XIII 1 La materia e la sua struttura 1.1. Le particelle fondamentali e la struttura dell atomo 2 1.2. Il numero atomico, il numero di massa, i nuclidi e gli isotopi
Indice PREFAZIONE ALLA SECONDA EDIZIONE XIII 1 La materia e la sua struttura 1.1. Le particelle fondamentali e la struttura dell atomo 2 1.2. Il numero atomico, il numero di massa, i nuclidi e gli isotopi
LE SOLUZIONI 1.molarità
 LE SOLUZIONI 1.molarità Per mole (n) si intende una quantità espressa in grammi di sostanza che contiene N particelle, N atomi di un elemento o N molecole di un composto dove N corrisponde al numero di
LE SOLUZIONI 1.molarità Per mole (n) si intende una quantità espressa in grammi di sostanza che contiene N particelle, N atomi di un elemento o N molecole di un composto dove N corrisponde al numero di
352&(662',&20%867,21(
 352&(662',&20%867,21( Il calore utilizzato come fonte energetica convertibile in lavoro nella maggior parte dei casi, è prodotto dalla combustione di sostanze (es. carbone, metano, gasolio) chiamate combustibili.
352&(662',&20%867,21( Il calore utilizzato come fonte energetica convertibile in lavoro nella maggior parte dei casi, è prodotto dalla combustione di sostanze (es. carbone, metano, gasolio) chiamate combustibili.
Trattamenti delle acque primarie
 Trattamenti Impianti Meccanici 1 ELIMINAZIONE DELL ANIDRIDE CARBONICA ELIMINAZIONE DELL OSSIGENO AEREAZIONE DELL ACQUA DEFERRITIZZAZIONE DEMANGANIZZAZIONE ADDOLCIMENTO Impianti Meccanici 2 1 Trattamenti
Trattamenti Impianti Meccanici 1 ELIMINAZIONE DELL ANIDRIDE CARBONICA ELIMINAZIONE DELL OSSIGENO AEREAZIONE DELL ACQUA DEFERRITIZZAZIONE DEMANGANIZZAZIONE ADDOLCIMENTO Impianti Meccanici 2 1 Trattamenti
