CORSO DI BIOCHIMICA PER INGEGNERIA BIOMEDICA 2 ESERCITAZIONE
|
|
|
- Simona Benedetti
- 7 anni fa
- Visualizzazioni
Transcript
1 CORSO DI BIOCHIMICA PER INGEGNERIA BIOMEDICA 2 ESERCITAZIONE 1) Il collagene è una proteina (globulare / fibrosa). È formata da tre (catene alfa/alfa eliche) con andamento (destrorso/sinistrorso) che vanno a formare il tropocollagene che ha andamento (destrorso /sinistrorso). La struttura primaria è caratterizzata dalla ripetizione del tripeptide (Gly-X-Y/Ala-X-Y); X e Y possono essere, residui che hanno subito modificazioni post-traduzionali. Queste modificazioni avvengono ad opera di un enzima che necessita di VITAMINA C GLY/X/Y FIBROSA CATENE ALFA SINISTRORSO DESTRORSO 4-IDROSSIPROLINA O 5-IDROSSILISINA (vitamina C/ vitamina B) e la cui carenza comporta SCORBUTO l insorgenza della malattia (pellagra / scorbuto).
2 Catena α sinistrorsa Collagene Tre eliche si arrotolano insieme con un andamento destrorso ( TROPOCOLLAGENE)
3 Unità tripeptidica ripetuta Gly -X-Y Collagene O O O O O O C C C C NH CH C NH CH C N CH H 2 C 5 3 CH 2 H 2 C 5 3 HCH 2 C 2 5 HO CH HO N CH CH N 1 4 CH 2 4-idrossiprolina CH 2 3 CHH 2 C 5 N 1 4 OH CH 2 CH 2 3 CH OH H CH 2 CH 2 C CH 2 OH H CH 2 CH 2 C CH 2 OH ACIDO ASCORBICO (vitamina C) NH 3 NH 3 5-idrossiLisina
4 Collagene Legami covalenti CROCIATI inter-intramolecolari tra Lys, HyLys, o His TROPOCOLLAGENE
5 MALATTIE DEL COLLAGENE DOVUTE A MUTAZIONI GENICHE: sostituzione di un residuo di Gly con Cys o Ser in ciascuna catena α: Sindrome di Ehlers-Danlos
6 MALATTIE DEL COLLAGENE DOVUTE A MUTAZIONI GENICHE: sostituzione di un residuo di Gly con Cys o Ser in ciascuna catena α: Osteogenesi imperfetta (sindrome ossa di vetro)
7 Collagene SCORBUTO carenza di vitamina C
8 2) Le -cheratine (rispondere vero o falso) a) sono proteine globulari b) sono formate prevalentemente da -eliche c) sono formate prevalentemente da residui aminoacidici di piccole dimensioni d) l unità fondamentale delle -cheratine è la protofibrilla e) le struttura delle -cheratine è resa stabile da legami idrogeno
9 -cheratina catena polipeptidica con oltre 100 residui, elica destrorsa due polipeptidi danno origine a un avvolgimento avvolto dimerico e sinistrorso 2 file sfalsate di dimeri si associano testa-coda 2 protofilamenti si associano e formano le protofibrille
10 -cheratina 4 protofibrille
11 Conformazione nativa -cheratina Il numero dei ponti disolfuro è indice della durezza delle α-cheratine
12 3. Disegnare la curva di ossigenazione di una emoglobina avente un valore di p50 pari a 30 torr e determinare come varierà (rappresentandole graficamente) questa curva al variare dei seguenti parametri: 1) diminuzione del ph 2) diminuzione della concentrazione di BPG 3) motivare le risposte ai punti 1) 2)
13 Curva di dissociazione dell O 2 per l emoglobina Hb + 4O 2 = Hb(O 2 ) 4 Hb sigmoidale L emoglobina lega l O 2 quando la pressione parziale del gas (po 2 ) è elevata (polmoni) e lo rilascia quando la pressione è bassa (tessuti).
14 pco 2 pco 2 tu Camera mia bella Influenza della pco 2
15 Influenza del ph tessuti polmoni
16 Influenza del 2,3- BPG
17 4. Data la seguente reazione: Fruttosio-6-fosfato Fruttosio-1,6-bisfosfato Fosfofruttochinasi Calcolare la velocità iniziale della reazione enzimatica della fosfofruttochinasi sapendo che la concentrazione iniziale del Fruttosio-6-fosfato è 0.03 mm, la concentrazione della fosfofruttochinasi è 10 mm, Km corrisponde a 0.1 mm, V max a 0.66 mm/min. Spiegare brevemente il significato di Km.
18
19 CINETICA ENZIMATICA: concentrazione del substrato La velocità di una reazione catalizzata da un enzima aumenta all aumentare della concentrazione del substrato fino a raggiungere una velocità massima (V max ). In questa condizione i siti attivi dell enzima sono saturi del substrato Quando tutto l enzima è saturato con il substrato: [ES] = [E tot ] V 0 = Vmax
20 La curva che esprime la relazione tra V 0 e S ha un andamento iperbolico ed è espressa algebricamente dalla equazione di Michaelis-Menten Costante di Michaelis e Menten La Km è quella concentrazione di substrato a cui la V 0 è pari a metà della Vmax
21 L equazione di Michaelis-Menten descrive la variazione della velocità di reazione al variare della concentrazione del substrato. v 0 = velocità iniziale della reazione V max = velocità massima K m = costante di Michaelis-Menten [S] = concentrazione del substrato
22 Caratteristiche della K m La K m è pari alla concentrazione di substrato alla quale la velocità della reazione (V 0 ) è 1/2 della V max. La K m riflette l affinità dell enzima per il substrato: K m piccola = alta affinità dell enzima per il substrato K m grande = bassa affinità dell enzima per il substrato. Ogni enzima ha una K m caratteristica per un dato substrato. La K m non varia al variare della [E].
23 I PARAMETRI CINETICI POSSONO ESSERE USATI PER CONFRONTARE LE ATTIVITA DEGLI ENZIMI
24 6) Che influenza possono avere temperatura e ph sull attività di un enzima?motivare la risposta
25 FATTORI CHE MODIFICANO LA VELOCITA DELLE REAZIONI ENZIMATICHE: 1) ph (curva a campana) 2) temperatura (curva bifasica a causa della denaturazione) 3) [S] (iperbole rettangolare a causa della saturazione) 4) inibitori CINETICA ENZIMATICA
26 CINETICA ENZIMATICA: ph Ciascun enzima ha un ph ottimale al quale la reazione è catalizzata con la massima efficienza. Esso in genere rispecchia il ph dell ambiente in cui l enzima svolge normalmente le sue funzioni. La concentrazione degli H + (ph) influenza l attività enzimatica modificando la geometria del sito attivo e la distribuzione delle cariche elettriche dei gruppi coinvolti nel legame del substrato o nel processo catalitico stesso. Valori di ph estremi possono anche provocare la denaturazione dell enzima.
27 CINETICA ENZIMATICA: ph
28 CINETICA ENZIMATICA: temperatura La velocità di reazione aumenta con l aumentare della temperatura fino a raggiungere un picco. Un ulteriore innalzamento della temperatura provoca una diminuzione della velocità di reazione a causa della denaturazione dell enzima.
29 CINETICA ENZIMATICA: temperatura
30 7) Indicare se le seguenti affermazioni relative al legame dell ossigeno all emoglobina sono vere o false. a) L effetto Bohr fa diminuire l affinità per l ossigeno in seguito all aumento del ph. b) Il biossido di carbonio fa aumentare l affinità per l ossigeno dell emoglobina, legandosi ai gruppi amminici terminali delle catene polipeptidiche. c) L affinità dell emoglobina per l ossigeno aumenta all aumentare della percentuale di saturazione. d) Il tetramero di emoglobina lega 4 molecole di 2,3-BPG. e) Il sangue fetale ha un affinità per l ossigeno più elevata del sangue dell adulto, perché la HbF ha una minore affinità per il 2,3-BPG. f) La composizione dell HbF è α2δ2.
31 Influenza del 2,3- BPG
32 Influenza del 2,3- BPG Il 2,3 BPG è una piccola molecola dotata di cariche negative che consentono il legame a una serie di cariche positive di catene laterali di AA situati sulle due catene β, formando ponti salini e stabilizzando la forma T. Il sito per il 2,3 BPG è presente solo nella forma tesa T.
33 Influenza del 2,3- BPG Nell Hb deossigenata (T) è presente una cavità centrale che si restringe consistentemente in Hb in forma R (ossigenata): tale cavità nella forma T ospita il 2,3 BPG, modulatore allosterico negativo.
34 EMOGLOBINA FETALE (HbF) Il significato del 2,3 BPG appare chiaro se si confronta la curva di saturazione dell HbA materna e dell Hb e fetale. Gli eritrociti fetali contengono un Hb con struttura quaternaria α2 2. Fra le catene il 2,3-BPG si lega più debolmente rispetto a quello che avviene nell HbA. La curva di saturazione dell Hb fetale è a sinistra rispetto a quella della HbA materna, indicando maggiore affinità per O 2. L'O 2 rilasciato nella circolazione placentare dall Hb materna a certe pressioni parziali, viene assunto dall Hb fetale, più affine, e ciò soddisfa l'esigenza fisiologica di rifornimento di O 2 al feto da parte della madre.
35 8) Come possono essere classificate le proteine di membrana?
36 Componente proteica INTEGRALI: strettamente associate al doppio strato lipidico tramite interazioni idrofobiche (rimovibili con detergenti oppure tramite reazioni enzimatiche) PERIFERICHE: interazioni elettrostatiche e legami a H con i domini idrofilici delle proteine integrali e con le teste polari dei lipidi di membrana (rimovibili con agenti in grado di interferire con il legame) ANFITROPICHE: si trovano sia nel citosol che associate alle membrane a seconda del tipo di regolazione a cui sono sottoposte
37 Componente proteica Proteine integrali di membrana Interazioni idrofobiche tra lipidi di membrana e domini idrofobici delle proteine
38 Componente Proteine integrali di membrana Barile β proteica Porine Consentono ai soluti polari di attraversare la membrana
39 9) Quali sono i costituenti di questi lipidi di membrana: a) triacilgligerolo b) acido fosfati dico c) ceramide
40 Triacilgliceroli (Trigliceridi)
41 Triacilgliceroli (Trigliceridi) T. Semplici: Glicerolo 3 ac. grassi uguali Legame estere T. Misti: Glicerolo 2 (o 3) ac. grassi diversi
42 Glicerofosfolipidi ( fosfogliceridi) Legame estere Legame fosfodiestere Legame estere
43 Glicerofosfolipidi (fosfogliceridi)
44 Glicerofosfolipidi (fosfogliceridi)
45 sfingolipidi Legame ammidico
46 10) Scrivere la formula di struttura di un triacilglicerolo a piacere e specificare: è un trigliceride misto o semplice? Che tipi di legami sono presenti tra le varie molecole costituenti?
47 Triacilgliceroli (Trigliceridi) T. Semplici: Glicerolo 3 ac. grassi uguali Legame estere T. Misti: Glicerolo 2 (o 3) ac. grassi diversi
48 11) Descrivere in modo sintetico le caratteristiche dei doppi strati lipidici. Inoltre, spiegare brevemente a cosa si riferiscono i seguenti termini: a) mobilità trasversale b) mobilità laterale c) asimmetria
49 Modello a mosaico fluido
50 Componente Lipidica Aggregazione di Lipidi Anfipatici in acqua Glicerofosfolipidi Sfingolipidi Liposoma
51 Dinamica delle membrane La struttura e la flessibilità delle membrane dipendono dalla temperatura e dalla composizione in lipidi
52 Le membrane sono FLUIDE La struttura e la flessibilità delle membrane dipendono dalla temperatura e dalla composizione in lipidi a temp. fisiologiche stato fluido ordinato
53 a temperature intermedie alla temperatura di transizione di fase (Tm) passano allo stato fluido La temperatura di transizione aumenta in proporzione alla lunghezza della catena degli acidi grassi e al grado di saturazione
54 Dinamica delle membrane a) Il calore produce un movimento termico delle catene laterali Transizione solido fluido b) Diffusione laterale nel piano del doppio strato I fosfolipidi, oltre a spostarsi lateralmente lungo il piano dello strato bimolecolare, possono passare da uno strato all altro per inversione testa-coda FLIP-FLOP c) Diffusione attraverso il doppio strato t1/2 da ore a giorni ( reazione non catalizzata). secondi (reazione catalizzata da flippasi)
55 Dinamica delle membrane A temperatura fisiologica FLIP-FLOP questo movimento è limitato dalla difficoltà di trasferire la testa idrofilica della molecola lipidica attraverso la zona centrale idrofobica dello strato bimolecolare.
56 Dinamica delle membrane Ca 2+ PE= fosfatidiletanolammina PS= fosfatidilserina
57 Interazione del Colesterolo con i lipidi di membrana
58 Interazione del Colesterolo con i lipidi di membrana
59 12) Descrivere le differenze tra trasporto attivo e trasporto passivo attraverso le membrane
60 Diffusione semplice Trasporto di soluti attraverso le membrane
61 Trasporto di soluti attraverso le membrane Soluti polari Diffusione facilitata trasporto passivo
62 Trasporto di soluti attraverso le membrane: cotrasporto
63 Trasporto di soluti attraverso le membrane Velocità ridotte, Saturabili Alta stereospecificità Velocità elevate non saturabili Minore stereospecificità Diffusione contro gradiente di concentrazione Diffusione secondo gradiente di concentrazione
64 Trasporto di soluti attraverso le Diffusione contro gradiente di concentrazione membrane
65 Trasporto di soluti attraverso le membrane Un esempio di trasporto attivo primario è dato dalle ATPasi: Na + K + ATPasi ha la funzione di mantenere la differenza di composizione ionica tra il citosol e il mezzo extracellulare [Na + ] [K + ]
66 13) Che cosa sono gli enzimi? Quale ruolo svolgono all interno degli esseri viventi?
67 catalizzatori biologici rendono possibile da un punto di vista cinetico le reazioni chimiche Gli Enzimi Sono le proteine più importanti e più specializzate Presentano un elevato grado di specificità per il substrato Operano in soluzioni acquose con temperature e ph blandi
68 Struttura generale degli enzimi Sono proteine globulari complesse: Addotto enzima-substrato Parte proteica Parte non-proteica Cofattore (ione metallico) Coenzima (natura organica: vitamina o altro) Gruppo Prostetico
69 SITO ATTIVO: specifica porzione dell enzima, deputata al legame con il substrato che porta alla formazione dell addotto ES Addotto ES
70 Proprietà dei Catalizzatori I catalizzatori sono sostanze capaci di abbassare l energia di attivazione rendendo piú facile la formazione dell addotto ES: la reazione diviene quindi piú veloce.
71 14) Sapendo che : a)il ΔG di idrolisi dell ATP ( ATP ADP + Pi) corrisponde a -31 KJ/n b)il ΔG di idrolisi della reazione Fruttosio 1,6 bisfosfato Pi + fruttosio 6-fosfato corrisponde a KJ/n Calcolare il ΔG della reazione ATP + Fruttosio 6 fosfato ADP + Pi + fruttosio 1,6-bisfosfato
72
73
74
75 Reazioni accoppiate Somma :
76 Reazioni accoppiate 1 semireazione endoergonica 2 semireazione esooergonica Reazione complessiva accoppiata
77 15) Spiegare in che cosa consiste la fosforilazione a livello del substrato. Fai un esempio
78 7) Fosforilazione a livello del substrato: ADP riceve un fosfato da un intermedio metabolico
79 10) Fosforilazione a livello del substrato: ADP riceve un fosfato da un intermedio metabolico
Elementi strutturali delle membrane biologiche Trasportatori di elettroni Messaggeri intracellulari Agenti emulsionanti del tratto intestinale
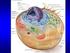 Forme di riserva di energia Cofattori enzimatici Pigmenti Ormoni Elementi strutturali delle membrane biologiche Trasportatori di elettroni Messaggeri intracellulari Agenti emulsionanti del tratto intestinale
Forme di riserva di energia Cofattori enzimatici Pigmenti Ormoni Elementi strutturali delle membrane biologiche Trasportatori di elettroni Messaggeri intracellulari Agenti emulsionanti del tratto intestinale
Vitamine Liposolubili
 Vitamine Liposolubili Vitamine Liposolubili A-D-E-K Sono composti ISOPRENOIDI isoprene Solo la K funziona da coenzima Difficile andare incontro a carenza a Si accumulano nel tessuto grasso o nel fegato
Vitamine Liposolubili Vitamine Liposolubili A-D-E-K Sono composti ISOPRENOIDI isoprene Solo la K funziona da coenzima Difficile andare incontro a carenza a Si accumulano nel tessuto grasso o nel fegato
Amminoacidi Peptidi Proteine
 Amminoacidi Peptidi Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Gli amminoacidi nelle molecole proteiche sono tutti stereoisomeri L IDROFOBOCI IDROFOBOCI IDROFILICI Secondo gruppo
Amminoacidi Peptidi Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Gli amminoacidi nelle molecole proteiche sono tutti stereoisomeri L IDROFOBOCI IDROFOBOCI IDROFILICI Secondo gruppo
- lipidi strutturali, costituenti fondamentali delle membrane cellulari ed intracellulari (fosfolipidi, glicolipidi e colesterolo)
 I lipidi, o grassi, costituiscono un gruppo eterogeneo di sostanze accomunate dalla proprietà fisica della insolubilità nei solventi polari (es. acqua) (idrofobicità) e dalla solubilità nei soventi organici
I lipidi, o grassi, costituiscono un gruppo eterogeneo di sostanze accomunate dalla proprietà fisica della insolubilità nei solventi polari (es. acqua) (idrofobicità) e dalla solubilità nei soventi organici
Gli Enzimi. catalizzatori biologici rendono possibile da un punto di vista cinetico le reazioni chimiche
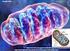 catalizzatori biologici rendono possibile da un punto di vista cinetico le reazioni chimiche Gli Enzimi Sono le proteine più importanti e più specializzate Presentano un elevato grado di specificità per
catalizzatori biologici rendono possibile da un punto di vista cinetico le reazioni chimiche Gli Enzimi Sono le proteine più importanti e più specializzate Presentano un elevato grado di specificità per
ENZIMI. Un enzima è un catalizzatore (acceleratore) di reazioni biologiche.
 ENZIMI ENZIMI Un enzima è un catalizzatore (acceleratore) di reazioni biologiche. Catalizzatore = sostanza in grado di accelerare lo svolgimento di una reazione chimica e quindi di aumentarne la sua velocità,
ENZIMI ENZIMI Un enzima è un catalizzatore (acceleratore) di reazioni biologiche. Catalizzatore = sostanza in grado di accelerare lo svolgimento di una reazione chimica e quindi di aumentarne la sua velocità,
FUNZIONI delle PROTEINE
 FUNZIONI delle PROTEINE Ha le dimensioni del reciproco di una concentrazione (M -1 ) Ha le dimensioni di una concentrazione (M) La frazione dei siti occupati rispetto ai siti totali è definita come θ FRAZIONE
FUNZIONI delle PROTEINE Ha le dimensioni del reciproco di una concentrazione (M -1 ) Ha le dimensioni di una concentrazione (M) La frazione dei siti occupati rispetto ai siti totali è definita come θ FRAZIONE
Proprietà comuni. Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici
 Gli aminoacidi Proprietà comuni Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici paragonabili Il gruppo α-aminico è un acido più forte (o una base più debole
Gli aminoacidi Proprietà comuni Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici paragonabili Il gruppo α-aminico è un acido più forte (o una base più debole
Nel corso dell evoluzione, con il passaggio dalla. progressivamente differenziati due meccanismi. un sistema circolatorio adeguato;
 PROTEINE RESPIRATORIE EMOGLOBINA & MIOGLOBINA Nel corso dell evoluzione, con il passaggio dalla vita anaerobia alla vita aerobia si sono progressivamente differenziati due meccanismi che sono in grado
PROTEINE RESPIRATORIE EMOGLOBINA & MIOGLOBINA Nel corso dell evoluzione, con il passaggio dalla vita anaerobia alla vita aerobia si sono progressivamente differenziati due meccanismi che sono in grado
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
La struttura delle proteine
 La struttura delle proteine Funzioni delle proteine Strutturali Contrattili Trasporto Riserva Ormonali Enzimatiche Protezione Struttura della proteina Struttura secondaria: ripiegamento locale della catena
La struttura delle proteine Funzioni delle proteine Strutturali Contrattili Trasporto Riserva Ormonali Enzimatiche Protezione Struttura della proteina Struttura secondaria: ripiegamento locale della catena
Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi)
 ENZIMI Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi) Sono in grado di aumentare la velocità dei processi catalizzati fino a
ENZIMI Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi) Sono in grado di aumentare la velocità dei processi catalizzati fino a
Le MEMBRANE in biologia
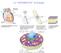 Le MEMBRANE in biologia Le membrana plasmatica Delimitazione delle cellule Genesi del potenziale elettrico trans-membrana Mantenimento delle differenze tra l ambiente intra ed extracellulare Trasferimento
Le MEMBRANE in biologia Le membrana plasmatica Delimitazione delle cellule Genesi del potenziale elettrico trans-membrana Mantenimento delle differenze tra l ambiente intra ed extracellulare Trasferimento
Aminoacidi. Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α
 Aminoacidi Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α 1 Isomeria ottica Tutti gli AA, esclusa la glicina, presentano almeno un atomo di carbonio asimmetrico, il
Aminoacidi Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α 1 Isomeria ottica Tutti gli AA, esclusa la glicina, presentano almeno un atomo di carbonio asimmetrico, il
Struttura e funzione delle membrane biologiche
 La membrana plasmatica delimita la cellula e separa l ambiente interno da quello esterno. Non impedisce però tutti gli scambi Struttura e funzione delle membrane biologiche Figure'11)1'!Essen&al!Cell!Biology!(
La membrana plasmatica delimita la cellula e separa l ambiente interno da quello esterno. Non impedisce però tutti gli scambi Struttura e funzione delle membrane biologiche Figure'11)1'!Essen&al!Cell!Biology!(
- utilizzano esclusivamente le reattività chimiche di alcuni residui AA
 Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Esempi di proteine: Mioglobina ed Emoglobina
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Esempi di proteine: Mioglobina ed Emoglobina Mioglobina: caratteristiche generali, funzione
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Esempi di proteine: Mioglobina ed Emoglobina Mioglobina: caratteristiche generali, funzione
PROTEINE DEFINIZIONE:
 Cap.4 Le PROTEINE DEFINIZIONE: Macromolecole formate di AA della serie L uniti tra loro da un legame peptidico. FUNZIONI DELLE PROTEINE Enzimi Proteine di riconoscimento Proteine di trasporto Proteine
Cap.4 Le PROTEINE DEFINIZIONE: Macromolecole formate di AA della serie L uniti tra loro da un legame peptidico. FUNZIONI DELLE PROTEINE Enzimi Proteine di riconoscimento Proteine di trasporto Proteine
PIANO DI LAVORO ANNUALE
 PIANO DI LAVORO ANNUALE Classe 5D2 A.S. 2015/2016 Disciplina: CHIMICA ORGANICA E BIOCHIMICA Docente: prof.ssa Palma Elena Ore settimanali: 4 (2 laboratorio) Libro di testo: Rippa, Ricciotti La chimica
PIANO DI LAVORO ANNUALE Classe 5D2 A.S. 2015/2016 Disciplina: CHIMICA ORGANICA E BIOCHIMICA Docente: prof.ssa Palma Elena Ore settimanali: 4 (2 laboratorio) Libro di testo: Rippa, Ricciotti La chimica
LIPIDI E MEMBRANE BIOLOGICHE
 Cap.8 LIPIDI E MEMBRANE BIOLOGICE Definizione (la parola deriva dal greco lípos, grasso): MOLECOLE INSOLUBILI IN ACQUA SOLUBILI NEI SOLVENTI ORGANICI NON POLARI Molecole con struttura chimica e funzioni
Cap.8 LIPIDI E MEMBRANE BIOLOGICE Definizione (la parola deriva dal greco lípos, grasso): MOLECOLE INSOLUBILI IN ACQUA SOLUBILI NEI SOLVENTI ORGANICI NON POLARI Molecole con struttura chimica e funzioni
CARBOIDRATI SEMPLICI
 CARBOIDRATI Dal greco glucos =dolce Glucidi Zuccheri Sostanze formate acqua e carbonio Hanno forma molecolare (CH₂O)n 1 CARBOIDRATI SEMPLICI Monosaccaridi, una sola unità di poliidrossi aldeide o di poliidrossi
CARBOIDRATI Dal greco glucos =dolce Glucidi Zuccheri Sostanze formate acqua e carbonio Hanno forma molecolare (CH₂O)n 1 CARBOIDRATI SEMPLICI Monosaccaridi, una sola unità di poliidrossi aldeide o di poliidrossi
Con il termine generico di lipidi si definisce una classe. eterogenea dal punto di vista chimico di composti
 on il termine generico di lipidi si definisce una classe eterogenea dal punto di vista chimico di composti presenti nei tessuti animali e vegetali, accomunati dalla somiglianza di proprietà fisiche, come
on il termine generico di lipidi si definisce una classe eterogenea dal punto di vista chimico di composti presenti nei tessuti animali e vegetali, accomunati dalla somiglianza di proprietà fisiche, come
Introduzione alla biologia della cellula. Lezione 2 Le biomolecole
 Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
GLI ENZIMI: proteine con attività CATALITICA
 Cap. 6 GLI ENZIMI: proteine con attività CATALITICA Catalizzatori biologici: permettono alle reazioni biochimiche di avvenire a temperature e pressioni fisiologiche e a velocità misurabile. Aumentano la
Cap. 6 GLI ENZIMI: proteine con attività CATALITICA Catalizzatori biologici: permettono alle reazioni biochimiche di avvenire a temperature e pressioni fisiologiche e a velocità misurabile. Aumentano la
9) Scrivere un disaccaride formato dal β-d-galattosio e dall α-d-n-acetil-glucosammina legati da un legame glicosidico β(1-4).
 CARBOIDRATI - AMMINOACIDI - PROTEINE 1) Scrivere la proiezione di Fisher del D-ribosio e del D-glucosio. La lettera D a cosa si riferisce? Disegnare inoltre il disaccaride ottenuto dalla condensazione
CARBOIDRATI - AMMINOACIDI - PROTEINE 1) Scrivere la proiezione di Fisher del D-ribosio e del D-glucosio. La lettera D a cosa si riferisce? Disegnare inoltre il disaccaride ottenuto dalla condensazione
LE MOLECOLE BIOLOGICHE
 LE MOLECOLE BIOLOGICHE Le cellule contengono quattro famiglie principali di molecole organiche Zuccheri (monosaccaridi) - forniscono una fonte di energia - subunità dei polisaccaridi Amminoacidi - subunità
LE MOLECOLE BIOLOGICHE Le cellule contengono quattro famiglie principali di molecole organiche Zuccheri (monosaccaridi) - forniscono una fonte di energia - subunità dei polisaccaridi Amminoacidi - subunità
Principi di Biochimica
 Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
LE PROTEINE. SONO Polimeri formati dall unione di AMMINOACIDI (AA) Rende diversi i 20 AA l uno dall altro UN ATOMO DI C AL CENTRO
 LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
I lipidi. Semplici Complessi
 Lipidi I lipidi I lipidi sono sostanze non polari (idrofobiche) solubili in solven8 organici. Mol8 dei lipidi che compongono le membrane biologiche sono anfipa8ci, hanno una parte polare ed una apolare
Lipidi I lipidi I lipidi sono sostanze non polari (idrofobiche) solubili in solven8 organici. Mol8 dei lipidi che compongono le membrane biologiche sono anfipa8ci, hanno una parte polare ed una apolare
Esempi di proteine: Mioglobina ed Emoglobina
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica Organica e Biochimica Esempi di proteine: Mioglobina ed Emoglobina Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica Organica e Biochimica Esempi di proteine: Mioglobina ed Emoglobina Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base
LE PROTEINE -struttura tridimensionale-
 LE PROTEINE -struttura tridimensionale- Struttura generale di una proteina Ceruloplasmina Cosa sono??? Sono biopolimeri con forme ben definite. composti da molteplici amminoacidi, legati con legami peptidici
LE PROTEINE -struttura tridimensionale- Struttura generale di una proteina Ceruloplasmina Cosa sono??? Sono biopolimeri con forme ben definite. composti da molteplici amminoacidi, legati con legami peptidici
MEMBRANE. struttura: fosfolipidi e proteine
 MEMBRANE struttura: fosfolipidi e proteine I lipidi sono sostanze di origine biologica insolubili in acqua. Vi fanno parte: trigliceridi, fosfolipidi, colesterolo, sfingolipidi, alcoli alifatici, cere,
MEMBRANE struttura: fosfolipidi e proteine I lipidi sono sostanze di origine biologica insolubili in acqua. Vi fanno parte: trigliceridi, fosfolipidi, colesterolo, sfingolipidi, alcoli alifatici, cere,
Funzioni delle proteine
 Funzioni delle proteine ENZIMI Proteine di trasporto Proteine di riserva Proteine contrattili o motili Proteine strutturali Proteine di difesa Proteine regolatrici Proteine di trasporto Emoglobina Lipoproteine
Funzioni delle proteine ENZIMI Proteine di trasporto Proteine di riserva Proteine contrattili o motili Proteine strutturali Proteine di difesa Proteine regolatrici Proteine di trasporto Emoglobina Lipoproteine
5. Trasporto di membrana
 5. Trasporto di membrana contiene materiale protetto da copyright, ad esclusivo uso personale; 1 non è consentita diffusione ed utilizzo di tipo commerciale Le membrane biologiche hanno una permeabilità
5. Trasporto di membrana contiene materiale protetto da copyright, ad esclusivo uso personale; 1 non è consentita diffusione ed utilizzo di tipo commerciale Le membrane biologiche hanno una permeabilità
Le macromolecole dei tessuti - 1
 Le macromolecole dei tessuti - 1 Che cosa sono le proteine? Sono macromolecole complesse ad alta informazione Sono costituite da una o più catene polipeptidiche Ogni catena peptidica è composta da centinaia
Le macromolecole dei tessuti - 1 Che cosa sono le proteine? Sono macromolecole complesse ad alta informazione Sono costituite da una o più catene polipeptidiche Ogni catena peptidica è composta da centinaia
Legami chimici. Covalente. Legami deboli
 Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici STRUTTURA TERZIARIA La struttura tridimensionale
Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici STRUTTURA TERZIARIA La struttura tridimensionale
LIPIDI. I lipidi (la parola deriva dal greco lìpos, grasso) sono un gruppo di sostanze grasse presente in tutti gli organismi viventi.
 LIPIDI I lipidi (la parola deriva dal greco lìpos, grasso) sono un gruppo di sostanze grasse presente in tutti gli organismi viventi. I lipidi sono composti idrofobi perché non sono solubili in acqua ma
LIPIDI I lipidi (la parola deriva dal greco lìpos, grasso) sono un gruppo di sostanze grasse presente in tutti gli organismi viventi. I lipidi sono composti idrofobi perché non sono solubili in acqua ma
RUOLI BIOLOGICI DELLE PROTEINE. Biochimica
 RUOLI BIOLOGICI DELLE PROTEINE Biochimica Il collagene una proteina strutturale Il collagene è un componente principale di tessuti quali la pelle, i capelli, i tendini, le ossa, il cartilagine, i vasi
RUOLI BIOLOGICI DELLE PROTEINE Biochimica Il collagene una proteina strutturale Il collagene è un componente principale di tessuti quali la pelle, i capelli, i tendini, le ossa, il cartilagine, i vasi
ENZIMI. Durante la reazione l enzima può essere temporaneamente modificato ma alla fine del processo ritorna nel suo stato originario, un enzima viene
 ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari, e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari, e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
La chimica della pelle
 La chimica della pelle 1 Gli amminoacidi Queste unità hanno la particolare caratteristica di contenere nella stessa molecola un gruppo acido (- COOH) ed uno basico (- NH 2 ), legati tra loro attraverso
La chimica della pelle 1 Gli amminoacidi Queste unità hanno la particolare caratteristica di contenere nella stessa molecola un gruppo acido (- COOH) ed uno basico (- NH 2 ), legati tra loro attraverso
Chimica Biologica A.A α-elica foglietto β reverse turn
 Chimica Biologica A.A. 2010-2011 α-elica foglietto β reverse turn Str. Secondaria sperimentalmente osservata: Si distinguono fondamentalmente tre tipi di strutture secondarie: α elica foglietto β reverse
Chimica Biologica A.A. 2010-2011 α-elica foglietto β reverse turn Str. Secondaria sperimentalmente osservata: Si distinguono fondamentalmente tre tipi di strutture secondarie: α elica foglietto β reverse
Polimorfismo genetico del collageno
 COLLAGENO È la proteina più abbondante del nostro corpo costituendo il 25% delle proteine totali. È la proteina principale dei tessuti connettivi, la cui matrice extracellulare contiene anche: -proteoglicani
COLLAGENO È la proteina più abbondante del nostro corpo costituendo il 25% delle proteine totali. È la proteina principale dei tessuti connettivi, la cui matrice extracellulare contiene anche: -proteoglicani
CARBOIDRATI C H O ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO
 CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
Struttura degli amminoacidi
 AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
Catalisi. Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A Modulo di Biologia Strutturale
 Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Catalisi Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie
Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Catalisi Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie
TEORIA DELLO STATO DI TRANSIZIONE (Henry Eyring anni 30)
 TEORIA DELLO STATO DI TRANSIZIONE (Henry Eyring anni 30) A + B-C A-B + C (A B C) Complesso attivato Stato di transizione Coordinata di reazione H A H B + H C H A + H B H C A+ K B X k' P + Q [ P] d dt =
TEORIA DELLO STATO DI TRANSIZIONE (Henry Eyring anni 30) A + B-C A-B + C (A B C) Complesso attivato Stato di transizione Coordinata di reazione H A H B + H C H A + H B H C A+ K B X k' P + Q [ P] d dt =
ACIDI GRASSI INSATURI
 LIPIDI ACIDI GRASSI SATURI ACIDI GRASSI INSATURI TRIGLICERIDI TRIGLICERIDI Grassi neutri o lipidi semplici glicerolo + 1 acido grasso monogliceride glicerolo + 2 acidi grassi digliceride glicerolo + 3
LIPIDI ACIDI GRASSI SATURI ACIDI GRASSI INSATURI TRIGLICERIDI TRIGLICERIDI Grassi neutri o lipidi semplici glicerolo + 1 acido grasso monogliceride glicerolo + 2 acidi grassi digliceride glicerolo + 3
L ACQUA E LE SUE PROPRIETÀ
 L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
CORSO DI BIOCHIMICA PER INGEGNERIA BIOMEDICA I ESERCITAZIONE
 CORSO DI BIOCHIMICA PER INGEGNERIA BIOMEDICA I ESERCITAZIONE 1) Che tipo di ibridazione ha il carbonio coinvolto nel doppio legame degli alcheni? Descrivi brevemente. Alcheni Ibridazione sp 2 2s p x p
CORSO DI BIOCHIMICA PER INGEGNERIA BIOMEDICA I ESERCITAZIONE 1) Che tipo di ibridazione ha il carbonio coinvolto nel doppio legame degli alcheni? Descrivi brevemente. Alcheni Ibridazione sp 2 2s p x p
Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi.
 ENZIMI Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. Svolgono il loro ruolo con modalità differenti
ENZIMI Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. Svolgono il loro ruolo con modalità differenti
Trasporto di O 2 nel sangue
 Trasporto di O 2 nel sangue Il 97% dell O 2 trasportato nel plasma è chimicamente legato all Hb nei globuli rossi, solo il 3% è fisicamente disciolto Trasporto O 2 nel plasma Trasporto O 2 legato ad Hb
Trasporto di O 2 nel sangue Il 97% dell O 2 trasportato nel plasma è chimicamente legato all Hb nei globuli rossi, solo il 3% è fisicamente disciolto Trasporto O 2 nel plasma Trasporto O 2 legato ad Hb
Emoglobina e mioglobina
 Emoglobina e mioglobina Per molti organismi, l O 2 è una molecola di importanza vitale: l'ossigeno è infatti l'accettore finale degli elettroni, che "fluendo" attraverso i complessi della catena respiratoria,
Emoglobina e mioglobina Per molti organismi, l O 2 è una molecola di importanza vitale: l'ossigeno è infatti l'accettore finale degli elettroni, che "fluendo" attraverso i complessi della catena respiratoria,
La classificazione dei lipidi
 La classificazione dei lipidi Concetti chiave Le proprietà fisiche di un acido grasso sono determinate dalla sua lunghezza e dal suo grado di saturazione. I triacilgliceroli e i glicerofosfolipidi contengono
La classificazione dei lipidi Concetti chiave Le proprietà fisiche di un acido grasso sono determinate dalla sua lunghezza e dal suo grado di saturazione. I triacilgliceroli e i glicerofosfolipidi contengono
α-cheratine (α-elica) collageni e cheratine β-cheratine (conformazione β) M.N. Gadaleta
 Per la scoperta delle conformazioni più comuni delle catene polipeptidiche cioè α-elica e β-conformazione è stato particolarmente importante lo studio delle cheratine, proteine fibrose, e l analisi della
Per la scoperta delle conformazioni più comuni delle catene polipeptidiche cioè α-elica e β-conformazione è stato particolarmente importante lo studio delle cheratine, proteine fibrose, e l analisi della
LIPIDI. Steroidi Acidi grassi Trigliceridi Fosfolipidi Prostaglandine Vitamine liposolubili
 LIPIDI Classe eterogenea di di sostanze organiche caratterizzate dal fatto di di non essere solubili in in acqua ma solubili in in solventi non polari aprotici. 1. 1. Acidi grassi 2. 2. Trigliceridi 3.
LIPIDI Classe eterogenea di di sostanze organiche caratterizzate dal fatto di di non essere solubili in in acqua ma solubili in in solventi non polari aprotici. 1. 1. Acidi grassi 2. 2. Trigliceridi 3.
I materiali della vita
 I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
Immagini e concetti della biologia
 Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
ENZIMI. A + B AB (100 Kcal= E. Attiv.) A + B AB (50 Kcal) SUBSTRATO ENZIMA E N E R G I A
 ENZIMI 1) sono catalizzatori di natura biologica e sono proteine 2) gli enzimi abbassano l energia di attivazione di un solo tipo di reazione senza intervenire nella reazione stessa cioè senza esserne
ENZIMI 1) sono catalizzatori di natura biologica e sono proteine 2) gli enzimi abbassano l energia di attivazione di un solo tipo di reazione senza intervenire nella reazione stessa cioè senza esserne
Le proteine che legano l ossigenol
 Le proteine che legano l ossigenol Protoporfirina IX EME (Fe-protoporfirina IX) L atomo di ferro del gruppo eme può formare sei legami Struttura della mioglobina di capodoglio (J. Kendrew, anni 50)
Le proteine che legano l ossigenol Protoporfirina IX EME (Fe-protoporfirina IX) L atomo di ferro del gruppo eme può formare sei legami Struttura della mioglobina di capodoglio (J. Kendrew, anni 50)
1/v
 1. Nel seguente grafico sono descritti i risultati di cinetica enzimatica ottenuti in 3 esperimenti condotti in assenza di inibitori e in presenza di un inibitore a due diverse concentrazioni. a) Individuare
1. Nel seguente grafico sono descritti i risultati di cinetica enzimatica ottenuti in 3 esperimenti condotti in assenza di inibitori e in presenza di un inibitore a due diverse concentrazioni. a) Individuare
Plasma membrane. Endoplasmic reticulum. Nucleus. Golgi apparatus. Mitochondrion Lysosome. Ribosome
 Endoplasmic reticulum Plasma membrane Nucleus Golgi apparatus Ribosome Mitochondrion Lysosome Funzioni 1- Compartimentazione 2- Localizzazione per attività biochimiche 3- Barriera selettiva 4- Trasporto
Endoplasmic reticulum Plasma membrane Nucleus Golgi apparatus Ribosome Mitochondrion Lysosome Funzioni 1- Compartimentazione 2- Localizzazione per attività biochimiche 3- Barriera selettiva 4- Trasporto
FUNZIONE DELLE PROTEINE RAPPORTO STRUTTURA-FUNZIONE
 FUNZIONE DELLE PROTEINE RAPPORTO STRUTTURA-FUNZIONE Principi basilari: 1.Le funzioni di molte proteine richiedono il legame reversibile con altre molecole (LIGANDO) Un ligando può essere di natura diversa,
FUNZIONE DELLE PROTEINE RAPPORTO STRUTTURA-FUNZIONE Principi basilari: 1.Le funzioni di molte proteine richiedono il legame reversibile con altre molecole (LIGANDO) Un ligando può essere di natura diversa,
Biologia. Lezione 09/11/2010
 Biologia Lezione 09/11/2010 Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono macromolecole formate da unità (MONOMERI)
Biologia Lezione 09/11/2010 Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono macromolecole formate da unità (MONOMERI)
LE PROTEINE DEL CONNETTIVO: IL COLLAGENO, L ELASTINA.
 UNITÀ BIOTEC. DIDATTICA DI BIOCHIMICA GENERALE LE PROTEINE DEL CONNETTIVO: IL COLLAGENO, L ELASTINA. Roberto Giacominelli Stuffler IL COLLAGENO 2 IL COLLAGENO E una famiglia di proteine fibrose con ruolo
UNITÀ BIOTEC. DIDATTICA DI BIOCHIMICA GENERALE LE PROTEINE DEL CONNETTIVO: IL COLLAGENO, L ELASTINA. Roberto Giacominelli Stuffler IL COLLAGENO 2 IL COLLAGENO E una famiglia di proteine fibrose con ruolo
LIPIDI. Classe eterogenea di di sostanze organiche caratterizzate dall essere insolubili in in acqua ma solubili in in solventi non polari aprotici
 LIPIDI Classe eterogenea di di sostanze organiche caratterizzate dall essere insolubili in in acqua ma solubili in in solventi non polari aprotici 1.Acidi grassi 2.Trigliceridi 3.Fosfolipidi 4.Prostaglandine
LIPIDI Classe eterogenea di di sostanze organiche caratterizzate dall essere insolubili in in acqua ma solubili in in solventi non polari aprotici 1.Acidi grassi 2.Trigliceridi 3.Fosfolipidi 4.Prostaglandine
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 10 Le basi della biochimica 3 Sommario 1. Le molecole biologiche si dividono in quattro classi 2. I carboidrati sono il «carburante»
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 10 Le basi della biochimica 3 Sommario 1. Le molecole biologiche si dividono in quattro classi 2. I carboidrati sono il «carburante»
scaricato da www.sunhope.it Proteine semplici costituite dai soli amminoacidi
 Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
le porzioni con strutture secondarie sono avvicinate e impaccate mediante anse e curve della catena. STRUTTURA TERZIARIA
 STRUTTURA TERZIARIA le porzioni con strutture secondarie sono avvicinate e impaccate mediante anse e curve della catena. Le proteine globulari dopo aver organizzato il proprio scheletro polipeptidico con
STRUTTURA TERZIARIA le porzioni con strutture secondarie sono avvicinate e impaccate mediante anse e curve della catena. Le proteine globulari dopo aver organizzato il proprio scheletro polipeptidico con
Il trasporto del glucosio
 Il trasporto del glucosio Il glucosio non può diffondere direttamente nelle cellule Esso entra nelle cellule mediante due meccanismi di trasporto: a) diffusione facilitata Na + indipendente b) co-trasporto
Il trasporto del glucosio Il glucosio non può diffondere direttamente nelle cellule Esso entra nelle cellule mediante due meccanismi di trasporto: a) diffusione facilitata Na + indipendente b) co-trasporto
Biologia generale Robert J. Brooker, Eric P. Widmaier, Linda E. Graham, Peter D. Stiling Copyright 2009 The McGraw-Hill Companies srl
 RISPOSTE AGLI SPUNTI DI RIFLESSIONE Figura 5.4 Capitolo 5 RISPOSTA : La bassa temperatura impedisce la diffusione laterale delle proteine di membrane. Quindi, dopo la fusione, tutte le proteine di topo
RISPOSTE AGLI SPUNTI DI RIFLESSIONE Figura 5.4 Capitolo 5 RISPOSTA : La bassa temperatura impedisce la diffusione laterale delle proteine di membrane. Quindi, dopo la fusione, tutte le proteine di topo
Composti organici. I composti organici. Atomi e molecole di carbonio. Atomi e molecole di carbonio. Gruppi funzionali. Isomeri
 I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
Il metalloma Struttura e reattività di metalloproteine. Il trasporto dell O 2
 Il metalloma Struttura e reattività di metalloproteine Il trasporto dell O 2 Il trasporto dell ossigeno Nel sangue la solubilità dell O 2 è molto maggiore che in H 2 O In H 2 O la solubilità è 6.59 cm
Il metalloma Struttura e reattività di metalloproteine Il trasporto dell O 2 Il trasporto dell ossigeno Nel sangue la solubilità dell O 2 è molto maggiore che in H 2 O In H 2 O la solubilità è 6.59 cm
SOLUZIONI DEGLI ESERCIZI
 Dal carbonio agli OGM Biochimica e biotecnologie SOLUZIONI DEGLI ESERCIZI Capitolo 0 Il mondo del carbonio 1. b, e 2. d 3. 7 4. 5. 6. 7. a) Isomeria di posizione; b) i due composti non sono isomeri; c)
Dal carbonio agli OGM Biochimica e biotecnologie SOLUZIONI DEGLI ESERCIZI Capitolo 0 Il mondo del carbonio 1. b, e 2. d 3. 7 4. 5. 6. 7. a) Isomeria di posizione; b) i due composti non sono isomeri; c)
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA)
 La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) L atomo del carbonio (C).. C. Atomo tetravalente. C C C C Gli idrocarburi I legami del carbonio 109.5 gradi
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) L atomo del carbonio (C).. C. Atomo tetravalente. C C C C Gli idrocarburi I legami del carbonio 109.5 gradi
MOLECOLE. 2 - i legami chimici. Prof. Vittoria Patti
 MOLECOLE 2 - i legami chimici Prof. Vittoria Patti Gli stati di aggregazione della materia STATO SOLIDO molecole ravvicinate, struttura ordinata, volume proprio, forma propria STATO LIQUIDO molecole
MOLECOLE 2 - i legami chimici Prof. Vittoria Patti Gli stati di aggregazione della materia STATO SOLIDO molecole ravvicinate, struttura ordinata, volume proprio, forma propria STATO LIQUIDO molecole
30/10/2015 LIVELLI DI ORGANIZZAZIONE STRUTTURALE DELLE PROTEINE
 LIVELLI DI ORGANIZZAZIONE STRUTTURALE DELLE PROTEINE 1 CARATTERISTICHE DEL LEGAME PEPTIDICO lunghezza intermedia tra un legame singolo e uno doppio ibrido di risonanza per il parziale carattere di doppio
LIVELLI DI ORGANIZZAZIONE STRUTTURALE DELLE PROTEINE 1 CARATTERISTICHE DEL LEGAME PEPTIDICO lunghezza intermedia tra un legame singolo e uno doppio ibrido di risonanza per il parziale carattere di doppio
Mioglobina ed emoglobina
 Mioglobina ed emoglobina α β Muscolo Deposito di O 2 Alta affinità per O 2 β α Globulo rosso Trasporto di O 2 Bassa affinità per O 2 Cooperativa ed allosterica Animali Mb-knockout (2003) : funzionalità
Mioglobina ed emoglobina α β Muscolo Deposito di O 2 Alta affinità per O 2 β α Globulo rosso Trasporto di O 2 Bassa affinità per O 2 Cooperativa ed allosterica Animali Mb-knockout (2003) : funzionalità
LA MEMBRANA CELLULARE O PLASMATICA E LA STRUTTURA CHE DELIMITA ESTERNAMENTE LA CELLULA, SIA EUCARIOTICA CHE PROCARIOTICA, SEPARANDO IL COMPARTO INTRAC
 MEMBRANA CELLULARE LA MEMBRANA CELLULARE O PLASMATICA E LA STRUTTURA CHE DELIMITA ESTERNAMENTE LA CELLULA, SIA EUCARIOTICA CHE PROCARIOTICA, SEPARANDO IL COMPARTO INTRACELLULARE DA QUELLO EXTRACELLULARE.
MEMBRANA CELLULARE LA MEMBRANA CELLULARE O PLASMATICA E LA STRUTTURA CHE DELIMITA ESTERNAMENTE LA CELLULA, SIA EUCARIOTICA CHE PROCARIOTICA, SEPARANDO IL COMPARTO INTRACELLULARE DA QUELLO EXTRACELLULARE.
Formazione. di un peptide.
 Formazione. di un peptide. Quando due aminoacidi si uniscono si forma un legame peptidico. In questo caso il dipeptide glicilalanina (Gly-Ala) viene mostrato come se si stesse formando in seguito a eliminazione
Formazione. di un peptide. Quando due aminoacidi si uniscono si forma un legame peptidico. In questo caso il dipeptide glicilalanina (Gly-Ala) viene mostrato come se si stesse formando in seguito a eliminazione
Regolano il metabolismo, sia come enzimi, sia come ormoni (insulina, glucagone, ecc.)
 Grazie alla elevata dinamicità delle strutture proteiche (gli atomi sono in continuo movimento fluttuante) e per la capacità che hanno di legarsi in modo selettivo ad altre molecole, le proteine svolgono
Grazie alla elevata dinamicità delle strutture proteiche (gli atomi sono in continuo movimento fluttuante) e per la capacità che hanno di legarsi in modo selettivo ad altre molecole, le proteine svolgono
Proprieta dei lipidi
 I LIPIDI 1 Proprieta dei lipidi Alta variabilita strutturale Non sono polimeri (cfr. acidi.nucl., proteine, polisaccaridi) Scarsa solubilita in acqua (estratti in fase organica) Presenti in olii & grassi
I LIPIDI 1 Proprieta dei lipidi Alta variabilita strutturale Non sono polimeri (cfr. acidi.nucl., proteine, polisaccaridi) Scarsa solubilita in acqua (estratti in fase organica) Presenti in olii & grassi
LIPIDI. I lipidi sono suddivisi in due gruppi principali.
 LIPIDI I lipidi sono una classe eterogenea di composti organici, raggruppati sulla base della loro solubilità. Sono insolubili in acqua, ma solubili nei solventi organici non polari, quali l etere dietilico,
LIPIDI I lipidi sono una classe eterogenea di composti organici, raggruppati sulla base della loro solubilità. Sono insolubili in acqua, ma solubili nei solventi organici non polari, quali l etere dietilico,
Lipidi e Micelle. Francesca Anna Scaramuzzo, PhD
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica Organica e Biochimica Lipidi e Micelle Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate per l Ingegneria
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica Organica e Biochimica Lipidi e Micelle Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate per l Ingegneria
LIPIDI. Costituenti basilari dei lipidi sono gli ACIDI GRASSI
 LIPIDI Riserve energetiche (trigliceridi), sono molecole più ridotte rispetto agli zuccheri e dalla loro ossidazione viene liberata una quantità di energia maggiore. Costituzione delle membrane biologiche
LIPIDI Riserve energetiche (trigliceridi), sono molecole più ridotte rispetto agli zuccheri e dalla loro ossidazione viene liberata una quantità di energia maggiore. Costituzione delle membrane biologiche
Trasporto di membrana
 Trasporto di membrana CdL Tecnici di Lab Biomedico AA. 2011/12 Prof.ssa Frabetti Trasporto di membrana molecole piccole molecole grosse trasporto passivo trasporto attivo (con pompe o cotrasportatori)
Trasporto di membrana CdL Tecnici di Lab Biomedico AA. 2011/12 Prof.ssa Frabetti Trasporto di membrana molecole piccole molecole grosse trasporto passivo trasporto attivo (con pompe o cotrasportatori)
Lipidi Semplici: Gliceridi (Mono, Di e Trigliceridi; esteri del GLICEROLO con Ac. Grassi a lunga catena). CERE
 I lipidi sono un gruppo eterogeneo di sostanze. Essi sono caratterizzati dalla insolubilità in acqua (o scarsa solubilità) e dalla affinità per i solventi apolari e per gli altri lipidi (natura fortemente
I lipidi sono un gruppo eterogeneo di sostanze. Essi sono caratterizzati dalla insolubilità in acqua (o scarsa solubilità) e dalla affinità per i solventi apolari e per gli altri lipidi (natura fortemente
Ioni inorganici (Mg 2+, Zn 2+ ), o molecole organiche o metallorganiche (coenzimi)
 ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO
 L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 23 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata all emoglobina: L O 2 totale
L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 23 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata all emoglobina: L O 2 totale
Digestione e assorbimento dei lipidi. β-ossidazione degli acidi grassi
 Digestione e assorbimento dei lipidi β-ossidazione degli acidi grassi I grassi della dieta sono assorbiti nell intestino tenue Il diametro della particella dei chilomicroni varia da circa 100 a circa 500
Digestione e assorbimento dei lipidi β-ossidazione degli acidi grassi I grassi della dieta sono assorbiti nell intestino tenue Il diametro della particella dei chilomicroni varia da circa 100 a circa 500
REGOLAZIONE ENZIMATICA
 REGOLAZIONE ENZIMATICA Cambio conformazionale In molte molecole proteiche, cambiamenti strutturali possono determinare profondi cambiamenti nella funzione o nell attività. Il cambio conformazionale può
REGOLAZIONE ENZIMATICA Cambio conformazionale In molte molecole proteiche, cambiamenti strutturali possono determinare profondi cambiamenti nella funzione o nell attività. Il cambio conformazionale può
Chimica Biologica A.A Cinetica Enzimatica. Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano
 Chimica Biologica A.A. 2010-2011 Cinetica Enzimatica Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Cinetica Chimica Termodinamica: fornisce
Chimica Biologica A.A. 2010-2011 Cinetica Enzimatica Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Cinetica Chimica Termodinamica: fornisce
LA CHIMICA DELLA VITA
 LA CHIMICA DELLA VITA L elemento presente in tutte le molecole caratteristiche degli esseri viventi è IL CARBONIO Il carbonio ha numero atomico 6 (Z=6). Ha valenza 4: ai suoi atomi mancano 4 elettroni
LA CHIMICA DELLA VITA L elemento presente in tutte le molecole caratteristiche degli esseri viventi è IL CARBONIO Il carbonio ha numero atomico 6 (Z=6). Ha valenza 4: ai suoi atomi mancano 4 elettroni
costruire un equazione che potesse descrivere in generale il comportamento cinetico degli enzimi e quindi di determinare parametri cinetici più
 Cinetica Enzimatica OBIETTIVO PRINCIPALE: costruire un equazione che potesse descrivere in generale il comportamento cinetico degli enzimi e quindi di determinare parametri cinetici più importanti (K M,
Cinetica Enzimatica OBIETTIVO PRINCIPALE: costruire un equazione che potesse descrivere in generale il comportamento cinetico degli enzimi e quindi di determinare parametri cinetici più importanti (K M,
Regolazione allosterica
 Macromolecole Biologiche Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Regolazione allosterica Marco Nardini Dipartimento
Macromolecole Biologiche Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Regolazione allosterica Marco Nardini Dipartimento
Lezione 1: Atomi e molecole:
 Lezione 1: Atomi e molecole: La materia è costituita da elementi chimici in forma pura o in combinazioni dette composti. La vita richiede circa 25 elementi chimici. La struttura atomica determina il comportamento
Lezione 1: Atomi e molecole: La materia è costituita da elementi chimici in forma pura o in combinazioni dette composti. La vita richiede circa 25 elementi chimici. La struttura atomica determina il comportamento
Lipidi: funzioni. Strutturale. Riserva energetica. Segnale.
 Lipidi: funzioni. Strutturale. Riserva energetica. Segnale. Lipidi:classificazione. Saponificabili Non saponificabili Semplici Complessi Prostaglandine Steroidi Cere Trigliceridi Fosfogliceridi Sfingolipidi
Lipidi: funzioni. Strutturale. Riserva energetica. Segnale. Lipidi:classificazione. Saponificabili Non saponificabili Semplici Complessi Prostaglandine Steroidi Cere Trigliceridi Fosfogliceridi Sfingolipidi
Gerard Tortora, Brian Derrickson. Conosciamo
 1 Gerard Tortora, Brian Derrickson Conosciamo il corpo umano Capitolo 1 L organizzazione del corpo umano 1. Che cosa sono l anatomia e la fisiologia 2. I livelli di organizzazione e gli apparati del corpo
1 Gerard Tortora, Brian Derrickson Conosciamo il corpo umano Capitolo 1 L organizzazione del corpo umano 1. Che cosa sono l anatomia e la fisiologia 2. I livelli di organizzazione e gli apparati del corpo
- CINETICA ENZIMATICA
 - CINETICA ENZIMATICA ENZIMI: - CATALIZZATORI aumenta la V di una reazione chimica senza subire trasformazioni durante l intero processo - PROTEINE gli enzimi sono proteine di struttura 3 o talora 4 -
- CINETICA ENZIMATICA ENZIMI: - CATALIZZATORI aumenta la V di una reazione chimica senza subire trasformazioni durante l intero processo - PROTEINE gli enzimi sono proteine di struttura 3 o talora 4 -
30/10/2015. Molte proteine sono. intrinsecamente disordinate. o destrutturate (IDP/IUP), cioè non hanno una struttura
 Molte proteine sono intrinsecamente disordinate o destrutturate (IDP/IUP), cioè non hanno una struttura terziaria e/o secondaria stabile. Le IUP sono caratterizzate da - scarso contenuto in aa apolari,
Molte proteine sono intrinsecamente disordinate o destrutturate (IDP/IUP), cioè non hanno una struttura terziaria e/o secondaria stabile. Le IUP sono caratterizzate da - scarso contenuto in aa apolari,
Ogni globina ha una tasca in cui lega un gruppo EME, quindi l Hb può legare e trasportare 4 molecole di O 2
 Emoglobina (Hb): tetramero (le globine si associano formando due copie di dimeri αβ (α 1 β 1 e α 2 β 2 ) che si associano a formare un tetramero attraverso interazioni idrofobiche, legami H e ponti salini
Emoglobina (Hb): tetramero (le globine si associano formando due copie di dimeri αβ (α 1 β 1 e α 2 β 2 ) che si associano a formare un tetramero attraverso interazioni idrofobiche, legami H e ponti salini
