delegate a conservare e trasmettere l'informazione genetica. Oggi é noto che sono gli acidi
|
|
|
- Gabriela Donati
- 7 anni fa
- Visualizzazioni
Transcript
1 8. Le proteine Il termine "proteina" (dal greco προτειος: di primaria importanza) fu coniato nel 1838 dal chimico svedese J. Berzelius 1 quando ancora si riteneva che le proteine fossero le molecole delegate a conservare e trasmettere l'informazione genetica. Oggi é noto che sono gli acidi nucleici a svolgere queste funzioni, ma il significato etimologico della parola rimane ancora valido. Le proteine hanno, infatti, un ruolo fondamentale praticamente in tutti i processi biologici. All'inizio del Capitolo 6 abbiamo accennato alle molte diverse funzioni biologiche svolte dalle proteine, vogliamo darne qui una grossolana classificazione. 1. Catalisi Enzimatica: le proteine (in questo contesto sono dette enzimi) sono in grado di far crescere (fino a qualche ordine di grandezza) la velocità di una reazione. 2. Trasporto e Deposito: alcune proteine svolgono il ruolo di trasportatori di ioni o piccole molecole. Tra gli esempi più importanti l'emoglobina (Hb) e la mioglobina (Mb) che sono i trasportatori dell'ossigeno, rispettivamente negli eritrociti e nei muscoli o la transferrina che si occupa del trasporto di ferro nel plasma. 3. Movimento: proteine come la miosina e l'actina sono fondamentali nel processo di contrazione muscolare, così come é dovuto all'azione di specifiche proteine il processo di segregazione dei cromosomi durante la mitosi. 4. Sostegno meccanico: un esempio di proteina che svolge questa funzione é il collagene che dà elasticità e resistenza a pelle ed ossa. 1 Vedi nota 3, Capitolo
2 5. Protezione immunitaria: gli anticorpi, che giocano un ruolo fondamentale nel processo di difesa degli organismi superiori dall'aggressione di agenti estranei e patogeni, sono proteine. 6. Produzione e trasmissione degli impulsi nervosi.: alcune particolari proteine sono mediatrici della risposta nervosa cellulare. Per esempio la rodopsina che é un fotorecettore proteico localizzato nei bastoncelli; o l'acetilcolina che é un mediatore della trasmissione degli impulsi nervosi attraverso le sinapsi (le giunzioni tra cellule nervose). 7. Controllo della crescita e del differenziamento: negli organismi superiori la crescita e il differenziamento sono controllati da fattori di crescita proteici. 8. Interazione con l'ambiente: sensori proteici controllano, in tutte le cellule, il flusso di energia e di materia. 9. etc. 8.1 Gli aminoacidi Le unità monomeriche con le quali sono costruiti i polimeri lineari che costituiscono le proteine sono gli amino acidi. Un amino acido consiste di un gruppo aminico, NH 2, un gruppo carbossilico, COOH, un atomo di idrogeno, H, e un gruppo, R, detto catena laterale che é diversa per ciascuno dei 20 amino acidi che costituiscono il repertorio 2. Tutti e tre questi gruppi sono legati ad un atomo di carbonio, il cosiddetto carbonio α (vedi Figura 8.1). 2 Venti sono gli aminoacidi di gran lunga più comuni. Anche se raramente si trovano aminoacidi chimicamente diversi dai venti principali. 146
3 Figura 8.1 Come mostrato in Figura gli amino acidi, a ph neutro, sono generalmente ioni bipolari (o zwitterioni) con il gruppo aminico protonato (-NH + 3 ) e il gruppo carbossilico dissociato (- COO - ). Naturalmente lo stato di ionizzazione dell'amino acido varia con il ph. In una soluzione fortemente acida, ph 1, il gruppo carbossilico non é dissociato, mentre il gruppo Valori di pk Amino acido α-coo - α-nh 3 + Alanina Arginina Acido Aspartico Asparagina Cisteina Acido Glutamico Glutamina Glicina Istidina Isoleucina Leucina Lisina Metionina Fenilalanina Prolina Serina Treonina Triptofano Tirosina Valina Tabella
4 aminico é protonato, viceversa in una soluzione fortemente alcalina, ph 11, il gruppo carbossilico é dissociato mentre il gruppo aminico é neutro. Il pk 3 di ionizzazione di un gruppo amino acido massa 4 Superficie Volume pk 5 pi 6 solubilità 7 densità 8 Alanina ALA A Arginina ARG R ~ Acido Aspartico ASP D Asparagina ASN N Cisteina CYS C very high - Acido Glutamico GLU E Glutamina GLN Q Glicina GLY G Istidina HIS H Isoleucina ILE I Leucina LEU L Lisina LYS K very high - 3 Il pk é il valore di ph per il quale un gruppo dissociabile é per metà dissociato. Per maggiori dettagli sulla definizione di pk e di curva di titolazione si veda per esempio: 4 La massa é in dalton; la superficie in Å 2 (C.Chothia, J. Mol. Biol., 105(1975)1-14) il volume in Å 3 (A.A. Zamyatin, Prog. Biophys. Mol. Biol., 24(1972) ). 5 Il pk si riferisce alle catene laterali (C. Tanford, Adv. Prot. Chem., 17(1962)69-165). 6 Il pi (punto isoelettrico) é misurato a 25 C (The Merck Index, Merck & Co. Inc., Nahway, N.J., 11(1989); CRC Handbook of Chem.& Phys., Cleveland, Ohio, 58(1977). 7 La solubilità é definita per g su 100g a 25 C (The Merck Index, Merck & Co. Inc., Nahway, N.J., 11(1989); CRC Handbook of Chem.& Phys., Cleveland, Ohio, 58(1977). 8 La densità é quella del cristallo in g/ml (The Merck Index, Merck & Co. Inc., Nahway, N.J., 11(1989); CRC Handbook of Chem.& Phys., Cleveland, Ohio, 58(1977). 148
5 Metionina MET M Fenilalanina PHE F Prolina PRO P Serina SER S Treonina THR T very high - Triptofano TRP W Tirosina TYR Y Valina VAL V Tabella 8.2 chimico dipende dal contesto in cui esso si trova, in particolare per i due terminali amino acidici il pk varia da amino acido a amino acido anche nel caso di amino acidi isolati (vedi Tabella 8.1). A causa del fatto che il valore del pk di dissociazione delle catene laterali dipende dal contesto chimico, la curva di titolazione di una proteina può dare indicazioni sulla localizzazione spaziale dell'amino acido nella proteina e, in ultima analisi, sulla struttura di quest'ultima. In Tabella 8.2 sono riportati i pk delle catene laterali degli amino acidi isolati, mentre la Tabella sono messi a confronto i pk dei gruppi dissociabili di alcuni amino acidi localizzati in proteine (e quindi in contesti chimici) diverse. Gruppo Proteina pk Acido aspartico e acido glutammico Istidina Seroalbumina Insulina Da: C.R.Cantor & P.R.Schimmel: "Biophysical Chemistry" W.H.Freeman and Company 149
6 Tirosina Lisina β-lactoglobulina Lisozima Insulina Seroalbumina Insulina Seroalbumina Seroalbumina Lisozima Tabella Le proprietà fisico-chimiche dei 20 principali residui amino acidici dipendono dalla composizione chimica delle loro catene laterali (indicate genericamente con R in Figura 8.1). Nelle figure che seguono gli amino acidi sono raggruppati in base ad alcune caratteristiche chimiche in: 1. Amino acidi non polari (Figura 8.2): Alanina (Ala, A); Isoleucina (Ile, I), Leucina (Leu, L), Valina (Val, V), Metionina (Met, M), Prolina (Pro, P), Fenilalanina (Phe, F), Triptofano (Trp, W) e Glicina (Gly, G). Due amino acidi di questo gruppo sono considerati speciali: la Glicina e la Prolina. La Glicina, a causa del fatto che la sua 150
7 Figura 8.2 catena laterale é costituita da un solo atomo di idrogeno, é spesso presente in regioni della catena polipeptidica dove sia richiesta un'elevata flessibilità. La Prolina non è propriamente un amino acido perché la sua catena laterale si richiude sulla catena principale, vincolando uno dei due gradi di libertà rotazionale. Questo implica che la presenza di Prolina impedisca la formazione di α-elica. 2. Amino acidi polari dissociabili (Figura 8.3): Asparagina (Asn, N), Cisteina (Cys, C), Glutamina (Gln, Q), Serina (Ser, S), Treonina (Thr, T) e Tirosina (Tyr, Y). In presenza di un numero pari di Cisteine, si formano quasi sempre ponti disolfuro. Questa struttura é così comune che il complesso Cys-S-S-Cys é detto Cistina, come se si trattasse del 21-esimo amino acido. 3. Amino acidi carichi (Figura 8.4): cinque amino acidi esibiscono una carica netta nelle loro catene laterali. Acido aspartico o Aspartato (Asp, D) e Acido Glutammico o Glutammato (Glu, E) hanno una carica netta negativa, mentre Arginina (Arg, R), Istidina (His, H) e Lisina (Lys, K) hanno una carica netta positiva 151
8 Figura 8.3 Figura 8.4 Come detto, la Glicina é l'amino acido più semplice poiché la sua catena laterale é costituita solo da un atomo di idrogeno ed é l'unico aminoacido in cui il C α é simmetrico. Nell'Alanina la catena laterale é costituita da un gruppo metilico. Valina, Leucina e Isoleucina hanno catene laterali più lunghe costituite da idrocarburi 10. Queste grosse catene laterali alifatiche sono fortemente idrofobiche. La Prolina, pur avendo anch'essa una catena laterale alifatica, si differenzia dagli altri perché ha un gruppo iminico al posto del gruppo aminico ed é quindi detta iminoacido. La Fenilalanina, il Triptofano e la Tirosina hanno catene laterali 10 Si dicono idrocarburi quelle sostanze organiche alifatiche (atomi di carbonio legati tra loro in catena lineare o ramificata) o aromatiche (composti chimici che fanno capo al benzene in cui gli elettroni sono delocalizzati) che contengono solo carboni e idrogeni. 152
9 aromatiche, ma la presenza di un gruppo ossidrile, -OH, dissociabile rende la Tirosina meno idrofobica delle altre due. Il Triptofano ha un anello indolico 11 unito ad un gruppo metilenico (CH 2 ). Due aminoacidi contengono zolfo nelle loro catene laterali, la Cisteina e la Metionina, entrambe le loro catene laterali sono idrofobiche. Il gruppo sulfidrilico (-SH) della cisteina é altamente reattivo e, come vedremo, ha una grande importanza strutturale. Due amino acidi, Serina e Treonina, contengono gruppi ossidrilici. La Serina può essere considerata come una versione idrossilata della Alanina e la Treonina della Valina. La presenza degli ossidrili rende i due aminoacidi idrofilici. Alcuni amino acidi sono altamente idrofilici per la presenza di catene laterali cariche o dissociabili a ph fisiologici. Lisina e Arginina sono cariche positivamente a ph neutro, mentre l'istidina può essere o no carica positivamente (vedi Tabella 8.2). Acido aspartico o Aspartato e Acido glutammico o glutammato hanno catene laterali cariche negativamente. Da questi due provengono due derivati neutri, Aspargina e Glutammina in cui il gruppo carbossilico (-COOH) é rimpiazzato da un gruppo aminico (NH 2 ) (vedi Figure 8.3 e 8.4). 8.2 Il legame peptidico e i polipeptidi. Gli amino acidi nelle catene proteiche formano un legame tra il gruppo carbossilico di un aminoacido e il gruppo aminico dell'amino acido che segue (Figura 8.5). 11 L'indolo é un composto organico eterociclico formato da un anello benzenico e uno pirrolico. 153
10 Figura 8.5 Tale legame é detto peptidico, e le catene proteiche sono dette catene polipeptidiche (Figura 8.6). Figura 8.6 Come mostrato nella Figura 8.5, la formazione di un dipeptide avviene con la produzione di una molecola d'acqua. L'equilibrio della reazione, in ambiente acquoso, é spostato verso l'idrolisi, per cui la biosintesi richiede energia. Per ragioni legate al meccanismo direzionale di sintesi, il gruppo aminico é considerato l'inizio della catena e il gruppo carbossilico la fine della catena. Gli aminoacidi della catena sono detti residui. Gli aminoacidi presenti nelle proteine sono tutti α-amino-α-carbossilici, con ciò intendendo che il gruppo aminico é legato al carbonio adiacente al gruppo carbossilico acido, detto carbonio α (C α ). 154
11 Tutti gli aminoacidi, con esclusione della Glicina in cui il C α é simmetrico, hanno una chiralità definita 12, che può essere rivelata con esperimenti di dicroismo circolare. Sono in linea di principio possibili entrambe le forme speculari (enanziomeri o stereoisomeri) di organizzazione degli atomi attorno al C α (vedi Figura 8.7) che sono dette isomero L (o levogiro) e isomero D (o destrogiro). Lo steroisomero naturale di origine biologica é la configurazione L. Infatti, sebbene siano stati occasionalmente trovati gli steroisomeri D, i ribosomi non sono in grado di utilizzarli nella sintesi. Figura 8.7 La presenza di queste regolarità (come per esempio l'essere gli aminoacidi tutti α-amino-αcarbossilici e levogiri) condivise da organismi geneticamente ed evolutivamente molto distanti tra loro, non é sempre giustificabile con meccanismi di evoluzione basati sulla selezione del più adatto. Analizziamo alcuni esempi di regolarità illustrando alcune ipotesi formulate sulle ragioni della loro insorgenza. 1. Tutti gli esseri viventi (a parte qualche rarissima eccezione) usano lo stesso insieme di 20 a.a. 12 Una molecola "chirale" è una molecola che non é sovrapponibile alla sua immagine speculare, come la mano destra e la mano sinistra. 155
12 La spiegazione di questa regolarità é da ricercarsi nel fatto che la produzione di proteine passa attraverso un processo di "traduzione" di una sequenza nucleotidica in una sequenza amino acidica durante il quale si utilizza il cosiddetto Codice Genetico (vedi Fig 7.4, cap. 7). Questo, come si é visto, é un codice a triplette che consentirebbe teoricamente la codifica di 64 a.a.. Il codice genetico é, quindi, ridondante (alcuni aminoacidi sono codificati da più di una tripletta). L'ipotesi più attendibile é che il sistema di traduzione abbia subito un processo evolutivo dalle doppiette alle triplette. Tale ipotesi é sostenuta, fra l'altro, dalla forte degenerazione della terza posizione nel codone. La terza base della tripletta é infatti spesso indifferente 13. L'evoluzione verso un codice a triplette può essere inoltre riconducibile al meccanismo chimico mediante il quale avviene la traduzione. Infatt,i poiché é cruciale che l'associazione della sequenza nucleotidica dell'mrna con il trna mediante accoppiamento delle basi sia altamente specifica, é probabile che la doppietta non fornisse una costante di associazione sufficientemente grande da garantire la necessaria specificità. Si è probabilmente passati da un codice a due basi ad uno a tre altamente degenere e, in un secondo momento, la degenerazione é stata parzialmente rimossa con l'aumento del numero di amino acidi codificati. Inoltre, in alcuni casi si osserva che aminoacidi che condividono alcuni passi del processo metabolico di sintesi hanno spesso triplette codificanti molto simili tra loro che suggerisce una coevoluzione di codice genetico e metabolismo Osservando il codice in Fig.7.4 si vede che molti amino acidi sono, in pratica, codificati da una doppietta e da una terza base qualsiasi. Per esempio: Serina, UCx (x=aminoacido qualsiasi); Leucina, CUx; Prolina, CCx; Arginina, CGx; etc. 14 Recentemente é stata proposta una spiegazione più fondamentale dell'esistenza di un codice a triplette, basata sull'idea che la sintesi proteica avvenga secondo le leggi del "Quantum Computing". L'ipotesi é suggestiva e, almeno in parte, sostenuta da dati sperimentali, ma, per adesso é lungi dall'essere universalmente accettata. Chi fosse curioso di conoscere di più sull'argomento può leggere: A.Patel "Why genetic information processing could have a quantum basis." (2001) J Biosci. 26(2):145-51; un altro lavoro si può trovare sul sito 156
13 2. Gli amino acidi di origine biologica sono prodotti tutti nella forma levogira. Si ritiene che questo sia semplicemente dovuto al fatto che l'efficienza e la competitività rispetto alla selezione della "macchina" che presiede alla sintesi delle proteine richiede che ci sia una configurazione standard degli amino acidi. La selezione di uno steroisomero rispetto all'altro é stata, con ogni probabilità casuale. Non ci sono infatti ragioni ovvie per preferire uno steroisomero rispetto alla sua immagine speculare. Probabilmente i due sistemi si sono sviluppati in parallelo e il sitema L ha "vinto" la competizione solo a causa di fluttuazioni casuali che lo hanno portato ad emergere numericamente 15. Figura Questo é un tipico esempio di evoluzione alla Eigen (Eigen M. and P. Schuster. (1979)"The Hypercycle: A principle of natural self-organization", Springer, Berlin.). 157
14 Una volta diventata prevalente, però, una modalità di per sè non rilevante come quella della chiralità può determinare conseguenze secondarie inaspettate. É probabile che la peculiarità che tutti gli aminoacidi naturali sono levogiri sia all'origine di un effetto biologico drammatico come quello del Talidomide. Il Talidomide (α-ftalimidoglutarimide) é una molecola chirale (vedi Figura 8.8). Il farmaco veniva prodotto in soluzione racemica con una proporzione (1:1) tra enanziomero D e L. Il Talidomide venne prodotto come farmaco calmante e specialmente indicato per i disturbi del sonno in gravidanza. Le conseguenze della somministrazione di Talidomide alle donne in gravidanza é considerato uno dei più gravi disastri farmacologici dello scorso secolo (l'uso massiccio risale agli anni '60). Infatti, il farmaco, somministrato nei primi tre mesi di gravidanza impediva il corretto sviluppo del feto (effetto teratogeno) provocando gravi malformazioni (quali la focomelia). Si scoprì che solo l'enanziomero D aveva effetti calmanti, mentre l'enanziomero L aveva effetti teratogeni. 3. Gli aminoacidi di origine biologica sono tutti nella forma α-amino-α-carbossilia. Se si compiono degli esperimenti alla Miller (vedi Capitolo 2, paragrafo 5) si ottiene una soluzione racemica 16 di aminoacidi che contiene, in proporzioni comparabili, amino acidi di tipo α e di tipo β (vedi Figura 8.9). Con aminoacidi di tipo β si intendono indicare quegli amino acidi in cui il primo atomo di carbonio della catena laterale (il cosiddetto C β ), presente in tutti gli amino acidi a parte la Glicina (vedi Figure 8.2, 8.3 e 8.4), appartenente alla 16 Si dice racemica una soluzione in cui sono presenti in egual proporzione gli stereoisomeri L e D. 158
15 Figura 8.9 catena principale. Per molti aspetti gli aminoacidi β sono assolutamente equivalenti a quelli α (lo dimostra il fatto che la produzione inorganica di aminoacidi produce in proporzioni comparabili aminoacidi di tipo α e di tipo β). Vediamo però che tra le due forme esiste una differenza sostanziale. Nel legame peptidico, come mostrato in Figura 8.10, tra CO e NH si forma quello che i chimici definiscono parziale doppio legame. Questo comporta che 159
16 Figura 8.10 la rotazione intorno al legame CO-NH non sia libera come quella intorno ai legami semplici che vi sono tra C α e CO e tra C α e NH (Fig. 8.11). Ogni aminoacido, in configurazione α provvede quindi due gradi di libertà torsionali lungo la catena polipetidica. Nella configurazione β ogni amino acido acquisisce un ulteriore grado di libertà dovuto alla possibile rotazione intorno legame semplice C α - C β. Tale maggiore flessibilità rende la possibilità di un "folding" spontaneo altamente improbabile 17, con ciò giustificando il processo di evoluzione che ha selezionato gli aminoacidi della forma α. É noto infatti che il processo di folding, mediante il quale la catena polipeptidica si avvolge (to fold) per arrivare alla struttura tridimensionale che ne determinerà la specificità funzionale, 17 Vedi Approfondimento A12 160
17 Figura 8.11 può essere aiutato da altre proteine (le cosiddette chaperonine). Tuttavia esso può avvenire, e in molti casi avviene, anche in modo spontaneo (in assenza cioè di fonti di energia esterne e/o con mediazione di altri enzimi). É ragionevolmente ipotizzabile che, nella fase iniziale di formazione e selezione delle prime strutture proteiche, la possibilità del folding spontaneo sia stata un elemento selettivo decisivo. 161
delegate a conservare e trasmettere l'informazione genetica. Oggi é noto che sono gli acidi
 8. Le proteine Il termine "proteina" (dal greco προτειος: di primaria importanza) fu coniato nel 1838 dal chimico svedese J. Berzelius 1 quando ancora si riteneva che le proteine fossero le molecole delegate
8. Le proteine Il termine "proteina" (dal greco προτειος: di primaria importanza) fu coniato nel 1838 dal chimico svedese J. Berzelius 1 quando ancora si riteneva che le proteine fossero le molecole delegate
Struttura degli amminoacidi
 AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
Struttura delle Proteine
 Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
α-amminoacidi O α O α R CH C O - NH 3 forma ionizzata sale interno (zwitterione) OH NH 2 forma non ionizzata (non esistente in realtà)
 Amminoacidi 2 forma non ionizzata (non esistente in realtà) 3 forma ionizzata sale interno (zwitterione) In soluzione acquosa c'è equilibrio tra tre forme 3 forma cationica p molto acidi 3 forma zwitterionica
Amminoacidi 2 forma non ionizzata (non esistente in realtà) 3 forma ionizzata sale interno (zwitterione) In soluzione acquosa c'è equilibrio tra tre forme 3 forma cationica p molto acidi 3 forma zwitterionica
Amminoacidi. Struttura base di un a-amminoacido
 Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
MACROMOLECOLE. Polimeri (lipidi a parte)
 MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente
 Gli amminoacidi naturali sono α-amminoacidi : il gruppo amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente formula generale: gruppo funzionale carbossilico
Gli amminoacidi naturali sono α-amminoacidi : il gruppo amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente formula generale: gruppo funzionale carbossilico
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH
 Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( OO) nella stessa molecola 3 N 2 α * OO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-himica Organica 1 Amminoacidi
Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( OO) nella stessa molecola 3 N 2 α * OO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-himica Organica 1 Amminoacidi
PROTIDI: LE PROTEINE E GLI AMMINOACIDI
 PROTIDI: LE PROTEINE E GLI AMMINOACIDI GLI AMMINOACIDI Struttura generica di un amminoacido. R rappresenta un gruppo laterale specifico di ogni amminoacido. In chimica, gli amminoacidi (impropriamente
PROTIDI: LE PROTEINE E GLI AMMINOACIDI GLI AMMINOACIDI Struttura generica di un amminoacido. R rappresenta un gruppo laterale specifico di ogni amminoacido. In chimica, gli amminoacidi (impropriamente
Caratteristiche generali
 AMMINOACIDI Gli amminoacidi sono le unità costruttive (building blocks) delle proteine. Come dice il termine, gli amminoacidi naturali sono costituiti da un gruppo amminico (-NH 2 ) e da un gruppo carbossilico
AMMINOACIDI Gli amminoacidi sono le unità costruttive (building blocks) delle proteine. Come dice il termine, gli amminoacidi naturali sono costituiti da un gruppo amminico (-NH 2 ) e da un gruppo carbossilico
sono le unità monomeriche che costituiscono le proteine hanno tutti una struttura comune
 AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
Vittoria Patti MACROMOLECOLE BIOLOGICHE. 4. proteine
 Vittoria Patti MACROMOLECOLE BIOLOGICHE 4. proteine 1 Funzioni principali delle proteine funzione cosa significa esempi ENZIMATICA STRUTTURALE TRASPORTO MOVIMENTO DIFESA IMMUNITARIA ORMONALE catalizzare
Vittoria Patti MACROMOLECOLE BIOLOGICHE 4. proteine 1 Funzioni principali delle proteine funzione cosa significa esempi ENZIMATICA STRUTTURALE TRASPORTO MOVIMENTO DIFESA IMMUNITARIA ORMONALE catalizzare
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH. ) ed un gruppo carbossilico ( COOH) nella stessa molecola
 Amminoacidi (1) Presentano un gruppo amminico ( NH 2 ) ed un gruppo carbossilico ( COOH) nella stessa molecola CH 3 NH 2 C H α * COOH Acido 2-ammino propanoico (acido α-ammino propionico) 1 Amminoacidi
Amminoacidi (1) Presentano un gruppo amminico ( NH 2 ) ed un gruppo carbossilico ( COOH) nella stessa molecola CH 3 NH 2 C H α * COOH Acido 2-ammino propanoico (acido α-ammino propionico) 1 Amminoacidi
La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa.
 La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa. Le cellule contengono 4 famiglie principali di piccole molecole organiche: Amminoacidi
La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa. Le cellule contengono 4 famiglie principali di piccole molecole organiche: Amminoacidi
Le proteine. Polimeri composto da 20 diversi aminoacidi
 Le proteine Polimeri composto da 20 diversi aminoacidi (D. Voet, J.G. Voet, Biochemistry, 3 ed., John Wiley & Sons, 2004) PROTEINE come ATTUATORI nella cellula Trasporto elettronico Trasporto di ioni e
Le proteine Polimeri composto da 20 diversi aminoacidi (D. Voet, J.G. Voet, Biochemistry, 3 ed., John Wiley & Sons, 2004) PROTEINE come ATTUATORI nella cellula Trasporto elettronico Trasporto di ioni e
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH
 Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( COO) nella stessa molecola C 3 N 2 C α * COO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-Chimica Organica
Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( COO) nella stessa molecola C 3 N 2 C α * COO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-Chimica Organica
Prof. Fulvio Ursini Dipartimento di Chimica Biologica (Vallisneri IV piano Nord) Viale G. Colombo, Padova. Tel.
 Prof. Fulvio Ursini Dipartimento di Chimica Biologica (Vallisneri IV piano Nord) Viale G. Colombo, 3-35121 Padova. Tel.:+39-049-8276104 Fax.:+39-049-8073310 E-mail: fulvio.ursini@unipd.it Funzioni delle
Prof. Fulvio Ursini Dipartimento di Chimica Biologica (Vallisneri IV piano Nord) Viale G. Colombo, 3-35121 Padova. Tel.:+39-049-8276104 Fax.:+39-049-8073310 E-mail: fulvio.ursini@unipd.it Funzioni delle
LE PROTEINE. SONO Polimeri formati dall unione di AMMINOACIDI (AA) Rende diversi i 20 AA l uno dall altro UN ATOMO DI C AL CENTRO
 LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
REPLICAZIONE DEL DNA
 REPLICAZIONE DEL DNA La replicazione (o anche duplicazione) è il meccanismo molecolare attraverso cui il DNA produce una copia di sé stesso. Ogni volta che una cellula si divide, infatti, l'intero genoma
REPLICAZIONE DEL DNA La replicazione (o anche duplicazione) è il meccanismo molecolare attraverso cui il DNA produce una copia di sé stesso. Ogni volta che una cellula si divide, infatti, l'intero genoma
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE Vengono chiamate amminoacidi quelle molecole organiche in cui sono contemporaneamente presenti sia un gruppo acido carbossilico -COO che un gruppo amminico -N2. Una molecola appartenente
AMMINOACIDI E PROTEINE Vengono chiamate amminoacidi quelle molecole organiche in cui sono contemporaneamente presenti sia un gruppo acido carbossilico -COO che un gruppo amminico -N2. Una molecola appartenente
lezione Prof. Spina miliardi di anni fa l universo comparve sotto forma di eruzioni
 Biochimica Matricole dispari 1 1^ lezione Prof. Spina LA BIOCHIMICA 15 20 miliardi di anni fa l universo comparve sotto forma di eruzioni d l f d inimmaginabili di particele subatomiche ricche di energia
Biochimica Matricole dispari 1 1^ lezione Prof. Spina LA BIOCHIMICA 15 20 miliardi di anni fa l universo comparve sotto forma di eruzioni d l f d inimmaginabili di particele subatomiche ricche di energia
I gruppi R differenziano i 20 amminoacidi standard. Tratto da D. Voet, G. Voet e C.W. Pratt Fondamenti di biochimica
 Gli aminoacidi NOMENCLATURA Aminoacido Abbr. tre lettere Abbr. una lettera Aminoacido Abbr. tre lettere Abbr. una lettera Alanina ALA A Lisina LYS K Arginina ARG R Metionina MET M Asparagina ASN N Fenilalanina
Gli aminoacidi NOMENCLATURA Aminoacido Abbr. tre lettere Abbr. una lettera Aminoacido Abbr. tre lettere Abbr. una lettera Alanina ALA A Lisina LYS K Arginina ARG R Metionina MET M Asparagina ASN N Fenilalanina
9) Scrivere un disaccaride formato dal β-d-galattosio e dall α-d-n-acetil-glucosammina legati da un legame glicosidico β(1-4).
 CARBOIDRATI - AMMINOACIDI - PROTEINE 1) Scrivere la proiezione di Fisher del D-ribosio e del D-glucosio. La lettera D a cosa si riferisce? Disegnare inoltre il disaccaride ottenuto dalla condensazione
CARBOIDRATI - AMMINOACIDI - PROTEINE 1) Scrivere la proiezione di Fisher del D-ribosio e del D-glucosio. La lettera D a cosa si riferisce? Disegnare inoltre il disaccaride ottenuto dalla condensazione
AMINOACIDI - 1 AMINOACIDI - 2
 AMINOAIDI - 1 Proteine (gr. pròtos = primo) 50-80% peso secco cellulare GENE POTEINA EFFETTO proteine calore idrolisi acida o alcalina α-aminoacidi proteasi Struttura generale degli α-aminoacidi primari
AMINOAIDI - 1 Proteine (gr. pròtos = primo) 50-80% peso secco cellulare GENE POTEINA EFFETTO proteine calore idrolisi acida o alcalina α-aminoacidi proteasi Struttura generale degli α-aminoacidi primari
4x4x4=4 3 =64 codoni. 20 aminoacidi
 4x4x4=4 3 =64 codoni 20 aminoacidi 1 Le 20 diverse catene laterali (gruppo R) che costituiscono gli aminoacidi si differenziano considerevolmente per dimensioni, volume e per le loro caratteristiche fisico-chimiche,
4x4x4=4 3 =64 codoni 20 aminoacidi 1 Le 20 diverse catene laterali (gruppo R) che costituiscono gli aminoacidi si differenziano considerevolmente per dimensioni, volume e per le loro caratteristiche fisico-chimiche,
AMINOACIDI. GENE PROTEINA EFFETTO. calore. idrolisi acida (o alcalina) Struttura generale degli α-aminoacidi primari (standard, normali):
 AMINOAIDI. Proteine (gr. pròtos = primo) > 50% peso secco cellulare GENE POTEINA EFFETTO proteine calore idrolisi acida (o alcalina) α-aminoacidi Struttura generale degli α-aminoacidi primari (standard,
AMINOAIDI. Proteine (gr. pròtos = primo) > 50% peso secco cellulare GENE POTEINA EFFETTO proteine calore idrolisi acida (o alcalina) α-aminoacidi Struttura generale degli α-aminoacidi primari (standard,
Le proteine. Sintetizzate nei ribosomi come una sequenza lineare di amminoacidi assumono in seguito una struttura tridimensionale
 Le proteine Elementi funzionali e strutturali di fondamentale importanza per lo svolgimento di funzioni metaboliche, di trasporto, di trasmissione nervosa o contrattile, ormonale o immunitaria Sintetizzate
Le proteine Elementi funzionali e strutturali di fondamentale importanza per lo svolgimento di funzioni metaboliche, di trasporto, di trasmissione nervosa o contrattile, ormonale o immunitaria Sintetizzate
Introduzione alla biologia della cellula. Lezione 2 Le biomolecole
 Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
E. Giordano 16/09/2010
 GRUPPO NAZIONALE DI BIOINGEGNERIA XXIX Scuola Annuale BIOLOGIA SINTETICA Bressanone 13-17 settembre 2010 1/41 COSTITUENTI MOLECOLARI DELLO CHASSIS CELLULARE Emanuele GIORDANO II Facoltà di Ingegneria Dipartimento
GRUPPO NAZIONALE DI BIOINGEGNERIA XXIX Scuola Annuale BIOLOGIA SINTETICA Bressanone 13-17 settembre 2010 1/41 COSTITUENTI MOLECOLARI DELLO CHASSIS CELLULARE Emanuele GIORDANO II Facoltà di Ingegneria Dipartimento
Proprietà comuni. Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici
 Gli aminoacidi Proprietà comuni Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici paragonabili Il gruppo α-aminico è un acido più forte (o una base più debole
Gli aminoacidi Proprietà comuni Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici paragonabili Il gruppo α-aminico è un acido più forte (o una base più debole
Prof. Maria Nicola GADALETA
 Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Nome e cognome: [Totale: 80 punti]
![Nome e cognome: [Totale: 80 punti] Nome e cognome: [Totale: 80 punti]](/thumbs/61/45962295.jpg) Nome e cognome: ruppo / candidato No. SIENZE SPERIMENTLI: BIOLOI [Totale: 80 punti] Raccomandazioni: Rispondere direttamente sui fogli Non separare i fogli Rispondere in modo sintetico e chiaro, usando
Nome e cognome: ruppo / candidato No. SIENZE SPERIMENTLI: BIOLOI [Totale: 80 punti] Raccomandazioni: Rispondere direttamente sui fogli Non separare i fogli Rispondere in modo sintetico e chiaro, usando
3.3.2. ALIMENTI DI ORIGINE VEGETALE. 3.3.2.1. Verdure
 3.3.2. ALIMENTI DI ORIGINE VEGETALE 3.3.2.1. Verdure Nella Tabella 9 sono riportati i valori degli aminoacidi liberi presenti in alcune fra le più diffuse verdure in commercio. In un passato recente era
3.3.2. ALIMENTI DI ORIGINE VEGETALE 3.3.2.1. Verdure Nella Tabella 9 sono riportati i valori degli aminoacidi liberi presenti in alcune fra le più diffuse verdure in commercio. In un passato recente era
Aminoacidi. Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α
 Aminoacidi Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α 1 Isomeria ottica Tutti gli AA, esclusa la glicina, presentano almeno un atomo di carbonio asimmetrico, il
Aminoacidi Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α 1 Isomeria ottica Tutti gli AA, esclusa la glicina, presentano almeno un atomo di carbonio asimmetrico, il
La chimica della pelle
 La chimica della pelle 1 Gli amminoacidi Queste unità hanno la particolare caratteristica di contenere nella stessa molecola un gruppo acido (- COOH) ed uno basico (- NH 2 ), legati tra loro attraverso
La chimica della pelle 1 Gli amminoacidi Queste unità hanno la particolare caratteristica di contenere nella stessa molecola un gruppo acido (- COOH) ed uno basico (- NH 2 ), legati tra loro attraverso
LE MACROMOLECOLE BIOLOGICHE Le cellule contengono 4 famiglie principali di molecole organiche:
 LEZIONE n 1 LE MACROMOLECOLE BIOLOGICHE Le cellule contengono 4 famiglie principali di molecole organiche: macromolecole Macromolecole macromolecole I componenti chimici di una cellula -Le macromolecole
LEZIONE n 1 LE MACROMOLECOLE BIOLOGICHE Le cellule contengono 4 famiglie principali di molecole organiche: macromolecole Macromolecole macromolecole I componenti chimici di una cellula -Le macromolecole
COMPORTAMENTO ANFOTERO DEGLI AA
 Proprietà acido-basiche degli aminoacidi FORMA NON IONICA Non esiste a nessun valore di ph FORMA ZWITTERIONICA È la forma prevalente a ph 7 COMPORTAMENTO ANFOTERO DEGLI AA CARICA NETTA +1 CARICA NETTA
Proprietà acido-basiche degli aminoacidi FORMA NON IONICA Non esiste a nessun valore di ph FORMA ZWITTERIONICA È la forma prevalente a ph 7 COMPORTAMENTO ANFOTERO DEGLI AA CARICA NETTA +1 CARICA NETTA
I materiali della vita
 I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
scaricato da www.sunhope.it Proteine semplici costituite dai soli amminoacidi
 Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
Biologia. Lezione 09/11/2010
 Biologia Lezione 09/11/2010 Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono macromolecole formate da unità (MONOMERI)
Biologia Lezione 09/11/2010 Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono macromolecole formate da unità (MONOMERI)
STRUTTURA E FUNZIONE DELLE PROTEINE
 STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
LE PROTEINE SINTESI PROTEICA. funzione delle proteine nel nostro organismo
 LE PTEIE Le proteine sono sostanze organiche presenti in tutte le cellule di tutti gli organismi viventi Le proteine sono costituite da,,,, (S) Struttura delle proteine Le proteine sono macromolecole (
LE PTEIE Le proteine sono sostanze organiche presenti in tutte le cellule di tutti gli organismi viventi Le proteine sono costituite da,,,, (S) Struttura delle proteine Le proteine sono macromolecole (
CARBOIDRATI C H O ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO
 CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
Università Telematica Pegaso. Indice
 LE PROTEINE PROF.SSA AUSILIA ELCE Indice 1 INTRODUZIONE -------------------------------------------------------------------------------------------------------------- 3 2 TRASCRIZIONE--------------------------------------------------------------------------------------------------------------
LE PROTEINE PROF.SSA AUSILIA ELCE Indice 1 INTRODUZIONE -------------------------------------------------------------------------------------------------------------- 3 2 TRASCRIZIONE--------------------------------------------------------------------------------------------------------------
2011 - G. Licini, Università di Padova. La riproduzione a fini commerciali è vietata
 Ammino acidi Composto che contiene una funziome acida e amminica. Usualmente però con amminoacidi si intendono gli alfa- amminoacidi. Tra questi composti ve ne sono 20 che vengono definiti geneticamente
Ammino acidi Composto che contiene una funziome acida e amminica. Usualmente però con amminoacidi si intendono gli alfa- amminoacidi. Tra questi composti ve ne sono 20 che vengono definiti geneticamente
Lezione 2. Bioinformatica. Mauro Ceccanti e Alberto Paoluzzi
 Lezione 2 Bioinformatica Mauro Ceccanti e Alberto Paoluzzi Dip. Informatica e Automazione Università Roma Tre Dip. Medicina Clinica Università La Sapienza Lezione 2: AMMINOACIDI E POLIPEPTIDI Aminoacidi
Lezione 2 Bioinformatica Mauro Ceccanti e Alberto Paoluzzi Dip. Informatica e Automazione Università Roma Tre Dip. Medicina Clinica Università La Sapienza Lezione 2: AMMINOACIDI E POLIPEPTIDI Aminoacidi
Immagini e concetti della biologia
 Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
Chimica Biologica A.A α-elica foglietto β reverse turn
 Chimica Biologica A.A. 2010-2011 α-elica foglietto β reverse turn Str. Secondaria sperimentalmente osservata: Si distinguono fondamentalmente tre tipi di strutture secondarie: α elica foglietto β reverse
Chimica Biologica A.A. 2010-2011 α-elica foglietto β reverse turn Str. Secondaria sperimentalmente osservata: Si distinguono fondamentalmente tre tipi di strutture secondarie: α elica foglietto β reverse
Somministrazione o assunzione di alimenti allo scopo di nutrire l organismo
 Definizioni Alimentazione Somministrazione o assunzione di alimenti allo scopo di nutrire l organismo Nutrizione complesso di processi biologici che consentono o condizionano la conservazione, l accrescimento,
Definizioni Alimentazione Somministrazione o assunzione di alimenti allo scopo di nutrire l organismo Nutrizione complesso di processi biologici che consentono o condizionano la conservazione, l accrescimento,
Emoglobina e mioglobina
 Emoglobina e mioglobina Per molti organismi, l O 2 è una molecola di importanza vitale: l'ossigeno è infatti l'accettore finale degli elettroni, che "fluendo" attraverso i complessi della catena respiratoria,
Emoglobina e mioglobina Per molti organismi, l O 2 è una molecola di importanza vitale: l'ossigeno è infatti l'accettore finale degli elettroni, che "fluendo" attraverso i complessi della catena respiratoria,
MFN0366-A1 (I. Perroteau) -traduzione e indirizzamento delle proteine. Solo per uso didattico, vietata la riproduzione, la diffusione o la vendita
 MFN0366-A1 (I. Perroteau) -traduzione e indirizzamento delle proteine MFN0366-A1 (I. Perroteau) -traduzione delle proteine trna Traduzione: mrna -------> proteine mrna MFN0366-A1 (I. Perroteau) -traduzione
MFN0366-A1 (I. Perroteau) -traduzione e indirizzamento delle proteine MFN0366-A1 (I. Perroteau) -traduzione delle proteine trna Traduzione: mrna -------> proteine mrna MFN0366-A1 (I. Perroteau) -traduzione
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA)
 La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) L atomo del carbonio (C).. C. Atomo tetravalente. C C C C Gli idrocarburi I legami del carbonio 109.5 gradi
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) L atomo del carbonio (C).. C. Atomo tetravalente. C C C C Gli idrocarburi I legami del carbonio 109.5 gradi
SOLUZIONI DEGLI ESERCIZI
 Dal carbonio agli OGM Biochimica e biotecnologie SOLUZIONI DEGLI ESERCIZI Capitolo 0 Il mondo del carbonio 1. b, e 2. d 3. 7 4. 5. 6. 7. a) Isomeria di posizione; b) i due composti non sono isomeri; c)
Dal carbonio agli OGM Biochimica e biotecnologie SOLUZIONI DEGLI ESERCIZI Capitolo 0 Il mondo del carbonio 1. b, e 2. d 3. 7 4. 5. 6. 7. a) Isomeria di posizione; b) i due composti non sono isomeri; c)
INTRODUZIONE ALLA PROTEINE BCP 1-2
 INTRODUZIONE ALLA BIOCHIMICA DELLE PROTEINE BCP 1-2 Pietre miliari Lehninger 1973 Biochemistry Proteine ricombinanti Protein engineering Cristallografia, NMR, EM, MS, spettroscopie... Computing Bioinformaticai
INTRODUZIONE ALLA BIOCHIMICA DELLE PROTEINE BCP 1-2 Pietre miliari Lehninger 1973 Biochemistry Proteine ricombinanti Protein engineering Cristallografia, NMR, EM, MS, spettroscopie... Computing Bioinformaticai
LE MOLECOLE BIOLOGICHE
 LE MOLECOLE BIOLOGICHE Le cellule contengono quattro famiglie principali di molecole organiche Zuccheri (monosaccaridi) - forniscono una fonte di energia - subunità dei polisaccaridi Amminoacidi - subunità
LE MOLECOLE BIOLOGICHE Le cellule contengono quattro famiglie principali di molecole organiche Zuccheri (monosaccaridi) - forniscono una fonte di energia - subunità dei polisaccaridi Amminoacidi - subunità
Composti organici. I composti organici. Atomi e molecole di carbonio. Atomi e molecole di carbonio. Gruppi funzionali. Isomeri
 I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
LEZIONE 2 COMPOSTI DEL CARBONIO: MACROMOLECOLE:
 LEZIONE 2 COMPONENTI CHIMICI DELLA CELLULA ACQUA COMPOSTI DEL CARBONIO: MACROMOLECOLE: ZUCCHERI ACIDI GRASSI PROTEINE NUCLEOTIDI percentuale di abbondanza relativa I componenti chimici di una cellula organismi
LEZIONE 2 COMPONENTI CHIMICI DELLA CELLULA ACQUA COMPOSTI DEL CARBONIO: MACROMOLECOLE: ZUCCHERI ACIDI GRASSI PROTEINE NUCLEOTIDI percentuale di abbondanza relativa I componenti chimici di una cellula organismi
Le macromolecole dei tessuti - 1
 Le macromolecole dei tessuti - 1 Che cosa sono le proteine? Sono macromolecole complesse ad alta informazione Sono costituite da una o più catene polipeptidiche Ogni catena peptidica è composta da centinaia
Le macromolecole dei tessuti - 1 Che cosa sono le proteine? Sono macromolecole complesse ad alta informazione Sono costituite da una o più catene polipeptidiche Ogni catena peptidica è composta da centinaia
LE PROTEINE -struttura tridimensionale-
 LE PROTEINE -struttura tridimensionale- Struttura generale di una proteina Ceruloplasmina Cosa sono??? Sono biopolimeri con forme ben definite. composti da molteplici amminoacidi, legati con legami peptidici
LE PROTEINE -struttura tridimensionale- Struttura generale di una proteina Ceruloplasmina Cosa sono??? Sono biopolimeri con forme ben definite. composti da molteplici amminoacidi, legati con legami peptidici
proteasi (distrugge le proteine) batteri virulenti del ceppo S e del ceppo R
 unità 1. La funzione del DN negli organismi La funzione del DN L acido desossiribonucleico o DN (dall inglese deoxyribonucleic acid) è la molecola informazionale delle cellule. Essa contiene e trasmette
unità 1. La funzione del DN negli organismi La funzione del DN L acido desossiribonucleico o DN (dall inglese deoxyribonucleic acid) è la molecola informazionale delle cellule. Essa contiene e trasmette
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 10 Le basi della biochimica 3 Sommario 1. Le molecole biologiche si dividono in quattro classi 2. I carboidrati sono il «carburante»
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 10 Le basi della biochimica 3 Sommario 1. Le molecole biologiche si dividono in quattro classi 2. I carboidrati sono il «carburante»
Amminoacidi e Proteine
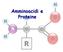 Amminoacidi e Proteine Struttura generale di un α-amminoacido R = catena laterale AMMINOACIDI (AA) CELLULARI Gli amminoacidi presenti nella cellula possono essere il prodotto di idrolisi delle proteine
Amminoacidi e Proteine Struttura generale di un α-amminoacido R = catena laterale AMMINOACIDI (AA) CELLULARI Gli amminoacidi presenti nella cellula possono essere il prodotto di idrolisi delle proteine
L ACQUA E LE SUE PROPRIETÀ
 L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
Legami chimici. Covalente. Legami deboli
 Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici STRUTTURA TERZIARIA La struttura tridimensionale
Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici STRUTTURA TERZIARIA La struttura tridimensionale
4.2. PRESENZA DI UMAMI NEGLI ALIMENTI ITTICI E DERIVATI
 4.2. PRESENZA DI UMAMI NEGLI ALIMENTI ITTICI E DERIVATI 4.2.1. PESCI, MOLLUSCHI E CROSTACEI Per la compilazione di questa parte, sono affiorati numerosi problemi di natura bibliografica che dimostrano
4.2. PRESENZA DI UMAMI NEGLI ALIMENTI ITTICI E DERIVATI 4.2.1. PESCI, MOLLUSCHI E CROSTACEI Per la compilazione di questa parte, sono affiorati numerosi problemi di natura bibliografica che dimostrano
Traduzione dell informazione genetica (1)
 Traduzione dell informazione genetica (1) 1 Traduzione dell informazione genetica (2) Il processo negli eucarioti richiede: 70 diverse proteine ribosomiali >20 enzimi che attivano i precursori degli amminoacidi
Traduzione dell informazione genetica (1) 1 Traduzione dell informazione genetica (2) Il processo negli eucarioti richiede: 70 diverse proteine ribosomiali >20 enzimi che attivano i precursori degli amminoacidi
30/10/2015 LIVELLI DI ORGANIZZAZIONE STRUTTURALE DELLE PROTEINE
 LIVELLI DI ORGANIZZAZIONE STRUTTURALE DELLE PROTEINE 1 CARATTERISTICHE DEL LEGAME PEPTIDICO lunghezza intermedia tra un legame singolo e uno doppio ibrido di risonanza per il parziale carattere di doppio
LIVELLI DI ORGANIZZAZIONE STRUTTURALE DELLE PROTEINE 1 CARATTERISTICHE DEL LEGAME PEPTIDICO lunghezza intermedia tra un legame singolo e uno doppio ibrido di risonanza per il parziale carattere di doppio
Amminoacidi - Peptidi - Proteine. Emoglobina
 Amminoacidi - Peptidi - Proteine Emoglobina 1 Emoglobina Gli amminoacidi sono le sostanze di base che costituiscono le proteine. Ogni proteina è caratterizzata da una precisa sequenza di mattoni di amminoacidi.
Amminoacidi - Peptidi - Proteine Emoglobina 1 Emoglobina Gli amminoacidi sono le sostanze di base che costituiscono le proteine. Ogni proteina è caratterizzata da una precisa sequenza di mattoni di amminoacidi.
Gli amminoacidi Il legame peptidico Motivi strutturali classificazione, architettura topologia delle strutture tridimensionali di proteine.
 Struttura di proteine Gli amminoacidi Il legame peptidico Motivi strutturali classificazione, architettura topologia delle strutture tridimensionali di proteine. Correlazioni struttura-funzione Gli amminoacidi
Struttura di proteine Gli amminoacidi Il legame peptidico Motivi strutturali classificazione, architettura topologia delle strutture tridimensionali di proteine. Correlazioni struttura-funzione Gli amminoacidi
IN UN ATOMO SI DISTINGUE UN NUCLEO CARICO POSITIVAMENTE ATTORNO AL QUALE RUOTANO PARTICELLE CARICHE NEGATIVAMENTE: GLI ELETTRONI (e - ) (-)
 LA VITA, LA CHIMICA E L ACQUA PER INIZIARE QUALCHE CENNO DI CHIMICA LA MATERIA E FATTA DI COMBINAZIONI DI ELEMENTI. GLI ELEMENTI SONO COMPOSTI DA SINGOLI ATOMI, LE PIU PICCOLE UNITA CHE MANTENGONO LE PROPRIETA
LA VITA, LA CHIMICA E L ACQUA PER INIZIARE QUALCHE CENNO DI CHIMICA LA MATERIA E FATTA DI COMBINAZIONI DI ELEMENTI. GLI ELEMENTI SONO COMPOSTI DA SINGOLI ATOMI, LE PIU PICCOLE UNITA CHE MANTENGONO LE PROPRIETA
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA. Angela Chambery Lezione 4
 Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 4 Scoperta degli amminoacidi: gli amminoacidi essenziali Gli amminoacidi essenziali sono quegli amminoacidi che un
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 4 Scoperta degli amminoacidi: gli amminoacidi essenziali Gli amminoacidi essenziali sono quegli amminoacidi che un
Polimorfismo genetico del collageno
 COLLAGENO È la proteina più abbondante del nostro corpo costituendo il 25% delle proteine totali. È la proteina principale dei tessuti connettivi, la cui matrice extracellulare contiene anche: -proteoglicani
COLLAGENO È la proteina più abbondante del nostro corpo costituendo il 25% delle proteine totali. È la proteina principale dei tessuti connettivi, la cui matrice extracellulare contiene anche: -proteoglicani
Capitolo 3 Le biomolecole
 apitolo 3 Le biomolecole opyright 2006 Zanichelli editore I composti organici e i loro polimeri 3.1 La diversità molecolare della vita è basata sulle proprietà del carbonio Un atomo di carbonio può formare
apitolo 3 Le biomolecole opyright 2006 Zanichelli editore I composti organici e i loro polimeri 3.1 La diversità molecolare della vita è basata sulle proprietà del carbonio Un atomo di carbonio può formare
Le proteine rappresentano gli elementi strutturali e funzionali più importanti nei sistemi viventi. Qualsiasi processo vitale dipende da questa
 Gli amminoacidi Le proteine rappresentano gli elementi strutturali e funzionali più importanti nei sistemi viventi. Qualsiasi processo vitale dipende da questa classe di molecole: p. es. la catalisi delle
Gli amminoacidi Le proteine rappresentano gli elementi strutturali e funzionali più importanti nei sistemi viventi. Qualsiasi processo vitale dipende da questa classe di molecole: p. es. la catalisi delle
aa 2013-14 Proteine Struttura delle Proteine α Amminoacidi
 Proteine Biopolimeri degli α-amino acidi. Amino acidi sono uniti attraverso il legame peptidico. Alcune funzioni: Struttura (collagene, cheratina ecc.) Enzimi (maltasi, deidrogenasi ecc) Trasporto (albumine,
Proteine Biopolimeri degli α-amino acidi. Amino acidi sono uniti attraverso il legame peptidico. Alcune funzioni: Struttura (collagene, cheratina ecc.) Enzimi (maltasi, deidrogenasi ecc) Trasporto (albumine,
Amminoacidi Peptidi Proteine
 Amminoacidi Peptidi Proteine Amminoacidi-Peptidi-Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Stereoisomeri: composti con la stessa connessione tra gli atomi, ma con una differente
Amminoacidi Peptidi Proteine Amminoacidi-Peptidi-Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Stereoisomeri: composti con la stessa connessione tra gli atomi, ma con una differente
Formazione del legame peptidico:
 Formazione del legame peptidico: Planare, ha una forza intermedia tra il legame semplice ed il legame doppio. 2^ lezione N R C C O O O + R N R C O C O O N R C C N C C O Ogni piano delle unità peptidiche
Formazione del legame peptidico: Planare, ha una forza intermedia tra il legame semplice ed il legame doppio. 2^ lezione N R C C O O O + R N R C O C O O N R C C N C C O Ogni piano delle unità peptidiche
3.3. UMAMI NEGLI ALIMENTI
 3.3. UMAMI NEGLI ALIMENTI In questo capitolo saranno esaminati i vari cibi, ad esclusione di quelli ittici che verranno presi in considerazione successivamente, allo scopo di scoprire se in essi è presente,
3.3. UMAMI NEGLI ALIMENTI In questo capitolo saranno esaminati i vari cibi, ad esclusione di quelli ittici che verranno presi in considerazione successivamente, allo scopo di scoprire se in essi è presente,
METABOLISMO DEGLI AMMINOACIDI
 PRINCIPI NUTRITIVI METABOLISMO DEGLI AMMINOACIDI Nel corso della digestione le proteine vengono degradate in amminoacidi. Contrariamente ai carboidrati, gli amminoacidi non vengono immagazzinati, ma vengono
PRINCIPI NUTRITIVI METABOLISMO DEGLI AMMINOACIDI Nel corso della digestione le proteine vengono degradate in amminoacidi. Contrariamente ai carboidrati, gli amminoacidi non vengono immagazzinati, ma vengono
Le Biomolecole I parte. Lezioni d'autore di Giorgio Benedetti
 Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
Chimotripsina Una proteina globulare. Glicina Un amminoacido
 Chimotripsina Una proteina globulare Glicina Un amminoacido - In teoria un numero enorme di differenti catene polipeptidiche potrebbe essere sintetizzato con i 20 amminoacidi standard. 20 4 = 160.000 differenti
Chimotripsina Una proteina globulare Glicina Un amminoacido - In teoria un numero enorme di differenti catene polipeptidiche potrebbe essere sintetizzato con i 20 amminoacidi standard. 20 4 = 160.000 differenti
BIOCHIMICA BIOCHIMICA APPLICATA
 BIOCHIMICA BIOCHIMICA APPLICATA Corso di Laurea in Farmacia Prof. Ivano F. Santarelli Introduzione Testi consigliati -I principi di Biochimica di Lehninger. D.L.Nelson, M.M. Cox. Zanichelli -Biochimica
BIOCHIMICA BIOCHIMICA APPLICATA Corso di Laurea in Farmacia Prof. Ivano F. Santarelli Introduzione Testi consigliati -I principi di Biochimica di Lehninger. D.L.Nelson, M.M. Cox. Zanichelli -Biochimica
Le proteine. Le proteine sono macromolecole che presentano differenze funzionali e strutturali
 Le proteine Le proteine sono macromolecole che presentano differenze funzionali e strutturali LE PROTEINE HANNO FUNZIONI BIOLOGICHE DIVERSE enzimi proteine di trasporto proteine strutturali proteine di
Le proteine Le proteine sono macromolecole che presentano differenze funzionali e strutturali LE PROTEINE HANNO FUNZIONI BIOLOGICHE DIVERSE enzimi proteine di trasporto proteine strutturali proteine di
FUNZIONI DELLE PROTEINE
 FUNZIONI DELLE PROTEINE 1 CATALISI ENZIMATICA 2 TRASPORTO E DEPOSITO 3 MOVIMENTO COORDINATO 4 SUPPORTO MECCANICO 5 PROTEZIONE IMMUNITARIA 6 GENERAZIONE E TRASMISSIONE DELL IMPULSO NERVOSO 7 CONTROLLO DELLA
FUNZIONI DELLE PROTEINE 1 CATALISI ENZIMATICA 2 TRASPORTO E DEPOSITO 3 MOVIMENTO COORDINATO 4 SUPPORTO MECCANICO 5 PROTEZIONE IMMUNITARIA 6 GENERAZIONE E TRASMISSIONE DELL IMPULSO NERVOSO 7 CONTROLLO DELLA
N 2, malgrado la sua abbondanza, è un fattore limitante la crescita della maggior parte degli organismi
 Glicina (Gly) Alanina (Ala) N 2, malgrado la sua abbondanza, è un fattore limitante la crescita della maggior parte degli organismi La digestione delle proteine endopeptidasi H O R H O R R H 3+ N -C-C-NH-C-C-NH-C-C-NH-C-C-NH-C-COO
Glicina (Gly) Alanina (Ala) N 2, malgrado la sua abbondanza, è un fattore limitante la crescita della maggior parte degli organismi La digestione delle proteine endopeptidasi H O R H O R R H 3+ N -C-C-NH-C-C-NH-C-C-NH-C-C-NH-C-COO
ARPAT Agenzia regionale per la protezione ambientale della Toscana
 ARPAT Agenzia regionale per la protezione ambientale della Toscana Dipartimento Provinciale di Livorno 114, Via Giovanni Marradi - 57126 LIVORNO Tel. 0586/263411 - Fax 0586/263477 E-mail: f.righini@arpat.toscana.it
ARPAT Agenzia regionale per la protezione ambientale della Toscana Dipartimento Provinciale di Livorno 114, Via Giovanni Marradi - 57126 LIVORNO Tel. 0586/263411 - Fax 0586/263477 E-mail: f.righini@arpat.toscana.it
PROTEINE. DEFINIZIONE: Macromolecole formate di AA della serie L uniti tra loro da un legame peptidico.
 LE PROTEINE PROTEINE DEFINIZIONE: Macromolecole formate di AA della serie L uniti tra loro da un legame peptidico. FUNZIONI: Strutturale: costruzione delle strutture cellulari Funzionale: Catalizzatori
LE PROTEINE PROTEINE DEFINIZIONE: Macromolecole formate di AA della serie L uniti tra loro da un legame peptidico. FUNZIONI: Strutturale: costruzione delle strutture cellulari Funzionale: Catalizzatori
LE BIOMOLECOLE LIPIDI, PROTEINE E ACIDI NUCLEICI GSCATULLO
 LE BIOMOLECOLE LIPIDI, PROTEINE E ACIDI NUCLEICI GSCATULLO ( Le Biomolecole I Lipidi Definizione e classificazione I lipidi rappresentano una vasta classe di composti chimicamente eterogenea per struttura
LE BIOMOLECOLE LIPIDI, PROTEINE E ACIDI NUCLEICI GSCATULLO ( Le Biomolecole I Lipidi Definizione e classificazione I lipidi rappresentano una vasta classe di composti chimicamente eterogenea per struttura
INTRODUZIONE ALLO STUDIO DELLA CHIMICA ORGANICA
 INTRODUZIONE ALLO STUDIO DELLA CHIMICA ORGANICA ai primi dell 800 Il chimico svedese Jacob Berzelius (1779-1848) indicava le sostanze con il termine organico se ottenute dagli organismi viventi (animali
INTRODUZIONE ALLO STUDIO DELLA CHIMICA ORGANICA ai primi dell 800 Il chimico svedese Jacob Berzelius (1779-1848) indicava le sostanze con il termine organico se ottenute dagli organismi viventi (animali
LIVELLI DI STRUTTURA DELLE PROTEINE
 FUNZIONI E STRUTTURA DELLE PROTEINE PROF.SSA AUSILIA ELCE Indice 1 INTRODUZIONE -------------------------------------------------------------------------------------------------------------- 3 2 LIVELLI
FUNZIONI E STRUTTURA DELLE PROTEINE PROF.SSA AUSILIA ELCE Indice 1 INTRODUZIONE -------------------------------------------------------------------------------------------------------------- 3 2 LIVELLI
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA)
 La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) IL CARBONIO E un non metallo, appartiene al IV gruppo ed al II periodo. Possiede 4 elettroni esterni per
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) IL CARBONIO E un non metallo, appartiene al IV gruppo ed al II periodo. Possiede 4 elettroni esterni per
Bioingegneria Elettronica I
 Bioingegneria Elettronica I Macromolecole biologiche A. Bonfiglio Composizione della cellula Acqua, ioni e piccole molecole costituiscono circa il 74% in peso di una cellula di mammifero. L acqua da sola
Bioingegneria Elettronica I Macromolecole biologiche A. Bonfiglio Composizione della cellula Acqua, ioni e piccole molecole costituiscono circa il 74% in peso di una cellula di mammifero. L acqua da sola
Parametri dell α-elica. residui/giro 3.6. passo dell elica
 GRAFICO DI RAMACHANDRAN Parametri dell α-elica residui/giro 3.6 spazio/residuo passo dell elica 1.5 Å 5.4 Å 1 L α-elica può essere destabilizzata da interazioni tra i gruppi R: repulsione/attrazione elettrostatica
GRAFICO DI RAMACHANDRAN Parametri dell α-elica residui/giro 3.6 spazio/residuo passo dell elica 1.5 Å 5.4 Å 1 L α-elica può essere destabilizzata da interazioni tra i gruppi R: repulsione/attrazione elettrostatica
Nucleotidi e Acidi Nucleici. Struttura di DNA e RNA
 Nucleotidi e Acidi Nucleici Nucleosidi Nucleotidi Funzioni biologiche dei nucleotidi Struttura di DNA e RNA Concatenazione e appaiamento dei nucleotidi Lo scheletro degli acidi nucleici Componenti degli
Nucleotidi e Acidi Nucleici Nucleosidi Nucleotidi Funzioni biologiche dei nucleotidi Struttura di DNA e RNA Concatenazione e appaiamento dei nucleotidi Lo scheletro degli acidi nucleici Componenti degli
Continua. Peptidasi H 2 O
 Continua Peptidasi H 2 O Classificazione delle peptidasi 1. Meccanismo catalitico 2. Tipo di reazione catalizzata 3. Struttura molecolare e omologia 1. Meccanismo catalitico (mostrato per la chimotripsina)
Continua Peptidasi H 2 O Classificazione delle peptidasi 1. Meccanismo catalitico 2. Tipo di reazione catalizzata 3. Struttura molecolare e omologia 1. Meccanismo catalitico (mostrato per la chimotripsina)
Analisi e purificazione di proteine
 Analisi e purificazione di proteine elettroforesi ultracentrifugazione cromatografia frammenti specifici sequenziamento struttura primaria livelli superiori contesto fisiologico funzione Condizioni denaturanti
Analisi e purificazione di proteine elettroforesi ultracentrifugazione cromatografia frammenti specifici sequenziamento struttura primaria livelli superiori contesto fisiologico funzione Condizioni denaturanti
Diagramma di Ramachandran
 Chimica Biologica A.A. 2010-2011 Diagramma di Ramachandran Diagramma di Ramachandran Catena polipeptidica La formazione in successione di legami peptidici genera la cosiddetta catena principale o scheletro
Chimica Biologica A.A. 2010-2011 Diagramma di Ramachandran Diagramma di Ramachandran Catena polipeptidica La formazione in successione di legami peptidici genera la cosiddetta catena principale o scheletro
Il DNA e la duplicazione cellulare. Acidi nucleici: DNA, materiale ereditario
 Il DN e la duplicazione cellulare Il DN, materiale ereditario Struttura del DN Replicazione del DN Dal DN alla proteina Il odice genetico iclo cellulare Mitosi Meiosi Da Figura 8-11 ampbell & Reece cidi
Il DN e la duplicazione cellulare Il DN, materiale ereditario Struttura del DN Replicazione del DN Dal DN alla proteina Il odice genetico iclo cellulare Mitosi Meiosi Da Figura 8-11 ampbell & Reece cidi
