Alcheni Idrocarburi con doppi legami Carbonio- Carbonio. 1. Struttura e Preparazione
|
|
|
- Luca Venturi
- 7 anni fa
- Visualizzazioni
Transcript
1 Alcheni 1
2 Alcheni Idrocarburi con doppi legami arbonio- arbonio 1. Struttura e Preparazione 2
3 Alcheni Sono anche chiamati olefine. Includono molti composti naturali e importanti prodotti industriali che costituiscono i composti base per processi industriali. Gli alcheni di maggior volume si preparano industrialmente per cracking termico di alcani lineari. 3 ( 2 ) n = = = 2 3
4 Uso di etilene polietilene etanolo polivinil cloruro etilene etilene glicole polivinil acetato polistirene 4
5 Alcheni importanti β-carotene (pigmento arancio delle carote) licopene (pigmento rosso dei pomodori) (S)-limonene (limoni) (R)-limonene (arance) α-farnesene (nella cera che ricopre le mele) zingiberene (olio di zenzero) 5
6 I. Nomenclatura Idrocarburi insaturi 2 = 2 etene (etilene) propene (propilene) 2-metilpropene (isobutilene) l cloroetene (vinil cloruro) α-pinene (trementina) (1S)-2,6,6-trimetilbiciclo[3.1.1]ept-2-ene acido oleico (un acido grasso monoinsaturo)
7 I. Nomenclatura Alchene come sostituente 2 = 2 = etenil (vinil) 2-propenil (allil) 1-metiletenil (isopropenil) metilene 2 Esempi vinil cloruro l alcool allilico isopropenil bromuro 1-vinilcicloesene metileneciclopentano 7
8 II. Relazione struttura-reattività 1. più sostituito = più stabile Stabilità R R R R R > > R R, R 2 2 > R 2 > R R trans più stabile del cis; E più stabile del Z repulsione trans-2-butene sterica cis-2-butene (Z)-2-butene (E)-2-butene 8
9 III. Preparazione di Alcheni: Reazioni di Eliminazione Il doppio legame si forma attraverso reazioni di eliminazione: X Y + X Y Reazione di Eliminazione β-eliminazione o 1,2-eliminazione A. Disidratazione di alcoli B. Deidroalogenazione di alogenuri alchilici. Dealogenazione di dibromuri vicinali 9
10 III. Preparazione di Alcheni: Reazioni di Eliminazione A. Disidratazione di alcoli K eq < 1 Esempi p.e. più alto p.e. più basso (si distilla l alchene per spostare la reazione a destra) 2 S 4 3 P 4 molecole simmetriche 10
11 III. Preparazione di Alcheni: Reazioni di Eliminazione A. Disidratazione di alcoli 1. Regola di Zaitsev: regioselettività e stereoselettività il prodotto principale della β-eliminazione è l alchene più stabile 2 S % 10% regioselettiva 3 P 4 + maggiore minore 2 S % 32% 12% stereoselettiva 11
12 III. Preparazione di Alcheni: Reazioni di Eliminazione A. Disidratazione di alcoli 2. Meccanismo E1 catalizzato da acido (E1 A ) - reversibile - facilità di disidratazione: 3 > 2º > 1º Stadio Protonazione alcool Stadio 2 (RDS) + 2 Formazione del carbocatione Stadio 3 (nessun Nu o presente) 2 2 Acqua funge da base
13 III. Preparazione di Alcheni: Reazioni di Eliminazione A. Disidratazione di alcoli 2. Meccanismo E1 catalizzato da acido (E1 A ) Stadio 1 Stadio 2 Stadio 3 R E a più alta RDS R + R alchene
14 III. Preparazione di Alcheni: Reazioni di Eliminazione A. Disidratazione di alcoli 2. Meccanismo E1 catalizzato da acido (E1 A ) Stadio 3 Entrambi i prodotti derivano dallo stesso carbocatione intermedio. R Il prodotto più stabile ha minore E a, si forma più velocemente. 14
15 III. Preparazione di Alcheni: Reazioni di Eliminazione A. Disidratazione di alcoli 3. Riarrangiamenti dei carbocationi Esempi 3 P % 33% 3% + maggiore minore % 32% 12% 15
16 III. Preparazione di Alcheni: Reazioni di Eliminazione A. Disidratazione di alcoli 3. Riarrangiamenti dei carbocationi shift 1,2: Il gruppo migra con la propria coppia di legame 3 shift di alchile (metile) shift di idruro 3 In generale: R + riarrangia in un altro R + di energia uguale o più bassa: 2 3 veloce lenti
17 III. Preparazione di Alcheni: Reazioni di Eliminazione A. Disidratazione di alcoli 3. Riarrangiamenti dei carbocationi veloce % 64% 33% 17
18 III. Preparazione di Alcheni: Reazioni di Eliminazione A. Disidratazione di alcoli 3. Riarrangiamenti dei carbocationi veloce a causa della diminuzione dello strain d anello arbocationi primari non si formano; ma la migrazione può avvenire ugualmente con concomitante perdita di 2 :
19 III. Preparazione di Alcheni: Reazioni di Eliminazione A. Disidratazione di alcoli 3. Riarrangiamenti dei carbocationi Sommario: I carbocationi possono: 1) addizionare un nucleofilo + R X R X 2) perdere un protone - + 3) riarrangiare a catione più stabile, poi step 1) o 2) 19
20 III. Preparazione di Alcheni: Reazioni di Eliminazione B. Deidroalogenazione di alogenuri alchilici X + B +B+X Eliminazione base forte: K/etanolo 3 2 Na/ 3 2 tbuk/tbu Meccanismo E2: Alogenuri alchilici 2 ingombrati e 3 danno buone rese. Effetti stereoelettronici: eliminazione anti Segue la regola di Zaitsev: si forma in prevalenza l alchene più stabile. Meccanismo E1: Alogenuri alchilici 3 con basi deboli Se la S N è competitiva (RX 1 ), usare una base ingombrata. Le basi ingombrate estraggono l idrogeno meno ingombrato formando l alchene meno sostituito. 20
21 Basi ingombrate _ ( 3 ) 2 N ( 3 ) 2 3 N 3 tert -butossido diisopropilammina 2,6-dimetilpiridina ( 3 2 ) 3 N: trietilammina 21
22 III. Preparazione di Alcheni: Reazioni di Eliminazione. Dibromuri vicinali Si usa NaI in acetone o Zn in acido acetico. Gli atomi di bromo devono essere antiperiplanari (E2). I 3 = 3 trans I = 3 3 cis Reazione stereospecifica 22
23 Reazioni di Alcheni 23
24 Il legame π Il legame π è un sito elettron-donatore debolmente basico e moderatamente nucleofilo È relativamente debole, ca. 65 kcal/mole 1. coordina acidi di Lewis 2. viene attaccato da elettrofili: Addizioni elettrofile 3. dà reazioni radicaliche: Addizioni radicaliche 24
25 IV. Reazioni di addizione Reazioni di Addizione + Y Z Y Z Reazioni di Addizione Le reazioni sono esotermiche: Esempio Legami che si rompono: π = e Somma: kcal/mole Legami che si formano: e Somma: kcal/mole alore di reazione 16.5 kcal/mole 25
26 IV. Reazioni di addizione Reazioni di Addizione Tipo di Addizione [Elemento aggiunto] Prodotto (senza stereochimica) idrogenazione [ 2 ], riduzione rottura ossidativa [ 2 ], ossidazione addizione X [X] X idrossilazione [], ossidazione idratazione [ 2 ] epossidazione [], ossidazione alogenazione [X 2 ], ossidazione formaz. aloidrine [X], ossidazione X X X ciclopropanazione [ 2 ] 26
27 IV. Reazioni di addizione Idrogenazione di Alcheni Pt, Pd, + 2 o Ni acido oleico (insaturo) 2,Ni acido stearico (saturo) 27
28 IV. Reazioni di addizione Idrogenazione di Alcheni [ 2 ]/Pt 1. alori di idrogenazione: º ~ 30 kcal/mol meno stabile più stabile
29 V. Reazioni di addizione Idrogenazione di Alcheni 2. Stereochimica di idrogenazione Y Z YZ YZ Y Z addizione anti addizione sin L idrogenazione catalitica procede per addizione sin: 2 3 Pt 3 cis 29
30 V. Reazioni di addizione Idrogenazione di Alcheni 2. Stereochimica di idrogenazione: sin Meccanismo probabile: superficie catalizzatore 30
31 IV. Reazioni di addizione B. Addizione Elettrofila Y Z Gli elettroni π sono mobili e nucleofili, reagiscono con elettrofili. nucleofilo elettrofilo δ+ δ- Y Z RDS Y Z Y Z acidi forti alogeni acidi ipoalosi L elettrofilo Y Z è formato da una parte elettrofila e da una nucleofila 31
32 IV. Addizione Elettrofila 1. Addizione di acidi alogenidrici Acidi deboli come acqua (pk a = 15.7) e acido acetico (pk a = 4.75) non reagiscono con i doppi legami. + X X (X = l,, I) alchil alogenuri Reattività: I > > l >> F (più forte l acido = miglior elettrofilo) δ + δ - X X RDS veloce X + planare: attacco di X sopra e sotto 32
33 IV. Addizione Elettrofila 1. Addizione di acidi alogenidrici I. Regola di Markovnikov a) Doppio legame simmetricamente sostituito: I I attacco indifferente b) Doppio legame non simmetricamente sostituito: non 3 2 Nell addizione di X a un alchene, l si lega al carbonio con più. 33
34 IV. Addizione Elettrofila 1. Addizione di acidi alogenidrici II. Meccanismo: 2 stadi con formazione del più stabile carbocatione carbocatione 1 meno stabile prodotto Markovnikov prodotto antimarkovnikov Interpretazione meccanicistica della regola di Markovnikov: La reazione procede attraverso l intermedio carbocationico più stabile. 34
35 IV. Addizione Elettrofila 1. Addizione di acidi alogenidrici II. Meccanismo E a più bassa maggior velocità di formazione + 35
36 IV. Addizione Elettrofila 1. Addizione di acidi alogenidrici III. riarrangiamenti carbocationici + 1,2- shift meccanismo 36
37 1. Addizione di acidi alogenidrici IV. Addizione radicalica di + senza perossidi orientazione Markovnikov con perossidi orientazione antimarkovnikov (effetto perossido) 37
38 1. Addizione di acidi alogenidrici IV. Addizione radicalica di : Meccanismo a catena radicalico R R 2R R + R + Iniziazione + Propagazione + + totale: + 38
39 IV. Addizione Elettrofila 1. Addizione di acidi alogenidrici IV. Addizione radicalica di 3º 1º La reazione procede attraverso l intermedio radicalico più stabile 39
40 1. Addizione di acidi alogenidrici IV. Addizione radicalica di Paragone: addizione di con e senza perossidi ( + ) orientamento Markovnikov Intermedio più stabile in entrambi i casi peross. ( ) orientamento antimarkovnikov controllo regiochimico 40
41 IV. Addizione Elettrofila 2. Addizione di acido solforico (industriale) + S 3 S 3 2 alchil idrogeno solfato totale: idratazione 2 S 4 S 3 2 orientamento Markovnikov 41
42 IV. Addizione Elettrofila 3. Idratazione acido-catalizzata inverso della disidratazione Es Principio di reversibilità microscopica 2 2 S 4 Markovnikov 42
43 IV. Addizione Elettrofila 4. Addizione di alogeni X + X 2 X dialogenuro vicinale (X = l or ) Addizione stereoselettiva anti: 2 l 4 solo trans 43
44 IV. Addizione Elettrofila 4. Addizione di alogeni Meccanismo: ioni alonio δ + δ - ione bromonio addizione anti prodotto trans 44
45 IV. Addizione Elettrofila 5. Addizione di acidi ipoalosi loro acquoso è in equilibrio con acido ipocloroso e acido cloridrico, K eq La concentrazione di l può essere aumentata aggiungendo Ag. l l + l L acido ipobromoso viene formato per idrolisi di N- bromoacetammide: 3 N N 2 Entrambi si formano per addizione di acido forte sui rispettivi sali: NaX + N 3 X + NaN 3 45
46 IV. Addizione Elettrofila 5. Addizione di acidi ipoalosi Formazione di aloidrine X 2 X 2 + X aloidrine vicinali 2 2 addizione anti
47 IV. Addizione Elettrofila 5. Addizione di acidi ipoalosi Regioselettività: l 2 2 l non l l l l l l maggiore contribuente del catione 1 forma contribuente maggiore 47
48 IV. Addizione Elettrofila 5. Addizione di acidi ipoalosi ibrido di risonanza: l δ + δ l Il più sostituito porta maggiore carica δ +, ha maggiore attrazione per il nucleofilo 48
49 IV. Addizione Elettrofila Altri nucleofili: 5. Formazione di eteri
50 IV. Addizione Elettrofila 6. Idroborazione-ossidazione BR R 2 2 B un boroidruro un organoborano orientamento anti-markovnikov addizione stereoselectiva sin nessun riarrangiamento B 2 6 2( ) 3 B 6 +2B() 3 diborano 3 1) B 2 6 2) 2 2, anti-markovnikov addizione sin 50
51 IV. Addizione Elettrofila Meccanismo: B 2 6 diborano δ - δ + B Idroborazione-ossidazione 2B 3 borano δ - δ + B 2 δ - B2 3 2 δ + un più sostituito porta maggior δ + trialchilborano B più elettropositivo di B addizione sin BR anti-markovnikov 51
52 IV. Addizione Elettrofila Meccanismo: 6. Idroborazione-ossidazione ione idroperossido R 2 B trialchilborano R = R R 2 B S N 2 interna la configurazione si mantiene acido 3 + B R trialcossiborano BR
53 IV. Addizione Elettrofila 6. Idroborazione-ossidazione ontrollo regiochimico: 2 2 S 4 Markovnikov 1) B 2 6 2) 2 2, - anti-markovnikov 53
54 7. ssimercuriazione/riduzione L alchene trattato con acetato di mercurio(ii) in TF. a luogo una rapida addizione elettrofila con formazione di un intermedio organomercurio. Il trattamento con sodio boroidruro NaB 4 dà l alcool. 3 = 3 2-Butene + g(ac) 2 Mercurio(II) acetato TF aq Ac 3 3 gac NaB Butanolo 54
55 Meccanismo 7. ssimercuriazione/riduzione D 3 g(ac) 2 2, TF D 3 g Ac 2 (R) D Acg 3 2 (R) 3 D NaB4 L acqua si avvicina allo ione mercurinio dal lato opposto (addizione anti). L acqua si addiziona al carbonio più sostituito per dare il prodotto Markovnikov. 3 D gac 55
56 8. Addizione di arbeni Inserzione di un gruppo 2 in un doppio legame per produrre un ciclopropano. Tre metodi: Diazometano Reazione di Simmons-Smith: metilene ioduro e Zn(u) α-eliminazione 56
57 Diazometano N N 2 N N 2 diazometano calore o luce uv N N 2 N 2 + N 2 R R carbene stereochimica 57
58 Reazione di Simmons-Smith Metodo migliore per preparare i ciclopropani 2 I 2 + Zn(u) I 2 ZnI un carbenoide 2 I 2 Zn, ul 58
59 lorocarbeni Un aloformio reagisce con una base. e X eliminati dallo stesso carbonio: α-eliminazione. Si forma un clorocarbene. l 3 + K K + l l l l l l + l clorocarbene l 3 K, 2 l l 59
60 V. Altre reazioni di alcheni 1. Idrossilazione Si formano glicoli sin: A. ssidazioni on KMn 4 in ambiente basico o con s 4 : R 1 R 3 R 2 R 4 + Mn 4 2, p>8 + s 4 piridina Mn R 1 R 3 R 2 R 4 s R 1 R 3 R 2 R 4 2 S o NaS 3 + Mn 4 2- R 1 R 3 R 2 R 4 +s stereoselettività sin 60
61 V. Altre reazioni di alcheni A. ssidazioni 2. Epossidazione + R perossiacido epossido Meccanismo: + R δ+ δ R 1 R 3 R 2 R 4 R R S.T. R 1 R 3 R 2 R 4 R 61
62 V. Altre reazioni di alcheni Perossidi 2. Epossidazione 3 acido perossiacetico A. ssidazioni Nomenclatura: epossietano (etilene ossido) 1,2-epossipropano (propilene ossido) l acido m-cloroperbenzoico (mpba) 1,2-epossicicloesano (cicloesene ossido) 62
63 V. Altre reazioni di alcheni 2. Epossidazione A. ssidazioni Addizione stereospecifica sin: 3 3 cis-2,3-epossibutano cis 3 3 trans trans-2,3-epossibutano 63
64 Sintesi glicoli anti Apertura degli epossidi in ambiente acido acquoso R 1 R R 1 R 2 2 : : R 1 R R 1 R2 64
65 V. Altre reazioni di alcheni 3. zonolisi A. ssidazioni 1) 3 + 2) 2, Zn rottura ossidativa R R R 1) 3 2) 2, Zn R R chetone + R aldeide R R 1) 3 2) 2, Zn R R chetone + formaldeide 65
66 V. Altre reazioni di alcheni 3. zonolisi: Meccanismo A. ssidazioni R 1 R 2 R 3 R 1 R 2 R 3 molozonuro R 1 R 2 R 3 workup riducente Zn/ 2 R 1 R 2 ozonuro R R 1 workup ossidante R 2 R R 2 R 3 R 2 R 3 R 1 R 1 δ δ + 66
67 V. Altre reazioni di alcheni A. ssidazioni 3. zonolisi: Sintesi 1) 3 2) 2, Zn 67
68 V. Altre reazioni di alcheni B. Polimerizzazione 2 Y monomero iniziatore radicalico 2 Y polimero n n = iniziatori radicalici: 2 dipivaloil perossido dibenzoil perossido 68
69 V. Altre reazioni di alcheni B. Polimerizzazione monomero polimero n etilene polietilene polipropilene propilene n 3 2 l 2 vinil cloruro l n poli(vinil cloruro) (PV) 2 Ph 2 polistirene stirene n 69
70 V. Altre reazioni di alcheni B. Polimerizzazione monomero polimero 2 l 2 vinilidene cloruro 2 l l n Poli(vinilidene cloruro) ( Saran A ) 2 N 2 acrilonitrile N n Poliacrilonitrile (PAN, rlon, Acrilan) F 2 F 2 tetrafluoroetilene F 2 F 2 n Politetrafluoroetilene (PTFE, Teflon ) 70
71 V. Altre reazioni di alcheni B. Polimerizzazione Polimerizzazione radicalica a catena: RR 2R Iniziazione R + 2 R 2 R R Markovnikov R 2 R + 2 R 2 R R 2 R Propagazione R etc. R R R polimerizzazione testa-coda 71
Reazioni Stereospecifiche e Stereoselettive
 Reazioni Stereospecifiche e Stereoselettive La stereospecificità in chimica è la proprietà di una stessa reazione di generare stereoisomeri diversi partendo da stereoisomeri diversi. Si differenzia dalla
Reazioni Stereospecifiche e Stereoselettive La stereospecificità in chimica è la proprietà di una stessa reazione di generare stereoisomeri diversi partendo da stereoisomeri diversi. Si differenzia dalla
Capitolo 4 Reazioni degli alcheni
 himica Organica Informazione Scientifica sul Farmaco apitolo 4 Reazioni degli alcheni Organic hemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: richiami generali sulle reazioni chimice reattività
himica Organica Informazione Scientifica sul Farmaco apitolo 4 Reazioni degli alcheni Organic hemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: richiami generali sulle reazioni chimice reattività
Alcheni: struttura e reattività
 Alcheni: struttura e reattività Alcheni Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n 2n Alcheni in biologia ormone delle piante che induce la maturazione dei frutti costituente
Alcheni: struttura e reattività Alcheni Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n 2n Alcheni in biologia ormone delle piante che induce la maturazione dei frutti costituente
Alcheni: : struttura e reattività. Alcheni. Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n. H 2n. Alcheni in biologia
 Alcheni: : struttura e reattività Alcheni Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n H 2n Alcheni in biologia ormone delle piante che induce la maturazione dei frutti costituente
Alcheni: : struttura e reattività Alcheni Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n H 2n Alcheni in biologia ormone delle piante che induce la maturazione dei frutti costituente
REAZIONI DI ADDIZIONE AL DOPPIO LEGAME NEGLI ALCHENI
 REAZIONI DI ADDIZIONE AL DOPPIO LEGAME NEGLI ALCHENI Un meccanismo di reazione, descrive come si rompe e forma un legame,mostra l ordine con cui si susseguono i vari stadi di formazione e di rottura dei
REAZIONI DI ADDIZIONE AL DOPPIO LEGAME NEGLI ALCHENI Un meccanismo di reazione, descrive come si rompe e forma un legame,mostra l ordine con cui si susseguono i vari stadi di formazione e di rottura dei
La barriera rotazionale attorno ad un doppio legame è di 50 Kcal / mol Due polimeri
 omposti organici che presentano uno o più doppi legami carbonio arbonio arattere non polare Molto poco solubili in acqua Densità più bassa dell acqua Grande presenza in natura NomenclaturaIUPA : Si identifica
omposti organici che presentano uno o più doppi legami carbonio arbonio arattere non polare Molto poco solubili in acqua Densità più bassa dell acqua Grande presenza in natura NomenclaturaIUPA : Si identifica
Gruppi funzionali. aldeidi
 Gruppi funzionali alcoli aldeidi chetoni Acidi carbossilici ' eteri ' esteri fenoli In grassetto il gruppo funzionale che definisce il carattere del composto 1 2 Gruppi funzionali: arrangiamento di pochi
Gruppi funzionali alcoli aldeidi chetoni Acidi carbossilici ' eteri ' esteri fenoli In grassetto il gruppo funzionale che definisce il carattere del composto 1 2 Gruppi funzionali: arrangiamento di pochi
Alchini (C n H 2n-2 ) Alcheni: idrocarburi insaturi con uno o più legami carbonio-carbonio doppi.
 himica rganica Alcheni Idrocarburi ( x y ) Alifatici Aromatici Alcani ( n 2n+2 ) Alcheni ( n 2n ) Alchini ( n 2n-2 ) icloalcani ( n 2n ) Alcheni: idrocarburi insaturi con uno o più legami carbonio-carbonio
himica rganica Alcheni Idrocarburi ( x y ) Alifatici Aromatici Alcani ( n 2n+2 ) Alcheni ( n 2n ) Alchini ( n 2n-2 ) icloalcani ( n 2n ) Alcheni: idrocarburi insaturi con uno o più legami carbonio-carbonio
Alchini. Francesca Anna Scaramuzzo, PhD
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alchini Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate per
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alchini Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate per
CHIMICA ORGANICA. Gli alchini
 1 C3-ALCHINI CHIMICA ORGANICA ALCHINI Formula generale C n n 2 Desinenza -ino Gli alchini Gli alchini sono caratterizzati dalla presenza di uno o più tripli legami carboniocarbonio e sono anch essi classificati
1 C3-ALCHINI CHIMICA ORGANICA ALCHINI Formula generale C n n 2 Desinenza -ino Gli alchini Gli alchini sono caratterizzati dalla presenza di uno o più tripli legami carboniocarbonio e sono anch essi classificati
CHIMICA ORGANICA. Gli alcheni
 1 2-ALENI IMIA ORGANIA ALENI Formula generale n 2n Desinenza -ene Gli alcheni La prima classe di idrocarburi insaturi è quella degli alcheni, detti anche olefine, che presentano lungo la catena uno o più
1 2-ALENI IMIA ORGANIA ALENI Formula generale n 2n Desinenza -ene Gli alcheni La prima classe di idrocarburi insaturi è quella degli alcheni, detti anche olefine, che presentano lungo la catena uno o più
Reazioni degli Alcheni
 Prof Mauro Tonellato Itis Natta Padova wwwpianetachimicait Reazioni degli Alcheni Indice delle reazioni 1) Addizione di acidi alogenidrici 2) Addizione di acqua ) Alogenazione 4) Formazione di aloidrine
Prof Mauro Tonellato Itis Natta Padova wwwpianetachimicait Reazioni degli Alcheni Indice delle reazioni 1) Addizione di acidi alogenidrici 2) Addizione di acqua ) Alogenazione 4) Formazione di aloidrine
Aromaticità. Addizione elettrofila alcheni
 Aromaticità Le molecole sono aromatiche se sono soddisfatte le seguenti condizioni: La molecola è ciclica La molecola è interamente coniugata La molecola è planare (atomi di carbonio con ibridazione sp
Aromaticità Le molecole sono aromatiche se sono soddisfatte le seguenti condizioni: La molecola è ciclica La molecola è interamente coniugata La molecola è planare (atomi di carbonio con ibridazione sp
R OH. alcol primario (1 ) alcol secondario (2 ) alcol terziario (3 )
 ALLI R Suffisso: -ol o olo R R R R R alcol primario (1 ) alcol secondario (2 ) alcol terziario (3 ) Si sceglie la catena carboniosa più lunga contenente anche l ossidrile e si deduce il nome dell alcano
ALLI R Suffisso: -ol o olo R R R R R alcol primario (1 ) alcol secondario (2 ) alcol terziario (3 ) Si sceglie la catena carboniosa più lunga contenente anche l ossidrile e si deduce il nome dell alcano
Reazioni degli alcoli
 Reazioni degli alcoli Indice: 1) Sintesi degli alcossidi. 2 2) Sintesi di Williamson degli eteri. 2 ) Trasformazione degli alcoli in alogenuri alchilici 4) Sintesi degli esteri. 6 5) Trasformazione degli
Reazioni degli alcoli Indice: 1) Sintesi degli alcossidi. 2 2) Sintesi di Williamson degli eteri. 2 ) Trasformazione degli alcoli in alogenuri alchilici 4) Sintesi degli esteri. 6 5) Trasformazione degli
Alcheni e alchini. idrocarburi. Insaturi C-C doppi/tripli. alcani. Saturi C-C semplici cicloalcani. aromatici
 Alcheni e alchini alcani Saturi C-C semplici cicloalcani idrocarburi Insaturi C-C doppi/tripli aromatici 1 Alcheni e Alchini Alcheni e alchini sono idrocarburi che hanno rispettivamente un doppio legame
Alcheni e alchini alcani Saturi C-C semplici cicloalcani idrocarburi Insaturi C-C doppi/tripli aromatici 1 Alcheni e Alchini Alcheni e alchini sono idrocarburi che hanno rispettivamente un doppio legame
Appunti di Chimica Organica Elementi per CdL Ostetricia CHIMICA ORGANICA. Appunti di Lezione. Elementi per il corso di Laurea In Ostetricia
 Appunti di himica Organica Elementi per dl Ostetricia IMIA ORGANIA Appunti di Lezione Elementi per il corso di Laurea In Ostetricia Autore: Roberto Zanrè A.A. 2009/2010 1 Appunti di himica Organica Elementi
Appunti di himica Organica Elementi per dl Ostetricia IMIA ORGANIA Appunti di Lezione Elementi per il corso di Laurea In Ostetricia Autore: Roberto Zanrè A.A. 2009/2010 1 Appunti di himica Organica Elementi
Alcoli, eteri, tioli, solfuri
 Alcoli, eteri, tioli, solfuri Alcoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Metanolo Sintesi industriale Tossico per l uomo (
Alcoli, eteri, tioli, solfuri Alcoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Metanolo Sintesi industriale Tossico per l uomo (
ALCOLI, ETERI, TIOLI. Alcool: molecola contenente un gruppo -OH legato ad un carbonio sp 3
 ALCOLI, ETERI, TIOLI Alcool: molecola contenente un gruppo -OH legato ad un carbonio sp 3 Etere: composto contenente un atomo di ossigeno legato a due carboni sp 3 Tiolo: molecola contenente un gruppo
ALCOLI, ETERI, TIOLI Alcool: molecola contenente un gruppo -OH legato ad un carbonio sp 3 Etere: composto contenente un atomo di ossigeno legato a due carboni sp 3 Tiolo: molecola contenente un gruppo
Introduzione alla Chimica Organica. Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display.
 Introduzione alla Chimica Organica Copyright The McGraw-ill Companies, Inc. Permission required for reproduction or display. 1 Elementi Comuni nei Composti Organici 2 Classificazione degli idrocarburi
Introduzione alla Chimica Organica Copyright The McGraw-ill Companies, Inc. Permission required for reproduction or display. 1 Elementi Comuni nei Composti Organici 2 Classificazione degli idrocarburi
prof. Mauro Tonellato ITIS Marconi Padova Alcheni
 prof Mauro Tonellato ITIS Marconi Padova Alcheni Indice delle reazioni 1 addizione di acidi alogenidrici 2 addizione di acqua alogenazione 4 formazione di aloidrine 5 idrogenazione catalitica 6 epossidazione
prof Mauro Tonellato ITIS Marconi Padova Alcheni Indice delle reazioni 1 addizione di acidi alogenidrici 2 addizione di acqua alogenazione 4 formazione di aloidrine 5 idrogenazione catalitica 6 epossidazione
ALCOLI, ETERI, TIOLI. Alcol: molecola contenente un gruppo -OH legato ad un carbonio sp 3
 ALCOLI, ETERI, TIOLI Alcol: molecola contenente un gruppo -OH legato ad un carbonio sp 3 Tiolo: molecola contenente un gruppo -SH legato ad un carbonio sp 3 Etere: composto contenente un atomo di ossigeno
ALCOLI, ETERI, TIOLI Alcol: molecola contenente un gruppo -OH legato ad un carbonio sp 3 Tiolo: molecola contenente un gruppo -SH legato ad un carbonio sp 3 Etere: composto contenente un atomo di ossigeno
Reazioni degli Alcheni e degli Alchini
 Reazioni degli Alcheni e degli Alchini Reazioni di addizione elettrofila La caratteristica comune a tutte le reazioni degli alcheni può essere riassunta dicendo che: gli elettroni del legame relativamente
Reazioni degli Alcheni e degli Alchini Reazioni di addizione elettrofila La caratteristica comune a tutte le reazioni degli alcheni può essere riassunta dicendo che: gli elettroni del legame relativamente
S N. Reazioni di Sostituzione Nucleofila. Nucleofilo: Nu: + C X C + Nu + X - Sostituzione Nucleofila:
 Reazioni di Sostituzione Nucleofila S N Sostituzione Nucleofila: Reazione in cui un nucleofilo è sostituito da un altro Nucleofilo: Atomo o gruppo che può donare una coppia di elettroni ad un altro atomo
Reazioni di Sostituzione Nucleofila S N Sostituzione Nucleofila: Reazione in cui un nucleofilo è sostituito da un altro Nucleofilo: Atomo o gruppo che può donare una coppia di elettroni ad un altro atomo
Alcoli, fenoli ed eteri
 Alcoli, fenoli ed eteri Alcoli e fenoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Fenoli: gruppo ossidrilico legato ad un anello aromatico Metanolo Sintesi industriale Tossico per l uomo
Alcoli, fenoli ed eteri Alcoli e fenoli Alcoli: gruppo ossidrilico legato ad un carbonio saturo Fenoli: gruppo ossidrilico legato ad un anello aromatico Metanolo Sintesi industriale Tossico per l uomo
Alcheni: struttura e proprietà
 Chimica Organica Informazione Scientifica sul Farmaco Alcheni: struttura e proprietà Organic Chemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: struttura degli alcheni nomenclatura proprietà fisiche
Chimica Organica Informazione Scientifica sul Farmaco Alcheni: struttura e proprietà Organic Chemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: struttura degli alcheni nomenclatura proprietà fisiche
Gli Alcheni : struttura e nomenclatura
 Gli Alcheni : struttura e nomenclatura Alcheni Gli alcheni sono idrocarburi che contengono un doppio legame carbonio-carbonio sono anche detti olefine o idrocarburi insaturi La formula molecolare è C n
Gli Alcheni : struttura e nomenclatura Alcheni Gli alcheni sono idrocarburi che contengono un doppio legame carbonio-carbonio sono anche detti olefine o idrocarburi insaturi La formula molecolare è C n
Unità didattica 7 (segue) Reattività del benzene. Il benzene è ricco di eletroni π, per cui è un nucleofilo che reagisce con gli elettrofili
 Unità didattica 7 (segue) Reattività del benzene Il benzene è ricco di eletroni π, per cui è un nucleofilo che reagisce con gli elettrofili Se avvenisse anche il secondo stadio dell addizione, il benzene
Unità didattica 7 (segue) Reattività del benzene Il benzene è ricco di eletroni π, per cui è un nucleofilo che reagisce con gli elettrofili Se avvenisse anche il secondo stadio dell addizione, il benzene
Ammine : caratteristiche strutturali
 Ammine : caratteristiche strutturali Le ammine sono composti formalmente derivanti dall ammoniaca in cui uno o più atomi di idrogeno sono stati sostituiti da gruppi alchilici Come per l ammonica l azoto
Ammine : caratteristiche strutturali Le ammine sono composti formalmente derivanti dall ammoniaca in cui uno o più atomi di idrogeno sono stati sostituiti da gruppi alchilici Come per l ammonica l azoto
SOSTITUZIONE NUCLEOFILA BIMOLECOLARE
 SOSTITUZIONE NUCLEOFILA BIMOLECOLARE Elettrofilo (atomo di C) Nucleofilo Alogenuri metilici, primari e molti secondari reagiscono con nucleofili attraverso un processo bimolecolare. 1 Processo a 10 e-,
SOSTITUZIONE NUCLEOFILA BIMOLECOLARE Elettrofilo (atomo di C) Nucleofilo Alogenuri metilici, primari e molti secondari reagiscono con nucleofili attraverso un processo bimolecolare. 1 Processo a 10 e-,
Sostituzione nucleofila Addizione a gruppi carbonilici Addizione a doppi legami attivati
 himica rganica II Sintesi di legami - Nella costruzione di molecole organiche complesse, gli stadi critici sono spesso quelli che comportano la formazione di legami carboni- carbonio. I legami - possono
himica rganica II Sintesi di legami - Nella costruzione di molecole organiche complesse, gli stadi critici sono spesso quelli che comportano la formazione di legami carboni- carbonio. I legami - possono
Acidi carbossilici e derivati
 Acidi carbossilici e derivati Acidi carbossilici Il gruppo funzionale di questa classe di sostanze è il carbossile: Il gruppo carbossilico è composto formalmente da un gruppo carbonilico legato ad un gruppo
Acidi carbossilici e derivati Acidi carbossilici Il gruppo funzionale di questa classe di sostanze è il carbossile: Il gruppo carbossilico è composto formalmente da un gruppo carbonilico legato ad un gruppo
REAZIONE DI SOSTITUZIONE NUCLEOFILA MONOMOLECOLARE SN1
 REAZIONE DI SOSTITUZIONE NUCLEOFILA MONOMOLECOLARE SN1 Gli alogenuri organici sono composti in cui un atomo di idrogeno è rimpiazzato con un atomo di alogeno. I due tipi di alogenuri organici più comuni
REAZIONE DI SOSTITUZIONE NUCLEOFILA MONOMOLECOLARE SN1 Gli alogenuri organici sono composti in cui un atomo di idrogeno è rimpiazzato con un atomo di alogeno. I due tipi di alogenuri organici più comuni
DIENI CONIUGATI. ADDIZIONE DI HCl. addotto 1,2 80% 20%
 DIENI NIUGATI wwwpianetachimicait I dieni coniugati sono diversi dai dieni isolati perché hanno lunghezze anomale dei legami e perché sono più stabili termodinamicamente dato che liberano meno energia
DIENI NIUGATI wwwpianetachimicait I dieni coniugati sono diversi dai dieni isolati perché hanno lunghezze anomale dei legami e perché sono più stabili termodinamicamente dato che liberano meno energia
COMPOSTI AROMATICI. Formula C 6 H 6
 COMPOSTI AROMATICI Gli alcani ed alcheni hanno diversa reattività chimica. Vi è un altra classe di idrocarburi che pur essendo insaturi hanno un comportamento chimico diverso dagli alcheni Sono i composti
COMPOSTI AROMATICI Gli alcani ed alcheni hanno diversa reattività chimica. Vi è un altra classe di idrocarburi che pur essendo insaturi hanno un comportamento chimico diverso dagli alcheni Sono i composti
CHIMICA ORGANICA I E LABORATORIO M - Z
 DIPARTIMENTO DI SCIENZE CHIMICHE Corso di laurea in Chimica Anno accademico 2016/2017-1 anno CHIMICA ORGANICA I E LABORATORIO M - Z 12 CFU - 2 semestre Docenti titolari dell'insegnamento SALVATORE FOTI
DIPARTIMENTO DI SCIENZE CHIMICHE Corso di laurea in Chimica Anno accademico 2016/2017-1 anno CHIMICA ORGANICA I E LABORATORIO M - Z 12 CFU - 2 semestre Docenti titolari dell'insegnamento SALVATORE FOTI
Nomenclatura. Gli idrocarburi alifatici
 Gli idrocarburi alifatici Gli idrocarburi sono i composti organici più semplici, sono infatti costituiti solo da carbonio e idrogeno (da cui il nome, appunto, di idro-carburi). Pur essendo relativamente
Gli idrocarburi alifatici Gli idrocarburi sono i composti organici più semplici, sono infatti costituiti solo da carbonio e idrogeno (da cui il nome, appunto, di idro-carburi). Pur essendo relativamente
Composti carbonilici Acidi carbossilici
 Composti carbonilici Acidi carbossilici Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli
Composti carbonilici Acidi carbossilici Acidi carbossilici: nomenclatura alcano -> acido alcanoico Acidi carbossilici: proprietà Il gruppo carbossilico ha caratteristiche comuni ai chetoni (C=O) e agli
IDROCARBURI AROMATICI
 IDROCARBURI AROMATICI IL BENZENE E una sostanza chimica liquida e incolore dal caratteristico odore aromatico pungente. A temperatura ambiente volatilizza assai facilmente. La maggior parte del benzene
IDROCARBURI AROMATICI IL BENZENE E una sostanza chimica liquida e incolore dal caratteristico odore aromatico pungente. A temperatura ambiente volatilizza assai facilmente. La maggior parte del benzene
Reazioni degli epossidi
 12-04-2016 Reazioni degli epossidi Apertura dell anello acido-catalizzata, esempi Struttura intermedio: 3 forme limiti di risonanza H H a a O O b b H O CH 3 CH 3 CH 3 H H H H Struttura ibrido intermedio
12-04-2016 Reazioni degli epossidi Apertura dell anello acido-catalizzata, esempi Struttura intermedio: 3 forme limiti di risonanza H H a a O O b b H O CH 3 CH 3 CH 3 H H H H Struttura ibrido intermedio
Aldeidi e chetoni. Struttura e proprietà Nomenclatura e nomi comuni Fonti Reazioni Principali aldeidi e chetoni
 Aldeidi e chetoni Struttura e proprietà Nomenclatura e nomi comuni Fonti Reazioni Principali aldeidi e chetoni Aldeidi e chetoni Aldeidi e chetoni Aldeidi e chetoni Il legame = è costituito da un legame
Aldeidi e chetoni Struttura e proprietà Nomenclatura e nomi comuni Fonti Reazioni Principali aldeidi e chetoni Aldeidi e chetoni Aldeidi e chetoni Aldeidi e chetoni Il legame = è costituito da un legame
Corso di Laurea in CTF Esame di CHIMICA ORGANICA II del 04 febbraio 2016
 Corso di Laurea in CTF Esame di CHIMICA RGAICA II del 04 febbraio 2016 1. Identificate il prodotto e discutete dettagliatamente la seguente reazione: 2. Progettate una via sintetica che porti alla formazione
Corso di Laurea in CTF Esame di CHIMICA RGAICA II del 04 febbraio 2016 1. Identificate il prodotto e discutete dettagliatamente la seguente reazione: 2. Progettate una via sintetica che porti alla formazione
Complementi di Chimica Organica. Composti Aromatici: Benzene C 6 H 6 (1825) (1865) Friedrich August Kekulé
 Composti Aromatici: Benzene C 6 6 (1825) (1865) Friedrich August Kekulé Composti Aromatici: Benzene, energia di coniugazione = -119.5 KJ/mol (-119.2 x 3 = -357.6) = -208.2 KJ/mol -357.6 KJ/mol (-208.2
Composti Aromatici: Benzene C 6 6 (1825) (1865) Friedrich August Kekulé Composti Aromatici: Benzene, energia di coniugazione = -119.5 KJ/mol (-119.2 x 3 = -357.6) = -208.2 KJ/mol -357.6 KJ/mol (-208.2
COMPOSTI AROMATICI POLICICLICI
 CHIMICA DEI COMPOSTI AROMATICI POLICICLICI CHIMICA DI PIRROLO, FURANO E TIOFENE CHIMICA DI IMIDAZOLI, OSSAZOLI E TIAZOLI CHIMICA DI ISOSSAZOLI, PIRAZOLI, ISOTIAZOLI LEZIONE 5 COMPOSTI AROMATICI POLICICLICI
CHIMICA DEI COMPOSTI AROMATICI POLICICLICI CHIMICA DI PIRROLO, FURANO E TIOFENE CHIMICA DI IMIDAZOLI, OSSAZOLI E TIAZOLI CHIMICA DI ISOSSAZOLI, PIRAZOLI, ISOTIAZOLI LEZIONE 5 COMPOSTI AROMATICI POLICICLICI
G. Licini, Università di Padova. La riproduzione a fini commerciali è vietata
 SSTITUZINI NUCLEFILE H H H H H + HBr + H H 2 H Br SUBSTRATI alogenuri, eteri, epossidi, esteri solfonici Possibili meccanismi S N 1, S N 2, S N 2, S n i 1 Generalità Gruppo uscente (LG) deve essere una
SSTITUZINI NUCLEFILE H H H H H + HBr + H H 2 H Br SUBSTRATI alogenuri, eteri, epossidi, esteri solfonici Possibili meccanismi S N 1, S N 2, S N 2, S n i 1 Generalità Gruppo uscente (LG) deve essere una
Proprietà fisiche di Alcani e Cicloalcani
 Proprietà fisiche di Alcani e Cicloalcani PUNTI DI EBOLLIZIONE DEGLI ALCANI sono regolati dalla entità delle forze di attrazione intermolecolari gli alcani sono composti non polari per cui non entrano
Proprietà fisiche di Alcani e Cicloalcani PUNTI DI EBOLLIZIONE DEGLI ALCANI sono regolati dalla entità delle forze di attrazione intermolecolari gli alcani sono composti non polari per cui non entrano
Programma di CHIMICA ORGANICA AA Corso di laurea in Farmacia Docente: Prof. Rocco RACIOPPI.
 Programma di CHIMICA ORGANICA AA. 2012-2013 Corso di laurea in Farmacia Docente: Prof. Rocco RACIOPPI e-mail rocco.racioppi@unibas.it Orario di ricevimento: lunedì, martedì e mercoledì dalle ore 11,30
Programma di CHIMICA ORGANICA AA. 2012-2013 Corso di laurea in Farmacia Docente: Prof. Rocco RACIOPPI e-mail rocco.racioppi@unibas.it Orario di ricevimento: lunedì, martedì e mercoledì dalle ore 11,30
Gli idrocarburi e il petrolio
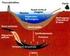 Gli idrocarburi e il petrolio Le proprietà degli atomi di carbonio di legarsi fra loro mediante legami semplici, doppi, tripli, formando catene stabili delle più diverse forme e lunghezze rende praticamente
Gli idrocarburi e il petrolio Le proprietà degli atomi di carbonio di legarsi fra loro mediante legami semplici, doppi, tripli, formando catene stabili delle più diverse forme e lunghezze rende praticamente
Composti organici del silicio
 Composti organici del silicio e B C N O F Ne P S Ar Br Kr : 1s 2 2s 2 2p 6 3s 2 3p 2 3d 0 Il silicio è un elemento della seconda riga della tavole periodica, è più grande, meno elettronegativo e più polarizzabile
Composti organici del silicio e B C N O F Ne P S Ar Br Kr : 1s 2 2s 2 2p 6 3s 2 3p 2 3d 0 Il silicio è un elemento della seconda riga della tavole periodica, è più grande, meno elettronegativo e più polarizzabile
Composti carbonilici: reazioni al carbonio in posizione a
 Composti carbonilici: reazioni al carbonio in posizione a Addizione nucleofila a composti carbonilici a,b-insaturi Nelle molecole contenenti carbonili coniugati con doppi legami sono presenti due siti
Composti carbonilici: reazioni al carbonio in posizione a Addizione nucleofila a composti carbonilici a,b-insaturi Nelle molecole contenenti carbonili coniugati con doppi legami sono presenti due siti
1. COS È LA CHIMICA ORGANICA?
 Università degli Studi di Bari Dipartimento di Farmacia Scienze del Farmaco Corso di Laurea in Tecniche Erboristiche A.A. 2013-2014 Chimica Organica Prof. Giuseppe Gerardo Carbonara Finalità. Scopo del
Università degli Studi di Bari Dipartimento di Farmacia Scienze del Farmaco Corso di Laurea in Tecniche Erboristiche A.A. 2013-2014 Chimica Organica Prof. Giuseppe Gerardo Carbonara Finalità. Scopo del
ETOILEPEDIA IL LEGAME CHIMICO
 IL LEGAME CHIMICO La teoria quantistica ha introdotto il concetto di valenza, cioè della capacità di un atomo di formare un determinato numero di legami a seconda della propria configurazione elettronica;
IL LEGAME CHIMICO La teoria quantistica ha introdotto il concetto di valenza, cioè della capacità di un atomo di formare un determinato numero di legami a seconda della propria configurazione elettronica;
CHIMICA ORGANICA - CLASSE 3 - RISPOSTE
 CHIMICA ORGANICA - CLASSE 3 - RISPOSTE Prof: Anna Rosa MASTELLARI. Specializzazione di CHIMICA Testo: CHIMICA ORGANICA, BIORGANICA E LABORATORIO ALCANI E CICLOALCANI (Capitolo 2) 1. Assegnare la nomenclatura
CHIMICA ORGANICA - CLASSE 3 - RISPOSTE Prof: Anna Rosa MASTELLARI. Specializzazione di CHIMICA Testo: CHIMICA ORGANICA, BIORGANICA E LABORATORIO ALCANI E CICLOALCANI (Capitolo 2) 1. Assegnare la nomenclatura
CHIMICA ORGANICA. Gli alcoli
 1 E1-ALCOLI CIMICA OGANICA ALCOLI Formula generale Desinenza -olo Gli alcoli Gli alcoli sono, dopo gli idrocarburi, i composti organici più comuni, che è possibile considerare come derivati dagli alcani
1 E1-ALCOLI CIMICA OGANICA ALCOLI Formula generale Desinenza -olo Gli alcoli Gli alcoli sono, dopo gli idrocarburi, i composti organici più comuni, che è possibile considerare come derivati dagli alcani
Ammine R N + H. ammina terziaria ammina secondaria ammina primaria sale di ammonio quaternario
 AMMINE Ammine Le ammine possono essere considerate dei derivati dell ammoniaca in cui uno o più atomi di idrogeno sono stati sostituiti con gruppi alchilici o arilici. Il simbolo generale per una ammina
AMMINE Ammine Le ammine possono essere considerate dei derivati dell ammoniaca in cui uno o più atomi di idrogeno sono stati sostituiti con gruppi alchilici o arilici. Il simbolo generale per una ammina
PIRIDINA N coinvolto nel ciclo non partecipa all aromaticità con i suoi elettroni N: coppia di non legame all esterno dell anello comportamento
 PIRIDINE LEZIONE 6 PIRIDINA N coinvolto nel ciclo non partecipa all aromaticità con i suoi elettroni N: coppia di non legame all esterno dell anello comportamento basico (pka=5.2) Nucleo della piridina
PIRIDINE LEZIONE 6 PIRIDINA N coinvolto nel ciclo non partecipa all aromaticità con i suoi elettroni N: coppia di non legame all esterno dell anello comportamento basico (pka=5.2) Nucleo della piridina
Isomeri. Unità didattica 5. Isomeri cis-trans. La stereochimica. I composti achirali hanno immagini speculari sovrapponibili
 Isomeri Composti non identici ma che hanno la stessa formula molecolare Unità didattica 5 La stereochimica La disposizione degli atomi nello spazio; La stereochimica delle reazioni di addizione Isomeri
Isomeri Composti non identici ma che hanno la stessa formula molecolare Unità didattica 5 La stereochimica La disposizione degli atomi nello spazio; La stereochimica delle reazioni di addizione Isomeri
DISSOLUZIONE DEI SALI IN ACQUA
 1 DISSLUZINE DEI SALI IN ACQUA 1. La dissoluzione di un sale è un equilibrio. 2. Diversi Sali hanno diverse solubilità (K ps ). 3. La solubilità dipende dall energia del reticolo ionico (U) e dall entalpia
1 DISSLUZINE DEI SALI IN ACQUA 1. La dissoluzione di un sale è un equilibrio. 2. Diversi Sali hanno diverse solubilità (K ps ). 3. La solubilità dipende dall energia del reticolo ionico (U) e dall entalpia
AMMINE. con acidi RNH 2. con O come elettrofilo RNH 2 + H + + R NH 3 NESSUNA REAZIONE. atomo basico, atomo nucleofilo
 AMME : 2 1. come atomo basico o nucleofilo atomo basico, atomo nucleofilo cattivo gruppo uscente, anche in seguito a protonazione ESSUA EAZE con acidi 2 con come elettrofilo SL con ammine terziarie 2 2
AMME : 2 1. come atomo basico o nucleofilo atomo basico, atomo nucleofilo cattivo gruppo uscente, anche in seguito a protonazione ESSUA EAZE con acidi 2 con come elettrofilo SL con ammine terziarie 2 2
N H CH 3 H 3 C. Ammine. Struttura. Classificazione. Nomenclatura. Reattività
 Ammine Struttura lassificazione omenclatura Reattività 3 3 elle ammine gli orbitali dell azoto sono ibridati sp 3. 3 degli orbitali ibridi sono impegnati nella formazione di legami con o. Il quarto orbitale
Ammine Struttura lassificazione omenclatura Reattività 3 3 elle ammine gli orbitali dell azoto sono ibridati sp 3. 3 degli orbitali ibridi sono impegnati nella formazione di legami con o. Il quarto orbitale
TAVOLA PERIODICA DEGLI ELEMENTI
 TAVOLA PERIODIA DEGLI ELEMENTI Idrogeno = 1 legame Ossigeno = 2 legami O Azoto = 3 legami N arbonio = 4 legami Questi sono gli atomi che intervengono maggiormente nelle reazioni che tratteremo nella
TAVOLA PERIODIA DEGLI ELEMENTI Idrogeno = 1 legame Ossigeno = 2 legami O Azoto = 3 legami N arbonio = 4 legami Questi sono gli atomi che intervengono maggiormente nelle reazioni che tratteremo nella
Indice generale. 1 Struttura e proprietà delle molecole organiche 1. 2 Struttura e reattività degli alcani 53 XIII. Prefazione
 Indice generale Prefazione XIII 1 Struttura e proprietà delle molecole organiche 1 Forze di legame, orbitali atomici e molecolari, acidità e basicità, molecole polari e apolari 1.1 Lo scopo della chimica
Indice generale Prefazione XIII 1 Struttura e proprietà delle molecole organiche 1 Forze di legame, orbitali atomici e molecolari, acidità e basicità, molecole polari e apolari 1.1 Lo scopo della chimica
Forze intermolecolari
 Forze intermolecolari Sono le forze che si instaurano tra le molecole di un composto e ne determinano lo stato di aggregazione (gas, liquido, solido) interazioni dipolo-dipolo attrazioni di van der Waals
Forze intermolecolari Sono le forze che si instaurano tra le molecole di un composto e ne determinano lo stato di aggregazione (gas, liquido, solido) interazioni dipolo-dipolo attrazioni di van der Waals
Idrocarburi aromatici. Idrocarburi. Idrocarburi
 Lezioni di himica Generale Elementi chimica organica Prof. Roberto Sebastiano Idrocarburi 1 Molecole costituite solo da atomi di carbonio e idrogeno Idrocarburi alifatici Idrocarburi saturi, solo legami
Lezioni di himica Generale Elementi chimica organica Prof. Roberto Sebastiano Idrocarburi 1 Molecole costituite solo da atomi di carbonio e idrogeno Idrocarburi alifatici Idrocarburi saturi, solo legami
Composti aromatici. Il capofamiglia... il benzene. Scoperta del benzene
 Scoperta del benzene Composti aromatici Prof.ssa Silvia ecchia Il capofamiglia... il benzene Una molecola può essere definita aromatica se contiene almeno un anello aromatico, cioè un anello composto da
Scoperta del benzene Composti aromatici Prof.ssa Silvia ecchia Il capofamiglia... il benzene Una molecola può essere definita aromatica se contiene almeno un anello aromatico, cioè un anello composto da
Ricerca qualitativa degli elementi
 Ricerca qualitativa degli elementi Identificazione degli elementi presenti nella struttura molecolare Riconoscimento di azoto, zolfo ed alogeni: Saggio di Lassaigne Il riconoscimento si basa sulla mineralizzazione
Ricerca qualitativa degli elementi Identificazione degli elementi presenti nella struttura molecolare Riconoscimento di azoto, zolfo ed alogeni: Saggio di Lassaigne Il riconoscimento si basa sulla mineralizzazione
Reazioni di Chimica Organica
 Reazioni di Chimica Organica 1. Sostituzione CH 4 + Cl 2 + energia > CH 3 Cl + HCl 2. Addizione C =C + XY C C X Y 3. Eliminazione 4. Riarrangiamento 1 Elettrofili e Nucleofili Reagenti elettrofili: composti
Reazioni di Chimica Organica 1. Sostituzione CH 4 + Cl 2 + energia > CH 3 Cl + HCl 2. Addizione C =C + XY C C X Y 3. Eliminazione 4. Riarrangiamento 1 Elettrofili e Nucleofili Reagenti elettrofili: composti
Alogenuri Alchilici R-Cl R-Br R-I R-F
 Alogenuri Alchilici R-Cl R-Br R-I I R-FR Alogenoalcani I composti contenenti un atomo di alogeno legato covalentemente ad un atomo di carbonio ibridato sp 3 sono chiamati alogenoalcani o alogenuri alchilici.
Alogenuri Alchilici R-Cl R-Br R-I I R-FR Alogenoalcani I composti contenenti un atomo di alogeno legato covalentemente ad un atomo di carbonio ibridato sp 3 sono chiamati alogenoalcani o alogenuri alchilici.
Capitolo 24 Le famiglie dei composti organici
 Capitolo 24 Le famiglie dei composti organici DOMANDE ED ESERCIZI (versione integrale) 24.1 I composti organici sono raggruppati in famiglie 1. Che cosa si intende per gruppo funzionale? Scrivi le formule
Capitolo 24 Le famiglie dei composti organici DOMANDE ED ESERCIZI (versione integrale) 24.1 I composti organici sono raggruppati in famiglie 1. Che cosa si intende per gruppo funzionale? Scrivi le formule
ALDEIDI E CHETONI. Struttura e proprietà. Il gruppo carbonilico. Reattività dei composti carbonilici IL GRUPPO CARBONILICO C O R C
 Struttura e proprietà ALDEIDI E ETNI ALDEIDI E ETNI NTENGN IL GUPP ABNILI Molti altri composti presentano questo gruppo: Acili, acidi, esteri, ammidi, carboidrati, proteine Il gruppo carbonilico E il più
Struttura e proprietà ALDEIDI E ETNI ALDEIDI E ETNI NTENGN IL GUPP ABNILI Molti altri composti presentano questo gruppo: Acili, acidi, esteri, ammidi, carboidrati, proteine Il gruppo carbonilico E il più
REAZIONI DI ADDIZIONE-ELIMINAZIONE DI ALDEIDI E CHETONI
 REAZIONI DI ADDIZIONE-ELIMINAZIONE DI ALDEIDI E CHETONI L azoto nucleofilo dell ammina attacca il carbonio elettrofilo del chetone Come potremmo rendere questa reazione più facile? Emiamminale La velocità
REAZIONI DI ADDIZIONE-ELIMINAZIONE DI ALDEIDI E CHETONI L azoto nucleofilo dell ammina attacca il carbonio elettrofilo del chetone Come potremmo rendere questa reazione più facile? Emiamminale La velocità
Addizioni Nucleofile di Enolati a Composti Carbonilici
 Addizioni Nucleofile di Enolati a Composti Carbonilici L addizione di nucleofili all ossigeno, azoto, zolfo a composti carbonilici è una reazione che avete già incontrato e studiato. Anche nucleofili al
Addizioni Nucleofile di Enolati a Composti Carbonilici L addizione di nucleofili all ossigeno, azoto, zolfo a composti carbonilici è una reazione che avete già incontrato e studiato. Anche nucleofili al
Stampa Preventivo. A.S Pagina 1 di 8
 Stampa Preventivo A.S. 2009-2010 Pagina 1 di 8 Insegnante POLESEL Classe 4LTS ART Materia chimica organica e biochimica preventivo consuntivo 106 0 titolo modulo 1. Idrocarburi 2. Composti ossigenati 3.
Stampa Preventivo A.S. 2009-2010 Pagina 1 di 8 Insegnante POLESEL Classe 4LTS ART Materia chimica organica e biochimica preventivo consuntivo 106 0 titolo modulo 1. Idrocarburi 2. Composti ossigenati 3.
Nome degli alcheni a catena lineare
 Gli alcheni sono idrocarboni insaturi. insaturi (almeno un doppio legame) idrocarboni (solo e ) n 2n 1-Esene 6 12 opyright 1999, Michael J. Wovkulich. All rights reserved. Nome degli alcheni a catena lineare
Gli alcheni sono idrocarboni insaturi. insaturi (almeno un doppio legame) idrocarboni (solo e ) n 2n 1-Esene 6 12 opyright 1999, Michael J. Wovkulich. All rights reserved. Nome degli alcheni a catena lineare
ACIDI CARBOSSILICI. ac. formico ac. acetico ac. benzoico
 ACIDI CARBOSSILICI ac. formico ac. acetico ac. benzoico Nomenclatura Nomenclatura acido malonico Acidi bicarbossilici a catena alifatica Proprietà fisiche I primi termini della serie sono liquidi incolori
ACIDI CARBOSSILICI ac. formico ac. acetico ac. benzoico Nomenclatura Nomenclatura acido malonico Acidi bicarbossilici a catena alifatica Proprietà fisiche I primi termini della serie sono liquidi incolori
DIENI CONIUGATI E ALCHINI
 Prof Mauro Tonellato ITI Marconi - Padova DIENI NIUGATI E ALINI M LUM wwwpianetachimicait DIENI NIUGATI In un diene i doppi legami sono detti cumulati se sono consecutivi, coniugati se sono separati da
Prof Mauro Tonellato ITI Marconi - Padova DIENI NIUGATI E ALINI M LUM wwwpianetachimicait DIENI NIUGATI In un diene i doppi legami sono detti cumulati se sono consecutivi, coniugati se sono separati da
PIANO DI LAVORO ANNUALE
 PIANO DI LAVORO ANNUALE Classe 3B A.S. 2013-14 Disciplina: Chimica Organica Docente: prof. Laura M. Iannone Ore settimanali: 4 Libro di testo: Percorsi di Chimica Organica, di Paolo De Maria ed. Zanichelli.
PIANO DI LAVORO ANNUALE Classe 3B A.S. 2013-14 Disciplina: Chimica Organica Docente: prof. Laura M. Iannone Ore settimanali: 4 Libro di testo: Percorsi di Chimica Organica, di Paolo De Maria ed. Zanichelli.
BENZENE E DERIVATI. Composto aromatico: termine usato per indicare il benzene ed i suoi derivati C 6 H 6. Arene: Idrocarburo aromatico
 BENZENE E DERIVATI Composto aromatico: termine usato per indicare il benzene ed i suoi derivati C 6 H 6 Arene: Idrocarburo aromatico Gruppo arilico: gruppo sostituente che deriva da un arene per rimozione
BENZENE E DERIVATI Composto aromatico: termine usato per indicare il benzene ed i suoi derivati C 6 H 6 Arene: Idrocarburo aromatico Gruppo arilico: gruppo sostituente che deriva da un arene per rimozione
Capitolo 13 Acidi Carbossilici e Derivati
 himica rganica Informazione Scientifica sul Farmaco apitolo 13 Acidi arbossilici e Derivati rganic hemistry, 5 th Edition L. G. Wade, Jr. Prentice Hall rganic hemistry, 3 rd Edition Paula Y. Bruice, Prentice
himica rganica Informazione Scientifica sul Farmaco apitolo 13 Acidi arbossilici e Derivati rganic hemistry, 5 th Edition L. G. Wade, Jr. Prentice Hall rganic hemistry, 3 rd Edition Paula Y. Bruice, Prentice
Figura. Benzene e aromaticità
 Figura Benzene e aromaticità Benzene e composti aromatici dal carbone da ciliegie pesche mandorle dal balsamo di Tolu Benzene e composti aromatici ormone steroideo naturale analgesico naturale tranquillante
Figura Benzene e aromaticità Benzene e composti aromatici dal carbone da ciliegie pesche mandorle dal balsamo di Tolu Benzene e composti aromatici ormone steroideo naturale analgesico naturale tranquillante
Capitolo 23 Dal carbonio agli idrocarburi
 Capitolo 23 Dal carbonio agli idrocarburi 1. I composti organici 2. Gli idrocarburi saturi: alcani e cicloalcani 3. L isomeria 4. La nomenclatura degli idrocarburi saturi 5. Proprietà fisiche e chimiche
Capitolo 23 Dal carbonio agli idrocarburi 1. I composti organici 2. Gli idrocarburi saturi: alcani e cicloalcani 3. L isomeria 4. La nomenclatura degli idrocarburi saturi 5. Proprietà fisiche e chimiche
Alogenuri Alchilici (o aloalcani)
 Capitolo 6 Alogenuri Alchilici: Sostituzioni Nucleofiliche ed Eliminazioni Alogenuri Alchilici (o aloalcani) Composti con un atomo di alogeno legato ad un carbonio sp 3 Diffusi in natura, raramente coinvolti
Capitolo 6 Alogenuri Alchilici: Sostituzioni Nucleofiliche ed Eliminazioni Alogenuri Alchilici (o aloalcani) Composti con un atomo di alogeno legato ad un carbonio sp 3 Diffusi in natura, raramente coinvolti
Il pentano ha 3 isomeri di catena CH 3 CH CH 2 CH 3 CH 3 C CH 3 CH 3 CH 2 CH 2 CH 2 CH 3 CH 3. Formula schematica. Formula razionale.
 Il pentano ha 3 isomeri di catena normalpentano Isopentano (2-metilbutano) Neopentano (2,2-dimetilpropano) CH 3 CH 2 CH 2 CH 2 CH 3 CH 3 CH CH 2 CH 3 CH 3 CH 3 CH 3 C CH 3 CH 3 Formula grezza Formula schematica
Il pentano ha 3 isomeri di catena normalpentano Isopentano (2-metilbutano) Neopentano (2,2-dimetilpropano) CH 3 CH 2 CH 2 CH 2 CH 3 CH 3 CH CH 2 CH 3 CH 3 CH 3 CH 3 C CH 3 CH 3 Formula grezza Formula schematica
ALCOLI ed ETERI. Glicerolo (glicerina) Mentolo Colesterolo
 ALLI ed ETEI La sostituzione formale di un idrogeno dell acqua con un radicale alchilico, oppure la sostituzione di un in un alcano con il gruppo (idrossilico), porta ad un alcol. La sostituzione di entrambi
ALLI ed ETEI La sostituzione formale di un idrogeno dell acqua con un radicale alchilico, oppure la sostituzione di un in un alcano con il gruppo (idrossilico), porta ad un alcol. La sostituzione di entrambi
Problema n.1 Bilanciare la seguente reazione redox utilizzando il metodo ionico elettronico: H 2 O 2(aq) + MnO 4
 Problema n.1 Bilanciare la seguente reazione redox utilizzando il metodo ionico elettronico: 2 2(aq) + Mn 4 -(aq) 2(g) + Mn 2(s) + - (aq) + 2 (l). Calcolare il volume di 2 (g), misurato a 1.0 atm e 25
Problema n.1 Bilanciare la seguente reazione redox utilizzando il metodo ionico elettronico: 2 2(aq) + Mn 4 -(aq) 2(g) + Mn 2(s) + - (aq) + 2 (l). Calcolare il volume di 2 (g), misurato a 1.0 atm e 25
LA CHIMICA DEL CARBONIO
 LA CHIMICA DEL CARBONIO E QUELLA PARTE DELLA CHIMICA CHE STUDIA IL CARBONIO E TUTTI I SUOI DERIVATI. I COMPOSTI DEL CARBONIO POSSONO ESSERE NATURALI (PROTEINE, ACIDI NUCLEICI, LIPIDI E CARBOIDRATI) O ESSERE
LA CHIMICA DEL CARBONIO E QUELLA PARTE DELLA CHIMICA CHE STUDIA IL CARBONIO E TUTTI I SUOI DERIVATI. I COMPOSTI DEL CARBONIO POSSONO ESSERE NATURALI (PROTEINE, ACIDI NUCLEICI, LIPIDI E CARBOIDRATI) O ESSERE
Acidi e Basi. Capitolo 15
 Acidi e Basi Capitolo 15 Acidi Hanno un sapore agro. L aceto deve il suo sapore all acido acetico Gli agrumi contengono acido citrico. Provocano il cambio di colore nei coloranti vegetali. Reagiscono con
Acidi e Basi Capitolo 15 Acidi Hanno un sapore agro. L aceto deve il suo sapore all acido acetico Gli agrumi contengono acido citrico. Provocano il cambio di colore nei coloranti vegetali. Reagiscono con
CHIMICA II (CHIMICA ORGANICA)
 CHIMICA II (CHIMICA ORGANICA) Prof. Gennaro Piccialli Prof. Aldo Galeone Prof. Giorgia Oliviero Testo Consigliato: gruppo 1 (matricole A-E) gruppo 2 (matricole F-O) gruppo 3 (matricole P-Z) Introduzione
CHIMICA II (CHIMICA ORGANICA) Prof. Gennaro Piccialli Prof. Aldo Galeone Prof. Giorgia Oliviero Testo Consigliato: gruppo 1 (matricole A-E) gruppo 2 (matricole F-O) gruppo 3 (matricole P-Z) Introduzione
Composti Carbonilici
 omposti arbonilici 1 Introduzione Due grandi classi di composti contengono il gruppo carbonilico: 1. omposti che hanno solo atomi di carbonio e di idrogeno legati al carbonile: aldeidi e chetoni. aldeidi
omposti arbonilici 1 Introduzione Due grandi classi di composti contengono il gruppo carbonilico: 1. omposti che hanno solo atomi di carbonio e di idrogeno legati al carbonile: aldeidi e chetoni. aldeidi
Aldeidi e chetoni. 1) Rottura α 2) Rottura i. Più pronunciate nei chetoni. 3) Rottura β con trasposizione di H in γ (McLafferty)
 Aldeidi e chetoni Hanno potenziale di ionizzazione inferiore a quello degli alcooli dunque lo ione molecolare è più intenso e più facilmente osservabile anche in aldeidi e chetoni superiori. 1) Rottura
Aldeidi e chetoni Hanno potenziale di ionizzazione inferiore a quello degli alcooli dunque lo ione molecolare è più intenso e più facilmente osservabile anche in aldeidi e chetoni superiori. 1) Rottura
Teorie Acido-Base. valutazione degli acidi
 Teorie Acido-Base valutazione degli acidi Teoria di Brønsted-Lowry Acidi donano ioni H + Basi accettano ioni H + CH 3 C 2 H + H 2 CH 3 C 2 + H 3 + acido acetico CH 3 NH 2 + H 2 CH 3 NH 3+ + H metilammina
Teorie Acido-Base valutazione degli acidi Teoria di Brønsted-Lowry Acidi donano ioni H + Basi accettano ioni H + CH 3 C 2 H + H 2 CH 3 C 2 + H 3 + acido acetico CH 3 NH 2 + H 2 CH 3 NH 3+ + H metilammina
CORSO DI LAUREA IN SCIENZE BIOLOGICHE III GRUPPO Prof. Antonio Evidente Monte S. Angelo 1P-14. Descrizione dell insegnamento
 CORSO DI LAUREA IN SCIENZE BIOLOGICHE III GRUPPO Prof. Antonio Evidente Monte S. Angelo 1P-14 Insegnamento: Chimica organica Descrizione dell insegnamento Settore Scientifico- Disciplinare: CHIM/06 CFU:
CORSO DI LAUREA IN SCIENZE BIOLOGICHE III GRUPPO Prof. Antonio Evidente Monte S. Angelo 1P-14 Insegnamento: Chimica organica Descrizione dell insegnamento Settore Scientifico- Disciplinare: CHIM/06 CFU:
26 Aprile 1915, 81 compleanno
 Reazioni di addizione-eliminazione eliminazione di composti carbonilici Ammine primarie reagiscono con composti carbonilici per dare immine, anche denominate basi di Schiff 1 Ugo Shiff (1834-1915) 1915)
Reazioni di addizione-eliminazione eliminazione di composti carbonilici Ammine primarie reagiscono con composti carbonilici per dare immine, anche denominate basi di Schiff 1 Ugo Shiff (1834-1915) 1915)
Lezione 5. Alogenuri, alcoli, fenoli ed eteri
 Lezione 5 Alogenuri, alcoli, fenoli ed eteri 1 I gruppi funzionali Un gruppo funzionale è un atomo o un gruppo di atomi che determina le proprietà chimiche di un composto organico, permettendone la classificazione.
Lezione 5 Alogenuri, alcoli, fenoli ed eteri 1 I gruppi funzionali Un gruppo funzionale è un atomo o un gruppo di atomi che determina le proprietà chimiche di un composto organico, permettendone la classificazione.
LIPIDI. I lipidi sono suddivisi in due gruppi principali.
 LIPIDI I lipidi sono una classe eterogenea di composti organici, raggruppati sulla base della loro solubilità. Sono insolubili in acqua, ma solubili nei solventi organici non polari, quali l etere dietilico,
LIPIDI I lipidi sono una classe eterogenea di composti organici, raggruppati sulla base della loro solubilità. Sono insolubili in acqua, ma solubili nei solventi organici non polari, quali l etere dietilico,
Composti organici dello zolfo
 Complementi di Chimica rganica Composti organici dello zolfo He B C e i P Cl Ar Br Kr : 1s 2 2s 2 2p 6 3s 2 3p 4 3d 0 Lo zolfo è un elemento della seconda riga della tavole periodica, è più grande, meno
Complementi di Chimica rganica Composti organici dello zolfo He B C e i P Cl Ar Br Kr : 1s 2 2s 2 2p 6 3s 2 3p 4 3d 0 Lo zolfo è un elemento della seconda riga della tavole periodica, è più grande, meno
