laboratorio di fisica moderna magnetismo e nanostrutture
|
|
|
- Corrado Bucci
- 7 anni fa
- Visualizzazioni
Transcript
1 laboratorio di fisica moderna magnetismo e nanostrutture
2 il comportamento magnetico dei materiali La materia contiene elettroni, che hanno la caratteristica di possedere un momento magnetico: ogni elettrone può quindi essere schematizzato come un dipolo magnetico. Visto questo, se applico un campo magnetico ad un materiale posso pensare che quest ultimo subisca una modifica; ciò che osservo è che il materiale tende a magnetizzarsi, ovvero a seguito dell applicazione del campo la disposizione dei momenti magnetici cambia. Per poter quantificare questa modifica si può fare riferimento al vettore magnetizzazione, ottenuto sommando tutti i momenti magnetici presenti nel materiale e dividendo il risultato per il volume del materiale stesso, così da ottenere una grandezza di tipo intensivo. μ μ Sulla base dell entità di tale modifica, si possono individuare almeno tre categorie di materiali: diamagnetici in presenza di un campo magnetico applicato i momenti magnetici tendono a disporsi antiparalleli al campo stesso, la magnetizzazione risulta quindi essere antiparallela al campo applicato. Tale effetto è di intensità molto ridotta. paramagnetici in presenza di un campo magnetico applicato i momenti magnetici tendono a disporsi paralleli al campo stesso, la magnetizzazione risulta quindi essere parallela al campo applicato. Tale effetto è di intensità molto ridotta. ferromagnetici in presenza di un campo magnetico applicato i momenti magnetici tendono a disporsi paralleli al campo stesso, la magnetizzazione risulta quindi essere parallela al campo applicato. Tale effetto è di intensità molto elevata.
3 il comportamento magnetico dei materiali materiali ferromagnetici In questi sistemi la risposta è simile, per direzione, a quella dei paramagneti, ma ha un intensità molto elevata. Se si confronta il valore dei singoli momenti magnetici in un sistema paramagnetico con quello dei singoli momenti magnetici di un sistema ferromagnetico si trovano valori simili tra loro, quindi la causa della diversa intensità dell effetto osservato va spiegata in un altro modo. Campo coercitivo Una possibile spiegazione è che nel caso dei ferromagneti i momenti magnetici siano correlati tra loro, in particolare tendano a restare paralleli gli uni agli altri. Per i ferromagneti, la dipendenza della magnetizzazione dal campo applicato ha l andamento rappresentato in figura. Per i diamagneti e per i paramagneti l andamento è lineare, e non si osserva la presenza di isteresi, il ciclo non è cioè aperto (come la curva blu e la verde nella figura).
4 il comportamento magnetico dei materiali Per spiegare quale fenomeno stia alla base del comportamento ferromagnetico, prendiamo come esempio il Fe. Osservando la struttura elettronica dell atomo di Fe si può osservare che ci sono degli elettroni spaiati, quindi l atomo di Fe si comporta come un dipolo magnetico. 3d 4s 3p 3s 2p 2s 1s Gli atomi di Fe, nel metallo, sono disposti secondo un reticolo di tipo cubico avente un atomo per vertice ed un ulteriore atomo al centro del cubo, ovvero un reticolo cubico a corpo centrato. Perché i dipoli magnetici rimangono allineati? In ogni livello ci sono al massimo 2 elettroni per il Principio di esclusione di Pauli, che valse a W. Pauli il premio Nobel per la fisica.
5 il comportamento magnetico dei materiali La presenza di un comportamento di tipo collettivo, ovvero il fatto che tutti i dipoli magnetici tendano a restare paralleli tra loro, può essere ricondotta all interazione di scambio, un tipo di interazione proposta da W.-K. Heisemberg. Tale interazione è riconducibile alle proprietà quantistiche degli elettroni. Ferromagnetismo : fenomeno di tipo cooperativo
6 il comportamento magnetico dei materiali L origine di tale interazione si può qualitativamente spiegare in questo modo: se due elettroni occupano due diversi livelli e tali elettroni hanno spin opposto, allora uno dei due si potrà spostare dal suo livello a quello dell altro elettrone, ovvero i due elettroni si possono avvicinare tra loro. Viceversa, se i due elettroni di partenza hanno lo stesso spin, allora essi non potranno occupare lo stesso livello, quindi non si possono avvicinare tra loro. Il fatto di non potersi avvicinare riduce l energia di repulsione elettrostatica, quindi il sistema può raggiungere una condizione di minore energia se mediamente gli spin degli elettroni (e quindi i loro momenti magnetici) tendono a restare paralleli tra loro. Le condizioni per cui questo meccanismo riesce ad instaurarsi non si osservano di frequente, quindi solo pochi elementi della tavola periodica risultano essere ferromagnetici.
7 2 µm = m 2 µm Un materiale ferromagnetico al suo interno tende a formare dei domini magnetici, le zone colorate nella figura. Ciascuna freccetta rappresenta la direzione dei momenti magnetici di un volumetto di materiale. Se il materiale viene confinato (ovvero se considero le proprietà di solo un pezzetto) ci si accorge che i momenti magnetici vicino ai bordi tendono a rimanere paralleli ai lati stessi.
8 il comportamento magnetico dei materiali NANOSTRUTTURATI Quanto appena visto ci indica che se un materiale viene confinato su una scala micrometrica o ancora meglio nanometrica, le sue proprietà possono dipendere dalla forma che viene data al materiale stesso. La forma del materiale diventa quindi un ulteriore grado di libertà nel determinare le proprietà dei materiali. L orientazione dei momenti magnetici è condizionata dalla forma del materiale in quanto, nel momento in cui i momenti magnetici si dispongono non paralleli ai lati del materiale stesso si sviluppano dei poli magnetici. se i momenti magnetici sono paralleli al bordo non si formano poli magnetici se i momenti magnetici non sono paralleli al bordo si formano poli magnetici
9 il comportamento magnetico dei materiali NANOSTRUTTURATI Quanto appena visto ci indica che se un materiale viene confinato su una scala micrometrica o ancora meglio nanometrica, le sue proprietà possono dipendere dalla forma che viene data al materiale stesso. La forma del materiale diventa quindi un ulteriore grado di libertà nel determinare le proprietà dei materiali. L orientazione dei momenti magnetici è condizionata dalla forma del materiale in quanto, nel momento in cui i momenti magnetici si dispongono non paralleli ai lati del materiale stesso si sviluppano dei poli magnetici. La presenza di poli magnetici implica che attorno al materiale si sviluppi un campo magnetico; questo aumenta l energia del sistema, in quanto l energia associata alla presenza del campo magnetico è proporzionale al quadrato del modulo del campo magnetico stesso. La possibilità che si formino poli magnetici dipende quindi, in ultima analisi, anche dalla forma del materiale, perciò esso cercherà di adottare configurazioni che risentono della forma stessa; questo aspetto influenzerà l andamento della magnetizzazione del materiale in funzione del campo applicato.
10 il comportamento magnetico dei materiali NANOSTRUTTURATI effetto della forma della nanostruttura sul ciclo di magnetizzazione
11 il comportamento magnetico dei materiali NANOSTRUTTURATI Possibili esempi di materiali nanostrutturati prodotti mediante litografia elettronica Nature Communications 4 (2013) 2381 Jacek Fiutowski, et al. 11 October 2012, SPIE Newsroom Scientific Reports 3 (2013) 3339
12 il comportamento magnetico dei materiali NANOSTRUTTURATI L esperienza di laboratorio consiste nel confrontare le proprietà magnetiche di un materiale con quelle dello stesso materiale una volta sottoposto al processo di nanostrutturazione. In particolare, verranno misurati i cicli di magnetizzazione dei seguenti sistemi: - strato sottile di permalloy, una lega composta da Ni e Fe; nella lega, il Ni ha una concentrazione pari a 80 %, il Fe pari a 20 % - sistema di nanostrutture a forma di anello triangolare, composte della stessa lega. Per la misura del ciclo di magnetizzazione dei due sistemi si sfrutta l effetto Kerr, ovvero il fatto che l indice di rifrazione di un materiale magnetico dipende dal suo stato di magnetizzazione e dalla polarizzazione della luce. bobine utilizzate per applicare il campo magnetico Lo stato di polarizzazione della luce riflessa dal materiale cambia a seconda di quanto sia il valore della sua magnetizzazione, quindi sfruttando l ottica è possibile avere informazioni sul comportamento magnetico del materiale. Così facendo non si ottiene una misura assoluta del valore della magnetizzazione ma una misura relativa; il valore di magnetizzazione viene perciò indicato in modo relativo al valore massimo possibile, ovvero quello ottenuto quando il materiale risulta uniformemente magnetizzato, ovvero saturo.
13 il comportamento magnetico dei materiali NANOSTRUTTURATI Anelli a forma di Triangoli equilateri di Py 50 nm 2 μm spessore di permalloy: 25 nm 250 nm
14 il comportamento magnetico dei materiali NANOSTRUTTURATI Ciclo di magnetizzazione dello strato sottile di permalloy Ciclo di magnetizzazione delle nanostrutture di permalloy Evoluzione della configurazione magnetica di una singola nanostruttura al variare del campo applicato
MAGNETISMO - 2a parte. pina di vito
 MAGNETISMO - 2a parte 1 Flusso del vettore B, l unità di misura è il weber (Wb) B Caso generale: Teorema di Gauss per il magnetismo F S ( B) = 0 Poli magnetici non separabili Il numero di linee entranti
MAGNETISMO - 2a parte 1 Flusso del vettore B, l unità di misura è il weber (Wb) B Caso generale: Teorema di Gauss per il magnetismo F S ( B) = 0 Poli magnetici non separabili Il numero di linee entranti
Magnetismo e nanostrutture. Federico Spizzo Dipartimento di Fisica e Scienze della Terra Università degli Studi di Ferrara
 Magnetismo e nanostrutture Federico Spizzo Dipartimento di Fisica e Scienze della Terra Università degli Studi di Ferrara nanometro = 10-9 m 1 atomo 0,3 nm + =?? Un po di storia... Un materiale magnetico
Magnetismo e nanostrutture Federico Spizzo Dipartimento di Fisica e Scienze della Terra Università degli Studi di Ferrara nanometro = 10-9 m 1 atomo 0,3 nm + =?? Un po di storia... Un materiale magnetico
PROPRIETÀ MAGNETICHE DELLA MATERIA
 PROPRIETÀ MAGNETICHE DELLA MATERIA G. Pugliese 1 Descrizione Macroscopica B 0 Definiamo il vettore: Consideriamo un solenoide vuoto: B0 = µ 0 ni H = B 0 µ 0 = ni u x Supponiamo di riempire completamente
PROPRIETÀ MAGNETICHE DELLA MATERIA G. Pugliese 1 Descrizione Macroscopica B 0 Definiamo il vettore: Consideriamo un solenoide vuoto: B0 = µ 0 ni H = B 0 µ 0 = ni u x Supponiamo di riempire completamente
MAGNETISMO NELLA MATERIA
 MAGNETISMO NELLA MATERIA Gli atomi hanno momenti magnetici di dipolo dovuti al moto dei loro elettroni. Ogni elettrone ha a sua volta un momento magnetico di dipolo intrinseco associato alla sua rotazione
MAGNETISMO NELLA MATERIA Gli atomi hanno momenti magnetici di dipolo dovuti al moto dei loro elettroni. Ogni elettrone ha a sua volta un momento magnetico di dipolo intrinseco associato alla sua rotazione
Fenomenologia (dia-, para- e ferro-magnetismo) Aspetti qualitativi della fenomenologia del ferromagnetismo: isteresi, saturazione, coercività,
 Università di Siena, DIISM, CdS in Ingegneria, Corso di fisica, slides lezione n.18, pag.1/8 In questa lezione: Magnetismo nella materia Fenomenologia (dia-, para- e ferro-magnetismo) Campi B. M, H e loro
Università di Siena, DIISM, CdS in Ingegneria, Corso di fisica, slides lezione n.18, pag.1/8 In questa lezione: Magnetismo nella materia Fenomenologia (dia-, para- e ferro-magnetismo) Campi B. M, H e loro
GLI ORBITALI ATOMICI
 GLI ORBITALI ATOMICI I numeri quantici Le funzioni d onda Ψ n, soluzioni dell equazione d onda, sono caratterizzate da certe combinazioni di numeri quantici: n, l, m l, m s n = numero quantico principale,
GLI ORBITALI ATOMICI I numeri quantici Le funzioni d onda Ψ n, soluzioni dell equazione d onda, sono caratterizzate da certe combinazioni di numeri quantici: n, l, m l, m s n = numero quantico principale,
Esercitazione 1. Invece, essendo il mezzo omogeneo, il vettore sarà espresso come segue
 1.1 Una sfera conduttrice di raggio R 1 = 10 cm ha una carica Q = 10-6 C ed è circondata da uno strato sferico di dielettrico di raggio (esterno) R 2 = 20 cm e costante dielettrica relativa. Determinare
1.1 Una sfera conduttrice di raggio R 1 = 10 cm ha una carica Q = 10-6 C ed è circondata da uno strato sferico di dielettrico di raggio (esterno) R 2 = 20 cm e costante dielettrica relativa. Determinare
MAGNETISM IN STAINLESS STEELS MAGNETISMO NEGLI ACCIAI INOSSIDABILI
 MAGNETISM IN STAINLESS STEELS MAGNETISMO NEGLI ACCIAI INOSSIDABILI Magnetic flow and electric current Flusso Magnetico e corrente Magnetic flow and electric current Flusso Magnetico e corrente Ferromagnetism-Ferromagnetismo
MAGNETISM IN STAINLESS STEELS MAGNETISMO NEGLI ACCIAI INOSSIDABILI Magnetic flow and electric current Flusso Magnetico e corrente Magnetic flow and electric current Flusso Magnetico e corrente Ferromagnetism-Ferromagnetismo
Configurazione elettronica e Tavola periodica. Lezioni 13-16
 Configurazione elettronica e Tavola periodica Lezioni 13-16 Orbitali possibili Gusci e sottogusci Gli elettroni che occupano orbitali con lo stesso valore di numero quantico principale n si dice che sono
Configurazione elettronica e Tavola periodica Lezioni 13-16 Orbitali possibili Gusci e sottogusci Gli elettroni che occupano orbitali con lo stesso valore di numero quantico principale n si dice che sono
Fenomeni magnetici. Capitolo. 1. Il magnetismo nella materia. Quali forze sperimenta un aghetto magnetico in un campo B?
 Capitolo 5 Fenomeni magnetici 1. l magnetismo nella materia Quali forze sperimenta un aghetto magnetico in un campo? L aghetto magnetico è lo strumento che definisce la direzione del campo in ogni punto.
Capitolo 5 Fenomeni magnetici 1. l magnetismo nella materia Quali forze sperimenta un aghetto magnetico in un campo? L aghetto magnetico è lo strumento che definisce la direzione del campo in ogni punto.
Questa proprietà, posseduta da alcuni corpi, viene definita MAGNETISMO.
 MAGNETISMO Cos è il MAGNETISMO Sin dall'antichità era noto che un minerale di ferro, la magnetite, ha la proprietà di attirare il ferro. Questa proprietà, posseduta da alcuni corpi, viene definita MAGNETISMO.
MAGNETISMO Cos è il MAGNETISMO Sin dall'antichità era noto che un minerale di ferro, la magnetite, ha la proprietà di attirare il ferro. Questa proprietà, posseduta da alcuni corpi, viene definita MAGNETISMO.
Interazione luce- atomo
 Interazione luce- atomo Descrizione semiclassica L interazione predominante è quella tra il campo elettrico e le cariche ASSORBIMENTO: Elettrone e protone formano un dipolo che viene messo in oscillazione
Interazione luce- atomo Descrizione semiclassica L interazione predominante è quella tra il campo elettrico e le cariche ASSORBIMENTO: Elettrone e protone formano un dipolo che viene messo in oscillazione
LA STRUTTURA DELLE MOLECOLE. Orbitali molecolari e legame chimico
 LA STRUTTURA DELLE MOLECOLE Orbitali molecolari e legame chimico GLI ORBITALI MOLECOLARI Quando degli atomi collidono tra di loro i loro nuclei ed elettroni vengono a trovarsi in prossimità influenzandosi
LA STRUTTURA DELLE MOLECOLE Orbitali molecolari e legame chimico GLI ORBITALI MOLECOLARI Quando degli atomi collidono tra di loro i loro nuclei ed elettroni vengono a trovarsi in prossimità influenzandosi
CHIMICA ORGANICA = STUDIO DEI COMPOSTI DEL CARBONIO. energia superiore. energia inferiore. orbitale s
 CIMICA ORGANICA = STUDIO DEI COMPOSTI DEL CARBONIO C elemento del secondo periodo della tavola periodica; numero atomico = 6 configurazione elettronica del C 2p 2s 1s energia superiore energia inferiore
CIMICA ORGANICA = STUDIO DEI COMPOSTI DEL CARBONIO C elemento del secondo periodo della tavola periodica; numero atomico = 6 configurazione elettronica del C 2p 2s 1s energia superiore energia inferiore
Indice. Elettrostatica in presenza di dielettrici Costante dielettrica Interpretazione microscopica 119. capitolo. capitolo.
 Indice Elettrostatica nel vuoto. Campo elettrico e potenziale 1 1. Azioni elettriche 1 2. Carica elettrica e legge di Coulomb 5 3. Campo elettrico 8 4. Campo elettrostatico generato da sistemi di cariche
Indice Elettrostatica nel vuoto. Campo elettrico e potenziale 1 1. Azioni elettriche 1 2. Carica elettrica e legge di Coulomb 5 3. Campo elettrico 8 4. Campo elettrostatico generato da sistemi di cariche
La teoria atomica moderna: il modello planetario L ELETTRONE SI MUOVE LUNGO UN ORBITA INTORNO AL NUCLEO
 La teoria atomica moderna: il modello planetario L ELETTRONE SI MUOVE LUNGO UN ORBITA INTORNO AL NUCLEO La luce La LUCE è una forma di energia detta radiazione elettromagnetica che si propaga nello spazio
La teoria atomica moderna: il modello planetario L ELETTRONE SI MUOVE LUNGO UN ORBITA INTORNO AL NUCLEO La luce La LUCE è una forma di energia detta radiazione elettromagnetica che si propaga nello spazio
Corso di CHIMICA LEZIONE 2
 Corso di CHIMICA LEZIONE 2 MODELLO ATOMICO DI THOMSON 1904 L atomo è formato da una sfera carica positivamente in cui gli elettroni con carica negativa, distribuiti uniformemente all interno, neutralizzano
Corso di CHIMICA LEZIONE 2 MODELLO ATOMICO DI THOMSON 1904 L atomo è formato da una sfera carica positivamente in cui gli elettroni con carica negativa, distribuiti uniformemente all interno, neutralizzano
GLI ORBITALI ATOMICI
 GLI ORBITALI ATOMICI Orbitali atomici e loro rappresentazione Le funzioni d onda Ψ n che derivano dalla risoluzione dell equazione d onda e descrivono il moto degli elettroni nell atomo si dicono orbitali
GLI ORBITALI ATOMICI Orbitali atomici e loro rappresentazione Le funzioni d onda Ψ n che derivano dalla risoluzione dell equazione d onda e descrivono il moto degli elettroni nell atomo si dicono orbitali
MISURA DELLA SUSCETTIVITA MAGNETICA. Elettroni e particelle nucleari sono dotati di spin. Si orientano in un campo magnetico.
 MISURA DELLA SUSCETTIVITA MAGNETICA Elettroni e particelle nucleari sono dotati di spin. Si orientano in un campo magnetico. EFFETTO DIAMAGNETICO (elettroni accoppiati) Quando una qualunque sostanza è
MISURA DELLA SUSCETTIVITA MAGNETICA Elettroni e particelle nucleari sono dotati di spin. Si orientano in un campo magnetico. EFFETTO DIAMAGNETICO (elettroni accoppiati) Quando una qualunque sostanza è
Struttura dell atomo atomo particelle sub-atomiche - protoni positiva - neutroni } nucleoni - elettroni negativa elemento
 Struttura dell atomo L atomo è la più piccola parte dell elemento che conserva le proprietà dell elemento Negli atomi ci sono tre diverse particelle sub-atomiche: - protoni (con carica positiva unitaria)
Struttura dell atomo L atomo è la più piccola parte dell elemento che conserva le proprietà dell elemento Negli atomi ci sono tre diverse particelle sub-atomiche: - protoni (con carica positiva unitaria)
IL LEGAME COVALENTE SECONDO LA MECCANICA ONDULATORIA L
 IL LEGAME COVALENTE SECONDO LA MECCANICA ONDULATORIA L elettrone è dissolto in una nube di carica, ovvero il concetto di orbitale sostituisce il di Lewis LEGAME DI VALENZA (VB) Sviluppo quantomeccanico
IL LEGAME COVALENTE SECONDO LA MECCANICA ONDULATORIA L elettrone è dissolto in una nube di carica, ovvero il concetto di orbitale sostituisce il di Lewis LEGAME DI VALENZA (VB) Sviluppo quantomeccanico
CHIMICA: studio della struttura e delle trasformazioni della materia
 CHIMICA: studio della struttura e delle trasformazioni della materia 1 Materia (materali) Sostanze (omogenee) Processo fisico Miscele Elementi (atomi) Reazioni chimiche Composti (molecole) Miscele omogenee
CHIMICA: studio della struttura e delle trasformazioni della materia 1 Materia (materali) Sostanze (omogenee) Processo fisico Miscele Elementi (atomi) Reazioni chimiche Composti (molecole) Miscele omogenee
Testi Consigliati. I. Bertini, C. Luchinat, F. Mani CHIMICA, Zanichelli. Qualsiasi altro testo che tratti gli argomenti elencati nel programma
 Chimica Generale ed Inorganica Testi Consigliati I. Bertini, C. Luchinat, F. Mani CHIMICA, Zanichelli Chimica Organica Hart-Craine Introduzione alla Chimica Organica Zanichelli. Qualsiasi altro testo che
Chimica Generale ed Inorganica Testi Consigliati I. Bertini, C. Luchinat, F. Mani CHIMICA, Zanichelli Chimica Organica Hart-Craine Introduzione alla Chimica Organica Zanichelli. Qualsiasi altro testo che
Effetto Zeeman anomalo
 Effetto Zeeman anomalo Direzione del campo B esempio: : j=3/2 Direzione del campo B j=1+1/2 = 3/2 s m j =+3/2 m j =+1/2 l m j =-1/2 m j =-3/2 La separazione tra i livelli é diversa l e µ l antiparalleli
Effetto Zeeman anomalo Direzione del campo B esempio: : j=3/2 Direzione del campo B j=1+1/2 = 3/2 s m j =+3/2 m j =+1/2 l m j =-1/2 m j =-3/2 La separazione tra i livelli é diversa l e µ l antiparalleli
Esercizi sui Complessi Metallici
 Insegnamento di Chimica Generale 083424 - CCS CHI e MAT A.A. 2015/2016 (I Semestre) Esercizi sui Complessi Metallici Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio Esercizi
Insegnamento di Chimica Generale 083424 - CCS CHI e MAT A.A. 2015/2016 (I Semestre) Esercizi sui Complessi Metallici Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio Esercizi
Legame chimico unità 1, modulo D del libro
 Legame chimico unità 1, modulo D del libro PERCHÉ IL LEGAME CHIMICO? Gli atomi si trovano raramente isolati, spesso due o più atomi si uniscono tramite un legame chimico. Perché ciò avviene? Perché l insieme
Legame chimico unità 1, modulo D del libro PERCHÉ IL LEGAME CHIMICO? Gli atomi si trovano raramente isolati, spesso due o più atomi si uniscono tramite un legame chimico. Perché ciò avviene? Perché l insieme
Lezione 1: Introduzione alle grandezze magnetiche
 Lezione 1: Introduzione alle grandezze magnetiche 1 Campi Magnetici Il campo magnetico è un campo vettoriale: associa, cioè, ad ogni punto nello spazio un vettore. Un campo magnetico si puo misurare per
Lezione 1: Introduzione alle grandezze magnetiche 1 Campi Magnetici Il campo magnetico è un campo vettoriale: associa, cioè, ad ogni punto nello spazio un vettore. Un campo magnetico si puo misurare per
Cristalli fotonici e loro applicazioni
 Dipartimento di fisica A. Volta, Università degli studi di Pavia 8 maggio 2009 solidi cristallini = reticolo + base Figura: alcuni reticoli di Bravais 3D con 3 vettori primitivi a,b,c; Figura: alcuni reticoli
Dipartimento di fisica A. Volta, Università degli studi di Pavia 8 maggio 2009 solidi cristallini = reticolo + base Figura: alcuni reticoli di Bravais 3D con 3 vettori primitivi a,b,c; Figura: alcuni reticoli
Conservazione della carica elettrica
 Elettrostatica La forza elettromagnetica è una delle interazioni fondamentali dell universo L elettrostatica studia le interazioni fra le cariche elettriche non in movimento Da esperimenti di elettrizzazione
Elettrostatica La forza elettromagnetica è una delle interazioni fondamentali dell universo L elettrostatica studia le interazioni fra le cariche elettriche non in movimento Da esperimenti di elettrizzazione
Il legame dativo o coordinativo: lo stesso atomo fornisce i due elettroni di legame.
 Il legame dativo o coordinativo: lo stesso atomo fornisce i due elettroni di legame. Non necessariamente i due elettroni che concorrono alla formazione del legame devono provenire da entrambi gli atomi
Il legame dativo o coordinativo: lo stesso atomo fornisce i due elettroni di legame. Non necessariamente i due elettroni che concorrono alla formazione del legame devono provenire da entrambi gli atomi
CONFIGURAZIONE ELETTRONICA. In generale la configurazione elettronica indica come sono posizionati gli elettroni intorno al nucleo di un atomo.
 CONFIGURAZIONE ELETTRONICA In generale la configurazione elettronica indica come sono posizionati gli elettroni intorno al nucleo di un atomo. ORBITA : Zona intorno al nucleo di diversa energia dove ruotano
CONFIGURAZIONE ELETTRONICA In generale la configurazione elettronica indica come sono posizionati gli elettroni intorno al nucleo di un atomo. ORBITA : Zona intorno al nucleo di diversa energia dove ruotano
Le Caratteristiche della Luce
 7. L Atomo Le Caratteristiche della Luce Quanti e Fotoni Spettri Atomici e Livelli Energetici L Atomo di Bohr I Modelli dell Atomo - Orbitali atomici - I numeri quantici e gli orbitali atomici - Lo spin
7. L Atomo Le Caratteristiche della Luce Quanti e Fotoni Spettri Atomici e Livelli Energetici L Atomo di Bohr I Modelli dell Atomo - Orbitali atomici - I numeri quantici e gli orbitali atomici - Lo spin
Struttura Elettronica degli Atomi Meccanica quantistica
 Prof. A. Martinelli Struttura Elettronica degli Atomi Meccanica quantistica Dipartimento di Farmacia 1 Il comportamento ondulatorio della materia 2 1 Il comportamento ondulatorio della materia La diffrazione
Prof. A. Martinelli Struttura Elettronica degli Atomi Meccanica quantistica Dipartimento di Farmacia 1 Il comportamento ondulatorio della materia 2 1 Il comportamento ondulatorio della materia La diffrazione
Esistono alcune sostanze che manifestano la capacità di attirare la limatura di ferro, in particolare, la magnetite
 59 Esistono alcune sostanze che manifestano la capacità di attirare la limatura di ferro, in particolare, la magnetite Questa proprietà non è uniforme su tutto il materiale, ma si localizza prevelentemente
59 Esistono alcune sostanze che manifestano la capacità di attirare la limatura di ferro, in particolare, la magnetite Questa proprietà non è uniforme su tutto il materiale, ma si localizza prevelentemente
CRISTALLOCHIMICA. La cristallochimica è la disciplina che studia le correlazioni tra la struttura cristallina e la composizione chimica dei minerali
 CRISTALLOCHIMICA La cristallochimica è la disciplina che studia le correlazioni tra la struttura cristallina e la composizione chimica dei minerali L atomo H orbitali Livelli energetici Lo ione Lo ione
CRISTALLOCHIMICA La cristallochimica è la disciplina che studia le correlazioni tra la struttura cristallina e la composizione chimica dei minerali L atomo H orbitali Livelli energetici Lo ione Lo ione
1.La forma delle molecole 2.La teoria VSEPR 3.Molecole polari e apolari 4.Le forze intermolecolari 5.Legami a confronto
 1.La forma delle molecole 2.La teoria VSEPR 3.Molecole polari e apolari 4.Le forze intermolecolari 5.Legami a confronto 1 1. La forma delle molecole Molte proprietà delle sostanze dipendono dalla forma
1.La forma delle molecole 2.La teoria VSEPR 3.Molecole polari e apolari 4.Le forze intermolecolari 5.Legami a confronto 1 1. La forma delle molecole Molte proprietà delle sostanze dipendono dalla forma
A1.1 Elettrostatica. Particella Carica elettrica Massa. Elettrone 1,602 x C 9,108 x kg. Protone 1,602 x C 1,672 x kg
 A1.1 Elettrostatica Nell affrontare lo studio dell elettrotecnica si segue di solito un percorso che vede, in successione, lo studio dell elettrostatica (campo elettrico), quindi della corrente elettrica,
A1.1 Elettrostatica Nell affrontare lo studio dell elettrotecnica si segue di solito un percorso che vede, in successione, lo studio dell elettrostatica (campo elettrico), quindi della corrente elettrica,
IL LEGAME SIGMA σ E IL LEGAME PI- GRECO π
 IL LEGAME SIGMA σ E IL LEGAME PI- GRECO π La teoria di Lewis considera gli elettroni di valenza degli atomi che formano legami,ma prescinde totalmente dal fatto che tali elettroni sono descritti da orbitali
IL LEGAME SIGMA σ E IL LEGAME PI- GRECO π La teoria di Lewis considera gli elettroni di valenza degli atomi che formano legami,ma prescinde totalmente dal fatto che tali elettroni sono descritti da orbitali
Composti di coordinazione
 Composti di coordinazione Nelle molecole di un COMPOSTO DI COORDINAZIONE l atomo centrale e legato ad un numero di atomi superiore al suo numero di ossidazione. Lo studio dei composti di coordinazione
Composti di coordinazione Nelle molecole di un COMPOSTO DI COORDINAZIONE l atomo centrale e legato ad un numero di atomi superiore al suo numero di ossidazione. Lo studio dei composti di coordinazione
Fisica Generale III con Laboratorio
 Fisica Generale III con Laboratorio Campi elettrici e magnetici nella materia Lezione 3 Polarizzazione permanente Formula di Langevin - I Polarizzazione per orientamento: Molecole polari Relazione approssimata
Fisica Generale III con Laboratorio Campi elettrici e magnetici nella materia Lezione 3 Polarizzazione permanente Formula di Langevin - I Polarizzazione per orientamento: Molecole polari Relazione approssimata
Festival della filosofia Agonismo Vinca il migliore
 Festival della filosofia 2016 - Agonismo Vinca il migliore Formazione degli studenti di scuola superiore in alternanza scuola-lavoro CAMPO ELETTRCO - Penna a sfera strofinata attira pezzetti di carta.
Festival della filosofia 2016 - Agonismo Vinca il migliore Formazione degli studenti di scuola superiore in alternanza scuola-lavoro CAMPO ELETTRCO - Penna a sfera strofinata attira pezzetti di carta.
Orbitali nei primi tre livelli
 Orbitali nei primi tre livelli La tavola periodica degli elementi Numeri quantici e tavola Configurazioni elettroniche degli atomi Elenco degli orbitali occupati in un atomo nel suo stato fondamentale
Orbitali nei primi tre livelli La tavola periodica degli elementi Numeri quantici e tavola Configurazioni elettroniche degli atomi Elenco degli orbitali occupati in un atomo nel suo stato fondamentale
Capitolo 8 La struttura dell atomo
 Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. La «luce» degli atomi 3. L atomo di Bohr 4. La doppia natura dell elettrone 5. L elettrone e la meccanica quantistica 6. L equazione
Capitolo 8 La struttura dell atomo 1. La doppia natura della luce 2. La «luce» degli atomi 3. L atomo di Bohr 4. La doppia natura dell elettrone 5. L elettrone e la meccanica quantistica 6. L equazione
1. L energia di legame
 legami chimici 1. L energia di legame Nonostante l enorme numero di combinazioni possibili fra gli atomi, non tutte sono realizzabili: un composto si forma solo se la sua energia potenziale è minore dei
legami chimici 1. L energia di legame Nonostante l enorme numero di combinazioni possibili fra gli atomi, non tutte sono realizzabili: un composto si forma solo se la sua energia potenziale è minore dei
1. L energia di legame. 2. I gas nobili e a regola dell ottetto. 3. Il legame covalente. 4. Il legame covalente dativo. 5. Il legame covalente polare
 Capitolo 10 I legami chimici 1. L energia di legame 2. I gas nobili e a regola dell ottetto 3. Il legame covalente 4. Il legame covalente dativo 5. Il legame covalente polare 6. Il legame ionico 7. I composti
Capitolo 10 I legami chimici 1. L energia di legame 2. I gas nobili e a regola dell ottetto 3. Il legame covalente 4. Il legame covalente dativo 5. Il legame covalente polare 6. Il legame ionico 7. I composti
CARATTERIZZAZIONE DI MATERIALE FERROMAGNETICO DOLCE
 Spin Applicazioni Magnetiche Srl propone anche un servizio di caratterizzazione di materiali ferromagnetici dolci per la realizzazione di curve di magnetizzazione, isteresi, misure di perdite specifiche.
Spin Applicazioni Magnetiche Srl propone anche un servizio di caratterizzazione di materiali ferromagnetici dolci per la realizzazione di curve di magnetizzazione, isteresi, misure di perdite specifiche.
Proprietà magnetiche della materia
 Proprietà magnetiche della materia La seguente presentazione è stata ideata per offrire agli studenti una sintesi dei più importanti fenomeni riguardanti l elettromagnetismo. La presente non deve sostituirsi
Proprietà magnetiche della materia La seguente presentazione è stata ideata per offrire agli studenti una sintesi dei più importanti fenomeni riguardanti l elettromagnetismo. La presente non deve sostituirsi
Lo Spettro Elettromagnetico
 Spettroscopia 1 Lo Spettro Elettromagnetico Lo spettro elettromagnetico è costituito da un insieme continuo di radiazioni (campi elettrici e magnetici che variano nel tempo, autogenerandosi) che va dai
Spettroscopia 1 Lo Spettro Elettromagnetico Lo spettro elettromagnetico è costituito da un insieme continuo di radiazioni (campi elettrici e magnetici che variano nel tempo, autogenerandosi) che va dai
Controlli magnetoscopici
 Controlli magnetoscopici DESCRIZIONE GENERALE Questa tecnica si basa sull analisi delle variazioni nel campo magnetico che si verificano in presenza di difetti superficiali o sub-superficiali Può essere
Controlli magnetoscopici DESCRIZIONE GENERALE Questa tecnica si basa sull analisi delle variazioni nel campo magnetico che si verificano in presenza di difetti superficiali o sub-superficiali Può essere
Particelle Subatomiche
 GLI ATOMI Particelle Subatomiche ELEMENTI I diversi atomi sono caratterizzati da un diverso numero di protoni e neutroni; il numero di elettroni è sempre uguale al numero dei protoni (negli atomi neutri)
GLI ATOMI Particelle Subatomiche ELEMENTI I diversi atomi sono caratterizzati da un diverso numero di protoni e neutroni; il numero di elettroni è sempre uguale al numero dei protoni (negli atomi neutri)
Recenti Scoperte Scientifiche in Ottica
 Recenti Scoperte Scientifiche in Ottica Luca Salasnich Dipartimento di Fisica e Astronomia Galileo Galilei, Università di Padova, Italy Padova, 26 Maggio 2014 Secondo Meeting di Ottica e Optometria a Padova
Recenti Scoperte Scientifiche in Ottica Luca Salasnich Dipartimento di Fisica e Astronomia Galileo Galilei, Università di Padova, Italy Padova, 26 Maggio 2014 Secondo Meeting di Ottica e Optometria a Padova
Per esempio, possiamo osservare il legame ionico nella molecola di cloruro di sodio. Il cloro e il sodio hanno le seguenti strutture di Lewis:
 IL LEGAME IONICO In natura solo i gas nobili presentano atomi allo stato libero. Tutte le altre sostanze consistono di molecole che sono aggregazioni di atomi. Le forze che tengono uniti gli atomi in una
IL LEGAME IONICO In natura solo i gas nobili presentano atomi allo stato libero. Tutte le altre sostanze consistono di molecole che sono aggregazioni di atomi. Le forze che tengono uniti gli atomi in una
Nome: Cognome: Matricola:
 Esercizio 1: Una porzione anello carico avente raggio R = 4 cm, giace sul piano x-y (uadrante x e y positivi) come indicato in figura 1. La densità lineare di carica dell anello è di 40 nc/m. i. Calcolare
Esercizio 1: Una porzione anello carico avente raggio R = 4 cm, giace sul piano x-y (uadrante x e y positivi) come indicato in figura 1. La densità lineare di carica dell anello è di 40 nc/m. i. Calcolare
S P E T T R O S C O P I A. Dispense di Chimica Fisica per Biotecnologie Dr.ssa Rosa Terracciano
 S P E T T R O S C O P I A SPETTROSCOPIA I PARTE Cenni generali di spettroscopia: La radiazione elettromagnetica e i parametri che la caratterizzano Le regioni dello spettro elettromagnetico Interazioni
S P E T T R O S C O P I A SPETTROSCOPIA I PARTE Cenni generali di spettroscopia: La radiazione elettromagnetica e i parametri che la caratterizzano Le regioni dello spettro elettromagnetico Interazioni
Misure di fenomeni di aberrazione di una lente
 Padova, gennaio 00 Misure di fenomeni di aberrazione di una lente Indicare il numero identificativo e le caratteristiche geometriche della lente utilizzata: Lente num. =... Spessore =... Spigolo =... Indice
Padova, gennaio 00 Misure di fenomeni di aberrazione di una lente Indicare il numero identificativo e le caratteristiche geometriche della lente utilizzata: Lente num. =... Spessore =... Spigolo =... Indice
IL LEGAME CHIMICO. Per descrivere come gli elettroni si distribuiscono nell atomo attorno al nucleo si può far riferimento al MODELLO A GUSCI
 IL LEGAME CIMICO Come dagli atomi si costruiscono le molecole 02/19/08 0959 PM 1 Per descrivere come gli elettroni si distribuiscono nell atomo attorno al nucleo si può far riferimento al MODELLO A GUSCI
IL LEGAME CIMICO Come dagli atomi si costruiscono le molecole 02/19/08 0959 PM 1 Per descrivere come gli elettroni si distribuiscono nell atomo attorno al nucleo si può far riferimento al MODELLO A GUSCI
STRUTTURA E FORMA DELLE MOLECOLE
 Ricapitolando Z numero atomico = n. di protoni A numero di massa = n. di protoni n. di neutroni 1 UMA = 1/12 x1.99 10 23 g = 1.66 10 24g = 1/12 massa 12C PA peso atomico massa media degli atomi contenuti
Ricapitolando Z numero atomico = n. di protoni A numero di massa = n. di protoni n. di neutroni 1 UMA = 1/12 x1.99 10 23 g = 1.66 10 24g = 1/12 massa 12C PA peso atomico massa media degli atomi contenuti
MICHELSON. Interferometro. A.Guarrera, Liceo Galilei CT
 L INTERFEROMETRO DI MICHELSON 1 A.Guarrera, Liceo Galilei CT L interferometria è un metodo di misura molto preciso e molto sensibile che permette di determinare, ad esempio, variazioni di lunghezza, densità
L INTERFEROMETRO DI MICHELSON 1 A.Guarrera, Liceo Galilei CT L interferometria è un metodo di misura molto preciso e molto sensibile che permette di determinare, ad esempio, variazioni di lunghezza, densità
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 13 I legami chimici 3 Sommario (I) 1. L energia di legame 2. I gas nobili e la regola dell ottetto 3. Il legame covalente 4.
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 13 I legami chimici 3 Sommario (I) 1. L energia di legame 2. I gas nobili e la regola dell ottetto 3. Il legame covalente 4.
FISICA APPLICATA 2 DIPOLI ELETTRICI E MAGNETICI
 FISICA APPLICATA 2 DIPOLI ELETTRICI E MAGNETICI DOWNLOAD Il pdf di questa lezione (ele2.pdf) è scaricabile dal sito http://www.ge.infn.it/ calvini/tsrm/ 26/11/2012 DIPOLO ELETTRICO La configurazione costituita
FISICA APPLICATA 2 DIPOLI ELETTRICI E MAGNETICI DOWNLOAD Il pdf di questa lezione (ele2.pdf) è scaricabile dal sito http://www.ge.infn.it/ calvini/tsrm/ 26/11/2012 DIPOLO ELETTRICO La configurazione costituita
Risonanza magnetica nucleare
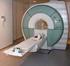 Risonanza magnetica nucleare Università di Firenze Corso di Tecnologie Biomediche Lezione del 31 ottobre 2003 Leonardo Bocchi Principi fisici Premessa Modello classico Visualizzazione semplificata Equazione
Risonanza magnetica nucleare Università di Firenze Corso di Tecnologie Biomediche Lezione del 31 ottobre 2003 Leonardo Bocchi Principi fisici Premessa Modello classico Visualizzazione semplificata Equazione
Lezione 3. Legame Chimico. Teoria degli Orbitali Molecolari
 Lezione 3 Legame Chimico Teoria degli Orbitali Molecolari 1 Perchè si formano i legami? Un diagramma di energia mostra che un legame fra due atomi si forma se l energia del sistema diminuisce quando i
Lezione 3 Legame Chimico Teoria degli Orbitali Molecolari 1 Perchè si formano i legami? Un diagramma di energia mostra che un legame fra due atomi si forma se l energia del sistema diminuisce quando i
CORSO DI LAUREA IN OTTICA E OPTOMETRIA
 CORSO DI LAUREA IN OTTICA E OPTOMETRIA Anno Accademico 007-008 CORSO di FISCA ED APPLICAZIONE DEI LASERS Questionario del Primo appello della Sessione Estiva NOME: COGNOME: MATRICOLA: VOTO: /30 COSTANTI
CORSO DI LAUREA IN OTTICA E OPTOMETRIA Anno Accademico 007-008 CORSO di FISCA ED APPLICAZIONE DEI LASERS Questionario del Primo appello della Sessione Estiva NOME: COGNOME: MATRICOLA: VOTO: /30 COSTANTI
M A G N E T I S M O in C H I M I C A
 M A G N E T I S M O in C H I M I C A Le sostanze in cui tutti gli elettroni sono accoppiati, poste in un campo magnetico esterno, sono respinte da questo; i piani degli orbitali vengono leggermente inclinati
M A G N E T I S M O in C H I M I C A Le sostanze in cui tutti gli elettroni sono accoppiati, poste in un campo magnetico esterno, sono respinte da questo; i piani degli orbitali vengono leggermente inclinati
I 4 NUMERI QUANTICI. I numeri quantici consentono di definire forma, dimensioni ed energia degli orbitali.
 I 4 NUMERI QUANTICI I numeri quantici consentono di definire forma, dimensioni ed energia degli orbitali. n, numero quantico principale, indica il livello energetico e le dimensioni degli orbitali. Può
I 4 NUMERI QUANTICI I numeri quantici consentono di definire forma, dimensioni ed energia degli orbitali. n, numero quantico principale, indica il livello energetico e le dimensioni degli orbitali. Può
MOLECOLE. 2 - i legami chimici. Prof. Vittoria Patti
 MOLECOLE 2 - i legami chimici Prof. Vittoria Patti Gli stati di aggregazione della materia STATO SOLIDO molecole ravvicinate, struttura ordinata, volume proprio, forma propria STATO LIQUIDO molecole
MOLECOLE 2 - i legami chimici Prof. Vittoria Patti Gli stati di aggregazione della materia STATO SOLIDO molecole ravvicinate, struttura ordinata, volume proprio, forma propria STATO LIQUIDO molecole
ITN DUCA DEGLI ABRUZZI di Catania Compito di elettrotecnica ed elettronica.
 TN DUCA DEGL ABRUZZ di Catania Compito di elettrotecnica ed elettronica. Cognome.. Nome... Classe. Data / / Quesiti Dalla 1 alla 15 16 17 18 19 0 tot Punteggio totale previsto 45 3 10 4 6 70 Esatte. x3
TN DUCA DEGL ABRUZZ di Catania Compito di elettrotecnica ed elettronica. Cognome.. Nome... Classe. Data / / Quesiti Dalla 1 alla 15 16 17 18 19 0 tot Punteggio totale previsto 45 3 10 4 6 70 Esatte. x3
1.2 Teoria classica del diamagnetismo: teoria di Langevin
 1. Teoria classica del diamagnetismo: teoria di angevin Il fenomeno del diamagnetismo causato dalla tendenza delle cariche elettriche (elettroni) a schermare in parte un corpo dall azione di un campo magnetico
1. Teoria classica del diamagnetismo: teoria di angevin Il fenomeno del diamagnetismo causato dalla tendenza delle cariche elettriche (elettroni) a schermare in parte un corpo dall azione di un campo magnetico
Il legame chimico II: la geometria molecolare e l ibridizzazione degli orbitali atomici. Capitolo 10
 Il legame chimico II: la geometria molecolare e l ibridizzazione degli orbitali atomici Capitolo 10 Legame tra un derivato del Buckyball e il sito dell HIV-Protease Repulsione delle coppie di elettroni
Il legame chimico II: la geometria molecolare e l ibridizzazione degli orbitali atomici Capitolo 10 Legame tra un derivato del Buckyball e il sito dell HIV-Protease Repulsione delle coppie di elettroni
LA LEGGE DI COULOMB PER I MAGNETI
 1 LA LEGGE DI COULOMB PER I MAGNETI Lo scopo di questo esperimento è quello di riprodurre quello storico e importante ormai scomparso dai testi scolastici perché ritenuto non attinente alla realtà. È noto,
1 LA LEGGE DI COULOMB PER I MAGNETI Lo scopo di questo esperimento è quello di riprodurre quello storico e importante ormai scomparso dai testi scolastici perché ritenuto non attinente alla realtà. È noto,
Orbitali e numeri quantici
 Orbitali e numeri quantici Un orbitale atomico viene approssimato con quella regione di spazio attorno al nucleo atomico in cui la probabilità di trovare un elettrone è massima (massima densità di probabilità)
Orbitali e numeri quantici Un orbitale atomico viene approssimato con quella regione di spazio attorno al nucleo atomico in cui la probabilità di trovare un elettrone è massima (massima densità di probabilità)
ASSORBIMENTO UV-VIS. Atomo
 ASSRBIMET UV-VIS 1 Atomo Molecola E 3 E 2 Livelli elettronici (interazioni UV) A Tipi di vibrazione molecolare: E 1 E 0 sottolivelli vibrazionali (interazioni IR) sottolivelli rotazionali (interazioni
ASSRBIMET UV-VIS 1 Atomo Molecola E 3 E 2 Livelli elettronici (interazioni UV) A Tipi di vibrazione molecolare: E 1 E 0 sottolivelli vibrazionali (interazioni IR) sottolivelli rotazionali (interazioni
RICHIAMI DI MAGNETISMO. µ o = 4 π 10-7 H/m
 ESERCITAZIONE 5 RICIAMARE LE RELAZIONI PRINCIPALI SUL MAGNETISMO. PRESENTARE E CLASSIFICARE I FENOMENI MAGNETICI NEI MATERIALI. FORNIRE UNA SPIEGAZIONE QUALITATIVA DI TALI FENOMENI. PRESENTARE I MATERIALI
ESERCITAZIONE 5 RICIAMARE LE RELAZIONI PRINCIPALI SUL MAGNETISMO. PRESENTARE E CLASSIFICARE I FENOMENI MAGNETICI NEI MATERIALI. FORNIRE UNA SPIEGAZIONE QUALITATIVA DI TALI FENOMENI. PRESENTARE I MATERIALI
LA PRODUZIONE DEI RAGGI X
 UNIVERSITA POLITECNICA DELLE MARCHE Facoltà di Medicina e Chirurgia Corso di Laurea in Tecniche di Radiologia Medica, per Immagini e Radioterapia LA PRODUZIONE DEI RAGGI X A.A. 2015-2016 Tecniche di Radiodiagnostica
UNIVERSITA POLITECNICA DELLE MARCHE Facoltà di Medicina e Chirurgia Corso di Laurea in Tecniche di Radiologia Medica, per Immagini e Radioterapia LA PRODUZIONE DEI RAGGI X A.A. 2015-2016 Tecniche di Radiodiagnostica
1. Qual è la posizione dell immagine fornita da uno specchio piano? Di che tipo di immagine si tratta?
 Specchi piani MPZ 1. Qual è la posizione dell immagine fornita da uno specchio piano? Di che tipo di immagine si tratta? Disponi il cilindro giallo dietro lo specchio, in modo che coincida con l immagine
Specchi piani MPZ 1. Qual è la posizione dell immagine fornita da uno specchio piano? Di che tipo di immagine si tratta? Disponi il cilindro giallo dietro lo specchio, in modo che coincida con l immagine
Lezione 15 Geometrie lineari di confinamento magnetico
 Lezione 15 Geometrie lineari di confinamento magnetico G. Bosia Universita di Torino G. Bosia Introduzione alla fisica del plasma Lezione 15 1 Disuniformità con gradiente in direzione del campo ( ) Una
Lezione 15 Geometrie lineari di confinamento magnetico G. Bosia Universita di Torino G. Bosia Introduzione alla fisica del plasma Lezione 15 1 Disuniformità con gradiente in direzione del campo ( ) Una
CICLO D ISTERESI DI UN MATERIALE FERROMAGNETICO
 CICLO D ISTERESI DI UN MATERIALE FERROMAGNETICO Le proprietà delle sostanze ferromagnetiche sono descritte dal ciclo d isteresi, che -con riferimento al testo adottato (Mazzoldi, Nigro, Voci: Elettromagnetismo)
CICLO D ISTERESI DI UN MATERIALE FERROMAGNETICO Le proprietà delle sostanze ferromagnetiche sono descritte dal ciclo d isteresi, che -con riferimento al testo adottato (Mazzoldi, Nigro, Voci: Elettromagnetismo)
Molecole e legami. Chimica generale
 Molecole e legami Chimica generale Atomi e molecole È estremamente difficile trovare in natura una sostanza formata solamente da atomi semplici Solo i gas inerti dell ottavo gruppo sono presenti in natura
Molecole e legami Chimica generale Atomi e molecole È estremamente difficile trovare in natura una sostanza formata solamente da atomi semplici Solo i gas inerti dell ottavo gruppo sono presenti in natura
1. La forza di Lorentz. Se un fascio catodico è in un campo magnetico:
 Il campo magnetico 1. La forza di Lorentz Se un fascio catodico è in un campo magnetico: La forza di Lorentz Gli elettroni risentono di una forza magnetica anche se non sono in un filo metallico; l'importante
Il campo magnetico 1. La forza di Lorentz Se un fascio catodico è in un campo magnetico: La forza di Lorentz Gli elettroni risentono di una forza magnetica anche se non sono in un filo metallico; l'importante
Misura del momento magnetico dell elettrone
 FACOLTÀ Università degli Studi di Roma Tre DI SCIENZE MATEMATICHE, FISICHE E NATURALI Corso di Laurea in Fisica Misura del momento magnetico dell elettrone Candidato: Andrea Sciandra Matricola 4480 Relatore:
FACOLTÀ Università degli Studi di Roma Tre DI SCIENZE MATEMATICHE, FISICHE E NATURALI Corso di Laurea in Fisica Misura del momento magnetico dell elettrone Candidato: Andrea Sciandra Matricola 4480 Relatore:
IBRIDAZIONE e GEOMETRIA MOLECOLARE
 IBRIDAZIONE e GEOMETRIA MOLECOLARE Esempio: struttura della molecola del metano CH 4 1s 2s 2p Configurazione elettronica del C Per esempio il carbonio può utilizzare la configurazione in cui un elettrone
IBRIDAZIONE e GEOMETRIA MOLECOLARE Esempio: struttura della molecola del metano CH 4 1s 2s 2p Configurazione elettronica del C Per esempio il carbonio può utilizzare la configurazione in cui un elettrone
L atomo. Il neutrone ha una massa 1839 volte superiore a quella dell elettrone. 3. Le particelle fondamentali dell atomo
 L atomo 3. Le particelle fondamentali dell atomo Gli atomi sono formati da tre particelle fondamentali: l elettrone con carica negativa; il protone con carica positiva; il neutrone privo di carica. Il
L atomo 3. Le particelle fondamentali dell atomo Gli atomi sono formati da tre particelle fondamentali: l elettrone con carica negativa; il protone con carica positiva; il neutrone privo di carica. Il
Prova Scritta di Elettricità e Magnetismo e di Elettromagnetismo A. A Febbraio 2008 (Proff. F.Lacava, C.Mariani, F.Ricci, D.
 Prova Scritta di Elettricità e Magnetismo e di Elettromagnetismo A. A. 2006-07 - 1 Febbraio 2008 (Proff. F.Lacava, C.Mariani, F.Ricci, D.Trevese) Modalità: - Prova scritta di Elettricità e Magnetismo:
Prova Scritta di Elettricità e Magnetismo e di Elettromagnetismo A. A. 2006-07 - 1 Febbraio 2008 (Proff. F.Lacava, C.Mariani, F.Ricci, D.Trevese) Modalità: - Prova scritta di Elettricità e Magnetismo:
SOLUZIONE ESERCIZIO 1.1
 SOLUZIONE ESERCIZIO 1.1 La temperatura di fusione ed il coefficiente di espansione termica di alcuni metalli sono riportati nella tabella e nel diagramma sottostante: Metallo Temperatura di fusione [ C]
SOLUZIONE ESERCIZIO 1.1 La temperatura di fusione ed il coefficiente di espansione termica di alcuni metalli sono riportati nella tabella e nel diagramma sottostante: Metallo Temperatura di fusione [ C]
PIANO DI LAVORO ANNUALE
 PIANO DI LAVORO ANNUALE Classe 2 B Disciplina: FISICA A.S. 2016/2017 Docente: prof. Vidhi Meri Ore settimanali: 3 Analisi della situazione di partenza della classe In generale i comportamento degli gli
PIANO DI LAVORO ANNUALE Classe 2 B Disciplina: FISICA A.S. 2016/2017 Docente: prof. Vidhi Meri Ore settimanali: 3 Analisi della situazione di partenza della classe In generale i comportamento degli gli
Magnete. Campo magnetico. Fenomeni magnetici. Esempio. Esempio. Che cos è un magnete? FENOMENI MAGNETICI
 Magnete FENOMENI MAGNETICI Che cos è un magnete? Un magnete è un materiale in grado di attrarre pezzi di ferro Prof. Crosetto Silvio 2 Prof. Crosetto Silvio Quando si avvicina ad un pezzo di magnetite
Magnete FENOMENI MAGNETICI Che cos è un magnete? Un magnete è un materiale in grado di attrarre pezzi di ferro Prof. Crosetto Silvio 2 Prof. Crosetto Silvio Quando si avvicina ad un pezzo di magnetite
Enrico Silva - diritti riservati - Non è permessa, fra l altro, l inclusione anche parziale in altre opere senza il consenso scritto dell autore
 Particelle della presente identiche. opera. Principio di Pauli. 1 Particelle identiche: sommario Finora: proprietà di particella singola. Volendo ottenere il comportamento di più particelle, è necessario
Particelle della presente identiche. opera. Principio di Pauli. 1 Particelle identiche: sommario Finora: proprietà di particella singola. Volendo ottenere il comportamento di più particelle, è necessario
IL LEGAME METALLICO. Metalli
 IL LGAM MTALLICO 1 Non metalli Metalli Metalloidi Proprietà dei metalli levata conducibilità elettrica; levata conducibilità termica; ffetto fotoelettrico; levata duttilità e malleabilità; Lucentezza;
IL LGAM MTALLICO 1 Non metalli Metalli Metalloidi Proprietà dei metalli levata conducibilità elettrica; levata conducibilità termica; ffetto fotoelettrico; levata duttilità e malleabilità; Lucentezza;
Energia degli orbitali
 Energia degli orbitali Il valore dell energia di un orbitale è, in modulo, il valore dell energia necessaria a portare l ele8rone a distanza infinita rispe8o al nucleo. Ha quindi valori sempre nega>vi.
Energia degli orbitali Il valore dell energia di un orbitale è, in modulo, il valore dell energia necessaria a portare l ele8rone a distanza infinita rispe8o al nucleo. Ha quindi valori sempre nega>vi.
Il magnetismo nella materia
 Le orbite degli elettroni in atomo di idrogeno Forma spaziale degli Orbitali elettronici di atomo di idrogeno Un solido Il magnetismo nella materia ferrimagnetismo Dr. Daniele Di Gioacchino Istituto Nazionale
Le orbite degli elettroni in atomo di idrogeno Forma spaziale degli Orbitali elettronici di atomo di idrogeno Un solido Il magnetismo nella materia ferrimagnetismo Dr. Daniele Di Gioacchino Istituto Nazionale
Programma di addestramento raccomandato per l esame con Particelle Magnetiche di 2 livello secondo EN 4179/NAS 410
 Programma di addestramento raccomandato per l esame con Particelle Magnetiche di 2 livello secondo EN 4179/NAS 410 -----0-----0-----0----- 1.0 PROCESSI SPECIALI Concetto di processo speciale Qualificazione
Programma di addestramento raccomandato per l esame con Particelle Magnetiche di 2 livello secondo EN 4179/NAS 410 -----0-----0-----0----- 1.0 PROCESSI SPECIALI Concetto di processo speciale Qualificazione
a) compressione adiabatica fino alla pressione p 2 = kg/cm 2 ;
 PROBLEMI I primi tre problemi sono tratti dal libro P. Fleury, J.P. Mathieu, Esercizi di Fisica, Zanichelli (Bologna, 1970) che contiene i testi e le relative soluzioni, indicati dal loro numero e pagina
PROBLEMI I primi tre problemi sono tratti dal libro P. Fleury, J.P. Mathieu, Esercizi di Fisica, Zanichelli (Bologna, 1970) che contiene i testi e le relative soluzioni, indicati dal loro numero e pagina
DIELETTRICI. 21/06/2007 Chimica e Scienza e Tecnologia dei Materiali Elettrici L16 1
 DIELETTRICI Materiali dielettrici (isolanti): sostanze con resistività elettrica molto elevata. Utilizzati praticamente come isolatori o come condensatori; ρ è maggiore di circa 10 6 Ωm. Nei dielettrici
DIELETTRICI Materiali dielettrici (isolanti): sostanze con resistività elettrica molto elevata. Utilizzati praticamente come isolatori o come condensatori; ρ è maggiore di circa 10 6 Ωm. Nei dielettrici
Teorie del legame chimico. Teorie del legame chimico
 Teorie del legame chimico Le teorie proposte per la trattazione del legame chimico si prefiggono i seguenti scopi: 1. Prevedere la formazione di un legame tra due elementi 2. Predire la lunghezza del legame
Teorie del legame chimico Le teorie proposte per la trattazione del legame chimico si prefiggono i seguenti scopi: 1. Prevedere la formazione di un legame tra due elementi 2. Predire la lunghezza del legame
MATERIALI E TECNOLOGIE ELETTRICHE MATERIALI MAGNETICI
 CORSO DI MATERIALI E TECNOLOGIE ELETTRICE MATERIALI MAGNETICI Prof. Giovanni Lupò Dipartimento di Ingegneria Elettrica Università di Napoli Federico II Corso di Laurea in Ingegneria Elettrica III anno
CORSO DI MATERIALI E TECNOLOGIE ELETTRICE MATERIALI MAGNETICI Prof. Giovanni Lupò Dipartimento di Ingegneria Elettrica Università di Napoli Federico II Corso di Laurea in Ingegneria Elettrica III anno
IIS Moro Dipartimento di matematica e fisica
 IIS Moro Dipartimento di matematica e fisica Obiettivi minimi per le classi prime - Fisica Poiché la disciplina Fisica è parte dell Asse Scientifico Tecnologico, essa concorre, attraverso lo studio dei
IIS Moro Dipartimento di matematica e fisica Obiettivi minimi per le classi prime - Fisica Poiché la disciplina Fisica è parte dell Asse Scientifico Tecnologico, essa concorre, attraverso lo studio dei
I rivelatori. Osservare il microcosmo. EEE- Cosmic Box proff.: M.Cottino, P.Porta
 I rivelatori Osservare il microcosmo Cose prima mai viste L occhio umano non riesce a distinguere oggetti con dimensioni inferiori a 0,1 mm (10-4 m). I primi microscopi vennero prodotti in Olanda alla
I rivelatori Osservare il microcosmo Cose prima mai viste L occhio umano non riesce a distinguere oggetti con dimensioni inferiori a 0,1 mm (10-4 m). I primi microscopi vennero prodotti in Olanda alla
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 8 La chimica dell acqua 3 Sommario 1. Come si formano i legami chimici 2. I legami covalenti ionici 3. La molecola dell acqua
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 8 La chimica dell acqua 3 Sommario 1. Come si formano i legami chimici 2. I legami covalenti ionici 3. La molecola dell acqua
L effetto del sostituente (induttivo e coniugativo) modifica:
 L effetto del sostituente (induttivo e coniugativo) modifica: 1 la densità elettronica del centro di reazione influenza la REATTIVITA Se da un atomo di ad un altro cambia la distribuzione degli elettroni
L effetto del sostituente (induttivo e coniugativo) modifica: 1 la densità elettronica del centro di reazione influenza la REATTIVITA Se da un atomo di ad un altro cambia la distribuzione degli elettroni
