REAZIONI ANALITICHE DELL ARGENTO Stati di ossidazione: 2, 1. Reazioni di Ag(I) Soluzione standard: AgNO 3 EQUAZIONE STECHIOMETRICA
|
|
|
- Andrea Romagnoli
- 7 anni fa
- Visualizzazioni
Transcript
1 I gruppo REAZINI ANALITICHE DELL ARGENT Stati di ossidazione: 2, 1 Reazioni di Ag(I) Soluzione standard: AgN 3 EQUAZINE STECHIMETRICA STAT DI AGGREGAZINE E CLRE DEL PRDTT 1 K 2 Cr 4 1M 2 Ag Cr 4 = Ag 2 Cr 4 precipitato microcristallino rosso-mattone 2 NaH 2 Ag 2 H - = Ag 2 H 2 precipitato microcristallino marroncinoargilla 3 HCl Ag Cl - = AgCl precipitato cristallino bianco 4 Soluzione da 3) NH 3 AgCl 2 NH 3 = Ag(NH 3 ) 2 Cl - 5 KBr Ag Br - = AgBr si scioglie il ppt bianco di AgCl precipitato colloidale di colore bianco con riflessi giallini 6 KI 0,1M Ag I - = AgI precipitato colloidale di colore giallo chiaro 7 Soluzione da 4) KI 0,1M Ag(NH 3 ) 2 I - = AgI 2 NH 3 precipitato colloidale di colore giallo chiaro 8 Soluzione da 6) Na 2 S 2 3 * AgI 2 S 2 3 = Ag(S 2 3 ) 2 3- I - complesso giallo ocra * Disciogliere qualche cristallo di Na 2 S 2 3 in poche gocce d acqua
2 REAZINI ANALITICHE DEL PIMB Stati di ossidazione: 4, 2 I gruppo Reazioni di Pb(II) Soluzione standard: Pb(N 3 ) 2 EQUAZINE STECHIMETRICA STAT DI AGGREGAZINE E CLRE DEL PRDTT 1 HCl Pb 2 2 Cl - PbCl 2 (a caldo) (a freddo) precipitato bianco cristallino aghiforme che a caldo si scioglie completamente 2 NaF* solido Pb 2 2 F - PbF 2 precipitato bianco microcristallino 3 H 2 S 4 Pb 2 S 4 PbS 4 precipitato bianco colloidale 4 KI 0,1M Pb 2 2 I - PbI 2 precipitato giallo cristallino 5 NaH diluito, o NH 3 Pb 2 3H - Pb(H) 2 precipitato di colore bianco 6 K 2 Cr 4 1M Pb 2 Cr 4 PbCr 4 precipitato giallo chiaro cristallino 7 Soluzione da 6) NaH PbCr 4 3 H - Pb(H) 3- Cr 4 si scioglie il ppt giallo di PbCr 4 * Disciogliere qualche cristallo di NaF in poche gocce d acqua.
3 I gruppo REAZINI ANALITICHE DEL MERCURI Stati di ossidazione: 2, 1 Reazioni di Hg(I) Soluzione standard: Hg 2 (N 3 ) 2 EQUAZINE STECHIMETRICA STAT DI AGGREGAZINE E CLRE DEL PRDTT 1 K 2 Cr 4 1M Hg 2 2 Cr 4 Hg 2 Cr 4 precipitato arancione microcristallino 2 HCl Hg Cl - Hg 2 Cl 2 precipitato bianco cristallino polverulento 3 KI 0,1M Hg I - Hg 2 I 2 (dismuta velocemente in Hg nero) precipitato verde giallo microcristallino 4 NaH Hg H - Hg Hg H 2 precipitato grigio scuro 5 6 Soluzione da 3) KI (eccesso) Soluzione da 2) NH 3 Hg 2 I 2 2 I - Hg HgI 4 si scioglie il ppt verde giallo di Hg 2 I 2 Hg 2 Cl 2 2 NH 3 Hg HgNH 2 Cl Cl - NH 4 precipitato di colore nero
4 I gruppo REAZINI ANALITICHE DEL TUNGSTEN Stati di ossidazione: 6, 5, 4, 3, 2 Reazioni di W(VI) Soluzione standard: Na 2 W 4 EQUAZINE STECHIMETRICA STAT DI AGGREGAZINE E CLRE DEL PRDTT 1 HCl (a freddo) 2 H W 4 X H 2 H 2 W 4 X H 2 precipitato di colore bianco 2 Soluzione da 1 a caldo 3 SnCl 2 * HCl 12M H 2 W 4 X H 2 H 2 W 4 X H 2 2 H 2 W 4 SnCl 4 2 Cl - 2 H W 2 5 SnCl 6 3 H 2 il ppt bianco diventa giallo intenso precipitato di colore blu intenso * Controllare se SnCl 2 è fresco con HgCl 2 (SnCl 2 ha tendenza ad ossidarsi all aria): Sn 2 2 HgCl 2 2 Cl - SnCl 4 Hg 2 Cl 2 precipita Hg 2 Cl 2 bianco polverulento
5 II gruppo Reazioni di Hg(II) Soluzione standard: HgCl 2 EQUAZINE STECHIMETRICA 1 NaH Hg 2 2 H - Hg H 2 STAT DI AGGREGAZINE E CLRE DEL PRDTT precipitato arancione-marrone colloidale 2 KI 0,1M Hg 2 2 I - HgI 2 precipitato rosso-arancio colloidale 3 Soluzione da 2) KI 0,1M HCl HgI 2 2 I - 2 H H 2 HgI 4 (estrarre in esone) si scioglie HgI 2 : la soluzione è incolore; in esone H 2 HgI 4 è giallo intenso 4 Lastra di Cu HgCl 2 Cu Hg(amalgama) CuCl 2 sopra la lamina di Cu. Per riscaldamento l amalgama si deposita una patina argentea scompare
6 II gruppo Reazioni di Bi(III) REAZINI ANALITICHE DEL BISMUT Stati di ossidazione: 5, 3 Soluzione standard: BiCl 3 in HCl EQUAZINE STECHIMETRICA STAT DI AGGREGAZ. E CLRE 1 H 2 * BiCl 4- H 2 BiCl 2 H 3 Cl - precipitato bianco molto colloidale 2 NaH diluito, o NH 3 Bi 3 3 H - Bi(H) 3 calore BiH H 2 3 KI 0,1M Bi 3 H 4 I - HBiI 4 (estrarre in esone) a freddo precipita Bi(H) 3 bianco, mentre a caldo si forma BiH giallo si sviluppa un colore rossosangue in esone 4 SnCl 2 NaH 2Bi 3 18H - 3Sn 2 2Bi(H) 3 3Sn(H) 4 2 Bi 3 Sn(H) 6 H 2 precipita istantaneamente Bi nero metallico * Due gocce di soluzione standard di BiCl 3 vanno diluite con molta acqua in una provetta grande.
7 II gruppo REAZINI ANALITICHE DEL RAME Stati di ossidazione: 3, 2, 1 Reazioni di Cu(II) Soluzione standard: CuS 4 EQUAZINE STECHIMETRICA STAT DI AGGREGAZINE. E CLRE 1 HCl Cu 2 4 Cl - CuCl 4 complesso di colore verde chiaro 2 KI 0,1M 2 Cu 2 4 I - 2 CuI I 2 (estrarre in esone) 3 K 2 Cr 4 1M Cu 2 Cr 4 CuCr 4 precipitato bianco (CuI) in fase acquosa e I 2 bruno in fase esonica precipitato di colore rossomarrone 4 K 4 Fe(CN) 6 0,1M 2 Cu 2 Fe(CN) 4- precipitato di colore rosso-bruno 6 Cu 2 Fe(CN) 6 scuro 5 NH 3 Cu 2 4 NH 3 Cu(NH 3 ) 2 complesso blu-azzurro molto 4 intenso 6 NaH dil. Cu 2 2 H - Cu(H) 2 precipitato colloidale azzurro turchino 7 NaH Cu 2 3 H - Cu(H) 3 - complesso blu con riflessi violetti 8 Na 2 S 2 4 solido NH 3 15M Cu(NH 3 ) 4 2 S H - Cu 2 S 3 4 NH 3 2 H 2 ppt grigio-rossiccio di Cu metallico
8 III gruppo REAZINI ANALITICHE DEL FERR Stati di ossidazione: 6, 3, 2 Reazioni di Fe(II) Soluzione standard: FeS 4 EQUAZINE STECHIMETRICA STAT DI AGGREGAZINE E CLRE DEL PRDTT 1 K 3 [Fe(CN) 6 ]0,1M K Fe 2 [Fe(CN) 6 ] 3- si forma un precipitato blu scuro KFe[Fe(CN) 6 ] 2 KN 2 H 2 S 4 2 Fe 2 N FeN 2 Fe 3 H 2 complesso marrone scuro in soluzione Reazioni di Fe(III) Soluzione standard: FeCl 3 3 NaH diluito, o NH 3 4 K 4 Fe(CN) 6 0,1M 5 K 3 Fe(CN) 6 0,1M 6 NH 4 SCN (sol. satura) 7 Soluzione da 6 NaFsolido EQUAZINE STECHIMETRICA Fe 3 3 NH 3 3 H 2 Fe(H) 3 3 NH 4 K Fe 3 [Fe(CN) 6 ] 4- KFe[Fe(CN) 6 ] STAT DI AGGREGAZINE E CLRE DEL PRDTT si forma Fe(H) 3, un precipitato rosso ruggine si forma un precipitato blu scuro Fe 3 [Fe(CN) 6 ] 3- Fe[Fe(CN) 6 ] composto verde scuro con tendenza a rimanere in soluzione anziché precipitare (complesso con spiccate proprietà colloidali) Fe 3 3 SCN - Fe(SCN) 3 (estrarre in esone) Fe(SCN) 3 3 F - FeF 3 3 SCN - in soluzione si forma una colorazione rosso sangue molto scura il complesso rosso sangue viene distrutto per formazione di FeF 3 che ha una K f molto più alta di Fe(SCN) 3
9 III gruppo Reazioni di V(V) REAZINI ANALITICHE DEL VANADI Stati di ossidazione: 5, 4, 3, 2 Soluzione standard: V 2 Cl EQUAZINE STECHIMETRICA STAT DI AGGREGAZINE E CLRE DEL PRDTT NH 4 Cl solido NH 3 15M Zn metallico in polvere HCl H 2 2 al 3% HN 3 3M V 2 NH 4 2 H - NH 4 V 3 H 2 2 V 2 Zn 4 H 2 V 2 Zn 2 2 H 2 2 V 2 Zn 4 H 2 V 3 Zn 2 2 H 2 2 V 3 Zn 2 V 2 Zn 2 V 2 H H V(H 2 2 ) 3 H 2 precipita il vanadato d ammonio giallo chiaro la soluzione è dapprima giallo chiaro [V(V)], poi diventa azzurro-blu [V(IV)], quindi diventa verde [V(III)], e infine diventa violetto scuro [V(II)] in soluzione si forma un complesso arancio intenso
10 III gruppo REAZINI ANALITICHE DEL CRM Reazioni di Cr(III) Soluzione standard: Cr(N 3 ) 3 Standard per il coccio: Cr(H) 3 1 NH 3 (a freddo) EQUAZINE STECHIMETRICA Cr 3 3 NH 3 3 H 2 Cr(H) 3 3 NH 4 STAT DI AGGREGAZINE E CLRE DEL PRDTT precipitato bianco-grigio colloidale 2 NaH diluito Cr 3 3 H - Cr(H) 3 precipitato bianco-grigio colloidale 3 NaH Cr(H) 3 H - Cr(H) 4 - complesso verde intenso 4 H 2 2 al 3% NaH 2 Cr(H) 4-3 H H - 2 Cr 4 8 H 2 la soluzione si colora istantaneamente di un colore giallo intenso
11 III gruppo 5 Na 2 C 3 solido KN 3 solido* 6 Solido fuso su coccio da 5) CH 3 CH ** REAZINI ANALITICHE DEL CRM (Coccio) 2 Cr(H) 3 2 Na 2 C 3 3 KN 3 2 Na 2 Cr 4 3 KN 2 2 C 2 3 H 2 Na 2 Cr 4 Cr 4 2 Na (se il ph è molto acido si ha anche: 2 Cr 4 2 H Cr 2 7 H 2 ) dopo la fusione con miscela ossidante è possibile riscontrare la presenza di un sale fuso di colore giallo intenso trattando la massa fusa con CH 3 CH si ha la sua dissoluzione con formazione di una soluzione giallino-bruna (stato intermedio di equilibrio fra la forma cromato e bicromato) 7 Surnatante da 6) Cr 4 Pb 2 PbCr 4 precipita il cromato di Pb di colore Pb(N 3 ) 2 giallo chiaro cristallino * Questa reazione avviene per fusione su coccio dello standard Cr(H) 3 con miscela fondente-ossidante: tale miscela è composta da 3 parti di Na 2 C 3 solido 1 parte di KN 3 solido. ** Aggiungere con cautela alcune gocce di CH 3 CH alla massa fusa (fredda!) sul coccio e raccogliere il liquido in una provetta da centrifuga. Quindi centrifugare e verificare che il ph sia acido (se necessario aggiungere altro acido acetico). Solo dopo tale procedura è possibile passare alla reazione 7).
12 III gruppo REAZINI ANALITICHE DEL MANGANESE Stati di ossidazione: 7, 6, 5, 4, 3, 2, 1 Reazioni di Mn(II) Soluzione standard: MnS 4 Standard per il coccio: MnC 3 EQUAZINE STECHIMETRICA STAT DI AGGREG. E CLRE 1 NH 3 Mn 2 2 NH 3 2 H 2 Mn(H) 2 2 NH 4 si forma un precipitato biancastro 2 NH Soluzione da 1) H 2 2 al 3% 4 NaBi 3 solido HN 3 4 Mn 2 8 NH H 2 4 Mn(H) 3 8 NH 4 si forma un precipitato marrone chiaro Mn(H) 2 H 2 2 Mn(H) 2 H 2 si forma un precipitato marrone scuro 2 Mn 2 5 NaBi 3 14 H 2 Mn 4-5 Bi 3 5 Na 7 H 2 con sodio bismutato la soluzione diventa subito viola intenso senza bisogno di scaldare a bagnomaria
13 III gruppo REAZINI ANALITICHE DEL MANGANESE (Coccio) Stati di ossidazione: 7, 6, 5, 4, 3, 2, 1 Reazioni di Mn(II) Soluzione standard: Mn(N 3 ) 2 Standard per il coccio: MnC 3 5 Na 2 C 3 solido KN 3 solido NaH pastiglie 6 Solido fuso su coccio da 5 CH 3 CH EQUAZINE STECHIMETRICA STAT DI AGGREG. E CLRE MnC 3 Na 2 C 3 2 KN 3 Na 2 Mn 4 2 C 2 il solido fuso assume una 2 KN 2 colorazione verde scuro 3 Mn 4 4 H 2 Mn 4- Mn 2 2 H 2 la soluzione diventa color violetto intenso, mentre sul fondo si ha un deposito marrone scuro
14 III gruppo REAZINI ANALITICHE DELL ALLUMINI Stati di ossidazione: 3 Reazioni di Al(III) Soluzione standard: Al 2 (S 4 ) 3 EQUAZINE STECHIMETRICA STAT DI AGGREGAZINE E CLRE DEL PRDTT 1 NaH diluito Al 3 3 H - Al(H) 3 precipitato bianco che precipita come lacca 2 NaH Al(H) 3 H - [Al(H) 4 ] - il precipitato bianco di Al(H) 3 si scioglie 3 NH 4 H 2 P 4 Al 3 H 2 P 4- AlP 4 2 H ppt bianco a fiocchi che precipita lentamente 4 Tampone acetato Aluminon (C 22 H 25 N 3 10 ) Al 3 3 H - Al(H) 3 Al(H) 3 Aluminon Aluminon adsorbito su Al(H) 3 un ppt bianco colloidale adsorbe il colorante Aluminon sulla propria superficie colorandosi di rosso e rendendo la soluzione incolore. La reazione si può eseguire anche su carta da cromatografia H C HNH 3 H 3 NH H C C H C HNH 3 H ALUMINN (Sale triammonico dell'acido aurintricarbossilico)
15 IV gruppo REAZINI ANALITICHE DEL CBALT Stati di ossidazione: 4, 3, 2, 0 Reazioni di Co(II) Soluzione standard: CoS 4 REAGEN TI 1 NH 3 diluito 2 Soluz. da 1) NH 3 (eccesso) 3 Soluz. da 2 2 (aria) 4 NH 4 SCN (sol. satura) 5 FeCl 3 NH 4 SCN (sol. satura) 6 Soluzione da 5 NaF solido EQUAZINE STECHIMETRICA 2 Co 2 2 NH 3 2 H 2 S 4 [Co(H)] 2 S 4 2 NH 4 [Co(H)] 2 S 4 12 NH 3 2 Co(NH 3 ) 6 2 S 4-2 H - STAT DI AGGREGAZINE E CLRE DEL PRDTT precipitato colloidale di colore bluverde subito dopo l aggiunta dell eccesso di NH 3 il precipitato che si era formato si scioglie: la soluzione è incolore 4 Co(NH 3 ) H 2 4 Co(NH 3 ) H - agitando e attendendo, si forma il complesso del Co(III) con l ammoniaca rosa scuro Co 2 2 SCN - Co(SCN) 2 (estrarre in esone) Fe 3 Co 2 5 SCN - Co(SCN) 2 Fe(SCN) 3 (estrarre in esone) in fase organica si ripartisce un complesso blu intenso di Co(SCN) 2 la fase organica assume prima una colorazione rosso intenso, che diventa rapidamente sempre più blu: il risultato finale è un insieme delle due colorazioni Co(SCN) 2 Fe(SCN) 3 3 F - Co(SCN) 2 FeF 3 aggiungendo NaF solido la colorazione 3 SCN - rossa in fase organica scompare e rimane solo quella blu intenso
16 IV gruppo 1 NaH diluito 2 Precipitato da 1) NH 3 3 HDMG 0,1M* REAZINI ANALITICHE DEL NICHEL Stati di ossidazione: 4, 3, 2, 1 Reazioni di Ni(II) Soluzione standard: Ni(CH 3 C) 2 EQUAZINE STECHIMETRICA Ni 2 2 H - Ni(H) 2 Ni(H) 2 6 NH 3 Ni(NH 3 ) H - Ni 2 2 HDMG Ni(DMG) 2 2 H STAT DI AGGREGAZINE E CLRE DEL PRDTT precipitato verdino si solubilizza il precipitato per formazione del complesso con NH 3 di colore blu indaco precipita un complesso rosso ciliegia * HDMG = Dimetilgliossima (C 4 H 8 N 2 2 ). Eseguire questa prova mediante spot test su piastra di porcellana bianca.
17 IV gruppo REAGEN TI REAZINI ANALITICHE DELL ZINC Stati di ossidazione: 2 Reazioni di Zn(II) Soluzione standard: ZnS 4 EQUAZINE STECHIMETRICA STAT DI AGGREGAZINE E CLRE DEL PRDTT 1 NaH dil. Zn 2 2 H - Zn(H) 2 precipitato bianco molto colloidale 2 3 NaH Zn(H) 2 2 H - Zn(H) 4 K 4 Fe(CN) 3 Zn 2 2 K 2 [Fe(CN) 4-6 ] 6 0,1 M K 2 Zn 3 [Fe(CN) 6 ] 2 il ppt bianco si scioglie: la soluzione è incolore precipitato bianco colloidale 4 HDz* Zn 2 2 HDz Zn(Dz) 2 2 H durante l eluizione si forma un anello rossorosa * HDz = Ditizone o Difeniltiocarbazone (C 13 H 12 N 4 S 0,1 g/l in cloroformio).
1 Gruppo: Ag + ; Hg 2 2+ ; Pb ++ Reattivo precipitante: HCl dil (2N).
 1 Gruppo: Ag + ; Hg + ; Pb ++ Reattivo precipitante: HCl dil (N). Procedimento: Polvere (punta di spatola; provetta da centrifuga) + Acqua deionizzata + HN 3 dil. (si usa dil. per evitare l ossidazione
1 Gruppo: Ag + ; Hg + ; Pb ++ Reattivo precipitante: HCl dil (N). Procedimento: Polvere (punta di spatola; provetta da centrifuga) + Acqua deionizzata + HN 3 dil. (si usa dil. per evitare l ossidazione
ALOGENURI (Cl -, Br -, I - ) 1
 ALOGENURI (Cl -, Br -, I - ) 1 Cloruri, bromuri e ioduri di tutti i metalli, eccetto quelli di Pb +,Ag + e Hg + (I), sono solubili in H O. Cloruri, bromuri e ioduri di Pb +,Ag + e Hg + (I) sono inoltre
ALOGENURI (Cl -, Br -, I - ) 1 Cloruri, bromuri e ioduri di tutti i metalli, eccetto quelli di Pb +,Ag + e Hg + (I), sono solubili in H O. Cloruri, bromuri e ioduri di Pb +,Ag + e Hg + (I) sono inoltre
(Si identificano Ag +, Hg 2. , Pb 2+ ) - 1 GRUPPO - Reattivo Generale: HCl 2N. Soluzione. Precipitato. Soluzione. Residuo. Soluzione.
 Reattivo Generale: HCl 2N - 1 GRUPPO - (Si identificano Ag +, Hg 2 2+, Pb 2+ ) Esame Sistematico: Nella provetta da centrifuga contenente la soluzione in esame (preparata sciogliendo la sostanza in H 2
Reattivo Generale: HCl 2N - 1 GRUPPO - (Si identificano Ag +, Hg 2 2+, Pb 2+ ) Esame Sistematico: Nella provetta da centrifuga contenente la soluzione in esame (preparata sciogliendo la sostanza in H 2
ANALISI SISTEMATICA DEI CATIONI
 ANALISI SISTEMATICA DEI CATIONI Particolare procedura analitica attraverso la quale tutte le specie cationiche presenti in una ipotetica miscela vengono inizialmente separate in gruppi, mediante l uso
ANALISI SISTEMATICA DEI CATIONI Particolare procedura analitica attraverso la quale tutte le specie cationiche presenti in una ipotetica miscela vengono inizialmente separate in gruppi, mediante l uso
IV Gruppo: H 2 S 2 H + + S = I solfuri insolubili nelle predette condizioni sono: ZnS. CoS. bianco. nero. MnS. rosa-salmone. nero.
 IV Gruppo: Comprende quei cationi che precipitano selettivamente come solfuri insolubili a ph = 9 in soluzione tampone: NH 4 OH/NH 4 Cl (esclusi quelli del I, II e III Gruppo). Il reattivo precipitante
IV Gruppo: Comprende quei cationi che precipitano selettivamente come solfuri insolubili a ph = 9 in soluzione tampone: NH 4 OH/NH 4 Cl (esclusi quelli del I, II e III Gruppo). Il reattivo precipitante
IV Gruppo: I solfuri insolubili nelle predette condizioni sono: ZnS. CoS. bianco. nero. MnS. nero. rosa-salmone. NiS
 IV Gruppo: Comprende quei cationi che precipitano selettivamente come solfuri insolubili a ph = 9 in soluzione tampone: NH 4 OH/NH 4 Cl (esclusi quelli del I, II e III Gruppo). Il reattivo precipitante
IV Gruppo: Comprende quei cationi che precipitano selettivamente come solfuri insolubili a ph = 9 in soluzione tampone: NH 4 OH/NH 4 Cl (esclusi quelli del I, II e III Gruppo). Il reattivo precipitante
Fe(OH) 3. Mn(OH) 2 2H 2 O
 III Gruppo: Comprende quei cationi che precipitano selettivamente come idrossidi insolubili a ph = 9 (esclusi quelli del I e II Gruppo). Il reattivo precipitante è NH 4 OH/NH 4 Cl (soluzione tampone a
III Gruppo: Comprende quei cationi che precipitano selettivamente come idrossidi insolubili a ph = 9 (esclusi quelli del I e II Gruppo). Il reattivo precipitante è NH 4 OH/NH 4 Cl (soluzione tampone a
Fe(OH) 3. Mn(OH) 2. bianco. MnO 2 2H 2 O
 III Gruppo: Comprende quei cationi che precipitano selettivamente come idrossidi insolubili a ph = 9 (esclusi quelli del I e II Gruppo). Il reattivo precipitante è NH 4 OH/NH 4 Cl (soluzione tampone a
III Gruppo: Comprende quei cationi che precipitano selettivamente come idrossidi insolubili a ph = 9 (esclusi quelli del I e II Gruppo). Il reattivo precipitante è NH 4 OH/NH 4 Cl (soluzione tampone a
II Gruppo: CH 3 - C + H 2 O CH 3 - C + H 2 S CH 3 - C + NH 4 OH TAA
 II Gruppo: Comprende quei cationi che precipitano selettivamente come solfuri insolubili nell intervallo di ph = 0 2 per HCl (esclusi quelli del I Gruppo). Il reattivo precipitante è la solfuro d ammonio
II Gruppo: Comprende quei cationi che precipitano selettivamente come solfuri insolubili nell intervallo di ph = 0 2 per HCl (esclusi quelli del I Gruppo). Il reattivo precipitante è la solfuro d ammonio
Reazioni analitiche dello ione alluminio L ammoniaca in soluzione acquosa provoca la precipitazione dell idrossido Al(OH) 3 bianco gelatinoso.
 Reazioni analitiche dello ione alluminio L ammoniaca in soluzione acquosa provoca la precipitazione dell idrossido Al(OH) bianco gelatinoso. Al NHOH Al(OH) NH L idrossido precipitato è quasi insolubile
Reazioni analitiche dello ione alluminio L ammoniaca in soluzione acquosa provoca la precipitazione dell idrossido Al(OH) bianco gelatinoso. Al NHOH Al(OH) NH L idrossido precipitato è quasi insolubile
RICERCA DEI CATIONI NELLE SOSTANZE INORGANICHE O ORGANO-METALLICHE RICERCA DEGLI ANIONI NEI SALI DI AMMINE O DI AMMONIO QUATERNARIO
 RICERCA DEI CATIONI NELLE SOSTANZE INORGANICHE O ORGANO-METALLICHE RICERCA DEGLI ANIONI NEI SALI DI AMMINE O DI AMMONIO QUATERNARIO Prof. Antonio Lavecchia Ricerca dei Cationi nelle Sostanze Inorganiche
RICERCA DEI CATIONI NELLE SOSTANZE INORGANICHE O ORGANO-METALLICHE RICERCA DEGLI ANIONI NEI SALI DI AMMINE O DI AMMONIO QUATERNARIO Prof. Antonio Lavecchia Ricerca dei Cationi nelle Sostanze Inorganiche
RICONOSCIMENTO degli ELEMENTI PRESENTI in un CAMPIONE INCOGNITO
 RICONOSCIMENTO degli ELEMENTI PRESENTI in un CAMPIONE INCOGNITO OBIETTIVO: individuare gli elementi presenti in un campione solido inorganico di composizione incognita. Approccio al problema: l analisi
RICONOSCIMENTO degli ELEMENTI PRESENTI in un CAMPIONE INCOGNITO OBIETTIVO: individuare gli elementi presenti in un campione solido inorganico di composizione incognita. Approccio al problema: l analisi
Le reazioni di ossidoriduzione
 Le reazioni di ossidoriduzione Le reazioni di ossidoriduzioni o redox sono reazioni nelle quali si ha variazione del numero di ossidazione ( n. o. ) di ioni o atomi. La specie chimica che si ossida cede
Le reazioni di ossidoriduzione Le reazioni di ossidoriduzioni o redox sono reazioni nelle quali si ha variazione del numero di ossidazione ( n. o. ) di ioni o atomi. La specie chimica che si ossida cede
Sostanze organiche: determinazioni qualitative
 Fenolo ((European Pharmacopoeia IV th, F.U. X edizione) Determinare il punto di fusione (41-42 C) Identificazione A. REAZIONE con acqua di Bromo. N.B. Si lavora sotto cappa! Aggiungere a 1 ml della soluzione
Fenolo ((European Pharmacopoeia IV th, F.U. X edizione) Determinare il punto di fusione (41-42 C) Identificazione A. REAZIONE con acqua di Bromo. N.B. Si lavora sotto cappa! Aggiungere a 1 ml della soluzione
I PROVA INCOGNITA. Cognome.. Nome. corso. Pesafiltri n...
 Cognome.. I PROVA INCOGNITA Nome. corso. Pesafiltri n... Cationi Data Anioni Firma 1 MISCELA INCOGNITA PbCO 3 CuCl 2 Co(NO 3 ) 2 SrCO 3 Piombo carbonato Cloruro rameico Cobalto nitrato Stronzio carbonato
Cognome.. I PROVA INCOGNITA Nome. corso. Pesafiltri n... Cationi Data Anioni Firma 1 MISCELA INCOGNITA PbCO 3 CuCl 2 Co(NO 3 ) 2 SrCO 3 Piombo carbonato Cloruro rameico Cobalto nitrato Stronzio carbonato
(appunti di Daniela Discalzi e Serena Fortino) Con l'analisi quantitativa si determina la quantità di componenti presenti in un miscuglio.
 ANALISI QUALITATIVA INRGANICA (appunti di Daniela Discalzi e Serena Fortino) Con l'analisi quantitativa si determina la quantità di componenti presenti in un miscuglio. L'analisi qualitativa indica quali
ANALISI QUALITATIVA INRGANICA (appunti di Daniela Discalzi e Serena Fortino) Con l'analisi quantitativa si determina la quantità di componenti presenti in un miscuglio. L'analisi qualitativa indica quali
Esercitazione 6. Chimica biologica del Fe. Il Ferro ) 2 (SO 4 6H 2. Fe(NH 4
 Esercitazione Preparazione del sale di Mohr Fe(NH 4 ) 2 (SO 4 ) 2 H 2 O Chimica biologica del Fe In un uomo di 75 kg sono presenti 4 g di Fe Nei Paesi occidentali ne assumiamo 15 mg/d Il Ferro Configurazione
Esercitazione Preparazione del sale di Mohr Fe(NH 4 ) 2 (SO 4 ) 2 H 2 O Chimica biologica del Fe In un uomo di 75 kg sono presenti 4 g di Fe Nei Paesi occidentali ne assumiamo 15 mg/d Il Ferro Configurazione
RICERCA RICERCA DEGLI ANIONI
 RICERCA DEGLI ANIONI 1 SOSTANZA INIZIALE Na 2 CO 3 Ricerca: ACETATI SOLFITI CARBONATI TARTRATI SOLUZIONE ALCALINA Limpida Incolore RESIDUO Si scarta Ricerca: SOLFATI OSSALATI ARSENIATI NITRITI NITRATI
RICERCA DEGLI ANIONI 1 SOSTANZA INIZIALE Na 2 CO 3 Ricerca: ACETATI SOLFITI CARBONATI TARTRATI SOLUZIONE ALCALINA Limpida Incolore RESIDUO Si scarta Ricerca: SOLFATI OSSALATI ARSENIATI NITRITI NITRATI
NUMERI DI OSSIDAZIONE
 NUMERI DI SSIDAZINE Il numero di ossidazione degli elementi allo stato libero è ZER La somma algebrica dei numeri di ossidazione di tutti gli atomi di una molecola neutra è ZER La somma algebrica dei numeri
NUMERI DI SSIDAZINE Il numero di ossidazione degli elementi allo stato libero è ZER La somma algebrica dei numeri di ossidazione di tutti gli atomi di una molecola neutra è ZER La somma algebrica dei numeri
Chimica generale ed inorganica per il Corso di Laurea magistrale in Farmacia
 Chimica generale ed inorganica per il Corso di Laurea magistrale in Farmacia 1) La NMECLATURA dei composti chimici La formula chimica dell ossido ferrico è: (a) Fe32 (b) Fe23 (c) Fe (d) Fe3 La formula
Chimica generale ed inorganica per il Corso di Laurea magistrale in Farmacia 1) La NMECLATURA dei composti chimici La formula chimica dell ossido ferrico è: (a) Fe32 (b) Fe23 (c) Fe (d) Fe3 La formula
Università degli Studi di Torino CORSO DI CHIMICA GENERALE ED INORGANICA C. Schede di valutazione relative alle esercitazioni pratiche in laboratorio
 Università degli Studi di Torino CORSO DI CHIMICA GENERALE ED INORGANICA C Schede di valutazione relative alle esercitazioni pratiche in laboratorio Anno accademico 2006-2007 Dott.ssa Elena Ghibaudi Dott.
Università degli Studi di Torino CORSO DI CHIMICA GENERALE ED INORGANICA C Schede di valutazione relative alle esercitazioni pratiche in laboratorio Anno accademico 2006-2007 Dott.ssa Elena Ghibaudi Dott.
Sostanze inorganiche: determinazioni qualitative
 Carbonati e Bicarbonati Indicare il tipo di sostanza basandosi sulle caratteristiche alla calcinazione e le prove di solubilità e il ph. Sodio carbonato anidro Na 2 CO 3 (F.U. X Edizione, European Pharmacopeia
Carbonati e Bicarbonati Indicare il tipo di sostanza basandosi sulle caratteristiche alla calcinazione e le prove di solubilità e il ph. Sodio carbonato anidro Na 2 CO 3 (F.U. X Edizione, European Pharmacopeia
I PROVA INCOGNITA. Cognome.. Nome. corso. Pesafiltri n...
 Cognome.. I PROVA INCOGNITA Nome. corso. Pesafiltri n... Cationi Data Anioni Firma MISCELA INCOGNITA 4 cationi e 3 anioni PbCO 3 CuCl 2 Co(NO 3 ) 2 SrCO 3 Piombo carbonato Cloruro rameico Cobalto nitrato
Cognome.. I PROVA INCOGNITA Nome. corso. Pesafiltri n... Cationi Data Anioni Firma MISCELA INCOGNITA 4 cationi e 3 anioni PbCO 3 CuCl 2 Co(NO 3 ) 2 SrCO 3 Piombo carbonato Cloruro rameico Cobalto nitrato
CORSO DI LAUREA IN BIOLOGIA ECOLOGICA. Esercitazioni di Laboratorio di Chimica Generale ed Inorganica
 CORSO DI LAUREA IN BIOLOGIA ECOLOGICA Esercitazioni di Laboratorio di Chimica Generale ed Inorganica Anno Accademico 2002-2003 1 ESERCITAZIONE Titolazione di una soluzione di HCl con una soluzione di NaOH
CORSO DI LAUREA IN BIOLOGIA ECOLOGICA Esercitazioni di Laboratorio di Chimica Generale ed Inorganica Anno Accademico 2002-2003 1 ESERCITAZIONE Titolazione di una soluzione di HCl con una soluzione di NaOH
Sostanze organiche: determinazioni qualitative
 Acido acetilsalicilico (European Pharmacopoeia IV th, F.U. X edizione) Determinare il punto di fusione (143 C) Aggiungere 4 ml di NaOH soluzione dil. a 0,2 gr della sostanza in esame e bollire per 3 minuti.
Acido acetilsalicilico (European Pharmacopoeia IV th, F.U. X edizione) Determinare il punto di fusione (143 C) Aggiungere 4 ml di NaOH soluzione dil. a 0,2 gr della sostanza in esame e bollire per 3 minuti.
Reazioni analitiche dello ione acetato
 Reazioni analitiche dello ione acetato Gli acetati trattati con acidi più forti dell acido acetico formano acido acetico, un liquido incolore, volatile che odora di aceto. Il composto generalmente utilizzato
Reazioni analitiche dello ione acetato Gli acetati trattati con acidi più forti dell acido acetico formano acido acetico, un liquido incolore, volatile che odora di aceto. Il composto generalmente utilizzato
ESAME DI ANALISI DELLE SOSTANZE INORGANICHE DI IMPIEGO FARMACEUTICO + LABORATORIO DI ANALISI QUALITATIVA. Nome e cognome: Numero di matricola:..
 ESAME DI ANALISI DELLE SOSTANZE INORGANICHE DI IMPIEGO FARMACEUTICO + LABORATORIO DI ANALISI QUALITATIVA Nome e cognome: Numero di matricola:.. 1) Indicare, motivando la risposta, il ph di una soluzione
ESAME DI ANALISI DELLE SOSTANZE INORGANICHE DI IMPIEGO FARMACEUTICO + LABORATORIO DI ANALISI QUALITATIVA Nome e cognome: Numero di matricola:.. 1) Indicare, motivando la risposta, il ph di una soluzione
PRIMA ESPERIENZA DI LABORATORIO. Prof. Antonio Lavecchia
 PRIMA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Prima Esperienza di Laboratorio Analisi Qualitativa Elementare di Sostanze Inorganiche (Via Umida e Via Secca) Ricerca dei Cationi Calcio, Magnesio,
PRIMA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Prima Esperienza di Laboratorio Analisi Qualitativa Elementare di Sostanze Inorganiche (Via Umida e Via Secca) Ricerca dei Cationi Calcio, Magnesio,
ANALISI ORGANICA Saggi preliminari
 ANALISI ORGANICA Le sostanze ORGANICHE sono per buona parte molecole strutturalmente complesse e a volte abbastanza simili tra di loro. Inoltre, il loro numero è grande per cui eseguire l identificazione
ANALISI ORGANICA Le sostanze ORGANICHE sono per buona parte molecole strutturalmente complesse e a volte abbastanza simili tra di loro. Inoltre, il loro numero è grande per cui eseguire l identificazione
OSSIDAZIONI CON PERMANGANATO DI POTASSIO
 OSSIDAZIONI CON PERMANGANATO DI POTASSIO Il permanganato di potassio è agente ossidante forte di colore viola intenso. In soluzioni fortemente acide (ph ~1) è ridotto a Mn 2+ incolore. MnO 4 + 8H + + 5e
OSSIDAZIONI CON PERMANGANATO DI POTASSIO Il permanganato di potassio è agente ossidante forte di colore viola intenso. In soluzioni fortemente acide (ph ~1) è ridotto a Mn 2+ incolore. MnO 4 + 8H + + 5e
RICERCA DEGLI ANIONI
 RICERCA DEGLI ANIONI RICERCA DEGLI ANIONI SOSTANZA INIZIALE via secca via umida (soluzione alcalina) Ricerca: ACETATI CARBONATI TARTRATI SOLFITI SOLUZIONE Limpida Incolore RESIDUO Si scarta Ricerca: CLORURI
RICERCA DEGLI ANIONI RICERCA DEGLI ANIONI SOSTANZA INIZIALE via secca via umida (soluzione alcalina) Ricerca: ACETATI CARBONATI TARTRATI SOLFITI SOLUZIONE Limpida Incolore RESIDUO Si scarta Ricerca: CLORURI
24. PRECIPITAZIONE Prodotto di solubilità (K s )
 24. PRECIPITAZIONE D. In un racconto di Primo Levi, a proposito di un analisi chimica di campioni di roccia, si incontrano queste parole apparentemente prive di senso: «... giù il ferro con ammoniaca,
24. PRECIPITAZIONE D. In un racconto di Primo Levi, a proposito di un analisi chimica di campioni di roccia, si incontrano queste parole apparentemente prive di senso: «... giù il ferro con ammoniaca,
Integrazione scuola-università una priorità verso il futuro
 Integrazione scuola-università una priorità verso il futuro Progetto Lauree Scientifiche Giulia Simunov Educandato statale della SS. Annunziata Firenze 5 maggio 2015 Progetto Lauree Scientifiche La chimica
Integrazione scuola-università una priorità verso il futuro Progetto Lauree Scientifiche Giulia Simunov Educandato statale della SS. Annunziata Firenze 5 maggio 2015 Progetto Lauree Scientifiche La chimica
SAGGI PER VIA SECCA. Fiamma Ossidante. Fiamma Riducente C C
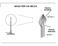 SAGGI PER VIA SECCA Fiamma Ossidante 1350-1500 C Fiamma Riducente 400-500 C Ricerca dei Cationi per Via Secca Gli elementi metallici presenti nei composti organometallici della F.U. sono: Sodio, Potassio,
SAGGI PER VIA SECCA Fiamma Ossidante 1350-1500 C Fiamma Riducente 400-500 C Ricerca dei Cationi per Via Secca Gli elementi metallici presenti nei composti organometallici della F.U. sono: Sodio, Potassio,
Esercitazione 3. Tipi di soluzioni. Cristallizzazione. Ricristallizzazione. Preparazione del nitrato di potassio
 Esercitazione 3 Preparazione del nitrato di potassio Tipi di soluzioni!la sostanza che si scioglie è detta SOLUTO!La sostanza che scioglie è detta SOLVENTE Soluzione non satura: soluzione che contiene
Esercitazione 3 Preparazione del nitrato di potassio Tipi di soluzioni!la sostanza che si scioglie è detta SOLUTO!La sostanza che scioglie è detta SOLVENTE Soluzione non satura: soluzione che contiene
LA TERRA E LA CHIMICA: LA TAVOLA PERIODICA DEGLI ELEMENTI ELEMENTI E COMPOSTI
 I.I.S. A. PACINOTTI IST. TECNICO STATALE INDUSTRIALE Antonio PACINOTTI IST. TECNICO STATALE per GEOMETRI "Giorgio MASSARI" http://www.iispacinottive.it/ Via Caneve, n. 93 30173 - Mestre (VE) tel. 041 5350355
I.I.S. A. PACINOTTI IST. TECNICO STATALE INDUSTRIALE Antonio PACINOTTI IST. TECNICO STATALE per GEOMETRI "Giorgio MASSARI" http://www.iispacinottive.it/ Via Caneve, n. 93 30173 - Mestre (VE) tel. 041 5350355
BaSO. BaSO 4 è una costante quindi: K ps = prodotto di solubilità
 Gli equilibri di solubilità sono equilibri eterogenei in quanto si stabiliscono tra due fasi: un solido e la soluzione satura dei suoi ioni. Sono gli equilibri che coinvolgono le reazioni di dissoluzione
Gli equilibri di solubilità sono equilibri eterogenei in quanto si stabiliscono tra due fasi: un solido e la soluzione satura dei suoi ioni. Sono gli equilibri che coinvolgono le reazioni di dissoluzione
ANALISI CHIMICA QUALITATIVA
 ANALISI CHIMICA QUALITATIVA Analisi per via secca: Saggi alla fiamma Scopo dell esperimento: Riconoscimento della presenza di alcuni elementi per via secca Premessa teorica: I saggi per via secca, così
ANALISI CHIMICA QUALITATIVA Analisi per via secca: Saggi alla fiamma Scopo dell esperimento: Riconoscimento della presenza di alcuni elementi per via secca Premessa teorica: I saggi per via secca, così
Prima esperienza di Laboratorio. Alcune reazioni del rame
 Prima esperienza di Laboratorio Alcune reazioni del rame Prelevare 20 cm 3 di soluzione di solfato di rame pentaidrato (CuSO 4 5H 2 O) e versarli in una provetta Da questa riserva di rame, preleverete
Prima esperienza di Laboratorio Alcune reazioni del rame Prelevare 20 cm 3 di soluzione di solfato di rame pentaidrato (CuSO 4 5H 2 O) e versarli in una provetta Da questa riserva di rame, preleverete
Titolazioni Redox. Analisi volumetrica basata su una reazione di ossido-riduzione. La somma delle due coppie coniugate ossido-riduttive
 Titolazioni Redox Analisi volumetrica basata su una reazione di ossido-riduzione Ossidante (accettore di elettroni si riduce) Riducente (donatore di elettroni si ossida) ox 1 + ne - rid 1 rid 2 ox 2 +
Titolazioni Redox Analisi volumetrica basata su una reazione di ossido-riduzione Ossidante (accettore di elettroni si riduce) Riducente (donatore di elettroni si ossida) ox 1 + ne - rid 1 rid 2 ox 2 +
Tipi di reazioni chimiche
 1 Approfondimento 7.1 Tipi di reazioni chimiche Reazioni di sintesi: A + B AB Nelle reazioni di sintesi da due o più elementi o composti semplici si ottiene un solo composto. Metallo + ossigeno ossido
1 Approfondimento 7.1 Tipi di reazioni chimiche Reazioni di sintesi: A + B AB Nelle reazioni di sintesi da due o più elementi o composti semplici si ottiene un solo composto. Metallo + ossigeno ossido
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Chimica Inorganica Biologica Composti di coordinazione. Simmetria Ottaedrica
 Simmetria Ottaedrica Simmetria Ottaedrica Simmetria Ottaedrica L E media degli orbitali d rimane invariata Δ O = 10 Dq [Ti(H 2 O) 6 ] 3+ Ti 3+ d 1 Simmetria Ottaedrica Δ o Δ ο = hν 20300cm 1 Simmetria
Simmetria Ottaedrica Simmetria Ottaedrica Simmetria Ottaedrica L E media degli orbitali d rimane invariata Δ O = 10 Dq [Ti(H 2 O) 6 ] 3+ Ti 3+ d 1 Simmetria Ottaedrica Δ o Δ ο = hν 20300cm 1 Simmetria
STECHIOMETRIA 1) Nella sintesi del Bianco S.Giovanni (CaCO 3 ) secondo la reazione CaCl 2 + Na 2 CO 3 = 2NaCl + CaCO 3 partendo da 8,3g (0,038 mol)
 STECHIOMETRIA 1) Nella sintesi del Bianco S.Giovanni (CaCO 3 ) secondo la reazione CaCl 2 + Na 2 CO 3 = 2NaCl + CaCO 3 partendo da 8,3g (0,038 mol) di cloruro di Calcio biidrato e 14,3g (0,050 mol) di
STECHIOMETRIA 1) Nella sintesi del Bianco S.Giovanni (CaCO 3 ) secondo la reazione CaCl 2 + Na 2 CO 3 = 2NaCl + CaCO 3 partendo da 8,3g (0,038 mol) di cloruro di Calcio biidrato e 14,3g (0,050 mol) di
Equilibri di Solubilità (in Acqua) K ps = Prodotto di Solubilità = [A + ][B - ] K ps = Prodotto di Solubilità = [A p+ ] m [B q- ] n
![Equilibri di Solubilità (in Acqua) K ps = Prodotto di Solubilità = [A + ][B - ] K ps = Prodotto di Solubilità = [A p+ ] m [B q- ] n Equilibri di Solubilità (in Acqua) K ps = Prodotto di Solubilità = [A + ][B - ] K ps = Prodotto di Solubilità = [A p+ ] m [B q- ] n](/thumbs/42/22904723.jpg) Equilibri di Solubilità (in Acqua) SALI SOLUBILI: dissociano completamente in soluzione acquosa (e.g. fluoruri, acetati, nitriti, nitrati ed i sali dei metalli alcalini) SALI POCO SOLUBILI: non dissociano
Equilibri di Solubilità (in Acqua) SALI SOLUBILI: dissociano completamente in soluzione acquosa (e.g. fluoruri, acetati, nitriti, nitrati ed i sali dei metalli alcalini) SALI POCO SOLUBILI: non dissociano
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2015/2016 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2015/2016 Dott. Giuseppe La Regina Tu,
SESTA ESPERIENZA DI LABORATORIO. Prof. Antonio Lavecchia
 SESTA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Settima Esperienza di Laboratorio Prove di solubilità Riconoscimento degli α-amminoacidi Saggio della ninidrina Riconoscimento dei Sulfamidici Misura
SESTA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Settima Esperienza di Laboratorio Prove di solubilità Riconoscimento degli α-amminoacidi Saggio della ninidrina Riconoscimento dei Sulfamidici Misura
Osservazioni su alcuni ossidanti comuni che agiscono in soluzione acquosa
 Osservazioni su alcuni ossidanti comuni che agiscono in soluzione acquosa Esercizio: scrivere la reazione corrispondente ad ogni asterisco e bilanciare. PERMANGANATO Il permanganato di potassio K è un
Osservazioni su alcuni ossidanti comuni che agiscono in soluzione acquosa Esercizio: scrivere la reazione corrispondente ad ogni asterisco e bilanciare. PERMANGANATO Il permanganato di potassio K è un
La serie elettrochimica
 La serie elettrochimica PREREQUISITI Gli studenti dovrebbero conoscere la struttura dell atomo, la tavola periodica ed avere il concetto di reazione chimica. OBIETTIVI: 1) Acquisizione, da parte degli
La serie elettrochimica PREREQUISITI Gli studenti dovrebbero conoscere la struttura dell atomo, la tavola periodica ed avere il concetto di reazione chimica. OBIETTIVI: 1) Acquisizione, da parte degli
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
Influenza della concentrazione dei reagenti e dei prodotti sull equilibrio chimico. Influenza della temperatura sull equilibrio chimico.
 Esperienza n. 5 Influenza della concentrazione dei reagenti e dei prodotti sull equilibrio chimico. Influenza della temperatura sull equilibrio chimico. una provetta da saggio, porta provette, spruzzetta
Esperienza n. 5 Influenza della concentrazione dei reagenti e dei prodotti sull equilibrio chimico. Influenza della temperatura sull equilibrio chimico. una provetta da saggio, porta provette, spruzzetta
1. Agli estremi di una resistenza di 30 ohm è applicata una tensione di 120 volt. Calcolare la quantità di elettricità passata in 12 ore.
 ESERCIZI pag: 458 1. Agli estremi di una resistenza di 30 ohm è applicata una tensione di 120 volt. Calcolare la quantità di elettricità passata in 12 ore. 2. Una dinamo produce 6 amp a 160 v. Calcolare
ESERCIZI pag: 458 1. Agli estremi di una resistenza di 30 ohm è applicata una tensione di 120 volt. Calcolare la quantità di elettricità passata in 12 ore. 2. Una dinamo produce 6 amp a 160 v. Calcolare
ACIDO ACETILSALICILICO. Fenomeni visibili con FeCl 3 dopo idrolisi
 ACID ACETILSALICILIC Fenomeni visibili con FeCl 3 dopo idrolisi AC. ACETILSALICILIC (PF 141-144 C) C CC 3 Aspirina. Attività antinfiammatoria, analgesica e antipiretica (FANS). Utilizzato a basso dosaggio
ACID ACETILSALICILIC Fenomeni visibili con FeCl 3 dopo idrolisi AC. ACETILSALICILIC (PF 141-144 C) C CC 3 Aspirina. Attività antinfiammatoria, analgesica e antipiretica (FANS). Utilizzato a basso dosaggio
Composti di coordinazione
 Composti di coordinazione Nelle molecole di un COMPOSTO DI COORDINAZIONE l atomo centrale e legato ad un numero di atomi superiore al suo numero di ossidazione. Lo studio dei composti di coordinazione
Composti di coordinazione Nelle molecole di un COMPOSTO DI COORDINAZIONE l atomo centrale e legato ad un numero di atomi superiore al suo numero di ossidazione. Lo studio dei composti di coordinazione
Chimica Generale ed Inorganica
 Chimica Generale ed Inorganica Chimica Generale prof. Dario Duca Cristalli blu di solfato di rame CH 3 COOH composti molecolari coefficienti stechiometrici C 2 H 2 - CH C 2 H 4 - CH 2 C 2 H 6 - CH 3 CH
Chimica Generale ed Inorganica Chimica Generale prof. Dario Duca Cristalli blu di solfato di rame CH 3 COOH composti molecolari coefficienti stechiometrici C 2 H 2 - CH C 2 H 4 - CH 2 C 2 H 6 - CH 3 CH
ACIDO ACETILSALICILICO. Fenomeni visibili con FeCl 3 dopo idrolisi
 ACID ACETILSALICILIC Fenomeni visibili con FeCl 3 dopo idrolisi AC. ACETILSALICILIC (PF 141-144 C) C CC 3 Aspirina. Attività antinfiammatoria, analgesica e antipiretica (FANS). Utilizzato a basso dosaggio
ACID ACETILSALICILIC Fenomeni visibili con FeCl 3 dopo idrolisi AC. ACETILSALICILIC (PF 141-144 C) C CC 3 Aspirina. Attività antinfiammatoria, analgesica e antipiretica (FANS). Utilizzato a basso dosaggio
bario cloruro biidrato (200 mg; PM ) ferro(iii) cloruro esaidrato (200 mg; PM ) rame(ii) acetato monoidrato (200 mg; PM 181.
 Una delle esercitazioni che effettueremo in laboratorio è la separazione di cationi metallici basata sulla loro precipitazione selettiva. In particolare, seguiremo una metodica che ci consentirà di separare
Una delle esercitazioni che effettueremo in laboratorio è la separazione di cationi metallici basata sulla loro precipitazione selettiva. In particolare, seguiremo una metodica che ci consentirà di separare
CAPITOLO 12 EQUILIBRI ACIDO-BASE E SOLUBILITA
 CAPITOLO 12 EQUILIBRI ACIDO-BASE E SOLUBILITA 12.1 (a) ph = 2,57 (b) ph = 4,44 12.3 (a) no. (b) no. (c) sì. (d) sì. (e) no. 12.5 ph = 8,88 12.7 0,024 12.9 0,58 12.11 ph = 9,25; ph = 9,18. 12.13 Na 2 A/NaHA.
CAPITOLO 12 EQUILIBRI ACIDO-BASE E SOLUBILITA 12.1 (a) ph = 2,57 (b) ph = 4,44 12.3 (a) no. (b) no. (c) sì. (d) sì. (e) no. 12.5 ph = 8,88 12.7 0,024 12.9 0,58 12.11 ph = 9,25; ph = 9,18. 12.13 Na 2 A/NaHA.
H N. Mn 2+ +.. Fe 3+ +.. H 2 O
 CHIMICA ANALITICA- PROVA SCRITTA 3 FEBBRAIO 2005-1a. Quanti microlitri di 1-nonene (densità 1-nonene = 0.73 g/ml) bisogna prelevare per preparare 50 ml di soluzione di concentrazione 1000 ppm in metanolo
CHIMICA ANALITICA- PROVA SCRITTA 3 FEBBRAIO 2005-1a. Quanti microlitri di 1-nonene (densità 1-nonene = 0.73 g/ml) bisogna prelevare per preparare 50 ml di soluzione di concentrazione 1000 ppm in metanolo
COMPORTAMENTO DI SALI CONTENENTI PARTICOLARI CATIONI IN SEGUITO A TRATTAMENTO CON COMPLESSANTI, BASI ED ACIDI
 COMPORTAMENTO DI SALI CONTENENTI PARTICOLARI CATIONI IN SEGUITO A TRATTAMENTO CON COMPLESSANTI, BASI ED ACIDI Perché le soluzioni dei cationi metallici di partenza sono acide. Una volta sciolto un sale
COMPORTAMENTO DI SALI CONTENENTI PARTICOLARI CATIONI IN SEGUITO A TRATTAMENTO CON COMPLESSANTI, BASI ED ACIDI Perché le soluzioni dei cationi metallici di partenza sono acide. Una volta sciolto un sale
L ANALISI CHIMICA 2 SOSTANZA INCOGNITA. Analisi degli anioni e dei cationi. Riconoscimento della sostanza
 L ANALISI CHIMICA 1 L Analisi Chimica è un insieme di operazioni che si eseguono per separare, riconoscere (Analisi Chimica Qualitativa) e dosare (Analisi Chimica Quantitativa) una sostanza o una miscela
L ANALISI CHIMICA 1 L Analisi Chimica è un insieme di operazioni che si eseguono per separare, riconoscere (Analisi Chimica Qualitativa) e dosare (Analisi Chimica Quantitativa) una sostanza o una miscela
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Formazione di complessi
 Formazione di complessi Struttura degli ioni complessi Gli ioni complessi sono formati da un catione metallico legato ad anioni come OH -, Cl -, CN -, SCN -, o a molecole neutre come H 2 O, NH 3., detti
Formazione di complessi Struttura degli ioni complessi Gli ioni complessi sono formati da un catione metallico legato ad anioni come OH -, Cl -, CN -, SCN -, o a molecole neutre come H 2 O, NH 3., detti
SOSTANZE INORGANICHE
 SOSTANZE INORGANICHE Na2B4O7 Na2HPO4 H3BO3 La soluzione acquosa, trattata con AgNO3 dà un precipitato solubile in HNO3 conc. Indicazioni Generali La sol. acq. si tratta a freddo con alcune gocce di AgNO3.
SOSTANZE INORGANICHE Na2B4O7 Na2HPO4 H3BO3 La soluzione acquosa, trattata con AgNO3 dà un precipitato solubile in HNO3 conc. Indicazioni Generali La sol. acq. si tratta a freddo con alcune gocce di AgNO3.
SAGGI PER VIA SECCA. Fiamma Ossidante. Fiamma Riducente C C
 SAGGI PER VIA SECCA Fiamma Ossidante 1350-1500 C Fiamma Riducente 400-500 C Ricerca dei Cationi per Via Secca Gli elementi metallici presenti nei composti organometallici della F.U. sono: Sodio, Potassio,
SAGGI PER VIA SECCA Fiamma Ossidante 1350-1500 C Fiamma Riducente 400-500 C Ricerca dei Cationi per Via Secca Gli elementi metallici presenti nei composti organometallici della F.U. sono: Sodio, Potassio,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
TEORIE DEGLI ACIDI E DELLE BASI
 TERIE DEGLI ACIDI E DELLE BASI Teoria di Arrhenius: Un acido è una sostanza che in soluzione acquosa libera ioni H + Es. HCl = H + (aq) + Cl - (aq) H 2 S 4 = 2 H + (aq) + S 4 2- (aq) Una base è una sostanza
TERIE DEGLI ACIDI E DELLE BASI Teoria di Arrhenius: Un acido è una sostanza che in soluzione acquosa libera ioni H + Es. HCl = H + (aq) + Cl - (aq) H 2 S 4 = 2 H + (aq) + S 4 2- (aq) Una base è una sostanza
Relazioni Ponderali. Es. 1 Data la reazione da bilanciare: Al H Es. 2 Data la reazione da bilanciare: C 3 CO 2 + H 2 + O 2
 Relazioni Ponderali Es. 1 Data la reazione da bilanciare: 0 +1-1 0 +3-1 Al + HCl H 2 + AlCl 3 calcolare quanti grammi di H 2 si ottengono da 235g di Al con eccesso di HCl. Al 0 +3 +3 H 0-1 -1 1 3 2Al +
Relazioni Ponderali Es. 1 Data la reazione da bilanciare: 0 +1-1 0 +3-1 Al + HCl H 2 + AlCl 3 calcolare quanti grammi di H 2 si ottengono da 235g di Al con eccesso di HCl. Al 0 +3 +3 H 0-1 -1 1 3 2Al +
Brady Senese Pignocchino Chimica.blu Zanichelli 2014 Soluzione degli esercizi Capitolo 23
 Brady Senese Pignocchino Chimica.blu Zanichelli 2014 Soluzione degli esercizi Capitolo 23 Esercizio PAG 541 ES 1 PAG 541 ES 2 PAG 541 ES 3 PAG 541 ES 4 PAG 541 ES 5 PAG 541 ES 6 PAG 541 ES 7 Al(s) Al 3+
Brady Senese Pignocchino Chimica.blu Zanichelli 2014 Soluzione degli esercizi Capitolo 23 Esercizio PAG 541 ES 1 PAG 541 ES 2 PAG 541 ES 3 PAG 541 ES 4 PAG 541 ES 5 PAG 541 ES 6 PAG 541 ES 7 Al(s) Al 3+
per HCl: H Cl Tipi differenti di composti con differenti Proprietà Chimiche ACIDO Cl - SALI Cs + F - FeCl 3 FeCl δ + δ - 0.
 0.7 4.0 Cs + F - 0.9 4.0 Na + F - 0.9 Na + 3.0 Cl - SALI 1.8 3.0 FeCl 1.8 3.0 FeCl 3 per HCl: H Cl.1 3.0 δ + δ - ACID Tipi differenti di composti con differenti Proprietà Chimiche SSIDI: combinazioni degli
0.7 4.0 Cs + F - 0.9 4.0 Na + F - 0.9 Na + 3.0 Cl - SALI 1.8 3.0 FeCl 1.8 3.0 FeCl 3 per HCl: H Cl.1 3.0 δ + δ - ACID Tipi differenti di composti con differenti Proprietà Chimiche SSIDI: combinazioni degli
Brady Senese Pignocchino Chimica.blu Zanichelli 2014 Soluzione degli esercizi Capitolo 17
 Brady Senese Pignocchino Chimica.blu Zanichelli 2014 Soluzione degli esercizi Capitolo 17 Esercizio Risposta PAG 387 ES 1 In una ossidazione il reagente perde elettroni e aumenta il proprio numero di ossidazione.
Brady Senese Pignocchino Chimica.blu Zanichelli 2014 Soluzione degli esercizi Capitolo 17 Esercizio Risposta PAG 387 ES 1 In una ossidazione il reagente perde elettroni e aumenta il proprio numero di ossidazione.
Esame (0) - solubilità dei composti e reaz - Codice Prova:
 1) Ci si aspetta la formazione di un precipitato quando una soluzione acquosa di ioduro di potassio è aggiunta ad una soluzione acquosa di: A. idrossido di bario B. perclorato di piombo C. cloruro di ferro(ii)
1) Ci si aspetta la formazione di un precipitato quando una soluzione acquosa di ioduro di potassio è aggiunta ad una soluzione acquosa di: A. idrossido di bario B. perclorato di piombo C. cloruro di ferro(ii)
SOLUBILITA EQUILIBRI ETEROGENEI
 SOLUBILITA EQUILIBRI ETEROGENEI Cosa succede quando si scioglie un sale (NaCl) in acqua Cl - LEGAME IONE DIPOLO Se sciogliamo in un solvente polare (tipo H 2 O) una sostanza ionica(tipo NaCl) questa si
SOLUBILITA EQUILIBRI ETEROGENEI Cosa succede quando si scioglie un sale (NaCl) in acqua Cl - LEGAME IONE DIPOLO Se sciogliamo in un solvente polare (tipo H 2 O) una sostanza ionica(tipo NaCl) questa si
PRIMA ESPERIENZA DI LABORATORIO. Prof. Antonio Lavecchia
 PRIMA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Prima Esperienza di Laboratorio Analisi Qualitativa Elementare di Sostanze Inorganiche (Via Umida) Ricerca dei Cationi Calcio, magnesio Ricerca degli
PRIMA ESPERIENZA DI LABORATORIO Prof. Antonio Lavecchia Prima Esperienza di Laboratorio Analisi Qualitativa Elementare di Sostanze Inorganiche (Via Umida) Ricerca dei Cationi Calcio, magnesio Ricerca degli
TUTORAGGIO CHIMICA A.A. 2018/2019 Tutoraggio Chimica (Prof. L. Pilia) Nicola Melis
 TUTORAGGIO CHIMICA 18.12.2018 1 Es. 1: Il fluoruro di calcio si discioglie in piccole quantità in acqua. Calcolare il valore di K ps sapendo che [Ca 2+ ] = 2,3*10-4 CaF 2 (s) Ca 2+ (aq) + 2 F - (aq) Es.
TUTORAGGIO CHIMICA 18.12.2018 1 Es. 1: Il fluoruro di calcio si discioglie in piccole quantità in acqua. Calcolare il valore di K ps sapendo che [Ca 2+ ] = 2,3*10-4 CaF 2 (s) Ca 2+ (aq) + 2 F - (aq) Es.
2.1 Iodimetria-iodometria
 .1 Iodimetria-iodometria Sono metodi analitici basati su reazioni di ossidoriduzione in cui una delle due coppie redox è I / I - Equazione della semireazione di riduzione dello iodio I + e - I - E = 0,535
.1 Iodimetria-iodometria Sono metodi analitici basati su reazioni di ossidoriduzione in cui una delle due coppie redox è I / I - Equazione della semireazione di riduzione dello iodio I + e - I - E = 0,535
REAZIONI ACIDO-BASE OSSERVARE, DESCRIVERE E DARE UNA SPIEGAZIONE DEI FENOMENI CHIMICI AVVENUTI
 ESPERIENZA 2 REAZIONI ACIDO-BASE OBIETTIVO. L'esperienza serve a completare la presa di contatto con le attrezzature di laboratorio e i reagenti chimici più comuni, verificando le conoscenze acquisite
ESPERIENZA 2 REAZIONI ACIDO-BASE OBIETTIVO. L'esperienza serve a completare la presa di contatto con le attrezzature di laboratorio e i reagenti chimici più comuni, verificando le conoscenze acquisite
Elettrochimica unità 2 e 3, modulo G del libro
 Elettrochimica unità 2 e 3, modulo G del libro Data una reazione chimica in cui si verifica uno scambio di elettroni, ci sarà una specie che si ossida, e cioè cede elettroni, ed una specie che si riduce
Elettrochimica unità 2 e 3, modulo G del libro Data una reazione chimica in cui si verifica uno scambio di elettroni, ci sarà una specie che si ossida, e cioè cede elettroni, ed una specie che si riduce
Sommario della lezione 7. Misure di concentrazione. Nomenclatura
 Sommario della lezione 7 Misure di concentrazione Nomenclatura Concentrazioni e Omeopatia Diluizione centesimale Uno dei rimedi omeopatici per l asma è il Natrium muriaticum
Sommario della lezione 7 Misure di concentrazione Nomenclatura Concentrazioni e Omeopatia Diluizione centesimale Uno dei rimedi omeopatici per l asma è il Natrium muriaticum
ESERCIZI I PARTE. 1 Bilanciamento
 ESERCIZI I PARTE 1 1 Bilanciamento 1. H 3 PO 3 + CuO Cu 3 (PO 3 ) 2 +3H 2 O ) 2. Cs 2 O + H 2 O CsOH 3. P 2 O 5 + H 2 O HPO 3 4. NaCl + H 2 SO 4 Na 2 SO 4 + HCl 5. NaF + Mg(OH) 2 MgF 2 + NaOH 6. Al(OH)
ESERCIZI I PARTE 1 1 Bilanciamento 1. H 3 PO 3 + CuO Cu 3 (PO 3 ) 2 +3H 2 O ) 2. Cs 2 O + H 2 O CsOH 3. P 2 O 5 + H 2 O HPO 3 4. NaCl + H 2 SO 4 Na 2 SO 4 + HCl 5. NaF + Mg(OH) 2 MgF 2 + NaOH 6. Al(OH)
Esperienza n 1 PREPARAZIONE DI SOLUZIONI A VARIA CONCENTRAZIONE PER PESATA E PER DILUIZIONE ESPERIENZE DI ANALISI QUALITATIVA DI VARIE SPECIE CHIMICHE
 Esperienza n 1 PREPARAZIONE DI SOLUZIONI A VARIA CONCENTRAZIONE PER PESATA E PER DILUIZIONE ESPERIENZE DI ANALISI QUALITATIVA DI VARIE SPECIE CHIMICHE PRIMA PARTE: preparazione di soluzioni a varia concentrazione
Esperienza n 1 PREPARAZIONE DI SOLUZIONI A VARIA CONCENTRAZIONE PER PESATA E PER DILUIZIONE ESPERIENZE DI ANALISI QUALITATIVA DI VARIE SPECIE CHIMICHE PRIMA PARTE: preparazione di soluzioni a varia concentrazione
Metatesi e Equilibri Eterogenei
 Corso di Chimica Generale CCS Ingegneria CHI-MAT (I Semestre) LABORATORIO 4 Metatesi e Equilibri Eterogenei Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio/it/education/chimica-generale-lab/
Corso di Chimica Generale CCS Ingegneria CHI-MAT (I Semestre) LABORATORIO 4 Metatesi e Equilibri Eterogenei Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio/it/education/chimica-generale-lab/
EQUILIBRI DI SOLUBILITÀ DI COMPOSTI IONICI POCO SOLUBILI
 EQUILIBRI DI SOLUBILITÀ DI COMPOSTI IONICI POCO SOLUBILI Quando abbiamo a che fare con dei composti ionici molto solubili, per raggiungere la saturazione 1 della soluzione è necessario aggiungere all'acqua
EQUILIBRI DI SOLUBILITÀ DI COMPOSTI IONICI POCO SOLUBILI Quando abbiamo a che fare con dei composti ionici molto solubili, per raggiungere la saturazione 1 della soluzione è necessario aggiungere all'acqua
1)Calcolare il ph di una soluzione che contenga al9%(w/w)naoh ed abbia una densità pari a 1.098g/ml.
 Compito di Analisi dei farmaci I Bari,3 febbraio 1999 1)Calcolare il ph di una soluzione che contenga al9%(w/w)naoh ed abbia una densità pari a 1.098g/ml. 1)Quale deve essere la sensibilità della bilancia
Compito di Analisi dei farmaci I Bari,3 febbraio 1999 1)Calcolare il ph di una soluzione che contenga al9%(w/w)naoh ed abbia una densità pari a 1.098g/ml. 1)Quale deve essere la sensibilità della bilancia
LABORATORIO DI CHIMICA GENERALE INORGANICA. Esperienze 2015/16
 LABORATORIO DI CHIMICA GENERALE ED INORGANICA Esperienze 2015/16 1 1 ESPERIENZA DETERMINAZIONE DEL REAGENTE LIMITANTE 3.1 PRIMA PARTE: REAGENTE LIMITANTE E DETERMINAZIONE DI NaHCO 3 NELLE COMPRESSE DI
LABORATORIO DI CHIMICA GENERALE ED INORGANICA Esperienze 2015/16 1 1 ESPERIENZA DETERMINAZIONE DEL REAGENTE LIMITANTE 3.1 PRIMA PARTE: REAGENTE LIMITANTE E DETERMINAZIONE DI NaHCO 3 NELLE COMPRESSE DI
SOLUZIONI COMPITO A DI CHIMICA DEL
 SOLUZIONI COMPITO A DI CHIMICA DEL 18-07-12 1A) 1.3 kg di un campione solido contenente il 40% di permanganato di potassio, il 50% di dicromato di potassio e il 10% di impurezze vengono sciolti in una
SOLUZIONI COMPITO A DI CHIMICA DEL 18-07-12 1A) 1.3 kg di un campione solido contenente il 40% di permanganato di potassio, il 50% di dicromato di potassio e il 10% di impurezze vengono sciolti in una
V gruppo (15) H He Li Be B C N O F Ne Na Mg Al Si P S Cl Ar K Ca Ga Ge As Se Br Kr Rb Sr In Sn Sb Te I Xe Cs Ba Tl Pb Bi Po At Rn
 V gruppo (15) H He Li Be B C N F Ne Na Mg Al Si P S Cl Ar K Ca Ga Ge As Se Br Kr Rb Sr In Sn Sb Te I Xe Cs Ba Tl Pb Bi Po At Rn Configurazione elettronica: ns 2 np 3 V gruppo N, P e As sono non-metalli;
V gruppo (15) H He Li Be B C N F Ne Na Mg Al Si P S Cl Ar K Ca Ga Ge As Se Br Kr Rb Sr In Sn Sb Te I Xe Cs Ba Tl Pb Bi Po At Rn Configurazione elettronica: ns 2 np 3 V gruppo N, P e As sono non-metalli;
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2014/2015 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
XANTINE R R 1 R 2. Xantina H H H. Caffeina (3,7-diidro-1,3,7- trimetil-1h-purina-2,6-dione) CH 3 CH 3 CH 3
 XATIE 1 2 Xantina Caffeina (3,7-diidro-1,3,7- trimetil-1-purina-2,6-dione) Teofillina (3,7-diidro-1,3-diimetil-1purina-2,6-dione) Teobromina (3,7-diidro-3,7-diimetil-1purina-2,6-dione) C 3 C 3 C 3 C 3
XATIE 1 2 Xantina Caffeina (3,7-diidro-1,3,7- trimetil-1-purina-2,6-dione) Teofillina (3,7-diidro-1,3-diimetil-1purina-2,6-dione) Teobromina (3,7-diidro-3,7-diimetil-1purina-2,6-dione) C 3 C 3 C 3 C 3
SULFAMMIDICI SOSTANZE ORGANICHE AZOTATE, INSOLUBILI IN ACQUA
 ULFAMMIDICI OTAZE ORGAICHE AZOTATE, IOLUBILI I ACQUA ono sostanze azotate e solforate (Lassaigne), poco solubili o insolubili in acqua, dotate di carattere basico e in molti casi anche di carattere acido.
ULFAMMIDICI OTAZE ORGAICHE AZOTATE, IOLUBILI I ACQUA ono sostanze azotate e solforate (Lassaigne), poco solubili o insolubili in acqua, dotate di carattere basico e in molti casi anche di carattere acido.
+ NO 2 + 3H 2 O = Ce +3 + NO 3 + 2H 3 O +, b) 0.478 g
 1) Una soluzione di Na 3 PO 4 (PM = 163.94) viene titolata con una soluzione di AgNO 3 (PM = 169.87) a) Scrivere l equazione chimica del processo di titolazione e specificare di quale tecnica si tratta
1) Una soluzione di Na 3 PO 4 (PM = 163.94) viene titolata con una soluzione di AgNO 3 (PM = 169.87) a) Scrivere l equazione chimica del processo di titolazione e specificare di quale tecnica si tratta
Total P Total S Ammonio NH 4
 2- - - LIMS Code Conductivity Calcio Magnesio Mg Sodio Na Potassio K Ione cloruro Cl- Solfati SO 4 Nitrati NO 3 Cation Total Anion Total Bromo Br Nitriti NO 2 µs cm -1 mg l -1 mg l -1 mg l -1 mg l -1 mg
2- - - LIMS Code Conductivity Calcio Magnesio Mg Sodio Na Potassio K Ione cloruro Cl- Solfati SO 4 Nitrati NO 3 Cation Total Anion Total Bromo Br Nitriti NO 2 µs cm -1 mg l -1 mg l -1 mg l -1 mg l -1 mg
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z)
 Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
Corso di Analisi Chimico-Farmaceutica e Tossicologica I (M-Z) Corso di Laurea in Chimica e Tecnologia Farmaceutiche Facoltà di Farmacia e Medicina Anno Accademico 2013/2014 Dott. Giuseppe La Regina Tu,
Capitolo 22 L elettrochimica
 Capitolo 22 L elettrochimica Hai capito? pag. 572 Le osservazioni sarebbero le stesse. 2 + Cu 2 Cu 2+ ; la soluzione assume un colore azzurro per la presenza di ioni Cu 2+ e si forma un deposito grigio
Capitolo 22 L elettrochimica Hai capito? pag. 572 Le osservazioni sarebbero le stesse. 2 + Cu 2 Cu 2+ ; la soluzione assume un colore azzurro per la presenza di ioni Cu 2+ e si forma un deposito grigio
Catodo ( ) 2H 3 O + + 2e - 2H 2 O + H 2 Anodo (+) 2Cl - 2e - + Cl 2
 Elettrolisi Con il termine elettrolisi si indica il complesso di fenomeni che avvengono in una soluzione elettrolitica o in un elettrolita fuso al passaggio della corrente elettrica, di norma continua,
Elettrolisi Con il termine elettrolisi si indica il complesso di fenomeni che avvengono in una soluzione elettrolitica o in un elettrolita fuso al passaggio della corrente elettrica, di norma continua,
