Dott.ssa Secondino Loredana
|
|
|
- Iolanda Costantini
- 7 anni fa
- Visualizzazioni
Transcript
1 Dott.ssa Secondino Loredana
2 ACCESSO VENOSO PERIFERICO ACCESSO VENOSO CENTRALE AGO CANNULA CANNULA PERIFERICA LUNGA CATETERE MIDLINE CATETERE AD INSERZIONE CENTRALE CICC CATETERE AD INSERZIONE PERIFERICA PICC CATETERE AD INSERZIONE FEMORALE
3 POLI-CHEMIOTERAPIE (che richiedono prelievi ematici multipli) Condizioni cliniche del paziente TRASFUSIONE di sangue ed emocomponenti Durata presunta della terapia TERAPIA ANTALGICA E PALLIATIVA Caratteristiche Chimico-fisiche della soluzione infusionale INFUSIONE di liquidi con elettroliti ph soluzione da infondere NUTRIZIONE ARTIFICIALE PARENTERALE
4 Per infusione è possibile somministrare numerose sostanze compresi liquidi, elettroliti, nutrienti, prodotti del sangue e farmaci. Le proprietà colligative delle soluzioni dipendono dalla concentrazione effettiva delle particelle presenti in soluzione, indipendentemente dalla loro natura. L osmolarità : Esprime la concentrazione di una soluzione, sottolineando il numero di particelle in essa disciolte indipendentemente dalla carica elettrica e dalle dimensioni. L osmolarità è espressa in osmoli per litro (osmol/l o OsM) oppure, quando la soluzione è particolarmente diluita, in milliosmoli per litro (mosm/l). Il suo valore esprime la concentrazione della soluzione, ma non dice nulla sulla natura delle particelle in essa contenute. Di riflesso, due soluzioni con uguale osmolarità avranno lo stesso contenuto numerico di particelle e le medesime proprietà colligative (stessa tensione di vapore, stessa pressione osmotica e stessa temperatura di congelamento ed ebollizione).
5 Se due soluzioni aventi diversa pressione osmotica sono separate da una membrana semipermeabile, si ha passaggio netto di solvente dalla soluzione ipotonica a quella ipertonica fino al raggiungimento di una condizione di equilibrio. Le soluzioni isotoniche, come la soluzione fisiologica (NaCl allo 0,9%) o il destrosio al 5%, hanno un osmolarità vicina a quella plasmatica (tra 240 e 340 mosm/l). Tali soluzioni sono in equilibrio con il flusso sanguigno e non incidono sul movimento dei liquidi verso e dalle cellule endoteliali delle vene. Per tale ragione essi sono i diluenti più comuni per numerosi farmaci somministrati per via endovenosa (per esempio la vancomicina).
6 Le soluzioni ipotoniche, come per esempio l acqua sterile, hanno un osmolarità inferiore a mosm/l. Tali soluzioni, quando entrano nel flusso sanguigno, causano il movimento dell acqua nelle cellule endoteliali della vena (emolisi),il risultato può essere un irritazione della vena o una flebite, se le cellule attirano troppa acqua fino a scoppiare. Per questa ragione, l acqua sterile e le altre soluzioni ipotoniche non sono generalmente infusioni adatte di per sé, ma possono essere utilizzate per diluire i farmaci ipertonici, specialmente nelle persone che hanno una quantità di liquidi in circolo limitata, come i bambini e i neonati. Ad es. i globuli rossi vengono conservati in soluzione fisiologica; se vengono immersi in una soluzione più diluita di quella fisiologica (ipotonica rispetto al contenuto cellulare), l acqua entra nella cellula e ne provoca il rigonfiamento fino a farla eventualmente scoppiare.
7 Le soluzioni ipertoniche hanno invece un osmolarità superiore a mosm/l con valori che raggiungono anche mosm/l e richiamano acqua dalle cellule dei vasi endoteliali nel lume vascolare (plasmolisi),causando il loro restringimento e l esposizione della membrana a ulteriori danni (flebiti chimiche, irritazioni, trombosi). Tra le soluzioni fortemente ipertoniche ci sono per esempio la soluzione glucosata al 20% (1.112 mosm/l) e il bicarbonato all 8,4% (2.000 mosm/l). L osmolarità delle soluzioni ipertoniche può provocare danni all endotelio della vena, innescando un processo infiammatorio e lo sviluppo di flebite. Solitamente queste soluzioni non sono diluenti adatti. In letteratura è dimostrato che le soluzioni ipertoniche che superano i 600 mosm/l possono indurre una flebite chimica in una vena periferica entro 24 ore.
8 ph : logaritmo della concentrazione negativa di ioni H₃O+ La scala del ph è compresa da 0 a 14 A ogni piccolo cambiamento di ph corrisponde una grande variazione della concentrazione degli ioni idrogeno. Per ridurre i rischi bisogna somministrare soluzioni per via periferica che abbiano un ph >5 e <9 perché i farmaci o le soluzioni molto acide o molto basiche possono danneggiare la tunica intima causando una flebite, con aumento di conseguenza del rischio di sclerosi della vena, di infiltrazione e di trombosi venosa.
9 Viene definito vescicante e necrotizzante un farmaco in grado di formare o ulcerazione in seguito a contatto diretto con il tessuto pervaso. NECROTIZZANTE DAUNOMICINA DOXORUBICINA EPIRUBICINA IDARUBICINA MITOMICINA VINCRISTINA VINDESINA VINBLASTINA VINORELBINA ACTINOMICINA D MECLORETAMINA VESCICANTE DOCETAXEL DACARBAZINA CISPLATINO ETOPOSIDE MITOXANTRONE OXALIPLATINO PACLITAXEL TENIPOSIDE
10 Non si possono infondere tramite tale via soluzioni con ph <5 o >9 e con un osmolarità che supera i 600 mosm/litro, né farmaci vescicanti. Il volume di sangue non è adeguato per garantire un emodiluizione significativa; di conseguenza la soluzione ipertonica attira l acqua dalle cellule endoteliali della vena, provocando una contrazione e lasciando la vena vulnerabile a flebiti, infiltrazioni e trombosi. Attraverso questa via è possibile infondere soluzioni di qualunque ph e osmolarità, anche farmaci vescicanti ed istolesivi, poiché l elevato flusso ematico 2litri/ minuto,diluendo la soluzione, abbassa la sua osmolarità.
11 Miscela ALL IN ONE Proteine Glucidi Lipidi SACCA Elettroliti Oligoelementi Vitamine
12 Soluzioni di Glucosio Concentrazione 5% 10% 20% 33% 50% 70% Kcal/litro mosm/litro In un allestimento personalizzato di miscela nutrizionale, devono essere conosciute le caratteristiche dei singoli componenti. L informazione più importante che caratterizza il glucosio è il valore della osmolarità. Quest ultimo condiziona la scelta della via di somministrazione.
13 Emulsioni lipidiche Kcal/litro mosm/litro Glicerolo (g) Emulsioni 10% Emulsioni 20% Emulsioni 30% ,7 A differenza del glucosio, ad un elevato apporto calorico non corrisponde un elavata osmolarità.
14 ERRORI DI MISCELAZIONE Deplezione di uno o più componenti presenti nella miscela Intorbidimento della soluzione Precipitazione Rottura dell emulsione lipidica Interazione Chimica La miscela complesso multivitaminico in elettrolitica è un esempio di deplezione per fotolisi La miscela ceftriaxone in elettrolitica La miscela cloruro di calcio e magnesio solfato in fisiologica Aggiunta ad una sacca tricompartimentale di magnesio solfato e/o calcio gluconato Miscela piperacillina/ tazobactam in sodio bicarbonato al 5% Le vitamine fotosensibili subiscono una degradazione quasi totale, soprattutto tiamina, retinolo e riboflavina. La presenza di ioni calcio presenti nel diluente, fa si che si formi ceftriaxone sale di calcio, insolubile Precipitato bianco insolubile Solfato di Calcio RCP dell oliclinomel riporta il rischio di flocculazione ed aggregazione particellare in presenza di ioni magnesio e calcio. Il ph basico determina l apertura dell anello beta lattamico per idrolisi;
15 Do not use, incompa.ble at usual concentra.ons Use with cau.on, compa.bility may depend on order of mixing or drug concentra.ons Reported compa.ble (data may be observa.onal, physical or chemical)? No data Not applicable or not generally recommended
16 A livello pratico le miscele, che hanno come denominatore comune quasi sempre la presenza di morfina, presentano dei problemi derivanti dai valori diversi del ph delle soluzioni di partenza. Ad esempio, in soluzioni concentrate la morfina, a causa di un abbassamento di ph, provoca la precipitazione del ketorolac. Il rischio di formazione di precipitati è minore se si aggiunge gradualmente la morfina ad una soluzione di ketorolac piuttosto che viceversa.
17 Lo studio di Vermeire and Remon (1998) sulla compa.bilità di due formulazioni di desametasone e di morfina cloridrato, che differenziavano solo per la concetrazione degli eccipien., ha dimostrato che gli eccipien1 giocano un ruolo importante nella stabilità e compa1bilità della miscela. POSSIAMO RITENERE CHE FARMACI EQUIVALENTI SI COMPORTINO ALLO STESSO MODO???
18 DIFFERENZE OSMOLARITA FARMACO A FARMACO B LISTA ECCIPIENTI Soluzione albumina umana(contenente sodio,caprilato di sodio e N-acetil DL Triptofanato) LISTA ECCIPIENTI Acido citrico,anidro. Macrogol glicerolo ricinoleato. Etanolo,anidro
19 RCP A CONFRONTO OSMOLARITA e ph ph NO Osmolarità NO ph
20 Verifica l appropriatezza terapeutica delle prescrizioni in termini di sicurezza, dosaggio, tossicita al fine di garantire un servizio assistenziale di alta qualita. Garantisce la stabilità chimico-fisica delle soluzioni da infondere, e la stabilità microbiologica così come riportato nelle NBP della F.U. XII ed Evita errori di miscelazione considerando volume di diluizione, concentrazione dei medicinali presenti nella miscela, velocità di infusione, tempo di infusione. Stabilisce la data limite di utilizzazione, valutando la natura delle sostanze, i processi di degradazione, le interazioni con il contenitore e i solventi, le condizioni di conservazione,e garantisce che i metodi di preparazione assicurino la sterilità
21 Dott.ssa Secondino Loredana
22 Linee Guida SIFO Linee Guida AIOM Handbook on Injectable Drugs (Trissel) Linee Guida SINPE Banca Dati AIFA Linee Guida aziendali per la prevenzione delle complicanze legate agli accessi venosi Ministero della Salute
27 Gennaio 2017 Dr.ssa Chiara Sturaro XVIII CONGRESSO REGIONALE FADOI EMILIA ROMAGNA
 27 Gennaio 2017 Dr.ssa Chiara Sturaro XVIII CONGRESSO REGIONALE FADOI EMILIA ROMAGNA L infusione endovenosa è l immissione diretta di liquidi, farmaci, nutrienti, sangue o emoderivati nel torrente ematico
27 Gennaio 2017 Dr.ssa Chiara Sturaro XVIII CONGRESSO REGIONALE FADOI EMILIA ROMAGNA L infusione endovenosa è l immissione diretta di liquidi, farmaci, nutrienti, sangue o emoderivati nel torrente ematico
dichiara X che negli ultimi due anni NON ha avuto rapporti diretti di finanziamento con
 Il sottoscritto Gabriella Busca ai sensi dell art. 3.3 sul Conflitto di Interessi, pag. 17 del Reg. Applicativo dell Accordo Stato Regione del 5 novembre 2009, dichiara X che negli ultimi due anni NON
Il sottoscritto Gabriella Busca ai sensi dell art. 3.3 sul Conflitto di Interessi, pag. 17 del Reg. Applicativo dell Accordo Stato Regione del 5 novembre 2009, dichiara X che negli ultimi due anni NON
Proprietà delle Soluzioni
 Proprietà delle Soluzioni Dissociazione Elettrolitica 2 In soluzione acquosa i composti ionici (sali, idrossidi) ed alcune sostanze polari (acidi) si dissociano in ioni Esempi: NaCl Na + + Cl HNO 3 H +
Proprietà delle Soluzioni Dissociazione Elettrolitica 2 In soluzione acquosa i composti ionici (sali, idrossidi) ed alcune sostanze polari (acidi) si dissociano in ioni Esempi: NaCl Na + + Cl HNO 3 H +
Scaricato da
 -Equilibrio diffusivo (chimico): in seguito alla diffusione la concentrazione delle molecole è uguale in tutte le parti del sistema C 1 Equilibrio diffusivo Le membrane cellulari sono selettivamente permeabili,
-Equilibrio diffusivo (chimico): in seguito alla diffusione la concentrazione delle molecole è uguale in tutte le parti del sistema C 1 Equilibrio diffusivo Le membrane cellulari sono selettivamente permeabili,
U.O. FARMACIA. SCHEDE INFORMATIVE SULL IMPIEGO DI SACCHE PER NUTRIZIONE PARENTERALE Linee Guida
 U.O. FARMACIA SCHEDE INFORMATIVE SULL IMPIEGO DI SACCHE PER NUTRIZIONE PARENTERALE Linee Guida LFA.P27 Rev.2 del 14.05.2015 La nutrizione parenterale (NP) consiste nell introduzione direttamente nel torrente
U.O. FARMACIA SCHEDE INFORMATIVE SULL IMPIEGO DI SACCHE PER NUTRIZIONE PARENTERALE Linee Guida LFA.P27 Rev.2 del 14.05.2015 La nutrizione parenterale (NP) consiste nell introduzione direttamente nel torrente
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 13 Le proprietà delle soluzioni 1. Perchè le sostanze si sciolgono? 2. La solubilità 3. La concentrazione
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 13 Le proprietà delle soluzioni 1. Perchè le sostanze si sciolgono? 2. La solubilità 3. La concentrazione
Si definisce soluzione un sistema omogeneo (costituito da una sola fase) con più di un componente
 Lezione 14 1.Soluzioni 2.Concentrazione 3.Proprietà colligative 1.Legge di Raoult 2.Abbassamento crioscopico 3.Innalzamento ebullioscopico 4.Pressione osmotica Le Soluzioni Si definisce soluzione un sistema
Lezione 14 1.Soluzioni 2.Concentrazione 3.Proprietà colligative 1.Legge di Raoult 2.Abbassamento crioscopico 3.Innalzamento ebullioscopico 4.Pressione osmotica Le Soluzioni Si definisce soluzione un sistema
25 Maggio Davide Giustivi Gian A. Cibinel
 25 Maggio 2018 Davide Giustivi Gian A. Cibinel IL PROBLEMA Il 90% dei pazienti ospedalizzati è portatore di un dispositivo di accesso vascolare perferico In Italia si utilizzano 32.8 Milioni di ago-cannula/
25 Maggio 2018 Davide Giustivi Gian A. Cibinel IL PROBLEMA Il 90% dei pazienti ospedalizzati è portatore di un dispositivo di accesso vascolare perferico In Italia si utilizzano 32.8 Milioni di ago-cannula/
Le proprietà colligative delle soluzioni Sappiamo dall esperienza quotidiana che una soluzione ha caratteristiche diverse dal solvente puro.
 Le proprietà colligative delle soluzioni Sappiamo dall esperienza quotidiana che una soluzione ha caratteristiche diverse dal solvente puro. Molte delle sue proprietà, come il sapore, il colore, l odore,
Le proprietà colligative delle soluzioni Sappiamo dall esperienza quotidiana che una soluzione ha caratteristiche diverse dal solvente puro. Molte delle sue proprietà, come il sapore, il colore, l odore,
Le proprietà colligative delle soluzioni
 1 Approfondimento 1.3 Le proprietà colligative delle soluzioni In un solvente puro, cioè senza soluti disciolti in esso, le molecole sono libere di interagire tra loro, attraendosi. L aggiunta di un soluto
1 Approfondimento 1.3 Le proprietà colligative delle soluzioni In un solvente puro, cioè senza soluti disciolti in esso, le molecole sono libere di interagire tra loro, attraendosi. L aggiunta di un soluto
Il binomio di van t Hoff Le proprietà colligative dipendono dal numero di particelle effettivamente presenti nella soluzione. Nel caso in cui il solut
 Proprietà colligative di soluzioni ideali Si definiscono proprietà colligative alcune proprietà delle soluzioni indipendenti dalla natura del soluto ma che dipendono soltanto dal numero delle particelle
Proprietà colligative di soluzioni ideali Si definiscono proprietà colligative alcune proprietà delle soluzioni indipendenti dalla natura del soluto ma che dipendono soltanto dal numero delle particelle
SOLUZIONI. Soluzione diluita: è costituita da un liquido (solvente) in cui è disciolta una piccola quantità di un altra sostanza (soluto).
 SOLUZIONI Soluzione diluita: è costituita da un liquido (solvente) in cui è disciolta una piccola quantità di un altra sostanza (soluto). Concentrazione di una soluzione: Molarità: Frazione molare: 1 SOLUZIONI
SOLUZIONI Soluzione diluita: è costituita da un liquido (solvente) in cui è disciolta una piccola quantità di un altra sostanza (soluto). Concentrazione di una soluzione: Molarità: Frazione molare: 1 SOLUZIONI
Una miscela ha composizione variabile. Se le proprietà di una miscela nonsono uniformi (fasi diverse), la miscela è eterogenea.
 Le Miscele Una miscela ha composizione variabile. Se le proprietà di una miscela nonsono uniformi (fasi diverse), la miscela è eterogenea. Se le proprietà sono uniformi, la miscela è una miscela omogenea
Le Miscele Una miscela ha composizione variabile. Se le proprietà di una miscela nonsono uniformi (fasi diverse), la miscela è eterogenea. Se le proprietà sono uniformi, la miscela è una miscela omogenea
Esercizi Concentrazioni e diluizioni
 Esercizi Concentrazioni e diluizioni Una soluzione 0.300 m di acido fosforico ha densità 1.010 g/ml. Calcolare la frazione molare, la percentuale in peso, la molarità. Molalità 0.300 m 0.300 moli di acido
Esercizi Concentrazioni e diluizioni Una soluzione 0.300 m di acido fosforico ha densità 1.010 g/ml. Calcolare la frazione molare, la percentuale in peso, la molarità. Molalità 0.300 m 0.300 moli di acido
Protocollo terapia infusionale SC e EV PA.GRC.1.16.F7. PROCEDURA AZIENDALE PER LA TERAPIA INFUSIONALE SC e EV
 1 di 14 PROCEDURA AZIENDALE PER LA TERAPIA INFUSIONALE SC e EV Indice delle revisioni Codice Documento Revisione Data emissione 0 01.08.2017 Firme Redatto Verificato Approvato U.O. Assicurazione Qualità
1 di 14 PROCEDURA AZIENDALE PER LA TERAPIA INFUSIONALE SC e EV Indice delle revisioni Codice Documento Revisione Data emissione 0 01.08.2017 Firme Redatto Verificato Approvato U.O. Assicurazione Qualità
COMPARTIMENTI IDRICI AMBIENTE ESTERNO AMBIENTE INTERNO
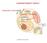 COMPARTIMENTI IDRICI AMBIENTE ESTERNO AMBIENTE INTERNO OMEOSTASI Stato di stabilità locale che tende a mantenersi lontano dallo stato di equilibrio EQUILIBRIO Stato di stabilità energetica, massima entropia
COMPARTIMENTI IDRICI AMBIENTE ESTERNO AMBIENTE INTERNO OMEOSTASI Stato di stabilità locale che tende a mantenersi lontano dallo stato di equilibrio EQUILIBRIO Stato di stabilità energetica, massima entropia
STATO LIQUIDO. Volume proprio Forma non definita Particelle moderatamente ordinate Energia cinetica delle particelle è dello stesso
 STATO LIQUIDO Caratteristiche: Volume proprio Forma non definita Particelle moderatamente ordinate Energia cinetica delle particelle è dello stesso intermolecolare I legami intermolecolari sono responsabili
STATO LIQUIDO Caratteristiche: Volume proprio Forma non definita Particelle moderatamente ordinate Energia cinetica delle particelle è dello stesso intermolecolare I legami intermolecolari sono responsabili
1. Perché le sostanze si sciolgono?
 1. Perché le sostanze si sciolgono? Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore quantità. Il soluto è il
1. Perché le sostanze si sciolgono? Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore quantità. Il soluto è il
Miscela omogenea monofasica i cui costituenti non è possibile separare meccanicamente
 Miscela omogenea monofasica i cui costituenti non è possibile separare meccanicamente Soluzioni Sistema Omogeneo (presenta le stesse proprietà in qualsiasi sua porzione) Monofasico Nella fase omogenea
Miscela omogenea monofasica i cui costituenti non è possibile separare meccanicamente Soluzioni Sistema Omogeneo (presenta le stesse proprietà in qualsiasi sua porzione) Monofasico Nella fase omogenea
Capitolo 14 Le proprietà delle soluzioni
 Capitolo 14 Le proprietà delle soluzioni 1. Perché le sostanze si sciolgono 2. Soluzioni acquose ed elettroliti 3. La concentrazione delle soluzioni 4. L effetto del soluto sul solvente: le proprietà colligative
Capitolo 14 Le proprietà delle soluzioni 1. Perché le sostanze si sciolgono 2. Soluzioni acquose ed elettroliti 3. La concentrazione delle soluzioni 4. L effetto del soluto sul solvente: le proprietà colligative
Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I
 Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I Osmosi Scaricaricato da www.sunhope.it A B 30 mm 5 mm [Soluto] A [Soluto] B [H 2 O] A < [H 2 O] B Scaricaricato da www.sunhope.it
Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I Osmosi Scaricaricato da www.sunhope.it A B 30 mm 5 mm [Soluto] A [Soluto] B [H 2 O] A < [H 2 O] B Scaricaricato da www.sunhope.it
Le soluzioni e il loro comportamento
 2017 Le soluzioni e il loro comportamento PERCENTUALE IN peso (% p/p) PERCENTUALE IN volume (% v/v) PERCENTUALE IN peso/volume (% p/v) MOLARITA (M) moli soluto / volume soluzione MOLALITA (m) moli soluto
2017 Le soluzioni e il loro comportamento PERCENTUALE IN peso (% p/p) PERCENTUALE IN volume (% v/v) PERCENTUALE IN peso/volume (% p/v) MOLARITA (M) moli soluto / volume soluzione MOLALITA (m) moli soluto
PROPRIETA DELLE SOLUZIONI ACQUOSE. Prof.ssa Patrizia Gallucci
 PROPRIETA DELLE SOLUZIONI ACQUOSE Prof.ssa Patrizia Gallucci L'acqua è un composto chimicamente semplice, formato da due atomi di idrogeno e uno di ossigeno (H2O), che riveste fondamentale importanza in
PROPRIETA DELLE SOLUZIONI ACQUOSE Prof.ssa Patrizia Gallucci L'acqua è un composto chimicamente semplice, formato da due atomi di idrogeno e uno di ossigeno (H2O), che riveste fondamentale importanza in
Le soluzioni. possono essere. solide (leghe) liquide aeriformi
 Le soluzioni Sono miscele omogenee di due o più sostanze (in forma di molecole, atomi, ioni) di cui quella presente in quantità maggiore è definita solvente, le altre soluti. possono essere solide (leghe)
Le soluzioni Sono miscele omogenee di due o più sostanze (in forma di molecole, atomi, ioni) di cui quella presente in quantità maggiore è definita solvente, le altre soluti. possono essere solide (leghe)
Il Paziente in nutrizione parenterale. CPSI Andrea Casal ASL Roma 2 Degenza Medica - Ospedale S. Pertini
 Il Paziente in nutrizione parenterale CPSI Andrea Casal ASL Roma 2 Degenza Medica - Ospedale S. Pertini Il sottoscritto Andrea Casal ai sensi dell art. 3.3 sul Conflitto di Interessi, pag. 17 del Reg.
Il Paziente in nutrizione parenterale CPSI Andrea Casal ASL Roma 2 Degenza Medica - Ospedale S. Pertini Il sottoscritto Andrea Casal ai sensi dell art. 3.3 sul Conflitto di Interessi, pag. 17 del Reg.
Aspetti farmaceutici: (in)compatibilità
 Le criticità Aspetti farmaceutici: (in)compatibilità valutazione delle (in)compatibilità dei componenti le miscele più utilizzate nella pratica clinica. Le schede tecniche consultate non prevedono le miscele
Le criticità Aspetti farmaceutici: (in)compatibilità valutazione delle (in)compatibilità dei componenti le miscele più utilizzate nella pratica clinica. Le schede tecniche consultate non prevedono le miscele
La sottoscritta TESEI LETIZIA
 La sottoscritta TESEI LETIZIA ai sensi dell art. 3.3 sul Conflitto di Interessi, pag. 17 del Reg. Applicativo dell Accordo Stato-Regione del 5 novembre 2009, dichiara X che negli ultimi due anni NON ha
La sottoscritta TESEI LETIZIA ai sensi dell art. 3.3 sul Conflitto di Interessi, pag. 17 del Reg. Applicativo dell Accordo Stato-Regione del 5 novembre 2009, dichiara X che negli ultimi due anni NON ha
Infermiere Giuliana Bettinazzi U.O. Oncologia medica, Ospedale Sacro Cuore Don Calabria
 Infermiere Giuliana Bettinazzi U.O. Oncologia medica, Ospedale Sacro Cuore Don Calabria La gestione medico-infermieristica delle urgenze da trattamenti antitumorali, Definizioni: Infiltrazione: somministrazione
Infermiere Giuliana Bettinazzi U.O. Oncologia medica, Ospedale Sacro Cuore Don Calabria La gestione medico-infermieristica delle urgenze da trattamenti antitumorali, Definizioni: Infiltrazione: somministrazione
TPN: indicazioni, rischi, modalità, complicanze. Dr Gianmariano Marchesi Rianimazione - TI Adulti Ospedali Riuniti di Bergamo
 TPN: indicazioni, rischi, modalità, complicanze Dr Gianmariano Marchesi Rianimazione - TI Adulti Ospedali Riuniti di Bergamo Quando impiegare PN 1. Quando non è possibile utilizzare l apparato digerente
TPN: indicazioni, rischi, modalità, complicanze Dr Gianmariano Marchesi Rianimazione - TI Adulti Ospedali Riuniti di Bergamo Quando impiegare PN 1. Quando non è possibile utilizzare l apparato digerente
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 17 Le proprietà delle soluzioni 3 Sommario (I) 1. Perché le sostanze si sciolgono? 2. Soluzioni acquose ed elettroliti 3. La
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 17 Le proprietà delle soluzioni 3 Sommario (I) 1. Perché le sostanze si sciolgono? 2. Soluzioni acquose ed elettroliti 3. La
Il rischio dello stravaso e la gestione del patrimonio venoso del paziente in trattamento infusionale
 Il rischio dello stravaso e la gestione del patrimonio venoso del paziente in trattamento infusionale Alessandro Inno Oncologia Medica Ospedale Sacro Cuore Don Calabria Negrar - Verona Stravaso Infiltrazione
Il rischio dello stravaso e la gestione del patrimonio venoso del paziente in trattamento infusionale Alessandro Inno Oncologia Medica Ospedale Sacro Cuore Don Calabria Negrar - Verona Stravaso Infiltrazione
Il corso è dedicato ad un numero massimo di 10 infermieri e sarà ECM accreditato e si terrà i giorni Marzo RAZIONALE DEL CORSO
 Associazione Amici di Isal, sezione di Benevento Sede U.O. di Terapia del Dolore e Cure Palliative A.O.R.N. G. Rummo via dell Angelo, 1 82100 Benevento Tel/fax 0824-57773 cell. 3343936370 e-mail isalbenevento@virgilio.it
Associazione Amici di Isal, sezione di Benevento Sede U.O. di Terapia del Dolore e Cure Palliative A.O.R.N. G. Rummo via dell Angelo, 1 82100 Benevento Tel/fax 0824-57773 cell. 3343936370 e-mail isalbenevento@virgilio.it
BANDO DI FORNITURE. Motivazione della rettifica: Per modifica basi asta e proroga termine scadenza offerte
 ENTE: Agenzia Regionale Sanitaria - Area Centrale Regionale di Acquisto Codice fiscale: 95113490106 Provincia di Genova, Comune di Genova Indirizzo: P.zza della Vittoria N 15 Cap: 16121 -- RETTIFICA --
ENTE: Agenzia Regionale Sanitaria - Area Centrale Regionale di Acquisto Codice fiscale: 95113490106 Provincia di Genova, Comune di Genova Indirizzo: P.zza della Vittoria N 15 Cap: 16121 -- RETTIFICA --
ALLEGATO E SCHEDA OFFERTA ECONOMICA lotto descrizione Codice prodotto offerto e nome commerciale
 ALLEGATO E SCHEDA OFFERTA ECONOMICA lotto descrizione Codice prodotto codice prodotto CND anno 8 UM Fabb..1 ACQUA PER PREPARAZIONI INIETTABILI ML n. 1..2 ACQUA PER PREPARAZIONI INIETTABILI 250ML n..3 ACQUA
ALLEGATO E SCHEDA OFFERTA ECONOMICA lotto descrizione Codice prodotto codice prodotto CND anno 8 UM Fabb..1 ACQUA PER PREPARAZIONI INIETTABILI ML n. 1..2 ACQUA PER PREPARAZIONI INIETTABILI 250ML n..3 ACQUA
Osmometria ed Emolisi
 Osmometria ed Emolisi 1 ADE: MISURA DELLA RESISTENZA OSMOTICA DEI GLOBULI ROSSI (2/12/08). Il globulo rosso è una piccola cellula del sangue deputata al trasporto dell'ossigeno e priva di nucleo e di organelli.
Osmometria ed Emolisi 1 ADE: MISURA DELLA RESISTENZA OSMOTICA DEI GLOBULI ROSSI (2/12/08). Il globulo rosso è una piccola cellula del sangue deputata al trasporto dell'ossigeno e priva di nucleo e di organelli.
ALLEGATO A CARATTERISTICHE TECNICHE E FABBISOGNO ANNUO
 ALLEGATO A CARATTERISTICHE TECNICHE E FABBISOGNO ANNUO lotto descrizione U.1 ACQUA PER PREPARAZIONI INIETTABILI 100L (FLACONE) n. 1.500 0,2450 367,5000.2 ACQUA PER PREPARAZIONI INIETTABILI 250L (FLACONE)
ALLEGATO A CARATTERISTICHE TECNICHE E FABBISOGNO ANNUO lotto descrizione U.1 ACQUA PER PREPARAZIONI INIETTABILI 100L (FLACONE) n. 1.500 0,2450 367,5000.2 ACQUA PER PREPARAZIONI INIETTABILI 250L (FLACONE)
1. Perché le sostanze si sciolgono 2. Soluzioni acquose ed elettroliti 3. La concentrazione delle soluzioni 4. L effetto del soluto sul solvente: le
 Unità n 14 Le proprietà delle soluzioni 1. Perché le sostanze si sciolgono 2. Soluzioni acquose ed elettroliti 3. La concentrazione delle soluzioni 4. L effetto del soluto sul solvente: le proprietà colligative
Unità n 14 Le proprietà delle soluzioni 1. Perché le sostanze si sciolgono 2. Soluzioni acquose ed elettroliti 3. La concentrazione delle soluzioni 4. L effetto del soluto sul solvente: le proprietà colligative
31/10/2014. La centralizzazione al S. Orsola-Malpighi di Bologna. Esigenza di Informatizzazione
 La centralizzazione al S. Orsola-Malpighi di Bologna 4 CORSO REGIONALE PER FARMACISTI, TECNICI E INFERMIERI DELL AREA ONCOLOGICA Servizio Politica del Farmaco, Regione Emilia-Romagna Bologna, 02 ottobre
La centralizzazione al S. Orsola-Malpighi di Bologna 4 CORSO REGIONALE PER FARMACISTI, TECNICI E INFERMIERI DELL AREA ONCOLOGICA Servizio Politica del Farmaco, Regione Emilia-Romagna Bologna, 02 ottobre
UNITA OPERATIVA COMPLESSA APPALTI E FORNITURE PALERMO Viale Strasburgo, n. 233 CAPITOLATO TECNICO
 UNITA OPERATIVA COMPLESSA APPALTI E FORNITURE 90146 PALERMO Viale Strasburgo, n. 233 CAPITOLATO TECNICO Allegato C FORNITURA TRIENNALE DI SOLUZIONI INFUSIONALI E GALENICI PER L AZIENDA OSPEDALIERA OSPEDALI
UNITA OPERATIVA COMPLESSA APPALTI E FORNITURE 90146 PALERMO Viale Strasburgo, n. 233 CAPITOLATO TECNICO Allegato C FORNITURA TRIENNALE DI SOLUZIONI INFUSIONALI E GALENICI PER L AZIENDA OSPEDALIERA OSPEDALI
Il corso è dedicato ad un numero massimo di 10 infermieri e sarà ECM accreditato e si terrà i giorni Marzo RAZIONALE DEL CORSO
 Associazione Amici di Isal, sezione di Benevento Sede U.O. di Terapia del Dolore e Cure Palliative A.O.R.N. G. Rummo via dell Angelo, 1 82100 Benevento Tel/fax 0824-57773 cell. 3343936370 e-mail isalbenevento@virgilio.it
Associazione Amici di Isal, sezione di Benevento Sede U.O. di Terapia del Dolore e Cure Palliative A.O.R.N. G. Rummo via dell Angelo, 1 82100 Benevento Tel/fax 0824-57773 cell. 3343936370 e-mail isalbenevento@virgilio.it
SOLUZIONI. Una soluzione è una miscela omogenea di più composti chimici. le miscele gassose sono sempre omogenee e quindi formano sempre una soluzione
 SOLUZIONI Una soluzione è una miscela omogenea di più composti chimici SOLUZIONI GASSOSE: SOLUZIONI LIQUIDE: SOLUZIONI SOLIDE: le miscele gassose sono sempre omogenee e quindi formano sempre una soluzione
SOLUZIONI Una soluzione è una miscela omogenea di più composti chimici SOLUZIONI GASSOSE: SOLUZIONI LIQUIDE: SOLUZIONI SOLIDE: le miscele gassose sono sempre omogenee e quindi formano sempre una soluzione
Allestimento personalizzato di sacche per NP. 21 maggio 2014 Davide Zenoni A.O.Bolognini
 Allestimento personalizzato di sacche per NP 21 maggio 2014 Davide Zenoni A.O.Bolognini Allestimento personalizzato di sacche per NP COME? QUANDO? PERCHE? STANDARD TECNICI SCOPO allestimento centralizzato
Allestimento personalizzato di sacche per NP 21 maggio 2014 Davide Zenoni A.O.Bolognini Allestimento personalizzato di sacche per NP COME? QUANDO? PERCHE? STANDARD TECNICI SCOPO allestimento centralizzato
-PROPRIETA COLLIGATIVE-
 -PROPRIETA COLLIGATIVE- Le proprietà colligative sono proprietà delle soluzioni e sono funzioni del numero e non della natura delle particelle di soluto che le compongono. Abbassamento della pressione
-PROPRIETA COLLIGATIVE- Le proprietà colligative sono proprietà delle soluzioni e sono funzioni del numero e non della natura delle particelle di soluto che le compongono. Abbassamento della pressione
RUOLO DELL ACCESSO PERIFERICO NELLE TERAPIE DOMICILIARI. Marco Ariotti RN, Cure Domiciliari Torino
 RUOLO DELL ACCESSO PERIFERICO NELLE TERAPIE DOMICILIARI Marco Ariotti RN, Cure Domiciliari Torino IL DOMICILIO 23/10/17 2 I DESTINATARI DELLE CURE DOMICILIARI Persone non autosufficienti o a rischio di
RUOLO DELL ACCESSO PERIFERICO NELLE TERAPIE DOMICILIARI Marco Ariotti RN, Cure Domiciliari Torino IL DOMICILIO 23/10/17 2 I DESTINATARI DELLE CURE DOMICILIARI Persone non autosufficienti o a rischio di
Soluzioni e miscugli eterogenei. Soluzioni e miscugli eterogenei. Soluzioni e miscugli eterogenei
 Le soluzioni Soluzioni e miscugli eterogenei Un sistema formato da due o più componenti è chiamato miscuglio. I miscugli possono essere : miscugli eterogenei; miscugli omogenei o soluzioni. 2 4 Soluzioni
Le soluzioni Soluzioni e miscugli eterogenei Un sistema formato da due o più componenti è chiamato miscuglio. I miscugli possono essere : miscugli eterogenei; miscugli omogenei o soluzioni. 2 4 Soluzioni
SOLUZIONI ELETTROLITICHE. Classificazione dello Shock Ipovolemico Traumatico Cardiogeno Settico (Hyperdynamic/Hypodynamic) Neurogeno Hypoadrenal
 SOLUZIONI ELETTROLITICHE Classificazione dello Shock Ipovolemico Traumatico Cardiogeno Settico (Hyperdynamic/Hypodynamic) Neurogeno Hypoadrenal 1 La terapia infusionale Lo scopo della terapia infusionale
SOLUZIONI ELETTROLITICHE Classificazione dello Shock Ipovolemico Traumatico Cardiogeno Settico (Hyperdynamic/Hypodynamic) Neurogeno Hypoadrenal 1 La terapia infusionale Lo scopo della terapia infusionale
APPROPRIATEZZA PRESCRITTIVA IN OSPEDALE REV. 1 Pag. 1 / 5 SOLUZIONI CONCENTRATE DI POTASSIO
 OSPEDALE REV. 1 Pag. 1 / 5 Stato delle Modifiche Rev. Data Causale 0 14/05/2011 Prima emissione 1) PREMESSA: - Il Ministero della Salute ha emanato una raccomandazione sul corretto utilizzo delle soluzioni
OSPEDALE REV. 1 Pag. 1 / 5 Stato delle Modifiche Rev. Data Causale 0 14/05/2011 Prima emissione 1) PREMESSA: - Il Ministero della Salute ha emanato una raccomandazione sul corretto utilizzo delle soluzioni
Termodinamica Chimica
 Universita degli Studi dell Insubria Corsi di Laurea in Scienze Chimiche e Chimica Industriale Termodinamica Chimica Miscele e Soluzioni dario.bressanini@uninsubria.it http://scienze-como.uninsubria.it/bressanini
Universita degli Studi dell Insubria Corsi di Laurea in Scienze Chimiche e Chimica Industriale Termodinamica Chimica Miscele e Soluzioni dario.bressanini@uninsubria.it http://scienze-como.uninsubria.it/bressanini
I compartimenti liquidi corporei
 I compartimenti liquidi corporei Il mantenimento di un volume relativamente costante e di una composizione stabile dei liquidi corporei è essenziale per l omeostasi. In condizioni di equilibrio, l assunzione
I compartimenti liquidi corporei Il mantenimento di un volume relativamente costante e di una composizione stabile dei liquidi corporei è essenziale per l omeostasi. In condizioni di equilibrio, l assunzione
PROPRIETA DELLE SOLUZIONI
 1 11 PROPRIETA DELLE SOLUZIONI 2 SOLUZIONI IDEALI H mix = 0 le interazioni fra le molecole di soluto e di solvente puri sono paragonabili a quelle fra soluto e solvente; durante il processo di dissoluzione
1 11 PROPRIETA DELLE SOLUZIONI 2 SOLUZIONI IDEALI H mix = 0 le interazioni fra le molecole di soluto e di solvente puri sono paragonabili a quelle fra soluto e solvente; durante il processo di dissoluzione
pressione esercitata dalle molecole di gas in equilibrio con Si consideri una soluzione di B in A. Per una soluzione ideale
 PROPRIETA COLLIGATIVE Proprietà che dipendono solo dal numero di particelle presenti in soluzione 1. TENSIONE DI VAPORE 2. INNALZAMENTO EBULLIOSCOPICO 3. ABBASSAMENTO CRIOSCOPICO 4. PRESSIONE OSMOTICA
PROPRIETA COLLIGATIVE Proprietà che dipendono solo dal numero di particelle presenti in soluzione 1. TENSIONE DI VAPORE 2. INNALZAMENTO EBULLIOSCOPICO 3. ABBASSAMENTO CRIOSCOPICO 4. PRESSIONE OSMOTICA
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 1. DENOMINAZIONE DEL MEDICINALE Sodio cloruro Galenica Senese 2 meq/ml concentrato per soluzione per infusione Sodio cloruro Galenica Senese 3 meq/ml concentrato per soluzione per infusione 2. COMPOSIZIONE
1. DENOMINAZIONE DEL MEDICINALE Sodio cloruro Galenica Senese 2 meq/ml concentrato per soluzione per infusione Sodio cloruro Galenica Senese 3 meq/ml concentrato per soluzione per infusione 2. COMPOSIZIONE
Ripassiamo insieme.la matematica a servizio della sicurezza dell assistito. Dott. Mattia Luciano
 Ripassiamo insieme.la matematica a servizio della sicurezza dell assistito Dott. Mattia Luciano CALCOLO PER I DOSAGGI FARMACOLOGICI I calcoli per la somministrazione possono riguardare: Ricostituzione
Ripassiamo insieme.la matematica a servizio della sicurezza dell assistito Dott. Mattia Luciano CALCOLO PER I DOSAGGI FARMACOLOGICI I calcoli per la somministrazione possono riguardare: Ricostituzione
Lezione n. 12. Proprietà colligative Variazione del punto crioscopico. Pressione osmotica. 02/03/2008 Antonino Polimeno 1
 Chimica Fisica - Chimica e Tecnologia Farmaceutiche Lezione n. 12 Proprietà colligative Variazione del punto ebullioscopico Variazione del punto crioscopico Pressione osmotica 02/03/2008 Antonino Polimeno
Chimica Fisica - Chimica e Tecnologia Farmaceutiche Lezione n. 12 Proprietà colligative Variazione del punto ebullioscopico Variazione del punto crioscopico Pressione osmotica 02/03/2008 Antonino Polimeno
INTERAZIONI FARMACOLOGICHE. Cosa deve sapere l infermiere in Unità Coronarica. Samuela Costantino. Cardiologia Universitaria
 INTERAZIONI FARMACOLOGICHE Cosa deve sapere l infermiere in Unità Coronarica Samuela Costantino Cardiologia Universitaria 1 Cosa deve sapere l infermiere in Unità Coronarica 2 PREMESSA Argomento vasto
INTERAZIONI FARMACOLOGICHE Cosa deve sapere l infermiere in Unità Coronarica Samuela Costantino Cardiologia Universitaria 1 Cosa deve sapere l infermiere in Unità Coronarica 2 PREMESSA Argomento vasto
 positiva, endotermico (la soluzione si raffredda) negativa, esotermico (la soluzione si scalda). DH sol = E ret + E solv concentrazione Molare Esempio: Preparare mezzo litro (0,5 l) di soluzione acquosa
positiva, endotermico (la soluzione si raffredda) negativa, esotermico (la soluzione si scalda). DH sol = E ret + E solv concentrazione Molare Esempio: Preparare mezzo litro (0,5 l) di soluzione acquosa
SOLUZIONI E CONCENTRAZIONE
 SOLUZIONI E CONCENTRAZIONE Miscela omogenea di due o più sostanze: solvente (presente in maggiore quantità) + soluto In genere il solvente è liquido (es.acqua) mentre il soluto può essere solido, liquido,
SOLUZIONI E CONCENTRAZIONE Miscela omogenea di due o più sostanze: solvente (presente in maggiore quantità) + soluto In genere il solvente è liquido (es.acqua) mentre il soluto può essere solido, liquido,
Modalità di trasporto di acqua attraverso la membrana plasmatica
 Modalità di trasporto di acqua attraverso la membrana plasmatica Membrana plasmatica H 2 O H 2 O acquaporina In genere la membrana plasmatica che riveste tutte le cellule di un organismo è permeabile all
Modalità di trasporto di acqua attraverso la membrana plasmatica Membrana plasmatica H 2 O H 2 O acquaporina In genere la membrana plasmatica che riveste tutte le cellule di un organismo è permeabile all
CAPITOLATO SPECIALE PER LA FORNITURA
 CAPITOLATO SPECIALE PER LA FORNITURA di PRODOTTI PER NUTRIZIONE PARENTERALE (FARMACI ed ACCESSORI) ART. 1 Oggetto della gara L appalto ha per oggetto la fornitura di PRODOTTI PER NUTRIZIONE PARENTERALE
CAPITOLATO SPECIALE PER LA FORNITURA di PRODOTTI PER NUTRIZIONE PARENTERALE (FARMACI ed ACCESSORI) ART. 1 Oggetto della gara L appalto ha per oggetto la fornitura di PRODOTTI PER NUTRIZIONE PARENTERALE
Soluzioni ed emulsioni infusionali ed elettrolitiche concentrate
 Soluzioni ed emulsioni infusionali ed elettrolitiche concentrate Lotto 1: Plasma-expanders: Gelatine Composizione litro > 30 e 25.000. e < 50.000 Da Concentrazione di elettroliti
Soluzioni ed emulsioni infusionali ed elettrolitiche concentrate Lotto 1: Plasma-expanders: Gelatine Composizione litro > 30 e 25.000. e < 50.000 Da Concentrazione di elettroliti
90146 PALERMO Viale Strasburgo, n. 233
 FORNITURA TRIENNALE DI SOLUZIONI INFUSIONALI E GALENICI PER L AZIENDA OSPEDALIERA OSPEDALI RIUNITI VILLASOFIA-CERVELLO DI PALERMO SCHEDA OFFERTA (da inserire nella BUSTA N. 3 Offerta economica) DITTA OFFERENTE:
FORNITURA TRIENNALE DI SOLUZIONI INFUSIONALI E GALENICI PER L AZIENDA OSPEDALIERA OSPEDALI RIUNITI VILLASOFIA-CERVELLO DI PALERMO SCHEDA OFFERTA (da inserire nella BUSTA N. 3 Offerta economica) DITTA OFFERENTE:
Le soluzioni. A cura della Prof. ssa Barone Antonina
 Le soluzioni A cura della Prof. ssa Barone Antonina Le soluzioni: caratteri generali Sono sistemi omogenei; In esse, in qualsiasi punto si esegue una misurazione, si ottengono le stesse caratteristiche
Le soluzioni A cura della Prof. ssa Barone Antonina Le soluzioni: caratteri generali Sono sistemi omogenei; In esse, in qualsiasi punto si esegue una misurazione, si ottengono le stesse caratteristiche
2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 ml di soluzione contengono: Principio attivo: Potassio Acetato 29.4 g (ogni ml contiene 3 meq di K + )
 1. DENOMINAZIONE DEL MEDICINALE Potassio Acetato MONICO 3 meq/ml Concentrato per soluzione per infusione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 ml di soluzione contengono: Principio attivo: Potassio
1. DENOMINAZIONE DEL MEDICINALE Potassio Acetato MONICO 3 meq/ml Concentrato per soluzione per infusione 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 100 ml di soluzione contengono: Principio attivo: Potassio
Importanza della pressione osmotica. Turgore delle cellule e dei tessuti Volume del sangue Scambio di liquidi tra il sangue e i tessuti Rene
 Importanza della pressione osmotica Turgore delle cellule e dei tessuti Volume del sangue Scambio di liquidi tra il sangue e i tessuti Rene Quali sono le forze che spingono le sostanze a spostarsi? Lo
Importanza della pressione osmotica Turgore delle cellule e dei tessuti Volume del sangue Scambio di liquidi tra il sangue e i tessuti Rene Quali sono le forze che spingono le sostanze a spostarsi? Lo
Confezione G13%E emulsione per infusione 10 sacche da 300 ml a 3 camere non PVC AIC n /M (in base 10) 16WBCU (in base 32)
 Autorizzazione all immissione in commercio del medicinale «Numeta» Estratto determinazione n. 2473/2011 MEDICINALE NUMETA TITOLARE AIC: BAXTER S.P.A. Piazzale dell Industria, 20 00144 ROMA G13%E emulsione
Autorizzazione all immissione in commercio del medicinale «Numeta» Estratto determinazione n. 2473/2011 MEDICINALE NUMETA TITOLARE AIC: BAXTER S.P.A. Piazzale dell Industria, 20 00144 ROMA G13%E emulsione
PERMEABILITA DI UN DOPPIO STRATO FOSFOLIPIDICO ARTIFICIALE (PRIVO DI PROTEINE)
 PERMEABILITA DI UN DOPPIO STRATO FOSFOLIPIDICO ARTIFICIALE (PRIVO DI PROTEINE) NELLE MEMBRANE CELLULARI IL COMPORTAMENTO PUÒ ESSERE MOLTO DIVERSO (GRAZIE ALLA PRESENZA DELLE PROTEINE) PICCOLE MOLECOLE
PERMEABILITA DI UN DOPPIO STRATO FOSFOLIPIDICO ARTIFICIALE (PRIVO DI PROTEINE) NELLE MEMBRANE CELLULARI IL COMPORTAMENTO PUÒ ESSERE MOLTO DIVERSO (GRAZIE ALLA PRESENZA DELLE PROTEINE) PICCOLE MOLECOLE
4ª UNITA DIDATTICA Modello Nutrizionale metabolico
 4ª UNITA DIDATTICA Modello Nutrizionale metabolico Contenuti Modello Nutrizionale metabolico Sezione del modello: Equilibrio idro-elettrolitico e acido-base Assistenza alla persona con problemi relativi
4ª UNITA DIDATTICA Modello Nutrizionale metabolico Contenuti Modello Nutrizionale metabolico Sezione del modello: Equilibrio idro-elettrolitico e acido-base Assistenza alla persona con problemi relativi
Proprietà colligative
 roprietà colligative Fra i sistemi reali è utile esaminare il comportamento di soluzioni diluite ottenuti da solidi o liquidi poco volatili rispetto al solvente. Le proprietà di tali soluzioni dipendono
roprietà colligative Fra i sistemi reali è utile esaminare il comportamento di soluzioni diluite ottenuti da solidi o liquidi poco volatili rispetto al solvente. Le proprietà di tali soluzioni dipendono
CONCENTRAZIONE. Le proprietà delle soluzioni di pendono dalle quantità relative delle sostanze che le compongono.
 1 CONCENTRAZIONE Le proprietà delle soluzioni di pendono dalle quantità relative delle sostanze che le compongono. La concentrazione esprime la composizione quantitiva soluzione. di una Unità di concentrazione
1 CONCENTRAZIONE Le proprietà delle soluzioni di pendono dalle quantità relative delle sostanze che le compongono. La concentrazione esprime la composizione quantitiva soluzione. di una Unità di concentrazione
AZIENDA USL ROMA H Borgo Garibaldi, Albano Laziale (Roma) Tel Fax
 FARMACIA POLO H/3 PRESIDIO OSPEDALE PAOLO COLOMBO VELLETRI PROCEDURA PER LA RICHIESTA DI SACCHE MAGISTRALI PER NTP REDAZIONE Direzione Sanitaria Polo H3: dr Paolo Angeletti Farmacia Polo H3: dott.ssa Giuseppa
FARMACIA POLO H/3 PRESIDIO OSPEDALE PAOLO COLOMBO VELLETRI PROCEDURA PER LA RICHIESTA DI SACCHE MAGISTRALI PER NTP REDAZIONE Direzione Sanitaria Polo H3: dr Paolo Angeletti Farmacia Polo H3: dott.ssa Giuseppa
RICOSTITUZIONE DILUIZIONE MODALITÀ DI SOMMINISTRAZIONE. TEMPO DI SOMM.
 PRINCIPIO ATTIVO Doxorubici na NOME COMMERCIALE Adriblastina fl 10 o 50 Melfalan Alkeran 50 fl RICOSTITUZIONE DILUIZIONE MODALITÀ DI SOMMINISTRAZIONE. TEMPO DI SOMM. 2 / o Sodio cloruro 0.9% ( 100) -Bolo
PRINCIPIO ATTIVO Doxorubici na NOME COMMERCIALE Adriblastina fl 10 o 50 Melfalan Alkeran 50 fl RICOSTITUZIONE DILUIZIONE MODALITÀ DI SOMMINISTRAZIONE. TEMPO DI SOMM. 2 / o Sodio cloruro 0.9% ( 100) -Bolo
Proprietà colligative. Proprietà che dipendono dal numero di particelle di soluto presenti in una soluzione ma non dalla loro natura
 Proprietà colligative Proprietà che dipendono dal numero di particelle di soluto presenti in una soluzione ma non dalla loro natura Grandezze colligative abbassamento della tensione di vapore innalzamento
Proprietà colligative Proprietà che dipendono dal numero di particelle di soluto presenti in una soluzione ma non dalla loro natura Grandezze colligative abbassamento della tensione di vapore innalzamento
Soluzioni infusionali in materiale plastico
 PROCEDURA APERTA PER LA FORNITURA DI SOLUZIONI INFUSIONALI, PER IRRIGAZIONE PER LE AA.SS.LL./AA.OO.UU./A.O. DELLA REGIONE SARDEGNA PER IL PERIODO DI 48 (quarantotto) MESI All. A) al Capitolato Speciale
PROCEDURA APERTA PER LA FORNITURA DI SOLUZIONI INFUSIONALI, PER IRRIGAZIONE PER LE AA.SS.LL./AA.OO.UU./A.O. DELLA REGIONE SARDEGNA PER IL PERIODO DI 48 (quarantotto) MESI All. A) al Capitolato Speciale
Medicine Specialistiche GESTIONE DEGLI STRAVASI DI FARMACI ANTIBLASTICI
 Pag. 1/7 GESTIONE DEGLI STRAVASI DI FARMACI ANTIBLASTICI 1. Lista di distribuzione...1 2. Emissione...1 3. Scopo...1 4. Campo di applicazione...1 5. Riferimenti...1 6. Definizioni...2 7. Responsabilità...2
Pag. 1/7 GESTIONE DEGLI STRAVASI DI FARMACI ANTIBLASTICI 1. Lista di distribuzione...1 2. Emissione...1 3. Scopo...1 4. Campo di applicazione...1 5. Riferimenti...1 6. Definizioni...2 7. Responsabilità...2
LE PROPRIETÀ DELLE SOLUZIONI
 LE PROPRIETÀ DELLE SOLUZIONI Le Soluzioni o Miscugli omogenei Solvente e soluto Energia sprigionata e acquisita Solvatazione e idratazione Le Soluzioni 3) 1. Composti Ionici (Dissociazione) 2. Composti
LE PROPRIETÀ DELLE SOLUZIONI Le Soluzioni o Miscugli omogenei Solvente e soluto Energia sprigionata e acquisita Solvatazione e idratazione Le Soluzioni 3) 1. Composti Ionici (Dissociazione) 2. Composti
SERVIZIO DI FARMACIA LA GESTIONE DEGLI ACCESSI VENOSI DOCUMENTI E STRUMENTI PER LA GESTIONE DEI DISPOSITIVI MEDICI
 LA GESTIONE DEGLI ACCESSI VENOSI DOCUMENTI E STRUMENTI PER LA GESTIONE DEI DISPOSITIVI MEDICI 1 DISPOSITIVI MEDICI EPIC 2014 INS 2016 2 QUELLO CHE VEDIAMO ci fornisce sempre le conoscenze che ci servono?
LA GESTIONE DEGLI ACCESSI VENOSI DOCUMENTI E STRUMENTI PER LA GESTIONE DEI DISPOSITIVI MEDICI 1 DISPOSITIVI MEDICI EPIC 2014 INS 2016 2 QUELLO CHE VEDIAMO ci fornisce sempre le conoscenze che ci servono?
Proprietà colligative
 Proprietà colligative Le proprietà che dipendono dalla proporzione tra le molecole del soluto e quelle del solvente ma non dall identità chimica del soluto si dicono proprietà colligative. Le proprietà
Proprietà colligative Le proprietà che dipendono dalla proporzione tra le molecole del soluto e quelle del solvente ma non dall identità chimica del soluto si dicono proprietà colligative. Le proprietà
Esercitazioni di Elementi di Chimica. Modulo 3 Trasformazioni della Materia
 Esercitazioni di Elementi di Chimica Modulo 3 Trasformazioni della Materia Esempi di quiz a risposta multipla e questionari a completamento L esame finale sarà composto da problemi simili Quale/i dei seguenti
Esercitazioni di Elementi di Chimica Modulo 3 Trasformazioni della Materia Esempi di quiz a risposta multipla e questionari a completamento L esame finale sarà composto da problemi simili Quale/i dei seguenti
Proprietà colligative. Proprietà che dipendono dal numero di particelle di soluto presenti in una soluzione ma non dalla loro natura
 Proprietà colligative Proprietà che dipendono dal numero di particelle di soluto presenti in una soluzione ma non dalla loro natura Grandezze colligative abbassamento della tensione di vapore innalzamento
Proprietà colligative Proprietà che dipendono dal numero di particelle di soluto presenti in una soluzione ma non dalla loro natura Grandezze colligative abbassamento della tensione di vapore innalzamento
LE SOLUZIONI. Una soluzione è un sistema omogeneo costituito da almeno due componenti
 LE SOLUZIONI Una soluzione è un sistema omogeneo costituito da almeno due componenti Il componente maggioritario e solitamente chiamato solvente mentre i componenti in quantita minore sono chiamati soluti
LE SOLUZIONI Una soluzione è un sistema omogeneo costituito da almeno due componenti Il componente maggioritario e solitamente chiamato solvente mentre i componenti in quantita minore sono chiamati soluti
Diffusione e osmosi. Roberto Cirio. Corso di Laurea in Chimica e Tecnologia Farmaceutiche Anno accademico Corso di Fisica
 Roberto Cirio Corso di Laurea in Chimica e Tecnologia Farmaceutiche Anno accademico 2007 2008 Corso di Fisica La lezione di oggi Sostanze sciolte in liquidi, se utilizzate con membrane, hanno comportamenti
Roberto Cirio Corso di Laurea in Chimica e Tecnologia Farmaceutiche Anno accademico 2007 2008 Corso di Fisica La lezione di oggi Sostanze sciolte in liquidi, se utilizzate con membrane, hanno comportamenti
Le proprietà colligative
 Le proprietà colligative Dr. Gabriella Giulia Pulcini Ph.D. Student, Development of new approaches to teaching and learning Natural and Environmental Sciences University of Camerino, ITALY 1 Abbassamento
Le proprietà colligative Dr. Gabriella Giulia Pulcini Ph.D. Student, Development of new approaches to teaching and learning Natural and Environmental Sciences University of Camerino, ITALY 1 Abbassamento
I compartimenti liquidi corporei
 Bilancio idrico I compartimenti liquidi corporei E essenziale per l omeostasi mantenere costanti volume ed osmolalità dei liquidi corporei, attraverso il bilancio tra assunzione ed eliminazione di H 2
Bilancio idrico I compartimenti liquidi corporei E essenziale per l omeostasi mantenere costanti volume ed osmolalità dei liquidi corporei, attraverso il bilancio tra assunzione ed eliminazione di H 2
Appropriata modalità di somministrazione delle principali molecole antibiotiche
 Appropriata modalità di somministrazione delle principali molecole antibiotiche Inf.ra Roberta Castellani Medicina generale Presidio Ospedaliero Cecina La sottoscritta ROBERTA CASTELLANI ai sensi dell
Appropriata modalità di somministrazione delle principali molecole antibiotiche Inf.ra Roberta Castellani Medicina generale Presidio Ospedaliero Cecina La sottoscritta ROBERTA CASTELLANI ai sensi dell
Picc e Midline New generation. Firenze 6 maggio Congresso Nazionale ANÌMO
 Picc e Midline New generation L evoluzione del cateterismo venoso Firenze 6 maggio 2008 3 Congresso Nazionale ANÌMO Claudia Gatta ASL BI - Biella - Accessi vascolari Accessi venosi a breve termine (durata
Picc e Midline New generation L evoluzione del cateterismo venoso Firenze 6 maggio 2008 3 Congresso Nazionale ANÌMO Claudia Gatta ASL BI - Biella - Accessi vascolari Accessi venosi a breve termine (durata
Fisicaa Applicata, Area Tecnica, M. Ruspa Esercizio. Data una massa m = 8,8 mg di CO 2, calcolare: 1) il numero di moli. 2) il numero di molecole
 Esercizio Data una massa m = 8,8 mg di CO 2, calcolare: 1) il numero di moli 2) il numero di molecole 1 GAS PERFETTO volume occupato dalle molecole è trascurabile; forze di attrazione tra molecole sono
Esercizio Data una massa m = 8,8 mg di CO 2, calcolare: 1) il numero di moli 2) il numero di molecole 1 GAS PERFETTO volume occupato dalle molecole è trascurabile; forze di attrazione tra molecole sono
METABOLISMO CELLULARE
 METABOLISMO CELLULARE Il funzionamento della cellula Le cellule sono veri e propri esseri viventi: sono capaci di alimentarsi, di crescere, di produrre nuove sostanze, di riprodursi, di espellere rifiuti
METABOLISMO CELLULARE Il funzionamento della cellula Le cellule sono veri e propri esseri viventi: sono capaci di alimentarsi, di crescere, di produrre nuove sostanze, di riprodursi, di espellere rifiuti
Informazioni nutrizionali
 Proteine 16% Carboidrati 51% Fibre alimentari 3% Alimento dietetico a fini medici speciali nutrizionalmente completo, sterile, a base di alimenti naturali omogeneizzati e arricchito con fibra alimentare
Proteine 16% Carboidrati 51% Fibre alimentari 3% Alimento dietetico a fini medici speciali nutrizionalmente completo, sterile, a base di alimenti naturali omogeneizzati e arricchito con fibra alimentare
Trasporto di membrana
 Trasporto di membrana CdL Tecnici di Lab Biomedico AA. 2011/12 Prof.ssa Frabetti Trasporto di membrana molecole piccole molecole grosse trasporto passivo trasporto attivo (con pompe o cotrasportatori)
Trasporto di membrana CdL Tecnici di Lab Biomedico AA. 2011/12 Prof.ssa Frabetti Trasporto di membrana molecole piccole molecole grosse trasporto passivo trasporto attivo (con pompe o cotrasportatori)
GESTIONE DEGLI ACCESSI VENOSI: prevenzione delle complicanze alla luce dell EBM. Gabriella Busca
 GESTIONE DEGLI ACCESSI VENOSI: prevenzione delle complicanze alla luce dell EBM Gabriella Busca Il sottoscritto Busca Gabriella ai sensi dell art. 3.3 sul Conflitto di Interessi, pag. 17 del Reg. Applicativo
GESTIONE DEGLI ACCESSI VENOSI: prevenzione delle complicanze alla luce dell EBM Gabriella Busca Il sottoscritto Busca Gabriella ai sensi dell art. 3.3 sul Conflitto di Interessi, pag. 17 del Reg. Applicativo
Cura e gestione del sito di emergenza e delle linee infusionali Anna Garrettino Firenze, 12 maggio 2019
 Cura e gestione del sito di emergenza e delle linee infusionali Anna Garrettino Firenze, 12 maggio 2019 La sottoscritta Anna Garrettino ai sensi dell art. 3.3 sul Conflitto di Interessi, pag. 17 del Reg.
Cura e gestione del sito di emergenza e delle linee infusionali Anna Garrettino Firenze, 12 maggio 2019 La sottoscritta Anna Garrettino ai sensi dell art. 3.3 sul Conflitto di Interessi, pag. 17 del Reg.
FOGLIO ILLUSTRATIVO. Sodio bicarbonato S.A.L.F. 1,4% soluzione per infusione Sodio bicarbonato S.A.L.F. 8,4% soluzione per infusione
 FOGLIO ILLUSTRATIVO Sodio bicarbonato S.A.L.F. 1,4% soluzione per infusione Sodio bicarbonato S.A.L.F. 8,4% soluzione per infusione CATEGORIA FARMACOTERAPEUTICA Elettroliti. INDICAZIONI TERAPEUTICHE Trattamento
FOGLIO ILLUSTRATIVO Sodio bicarbonato S.A.L.F. 1,4% soluzione per infusione Sodio bicarbonato S.A.L.F. 8,4% soluzione per infusione CATEGORIA FARMACOTERAPEUTICA Elettroliti. INDICAZIONI TERAPEUTICHE Trattamento
POTENZA METABOLICA. Fisica Applicata, Area Infermieristica, M. Ruspa
 POTENZA METABOLICA La potenza metabolica (MR) e l energia prodotta all interno del corpo umano nell unita di tempo. Se con U indichiamo l energia interna del nostro organismo L energia minima per unita
POTENZA METABOLICA La potenza metabolica (MR) e l energia prodotta all interno del corpo umano nell unita di tempo. Se con U indichiamo l energia interna del nostro organismo L energia minima per unita
GLI STATI DELLA MATERIA
 GLI STATI DELLA MATERIA E LE SOLUZIONI Stati di aggregazione della materia Cambiamenti di stato La temperatura del cubetto di ghiaccio aumenta fino a raggiungere un valore detto PUNTO (O TEMPERATURA) DI
GLI STATI DELLA MATERIA E LE SOLUZIONI Stati di aggregazione della materia Cambiamenti di stato La temperatura del cubetto di ghiaccio aumenta fino a raggiungere un valore detto PUNTO (O TEMPERATURA) DI
FARMACOCINETICA 1. Farmacologia generale FARMACOCINETICA FARMACOLOGIA FARMACODINAMICA
 FARMACOCINETICA 1 Farmacologia generale FARMACOCINETICA FARMACOLOGIA FARMACODINAMICA 1 ASSORBIMENTO DEI FARMACI cioè il processo per mezzo del quale un farmaco passa dal sito di somministrazione al plasma
FARMACOCINETICA 1 Farmacologia generale FARMACOCINETICA FARMACOLOGIA FARMACODINAMICA 1 ASSORBIMENTO DEI FARMACI cioè il processo per mezzo del quale un farmaco passa dal sito di somministrazione al plasma
Oggetto : Sicurezza d uso di Olimel (aminoacidi elettroliti glucosio anidro lipidi)
 Regione Lombardia - Giunta DIREZIONE GENERALE SALUTE GOVERNO DEI DATI, DELLE STRATEGIE E PIANI DEL SISTEMA SANITARIO FARMACEUTICA, PROTESICA E DISPOSITIVI MEDICI Piazza Città di Lombardia n.1 20124 Milano
Regione Lombardia - Giunta DIREZIONE GENERALE SALUTE GOVERNO DEI DATI, DELLE STRATEGIE E PIANI DEL SISTEMA SANITARIO FARMACEUTICA, PROTESICA E DISPOSITIVI MEDICI Piazza Città di Lombardia n.1 20124 Milano
7HFQLFKHGLHVWLQ]LRQH,QLEL]LRQHFKLPLFDRD]LRQHDQWLFDWDOLWLFD
![7HFQLFKHGLHVWLQ]LRQH,QLEL]LRQHFKLPLFDRD]LRQHDQWLFDWDOLWLFD 7HFQLFKHGLHVWLQ]LRQH,QLEL]LRQHFKLPLFDRD]LRQHDQWLFDWDOLWLFD](/thumbs/59/43238545.jpg) 7HFQLFKHGLHVWLQ]LRQH,QLEL]LRQHFKLPLFDRD]LRQHDQWLFDWDOLWLFD $UUHVWR GHOOH UHD]LRQL D FDWHQD FKH VL YHULILFDQRQHOODFRPEXVWLRQH Tipicamente si ottiene con polveri e gas. / (67,1=,21('(*/,,1&(1', /HVRVWDQ]HHVWLQJXHQWL
7HFQLFKHGLHVWLQ]LRQH,QLEL]LRQHFKLPLFDRD]LRQHDQWLFDWDOLWLFD $UUHVWR GHOOH UHD]LRQL D FDWHQD FKH VL YHULILFDQRQHOODFRPEXVWLRQH Tipicamente si ottiene con polveri e gas. / (67,1=,21('(*/,,1&(1', /HVRVWDQ]HHVWLQJXHQWL
Lo stato liquido. i liquidi molecolari con legami a idrogeno: le interazioni tra le molecole si stabiliscono soprattutto attraverso legami a idrogeno
 Lo stato liquido Le particelle sono in continuo movimento, anche se questo risulta più limitato rispetto al caso dei gas. Il movimento caratteristico a zig-zag delle particelle è chiamato moto Browniano.
Lo stato liquido Le particelle sono in continuo movimento, anche se questo risulta più limitato rispetto al caso dei gas. Il movimento caratteristico a zig-zag delle particelle è chiamato moto Browniano.
Le proprietà colligative delle soluzioni
 Le proprietà colligative delle soluzioni Alcune immagine sono state prese e modificate da Chimica di Kotz, Treichel & Weaver, Edises 2007, III edizione 1 Le proprietà colligative Alcune proprietà delle
Le proprietà colligative delle soluzioni Alcune immagine sono state prese e modificate da Chimica di Kotz, Treichel & Weaver, Edises 2007, III edizione 1 Le proprietà colligative Alcune proprietà delle
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Sodio Cloruro Fresenius Kabi Italia 0,9%, soluzione per infusione Sodio Cloruro Fresenius Kabi Italia 2%, soluzione per infusione
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Sodio Cloruro Fresenius Kabi Italia 0,9%, soluzione per infusione Sodio Cloruro Fresenius Kabi Italia 2%, soluzione per infusione
