a.a CHIMICA ORGANICA 1 Prof. Giuliana Pitacco lab 337; tel Orario: L M M Aula A1
|
|
|
- Luciano Riva
- 7 anni fa
- Visualizzazioni
Transcript
1 a.a CIMICA ORGANICA 1 Prof. Giuliana Pitacco gpitacco@units.it lab 337; tel Orario: L M M Aula A1 ricevimento: appuntamento in qualsiasi momento 1
2 FEBBRAIO MARZO L 26 L M M M M G G V V S S D D APRILE MAGGIO L L M M M M G G V V S S D D ore a disposizione per 64 ore frontali: Previste 49 ore di lezione, 12 di esercizi, 3 prove 2
3 Testi consigliati W.. Brown & C. S. Foote, Chimica Organica, EdiSES J. McMurry, Chimica Organica, PICCIN S. N. Ege, Chimica Organica, Ed. Sorbona K. Peter, P. Vollhardt, N. E. Schore, Chimica Organica, Zanichelli. P. Y. Bruice, Chimica Organica, EdiSES. T. W. Graham Solomons, Organic Chemistry, J. Wiley&Sons. 3
4 CIMICA ORGANICA 4
5 Definizioni Vecchia: derivata da organismi viventi Nuova: la chimica dei composti del carbonio Da inorganico a organico, Wöhler, 1828 N 4 + OCN - ammonio cianato calore O 2 N C N 2 urea Friedrich Wöhler
6 La chimica organica oggi KC Li Be Na Mg C la chimica dei composti del carbonio..combinato con pochi altri elementi B Al Si N P O S F Cl Br I 6
7 Unicità del carbonio Il carbonio ha una chimica unica Si lega ad ogni altro elemento Si lega a sé stesso in lunghe catene la chimica organica comporta una enorme varietà di composti, di strutture, di reazioni 7
8 Chimica organica La chimica organica è presente in ogni aspetto della nostra vita. biomolecole: Biochimica proteine Chimica Industriale DNA Chimica Farmaceutica cibo vestiti medicine. 8
9 Chimica organica La disciplina chimica organica organizza i composti organici sulla base della loro struttura. Ne studia poi la reattività. E correla struttura con reattività. STRUTTURA REATTIVITÀ 9
10 Obiettivi del corso 1. Assegnare struttura e nome ai composti organici. 2. Predire di una molecola: La struttura tridimensionale L effetto della struttura sulla reattività (velocità della reazione e posizione dell equilibrio) 3. Comunicare tali conoscenze con opportuno linguaggio. 4. Disegnare percorsi sintetici semplici. 10
11 Obiettivi del corso Sarà sufficiente: Conoscere un numero limitato di reazioni permesse e regole semplici di analogia per poter estendere i concetti a un numero illimitato di trasformazioni chimiche. Acquisire automatismi nel riconoscimento di strutture e nella loro trascrizione. Risolvere esercizi per una autovalutazione. 11
12 Struttura Atomica Nucleo carico positivamente molto denso e piccolo: protoni, neutroni (10-15 m) Elettroni carichi negativamente in una nuvola intorno al nucleo (10-10 m) numero di massa A = 6 p + 6 n = 12 amu 12 C 6 nucleo 14 6C isotopo diametro: m (200 pm) numero atomico Z Tutti gli atomi di un dato elemento hanno lo stesso numero atomico. Gli isotopi sono atomi dello stesso elemento che hanno numero di neutroni diverso e quindi differiscono nel numero di massa.
13 Orbitali Quantomeccanica: descrive le energie degli elettroni e la loro posizione mediante una equazione d onda La funzione d onda è la soluzione dell equazione d onda Ogni funzione d onda è un orbitale, ψ ψ 2 descrive la regione di spazio nel quale un elettrone ha maggiore probabilità di trovarsi La nube elettronica non ha confini, ha solo aree più probabili. 13
14 Forme degli orbitali Gli elettroni sono confinati in regioni di spazio = livelli energetici principali o gusci ogni guscio può contenere 2n 2 elettroni (n = 1, 2, 3, 4..) I gusci sono divisi in sottogusci chiamati orbitali, indicati con le lettere s, p, d,... s (uno per guscio) p (set di tre per il guscio 2 e superiori) d (set of cinque per il guscio 3 e superiori)... 14
15 Gusci e orbitali Ogni orbitale può contenere 2 elettroni 3 guscio capacità: 18 elettroni Energia 2 guscio capacità: 8 elettroni 1 guscio capacità: 2 elettroni 2p 1s 2s 15
16 Riempimento Orbitali Atomici 1. Principio dello Aufbau: gli orbitali si riempiono dal basso in alto (energia crescente: 1s 2s 2p 3s 3p 4s 3d ). 2. Principio di esclusione di Pauli: solo due elettroni per orbitale: spin su e spin giù. 3. Regola di und: per un set di orbitali degeneri, aggiungere un elettrone in ciascuno, appaiati, prima di aggiungerne un secondo. 16
17 Configurazioni elettroniche degli elementi del primo e secondo periodo Elemento e Li Be B C N O F Ne Configurazione 1s 1 1s 2 1s 2 2s 1 = [e]2s 1 1s 2 2s 2 = [e]2s 2 1s 2 2s 2 2p 1 x = [e]2s 2 2p 1 x 1s 2 2s 2 2p x1 2p 1 y = [e]2s 2 2p x1 2p 1 y 1s 2 2s 2 2p x1 2p y1 2p 1 z = [e]2s 2 2p x1 2p y1 2p 1 z 1s 2 2s 2 2p x2 2p y1 2p 1 z = [e]2s 2 2p x2 2p y1 2p 1 z 1s 2 2s 2 2p x2 2p y2 2p 1 z =[e]2s 2 2p x2 2p y2 2p 1 z 1s 2 2s 2 2p x2 2p y2 2p 2 z Elettroni di valenza
18 Elettroni di Valenza Gli elettroni si dividono in elettroni di core e elettroni di valenza. Na 1s 2 2s 2 2p 6 3s 1 core = [Ne] valenza = 3s 1 Br [Ar] 3d 10 4s 2 4p 5 core = [Ar] 3d 10 valenza = 4s 2 4p 5 18
19 Teoria del Legame Gli atomi si legano perché il composto che ne deriva è più stabile degli atomi separati. Il legame è il risultato di un bilanciamento tra forze attrattive (elettroni e nuclei) e repulsive (elettronielettroni e nuclei-nuclei). 19
20 La regola dell Ottetto Gli atomi tendono a guadagnare, perdere, condividere elettroni in modo da essere circondati da otto elettroni di valenza (tranne l idrogeno che ne ha due). 20
21 Polarità del legame Differenza elettronegatività ( X) degli atomi Generalmente: Quando X < 0.5 legame covalente Quando X = legame covalente polare Quando X > 1.9 legame ionico Scala di Pauling elettronegatività crescente elettronegatività crescente 21
22 Tipi di legami chimici Legame ionico: trasferimento di elettroni da un atomo a un altro. Legame covalente: la coppia di elettroni è condivisa da due atomi. legame covalente non polare legame covalente polare legame ionico 22
23 Mappe di potenziale elettrostatico Li F potenziale elettrostatico più negativo rosso < arancio < giallo < verde < blu potenziale elettrostatico più positivo 23
24 Strutture di Lewis Elettroni di legame: i composti organici formano legami che derivano dalla compartecipazione di elettroni. Elettroni di valenza non usati in legami sono chiamati elettroni di non legame o elettroni di lone-pair. densità elettronica bassa densità elettronica alta δ+ δ Cl coppia di legame o condivisa Cl Gilbert N. Lewis ( ) lone pair (LP) coppia di non legame o non condivisa 24
25 Strutture di Lewis Configurazione Elettronica C [e]2s 2 2p 2 N [e]2s 2 2p 3 O [e]2s 2 2p 4 F [e]2s 2 2p 5 Cl [Ne]2s 2 2p 5 Simbolo di Lewis C N O F Cl Valenza 4 elettroni di valenza: 4 legami 5 elettroni di valenza: 3 legami, 1 lone pair 6 elettroni di valenza: 2 legami, 2 lone pair 7 elettroni di valenza: 1 legame, 3 lone pair 7 elettroni di valenza: 1 legame, 3 lone pair 25
26 Disegnare le strutture di Lewis Cl Cl C Cl O Cl C C C CCl 4 C 2 O C 2 2 C O C C C C N C 3 O C 3 CC 2 CN 26
27 Assegnare cariche formali 1. Dividere gli elettroni di ogni legame per due assegnando ciascun elettrone a un atomo. 2. Contare il numero di elettroni posseduto da ciascun atomo paragonandolo con la sua valenza. elettroni in eccesso carica formale negativa elettroni in difetto carica formale positiva 27
28 Esercizio Disegnare le strutture di Lewis, determinare la carica formale su ogni atomo delle seguenti molecole o ioni. 3 O + C 3 O C 3 + CO N 3 28
29 Risposta O O: 6 5=+1 C O C: 4 4=0 O: 6 7= 1 C C: 4 3=+1 C O N N N N N N C: 4 5= 1 O: 6 5=+1 N 1 : 5 5 =0 N 2 : 5 4 =+1 N 3 : 5 7 = 2 N 1 :5 6 = 1 N 2 :5 4 =+1 N 3 : 5 6 = 1 29
30 2 Strutture di Lewis Quando per una molecola o ione è possibile scrivere due o più strutture di Lewis non equivalenti, la migliore (= la più stabile) è quella che ha: il maggior numero di ottetti il minor numero di cariche formali una carica su un atomo più elettronegativo, una carica + su un atomo più elettropositivo minor separazione di carica possibile In ordine decrescente di importanza 30
31 Teoria del legame di Valenza I legami si formano per sovrapposizione di orbitali atomici occupati ciascuno da un elettrone. Gli elettroni sono localizzati e condivisi e attratti da entrambi i nuclei. Maggiore è la sovrapposizione tra gli orbitali, più forte è il legame. 1s A 1s B 31
32 Energia del legame La reazione 2 2 rilascia 436 kj/mol. Il prodotto ha un energia minore dei due atomi di 436 kj/mol: ha una forza di legame di 436 kj/mol. (1 kj = kcal; 1 kcal = kj) Energia kj/mol E rilasciata quando si forma il legame E assorbita quando i legami si rompono 32
33 Lunghezza del legame È la distanza tra i nuclei che porta al massimo della stabilità. Se troppo vicini, si respingono perché entrambi carichi positivamente Se troppo lontani, il legame è debole. Energia (troppo vicini) distanza di legame distanza internucleare (troppo lontani) 33
34 Teoria Orbitale Molecolare Robert Mulliken ( ) Gli elettroni di valenza sono delocalizzati. Gli elettroni di valenza sono in orbitali (chiamati orbitali molecolari) distribuiti sull intera molecola. 34
35 Orbitali Molecolari Descrivono regioni di spazio in una molecola di forma, grandezza e energia specifici Sono formati combinando orbitali atomici quelli che hanno energia minore degli orbitali atomici di partenza sono di legame quelli che hanno energia maggiore sono di antilegame. 35
36 Orbitali Molecolari E n e r g i a orbitale 1s OM antilegante - OM legante - orbitale 1s 36
37 Orbitali Molecolari Terminologia stato fondamentale = a più bassa energia stato eccitato = non a più bassa energia σ = OM sigma legante σ* = OM sigma antilegante π = OM pi legante π* = OM pi antilegante 37
38 Legami σ 1s σ 1s-2p 2p simmetrico rispetto alla rotazione attorno all asse internucleare 2p 2p sovrapposizione coda-coda σ 2p-2p 38
39 Orbitali Molecolari σ 1s E n e r g i a orbitale sigma antilegante (1 nodo) orbitale sigma legante 1s 1s 39
40 Orbitali Molecolari σ 2p 40
41 Legame π 2p 2p sovrapposizione fianco a fianco π 2p-2p non simmetrico rispetto alla rotazione attorno all asse internucleare 41
42 Orbitali molecolari π 42
43 Forma delle molecole Possiamo predire la forma delle molecole semplicemente combinando gli orbitali atomici disponibili su ciascun atomo? No 43
44 Risultati Sperimentali 2 O O = [e]2s 2 2p x2 2p y1 2p z 1 = 1s 1 2 orbitali semivuoti a o O l effettivo angolo -O- (misurato con la diffrazione elettronica) è di o Non c è accordo con il modello atomico! 44
45 Teoria VSEPR Gli elettroni di valenza possono formare legami singoli, doppi, tripli o restare non condivisi. In ogni caso le regioni di densità elettronica attorno al nucleo devono stare il più distanti possibili per minimizzare le repulsioni. La necessità di minimizzare le repulsioni determina la geometria della molecola. 45
46 Geometria delle Molecole Geometria 4 regioni di densità elettronica attorno all atomo 3 regioni di densità elettronica attorno all atomo 2 regioni di densità elettronica attorno all atomo TETRAEDRICA TRIGONALE PLANARE LINEARE 46
47 Geometria tetraedrica 4 linee che si irradiano da un atomo centrale formando angoli uguali descrivono un tetraedro. Gli angoli sono di ' atomo centrale ' 47
48 L atomo centrale può essere C, N, O, etc. C N O C tetraedrico La repulsione tra coppia di legame e lone pair è maggiore della repulsione tra coppie di legame e quindi l angolo aumenta. La repulsione tra lone pairs è ancora maggiore. 48
49 Variazioni sul tetraedrico Tetraedrico Piramidale C.. N Angolare O.... In chimica generale si fanno delle distinzioni. Sebbene le molecole abbiano forme differenti, gli orbitali usano un arrangiamento tetraedrico (coppie incluse) 49
50 Repulsioni steriche C 3 I gruppi C 3 sono più voluminosi degli, si respingono allargando l angolo C C 3 C o C C 106 o 3 50
51 Elementi del 3 periodo non hanno tendenza a diventare tetraedrici.. N repulsioni maggiori.. 2 PERIODO.. P.. 3 PERIODO repulsioni minori: gli elettroni sono più diffusi e più lontani dal nucleo. P 93 o N 107 o La coppia non condivisa sul P occupa molto più spazio di quella dell azoto 51
52 Geometria trigonale planare 3 linee che si irradiano da un atomo centrale descrivono un triangolo equilatero, con angoli di
53 Atomi trigonali planari C.. N C + + N.. O + 53
54 Geometria lineare 2linee che si irradiano da un atomo formando angoli uguali, stanno su una retta, con angoli di C C N.. 54
55 In qual modo la molecola acquisisce la geometria osservata? IBRIDAZIONE 55
56 Orbitali ibridi Gli orbitali ibridi, che sono un astrazione, consentono di prevedere correttamente la forma della molecola. Tre sono i tipi di orbitali ibridi: sp 3 (1 orbitale s + 3 orbitali p) sp 2 (1 orbitale s + 2 orbitali p) sp (1 orbitale s + 1 orbitale p) 56
57 Metano C 4 Sperimentalmente: 4 legami σ C- a 109 Per formare 4 legami σ C- a 109 bisogna usare 4 orbitali atomici del carbonio s, p x,p y, ep z e costruire 4 nuovi orbitali equivalenti che puntino nella corretta direzione. I 4 orbitali ibridizzano a dare 4 orbitali atomici ibridi equivalenti sp 3. 57
58 C 2s 2p 4 orbitali atomici promozione elettrone Ibridazione sp 3 2s 2p ibridazione L energia degli orbitali ibridi è intermedia fra le energie degli orbitali s e p di cui sono formati. 4 orbitali atomici ibridi sp 3 orbitali sp 3 C C sp 3 tetraedrico 4 C sovrapposizione orbitali sp 3 e 1s orbitali 1s σ(sp 3 C +1s ) i legami C sono legami σ 58
59 Ibridazione sp 3 2p z 4 sp 3 2p y 2p x 4 orbitali atomici 4 orbitali ibridi 2s, 2p x,2p y,2p z sp 3 tetraedro 59
60 3 e val Atomi diversi dal C 6C 2s 7N 2s 8O 2s 2p 4 orbitali atomici 2p 2p promozione elettrone promozione elettrone promozione elettrone 2s 2s 2s 2p 2p 2p ibridazione ibridazione ibridazione 4 orbitali atomici ibridi sp 3 4 orbitali atomici ibridi sp 3 4 orbitali atomici ibridi sp 3 60
61 Confronto C N lone pairs O in OA sp 3 C C C N C O σ(sp 3 C+sp 3 C) σ(sp 3 C+sp 3 N) σ(sp 3 C+sp 3 O) 61
62 Struttura dell etano C 3 C 3 C sp 3 C sp 3 legame σ sp 3 C+ sp 3 C C 3 C 3 62
63 Disegnare un atomo tetraedrico linee continue nel piano linea a cuneo tratteggiata dietro il piano del foglio C linea a cuneo davanti il piano del foglio (verso l osservatore) 63
64 Etilene C 2 = C 2 Sperimentalmente: tutti e 6 gli atomi in un piano angoli di 120 Per formare 3 legami σ C- a 120 bisogna usare 3 dei 4 OA del carbonio s, p x,p y, e p z e costruire 3 nuovi orbitali equivalenti C C L orbitale 2p non ibridizzato è perpendicolare al piano degli orbitali sp 2 64
65 Ibridazione sp 2 del carbonio promozione C 2p elettrone 2p 2s 2s 2p ibridazione π 3 orbitali atomici ibridi sp 2 2p C C σ(sp 2 C +1s ) σ(sp 2 C + sp 2 C) sovrapposizione orbitali 2p C C tutti gli atomi coplanari sovrapposizione orbitali p = C C doppio legame = 1σ + 1π 133 pm 65
66 Ibridazione sp 2 del carbonio 2p z 90 3 sp p x 2p y 4 orbitali atomici 2s, 2p x,2p y,2p z 3 orbitali ibridi sp 2 1 orbitale atomico 2p trigonale planare 66
67 Etilene orbitali 2p legame π legame σ orbitali sp 2 legame p C sp 2 C sp 2 doppio legame C=C 67
68 Legame π visto dall alto 68
69 Ossigeno sp 2 C 2 O formaldeide O C O C O π lone pairs in OA sp 2 tutti gli atomi coplanari sovrapposizione orbitali p σ(sp 2 C + sp 2 O)+π 69
70 Acetilene C 2 2 Sperimentalmente: La molecola è lineare Gli angoli sono di 180 Per formare 2 legami σ C- a 180 bisogna usare 2 dei 4 orbitali atomici del carbonio s,p x,p y, e p z ecostruire 2 nuovi orbitali equivalenti. C C Gli orbitali 2p non ibridizzati sono perpendicolari tra loro. 70
71 C sp promozione C 2p elettrone 2p 2s 2s ibridazione 2 orbitali atomici ibridi sp 2p 2p 2 legami π C C C C = C C σ (sp C +1s ) σ (sp C + sp C ) triplo legame = 1 legame σ + 2 legami π 120 pm 71
72 Ibridazione sp orbitali non ibridizzati 2p y 2p z 2p z z 2 sp y + 2p z x 2p y 2p x 2p y orbitali ibridi sp 4 orbitali atomici 2s, 2p x,2p y,2p z 2 orbitali ibridi sp 2 2 orbitali atomici 2p lineare 72
73 Acetilene π py py π pz pz legame σ sp-s legame σ sp-sp 73
74 Azoto sp -C N N 2p 2 legami π C N C C = C N σ(sp C + sp N )+2π lone pair in OA sp 74
75 Gli orbitali ibridi: un ipotetico stadio intermedio nel processo di formazione dei legami orbitali atomici 2s, 2p x,2p y,2p z orbitali atomici ibridi sp 3, sp 2,sp orbitali molecolari σ, π, n processo di formazione dei legami le sovrapposizioni tra gli orbitali ibridi degli atomi porta ai legami finali nella molecola che sono rappresentati dagli orbitali molecolari 75
76 Perché si formano gli ibridi? 1. Vengono minimizzate le repulsioni tra le minore coppie energia 2. Si formano legami più forti minore energia 3. Gli ibridi hanno migliore direzionalità per formare legami 4. Poiché di solito si verifica una promozione di almeno un elettrone, gli ibridi dispongono di un maggior numero di legami minore energia 76
77 UNITÀ DI LEGAME Gli atomi partecipano alla formazione delle molecole secondo pattern ben definiti 77
78 Unità di legame di Lewis per i più comuni elementi I III IV V VI VII B C N:.. O.... F :.. Al C Ṅ... O.... :Cl.. C N:.. S.... : Br.. monovalente trivalente C tetravalente.. P: Ṣ. :.... I trivalente bivalente monovalente 78
79 Comuni unità di legame di Lewis con carica Quando gli atomi hanno un numero di legami diverso dalla loro valenza avranno una carica + C + O : N + CATIONI + Ọ. N + N + B - C: - ANIONI Ȯ... :- Il tipo di carica dipenderà dal confronto tra elettroni posseduti e elettroni di valenza dell atomo... - Ṇ. Ṅ
80 Strutture con l ottetto incompleto Gli elementi del terzo gruppo possono formare strutture stabili con l ottetto incompleto. Il Boro ha 3 elettroni di valenza e quindi può formare solo 3 legami... B. BF 3 = F B F F trigonale planare 120 o 80
81 Promozione Quando formano legami covalenti, tutti gli elementi dei gruppi 2A, 3A, 4A promuovono un elettrone al livello superiore in modo da poter formare un maggior numero di legami GUSCI DI VALENZA 2A 3A 4A Be B C Be B C simboli di Lewis Be 4 1s 2 2s 2 [1s 2 ]2s 2 [e]2s 1 2p 1 x B 5 1s 2 2s 2 2p 1 [1s 2 ]2s 2 2p 1 x [e]2s 1 2p x1 2p 1 y C 6 1s 2 2s 2 2p 2 [1s 2 ]2s 2 2p x1 2p 1 y [e]2s 1 2p x1 2p y1 2p 1 z 81
82 Strutture con l ottetto incompleto 120 o + C carbocatione Non è una molecola stabile, è uno ione intermedio - reagisce velocemente 82
83 Strutture con l ottetto espanso Sempre con lo scopo di formare il maggior numero possibile di legami elementi dei gruppi 5A e 6A possono espandere l ottetto Il Fosforo può formare fino a 5 legami P Lo Zolfo può formare fino a 6 legami S PCl 5 = Cl P Cl SF = 6 S F F F Cl Cl S 15 [Ne]3s 2 3p x 1 3p y 1 [Ne]3s 1 3p x 1 3p y 1 3p z 1 3d 1 3d 1 F F F Cl GRUPPO 5A GRUPPO 6A Sono disponibili gli orbitali 3d 83
84 Domanda. Quale è l ibridazione degli atomi indicati? C 3 O C C O 17-etinilestradiolo ( La Pillola ) 84
85 Risposta sp 3 sp 3 C 3 O C C sp O sp 2 sp 3 17-etinilestradiolo ( La Pillola ) 85
86 Appendice 86
87 Paragone degli orbitali ibridi sp x maggiore coda carattere p sp 3 sp 2 sp Per evitare confusione il lobo posteriore è di solito omesso nelle rappresentazioni e il lobo anteriore viene elongato per mostrare la sua direzione omesso carattere s maggiore densità elettronica nel lobo legante 87
88 Comuni Legami σ σ 1s 1s σ 2p 1s σ 2p 2p σ sp 3 1s σ sp 3 sp 3 88
89 Comuni Legami π π 2p 2p sovrapposizione fianco-a-fianco π 2p 3d 89
90 Forza dei legami C- legame C- tipo Lunghezza Å Energia Kcal KJ Molecola misurata [C 2 ] 2p-1s C sp 3-1s C 3 C 3 C= sp 2-1s C 2 =C 2 C sp-1s C C carattere s più corto più s = più corto 90 = più forte
91 Forza dei legami singoli C C legame C-C tipo Lunghezza Å Energia Kcal KJ Molecola misurata C C sp 3 -sp C 3 C 3 C C= sp 3 -sp C 3 C=C 2 C C sp 3 -sp C 3 C C carattere s più corto Legami σ tipici hanno energie di circa kcal/mole 91
92 Forza dei legami multipli C C legame tipo Lunghezza Å Energia Kcal KJ Molecola misurata C C sp 3 -sp C 3 C 3 C=C sp 2 -sp C 2 =C 2 C C sp - sp C C carattere s più corto Legami π tipici hanno energie di circa kcal/mole 92
93 93 Energie medie di legame per legami singoli (Kcal/mole) I 36 Br - 46 Cl S Si F O N C I Br Cl S Si F O N C
Definizioni. Vecchia: derivata da organismi viventi Nuova: la chimica dei composti del carbonio Da inorganico a organico, Wöhler, 1828
 CHIMICA ORGANICA 4 Definizioni Vecchia: derivata da organismi viventi Nuova: la chimica dei composti del carbonio Da inorganico a organico, Wöhler, 828 + - NH 4 OCN ammonio cianato calore O H 2 N C NH
CHIMICA ORGANICA 4 Definizioni Vecchia: derivata da organismi viventi Nuova: la chimica dei composti del carbonio Da inorganico a organico, Wöhler, 828 + - NH 4 OCN ammonio cianato calore O H 2 N C NH
Il Legame Chimico e la Struttura Molecolare
 2017 1 Il Legame Chimico e la Struttura Molecolare LEGAME CIMICO 2 In che modo gli atomi in una molecola o uno ione poliatomico interagiscono?! Perchè alcune molecole sono planari ed altre non lo sono?!
2017 1 Il Legame Chimico e la Struttura Molecolare LEGAME CIMICO 2 In che modo gli atomi in una molecola o uno ione poliatomico interagiscono?! Perchè alcune molecole sono planari ed altre non lo sono?!
Il Legame Chimico e la Struttura Molecolare
 A.A.2016 2017 CCS-Biologia CCS-Scienze Geologiche 1 Il Legame Chimico e la Struttura Molecolare Energia di interazione di due atomi di idrogeno Cap 8. 1-7, 9, 10(a/b), 17-20, 27-28, 31-33, 37-40, 52, 93-96
A.A.2016 2017 CCS-Biologia CCS-Scienze Geologiche 1 Il Legame Chimico e la Struttura Molecolare Energia di interazione di due atomi di idrogeno Cap 8. 1-7, 9, 10(a/b), 17-20, 27-28, 31-33, 37-40, 52, 93-96
Il legame chimico ATOMI MOLECOLE
 Il legame chimico Gli atomi tendono a combinarsi con altri atomi per dare un sistema finale più stabile di quello iniziale (a minor contenuto di energia). ATOMI MOLECOLE 1 Stati repulsivi di non legame
Il legame chimico Gli atomi tendono a combinarsi con altri atomi per dare un sistema finale più stabile di quello iniziale (a minor contenuto di energia). ATOMI MOLECOLE 1 Stati repulsivi di non legame
Il Legame Chimico e la Struttura Molecolare
 A.A.2016 2017 CCS-Biologia CCS-Scienze Geologiche 1 Il Legame Chimico e la Struttura Molecolare Energia di interazione di due atomi di idrogeno Cap 8. 1-7, 9, 10(a/b), 17-20, 27-28, 31-33, 37-40, 52, 93-96
A.A.2016 2017 CCS-Biologia CCS-Scienze Geologiche 1 Il Legame Chimico e la Struttura Molecolare Energia di interazione di due atomi di idrogeno Cap 8. 1-7, 9, 10(a/b), 17-20, 27-28, 31-33, 37-40, 52, 93-96
Il legame chimico II: la geometria molecolare e l ibridizzazione degli orbitali atomici. Capitolo 10
 Il legame chimico II: la geometria molecolare e l ibridizzazione degli orbitali atomici Capitolo 10 Legame tra un derivato del Buckyball e il sito dell HIV-Protease Repulsione delle coppie di elettroni
Il legame chimico II: la geometria molecolare e l ibridizzazione degli orbitali atomici Capitolo 10 Legame tra un derivato del Buckyball e il sito dell HIV-Protease Repulsione delle coppie di elettroni
STRUTTURA ATOMICA. tutti gli atomi hanno un nucleo carico positivamente che possiede quasi tutta la massa atomica
 STRUTTURA ATOMICA tutti gli atomi hanno un nucleo carico positivamente che possiede quasi tutta la massa atomica il nucleo è composto da protoni e neutroni che hanno massa = 1 nella scala dei pesi atomici
STRUTTURA ATOMICA tutti gli atomi hanno un nucleo carico positivamente che possiede quasi tutta la massa atomica il nucleo è composto da protoni e neutroni che hanno massa = 1 nella scala dei pesi atomici
CORSO DI LAUREA IN BIOTECNOLOGIE CHIMICA ORGANICA. - Brown, Poon, INTRODUZIONE ALLA CHIMICA ORGANICA, EdiSES
 CORSO DI LAUREA IN BIOTECNOLOGIE CHIMICA ORGANICA TESTI: - John McMurry, CHIMICA ORGANICA, PICCIN - Brown, Poon, INTRODUZIONE ALLA CHIMICA ORGANICA, EdiSES - Janice Gorzynski Smith, FONDAMENTI DI CHIMICA
CORSO DI LAUREA IN BIOTECNOLOGIE CHIMICA ORGANICA TESTI: - John McMurry, CHIMICA ORGANICA, PICCIN - Brown, Poon, INTRODUZIONE ALLA CHIMICA ORGANICA, EdiSES - Janice Gorzynski Smith, FONDAMENTI DI CHIMICA
06/03/2012. Elementi in chimica organica
 CORSO DI LAUREA IN BIOINFORMATICA CHIMICA ORGANICA E DELLE MACROMOLECOLE BIOLOGICHE MICHAEL ASSFALG Lezione: 6 CFU = 48 ORE Lun 14:30-16:30, 16:30, Mer 8:30-10:30 PROVA FINALE: SCRITTO (+ ORALE) TESTI:
CORSO DI LAUREA IN BIOINFORMATICA CHIMICA ORGANICA E DELLE MACROMOLECOLE BIOLOGICHE MICHAEL ASSFALG Lezione: 6 CFU = 48 ORE Lun 14:30-16:30, 16:30, Mer 8:30-10:30 PROVA FINALE: SCRITTO (+ ORALE) TESTI:
CHIMICA II (CHIMICA ORGANICA)
 CHIMICA II (CHIMICA ORGANICA) Prof. Gennaro Piccialli Prof. Aldo Galeone Prof. Giorgia Oliviero Testo Consigliato: gruppo 1 (matricole A-E) gruppo 2 (matricole F-O) gruppo 3 (matricole P-Z) Introduzione
CHIMICA II (CHIMICA ORGANICA) Prof. Gennaro Piccialli Prof. Aldo Galeone Prof. Giorgia Oliviero Testo Consigliato: gruppo 1 (matricole A-E) gruppo 2 (matricole F-O) gruppo 3 (matricole P-Z) Introduzione
CHIMICA ORGANICA (CANALE M-Z)
 CHIMICA ORGANICA (CANALE M-Z) Durata corso (8 marzo-10 maggio) + settimana recupero Orario lezioni Esercitazioni Modalità d esame Esoneri Libri di testo Ricevimento studenti e-mail/telefono docente: Michela.Salamone@uniroma2.it
CHIMICA ORGANICA (CANALE M-Z) Durata corso (8 marzo-10 maggio) + settimana recupero Orario lezioni Esercitazioni Modalità d esame Esoneri Libri di testo Ricevimento studenti e-mail/telefono docente: Michela.Salamone@uniroma2.it
Fondamenti di chimica organica Janice Gorzynski Smith Copyright 2009 The McGraw Hill Companies srl
 Soluzioni ai problemi proposti nel libro Capitolo 1 1.1 Il numero di massa è il numero dei protoni e dei neutroni. Il numero atomico è il numero dei protoni ed è identico per tutti gli isotopi. a. Numero
Soluzioni ai problemi proposti nel libro Capitolo 1 1.1 Il numero di massa è il numero dei protoni e dei neutroni. Il numero atomico è il numero dei protoni ed è identico per tutti gli isotopi. a. Numero
CORSO DI CHIMICA ORGANICA. Testo consigliato: Chimica Organica H.Hart,D.J.Hart, L.E.Craine Zanichelli
 CORSO DI CIMICA ORGANICA Testo consigliato: Chimica Organica.art,D.J.art, L.E.Craine Zanichelli Nucleo contenente neutroni e protoni 10-2 m Spazio extranucleare contenente elettroni NUMERO ATOMICO: numero
CORSO DI CIMICA ORGANICA Testo consigliato: Chimica Organica.art,D.J.art, L.E.Craine Zanichelli Nucleo contenente neutroni e protoni 10-2 m Spazio extranucleare contenente elettroni NUMERO ATOMICO: numero
I legami covalenti eteronucleari spostano la carica del legame sull atomo più elettronegativo
 La polarità I legami covalenti eteronucleari spostano la carica del legame sull atomo più elettronegativo L elettronegatività è il parametro di riferimento utilizzato per valutare il trasferimento di carica
La polarità I legami covalenti eteronucleari spostano la carica del legame sull atomo più elettronegativo L elettronegatività è il parametro di riferimento utilizzato per valutare il trasferimento di carica
CHIMICA ORGANICA (CANALE M-Z)
 CHIMICA ORGANICA (CANALE M-Z) Durata corso (1 ottobre-21 dicembre 2018) Orario lezioni (mar 11-13, mer 9-11, ven 11-13) Esercitazioni (1 CFU, 12 ore) Chimica Generale Modalità d esame: semplice test scritto
CHIMICA ORGANICA (CANALE M-Z) Durata corso (1 ottobre-21 dicembre 2018) Orario lezioni (mar 11-13, mer 9-11, ven 11-13) Esercitazioni (1 CFU, 12 ore) Chimica Generale Modalità d esame: semplice test scritto
Elementi di Chimica Organica
 CORSO DI LAUREA IN BIOINFORMATICA Elementi di Chimica Organica Mariapina D Onofrio (mariapina.donofrio@univr.it) Orario ricevimento: mar e giov 11:30-13:30 Corso: 6 CFU = 48 ORE Lezioni: Mar 8:30-10:30,
CORSO DI LAUREA IN BIOINFORMATICA Elementi di Chimica Organica Mariapina D Onofrio (mariapina.donofrio@univr.it) Orario ricevimento: mar e giov 11:30-13:30 Corso: 6 CFU = 48 ORE Lezioni: Mar 8:30-10:30,
un legame covalente due legami covalenti? tre legami covalenti due legami covalenti un legame covalente
 e C N un legame covalente due legami covalenti? tre legami covalenti O F Ne 1s 2s 2p due legami covalenti un legame covalente C 1s 2s 2p ibridazione quattro legami covalenti Cariche Formali Usando le strutture
e C N un legame covalente due legami covalenti? tre legami covalenti O F Ne 1s 2s 2p due legami covalenti un legame covalente C 1s 2s 2p ibridazione quattro legami covalenti Cariche Formali Usando le strutture
Esercizi sulle Geometrie Molecolari
 Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Esercizi sulle Geometrie Molecolari Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio/education/general-chemistry-exercises/
Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Esercizi sulle Geometrie Molecolari Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio/education/general-chemistry-exercises/
Forme molecolari - Teoria VSEPR Teoria della repulsione dei doppietti elettronici di valenza
 Lezione 8 1. Teoria VSEPR 2. Il legame chimico 3. Legame covalente - Valence Bond 4. Legami e 5. Sovrapposizione di orbitali atomici 6. Intro IBRIDAZIONE Forme molecolari - Teoria VSEPR Teoria della repulsione
Lezione 8 1. Teoria VSEPR 2. Il legame chimico 3. Legame covalente - Valence Bond 4. Legami e 5. Sovrapposizione di orbitali atomici 6. Intro IBRIDAZIONE Forme molecolari - Teoria VSEPR Teoria della repulsione
Perché H 2 e non H? He e non He 2? H 2 O e non H 3 O?
 IL LEGAME CHIMICO Perché H 2 e non H? He e non He 2? H 2 O e non H 3 O? Configurazione degli elettroni diversa ed energeticamente più favorevole di quella degli atomi isolati? Ionico (trasferimento di
IL LEGAME CHIMICO Perché H 2 e non H? He e non He 2? H 2 O e non H 3 O? Configurazione degli elettroni diversa ed energeticamente più favorevole di quella degli atomi isolati? Ionico (trasferimento di
IL LEGAME COVALENTE SECONDO LA MECCANICA ONDULATORIA L
 IL LEGAME COVALENTE SECONDO LA MECCANICA ONDULATORIA L elettrone è dissolto in una nube di carica, ovvero il concetto di orbitale sostituisce il di Lewis LEGAME DI VALENZA (VB) Sviluppo quantomeccanico
IL LEGAME COVALENTE SECONDO LA MECCANICA ONDULATORIA L elettrone è dissolto in una nube di carica, ovvero il concetto di orbitale sostituisce il di Lewis LEGAME DI VALENZA (VB) Sviluppo quantomeccanico
ORBITALE ATOMICO. Forma
 L ATOMO ORBITALE ATOMICO n (numero quantico principale) Energia e Dimensione l (numero quantico azimutale) Forma m l (numero quantico magnetico) Orientazione nello spazio l dipende da n assume n valori:
L ATOMO ORBITALE ATOMICO n (numero quantico principale) Energia e Dimensione l (numero quantico azimutale) Forma m l (numero quantico magnetico) Orientazione nello spazio l dipende da n assume n valori:
Il legame chimico. Legame metallico
 Il legame chimico Legame ionico: un atomo cede elettroni e un altro li acquista con formazione di ioni di carica opposta che vengono tenuti insieme da forze elettrostatiche. Legame covalente: si realizza
Il legame chimico Legame ionico: un atomo cede elettroni e un altro li acquista con formazione di ioni di carica opposta che vengono tenuti insieme da forze elettrostatiche. Legame covalente: si realizza
DEL LEGAME DI VALENZA
 Chimica Silvia LICOCCIA Professore Ordinario di Fondamenti Chimici per le Tecnologie Dipartimento di Scienze e Tecnologie Chimiche Università di Roma Tor Vergata TEORIA DEL LEGAME DI VALENZA Teoria del
Chimica Silvia LICOCCIA Professore Ordinario di Fondamenti Chimici per le Tecnologie Dipartimento di Scienze e Tecnologie Chimiche Università di Roma Tor Vergata TEORIA DEL LEGAME DI VALENZA Teoria del
IBRIDAZIONE e GEOMETRIA MOLECOLARE
 IBRIDAZIONE e GEOMETRIA MOLECOLARE Esempio: struttura della molecola del metano CH 4 1s 2s 2p Configurazione elettronica del C Per esempio il carbonio può utilizzare la configurazione in cui un elettrone
IBRIDAZIONE e GEOMETRIA MOLECOLARE Esempio: struttura della molecola del metano CH 4 1s 2s 2p Configurazione elettronica del C Per esempio il carbonio può utilizzare la configurazione in cui un elettrone
Il legame covalente , P 4 , O 3 , N 2
 Il legame covalente Nel legame covalente gli elettroni responsabili del legame sono condivisi tra i due atomi legati: essi percorrono nel tempo lo spazio intorno a entrambi gli atomi, nonché la regione
Il legame covalente Nel legame covalente gli elettroni responsabili del legame sono condivisi tra i due atomi legati: essi percorrono nel tempo lo spazio intorno a entrambi gli atomi, nonché la regione
IL LEGAME CHIMICO. Per descrivere come gli elettroni si distribuiscono nell atomo attorno al nucleo si può far riferimento al MODELLO A GUSCI
 IL LEGAME CIMICO Come dagli atomi si costruiscono le molecole 02/19/08 0959 PM 1 Per descrivere come gli elettroni si distribuiscono nell atomo attorno al nucleo si può far riferimento al MODELLO A GUSCI
IL LEGAME CIMICO Come dagli atomi si costruiscono le molecole 02/19/08 0959 PM 1 Per descrivere come gli elettroni si distribuiscono nell atomo attorno al nucleo si può far riferimento al MODELLO A GUSCI
La struttura di ioni e molecole
 La struttura di ioni e molecole Inizialmente: consideriamo atomi che non danno espansione dell ottetto e non ci interessiamo della geometria delle molecole Alcune regole per individuare la posizione degli
La struttura di ioni e molecole Inizialmente: consideriamo atomi che non danno espansione dell ottetto e non ci interessiamo della geometria delle molecole Alcune regole per individuare la posizione degli
La Teoria del Legame di Valenza
 La Teoria del Legame di Valenza Un legame covalente tra due atomi A e B viene spiegato in termini di sovrapposizione tra due orbitali atomici appartenenti ai due atomi e descrittivi dei due elettroni di
La Teoria del Legame di Valenza Un legame covalente tra due atomi A e B viene spiegato in termini di sovrapposizione tra due orbitali atomici appartenenti ai due atomi e descrittivi dei due elettroni di
STRUTTURA DEGLI OSSIACIDI
 Chimica Silvia LICOCCIA Professore Ordinario di Fondamenti Chimici per le Tecnologie Dipartimento di Scienze e Tecnologie Chimiche Università di Roma Tor Vergata STRUTTURA DEGLI OSSIACIDI Orbitali ibridi
Chimica Silvia LICOCCIA Professore Ordinario di Fondamenti Chimici per le Tecnologie Dipartimento di Scienze e Tecnologie Chimiche Università di Roma Tor Vergata STRUTTURA DEGLI OSSIACIDI Orbitali ibridi
Premessa al legame chimico
 Premessa al legame chimico La tendenza di due o più atomi a legarsi spontaneamente fra loro formando legami chimici è un aspetto della tendenza di ogni sistema a diminuire il proprio contenuto di energia.
Premessa al legame chimico La tendenza di due o più atomi a legarsi spontaneamente fra loro formando legami chimici è un aspetto della tendenza di ogni sistema a diminuire il proprio contenuto di energia.
Sommario delle lezioni Legami chimici
 Sommario delle lezioni 8 9-10 Legami chimici Legami chimici Complessità molecolare I legami chimici possono portare alla formazione di molecole particolarmente complesse Acqua Glucosio Emoglobina H 2
Sommario delle lezioni 8 9-10 Legami chimici Legami chimici Complessità molecolare I legami chimici possono portare alla formazione di molecole particolarmente complesse Acqua Glucosio Emoglobina H 2
TEORIA DEL LEGAME DI VALENZA
 TERIA DEL LEGAME DI VALENZA ( Strutture di LEWIS ) Tutti gli atomi tendono ad acquisire la struttura elettronica dei gas nobili Il tipo di legame è correlato alla elettronegatività degli atomi che si legano
TERIA DEL LEGAME DI VALENZA ( Strutture di LEWIS ) Tutti gli atomi tendono ad acquisire la struttura elettronica dei gas nobili Il tipo di legame è correlato alla elettronegatività degli atomi che si legano
Formule di Lewis e regola dell ottetto
 Formule di Lewis e regola dell ottetto 1916-1919 Lewis si accorse che: Qualcosa di unico nelle configurazioni elettroniche dei gas nobili è responsabile della loro inerzia; gli atomi degli altri elementi
Formule di Lewis e regola dell ottetto 1916-1919 Lewis si accorse che: Qualcosa di unico nelle configurazioni elettroniche dei gas nobili è responsabile della loro inerzia; gli atomi degli altri elementi
IBRIDAZIONE. MODELLO DELL ORBITALE di LEGAME
 IBRIDAZIONE MODELLO DELL ORBITALE di LEGAME Approccio più semplice per descrivere la struttura elettronica di una specie sfruttando il concetto di orbitale. METANO Gli atomi nel formare legami usano elettroni
IBRIDAZIONE MODELLO DELL ORBITALE di LEGAME Approccio più semplice per descrivere la struttura elettronica di una specie sfruttando il concetto di orbitale. METANO Gli atomi nel formare legami usano elettroni
LEGAMI CHIMICI e GEOMETRIA MOLECOLARE
 DAI LEGAMI CH HIMICI ALLA GEOMETRIA DELLE MOLECOLE. LEGAMI CHIMICI e GEOMETRIA MOLECOLARE Cos è un legame chimico? Il legame chimico non esiste Quanti tipi di legame? Legame ionico Legame covalente LEGAME
DAI LEGAMI CH HIMICI ALLA GEOMETRIA DELLE MOLECOLE. LEGAMI CHIMICI e GEOMETRIA MOLECOLARE Cos è un legame chimico? Il legame chimico non esiste Quanti tipi di legame? Legame ionico Legame covalente LEGAME
Legame e struttura molecolare
 2016 2017 CCS Biologia CCS-Scienze Geologiche 1 Legame e struttura molecolare Orbitali atomici Molecole Cap 9. 1-3, 15-16, 18, 21-23, 40 CONSIDERAZIONI PRELIMINARI 2 Le strutture di Lewis e la teoria VSEPR
2016 2017 CCS Biologia CCS-Scienze Geologiche 1 Legame e struttura molecolare Orbitali atomici Molecole Cap 9. 1-3, 15-16, 18, 21-23, 40 CONSIDERAZIONI PRELIMINARI 2 Le strutture di Lewis e la teoria VSEPR
GEOMETRIA MOLECOLARE. Ibridazione La teoria VSEPR
 GEOMETRIA MOLECOLARE Ibridazione La teoria VSEPR 1 Ibridazione e geometria molecolare Teoria di Lewis e VB vista finora non sono in grado di descrivere correttamente la geometria di molte molecole anche
GEOMETRIA MOLECOLARE Ibridazione La teoria VSEPR 1 Ibridazione e geometria molecolare Teoria di Lewis e VB vista finora non sono in grado di descrivere correttamente la geometria di molte molecole anche
CHIMICA ORGANICA = STUDIO DEI COMPOSTI DEL CARBONIO. energia superiore. energia inferiore. orbitale s
 CIMICA ORGANICA = STUDIO DEI COMPOSTI DEL CARBONIO C elemento del secondo periodo della tavola periodica; numero atomico = 6 configurazione elettronica del C 2p 2s 1s energia superiore energia inferiore
CIMICA ORGANICA = STUDIO DEI COMPOSTI DEL CARBONIO C elemento del secondo periodo della tavola periodica; numero atomico = 6 configurazione elettronica del C 2p 2s 1s energia superiore energia inferiore
Legame covalente polare
 Legame covalente polare Nel caso di legame covalente omeopolare (H 2 o Cl 2 ) gli elettroni di legame sono equamente condivisi. Quando invece il legame è covalente eteropolare (HCl) gli elettroni di legame
Legame covalente polare Nel caso di legame covalente omeopolare (H 2 o Cl 2 ) gli elettroni di legame sono equamente condivisi. Quando invece il legame è covalente eteropolare (HCl) gli elettroni di legame
Teoria VSEPR Geometria molecolare
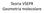 Teoria VSEPR Geometria molecolare la teoria VSEPR la forma delle molecole Massima distanza possibile! Teoria della repulsione delle coppie di elettroni di valenza VSEPR Struttura delle molecole Le regioni
Teoria VSEPR Geometria molecolare la teoria VSEPR la forma delle molecole Massima distanza possibile! Teoria della repulsione delle coppie di elettroni di valenza VSEPR Struttura delle molecole Le regioni
CHIMICA ORGANICA PER BIOTECNOLOGIE con esercitazioni di LABORATORIO D. Savoia
 CHIMICA RGANICA PER BITECNLGIE con esercitazioni di LABRATRI D. Savoia Brown, Poon - Introduzione alla Chimica rganica Brown, Foote - Chimica rganica Bruyce - Chimica rganica Solomons McMurray Etc Cos
CHIMICA RGANICA PER BITECNLGIE con esercitazioni di LABRATRI D. Savoia Brown, Poon - Introduzione alla Chimica rganica Brown, Foote - Chimica rganica Bruyce - Chimica rganica Solomons McMurray Etc Cos
1.039 g g/mol g g/mol
 Un campione di un liquido di massa 0.5438 g, formato da C, H e O, viene bruciato in ossigeno puro. Si ottengono 1.039 g di CO 2 ed 0.6369 g di H 2 O. Determinare la formula chimica (molecolare) Se X(C,H,O)
Un campione di un liquido di massa 0.5438 g, formato da C, H e O, viene bruciato in ossigeno puro. Si ottengono 1.039 g di CO 2 ed 0.6369 g di H 2 O. Determinare la formula chimica (molecolare) Se X(C,H,O)
Geometria molecolare
 Geometria molecolare Le molecole possono essere rappresentate disponendo gli atomi in posizioni definite nello spazio in modo da costruire una figura geometrica Il modo più semplice per assegnare la geometria
Geometria molecolare Le molecole possono essere rappresentate disponendo gli atomi in posizioni definite nello spazio in modo da costruire una figura geometrica Il modo più semplice per assegnare la geometria
ALTRI TIPI DI IBRIDAZIONE. Trigonale bipiramidale 1(s)+3(p)+1(d)d5(sp 3 d) P [Ne] 3s 2 3p 3 d[ne]3s 1 3p 3 3d 1 (Es. PCl 5 )
![ALTRI TIPI DI IBRIDAZIONE. Trigonale bipiramidale 1(s)+3(p)+1(d)d5(sp 3 d) P [Ne] 3s 2 3p 3 d[ne]3s 1 3p 3 3d 1 (Es. PCl 5 ) ALTRI TIPI DI IBRIDAZIONE. Trigonale bipiramidale 1(s)+3(p)+1(d)d5(sp 3 d) P [Ne] 3s 2 3p 3 d[ne]3s 1 3p 3 3d 1 (Es. PCl 5 )](/thumbs/85/92177402.jpg) ALTRI TIPI DI IBRIDAZIONE Trigonale bipiramidale 1(s)+3(p)+1(d)d5(sp 3 d) P [Ne] 3s 2 3p 3 d[ne]3s 1 3p 3 3d 1 (Es. PCl 5 ) Ottaedrica 1(s)+3(p)+2(d)d6(sp 3 d 2 ) S [Ne]3s 2 3p 4 d[ne] 3s 1 3p 3 3d 2 (Es.
ALTRI TIPI DI IBRIDAZIONE Trigonale bipiramidale 1(s)+3(p)+1(d)d5(sp 3 d) P [Ne] 3s 2 3p 3 d[ne]3s 1 3p 3 3d 1 (Es. PCl 5 ) Ottaedrica 1(s)+3(p)+2(d)d6(sp 3 d 2 ) S [Ne]3s 2 3p 4 d[ne] 3s 1 3p 3 3d 2 (Es.
Teorie del legame chimico. Teorie del legame chimico
 Teorie del legame chimico Le teorie proposte per la trattazione del legame chimico si prefiggono i seguenti scopi: 1. Prevedere la formazione di un legame tra due elementi 2. Predire la lunghezza del legame
Teorie del legame chimico Le teorie proposte per la trattazione del legame chimico si prefiggono i seguenti scopi: 1. Prevedere la formazione di un legame tra due elementi 2. Predire la lunghezza del legame
TEORIA DEL LEGAME DI VALENZA (VB) e GEOMETRIA MOLECOLARE (teoria VSEPR)
 TEORIA DEL LEGAME DI VALENZA (VB) e GEOMETRIA MOLECOLARE (teoria VSEPR) Metodi basati sulla meccanica quantistica: VB e MO La descrizione più corretta della struttura elettronica delle molecole, come quella
TEORIA DEL LEGAME DI VALENZA (VB) e GEOMETRIA MOLECOLARE (teoria VSEPR) Metodi basati sulla meccanica quantistica: VB e MO La descrizione più corretta della struttura elettronica delle molecole, come quella
Metodi basati sulla meccanica quantistica
 Metodi basati sulla meccanica quantistica La descrizione più corretta della struttura elettronica delle molecole, come quella degli atomi, è basata sulla meccanica quantistica. Esistono due principali
Metodi basati sulla meccanica quantistica La descrizione più corretta della struttura elettronica delle molecole, come quella degli atomi, è basata sulla meccanica quantistica. Esistono due principali
TEORIA DEL LEGAME DI VALENZA (VB) e GEOMETRIA MOLECOLARE (teoria VSEPR)
 TEORIA DEL LEGAME DI VALENZA (VB) e GEOMETRIA MOLECOLARE (teoria VSEPR) Metodi basati sulla meccanica quantistica: VB e MO La descrizione più corretta e quantitativa della struttura elettronica delle molecole,
TEORIA DEL LEGAME DI VALENZA (VB) e GEOMETRIA MOLECOLARE (teoria VSEPR) Metodi basati sulla meccanica quantistica: VB e MO La descrizione più corretta e quantitativa della struttura elettronica delle molecole,
LEGAME COVALENTE: TEORIA DEGLI ORBITALI MOLECOLARI
 LEGAME COVALENTE: TEORIA DEGLI ORBITALI MOLECOLARI Il legame covalente e la geometria delle molecole possono essere descritti dalla teoria del legame di valenza: i legami risultano dalla condivisione di
LEGAME COVALENTE: TEORIA DEGLI ORBITALI MOLECOLARI Il legame covalente e la geometria delle molecole possono essere descritti dalla teoria del legame di valenza: i legami risultano dalla condivisione di
Aspetti generali della Chimica Organica 1 parte
 Aspetti generali della Chimica Organica 1 parte Struttura e Legame: Il Carbonio nella Tabella Periodica Il Modello di Lewis Calcolo delle cariche formali Teoria della Risonanza Dove troviamo il carbonio
Aspetti generali della Chimica Organica 1 parte Struttura e Legame: Il Carbonio nella Tabella Periodica Il Modello di Lewis Calcolo delle cariche formali Teoria della Risonanza Dove troviamo il carbonio
IBRIDAZIONE. Approccio più semplice per descrivere la struttura elettronica di una specie sfruttando il concetto di orbitale.
 IBRIDAZIONE MODELLO DELL ORBITALE di LEGAME Approccio più semplice per descrivere la struttura elettronica di una specie sfruttando il concetto di orbitale. METANO Gli atomi nel formare legami usano elettroni
IBRIDAZIONE MODELLO DELL ORBITALE di LEGAME Approccio più semplice per descrivere la struttura elettronica di una specie sfruttando il concetto di orbitale. METANO Gli atomi nel formare legami usano elettroni
Zolfo (Z = 16) Conf. Elettronica 1s 2 2s 2 2p 6 3s 2 3p 4 Conf. Elettronica esterna 3s 2 3p 4
 TAVOLA PERIODICA DEGLI ELEMENTI Gli elementi sono ordinati nella tavola periodica secondo numero atomico crescente ed in base alle loro proprietà chimico-fisiche che seguono un andamento periodico. Gli
TAVOLA PERIODICA DEGLI ELEMENTI Gli elementi sono ordinati nella tavola periodica secondo numero atomico crescente ed in base alle loro proprietà chimico-fisiche che seguono un andamento periodico. Gli
Legame covalente. H 1s un protone e un elettrone
 Legame covalente H 1s un protone e un elettrone Il legame covalente è formato da una coppia di elettroni condivisa fra due atomi. L energia richiesta per separare gli atomi legati è detta energia di legame.
Legame covalente H 1s un protone e un elettrone Il legame covalente è formato da una coppia di elettroni condivisa fra due atomi. L energia richiesta per separare gli atomi legati è detta energia di legame.
GEOMETRIA MOLECOLARE
 GEOMETRIA MOLECOLARE Ibridazione La teoria VSEPR 1 Ibridazione e geometria molecolare Teoria di Lewis e VB vista finora non sono in grado di descrivere correttamente la geometria di molte molecole anche
GEOMETRIA MOLECOLARE Ibridazione La teoria VSEPR 1 Ibridazione e geometria molecolare Teoria di Lewis e VB vista finora non sono in grado di descrivere correttamente la geometria di molte molecole anche
Legame chimico: legame ionico, legame covalente, legame metallico
 Legame chimico: legame ionico, legame covalente, legame metallico Elettroni interni Categorie di elettroni elettroni del gas nobile che precede l elemento nella tavola periodica, riempiono tutti i livelli
Legame chimico: legame ionico, legame covalente, legame metallico Elettroni interni Categorie di elettroni elettroni del gas nobile che precede l elemento nella tavola periodica, riempiono tutti i livelli
Metodi basati sulla meccanica quantistica
 Metodi basati sulla meccanica quantistica La descrizione più corretta della struttura elettronica delle molecole, come quella degli atomi, è basata sulla meccanica quantistica. Esistono due principali
Metodi basati sulla meccanica quantistica La descrizione più corretta della struttura elettronica delle molecole, come quella degli atomi, è basata sulla meccanica quantistica. Esistono due principali
Legame covalente polare
 Legame chimico: covalente polare Legame covalente polare Il passaggio dal legame covalente al legame ionico è il risultato di una distribuzione elettronica non simmetrica. Il simbolo δ (lettera greca delta
Legame chimico: covalente polare Legame covalente polare Il passaggio dal legame covalente al legame ionico è il risultato di una distribuzione elettronica non simmetrica. Il simbolo δ (lettera greca delta
Legame covalente polare
 Legame chimico: covalente polare Legame covalente polare Il passaggio dal legame covalente al legame ionico è il risultato di una distribuzione elettronica non simmetrica. Il simbolo δ (lettera greca delta
Legame chimico: covalente polare Legame covalente polare Il passaggio dal legame covalente al legame ionico è il risultato di una distribuzione elettronica non simmetrica. Il simbolo δ (lettera greca delta
GEOMETRIE MOLECOLARI: TEORIE VSEPR
 GEOMETRIE MOLECOLARI: TEORIE VSEPR (Valence shell Electron Pair Repulsion: repulsione delle coppie di elettroni di valenza) e VB (Valence Bond: legame di valenza) Rappresentazione delle molecole con le
GEOMETRIE MOLECOLARI: TEORIE VSEPR (Valence shell Electron Pair Repulsion: repulsione delle coppie di elettroni di valenza) e VB (Valence Bond: legame di valenza) Rappresentazione delle molecole con le
Prof.Patrizia Gallucci
 Prof.Patrizia Gallucci MAPPA CONCETTUALE Gli atomi,ad eccezione dei gas nobili, si legano tra di loro a formare molecole o aggregati di ioni. Teoria di Lewis: Gli elettroni esterni, di valenza, sono implicati
Prof.Patrizia Gallucci MAPPA CONCETTUALE Gli atomi,ad eccezione dei gas nobili, si legano tra di loro a formare molecole o aggregati di ioni. Teoria di Lewis: Gli elettroni esterni, di valenza, sono implicati
LEGAMI CHIMICI. Gli elettroni esterni sono implicati nella formazione dei legami chimici
 LEGAMI CHIMICI Gli elettroni esterni sono implicati nella formazione dei legami chimici La VALENZA di un elemento è data dal numero di elettroni che esso deve perdere, o acquistare, o mettere in comune
LEGAMI CHIMICI Gli elettroni esterni sono implicati nella formazione dei legami chimici La VALENZA di un elemento è data dal numero di elettroni che esso deve perdere, o acquistare, o mettere in comune
Le Proprietà Periodiche degli Elementi
 Le Proprietà Periodiche degli Elementi Il Legame Chimico Energia nel sistema biatomico. Il Legame Chimico Il Legame Chimico Il Legame Chimico Il Legame Chimico Il Legame Chimico Il Legame Chimico Il Legame
Le Proprietà Periodiche degli Elementi Il Legame Chimico Energia nel sistema biatomico. Il Legame Chimico Il Legame Chimico Il Legame Chimico Il Legame Chimico Il Legame Chimico Il Legame Chimico Il Legame
le SOSTANZE Sostanze elementari (ELEMENTI) COMPOSTI Costituiti da due o più atomi DIVERSI tra loro
 Il legame chimico In natura gli atomi sono solitamente legati ad altri in unità più complesse che, se aggregate fra loro costituiscono quello che macroscopicamente percepiamo come materia, le SOSTANZE
Il legame chimico In natura gli atomi sono solitamente legati ad altri in unità più complesse che, se aggregate fra loro costituiscono quello che macroscopicamente percepiamo come materia, le SOSTANZE
Teoria del legame di valenza (VB) Ibridazione Geometria molecolare. Teoria dell orbitale molecolare (MO)
 IL LEGAME CHIMICO Parte 2 a Teoria del legame di valenza (VB) Ibridazione Geometria molecolare Teoria dell orbitale molecolare (MO) 1 Struttura molecolare Nella nostra discussione sulle teorie del legame
IL LEGAME CHIMICO Parte 2 a Teoria del legame di valenza (VB) Ibridazione Geometria molecolare Teoria dell orbitale molecolare (MO) 1 Struttura molecolare Nella nostra discussione sulle teorie del legame
Le proprietà delle sostanze dipendono dal tipo di legame che unisce gli atomi e dalla forma delle molecole.
 4.1 Angolo di legame e forma delle molecole Le proprietà delle sostanze dipendono dal tipo di legame che unisce gli atomi e dalla forma delle molecole. La forma e le dimensioni delle molecole, la disposizione
4.1 Angolo di legame e forma delle molecole Le proprietà delle sostanze dipendono dal tipo di legame che unisce gli atomi e dalla forma delle molecole. La forma e le dimensioni delle molecole, la disposizione
LEGAME CHIMICO E GEOMETRIA MOLECOLARE-2
 LEGAME CHIMICO E GEOMETRIA MOLECOLARE-2 Il legame covalente (Cap. 9) Orbitali e teorie del legame chimico Teoria del legame di valenza (VB) Ibridazione degli orbitali atomici (orbitali ibridi sp, sp 2,
LEGAME CHIMICO E GEOMETRIA MOLECOLARE-2 Il legame covalente (Cap. 9) Orbitali e teorie del legame chimico Teoria del legame di valenza (VB) Ibridazione degli orbitali atomici (orbitali ibridi sp, sp 2,
Legame chimico unità 1, modulo D del libro
 Legame chimico unità 1, modulo D del libro PERCHÉ IL LEGAME CHIMICO? Gli atomi si trovano raramente isolati, spesso due o più atomi si uniscono tramite un legame chimico. Perché ciò avviene? Perché l insieme
Legame chimico unità 1, modulo D del libro PERCHÉ IL LEGAME CHIMICO? Gli atomi si trovano raramente isolati, spesso due o più atomi si uniscono tramite un legame chimico. Perché ciò avviene? Perché l insieme
LEGAME CHIMICO In genere gli atomi si trovano combinati fra loro in composti molecolari, ionici o metallici.
 LEGAME CIMICO In genere gli atomi si trovano combinati fra loro in composti molecolari, ionici o metallici. Fra le poche eccezioni notiamo i gas nobili che sono particolarmente stabili e non reattivi.
LEGAME CIMICO In genere gli atomi si trovano combinati fra loro in composti molecolari, ionici o metallici. Fra le poche eccezioni notiamo i gas nobili che sono particolarmente stabili e non reattivi.
Regola dell'ottetto e suo superamento Legame ionico Covalenza e ordine di legame Carica formale Risonanza ElettronegativitÄ e polaritä del legame
 IL LEGAME CHIMICO Regola dell'ottetto e suo superamento Legame ionico Covalenza e ordine di legame Carica formale Risonanza ElettronegativitÄ e polaritä del legame 1 IL LEGAME CHIMICO Il legame chimico
IL LEGAME CHIMICO Regola dell'ottetto e suo superamento Legame ionico Covalenza e ordine di legame Carica formale Risonanza ElettronegativitÄ e polaritä del legame 1 IL LEGAME CHIMICO Il legame chimico
CAPITOLO 4 STRUTTURE MOLECOLARI
 APITL 4 STRUTTURE MLELARI 4.1 (a) Di seguito è mostrata la struttura di Lewis di P 3. Nella teoria VSEPR il numero di coppie di elettroni attorno all atomo centrale è fondamentale per determinare la struttura.
APITL 4 STRUTTURE MLELARI 4.1 (a) Di seguito è mostrata la struttura di Lewis di P 3. Nella teoria VSEPR il numero di coppie di elettroni attorno all atomo centrale è fondamentale per determinare la struttura.
I due atomi di idrogeno condividono un elettrone ciascuno, raggiungendo ambedue la configurazione stabile 1s 2 guadagno globale di energia.
 LEGAME COVALENTE H. +.H d H:H Lewis (oppure H-H Kekulè) 1s 1s 1s 2 1s 2 I due atomi di idrogeno condividono un elettrone ciascuno, raggiungendo ambedue la configurazione stabile 1s 2 guadagno globale di
LEGAME COVALENTE H. +.H d H:H Lewis (oppure H-H Kekulè) 1s 1s 1s 2 1s 2 I due atomi di idrogeno condividono un elettrone ciascuno, raggiungendo ambedue la configurazione stabile 1s 2 guadagno globale di
Corso di Laurea in CHIMICA (L.T.) Esercitazione n. 1 - Struttura delle molecole e modo di scrivere le formule
 orso di Laurea in IMIA (L.T.) IMIA RGANIA I con Elementi di Laboratorio Esercitazione n. 1 - Struttura delle molecole e modo di scrivere le formule TERMINI ED ARGMENTI DA NSERE PER L SVLGIMENT DEGLI ESERIZI
orso di Laurea in IMIA (L.T.) IMIA RGANIA I con Elementi di Laboratorio Esercitazione n. 1 - Struttura delle molecole e modo di scrivere le formule TERMINI ED ARGMENTI DA NSERE PER L SVLGIMENT DEGLI ESERIZI
La chimica organica. Corso di Chimica Organica. I composti organici contengono carbonio Struttura elettronica e legame chimico
 2 nm Corso di Chimica Organica Synthesis of Anthropomorphic Molecules: The NanoPutians Di Stephanie H. Chanteau and James M. Tour J. Org. Chem., 68 (23), 8750-8766, 2003. Argomenti e materiale del corso:
2 nm Corso di Chimica Organica Synthesis of Anthropomorphic Molecules: The NanoPutians Di Stephanie H. Chanteau and James M. Tour J. Org. Chem., 68 (23), 8750-8766, 2003. Argomenti e materiale del corso:
Legame chimico: covalente polare Legame covalente polare
 Legame chimico: covalente polare Legame covalente polare Il passaggio dal legame covalente al legame ionico è il risultato di una distribuzione elettronica non simmetrica. Il simbolo δ (lettera greca delta
Legame chimico: covalente polare Legame covalente polare Il passaggio dal legame covalente al legame ionico è il risultato di una distribuzione elettronica non simmetrica. Il simbolo δ (lettera greca delta
Riassunto modelli atomici.
 Lezione 6 1. La teoria atomica moderna 2. Il modello quantomeccanico dell atomo 3. Gli orbitali 4. Carica nucleare efficace 5. Principi di Pauli e Hund 6. Configurazioni elettroniche 7. AUFBAU Riassunto
Lezione 6 1. La teoria atomica moderna 2. Il modello quantomeccanico dell atomo 3. Gli orbitali 4. Carica nucleare efficace 5. Principi di Pauli e Hund 6. Configurazioni elettroniche 7. AUFBAU Riassunto
Il legame chimico. Lezioni 17-20
 Il legame chimico Lezioni 17-20 1 Il legame chimico Le forze attrattive di natura elettrica che tengono uniti gli atomi in molecole o in composti ionici sono dette legami chimici. Legami atomici: covalente
Il legame chimico Lezioni 17-20 1 Il legame chimico Le forze attrattive di natura elettrica che tengono uniti gli atomi in molecole o in composti ionici sono dette legami chimici. Legami atomici: covalente
ESERCIZI ESERCIZI. il basso d. aumenta lungo un periodo da sinistra verso
 ESERCIZI 1) L elettronegatività di un elemento: a è l energia che esso libera acquistando un elettrone e trasformandosi in ione negativo b è l energia necessaria per trasformarlo in ione positivo c indica
ESERCIZI 1) L elettronegatività di un elemento: a è l energia che esso libera acquistando un elettrone e trasformandosi in ione negativo b è l energia necessaria per trasformarlo in ione positivo c indica
GEOMETRIA MOLECOLARE. La struttura di Lewis non fornisce alcuna indicazione sulla forma delle molecole in
 GEOMETRIA MOLECOLARE La struttura di Lewis non fornisce alcuna indicazione sulla forma delle molecole in quanto dipende dagli ANGOLI DI LEGAME cioè gli angoli tra le linee che congiungono i nuclei degli
GEOMETRIA MOLECOLARE La struttura di Lewis non fornisce alcuna indicazione sulla forma delle molecole in quanto dipende dagli ANGOLI DI LEGAME cioè gli angoli tra le linee che congiungono i nuclei degli
IL LEGAME SIGMA σ E IL LEGAME PI- GRECO π
 IL LEGAME SIGMA σ E IL LEGAME PI- GRECO π La teoria di Lewis considera gli elettroni di valenza degli atomi che formano legami,ma prescinde totalmente dal fatto che tali elettroni sono descritti da orbitali
IL LEGAME SIGMA σ E IL LEGAME PI- GRECO π La teoria di Lewis considera gli elettroni di valenza degli atomi che formano legami,ma prescinde totalmente dal fatto che tali elettroni sono descritti da orbitali
LA STRUTTURA DELLE MOLECOLE. Orbitali molecolari e legame chimico
 LA STRUTTURA DELLE MOLECOLE Orbitali molecolari e legame chimico GLI ORBITALI MOLECOLARI Quando degli atomi collidono tra di loro i loro nuclei ed elettroni vengono a trovarsi in prossimità influenzandosi
LA STRUTTURA DELLE MOLECOLE Orbitali molecolari e legame chimico GLI ORBITALI MOLECOLARI Quando degli atomi collidono tra di loro i loro nuclei ed elettroni vengono a trovarsi in prossimità influenzandosi
FORMAZIONE DI LEGAMI. Il legame chimico si definisce quando fra due atomi esistono delle forze che danno luogo alla formazione di un aggregato.
 FORMAZIONE DI LEGAMI Il legame chimico si definisce quando fra due atomi esistono delle forze che danno luogo alla formazione di un aggregato. Presa r come distanza internucleare si osserva che l'energia
FORMAZIONE DI LEGAMI Il legame chimico si definisce quando fra due atomi esistono delle forze che danno luogo alla formazione di un aggregato. Presa r come distanza internucleare si osserva che l'energia
Evoluzione spontanea verso stati a minore energia
 1 LEGAME CHIMICO Con legame chimico indichiamo le interazioni fra gli atomi nei composti chimici, le quali hanno un influenza decisiva sulle proprietà chimiche e fisiche Due o più atomi si legano allo
1 LEGAME CHIMICO Con legame chimico indichiamo le interazioni fra gli atomi nei composti chimici, le quali hanno un influenza decisiva sulle proprietà chimiche e fisiche Due o più atomi si legano allo
Corso di Studi di Fisica Corso di Chimica
 Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Lezioni 13-14 2010 Configurazioni elettroniche Descrizioni diverse Sistema periodico Configurazioni elettroniche Il modello
Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Lezioni 13-14 2010 Configurazioni elettroniche Descrizioni diverse Sistema periodico Configurazioni elettroniche Il modello
Il modello di Lewis Le regole
 Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Configurazioni elettroniche Descrizioni diverse Lezioni 13-14 2010 Sistema periodico Configurazioni elettroniche Il modello
Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Configurazioni elettroniche Descrizioni diverse Lezioni 13-14 2010 Sistema periodico Configurazioni elettroniche Il modello
Teoria degli orbitali ibridi
 Legami σ e π Teoria degli orbitali ibridi FORMAZIONE DEI LEGAMI CHIMICI COVALENTI L orbitale della molecola H 2 ha simmetria cilindrica intorno all asse internucleare H-H LEGAME SIGMA Gli orbitali molecolari
Legami σ e π Teoria degli orbitali ibridi FORMAZIONE DEI LEGAMI CHIMICI COVALENTI L orbitale della molecola H 2 ha simmetria cilindrica intorno all asse internucleare H-H LEGAME SIGMA Gli orbitali molecolari
= GEOMETRIA MOLECOLARE. (numero di legami) + (angolo di legame) = geometria. V.S.E.P.R.: Valence Shell Electron Pair Repulsion
 GEOMETRIA MOLECOLARE I legami covalenti sono direzionali I metodi sperimentali moderni permettono di conoscere sia la DISTANZA di legame (d) che l ANGOLO di legame (α), quindi una buona teoria del legame
GEOMETRIA MOLECOLARE I legami covalenti sono direzionali I metodi sperimentali moderni permettono di conoscere sia la DISTANZA di legame (d) che l ANGOLO di legame (α), quindi una buona teoria del legame
Energia potenziale. d l. E p
 IL LEGAME COVALENTE Legame covalente Si riscontra in composti molecolari i cui atomi costituenti sono uguali o per i quali non si può avere trasferimento elettronico. H 2 N 2 Cl 2 HCl CO in un legame covalente
IL LEGAME COVALENTE Legame covalente Si riscontra in composti molecolari i cui atomi costituenti sono uguali o per i quali non si può avere trasferimento elettronico. H 2 N 2 Cl 2 HCl CO in un legame covalente
Per conoscere le proprietà di una sostanza ne dobbiamo conoscere: * la struttura * il tipo di legame presente tra gli atomi
 LE MOLECOLE Per conoscere le proprietà di una sostanza ne dobbiamo conoscere: * la struttura * il tipo di legame presente tra gli atomi ChimicaGenerale_lezione8 1 Risonanza * La teoria della risonanza
LE MOLECOLE Per conoscere le proprietà di una sostanza ne dobbiamo conoscere: * la struttura * il tipo di legame presente tra gli atomi ChimicaGenerale_lezione8 1 Risonanza * La teoria della risonanza
Che cosa è il Legame Chimico
 Che cosa è il Legame Chimico Le molecole sono aggregati stabili ed identici contenenti più atomi La loro geometria non cambia al cambiare dello stato di aggregazione Deve esistere una forma di interazione
Che cosa è il Legame Chimico Le molecole sono aggregati stabili ed identici contenenti più atomi La loro geometria non cambia al cambiare dello stato di aggregazione Deve esistere una forma di interazione
Legame chimico: covalente polare Legame covalente polare
 Legame chimico: covalente polare Legame covalente polare Il passaggio dal legame covalente al legame ionico è il risultato di una distribuzione elettronica non simmetrica. Il simbolo δ (lettera greca delta
Legame chimico: covalente polare Legame covalente polare Il passaggio dal legame covalente al legame ionico è il risultato di una distribuzione elettronica non simmetrica. Il simbolo δ (lettera greca delta
Introduzione alla chimica organica. 1. Regola ottetto 2. Teoria del legame 3. Geometria delle molecole
 Introduzione alla chimica organica 1. Regola ottetto 2. Teoria del legame 3. Geometria delle molecole La chimica organica tratta di pochissimi atomi che si possono combinare in moltissimi modi Grande importanza
Introduzione alla chimica organica 1. Regola ottetto 2. Teoria del legame 3. Geometria delle molecole La chimica organica tratta di pochissimi atomi che si possono combinare in moltissimi modi Grande importanza
STRUTTURA E FORMA DELLE MOLECOLE
 Ricapitolando Z numero atomico = n. di protoni A numero di massa = n. di protoni n. di neutroni 1 UMA = 1/12 x1.99 10 23 g = 1.66 10 24g = 1/12 massa 12C PA peso atomico massa media degli atomi contenuti
Ricapitolando Z numero atomico = n. di protoni A numero di massa = n. di protoni n. di neutroni 1 UMA = 1/12 x1.99 10 23 g = 1.66 10 24g = 1/12 massa 12C PA peso atomico massa media degli atomi contenuti
Legame metallico Legame costituito dalla non più di una coppia di elettroni tra una sola coppia di atomi ma dalla messa in compartecipazione di
 Legame metallico Legame costituito dalla messa in compartecipazione non più di una coppia di elettroni tra una sola coppia di atomi ma dalla messa in compartecipazione di numerosi elettroni tra numerosi
Legame metallico Legame costituito dalla messa in compartecipazione non più di una coppia di elettroni tra una sola coppia di atomi ma dalla messa in compartecipazione di numerosi elettroni tra numerosi
7.1 LA TEORIA DEL LEGAME DI VALENZA INDICA CHE I LEGAMI SI FORMANO PER SOVRAPPOSIZIONE DEGLI ORBITALI
 7.1 LA TEORIA DEL LEGAME DI VALENZA INDICA CHE I LEGAMI SI FORMANO PER SOVRAPPOSIZIONE DEGLI ORBITALI Le strutture di Lewis non ci dicono nulla sul perché i legami covalenti si formano, né di come gli
7.1 LA TEORIA DEL LEGAME DI VALENZA INDICA CHE I LEGAMI SI FORMANO PER SOVRAPPOSIZIONE DEGLI ORBITALI Le strutture di Lewis non ci dicono nulla sul perché i legami covalenti si formano, né di come gli
Trasformazioni chimiche:
 Il legame chimico 1 Trasformazioni chimiche Trasformazioni chimiche: Le sostanze si trasformano in altre sostanze aventi proprietà differenti (livello macroscopico). Le trasformazioni chimiche avvengono
Il legame chimico 1 Trasformazioni chimiche Trasformazioni chimiche: Le sostanze si trasformano in altre sostanze aventi proprietà differenti (livello macroscopico). Le trasformazioni chimiche avvengono
Legame covalente: la teoria del legame di valenza
 Legame covalente: la teoria del legame di valenza La teoria di Lewis, un legame è costituito da una coppia di elettroni (postulata prima della meccanica quantistica), considera gli elettroni di valenza
Legame covalente: la teoria del legame di valenza La teoria di Lewis, un legame è costituito da una coppia di elettroni (postulata prima della meccanica quantistica), considera gli elettroni di valenza
Il legame chimico. Gli atomi sia nelle sostanze elementari che nei composti sono tenuti insieme dai legami chimici
 Il legame chimico Gli atomi sia nelle sostanze elementari che nei composti sono tenuti insieme dai legami chimici Fra due atomi o fra due gruppi di atomi è presente un legame chimico quando l entità che
Il legame chimico Gli atomi sia nelle sostanze elementari che nei composti sono tenuti insieme dai legami chimici Fra due atomi o fra due gruppi di atomi è presente un legame chimico quando l entità che
