Tamponi Biologici. AO/Febbraio 2016
|
|
|
- Bruno Ceccarelli
- 7 anni fa
- Visualizzazioni
Transcript
1 Tamponi Biologici AO/Febbraio 2016
2 Le soluzioni tampone Le soluzioni tampone contengono una coppia acido-base coniugata in cui le concentrazioni di acido e di base, entrambi non forti, sono circa dello stesso ordine di grandezza. Le soluzioni tampone sono soluzioni che resistono al cambiamento del ph per moderate aggiunte di acido o di base. 2
3 Come si realizza un tampone? Un tampone è generalmente costituito da due soluti, uno che si comporta come acido debole di Brønsted, l altro come base debole di Brønsted. Se l acido è molecolare, la base coniugata è fornita da un sale solubile dell acido. È possibile preparare tamponi che funzionino ad un dato valore di ph scegliendo un acido debole e un suo sale, negli opportuni rapporti molari-
4 Come funziona un tampone? Una sostanza del tampone neutralizza gli H+ eventualmente aggiunti alla soluzione mentre l altra sostanza neutralizza gli OH-. Consideriamo un sistema tampone del tipo HA/A-: Quando aggiungiamo H+ (da un acido forte) al tampone, la base debole coniugata reagisce nel seguente modo: H+(aq) + A-(aq) HA(aq) Quando aggiungiamo OH- (da una base forte) al tampone l acido debole HA del tampone reagisce nel seguente modo: HA(aq) + OH-(aq) A-(aq) + H2O
5 L'equazione di Henderson-Hasselbalch Il ph di una soluzione tampone si calcola con la relazione dove C a = concentrazione iniziale di acido C s = concentrazione del sale disciolto Quando prepariamo un tampone in modo che le concentrazioni dei due componenti siano uguali, il rapporto Cs/Ca risulta uguale a 1, quindi il fattore principale è il pka dell acido debole. 5
6 Quando funziona un tampone? Quando il ph è uguale al pka si hanno le minime variazioni di ph all aggiunta di acidi o di basi Un tampone funziona bene se il ph SOLUZIONE pka -1 < < pka +1 Per l acido acetico il pk =4.7 Qual è il range di ph a cui lo usereste come tampone?
7 Esempio di risposta: Acido Acetico pka= 4,7 A bassi valori di ph (per es. ph 3.7) la forma dominante nell equilibrio chimico è l acido acetico, mentre ad alti valori di ph (per es. ph 5.7) la forma dominante è quello dello ione acetato. Quando il ph = pk a, l acido acetico (CH 3 COOH) è dissociato al 50%. CH 3 COOH + H 2 O H 3 O + + CH 3 COO -
8 Importante! La scelta di una soluzione tampone dipende sempre dal valore di ph che deve essere mantenuto costante Il ph del sangue è mantenuto costante da alcuni soluti che svolgono una efficace azione tampone; nell uomo sano a riposo il ph del sangue è 7,35-7,45 (arterioso 7,4 venoso 7,37) Tampone acido acetico/acetato: è un tampone utile a mantenere il ph di una soluzione intorno a 5, e non al valore fisiologico di 7,4 quindi non è adatto all utilizzo negli organismi viventi.
9 Regolazione ph nell organismo Il ph dei fluidi del'organismo, in particolare del sangue, è regolato attraverso un complesso meccanismo omeostatico. Esistono principalmente tre sistemi tampone: 1. diidrogenofosfato - idrogenofosfato H 2 PO 4- + H 2 O = H 3 O + + HPO acido carbonico - idrogenocarbonato CO 2 + H 2 O = H 2 CO 3 = H + + HCO 3 3. proteine - anioni proteinato proteina = H + + ione proteinato - Se il ph raggiunge valori inferiori a 7.35 e superori a 7.45, i patologi parlano rispettivamente di acidosi e alcalosi. Valori di ph inferiori a 7 e superiori a 7.8 sono incompatibili con la vita.
10 Perché è importante? 1. Regola il funzionamento degli Enzimi:il ph può influenzare il legame di un enzima con il substrato e l'attività catalitica dell enzima 2. Modifica l affinità dell Hb per l ossigeno: in ambiente acido l'emoglobina rilascia più facilmente l'ossigeno, mentre in ambiente basico il legame con l'ossigeno è più forte (Effetto Bohr) 3. Contrazione muscolare: abbassando il ph intracellulare nel muscolo cardiaco si ottiene una riduzione della forza di contrazione.
11 Regolazione acido base: Produzione metabolica ed eliminazione di acidi ed alcali Le variazioni di ph nei liquidi organici devono mantenute entro limiti molto ristretti (mammiferi tra ) Liquidi corporei ph Bile cistica 5,6 8,0 Citoplasma cellule muscolari scheletriche 6,9 Feci 5,9 8,5 Liquido cerebro-spinale 7,35 Saliva 5,8 7,1 Sangue arterioso 7,40 Sangue venoso 7,35 Succo gastrico 0,7 3,8 Succo intestinale 7,0 8,0 Succo pancreatico 7,5 8,8 Urina 4,5 8,0
12 Da Dove arriva H +? Ogni giorno il nostro organismo produce acidi. La maggior quantità di acido prodotto è conseguenza della respirazione cellulare. CO 2 + H 2 O H 2 CO 3 H + + HCO 3 - Acido carbonico (pk1= 6,1) mmoli/die vs 80 mmol/die altri acidi La reazione di idratazione è spontanea ma troppo lenta per i ritmi metabolici: l enzima eritrocitario anidrasi carbonica consente una velocità di reazione di 100 volte superiore rispetto a quella spontanea e ciò evita l accumulo della CO 2 nel sangue sotto forma gassosa, avendo l enzima la capacità di catalizzare l idratazione di molecole di CO 2 al secondo.
13 Lo ione HCO3 -, che costituisce il sistema tampone più importante del sangue, si trova in una condizione di equilibrio dinamico, in risposta alle variazioni del ph e alla concentrazione di CO2 nei vari tessuti umani. pk= 6.1 H 2 O +CO 2 H 2 CO 3 HCO3 - + H + Se si alcalinizza il ph nel sangue, H 2 O e CO 2 reagiscono a dare H 2 CO 3 che dissocia un H+ e lo ione HCO3 - acidificando il sangue Se si abbassa il ph nel sangue, lo ione HCO3 - si protona a dare H 2 CO 3 che, in eccesso, si dissocia a dare H 2 O +CO 2
14 Applicazioni dell Equazione di Henderson- Hasselbach Quale dovrà essere il rapporto tra bicarbonato e acido affinchè il valore di ph sia 7,40? Riprendendo l equazione di H.H.: 7,40=pK + log Cs (bicarbonato) Ca (acido) 1,3= log Cs (bicarbonato) Ca (acido) 20/1 =Cs/Ca Ogni rapporto tra bicarbonato e acido carbonico che sia 20/1 produrrà un ph normale. L organismo cercherà di correggere gli squilibri di tale rapporto per mantenere un ph normale. CO 2 è sotto il controllo dei polmoni Bicarbonato è sotto controllo renale
15 Compensazione dei Tamponi COMPONENTE RESPIRATORIA CO 2 H 2 CO 3 Agisce entro alcuni minuti eliminando ioni idrogeno sotto forma di anidride carbonica COMPONENTE METABOLICA O RENALE HCO 3 - Richiede ore o giorni per sintetizzare nuovo bicarbonato e per eliminare gli ioni idogeno in eccesso. Sia i polmoni che i reni, in condizioni normali, hanno la capacità di aumentare o diminuire il livello del loro rispettivo costituente tampone al fine di raggiungere l obiettivo primario, il rapporto 20:1 essenziale per il mantenimento del ph normale nel sangue
16 Se aggiungiamo H+ al sangue aumenta la [ H2CO3] Questo porta ad un aumento della CO2 disciolta e di conseguenza la pco2 nei polmoni viene eliminata con la respirazione Se aggiungiamo OH- la reazione è opposta perciò diminuzione della [H+] che sposta l equilibrio verso destra ; diminuzione di [H2CO3] e diminuzione [CO2] disciolta e aumenta la SOLUBILIZZAZIONE della CO2 nel plasma LA VELOCITA DELLA RESPIRAZIONE REGOLA e MANTIENE COSTANTE il ph
17 Cause di squilibrio dell equilibrio acido-base del sangue: ACIDOSI RESPIRATORIA: incapacità del polmone a eliminare CO2. Cs/Ca < 20/1 Il Rene, per compensare l eccesso di acido, produce più bicarbonato ALCALOSI RESPIRATORIA : Eccessiva eliminazione CO2 da parte dei polmoni Cs/Ca > 20/1 Il rene riduce l escrezione di acidi e produce meno bicarbonate ACIDOSI METABOLICA : il rene non riesce a eliminare gli H in eccesso e a recuperare il bicarbonate Cs/Ca < 20/1 I polmoni compensano eliminando più CO2 (iperventilazione) ALCALOSI METABOLICA : bicarbonate in eccesso Cs/Ca > 20/1 Il centro del respiro induce ipoventilazione per trattenere CO2
18 ricapitolando Quando il disturbo primario è METABOLICO il compenso è respiratorio e avviene immediatamente Quando l alterazione è RESPIRATORIA il compenso è metabolico e viene operato dal rene nell ambito di alcuni giorni L esame con cui il medico valuta l equilibrio acidobase del sangue è l EMOGASANALISI, che misura ph, po2 e pco2. Si usa sangue arterioso.
Tamponi biologici per il controllo del ph
 Tamponi biologici per il controllo del ph 1 Si definisce una soluzione tampone una soluzione che si oppone alla variazione del ph per aggiunte moderate di acidi o basi Si tratta generalmente di soluzioni
Tamponi biologici per il controllo del ph 1 Si definisce una soluzione tampone una soluzione che si oppone alla variazione del ph per aggiunte moderate di acidi o basi Si tratta generalmente di soluzioni
Le soluzioni tampone
 Le soluzioni tampone Se in una soluzione acquosa sono presenti un acido debole e la sua base coniugata (CH 3 COOH e CH 3 COO - ;H 2 CO 3 e HCO 3 -, etc.) si ha una soluzione tampone (o come detto in alcuni
Le soluzioni tampone Se in una soluzione acquosa sono presenti un acido debole e la sua base coniugata (CH 3 COOH e CH 3 COO - ;H 2 CO 3 e HCO 3 -, etc.) si ha una soluzione tampone (o come detto in alcuni
Plasma ph Tamponi: LEC: HCO 3 LIC: Proteine, Emoglobina, Fosfati Urina: Fosfati e ammoniaca
 Equilibrio acidobase Dieta: Acidi grassi Aminoacidi Assunzione H + CO 2, acido lattico, chetoacidi Plasma ph 7.357.42 Tamponi: LEC: HCO 3 LIC: Proteine, Emoglobina, Fosfati Urina: Fosfati e ammoniaca Ventilazione:
Equilibrio acidobase Dieta: Acidi grassi Aminoacidi Assunzione H + CO 2, acido lattico, chetoacidi Plasma ph 7.357.42 Tamponi: LEC: HCO 3 LIC: Proteine, Emoglobina, Fosfati Urina: Fosfati e ammoniaca Ventilazione:
Raffaele Alvisi 14 gennaio 1916
 Raffaele Alvisi 14 gennaio 1916 Alterazioni del ph = Alterazioni dell equilibrio Acido-Base X 1 2 3 4 5 6 7 8 9 Conoscenze o Capacità Acquisite SI/NO Il clinico sospetta e dimostra l alterazione dell equilibrio
Raffaele Alvisi 14 gennaio 1916 Alterazioni del ph = Alterazioni dell equilibrio Acido-Base X 1 2 3 4 5 6 7 8 9 Conoscenze o Capacità Acquisite SI/NO Il clinico sospetta e dimostra l alterazione dell equilibrio
L EQUILIBRIO ACIDO-BASE NEL SANGUE
 L EQUILIBRIO ACIDO-BASE NEL SANGUE 1 I tamponi fisiologici del ph 1 - Il sistema acido carbonico-bicarbonato: H 2 CO 3 H + + HCO 3 pka = 6.1 ph = 6.1 + log [HCO 3 ] [H 2 CO 3 ] 2 - Il sistema fosfato:
L EQUILIBRIO ACIDO-BASE NEL SANGUE 1 I tamponi fisiologici del ph 1 - Il sistema acido carbonico-bicarbonato: H 2 CO 3 H + + HCO 3 pka = 6.1 ph = 6.1 + log [HCO 3 ] [H 2 CO 3 ] 2 - Il sistema fosfato:
L EQUILIBRIO ACIDO-BASE NEL SANGUE
 L EQUILIBRIO ACIDO-BASE NEL SANGUE ph fisiologico: 7.35-7.45 ph < 7.35 acidosi ph > 7.45 alcalosi 1 L equazione di Henderson-Hasselbalch HA H + + A - La costante di equilibrio (K) (o costante di dissociazione
L EQUILIBRIO ACIDO-BASE NEL SANGUE ph fisiologico: 7.35-7.45 ph < 7.35 acidosi ph > 7.45 alcalosi 1 L equazione di Henderson-Hasselbalch HA H + + A - La costante di equilibrio (K) (o costante di dissociazione
L EQUILIBRIO ACIDO-BASE NEL SANGUE
 L EQUILIBRIO ACIDO-BASE NEL SANGUE ph fisiologico: 7.35-7.45 ph < 7.35 acidosi ph > 7.45 alcalosi Lezione 24 1 L equazione di Henderson-Hasselbalch HA H + + A - La costante di equilibrio (K) (o costante
L EQUILIBRIO ACIDO-BASE NEL SANGUE ph fisiologico: 7.35-7.45 ph < 7.35 acidosi ph > 7.45 alcalosi Lezione 24 1 L equazione di Henderson-Hasselbalch HA H + + A - La costante di equilibrio (K) (o costante
SOLUZIONE TAMPONE. Soluzione il cui ph non è modificato dall aggiunta di modiche quantità di acido o di base forti
 SOLUZIONE TAMPONE Soluzione il cui ph non è modificato dall aggiunta di modiche quantità di acido o di base forti Una soluzione tampone è costituita da Acido debole in presenza della propria base coniugata
SOLUZIONE TAMPONE Soluzione il cui ph non è modificato dall aggiunta di modiche quantità di acido o di base forti Una soluzione tampone è costituita da Acido debole in presenza della propria base coniugata
I tre sistemi per la regolazione del ph
 I tre sistemi per la regolazione del ph Se vuoi finalmente capire quali sono e come funzionano i sistemi per la regolazione del ph questo breve articolo fa proprio al caso tuo. In questo articolo parleremo
I tre sistemi per la regolazione del ph Se vuoi finalmente capire quali sono e come funzionano i sistemi per la regolazione del ph questo breve articolo fa proprio al caso tuo. In questo articolo parleremo
EQUILIBRI DEI SISTEMI TAMPONE ACIDO-BASE
 EQUILIBRI DEI SISTEMI TAMPONE ACIDO-BASE E importante per poter controllare l andamento di una reazione mantenere costante il ph di una soluzione. Ad esempio il ph del plasma può variare, senza influenzare
EQUILIBRI DEI SISTEMI TAMPONE ACIDO-BASE E importante per poter controllare l andamento di una reazione mantenere costante il ph di una soluzione. Ad esempio il ph del plasma può variare, senza influenzare
Soluzioni tampone. Se ad un litro di acqua pura (ph=7) vengono aggiunte 0,01 moli di HCl il ph varia da 7 a 2 (ph=-log(0,01) =2,0), ovvero di 5 unità.
 Soluzioni tampone Se ad un litro di acqua pura (ph=7) vengono aggiunte 0,01 moli di HCl il ph varia da 7 a 2 (ph=-log(0,01) =2,0), ovvero di 5 unità. Un tampone è una soluzione che varia in maniera trascurabile
Soluzioni tampone Se ad un litro di acqua pura (ph=7) vengono aggiunte 0,01 moli di HCl il ph varia da 7 a 2 (ph=-log(0,01) =2,0), ovvero di 5 unità. Un tampone è una soluzione che varia in maniera trascurabile
Le reazioni metaboliche sono estremamente sensibili alla concentrazione degli ioni H + nel liquido in cui avvengono, perché gli ioni H + influenzano
 EQUILIBRIO ACIDOBASE Le reazioni metaboliche sono estremamente sensibili alla concentrazione degli ioni H + nel liquido in cui avvengono, perché gli ioni H + influenzano il funzionamento degli enzimi.
EQUILIBRIO ACIDOBASE Le reazioni metaboliche sono estremamente sensibili alla concentrazione degli ioni H + nel liquido in cui avvengono, perché gli ioni H + influenzano il funzionamento degli enzimi.
Equilibrio acido base
 Equilibrio acido base In una soluzione acquosa: [H+] x [OH-]= 10-14 M ph= logaritmo in base 10 dell inverso della [ H+] (-log[h+]) Variazioni di ph possono portare a variazioni di molec organiche e al
Equilibrio acido base In una soluzione acquosa: [H+] x [OH-]= 10-14 M ph= logaritmo in base 10 dell inverso della [ H+] (-log[h+]) Variazioni di ph possono portare a variazioni di molec organiche e al
EQUILIBRIO ACIDO-BASE ED APPLICAZIONE ALL EMOGAS EMOGAS-ANALISIANALISI
 EQUILIBRIO ACIDO-BASE ED APPLICAZIONE ALL EMOGAS EMOGAS-ANALISIANALISI SOMMARIO ASPETTI GENERALI DELL EQUILIBRIO EQUILIBRIO ACIDO-BASE EGA (EMOGAS-ANALISI) ANALISI) ASPETTI GENERALI DELL EQUILIBRIO EQUILIBRIO
EQUILIBRIO ACIDO-BASE ED APPLICAZIONE ALL EMOGAS EMOGAS-ANALISIANALISI SOMMARIO ASPETTI GENERALI DELL EQUILIBRIO EQUILIBRIO ACIDO-BASE EGA (EMOGAS-ANALISI) ANALISI) ASPETTI GENERALI DELL EQUILIBRIO EQUILIBRIO
a.a. 2017/18 Prof.ssa Pia Lucidi Laboratorio di Cognizione e Benessere Animale RICEVIMENTO: Lunedì 17:30-18:30
 a.a. 2017/18 Prof.ssa Pia Lucidi Laboratorio di Cognizione e Benessere Animale RICEVIMENTO: Lunedì 17:3018:30 Omeostasi acidobasica Gli enzimi operano ad un ph ottimale in un range molto ristretto (7.4
a.a. 2017/18 Prof.ssa Pia Lucidi Laboratorio di Cognizione e Benessere Animale RICEVIMENTO: Lunedì 17:3018:30 Omeostasi acidobasica Gli enzimi operano ad un ph ottimale in un range molto ristretto (7.4
Equilibri acido-base, ph e sistemi tampone
 Equilibri acido-base, ph e sistemi tampone Tiziana Bellini Dipartimento di Scienze Biomediche Chirurgico Specialistiche Facoltà di Medicina Farmacia e Prevenzione Università di Ferrara Cos è un acido?
Equilibri acido-base, ph e sistemi tampone Tiziana Bellini Dipartimento di Scienze Biomediche Chirurgico Specialistiche Facoltà di Medicina Farmacia e Prevenzione Università di Ferrara Cos è un acido?
1. Controllo dell equilibrio acido-base. Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona
 1. Controllo dell equilibrio acido-base Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona Misura dell acidità di una soluzione Definizione di acido: qualsiasi sostanza chimica che
1. Controllo dell equilibrio acido-base Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona Misura dell acidità di una soluzione Definizione di acido: qualsiasi sostanza chimica che
Teorie Acido-Base. Gli acidi in acqua si dissociano e rilasciano H + Le basi in acqua si dissociano e rilasciano OH -
 Teorie Acido-Base Arrhenius: Gli acidi in acqua si dissociano e rilasciano H + Le basi in acqua si dissociano e rilasciano OH - Broensted-Lowry: Gli acidi rilasciano H + Le basi accettano H + Lewis gli
Teorie Acido-Base Arrhenius: Gli acidi in acqua si dissociano e rilasciano H + Le basi in acqua si dissociano e rilasciano OH - Broensted-Lowry: Gli acidi rilasciano H + Le basi accettano H + Lewis gli
In acqua pura o in soluzione acquosa, si ha sempre il seguente equilibrio: + +
 Ionizzazione dell Acqua e ph In acqua pura o in soluzione acquosa, si ha sempre il seguente equilibrio: + + L acqua è una sostanza anfiprotica, cioè può sia donare che accettare protoni (ioni H + ). Costante
Ionizzazione dell Acqua e ph In acqua pura o in soluzione acquosa, si ha sempre il seguente equilibrio: + + L acqua è una sostanza anfiprotica, cioè può sia donare che accettare protoni (ioni H + ). Costante
Per le lezioni del prof. P.P. Battaglini Schemi di. v 3.2. ph = pka + log10 [!$]
![Per le lezioni del prof. P.P. Battaglini Schemi di. v 3.2. ph = pka + log10 [!$] Per le lezioni del prof. P.P. Battaglini Schemi di. v 3.2. ph = pka + log10 [!$]](/thumbs/92/108719223.jpg) Per le lezioni del prof. P.P. Battaglini Schemi di v 3.2 ph = pka + log10! " [!$] Dichiarazione Le immagini presenti in questo file sono state reperite in rete o modificate da testi cartacei. Queste immagini
Per le lezioni del prof. P.P. Battaglini Schemi di v 3.2 ph = pka + log10! " [!$] Dichiarazione Le immagini presenti in questo file sono state reperite in rete o modificate da testi cartacei. Queste immagini
Trasporto dei gas respiratori nel sangue
 Trasporto dei gas respiratori nel sangue La soluzione dei gas nei liquidi C Legge di Henry acq P gas S gas C acq = quantità di gas disciolta nella fase acquosa P gas = pressione parziale del gas nella
Trasporto dei gas respiratori nel sangue La soluzione dei gas nei liquidi C Legge di Henry acq P gas S gas C acq = quantità di gas disciolta nella fase acquosa P gas = pressione parziale del gas nella
2.Controllo dell equilibrio acido-base - II. Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona
 2.Controllo dell equilibrio acidobase II Carlo Capelli Fisiologia Facoltà di Scienze Motorie Università di Verona 1. Tampone bicarbonatoco 2 E il sistema tampone fisiologico più importante [ CO 2] = PCO
2.Controllo dell equilibrio acidobase II Carlo Capelli Fisiologia Facoltà di Scienze Motorie Università di Verona 1. Tampone bicarbonatoco 2 E il sistema tampone fisiologico più importante [ CO 2] = PCO
SOLUZIONI derivate da: Acido debole/ sale (CH 3 COOH/CH 3 COONa) Base debole/ suo sale (NH 4 OH/NH 4 Cl)
 Soluzioni Tampone Si definiscono soluzioni tampone quelle soluzioni in grado di mantenere pressoché costante il proprio ph per aggiunta di una ragionevole quantità di acido o di base forte o per moderata
Soluzioni Tampone Si definiscono soluzioni tampone quelle soluzioni in grado di mantenere pressoché costante il proprio ph per aggiunta di una ragionevole quantità di acido o di base forte o per moderata
Escrezione cataboliti, farmaci, droghe Regolazione equilibrio idrico Regolazione osmolarità concentrazione elettroliti Regolazione equilibrio
 Il rene Escrezione cataboliti, farmaci, droghe Regolazione equilibrio idrico Regolazione osmolarità concentrazione elettroliti Regolazione equilibrio acido-base Regolazione Pressione Arteriosa Secrezione
Il rene Escrezione cataboliti, farmaci, droghe Regolazione equilibrio idrico Regolazione osmolarità concentrazione elettroliti Regolazione equilibrio acido-base Regolazione Pressione Arteriosa Secrezione
Molti sali contengono un anione o un catione che possono reagire con acqua rendendo le loro soluzioni ACIDE o BASICHE
 Molti sali contengono un anione o un catione che possono reagire con acqua rendendo le loro soluzioni ACIDE o BASICHE Molti sali reagiscono con l acqua alterando il suo rapporto molare tra [H] e [OH] -
Molti sali contengono un anione o un catione che possono reagire con acqua rendendo le loro soluzioni ACIDE o BASICHE Molti sali reagiscono con l acqua alterando il suo rapporto molare tra [H] e [OH] -
PRINCIPALI SISTEMI TAMPONE
 SISTEMI TAMPONE PROF.SSA AUSILIA ELCE Indice 1 INTRODUZIONE -------------------------------------------------------------------------------------------------------------- 3 2 PRINCIPALI SISTEMI TAMPONE
SISTEMI TAMPONE PROF.SSA AUSILIA ELCE Indice 1 INTRODUZIONE -------------------------------------------------------------------------------------------------------------- 3 2 PRINCIPALI SISTEMI TAMPONE
 2NH3(g) Pa(Ag)=108 Pa(I)=127 pf(agi)=235 -> S(g/l) =S(m/l) pf = 9.2 10-9 235 =2162 10-9 = 2.16 10-6 (g/l) Effetto del ph Anche il ph può influenzare la solubilità di un sale poco solubile. E ciò
2NH3(g) Pa(Ag)=108 Pa(I)=127 pf(agi)=235 -> S(g/l) =S(m/l) pf = 9.2 10-9 235 =2162 10-9 = 2.16 10-6 (g/l) Effetto del ph Anche il ph può influenzare la solubilità di un sale poco solubile. E ciò
L'EQUILIBRIO ACIDO-BASE
 L'EQUILIBRIO ACIDO-BASE La concentrazione nell'organismo degli ioni H+ è finemente regolata perché quasi tutte le attività enzimatiche sono influenzate sostanzialmente dalle variazioni di ph. Quindi l'attività
L'EQUILIBRIO ACIDO-BASE La concentrazione nell'organismo degli ioni H+ è finemente regolata perché quasi tutte le attività enzimatiche sono influenzate sostanzialmente dalle variazioni di ph. Quindi l'attività
Sommario della lezione 22. Idrolisi Indicatori di ph Soluzioni tampone - Titolazioni
 Sommario della lezione 22 Idrolisi Indicatori di ph Soluzioni tampone - Titolazioni Determinazione del ph Il ph di una soluzione può essere determinato in modo approssimato mediante l uso di un indicatore.
Sommario della lezione 22 Idrolisi Indicatori di ph Soluzioni tampone - Titolazioni Determinazione del ph Il ph di una soluzione può essere determinato in modo approssimato mediante l uso di un indicatore.
ph = log 1/[H + ] = log [H + ]
![ph = log 1/[H + ] = log [H + ] ph = log 1/[H + ] = log [H + ]](/thumbs/49/24977942.jpg) ph = log 1/[H ] = log [H ] Sangue arterioso ph = 7.4 Sangue venoso ph = 7.35 ph inferiori = acidosi (limite ph = 6.8) ph superiori = alcalosi (limite ph = 8) ph intracellulare = 6 7.4 ph urina 4.5 8 Produzione
ph = log 1/[H ] = log [H ] Sangue arterioso ph = 7.4 Sangue venoso ph = 7.35 ph inferiori = acidosi (limite ph = 6.8) ph superiori = alcalosi (limite ph = 8) ph intracellulare = 6 7.4 ph urina 4.5 8 Produzione
 Trigliceridi Colesterolo Esteri del Colesterolo Fosfolipidi Trasporti attraverso le membrane Diffusione facilitata: Scambio dei cloruri o Scambio Cl - /HCO - 3 Cl - HCO3
Trigliceridi Colesterolo Esteri del Colesterolo Fosfolipidi Trasporti attraverso le membrane Diffusione facilitata: Scambio dei cloruri o Scambio Cl - /HCO - 3 Cl - HCO3
Cap. 1 Interazioni delle molecole con l acqua
 Cap. 1 nterazioni delle molecole con l acqua Ci sono legami idrogeno nel metano liquido (CH 4 mantenuto a -165 C)? Perché? No, perché il legame C-H non è sufficientemente polare da avere una distribuzione
Cap. 1 nterazioni delle molecole con l acqua Ci sono legami idrogeno nel metano liquido (CH 4 mantenuto a -165 C)? Perché? No, perché il legame C-H non è sufficientemente polare da avere una distribuzione
ACIDI E BASI ORGANICI: pka e ph
 Soluzione ph NaOH, 0,1 M Candeggina domestica Ammoniaca domestica ACIDI E BASI ORGANICI: pka e ph Magnesia Borace Bicarbonato Acqua di mare, albume Sangue, lacrime Latte Saliva Pioggia Caffè Pomodori Vino
Soluzione ph NaOH, 0,1 M Candeggina domestica Ammoniaca domestica ACIDI E BASI ORGANICI: pka e ph Magnesia Borace Bicarbonato Acqua di mare, albume Sangue, lacrime Latte Saliva Pioggia Caffè Pomodori Vino
Soluzioni tampone. Francesca Montemurro
 Soluzioni tampone Francesca Montemurro DEFINIZIONE ACIDO BASE ü ARRENIUS: acido libera H + e la base OH -, era una definizione che andava bene per reazioni in soluzione acquosa ma non in ambiente gassoso.
Soluzioni tampone Francesca Montemurro DEFINIZIONE ACIDO BASE ü ARRENIUS: acido libera H + e la base OH -, era una definizione che andava bene per reazioni in soluzione acquosa ma non in ambiente gassoso.
Fisiologia Renale 4. Equilibrio acido-base: Fisiologia e fisiopatologia
 Fisiologia Renale 4. Equilibrio acido-base: Fisiologia e fisiopatologia Fisiologia Generale e dell Esercizio Carlo Capelli Facoltà di Scienze Motorie, Università di Verona Obiettivi Tamponi fisiologici
Fisiologia Renale 4. Equilibrio acido-base: Fisiologia e fisiopatologia Fisiologia Generale e dell Esercizio Carlo Capelli Facoltà di Scienze Motorie, Università di Verona Obiettivi Tamponi fisiologici
Acidi e basi ph, costanti di acidità e basicità Idrolisi, soluzioni tampone
 Acidi e basi ph, costanti di acidità e basicità Idrolisi, soluzioni tampone Dr. Gabriella Giulia Pulcini Ph.D. Student, Development of new approaches to teaching and learning Natural and Environmental
Acidi e basi ph, costanti di acidità e basicità Idrolisi, soluzioni tampone Dr. Gabriella Giulia Pulcini Ph.D. Student, Development of new approaches to teaching and learning Natural and Environmental
AUTOIONIZZAZIONE DELL ACQUA
 AUTOIONIZZAZIONE DELL ACQUA H 2 O si comporta da acido e da base anfiprotica CH 3 COOH + H 2 O CH 3 COO - + H 3 O + NH 3 +H 2 O NH 4 + + OH - A1 B2 H 2 O + H 2 O H 3 O + + OH - B1 A1 K eq [ H O ][ OH 3
AUTOIONIZZAZIONE DELL ACQUA H 2 O si comporta da acido e da base anfiprotica CH 3 COOH + H 2 O CH 3 COO - + H 3 O + NH 3 +H 2 O NH 4 + + OH - A1 B2 H 2 O + H 2 O H 3 O + + OH - B1 A1 K eq [ H O ][ OH 3
EQUILIBRI IN SOLUZIONE ACQUOSA
 EQUILIBRI IN SOLUZIONE ACQUOSA Costante di equilibrio Si consideri la seguente reazione di equilibrio: aa + bb cc + dd La costante di equilibrio della reazione ad una data temperatura è definita come il
EQUILIBRI IN SOLUZIONE ACQUOSA Costante di equilibrio Si consideri la seguente reazione di equilibrio: aa + bb cc + dd La costante di equilibrio della reazione ad una data temperatura è definita come il
LEGGE di AZIONE di MASSA
 LEGGE di AZIONE di MASSA Lo stato di equilibrio di una reazione chimica è rappresentata dalla concentrazione di reagenti e prodotti tali da soddisfare una opportuna relazione matematica: a A + b B + c
LEGGE di AZIONE di MASSA Lo stato di equilibrio di una reazione chimica è rappresentata dalla concentrazione di reagenti e prodotti tali da soddisfare una opportuna relazione matematica: a A + b B + c
Scambi gassosi e regolazione del respiro
 Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I Scambi gassosi e regolazione del respiro Ventilazione polmonare Ruolo del Sistema Respiratorio: 1 2 - fornire O 2 - rimuovere
Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I Scambi gassosi e regolazione del respiro Ventilazione polmonare Ruolo del Sistema Respiratorio: 1 2 - fornire O 2 - rimuovere
SOLUZIONI TAMPONE SOLUZIONI TAMPONE
 SOLUZIONI TAMPONE Le soluzioni tampone (o tamponi) sono costituite da: un acido debole e un suo sale (tampone acido) oppure una base debole e un suo sale (tampone basico) Una soluzione di un acido debole
SOLUZIONI TAMPONE Le soluzioni tampone (o tamponi) sono costituite da: un acido debole e un suo sale (tampone acido) oppure una base debole e un suo sale (tampone basico) Una soluzione di un acido debole
Acidi e Basi. Qual è la definizione di acido e di base dal punto di vista della chimica?
 Acidi e Basi Acido è una parola che deriva dal latino acetum (aceto). Col tempo la parola si è estesa a tutte le sostanze che hanno un sapore acidulo. Basi o alcali (dall arabo al kali = la cenere delle
Acidi e Basi Acido è una parola che deriva dal latino acetum (aceto). Col tempo la parola si è estesa a tutte le sostanze che hanno un sapore acidulo. Basi o alcali (dall arabo al kali = la cenere delle
Equilibrio Acido base
 Equilibrio Acido base Acido e base secondo ARRHENIUS Un acido è una sostanza che in soluzione acquosa libera ioni idrogeno HA à H A - HCl à H Cl - Un base è una sostanza che in soluzione acquosa libera
Equilibrio Acido base Acido e base secondo ARRHENIUS Un acido è una sostanza che in soluzione acquosa libera ioni idrogeno HA à H A - HCl à H Cl - Un base è una sostanza che in soluzione acquosa libera
LEZIONE 25: EMOGLOBINA L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO
 LEZIONE 25: EMOGLOBINA L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 25_emoglobina 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata
LEZIONE 25: EMOGLOBINA L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 25_emoglobina 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata
Scambi gassosi e regolazione del respiro
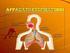 Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I Scambi gassosi e regolazione del respiro Ruolo del Sistema Respiratorio: - fornire O 2 - rimuovere CO 2 Scaricato da www.sunhope.it
Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I Scambi gassosi e regolazione del respiro Ruolo del Sistema Respiratorio: - fornire O 2 - rimuovere CO 2 Scaricato da www.sunhope.it
L acqua. Ci devono essere delle forze che tengono saldamente insieme le molecole d acqua
 L acqua Comparata a molecole con caratteristiche atomiche simili e di grandezza comparabile, l acqua presenta alcune caratteristiche peculiari Comparando l idruro dell ossigeno con gli idruri degli elementi
L acqua Comparata a molecole con caratteristiche atomiche simili e di grandezza comparabile, l acqua presenta alcune caratteristiche peculiari Comparando l idruro dell ossigeno con gli idruri degli elementi
ph e indicatori acido-base
 ph e indicatori acido-base La dissociazione ionica dell acqua H 2 O + H 2 O OH - + H 3 O + acido base base acido coniugata coniugato 2 H 2 O (l) OH - (aq) + H 3 O + (aq) Il numero di molecole di acqua
ph e indicatori acido-base La dissociazione ionica dell acqua H 2 O + H 2 O OH - + H 3 O + acido base base acido coniugata coniugato 2 H 2 O (l) OH - (aq) + H 3 O + (aq) Il numero di molecole di acqua
Equilibrio acido-base
 Equilibrio acidobase ph = log 1/[H ] = log [H ] Sangue arterioso ph = 7.4 Sangue venoso ph = 7.35 ph inferiori = acidosi (limite ph = 6.8) ph superiori = alcalosi (limite ph = 8) ph intracellulare = 6
Equilibrio acidobase ph = log 1/[H ] = log [H ] Sangue arterioso ph = 7.4 Sangue venoso ph = 7.35 ph inferiori = acidosi (limite ph = 6.8) ph superiori = alcalosi (limite ph = 8) ph intracellulare = 6
Analizziamo i casi più frequenti. Acido forte Base forte Acido debole Base debole Idrolisi Tampone
 Lezione 17 1. Acidi e basi deboli 2. Relazione tra a e b 3. ph di acidi e basi deboli (esempi) 4. Idrolisi salina acida e basica 5. Soluzioni tampone 6. Equilibrio eterogeneo 7. Idrolisi salina acida e
Lezione 17 1. Acidi e basi deboli 2. Relazione tra a e b 3. ph di acidi e basi deboli (esempi) 4. Idrolisi salina acida e basica 5. Soluzioni tampone 6. Equilibrio eterogeneo 7. Idrolisi salina acida e
Es: consideriamo una soluzione contenente acido K = 1, [CH 3 COOH]
![Es: consideriamo una soluzione contenente acido K = 1, [CH 3 COOH] Es: consideriamo una soluzione contenente acido K = 1, [CH 3 COOH]](/thumbs/103/157927484.jpg) SOLUZIONI TAMPONE Una soluzione tampone è una soluzione che contiene quantità paragonabili (dello stesso ordine di grandezza) di un acido debole e della sua base coniugata o di una base debole e del suo
SOLUZIONI TAMPONE Una soluzione tampone è una soluzione che contiene quantità paragonabili (dello stesso ordine di grandezza) di un acido debole e della sua base coniugata o di una base debole e del suo
10. Acidi e basi deboli, tamponi e titolazioni
 Lezione. cidi e basi deboli, tamponi e titolazioni cidi e basi deboli Generalmente possiamo parlare di elettrolita, cioè una sostanza che in acqua si dissocia. Possono essere distinti elettroliti forti,
Lezione. cidi e basi deboli, tamponi e titolazioni cidi e basi deboli Generalmente possiamo parlare di elettrolita, cioè una sostanza che in acqua si dissocia. Possono essere distinti elettroliti forti,
L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO
 L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 23 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata all emoglobina: L O 2 totale
L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 23 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata all emoglobina: L O 2 totale
CALCOLO DEL ph. ph = - log [1,0x10-3 ] = 3,00
![CALCOLO DEL ph. ph = - log [1,0x10-3 ] = 3,00 CALCOLO DEL ph. ph = - log [1,0x10-3 ] = 3,00](/thumbs/68/59131328.jpg) CALCOLO DEL ph Calcolare il ph di una soluzione di HCl 1,0x10-3 M HCl acido forte che si dissocia completamente HCl H + + Cl - 1 mol di HCl produce 1 mol di H + ph = - log [1,0x10-3 ] = 3,00 Tipici acidi
CALCOLO DEL ph Calcolare il ph di una soluzione di HCl 1,0x10-3 M HCl acido forte che si dissocia completamente HCl H + + Cl - 1 mol di HCl produce 1 mol di H + ph = - log [1,0x10-3 ] = 3,00 Tipici acidi
Controllo nervoso del respiro
 Controllo nervoso del respiro La respirazione è una funzione involontaria controllata da 3 gruppi di neuroni (centri) localizzati nel tronco encefalico: Controllo nervoso del respiro Centro respiratorio
Controllo nervoso del respiro La respirazione è una funzione involontaria controllata da 3 gruppi di neuroni (centri) localizzati nel tronco encefalico: Controllo nervoso del respiro Centro respiratorio
ACIDI e BASI. La definizione di acido e base si è evoluta nel corso degli anni, sviluppando modelli sempre più generali.
 ACIDI e BASI La definizione di acido e base si è evoluta nel corso degli anni, sviluppando modelli sempre più generali. Il modello di Arrhenius è stato ampliato dal modello di Brønsted-Lowry. Ancora più
ACIDI e BASI La definizione di acido e base si è evoluta nel corso degli anni, sviluppando modelli sempre più generali. Il modello di Arrhenius è stato ampliato dal modello di Brønsted-Lowry. Ancora più
21/03/2017 EQUILIBRI IN SOLUZIONE ACQUOSA EQUILIBRI IN SOLUZIONE ACQUOSA EQUILIBRI IN SOLUZIONE ACQUOSA
 EQUILIBRI IN SOLUZIONE ACQUOSA EQUILIBRI IN SOLUZIONE ACQUOSA EQUILIBRI IN SOLUZIONE ACQUOSA 1 Concentrazione Molarità : numero di moli di soluto per litro di soluzione. Molalità : numero di moli di soluto
EQUILIBRI IN SOLUZIONE ACQUOSA EQUILIBRI IN SOLUZIONE ACQUOSA EQUILIBRI IN SOLUZIONE ACQUOSA 1 Concentrazione Molarità : numero di moli di soluto per litro di soluzione. Molalità : numero di moli di soluto
EQUILIBRI IN SOLUZIONE
 EQUILIBRI IN SOLUZIONE Tra tutti i solventi l acqua è quello che maggiormente favorisce la dissociazione elettrolitica. Gli equilibri in soluzione costituiscono quindi una classe di reazioni molto importanti.
EQUILIBRI IN SOLUZIONE Tra tutti i solventi l acqua è quello che maggiormente favorisce la dissociazione elettrolitica. Gli equilibri in soluzione costituiscono quindi una classe di reazioni molto importanti.
Una soluzione tampone contiene quindi una coppia acidobase
 Soluzioni tampone Un tampone è una soluzione che varia in maniera trascurabile il proprio ph in seguito all aggiunta di quantità moderate di un acido o di una base forte. Se ad un litro di acqua pura vengono
Soluzioni tampone Un tampone è una soluzione che varia in maniera trascurabile il proprio ph in seguito all aggiunta di quantità moderate di un acido o di una base forte. Se ad un litro di acqua pura vengono
Acidi e Basi. Capitolo 15
 Acidi e Basi Capitolo 15 Acidi Hanno un sapore agro. L aceto deve il suo sapore all acido acetico Gli agrumi contengono acido citrico. Provocano il cambio di colore nei coloranti vegetali. Reagiscono con
Acidi e Basi Capitolo 15 Acidi Hanno un sapore agro. L aceto deve il suo sapore all acido acetico Gli agrumi contengono acido citrico. Provocano il cambio di colore nei coloranti vegetali. Reagiscono con
ACIDI e BASI. Definizione di Brønsted-Lowry (non solo limitata alle soluzioni acquose)
 ACIDI e BASI Definizione di Brønsted-Lowry (non solo limitata alle soluzioni acquose) ACIDO = Sostanza in grado di donare ioni H + (protoni o ioni idrogeno) BASE = Sostanza in grado di accettare ioni H
ACIDI e BASI Definizione di Brønsted-Lowry (non solo limitata alle soluzioni acquose) ACIDO = Sostanza in grado di donare ioni H + (protoni o ioni idrogeno) BASE = Sostanza in grado di accettare ioni H
Acidi e basi sono sostanze note da molto tempo e diverse classificazioni sono state fatte nel corso del tempo in base alle loro proprietà.
 TEORIE ACIDO-BASE Acidi e basi sono sostanze note da molto tempo e diverse classificazioni sono state fatte nel corso del tempo in base alle loro proprietà. Teoria di Arrhenius Arrhenius fu il primo a
TEORIE ACIDO-BASE Acidi e basi sono sostanze note da molto tempo e diverse classificazioni sono state fatte nel corso del tempo in base alle loro proprietà. Teoria di Arrhenius Arrhenius fu il primo a
Olimpiadi di Chimica
 Olimpiadi di Chimica Acqua Oro Zucchero Acidi e basi Una soluzione è una miscela omogenea di 2 o più sostanze Il soluto è(sono) la(le) sostanza(e) presente(i) in minore quantità Il solvente è la sostanza
Olimpiadi di Chimica Acqua Oro Zucchero Acidi e basi Una soluzione è una miscela omogenea di 2 o più sostanze Il soluto è(sono) la(le) sostanza(e) presente(i) in minore quantità Il solvente è la sostanza
Rene ed equilibrio acido-base
 Rene ed equilibrio acidobase Produzione H Acidi volatili (15.000 mmol/dì) CO 2 H 2 O H 2 CO 3 H HCO 3 non costituisce guadagno H perché CO 2 (volatile) eliminata con la respirazione Acidi fissi, non volatili
Rene ed equilibrio acidobase Produzione H Acidi volatili (15.000 mmol/dì) CO 2 H 2 O H 2 CO 3 H HCO 3 non costituisce guadagno H perché CO 2 (volatile) eliminata con la respirazione Acidi fissi, non volatili
mentre l'acetato di sodio si dissocia completamente:
 Un sistema tampone è un sistema che impedisce (o attuisce) significative variazioni di ph per aggiunta di limitate quantità di acidi o basi. Per poter funzionare in entrambi le direzioni, cioè neutralizzare
Un sistema tampone è un sistema che impedisce (o attuisce) significative variazioni di ph per aggiunta di limitate quantità di acidi o basi. Per poter funzionare in entrambi le direzioni, cioè neutralizzare
Esperienza 4: Preparazione di soluzioni tampone e verifica del potere tamponante
 Esperienza 4: Preparazione di soluzioni tampone e verifica del potere tamponante Soluzione tampone: soluzione il cui ph non varia in modo apprezzabile per piccole aggiunte di acidi o di basi. Inoltre,
Esperienza 4: Preparazione di soluzioni tampone e verifica del potere tamponante Soluzione tampone: soluzione il cui ph non varia in modo apprezzabile per piccole aggiunte di acidi o di basi. Inoltre,
Equilibrio acido-base: il ph è importante
 Equilibrio acido-base: il ph è importante il ph è strettamente controllato il ph influenza l attività enzimatica il ph è diverso nei vari compartimenti: Esempio: stomaco- acido duodeno alcalino Il ph varia
Equilibrio acido-base: il ph è importante il ph è strettamente controllato il ph influenza l attività enzimatica il ph è diverso nei vari compartimenti: Esempio: stomaco- acido duodeno alcalino Il ph varia
Percorso verso l equilibrio
 EQUILIBRI CIMIC Se una o più sostanze, dette reagenti, sono poste nelle condizioni sperimentali adatte, si possono trasformare in altre sostanze, dette prodotti. Durante un processo di reazione chimica,
EQUILIBRI CIMIC Se una o più sostanze, dette reagenti, sono poste nelle condizioni sperimentali adatte, si possono trasformare in altre sostanze, dette prodotti. Durante un processo di reazione chimica,
FORZA DI ACIDI E BASI HA + :B HB + + A
 FORZA DI ACIDI E BASI n La forza di un acido è la misura della tendenza di una sostanza a cedere un protone. n La forza di una base è una misura dell'affinità di un composto ad accettare un protone. n
FORZA DI ACIDI E BASI n La forza di un acido è la misura della tendenza di una sostanza a cedere un protone. n La forza di una base è una misura dell'affinità di un composto ad accettare un protone. n
INTRODUZIONE ALLA BIOCHIMICA
 INTRODUZIONE ALLA BIOCHIMICA Sistema vivente sistema complesso ed altamente organizzato dotato di una composizione chimica determinata e unica grazie a tale composizione chimica al suo interno si formano
INTRODUZIONE ALLA BIOCHIMICA Sistema vivente sistema complesso ed altamente organizzato dotato di una composizione chimica determinata e unica grazie a tale composizione chimica al suo interno si formano
Le variazioni di ph nei liquidi organici devono mantenute entro limiti molto ristretti (mammiferi tra ). La stabilità del ph è insidiata da
 Le variazioni di ph nei liquidi organici devono mantenute entro limiti molto ristretti (mammiferi tra 6.8 7.8). La stabilità del ph è insidiata da acidi forti (solforico, cloridrico e fosforico) prodotti
Le variazioni di ph nei liquidi organici devono mantenute entro limiti molto ristretti (mammiferi tra 6.8 7.8). La stabilità del ph è insidiata da acidi forti (solforico, cloridrico e fosforico) prodotti
1. Le teorie sugli acidi e sulle basi 2. La ionizzazione dell acqua 3. Il ph 4. La forza degli acidi e delle basi 5. Come calcolare il ph di
 Unità 19 Acidi e basi si scambiano protoni 1. Le teorie sugli acidi e sulle basi 2. La ionizzazione dell acqua 3. Il ph 4. La forza degli acidi e delle basi 5. Come calcolare il ph di soluzioni acide e
Unità 19 Acidi e basi si scambiano protoni 1. Le teorie sugli acidi e sulle basi 2. La ionizzazione dell acqua 3. Il ph 4. La forza degli acidi e delle basi 5. Come calcolare il ph di soluzioni acide e
Equilibrio Acido base
 Equilibrio Acido base Acido e base secondo ARRHENIUS Un acido è una sostanza che in soluzione acquosa libera ioni idrogeno HA H + +A - HCl H + + Cl - Un base è una sostanza che in soluzione acquosa libera
Equilibrio Acido base Acido e base secondo ARRHENIUS Un acido è una sostanza che in soluzione acquosa libera ioni idrogeno HA H + +A - HCl H + + Cl - Un base è una sostanza che in soluzione acquosa libera
Interpretazione dell emogasanalisi
 Interpretazione dell emogasanalisi Guglielmo IMBRIACO Gaetano TAMMARO Rianimazione Terapia Intensiva Ospedale MAGGIORE - Bologna A cosa serve l emogasanalisi? Esame rapido Valutare la ventilazione Valutare
Interpretazione dell emogasanalisi Guglielmo IMBRIACO Gaetano TAMMARO Rianimazione Terapia Intensiva Ospedale MAGGIORE - Bologna A cosa serve l emogasanalisi? Esame rapido Valutare la ventilazione Valutare
Acidi e basi di Lewis
 Gli acidi e le basi Acidi e basi di Lewis Acidi di Lewis= specie che possono accettare in compartecipazione una coppia di elettroni da un altra specie. Base di Lewis = specie che può cedere in compartecipazione
Gli acidi e le basi Acidi e basi di Lewis Acidi di Lewis= specie che possono accettare in compartecipazione una coppia di elettroni da un altra specie. Base di Lewis = specie che può cedere in compartecipazione
L EMOGASANALISI. P. Scavalli, M. Vitto, S. Mosillo
 L EMOGASANALISI P. Scavalli, M. Vitto, S. Mosillo EMOGASANALISI Consente la misurazione immediata dei due gas più importanti del sangue e di un terzo parametro fondamentale per la valutazione dell omeostasi
L EMOGASANALISI P. Scavalli, M. Vitto, S. Mosillo EMOGASANALISI Consente la misurazione immediata dei due gas più importanti del sangue e di un terzo parametro fondamentale per la valutazione dell omeostasi
In base all equazione di Henderson-Hasselbalch
 Alterazioni dell equilibrio acidobase In base all equazione di HendersonHasselbalch ph = pk+ log [HCO 3 ] [CO 2 ] Si ha acidosi quando il rapporto HCO 3 /CO 2 diminuisce, causando una diminuzione del ph.
Alterazioni dell equilibrio acidobase In base all equazione di HendersonHasselbalch ph = pk+ log [HCO 3 ] [CO 2 ] Si ha acidosi quando il rapporto HCO 3 /CO 2 diminuisce, causando una diminuzione del ph.
SCOPI DELL EMOGASANALISI
 EMOGASANALISI SCOPI DELL EMOGASANALISI La funzione principale della respirazione è quella di assicurare ossigeno all organismo e di eliminare l eccesso di anidride carbonica. L emogasanalisi arteriosa
EMOGASANALISI SCOPI DELL EMOGASANALISI La funzione principale della respirazione è quella di assicurare ossigeno all organismo e di eliminare l eccesso di anidride carbonica. L emogasanalisi arteriosa
L equilibrio dell acqua
 L equilibrio dell acqua Il ph e la reazione di autoprotolisi dell acqua Corpaci Ivana La molecola dell acqua H O H! L acqua è un composto molecolare covalente! La sua molecola è polare per la differenza
L equilibrio dell acqua Il ph e la reazione di autoprotolisi dell acqua Corpaci Ivana La molecola dell acqua H O H! L acqua è un composto molecolare covalente! La sua molecola è polare per la differenza
Arrhenius. HCl H + + Cl - NaOH Na + + OH -
 Arrhenius Un acido è una sostanza che contiene H ed è in grado di cedere ioni H + e base è una sostanza che ha tendenza a cedere ioni OH - in acqua H 2 O HCl H + + Cl - H 2 O NaOH Na + + OH - Reazione
Arrhenius Un acido è una sostanza che contiene H ed è in grado di cedere ioni H + e base è una sostanza che ha tendenza a cedere ioni OH - in acqua H 2 O HCl H + + Cl - H 2 O NaOH Na + + OH - Reazione
ACIDI e BASI. Teoria di Arrhenius. Un acido è una sostanza che, sciolta in acqua, provoca un aumento della concentrazione degli ioni H +.
 ACIDI e BASI Teoria di Arrhenius Arrhenius fu il primo a proporre una teoria acido-base a partire dal comportamento di queste sostanze in acqua. Un acido è una sostanza che, sciolta in acqua, provoca un
ACIDI e BASI Teoria di Arrhenius Arrhenius fu il primo a proporre una teoria acido-base a partire dal comportamento di queste sostanze in acqua. Un acido è una sostanza che, sciolta in acqua, provoca un
BASI B + H 2 O BH+ + OH. Basi Forti
 BASI Basi Forti B + H 2 O BH+ + OH Consideriamo un idrossido metallico MOH (a concentrazione C b ) che in H 2 O dia: MOH + H 2 O M+ + OH + H 2 O 2 H 2 O OH + H 3 O+ Incognite : [M+], [OH ], [H 3 O+] Equazioni:
BASI Basi Forti B + H 2 O BH+ + OH Consideriamo un idrossido metallico MOH (a concentrazione C b ) che in H 2 O dia: MOH + H 2 O M+ + OH + H 2 O 2 H 2 O OH + H 3 O+ Incognite : [M+], [OH ], [H 3 O+] Equazioni:
Teoria di Lewis. Un acido di Lewis è una specie chimica che può formare un legame covalente accettando una coppia di elettroni da un altra specie.
 Teoria di Lewis Spiega perché alcune reazioni hanno proprietà acidobase pur non avendo idrogeni. Nella teoria di Lewis le reazioni acido-base hanno come protagonista la messa in condivisione di una coppia
Teoria di Lewis Spiega perché alcune reazioni hanno proprietà acidobase pur non avendo idrogeni. Nella teoria di Lewis le reazioni acido-base hanno come protagonista la messa in condivisione di una coppia
legge dell azione di massa: all equilibrio K c = [C] c [D] d / [A] a [B] b = k 1 /k -1
![legge dell azione di massa: all equilibrio K c = [C] c [D] d / [A] a [B] b = k 1 /k -1 legge dell azione di massa: all equilibrio K c = [C] c [D] d / [A] a [B] b = k 1 /k -1](/thumbs/71/65830231.jpg) EQUILIBRIO CHIMICO 1 Consideriamo la reazione chimica seguente: CH 3 COOH + C 2 H 5 OH CH 3 COOC 2 H 5 + H 2 O K c = [estere] [acqua] / [acido] [alcol] K c = costante di equilibrio legge dell azione di
EQUILIBRIO CHIMICO 1 Consideriamo la reazione chimica seguente: CH 3 COOH + C 2 H 5 OH CH 3 COOC 2 H 5 + H 2 O K c = [estere] [acqua] / [acido] [alcol] K c = costante di equilibrio legge dell azione di
[H + ] X [A - ] [ HA ]
![[H + ] X [A - ] [ HA ] [H + ] X [A - ] [ HA ]](/thumbs/81/84332766.jpg) Equazione di Handerson-HasselbalchHasselbalch [H + ] X [A - ] [ HA ] = K [H + ]X[HCO3 - ] [H2C03] = K 1 Composizione aria O 2 = 20.93% CO 2 = 0.03% N 2 + gas nobili = 79.04% Pressione esercitata dai gas
Equazione di Handerson-HasselbalchHasselbalch [H + ] X [A - ] [ HA ] = K [H + ]X[HCO3 - ] [H2C03] = K 1 Composizione aria O 2 = 20.93% CO 2 = 0.03% N 2 + gas nobili = 79.04% Pressione esercitata dai gas
Farmacocinetica. Lo studio di questi quattro processi viene definito come FARMACOCINETICA del farmaco
 Farmacocinetica Affinché un farmaco possa raggiungere il sito d azione ad una concentrazione sufficiente per esercitare il proprio effetto terapeutico specifico deve generalmente essere: assorbito dal
Farmacocinetica Affinché un farmaco possa raggiungere il sito d azione ad una concentrazione sufficiente per esercitare il proprio effetto terapeutico specifico deve generalmente essere: assorbito dal
Emogasanalisi in t.i.
 Emogasanalisi in t.i. 9 volte su 10 6 volte su 10 100 e più alterati rispetto ai v.n. interpretazioni inesatte diagrammi, nomogrammi, equazioni e sistemi di valutazione 100 anni dall equazione di Handerson
Emogasanalisi in t.i. 9 volte su 10 6 volte su 10 100 e più alterati rispetto ai v.n. interpretazioni inesatte diagrammi, nomogrammi, equazioni e sistemi di valutazione 100 anni dall equazione di Handerson
LA MOLE. Si definisce MOLE una quantita di sostanza di un sistema che contiene tante entita elementari quanti sono gli atomi (NA) in 12g di C 12
 LA MOLE Si definisce MOLE una quantita di sostanza di un sistema che contiene tante entita elementari quanti sono gli atomi (NA) in 12g di C 12 NA = 6,022 x 10 23 particelle /mol numero di Avogadro 1 mole
LA MOLE Si definisce MOLE una quantita di sostanza di un sistema che contiene tante entita elementari quanti sono gli atomi (NA) in 12g di C 12 NA = 6,022 x 10 23 particelle /mol numero di Avogadro 1 mole
Acqua: nutriente essenziale
 Acqua: nutriente essenziale Funzioni dell acqua 1. Solvente delle reazioni metaboliche; 2. Regola il volume cellulare; 3. Regola la temperatura corporea; 4. Permette il trasporto dei nutrienti; 5. Permette
Acqua: nutriente essenziale Funzioni dell acqua 1. Solvente delle reazioni metaboliche; 2. Regola il volume cellulare; 3. Regola la temperatura corporea; 4. Permette il trasporto dei nutrienti; 5. Permette
equilibrio acido base
 Alterazioni dell equilibrio equilibrio acidobase In base all equazione di HendersonHasselbalch ph = pk+ log [ ] [CO 2 ] Si ha acidosi quando, per diminuzione del rapporto /CO 2 il ph diminuisce. L acidosi
Alterazioni dell equilibrio equilibrio acidobase In base all equazione di HendersonHasselbalch ph = pk+ log [ ] [CO 2 ] Si ha acidosi quando, per diminuzione del rapporto /CO 2 il ph diminuisce. L acidosi
Appunti di Stechiometria per Chimica
 Appunti di Stechiometria per Chimica Equilibri in soluzione acquosa Teoria degli acidi/basi secondo Brönsted-Lowry Acido una qualunque sostanza che è capace di donare uno ione idrogeno ad un altra sostanza
Appunti di Stechiometria per Chimica Equilibri in soluzione acquosa Teoria degli acidi/basi secondo Brönsted-Lowry Acido una qualunque sostanza che è capace di donare uno ione idrogeno ad un altra sostanza
Parte terza b: Elementi di termodinamica, equilibrio chimico, stati della materia, soluzioni. Prof. Stefano Piotto Università di Salerno
 Parte terza b: Elementi di termodinamica, equilibrio chimico, stati della materia, soluzioni Prof. Stefano Piotto Università di Salerno 1. Definizioni di acido e base (Arrhenius) 2. Coppie coniugate acido-base
Parte terza b: Elementi di termodinamica, equilibrio chimico, stati della materia, soluzioni Prof. Stefano Piotto Università di Salerno 1. Definizioni di acido e base (Arrhenius) 2. Coppie coniugate acido-base
Le variazioni di ph nei liquidi organici devono mantenute entro limiti molto ristretti (mammiferi tra 6.8 7.8). La stabilità del ph è insidiata da
 Le variazioni di ph nei liquidi organici devono mantenute entro limiti molto ristretti (mammiferi tra 6.8 7.8). La stabilità del ph è insidiata da acidi forti (solforico, cloridrico e fosforico) prodotti
Le variazioni di ph nei liquidi organici devono mantenute entro limiti molto ristretti (mammiferi tra 6.8 7.8). La stabilità del ph è insidiata da acidi forti (solforico, cloridrico e fosforico) prodotti
Reazioni in soluzione acquosa
 Reazioni in soluzione acquosa Equazioni ioniche e molecolari Consideriamo le seguente reazione: Ca(OH) 2 (aq) + Na 2 CO 3 (aq) CaCO 3 (s) + 2 NaOH (aq) Essa è scritta come equazione molecolare anche se
Reazioni in soluzione acquosa Equazioni ioniche e molecolari Consideriamo le seguente reazione: Ca(OH) 2 (aq) + Na 2 CO 3 (aq) CaCO 3 (s) + 2 NaOH (aq) Essa è scritta come equazione molecolare anche se
APPARATO RESPIRATORIO
 Corso di Laurea Magistrale in Medicina e Chirurgia Fisiologia Medica A.A. 2017-18 APPARATO RESPIRATORIO Prof. Clara Iannuzzi Dipartimento di Biochimica, Biofisica e Patologia Generale clara.iannuzzi@unicampania.it
Corso di Laurea Magistrale in Medicina e Chirurgia Fisiologia Medica A.A. 2017-18 APPARATO RESPIRATORIO Prof. Clara Iannuzzi Dipartimento di Biochimica, Biofisica e Patologia Generale clara.iannuzzi@unicampania.it
IL PH DELLE SOLUZIONI TAMPONE E BIOCHIMICA
 http://www. IL PH DELLE SOLUZIONI TAMPONE E BIOCHIMICA COSA SONO I TAMPONI? Si definiscono TAMPONI le soluzioni costituite da: a) UN ACIDO DEBOLE IN PRESENZA DI UN SUO SALE ESEMPIO: ACIDO ACETICO ED ACETATO
http://www. IL PH DELLE SOLUZIONI TAMPONE E BIOCHIMICA COSA SONO I TAMPONI? Si definiscono TAMPONI le soluzioni costituite da: a) UN ACIDO DEBOLE IN PRESENZA DI UN SUO SALE ESEMPIO: ACIDO ACETICO ED ACETATO
Costante di dissociazione acida e grado di dissociazione
 Costante di dissociazione acida e grado di dissociazione K a nαnα = Vn(1 α) = n V 2 α (1 α) = 2 cα (1 α) c : concentrazione analitica = rapporto tra numero di moli iniziali dell acido e V della soluzione
Costante di dissociazione acida e grado di dissociazione K a nαnα = Vn(1 α) = n V 2 α (1 α) = 2 cα (1 α) c : concentrazione analitica = rapporto tra numero di moli iniziali dell acido e V della soluzione
Proprietà delle Soluzioni
 Proprietà delle Soluzioni Dissociazione Elettrolitica 2 In soluzione acquosa i composti ionici (sali, idrossidi) ed alcune sostanze polari (acidi) si dissociano in ioni Esempi: NaCl Na + + Cl HNO 3 H +
Proprietà delle Soluzioni Dissociazione Elettrolitica 2 In soluzione acquosa i composti ionici (sali, idrossidi) ed alcune sostanze polari (acidi) si dissociano in ioni Esempi: NaCl Na + + Cl HNO 3 H +
diminuito aumentato I disordini acido-base primari metabolici si riconoscono attraverso la valutazione della concentrazione di HCO3-
 diminuito aumentato I disordini acido-base primari metabolici si riconoscono attraverso la valutazione della concentrazione di HCO3- Risposta compensatoria all acidosi metabolica Compensazione polmonare
diminuito aumentato I disordini acido-base primari metabolici si riconoscono attraverso la valutazione della concentrazione di HCO3- Risposta compensatoria all acidosi metabolica Compensazione polmonare
Corso di Laboratorio Integrato di Chimica Generale BIOTEC-2011 Esercizi Svolti su Equilibri acido-base
 Corso di Laboratorio Integrato di Chimica Generale BIOTEC2011 Esercizi Svolti su Equilibri acidobase 1. Quanto vale il ph di una soluzione 0.1 M di CO 2 se si ritiene che essa non esiste più come tale
Corso di Laboratorio Integrato di Chimica Generale BIOTEC2011 Esercizi Svolti su Equilibri acidobase 1. Quanto vale il ph di una soluzione 0.1 M di CO 2 se si ritiene che essa non esiste più come tale
