Sinossi Prot.GOIM 2802
|
|
|
- Dorotea Marchi
- 7 anni fa
- Visualizzazioni
Transcript
1 1 Sinossi Prot.GOIM 2802 TRATTAMENTO DI I LINEA CON BEVACIZUMAB + FOLFOX4 O XELOX2 NEL CARCINOMA COLORETTALE. STUDIO DI FASE II RANDOMIZZATO Ricercatore responsabile: Evaristo Maiello Dipartimento di Oncoematologia U.O. Oncologia IRCCS Casa Sollievo della Sofferenza Viale Cappuccini San Giovanni Rotondo (FG) Coordinatore: Gabriele Di Maggio U.O.C. Oncologia IRCCS Casa Sollievo della Sofferenza Viale Cappuccini San Giovanni Rotondo (FG)
2 2 Titolo del protocollo: Versione del protocollo Fase Indicazione Obiettivi TRATTAMENTO DI I LINEA CON BEVACIZUMAB + FOLFOX4 O XELOX2 NEL CARCINOMA COLORETTALE. STUDIO DI FASE II RANDOMIZZATO II Carcinoma colorettale localmente avanzato o metastatico non pretrattato Obiettivo Primario: Valutare l efficacia della combinazione Oxaliplatino e Capecitabina bisettimanale (XELOX-2) + bevacizumab misurato in termini di tasso di risposte obiettive nel trattamento del carcinoma colo-rettale avanzato non pretrattato. Obiettivi Secondari: Tollerabilità dello schema Bevacizumab+XELOX2. Sopravvivenza globale. Tempo alla progressione della malattia. Valutazione dei risultati nei pazienti K-ras mutati e non mutati. Valutazione tempo alla progressione e sopravvivenza globale dopo mantenimento con bevacizumab da solo o in combinazione con fluoro pirimidine. Valutazione delle possibili correlazioni tra le determinazioni molecolari dei livelli di espressione dei geni appartenenti al pathway del VEGF e ad esso correlati con la risposta al trattamento con bevacizumab nei pazienti con carcinoma colorettale avanzato non pretrattato. Disegno dello studio E uno studio di fase II randomizzato, multicentrico con la combinazione FOLFOX4 + bevacizumab versus XELOX-2 + bevacizumab in pazienti con carcinoma colorettale avanzato non pretrattati. ll periodo di arruolamento e stimato in 18 mesi. La valutazione della risposta sara effettuata secondo i criteri RECIST. Le valutazioni delle risposte saranno effettuate ogni 4 cicli di trattamento. I pazienti in risposta o stazionarietà di malattia effettueranno massimo 12 cicli in entrambi i bracci. Successivamente verranno randomizzati a ricevere un trattamento di mantenimento con solo bevacizumab o con bevacizumab + fluoropirimidine (capecitabina o fluorouracile folinico potenziato secondo lo schema de Gramont). Numerosità campionaria prevista No. totale dei centri 88 pazienti per il braccio sperimentale e 44 per il braccio di controllo e quindi132 pazienti in totale. Circa 40 centri
3 3 Criteri di selezione Regime farmacologico Pazienti naive (prima linea) con carcinoma colorettale localmente avanzato o metastatico. Braccio A Oxaliplatino 85 mg/mq diluito in 500 ml di soluzione glucosata al 5% in infusione di 120 minuti, giorno 1; Acido Folinico 100 mg/mq e.v.diluito in 500 ml soluzione glucosata durata 120 min giorni 1-2 5Fluorouracile 400 mg/mq e.v. push giorni 1-2 5Fluorouracile 600 mg/mq in soluzione fisiologica 500 ml in infusione continua oppure giorni 1-2 oppure in pompa elastomerica two days. a 90 minuti giorno 1. La prima somministrazione va fatta dopo la chemioterapia, le successive indifferentemente prima o dopo. Braccio B Oxaliplatino 100 mg/mq diluito in 500 ml di soluzione glucosata al 5% in infusione di 120 minuti, giorno 1; Capecitabina 2000 mg/mq per os in due somministrazioni giornaliere, dal giorno 1 al giorno 7; a 90 minuti giorno 1. prima somministrazione va fatta prima della chemioterapia, le successive indifferentemente prima o dopo la chemioterapia Terapia di mantenimento I pazienti in risposta e/o stazionarietà dopo 12 cicli verranno randomizzati in ulteriori due bracci di trattamento e precisamente: Braccio C I pazienti continueranno a ricevere la fluoro pirimidina utilizzata nel precedente trattamento chemioterapico. Pertanto i pazienti inizialmente trattati con Folfox riceveranno: C-A Acido Folinico 100 mg/mq e.v.diluito in 500 ml soluzione glucosata durata 120 min giorni 1-2 5Fluorouracile 400 mg/mq e.v. push giorni 1-2 5Fluorouracile 600 mg/mq in soluzione fisiologica 500 ml in infusione continua oppure giorni 1-2 oppure in pompa elastomerica two days a 90 minuti giorno 1. I pazienti inizialmente trattati con Xelox2 riceveranno: C-B Capecitabina 2000 mg/mq per os in due somministrazioni giornaliere,
4 4 dal giorno 1 al giorno7; a 90 minuti giorno 1. Braccio D a 90 minuti giorno 1. CRITERI DI INCLUSIONE Diagnosi istologica di carcinoma del colon-retto Determinazione stato mutazionale di K-ras ; Presenza di malattia misurabile; Nessun precedente trattamento chemioterapico di prima linea (e ammesso un trattamento chemioterapico adiuvante, purche terminato da almeno 6 mesi); Performance status ECOG 0-1 Eta compresa tra 18 e 75 anni; Aspettativa di vita > 3 mesi; Adeguata funzionalita renale (creatinina < 1,5 mg/dl), epatica (transaminasi < 2,5xN in assenza e < 5xN in presenza di metastasi epatiche) e midollare (neutrofili > 2.000/mm3 e piastrine > /mm3); Proteinuria con stick urinario <2+, se 2+ occorre eseguire dosaggio della proteinuria delle 24 ore ed essere <1 gr di proteine nelle urine delle 24 ore. Consenso informato scritto. CRITERI DI ESCLUSIONE Presenza di metastasi cerebrali; Precedente trattamento chemioterapico di prima linea ; Precedente neoplasia maligna ad eccezione del basalioma cutaneo e del carcinoma in situ della cervice uterina purche adeguatamente trattati;,anamnesi di infarto acuto del miocardio negli ultimi 12 mesi o segni clinici rilevanti di coronaropatia; Presenza di infarto in fase attiva, scompenso cardiaco o grave aritmia non controllata farmacologicamente; Occlusione intestinale acuta o subacuta o anamnesi di malattia infiammatoria del colon; Pazienti con neuropatia periferica (NCI CTC 1); Reazioni allergiche di grado 3-4 note ai componenti del trattamento Evidenza di diatesi emorragica o coagulopatia
5 5 Principali parametri di safety Principali parametri di efficacia Procedure Ipertensione arteriosa non controllata Radioterapia nelle 4 settimane prima dell inizio dello studio Assunzione a scopo terapeutico da meno di 10 giorni di anticoagulanti Assunzione cronica giornaliera di aspirina a dosi elevate (>325 mg/day) Procedure chirurgiche, biopsia a cielo aperto o significativi traumi entro i 28 giorni dall inizio dello studio Neuropatia periferica sintomatica grado 1 secondo i NCI Common Toxoicity Criteria. Eventi avversi, parametri di laboratorio. Tutti gli eventi avversi saranno classificati per gravità utilizzando gli NCI Common Toxicity Criteria version 3.0 Risposta completa (CR): scomparsa completa di tutte le lesioni precedentemente rilevabili per un periodo di almeno 28 giorni, e nessuna nuova lesione. Risposta parziale (PR): riduzione di più del 30% della somma dei diametri massimi di tutte le lesioni target per un periodo di almeno 28 giorni, e nessuna nuova lesione. Malattia stabile (SD): riduzione non sufficiente per la definizione di PR, o incremento non sufficiente per la definizione di PD. Progressione di malattia (PD): aumento di più del 20% della somma dei diametri maggiori delle lesioni target, o comparsa di malattia in qualunque sede. La sopravvivenza libera da progressione (PFS) sarà calcolata dal primo giorno di trattamento fino alla prima osservazione di progressione di malattia, al decesso per qualunque causa o all ultima data nella quale il paziente risultava libero da progressione o vivo. La sopravvivenza globale (OS) sarà calcolata come il tempo tra il primo giorno di trattamento e la data di decesso o l ultima data in cui il paziente risultava vivo. Al basale: Anamnesi completa, ECOG PS, esame obiettivo (compresi esame neurologico, altezza e peso) e parametri vitali (compresi pressione ematica e polso) ECG Parametri ematochimici: bilirubina (totale e diretta), ASAT, ALAT, fosfatasi alcalina, albumina, LDH, creatinina sierica, glucosio, elettroliti (sodio, potassio), calcio, test di gravidanza (se indicato). Esame emocromocitometrico, con conta ematica completa e differenziale. International normalized ratio (INR)/Tempo di tromboplastina parziale attivata (APTT). Stick urinario per proteinuria Radiografia del torace Tomografia Computerizzata o Risonanza Magnetica di torace/addome
6 6 Procedura di randomizzazione Statistical considerations Consenso informato scritto. Prelievo determinazioni molecolari (vedi manuale parte biologica ) previo consenso. Durante il trattamento- ogni ciclo: Parametri ematochimici Esame emocromocitometrico, con conta ematica completa e differenziale Stick urinario per proteinuria Valutazione della tossicità Esame obiettivo e parametri vitali Durante il trattamento Ogni 4 cicli ECG (se clinicamente indicato) ECOG PS Valutazione del tumore con la stessa metodica utilizzata al basale. Prelievo determinazioni molecolari (vedi manuale parte biologica )previo consenso. Follow up a lungo termine - Ogni 3 mesi Valutazione del tumore Sopravvivenza Scheda generale di randomizzazione da inviare al momento dell inserimento in studio della paziente al centro coordinatore Le caratteristiche di base dei pazienti reclutati verranno riportate come numerosità totale, media ±deviazione standard, mediana e range interquartile o frequenze e percentuali a seconda della natura della variabile. Eventuali differenze al baseline tra gruppi saranno statisticamente verificate con l utilizzo del test Chi-quadrato o del test esatto di Fisher per variabili categoriche e con l utilizzo del Mann-Whitney U-test, del Kruskall-Wallis test, del t-test e dell ANOVA per quelle continue. La scelta di applicare test parametrici o non-parametrici sarà conseguente ai risultati dei test di normalità di Shapiro-Wilk e di Kolmogorov-Smirnov, oltreché dall analisi grafica dell istogramma e della densità stimata con un kernel non-parametrico. Saranno possibili trasformazioni affini dei dati con lo scopo di catturare una possibile normalità nella distribuzione degli stessi. La sopravvivenza totale verrà misurata dalla data di randomizzazione alla data di morte per qualsiasi causa. Il tempo alla progressione di malattia verrà misurato dalla data di randomizzazione alla prima evidenza di progressione di malattia od alla data di morte se non nessuna progressione verrà documentata prima. I modelli statistici di sopravvivenza verranno stimati usando il metodo di Kaplan-Meier e la diversità tra gruppi attraverso il log-rank test. Il modello a rischi proporzionali di Cox verrà utilizzato per stimare modelli multivariati: i rischi verranno presentati in termini di hazard ratio con relativi intervalli di confidenza al 95%. Differenziali di risposta al trattamento verranno stimati attraverso opportuni utilizzi del modello lineare generalizzato.
7 7 I risultati saranno considerati statisticamente significativi per valori di p- value minori di Le analisi verranno condotte mediante l utilizzo del software SAS (Versione 9.1, SAS Institute, Cary, NC, USA) e il software R - Language and environment for statistical computing (Versione 2.8.1). Durata dello studio Periodo di reclutamento: 18 mesi Follow up: 24 mesi
8 8
II GOIM Prof. Giuseppe Colucci Direttore Dipartimento Oncologia Medica Istituto Tumori G.PaoloII, Bari
 1 Sinossi TITOLO FASE CLINICA SPONSOR CENTRO COORDINATORE AREA TERAPEUTICA OBIETTIVI Strategia terapeutica ottimale nei pazienti con tumore del colon-retto metastatico K ras wild type: cetuximab in associazione
1 Sinossi TITOLO FASE CLINICA SPONSOR CENTRO COORDINATORE AREA TERAPEUTICA OBIETTIVI Strategia terapeutica ottimale nei pazienti con tumore del colon-retto metastatico K ras wild type: cetuximab in associazione
Gruppo Oncologico Nord Ovest (G.O.N.O.) Italy. Studio di fase II randomizzato, open-label. Carcinoma Colorettale (CCR) Metastatico
 VERS. PROTOCOLLO 3.0 25 Novembre 2013 SPONSOR FASE STUO INCAZIONE RAZIONALE DELLO STUO Gruppo Oncologico Nord Ovest (G.O.N.O.) Italy Studio di fase II randomizzato, open-label Carcinoma Colorettale (CCR)
VERS. PROTOCOLLO 3.0 25 Novembre 2013 SPONSOR FASE STUO INCAZIONE RAZIONALE DELLO STUO Gruppo Oncologico Nord Ovest (G.O.N.O.) Italy Studio di fase II randomizzato, open-label Carcinoma Colorettale (CCR)
STUDIO GRUPPO ITALIANO PANCREAS GIP-2
 STUDIO ITALIANO MULTICENTRICO RANDOMIZZATO DI FASE III DI CONFRONTO TRA LA COMBINAZIONE DI 5- FLUOROURACILE/ACIDO FOLINICO, OXALIPLATINO E IRINOTECAN (FOLFOXIRI) VERSO GEMCITABINA NEL TRATTAMENTO ADIUVANTE
STUDIO ITALIANO MULTICENTRICO RANDOMIZZATO DI FASE III DI CONFRONTO TRA LA COMBINAZIONE DI 5- FLUOROURACILE/ACIDO FOLINICO, OXALIPLATINO E IRINOTECAN (FOLFOXIRI) VERSO GEMCITABINA NEL TRATTAMENTO ADIUVANTE
EMR Merck KGaA, Darmstadt, Germania. Fase clinica IIIb
 1/7 Sinossi Titolo della Numero della NEXT NSCLC ErbituX Trial Sperimentazione in aperto, randomizzata, multinazionale, di fase IIIb, di valutazione dell attività e della sicurezza di cetuximab come terapia
1/7 Sinossi Titolo della Numero della NEXT NSCLC ErbituX Trial Sperimentazione in aperto, randomizzata, multinazionale, di fase IIIb, di valutazione dell attività e della sicurezza di cetuximab come terapia
SINOSSI DEL PROTOCOLLO
 Allegato 13 SINOSSI DEL PROTOCOLLO Studio di fase II, Randomizzato, condotto in doppio cieco, a due bracci paralleli di Vandetanib (ZACTIMA, ZD6474) più Gemcitabina(Gemzar ) o Gemcitabina più Placebo come
Allegato 13 SINOSSI DEL PROTOCOLLO Studio di fase II, Randomizzato, condotto in doppio cieco, a due bracci paralleli di Vandetanib (ZACTIMA, ZD6474) più Gemcitabina(Gemzar ) o Gemcitabina più Placebo come
STUDIO PANDA. Sinossi
 Titolo Studio di fase II randomizzato di prima linea con FOLFO/panitumumab e 5FU/panitumumab in pazienti anziani con carcinoma colorettale metastatico RAS e BRAF wild-type. Versione 2.2 del 18.04.2016
Titolo Studio di fase II randomizzato di prima linea con FOLFO/panitumumab e 5FU/panitumumab in pazienti anziani con carcinoma colorettale metastatico RAS e BRAF wild-type. Versione 2.2 del 18.04.2016
SINOSSI Protocollo MO19390 SAIL
 SINOSSI Protocollo MO19390 SAIL TITOLO INDICAZIONE OBIETTIVI DISEGNO DELLO STUDIO Studio in aperto con bevacizumab (Avastin ) in combinazione con un regime chemioterapico contenente platino per il trattamento
SINOSSI Protocollo MO19390 SAIL TITOLO INDICAZIONE OBIETTIVI DISEGNO DELLO STUDIO Studio in aperto con bevacizumab (Avastin ) in combinazione con un regime chemioterapico contenente platino per il trattamento
Sinossi Protocollo Sperimentale GOIM 21002
 1 Sinossi Protocollo Sperimentale GOIM 21002 STUDIO MULTICENTRICO DI FASE II SULL UTILIZZO DI NANOPARTICLE ALBUMIN- BOUND PACLITAXEL (ABX) IN ASSOCIAZIONE A CAPECITABINA NEL TRATTAMENTO DI PRIMA LINEA
1 Sinossi Protocollo Sperimentale GOIM 21002 STUDIO MULTICENTRICO DI FASE II SULL UTILIZZO DI NANOPARTICLE ALBUMIN- BOUND PACLITAXEL (ABX) IN ASSOCIAZIONE A CAPECITABINA NEL TRATTAMENTO DI PRIMA LINEA
I pazienti saranno valutati ogni 9 settimane di trattamento mediante esame radiologico e la progressione sara valutata secondo i criteri RECIST 1.1.
 Sinossi Numero EudraCT: 2017-004099-71 Titolo Fase dello studio: Centri satelliti: Disegno dello studio: Studio randomizzato di Fase II su Decitabina in combinazione a Carboplatino rispetto al trattamento
Sinossi Numero EudraCT: 2017-004099-71 Titolo Fase dello studio: Centri satelliti: Disegno dello studio: Studio randomizzato di Fase II su Decitabina in combinazione a Carboplatino rispetto al trattamento
STUDIO RANDOMIZZATO DI FASE II CON CARBOPLATINO E PACLITAXEL +/- CETUXIMAB NEL CARCINOMA DELLA CERVICE AVANZATO E/O RECIDIVATO
 Multicentre Italian Trials in Ovarian Cancer MITO CERV-2 STUDIO RANDOMIZZATO DI FASE II CON CARBOPLATINO E PACLITAXEL +/- CETUXIMAB NEL CARCINOMA DELLA CERVICE AVANZATO E/O RECIDIVATO NONA RELAZIONE DI
Multicentre Italian Trials in Ovarian Cancer MITO CERV-2 STUDIO RANDOMIZZATO DI FASE II CON CARBOPLATINO E PACLITAXEL +/- CETUXIMAB NEL CARCINOMA DELLA CERVICE AVANZATO E/O RECIDIVATO NONA RELAZIONE DI
(CRICKET) - EUDRACT Gruppo Oncologico Nord-Ovest (G.O.N.O.)
 APPENDI II: SINOSSI (ITALIAN VERSION) STUDIO DI FASE II, A SINGOLO BRACCIO, DI TERAPIA DI III LINEA CON RECHALLENGE DI CETUIMAB ED IRINOTECANO IN PAZIENTI CON CARCINOMA COLORETTALE METASTATICO KRAS, NRAS
APPENDI II: SINOSSI (ITALIAN VERSION) STUDIO DI FASE II, A SINGOLO BRACCIO, DI TERAPIA DI III LINEA CON RECHALLENGE DI CETUIMAB ED IRINOTECANO IN PAZIENTI CON CARCINOMA COLORETTALE METASTATICO KRAS, NRAS
Sinossi Protocollo LEGA Versione No. 1 Finale, 11 Novembre 2011
 1. SINOSSI 1.1. Identificativi del Protocollo Prodotto: Indicazione: Codice Protocollo: EudraCT No.: 2011-005537-39 Titolo dello Studio: 1.2. Razionale dello Studio Combinazioni chemioterapiche: Epirubicina
1. SINOSSI 1.1. Identificativi del Protocollo Prodotto: Indicazione: Codice Protocollo: EudraCT No.: 2011-005537-39 Titolo dello Studio: 1.2. Razionale dello Studio Combinazioni chemioterapiche: Epirubicina
SINOSSI protocollo 2903 [v. 13 settembre 2009]
![SINOSSI protocollo 2903 [v. 13 settembre 2009] SINOSSI protocollo 2903 [v. 13 settembre 2009]](/thumbs/69/60075672.jpg) GOIM 2903 Titolo dello studio: Cisplatino e Pemetrexed seguita da pemetrexed in mantenimento vs Carboplatino- Paclitaxel e Bevacizumab seguita da Bevacizumab in mantenimento: studio multicentrico randomizzato
GOIM 2903 Titolo dello studio: Cisplatino e Pemetrexed seguita da pemetrexed in mantenimento vs Carboplatino- Paclitaxel e Bevacizumab seguita da Bevacizumab in mantenimento: studio multicentrico randomizzato
STUDIO TRIBE 2 EUDRACT SINOSSI
 EUDRACT 2014-004436-19 Titolo Studio di fase III randomizzato di prima linea con FOLFOXIRI/bevacizumab seguito da reintroduzione di FOLFOXIRI/bevacizumab alla progressione versus prima linea con FOLFOX/bevacizumab
EUDRACT 2014-004436-19 Titolo Studio di fase III randomizzato di prima linea con FOLFOXIRI/bevacizumab seguito da reintroduzione di FOLFOXIRI/bevacizumab alla progressione versus prima linea con FOLFOX/bevacizumab
Farmaci innovativi nel carcinoma colo-rettale
 Incontri Triveneti Padova, 03 dicembre 2015 Farmaci innovativi nel carcinoma colo-rettale Sara Lonardi SS Neoplasie colo-rettali, UOC Oncologia Medica 1 Istituto Oncologico Veneto IRCCS, Padova Anti-angiogenic
Incontri Triveneti Padova, 03 dicembre 2015 Farmaci innovativi nel carcinoma colo-rettale Sara Lonardi SS Neoplasie colo-rettali, UOC Oncologia Medica 1 Istituto Oncologico Veneto IRCCS, Padova Anti-angiogenic
APPENDIX IV: SYNOPSIS (ITALIAN VERSION)
 APPENDIX IV: SYNOPSIS (ITALIAN VERSION) SINOSSI I/XI VERSIONE 1.0 26 Novembre 2011 FASE INDICAZIONE RAZIONALE Fase II randomizzata Carcinoma colorettale metastatico Bevacizumab, anticorpo monoclonale anti-vegf,
APPENDIX IV: SYNOPSIS (ITALIAN VERSION) SINOSSI I/XI VERSIONE 1.0 26 Novembre 2011 FASE INDICAZIONE RAZIONALE Fase II randomizzata Carcinoma colorettale metastatico Bevacizumab, anticorpo monoclonale anti-vegf,
IL CARCINOMA DEL COLON - RETTO METASTICO TRA RICERCA E PRATICA CLINICA: NUOVI AGGIORNAMENTI
 IL CARCINOMA DEL COLON - RETTO METASTICO TRA RICERCA E PRATICA CLINICA: NUOVI AGGIORNAMENTI CAGLIARI CAESAR S HOTEL 10 OTTOBRE 2015 Alessio Cubeddu Manuela Dettori CASO CLINICO N 1 PAZIENTE RAS WT NON
IL CARCINOMA DEL COLON - RETTO METASTICO TRA RICERCA E PRATICA CLINICA: NUOVI AGGIORNAMENTI CAGLIARI CAESAR S HOTEL 10 OTTOBRE 2015 Alessio Cubeddu Manuela Dettori CASO CLINICO N 1 PAZIENTE RAS WT NON
STUDIO DI FASE III RANDOMIZZATO DI PRIMA LINEA CON
 SINOSSI Titolo dello studio Studio TRIPLETE: STUDIO DI FASE III RANDOMIZZATO DI PRIMA LINEA CON mfolfoiri E PANITUMUMAB versus mfolfo6 E PANITUMUMAB IN PAZIENTI CON CARCINOMA COLORETTALE METASTATICO NON
SINOSSI Titolo dello studio Studio TRIPLETE: STUDIO DI FASE III RANDOMIZZATO DI PRIMA LINEA CON mfolfoiri E PANITUMUMAB versus mfolfo6 E PANITUMUMAB IN PAZIENTI CON CARCINOMA COLORETTALE METASTATICO NON
Bevacizumab e Cetuximab nel cancro colorettale metastastico in donne e uomini: Studio Multicentrico Retrospettivo in Toscana
 Bevacizumab e Cetuximab nel cancro colorettale metastastico in donne e uomini: Studio Multicentrico Retrospettivo in Toscana L. Bazzani, E. Terzuoli, S. Giorgi, G. Francini, L. Antonuzzo, F. Di Costanzo,
Bevacizumab e Cetuximab nel cancro colorettale metastastico in donne e uomini: Studio Multicentrico Retrospettivo in Toscana L. Bazzani, E. Terzuoli, S. Giorgi, G. Francini, L. Antonuzzo, F. Di Costanzo,
SINOSSI DEL PROTOCOLLO ML21868
 TITOLO SPONSOR FASE CLINICA INDICAZIONE OBIETTIVI SINOSSI DEL PROTOCOLLO ML21868 Studio clinico randomizzato di fase II con bevacizumab (AVASTIN ) in combinazione con gemcitabina o con dosi ridotte di
TITOLO SPONSOR FASE CLINICA INDICAZIONE OBIETTIVI SINOSSI DEL PROTOCOLLO ML21868 Studio clinico randomizzato di fase II con bevacizumab (AVASTIN ) in combinazione con gemcitabina o con dosi ridotte di
Farmaci sottoposti a monitoraggio Aifa: Tumori Gastroenterici. Dr Andrea Rocchi Oncologia-Foligno
 Farmaci sottoposti a monitoraggio Aifa: Tumori Gastroenterici Dr Andrea Rocchi Oncologia-Foligno Carcinoma del colon: Bevacizumab I e II linea Aflibercept II linea Panitumumab I, II, III linea Carcinoma
Farmaci sottoposti a monitoraggio Aifa: Tumori Gastroenterici Dr Andrea Rocchi Oncologia-Foligno Carcinoma del colon: Bevacizumab I e II linea Aflibercept II linea Panitumumab I, II, III linea Carcinoma
RIASSUNTO DEL PROTOCOLLO
 RIASSUNTO DEL PROTOCOLLO Titolo: Studio a 2-corti di fase II, randomizzato a due dosi di BMS-275183 somministrato secondo una schedula settimanale continua in pazienti affetti da NSCLC già pretrattati.
RIASSUNTO DEL PROTOCOLLO Titolo: Studio a 2-corti di fase II, randomizzato a due dosi di BMS-275183 somministrato secondo una schedula settimanale continua in pazienti affetti da NSCLC già pretrattati.
SINOSSI DEL PROTOCOLLO ML21869
 SINOSSI DEL PROTOCOLLO ML21869 TITOLO SPONSOR FASE CLINICA INDICAZIONE OBIETTIVI DISEGNO DELLO STUDIO NUMERO DI PAZIENTI POPOLAZIONE TARGET Studio randomizzato di fase II su erlotinib (TARCEVA ) o somministrazione
SINOSSI DEL PROTOCOLLO ML21869 TITOLO SPONSOR FASE CLINICA INDICAZIONE OBIETTIVI DISEGNO DELLO STUDIO NUMERO DI PAZIENTI POPOLAZIONE TARGET Studio randomizzato di fase II su erlotinib (TARCEVA ) o somministrazione
Sopravvivenza globale (OS)
 Sinossi Titolo Fase dello studio: Centri satellite: Disegno dello studio: Trattamento in studio Studio randomizzato di fase II con chemioterapia in combinazione a Pembrolizumab (MK-3475) vs chemioterapia,
Sinossi Titolo Fase dello studio: Centri satellite: Disegno dello studio: Trattamento in studio Studio randomizzato di fase II con chemioterapia in combinazione a Pembrolizumab (MK-3475) vs chemioterapia,
Versione PROTOCOLLO DI STUDIO
 Versione 04.06.2012 PROTOCOLLO DI STUDIO Studio randomizzato di fase III di chemio-radioterapia nel carcinoma squamoso dell orofaringe in stadio localmente avanzato: IGRT-IMRT con moderato ipofrazionamento
Versione 04.06.2012 PROTOCOLLO DI STUDIO Studio randomizzato di fase III di chemio-radioterapia nel carcinoma squamoso dell orofaringe in stadio localmente avanzato: IGRT-IMRT con moderato ipofrazionamento
SINOSSI STUDIO IRST ITACa: Italian Trial in Advanced Colorectal Cancer
 SINOSSI STUDIO IRST 153 01 - ITACa: Italian Trial in Advanced Colorectal Cancer Titolo Responsabile dello studio Centri partecipanti Background e razionale Strategia di terapia sistemica nel carcinoma
SINOSSI STUDIO IRST 153 01 - ITACa: Italian Trial in Advanced Colorectal Cancer Titolo Responsabile dello studio Centri partecipanti Background e razionale Strategia di terapia sistemica nel carcinoma
Codice Studio: D7913L00138 Protocollo Versione No: 1 Data: 7 November 2011
 SINOSSI DEL PROTOCOLLO Studio di fase II in aperto, multicentrico, a singolo braccio per indagare l efficacia, la sicurezza e la tollerabilità di Gefitinib 250 mg (IRESSA ) come trattamento ri-sfida in
SINOSSI DEL PROTOCOLLO Studio di fase II in aperto, multicentrico, a singolo braccio per indagare l efficacia, la sicurezza e la tollerabilità di Gefitinib 250 mg (IRESSA ) come trattamento ri-sfida in
Questionario conoscitivo ONCOLOGO. n. questionari compilati: 73
 Questionario conoscitivo ONCOLOGO n. questionari compilati: 73 D1: Quali sono le caratteristiche più frequenti del paziente che la orientano sulla scelta della terapia di combinazione in termini di età
Questionario conoscitivo ONCOLOGO n. questionari compilati: 73 D1: Quali sono le caratteristiche più frequenti del paziente che la orientano sulla scelta della terapia di combinazione in termini di età
Trabectedina nel sarcoma dei tessuti molli. Un analisi retrospettiva TrObs
 Trabectedina nel sarcoma dei tessuti molli. Un analisi retrospettiva TrObs Titolo dello studio: Codice dello studio: Disegno dello studio: Popolazione in studio: Trabectedina nel sarcoma dei tessuti molli.
Trabectedina nel sarcoma dei tessuti molli. Un analisi retrospettiva TrObs Titolo dello studio: Codice dello studio: Disegno dello studio: Popolazione in studio: Trabectedina nel sarcoma dei tessuti molli.
ICON 9 Relazione di Avanzamento 21 GIUGNO 2018 ICON 9
 ICON 9 Studio randomizzato internazionale di fase III per valutare l'efficacia della terapia di mantenimento con olaparib e cediranib o olaparib da solo nei pazienti con carcinoma ovarico recidivato di
ICON 9 Studio randomizzato internazionale di fase III per valutare l'efficacia della terapia di mantenimento con olaparib e cediranib o olaparib da solo nei pazienti con carcinoma ovarico recidivato di
Protocollo ACC Lung. Dott.ssa G. Improta S.I.C. Anatomia Patologica IRCCS-CROB Rionero in Vulture (PZ)
 Protocollo ACC Lung Dott.ssa G. Improta S.I.C. Anatomia Patologica IRCCS-CROB Rionero in Vulture (PZ) ACC: Associazione di ricerca oncologica italiana no-profit ACC Genomics: Programma diagnostico-terapeutico
Protocollo ACC Lung Dott.ssa G. Improta S.I.C. Anatomia Patologica IRCCS-CROB Rionero in Vulture (PZ) ACC: Associazione di ricerca oncologica italiana no-profit ACC Genomics: Programma diagnostico-terapeutico
EudraCT number:
 EudraCT number: 2011-006097-76 Studio randomizzato di fase 3 sull efficacia della terapia locoregionale epatica mediante embolizzazione transarteriosa (TAE) in associazione a terapia medica in pazienti
EudraCT number: 2011-006097-76 Studio randomizzato di fase 3 sull efficacia della terapia locoregionale epatica mediante embolizzazione transarteriosa (TAE) in associazione a terapia medica in pazienti
CASO CLINICO INTERATTIVO: TUMORE DELLO STOMACO. Maria Maddalena Laterza Oncologia Medica Università Degli Studi della Campania L.
 CASO CLINICO INTERATTIVO: TUMORE DELLO STOMACO Maria Maddalena Laterza Oncologia Medica Università Degli Studi della Campania L. Vanvitelli CASO CLINICO M.G., uomo di 67 aa Anamnesi patologica remota:
CASO CLINICO INTERATTIVO: TUMORE DELLO STOMACO Maria Maddalena Laterza Oncologia Medica Università Degli Studi della Campania L. Vanvitelli CASO CLINICO M.G., uomo di 67 aa Anamnesi patologica remota:
STUDY ID: FIL_RENOIR12 EUDRACT NUMBER
 Studio randomizzato multicentrico di fase III con combinazione di Rituximab e Lenalidomide vs solo Rituximab come terapia di mantenimento dopo chemioimmunoterapia con Rituximab e Bendamustina per pazienti
Studio randomizzato multicentrico di fase III con combinazione di Rituximab e Lenalidomide vs solo Rituximab come terapia di mantenimento dopo chemioimmunoterapia con Rituximab e Bendamustina per pazienti
STUDY ID: FIL_RENOIR12 EUDRACT NUMBER
 Studio randomizzato multicentrico di fase III con combinazione di Rituximab e Lenalidomide vs solo Rituximab come terapia di mantenimento dopo chemioimmunoterapia con Rituximab e Bendamustina per pazienti
Studio randomizzato multicentrico di fase III con combinazione di Rituximab e Lenalidomide vs solo Rituximab come terapia di mantenimento dopo chemioimmunoterapia con Rituximab e Bendamustina per pazienti
1 step: 30 pazienti se EFS 40% e TRM 5%
 PROSPETTICO DI FASE II DI TERAPIA MIELOABLATIVA AD ALTE DOSI, CON SUPPORTO DI CELLULE STAMINALI PERIFERICHE, IN PAZIENTI ANZIANI (65 E 75 ANNI) AFFETTI DA LINFOMA NON HODGKIN AGGRESSIVO RECIDIVATO O RESISTENTE
PROSPETTICO DI FASE II DI TERAPIA MIELOABLATIVA AD ALTE DOSI, CON SUPPORTO DI CELLULE STAMINALI PERIFERICHE, IN PAZIENTI ANZIANI (65 E 75 ANNI) AFFETTI DA LINFOMA NON HODGKIN AGGRESSIVO RECIDIVATO O RESISTENTE
SINOSSI DEL PROTOCCOLO
 SINOSSI DEL PROTOCCOLO TITOLO: NUMERO DI PROTOCOLLO: STUDIO DI FASE II,RANDOMIZZATO, MULTICENTRICO, IN DOPPIO CIECO, CONTROLLATO VERSO PLACEBO, PER VALUTARE L'EFFICACIA E LA SICUREZZA DI MetMAb IN COMBINAZIONE
SINOSSI DEL PROTOCCOLO TITOLO: NUMERO DI PROTOCOLLO: STUDIO DI FASE II,RANDOMIZZATO, MULTICENTRICO, IN DOPPIO CIECO, CONTROLLATO VERSO PLACEBO, PER VALUTARE L'EFFICACIA E LA SICUREZZA DI MetMAb IN COMBINAZIONE
O.R.I.A. OSSERVATORIO RICERCA E INNOVAZIONE AZIENDALE. Reggio Emilia 4 giugno 2008
 O.R.I.A. OSSERVATORIO RICERCA E INNOVAZIONE AZIENDALE Reggio Emilia 4 giugno 2008 Protocollo I.R.M.A. Innovazione in Radioterapia Mammaria CARCINOMA DELLA MAMMELLA A BASSO RISCHIO DI RECIDIVA LOCALE: IRRADIAZIONE
O.R.I.A. OSSERVATORIO RICERCA E INNOVAZIONE AZIENDALE Reggio Emilia 4 giugno 2008 Protocollo I.R.M.A. Innovazione in Radioterapia Mammaria CARCINOMA DELLA MAMMELLA A BASSO RISCHIO DI RECIDIVA LOCALE: IRRADIAZIONE
LE TERAPIE MEDICHE DI II LINEA
 LE TERAPIE MEDICHE DI II LINEA Benedetta Urbini U.O. Oncologia AOUFE Direttore Prof. Antonio Frassoldati TERAPIA MEDICA CDT/CMT - Carcinomi differenziati della tiroide (CDT) iodiorefrattari - Carcinoma
LE TERAPIE MEDICHE DI II LINEA Benedetta Urbini U.O. Oncologia AOUFE Direttore Prof. Antonio Frassoldati TERAPIA MEDICA CDT/CMT - Carcinomi differenziati della tiroide (CDT) iodiorefrattari - Carcinoma
31 centri italiani afferenti alla Fondazione Italiana Linfomi
 SINOSSI Study ID FIL_ReRi Eudract N 2015-003371-29 Titolo dello studio Popolazione in studio Farmaco in sperimentazione Studio di fase II della Fondazione Italiana Linfomi (FIL) per valutare la combinazione
SINOSSI Study ID FIL_ReRi Eudract N 2015-003371-29 Titolo dello studio Popolazione in studio Farmaco in sperimentazione Studio di fase II della Fondazione Italiana Linfomi (FIL) per valutare la combinazione
Approssimativamente 20 sperimentatori (oncologi o pneumologi). Approssimativamente 20 centri in tutto il mondo.
 SINOSSI Nome dello sponsor/azienda: Eisai Inc. Riservato alle Autorità Titolo dello studio: N. di protocollo: Sperimentatori: Centri dello studio: Studio in aperto, multicentrico, randomizzato, di fase
SINOSSI Nome dello sponsor/azienda: Eisai Inc. Riservato alle Autorità Titolo dello studio: N. di protocollo: Sperimentatori: Centri dello studio: Studio in aperto, multicentrico, randomizzato, di fase
IV Meeting Uro-Oncologico UP DATE 2016 SUI TUMORI UROLOGICI. Dott.ssa T. Tamburrano Dirigente Medico Oncologia A.O. Marche Nord
 IV Meeting Uro-Oncologico UP DATE 2016 SUI TUMORI UROLOGICI Fano 11-12 Novembre 2016 TUMORE DELLA PROSTATA-MALATTIA METASTATICA- LA TERAPIA DELLA MALATTIA ORMONOSENSIBILE Dott.ssa T. Tamburrano Dirigente
IV Meeting Uro-Oncologico UP DATE 2016 SUI TUMORI UROLOGICI Fano 11-12 Novembre 2016 TUMORE DELLA PROSTATA-MALATTIA METASTATICA- LA TERAPIA DELLA MALATTIA ORMONOSENSIBILE Dott.ssa T. Tamburrano Dirigente
MORTALITÀ A TRENTA GIORNI DALL INTERVENTO PER TUMORE MALIGNO DEL POLMONE PROTOCOLLO OPERATIVO
 MORTALITÀ A TRENTA GIORNI DALL INTERVENTO PER TUMORE MALIGNO DEL POLMONE PROTOCOLLO OPERATIVO - Definizione Per struttura di ricovero o area di residenza: proporzione di morti a trenta giorni dall intervento
MORTALITÀ A TRENTA GIORNI DALL INTERVENTO PER TUMORE MALIGNO DEL POLMONE PROTOCOLLO OPERATIVO - Definizione Per struttura di ricovero o area di residenza: proporzione di morti a trenta giorni dall intervento
Esperienza preliminare. Autori: A. Zeneli, O. Nanni, I. Barlati, R. Tedaldi, L. Cecconetto, A.
 STUDIO DI COORTE PROSPETTICO SU VELOCITÀ E COMPLICANZE DELLE INFUSIONI CISPLATINO-ASSOCIATE ASSOCIATE Esperienza preliminare Autori: A. Zeneli, O. Nanni, I. Barlati, R. Tedaldi, L. Cecconetto, A. Passardi
STUDIO DI COORTE PROSPETTICO SU VELOCITÀ E COMPLICANZE DELLE INFUSIONI CISPLATINO-ASSOCIATE ASSOCIATE Esperienza preliminare Autori: A. Zeneli, O. Nanni, I. Barlati, R. Tedaldi, L. Cecconetto, A. Passardi
Gli studi longitudinali (o di coorte) sono utilizzati: per la stima dell incidenza delle patologie per la stima della mortalità
 Prof.ssa G. Serio, Prof. P. Trerotoli, Cattedra di Statistica Medica, Università di Bari /6 Gli studi longitudinali (o di coorte) sono utilizzati: per la stima dell incidenza delle patologie per la stima
Prof.ssa G. Serio, Prof. P. Trerotoli, Cattedra di Statistica Medica, Università di Bari /6 Gli studi longitudinali (o di coorte) sono utilizzati: per la stima dell incidenza delle patologie per la stima
Scelta della sequenza terapeutica in paziente con mrcc a prognosi intermedia
 Scelta della sequenza terapeutica in paziente con mrcc a prognosi intermedia Dr.ssa Emanuela Fantinel Policlinico GB Rossi, UOC Oncologia manuf86@hotmail.it AIOM Giovani- Neoplasie Genitourinarie, Caso
Scelta della sequenza terapeutica in paziente con mrcc a prognosi intermedia Dr.ssa Emanuela Fantinel Policlinico GB Rossi, UOC Oncologia manuf86@hotmail.it AIOM Giovani- Neoplasie Genitourinarie, Caso
1 Sinossi. Numero dello Studio EMR Numero EudraCT Merck KGaA, Darmstadt, Germania. Studio in IND sì no
 1 Sinossi Titolo dello Studio Cilengitide e cetuximab in combinazione con chemioterapia a base di platino come trattamento di prima linea in pazienti con NSCLC in fase avanzata Studio multicentrico in
1 Sinossi Titolo dello Studio Cilengitide e cetuximab in combinazione con chemioterapia a base di platino come trattamento di prima linea in pazienti con NSCLC in fase avanzata Studio multicentrico in
SINOSSI. EudraCT number Versione del protocollo Version Octobre 2013
 SINOSSI Codice Studio Titolo IELSG38 EudraCT number 2012 004896 38 Versione del protocollo Version 1.3 18 Octobre 2013 Farmaci in studio Sponsor Fase Disegno Coordinatori Studio di fase II di combinazione
SINOSSI Codice Studio Titolo IELSG38 EudraCT number 2012 004896 38 Versione del protocollo Version 1.3 18 Octobre 2013 Farmaci in studio Sponsor Fase Disegno Coordinatori Studio di fase II di combinazione
Oncology Division, Breats Unit Ospedale Perrino, Brindisi, Italy Phone: Fax: Versione n.
 A phase II study of metronomic oral chemotherapy with cyclophosphamide plus capecitabine combined with trastuzumab in advanced breast cancer (GOIM 2905) Oncology Division, Breats Unit Ospedale Perrino,
A phase II study of metronomic oral chemotherapy with cyclophosphamide plus capecitabine combined with trastuzumab in advanced breast cancer (GOIM 2905) Oncology Division, Breats Unit Ospedale Perrino,
Presentazione dell edizione italiana
 Presentazione dell edizione italiana Prefazione xiii xvii 1 Introduzione 1 1.1 Statistica e medicina.......................... 1 1.2 Statistica e matematica........................ 2 1.3 Statistica ed
Presentazione dell edizione italiana Prefazione xiii xvii 1 Introduzione 1 1.1 Statistica e medicina.......................... 1 1.2 Statistica e matematica........................ 2 1.3 Statistica ed
Trattamento medico del carcinoma colo rettale metastatico non candidabile a chirurgia
 Trattamento medico del carcinoma colo rettale metastatico non candidabile a chirurgia Gruppo di Studio sul carcinoma del colon-retto Coordinatore: Patrizia Racca Comitato Estensore: F. Leone, P. Racca,
Trattamento medico del carcinoma colo rettale metastatico non candidabile a chirurgia Gruppo di Studio sul carcinoma del colon-retto Coordinatore: Patrizia Racca Comitato Estensore: F. Leone, P. Racca,
SINOSSI. Studio di Fase II: Obiettivo primario Determinare l attività antitumorale della combinazione in termini di tempo alla progressione
 SINOSSI TITOLO Studio di fase I-II con Lapatinib in combinazione con capecitabina e vinorelbina come seconda linea di trattamento in pazienti con carcinoma mammario con iperespressione di ErbB2 localmente
SINOSSI TITOLO Studio di fase I-II con Lapatinib in combinazione con capecitabina e vinorelbina come seconda linea di trattamento in pazienti con carcinoma mammario con iperespressione di ErbB2 localmente
Relatrice: Elisa Malnis
 ASSISTENZA AL PAZIENTE CON NEOPLASIA DEL COLON Relatrice: Elisa Malnis 1 CRO Avian o SEDI DELLA MALATTIA Neoplasia del piccolo intestino Neoplasia del colon-retto Neoplasia dell ano 2 INCIDENZA CARCINOMA
ASSISTENZA AL PAZIENTE CON NEOPLASIA DEL COLON Relatrice: Elisa Malnis 1 CRO Avian o SEDI DELLA MALATTIA Neoplasia del piccolo intestino Neoplasia del colon-retto Neoplasia dell ano 2 INCIDENZA CARCINOMA
Attività Scientifica AIOM Lazio
 Attività Scientifica AIOM Lazio 2016-2017 SURVEY FERTILITA E SESSUALITA IN ONCOLOGIA Società I taliana di Psico-Oncologia AIGO 237 Questionari 34% 66% Sesso 7% Femmine Maschi 16% 10% 67% Ospedale IRCCS
Attività Scientifica AIOM Lazio 2016-2017 SURVEY FERTILITA E SESSUALITA IN ONCOLOGIA Società I taliana di Psico-Oncologia AIGO 237 Questionari 34% 66% Sesso 7% Femmine Maschi 16% 10% 67% Ospedale IRCCS
BEVACIZUMAB - AVASTIN
 giunta regionale Allegato B al Decreto n. 139 del 3 giugno 2015 pag. 1/8 Regione del Veneto Area Sanità e Sociale RACCOMANDAZIONI EVIDENCE BASED BEVACIZUMAB - AVASTIN Indicazione in esame: Bevacizumab
giunta regionale Allegato B al Decreto n. 139 del 3 giugno 2015 pag. 1/8 Regione del Veneto Area Sanità e Sociale RACCOMANDAZIONI EVIDENCE BASED BEVACIZUMAB - AVASTIN Indicazione in esame: Bevacizumab
Studio multicentrico di Fase II con capecitabina in monochemioterapia nel trattamento del carcinoma dell ovaio resistente o refrattario al platino
 Multicentre Italian Trials in Ovarian Cancer MITO-6 Studio multicentrico di Fase II con capecitabina in monochemioterapia nel trattamento del carcinoma dell ovaio resistente o refrattario al platino TERZA
Multicentre Italian Trials in Ovarian Cancer MITO-6 Studio multicentrico di Fase II con capecitabina in monochemioterapia nel trattamento del carcinoma dell ovaio resistente o refrattario al platino TERZA
Sinossi Studio MAS TITOLO DELLO STUDIO CODICE DELLO STUDIO
 Sinossi Studio MAS TITOLO DELLO STUDIO CODICE DELLO STUDIO SPONSOR BACKGROUND E RAZIONALE Misura dei livelli di anticoagulazione in pazienti con fibrillazione atriale in trattamento con farmaci anticoagulanti
Sinossi Studio MAS TITOLO DELLO STUDIO CODICE DELLO STUDIO SPONSOR BACKGROUND E RAZIONALE Misura dei livelli di anticoagulazione in pazienti con fibrillazione atriale in trattamento con farmaci anticoagulanti
viii Indice generale
 Indice generale 1 Introduzione al processo di ricerca 1 Sommario 1 Il processo di ricerca 3 Concetti e variabili 5 Scale di misura 8 Test di ipotesi 10 Evidenza empirica 10 Disegni di ricerca 11 Sintesi
Indice generale 1 Introduzione al processo di ricerca 1 Sommario 1 Il processo di ricerca 3 Concetti e variabili 5 Scale di misura 8 Test di ipotesi 10 Evidenza empirica 10 Disegni di ricerca 11 Sintesi
Gruppo Italiano per lo Studio dei Linfomi
 Gruppo Italiano per lo Studio dei Linfomi PROTOCOLLO: R-COMP05 STUDIO DI FASE II PER IL TRATTAMENTO DI PAZIENTI CON LINFOMA MARGINALE SPLENICO CON LA COMBINAZIONE DI CICLOFOSFAMIDE, VINCRISTINA, DOXORUBICINA
Gruppo Italiano per lo Studio dei Linfomi PROTOCOLLO: R-COMP05 STUDIO DI FASE II PER IL TRATTAMENTO DI PAZIENTI CON LINFOMA MARGINALE SPLENICO CON LA COMBINAZIONE DI CICLOFOSFAMIDE, VINCRISTINA, DOXORUBICINA
STUDIO CLINICO di Fase II MYETT MYocet Endoxan Taxotere Trastuzumab. Sinossi del protocollo
 1 STUDIO CLINICO di Fase II MYETT MYocet Endoxan Taxotere Trastuzumab Sinossi del protocollo Titolo Protocollo: Studio di fase II con doxorubicina liposomiale più ciclofosfamide in associazione a trastuzumab,
1 STUDIO CLINICO di Fase II MYETT MYocet Endoxan Taxotere Trastuzumab Sinossi del protocollo Titolo Protocollo: Studio di fase II con doxorubicina liposomiale più ciclofosfamide in associazione a trastuzumab,
MORTALITÀ A TRENTA GIORNI DALL INTERVENTO PER TUMORE MALIGNO DEL FEGATO PROTOCOLLO OPERATIVO
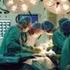 MORTALITÀ A TRENTA GIORNI DALL INTERVENTO PER TUMORE MALIGNO DEL FEGATO PROTOCOLLO OPERATIVO - Definizione Per struttura di ricovero o area di residenza: proporzione di morti a trenta giorni dall intervento
MORTALITÀ A TRENTA GIORNI DALL INTERVENTO PER TUMORE MALIGNO DEL FEGATO PROTOCOLLO OPERATIVO - Definizione Per struttura di ricovero o area di residenza: proporzione di morti a trenta giorni dall intervento
STUDIO PROSPETTICO OSSERVAZIONALE MULTICENTRICO SUL TRATTAMENTO DI PAZIENTI AFFETTI DA LEUCEMIA MIELOIDE ACUTA CON ETA SUPERIORE OD UGUALE A 65 ANNI
 STUDIO PROSPETTICO OSSERVAZIONALE MULTICENTRICO SUL TRATTAMENTO DI PAZIENTI AFFETTI DA LEUCEMIA MIELOIDE ACUTA CON ETA SUPERIORE OD UGUALE A 65 ANNI Dott. Marino Clavio Ospedale Policlinico S Martino-IST
STUDIO PROSPETTICO OSSERVAZIONALE MULTICENTRICO SUL TRATTAMENTO DI PAZIENTI AFFETTI DA LEUCEMIA MIELOIDE ACUTA CON ETA SUPERIORE OD UGUALE A 65 ANNI Dott. Marino Clavio Ospedale Policlinico S Martino-IST
U.O. di Radioterapia Oncologica Ospedale Clinicizzato SS. Annunziata, Chieti
 Saide Di Biase Accuratezza delle immagini RM acquisite in diffusione nella valutazione precoce della risposta al trattamento radio chemioterapico in pazienti con tumore del retto localmente avanzato. U.O.
Saide Di Biase Accuratezza delle immagini RM acquisite in diffusione nella valutazione precoce della risposta al trattamento radio chemioterapico in pazienti con tumore del retto localmente avanzato. U.O.
Uso di etanolo nell'embolizzazione trans-arteriosa (TAELE) in miscela 1:1 con lipiodol VS TACE nell HCC: Studio di tossicità e sopravvivenza
 S.C. RADIOLOGIA INTERVENTISTICA DIRETTORE PROF. FRANCESCO FIORE Uso di etanolo nell'embolizzazione trans-arteriosa (TAELE) in miscela 1:1 con lipiodol VS TACE nell HCC: Studio di tossicità e sopravvivenza
S.C. RADIOLOGIA INTERVENTISTICA DIRETTORE PROF. FRANCESCO FIORE Uso di etanolo nell'embolizzazione trans-arteriosa (TAELE) in miscela 1:1 con lipiodol VS TACE nell HCC: Studio di tossicità e sopravvivenza
Benefici e rischi della terapia neoadiuvante
 METASTASI EPATICHE DA CANCRO COLO-RETTALE Benefici e rischi della terapia neoadiuvante Dr.ssa Alessandra Auriemma Oncologia A.O.U.I. Verona CURA DELLE METASTASI EPATICHE DA CANCRO COLO-RETTALE QUESTIONE
METASTASI EPATICHE DA CANCRO COLO-RETTALE Benefici e rischi della terapia neoadiuvante Dr.ssa Alessandra Auriemma Oncologia A.O.U.I. Verona CURA DELLE METASTASI EPATICHE DA CANCRO COLO-RETTALE QUESTIONE
Studio di fase II con Ribomustin in combinazione con Bortezomib e Rituximab (WM-BBR)
 Studio di fase II con Ribomustin in combinazione con Bortezomib e Rituximab (WM-BBR) in pazienti affetti da linfoma non Hodgkin linfoplasmocitico/morbo di Waldenstrom in seconda linea. Lorella Orsucci
Studio di fase II con Ribomustin in combinazione con Bortezomib e Rituximab (WM-BBR) in pazienti affetti da linfoma non Hodgkin linfoplasmocitico/morbo di Waldenstrom in seconda linea. Lorella Orsucci
Ictus Acuto: Fase di Ospedalizzazione (Diagnosi) Ictus Cerebrale: Linee Guida Italiane di Prevenzione e Trattamento
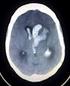 Ictus Acuto: Fase di Ospedalizzazione (Diagnosi) Ictus Cerebrale: Linee Guida Italiane di Prevenzione e Trattamento L'approccio clinico al paziente con sospetto ictus cerebrale che arriva in ospedale deve
Ictus Acuto: Fase di Ospedalizzazione (Diagnosi) Ictus Cerebrale: Linee Guida Italiane di Prevenzione e Trattamento L'approccio clinico al paziente con sospetto ictus cerebrale che arriva in ospedale deve
Le recidive e il loro trattamento
 PDTA nel K del colon-retto Le recidive e il loro trattamento Dott. Gaetano Auletta CPSI Oncologia AOU NOVARA AFD Carla Rigo CAD Dip. Oncologico AOU Novara Dati epidemiologici Seconda causa di morte per
PDTA nel K del colon-retto Le recidive e il loro trattamento Dott. Gaetano Auletta CPSI Oncologia AOU NOVARA AFD Carla Rigo CAD Dip. Oncologico AOU Novara Dati epidemiologici Seconda causa di morte per
RIAMMISSIONE A TRENTA GIORNI DALL INTERVENTO PER TUMORE MALIGNO DELLA PROSTATA PROTOCOLLO OPERATIVO
 RIAMMISSIONE A TRENTA GIORNI DALL INTERVENTO PER TUMORE MALIGNO DELLA PROSTATA PROTOCOLLO OPERATIVO - Definizione Per struttura di ricovero o area di residenza: proporzione di riammissioni ospedaliere
RIAMMISSIONE A TRENTA GIORNI DALL INTERVENTO PER TUMORE MALIGNO DELLA PROSTATA PROTOCOLLO OPERATIVO - Definizione Per struttura di ricovero o area di residenza: proporzione di riammissioni ospedaliere
Terapia radiorecettoriale in 117 pazienti affetti da carcinoide bronchiale avanzato: efficacia e tossicità a lungo termine
 Terapia radiorecettoriale in 117 pazienti affetti da carcinoide bronchiale avanzato: efficacia e tossicità a lungo termine Annapaola Mariniello (1), Lisa Bodei (1), Silvia Melania Baio (1), Laura Gilardi
Terapia radiorecettoriale in 117 pazienti affetti da carcinoide bronchiale avanzato: efficacia e tossicità a lungo termine Annapaola Mariniello (1), Lisa Bodei (1), Silvia Melania Baio (1), Laura Gilardi
Linee guida AIOM. Giulio Metro S.C. Oncologia Medica Ospedale Santa Maria della Misericordia, Azienda Ospedaliera di Perugia
 Linee guida AIOM Giulio Metro S.C. Oncologia Medica Ospedale Santa Maria della Misericordia, Azienda Ospedaliera di Perugia AIOM Interregionale polmone Roma, 21-22.9.18 LG 2018: declinazione del quesito
Linee guida AIOM Giulio Metro S.C. Oncologia Medica Ospedale Santa Maria della Misericordia, Azienda Ospedaliera di Perugia AIOM Interregionale polmone Roma, 21-22.9.18 LG 2018: declinazione del quesito
Studio: Responsabile. Studio INDICE. Pagina 1 di 71
 Pagina 1 di 71 Strategia terapeutica ottimale nei pazienti con tumore del colon-retto metastatico K-ras wild type: cetuximab in associazione con FOLFIRI seguito dal FOLFOX +/- cetuximab. Studio multicentrico
Pagina 1 di 71 Strategia terapeutica ottimale nei pazienti con tumore del colon-retto metastatico K-ras wild type: cetuximab in associazione con FOLFIRI seguito dal FOLFOX +/- cetuximab. Studio multicentrico
Sinossi dello Studio GIMEMA LLC1315
 Studio osservazionale per valutare efficacia e sicurezza dell associazione di bendamustina e rituximab in pazienti affetti da leucemia linfatica cronica. Sinossi dello Studio GIMEMA LLC1315 Clinical Trial
Studio osservazionale per valutare efficacia e sicurezza dell associazione di bendamustina e rituximab in pazienti affetti da leucemia linfatica cronica. Sinossi dello Studio GIMEMA LLC1315 Clinical Trial
Responsabile: Prof. Stefano Milani SINTESI DEL PROTOCOLLO DI STUDIO
 Assegno di Ricerca dal titolo: Sperimentazione, studio, sviluppo e collaudo di nuovi metodi di prevenzione avanzata del cancro al colon-retto mediante colonscopia virtuale in modalità di telediagnosi.
Assegno di Ricerca dal titolo: Sperimentazione, studio, sviluppo e collaudo di nuovi metodi di prevenzione avanzata del cancro al colon-retto mediante colonscopia virtuale in modalità di telediagnosi.
PRI E-R Programma Ricerca e Innovazione Emilia-Romagna
 PRI E-R Programma Ricerca e Innovazione Emilia-Romagna RACCOMANDAZIONI SUL TRATTAMENTO DELLA FASE AVANZATA DEI TUMORI DEL COLON RETTO E STOMACO RACCOMANDAZIONE sull impiego del Bevacizumab in prima linea
PRI E-R Programma Ricerca e Innovazione Emilia-Romagna RACCOMANDAZIONI SUL TRATTAMENTO DELLA FASE AVANZATA DEI TUMORI DEL COLON RETTO E STOMACO RACCOMANDAZIONE sull impiego del Bevacizumab in prima linea
Caso clinico 2: il paziente con carcinoma del colon retto RAS MT
 Dott. Giovanna Manuguerra UOC Ivrea Direttore: Giorgio Vellani Caso clinico 2: il paziente con carcinoma del colon retto RAS MT Anamnesi Uomo di 75 aa alla diagnosi Non fumatore 1 bicchiere di vino ai
Dott. Giovanna Manuguerra UOC Ivrea Direttore: Giorgio Vellani Caso clinico 2: il paziente con carcinoma del colon retto RAS MT Anamnesi Uomo di 75 aa alla diagnosi Non fumatore 1 bicchiere di vino ai
MONOGRAFIA SINTESI. IBRANCE (palbociclib) Carcinoma Mammario. A cura della Commissione Terapeutica Oncologica
 MONOGRAFIA SINTESI IBRANCE (palbociclib) Carcinoma Mammario A cura della Commissione Terapeutica Oncologica 1 SINTESI DELLA VALUTAZIONE 1.1 SINTESI DELLE EVIDENZE Palbociclib è indicato per il trattamento
MONOGRAFIA SINTESI IBRANCE (palbociclib) Carcinoma Mammario A cura della Commissione Terapeutica Oncologica 1 SINTESI DELLA VALUTAZIONE 1.1 SINTESI DELLE EVIDENZE Palbociclib è indicato per il trattamento
Protocollo clinico. Codice dello studio: FIL R2-B Fase II Numero EudraCT: VERSIONE N MARZO 2012
 Fondazione Italiana Linfomi ONLUS Sede legale : piazza Turati 5, 15121 - Alessandria Segreteria: c/o S.C. Ematologia Azienda Ospedaliera Santi Antonio e Biagio e Cesare Arrigo, Via Venezia 16, 15121 Alessandria
Fondazione Italiana Linfomi ONLUS Sede legale : piazza Turati 5, 15121 - Alessandria Segreteria: c/o S.C. Ematologia Azienda Ospedaliera Santi Antonio e Biagio e Cesare Arrigo, Via Venezia 16, 15121 Alessandria
MORTALITÀ A TRENTA GIORNI DALL INTERVENTO PER TUMORE MALIGNO DEL RENE PROTOCOLLO OPERATIVO
 MORTALITÀ A TRENTA GIORNI DALL INTERVENTO PER TUMORE MALIGNO DEL RENE PROTOCOLLO OPERATIVO - Definizione Per struttura di ricovero o area di residenza: proporzione di morti a trenta giorni dall intervento
MORTALITÀ A TRENTA GIORNI DALL INTERVENTO PER TUMORE MALIGNO DEL RENE PROTOCOLLO OPERATIVO - Definizione Per struttura di ricovero o area di residenza: proporzione di morti a trenta giorni dall intervento
Algoritmo per il trattamento dei NETs pancreatici
 Algoritmo per il trattamento dei NETs pancreatici Monza, 06/05/2011 Emilio Bajetta Centro di Riferimento per lo Studio e la Cura dei Carcinoidi e dei Tumori Neuroendocrini S. Oberndorfer e i suoi maestri
Algoritmo per il trattamento dei NETs pancreatici Monza, 06/05/2011 Emilio Bajetta Centro di Riferimento per lo Studio e la Cura dei Carcinoidi e dei Tumori Neuroendocrini S. Oberndorfer e i suoi maestri
MORTALITÀ A TRENTA GIORNI DALL INTERVENTO ISOLATO PER TUMORE MALIGNO DEL RETTO PROTOCOLLO OPERATIVO
 MORTALITÀ A TRENTA GIORNI DALL INTERVENTO ISOLATO PER TUMORE MALIGNO DEL RETTO PROTOCOLLO OPERATIVO - Definizione Per struttura di ricovero o area di residenza: proporzione di morti a trenta giorni dall
MORTALITÀ A TRENTA GIORNI DALL INTERVENTO ISOLATO PER TUMORE MALIGNO DEL RETTO PROTOCOLLO OPERATIVO - Definizione Per struttura di ricovero o area di residenza: proporzione di morti a trenta giorni dall
Caso Clinico Tumore del Colon-Retto
 INTEGRAZIONE TRA ASSISTENZA TERRITORIALE ED OSPEDALIERA Pisa, 14 Novembre 2015 Caso Clinico Tumore del Colon-Retto Carlotta Antoniotti Polo Oncologico Azienda Ospedaliero-Universitaria Pisana Università
INTEGRAZIONE TRA ASSISTENZA TERRITORIALE ED OSPEDALIERA Pisa, 14 Novembre 2015 Caso Clinico Tumore del Colon-Retto Carlotta Antoniotti Polo Oncologico Azienda Ospedaliero-Universitaria Pisana Università
FARMACOECONOMIA NELLA GESTIONE DEL MALATO ONCOLOGICO
 FARMACOECONOMIA NELLA GESTIONE DEL MALATO ONCOLOGICO Analisi dei costi e benefici nel Carcinoma del Colon Prof. Giuseppe Comella Struttura Complessa di Oncologia Medica A Istituto Nazionale Tumori di Napoli
FARMACOECONOMIA NELLA GESTIONE DEL MALATO ONCOLOGICO Analisi dei costi e benefici nel Carcinoma del Colon Prof. Giuseppe Comella Struttura Complessa di Oncologia Medica A Istituto Nazionale Tumori di Napoli
KIDNEY CANCER new options in the first line treatment of metastatic RCC. Axitinib + Pembrolizumab. Francesco Ferraù Oncologia Medica, Taormina
 KIDNEY CANCER new options in the first line treatment of metastatic RCC Axitinib + Pembrolizumab Francesco Ferraù Oncologia Medica, Taormina Axitinib + Pembrolizumab in Pts con Carcinoma Renale Metastatico
KIDNEY CANCER new options in the first line treatment of metastatic RCC Axitinib + Pembrolizumab Francesco Ferraù Oncologia Medica, Taormina Axitinib + Pembrolizumab in Pts con Carcinoma Renale Metastatico
Mortalità a 12 anni in soggetti anziani con insufficienza cardiaca cronica: ruolo della fragilità-mortalità
 Università degli Studi di Napoli Federico II Scuola di Specializzazione in Geriatria Mortalità a 12 anni in soggetti anziani con insufficienza cardiaca cronica: ruolo della fragilità-mortalità D. D Ambrosio,
Università degli Studi di Napoli Federico II Scuola di Specializzazione in Geriatria Mortalità a 12 anni in soggetti anziani con insufficienza cardiaca cronica: ruolo della fragilità-mortalità D. D Ambrosio,
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE Avastin 25 mg/ml concentrato per soluzione per infusione. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Bevacizumab
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 1. DENOMINAZIONE DEL MEDICINALE Avastin 25 mg/ml concentrato per soluzione per infusione. 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Bevacizumab
Università del Piemonte Orientale. Corso di Laurea in Medicina e Chirurgia. Corso di Statistica Medica. I modelli di studio
 Università del Piemonte Orientale Corso di Laurea in Medicina e Chirurgia Corso di Statistica Medica I modelli di studio Corso di laurea in medicina e chirurgia - Statistica Medica Disegno dello studio
Università del Piemonte Orientale Corso di Laurea in Medicina e Chirurgia Corso di Statistica Medica I modelli di studio Corso di laurea in medicina e chirurgia - Statistica Medica Disegno dello studio
Innovatività per i pazienti
 Innovatività per i pazienti Attenzione crescente alla qualità di vita Allungare la speranza di vita post-diagnosi Considerare la qualità del tempo guadagnato Contenere i costi sociali diretti e indiretti
Innovatività per i pazienti Attenzione crescente alla qualità di vita Allungare la speranza di vita post-diagnosi Considerare la qualità del tempo guadagnato Contenere i costi sociali diretti e indiretti
Incidenza, mortalità e sopravvivenza per tumore in Italia nel 2016
 I numeri del cancro in Italia 2016 Ministero della Salute - Roma 27 Settembre 2016 Incidenza, mortalità e sopravvivenza per tumore in Italia nel 2016 Carmine Pinto Presidente Nazionale AIOM Programmare
I numeri del cancro in Italia 2016 Ministero della Salute - Roma 27 Settembre 2016 Incidenza, mortalità e sopravvivenza per tumore in Italia nel 2016 Carmine Pinto Presidente Nazionale AIOM Programmare
CRITERI RECIST E IMAGING
 CRITERI RECIST E IMAGING Negrar 11 ottobre 2017 L. ROMANO E. DEMOZZI CRITERI RECIST 1.1 Tecnica standardizzata per la misura dei Tumori Scopo: garantire l obiettività e ridurre la variabilità inter-osservatore
CRITERI RECIST E IMAGING Negrar 11 ottobre 2017 L. ROMANO E. DEMOZZI CRITERI RECIST 1.1 Tecnica standardizzata per la misura dei Tumori Scopo: garantire l obiettività e ridurre la variabilità inter-osservatore
Dott. Francesco Fiorica
 Dottorato di ricerca XXII ciclo Università degli Studi di Catania: Approccio Oncologico Multimodale in età geriatrica FATTIBILITA ED EFFICACIA DI UN TRATTAMENTO DI RADIOTERAPIA IN PAZIENTI ANZIANI CON
Dottorato di ricerca XXII ciclo Università degli Studi di Catania: Approccio Oncologico Multimodale in età geriatrica FATTIBILITA ED EFFICACIA DI UN TRATTAMENTO DI RADIOTERAPIA IN PAZIENTI ANZIANI CON
Sinossi del Protocollo e Cronologia degli Eventi in Programma nello Studio
 Sinossi del Protocollo e Cronologia degli Eventi in Programma nello Studio Sperimentatore/i, Centro/i di studio: Durata e date dello studio: Titolo: Studio multinazionale di Fase III, randomizzato e in
Sinossi del Protocollo e Cronologia degli Eventi in Programma nello Studio Sperimentatore/i, Centro/i di studio: Durata e date dello studio: Titolo: Studio multinazionale di Fase III, randomizzato e in
PROTOCOLLO DELLO STUDIO
 PROTOCOLLO DELLO STUDIO TITOLO DELLO STUDIO TRATTAMENTO CON IMMUNOGLOBULINE NELLA SINDROME POST-POLIO DISEGNO DELLO STUDIO Studio clinico randomizzato, in doppio cieco, a due bracci (trattamento vs placebo)
PROTOCOLLO DELLO STUDIO TITOLO DELLO STUDIO TRATTAMENTO CON IMMUNOGLOBULINE NELLA SINDROME POST-POLIO DISEGNO DELLO STUDIO Studio clinico randomizzato, in doppio cieco, a due bracci (trattamento vs placebo)
ZACTIMA è un marchio commerciale del gruppo di società AstraZeneca.
 Protocollo di studio clinico Numero edizione 1 Uno studio di fase III, internazionale, randomizzato, in doppio cieco, a gruppi paralleli, multicentrico per valutare l efficacia di ZD6474 (ZACTIMA ) più
Protocollo di studio clinico Numero edizione 1 Uno studio di fase III, internazionale, randomizzato, in doppio cieco, a gruppi paralleli, multicentrico per valutare l efficacia di ZD6474 (ZACTIMA ) più
PROGETTO PROGNOSTICO SUI LINFOMI INDOLENTI NON-FOLLICOLARI
 PROGETTO PROGNOSTICO SUI LINFOMI INDOLENTI NON-FOLLICOLARI SINOSSI NF2010 Sponsor: Coordinatori dello studio: Writing committee: Biostatico: Data Management: Fondazione Italiana Linfomi Luca Arcaini (Pavia)
PROGETTO PROGNOSTICO SUI LINFOMI INDOLENTI NON-FOLLICOLARI SINOSSI NF2010 Sponsor: Coordinatori dello studio: Writing committee: Biostatico: Data Management: Fondazione Italiana Linfomi Luca Arcaini (Pavia)
PROFILASSI ANTITROMBOTICA IN CHIRURGIA GENERALE
 CHIRURGIA GENERALE MAGGIORE (tutti gli interventi di durata > 30 minuti o di chirurgia addominale) TIPO DI PATOLOGIA TIPO DI CHIRURGIA MIRE (tutti gli interventi di durata < 30 minuti, esclusa la chirurgia
CHIRURGIA GENERALE MAGGIORE (tutti gli interventi di durata > 30 minuti o di chirurgia addominale) TIPO DI PATOLOGIA TIPO DI CHIRURGIA MIRE (tutti gli interventi di durata < 30 minuti, esclusa la chirurgia
Commissione Regionale Farmaco LAPATINIB
 Commissione Regionale Farmaco (D.G.R. 1540/2006 e D.G.R. 490 dell 11 aprile 2011) Documento relativo a: LAPATINIB Settembre 2011 Indicazioni registrate Lapatinib Il lapatinib ha ricevuto la seguente estensione
Commissione Regionale Farmaco (D.G.R. 1540/2006 e D.G.R. 490 dell 11 aprile 2011) Documento relativo a: LAPATINIB Settembre 2011 Indicazioni registrate Lapatinib Il lapatinib ha ricevuto la seguente estensione
AMPHOTERICIN B (AMBISOME
 SYNOPSIS Titolo dello Studio LIPOSOMAL AMPHOTERICIN B (AMBISOME ) 10 mg/kg once a week for 10 weeks as maintenance antifungal therapy for Proven/Probable Invasive Fungal Infection in hematologic patients
SYNOPSIS Titolo dello Studio LIPOSOMAL AMPHOTERICIN B (AMBISOME ) 10 mg/kg once a week for 10 weeks as maintenance antifungal therapy for Proven/Probable Invasive Fungal Infection in hematologic patients
SINTESI DEL PROTOCOLLO
 SINTESI DEL PROTOCOLLO Titolo dello studio Studio di Fase 2, randomizzato, multicentrico, in aperto per valutare l efficacia e la sicurezza di Azacitidina sottocutanea somministrata in combinazione con
SINTESI DEL PROTOCOLLO Titolo dello studio Studio di Fase 2, randomizzato, multicentrico, in aperto per valutare l efficacia e la sicurezza di Azacitidina sottocutanea somministrata in combinazione con
Sessione Educazionale Carcinoma Polmonare. Caso Clinico Saper Scegliere. La malattia Oligometastatica ed il miglior approccio terapeutico
 Sessione Educazionale Carcinoma Polmonare Caso Clinico Saper Scegliere. La malattia Oligometastatica ed il miglior approccio terapeutico Marco Filetti Scuola di Specializzazione in Oncologia Medica Università
Sessione Educazionale Carcinoma Polmonare Caso Clinico Saper Scegliere. La malattia Oligometastatica ed il miglior approccio terapeutico Marco Filetti Scuola di Specializzazione in Oncologia Medica Università
