GLI ENZIMI. Gli enzimi sono (quasi sempre) molecole proteiche che catalizzano tutte le reazioni chimiche che avvengono negli organismi viventi.
|
|
|
- Valentina Gianni
- 7 anni fa
- Visualizzazioni
Transcript
1 GLI ENZIMI Gli enzimi sono (quasi sempre) molecole proteiche che catalizzano tutte le reazioni chimiche che avvengono negli organismi viventi. - Sono catalizzatori biologici non vengono alterati dalla reazione che catalizzano ACCELERANO reazioni chimiche fino a volte!!! (efficienza catalitica) accelerazione da catalizzatori non enzimatici: Rendono più moderate le condizioni di reazione altrimenti drastiche per ph, temperatura, pressione
2 GLI ENZIMI. Possono legare altre molecole (cofattori) Agiscono abbassando l energia libera di attivazione Svolgono il loro ruolo con modalità differenti, ma in tutti i casi la catalisi procede attraverso la formazione di complessi tra l'enzima e i reagenti specificità di substrato substrati = reagenti su cui gli enzimi agiscono specificità di reazione (assenza di prodotti secondari) Possono essere regolati in funzione delle specifiche esigenze
3 Che cosa gli enzimi NON fanno: -NON cambiano l equilibrio di una reazione - NON rendono possibile una reazione termodinamicamente impossibile
4
5 -Gli enzimi possono avere dimensioni variabili -Solo una piccola parte della molecola è coinvolta nella catalisi (sito catalitico o sito attivo), ma tutta la molecola è importante per la funzione -Alterazioni a siti distanti dal sito catalitico (anche in un solo aa!!!) possono ridurre o annullare l attività dell enzima Per svolgere la sua funzione l enzima DEVE legare il substrato Formazione di un complesso enzima-substrato (ES)
6 Nomenclatura degli enzimi * Nome del substrato su cui agiscono (o del tipo di reazione che catalizzano) + suffisso asi Es: - ureasi - Alcool deidrogenasi - glucosio 6-fosfato isomerasi - DNA ligasi - esochinasi * Altri come la tripsina e la chimotripsina sono conosciuti dai loro nomi storici.
7 REGOLE PER LA CLASSIFICAZIONE DEGLI ENZIMI La International Union of Biochemistry and Molecular Biology (IUBMB) stabilisce che gli enzimi vengono classificati in base al tipo di reazione chimica che catalizzano
8 NOMENCLATURA DEGLI ENZIMI Classificazione Tipo di reazione catalizzata 1. Ossidoreduttasi Reazioni di ossidoriduzione (deidrogenasi, ossidasi, perossidasi, reduttasi) 2. Trasferasi trasferimento di gruppi funzionali 3. Idrolasi idrolisi 4. Liasi lisi del substrato con formazione di doppi legami (reazioni di eliminazione) 5. Isomerasi isomerizzazione (nella reazione inversa -reazione di addizione - agiscono da sintasi) 6. Ligasi formazione di legami accoppiata all idrolisi di ATP (anche denominate sintetasi ) Gli enzimi sono classificati in accordo al tipo di reazione. Ci sono sei classi principali (con sottoclassi che definiscono il substrato o il legame coinvolto)
9 CLASSI DI ENZIMI
10 No. Classes ENZYME CLASSES AND SUBCLASSES (type of reaction catalyzed) 1 Oxidoreductases (oxidation-reduction reactions) dehydrogenases oxidases oxygenases reductases peroxidases catalases hydroxylases 2 Transferases (transfer of functional groups) transaldolases kinases 3 Hydrolases (hydrolysis reactions) transketolases acyl, methyl, phosphoryl transferases esterases glycosidases peptidases phosphatases phospholipases thiolases amidases ribonucleases 4 Lyases (formation of double bonds) decarboxylases aldolases hydratases dehydratases synthases lyases 5 Isomerases (isomerization reactions) racemases epimerases isomerases 6 Ligases (formation of covalent bonds) synthetases carboxylases
11 UN ESEMPIO DI NOMENCLATURA A ciascun enzima vengono assegnati due nomi e un numero di classificazione: -Nome corrente (es. esochinasi) -Nome sistematico (es: ATP glucosio fosfotransferasi) -Numero di classificazione (es: EC ) Enzyme Commission classe numero di serie sottoclasse sotto-sottoclasse
12 Numero di classificazione [ E C ] classe (reazione catalizzata): trasferasi 2 sottoclasse (substrato o legame coinvolto): fosfotrasferasi 7 trasferimento di un gruppo fosfato sotto-sottoclasse: un gruppo ossidrilico come accettore 1 numero di serie nell ambito della sotto-sottoclasse 1
13 Cofattori e coenzimi Alcuni enzimi esplicano la loro funzione catalitica utilizzando esclusivamente la reattività chimica dei loro residui aminoacidici. Molti enzimi richiedono invece la partecipazione di cofattori o coenzimi che non sono parte della struttura proteica. Cofattore una piccola molecola organica o inorganica (ioni metallici Fe2+, Cu2+, Mg2+, Zn2+) che contribuisce al mantenimento della struttura terziaria dell enzima ed è dunque necessaria per l attività enzimatica. Gli ioni metallici: se debolmente legati (K, Mg, o Ca) partecipano al legame del substrato (enzimi attivati da metallo). se strettamente legati (Fe, Zn, e Co) partecipano direttamente alla reazione (metalloenzimi). Se il cofattore viene rimosso, l enzima assume il nome di apoenzima ed è privo di attività.
14 COFATTORI ORGANICI (COENZIMI) I coenzimi sono molecole organiche. Agiscono come reagenti per il trasferimento di gruppi accettando o donando gruppi funzionali. Derivano spesso da precursori della dieta (vitamine) o da metaboliti. I coenzimi sono chimicamente modificati in seguito alla reazione enzimatica ovvero funzionano come cosubstrati.
15 Oloenzima (attivo) Enzima cofattore Enzima cofattore Apoenzima (inattivo) Il coenzima legato saldamente all enzima attraverso un legame covalente o un legame di coordinazione viene detto gruppo prostetico
16
17 VITAMINE E COENZIMI
18 MOLTI COENZIMI SONO DERIVATI DALLE VITAMINE Coenzyme Reaction catalyzed Vitamin source Thiamine pyrophosphate Flavin adenine dinucleotide Nicotinamide adenine dinucleotide Aldehyde transfersdecarboxilation Oxidation-reduction reactions (electron transfers) Oxidation-reduction reactions (hydride transfers) Thiamine (Vitamin B 1 ) Riboflavin (Vitamin B 2 ) Nicotinamide (niacin) Coenzyme A Acyl transfers Pantothenic acid Pyridoxal phosphate Amino group transfers Pyridoxine (Vitamin B 6 ) Coenzyme B 12 Alkylation reactions Cobalamin (Vitamin B 12 ) Biocytin Carboxylation reactions Biotin Tetrahydrofolic acid One-carbon transfers Folic acid Lipoic acid Acyl transfers
19 Alcuni importanti coenzimi
20
21 Coenzimi NAD + e NADP + Nicotinamide adenin dinucleotide (NAD+) e Nicotinamide adenin dinucleotide fosfato (NADP + ) Derivano dalla vitamina Niacina Svolgono un ruolo nelle reazioni di ossidoriduzione che implicano trasferimenti di due elettroni. NAD + NADH + H + Malato Malato Deidrogenasi Ossalacetato NAD + NADH + H +
22 Coenzimi FMN e FAD Flavin mononucleotide (FMN) e flavin adenine dinucleotide (FAD) Derivano dalla vitamina Riboflavina (B 2 ) Ruolo nelle reazioni di ossidoriduzione che implicano il trasferimento di uno o due elettroni FAD FADH 2 Succinato Succinato Deidrogenasi Fumarato FAD FADH 2
23 ISOENZIMI Gli isoenzimi sono forme distinte di un enzima che hanno la stessa attività catalitica e sono presenti in differenti tipi cellulari o compartimenti subcellulari. Differiscono in: Parametri cinetici; Specificità; ph ottimale; Caratteristiche di carica (pi); Sensibilità all inibizione; Sensibilità al calore (termostabilità). Sono distinguibili elettroforeticamente a causa di una o più sostituzioni amminoacidiche in porzioni non critiche della proteina.
24 Separazione elettroforetica di isoenzimi della lattico deidrogenasi estratti da tessuti diversi LDH 1 + LDH 2 LDH 3 LDH 4 LDH 5 Cuore Rene Fegato Muscolo Siero Origine Per la classificazione degli isoenzimi si inizia dalle specie che hanno la maggiore mobilità elettroforetica verso l anodo.
25 Isoenzimi lattico deidrogenasi LDH NADH + piruvato lattato + NAD LDH-1 (H4) miocardio, eritrociti, rene... LDH-2 (H3M) miocardio, eritrociti, rene, pancreas, polmoni.. LDH-3 (H2M2) polmoni, placenta, pancreas, muscolo scheletrico LDH-4 (HM3) muscolo scheletrico, polmone LDH-5 (M4) fegato, muscolo scheletrico... Differenze tra H M 1aa differenti K M e V max stabilità termica µ elettroforetica
26 Complessi multienzimatici I complessi multienzimatici sono gruppi di enzimi associati mediante legami non covalenti, che catalizzano due o più passaggi successivi lungo una via metabolica. Essi rappresentano un miglioramento dell efficienza catalitica da un punto di vista evolutivo. Migliore catalisi. Riduzione dei tempi di diffusione di un intermedio da un enzima all altro. Channelling del substrato. Permette di trasferire un intemedio di una via biosintetica direttamente ad un altra subunità evitando competizione. Sequestro di intermedi reattivi. Protezione di specie che sarebbero chimicamente instabili in soluzioni acquose. Servicing. Una subunità può trasferire un reagente a differenti altre subunità. Regolazione ed espressione coordinate.
27 COMPLESSO DELLA PIRUVATO DEIDROGENASI E1 piruvato deidrogenasi (24) E2 diidrolipoiltransacetilasi (24) E3 diidrolipoildeidrogenasi (12) In E.coli PM 4600 KDa;negli eucarioti (mitocondri) KDa
28
29 Come funzionano gli enzimi??
30 Il meccanismo d azione degli enzimi può essere trattato da tre punti di vista: -analizzando i cambiamenti energetici che si verificano nel corso della reazione - esaminando il modo in cui il sito attivo favorisce la catalisi dal punto di vista chimico -Studiando la cinetica della reazione catalizzata
31 Cambiamenti energetici che si verificano durante una reazione G = H T S G = variazione dell energia libera. H = variazione dell entalpia S = variazione dell entropia. T= temperatura assoluta. G < 0 (reazione spontanea) G > 0 (reazione non spontanea) G = 0 (reazione in equilibrio) Per avere G < 0: 1) H < 0; S > 0 I due fattori vanno nella stessa direzione. 2) H < 0 ; S < 0 Il fattore entalpico deve prevalere sul quello entropico. 3) H > 0 ; S > 0 Il fattore entropico deve prevalere sul quello entalpico.
32 CENNI DI TERMODINAMICA CHIMICA A + B C + D Quando la reazione è all equilibrio G = 0 K e = [C] c [D] d [A] a [B] b Quando un sistema non è all equilibrio, la forza trainante che all equilibrio è la variazione di energia libera standard, G. lo spinge G = - RT ln [C] [D] [A] [B]
33 ..correlata alla costante di equilibrio dalla relazione: G = RT ln K e Il G di una reazione è un modo matematico alternativo di esprimere la costante di equilibrio, ma non dà informazioni sulla velocità di una reazione G o = variazione di energia libera in condizioni standard Concentrazione: 1 M di reagenti e prodotti Pressione: 1 Atm Temperatura : 298 K (25 C) ph 7
34 Per capire cosa determina la velocità di una reazione bisogna capire cosa accade durante la transizione da reagenti a prodotti
35 Teoria dello stato di transizione: Reazione non catalizzata La teoria dello stato di transizione non prende in considerazione i meccanismi di reazione, ma permette di correlare la velocità di una reazione con la differenza di energia libera di attivazione tra lo stato fondamentale e lo stato di transizione. Lo stato di transizione corrisponde ad una specie chimica instabile con legami non completamente formati e si situa, nel diagramma di reazione, nel picco a più alta energia libera. L energia di attivazione, G ±, rappresenta l energia libera supplementare che le molecole devono possedere per raggiungere lo stato di transizione.
36 La velocità della reazione dipende dal superamento della barriera energetica per il raggiungimento dello stato di transizione in una reazione non catalizzata solo un piccolo numero di molecole possiede energia sufficiente per raggiungere lo stato di transizione
37 Diagramma dell energia libera per una reazione semplice A B. Studio all equilibrio Differenza in energia libera tra lo stato iniziale e quello finale G A e G B rappresentano le energie libere medie per mole delle molecole di A e B. G rappresenta la variazione di energia libera standard della reazione Diagramma dell energia libera esteso a comprendere lo stato di transizione ( ± ) attraverso cui le molecole devono passare per andare da A a B e viceversa. G ± 1 indica l energia di attivazione per la transizione A B; G -1 ± indica l energia di attivazione per la transizione B A G è proprio la differenza tra le variazioni di energia libera dei due stati di attivazione. Una probabile via di transizione di un piranosio (come il glucosio) dalla forma a barca a quella a sedia. Lo stato energetico più elevato (stato di transizione) assomiglierà alla struttura a semisedia
38 Teoria dello stato di transizione Reazione catalizzata Reazione catalizzata Gli enzimi provocano una diminuzione dell energia libera di attivazione ( G # ) dello stato di transizione consentendo che una frazione più ampia di molecole reagenti disponga di sufficiente energia per raggiungere questo più basso stato di transizione. Il catalizzatore abbassa l energia libera dello stato di transizione (ovvero stabilizza lo stato di transizione della reazione catalizzata) in modo che si raggiunga l equilibrio più rapidamente senza alterare l equilibrio della reazione. L effettiva velocità con cui i reagenti sono convertiti in prodotti dipende dalla cinetica
39 Interazione E-S Stato di transizione formazione del prodotto rilascio del prodotto E + S <====> E S ====> E + P Legame di uno o più substrati Abbassamento dell energia dello stato di transizione Promozione dell evento catalitico
40 Come fanno gli enzimi ad abbassare l energia di attivazione?.. meccanismo???... EFFETTI DI LEGAME energia di legame stabilizzazione dello stato di transizione prossimità e tensione EFFETTI CHIMICI catalisi acido-base catalisi covalente
41 Due modelli per spiegare l interazione enzima-substrato MODELLO CHIAVE-SERRATURA. In questo modello il sito attivo dell enzima si adatta al substrato come una chiave in una serratura (Fisher, 1894). MODELLO DELL ADATTAMENTO INDOTTO. In questa elaborazione del modello precedente sia l enzima sia il substrato vengono distorti quando si legano tra loro. Il substrato viene forzato ad assumere una conformazione vicina allo stato di transizione; l enzima mantiene il substrato in tensione (Koshland, 1958)
42 Il cambio conformazionale indotto nell esochinasi L enzima induce la molecola del substrato ad adottare una conformazione simile allo stato di transizione
43 EFFETTI DI LEGAME: Energia di legame Energia di legame = energia che si libera dall interazione enzima-substrato Il numero di interazioni deboli è massimo allo stato di transizione - Massima energia liberata- Le interazioni deboli sono ottimali allo stato di transizione Abbassamento dell energia di attivazione Stabilizzazione dello stato di transizione Specificità di substrato
44 Importanza dello stato di transizione In alcuni casi un catalizzatore lega il substrato in una conformazione che è un intermedio obbligato della reazione, ma che possiede una energia minore grazie al favorevole stato energetico dovuto al legame con il catalizzatore. Il risultato è che due barriere più basse sostituiscono una singola barriera di valore elevato. Lo stato intermedio (di transizione) è uno stato semistabile della molecola Postulato di Hammond: se c e un intermedio instabile, lo stato di transizione gli rassomiglierà e quanto più lo stato di transizione assomiglia al prodotto, tanto più veloce è la reazione.
45 EFFETTI DI LEGAME: Energia di legame; prossimità e orientamento Fattori entropici ed entalpici nella catalisi Un enzima lega due reagenti assicurando un corretto orientamento reciproco, o una distanza opportuna e unendoli più saldamente nello stato di transizione
46 Gruppi funzionali vicini e nel corretto orientamento
47 Punti = elettroni non condivisi Frecce ricurve = movimento della coppia di elettroni (direzione: nucleofilo elettrofilo) Come leggere un meccanismo di reazione Se la freccia va da un atomo a un altro atomo: si forma un nuovo legame tra i due atomi.. Se la freccia va da un legame a un atomo: rottura del legame; gli elettroni compaiono come doppietto non condiviso (o carica negativa) sull atomo indicato dalla freccia Se la freccia va da un legame singolo a un altro legame singolo: si forma un doppio legame C C C C C C
48 GRUPPI NUCLEOFILI ED ELETTROFILI DI RILEVANZA BIOLOGICA
49 EFFETTI CHIMICI Catalisi acido-base il pka della catena laterale degli aa può variare in una proteina
50 Catalisi acido-base
51 EFFETTI CHIMICI Catalisi covalente (Ser, Cys, Glu, Asp, Tyr, His) H 2 O R1-COOH
52 EFFETTI CHIMICI Catalisi covalente Triade catalitica: Asp His - Ser His57: posiziona correttamente il gruppo OH della Ser e ne aumenta la nucleofilicità Asp102: posiziona correttamente His57 e ne aumenta la capacità di accettare protoni
53
54 Triade catalitica: Asp His Ser presente anche in altre proteasi Es: tripsina (specificità: Lys, Arg) elastasi (specificità: amminoacidi con catene laterali piccole (es: Ala, Ser chimotripsina (specificità amminoacidi aromatici, idrofobici voluminosi) Che cosa conferisce specificità?...
55 ENZIMI CHE RICHIEDONO COFATTORI Catalisi da ioni metallici - orientamento del substrato nel sito attivo - stabilizzazione dello stato di transizione - ossidoriduzione
56 Enzimi che richiedono cofattori
57 MECCANISMI GENERALI DI CATALISI IMPIEGATI DAGLI ENZIMI: riepilogo Effetti di legame: 1. Effetti di vicinanza e orientamento 2. Legame preferenziale dell enzima allo stato di transizione rispetto a reagenti e prodotti Effetti chimici: 3. Catalisi acido-base (trasferimento di protoni da un acido o accettazione di protoni da una base) 4. Catalisi covalente (formazione transiente di un legame covalente tra l enzima e il substrato) 5. Catalisi da metalli (favoriscono il corretto orientamento dei substrati, mediano reazioni redox e stabilizzano/schermano cariche opposte)
58
59
Il laboratorio di Biochimica si svolgerà nei seguenti giorni;
 Il laboratorio di Biochimica si svolgerà nei seguenti giorni; Lunedì 7 marzo 2016 Lezione 9-11 aula 1 Martedì 8 marzo Mercoledì 9 marzo ESERCITAZ. Lab. PP1 Giovedì 10 marzo 14:00-18:00 La frequenza è obbligatoria
Il laboratorio di Biochimica si svolgerà nei seguenti giorni; Lunedì 7 marzo 2016 Lezione 9-11 aula 1 Martedì 8 marzo Mercoledì 9 marzo ESERCITAZ. Lab. PP1 Giovedì 10 marzo 14:00-18:00 La frequenza è obbligatoria
Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi.
 ENZIMI Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. Svolgono il loro ruolo con modalità differenti
ENZIMI Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. Svolgono il loro ruolo con modalità differenti
Gli enzimi. Gli enzimi sono le proteine 1 che catalizzano 2 le reazioni chimiche che avvengono nei sistemi biologici
 Gli enzimi Gli enzimi sono le proteine 1 che catalizzano 2 le reazioni chimiche che avvengono nei sistemi biologici 1 con l eccezione dei ribozimi (RNA catalitici) 2 un catalizzatore è una sostanza che
Gli enzimi Gli enzimi sono le proteine 1 che catalizzano 2 le reazioni chimiche che avvengono nei sistemi biologici 1 con l eccezione dei ribozimi (RNA catalitici) 2 un catalizzatore è una sostanza che
ENZIMI. Durante la reazione l enzima può essere temporaneamente modificato ma alla fine del processo ritorna nel suo stato originario, un enzima viene
 ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari, e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari, e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
ENZIMI. Un enzima è un catalizzatore (acceleratore) di reazioni biologiche.
 ENZIMI ENZIMI Un enzima è un catalizzatore (acceleratore) di reazioni biologiche. Catalizzatore = sostanza in grado di accelerare lo svolgimento di una reazione chimica e quindi di aumentarne la sua velocità,
ENZIMI ENZIMI Un enzima è un catalizzatore (acceleratore) di reazioni biologiche. Catalizzatore = sostanza in grado di accelerare lo svolgimento di una reazione chimica e quindi di aumentarne la sua velocità,
catalizzatori biologici RUOLO DEGLI ENZIMI: 16/03/15
 I sistemi viventi sono caratterizzati da un enorme varietà reazioni chimiche la maggior parte delle quali è mediata da una serie di eccezionali CATALIZZATORI BIOLOGICI : GLI ENZIMI L ENZIMOLOGIA E UNA
I sistemi viventi sono caratterizzati da un enorme varietà reazioni chimiche la maggior parte delle quali è mediata da una serie di eccezionali CATALIZZATORI BIOLOGICI : GLI ENZIMI L ENZIMOLOGIA E UNA
Gli enzimi e la catalisi
 Gli enzimi e la catalisi Distribuzione di energia in una popolazione di molecole Normalmente, le molecole stabili sono per lo più presenti ad un livello di energia relativamente basso Solo una piccola
Gli enzimi e la catalisi Distribuzione di energia in una popolazione di molecole Normalmente, le molecole stabili sono per lo più presenti ad un livello di energia relativamente basso Solo una piccola
STRUTTURA E MECCANISMI D AZIONE DEGLI ENZIMI
 STRUTTURA E MECCANISMI D AZIONE DEGLI ENZIMI Confronto tra gli enzimi e i catalizzatori chimici Gli enzimi sono caratterizzati da: Velocità di reazione più elevate Condizioni di reazione più moderate
STRUTTURA E MECCANISMI D AZIONE DEGLI ENZIMI Confronto tra gli enzimi e i catalizzatori chimici Gli enzimi sono caratterizzati da: Velocità di reazione più elevate Condizioni di reazione più moderate
Coenzimi. Ioni essenziali. Molti coenzimi hanno come precursori le vitamine.
 COENZIMI Molti enzimi richiedono l associazione con particolari COFATTORI per poter esplicare la loro attività catalitica. Ioni essenziali Coenzimi Ioni attivatori, Mg 2+, K +, Ca 2+ (legati debolmente)
COENZIMI Molti enzimi richiedono l associazione con particolari COFATTORI per poter esplicare la loro attività catalitica. Ioni essenziali Coenzimi Ioni attivatori, Mg 2+, K +, Ca 2+ (legati debolmente)
CLASSIFICAZIONE O.T.I.L.Is. Lig
 GLI ENZIMI CHE COSA SONO? Sono delle proteine altamente specializzate con attività catalitica, accelerano le reazioni chimiche rimanendo inalterati al termine della reazione stessa. CLASSIFICAZIONE O.T.I.L.Is.
GLI ENZIMI CHE COSA SONO? Sono delle proteine altamente specializzate con attività catalitica, accelerano le reazioni chimiche rimanendo inalterati al termine della reazione stessa. CLASSIFICAZIONE O.T.I.L.Is.
2) La presenza di gruppi funzionali specifici che partecipano alla catalisi (quelli delle catene laterali dei suoi residui amminoacidici e/o quelli
 ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari (sono in grado di aumentare la velocità delle reazioni biologiche anche di 10 20 volte). Durante
ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari (sono in grado di aumentare la velocità delle reazioni biologiche anche di 10 20 volte). Durante
REAZIONI CHIMICHE. Perché una reazione chimica avvenga devono essere soddisfatte tre condizioni: I reagenti (substrati) devono entrare in collisione
 ENZIMI 1 REAZIONI CHIMICHE Perché una reazione chimica avvenga devono essere soddisfatte tre condizioni: 2 I reagenti (substrati) devono entrare in collisione Le collisione tra le molecole dei reagenti
ENZIMI 1 REAZIONI CHIMICHE Perché una reazione chimica avvenga devono essere soddisfatte tre condizioni: 2 I reagenti (substrati) devono entrare in collisione Le collisione tra le molecole dei reagenti
Termodinamica ENTALPIA...6
 Termodinamica ORGANISMI PRIMO VIVENTI ED ENERGIA...2 PRINCIPIO DELLA TERMODINAMICA...5 ENTALPIA...6 SECONDO PRINCIPIO DELLA TERMODINAMICA... 7 energia libera di Gibbs (G)...9 Variazione di energia libera
Termodinamica ORGANISMI PRIMO VIVENTI ED ENERGIA...2 PRINCIPIO DELLA TERMODINAMICA...5 ENTALPIA...6 SECONDO PRINCIPIO DELLA TERMODINAMICA... 7 energia libera di Gibbs (G)...9 Variazione di energia libera
3) La presenza di gruppi funzionali specifici che partecipano alla catalisi (quelli delle catene laterali dei suoi residui amminoacidici e/o quelli
 ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari (sono in grado di aumentare la velocità delle reazioni biologiche anche di 10 20 volte). Durante
ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari (sono in grado di aumentare la velocità delle reazioni biologiche anche di 10 20 volte). Durante
REAZIONI CHIMICHE. Perché una reazione chimica avvenga devono essere soddisfatte tre condizioni: I reagenti (substrati) devono entrare in collisione
 ENZIMI 1 REAZIONI CHIMICHE Perché una reazione chimica avvenga devono essere soddisfatte tre condizioni: 2 I reagenti (substrati) devono entrare in collisione Le collisione tra le molecole dei reagenti
ENZIMI 1 REAZIONI CHIMICHE Perché una reazione chimica avvenga devono essere soddisfatte tre condizioni: 2 I reagenti (substrati) devono entrare in collisione Le collisione tra le molecole dei reagenti
La catalisi enzimatica. Copyright 2013 Zanichelli editore S.p.A.
 La catalisi enzimatica Copyright 2013 Zanichelli editore S.p.A. Le proprietà generali degli enzimi Concetti chiave Gli enzimi si differenziano dai catalizzatori chimici di uso comune per velocità, condizioni,
La catalisi enzimatica Copyright 2013 Zanichelli editore S.p.A. Le proprietà generali degli enzimi Concetti chiave Gli enzimi si differenziano dai catalizzatori chimici di uso comune per velocità, condizioni,
- utilizzano esclusivamente le reattività chimiche di alcuni residui AA
 Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Funzioni dei nucleotidi
 Funzioni dei nucleotidi monomeri degli acidi nucleici esempi di altre funzioni ATP: moneta energetica GTP: fonte di energia nella sintesi proteica camp: secondo messaggero nella trasduzione del segnale
Funzioni dei nucleotidi monomeri degli acidi nucleici esempi di altre funzioni ATP: moneta energetica GTP: fonte di energia nella sintesi proteica camp: secondo messaggero nella trasduzione del segnale
Determinazione dell attività enzimatica
 Determinazione dell attività enzimatica Gli enzimi sono una percentuale rilevante delle proteine cellulari anche se ciascun tipo di enzima è presente nella cellula in quantità molto bassa. Controllano
Determinazione dell attività enzimatica Gli enzimi sono una percentuale rilevante delle proteine cellulari anche se ciascun tipo di enzima è presente nella cellula in quantità molto bassa. Controllano
Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi)
 ENZIMI Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi) Sono in grado di aumentare la velocità dei processi catalizzati fino a
ENZIMI Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi) Sono in grado di aumentare la velocità dei processi catalizzati fino a
Enzimi: catalizzatori biologici
 Enzimi: catalizzatori biologici praticamente tutte le reazioni biochimiche della chimica della vita sono catalizzate da enzimi gli enzimi sono proteine la velocità di reazioni enzimatiche è aumentata di
Enzimi: catalizzatori biologici praticamente tutte le reazioni biochimiche della chimica della vita sono catalizzate da enzimi gli enzimi sono proteine la velocità di reazioni enzimatiche è aumentata di
proteine enzimi RNA ribozimi substrati altamente specifici -asi
 I catalizzatori sono sostanze che aumentano la velocità delle reazioni senza subire modificazioni. Un catalizzatore non induce una reazione che non può avvenire, fa solo in modo che avvenga più velocemente.
I catalizzatori sono sostanze che aumentano la velocità delle reazioni senza subire modificazioni. Un catalizzatore non induce una reazione che non può avvenire, fa solo in modo che avvenga più velocemente.
Regolazione enzimatica Isoenzimi
 Regolazione enzimatica Isoenzimi Gli enzimi regolatori nel metabolismo gruppi di enzimi lavorano insieme per produrre una via metabolica in cui il prodotto del primo enzima diventa il substrato del secondo
Regolazione enzimatica Isoenzimi Gli enzimi regolatori nel metabolismo gruppi di enzimi lavorano insieme per produrre una via metabolica in cui il prodotto del primo enzima diventa il substrato del secondo
I Mitocondri Centrale elettrica cellulare
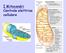 I Mitocondri Centrale elettrica cellulare Potenziale redox standard Fe 2+ D Fe 3+ + e - Fe 2+ + Cu 2+ D Fe 3+ + Cu + Cu 2+ + e - D Cu + Ε = E + RT nf ln [accettore elettroni] [donatore elettroni] n = n
I Mitocondri Centrale elettrica cellulare Potenziale redox standard Fe 2+ D Fe 3+ + e - Fe 2+ + Cu 2+ D Fe 3+ + Cu + Cu 2+ + e - D Cu + Ε = E + RT nf ln [accettore elettroni] [donatore elettroni] n = n
Nicotinamide adenin dinucleotide (NAD + ) H - NMN R AMP. Nel NADP + questo gruppo ossidrilico è esterificato con un gruppo fosforico
 Nicotinamide adenin dinucleotide (NAD + ) H - NMN R AMP Nel NADP + questo gruppo ossidrilico è esterificato con un gruppo fosforico FMN riboflavina. FADH. (FMNH. ) (semichinone) AMP Flavin adenin dinucleotide
Nicotinamide adenin dinucleotide (NAD + ) H - NMN R AMP Nel NADP + questo gruppo ossidrilico è esterificato con un gruppo fosforico FMN riboflavina. FADH. (FMNH. ) (semichinone) AMP Flavin adenin dinucleotide
Via finale comune per l ossidazione di tutti i combustibili metabolici che entrano nella via come molecola di acetil CoA
 Via finale comune per l ossidazione di tutti i combustibili metabolici che entrano nella via come molecola di acetil CoA C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O Processi molecolari in cui è coinvolto il consumo
Via finale comune per l ossidazione di tutti i combustibili metabolici che entrano nella via come molecola di acetil CoA C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O Processi molecolari in cui è coinvolto il consumo
Enzimi = catalizzatori di una reazione biochimica Caratteristiche: Specificità: ogni enzima riconosce specificamente il/i substrato/i e non altre
 Enzimi = catalizzatori di una reazione biochimica Caratteristiche: Specificità: ogni enzima riconosce specificamente il/i substrato/i e non altre molecole, anche chimicamente simili al substrato. Saturabilità:
Enzimi = catalizzatori di una reazione biochimica Caratteristiche: Specificità: ogni enzima riconosce specificamente il/i substrato/i e non altre molecole, anche chimicamente simili al substrato. Saturabilità:
ENZIMI. Molecole proteiche globulari che consentono alle reazioni biochimiche di procedere ad una velocità adeguata alle
 ENZIMI Molecole proteiche globulari che consentono alle reazioni biochimiche di procedere ad una velocità adeguata alle condizioni fisiologiche Aumentano la velocità delle reazioni senza alterarne l equilibrio
ENZIMI Molecole proteiche globulari che consentono alle reazioni biochimiche di procedere ad una velocità adeguata alle condizioni fisiologiche Aumentano la velocità delle reazioni senza alterarne l equilibrio
BIOENERGETICA IL METABOLISMO RISULTA DALL INSIEME DELLE REAZIONI CHIMICHE CHE PERMETTONO AI SISTEMI VIVENTI DI UTILIZZARE ENERGIA E MATERIA
 Cap.15 BIOENERGETICA IL METABOLISMO RISULTA DALL INSIEME DELLE REAZIONI CHIMICHE CHE PERMETTONO AI SISTEMI VIVENTI DI UTILIZZARE ENERGIA E MATERIA I Legge della Termodinamica: Il contenuto energetico dell
Cap.15 BIOENERGETICA IL METABOLISMO RISULTA DALL INSIEME DELLE REAZIONI CHIMICHE CHE PERMETTONO AI SISTEMI VIVENTI DI UTILIZZARE ENERGIA E MATERIA I Legge della Termodinamica: Il contenuto energetico dell
NADH FADH 2 (trasportatori ridotti di elettroni) Catena respiratoria (trasferimento degli
 NADH FADH 2 (trasportatori ridotti di elettroni) Fase 3 Trasferimento degli elettroni e fosforilazione ossidativa Catena respiratoria (trasferimento degli elettroni) Nicotinamide adenin dinucleotide (NAD
NADH FADH 2 (trasportatori ridotti di elettroni) Fase 3 Trasferimento degli elettroni e fosforilazione ossidativa Catena respiratoria (trasferimento degli elettroni) Nicotinamide adenin dinucleotide (NAD
Esempi di funzioni svolte dalle proteine
 Esempi di funzioni svolte dalle proteine Trasporto di sostanze Esempi di funzioni svolte dalle proteine Trasporto di sostanze Funzioni strutturali Esempi di funzioni svolte dalle proteine Trasporto di
Esempi di funzioni svolte dalle proteine Trasporto di sostanze Esempi di funzioni svolte dalle proteine Trasporto di sostanze Funzioni strutturali Esempi di funzioni svolte dalle proteine Trasporto di
Gli enzimi e l inibizione enzimatica.
 Gli enzimi e l inibizione enzimatica. Catalisi enzimatica La velocità di una reazione è descritta dall equazione di Arrhenius: k = Ae -Ea/RT in cui A è il fattore pre-esponenziale R è la costante dei gas
Gli enzimi e l inibizione enzimatica. Catalisi enzimatica La velocità di una reazione è descritta dall equazione di Arrhenius: k = Ae -Ea/RT in cui A è il fattore pre-esponenziale R è la costante dei gas
BIOCHIMICA e BIOTECNOLOGIE degli ALIMENTI
 Seconda Università degli Studi di Napoli DiSTABiF Anno Accademico 2016-17 Corso di Laurea Magistrale in SCIENZE DEGLI ALIMENTI E DELLA NUTRIZIONE UMANA Insegnamento di BIOCHIMICA e BIOTECNOLOGIE degli
Seconda Università degli Studi di Napoli DiSTABiF Anno Accademico 2016-17 Corso di Laurea Magistrale in SCIENZE DEGLI ALIMENTI E DELLA NUTRIZIONE UMANA Insegnamento di BIOCHIMICA e BIOTECNOLOGIE degli
Principi di Biochimica
 Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
BIOLOGIA GENERALE 19 dicembre 2006
 Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE 19 dicembre 2006 Facoltà di Psicologia Corso di Laurea in Scienze e Tecniche di Psicologia Generale e Sperimentale
Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE 19 dicembre 2006 Facoltà di Psicologia Corso di Laurea in Scienze e Tecniche di Psicologia Generale e Sperimentale
2015 /2016. scaricato da
 Enzimi Prof Spina Riabilitativa 2015 /2016 Gli enzimi i sono catalizzatori t i biologici i i molto efficienti: i caratterizzati da potere catalitico e specificità, possegono una porzione dedicata: il
Enzimi Prof Spina Riabilitativa 2015 /2016 Gli enzimi i sono catalizzatori t i biologici i i molto efficienti: i caratterizzati da potere catalitico e specificità, possegono una porzione dedicata: il
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio. GLUCONEOGENESI (sintesi da precursori non glucidici)
 DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) La gluconeogenesi utilizza il piruvato e altri composti a
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) La gluconeogenesi utilizza il piruvato e altri composti a
ENZIMI : catalizzatori biologici
 ENZIMI : catalizzatori biologici 1 Nell organismo sono indispensabili alla vita: per esempio le reazioni chimiche connesse con un singolo respiro, in assenza di enzimi, durerebbero ore. L enzima anidrasi
ENZIMI : catalizzatori biologici 1 Nell organismo sono indispensabili alla vita: per esempio le reazioni chimiche connesse con un singolo respiro, in assenza di enzimi, durerebbero ore. L enzima anidrasi
Come le cellule traggono energia dal cibo: produzione di ATP
 Come le cellule traggono energia dal cibo: produzione di ATP L energia è contenuta nei legami chimici delle molecole nutritive; la cellula estrae questa energia e la conserva nell ATP: respirazione cellulare
Come le cellule traggono energia dal cibo: produzione di ATP L energia è contenuta nei legami chimici delle molecole nutritive; la cellula estrae questa energia e la conserva nell ATP: respirazione cellulare
: : H-Cl + H-N: H-N-H + : Cl : H
 Negli organismi viventi la maggior parte dell energia libera richiesta per promuovere le reazioni biochimiche deriva dall ossidazione dei substrati organici. L ossigeno, l accettore finale degli elettroni
Negli organismi viventi la maggior parte dell energia libera richiesta per promuovere le reazioni biochimiche deriva dall ossidazione dei substrati organici. L ossigeno, l accettore finale degli elettroni
INIBIZIONE ENZIMATICA REVERSIBILE
 INIBIZIONE ENZIMATICA REVERSIBILE La reazione enzimatica in vitro o in vivo può essere INIBITA REVERSIBILMENTE. Un inibitore (I) legandosi all enzima interferisce con la sua attività modificando la Vmax,
INIBIZIONE ENZIMATICA REVERSIBILE La reazione enzimatica in vitro o in vivo può essere INIBITA REVERSIBILMENTE. Un inibitore (I) legandosi all enzima interferisce con la sua attività modificando la Vmax,
ENERGIA LIBERA DI GIBBS (G)
 METABOLISMO: Descrive tutte le numerose reazioni con cui le molecole biologiche sono sintetizzate e degradate, e che permettono di ricavare, accumulare e utilizzare energia Ogni reazione metabolica comporta
METABOLISMO: Descrive tutte le numerose reazioni con cui le molecole biologiche sono sintetizzate e degradate, e che permettono di ricavare, accumulare e utilizzare energia Ogni reazione metabolica comporta
INTRODUZIONE AL METABOLISMO
 INTRODUZIONE AL METABOLISMO METABOLISMO Il metabolismo (dal greco metabolé = trasformazione) è il complesso delle reazioni chimiche coordinate ed integrate che avvengono in una cellula. Il metabolismo
INTRODUZIONE AL METABOLISMO METABOLISMO Il metabolismo (dal greco metabolé = trasformazione) è il complesso delle reazioni chimiche coordinate ed integrate che avvengono in una cellula. Il metabolismo
FADH ADP + Pi ATP...29 AG ' = -30,5 kj/mol...29 Resa di ATP per l ossidazione completa del glucosio...31
 FOSFORILAZIONE OSSIDATIVA FOSFORILAZIONE OSSIDATIVA...1 Glicolisi e ciclo di Krebs...3 il NADH il NADPH e il FADH2 sono traportatori solubili di elettroni...4 LA FOSFORILAZIONE OSSIDATIVA...5 Il mitocondrio...5
FOSFORILAZIONE OSSIDATIVA FOSFORILAZIONE OSSIDATIVA...1 Glicolisi e ciclo di Krebs...3 il NADH il NADPH e il FADH2 sono traportatori solubili di elettroni...4 LA FOSFORILAZIONE OSSIDATIVA...5 Il mitocondrio...5
Catalisi. Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A Modulo di Biologia Strutturale
 Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Catalisi Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie
Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Catalisi Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie
Enzimi come catalizzatori biologici
 Enzimi come catalizzatori biologici Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. La catalisi procede
Enzimi come catalizzatori biologici Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. La catalisi procede
CLASSIFICAZIONE ENZIMI
 CLASSIFICAZIONE ENZIMI nome raccomandato nome sistematico reazione catalizzata Classe di enzima Reazione catalizzata 1. Ossidoreduttasi Ossido-riduzione 2. Transferasi Trasferimento di gruppi funzionali
CLASSIFICAZIONE ENZIMI nome raccomandato nome sistematico reazione catalizzata Classe di enzima Reazione catalizzata 1. Ossidoreduttasi Ossido-riduzione 2. Transferasi Trasferimento di gruppi funzionali
CHIMICA BIOLOGICA. Seconda Università degli Studi di Napoli. DiSTABiF. Corso di Laurea in Scienze Biologiche. Insegnamento di. Anno Accademico
 Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Prof. Antimo Di Maro Anno Accademico 2016-17 Lezione 14 Ciclo di Krebs L ossidazione
Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Prof. Antimo Di Maro Anno Accademico 2016-17 Lezione 14 Ciclo di Krebs L ossidazione
Funzione catalitica delle proteine. Enzimi
 Funzione catalitica delle proteine Enzimi Gli enzimi sono proteine che fungono da catalizzatori delle reazioni chimiche che avvengono nei sistemi biologici concentrazione In una reazione chimica i reagenti
Funzione catalitica delle proteine Enzimi Gli enzimi sono proteine che fungono da catalizzatori delle reazioni chimiche che avvengono nei sistemi biologici concentrazione In una reazione chimica i reagenti
Introduzione allo studio del metabolismo Parte I
 Introduzione allo studio del metabolismo Parte I FOTOTROFI Le piante ed alcuni tipi di batteri ricavano l energia libera dal Sole mediante la fotosintesi, un processo in cui l energia luminosa è convertita
Introduzione allo studio del metabolismo Parte I FOTOTROFI Le piante ed alcuni tipi di batteri ricavano l energia libera dal Sole mediante la fotosintesi, un processo in cui l energia luminosa è convertita
Regolazione dell attività enzimatica. Allosteria Modificazioni covalenti Isoenzimi
 Regolazione dell attività enzimatica Allosteria Modificazioni covalenti Isoenzimi Regolazione della attività enzimatica L attività enzimatica deve potere essere regolata in base alle specifiche richieste
Regolazione dell attività enzimatica Allosteria Modificazioni covalenti Isoenzimi Regolazione della attività enzimatica L attività enzimatica deve potere essere regolata in base alle specifiche richieste
SOLUZIONI DEGLI ESERCIZI
 Niccolò Taddei - Biochimica Capitolo 4 GLI ENZIMI 1 Un enzima è un particolare tipo di proteina con funzione di catalizzatore, cioè è in grado di aumentare la velocità di una reazione chimica. Gli enzimi
Niccolò Taddei - Biochimica Capitolo 4 GLI ENZIMI 1 Un enzima è un particolare tipo di proteina con funzione di catalizzatore, cioè è in grado di aumentare la velocità di una reazione chimica. Gli enzimi
B. Classificazione degli organismi 1. Autotrofi - si nutrono da soli a. ottengono il carbonio dalla CO 2 b. fonte di energia - fotosintetica: uso
 Outline Classificazione degli organismi Energia e metabolismo Energia libera Composti ad alta energia Ossidazione, riduzione e trasferimento energetico Ruolo degli enzimi Introduzione A. La vita è organica
Outline Classificazione degli organismi Energia e metabolismo Energia libera Composti ad alta energia Ossidazione, riduzione e trasferimento energetico Ruolo degli enzimi Introduzione A. La vita è organica
CICLO DI KREBS (o DELL ACIDO CITRICO)
 CICLO DI KREBS (o DELL ACIDO CITRICO) È un processo ossidativo che ha un ruolo centrale nel metabolismo energetico delle cellule eucariotiche. Avviene nella matrice mitocondriale. È alimentato soprattutto
CICLO DI KREBS (o DELL ACIDO CITRICO) È un processo ossidativo che ha un ruolo centrale nel metabolismo energetico delle cellule eucariotiche. Avviene nella matrice mitocondriale. È alimentato soprattutto
Enzimi e loro ruolo nel metabolismo
 Enzimi e loro ruolo nel metabolismo Definizioni e ruoli degli enzimi Cinetica enzimatica Localizzazione degli enzimi Enzimi come bersaglio di farmaci Enzimi come markers in Biochimica Clinica Errori congeniti
Enzimi e loro ruolo nel metabolismo Definizioni e ruoli degli enzimi Cinetica enzimatica Localizzazione degli enzimi Enzimi come bersaglio di farmaci Enzimi come markers in Biochimica Clinica Errori congeniti
Gli enzimi e l inibizione enzimatica.
 Gli enzimi e l inibizione enzimatica. Catalisi enzimatica La velocità di una reazione è descritta dall equazione di Arrhenius: k = Ae -Ea/RT in cui A è il fattore pre-esponenziale R è la costante dei gas
Gli enzimi e l inibizione enzimatica. Catalisi enzimatica La velocità di una reazione è descritta dall equazione di Arrhenius: k = Ae -Ea/RT in cui A è il fattore pre-esponenziale R è la costante dei gas
di piccoli gruppi di molecole di RNA catalitico tutti gli enzimi sono proteine Molti enzimi per poter funzionare richiedono la presenza di cofattori.
 Enzimi Con l eccezione l di piccoli gruppi di molecole di RNA catalitico tutti gli enzimi sono proteine Molti enzimi per poter funzionare richiedono la presenza di cofattori. apoenzima + cofattore = oloenzima
Enzimi Con l eccezione l di piccoli gruppi di molecole di RNA catalitico tutti gli enzimi sono proteine Molti enzimi per poter funzionare richiedono la presenza di cofattori. apoenzima + cofattore = oloenzima
catabolismo anabolismo
 Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in un organismo o in una cellula Il catabolismo è l insieme delle reazioni che portano alla scissione di molecole complesse (ricche
Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in un organismo o in una cellula Il catabolismo è l insieme delle reazioni che portano alla scissione di molecole complesse (ricche
Una panoramica del ciclo dell acido ciclico
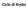 Ciclo di Krebs Una panoramica del ciclo dell acido ciclico Concetti chiave Il ciclo dell acido citrico, o ciclo di Krebs, o ciclo degli acidi tricarbossilici (TCA), è un processo catalitico a 8 tappe che
Ciclo di Krebs Una panoramica del ciclo dell acido ciclico Concetti chiave Il ciclo dell acido citrico, o ciclo di Krebs, o ciclo degli acidi tricarbossilici (TCA), è un processo catalitico a 8 tappe che
Aerobiosi C A T A B O L I S M O. Lez 4A. Schema generale del metabolismo dei glucidi
 Schema generale del metabolismo dei glucidi -1- Aerobiosi In condizioni aerobiche il piruvato prodotto dalla glicolisi e dalla degradazione di alcuni aminoacidi è ossidato a H 2 O e CO 2 nella respirazione
Schema generale del metabolismo dei glucidi -1- Aerobiosi In condizioni aerobiche il piruvato prodotto dalla glicolisi e dalla degradazione di alcuni aminoacidi è ossidato a H 2 O e CO 2 nella respirazione
Prof. Maria Nicola GADALETA
 Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
DESTINI METABOLICI DEL PIRUVATO
 DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Complesso della Piruvato deidrogenasi
DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Complesso della Piruvato deidrogenasi
Ossidazione dell α-chetoglutarato: questa reazione porta alla formazione di un legame TIOESTERE ad alta energia e alla produzione di NADH
 Ossidazione dell α-chetoglutarato: questa reazione porta alla formazione di un legame TIOESTERE ad alta energia e alla produzione di NADH TPP Lipoammide FAD α-chetoglutarato Complesso dell αchetoglutarato
Ossidazione dell α-chetoglutarato: questa reazione porta alla formazione di un legame TIOESTERE ad alta energia e alla produzione di NADH TPP Lipoammide FAD α-chetoglutarato Complesso dell αchetoglutarato
GLI ENZIMI: proteine con attività CATALITICA
 Cap. 6 GLI ENZIMI: proteine con attività CATALITICA Catalizzatori biologici: permettono alle reazioni biochimiche di avvenire a temperature e pressioni fisiologiche e a velocità misurabile. Aumentano la
Cap. 6 GLI ENZIMI: proteine con attività CATALITICA Catalizzatori biologici: permettono alle reazioni biochimiche di avvenire a temperature e pressioni fisiologiche e a velocità misurabile. Aumentano la
Seminario. Ciclo di Krebs 1. La citrato sintasi forma citrato a partire dall ossaloacetato e dall acetilcoenzima A
 Seminario PASSO PER PASSO 1. La citrato sintasi forma citrato a partire dall ossaloacetato e dall acetilcoenzima A Il ciclo dell acido citrico inizia con la reazione di condensazione di un unità con 4
Seminario PASSO PER PASSO 1. La citrato sintasi forma citrato a partire dall ossaloacetato e dall acetilcoenzima A Il ciclo dell acido citrico inizia con la reazione di condensazione di un unità con 4
La glicolisi non è l unica via catabolica in grado di produrre energia. Se il suo prodotto viene ulteriormente ossidato si ottiene molta più energia.
 La glicolisi non è l unica via catabolica in grado di produrre energia. Se il suo prodotto viene ulteriormente ossidato si ottiene molta più energia. Il ciclo dell acido citrico è una via metabolica centrale
La glicolisi non è l unica via catabolica in grado di produrre energia. Se il suo prodotto viene ulteriormente ossidato si ottiene molta più energia. Il ciclo dell acido citrico è una via metabolica centrale
DESTINI DEL PIRUVATO
 DESTINI DEL PIRUVATO LA GLICOLISI RILASCIA SOLO UNA PICCOLA PARTE DELL ENERGIA TOTALE DISPONIBILE NELLA MOLECOLA DI GLUCOSIO Le due molecole di piruvato prodotte dalla glicolisi sono ancora relativamente
DESTINI DEL PIRUVATO LA GLICOLISI RILASCIA SOLO UNA PICCOLA PARTE DELL ENERGIA TOTALE DISPONIBILE NELLA MOLECOLA DI GLUCOSIO Le due molecole di piruvato prodotte dalla glicolisi sono ancora relativamente
Il metabolismo cellulare
 Il metabolismo cellulare 1 Il metabolismo cellulare CATABOLISMO Processo esoergonico (per produrre energia) Nutriliti NAD FAD NADP e - +H + ANABOLISMO Processo endoergonico Biopolimeri (x es. proteine)
Il metabolismo cellulare 1 Il metabolismo cellulare CATABOLISMO Processo esoergonico (per produrre energia) Nutriliti NAD FAD NADP e - +H + ANABOLISMO Processo endoergonico Biopolimeri (x es. proteine)
NADH e NADPH. ATP = 1 moneta (energetica) della cellula NADH, NADPH = 2 moneta (potere riducente)
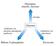 NADH e NADPH ATP = 1 moneta (energetica) della cellula NADH, NADPH = 2 moneta (potere riducente) NADH e NADPH non sono funzionalmente intercambiabili. [NAD + ]/[NADH] ~ 1000 favorisce ossidazione [NADP
NADH e NADPH ATP = 1 moneta (energetica) della cellula NADH, NADPH = 2 moneta (potere riducente) NADH e NADPH non sono funzionalmente intercambiabili. [NAD + ]/[NADH] ~ 1000 favorisce ossidazione [NADP
Helena Curtis N. Sue Barnes
 Helena Curtis N. Sue Barnes LA FOTOSINTESI INDICE Organismi autotrofi ed eterotrofi Confronto tra fotosintesi e respirazione Reazioni endoergoniche ed esoergoniche Reazioni accoppiate Fase luce-dipendente
Helena Curtis N. Sue Barnes LA FOTOSINTESI INDICE Organismi autotrofi ed eterotrofi Confronto tra fotosintesi e respirazione Reazioni endoergoniche ed esoergoniche Reazioni accoppiate Fase luce-dipendente
La catalisi enzimatica. Copyright 2013 Zanichelli editore S.p.A.
 La catalisi enzimatica Copyright 2013 Zanichelli editore S.p.A. Le proprietà generali degli enzimi Conce& chiave Gli enzimi si differenziano dai catalizzatori chimici di uso comune per velocità, condizioni,
La catalisi enzimatica Copyright 2013 Zanichelli editore S.p.A. Le proprietà generali degli enzimi Conce& chiave Gli enzimi si differenziano dai catalizzatori chimici di uso comune per velocità, condizioni,
FUNZIONI BIOLOGICHE DELLE PROTEINE
 FUNZIONI BIOLOGICHE DELLE PROTEINE ENZIMI PROTEINE DI TRASPORTO PROTEINE DI RISERVA PROTEINE CONTRATTILI PROTEINE DI DIFESA PROTEINE REGOLATRICI PROTEINE STRUTTURALI ENERGIA LIBERA (G) ΔG = ΔH - TΔS Variazioni
FUNZIONI BIOLOGICHE DELLE PROTEINE ENZIMI PROTEINE DI TRASPORTO PROTEINE DI RISERVA PROTEINE CONTRATTILI PROTEINE DI DIFESA PROTEINE REGOLATRICI PROTEINE STRUTTURALI ENERGIA LIBERA (G) ΔG = ΔH - TΔS Variazioni
CATALISI COVALENTE. H 2 O Enz-R-OH + P. Enz-R-O S Enz-R-O-S
 CATALISI COVALENTE Comporta la formazione di intermedi in cui il substrato è legato covalentemente con un residuo amminoacidico del sito attivo dell enzima. La catena laterale re dell enzima può comportarsi
CATALISI COVALENTE Comporta la formazione di intermedi in cui il substrato è legato covalentemente con un residuo amminoacidico del sito attivo dell enzima. La catena laterale re dell enzima può comportarsi
Respirazione cellulare: processi molecolari medianti i quali le cellule consumano O 2 e producono CO 2
 AVVERTENZA Il presente materiale didattico è messo a disposizione degli studenti per facilitare la comprensione degli argomenti trattati nel corso delle lezioni e lo studio individuale Non sostituisce
AVVERTENZA Il presente materiale didattico è messo a disposizione degli studenti per facilitare la comprensione degli argomenti trattati nel corso delle lezioni e lo studio individuale Non sostituisce
L ossidazione completa del glucosio da parte dell O 2. può essere suddivisa in due semi-reazioni
 L ossidazione completa del glucosio da parte dell O 2 C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O può essere suddivisa in due semi-reazioni C 6 H 12 O 6 + 6 O 2 6 CO 2 + 24 H + + 24 e - (si ossidano gli atomi
L ossidazione completa del glucosio da parte dell O 2 C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O può essere suddivisa in due semi-reazioni C 6 H 12 O 6 + 6 O 2 6 CO 2 + 24 H + + 24 e - (si ossidano gli atomi
L ossidazione completa del glucosio da parte dell O 2. può essere suddivisa in due semi-reazioni
 L ossidazione completa del glucosio da parte dell O 2 C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O può essere suddivisa in due semi-reazioni C 6 H 12 O 6 + 6 O 2 6 CO 2 + 24 H + + 24 e - (si ossidano gli atomi
L ossidazione completa del glucosio da parte dell O 2 C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O può essere suddivisa in due semi-reazioni C 6 H 12 O 6 + 6 O 2 6 CO 2 + 24 H + + 24 e - (si ossidano gli atomi
ENZIMI : catalizzatori biologici
 ENZIMI : catalizzatori biologici 1 Nell organismo sono indispensabili alla vita: per esempio le reazioni chimiche connesse con un singolo respiro, in assenza di enzimi, durerebbero ore. L enzima anidrasi
ENZIMI : catalizzatori biologici 1 Nell organismo sono indispensabili alla vita: per esempio le reazioni chimiche connesse con un singolo respiro, in assenza di enzimi, durerebbero ore. L enzima anidrasi
DESTINI METABOLICI DEL PIRUVATO
 DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Piruvato Complesso della Piruvato
DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Piruvato Complesso della Piruvato
Acetil-CoA. NADH (prodotto nella glicolisi) PIRUVATO. Condizioni anaerobiche. Condizioni. aerobiche
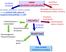 Condizioni aerobiche NADH (prodotto nella glicolisi) Condizioni anaerobiche Riossidato attraverso i sistemi navetta >>> e - trasferiti nella catena di trasporto mitocondriale >>> ATP Carbossilazione a
Condizioni aerobiche NADH (prodotto nella glicolisi) Condizioni anaerobiche Riossidato attraverso i sistemi navetta >>> e - trasferiti nella catena di trasporto mitocondriale >>> ATP Carbossilazione a
GLUCOSIO. Vena porta DIGESTIONE DEI DISACCARIDI. Enzimi parete intestinale
 DIGESTIONE DELL AMIDO AMIDO Amilasi salivare DESTRINE Amilasi pancreatica MALTOSIO Enzimi parete intestinale GLUCOSIO Vena porta DIGESTIONE DEI DISACCARIDI DISACCARIDI Enzimi parete intestinale MONOSACCARIDI
DIGESTIONE DELL AMIDO AMIDO Amilasi salivare DESTRINE Amilasi pancreatica MALTOSIO Enzimi parete intestinale GLUCOSIO Vena porta DIGESTIONE DEI DISACCARIDI DISACCARIDI Enzimi parete intestinale MONOSACCARIDI
1. Ossidoreduttasi 2. Transferasi 3. Idrolasi 4. Liasi 5. Isomerasi 6. Ligasi
 1. Ossidoreduttasi 2. Transferasi 3. Idrolasi 4. Liasi 5. Isomerasi 6. Ligasi ATP + glucosio glucochinasi ADP + glucosio-6-p E.C 2.7.1.2 glucochinasi E.C 2.7.1.1 esochinasi Energia libera,g S k 1 k 1 =
1. Ossidoreduttasi 2. Transferasi 3. Idrolasi 4. Liasi 5. Isomerasi 6. Ligasi ATP + glucosio glucochinasi ADP + glucosio-6-p E.C 2.7.1.2 glucochinasi E.C 2.7.1.1 esochinasi Energia libera,g S k 1 k 1 =
Scaricato da 1
 A AB B Scaricato da www.sunhope.it 1 1 1 1 2 2 2 3 45 5 5 4 20 20 5 40 40 6 40 20 23 7 5 12 8 35 2 6 9 1 1 Numero di mole ecole 30 25 20 15 10 5 0 0 2 4 6 8 10 Energia Scaricato da www.sunhope.it 2 Scaricato
A AB B Scaricato da www.sunhope.it 1 1 1 1 2 2 2 3 45 5 5 4 20 20 5 40 40 6 40 20 23 7 5 12 8 35 2 6 9 1 1 Numero di mole ecole 30 25 20 15 10 5 0 0 2 4 6 8 10 Energia Scaricato da www.sunhope.it 2 Scaricato
BIOCHIMICA e BIOTECNOLOGIE degli ALIMENTI
 Seconda Università degli Studi di Napoli DiSTABiF Anno Accademico 2016-17 Corso di Laurea Magistrale in SCIENZE DEGLI ALIMENTI E DELLA NUTRIZIONE UMANA Insegnamento di BIOCHIMICA e BIOTECNOLOGIE degli
Seconda Università degli Studi di Napoli DiSTABiF Anno Accademico 2016-17 Corso di Laurea Magistrale in SCIENZE DEGLI ALIMENTI E DELLA NUTRIZIONE UMANA Insegnamento di BIOCHIMICA e BIOTECNOLOGIE degli
Il metabolismo cellulare
 Il metabolismo cellulare L obesità è problema sanitario e sociale Tessuto adiposo bianco e bruno È tutta una questione di energia: Se si assumono più molecole energetiche di quelle che ci servono per costruire
Il metabolismo cellulare L obesità è problema sanitario e sociale Tessuto adiposo bianco e bruno È tutta una questione di energia: Se si assumono più molecole energetiche di quelle che ci servono per costruire
L ATTIVITA DELLA CELLULA
 L ATTIVITA DELLA CELLULA nutrizione crescita eliminare i rifiuti mantenimento delle strutture movimento riproduzione comunicazione per svolgere tutte queste attività, le cellule hanno bisogno di ENERGIA
L ATTIVITA DELLA CELLULA nutrizione crescita eliminare i rifiuti mantenimento delle strutture movimento riproduzione comunicazione per svolgere tutte queste attività, le cellule hanno bisogno di ENERGIA
Modulo 14 Il ciclo di Krebs
 Modulo 14 Il ciclo di Krebs Il destino ossidativo del piruvato In condizioni aerobie il piruvato viene decarbossilato ad acetato. L acetato è ossidato ulteriormente nel ciclo dell acido citrico. Una serie
Modulo 14 Il ciclo di Krebs Il destino ossidativo del piruvato In condizioni aerobie il piruvato viene decarbossilato ad acetato. L acetato è ossidato ulteriormente nel ciclo dell acido citrico. Una serie
IL METABOLISMO. Dal carbonio agli OGM Capitolo 2
 IL METABOLISMO Dal carbonio agli OGM Capitolo 2 IL METABOLISMO L'insieme delle trasformazioni chimiche ed energetiche che si verificano nelle cellule di un organismo vivente e ne garantiscono la conservazione,
IL METABOLISMO Dal carbonio agli OGM Capitolo 2 IL METABOLISMO L'insieme delle trasformazioni chimiche ed energetiche che si verificano nelle cellule di un organismo vivente e ne garantiscono la conservazione,
Modulo 12 : Il metabolismo: concetti di base
 Modulo 12 : Il metabolismo: concetti di base Il metabolismo Il metabolismo è l insieme di tutte le trasformazioni chimiche che avvengono nelle cellule (ed in ultima analisi negli organismi) per adempiere
Modulo 12 : Il metabolismo: concetti di base Il metabolismo Il metabolismo è l insieme di tutte le trasformazioni chimiche che avvengono nelle cellule (ed in ultima analisi negli organismi) per adempiere
2. Quale delle seguenti affermazioni relative ad una reazione enzimatica è vera?
 1. Gli enzimi agendo come catalizzatori: a) innalzano l'energia di attivazione b) innalzano il livello energetico dei prodotti c) abbassano il livello energetico dei reagenti d) diminuiscono l'energia
1. Gli enzimi agendo come catalizzatori: a) innalzano l'energia di attivazione b) innalzano il livello energetico dei prodotti c) abbassano il livello energetico dei reagenti d) diminuiscono l'energia
INIBIZIONE ENZIMATICA REVERSIBILE Gli inibitori (I) legano l enzima e interferiscono con la loro attività modificando la Vmax, la Km o entrambe.
 INIBIZIONE ENZIMATICA REVERSIBILE Gli inibitori (I) legano l enzima e interferiscono con la loro attività modificando la Vmax, la Km o entrambe. Gli inibitori reversibili si legano all enzima mediante
INIBIZIONE ENZIMATICA REVERSIBILE Gli inibitori (I) legano l enzima e interferiscono con la loro attività modificando la Vmax, la Km o entrambe. Gli inibitori reversibili si legano all enzima mediante
Energia e metabolismi energetici
 Energia e metabolismi energetici L energia è la capacità di produrre lavoro Tutti gli organismi hanno bisogno di energia per vivere. L energia è definita come la capacità di effettuare un lavoro L energia
Energia e metabolismi energetici L energia è la capacità di produrre lavoro Tutti gli organismi hanno bisogno di energia per vivere. L energia è definita come la capacità di effettuare un lavoro L energia
Attività cellulare altamente coordinata svolta da sistemi multienzimatici, con i seguenti scopi: ottenere energia chimica dall ambiente attraverso la
 Metabolismo Attività cellulare altamente coordinata svolta da sistemi multienzimatici, con i seguenti scopi: ottenere energia chimica dall ambiente attraverso la degradazione di nutrienti operare la sintesi
Metabolismo Attività cellulare altamente coordinata svolta da sistemi multienzimatici, con i seguenti scopi: ottenere energia chimica dall ambiente attraverso la degradazione di nutrienti operare la sintesi
I MITOCONDRI: LE CENTRALI ENERGETICHE DELLA CELLULA
 I MITOCONDRI: LE CENTRALI ENERGETICHE DELLA CELLULA MITOCONDRIO OSSERVATO AL SEM Localizzazione dei mitocondri SONO IN GENERE PIÙ ABBONDANTI DELLE ZONE DELLA CELLULA CHE RICHIEDONO MAGGIORI QUANTITA DI
I MITOCONDRI: LE CENTRALI ENERGETICHE DELLA CELLULA MITOCONDRIO OSSERVATO AL SEM Localizzazione dei mitocondri SONO IN GENERE PIÙ ABBONDANTI DELLE ZONE DELLA CELLULA CHE RICHIEDONO MAGGIORI QUANTITA DI
Cap.19. Ciclo di Krebs. o Ciclo degli acidi Tricarbossilici o Ciclo dell acido Citrico
 Cap.19 Ciclo di Krebs o Ciclo degli acidi Tricarbossilici o Ciclo dell acido Citrico Acetil-CoA OSSIDAZIONE DEL GLUCOSIO C 6 H 12 O 6 (glucosio) + 6O 2.. 6CO 2 + 6H 2 O I tappa: GLICOLISI 2 + 2 H 2 O II
Cap.19 Ciclo di Krebs o Ciclo degli acidi Tricarbossilici o Ciclo dell acido Citrico Acetil-CoA OSSIDAZIONE DEL GLUCOSIO C 6 H 12 O 6 (glucosio) + 6O 2.. 6CO 2 + 6H 2 O I tappa: GLICOLISI 2 + 2 H 2 O II
Struttura e meccanismo d azione degli enzimi
 Macromolecole Biologiche Chimica Biologica A.A. 2010-2011 Struttura e meccanismo d azione degli enzimi Catalisi chimica Catalisi chimica: teoria dello stato di transizione - descrizione microscopica del
Macromolecole Biologiche Chimica Biologica A.A. 2010-2011 Struttura e meccanismo d azione degli enzimi Catalisi chimica Catalisi chimica: teoria dello stato di transizione - descrizione microscopica del
