AZIENDA OSPEDALIERA UNIVERSITARIA INTEGRATA - VERONA (D.Lgs. n. 517/ Art. 3 L.R.Veneto n. 18/2009) D I M T
|
|
|
- Benvenuto Caselli
- 7 anni fa
- Visualizzazioni
Transcript
1 1 Allegato 1 D I M T PROCEDURA APERTA PER LA FORNITURA QUINQUENNALE PER IL DIPARTIMENTO INTERAZIENDALE DI MEDICINA TRASFUSIONALE DI PRODOTTI PER LA TIPIZZAZIONE GENOMICA A BASSA E ALTA RISOLUZIONE SUDDIVISA IN LOTTI ALLEGATO TECNICO al Capitolato Speciale d appalto
2 2 ALLEGATO TECNICO ARTICOLO 1 OGGETTO E CARATTERISTICHE DELLA FORNITURA La gara ha per oggetto la fornitura di prodotti per TIPIZZAZIONE GENOMICA HLA DI I e di II CLASSE per l Unita Operativa Complessa di Medicina Trasfusionale presso l Ospedale di Borgo Trento nell ambito del Dipartimento Interaziendale di Medicina Trasfusionale (DIMT) Per la tipizzazione del sistema HLA in biologia molecolare viene utilizzata la metodica di PCR-SSP. Al fine di garantire una corretta tipizzazione in biologia molecolare a bassa e alta risoluzione sono necessari kit a diversa tipologia suddivisi nei seguenti 2 lotti: LOTTO N.1 CIG. NR F TIPIZZAZIONE HLA DI 1-2 CLASSE A BASSA RISOLUZIONE CARATTERISTICHE QUALITATIVE ESSENZIALI DEI PRODOTTI E MATERIALI Per la tipizzazione dei loci HLA-A,B,C devono essere forniti tre distinti kit per permettere la tipizzazione genomica di I classe (A,B,C) a bassa risoluzione separatamente. Per la tipizzazione genomica del locus HLA-A* a bassa risoluzione il kit deve contenere i primers per identificare gli alleli da HLA-A*01:01 all HLA-A*80:02 corrispondenti agli antigeni dal A1 all antigene A80. Per la tipizzazione genomica del locus HLA-B* a bassa risoluzione il kit deve contenere i primers per identificare gli alleli da HLA-B*07:02 all HLA-B*83:01 corrispondenti agli antigeni dal B7 all antigene B-. Per la tipizzazione genomica del locus HLA-C* a bassa risoluzione il kit deve contenere i primers per identificare gli alleli da HLA-C*01:02 all HLA-C*18:03 corrispondenti agli antigeni dal Cw1 all antigene Cw-. Ciascun test del kit deve essere costituito dall insieme di soluzioni di primers prealiquotate in provette da PCR da 0.2 ml. come una soluzione disidratata di primers a sequenza specifica e da coppie di primers di controllo per le sequenze non alleliche
3 3 (controllo interno positivo) e deve essere previsto e incluso in ogni test un controllo negativo costituito da una soluzione pre-aliquotata/disidratata di primers, per poter documentare ad ogni uso che i reagenti siano liberi da contaminazione secondo quanto richiesto dagli standards EFI (European Federation for Immunogenetics Version L L1.3300). I kit devono contenere la miscela di pre-amplificazione senza Taq DNA Polimerasi secondo le raccomandazioni degli standards EFI (European Federation for Immunogenetics Version L1.3300). Per ogni campione si devono eseguire non meno di: 24 reazioni di PCR per il locus A*, 48 reazioni per il locus B* e 24 reazioni per il locus C* con un volume massimo di 10 ul ciascuna. L'interpretazione dei risultati deve garantire la identificazione di tutte le specificità alleliche approvate dal Comitato Internazionale WHO ed in particolare le seguenti: A*01:13/21/28/51 A*02:17/55/78/135/146/169/237/243 A*03:08/12/30/41/63/75/88/95 A*24:18/82/92 A*25:05/06 A*26:02/09/16/19/22/54 A*29:07/13 A*30:08 A*31:03/04/08/29/35 A*32:03/04/05/13/15 A*33:13/19/22/24 A*34:04 A*34:08 A*34:09 A*36:02/04 A*66:09/12 A*68:29/45/66 A*74:07/13 A*80:01/02 N. di test annuo 100 B*07:27/28/38/47/50/54/60/65/73/78/84 B*08:04/09/21/25/32/35/36/38/49/55/60
4 4 B*13:03/06/13:07N/09/11/14/16/26/31/36 B*14:10 B*15:04/13/29/31/36/42/43/45/46/53/54/55/57/62/64/66/68/69/73/74/76/77/80/83/86/89 /101/106/116/124/137/138/142/143/144/161/180/186/189 B*18:04/09/12/19/22/37/44/48/49 B*27:01/12/18/19/23/24/25/29/30/33/41/52/62 B*35:13/16/19/22/26/27/35/38/44/46/47/60/63/76/87 B*37:02/05/07/08/09/11/12/14 B*38:03/04/05/06/07/10/17/20/22 B*39:04/07/17/18/22/36/39/42/43 B*40:05/08/12/16/21/23/26/28/46/47/48/58/59/60/68/71/74/76/83/93/95/96/98 B*41:05/08 B*42:04/08/09/11/13 B*44:06/08/09/10/12/14/15/18/20/31/40/44/49/54/57/60/62/83/90/95/97 B*45:04/06/08/09/10 B*46:02/06/17/18 B*47:02/03 B*48:06/14/15/16/18/21 B*49:02/03/07 B*50:02/06/07/09 B*51:15/36/42/45/50/61/62/64/68/93 B*52:16/19/20 B*53:02/06/14/17/22 B*54:03/06/12/20 B*55:14/18/20/21/22/34/35/40 B*56:03/06/07/09/10/13/17/21/23/25 B*57:04/07/09/12/14/24 B*58:07/08/09/58:17N/18/20/27/28 B*59:04 B*73:01 B*78:05/06 B*81:01 B*82:01 B*83:01 N. di test annuo 100 C*01:04/09/10/14/21/43 C*02:02/04/06/12/14/22/26/27 C*03:15/16/58/67/81/86/94/99
5 5 C*04:10/11/16/29/37/42/58 C*05:16/23/26/36/42/46 C*06:03/05/06/08/09/17/31/32 C*07:31/64/96/123/125 C*08:05/07/10/12/21/25/31 C*12:05/08/09/15/16/21/24/28/31/41/44/49 C*14:04/10/12/15/16/17/25 C*15:07/10/11/12/21/22/23/25/36/37/42/43 C*16:04/15/18/20/29 C*17:05/07 C*18:03 N. di test annuo 200 La Ditta aggiudicatrice dovrà aggiornare periodicamente i kit con i primers per la definizione di tutti gli alleli approvati dal comitato WHO secondo la nuova nomenclatura internazionale; inoltre dovrà aggiornare almeno una volta all anno il Software Database delle sequenze HLA utilizzato per l assegnazione degli alleli, secondo la versione di nomenclatura internazionale più aggiornata del Database IMGT/HLA per la definizione di tutti gli alleli approvati dal Comitato Internazionale WHO come richiesto dagli standards EFI (European Federation for Immunogenetics Version C1.930). Per la tipizzazione dei loci DRB1* e DQB1* devono essere forniti due distinti kit per permettere la tipizzazione genomica di II classe a bassa risoluzione separatamente. Per la tipizzazione genomica del DRB1* a bassa risoluzione il kit deve contenere i primers per identificare gli alleli dal DRB1*01:01 al DRB1*16:17 corrispondenti agli antigeni dal DR1 al DR18 e le superspecificità alleliche DRB3*, DRB4* e DRB5* corrispondenti alle superspecificità antigeniche DR51, 52 e 53. Per la tipizzazione genomica del DQB1* a bassa risoluzione il kit deve contenere i primers per identificare gli alleli dal DQB1* 02:01 al DQB1* 06:29 corrispondenti agli antigeni dal DQ2 al DQ9. Ciascun test del kit deve essere costituito dall insieme di soluzioni di primers prealiquotate in provette da PCR da 0.2 ml. come una soluzione disidratata di primers a
6 6 sequenza specifica e da coppie di primers di controllo per le sequenze non alleliche (controllo interno positivo) e deve essere previsto e incluso in ogni test un controllo negativo costituito da una soluzione pre-aliquotata/disidratata di primers, per poter documentare ad ogni uso che i reagenti siano liberi da contaminazione secondo quanto richiesto dagli standards EFI (European Federation for Immunogenetics Version L L ). I kit devono contenere la miscela di pre-amplificazione senza Taq DNA Polimerasi secondo le raccomandazioni degli standards EFI (European Federation for Immunogenetics Version L1.3300). Per ogni campione si devono eseguire non meno di: 24 reazioni di PCR per il locus DRB1* e non meno di 8 reazioni di PCR per il locus DQB1* con un volume massimo di 10 ul ciascuna. L'interpretazione dei risultati deve garantire la identificazione di tutte le specificità alleliche approvate dal Comitato Internazionale WHO ed in particolare le seguenti: DRB1* 01:03 DRB1* 03:08/10/42/46 DRB1* 08:08/21/32/35/40 DRB1*11:05/55/89 DRB1* 12:04/16/22 DRB1*13:09/17/26/43/45/85 DRB1*14:11/16/22/24/27/37/42/49/50/58/65/69/73/74/82/89/95/98 DRB1*15:21/25 DRB1* 16:04 N. di test annuo 1000 DQB1*06:29 N. di test annuo 400 La Ditta aggiudicatrice dovrà aggiornare periodicamente i kit con i primers per la definizione di tutti gli alleli approvati dal Comitato Internazionale WHO secondo la nuova nomenclatura internazionale; inoltre dovrà aggiornare almeno una volta all anno il Software Database delle sequenze HLA utilizzato per l assegnazione degli alleli,
7 7 secondo la versione di nomenclatura internazionale più aggiornata del Database IMGT/HLA per la definizione di tutti gli alleli approvati dal Comitato Internazionale WHO come richiesto dagli standards EFI (European Federation for Immunogenetics Version C1.930). FORNITURA DI CONTROLLO DI CONTAMINAZIONE (WIPE TEST) Per la determinazione del sistema HLA di I e II Classe in biologia molecolare è necessario che la Ditta aggiudicatrice fornisca un kit per il Controllo di contaminazione ( Wipe Test ) da utilizzare nell'area di pre-amplificazione allo scopo di verificare che le attrezzature non siano contaminate da DNA amplificato tale da interferire con le analisi in corso, come richiesto dagli standards EFI (European Federation for Immunogenetics Version L1.2000). Il Controllo di contaminazione (Wipe Test) deve essere costituito da coppie di primers disidratate, pre-aliquotate in provette da PCR da 0.2ml. Ogni provetta deve contenere coppie di primers che amplificano più del 90% degli alleli HLA-A*,-B*,-C*, DRB1*, DQB1* e DPB1* oltre che primers di controllo per le sequenze non alleliche (controllo interno positivo). Il kit deve contenere la miscela di pre-amplificazione senza Taq DNA Polimerasi secondo le raccomandazioni degli standards EFI (European Federation for Immunogenetics Version L1.3300). N. di test annuo 200 FORNITURA DI MARCATORE DI PESO MOLECOLARE Per la determinazione del sistema HLA di I e II Classe in biologia molecolare è necessario che la Ditta aggiudicatrice fornisca un reagente per la determinazione del range di peso molecolare delle bande (da 1000bp a 50 bp) ottenute per gel-elettroforesi da includere in ciascun gel, come richiesto dagli standards EFI (European Federation for Immunogenetics Version L2.2000). N. di confezioni annuo 150 FORNITURA DI ETIDIO BROMURO Per la determinazione del sistema HLA di I e II Classe in biologia molecolare è necessario che la Ditta aggiudicatrice fornisca il reagente etidio bromuro per la
8 8 colorazione delle bande di DNA ottenute per gel-elettroforesi per la rilevazione post PCR-SSP (conc. finale nel gel raccomandata 0.5ug/ml). N. di confezioni annuo 30 LOTTO N.2 CIG. NR TIPIZZAZIONE HLA DI 1-2 CLASSE AD ALTA RISOLUZIONE CARATTERISTICHE QUALITATIVE ESSENZIALI DEI PRODOTTI E MATERIALI I kit, con numero variabile di primers, devono essere forniti distinti per permettere la tipizzazione genomica HLA di I classe in alta risoluzione separatamente, delle seguenti specificità alleliche: ALLELE N. TEST PREVISTI / ANNO HLA-A *01:01-*01:66 45 HLA-A *02:01-*02: HLA-A *03:01-*03:76 20 HLA-A *11:01-*11:80 15 HLA-A *23:01-*23:31 05 HLA-A *24:02-*24: HLA-A *25:01-*25:13 05 HLA-A *26:01-*26:65 10 HLA-A *29:01-*29:22 15 HLA-A *30:01-*30:34 10 HLA-A *31:01-*31:28 10 HLA-A *32:01-*32:25 15 HLA-A *33:01-*33:34 05 HLA-A *34:01-*34:08 01 HLA-A *36:01-*36:05 01 HLA-A *66:01-*66:04 05 HLA-A *68:01-*68:54,*69:01 05 HLA-A *74:01-*74:14 01 HLA-B *07:02-*07 :117 30
9 9 HLA-B *08:01-*08:61 25 HLA-B*13:01-*13 :37 10 HLA-B*14:01-*14 :19 10 HLA-B*15:01- *15:209N 05 HLA-B*18:01-*18 :49 30 HLA-B*27:01-*27:73 10 HLA-B*35:01-*35: HLA-B*37:01-*37:25 05 HLA-B*38:01-*38:22 10 HLA-B*39:01-*39:54 15 HLA-B*40:01-*40 :99 10 HLA-B*41:01-*41:16 05 HLA-B*42:01-*42:14 01 HLA-B*44:02-*44:99 20 HLA-B*45:01-*45:11 05 HLA-B*46:01-*46 :22 01 HLA-B*47:01-*47:07 01 HLA-B*48:01-*48 :23 01 HLA-B*49 01-*49:15 05 HLA-B*50:01-*50:09 05 HLA-B*51:01-*51:95 20 HLA-B*52:01-*52:21 05 HLA-B*53:01-*53:24 05 HLA-B*54:01-*54 :19 01 HLA-B*55:01-*55:48 05 HLA-B*56:01-*56:29 05 HLA-B*57:01-*57:37 10 HLA-B*58:01-*58:31N 01 HLA-B*59:01-*59:05 01 HLA-B*73 :01-*73 :02 05 HLA-B*67:01-*67:02 01 HLA-B*78:01-*78:07 01 HLA-B*81:01-*81:05 01 HLA-B*82:01-*82:03 01 HLA-C*01:02-01:45 10 HLA-C*02:02-02:47 10 HLA-C*03:02-03: HLA-C*04:01-04:84 30 HLA-C*05:01-05:13 20
10 10 HLA-C*06:02-06:37 25 HLA-C*07:01-07:99 75 HLA-C*08:01-08:13 10 HLA-C*12:02-12:50 40 HLA-C*14:01-14:29 05 HLA-C*15:02-15:48 20 HLA-C*16:01-16: HLA-C*17:01-17:07 05 HLA-C*18:1-18:04 01 Ciascun test del kit deve essere costituito dall insieme di soluzioni di primers prealiquotate in provette da PCR da 0.2 ml. come una soluzione disidratata di primers a sequenza specifica e inoltre da coppie di primers di controllo per le sequenze non alleliche (controllo interno positivo) come richiesto dagli standards EFI (European Federation for Immunogenetics Version L ). I kit devono contenere la miscela di pre-amplificazione senza Taq DNA Polimerasi secondo le raccomandazioni degli standards EFI (European Federation for Immunogenetics Version L1.3300). La Ditta aggiudicatrice dovrà aggiornare periodicamente i kit con i primers per la definizione di tutti gli alleli approvati dal Comitato Internazionale WHO secondo la nuova nomenclatura internazionale; inoltre dovrà aggiornare almeno una volta all anno il Software Database delle sequenze HLA utilizzato per l assegnazione degli alleli, secondo la versione di nomenclatura internazionale più aggiornata del Database IMGT/HLA per la definizione di tutti gli alleli approvati dal Comitato Internazionale WHO come richiesto dagli standards EFI (European Federation for Immunogenetics Version C1.930).
11 11 I kit, con numero variabile di primers, devono essere forniti distinti per permettere la tipizzazione genomica HLA di II classe in alta risoluzione separatamente, delle seguenti specificità alleliche: ALLELE N. TEST PREVISTI / ANNO DRB3*01:01 -*01:14, *02:01-*02:25,*03:01-*03: DRB4*01:01 -*03:01N 100 DRB5*01:01 -*01:14, *02:02 - *02: DRB1*01:01 - *01:31 20 DRB1*03:01 - *03:52 25 DRB1*04:01 - *04:89 20 DRB1*07:01 - *07:19 25 DRB1*08:01 - *08:41 10 DRB1*09:01 - *09:09 05 DRB1*10:01-*10:03 20 DRB1*11:01 - *11:94 50 DRB1*12:01 - *12:26 05 DRB1*13:01 - *13: DRB1*14:01 - *14: DRB1*15:01 - *15:44 20 DRB1*16: , 16:07-16:18 15 DQB1*02:01 - *02: DQB1*03:01 - *03: DQB1*04:01 - *04:05 15 DQB1*05:01 - *05: DQB1*06:01 - *06:40 50 DQA1*01:01-*01:07, *02:01, *03:01-*03:03,* 04:01-*04:04, 200 *05:01-*05:10, 06:01-06:02 DPB1*01:01 -* 99:01, *100:01-125:01 200
12 12 FORNITURA DI KIT DEDICATI Per la determinazione del sistema HLA di I e II Classe in biologia molecolare a alta risoluzione è necessario che la Ditta aggiudicatrice fornisca dei kit per la definizione di un singolo o limitato numero di loci: HLA-*B27 N. di test annuo 200 HLA-B*57:01 N. di test annuo 100 HLA-DQ2/DQ8 A1*,DQB1*) N. di test annuo 150 A*2409N N. di test annuo 5 B*5111N N. di test annuo 5 C*0409N N. di test annuo 5 DRB4* N N. di test annuo 5 DRB5*0108N N. di test annuo 5 Ciascun test del kit deve essere costituito dall insieme di soluzioni di primers prealiquotate in provette da PCR da 0.2 ml. come una soluzione disidratata di primers a sequenza specifica e inoltre da coppie di primers di controllo per le sequenze non alleliche (controllo interno positivo) come richiesto dagli standards EFI (European Federation for Immunogenetics Version L ). I kit devono contenere la miscela di pre-amplificazione senza Taq DNA Polimerasi secondo le raccomandazioni degli standards EFI (European Federation for Immunogenetics Version L1.3300). La Ditta aggiudicatrice dovrà aggiornare periodicamente i kit con i primers per la definizione di tutti gli alleli approvati dal Comitato Internazionale WHO secondo la nuova nomenclatura internazionale; inoltre dovrà aggiornare almeno una volta all anno il Software Database delle sequenze HLA utilizzato per l assegnazione degli alleli, secondo la versione di nomenclatura internazionale più aggiornata del Database IMGT/HLA per la definizione di tutti gli alleli approvati dal Comitato Internazionale WHO come richiesto dagli standards EFI (European Federation for Immunogenetics Version C1.930).
13 13 L Unità Ooerativa Complessa di Medicina Trasfusionale do nelll ambito del Dipartimento Interaziendale di Medicina trasfusionale (DIMT) dell Azienda Ospedaliera di Verona è certificato UNI EN ISO 9001 per "Progettazione ed effettuazione di servizi di : immunoematologia, produzione di sangue ed emocomponenti, medicina trasfusionale, biologia dei trapianti e allergologia" Si ricorda che i prodotti diagnostici, dovranno avere la marcatura CE, secondo la normativa vigente, ai sensi del D.Lgs. 332/2000, in attuazione alla direttiva 98/79/CE Dispositivi medico diagnostici in vitro.
Capitolato tecnico di fornitura in Service di Sistemi per l esecuzione di esami di Istocompatibilita e tipizzazione tissutale HLA a scopo diagnostico
 Capitolato tecnico di fornitura in Service di Sistemi per l esecuzione di esami di Istocompatibilita e tipizzazione tissutale HLA a scopo diagnostico DESCRIZIONE E SCOPO DELLA FORNITURA Sistemi analitici
Capitolato tecnico di fornitura in Service di Sistemi per l esecuzione di esami di Istocompatibilita e tipizzazione tissutale HLA a scopo diagnostico DESCRIZIONE E SCOPO DELLA FORNITURA Sistemi analitici
ALL. 1 ELENCO DEI LOTTI
 ALL. 1 ELENCO DEI LOTTI GARA A PROCEDURA APERTA PER LA FORNITURA IN SERVICE DI UN SISTEMA MEDIANTE METODICA SSO REVERSE AUTOMATICO PER LA TIPIZZAZIONE MOLECOLARE PCR SSO REVERSE DEL COMPLESSO HLA PER L
ALL. 1 ELENCO DEI LOTTI GARA A PROCEDURA APERTA PER LA FORNITURA IN SERVICE DI UN SISTEMA MEDIANTE METODICA SSO REVERSE AUTOMATICO PER LA TIPIZZAZIONE MOLECOLARE PCR SSO REVERSE DEL COMPLESSO HLA PER L
Requisiti essenziali di ingresso da possedere tutti, pena l'esclusione
 LOTTO 1 - DIVISIBILE: PER LA TIPIZZAZIONE GENOMICA HLA PCR-SSO REVERSE E PER L'IDENTIFICAZIONE DI ANTICORPI ANTI-HLA MEDIANTE TECNOLOGIA LUMINEX SUB-LOTTO 1 INDIVISIBILE: TIPIZZAZIONE GENOMICA HLA PCR-SSO
LOTTO 1 - DIVISIBILE: PER LA TIPIZZAZIONE GENOMICA HLA PCR-SSO REVERSE E PER L'IDENTIFICAZIONE DI ANTICORPI ANTI-HLA MEDIANTE TECNOLOGIA LUMINEX SUB-LOTTO 1 INDIVISIBILE: TIPIZZAZIONE GENOMICA HLA PCR-SSO
Provincia Autonoma di Trento REPORT DI ATTIVITA Prelievo e trapianto di organi
 REPORT DI ATTIVITA 2011 Prelievo e trapianto di organi Dati aggiornati al 08 febbraio 2012 INDICE ATTIVITA DI REPERIMENTO Attività di reperimento nei centri pag. 3 LISTE D ATTESA E ATTIVITA DI TRAPIANTO
REPORT DI ATTIVITA 2011 Prelievo e trapianto di organi Dati aggiornati al 08 febbraio 2012 INDICE ATTIVITA DI REPERIMENTO Attività di reperimento nei centri pag. 3 LISTE D ATTESA E ATTIVITA DI TRAPIANTO
DELIBERAZIONE DEL DIRETTORE GENERALE. N. 779... DEL 10 dicembre 2012..
 AZIENDA OSPEDALIERA S. CROCE E CARLE - CUNEO Ente di rilievo nazionale e di alta specializzazione D.P.C.M. 23.4.1993 RINNOVO kit tipizzazz HLA sit del. 655/2011 PG/GG DELIBERAZIONE DEL DIRETTORE GENERALE
AZIENDA OSPEDALIERA S. CROCE E CARLE - CUNEO Ente di rilievo nazionale e di alta specializzazione D.P.C.M. 23.4.1993 RINNOVO kit tipizzazz HLA sit del. 655/2011 PG/GG DELIBERAZIONE DEL DIRETTORE GENERALE
CAPITOLATO TECNICO PER DIAGNOSTICI PER TIPIZZAZIONE MOLECOLARE DA DESTINARSI AL LABORATORIO DI GENETICA MOLECOLARE-MEDICINA LEGALE P.O.
 ALLEGATO A CAPITOLATO TECNICO PER DIAGNOSTICI PER TIPIZZAZIONE MOLECOLARE DA DESTINARSI AL LABORATORIO DI GENETICA MOLECOLARE-MEDICINA LEGALE P.O. MONSERRATO Durata della fornitura: 1 anno + 1 rinnovabile
ALLEGATO A CAPITOLATO TECNICO PER DIAGNOSTICI PER TIPIZZAZIONE MOLECOLARE DA DESTINARSI AL LABORATORIO DI GENETICA MOLECOLARE-MEDICINA LEGALE P.O. MONSERRATO Durata della fornitura: 1 anno + 1 rinnovabile
FORNITURA DI SACCHE E DISPOSITIVI ACCESSORI PER LA RACCOLTA, LA LAVORAZIONE E LA PRODUZIONE DI EMOCOMPONENTI
 Regione del Veneto AZIENDA U.L.S.S. N. 6 EUGANEA www.aulss6.veneto.it P.E.C.: protocollo.aulss6@pecveneto.it Via Enrico degli Scrovegni n. 14 35131 PADOVA ---------------------------------------- Cod.
Regione del Veneto AZIENDA U.L.S.S. N. 6 EUGANEA www.aulss6.veneto.it P.E.C.: protocollo.aulss6@pecveneto.it Via Enrico degli Scrovegni n. 14 35131 PADOVA ---------------------------------------- Cod.
REGIONE DEL VENETO AZIENDA UNITA LOCALE SOCIO-SANITARIA N. 6 VICENZA DELIBERAZIONE. n. 136 del 18-3-2015 O G G E T T O
 REGIONE DEL VENETO AZIENDA UNITA LOCALE SOCIO-SANITARIA N. 6 VICENZA DELIBERAZIONE n. 136 del 18-3-2015 O G G E T T O Fornitura Prodotti per tipizzazione HLA ad uso del DIMT: proroga contratti. Proponente:
REGIONE DEL VENETO AZIENDA UNITA LOCALE SOCIO-SANITARIA N. 6 VICENZA DELIBERAZIONE n. 136 del 18-3-2015 O G G E T T O Fornitura Prodotti per tipizzazione HLA ad uso del DIMT: proroga contratti. Proponente:
Lo screening dell aplotiplo nella diagnosi della celiachia
 Martedì 7 giugno 2011 Lo screening dell aplotiplo nella diagnosi della celiachia Dott.ssa Lucia Terzuoli Dipartimento di Medicina Interna, Scienze Endocrino-Metaboliche e Biochimica Università degli Studi
Martedì 7 giugno 2011 Lo screening dell aplotiplo nella diagnosi della celiachia Dott.ssa Lucia Terzuoli Dipartimento di Medicina Interna, Scienze Endocrino-Metaboliche e Biochimica Università degli Studi
I quantitativi ed il numero di apparecchiature richiesto è riportato nella descrizione dei singoli lotti.
 CAPITOLATO TECNICO E D ONERI PER LA FORNITURA DI REAGENTI E NOLEGGIO DI ATTREZZATURE PER IL LABORATORIO HLA DEL DIPARTIMENTO INTERAZIENDALE DI MEDICINA TRASFUSIONALE DELLA PROVINCIA DI VENEZIA ARTICOLO
CAPITOLATO TECNICO E D ONERI PER LA FORNITURA DI REAGENTI E NOLEGGIO DI ATTREZZATURE PER IL LABORATORIO HLA DEL DIPARTIMENTO INTERAZIENDALE DI MEDICINA TRASFUSIONALE DELLA PROVINCIA DI VENEZIA ARTICOLO
Procedura negoziata per la fornitura di diagnostici per Laboratorio di Genetica Molecolare settore Oncoematologia. Numero di gara
 Procedura negoziata per la fornitura di diagnostici per Laboratorio di Genetica Molecolare settore Oncoematologia Numero di gara 6581966 CAPITOLATO TECNICO Item Voce Descrizione Quantità/anno 1.1 Sistema
Procedura negoziata per la fornitura di diagnostici per Laboratorio di Genetica Molecolare settore Oncoematologia Numero di gara 6581966 CAPITOLATO TECNICO Item Voce Descrizione Quantità/anno 1.1 Sistema
REGIONE VENETO AZIENDA ULSS N.15 ALTA PADOVANA FORNITURA DI SISTEMI DIAGNOSTICI E REAGENTI PER L ESECUZIONE DEGLI ESAMI DI IMMUNOEMATOLOGIA
 Allegato B/1 REGIONE VENETO AZIENDA ULSS N.15 ALTA PADOVANA FORNITURA DI SISTEMI DIAGNOSTICI E REAGENTI PER L ESECUZIONE DEGLI ESAMI DI IMMUNOEMATOLOGIA E PER LO STUDIO DEGLI ANTIGENI ERITROCITARI IN BIOLOGIA
Allegato B/1 REGIONE VENETO AZIENDA ULSS N.15 ALTA PADOVANA FORNITURA DI SISTEMI DIAGNOSTICI E REAGENTI PER L ESECUZIONE DEGLI ESAMI DI IMMUNOEMATOLOGIA E PER LO STUDIO DEGLI ANTIGENI ERITROCITARI IN BIOLOGIA
Diagnostica HLA nel laboratorio di A.V.R. Pievesestina 23 novembre 2013
 Diagnostica HLA nel laboratorio di A.V.R Pievesestina 23 novembre 2013 Sistema HLA Ruolo del sistema HLA (Human Leukocyte Antigens) Nomenclatura Metodiche utilizzate Correlazione a patologie autoimmuni
Diagnostica HLA nel laboratorio di A.V.R Pievesestina 23 novembre 2013 Sistema HLA Ruolo del sistema HLA (Human Leukocyte Antigens) Nomenclatura Metodiche utilizzate Correlazione a patologie autoimmuni
CAPITOLATO SPECIALE. n. ID GARA14D064 PER LA FORNITURA DI REAGENTI PER TIPIZZAZIONE HLA SIEROLOGICA E MOLECOLARE PER IL FABBISOGNO DELLA
 Regione del Veneto AZIENDA OSPEDALIERA - PADOVA via Giustiniani, 1 35128 PADOVA Cod.Fisc./P.IVA 00349040287 CAPITOLATO SPECIALE n. ID GARA14D064 PER LA FORNITURA DI REAGENTI PER TIPIZZAZIONE HLA SIEROLOGICA
Regione del Veneto AZIENDA OSPEDALIERA - PADOVA via Giustiniani, 1 35128 PADOVA Cod.Fisc./P.IVA 00349040287 CAPITOLATO SPECIALE n. ID GARA14D064 PER LA FORNITURA DI REAGENTI PER TIPIZZAZIONE HLA SIEROLOGICA
Si richiede la fornitura annuale di un sistema di determinazione dell HPV per l Asl Roma1, relativo a tests.
 Oggetto: gara HPV Test primario nello Screening cervico-vaginale. Si richiede la fornitura annuale di un sistema di determinazione dell HPV per l Asl Roma1, relativo a 20.000 tests. Requisiti minimi indispensabili
Oggetto: gara HPV Test primario nello Screening cervico-vaginale. Si richiede la fornitura annuale di un sistema di determinazione dell HPV per l Asl Roma1, relativo a 20.000 tests. Requisiti minimi indispensabili
Texas BioGene, Inc. HLAssure TM SE SBT Typing Kit IVD. Istruzioni per l uso REF 50110, 50145, 50185 REF 50210, 50245, 50285 REF 50350, 50345, 50385
 Texas BioGene, Inc. HLAssure TM SE SBT Typing Kit Istruzioni per l uso REF 50110, 50145, 50185 REF 50210, 50245, 50285 REF 50350, 50345, 50385 REF 50310 REF 50410, 50445, 50485 REF 50510, 50545, 50585
Texas BioGene, Inc. HLAssure TM SE SBT Typing Kit Istruzioni per l uso REF 50110, 50145, 50185 REF 50210, 50245, 50285 REF 50350, 50345, 50385 REF 50310 REF 50410, 50445, 50485 REF 50510, 50545, 50585
USO DEI MARCATORI MOLECOLARI A DNA PER LA TRACCIABILITÀ DEI VITIGNI NEI VINI
 USO DEI MARCATORI MOLECOLARI A DNA PER LA TRACCIABILITÀ DEI VITIGNI NEI VINI CLAUDIO D ONOFRIO*, FABIOLA MATESE*, ELEONORA DUCCI E GIUSEPPE CELANO *UNIVERSITÀ DI PISA, DIPARTIMENTO DI SCIENZE AGRARIE,
USO DEI MARCATORI MOLECOLARI A DNA PER LA TRACCIABILITÀ DEI VITIGNI NEI VINI CLAUDIO D ONOFRIO*, FABIOLA MATESE*, ELEONORA DUCCI E GIUSEPPE CELANO *UNIVERSITÀ DI PISA, DIPARTIMENTO DI SCIENZE AGRARIE,
Scienze tecniche di Medicina di Laboratorio
 Corso di Laurea Magistrale delle Professioni Sanitarie Tecnico-Diagnostiche LM/SNT3 2 anno Scienze tecniche di Medicina di Laboratorio Argomenti della lezione Il controllo di qualità nella diagnostica
Corso di Laurea Magistrale delle Professioni Sanitarie Tecnico-Diagnostiche LM/SNT3 2 anno Scienze tecniche di Medicina di Laboratorio Argomenti della lezione Il controllo di qualità nella diagnostica
FONDAZIONE IRCCS POLICLINICO SAN MATTEO Istituto di Ricovero e Cura a Carattere Scientifico di diritto pubblico (D.M. 28/4/2006)
 FONDAZIONE IRCCS POLICLINICO SAN MATTEO Istituto di Ricovero e Cura a Carattere Scientifico di diritto pubblico (D.M. 28/4/2006) C.F. 00303490189 - P. IVA 00580590180 V.le Golgi, 19-27100 PAVIA Tel. 0382
FONDAZIONE IRCCS POLICLINICO SAN MATTEO Istituto di Ricovero e Cura a Carattere Scientifico di diritto pubblico (D.M. 28/4/2006) C.F. 00303490189 - P. IVA 00580590180 V.le Golgi, 19-27100 PAVIA Tel. 0382
LA REAZIONE A CATENA DELLA POLIMERASI PCR
 LA REAZIONE A CATENA DELLA POLIMERASI PCR INTRODUZIONE Tecnica ideata da Mullis e collaboratori nel 1984 La possibilita' di disporre di quantità virtualmente illimitate di un determinato frammento di DNA,
LA REAZIONE A CATENA DELLA POLIMERASI PCR INTRODUZIONE Tecnica ideata da Mullis e collaboratori nel 1984 La possibilita' di disporre di quantità virtualmente illimitate di un determinato frammento di DNA,
Amplificazione mediante PCR (Polymerase Chain Reaction) del DNA estratto dalla saliva.
 OBIETTIVO DEL LAVORO SPERIMENTALE: TIPIZZAZIONE DEI CROMOSOMI SESSUALI X e Y Amplificazione mediante PCR (Polymerase Chain Reaction) del DNA estratto dalla saliva. Cromosoma X Cromosoma y La tipizzazione
OBIETTIVO DEL LAVORO SPERIMENTALE: TIPIZZAZIONE DEI CROMOSOMI SESSUALI X e Y Amplificazione mediante PCR (Polymerase Chain Reaction) del DNA estratto dalla saliva. Cromosoma X Cromosoma y La tipizzazione
ALLEGATO T SCHEMA DI OFFERTA TECNICA
 PROCEDURA APERTA PER LA FORNITURA IN SERVICE DI DIAGNOSTICI E CONSUMABILI PER LA DETERMINAZIONE QUALITATIVA E/O QUANTITATIVA DI ACIDI NUCLEICI DI AGENTI PATOGENI OCCORRENTI AL FABBISOGNO DEI LABORATORI
PROCEDURA APERTA PER LA FORNITURA IN SERVICE DI DIAGNOSTICI E CONSUMABILI PER LA DETERMINAZIONE QUALITATIVA E/O QUANTITATIVA DI ACIDI NUCLEICI DI AGENTI PATOGENI OCCORRENTI AL FABBISOGNO DEI LABORATORI
REGIONE DEL VENETO AZIENDA UNITA LOCALE SOCIO-SANITARIA N. 6 VICENZA DELIBERAZIONE. n. 660 del O G G E T T O
 REGIONE DEL VENETO AZIENDA UNITA LOCALE SOCIO-SANITARIA N. 6 VICENZA DELIBERAZIONE n. 660 del 25-8-2016 O G G E T T O Gara regionale per la fornitura quinquennale di Sistemi completi per sierologia virologica
REGIONE DEL VENETO AZIENDA UNITA LOCALE SOCIO-SANITARIA N. 6 VICENZA DELIBERAZIONE n. 660 del 25-8-2016 O G G E T T O Gara regionale per la fornitura quinquennale di Sistemi completi per sierologia virologica
SPECIFICHE TECNICHE DEI SISTEMI DIAGNOSTICI COAGULAZIONE PESCARA, PENNE E POPOLI. LOTTO n 2
 SPECIFICHE TECNICHE DEI SISTEMI DIAGNOSTICI COAGULAZIONE PESCARA, PENNE E POPOLI. LOTTO n 2 E richiesta la presentazione di un progetto tecnico dettagliato che descriva la soluzione operativa proposta
SPECIFICHE TECNICHE DEI SISTEMI DIAGNOSTICI COAGULAZIONE PESCARA, PENNE E POPOLI. LOTTO n 2 E richiesta la presentazione di un progetto tecnico dettagliato che descriva la soluzione operativa proposta
CAPITOLATO DI GARA PER L APPALTO DI DISPOSITIVI PER IL SERVIZIO DI ANATOMIA PATOLOGICA
 Allegato 2 CAPITOLATO DI GARA PER L APPALTO DI DISPOSITIVI PER IL SERVIZIO DI ANATOMIA PATOLOGICA ART.1- OGGETTO DELL APPALTO L appalto ha per oggetto la fornitura di dispositivi, per il Servizio di Anatomia
Allegato 2 CAPITOLATO DI GARA PER L APPALTO DI DISPOSITIVI PER IL SERVIZIO DI ANATOMIA PATOLOGICA ART.1- OGGETTO DELL APPALTO L appalto ha per oggetto la fornitura di dispositivi, per il Servizio di Anatomia
Regione Emilia Romagna. Attività di donazione e trapianto di organi, tessuti e cellule
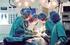 Regione Emilia Romagna Attività di donazione e trapianto di organi, tessuti e cellule Resoconto 2010 Immunogenetica di riferimento regionale per il trapianto di cellule staminali emopoietiche e per il
Regione Emilia Romagna Attività di donazione e trapianto di organi, tessuti e cellule Resoconto 2010 Immunogenetica di riferimento regionale per il trapianto di cellule staminali emopoietiche e per il
La superficie del globulo rosso è ricca di complesse strutture aventi caratteristiche antigeniche
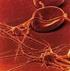 La superficie del globulo rosso è ricca di complesse strutture aventi caratteristiche antigeniche galattosio Fucosio N-acetil-glucosamina N-acetil-galattosamina Glicolipide di base eritrocita galattosio
La superficie del globulo rosso è ricca di complesse strutture aventi caratteristiche antigeniche galattosio Fucosio N-acetil-glucosamina N-acetil-galattosamina Glicolipide di base eritrocita galattosio
Marcatori molecolari
 Marcatori molecolari Caratteristiche e applicazioni Luca Gianfranceschi e Rosanna Marino 1 I marcatori molecolari Strumento per l analisi genetica Strumento Molecolari Analisi genetica Marcatori non oggetto
Marcatori molecolari Caratteristiche e applicazioni Luca Gianfranceschi e Rosanna Marino 1 I marcatori molecolari Strumento per l analisi genetica Strumento Molecolari Analisi genetica Marcatori non oggetto
Allegato C al Decreto n. 108 del pag. 1/6
 giunta regionale Allegato C al Decreto n. 108 del 23.12.2015 pag. 1/6 R E G I O N E V E N E T O Segreteria Regionale per la Sanità Coordinamento Regionale Acquisti per la Sanità * * * * * * LOTTO N. 5
giunta regionale Allegato C al Decreto n. 108 del 23.12.2015 pag. 1/6 R E G I O N E V E N E T O Segreteria Regionale per la Sanità Coordinamento Regionale Acquisti per la Sanità * * * * * * LOTTO N. 5
- CARATTERISTICHE TECNICHE LOTTI -
 REGIONE ABRUZZO AZIENDA SANITARIA LOCALE N 1 AVEZZANO - SULMONA - L AQUILA - U.O. COMPLESSA ACQUISIZIONE E GESTIONE BENI E SERVIZI DIRETTORE (dott. Franca Milani) Procedura ristretta accelerata, per mezzo
REGIONE ABRUZZO AZIENDA SANITARIA LOCALE N 1 AVEZZANO - SULMONA - L AQUILA - U.O. COMPLESSA ACQUISIZIONE E GESTIONE BENI E SERVIZI DIRETTORE (dott. Franca Milani) Procedura ristretta accelerata, per mezzo
REGIONE VENETO AZIENDA ULSS N.15 ALTA PADOVANA FORNITURA DI SISTEMI PER L ESECUZIONE DI PROCEDURE DI AFERESI TERAPEUTICA
 Allegato B/1) REGIONE VENETO AZIENDA ULSS N.15 ALTA PADOVANA FORNITURA DI SISTEMI PER L ESECUZIONE DI PROCEDURE DI AFERESI TERAPEUTICA PER IL DIPARTIMENTO INTERAZIENDALE DI MEDICINA TRASFUSIONALE DELLA
Allegato B/1) REGIONE VENETO AZIENDA ULSS N.15 ALTA PADOVANA FORNITURA DI SISTEMI PER L ESECUZIONE DI PROCEDURE DI AFERESI TERAPEUTICA PER IL DIPARTIMENTO INTERAZIENDALE DI MEDICINA TRASFUSIONALE DELLA
Allegato C al Decreto n. 108 del pag. 1/7
 giunta regionale Allegato C al Decreto n. 108 del 23.12.2015 pag. 1/7 R E G I O N E V E N E T O Segreteria Regionale per la Sanità Coordinamento Regionale Acquisti per la Sanità LOTTO N. 1 FORNITURA DI
giunta regionale Allegato C al Decreto n. 108 del 23.12.2015 pag. 1/7 R E G I O N E V E N E T O Segreteria Regionale per la Sanità Coordinamento Regionale Acquisti per la Sanità LOTTO N. 1 FORNITURA DI
laboratorio biotecnologie zootecniche BAA/LM 3CFU
 laboratorio biotecnologie zootecniche BAA/LM 3CFU Calendario accademico Inizio delle Lezioni: 6 Marzo 2012 Fine delle Lezioni : 5 Giugno 2012 Inizio vacanze di Pasqua: 6 Aprile Fine vacanze di Pasqua:
laboratorio biotecnologie zootecniche BAA/LM 3CFU Calendario accademico Inizio delle Lezioni: 6 Marzo 2012 Fine delle Lezioni : 5 Giugno 2012 Inizio vacanze di Pasqua: 6 Aprile Fine vacanze di Pasqua:
U.O.C. di Epatologia Clinica e Biomolecolare. Unità di misura. Repertorio. 200 ml 10.000 U. 500 test
 U.O.C. di Epatologia Clinica e Biomolecolare Lotto N. DESCRIZIONE PRODOTTO Quantità annua richiesta Unità di misura Repertorio CND Codice Prodotto, Confezione Offerta e nome commerciale Prezzo unitario
U.O.C. di Epatologia Clinica e Biomolecolare Lotto N. DESCRIZIONE PRODOTTO Quantità annua richiesta Unità di misura Repertorio CND Codice Prodotto, Confezione Offerta e nome commerciale Prezzo unitario
dott.ssa Sara Masci L'organizzazione del laboratorio di biologia molecolare: gli spazi, i percorsi, i controlli
 dott.ssa Sara Masci L'organizzazione del laboratorio di biologia molecolare: gli spazi, i percorsi, i controlli Quando si progetta un laboratorio di BM bisogna rispettare dei criteri di sicurezza che tutelino
dott.ssa Sara Masci L'organizzazione del laboratorio di biologia molecolare: gli spazi, i percorsi, i controlli Quando si progetta un laboratorio di BM bisogna rispettare dei criteri di sicurezza che tutelino
Polymerase chain reaction - PCR. Biotecnologie applicate all ispezione degli alimenti di origine animale
 Prof.ssa Tiziana Pepe Polymerase chain reaction - PCR Biotecnologie applicate all ispezione degli alimenti di origine animale Dip. di Medicina Veterinaria e Produzioni animali tiziana.pepe@unina.it Metodologia
Prof.ssa Tiziana Pepe Polymerase chain reaction - PCR Biotecnologie applicate all ispezione degli alimenti di origine animale Dip. di Medicina Veterinaria e Produzioni animali tiziana.pepe@unina.it Metodologia
VALUTAZIONE DELLA BIODIVERSITÀ MICROBICA MEDIANTE L UTILIZZO DI TECNICHE MOLECOLARI
 VALUTAZIONE DELLA BIODIVERSITÀ MICROBICA MEDIANTE L UTILIZZO DI TECNICHE MOLECOLARI Laboratorio di Genetica dei Microrganismi (Responsabile attività: Prof. Giovanni Salzano; Tutor: Dr.ssa Maria Grazia
VALUTAZIONE DELLA BIODIVERSITÀ MICROBICA MEDIANTE L UTILIZZO DI TECNICHE MOLECOLARI Laboratorio di Genetica dei Microrganismi (Responsabile attività: Prof. Giovanni Salzano; Tutor: Dr.ssa Maria Grazia
Servizio di Analisi Molecolari
 Servizio di Analisi Molecolari Laboratorio di Genetica Animale Il laboratorio di Genetica Animale esegue analisi mediante tecniche di biologia molecolare atte ad evidenziare caratteristiche specifiche
Servizio di Analisi Molecolari Laboratorio di Genetica Animale Il laboratorio di Genetica Animale esegue analisi mediante tecniche di biologia molecolare atte ad evidenziare caratteristiche specifiche
Biotecnologie applicate all ispezione degli alimenti di origine animale
 Prof.ssa Tiziana Pepe Evoluzioni della tecnica PCR Biotecnologie applicate all ispezione degli alimenti di origine animale Dip. di Medicina Veterinaria e Produzioni animali tiziana.pepe@unina.it Nested
Prof.ssa Tiziana Pepe Evoluzioni della tecnica PCR Biotecnologie applicate all ispezione degli alimenti di origine animale Dip. di Medicina Veterinaria e Produzioni animali tiziana.pepe@unina.it Nested
Italia-Napoli: Reattivi per l'analisi del sangue 2015/S 232-421421. Bando di gara. Forniture
 1 / 8 Avviso nel sito web TED: http://ted.europa.eu/udl?uri=ted:notice:421421-2015:text:it:html Italia-Napoli: Reattivi per l'analisi del sangue 2015/S 232-421421 Bando di gara Forniture Direttiva 2004/18/CE
1 / 8 Avviso nel sito web TED: http://ted.europa.eu/udl?uri=ted:notice:421421-2015:text:it:html Italia-Napoli: Reattivi per l'analisi del sangue 2015/S 232-421421 Bando di gara Forniture Direttiva 2004/18/CE
REGIONE DEL VENETO AZIENDA UNITA LOCALE SOCIO-SANITARIA N. 6 VICENZA DELIBERAZIONE. n. 944 del O G G E T T O
 REGIONE DEL VENETO AZIENDA UNITA LOCALE SOCIO-SANITARIA N. 6 VICENZA DELIBERAZIONE n. 944 del 30-11-2016 O G G E T T O Gara regionale per la fornitura triennale di Sistemi completi per prelievo, lavorazione
REGIONE DEL VENETO AZIENDA UNITA LOCALE SOCIO-SANITARIA N. 6 VICENZA DELIBERAZIONE n. 944 del 30-11-2016 O G G E T T O Gara regionale per la fornitura triennale di Sistemi completi per prelievo, lavorazione
A tutte le Società interessate
 U.O. Programmazione Acquisti E Gestione Beni e Servizi Ufficio Gare e Contratti Tel 02/81842116 Fax 02/81844000 Prot. n. 9266 del 28/04/2009 A tutte le Società interessate Oggetto: Procedura aperta per
U.O. Programmazione Acquisti E Gestione Beni e Servizi Ufficio Gare e Contratti Tel 02/81842116 Fax 02/81844000 Prot. n. 9266 del 28/04/2009 A tutte le Società interessate Oggetto: Procedura aperta per
pronto all uso, prealiquotato
 IT Istruzioni d uso CYCLER CHECK REF 7104 (10 test) REF 71044 (4 test) Kit per la validazione dell uniformità della temperatura nei termociclatori pronto all uso, prealiquotato Indice 1. Descrizione del
IT Istruzioni d uso CYCLER CHECK REF 7104 (10 test) REF 71044 (4 test) Kit per la validazione dell uniformità della temperatura nei termociclatori pronto all uso, prealiquotato Indice 1. Descrizione del
Kit per la determinazione di contaminazioni in biologia molecolare REF 7091. 40 Reazioni
 IT Istruzioni d uso Wipe test Controllo di contaminazione Kit per la determinazione di contaminazioni in biologia molecolare REF 7091 40 Reazioni 1. Descrizione del prodotto Per impedire le contaminazioni
IT Istruzioni d uso Wipe test Controllo di contaminazione Kit per la determinazione di contaminazioni in biologia molecolare REF 7091 40 Reazioni 1. Descrizione del prodotto Per impedire le contaminazioni
SCHEDA E PROCEDURA APERTAPER LA FORNITURA IN SERVICE DI SISTEMI ANALITICI PER I LABORATORI
 SCHEDA E PROCEDURA APERTAPER LA FORNITURA IN SERVICE DI SISTEMI ANALITICI PER I LABORATORI OGGETTO DI VALUTAZIONE AL FINE DI STABILIRE IL PUNTEGGIO QUALITATIVO DEI PRODOTTI A GARA. Il punteggio qualitativo
SCHEDA E PROCEDURA APERTAPER LA FORNITURA IN SERVICE DI SISTEMI ANALITICI PER I LABORATORI OGGETTO DI VALUTAZIONE AL FINE DI STABILIRE IL PUNTEGGIO QUALITATIVO DEI PRODOTTI A GARA. Il punteggio qualitativo
PROGETTO BIOFORM Corso didattico sperimentale. Esercizio. Tipizzazione del gene PV92
 PROGETTO BIOFORM Corso didattico sperimentale Esercizio Tipizzazione del gene PV92 Elementi trasponibili Che cosa sono gli elementi trasponibili? Sono segmenti di DNA che sono in grado di trasferirsi in
PROGETTO BIOFORM Corso didattico sperimentale Esercizio Tipizzazione del gene PV92 Elementi trasponibili Che cosa sono gli elementi trasponibili? Sono segmenti di DNA che sono in grado di trasferirsi in
I-Roma: Apparecchiature mediche, prodotti farmaceutici e per la cura personale 2012/S Avviso di aggiudicazione di appalto.
 1/7 Avviso nel sito web TED: http://ted.europa.eu/udl?uri=ted:notice:132245-2012:text:it:html I-Roma: Apparecchiature mediche, prodotti farmaceutici e per la cura personale 2012/S 81-132245 Avviso di aggiudicazione
1/7 Avviso nel sito web TED: http://ted.europa.eu/udl?uri=ted:notice:132245-2012:text:it:html I-Roma: Apparecchiature mediche, prodotti farmaceutici e per la cura personale 2012/S 81-132245 Avviso di aggiudicazione
I marcatori molecolari. Dipartimento di Scienze Agronomiche e Genetica Vegetale Agraria Corso di Genetica Agraria Giovanna Attene
 I marcatori molecolari Dipartimento di Scienze Agronomiche e Genetica Vegetale Agraria Corso di Genetica Agraria Giovanna Attene Marcatori molecolari del DNA I marcatori molecolari sono sequenze di DNA
I marcatori molecolari Dipartimento di Scienze Agronomiche e Genetica Vegetale Agraria Corso di Genetica Agraria Giovanna Attene Marcatori molecolari del DNA I marcatori molecolari sono sequenze di DNA
Laboratorio di Genetica Molecolare: Prof. Davide Bizzaro, Prof. Anna La Teana
 Laboratorio di Genetica Molecolare: Prof. Davide Bizzaro, Prof. Anna La Teana Determinazione del polimorfismo del gene TAS2R38 coinvolto nella percezione dell amaro. I mammiferi riconoscono soltanto 5
Laboratorio di Genetica Molecolare: Prof. Davide Bizzaro, Prof. Anna La Teana Determinazione del polimorfismo del gene TAS2R38 coinvolto nella percezione dell amaro. I mammiferi riconoscono soltanto 5
Olerup SSP Istruzioni per l'uso
 Olerup SSP Foglio illustrativo Pagina 1 di 34 Olerup SSP USO PREVISTO I kit di tipizzazione HLA Olerup SSP sono kit diagnostici qualitativi in vitro per la tipizzazione del DNA degli alleli HLA di Classe
Olerup SSP Foglio illustrativo Pagina 1 di 34 Olerup SSP USO PREVISTO I kit di tipizzazione HLA Olerup SSP sono kit diagnostici qualitativi in vitro per la tipizzazione del DNA degli alleli HLA di Classe
Istruzioni d uso HISTO TYPE SSP Kits Bassa risoluzione
 Istruzioni d uso HISTO TYPE SSP Kits Bassa risoluzione 0123 Kits per la tipizzazione tissutale degli alleli HLA (Classe I: HLA-A, B, C e Classe II: HLA-DR, DQ) in biologia molecolare IVD 20 tipizzazioni
Istruzioni d uso HISTO TYPE SSP Kits Bassa risoluzione 0123 Kits per la tipizzazione tissutale degli alleli HLA (Classe I: HLA-A, B, C e Classe II: HLA-DR, DQ) in biologia molecolare IVD 20 tipizzazioni
CAPITOLATO SPECIALE. GARA AIC 1 18/2015 GARA ASLTO3 N 43/2016 N. gara SIMOG: CIG Lotti: vd. art. 17 PARTE II - DISCIPLINARE TECNICO
 CAPITOLATO SPECIALE GARA INTERAZIENDALE PER LA FORNITURA DI PLACCHE MONOUSO PER DEFIBRILLATORI OCCORRENTI ALLE AZIENDE: ASLTO1, ASLTO3, ASLTO5, A.O. ORDINE MAURIZIANO, A.O.U. SAN LUIGI GONZAGA GARA AIC
CAPITOLATO SPECIALE GARA INTERAZIENDALE PER LA FORNITURA DI PLACCHE MONOUSO PER DEFIBRILLATORI OCCORRENTI ALLE AZIENDE: ASLTO1, ASLTO3, ASLTO5, A.O. ORDINE MAURIZIANO, A.O.U. SAN LUIGI GONZAGA GARA AIC
Sistema Qualità Diatech PERICOLO DIAGNOSTICA FAI DA TE
 Sistema Qualità Diatech PERICOLO DIAGNOSTICA FAI DA TE 1 Sistema Qualità Diatech dal controllo della qualità alla qualità dei risultati Operare in un settore di alta tecnologia richiede uno strettissimo
Sistema Qualità Diatech PERICOLO DIAGNOSTICA FAI DA TE 1 Sistema Qualità Diatech dal controllo della qualità alla qualità dei risultati Operare in un settore di alta tecnologia richiede uno strettissimo
15 Anti-D policlonale / incompleto
 Scheda Tecnica 0123 Technical File No.: Prodotto: 15 Anti-D policlonale / incompleto Categoria di prodotto secondo la classificazione CE: Allegato II Lista A Struttura della scheda tecnica Descrizione
Scheda Tecnica 0123 Technical File No.: Prodotto: 15 Anti-D policlonale / incompleto Categoria di prodotto secondo la classificazione CE: Allegato II Lista A Struttura della scheda tecnica Descrizione
CAPITOLATO TECNICO DI GARA PER LA FORNITURA DI UN SISTEMA DIAGNOSTICO PER ALLERGOLOGIA
 CAPITOLATO TECNICO DI GARA PER LA FORNITURA DI UN SISTEMA DIAGNOSTICO PER ALLERGOLOGIA OGGETTO: FORNITURA DI UN SISTEMA DIAGNOSTICO PER INDAGINI SIEROLOGICHE (RICERCA ANTICORPI) MEDIANTE TECNICHE IMMUNOMETRICHE
CAPITOLATO TECNICO DI GARA PER LA FORNITURA DI UN SISTEMA DIAGNOSTICO PER ALLERGOLOGIA OGGETTO: FORNITURA DI UN SISTEMA DIAGNOSTICO PER INDAGINI SIEROLOGICHE (RICERCA ANTICORPI) MEDIANTE TECNICHE IMMUNOMETRICHE
REAZIONE A CATENA DELLA POLIMERASI. ( PCR =Polymerase Chain Reaction)
 REAZIONE A CATENA DELLA POLIMERASI ( PCR =Polymerase Chain Reaction) Verso la metà degli anni 80, il biochimico Kary Mullis mise a punto un metodo estremamente rapido e semplice per produrre una quantità
REAZIONE A CATENA DELLA POLIMERASI ( PCR =Polymerase Chain Reaction) Verso la metà degli anni 80, il biochimico Kary Mullis mise a punto un metodo estremamente rapido e semplice per produrre una quantità
ISTRUZIONE OPERATIVA Gestione della cartella clinica del donatore di sangue ed emocomponenti REDAZIONE, VERIFICA, APPROVAZIONE, EMISSIONE
 REDAZIONE, VERIFICA, APPROVAZIONE, EMISSIONE REDAZIONE Dott. Gino Bernuzzi, Dirigente Medico Servizio Immunoematologia e Medicina Trasfusionale APPROVAZIONE Dott. Alessandro Formentini Dirigente Medico.
REDAZIONE, VERIFICA, APPROVAZIONE, EMISSIONE REDAZIONE Dott. Gino Bernuzzi, Dirigente Medico Servizio Immunoematologia e Medicina Trasfusionale APPROVAZIONE Dott. Alessandro Formentini Dirigente Medico.
Allegato A Criteri di valutazione
 POLITECNICO DI TORINO Allegato A Criteri di valutazione Procedura aperta per l individuazione di un operatore economico con cui concludere un Accordo Quadro, ai sensi dell art. 59, comma 4, D.lgs. 163/2006,
POLITECNICO DI TORINO Allegato A Criteri di valutazione Procedura aperta per l individuazione di un operatore economico con cui concludere un Accordo Quadro, ai sensi dell art. 59, comma 4, D.lgs. 163/2006,
La valutazione della Emorragia Feto-Materna: tecniche a confronto
 La valutazione della Emorragia Feto-Materna: tecniche a confronto Dr. Roberto Distefano Servizio di Immunoematologia e Medicina Trasfusionale RAGUSA 6 UK NEQAS Users Meeting Milano 20 novembre 2013 F M
La valutazione della Emorragia Feto-Materna: tecniche a confronto Dr. Roberto Distefano Servizio di Immunoematologia e Medicina Trasfusionale RAGUSA 6 UK NEQAS Users Meeting Milano 20 novembre 2013 F M
C V C. Istruzioni per l'uso del Biofortuna SSPGo TM HLA No Template Control Kit BF-40-02. Revisione 2. Luglio 2014
 DOT136v1 Instructions for Use Biofortuna SSPGo TM HLA No Template Control Kit BF-40-02 Pagina 1 di 7 Istruzioni per l'uso del Biofortuna SSPGo TM HLA No Template Control Kit BF-40-02 Revisione 2 Luglio
DOT136v1 Instructions for Use Biofortuna SSPGo TM HLA No Template Control Kit BF-40-02 Pagina 1 di 7 Istruzioni per l'uso del Biofortuna SSPGo TM HLA No Template Control Kit BF-40-02 Revisione 2 Luglio
DESCRIZIONE DEI DIFFERENTI METODI MOLECOLARI DISPONIBILI PER LA RILEVAZIONE DI HPV E L L IDENTIFICAZIONE DEI GENOTIPI
 DESCRIZIONE DEI DIFFERENTI METODI MOLECOLARI DISPONIBILI PER LA RILEVAZIONE DI HPV E L L IDENTIFICAZIONE DEI GENOTIPI Relatore:Paola Alberizzi-TLBM Responsabile:Dr.ssa Barbara Dal Bello INTRODUZIONE L
DESCRIZIONE DEI DIFFERENTI METODI MOLECOLARI DISPONIBILI PER LA RILEVAZIONE DI HPV E L L IDENTIFICAZIONE DEI GENOTIPI Relatore:Paola Alberizzi-TLBM Responsabile:Dr.ssa Barbara Dal Bello INTRODUZIONE L
Metodologie citogenetiche. Metodologie molecolari. Formulare la domanda Utilizzare la metodica appropriata
 In base al potere di risoluzione della tecnica Metodologie citogenetiche Metodologie molecolari Formulare la domanda Utilizzare la metodica appropriata 1 DNA RNA PROTEINE DNA Cromosomi (cariotipo, FISH,
In base al potere di risoluzione della tecnica Metodologie citogenetiche Metodologie molecolari Formulare la domanda Utilizzare la metodica appropriata 1 DNA RNA PROTEINE DNA Cromosomi (cariotipo, FISH,
Modificazione del 1 gennaio 2017
 Ornanza del DFI del 29 settembre 1995 sulle prestazioni dell assicurazione obbligatoria delle cure meco-sanitarie (Ornanza sulle prestazioni, OPre, allegato 3) RS 832.112.31 Moficazione del 1 gennaio 2017
Ornanza del DFI del 29 settembre 1995 sulle prestazioni dell assicurazione obbligatoria delle cure meco-sanitarie (Ornanza sulle prestazioni, OPre, allegato 3) RS 832.112.31 Moficazione del 1 gennaio 2017
Il percorso del sangue: le attività trasfusionali. ANCONA 26/11/2010 Relatore: Gabriele dr. Amadei
 Il percorso del sangue: le attività trasfusionali ANCONA 26/11/2010 Relatore: Gabriele dr. Amadei Raccolta Sangue: una evoluzione 2 La filiera del Servizio Trasfusionale QuickTime e un decompressore TIFF
Il percorso del sangue: le attività trasfusionali ANCONA 26/11/2010 Relatore: Gabriele dr. Amadei Raccolta Sangue: una evoluzione 2 La filiera del Servizio Trasfusionale QuickTime e un decompressore TIFF
PREMESSE *****************
 OGGETTO: Capitolato per la fornitura omnicomprensiva di sistemi completi di diagnostica per l effettuazione in routine e urgenza dell esame emocromocitometrico per la Struttura Complessa Laboratorio Analisi
OGGETTO: Capitolato per la fornitura omnicomprensiva di sistemi completi di diagnostica per l effettuazione in routine e urgenza dell esame emocromocitometrico per la Struttura Complessa Laboratorio Analisi
Allegato E al Decreto n. 17 del 23.02.2016 pag. 1/5
 Allegato E al Decreto n. 17 del 23.02.2016 pag. 1/5 R E G I O N E V E N E T O Segreteria Regionale per la Sanità Coordinamento Regionale Acquisti per la Sanità * * * * * * LOTTO N. 2 FORNITURA DI SISTEMI
Allegato E al Decreto n. 17 del 23.02.2016 pag. 1/5 R E G I O N E V E N E T O Segreteria Regionale per la Sanità Coordinamento Regionale Acquisti per la Sanità * * * * * * LOTTO N. 2 FORNITURA DI SISTEMI
NUCLEAR LASER MEDICINE
 NUCLEARLASERMEDICINE C A T A L O GO 2 0 1 4 / 1 5 Biologia Molecolare Certificati La Nuclear Laser Medicine srl, grazie ad un radicato e ottimizzato Sistema di Gestione della Qualità (certificazioni secondo
NUCLEARLASERMEDICINE C A T A L O GO 2 0 1 4 / 1 5 Biologia Molecolare Certificati La Nuclear Laser Medicine srl, grazie ad un radicato e ottimizzato Sistema di Gestione della Qualità (certificazioni secondo
PO-TR-010 ACCERTAMENTI DIAGNOSTICI DI QUALIFICAZIONE BIOLOGICA DEGLI EMOCOMPONENTI SUI DONATORI E ASPIRANTI DONATORI
 Unità emittente SGQ Unità destinataria DIR TAL IMM Udr CQB SGQ BSCS SGA LAB CRIO CAR CR X X X X X X X X X X X X REDATTO Dott.ssa P. Carta 25/10/2013 REVISIONATO Dott.ssa M. Ferraro EMESSO Dott. P. A. Accardo
Unità emittente SGQ Unità destinataria DIR TAL IMM Udr CQB SGQ BSCS SGA LAB CRIO CAR CR X X X X X X X X X X X X REDATTO Dott.ssa P. Carta 25/10/2013 REVISIONATO Dott.ssa M. Ferraro EMESSO Dott. P. A. Accardo
Diagnostica Biomolecolare: Tecnologie e Applicazioni
 Diagnostica Biomolecolare: Tecnologie e Applicazioni Preparazione dei campioni: (Estrazione del DNA o dell RNA dal tessuto di interesse) Analisi delle mutazioni: SSCP DHPLC Dot blot - Southern - PCR (ARMS
Diagnostica Biomolecolare: Tecnologie e Applicazioni Preparazione dei campioni: (Estrazione del DNA o dell RNA dal tessuto di interesse) Analisi delle mutazioni: SSCP DHPLC Dot blot - Southern - PCR (ARMS
Italia-Monza: Sistemi diagnostici 2013/S 236-409738. Bando di gara. Forniture
 1/5 Avviso nel sito web TED: http://ted.europa.eu/udl?uri=ted:notice:409738-2013:text:it:html Italia-Monza: Sistemi diagnostici 2013/S 236-409738 Bando di gara Forniture Direttiva 2004/18/CE Sezione I:
1/5 Avviso nel sito web TED: http://ted.europa.eu/udl?uri=ted:notice:409738-2013:text:it:html Italia-Monza: Sistemi diagnostici 2013/S 236-409738 Bando di gara Forniture Direttiva 2004/18/CE Sezione I:
MALATTIA CELIACA. Il test HLA per la celiachia. Le malattie genetiche si distinguono tra monogeniche e multifattoriali
 MALATTIA CELIACA La ricerca della malattia celiaca si esegue evidenziando nel sangue e quindi nel DNA gli alleli che codificano per le molecole DQ2 DQ8. La presenza di questi determina la possibilità che
MALATTIA CELIACA La ricerca della malattia celiaca si esegue evidenziando nel sangue e quindi nel DNA gli alleli che codificano per le molecole DQ2 DQ8. La presenza di questi determina la possibilità che
Tecnologia del DNA ricombinante
 Tecnologia del DNA ricombinante Scoperte rivoluzionarie che hanno permesso lo studio del genoma e della funzione dei singoli geni Implicazioni enormi nel progresso della medicina: comprensione malattie
Tecnologia del DNA ricombinante Scoperte rivoluzionarie che hanno permesso lo studio del genoma e della funzione dei singoli geni Implicazioni enormi nel progresso della medicina: comprensione malattie
HLA: Stato dell arte della ricerca e delle patologie correlate
 HLA: Stato dell arte della ricerca e delle patologie correlate Andrea Bontadini Immunogenetica Policlinico S.Orsola-Malpighi Bologna Centro Servizi Pievesestina 23 novembre 2013 Ciclo di Incontri Scientifici
HLA: Stato dell arte della ricerca e delle patologie correlate Andrea Bontadini Immunogenetica Policlinico S.Orsola-Malpighi Bologna Centro Servizi Pievesestina 23 novembre 2013 Ciclo di Incontri Scientifici
AZIENDA OSPEDALIERO UNIVERSITARIA DI CAGLIARI
 AZIENDA OSPEDALIERO UNIVERSITARIA DI CAGLIARI Procedura aperta, ai sensi dell' art. 55, D.Lgs. 2006, n. 163, ai fini dell'aggiudicazione di una fornitura quadriennale in service per l'esecuzione della
AZIENDA OSPEDALIERO UNIVERSITARIA DI CAGLIARI Procedura aperta, ai sensi dell' art. 55, D.Lgs. 2006, n. 163, ai fini dell'aggiudicazione di una fornitura quadriennale in service per l'esecuzione della
Diagnosi Molecolare delle
 Diagnosi Molecolare delle Malattie infettive Diagnosimolecolare Biologiamolecolare Cosa è la Biologia molecolare? E una branca della biologia che studia gli esseri viventi a livello dei meccanismi molecolari
Diagnosi Molecolare delle Malattie infettive Diagnosimolecolare Biologiamolecolare Cosa è la Biologia molecolare? E una branca della biologia che studia gli esseri viventi a livello dei meccanismi molecolari
AZIENDA OSPEDALIERA DI PERUGIA. Bando di gara - procedura ristretta per la fornitura con la forma del service
 AZIENDA OSPEDALIERA DI PERUGIA Bando di gara - procedura ristretta per la fornitura con la forma del service di strumentazione e reagenti per tipizzazzione molecolare di alleli hla con tecnica pcr-sso
AZIENDA OSPEDALIERA DI PERUGIA Bando di gara - procedura ristretta per la fornitura con la forma del service di strumentazione e reagenti per tipizzazzione molecolare di alleli hla con tecnica pcr-sso
Direttore Dr.ssa Tiziana Riscaldati. SIMT-POS 029 Criteri di Refertazione
 1 1 2 1 SCOPO.Scopo della Presente Procedura è quello di indicare i criteri utilizzati presso il laboratorio di Immunoematologia del SIMT di Viterbo 2 CAMPO D APPLICAZIONE La presente procedura si applica
1 1 2 1 SCOPO.Scopo della Presente Procedura è quello di indicare i criteri utilizzati presso il laboratorio di Immunoematologia del SIMT di Viterbo 2 CAMPO D APPLICAZIONE La presente procedura si applica
Linee guida legionellosi Roma Novembre 2016
 Linee guida legionellosi Roma 10-11 Novembre 2016 La Real-Time PCR per la ricerca di Legionella in campioni ambientali Maria Scaturro Dipartimento di Malattie infettive parassitarie ed immunomediate maria.scaturro@iss.it
Linee guida legionellosi Roma 10-11 Novembre 2016 La Real-Time PCR per la ricerca di Legionella in campioni ambientali Maria Scaturro Dipartimento di Malattie infettive parassitarie ed immunomediate maria.scaturro@iss.it
Istruzioni per l uso HISTO SPOT SSO Kit
 Istruzioni per l uso HISTO SPOT SSO Kit Kit per test di tipizzazione tissutale HLA in biologia molecolare 96 Tipizzazioni IVD 0123 REF 726010: HISTO SPOT A Versione: 05/2012 REF 726020: HISTO SPOT B REF
Istruzioni per l uso HISTO SPOT SSO Kit Kit per test di tipizzazione tissutale HLA in biologia molecolare 96 Tipizzazioni IVD 0123 REF 726010: HISTO SPOT A Versione: 05/2012 REF 726020: HISTO SPOT B REF
AZIENDA OSPEDALIERA S. CROCE E CARLE - CUNEO Ente di rilievo nazionale e di alta specializzazione D.P.C.M. 23.4.1993
 AZIENDA OSPEDALIERA S. CROCE E CARLE - CUNEO Ente di rilievo nazionale e di alta specializzazione D.P.C.M. 23.4.1993 PG/GG ESCLUSIVA esecuz. dosaggio endotossine batteriche med. nucleare DELIBERAZIONE
AZIENDA OSPEDALIERA S. CROCE E CARLE - CUNEO Ente di rilievo nazionale e di alta specializzazione D.P.C.M. 23.4.1993 PG/GG ESCLUSIVA esecuz. dosaggio endotossine batteriche med. nucleare DELIBERAZIONE
Chiarimenti al Si conferma che detta previsione va applicata anche qualora si partecipi ad un lotto in qualità di impresa singola.
 PROCEDURA APERTA CONSORZIATA DA ESPERIRE AI SENSI DEL D. LGS. N. 163/2006 E S.M.I. PER L AFFIDAMENTO DELLA FORNITURA, PER 5 ANNI, IN FULL SERVICE, SUDDIVISO IN N. 111 LOTTI, DI SISTEMI DIAGNOSTICI DI LABORATORIO
PROCEDURA APERTA CONSORZIATA DA ESPERIRE AI SENSI DEL D. LGS. N. 163/2006 E S.M.I. PER L AFFIDAMENTO DELLA FORNITURA, PER 5 ANNI, IN FULL SERVICE, SUDDIVISO IN N. 111 LOTTI, DI SISTEMI DIAGNOSTICI DI LABORATORIO
1. A. MENARINI INDUSTRIE FARMACEUTICHE RIUNITE SRL di Firenze 2. BIO-RAD LABORATORIES SRL di Segrate (MI) 3. TOSOH BIOSCIENCE SRL di Rivoli (TO)
 Allegato A.1 alla Determinazione VERBALE N. 1 DELLA GARA A PROCEDURA APERTA PER L AFFIDAMENTO DELLA FORNITURA IN FULL SERVICE DI SISTEMA DIAGNOSTICO PER EMOGLOBINA GLICATA E VARIANTI EMOGLOBINICHE CON
Allegato A.1 alla Determinazione VERBALE N. 1 DELLA GARA A PROCEDURA APERTA PER L AFFIDAMENTO DELLA FORNITURA IN FULL SERVICE DI SISTEMA DIAGNOSTICO PER EMOGLOBINA GLICATA E VARIANTI EMOGLOBINICHE CON
DRUGFIT LEV1 LEV2 LEV3 REF KCQDRAB1 - KCQDRAB2 - KCQDRAB3
 DRUGFIT LEV1 LEV2 LEV3 REF KCQDRAB1 - KCQDRAB2 - KCQDRAB3 Per Uso Diagnostico In Vitro APPLICAZIONE D USO: Il DRUGFIT è destinato all uso come campione di controllo per monitorare le condizioni di dosaggio
DRUGFIT LEV1 LEV2 LEV3 REF KCQDRAB1 - KCQDRAB2 - KCQDRAB3 Per Uso Diagnostico In Vitro APPLICAZIONE D USO: Il DRUGFIT è destinato all uso come campione di controllo per monitorare le condizioni di dosaggio
Registro nazionale Italiano Donatori Midollo Osseo e Banche di Sangue Cordonale Italian Bone Marrow Donor Registry
 Registro nazionale Italiano Donatori Midollo Osseo e Banche di Sangue Cordonale Italian Bone Marrow Donor Registry TARIFFARIO PER LE PRESTAZIONI PER LA RICERCA E REPERIMENTO DI CELLULE STAMINALI EMATOPOIETICHE
Registro nazionale Italiano Donatori Midollo Osseo e Banche di Sangue Cordonale Italian Bone Marrow Donor Registry TARIFFARIO PER LE PRESTAZIONI PER LA RICERCA E REPERIMENTO DI CELLULE STAMINALI EMATOPOIETICHE
Marcatori molecolari per l analisi genica, genetica e genomica
 Marcatori molecolari per l analisi genica, genetica e genomica (RFLP e PCR-derivati, inclusi SSR e SNP) DNA fingerprinting DNA genotyping DNA haplotyping cp/mtdna barcoding MG/QTL mapping MAS breeding
Marcatori molecolari per l analisi genica, genetica e genomica (RFLP e PCR-derivati, inclusi SSR e SNP) DNA fingerprinting DNA genotyping DNA haplotyping cp/mtdna barcoding MG/QTL mapping MAS breeding
Istruzioni d uso. BAG Cycler Check. REF 7104 (10 test) REF 71044 (4 test) Kit per la validazione dell uniformità della temperatura nei termociclatori
 Istruzioni d uso BAG Cycler Check REF 7104 (10 test) REF 71044 (4 test) Kit per la validazione dell uniformità della temperatura nei termociclatori pronto all uso, prealiquotato Indice 1. Descrizione del
Istruzioni d uso BAG Cycler Check REF 7104 (10 test) REF 71044 (4 test) Kit per la validazione dell uniformità della temperatura nei termociclatori pronto all uso, prealiquotato Indice 1. Descrizione del
Il donatore di emocomponenti e di cellule staminali emopoietiche: attualità e prospettive Compatibilità nel trapianto di CSE e sistema HLA
 Il donatore di emocomponenti e di cellule staminali emopoietiche: attualità e prospettive Compatibilità nel trapianto di CSE e sistema HLA Nicoletta Sacchi Italian Bone Marrow Donor Registry E.O. Ospedali
Il donatore di emocomponenti e di cellule staminali emopoietiche: attualità e prospettive Compatibilità nel trapianto di CSE e sistema HLA Nicoletta Sacchi Italian Bone Marrow Donor Registry E.O. Ospedali
PCR. PCR o reazione di polimerizzazione a catena. Amplificazione esponenziale di DNA. Puo amplificare un tratto di DNA per piu di 1 milione di volte
 PCR Prof.ssa Flavia Frabetti PCR o reazione di polimerizzazione a catena Fine anni 80 Amplificazione esponenziale di DNA. Puo amplificare un tratto di DNA per piu di 1 milione di volte Permette di estrarre
PCR Prof.ssa Flavia Frabetti PCR o reazione di polimerizzazione a catena Fine anni 80 Amplificazione esponenziale di DNA. Puo amplificare un tratto di DNA per piu di 1 milione di volte Permette di estrarre
Allegato III Autocertificazione del produttore
 Scheda Tecnica 0123 Technical File No.: 24 Prodotto: Categoria di prodotto secondo la classificazione CE: Anti-Lua, Anti-Lub coombsreactive Allegato III Autocertificazione del produttore Struttura della
Scheda Tecnica 0123 Technical File No.: 24 Prodotto: Categoria di prodotto secondo la classificazione CE: Anti-Lua, Anti-Lub coombsreactive Allegato III Autocertificazione del produttore Struttura della
Identificazione dei microrganismi mediante tecniche di biologia molecolare Esercitazione n 3. Criteri di identificazione
 Identificazione dei microrganismi mediante tecniche di biologia molecolare Esercitazione n 3 Criteri di identificazione Tradizionale (fenotipo) Tecniche di biologia molecolare Il livello di risoluzione
Identificazione dei microrganismi mediante tecniche di biologia molecolare Esercitazione n 3 Criteri di identificazione Tradizionale (fenotipo) Tecniche di biologia molecolare Il livello di risoluzione
Dott.ssa Patrizia Ferri Segretario Generale
 INTEGRAZIONE DI SISTEMA I fattori chiave nella gestione completa e integrale del servizio di sterilizzazione: certificazioni, logistica, tracciabilità, aggiornamenti normativi Dott.ssa Patrizia Ferri Segretario
INTEGRAZIONE DI SISTEMA I fattori chiave nella gestione completa e integrale del servizio di sterilizzazione: certificazioni, logistica, tracciabilità, aggiornamenti normativi Dott.ssa Patrizia Ferri Segretario
INDICE REDAZIONE: RESPONSABILE DEI CONTENUTI: Dr.ssa Michela Zortea, Direttore Sanitario. CS, versione 2.0 del 25/06/2013 Pag.
 Università degli Studi di Trento CIBIO - DMA Diagnostica Molecolare Avanzata Direttore Sanitario: dott.ssa Michela Zortea Direttore CIBIO: prof. Alessandro Quattrone Pag. 1 di 7 CARTA DEI SERVIZI CIBIO-DMA
Università degli Studi di Trento CIBIO - DMA Diagnostica Molecolare Avanzata Direttore Sanitario: dott.ssa Michela Zortea Direttore CIBIO: prof. Alessandro Quattrone Pag. 1 di 7 CARTA DEI SERVIZI CIBIO-DMA
AZIENDA SOCIO-SANITARIA TERRITORIALE di BERGAMO OVEST. Sede: Treviglio - P.le Ospedale n.1 C.F. - P.I. n
 ORIGINALE AZIENDA SOCIO-SANITARIA TERRITORIALE di BERGAMO OVEST Sede: 24047 Treviglio - P.le Ospedale n.1 C.F. - P.I. n.04114450168 Verbale di Deliberazione del Direttore Generale n 248 del 20-03-2017
ORIGINALE AZIENDA SOCIO-SANITARIA TERRITORIALE di BERGAMO OVEST Sede: 24047 Treviglio - P.le Ospedale n.1 C.F. - P.I. n.04114450168 Verbale di Deliberazione del Direttore Generale n 248 del 20-03-2017
BANDO DI GARA SEZIONE I: AMMINISTRAZIONE AGGIUDICATRICE - I.1) DENOMINAZIONE, INDIRIZZI E PUNTI DI CONTATTO: Denominazione
 AZIENDA OSPEDALIERA S. MARIA -TERNI BANDO DI GARA SEZIONE I: AMMINISTRAZIONE AGGIUDICATRICE - I.1) DENOMINAZIONE, INDIRIZZI E PUNTI DI CONTATTO: Denominazione ufficiale: Azienda Ospedaliera S.Maria Terni;
AZIENDA OSPEDALIERA S. MARIA -TERNI BANDO DI GARA SEZIONE I: AMMINISTRAZIONE AGGIUDICATRICE - I.1) DENOMINAZIONE, INDIRIZZI E PUNTI DI CONTATTO: Denominazione ufficiale: Azienda Ospedaliera S.Maria Terni;
Corso STEM Il papilloma virus (Prof.ssa Gabriella Di Cola)
 Corso STEM Il papilloma virus (Prof.ssa Gabriella Di Cola) Il papilloma virus (HPV) interessa maggiormente le donne intorno ai 25 anni di età; esso intacca la zona genitale, in particolare le cellule dell
Corso STEM Il papilloma virus (Prof.ssa Gabriella Di Cola) Il papilloma virus (HPV) interessa maggiormente le donne intorno ai 25 anni di età; esso intacca la zona genitale, in particolare le cellule dell
RACCOMANDAZIONE REGIONALE PER LA SICUREZZA DELLA TERAPIA FARMACOLOGICA N 3 «GESTIONE SICURA DEI FARMACI ANTINEOPLASTICI»
 RACCOMANDAZIONE REGIONALE PER LA SICUREZZA DELLA TERAPIA FARMACOLOGICA N 3 «GESTIONE SICURA DEI FARMACI ANTINEOPLASTICI» Bologna 8 Aprile 2014 APPROVVIGIONAMENTO e STOCCAGGIO del FARMACO ANTINEOPLASTICO
RACCOMANDAZIONE REGIONALE PER LA SICUREZZA DELLA TERAPIA FARMACOLOGICA N 3 «GESTIONE SICURA DEI FARMACI ANTINEOPLASTICI» Bologna 8 Aprile 2014 APPROVVIGIONAMENTO e STOCCAGGIO del FARMACO ANTINEOPLASTICO
Protocollo Crime Scene Investigation
 Protocollo Crime Scene Investigation Precauzioni da adottare in laboratorio: - non mangiare o bere - indossare sempre i guanti quando si maneggiano i tubini, i gel, le micropipette - nel dubbio, chiedere!
Protocollo Crime Scene Investigation Precauzioni da adottare in laboratorio: - non mangiare o bere - indossare sempre i guanti quando si maneggiano i tubini, i gel, le micropipette - nel dubbio, chiedere!
REGIONE AUTONOMA DELLA SARDEGNA ENTE FORESTE DELLA SARDEGNA VERBALE DI VERIFICA TECNICO/ANALITICA DELLE OFFERTE
 VERBALE DI VERIFICA TECNICO/ANALITICA DELLE OFFERTE Oggetto: Procedura aperta per la fornitura di Dispositivi di Protezione Individuale. Determinazione n. 179 del 22/12/2009. Il giorno 21 del mese di giugno
VERBALE DI VERIFICA TECNICO/ANALITICA DELLE OFFERTE Oggetto: Procedura aperta per la fornitura di Dispositivi di Protezione Individuale. Determinazione n. 179 del 22/12/2009. Il giorno 21 del mese di giugno
RIPARTIZIONE DEL FABBISOGNO ANNUO NUMERO PRODOTTO UNITA' DI MISURA. GR NO 4.000 0 3.000 0 500 500 10%. Esente da Dnase e Rnase.
 NUMERO Agarosio tipo Seakem per elettroforesi di acidi nucleici. Temperatura 1 AGAROSIO di solidificazione (1,5%): 34,5-37,5. - Resistenza del Gel (1%) >= 1,200gr.cm2 - EEO solfati minore di
NUMERO Agarosio tipo Seakem per elettroforesi di acidi nucleici. Temperatura 1 AGAROSIO di solidificazione (1,5%): 34,5-37,5. - Resistenza del Gel (1%) >= 1,200gr.cm2 - EEO solfati minore di
1. DESCRIZIONE DEL PRODOTTO
 Istruzioni per l uso HISTO SPOT SSO Kit Kit per test di tipizzazione tissutale HLA in biologia molecolare 96 Tipizzazioni IVD 0123 REF 726010: HISTO SPOT A 4D (96 test) Versione: 11/2013 REF 726020: HISTO
Istruzioni per l uso HISTO SPOT SSO Kit Kit per test di tipizzazione tissutale HLA in biologia molecolare 96 Tipizzazioni IVD 0123 REF 726010: HISTO SPOT A 4D (96 test) Versione: 11/2013 REF 726020: HISTO
