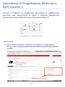
Shortcut Simulation Figura 1: Diagramma di flusso colonna shortcut
|
|
|
- Ignazio Orsini
- 7 anni fa
- Visualizzazioni
Transcript
1 Shortcut Simulation Presentazione del problema/definizione degli obiettivi: La simulazione con metodo shortcut delimita l'ambito operativo ottimale di una colonna di rettifica per miscele che si comportano in modo quasi ideale. I risultati sono da considerare solo come valori orientativi. Una simulazione su colonna dettagliata e la simulazione di miscele non ideali vengono eseguite utilizzando una simulazione su colonna rigorosa, ad es. SCDS. Il vantaggio della colonna shortcut è dato dalla delimitazione del campo di rapporti di riflusso e dal calcolo diretto del piatto di alimentazione. Se ne trae una rapida panoramica della soluzione nel suo complesso. In questo tutorial viene considerata una semplice miscela di due componenti, costituita da benzene e o-xilene. Questa miscela deve essere separata mediante rettifica, raggiungendo una purezza del benzolo minima del 99% in testa. Nella coda non si deve superare una concentrazione di benzene superiore all'1%. La simulazione avviene tramite colonna shortcut per determinare il rapporto di riflusso ottimale e il piatto di alimentazione. Figura 1: Diagramma di flusso colonna shortcut Trasferimento della simulazione con metodo shortcut in CHEMCAD: La simulazione viene eseguita con CHEMCAD Steady State. Prima della simulazione devono essere impostati i componenti e i modelli termodinamici. Sotto "Select Components" vengono selezionati i componenti benzene (CAS-Nr.: ) e o- xilene (CAS-Nr.: ). Il "wizard termodinamico" che si apre successivamente, propone un modello idoneo secondo la specifica della pressione e della temperatura. CHEMCAD propone per l'esempio indicato il modello di valore k (k-value Model) UNIFAC. Come modello di entalpia (Enthaply Model) viene proposto LATE (Latent Heat). Pagina 1 di 11
2 Questa selezione è una decisione preliminare del programma e dovrebbe essere sempre verificata dall'utente o definita con un albero di decisione ([3], Figure 8/9]. Dapprima sotto [Plot] [TPXY] viene tracciato il diagramma T-x e il diagramma di equilibrio per analizzare il comportamento della miscela. Nel diagramma T-x è mostrata la lente di ebollizione dalla quale è possibile leggere immediatamente il componente bassobollente e quello altobollente. Nel diagramma di equilibrio è riconoscibile che la miscela benzene/o-xilene non forma un azeotropo e presenta un comportamento quasi ideale. La simulazione con metodo shortcut è applicabile alla miscela. Figura 2: Diagramma T-x e diagramma di equilibrio Nel diagramma di flusso viene aggiunta la UnitOp (Unit Operation) per la colonna shortcut e questa viene dotata di un flusso di feed e di due flussi di prodotto Il flusso di feed viene importato con i dati indicati nella tabella 1, vedere figura 3. Tabella 1: Dati rilevanti per la simulazione esemplificativa Unità Componenti Termodinamica Flussi di feed Unit Operation SI Benzene (feed) o- xilene (feed) K: UNIFAC, H: LATE Benzene: 50 kg/h o-xilene: 50 kg/h t = 20 C p = 1,013 bar 1 colonna shortcut 1 feed 2 prodotti Pagina 2 di 11
3 Nella fase successiva viene inizializzata la colonna shortcut. Nella finestra di impostazione (figura 3) è possibile selezionare sotto "Select Mode" tre diverse opzioni di progettazione. Figura 3: Finestra di impostazione della colonna shortcut La prima possibilità di selezione "Rating: Fenske- Underwood- Gilliland" non può essere usata per la progettazione. Viene usata se i dati della colonna sono già disponibili e il comportamento di separazione deve essere analizzato rapidamente. Le altre due possibilità di selezione "2 Design; FUG with Fenske feed tray location" e "3 Design; FUG with Kirkbride feed tray location" sono necessarie per la progettazione della colonna shortcut. La differenza fra questi metodi è riassunta nella tabella 2. Tabella 2: Confronto delle opzioni di progettazione nella colonna shortcut 2 Design; FUG with Fenske feed tray location Base di calcolo per -numero di stadi minimo -rapporto di riflusso minimo -numero di stadi teorico Base di calcolo per - piatto di alimentazione teorico Differenza secondo Fenske- Underwood- Gilliland secondo Fenske Calcolo del piatto di alimentazione teorico rispetto al numero di stadi minimo e teorico 3 Design; FUG with Kirkbride feed tray location secondo Fenske- Underwood- Gilliland secondo Kirkbride Calcolo del piatto di alimentazione teorico rispetto al rapporto degli stadi nella sezione di rinforzo e di strippaggio Pagina 3 di 11
4 Per questo tutorial viene scelto il caso 2 "FUG with Fenske feed tray location". Sono necessari tre dati per l'inizializzazione della colonna shortcut: Light Keysplit,Heavy Keysplit e il rapporto. I Keysplit indicano il rapporto tra il bassobollente o l altobollente uscente in testa e quello in entrata nel feed. Questo non è equivalente alla purezza desiderata in testa. La semplificazione del metodo shortcut consiste nel fatto che la miscela da analizzare viene ridotta a un sistema binario. I due componenti da separare vengono indicati come Lightkey e Heavykey. Tramite un bilancio è possibile determinare i flussi di massa in testa ( ) e in coda ( ) per la purezza desiderata (. w indica la frazione massiva. w D m D w F m F w B m B Figura 4: Schizzo della colonna Successivamente è possibile calcolare Light e Heavy Keysplit. Secondo il compito prefisso, è richiesta una concentrazione di benzene minima del 99% in testa (. o-xilene non deve superare una concentrazione massima dell'1% in testa (. In tal modo per i dati indicati nella tabelle 1 si ottiene un Light Keysplit di LKS = 0,99 e un Heavy Keysplit di HKS =0,01. L'ultimo dato necessario per il calcolo della colonna shortcut in CHEMCAD è l'indicazione del rapporto tra rapporto di riflusso teorico e minimo. Lo scopo della simulazione è calcolare il rapporto di riflusso ottimale. Dapprima viene quindi preimpostato solo un valore iniziale che viene in seguito ottimizzato con un Sensitivity Study. Come regola empirica 1 viene indicato in genere un rapporto tra (1 3). Se il rapporto è 1, il rapporto di riflusso corrisponde al rapporto di riflusso minimo, il che darebbe un numero di stadi infinito. Per questo motivo si deve assumere come valore iniziale 1,1. Löwe, Eberhard : Destillation Rektifikation, TFH Berlin, 1989 Pagina 4 di 11
5 Tutte le impostazioni sono inserite e la simulazione può ora essere avviata. Si deve attendere che la colonna arrivi a convergenza. Tramite un Sensitivity Study [6] viene tracciata nella fase successiva la curva energetica delle apparecchiature (figura 5). A tal fine il rapporto viene variato da 1,01 a 3 e viene riportato il relativo numero di stadi teorico calcolato. Figura 5: Curva energetica delle apparecchiature Dalla curva energetica delle apparecchiature si può riconoscere che il numero di stadi diminuisce all'aumentare del rapporto. Tuttavia nella scelta del rapporto ottimale si deve osservare che con un rapporto crescente anche la potenza dell'evaporatore aumenta e di conseguenza i costi di esercizio. Come rapporto ottimale viene impostato e la simulazione viene riavviata. Pagina 5 di 11
6 Valutazione dei risultati della simulazione Le caratteristiche calcolate della colonna sono mostrate nella finestra di impostazione della colonna di shortcut, vedere figura 6. Con i dati impostati è stato calcolato un numero di stadi teorico di 13. Il piatto di alimentazione si trova al 7 stadio. Dai risultati è possibile anche dedurre il rapporto di riflusso, il numero di stadi minimo, la potenza dell'evaporatore e del condensatore. Figura 6: Risultati della simulazione con metodo shortcut Una rappresentazione delle caratteristiche dei flussi di processo (vedere figura 8) avviene sotto [Format] [Add Stream Box]. Figura 7: Caratteristiche dei flussi Pagina 6 di 11
7 Dalla "Stream Box" è possibile leggere le frazioni molari dei componenti in testa, coda e nel feed. Si riconosce che i requisiti definiti dal compito prefissato sono stati raggiunti. Il benzene è stato ottenuto nella sua forma quasi pura. L o-xilene viene rilasciato in testa, solo in concentrazione molto bassa. I risultati della simulazione sono valori orientativi non idonei per una progettazione reale della colonna. Una simulazione dettagliata deve essere eseguita con una colonna rigorosa. Tuttavia le caratteristiche calcolate della colonna delimitano l'ambito operativo, per cui è possibile risparmiare tempo e lavoro effettuando la simulazione con la colonna rigorosa. Basi di processo Di seguito vengono approfondite le conoscenze teoriche di base che si trovano dietro la funzione shortcut e vengono fornite tutte le informazioni dettagliate in merito. Con il metodo shortcut diventa possibile una stima semplice e rapida delle caratteristiche della colonna per la separazione di miscele ideali, in quanto il sistema osservato viene fortemente semplificato. La semplificazione del metodo shortcut consiste nel fatto che la miscela da analizzare viene ridotta a un sistema binario. I due componenti da separare vengono chiamati Lightkey e Heavykey, e vengono osservati nel calcolo idealizzato. Altri componenti influenzano la volatilità relativa ma non vengono tenuti in considerazione nel calcolo. Un'altra semplificazione è che la volatilità relativa e i fattori di separazione sono considerati costanti all'interno dell'intervallo di temperatura osservato. La volatilità relativa è definita come: Si imposta qui per le frazioni in fase vapore la legge di Dalton con la pressione parziale p i e per le frazioni in fase liquida la legge di Raoult (1) (2) con il coefficiente di attività e la pressione di vapore si arriva a (3) CHEMCAD necessita, per il calcolo delle volatilità relative, solo dei coefficienti di attività e delle pressioni di vapore del bassobollente e dell'altobollente. Il calcolo impostato nel modello shortcut, avviene secondo i metodi di calcolo di Fenske Underwood e Gilliland, descritti di seguito. (4) Pagina 7 di 11
8 Con l'equazione di Fenske (5) viene calcolato il numero minimo di piatti in presenza di riflusso totale e frazione di componente/massiva nota nel distillato e nella coda. Si suppone che la volatilità relativa sia in questo caso costante. Poiché la volatilità relativa dipende tuttavia sia dalla composizione della miscela che dalla pressione e dalla temperatura, si effettua il calcolo con una volatilità relativa media, con la volatilità relativa media ( ) (6) è la frazione molare del bassobollente in testa e la frazione molare dell'altobollente nella coda. Con l'equazione di Underwood (7) viene calcolato nella fase successiva il rapporto di riflusso minimo con numero di piatti infinito. Si tratta di un calcolo approssimativo che dipende dall'equilibrio di fase e dalle proprietà del feed. (5) [ ] (7) è la frazione molare del bassobollente nel feed. Come regola empirica viene in genere moltiplicato il rapporto di riflusso minimo per un moltiplicatore. L'equazione di Gilliland è un approccio empirico per calcolare il numero teorico di piatti. Questo approccio empirico è mostrato in un diagramma e può essere descritto con l'equazione di Molokanov. Tale diagramma può essere preso dalla letteratura ([5], pag.199). Il piatto di alimentazione può essere calcolato in due modi. La prima possibilità è secondo Fenske. Dapprima viene definito il numero di piatti con riflusso massimo tramite Fenske (9). Questo numero di piatti corrisponde al numero di piatti necessario per ottenere le concentrazioni desiderate di Lightkey e Heavykey, riferite alla concentrazione di feed. ( ) Con il numero minimo di piatti e il numero di piatti secondo Fenske è possibile calcolare il piatto di alimentazione teorico. (8) (9) (10) Pagina 8 di 11
9 In alternativa il piatto di alimentazione può essere calcolato con l'equazione di Kirkbride. Questa si basa su dati empirici. Viene determinato un rapporto tra il numero teorico di piatti nella sezione di rinforzo e il numero teorico di piatti nella sezione di strippaggio. Da ciò si calcola poi il piatto di alimentazione. [( ) ( ) ] (11) con (12) Nella tabella 3 è riportata una panoramica dei metodi Fenske, Underwood e Gilliand e dei parametri di calcolo più importanti. Tabella 3: Panoramica dell'equazione precedentemente usata Fenske Underwood Gilliland Kirkbride Valori predefiniti - Concentrazioni di testa e coda - Volatilità relative - Concentrazioni di feed e testa - Volatilità relative - Numero minimo di piatti - Rapporto di riflusso minimo -Flusso molare dalla testa e coda - Concentrazioni di feed, testa e coda Valori da calcolare - Numero minimo di piatti - Piatto di alimentazione con riflusso massimo - Rapporto di riflusso massimo con numero di stadi infinito - Rapporto di riflusso effettivo - Numero teorico di piatti con rapporto di riflusso calcolato - Piatto di alimentazione teorico - Piatto di alimentazione teorico La presente simulazione è stata creata in CHEMCAD Pagina 9 di 11
10 Per ricevere ulteriori informazioni su tutorial, seminari o soluzioni inerenti CHEMCAD consultate il sito web. Oppure inviare una mail all'indirizzo: support@chemstations.eu oppure telefonare al numero : +49 (0) Autori: Lisa Weise Daniel Seidl Fonti: [1] Kister, Henry Z.: Distillation design. McGraw-Hill, 1992 [2] Gmehling, Jürgen: Kolbe, Bärbel: Kleiber, Micheal: Rarey, Jürgen: Chemical Thermodynamics for Process Simulation. Wiley-VCH Verlag, 2012 [3] Edwards, John: Process Modeling Selection of Thermodynamic Methods [4] Schmidt, Wolfgang: Ideales Phasengleichgewicht und Shortcut Kolonne, Juli 2011 [5] Sattler, Klaus: Thermische Trennverfahren: Grundlagen, Auslegung, Apparate. Wiley-VCH Verlag, S [6] CHEMCAD Hilfe Pagina 10 di 11
11 Elenco formule Formula Significato Flusso di massa Frazione molare nella fase vapore Frazione massiva Rapporto di riflusso Volatilità relativa Fattore k Frazione molare nella fase liquida Pressione Pressione di saturazione Numero di stadi Flusso molare Elenco indici Indici Significato F Feed D Distillato (Distillate) B Coda (Bottom) L Bassobollente (Light component) H Altobollente (Heavy component) min Minimo 1,2 Componenti 1 & 2 i i-esimo componente Pagina 11 di 11
Simulazione rigorosa su colonna - SCDS
 Simulazione rigorosa su colonna - SCDS Esposizione del problema e principio di risoluzione: Una rettifica può essere rappresentata in modo realistico con una rigorosa simulazione su colonna. È possibile
Simulazione rigorosa su colonna - SCDS Esposizione del problema e principio di risoluzione: Una rettifica può essere rappresentata in modo realistico con una rigorosa simulazione su colonna. È possibile
Rettifica azeotropica
 Rettifica azeotropica Esposizione del problema e principio di risoluzione Data la presenza di un azeotropo, non è possibile estrarre etanolo da una miscela etanoloacqua tramite semplice rettifica. A tale
Rettifica azeotropica Esposizione del problema e principio di risoluzione Data la presenza di un azeotropo, non è possibile estrarre etanolo da una miscela etanoloacqua tramite semplice rettifica. A tale
Distillazione frazionata a batch
 Distillazione frazionata a batch Esposizione del problema e principio di risoluzione Separazione per distillazione di una miscela contenente tre sostanze, in seguito alla quale i costituenti (benzene,
Distillazione frazionata a batch Esposizione del problema e principio di risoluzione Separazione per distillazione di una miscela contenente tre sostanze, in seguito alla quale i costituenti (benzene,
Progettazione di un reattore con flusso a pistone (PFR)
 Progettazione di un reattore con flusso a pistone (PFR) Definizione del problema Il seguente problema di configurazione del reattore è stato preso da Fogler [1] pagina 149, esempio 4-4: Determinare il
Progettazione di un reattore con flusso a pistone (PFR) Definizione del problema Il seguente problema di configurazione del reattore è stato preso da Fogler [1] pagina 149, esempio 4-4: Determinare il
DISTILLAZIONE È un processo di separazione liquido-liquido con trasporto di materia. É finalizzata alla separazione dei componenti di una miscela omog
 DISTILLAZIONE 1 ITIS Marconi Forlì Dicembre 2014 Roberto Zannoni DISTILLAZIONE È un processo di separazione liquido-liquido con trasporto di materia. É finalizzata alla separazione dei componenti di una
DISTILLAZIONE 1 ITIS Marconi Forlì Dicembre 2014 Roberto Zannoni DISTILLAZIONE È un processo di separazione liquido-liquido con trasporto di materia. É finalizzata alla separazione dei componenti di una
Il calcolo di una colonna di rettifica. Metodo di McCabe-Thiele
 Il calcolo di una colonna di rettifica Metodo di McCabe-Thiele Il calcolo di una colonna di rettifica deve immancabilmente iniziare dalla risoluzione del sistema di equazioni costituito dal bilancio globale
Il calcolo di una colonna di rettifica Metodo di McCabe-Thiele Il calcolo di una colonna di rettifica deve immancabilmente iniziare dalla risoluzione del sistema di equazioni costituito dal bilancio globale
Università Degli Studi di Cagliari Facoltà Farmacia Corso di laurea in Tossicologia. Corso di Analisi Chimico-Tossicologica.
 Università Degli Studi di Cagliari Facoltà Farmacia Corso di laurea in Tossicologia Corso di Analisi Chimico-Tossicologica Distillazione La distillazione La distillazione consiste nel vaporizzare un liquido
Università Degli Studi di Cagliari Facoltà Farmacia Corso di laurea in Tossicologia Corso di Analisi Chimico-Tossicologica Distillazione La distillazione La distillazione consiste nel vaporizzare un liquido
DIMENSIONAMENTO Determinazione delle portate F, D, W a determinate condizioni di concentrazione z F, x D e x W Determinazione del numero teorico dei p
 2 ITIS Marconi Forlì Dicembre 204 Roberto Zannoni DIMENSIONAMENTO Determinazione delle portate F, D, W a determinate condizioni di concentrazione z F, x D e x W Determinazione del numero teorico dei piatti.
2 ITIS Marconi Forlì Dicembre 204 Roberto Zannoni DIMENSIONAMENTO Determinazione delle portate F, D, W a determinate condizioni di concentrazione z F, x D e x W Determinazione del numero teorico dei piatti.
PRINCIPIO DISTILLAZIONE
 DISTILLAZIONE Operazione unitaria di separazione più impiegata nell'industria. L'agente di separazione è il calore => non contamina la miscela da separare. PRINCIPIO Fornire calore a una miscela liquida
DISTILLAZIONE Operazione unitaria di separazione più impiegata nell'industria. L'agente di separazione è il calore => non contamina la miscela da separare. PRINCIPIO Fornire calore a una miscela liquida
FONDAMENTI DELLE OPERAZIONI UNITARIE DELL INDUSTRIA CHIMICA Anno Accademico Esercitazione numerica n. 3 Distillazione
 Esercitazione numerica n. 3 Distillazione 1) Una miscela liquida (50% in moli di n-eptano, 50% n-ottano) a 30 C deve essere vaporizzata in continuo in un uno stadio flash ad 1 atm per ottenere il 60% di
Esercitazione numerica n. 3 Distillazione 1) Una miscela liquida (50% in moli di n-eptano, 50% n-ottano) a 30 C deve essere vaporizzata in continuo in un uno stadio flash ad 1 atm per ottenere il 60% di
Controllo dei Processi. Distillazione: processo e modello matematico
 Università di Roma La Sapienza A.A. 2004/2005 Controllo dei Processi Distillazione: processo e modello matematico A cura di Leonardo Cavarischia DIS, Università di Roma La Sapienza Distillazione: processo
Università di Roma La Sapienza A.A. 2004/2005 Controllo dei Processi Distillazione: processo e modello matematico A cura di Leonardo Cavarischia DIS, Università di Roma La Sapienza Distillazione: processo
Un sistema eterogeneo è in equilibrio quando in ogni sua parte è stato raggiunto l equilibrio:
 equilibri eterogenei Un sistema eterogeneo è in equilibrio quando in ogni sua parte è stato raggiunto l equilibrio: (a) termico (temperatura uguale dappertutto); (b) meccanico (pressione uniformemente
equilibri eterogenei Un sistema eterogeneo è in equilibrio quando in ogni sua parte è stato raggiunto l equilibrio: (a) termico (temperatura uguale dappertutto); (b) meccanico (pressione uniformemente
SEQUENZE DI COLONNE DI DISTILLAZIONE
 SEQUENZE DI COLONNE DI DISTILLAZIONE Distillazione => operazione unitaria di separazione più impiegata nell'industria. L'agente di separazione è il calore => non contamina la miscela da separare. Operazione
SEQUENZE DI COLONNE DI DISTILLAZIONE Distillazione => operazione unitaria di separazione più impiegata nell'industria. L'agente di separazione è il calore => non contamina la miscela da separare. Operazione
Applicazione della TSVD allo studio di una colonna di distillazione
 UNIVERSITÀ DEGLI STUDI DI CAGLIARI SCUOLA DI DOTTORATO IN INGEGNERIA INDUSTRIALE Tesina di Metodi Iterativi per la Risoluzione di Sistemi Lineari e Non Lineari Applicazione della TSVD allo studio di una
UNIVERSITÀ DEGLI STUDI DI CAGLIARI SCUOLA DI DOTTORATO IN INGEGNERIA INDUSTRIALE Tesina di Metodi Iterativi per la Risoluzione di Sistemi Lineari e Non Lineari Applicazione della TSVD allo studio di una
Una colonna di rettifica, funzionante a pressione atmosferica, viene alimentata in continuo da 200 kmol/h di una miscela formata da 40 % di benzene e
 4 ITIS Marconi Forlì V m L Dicembre 204 D F V' Roberto Zannoni V B VB L' W Una colonna di rettifica, funzionante a pressione atmosferica, viene alimentata in continuo da 200 kmol/h di una miscela formata
4 ITIS Marconi Forlì V m L Dicembre 204 D F V' Roberto Zannoni V B VB L' W Una colonna di rettifica, funzionante a pressione atmosferica, viene alimentata in continuo da 200 kmol/h di una miscela formata
Rev. 02/13. Antonio Coviello. ITIS Fermi TV
 ASSORBIMENTO Rev. 02/13 Antonio Coviello ITIS Fermi TV SCHEMA COSTRUTTIVO TORRE DI ASSORBIMENTO CON RIEMPIMENTO ASS-ES01: Biossido di Zolfo / Aria / Acqua Una portata di 125 Kmoli/h di aria contenente
ASSORBIMENTO Rev. 02/13 Antonio Coviello ITIS Fermi TV SCHEMA COSTRUTTIVO TORRE DI ASSORBIMENTO CON RIEMPIMENTO ASS-ES01: Biossido di Zolfo / Aria / Acqua Una portata di 125 Kmoli/h di aria contenente
DISTILLAZIONE. Chimica
 Chimica Silvia LICOCCIA Professore Ordinario di Fondamenti Chimici per le Tecnologie Dipartimento di Scienze e Tecnologie Chimiche Università di Roma Tor Vergata DISTILLAZIONE Diagramma P di vapore/composizione
Chimica Silvia LICOCCIA Professore Ordinario di Fondamenti Chimici per le Tecnologie Dipartimento di Scienze e Tecnologie Chimiche Università di Roma Tor Vergata DISTILLAZIONE Diagramma P di vapore/composizione
PROPRIETA DELLE SOLUZIONI
 1 11 PROPRIETA DELLE SOLUZIONI 2 SOLUZIONI IDEALI H mix = 0 le interazioni fra le molecole di soluto e di solvente puri sono paragonabili a quelle fra soluto e solvente; durante il processo di dissoluzione
1 11 PROPRIETA DELLE SOLUZIONI 2 SOLUZIONI IDEALI H mix = 0 le interazioni fra le molecole di soluto e di solvente puri sono paragonabili a quelle fra soluto e solvente; durante il processo di dissoluzione
Deviazioni dall idealità per miscele liquido-vapore. Termodinamica dell Ingegneria Chimica
 Deviazioni dall idealità per miscele liquido-vapore Termodinamica dell Ingegneria Chimica il diagramma P, x per una miscela bicomponente non-ideale La legge di Raoult si applica per pressioni basse e per
Deviazioni dall idealità per miscele liquido-vapore Termodinamica dell Ingegneria Chimica il diagramma P, x per una miscela bicomponente non-ideale La legge di Raoult si applica per pressioni basse e per
Tecniche generali laboratorio. 03 La distillazione
 Tecniche generali laboratorio 03 La distillazione Principi teorici Il processo della distillazione sfrutta due successivi e opposti passaggi di stato: evaporazione/ ebollizione e condensazione. Ogni sostanza
Tecniche generali laboratorio 03 La distillazione Principi teorici Il processo della distillazione sfrutta due successivi e opposti passaggi di stato: evaporazione/ ebollizione e condensazione. Ogni sostanza
Studio concettuale del processo di distillazione per le miscele ternarie
 Università degli Studi dell Aquila Facoltà di Ingegneria Corso di Laurea in Ingegneria Chimica Studio concettuale del processo di distillazione per le miscele ternarie Relatore Prof. Nader Jand Studente
Università degli Studi dell Aquila Facoltà di Ingegneria Corso di Laurea in Ingegneria Chimica Studio concettuale del processo di distillazione per le miscele ternarie Relatore Prof. Nader Jand Studente
Determinazione e confronto delle prestazioni di impianti geotermoelettrici
 Determinazione e confronto delle prestazioni di impianti geotermoelettrici Si ipotizzi di avere una potenza geotermica disponibile pari a 600 MW. La temperatura dell'acqua di refrigerazione all'uscita
Determinazione e confronto delle prestazioni di impianti geotermoelettrici Si ipotizzi di avere una potenza geotermica disponibile pari a 600 MW. La temperatura dell'acqua di refrigerazione all'uscita
ATTREZZATURE PER ESTRAZIONE CON SOLVENTE LIQUIDO/LIQUIDO,
 ISTITUTO TECNICO INDUSTRIALE «G. MARCONI» FORLI Tecnologie chimiche industriali CLASSE V ATTREZZATURE PER ESTRAZIONE CON SOLVENTE LIQUIDO/LIQUIDO, Prof. Roberto Riguzzi ESTRAZIONE LIQUIDO/LIQUIDO L estrattore
ISTITUTO TECNICO INDUSTRIALE «G. MARCONI» FORLI Tecnologie chimiche industriali CLASSE V ATTREZZATURE PER ESTRAZIONE CON SOLVENTE LIQUIDO/LIQUIDO, Prof. Roberto Riguzzi ESTRAZIONE LIQUIDO/LIQUIDO L estrattore
Il punto di fusione di una sostanza è la temperatura alla quale la fase liquida e quella solida si trovano in equilibrio alla pressione di 1 atm.
 Il punto di fusione di una sostanza è la temperatura alla quale la fase liquida e quella solida si trovano in equilibrio alla pressione di 1 atm. Punto di Fusione Il fenomeno della fusione di un solido
Il punto di fusione di una sostanza è la temperatura alla quale la fase liquida e quella solida si trovano in equilibrio alla pressione di 1 atm. Punto di Fusione Il fenomeno della fusione di un solido
Simulazione di scambiatore di calore
 Simulazione di scambiatore di calore Presentazione del problema In questo tutorial viene mostrata la simulazione di uno scambiatore di calore ricorrendo a un esempio. L acqua (1,5 bar, 20 m³/h) deve essere
Simulazione di scambiatore di calore Presentazione del problema In questo tutorial viene mostrata la simulazione di uno scambiatore di calore ricorrendo a un esempio. L acqua (1,5 bar, 20 m³/h) deve essere
EVAPORAZIONE 2. Dati di progetto relativi ai vapori circolanti nell impianto:
 EVAPORAZIONE 2 1. Una soluzione acquosa deve essere concentrata dal 10% al 25% in massa mediante un sistema di evaporazione a doppio effetto in controcorrente. Sapendo che: a) la soluzione diluita entra
EVAPORAZIONE 2 1. Una soluzione acquosa deve essere concentrata dal 10% al 25% in massa mediante un sistema di evaporazione a doppio effetto in controcorrente. Sapendo che: a) la soluzione diluita entra
X disciplinare docenti: Terreni Federica Colombo Pietro
 DISCIPLINA TECNOLOGIE CHIMICHE INDUSTRIALI, PRINCIPI DI A.S. 2013/14 AUTOMAZIONE E ORGANIZZAZIONE INDUSTRIALE X disciplinare docenti: Terreni Federica Colombo Pietro per la classe V CH serale 1) PREREQUISITI
DISCIPLINA TECNOLOGIE CHIMICHE INDUSTRIALI, PRINCIPI DI A.S. 2013/14 AUTOMAZIONE E ORGANIZZAZIONE INDUSTRIALE X disciplinare docenti: Terreni Federica Colombo Pietro per la classe V CH serale 1) PREREQUISITI
Nella seguente tabella sono riportati i dati relativi ai vapori saturi circolanti nell impianto, dove W è il vapore di rete e V il vapore sviluppato:
 EVAPORAZIONE 1 1. Una soluzione acquosa al 10% con una portata di 400 kg/min preriscaldata a 50 C viene concentrata al 25% mediante un evaporatore operante alla pressione di 0,54 ata.tenendo presente che:
EVAPORAZIONE 1 1. Una soluzione acquosa al 10% con una portata di 400 kg/min preriscaldata a 50 C viene concentrata al 25% mediante un evaporatore operante alla pressione di 0,54 ata.tenendo presente che:
Tensione di vapore dei Liquidi A) Alcuni valori di tensione di vapore di Liquidi
 Tensione di vapore dei Liquidi A) Alcuni valori di tensione di vapore di Liquidi Molti valori della tensione di vapore di liquidi sono riportati sul Perry, capitolo 2, 7 a edizione e su altri testi (Gallant,
Tensione di vapore dei Liquidi A) Alcuni valori di tensione di vapore di Liquidi Molti valori della tensione di vapore di liquidi sono riportati sul Perry, capitolo 2, 7 a edizione e su altri testi (Gallant,
IC18DV/92 - Impianto Distillazione Multifunzionale - Cod. 991200
 CHIMICA INDUSTRIALE IC18DV/92 - Impianto Distillazione Multifunzionale - Cod. 991200 IC18DV/92 - Impianto Distillazione Multifunzionale DIDACTA Italia S.r.l. - Strada del Cascinotto, 139/30-10156 Torino
CHIMICA INDUSTRIALE IC18DV/92 - Impianto Distillazione Multifunzionale - Cod. 991200 IC18DV/92 - Impianto Distillazione Multifunzionale DIDACTA Italia S.r.l. - Strada del Cascinotto, 139/30-10156 Torino
Note sulla DISTILLAZIONE
 Note sulla DISTILLAZIONE Dal punto di vista tecnico il processo di "distillazione" è noto fin dai tempi antichi e, pare, spesso usato dagli egizi e dagli alchimisti per ottenere vari tipi di bevande super
Note sulla DISTILLAZIONE Dal punto di vista tecnico il processo di "distillazione" è noto fin dai tempi antichi e, pare, spesso usato dagli egizi e dagli alchimisti per ottenere vari tipi di bevande super
( ) 1 SCOPO 2 CAMPO DI APPLICAZIONE
 Stima della capacità delle valvole di espansione termostatiche 1 Scopo 2 Campo di applicazione 3 Definizioni 3.1 Capacità 3.2 Surriscaldamento 4 Condizioni nominali per refrigeranti azeotropici 5 Condizioni
Stima della capacità delle valvole di espansione termostatiche 1 Scopo 2 Campo di applicazione 3 Definizioni 3.1 Capacità 3.2 Surriscaldamento 4 Condizioni nominali per refrigeranti azeotropici 5 Condizioni
Laboratorio di Impianti Chimici
 Università degli Studi di Torino Corso di Studi in Chimica Industriale Laboratorio di Impianti Chimici Docente: Guido Sassi 1. Simulazione di Processi e Apparecchiature Chimiche in ambiente ASPENPLUS A
Università degli Studi di Torino Corso di Studi in Chimica Industriale Laboratorio di Impianti Chimici Docente: Guido Sassi 1. Simulazione di Processi e Apparecchiature Chimiche in ambiente ASPENPLUS A
2 febbraio con 10 Pa, Pa, K, 1760 J mol e m mol. Con questi dati si ricava la temperatura finale. exp 422.
 febbraio 08. La temperatura di fusione dello zolfo monoclino alla pressione di un bar è 9.3 C. La variazione di volume molare durante la fusione è di.3 cm 3 mol -, mentre il calore latente di fusione è
febbraio 08. La temperatura di fusione dello zolfo monoclino alla pressione di un bar è 9.3 C. La variazione di volume molare durante la fusione è di.3 cm 3 mol -, mentre il calore latente di fusione è
Sistemi di separatore a membrana per processi in vuoto
 Informazioni tecniche Sistemi di separatore a membrana per processi in vuoto Scheda tecnica WIKA IN 00.2 Vuoto Il termine vuoto (dal latino: vacuus) significa "spazio (assolutamente) vuoto o libero". I
Informazioni tecniche Sistemi di separatore a membrana per processi in vuoto Scheda tecnica WIKA IN 00.2 Vuoto Il termine vuoto (dal latino: vacuus) significa "spazio (assolutamente) vuoto o libero". I
La Distillazione: Processo e modello matematico
 La Distillazione: Processo e modello matematico L. Cavarischia Dipartimento di Informatica e Sistemistica, Università di Roma La Sapienza Via Eudossiana 18, 00184 Roma, Italy 1 Introduzione La distillazione
La Distillazione: Processo e modello matematico L. Cavarischia Dipartimento di Informatica e Sistemistica, Università di Roma La Sapienza Via Eudossiana 18, 00184 Roma, Italy 1 Introduzione La distillazione
5. Esercitazione 5: Dimensionamento del primo stadio di una turbina assiale
 5. Esercitazione 5: Dimensionamento del primo stadio di una turbina assiale Lo scopo della presente esercitazione è il dimensionamento del primo stadio di una turbina assiale con i seguenti valori di progetto:
5. Esercitazione 5: Dimensionamento del primo stadio di una turbina assiale Lo scopo della presente esercitazione è il dimensionamento del primo stadio di una turbina assiale con i seguenti valori di progetto:
Le soluzioni e il loro comportamento
 2017 Le soluzioni e il loro comportamento PERCENTUALE IN peso (% p/p) PERCENTUALE IN volume (% v/v) PERCENTUALE IN peso/volume (% p/v) MOLARITA (M) moli soluto / volume soluzione MOLALITA (m) moli soluto
2017 Le soluzioni e il loro comportamento PERCENTUALE IN peso (% p/p) PERCENTUALE IN volume (% v/v) PERCENTUALE IN peso/volume (% p/v) MOLARITA (M) moli soluto / volume soluzione MOLALITA (m) moli soluto
Struttura generale di un processo chimico
 1. Introduzione Struttura generale di un processo chimico Preparazione delle materie prime Reazione Purificazione dei prodotti Operazioni Unitarie: - Riscaldamento - ComminuzioneSize reduction - Miscelazione
1. Introduzione Struttura generale di un processo chimico Preparazione delle materie prime Reazione Purificazione dei prodotti Operazioni Unitarie: - Riscaldamento - ComminuzioneSize reduction - Miscelazione
SVILUPPO DI SENSORI SOFTWARE PER COLONNE DI DISTILLAZIONE MULTICOMPONENTE
 (1) UNIVERSITA DEGLI STUDI DI CAGLIARI Dipartimento di Ingegneria meccanica, chimica e dei materiali (ITALIA) (2) UNIVERSIDAD AUTÓNOMA METROPOLITANA UNIDAD IZTAPALAPA Departamento de Ingeniería de procesos
(1) UNIVERSITA DEGLI STUDI DI CAGLIARI Dipartimento di Ingegneria meccanica, chimica e dei materiali (ITALIA) (2) UNIVERSIDAD AUTÓNOMA METROPOLITANA UNIDAD IZTAPALAPA Departamento de Ingeniería de procesos
Avviate Specifi dall icona presente sul vostro Desktop.
 Avviate Specifi dall icona presente sul vostro Desktop. Nota: Se state utilizzando una versione dimostrativa, una volta caricato il programma, un messaggio vi comunicherà i giorni rimanenti del periodo
Avviate Specifi dall icona presente sul vostro Desktop. Nota: Se state utilizzando una versione dimostrativa, una volta caricato il programma, un messaggio vi comunicherà i giorni rimanenti del periodo
Regolatore bypass gas caldo Tipo KVC
 Scheda tecnica Regolatore bypass gas caldo KVC Il KVC è un regolatore di by-pass di gas caldo utilizzato per adattare la capacità del compressore al carico effettivo dell evaporatore. Posizionato in un
Scheda tecnica Regolatore bypass gas caldo KVC Il KVC è un regolatore di by-pass di gas caldo utilizzato per adattare la capacità del compressore al carico effettivo dell evaporatore. Posizionato in un
DIAGRAMMA DI MOLLIER TABELLE DEL VAPOR D'ACQUA
 DIAGRAMMA DI MOLLIER TABELLE DEL VAPOR D'ACQUA 1 DIAGRAMMA DI MOLLIER DEL VAPORE D'ACQUA RAPPRESENTA I VALORI DELLE VARIABILI TERMODINAMICHE DEL VAPOR D'ACQUA IN UN PIANO h (ASSE Y) / s (ASSE X) h = ENTALPIA
DIAGRAMMA DI MOLLIER TABELLE DEL VAPOR D'ACQUA 1 DIAGRAMMA DI MOLLIER DEL VAPORE D'ACQUA RAPPRESENTA I VALORI DELLE VARIABILI TERMODINAMICHE DEL VAPOR D'ACQUA IN UN PIANO h (ASSE Y) / s (ASSE X) h = ENTALPIA
Corso di Studi di Fisica Corso di Chimica
 Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Lezioni 35-36 2010 Regola delle fasi di Gibbs Lo stato di un sistema fisico è definito quando si conoscono i valori di tutte
Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Lezioni 35-36 2010 Regola delle fasi di Gibbs Lo stato di un sistema fisico è definito quando si conoscono i valori di tutte
Le tensioni di alimentazione +Va e Va devono essere applicate rispetto alla zona di massa.
 4.2 Sul calcolo del guadagno di un microamplificatore Uno schema elettrico che mostra il più semplice impiego di un circuito integrato è tracciato in figura 4.4, in essa è riportato un microamplificatore
4.2 Sul calcolo del guadagno di un microamplificatore Uno schema elettrico che mostra il più semplice impiego di un circuito integrato è tracciato in figura 4.4, in essa è riportato un microamplificatore
SOLUZIONI. solide (es. leghe)
 SOLUZIONI Definizione: Miscela omogenea (una sola fase) di due o più componenti Soluzioni liquide (es. bevande alcoliche) gassose (es. aria) solide (es. leghe) 1 Unità di misura della concentrazione %
SOLUZIONI Definizione: Miscela omogenea (una sola fase) di due o più componenti Soluzioni liquide (es. bevande alcoliche) gassose (es. aria) solide (es. leghe) 1 Unità di misura della concentrazione %
Distributore di liquido Tipo RD
 MAKING MODERN LIVING POSSIBLE Scheda tecnica Distributore di liquido Tipo RD I distributori di refrigerante RD distribuiscono i liquidi refrigeranti dalla valvola di espansione termostatica a singole sezioni
MAKING MODERN LIVING POSSIBLE Scheda tecnica Distributore di liquido Tipo RD I distributori di refrigerante RD distribuiscono i liquidi refrigeranti dalla valvola di espansione termostatica a singole sezioni
Algoritmo per la valutazione della legge di rilascio del calore a partire dal segnale di pressione Parte 1
 Algoritmo per la valutazione della legge di rilascio del calore a partire dal segnale di pressione Parte 1 8.5.212 1. Ciclo (diagramma) indicato 2. Rilievo sperimentale del ciclo indicato 8.5.212 3. Definizione
Algoritmo per la valutazione della legge di rilascio del calore a partire dal segnale di pressione Parte 1 8.5.212 1. Ciclo (diagramma) indicato 2. Rilievo sperimentale del ciclo indicato 8.5.212 3. Definizione
Lo stato liquido. i liquidi molecolari con legami a idrogeno: le interazioni tra le molecole si stabiliscono soprattutto attraverso legami a idrogeno
 Lo stato liquido Le particelle sono in continuo movimento, anche se questo risulta più limitato rispetto al caso dei gas. Il movimento caratteristico a zig-zag delle particelle è chiamato moto Browniano.
Lo stato liquido Le particelle sono in continuo movimento, anche se questo risulta più limitato rispetto al caso dei gas. Il movimento caratteristico a zig-zag delle particelle è chiamato moto Browniano.
Relazione di Sistemi Energetici: Calcolo semplificato del rendimento di una caldaia con e senza "air-heater" rigenerativo.
 Relazione di Sistemi Energetici: Calcolo semplificato del rendimento di una caldaia con e senza "air-heater" rigenerativo. Palagiano, Riccardo matricola 792668 Ostojic, Roberto matricola 811142 Perucchini,
Relazione di Sistemi Energetici: Calcolo semplificato del rendimento di una caldaia con e senza "air-heater" rigenerativo. Palagiano, Riccardo matricola 792668 Ostojic, Roberto matricola 811142 Perucchini,
CHEMCAD aiuta a ridurre il fuori specifica dei prodotti dovuto alla variabilità delle materie prime
 CHEMCAD aiuta a ridurre il fuori specifica dei prodotti dovuto alla variabilità delle materie prime Introduzione L'attenzione crescente verso la variabilità delle materie prime ed il risparmio energetico
CHEMCAD aiuta a ridurre il fuori specifica dei prodotti dovuto alla variabilità delle materie prime Introduzione L'attenzione crescente verso la variabilità delle materie prime ed il risparmio energetico
UNIVERSITÀ DEGLI STUDI DI BRESCIA
 UNIVERSITÀ DEGLI STUDI DI BRESCIA ESAME DI STATO DI ABILITAZIONE ALL'ESERCIZIO DELLA PROFESSIONE DI INGEGNERE (Lauree di primo livello D.M. 509/99 e D.M. 270/04 e Diploma Universitario) SEZIONE B - Seconda
UNIVERSITÀ DEGLI STUDI DI BRESCIA ESAME DI STATO DI ABILITAZIONE ALL'ESERCIZIO DELLA PROFESSIONE DI INGEGNERE (Lauree di primo livello D.M. 509/99 e D.M. 270/04 e Diploma Universitario) SEZIONE B - Seconda
Facoltà di Ingegneria
 Facoltà di Ingegneria Corso di Laurea in Ingegneria per l Ambiente ed il Territorio CONFRONTO TRA METODI PREDITTIVI PER LA STIMA DELLA TEMPERATURA DI FLASH POINT Relatore : prof. Roberto Andreozzi Candidata
Facoltà di Ingegneria Corso di Laurea in Ingegneria per l Ambiente ed il Territorio CONFRONTO TRA METODI PREDITTIVI PER LA STIMA DELLA TEMPERATURA DI FLASH POINT Relatore : prof. Roberto Andreozzi Candidata
REFRIGERAZIONE. Refrigerazione Riduzione e/o mantenimento della temperatura a valori più bassi della temperatura ambiente (<8 C)
 Refrigerazione Riduzione e/o mantenimento della temperatura a valori più bassi della temperatura ambiente (
Refrigerazione Riduzione e/o mantenimento della temperatura a valori più bassi della temperatura ambiente (
Distillatore da laboratorio
 Distillatore da laboratorio Colonna di distillazione Topping LA DISTILLAZIONE La distillazione è una operazione unitaria (avvengono fenomeni fisici) finalizzata alla separazione dei componenti di una miscela,
Distillatore da laboratorio Colonna di distillazione Topping LA DISTILLAZIONE La distillazione è una operazione unitaria (avvengono fenomeni fisici) finalizzata alla separazione dei componenti di una miscela,
PROBLEMA 1. Adottando un ugual salto termico nei tre concentratori e tenendo conto che i fluidi ausiliari sono disponibili alle seguenti condizioni:
 I primi due esercizi sono da impostare e svolgere in classe. Insistere a disegnare impianto e fare tabelle dei vapori. PROBLEMA 1 Una portata di 650 L/h di una soluzione acquosa al 3% in massa di un sale
I primi due esercizi sono da impostare e svolgere in classe. Insistere a disegnare impianto e fare tabelle dei vapori. PROBLEMA 1 Una portata di 650 L/h di una soluzione acquosa al 3% in massa di un sale
Soluzione Esame di Stato ITIS Termotecnica 2013 SVOLGIMENTO :
 Soluzione Esame di Stato ITIS Termotecnica 2013 SVOLGIMENTO : Come è noto, nella fase 3-4 del diagramma T-s di Rankine-Hirn sotto riportato, il fluido, dalla pressione vigente P2 e temperatura T3, si espande
Soluzione Esame di Stato ITIS Termotecnica 2013 SVOLGIMENTO : Come è noto, nella fase 3-4 del diagramma T-s di Rankine-Hirn sotto riportato, il fluido, dalla pressione vigente P2 e temperatura T3, si espande
Scambiatore di calore tubo-in-tubo Tipo HE
 MAKING MODERN LIVING POSSIBLE Scheda tecnica Scambiatore di calore tubo-in-tubo Tipo HE Gli scambiatori di calore HE sono usati principalmente per trasferire calore dalla linea di liquido a quella di aspirazione
MAKING MODERN LIVING POSSIBLE Scheda tecnica Scambiatore di calore tubo-in-tubo Tipo HE Gli scambiatori di calore HE sono usati principalmente per trasferire calore dalla linea di liquido a quella di aspirazione
Ciclo Rankine - Clausius
 Ciclo Rankine - Clausius Si inizia considerando il ciclo di Rankine Clausius anche chiamato ciclo di Hirn semplice avente le seguenti caratteristiche: Temperatura ambiente 30 C Pressione massima 151 bar
Ciclo Rankine - Clausius Si inizia considerando il ciclo di Rankine Clausius anche chiamato ciclo di Hirn semplice avente le seguenti caratteristiche: Temperatura ambiente 30 C Pressione massima 151 bar
Il calcolo del fabbisogno standard complessivo
 Il calcolo del fabbisogno standard complessivo in base all art. 6 D. Lgs. 26 novembre 2010, n. 216 SOSE - Soluzioni per il Sistema Economico S.p.a. 22/11/2016 I FABBISOGNI STANDARD DEI COMUNI ESPRESSI
Il calcolo del fabbisogno standard complessivo in base all art. 6 D. Lgs. 26 novembre 2010, n. 216 SOSE - Soluzioni per il Sistema Economico S.p.a. 22/11/2016 I FABBISOGNI STANDARD DEI COMUNI ESPRESSI
Deviazioni dall idealità: equilibri liquido-liquido. Termodinamica dell Ingegneria Chimica
 Deviazioni dall idealità: equilibri liquido-liquido Termodinamica dell Ingegneria Chimica 1 RT G G = E RT Equilibri liquido-liquido consideriamo ad es. il modello di Margules ad 1 parametro ln(c 1 ) =
Deviazioni dall idealità: equilibri liquido-liquido Termodinamica dell Ingegneria Chimica 1 RT G G = E RT Equilibri liquido-liquido consideriamo ad es. il modello di Margules ad 1 parametro ln(c 1 ) =
Corso di Termofluidodinamica
 Corso di Termofluidodinamica Modulo di Termodinamica Tecnica A.A. 2014-2015 - Esercizi di preparazione alla prima prova intermedia Problema N. 1 Un serbatoio deve essere dimensionato per contenere 200
Corso di Termofluidodinamica Modulo di Termodinamica Tecnica A.A. 2014-2015 - Esercizi di preparazione alla prima prova intermedia Problema N. 1 Un serbatoio deve essere dimensionato per contenere 200
Laboratorio di Progettazione Elettronica Esercitazione 1
 Laboratorio di Progettazione Elettronica Esercitazione 1 Esercizio 1: Progettare un amplificatore operazionale in configurazione invertente come rappresentato in Figura 1. Utilizzare l ampificatore operazionale
Laboratorio di Progettazione Elettronica Esercitazione 1 Esercizio 1: Progettare un amplificatore operazionale in configurazione invertente come rappresentato in Figura 1. Utilizzare l ampificatore operazionale
L Equilibrio chimico
 L Equilibrio chimico 2SO 2 (g) + O 2 (g) 2SO 3 (g) EQUILIBRIO DINAMICO: un equilibrio in cui la costanza dei parametri che caratterizzano il sistema è dovuta alla uguaglianza di tendenze opposte. POSIZIONE
L Equilibrio chimico 2SO 2 (g) + O 2 (g) 2SO 3 (g) EQUILIBRIO DINAMICO: un equilibrio in cui la costanza dei parametri che caratterizzano il sistema è dovuta alla uguaglianza di tendenze opposte. POSIZIONE
La Retta Ogni funzione di primo grado rappresenta, graficamente, una retta. L equazione della retta può essere scritta in due modi
 La Retta Ogni funzione di primo grado rappresenta, graficamente, una retta. L equazione della retta può essere scritta in due modi Forma implicita Forma esplicita a x b y c 0 y m x q a c y x b b Esempio
La Retta Ogni funzione di primo grado rappresenta, graficamente, una retta. L equazione della retta può essere scritta in due modi Forma implicita Forma esplicita a x b y c 0 y m x q a c y x b b Esempio
SCIENZA DEI MATERIALI. Chimica Fisica. VI Lezione. Dr. Fabio Mavelli. Dipartimento di Chimica Università degli Studi di Bari
 SCIENZA DEI MATERIALI Chimica Fisica VI Lezione Dr. Fabio Mavelli Dipartimento di Chimica Università degli Studi di Bari Energia Libera di Helmholtz F 2 Definiamo la funzione di stato Energia Libera di
SCIENZA DEI MATERIALI Chimica Fisica VI Lezione Dr. Fabio Mavelli Dipartimento di Chimica Università degli Studi di Bari Energia Libera di Helmholtz F 2 Definiamo la funzione di stato Energia Libera di
PROCEDURE DI CALCOLO DELLA COMBINAZIONE DEGLI INERTI REALI
 PROCEDURE DI CALCOLO DELLA COMBINAZIONE DEGLI INERTI REALI Non esistono già disponibili in natura materiali lapidei con distribuzione granulometrica eguale a quella ideale richiesta per un inerte da destinare
PROCEDURE DI CALCOLO DELLA COMBINAZIONE DEGLI INERTI REALI Non esistono già disponibili in natura materiali lapidei con distribuzione granulometrica eguale a quella ideale richiesta per un inerte da destinare
miscela di reazione miscela di reazione
 Alla fine della reazione: miscela di reazione 1.Si tratta con acqua o acqua e ghiaccio 2.Si aggiunge un solvente organico immiscibile e si agita Si lava (estrae) con una base Si lava (estrae) con un acido
Alla fine della reazione: miscela di reazione 1.Si tratta con acqua o acqua e ghiaccio 2.Si aggiunge un solvente organico immiscibile e si agita Si lava (estrae) con una base Si lava (estrae) con un acido
ENERGIA E CALORE energia Joule (J) KJ (Kilojoule). Kilowattora (KWh) calore Caloria (Cal o KCal) Caloria calore British Thermal Unit (Btu)
 ENERGIA E CALORE Unità di misura dell'energia: Joule (J), unità troppo piccola; comunemente si usa il suo multiplo, il KJ (Kilojoule). Importante è anche il Kilowattora (KWh), unità usata nella misura
ENERGIA E CALORE Unità di misura dell'energia: Joule (J), unità troppo piccola; comunemente si usa il suo multiplo, il KJ (Kilojoule). Importante è anche il Kilowattora (KWh), unità usata nella misura
Formule empiriche e formule molecolari
 COMPLEMENTI A Formule empiriche e formule molecolari Nella prima metà del diciannovesimo secolo J.J. Berzelius, J.B. A. Dumas, Justus Liebig e Stanislao Cannizzaro misero a punto i metodi per la determinazione
COMPLEMENTI A Formule empiriche e formule molecolari Nella prima metà del diciannovesimo secolo J.J. Berzelius, J.B. A. Dumas, Justus Liebig e Stanislao Cannizzaro misero a punto i metodi per la determinazione
Figura 1 - Schema dell'impianto
 File:C:\Esercitazioni FTMAC\EES\Impianto vapore 2 spill.ees 12/05/2005 8.23.20 Page 1 4 3 16 5 6 13 10 7 2 1 18 17 15 12 14 11 9 8 T DTI Spillamento Acqua alimento DTU Figura 1 - Schema dell'impianto 0
File:C:\Esercitazioni FTMAC\EES\Impianto vapore 2 spill.ees 12/05/2005 8.23.20 Page 1 4 3 16 5 6 13 10 7 2 1 18 17 15 12 14 11 9 8 T DTI Spillamento Acqua alimento DTU Figura 1 - Schema dell'impianto 0
Le soluzioni e il loro comportamento
 A. A. 2016 2017 1 CCS Scienze geologiche CCS Biologia Le soluzioni e il loro comportamento PERCENTUALE IN peso (% p/p) PERCENTUALE IN volume (% v/v) PERCENTUALE IN peso/volume (% p/v) MOLARITA (M) moli
A. A. 2016 2017 1 CCS Scienze geologiche CCS Biologia Le soluzioni e il loro comportamento PERCENTUALE IN peso (% p/p) PERCENTUALE IN volume (% v/v) PERCENTUALE IN peso/volume (% p/v) MOLARITA (M) moli
ESERCIZI DI TERMODINAMICA. costante di equilibrio della reazione. costante di equilibrio della reazione
 ESECIZI DI EMODINAMICA Esercizio Calcolare a c.s. la costante di equilibrio della seguente reazione: CO (g) + H CH OH (g) H f (kj/mole) CH OH (g) -, CO (g) -,5 H (g) S (J/mole K) CH OH (g) 6,8 CO (g) 97,9
ESECIZI DI EMODINAMICA Esercizio Calcolare a c.s. la costante di equilibrio della seguente reazione: CO (g) + H CH OH (g) H f (kj/mole) CH OH (g) -, CO (g) -,5 H (g) S (J/mole K) CH OH (g) 6,8 CO (g) 97,9
Un modello per il gas ideale
 Un modello per il gas ideale Un gas ideale consiste di particelle (atomi o molecole) che hanno le seguenti proprietà 1. Il volume proprio delle particelle è trascurabile rispetto al volume occupato dal
Un modello per il gas ideale Un gas ideale consiste di particelle (atomi o molecole) che hanno le seguenti proprietà 1. Il volume proprio delle particelle è trascurabile rispetto al volume occupato dal
REFORMING dei COMBUSTIBILI
 MODELLAZIONE e SIMULAZIONE dei SISTEMI ENERGETICI REFORMING dei COMBUSTIBILI Ing. Vittorio Tola DIMCM - Dipartimento di Ingegneria Meccanica, Chimica e dei Materiali PRODUZIONE di IDROGENO Negli ultimi
MODELLAZIONE e SIMULAZIONE dei SISTEMI ENERGETICI REFORMING dei COMBUSTIBILI Ing. Vittorio Tola DIMCM - Dipartimento di Ingegneria Meccanica, Chimica e dei Materiali PRODUZIONE di IDROGENO Negli ultimi
PSICROMETRIA PROPRIETÀ TERMODINAMICHE DEI GAS PERFETTI
 PSICROMETRIA PROPRIETÀ TERMODINAMICHE DEI GAS PERFETTI Un modello di comportamento interessante per la termodinamica è quello cosiddetto di gas perfetto. Il gas perfetto è naturalmente un astrazione, tuttavia
PSICROMETRIA PROPRIETÀ TERMODINAMICHE DEI GAS PERFETTI Un modello di comportamento interessante per la termodinamica è quello cosiddetto di gas perfetto. Il gas perfetto è naturalmente un astrazione, tuttavia
Regolatore della pressione dell evaporatore Tipo KVP
 Fiche technique Regolatore della pressione dell evaporatore KVP Il regolatore KVP viene montato sulla linea di aspirazione a valle dell evaporatore e viene utilizzato per le seguenti funzioni:. Mantenimento
Fiche technique Regolatore della pressione dell evaporatore KVP Il regolatore KVP viene montato sulla linea di aspirazione a valle dell evaporatore e viene utilizzato per le seguenti funzioni:. Mantenimento
ISIS A PONTI Gallarate
 4 A TCB 1 IL CROMATOGRAMMA: E il tracciato che descrive l andamento del segnale del rivelatore in funzione del tempo o del volume di eluente a partire dall istante in cui la miscela viene introdotta nella
4 A TCB 1 IL CROMATOGRAMMA: E il tracciato che descrive l andamento del segnale del rivelatore in funzione del tempo o del volume di eluente a partire dall istante in cui la miscela viene introdotta nella
Proprietà volumetriche delle sostanze pure. Principi di Ingegneria Chimica Ambientale
 Proprietà volumetriche delle sostanze pure Principi di Ingegneria Chimica Ambientale le fasi di una specie pura Una sostanza la cui composizione chimica non varia in tutta la massa presa in considerazione
Proprietà volumetriche delle sostanze pure Principi di Ingegneria Chimica Ambientale le fasi di una specie pura Una sostanza la cui composizione chimica non varia in tutta la massa presa in considerazione
UNIVERSITÀ DEGLI STUDI DI PADOVA
 PROVA N. 2. Ramo Gestionale Un'azienda sta valutando la convenienza economica di una macchina che è in grado di apportare benefici al processo produttivo esistente sulla base dei seguenti dati: investimento
PROVA N. 2. Ramo Gestionale Un'azienda sta valutando la convenienza economica di una macchina che è in grado di apportare benefici al processo produttivo esistente sulla base dei seguenti dati: investimento
Le proprietà colligative delle soluzioni Sappiamo dall esperienza quotidiana che una soluzione ha caratteristiche diverse dal solvente puro.
 Le proprietà colligative delle soluzioni Sappiamo dall esperienza quotidiana che una soluzione ha caratteristiche diverse dal solvente puro. Molte delle sue proprietà, come il sapore, il colore, l odore,
Le proprietà colligative delle soluzioni Sappiamo dall esperienza quotidiana che una soluzione ha caratteristiche diverse dal solvente puro. Molte delle sue proprietà, come il sapore, il colore, l odore,
UNIVERSITA DEGLI STUDI DI BRESCIA Facoltà di Ingegneria
 PRIMA PROVA SCRITTA DEL 22 giugno 2011 SETTORE INDUSTRIALE TEMA N. 1 Il candidato fornisca una panoramica generale sugli scambiatori di calore, indicandone le principali tipologie e caratteristiche. Ne
PRIMA PROVA SCRITTA DEL 22 giugno 2011 SETTORE INDUSTRIALE TEMA N. 1 Il candidato fornisca una panoramica generale sugli scambiatori di calore, indicandone le principali tipologie e caratteristiche. Ne
10.1 Sono date le frazioni molari dei costituenti dell'aria umida. Si devono determinare le frazioni di massa dei costituenti.
 1 RISOLUZIONI cap.10 10.1 Sono date le frazioni molari dei costituenti dell'aria umida. Si devono determinare le frazioni di massa dei costituenti. Ipotesi Si trascurano le piccole quantità di gas nell'aria
1 RISOLUZIONI cap.10 10.1 Sono date le frazioni molari dei costituenti dell'aria umida. Si devono determinare le frazioni di massa dei costituenti. Ipotesi Si trascurano le piccole quantità di gas nell'aria
Corso Avanzato sul sondaggio termodinamico dell atmosfera
 Istituto Tecnico Aeronautico Statale Euclide Seminari di Meteorologia Corso Avanzato sul sondaggio termodinamico Parte IV A cura di Vittorio Villasmunta Previsore del Servizio Meteorologico dell Aeronautica
Istituto Tecnico Aeronautico Statale Euclide Seminari di Meteorologia Corso Avanzato sul sondaggio termodinamico Parte IV A cura di Vittorio Villasmunta Previsore del Servizio Meteorologico dell Aeronautica
Studio dei diagrammi di fase per sistemi a due componenti
 Studio dei diagrammi di fase per sistemi a due componenti Per affrontare questo studio dobbiamo conoscere la REGOLA DELLE FASI Le condizioni per l equilibrio tra le fasi possono essere sintetizzate in
Studio dei diagrammi di fase per sistemi a due componenti Per affrontare questo studio dobbiamo conoscere la REGOLA DELLE FASI Le condizioni per l equilibrio tra le fasi possono essere sintetizzate in
CORSO DI TERMODINAMICA A.A
 CORSO DI TERMODINAMICA A.A. 2006-07 ESERCITAZIONE N. 2 Miscele ideali 1. Calcolare la composizione di una soluzione liquida di benzene e toluene, satura alla pressione di 1 atm ed alla temperatura di 100
CORSO DI TERMODINAMICA A.A. 2006-07 ESERCITAZIONE N. 2 Miscele ideali 1. Calcolare la composizione di una soluzione liquida di benzene e toluene, satura alla pressione di 1 atm ed alla temperatura di 100
CORSO DI TERMODINAMICA A.A
 CORSO DI TERMODINAMICA A.A. 2006-07 ESERCITAZIONE N. 2 Miscele ideali 1. Calcolare la composizione di una soluzione liquida di benzene e toluene, satura alla pressione di 1 atm ed alla temperatura di 100
CORSO DI TERMODINAMICA A.A. 2006-07 ESERCITAZIONE N. 2 Miscele ideali 1. Calcolare la composizione di una soluzione liquida di benzene e toluene, satura alla pressione di 1 atm ed alla temperatura di 100
air protection technology
 ADS Adsorbimento su carboni attivi e rigenerazione Campo di applicazione Recupero solventi clorurati e non clorurati. Descrizione del processo Le S.O.V. adsorbite sui carboni attivi possono essere strippate
ADS Adsorbimento su carboni attivi e rigenerazione Campo di applicazione Recupero solventi clorurati e non clorurati. Descrizione del processo Le S.O.V. adsorbite sui carboni attivi possono essere strippate
Corso Termodinamica. Esercitazione 3. II Principio
 Corso Termodinamica Esercitazione 3 II Principio 1. Una mole di metano fluisce in un condotto; la sua pressione passa da 1.5 a 0.5 atm a temperatura costante. Calcolare la variazione di entropia. 2. Calcolare
Corso Termodinamica Esercitazione 3 II Principio 1. Una mole di metano fluisce in un condotto; la sua pressione passa da 1.5 a 0.5 atm a temperatura costante. Calcolare la variazione di entropia. 2. Calcolare
IMPIANTO FRIGORIFERO A COMPRESSIONE DI VAPORE CON CAMERA DI SEPARAZIONE (liquido - vapore) E COMPRESSIONE A DUE STADI
 IMPIANTO FRIGORIFERO A COMPRESSIONE DI VAPORE CON CAMERA DI SEPARAZIONE (liquido - vapore) E COMPRESSIONE A DUE STADI IMPIANTO FRIGORIFERO A COMPRESSIONE DI VAPORE CON CAMERA DI SEPARAZIONE (liquido -
IMPIANTO FRIGORIFERO A COMPRESSIONE DI VAPORE CON CAMERA DI SEPARAZIONE (liquido - vapore) E COMPRESSIONE A DUE STADI IMPIANTO FRIGORIFERO A COMPRESSIONE DI VAPORE CON CAMERA DI SEPARAZIONE (liquido -
Diagramma di fase f(p,v,t)=0
 Diagramma di fase f(p,v,t)=0 Taglio P(V) (per diversi valori di T) Prospetto P(T) Prospetto P(T): variazione di volume alla fusione Congelando si contrae Es: anidride carbonica Congelando si espande
Diagramma di fase f(p,v,t)=0 Taglio P(V) (per diversi valori di T) Prospetto P(T) Prospetto P(T): variazione di volume alla fusione Congelando si contrae Es: anidride carbonica Congelando si espande
SCHEDA PROGRAMMAZIONE UNITÀ FORMATIVE DISCIPLINARI
 SCHEDA PROGRAMMAZIONE UNITÀ FORMATIVE DISCIPLINARI UNITÀ FORMATIVA N 1 - CLASSE 2 A Professionale TITOLO: Le formule dei composti e le reazioni chimiche Periodo/Durata: settembre-ottobre/ 12 ore Saper
SCHEDA PROGRAMMAZIONE UNITÀ FORMATIVE DISCIPLINARI UNITÀ FORMATIVA N 1 - CLASSE 2 A Professionale TITOLO: Le formule dei composti e le reazioni chimiche Periodo/Durata: settembre-ottobre/ 12 ore Saper
66 Congresso Nazionale ATI Cosenza, 5-9 Settembre 2011
 66 Congresso Nazionale ATI Cosenza, STABILITÀ TERMICA DI FLUIDI DI LAVORO E PRESTAZIONI TERMODINAMICHE DEL REFRIGERANTE HFC-245FA IN CICLI PER APPLICAZIONI GEOTERMICHE Paola Bombarda 1, Costante M. Invernizzi
66 Congresso Nazionale ATI Cosenza, STABILITÀ TERMICA DI FLUIDI DI LAVORO E PRESTAZIONI TERMODINAMICHE DEL REFRIGERANTE HFC-245FA IN CICLI PER APPLICAZIONI GEOTERMICHE Paola Bombarda 1, Costante M. Invernizzi
GUIDA NUOVA FUNZIONE CARICO FLUSSI. Sommario. Carico Flussi pag. 2 Opzioni pag. 4 Sostituzioni pag. 5 Esiti pag. 7
 GUIDA NUOVA FUNZIONE CARICO FLUSSI Sommario Carico Flussi pag. 2 Opzioni pag. 4 Sostituzioni pag. 5 Esiti pag. 7 Aggiornamento al 13.10.2016 1 CARICO FLUSSI Questa funzione consente di effettuare l upload
GUIDA NUOVA FUNZIONE CARICO FLUSSI Sommario Carico Flussi pag. 2 Opzioni pag. 4 Sostituzioni pag. 5 Esiti pag. 7 Aggiornamento al 13.10.2016 1 CARICO FLUSSI Questa funzione consente di effettuare l upload
Proprietà volumetriche delle sostanze pure. Termodinamica dell Ingegneria Chimica
 Proprietà volumetriche delle sostanze pure Termodinamica dell Ingegneria Chimica le fasi di una specie pura Una sostanza la cui composizione chimica non varia in tutta la massa presa in considerazione
Proprietà volumetriche delle sostanze pure Termodinamica dell Ingegneria Chimica le fasi di una specie pura Una sostanza la cui composizione chimica non varia in tutta la massa presa in considerazione
ISTITUZIONI DI ECONOMIA (a.a ) PROVE D ESAME
 Giuseppe Garofalo Dipartimento di Economia pubblica Facoltà di Economia Università degli studi di Roma La Sapienza ISTITUZIONI DI ECONOMIA (a.a. 1999-2000) PROVE D ESAME Prova intermedia di Macro (4-3-2000)
Giuseppe Garofalo Dipartimento di Economia pubblica Facoltà di Economia Università degli studi di Roma La Sapienza ISTITUZIONI DI ECONOMIA (a.a. 1999-2000) PROVE D ESAME Prova intermedia di Macro (4-3-2000)
Applicazioni del primo principio della termodinamica ed utilizzo delle tabelle del vapore: Esercizi svolti
 Applicazioni del primo principio della termodinamica ed utilizzo delle tabelle del vapore: Esercizi svolti 19 marzo 23 Esercizio 1 Un recipiente di volume ssato e con pareti adiabatiche è diviso in due
Applicazioni del primo principio della termodinamica ed utilizzo delle tabelle del vapore: Esercizi svolti 19 marzo 23 Esercizio 1 Un recipiente di volume ssato e con pareti adiabatiche è diviso in due
LA MATERIA ED I SUOI STATI
 LA MATERIA ED I SUOI STATI GAS COMPOSIZIONE DELL ARIA 1. I gas ideali e la teoria cineticomolecolare Nel modello del gas ideale le particelle 1. l energia cinetica media delle particelle è proporzionale
LA MATERIA ED I SUOI STATI GAS COMPOSIZIONE DELL ARIA 1. I gas ideali e la teoria cineticomolecolare Nel modello del gas ideale le particelle 1. l energia cinetica media delle particelle è proporzionale
