Trasporto dell ossigeno
|
|
|
- Emanuele Bartolini
- 7 anni fa
- Visualizzazioni
Transcript
1 Prof. Giorgio Sartor Trasporto dell ossigeno Copyright by Giorgio Sartor. All rights reserved. Versione 0.1 oct 2011 Trasporto dell ossigeno egli organismi aerobi il trasporto dell ossigeno avviene ad opera di PIGMETI RESPIRATORI Proteine coniugate con metalli che legano O 2, lo trasportano attraverso i fluidi, lo convogliano nei tessuti dove viene rilasciato ed utilizzato. gs ver 0.1 L05 - Trasporto dell ossigeno 2 1
2 I pigmenti respiratori Pigmento Colore Struttura Sito per O 2 Localizzazione Mioglobina (Mb) - Proteina Eme Fe ++ 1O 2 /1Fe ++ Muscolo Emoglobina (Hb) Rosso Proteina Eme Fe ++ 1O 2 /1Fe ++ Globuli rossi Soluzione Clorocruorina (Ch) Verde Proteina Eme Fe ++ 1O 2 /1Fe ++ Soluzione Emeritrina (Hr) Violetto Incolore Proteina Fe ++ 1O 2 /2Fe ++ Soluzione (Globuli rossi) Emocianina (Hc) Blu Incolore Proteina Cu ++ 1O 2 /2Cu ++ Soluzione gs ver 0.1 L05 - Trasporto dell ossigeno 3 I pigmenti respiratori Pigmento Mioglobina (Mb) Emoglobina (Hb) Clorocruorina (Ch) Emeritrina (Hr) Emocianina (Hc) gs ver 0.1 L05 - Trasporto dell ossigeno 4 2
3 gs ver 0.1 L05 - Trasporto dell ossigeno 5 Proteine multimeriche I pigmenti respiratori dedicati al trasporto dell ossigeno sono formati da più subunità: Mioglobina, immagazzina O 2, una subunità Emoglobina, trasporta O 2, da 2 a 10 subunità a secondo dell organismo Emocianina, trasporta O 2, da 1 6 subunità a 8 6 subunità a secondo dell organismo La presenza di più subunità rende il legame dell O 2 cooperativo permettendone un trasporto efficiente. gs ver 0.1 L05 - Trasporto dell ossigeno 6 3
4 Aria Perché i pigmenti respiratori Volume occupato da 1 mole di gas: 22.4 litri (STP) Contenuto di gas in 1 litro di aria: 1/22.4 = moli = 45 millimoli Solo 21% dei gas dell aria è O 2, quindi 45x21/100 = 9.5 millimoli Acqua o plasma Solubilità di O 2 in acqua (α): 1.4 x 10-6 moli/l/mmhg (a 37 C) [O 2 ] = α x PO 2 = 1.4 x 10-6 x 150 = moli o 0.21 mmoli Emoglobina (160 g/l, globuli rossi concentrati) PM = 16,000 [Hb ]= 160/16,000 = 10 mm Sangue (50% plasma + 50% globuli rossi) Plasma: [O 2 ] = 0.21 mm Emoglobina: [O 2 ] = 10 mm Sangue: [O 2 ] = (0.21 x 0.5) + (10 x 0.5) = = mmoli (2% + 98%) 98% dell O 2 del sangue è legato a Hb, 2% è fisicamente disciolto nel plasma. gs ver 0.1 L05 - Trasporto dell ossigeno 7 Cellule specializzate Globuli rossi Prive di nucleo Alto contenuto in Hb gs ver 0.1 L05 - Trasporto dell ossigeno 8 4
5 Legame con l ossigeno Dipende da po 2 Alta po 2 PR + O 2 PR-O 2 O SATURATO Bassa po 2 SATURATO gs ver 0.1 L05 - Trasporto dell ossigeno 9 Legame con l ossigeno Dipende da po 2 gs ver 0.1 L05 - Trasporto dell ossigeno 10 5
6 Mioglobina ed Emoglobina Le funzioni biologiche delle due proteine sono diverse: Mioglobina: lega strettamente l O 2 e lo rende disponibile SOLO quando la po 2 è molto bassa (muscolo, cetacei in immersione). Emoglobina: lega l O 2 quando la po 2 è alta (polmoni, branchie) rilascia l O 2 quando la po 2 è bassa (tessuti, cellule). La struttura delle due proteine è diversa: Mioglobina: monomero con gruppo prostetico (eme) che complessa uno ione Fe 2+. Emoglobina: tetramero (nei mammiferi) fatto di subunità (α 2 β 2 ) ognuna delle quali è simile alla mioglobina e contiene un gruppo prostetico (eme) che complessa uno ione Fe 2+. gs ver 0.1 L05 - Trasporto dell ossigeno 11 Mioglobina e emoglobina gs ver 0.1 L05 - Trasporto dell ossigeno 12 6
7 Mioglobina Trasporto dell O 2, immagazzinamento nella cellula. Due parti: proteina gruppo prostetico Proteina: 155 aminoacidi, ~ 17 kda. Compatta, globina. 75% α-elica. gs ver 0.1 L05 - Trasporto dell ossigeno 13 Mioglobina Trasporto dell O 2, immagazzinamento nella cellula. Due parti: proteina gruppo prostetico Proteina: 155 aminoacidi, ~ 17 kda. Compatta, globina. 75% α-elica. gs ver 0.1 L05 - Trasporto dell ossigeno 14 7
8 Gruppo eme Il gruppo eme è composta di porfirina e Fe 2+. La porfirina è un gruppo non polare, ci sono inoltre due gruppi polari di propionato. La porfirina lega O 2, CO. CO è 10,000 volte più affine alla porfirina del O 2. Propionato O O CH 3 CH 3 CH2 Fe ++ O O CH 3 CH 2 CH 3 gs ver 0.1 Fe ++ L05 - Trasporto dell ossigeno 15 Ligandi al gruppo eme Lo ione Fe ++ coordina sei atomi. Quattro atomi di azoto del gruppo eme Una molecola di ossigeno Ossiemoglobina lega O 2 Deossiglobina lega H 2 O Carbossiglobina lega CO. Un atomo di azoto dall His prossimale. gs ver 0.1 L05 - Trasporto dell ossigeno 16 8
9 Ligandi al gruppo eme Lo ione Fe ++ coordina sei atomi. Quattro atomi di azoto del gruppo eme Una molecola di ossigeno Ossiemoglobina lega O 2 Deossiglobina lega H 2 O Carbossiglobina lega CO. Un atomo di azoto dall His prossimale. gs ver 0.1 L05 - Trasporto dell ossigeno 17 Ligandi al gruppo eme Lo ione Fe ++ coordina sei atomi. Quattro atomi di azoto del gruppo eme Una molecola di ossigeno Ossiemoglobina lega O 2 Deossiglobina lega H 2 O Carbossiglobina lega CO. Un atomo di azoto dall His prossimale. gs ver 0.1 L05 - Trasporto dell ossigeno 18 9
10 Ligandi al gruppo eme Lo ione Fe ++ coordina sei atomi. Quattro atomi di azoto del gruppo eme Una molecola di ossigeno Ossiemoglobina lega O 2 Deossiglobina lega H 2 O Carbossiglobina lega CO. Un atomo di azoto dall His prossimale. gs ver 0.1 L05 - Trasporto dell ossigeno 19 Ligandi al gruppo eme Lo spazio compreso tra il Fe ++ His distale permette il legame di ligandi bimolecolari (O 2, CO) solo con angoli di legame diversi da 180. Il legame tra il Fe ++ e il ligando con questo angolo è più labile di quello a 180. O O gs ver 0.1 L05 - Trasporto dell ossigeno 20 10
11 Ligandi al gruppo eme Lo spazio compreso tra il Fe ++ His distale permette il legame di ligandi bimolecolari (O 2, CO) solo con angoli di legame diversi da 180. Il legame tra il Fe ++ e il ligando con questo angolo è più labile di quello a 180. C O gs ver 0.1 L05 - Trasporto dell ossigeno 21 Interazione eme proteina Il gruppo eme stabilizza il ripiegamento della proteina. Il legame è del tipo interazione idrofobica. I gruppi propionato sono presenti nella superficie. Gruppi carbossilici del propionato gs ver 0.1 L05 - Trasporto dell ossigeno 22 11
12 Mioglobina La proteina circonda completamente il gruppo eme. Funzione della proteina: aumentare la solubilità del gruppo eme. Impedisce l ossidazione del gruppo eme (Fe 2+ Fe 3+ ) La metamioglobina (Fe 3+ ) è inattiva. Diminuisce il legame di CO. gs ver 0.1 L05 - Trasporto dell ossigeno 23 Ossidazione del Fe ++ Il legame del Fe ++ attraverso la proteina impedisce l ossidazione a Fe +++ a seguito del legame con l ossigeno: 2 eme-fe ++ + ½ 2O 2 + 2H + 2 eme-fe H 2 O O Fe++ 2 Fe ++ + ½ O 2 + 2H + 2 Fe H Fe ++ 2 O O gs ver 0.1 L05 - Trasporto dell ossigeno 24 12
13 Emoglobina, enzima honoris causa In tutti gli animali superiori il metabolismo è aerobico, Assunzione diretta di O 2 efficace solo in organismi unicellulari, Emoglobina (Hb): trasporta O 2 dai polmoni ai tessuti, Mioglobina (Mb): presente nei tessuti muscolari, funge da deposito di O 2, Se non ci fosse Hb, il cuore dovrebbe pompare sangue ad un flusso >100 maggiore. gs ver 0.1 L05 - Trasporto dell ossigeno 25 Premio obel per la Chimica nel 1962 gs ver 0.1 L05 - Trasporto dell ossigeno 26 13
14 Il colore del sangue Il colore della proteina è diverso a seconda del fatto che l ossigeno sia o no legato al Fe ++. gs ver 0.1 L05 - Trasporto dell ossigeno 27 Deossiglobine Il colore del sangue Ossiglobine Carbossiglobine Metaglobine gs ver 0.1 L05 - Trasporto dell ossigeno 28 14
15 Mioglobina e emoglobina gs ver 0.1 L05 - Trasporto dell ossigeno 29 Similarità strutturale Emoglobina e mioglobina Le quattro subunità della emoglobina sono strutturalmente simili alla mioglobina, Il legame con l ossigeno avviene sempre attraverso lo ione Fe ++ del gruppo eme gs ver 0.1 L05 - Trasporto dell ossigeno 30 15
16 Emoglobina dei mammiferi Proteina tetramerica Dimero di dimeri, (αβ) 2 Le catene α, β sono simili alla Mb. Ogni catena contiene un gruppo eme. Ogni gruppo eme lega un O 2. L interfaccia αβ è diversa dall interfaccia αα e ββ. Legami a ponte salino stabilizzano la struttura deossi. gs ver 0.1 L05 - Trasporto dell ossigeno 31 Il legame con l ossigeno ella mioglobina Mb + O 2 MbO 2 K D = [Mb] [O 2 ] [MbO 2 ] Si definisce la saturazione frazionale (γo 2 ) la frazione di siti che hanno ossigeno legato: γo 2 = [MbO 2 ] [Mb] + [O 2 ] γo 2 = [O 2 ] K D + [O 2 ] gs ver 0.1 L05 - Trasporto dell ossigeno 32 16
17 Il legame con l ossigeno ell emoglobina O 2 O 2 O 2 O 2 Hb Hb(O 2 ) Hb(O 2 ) 2 Hb(O 2 ) 3 Hb(O 2 ) 4 O 2 O 2 O 2 O 2 K D = [Hb] [O 2 ]n [Hb(O 2 ) n ] Si definisce la saturazione frazionale (γo 2 ) la frazione di siti che hanno ossigeno legato: γo 2 = n[hb(o 2 ) n ] n([hb] + [Hb(O 2 ) n ] γo 2 = [O 2 ] n K D + [O 2 ] n gs ver 0.1 L05 - Trasporto dell ossigeno 33 Saturazione e po 2 HbO 2 /(Hb+HbO 2 ), % o unità 100% P 0.5 = 3 mmhg Mioglobina Emoglobina P 0.5 = mmhg 50% 0% 0 P Pressione parziale di O 2 o tensione di O 2 o po 2 (mmhg, torr o kpa) gs ver 0.1 L05 - Trasporto dell ossigeno 34 17
18 Cooperatività γo 2 = [O 2 ] n K D + [O 2 ] n n = costante di Hill n = 1 nessuna cooperatività n > 1 cooperatività positiva Per l emoglobina n 2.5 gs ver 0.1 L05 - Trasporto dell ossigeno 35 Cooperatività Legame dell ossigeno a Hb: Il legame dell ossigeno alla Hb nello stato deossi avviene con una data affinità (K D ) Le molecole di ossigeno che si legano successivamente hanno un affinità maggiore per il sito di legame. Ciò viene definito come cooperatività positiva. Avviene solo in proteine multimeriche. Il coefficiente di Hill ha un valore vicino al numero delle subunità. Il vantaggio è che l affinità del legame è sensibile a piccole variazioni in concentrazioni del ligando. gs ver 0.1 L05 - Trasporto dell ossigeno 36 18
19 Immagazzinamento e trasporto La mioglobina è un ottimo sistema per immagazzinare O 2 : riesce a caricarsi di ossigeno anche a bassi valori di po 2 per tenerlo strettamente legato P 0.5 (γo 2 = 0.5) a po 2 = 2.8 torr. L emoglobina è un ottimo sistema per trasportare l O 2 : Si carica di O 2 quando po 2 è alta, cede O 2 quando po 2 è basso P 0.5 (γo 2 = 0.5) a po 2 = torr. gs ver 0.1 L05 - Trasporto dell ossigeno 37 HbO 2 /(Hb+HbO 2 ) Saturazione 100% O 2 ceduto a Mb O 2 ceduto da HbO 2 0% 0 Sangue venoso Sangue arterioso po 2 (mmhg) gs ver 0.1 L05 - Trasporto dell ossigeno 38 19
20 Modello Molecolare ello stato deossi il Fe ++ è fuori dal piano del gruppo eme. Il legame con O 2, sposta il Fe ++. Trascina la His prossimale e l elica Å His93 (prossimale) His64 (distale) H Fe++ H 0.33 Å Piano del gruppo eme H Fe++ O O His64 (distale) H His93 (prossimale) 0.22 Å Il movimento altera l interfaccia α/β. Stato deossi = stato T (Tense) T R Stato ossi = stato R (Relaxed) gs ver 0.1 L05 - Trasporto dell ossigeno 39 Modello Molecolare L alterazione dell interfaccia α/β provoca la variazione dell affinità nelle subunità adiacenti. Stato deossi = stato T (Tense) 0.55 Å His93 (prossimale) His64 (distale) H Fe++ H 0.33 Å Piano del gruppo eme H Fe++ O O His64 (distale) H His93 (prossimale) 0.22 Å Stato ossi = stato R (Relaxed) T R gs ver 0.1 L05 - Trasporto dell ossigeno 40 20
21 α 2 β 1 β 2 α 1 gs ver 0.1 L05 - Trasporto dell ossigeno 41 α 2 β 1 β 2 α 1 gs ver 0.1 L05 - Trasporto dell ossigeno 42 21
22 Deossiemoglobina gs ver 0.1 L05 - Trasporto dell ossigeno 43 Ossiemoglobina gs ver 0.1 L05 - Trasporto dell ossigeno 44 22
23 Emoglobina DEOSSI OSSI gs ver 0.1 L05 - Trasporto dell ossigeno 45 Transizione T R ella transizione fra lo stato T (deossigenata) e lo stato R (ossigenata) la coppia di subunità α 1 β 1 si comporta come un unica subunità. gs ver 0.1 L05 - Trasporto dell ossigeno 46 23
24 Transizione T R α 2 β 1 α 2 β 1 I maggiori riarrangiamenti avvengono all interfaccia tra i due dimeri α 2 /β 1 e α 1 /β 2. gs ver 0.1 L05 - Trasporto dell ossigeno 47 Transizione T R ella proteina deossigenata esiste un legame idrogeno tra Asp nell elica e His amino terminale. Il piccolo movimento causato dal legame con l ossigeno viene amplificato attraverso una ridistribuzione dei legami idrogeno all interfaccia α 2 /β 1 gs ver 0.1 L05 - Trasporto dell ossigeno 48 24
25 Transizione T R Il legame dell ossigeno sposta lo ione Fe ++ il quale si trascina l elica e si rompe il legame idrogeno tra Asp e His. gs ver 0.1 L05 - Trasporto dell ossigeno 49 Transizione T R α 2 stato T α 2 stato R β 1 stato R β 1 stato R Cambia quindi la distribuzione dei legami idrogeno all interfaccia α/β e cambia quindi lo stato della subunità adiacente che passa da T a R con aumento dell affinità per O 2. gs ver 0.1 L05 - Trasporto dell ossigeno 50 25
26 Regolazione ph Effetto Bohr Effetto Root CO 2 Formazione di bicarbonato, (anidrasi carbonica) Formazione di carbammati Cl - Scambio Cl - /HCO 3 - Formazione di ponti salini Composti fosforilati 2,3 bifosfoglicerato Inositoli fosfati ATP, GTP gs ver 0.1 L05 - Trasporto dell ossigeno 51 Effetto Bohr L affinità per l O 2 è sensibile al ph. ph acido; diminuzione dell affinità. Il ponte salino tra Glu94 e His146 si forma solo nello stato T. L eccesso di H + forma il ponte salino e favorisce lo stato deossi. His146 Glu94 1 γo ph = 7.5 ph = 7.2 ph = po 2 gs ver 0.1 L05 - Trasporto dell ossigeno 52 26
27 CO 2 ed effetto Bohr ei polmoni Bassa pco 2 la reazione avviene in senso opposto CO 2 e H + rilasciati da Hb Aumenta l affinità per O 2 CO 2 2CO 2 + H 2 O Anidrasi carbonica EC H 2 CO 3 2HCO H + SAGUE Hb 4O 2 el tessuto La CO 2 è legata alla Hb per formare un carbammato o convertita in bicarbonato dall enzima Anidrasi Carbonica (EC ). Sistema tampone del sangue La Hb lega 2 H + ogni 4 O 2 rilasciati (effetto Bohr). TESSUTO POLMOI 4O 2 Hb 2H + 4O 2 2HCO H + 2H 2 CO 3 Anidrasi carbonica EC Metabolismo 2CO 2 + H 2 O gs ver 0.1 L05 - Trasporto dell ossigeno 53 HbH + O 2 H + + Hb-H-COO - HbO 2 + H + HCO H + HbO 2 Hb-H 2 + O 2 Anidrasi carbonica EC H 2 O + CO 2 CO 2 CO 2 Krebs Ciclo di HbO 2 Hb + O 2 O 2 ADH ADP Hb + Cl - HbCl - H 2 O AD + K + ATP HCO 3 - Cl - Lento a + H 2 O + CO 2 gs ver 0.1 L05 - Trasporto dell ossigeno 54 27
28 Anidrasi carbonica gs ver 0.1 L05 - Trasporto dell ossigeno 55 Effetto Root ei mammiferi l aumento di acidità provoca l effetto Bohr con una diminuzione di affinità per O 2 attraverso un aumento della K m apparente, ei pesci l aumento di acidità provoca anche l effetto Root con una diminuzione della massima quantità di O 2 che si può legare (varia la V max apparente). L acidosi, metabolica (acido lattico) o respiratoria (CO 2 ) porta ad una riduzione dell affinità dell Hb per O 2, IMPORTATE PER IL RIEMPIMETO DELLA VESCICA ATATORIA. Root RW. The respiratory function of the blood of marine fishes. Biol Bull 61: , gs ver 0.1 L05 - Trasporto dell ossigeno 56 28
29 Effetto Borh ed effetto Root gs ver 0.1 L05 - Trasporto dell ossigeno 57 Emoglobine di pesci Al contrario dei mammiferi nei pesci c è una grande varietà di emoglobine e nel meccanismo di modulazione del legame con l ossigeno per adattarsi alle differenti condizioni ambientali Convenzionalmente le emoglobine dei pesci si dividono in due categorie eletroforetiche: Emoglobine catodiche con punto isoelettrico alto (pi 8) Emoglobine anodiche con punto isolettrico basso (pi 8) Con differenti proprietà di modulazione del legame con l O 2 gs ver 0.1 L05 - Trasporto dell ossigeno 58 29
30 Emoglobine di pesci L anguilla europea (Anguilla anguilla) viene considerata come specie modello con due distinte emoglobine: Una Hb catodica la cui affinità con l O 2 è debolmente influenzata dal ph (piccolo effetto Bohr) Una Hb anodica che ha una minore affinità per l O 2 e con un grande effetto Bohr e Root. Oltre a nuotare, striscia. gs ver 0.1 L05 - Trasporto dell ossigeno 59 Effetto Root e galleggiamento Il gas che riempie la vescica natatoria è principalmente O 2 La Hb dei pesci è estremamente sensibile all acidità, l ambiente acido a causa della produzione di acido lattico o CO 2 Il valore della costante di Hill, n γo 2 = [O 2 ] n K D + [O 2 ] n diminuisce fino a valori al disotto dell unità (cooperatività negativa) con rilascio (fino al 80%) dell ossigeno legato all Hb in prossimità della vescica natatoria. gs ver 0.1 L05 - Trasporto dell ossigeno 60 30
31 Vescica natatoria Le cellule producono acido lattico da glucoso L acidità generata dall acido lattico provoca l effetto Root gs ver 0.1 L05 - Trasporto dell ossigeno 61 H 2 O + CO 2 AnCarb H + + HCO 3 - H + + HbO 2 HHb + O 2 Cl - Sangue HCO 3 - Cl - H + H+ H + + HCO 3 - H 2 O + CO 2 AnCarb Endotelio ADP ATP Glucoso a + H + Lattato + H + Glicolisi G6P Piruvato CO 2 Cellule della ghiandola del gas Krebs PPO Lume della vescica natatoria O 2 Adattato da:the Generation of Hyperbaric Oxygen Tensions in Fish. Bernd Pelster. ews Physiol. Sci. (2001), 16, gs ver 0.1 L05 - Trasporto dell ossigeno 62 31
32 Altri pigmenti respiratori Clorocruine OSSI - DEOSSI Utilizzate fondamentalmente dagli anellidi. Proteine con gruppo eme, Formano dimeri e trimeri di trimeri Emocianine OSSI - DEOSSI Utilizzata da bivalvi, cefalopodi, gasteropodi, crostacei Proteine con due ioni Cu 2+ per subunità. Formano insiemi di trimeri (esameri, dodecameri, 24-meri) Emeritrine OSSI - DEOSSI Utilizzata fondamentalmente dagli anellidi. Proteine con due ioni Fe 2+ tenuti insieme da un atomo di ossigeno per subunità. gs ver 0.1 L05 - Trasporto dell ossigeno 63 Emocianina da Rapana thomasiana Monomero Struttura β-sandwich Structure of a Hemocyanin Functional Unit. M. Perbandt, E.W. Guthöhrlein, W. Rypniewski, K. Idakieva, S. Stoeva, W. Voelter,. Genov, C. Betzel. Biochemistry 2003, 42, gs ver 0.1 L05 - Trasporto dell ossigeno 64 32
33 Rapana thomasiana gs ver 0.1 L05 - Trasporto dell ossigeno 65 Emocianina da Rapana thomasiana Trimero gs ver 0.1 L05 - Trasporto dell ossigeno 66 33
34 Emocianina da Rapana thomasiana gs ver 0.1 L05 - Trasporto dell ossigeno 67 34
35 Emocianina da Rapana thomasiana Il meccanismo alla base della cooperatività del legame con l ossigeno è stato postulato sulla base del trasferimento del cambiamento conformazionale da un sito attivo alla subunità vicina. Le regioni coinvolte sono colorate in rosso. gs ver 0.1 L05 - Trasporto dell ossigeno 69 Panulirus Interruptus gs ver 0.1 L05 - Trasporto dell ossigeno 70 35
36 Emocianina da Panulirus Interruptus (monomero) gs ver 0.1 L05 - Trasporto dell ossigeno 71 Emocianina da Panulirus Interruptus (monomero) gs ver 0.1 L05 - Trasporto dell ossigeno 72 36
37 Themiste Dyscrita gs ver 0.1 L05 - Trasporto dell ossigeno 73 Emeritina di Themiste Dyscrita gs ver 0.1 L05 - Trasporto dell ossigeno 74 37
38 Emeritina di Themiste Dyscrita DEOSSI OSSI gs ver 0.1 L05 - Trasporto dell ossigeno 75 Phascolopsis Gouldii gs ver 0.1 L05 - Trasporto dell ossigeno 76 38
39 Emeritina da Phascolopsis Gouldii (deossigenata) gs ver 0.1 L05 - Trasporto dell ossigeno 77 Emeritina da Phascolopsis Gouldii (deossigenata) Le dimensioni del sito di legame con l ossigeno vengono definite da un residuo di Leucina. gs ver 0.1 L05 - Trasporto dell ossigeno 78 39
40 Adattamento a lungo termine gs ver 0.1 L05 - Trasporto dell ossigeno 79 Composti fosforilati Il 2,3 bifosfoglicerato (2,3-BPG) è un sottoprodotto della glicolisi. La sua presenza è un segnale di necessità di O 2. Si lega alla forma T nella regione cationica. Una volta legato favorisce la forma deossi, favorisce quindi il rilascio di O 2 al tessuto. gs ver 0.1 L05 - Trasporto dell ossigeno 80 40
41 Altra vista del 2,3-BPG ei mammiferi il 2,3- BPG funziona come una zeppa che favorisce lo stato T dell emoglobina. Forza il rilascio di O 2 nel tessuto. È largamente responsabile dell adattamento all altitudine. gs ver 0.1 L05 - Trasporto dell ossigeno 81 Altra vista del 2,3-BPG ei mammiferi il 2,3- BPG funziona come una zeppa che favorisce lo stato T dell emoglobina. Forza il rilascio di O 2 nel tessuto. È largamente responsabile dell adattamento all altitudine. gs ver 0.1 L05 - Trasporto dell ossigeno 82 41
42 Composti fosforilati Il 2,3 bifosfoglicerato (2,3-BPG) è un sottoprodotto della glicolisi. La sua presenza è un segnale di necessità di O 2. Si lega alla forma T nella regione cationica. Una volta legato favorisce la forma deossi, favorisce quindi il rilascio di O 2 al tessuto. gs ver 0.1 L05 - Trasporto dell ossigeno 83 Modulazione In altri organismi (Pesci teleostei, elasmobranchi, rettili ecc.) tale effetto viene provocato da altri composti fosforilati: Inositoli fosfati, ATP, GTP. gs ver 0.1 L05 - Trasporto dell ossigeno 84 42
43 Emoglobina? O grazie! gs ver 0.1 L05 - Trasporto dell ossigeno 85 Pesci antartici Temperatura corporea bassa ( 1.7 C) l acqua salata congela a 1.8 C Solubilità O 2 0.3% Basso metabolismo essun pigmento respiratorio Risparmio di sintesi proteica Bassa viscosità del sangue Facile da pompare Poca spesa energetica gs ver 0.1 L05 - Trasporto dell ossigeno 86 43
44 Tutorial Per visualizzare un tutorial su mioglobina ed emoglobina visitare il sito: Utilizzando la versione 4.7 di ETSCAPE completo di plugin CHIME. Entrambi sono scaricabili da: gs ver 0.1 L05 - Trasporto dell ossigeno 87 Referenze sul WEB Vie metaboliche KEGG: Degradazione degli xenobiotici: Struttura delle proteine: Protein data bank (Brookhaven): Hexpasy Expert Protein Analysis System: Prosite (protein families and domains): Enzyme (Enzyme nomenclature database): Scop (famiglie strutturali): Enzimi: omenclatura - IUBMB: Proprietà - Brenda: Expasy (Enzyme nomenclature database): Database di biocatalisi e biodegradazione: Citocromo P450: Metallotioneine: Tossicità degli xenobiotici: Agency for Toxic Substances and Disease Registry gs ver 0.1 L05 - Trasporto dell ossigeno 88 44
45 Crediti e autorizzazioni all utilizzo Questo ed altro materiale può essere reperito a partire da: Il materiale di questa presentazione è di libero uso per didattica e ricerca e può essere usato senza limitazione, purché venga riconosciuto l autore usando questa frase: Materiale ottenuto dal Prof. Giorgio Sartor Università di Bologna a Ravenna Giorgio Sartor - giorgio.sartor@unibo.it 45
Il trasporto dell ossigeno
 Prof. Giorgio Sartor Il trasporto dell ossigeno Copyright 2001-2016 by Giorgio Sartor. All rights reserved. Versione 1.9.2 mar 2016 Trasporto dell ossigeno egli organismi aerobi il trasporto dell ossigeno
Prof. Giorgio Sartor Il trasporto dell ossigeno Copyright 2001-2016 by Giorgio Sartor. All rights reserved. Versione 1.9.2 mar 2016 Trasporto dell ossigeno egli organismi aerobi il trasporto dell ossigeno
Il trasporto dell ossigeno
 Prof. Giorgio Sartor Il trasporto dell ossigeno Copyright 2001-2013 by Giorgio Sartor. All rights reserved. Versione 1.9 mar 2013 Trasporto dell ossigeno egli organismi aerobi il trasporto dell ossigeno
Prof. Giorgio Sartor Il trasporto dell ossigeno Copyright 2001-2013 by Giorgio Sartor. All rights reserved. Versione 1.9 mar 2013 Trasporto dell ossigeno egli organismi aerobi il trasporto dell ossigeno
Mioglobina ed emoglobina
 Mioglobina ed emoglobina α β Muscolo Deposito di O 2 Alta affinità per O 2 β α Globulo rosso Trasporto di O 2 Bassa affinità per O 2 Cooperativa ed allosterica Animali Mb-knockout (2003) : funzionalità
Mioglobina ed emoglobina α β Muscolo Deposito di O 2 Alta affinità per O 2 β α Globulo rosso Trasporto di O 2 Bassa affinità per O 2 Cooperativa ed allosterica Animali Mb-knockout (2003) : funzionalità
Modulo 4. Una proteina in azione
 Modulo 4 Una proteina in azione Mioglobina ed emoglobina: un esempio di funzionamento di una proteina La funzione della maggior parte della proteine globulari è mediata dall interazione reversibile con
Modulo 4 Una proteina in azione Mioglobina ed emoglobina: un esempio di funzionamento di una proteina La funzione della maggior parte della proteine globulari è mediata dall interazione reversibile con
IL GRUPPO EME. PROTOPORFIRINA IX: struttura organica ad anello costituita da 4 anelli pirrolici uniti da ponti metinici.
 IL GRUPPO EME PROTOPORFIRINA IX: struttura organica ad anello costituita da 4 anelli pirrolici uniti da ponti metinici. L inserimento di un atomo di ferro nello stato di ossidazione ferroso (Fe 2+ ) determina
IL GRUPPO EME PROTOPORFIRINA IX: struttura organica ad anello costituita da 4 anelli pirrolici uniti da ponti metinici. L inserimento di un atomo di ferro nello stato di ossidazione ferroso (Fe 2+ ) determina
FUNZIONI delle PROTEINE
 FUNZIONI delle PROTEINE Ha le dimensioni del reciproco di una concentrazione (M -1 ) Ha le dimensioni di una concentrazione (M) La frazione dei siti occupati rispetto ai siti totali è definita come θ FRAZIONE
FUNZIONI delle PROTEINE Ha le dimensioni del reciproco di una concentrazione (M -1 ) Ha le dimensioni di una concentrazione (M) La frazione dei siti occupati rispetto ai siti totali è definita come θ FRAZIONE
Coefficiente di Hill ( n o n H ) = quanto i siti di legame per l O 2 sono cooperativi tra di loro.
 Cos è n? po n 2 Y= n n p50 + po 2 Coefficiente di Hill ( n o n H ) = quanto i siti di legame per l O 2 sono cooperativi tra di loro. Per l Hb non è mai uguale al numero dei siti per l O 2, Le diverse emoproteine
Cos è n? po n 2 Y= n n p50 + po 2 Coefficiente di Hill ( n o n H ) = quanto i siti di legame per l O 2 sono cooperativi tra di loro. Per l Hb non è mai uguale al numero dei siti per l O 2, Le diverse emoproteine
EMOGLOBINA, MIOGLOBINA MIOGLOBINA ED EMOGLOBINA NEL TRASPORTO DELL OSSIGENO
 EMOGLOBINA, MIOGLOBINA MIOGLOBINA ED EMOGLOBINA NEL TRASPORTO DELL OSSIGENO Trasporto dell ossigeno In tutti gli animali superiori, il metabolismo è aerobico L energia che si può estrarre dal glucosio
EMOGLOBINA, MIOGLOBINA MIOGLOBINA ED EMOGLOBINA NEL TRASPORTO DELL OSSIGENO Trasporto dell ossigeno In tutti gli animali superiori, il metabolismo è aerobico L energia che si può estrarre dal glucosio
L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO
 L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 23 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata all emoglobina: L O 2 totale
L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 23 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata all emoglobina: L O 2 totale
Le proteine che legano ossigeno:
 Le proteine che legano ossigeno: . I cristalli si ottengono per precipitazione lenta della molecola da una soluzione, in condizioni che non dovrebbero alterare la sua struttura Un cristallo proteico È
Le proteine che legano ossigeno: . I cristalli si ottengono per precipitazione lenta della molecola da una soluzione, in condizioni che non dovrebbero alterare la sua struttura Un cristallo proteico È
Il metalloma Struttura e reattività di metalloproteine. Il trasporto dell O 2
 Il metalloma Struttura e reattività di metalloproteine Il trasporto dell O 2 Il trasporto dell ossigeno Nel sangue la solubilità dell O 2 è molto maggiore che in H 2 O In H 2 O la solubilità è 6.59 cm
Il metalloma Struttura e reattività di metalloproteine Il trasporto dell O 2 Il trasporto dell ossigeno Nel sangue la solubilità dell O 2 è molto maggiore che in H 2 O In H 2 O la solubilità è 6.59 cm
EMOGLOBINA (Hb) nei globuli rossi e
 Nel metabolismo aerobio l O 2 è l accettore finale nel mitocondrio degli elettroni liberati dai composti carboniosi Proteine leganti l O 2 sono EMOGLOBINA (Hb) nei globuli rossi e MIOGLOBINA nelle fibre
Nel metabolismo aerobio l O 2 è l accettore finale nel mitocondrio degli elettroni liberati dai composti carboniosi Proteine leganti l O 2 sono EMOGLOBINA (Hb) nei globuli rossi e MIOGLOBINA nelle fibre
Emoglobina e mioglobina
 Emoglobina e mioglobina Per molti organismi, l O 2 è una molecola di importanza vitale: l'ossigeno è infatti l'accettore finale degli elettroni, che "fluendo" attraverso i complessi della catena respiratoria,
Emoglobina e mioglobina Per molti organismi, l O 2 è una molecola di importanza vitale: l'ossigeno è infatti l'accettore finale degli elettroni, che "fluendo" attraverso i complessi della catena respiratoria,
STRUTTURA E FUNZIONE
 STRUTTURA E FUNZIONE O 2 non solubile in acqua Esistono due proteine che permettono il trasporto di O 2 nel corpo emoglobina (Hb) si trova nei globuli rossi Trasporta anche CO 2 and H + Mioglobina (Mb)
STRUTTURA E FUNZIONE O 2 non solubile in acqua Esistono due proteine che permettono il trasporto di O 2 nel corpo emoglobina (Hb) si trova nei globuli rossi Trasporta anche CO 2 and H + Mioglobina (Mb)
La struttura di una proteina e ruolo biologico da essa svolto sono strettamente connessi. Alcune funzioni biologiche delle proteine:
 La struttura di una proteina e ruolo biologico da essa svolto sono strettamente connessi. Alcune funzioni biologiche delle proteine: Catalizzatori = Enzimi Accumulo e trasporto di ossigeno = mioglobina
La struttura di una proteina e ruolo biologico da essa svolto sono strettamente connessi. Alcune funzioni biologiche delle proteine: Catalizzatori = Enzimi Accumulo e trasporto di ossigeno = mioglobina
Nel corso dell evoluzione, con il passaggio dalla. progressivamente differenziati due meccanismi. un sistema circolatorio adeguato;
 PROTEINE RESPIRATORIE EMOGLOBINA & MIOGLOBINA Nel corso dell evoluzione, con il passaggio dalla vita anaerobia alla vita aerobia si sono progressivamente differenziati due meccanismi che sono in grado
PROTEINE RESPIRATORIE EMOGLOBINA & MIOGLOBINA Nel corso dell evoluzione, con il passaggio dalla vita anaerobia alla vita aerobia si sono progressivamente differenziati due meccanismi che sono in grado
Le proteine che legano l ossigenol
 Le proteine che legano l ossigenol Protoporfirina IX EME (Fe-protoporfirina IX) L atomo di ferro del gruppo eme può formare sei legami Struttura della mioglobina di capodoglio (J. Kendrew, anni 50)
Le proteine che legano l ossigenol Protoporfirina IX EME (Fe-protoporfirina IX) L atomo di ferro del gruppo eme può formare sei legami Struttura della mioglobina di capodoglio (J. Kendrew, anni 50)
Regolano il metabolismo, sia come enzimi, sia come ormoni (insulina, glucagone, ecc.)
 Grazie alla elevata dinamicità delle strutture proteiche (gli atomi sono in continuo movimento fluttuante) e per la capacità che hanno di legarsi in modo selettivo ad altre molecole, le proteine svolgono
Grazie alla elevata dinamicità delle strutture proteiche (gli atomi sono in continuo movimento fluttuante) e per la capacità che hanno di legarsi in modo selettivo ad altre molecole, le proteine svolgono
Esempi di proteine: Mioglobina ed Emoglobina
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Esempi di proteine: Mioglobina ed Emoglobina Mioglobina: caratteristiche generali, funzione
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Esempi di proteine: Mioglobina ed Emoglobina Mioglobina: caratteristiche generali, funzione
Trasporto di O 2 nel sangue
 Trasporto di O 2 nel sangue Il 97% dell O 2 trasportato nel plasma è chimicamente legato all Hb nei globuli rossi, solo il 3% è fisicamente disciolto Trasporto O 2 nel plasma Trasporto O 2 legato ad Hb
Trasporto di O 2 nel sangue Il 97% dell O 2 trasportato nel plasma è chimicamente legato all Hb nei globuli rossi, solo il 3% è fisicamente disciolto Trasporto O 2 nel plasma Trasporto O 2 legato ad Hb
Esempi di proteine: Mioglobina ed Emoglobina
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica Organica e Biochimica Esempi di proteine: Mioglobina ed Emoglobina Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica Organica e Biochimica Esempi di proteine: Mioglobina ed Emoglobina Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base
Formula generale di un amminoacido
 Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
Mioglobina Emoglobina
 Mioglobina Emoglobina Eventi successivi i alla comparsa dell O 2 Possibilità di ottenere circa 20 volte più energia dalla combustione del glucosio Sviluppo di un sistema circolatorio per la distribuzione
Mioglobina Emoglobina Eventi successivi i alla comparsa dell O 2 Possibilità di ottenere circa 20 volte più energia dalla combustione del glucosio Sviluppo di un sistema circolatorio per la distribuzione
Metabolismo degli xenobiotici
 Prof. Giorgio Sartor degli xenobiotici Copyright 00100 by Giorgio Sartor. All rights reserved. Versione 3. oct 00 degli xenobiotici Scopo Convertire sostanze lipofile in idrofile Facilitare l escrezione
Prof. Giorgio Sartor degli xenobiotici Copyright 00100 by Giorgio Sartor. All rights reserved. Versione 3. oct 00 degli xenobiotici Scopo Convertire sostanze lipofile in idrofile Facilitare l escrezione
Emoglobina e mioglobina
 Emoglobina e mioglobina Per poter parlare in modo comprensibile dell emoglobina (Hb), è utile occuparsi prima della mioglobina (Mb) che è molto simile all emoglobina ma è molto più semplice. Tra emoglobina
Emoglobina e mioglobina Per poter parlare in modo comprensibile dell emoglobina (Hb), è utile occuparsi prima della mioglobina (Mb) che è molto simile all emoglobina ma è molto più semplice. Tra emoglobina
Ogni globina ha una tasca in cui lega un gruppo EME, quindi l Hb può legare e trasportare 4 molecole di O 2
 Emoglobina (Hb): tetramero (le globine si associano formando due copie di dimeri αβ (α 1 β 1 e α 2 β 2 ) che si associano a formare un tetramero attraverso interazioni idrofobiche, legami H e ponti salini
Emoglobina (Hb): tetramero (le globine si associano formando due copie di dimeri αβ (α 1 β 1 e α 2 β 2 ) che si associano a formare un tetramero attraverso interazioni idrofobiche, legami H e ponti salini
FUNZIONE DELLE PROTEINE RAPPORTO STRUTTURA-FUNZIONE
 FUNZIONE DELLE PROTEINE RAPPORTO STRUTTURA-FUNZIONE Principi basilari: 1.Le funzioni di molte proteine richiedono il legame reversibile con altre molecole (LIGANDO) Un ligando può essere di natura diversa,
FUNZIONE DELLE PROTEINE RAPPORTO STRUTTURA-FUNZIONE Principi basilari: 1.Le funzioni di molte proteine richiedono il legame reversibile con altre molecole (LIGANDO) Un ligando può essere di natura diversa,
Fisiologia della Respirazione
 Fisiologia della Respirazione 8.Trasporto dei gas nel sangue FGE aa.2016-17 Obiettivi Necessità di un sistema di trasporto chimico ad alta capacità dell O 2 nel sangue: l emoglobina Curva di dissociazione
Fisiologia della Respirazione 8.Trasporto dei gas nel sangue FGE aa.2016-17 Obiettivi Necessità di un sistema di trasporto chimico ad alta capacità dell O 2 nel sangue: l emoglobina Curva di dissociazione
Fisiologia della Respirazione 8.Trasporto dei gas nel sangue. Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona
 Fisiologia della Respirazione 8.Trasporto dei gas nel sangue Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona Obiettivi Necessità di un sistema di trasporto chimico ad alta capacità
Fisiologia della Respirazione 8.Trasporto dei gas nel sangue Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona Obiettivi Necessità di un sistema di trasporto chimico ad alta capacità
Dopo la ventilazione alveolare, il passaggio successivo del processo respiratorio consiste nella diffusione dell O2 dagli alveoli al sangue e della
 Dopo la ventilazione alveolare, il passaggio successivo del processo respiratorio consiste nella diffusione dell O2 dagli alveoli al sangue e della CO2 in direzione opposta. R = quoziente respiratorio,
Dopo la ventilazione alveolare, il passaggio successivo del processo respiratorio consiste nella diffusione dell O2 dagli alveoli al sangue e della CO2 in direzione opposta. R = quoziente respiratorio,
Emoglobina e mioglobina
 Emoglobina e mioglobina L emoglobina e la mioglobina proteine centrali per l evoluzione La transizione dalla vita anaerobica a quella aerobica rappresenta un passo fondamentale dell'evoluzione perchè ha
Emoglobina e mioglobina L emoglobina e la mioglobina proteine centrali per l evoluzione La transizione dalla vita anaerobica a quella aerobica rappresenta un passo fondamentale dell'evoluzione perchè ha
ACQUISIZIONE SPERIMENTALE DELLA CONOSCENZA NELLE SCIENZE DELLA NATURA.
 CLM C IN MEDICINA E CHIRURGIA C.I. Metodologia medico-scientifica di base II (Scienze umane 2 Epistemologia) A.A. 2013-2014 I anno, 2 semestre ACQUISIZIONE SPERIMENTALE DELLA CONOSCENZA NELLE SCIENZE DELLA
CLM C IN MEDICINA E CHIRURGIA C.I. Metodologia medico-scientifica di base II (Scienze umane 2 Epistemologia) A.A. 2013-2014 I anno, 2 semestre ACQUISIZIONE SPERIMENTALE DELLA CONOSCENZA NELLE SCIENZE DELLA
Prof. Maria Nicola GADALETA
 Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Prof. Giorgio Sartor. Invertebrati marini. I nutrienti. Fonti di carbonio ed energia. Fonte di carbonio. Fonte di energia. Composti organici.
 Prof. Giorgio Sartor Invertebrati marini I nutrienti Copyright 2001-2008 by Giorgio Sartor. All rights reserved. Versione 1.1 nov 2008 Fonti di carbonio ed energia Organismo Fonte di carbonio Fonte di
Prof. Giorgio Sartor Invertebrati marini I nutrienti Copyright 2001-2008 by Giorgio Sartor. All rights reserved. Versione 1.1 nov 2008 Fonti di carbonio ed energia Organismo Fonte di carbonio Fonte di
Foto funzioni apparato respiratorio
 RESPIRAZIONE ESTERNA Foto funzioni apparato respiratorio RESPIRAZIONE INTERNA GLI SCAMBI GASSOSI QUOZIENTE RESPIRATORIO = CO 2 PRODOTTA O 2 CONSUMATO A riposo: Epitelio alveolare 200 ml/min 250 ml/min
RESPIRAZIONE ESTERNA Foto funzioni apparato respiratorio RESPIRAZIONE INTERNA GLI SCAMBI GASSOSI QUOZIENTE RESPIRATORIO = CO 2 PRODOTTA O 2 CONSUMATO A riposo: Epitelio alveolare 200 ml/min 250 ml/min
Plasma ph Tamponi: LEC: HCO 3 LIC: Proteine, Emoglobina, Fosfati Urina: Fosfati e ammoniaca
 Equilibrio acidobase Dieta: Acidi grassi Aminoacidi Assunzione H + CO 2, acido lattico, chetoacidi Plasma ph 7.357.42 Tamponi: LEC: HCO 3 LIC: Proteine, Emoglobina, Fosfati Urina: Fosfati e ammoniaca Ventilazione:
Equilibrio acidobase Dieta: Acidi grassi Aminoacidi Assunzione H + CO 2, acido lattico, chetoacidi Plasma ph 7.357.42 Tamponi: LEC: HCO 3 LIC: Proteine, Emoglobina, Fosfati Urina: Fosfati e ammoniaca Ventilazione:
Trasporto dei gas. Pressioni Volumi
 Trasporto dei gas Pressioni Volumi Il 97% dell O 2 trasportato nel plasma si trova chimicamente legato all Hb nei globuli rossi, solo lo 3% è fisicamente disciolto Trasporto O 2 nel plasma Trasporto O
Trasporto dei gas Pressioni Volumi Il 97% dell O 2 trasportato nel plasma si trova chimicamente legato all Hb nei globuli rossi, solo lo 3% è fisicamente disciolto Trasporto O 2 nel plasma Trasporto O
Trasporto dei gas respiratori nel sangue
 Trasporto dei gas respiratori nel sangue La soluzione dei gas nei liquidi C Legge di Henry acq P gas S gas C acq = quantità di gas disciolta nella fase acquosa P gas = pressione parziale del gas nella
Trasporto dei gas respiratori nel sangue La soluzione dei gas nei liquidi C Legge di Henry acq P gas S gas C acq = quantità di gas disciolta nella fase acquosa P gas = pressione parziale del gas nella
degli eritrociti è una proteina di trasporto indispensabile per veicolare l ossigeno l l anidride carbonica tra i polmoni e i tessuti
 l emoglobina degli eritrociti è una proteina di trasporto indispensabile per veicolare l ossigeno l e l anidride carbonica tra i polmoni e i tessuti Mioglobina, proteina di deposito,, presente nelle fibrocellule
l emoglobina degli eritrociti è una proteina di trasporto indispensabile per veicolare l ossigeno l e l anidride carbonica tra i polmoni e i tessuti Mioglobina, proteina di deposito,, presente nelle fibrocellule
Trasporto O 2 nel sangue
 Trasporto O 2 nel sangue 97% legato all Hb nei globuli rossi 3% fisicamente disciolto (determina il valore di po 2 ) Trasporto O 2 nel plasma Trasporto O 2 legato ad Hb Saturazione Hb 97% 0.3 ml/100ml
Trasporto O 2 nel sangue 97% legato all Hb nei globuli rossi 3% fisicamente disciolto (determina il valore di po 2 ) Trasporto O 2 nel plasma Trasporto O 2 legato ad Hb Saturazione Hb 97% 0.3 ml/100ml
MOVIMENTO. Motori molecolari. IV Movimento Miosina e actina. Prof. Giorgio Sartor. P04 - Versione 2.0 oct 2013
 Prof. Giorgio Sartor Motori molecolari IV Movimento Miosina e actina Copyright 2001-2013 by Giorgio Sartor. All rights reserved. P04 - Versione 2.0 oct 2013 MOVIMENTO Miosina Actina P04 v. 2.0 gsartor
Prof. Giorgio Sartor Motori molecolari IV Movimento Miosina e actina Copyright 2001-2013 by Giorgio Sartor. All rights reserved. P04 - Versione 2.0 oct 2013 MOVIMENTO Miosina Actina P04 v. 2.0 gsartor
Le proteine III. Corso di Biochimica 1. Prof. Giuseppina Pitari
 Le proteine III Corso di Biochimica 1 Prof. Giuseppina Pitari Ossi-mioglobina legame idrogeno lato distale La mioglobina L eme quindi consiste di una struttura organica alla quale è legato un atomo di
Le proteine III Corso di Biochimica 1 Prof. Giuseppina Pitari Ossi-mioglobina legame idrogeno lato distale La mioglobina L eme quindi consiste di una struttura organica alla quale è legato un atomo di
Come le cellule traggono energia dal cibo: produzione di ATP
 Come le cellule traggono energia dal cibo: produzione di ATP L energia è contenuta nei legami chimici delle molecole nutritive; la cellula estrae questa energia e la conserva nell ATP: respirazione cellulare
Come le cellule traggono energia dal cibo: produzione di ATP L energia è contenuta nei legami chimici delle molecole nutritive; la cellula estrae questa energia e la conserva nell ATP: respirazione cellulare
Gli Enzimi. catalizzatori biologici rendono possibile da un punto di vista cinetico le reazioni chimiche
 catalizzatori biologici rendono possibile da un punto di vista cinetico le reazioni chimiche Gli Enzimi Sono le proteine più importanti e più specializzate Presentano un elevato grado di specificità per
catalizzatori biologici rendono possibile da un punto di vista cinetico le reazioni chimiche Gli Enzimi Sono le proteine più importanti e più specializzate Presentano un elevato grado di specificità per
METABOLISMO CELLULARE
 METABOLISMO CELLULARE Struttura dell ATP (Adenosintrifosfato) Adenina (base azotata), Ribosio (zucchero) e un gruppo fosforico ATP Il legame covalente tra i gruppi fosforici si spezza facilmente liberando
METABOLISMO CELLULARE Struttura dell ATP (Adenosintrifosfato) Adenina (base azotata), Ribosio (zucchero) e un gruppo fosforico ATP Il legame covalente tra i gruppi fosforici si spezza facilmente liberando
COMPOSIZIONE DELL ARIA ATMOSFERICA SECCA E PRESSIONI PARZIALI DEI GAS - (760 TORR, 15 C)
 COMPOSIZIONE DELL ARIA ATMOSFERICA SECCA E PRESSIONI PARZIALI DEI GAS - (760 TORR, 15 C) COMPOSIZIONE ARIA NELL ATMOSFERA = COSTANTE A PARTE LE VARIAZIONI DELLA QUANTITA DI VAPORE ACQUEO A 0 C 1 torr =
COMPOSIZIONE DELL ARIA ATMOSFERICA SECCA E PRESSIONI PARZIALI DEI GAS - (760 TORR, 15 C) COMPOSIZIONE ARIA NELL ATMOSFERA = COSTANTE A PARTE LE VARIAZIONI DELLA QUANTITA DI VAPORE ACQUEO A 0 C 1 torr =
CLASSIFICAZIONE O.T.I.L.Is. Lig
 GLI ENZIMI CHE COSA SONO? Sono delle proteine altamente specializzate con attività catalitica, accelerano le reazioni chimiche rimanendo inalterati al termine della reazione stessa. CLASSIFICAZIONE O.T.I.L.Is.
GLI ENZIMI CHE COSA SONO? Sono delle proteine altamente specializzate con attività catalitica, accelerano le reazioni chimiche rimanendo inalterati al termine della reazione stessa. CLASSIFICAZIONE O.T.I.L.Is.
Tamponi biologici per il controllo del ph
 Tamponi biologici per il controllo del ph 1 Si definisce una soluzione tampone una soluzione che si oppone alla variazione del ph per aggiunte moderate di acidi o basi Si tratta generalmente di soluzioni
Tamponi biologici per il controllo del ph 1 Si definisce una soluzione tampone una soluzione che si oppone alla variazione del ph per aggiunte moderate di acidi o basi Si tratta generalmente di soluzioni
BIOMOLECOLE (PROTEINE)
 BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
DISTRIBUZIONE DELLA PERFUSIONE POLMONARE DISTRIBUZIONE DELLA VENTILAZIONE POLMONARE DEFINIRE LA COMPLIANCE POLMONARE
 VOLUMI POLMONARI DISTRIBUZIONE DELLA PERFUSIONE POLMONARE DISTRIBUZIONE DELLA VENTILAZIONE POLMONARE DEFINIRE LA COMPLIANCE POLMONARE DEFINIRE LE RESISTENZE POLMONARI DEFINIRE IL LAVORO POLMONARE Equazione
VOLUMI POLMONARI DISTRIBUZIONE DELLA PERFUSIONE POLMONARE DISTRIBUZIONE DELLA VENTILAZIONE POLMONARE DEFINIRE LA COMPLIANCE POLMONARE DEFINIRE LE RESISTENZE POLMONARI DEFINIRE IL LAVORO POLMONARE Equazione
- utilizzano esclusivamente le reattività chimiche di alcuni residui AA
 Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Prof. Giorgio Sartor. Il metabolismo. Metabolismo. È il processo che permette di ricavare energia da legami chimici (sottoforma di
 Prof. Giorgio Sartor Il metabolismo Copyright 2001-2008 by Giorgio Sartor. All rights reserved. Versione 1.4 oct 2008 Metabolismo È il processo che permette di ricavare energia da legami chimici (sottoforma
Prof. Giorgio Sartor Il metabolismo Copyright 2001-2008 by Giorgio Sartor. All rights reserved. Versione 1.4 oct 2008 Metabolismo È il processo che permette di ricavare energia da legami chimici (sottoforma
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 10
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 10 Funzioni delle proteine Concetti chiave: La varietà strutturale delle proteine consente loro di svolgere un enorme quantità
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 10 Funzioni delle proteine Concetti chiave: La varietà strutturale delle proteine consente loro di svolgere un enorme quantità
Rapporto Struttura/Funzione delle Proteine
 Macromolecole Biologiche Chimica Biologica A.A. 2010-2011 Rapporto Struttura/Funzione delle Proteine Struttura/Funzione delle Proteine Interazioni proteina-ligando come base della funzione di molte proteine
Macromolecole Biologiche Chimica Biologica A.A. 2010-2011 Rapporto Struttura/Funzione delle Proteine Struttura/Funzione delle Proteine Interazioni proteina-ligando come base della funzione di molte proteine
CHIMICA BIOLOGICA. Seconda Università degli Studi di Napoli. Prof. Augusto Parente. Lezione 7. DiSTABiF. Corso di Laurea in SCIENZE BIOLOGICHE
 Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in SCIENZE BIOLOGICHE Insegnamento di CHIMICA BIOLOGICA Prof. Augusto Parente Anno Accademico 2014-15 Lezione 7 Mioglobina Emoglobina po
Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in SCIENZE BIOLOGICHE Insegnamento di CHIMICA BIOLOGICA Prof. Augusto Parente Anno Accademico 2014-15 Lezione 7 Mioglobina Emoglobina po
Regolazione allosterica
 Macromolecole Biologiche Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Regolazione allosterica Marco Nardini Dipartimento
Macromolecole Biologiche Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Regolazione allosterica Marco Nardini Dipartimento
Connessioni. Le cellule cardiache sono unite tra loro da parti più ispessite del sarcolemma dette: Gap - junction
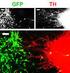 Muscolo cardiaco Le fibrocellule cardiache sono simili alle fibrocellule muscolari di tipo I (fibre rosse), ma si differenziano, infatti: Sono più piccole Non sono polinucleate Minor massa fibrillare (50%
Muscolo cardiaco Le fibrocellule cardiache sono simili alle fibrocellule muscolari di tipo I (fibre rosse), ma si differenziano, infatti: Sono più piccole Non sono polinucleate Minor massa fibrillare (50%
- CINETICA ENZIMATICA
 - CINETICA ENZIMATICA ENZIMI: - CATALIZZATORI aumenta la V di una reazione chimica senza subire trasformazioni durante l intero processo - PROTEINE gli enzimi sono proteine di struttura 3 o talora 4 -
- CINETICA ENZIMATICA ENZIMI: - CATALIZZATORI aumenta la V di una reazione chimica senza subire trasformazioni durante l intero processo - PROTEINE gli enzimi sono proteine di struttura 3 o talora 4 -
1. Controllo dell equilibrio acido-base. Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona
 1. Controllo dell equilibrio acido-base Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona Misura dell acidità di una soluzione Definizione di acido: qualsiasi sostanza chimica che
1. Controllo dell equilibrio acido-base Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona Misura dell acidità di una soluzione Definizione di acido: qualsiasi sostanza chimica che
Scambi gassosi e regolazione del respiro
 Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I Scambi gassosi e regolazione del respiro Ruolo del Sistema Respiratorio: - fornire O 2 - rimuovere CO 2 Scaricato da www.sunhope.it
Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I Scambi gassosi e regolazione del respiro Ruolo del Sistema Respiratorio: - fornire O 2 - rimuovere CO 2 Scaricato da www.sunhope.it
L EQUILIBRIO ACIDO-BASE NEL SANGUE
 L EQUILIBRIO ACIDO-BASE NEL SANGUE ph fisiologico: 7.35-7.45 ph < 7.35 acidosi ph > 7.45 alcalosi Lezione 24 1 L equazione di Henderson-Hasselbalch HA H + + A - La costante di equilibrio (K) (o costante
L EQUILIBRIO ACIDO-BASE NEL SANGUE ph fisiologico: 7.35-7.45 ph < 7.35 acidosi ph > 7.45 alcalosi Lezione 24 1 L equazione di Henderson-Hasselbalch HA H + + A - La costante di equilibrio (K) (o costante
Prof. Maria Nicola GADALETA
 Prof. Maria Nicola GADALETA Email: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA Email: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
PORTA AGLI ORGANI E AI TESSUTI: RIMUOVE: OMEOTERMI INTERVIENE NELLA TERMOREGOLAZIONE FUNZIONI DELLA CIRCOLAZIONE SANGUIGNA IL GLOBULO ROSSO
 FUNZIONI DELLA CIRCOLAZIONE SANGUIGNA IL GLOBULO ROSSO PORTA AGLI ORGANI E AI TESSUTI: a. L OSSIGENO (O 2 ), b. LE SOSTANZE NUTRITIZIE ASSORBITE, c. I SECRETI DELLE GHIANDOLE ENDOCRINE. RIMUOVE: a. L ANIDRIDE
FUNZIONI DELLA CIRCOLAZIONE SANGUIGNA IL GLOBULO ROSSO PORTA AGLI ORGANI E AI TESSUTI: a. L OSSIGENO (O 2 ), b. LE SOSTANZE NUTRITIZIE ASSORBITE, c. I SECRETI DELLE GHIANDOLE ENDOCRINE. RIMUOVE: a. L ANIDRIDE
LE REAZIONI DI FISSAZIONE DEL CARBONIO
 LE REAZIONI DI FISSAZIONE DEL CARBONIO Reazioni al buio ogni anno 200 miliardi di tonnellate di CO 2 vengono convertite in biomassa 40% fitoplancton CICLO DI CALVIN ciclo riduttivo dei pentosi fosfati,
LE REAZIONI DI FISSAZIONE DEL CARBONIO Reazioni al buio ogni anno 200 miliardi di tonnellate di CO 2 vengono convertite in biomassa 40% fitoplancton CICLO DI CALVIN ciclo riduttivo dei pentosi fosfati,
PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA
 PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA Svolgono la loro funzione legando reversibilmente l OSSIGENO. Aumentano la solubilità dell ossigeno nel plasma, da 3ml/L a 220 ml/l. La mioglobina
PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA Svolgono la loro funzione legando reversibilmente l OSSIGENO. Aumentano la solubilità dell ossigeno nel plasma, da 3ml/L a 220 ml/l. La mioglobina
Respirazione cellulare
 Respirazione cellulare L equazione generale della respirazione C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O + 36 ATP 1 molec zucchero 6 molec ossigeno 6 molec anidride carbonica 6 molec acqua + = + + 36 molecole
Respirazione cellulare L equazione generale della respirazione C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O + 36 ATP 1 molec zucchero 6 molec ossigeno 6 molec anidride carbonica 6 molec acqua + = + + 36 molecole
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
UNIVERSITÀ DEGLI STUDI DI TERAMO CORSO DI LAUREA IN BIOTECNOLOGIE CORSO MONODISCIPLINARE: BIOCHIMICA (6CFU)
 UNIVERSITÀ DEGLI STUDI DI TERAMO CORSO DI LAUREA IN BIOTECNOLOGIE CORSO MONODISCIPLINARE: BIOCHIMICA (6CFU) Roberto Giacominelli Stuffler IL C.M. BIOCHIMICA È SUDDIVISO IN DUE UNITÀ DIDATTICHE: A) BIOCHIMICA
UNIVERSITÀ DEGLI STUDI DI TERAMO CORSO DI LAUREA IN BIOTECNOLOGIE CORSO MONODISCIPLINARE: BIOCHIMICA (6CFU) Roberto Giacominelli Stuffler IL C.M. BIOCHIMICA È SUDDIVISO IN DUE UNITÀ DIDATTICHE: A) BIOCHIMICA
Specie radicaliche e stress ossidativo
 Prof. Giorgio Sartor Specie radicaliche e stress ossidativo Copyright 2001-2008 by Giorgio Sartor. All rights reserved. Versione 4.1 apr 2008 adicali Specie chimiche con elettroni spaiati occupano da soli
Prof. Giorgio Sartor Specie radicaliche e stress ossidativo Copyright 2001-2008 by Giorgio Sartor. All rights reserved. Versione 4.1 apr 2008 adicali Specie chimiche con elettroni spaiati occupano da soli
Prof. Maria Nicola GADALETA FOSFORILAZIONE OSSIDATIVA 4
 Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche FOSFORILAZIONE
Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche FOSFORILAZIONE
IL METABOLISMO ENERGETICO
 IL METABOLISMO ENERGETICO IL METABOLISMO L insieme delle reazioni chimiche che riforniscono la cellula e l organismo di energia e materia SI DIVIDE IN: CATABOLISMO produce ENERGIA METABOLISMO ENERGETICO
IL METABOLISMO ENERGETICO IL METABOLISMO L insieme delle reazioni chimiche che riforniscono la cellula e l organismo di energia e materia SI DIVIDE IN: CATABOLISMO produce ENERGIA METABOLISMO ENERGETICO
Regolazione enzimatica Isoenzimi
 Regolazione enzimatica Isoenzimi Gli enzimi regolatori nel metabolismo gruppi di enzimi lavorano insieme per produrre una via metabolica in cui il prodotto del primo enzima diventa il substrato del secondo
Regolazione enzimatica Isoenzimi Gli enzimi regolatori nel metabolismo gruppi di enzimi lavorano insieme per produrre una via metabolica in cui il prodotto del primo enzima diventa il substrato del secondo
Trasporto O 2 nel sangue
 Trasporto O 2 nel sangue 97% legato all Hb nei globuli rossi 3% fisicamente disciolto, determina il valore di po 2 Trasporto O 2 nel plasma Trasporto O 2 legato ad Hb SaturazioneHb 97% 0.3 ml/100ml 19.4
Trasporto O 2 nel sangue 97% legato all Hb nei globuli rossi 3% fisicamente disciolto, determina il valore di po 2 Trasporto O 2 nel plasma Trasporto O 2 legato ad Hb SaturazioneHb 97% 0.3 ml/100ml 19.4
Ruolo chiave nella Protein Science Cristallizzata nel 1840 Handbook of Hb crystals 1909 (Reichert & Brown)
 Mb & Hb EMOGLOBINA Ruolo chiave nella Protein Science Cristallizzata nel 1840 Handbook of Hb crystals 1909 (Reichert & Brown) 1 proteina caratterizzata t in ultracentrifuga t 1 proteina a funzione fisiologica
Mb & Hb EMOGLOBINA Ruolo chiave nella Protein Science Cristallizzata nel 1840 Handbook of Hb crystals 1909 (Reichert & Brown) 1 proteina caratterizzata t in ultracentrifuga t 1 proteina a funzione fisiologica
LE PROTEINE. SONO Polimeri formati dall unione di AMMINOACIDI (AA) Rende diversi i 20 AA l uno dall altro UN ATOMO DI C AL CENTRO
 LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
Struttura delle proteine
 Struttura delle proteine I II III Copyright 2001-2015 by Giorgio Sartor. All rights reserved. Versione 1.0.2 oct 2015 Struttura quaternaria Èil livello di organizzazione per il quale si formano strutture
Struttura delle proteine I II III Copyright 2001-2015 by Giorgio Sartor. All rights reserved. Versione 1.0.2 oct 2015 Struttura quaternaria Èil livello di organizzazione per il quale si formano strutture
Introduzione all Adattamento
 Seminari di rientamento in Biologia Introduzione all Adattamento Giovanni Cercignani Che cosa intendiamo per adattamento? Questo è forse il paradigma più vasto e generale della biologia, un edificio concettuale
Seminari di rientamento in Biologia Introduzione all Adattamento Giovanni Cercignani Che cosa intendiamo per adattamento? Questo è forse il paradigma più vasto e generale della biologia, un edificio concettuale
Le reazioni esoergoniche e quelle endoergoniche del metabolismo cellulare sono legate dalla molecola di ATP.
 1 METABOLISMO CELLULARE Definizione Metabolismo cellulare insieme delle reazioni che producono e necessitano energia nel nostro corpo. Nel metabolismo si distinguono due fasi: Fase catabolica Insieme delle
1 METABOLISMO CELLULARE Definizione Metabolismo cellulare insieme delle reazioni che producono e necessitano energia nel nostro corpo. Nel metabolismo si distinguono due fasi: Fase catabolica Insieme delle
Equilibrio acido base
 Equilibrio acido base In una soluzione acquosa: [H+] x [OH-]= 10-14 M ph= logaritmo in base 10 dell inverso della [ H+] (-log[h+]) Variazioni di ph possono portare a variazioni di molec organiche e al
Equilibrio acido base In una soluzione acquosa: [H+] x [OH-]= 10-14 M ph= logaritmo in base 10 dell inverso della [ H+] (-log[h+]) Variazioni di ph possono portare a variazioni di molec organiche e al
Tamponi Biologici. AO/Febbraio 2016
 Tamponi Biologici AO/Febbraio 2016 Le soluzioni tampone Le soluzioni tampone contengono una coppia acido-base coniugata in cui le concentrazioni di acido e di base, entrambi non forti, sono circa dello
Tamponi Biologici AO/Febbraio 2016 Le soluzioni tampone Le soluzioni tampone contengono una coppia acido-base coniugata in cui le concentrazioni di acido e di base, entrambi non forti, sono circa dello
fornire energia chimica in vettori attivati ATP e NADH e NADPH e FADH.
 Cibo ed Energia Il glucosio e altre molecole nutritive per esempio i grassi vengono demolite attraverso un ossidazione graduale controllata per fornire energia chimica in una forma utilizzabile dalla cellula,
Cibo ed Energia Il glucosio e altre molecole nutritive per esempio i grassi vengono demolite attraverso un ossidazione graduale controllata per fornire energia chimica in una forma utilizzabile dalla cellula,
La fissazione dell azoto
 La fissazione dell azoto Complesso della nitrogenasi N +10H + + 8e + 16ATP N 2 + 10 H + 8e + 16ATP 2NH 4+ + 16ADP + 16P + H2 Metabolismo degli aminoacidi Metabolismo degli aminoacidi Gli aminoacidi
La fissazione dell azoto Complesso della nitrogenasi N +10H + + 8e + 16ATP N 2 + 10 H + 8e + 16ATP 2NH 4+ + 16ADP + 16P + H2 Metabolismo degli aminoacidi Metabolismo degli aminoacidi Gli aminoacidi
Cap.19. Ciclo di Krebs. o Ciclo degli acidi Tricarbossilici o Ciclo dell acido Citrico
 Cap.19 Ciclo di Krebs o Ciclo degli acidi Tricarbossilici o Ciclo dell acido Citrico Acetil-CoA OSSIDAZIONE DEL GLUCOSIO C 6 H 12 O 6 (glucosio) + 6O 2.. 6CO 2 + 6H 2 O I tappa: GLICOLISI 2 + 2 H 2 O II
Cap.19 Ciclo di Krebs o Ciclo degli acidi Tricarbossilici o Ciclo dell acido Citrico Acetil-CoA OSSIDAZIONE DEL GLUCOSIO C 6 H 12 O 6 (glucosio) + 6O 2.. 6CO 2 + 6H 2 O I tappa: GLICOLISI 2 + 2 H 2 O II
Riabilitativa 2015/2016
 Emoglobina e collageno Spina Riabilitativa 2015/2016 WWW.SUNHOPE.IT Alla grande varietà di strutture tridimensionali corrisponde una grande varietà di funzioni Ogni proteina presenta diversi livelli di
Emoglobina e collageno Spina Riabilitativa 2015/2016 WWW.SUNHOPE.IT Alla grande varietà di strutture tridimensionali corrisponde una grande varietà di funzioni Ogni proteina presenta diversi livelli di
NADH e NADPH. ATP = 1 moneta (energetica) della cellula NADH, NADPH = 2 moneta (potere riducente)
 NADH e NADPH ATP = 1 moneta (energetica) della cellula NADH, NADPH = 2 moneta (potere riducente) NADH e NADPH non sono funzionalmente intercambiabili. [NAD + ]/[NADH] ~ 1000 favorisce ossidazione [NADP
NADH e NADPH ATP = 1 moneta (energetica) della cellula NADH, NADPH = 2 moneta (potere riducente) NADH e NADPH non sono funzionalmente intercambiabili. [NAD + ]/[NADH] ~ 1000 favorisce ossidazione [NADP
Indice generale 1. Introduzione alla biochimica 2. Acqua, ph, acidi, basi, sali, tamponi
 Indice generale 1. Introduzione alla biochimica 1 Unità di misura 1 Energia e calore 3 Struttura dell atomo 3 Tavola periodica degli elementi 4 Legami chimici 8 Legami covalenti 8 Legami non covalenti
Indice generale 1. Introduzione alla biochimica 1 Unità di misura 1 Energia e calore 3 Struttura dell atomo 3 Tavola periodica degli elementi 4 Legami chimici 8 Legami covalenti 8 Legami non covalenti
2.Controllo dell equilibrio acido-base - II. Carlo Capelli Fisiologia Facoltà di Scienze Motorie- Università di Verona
 2.Controllo dell equilibrio acidobase II Carlo Capelli Fisiologia Facoltà di Scienze Motorie Università di Verona 1. Tampone bicarbonatoco 2 E il sistema tampone fisiologico più importante [ CO 2] = PCO
2.Controllo dell equilibrio acidobase II Carlo Capelli Fisiologia Facoltà di Scienze Motorie Università di Verona 1. Tampone bicarbonatoco 2 E il sistema tampone fisiologico più importante [ CO 2] = PCO
ph = log 1/[H + ] = log [H + ]
![ph = log 1/[H + ] = log [H + ] ph = log 1/[H + ] = log [H + ]](/thumbs/49/24977942.jpg) ph = log 1/[H ] = log [H ] Sangue arterioso ph = 7.4 Sangue venoso ph = 7.35 ph inferiori = acidosi (limite ph = 6.8) ph superiori = alcalosi (limite ph = 8) ph intracellulare = 6 7.4 ph urina 4.5 8 Produzione
ph = log 1/[H ] = log [H ] Sangue arterioso ph = 7.4 Sangue venoso ph = 7.35 ph inferiori = acidosi (limite ph = 6.8) ph superiori = alcalosi (limite ph = 8) ph intracellulare = 6 7.4 ph urina 4.5 8 Produzione
FISIOLOGIA dell ALLENAMENTO. dai processi fisiologici alle metodiche di allenamento
 FISIOLOGIA dell ALLENAMENTO dai processi fisiologici alle metodiche di allenamento Introduzione alla fisiologia Metabolismo cellulare Il sistema cardiovascolare: funzione cardiaca vasi, flusso, pressione
FISIOLOGIA dell ALLENAMENTO dai processi fisiologici alle metodiche di allenamento Introduzione alla fisiologia Metabolismo cellulare Il sistema cardiovascolare: funzione cardiaca vasi, flusso, pressione
Gli elementi corpuscolati del sangue sono vere cellule o derivati cellulari.
 I GLOBULI ROSSI Gli elementi corpuscolati del sangue sono vere cellule o derivati cellulari. I globuli rossi sono i più numerosi (5 milioni per mm 3 nell uomo, 4.5 milioni per mm 3 nella donna) sono detti
I GLOBULI ROSSI Gli elementi corpuscolati del sangue sono vere cellule o derivati cellulari. I globuli rossi sono i più numerosi (5 milioni per mm 3 nell uomo, 4.5 milioni per mm 3 nella donna) sono detti
Lattato. Glicolisi. Piruvato
 Lattato Glicolisi Piruvato REAZIONI MITOCONDRIALI DEL PIRUVATO + Piruvato Deidrogenasi + CO 2 + H 2 O ATP ADP + Pi Piruvato Carbossilasi + 2 H + ossalacetato La Piruvato Carbossilasi è una proteina Mitocondriale
Lattato Glicolisi Piruvato REAZIONI MITOCONDRIALI DEL PIRUVATO + Piruvato Deidrogenasi + CO 2 + H 2 O ATP ADP + Pi Piruvato Carbossilasi + 2 H + ossalacetato La Piruvato Carbossilasi è una proteina Mitocondriale
Regolazione della Glicolisi
 Regolazione della Glicolisi Enzimi regolati della glicolisi: 1) esochinasi. da: Champe La esochinasi: ha bassa Km per Glu 0,2mM: questo assicura la captazione anche di poche molecole di glucosio, presenti
Regolazione della Glicolisi Enzimi regolati della glicolisi: 1) esochinasi. da: Champe La esochinasi: ha bassa Km per Glu 0,2mM: questo assicura la captazione anche di poche molecole di glucosio, presenti
METABOLISMO DEL GLICOGENO
 METABOLISMO DEL GLICOGENO GLICOGENO: Polisaccaride di riserva del regno animale Organi principali: FEGATO MUSCOLO SCHELETRICO Glicogeno Glucosio Glucosio-6P Via del pentoso fosfato Glucosio Fruttosio-6P
METABOLISMO DEL GLICOGENO GLICOGENO: Polisaccaride di riserva del regno animale Organi principali: FEGATO MUSCOLO SCHELETRICO Glicogeno Glucosio Glucosio-6P Via del pentoso fosfato Glucosio Fruttosio-6P
Utilizzo del glucosio: la glicolisi
 Utilizzo del glucosio: la glicolisi GLUCOSIO Sistema rapido, reversibile, GLICOLISI avviene anche in assenza di ossigeno. Produce poca energia OSSIDAZIONE PIRUVATO Fermentazione LATTATO ACETATO CICLO DI
Utilizzo del glucosio: la glicolisi GLUCOSIO Sistema rapido, reversibile, GLICOLISI avviene anche in assenza di ossigeno. Produce poca energia OSSIDAZIONE PIRUVATO Fermentazione LATTATO ACETATO CICLO DI
Interazione tra xenobiotici ed organismi
 Prof. Giorgio Sartor Interazione tra xenobiotici ed organismi Copyright 2001-2008 by Giorgio Sartor. All rights reserved. Versione 4.1 oct 2008 Interazione tra un composto inquinante (xenobiotico) e un
Prof. Giorgio Sartor Interazione tra xenobiotici ed organismi Copyright 2001-2008 by Giorgio Sartor. All rights reserved. Versione 4.1 oct 2008 Interazione tra un composto inquinante (xenobiotico) e un
Laboratorio Fitness & Wellness
 Laboratorio Fitness & Wellness Anno Accademico 2015/2016 Ewan Thomas, MSc Principi di Bioenergetica e Biomeccanica Metabolismo Catabolismo Processi di degradazione che permettono di liberare energia Anabolismo
Laboratorio Fitness & Wellness Anno Accademico 2015/2016 Ewan Thomas, MSc Principi di Bioenergetica e Biomeccanica Metabolismo Catabolismo Processi di degradazione che permettono di liberare energia Anabolismo
I MITOCONDRI: LE CENTRALI ENERGETICHE DELLA CELLULA
 I MITOCONDRI: LE CENTRALI ENERGETICHE DELLA CELLULA MITOCONDRIO OSSERVATO AL SEM Localizzazione dei mitocondri SONO IN GENERE PIÙ ABBONDANTI DELLE ZONE DELLA CELLULA CHE RICHIEDONO MAGGIORI QUANTITA DI
I MITOCONDRI: LE CENTRALI ENERGETICHE DELLA CELLULA MITOCONDRIO OSSERVATO AL SEM Localizzazione dei mitocondri SONO IN GENERE PIÙ ABBONDANTI DELLE ZONE DELLA CELLULA CHE RICHIEDONO MAGGIORI QUANTITA DI
Carboidrati! Oligosaccaridi Polisaccaridi. B) Carboidrati complessi
 Carboidrati! Sono i composti organici più abbondanti sulla terra Contengono: C, H, O Sono Aldeidi o Chetoni poliossidrilici Possono essere suddivisi in: A) Zuccheri semplici Monosaccaridi B) Carboidrati
Carboidrati! Sono i composti organici più abbondanti sulla terra Contengono: C, H, O Sono Aldeidi o Chetoni poliossidrilici Possono essere suddivisi in: A) Zuccheri semplici Monosaccaridi B) Carboidrati
