La complessa semplicità dell'atomo di idrogeno!
|
|
|
- Sergio Bucci
- 6 anni fa
- Visualizzazioni
Transcript
1 La complessa semplicità dell'atomo di idrogeno Bergamo, venerdì 1 Febbraio 2013 Stefano Covino INAF - Osservatorio Astronomico di Brera
2 Un po di terminologia Atomo (dal greco, indivisibile): atomismo (Leucippo, Democrito, Epicuro) Leucippo - V secolo a.c. Democrito a.c. 360 a.c. Epicuro 10/2/241 a.c. 271 a.c.
3 Gli atomi come sferette L idea che la materia sia, a livello microscopico, formata da atomi, ovvero particelle indivisibili, viene ripreso da Dalton ad inzio 800. John Dalton 6/9/ /7/1844
4 Gli atomi però non sono tutti uguali D.I. Mendeleev 8/2/1834 2/2/1907
5 Si aveva anche un idea delle dimensioni atomiche Numero di Avogadro, densità e peso atomico Fe: N A "6x10 23, #"7,87 g/cm 3, A"56 1 mol Fe = A g = N A atomi atomi (1gr) = N A /A 1,1x10 22 volume (1gr) = 1/# 0.13 cm -3 volume / atomo 1,2x10-23 cm -3 volume = 4%r 3 r 10-8 cm = m Amedeo Avogadro 9/8/1776 9/7/1856 Per sapere come si ricava N A :
6 All inizio del ventesimo secolo, si sapeva che: gli atomi contenevano elettroni (diffrazione raggi X, effetto foto-elettrico, ecc.); il numero di elettroni, Z, era circa metà del peso atomico, A; gli atomi sono normalmente neutri, e quindi dovevano contenere cariche positive; la massa degli elettroni è piccolissima rispetto a qualunque atomo: la massa è concentrata nella carica positiva (m e = m p /1836); Il raggio degli atomi era ~10-10 m.
7 E quindi le prime idee quantitative sull atomo Come sono distribuite le cariche? il modello a plum pudding per avere neutralità e stabilità le cariche sono distribuite uniformemente. Joseph J. Thomson 18/12/ /8/1940
8 Curiosità George P. Thomson 3/5/ /9/1975 J.J. Thomson, padre, fu insignito del premio Nobel nel 1906 per avere mostrato che l elettrone era una particella subatomica. G.P. Thomson, figlio, fu insignito del premio Nobel nel 1937 per avere messo in evidenza le proprietà ondulatorie dell elettrone.
9 L esperimento di Geiger e Marsden Ernest Marsden - Hans Geiger Si tratta di un classico esperimento di scattering : Un fascio di particelle alfa (nuclei di elio) è lanciato attraverso un sottile foglio di metallo. Nel modello di Thomson l angolo di deviazione risulta essere molto piccolo. Per calcolare lo scattering previsto (in inglese):
10 L interpretazione di Rutherford Fatti osservati: Praticamente tutte le particelle & attraversano il foglio di metallo (quasi) indisturbate Occasionalmente abbiamo però deviazioni a grandi angoli. Anche autentici rimbalzi. La probabilità di questi ultimi dipende dal peso atomico del materiale bersaglio. Ernest Rutherford 30/8/ /10/1937 Quindi l ipotesi: la massa (e la carica positiva) è concentrata nel nucleo dell atomo, circondata dagli elettroni che occupano praticamente tutto il volume Per calcolare lo scattering previsto (in inglese):
11 Secondo le parole dello stesso Rutherford: It was quite the most incredible event that ever happened to me in my life. It was as incredible as if you fired a 15-inch shell at a piece of tissue paper and it came back and hit you. Analizzando i risultati degli esperimenti si poté anche stimare la dimensione del nucleo: m
12 Problema: può una struttura del genere essere stabile? Gli elettroni non possono essere fermi nel modello di Rutherford, devono quindi orbitare. Però cariche accelerate emetteranno radiazione e perderanno energia. L atomo dovrebbe collassare in s
13 Gli spettri atomici Effettivamente gli atomi emettono radiazioni, ma sono anche osservati essere stabili. Che tipo di radiazione emettono? k = 1/' = R H (1/2 2 -n 2 ) Serie di Balmer, R H costante di Rydberg Spettro dell atomo di idrogeno
14 Come interpretare gli spettri atomici? Nel 1913 Niels Bohr ideò un modello che descriva accuratamente le osservazioni. Si basava però su alcuni postulati: 1. Un elettrone in un atomo si muove in orbite circolari sotto l influenza della forza di Coulomb. 2. Invece delle infinite orbite possibili solo quelle per cui il momento angolare orbitale è un multiplo di h/2% sono possibili. 3. In queste orbite gli elettroni sebbene accelerati non emettono radiazione. 4. Si ha invece emissione se un elettrone salta da un orbita ad un altra. Niels Bohr 7/10/ /11/1962
15 Momento angolare ed energia Supponiamo di avere un elettrone in orbita circolare attorno ad un nucleo di carica Z ad una distanza r: Forza di Coulomb: F = 1/4%( 0 Ze 2 /r 2 Forza Centripreta: F = m v 2 / r Momento Angolare: L = mvr 1/4%( 0 Ze 2 /r 2 = m v 2 / r con un po di algebra mvr = n h/2% r = 4%( 0 n 2 (h/2%) / (mze 2 )
16 Livelli energetici Sempre con un po di algebra Energia orbitale: E = {-mz 2 e 4 / [(4%( 0 ) 2 2(h/2%) 2 ]} 1/n 2 [n = 1,2,3 ] In pratica la quantizzazione del momento angolare orbitale degli elettroni porta alla quantizzazione dell energia totale
17 Emissione o assorbimento di fotoni Conoscendo l energia associata ad ogni livello, il salto di livello corrisponde ad assorbimento od emissione. I livelli energetici permessi sono quelli per un numero intero di lunghezze d onda si chiudono nella circonferenza.
18 Meccanica Quantistica? Il modello di Bohr, con sviluppo successivi (Sommerfield, ecc.) ha un grosso pregio: funziona. Tuttavia ci sono anche una serie di fenomeni che in questo scenario non sono riproducibili (atomi a più elettroni, ecc.) E, non ultimo, tutto lo scenario appare un po artificioso, mancante di coerenza intellettuale.
19 Verso la moderna meccanica quantistica Il concetto di quantizzazione era presente sotto diversi aspetti all inizio del 900. Si pensi ai lavori di Einstein, Planck, de Broglie, ecc. Il passo successivo avrà però delle caratteristiche diverse: introdurrà una maniera nuova di affrontare i problemi fisici con un approccio statistico anziché rigidamente deterministico. Si arriva così ad un concetto fondamentale della moderna meccanica quantistica: quello di funzione d onda.
20 Dualismo onda-corpuscolo Diverse evidenze sperimentali hanno mostrato come sia i fotoni che le particelle subatomiche possono essere descritte a seconda dei fenomeni come particelle o come onde. Pensiamo, per esempio, ai fenomeni di interferenza e diffrazione. Louis de Broglie 15/8/ /3/1987
21 La funzione d onda L idea di base è che lo stato di un sistema fisico dipenda dalla sua funzione d onda, una funzione complessa delle coordinate spaziali e temporali. Discutere di funzioni d onda è complesso e dire cose come: è la proiezione di uno stato quantistico sulla base degli autostati di un osservabile la cui dinamica è descritta dall equazione di Schrödinger non è che aiuti molto Erwin Schrödinger 12/8/1887 4/1/1961
22 Proprietà (sunto ) delle funzioni d onda La funzione d onda è associata una densità probabilità (interpretazione dovuta in realtà a Born) Max Born 11/12/1882 5/1/1970 di
23 Vediamo un esempio semplice mono-dimensionale Gli elettroni non saranno mai rivelati qui La probabilità di rivelare un elettrone è ψ 2 o qui Gli elettroni saranno con maggiore probabilità qui
24 Ma cosa significa tutto quanto? La meccanica quantistica funziona, e molto bene. Rimane però sempre aperto un dibattito importante: è una buona rappresentazione della realtà o è la realtà? Ad esempio il ben noto paradosso del gatto di Schrödinger
25 Grazie per l attenzione
Unità Didattica 3. L atomo di idrogeno
 Diapositiva 1 Unità Didattica 3 L atomo di idrogeno Questa unità contiene informazioni sull atomo di idrogeno, i modelli di Tomson, Ruterford e Bor, l esperimento di Frank-Hertz e infine la formula di
Diapositiva 1 Unità Didattica 3 L atomo di idrogeno Questa unità contiene informazioni sull atomo di idrogeno, i modelli di Tomson, Ruterford e Bor, l esperimento di Frank-Hertz e infine la formula di
Lezioni di Meccanica Quantistica
 Luigi E. Picasso Lezioni di Meccanica Quantistica seconda edizione Edizioni ETS www.edizioniets.com Copyright 2015 EDIZIONI ETS Piazza Carrara, 16-19, I-56126 Pisa info@edizioniets.com www.edizioniets.com
Luigi E. Picasso Lezioni di Meccanica Quantistica seconda edizione Edizioni ETS www.edizioniets.com Copyright 2015 EDIZIONI ETS Piazza Carrara, 16-19, I-56126 Pisa info@edizioniets.com www.edizioniets.com
Capitolo 2. Cenni alla Composizione e Struttura dell atomo
 Master in Verifiche di qualità in radiodiagnostica, medicina nucleare e radioterapiar Capitolo 2 Cenni alla Composizione e Struttura dell atomo 24 Atomi, Molecole,, e Ioni L idea di Atomo è antica come
Master in Verifiche di qualità in radiodiagnostica, medicina nucleare e radioterapiar Capitolo 2 Cenni alla Composizione e Struttura dell atomo 24 Atomi, Molecole,, e Ioni L idea di Atomo è antica come
Sulla nascita di questo libro. Introduzione 1
 Indice Sulla nascita di questo libro V Introduzione 1 1 Luce e materia 7 Che cos è veramente la luce? 7 Ma qui che cosa oscilla? 9 Che cosa sono la frequenza e la lunghezza d onda della luce? 11 Che cos
Indice Sulla nascita di questo libro V Introduzione 1 1 Luce e materia 7 Che cos è veramente la luce? 7 Ma qui che cosa oscilla? 9 Che cosa sono la frequenza e la lunghezza d onda della luce? 11 Che cos
ATOMO. Legge della conservazione della massa Legge delle proporzioni definite Dalton
 Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti interi
Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti interi
il modello atomico di Bohr
 il modello atomico di Bohr Lo scienziato Niels Bohr, ospite nel laboratorio di Rutherford a Manchester ma anche allievo di Planck, nel 93 pubblicò alcuni saggi in cui, accettando il modello planetario
il modello atomico di Bohr Lo scienziato Niels Bohr, ospite nel laboratorio di Rutherford a Manchester ma anche allievo di Planck, nel 93 pubblicò alcuni saggi in cui, accettando il modello planetario
Le particelle dell atomo
 La carica elettrica I fenomeni elettrici sono noti fin dall antichità: gli antichi Greci usavano la parola elektron per spiegare il fenomeno dell elettrizzazione dell ambra. I Greci sapevano che strofinando
La carica elettrica I fenomeni elettrici sono noti fin dall antichità: gli antichi Greci usavano la parola elektron per spiegare il fenomeno dell elettrizzazione dell ambra. I Greci sapevano che strofinando
I modelli atomici da Dalton a Bohr
 1 Espansione 2.1 I modelli atomici da Dalton a Bohr Modello atomico di Dalton: l atomo è una particella indivisibile. Modello atomico di Dalton Nel 1808 John Dalton (Eaglesfield, 1766 Manchester, 1844)
1 Espansione 2.1 I modelli atomici da Dalton a Bohr Modello atomico di Dalton: l atomo è una particella indivisibile. Modello atomico di Dalton Nel 1808 John Dalton (Eaglesfield, 1766 Manchester, 1844)
Modelli atomici. Teoria atomica Dalton (1803) La materia non è continua, ma costituita da particelle.
 Modelli atomici Teoria atomica Dalton (1803) La materia non è continua, ma costituita da particelle. Presupposti 1. Legge di Lavoisier della conservazione della massa: in una reazione chimica nulla si
Modelli atomici Teoria atomica Dalton (1803) La materia non è continua, ma costituita da particelle. Presupposti 1. Legge di Lavoisier della conservazione della massa: in una reazione chimica nulla si
Struttura Elettronica degli Atomi Meccanica quantistica
 Prof. A. Martinelli Struttura Elettronica degli Atomi Meccanica quantistica Dipartimento di Farmacia 1 Il comportamento ondulatorio della materia 2 1 Il comportamento ondulatorio della materia La diffrazione
Prof. A. Martinelli Struttura Elettronica degli Atomi Meccanica quantistica Dipartimento di Farmacia 1 Il comportamento ondulatorio della materia 2 1 Il comportamento ondulatorio della materia La diffrazione
Bohr e la struttura dell atomo. Lezioni 11-12
 Bohr e la struttura dell atomo Lezioni 11-12 Onde elettromagnetiche Radiazione Elettromagnetica raggi X e raggi > 10 3 Hz
Bohr e la struttura dell atomo Lezioni 11-12 Onde elettromagnetiche Radiazione Elettromagnetica raggi X e raggi > 10 3 Hz
LE RIVOLUZIONI QUANTISTICHE e ERWIN SCHRÖDINGER. Alice Marchi 5 G Liceo Scientifico Giacomo Ulivi A.S. 2015/2016
 LE RIVOLUZIONI QUANTISTICHE e ERWIN SCHRÖDINGER Alice Marchi 5 G Liceo Scientifico Giacomo Ulivi A.S. 2015/2016 INDICE 1. Introduzione 2. Prima rivoluzione quantistica 2.1 Planck 2.2 Einstein 2.3 Bohr
LE RIVOLUZIONI QUANTISTICHE e ERWIN SCHRÖDINGER Alice Marchi 5 G Liceo Scientifico Giacomo Ulivi A.S. 2015/2016 INDICE 1. Introduzione 2. Prima rivoluzione quantistica 2.1 Planck 2.2 Einstein 2.3 Bohr
La Teoria dei Quanti e la Struttura Elettronica degli Atomi. Capitolo 7
 La Teoria dei Quanti e la Struttura Elettronica degli Atomi Capitolo 7 Proprietà delle Onde Lunghezza d onda (λ) E la distanza tra due punti identici su due onde successive. Ampiezza è la distanza verticale
La Teoria dei Quanti e la Struttura Elettronica degli Atomi Capitolo 7 Proprietà delle Onde Lunghezza d onda (λ) E la distanza tra due punti identici su due onde successive. Ampiezza è la distanza verticale
Il metodo scientifico
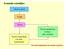 Il metodo scientifico Osservazioni Legge Teoria Teoria controllata con altri esperimenti Teoria modificata in base alle verifiche Gli stadi fondamentali del metodo scientifico 1 Leggi ponderali Legge della
Il metodo scientifico Osservazioni Legge Teoria Teoria controllata con altri esperimenti Teoria modificata in base alle verifiche Gli stadi fondamentali del metodo scientifico 1 Leggi ponderali Legge della
CHIMICAMENTE. Lezioni del prof. Puletti Classe II B
 CHIMICAMENTE Lezioni del prof. Puletti Classe II B Scuola Media PIO X Artigianelli A.S. 2011-2012 PERCORSO - cos è la materia e da cosa è costituita - le particelle atomiche fondamentali: protoni, neutroni
CHIMICAMENTE Lezioni del prof. Puletti Classe II B Scuola Media PIO X Artigianelli A.S. 2011-2012 PERCORSO - cos è la materia e da cosa è costituita - le particelle atomiche fondamentali: protoni, neutroni
Quadro di Riferimento della II prova di Fisica dell esame di Stato per i Licei Scientifici
 Quadro di Riferimento della II prova di Fisica dell esame di Stato per i Licei Scientifici Il presente documento individua le conoscenze, abilità e competenze che lo studente dovrà aver acquisito al termine
Quadro di Riferimento della II prova di Fisica dell esame di Stato per i Licei Scientifici Il presente documento individua le conoscenze, abilità e competenze che lo studente dovrà aver acquisito al termine
La Meccanica Quantistica
 La Meccanica Quantistica Se quando pensiamo a un atomo ci immaginiamo qualcosa di questo tipo Dobbiamo rivedere le nostre idee LA CRISI DELLA FISICA CLASSICA La crisi della fisica classica Un secolo fa
La Meccanica Quantistica Se quando pensiamo a un atomo ci immaginiamo qualcosa di questo tipo Dobbiamo rivedere le nostre idee LA CRISI DELLA FISICA CLASSICA La crisi della fisica classica Un secolo fa
Storia della meccanica quantistica
 Storia della meccanica quantistica Prof. Daniele Ippolito Liceo Scientifico Amedeo di Savoia di Pistoia La quantizzazione della luce La quantizzazione della materia La nuova meccanica quantistica La quantizzazione
Storia della meccanica quantistica Prof. Daniele Ippolito Liceo Scientifico Amedeo di Savoia di Pistoia La quantizzazione della luce La quantizzazione della materia La nuova meccanica quantistica La quantizzazione
3. Struttura dell atomo
 Di cosa parleremo L organizzazione interna delle particelle che costituiscono gli atomi è stata oggetto di studio per lungo tempo e le ipotesi sulla struttura atomica si sono evolute nel tempo in base
Di cosa parleremo L organizzazione interna delle particelle che costituiscono gli atomi è stata oggetto di studio per lungo tempo e le ipotesi sulla struttura atomica si sono evolute nel tempo in base
INDICE 1. LA CRISI DELLA FISICA CLASSICA
 INDICE 1. LA CRISI DELLA FISICA CLASSICA 1.1 Modelli atomici... 1 1.2 Il problema delle dimensioni atomiche e del collasso per irraggiamento 4 1.3 Difficoltà connesse con i calori specifici... 7 1.4 L
INDICE 1. LA CRISI DELLA FISICA CLASSICA 1.1 Modelli atomici... 1 1.2 Il problema delle dimensioni atomiche e del collasso per irraggiamento 4 1.3 Difficoltà connesse con i calori specifici... 7 1.4 L
May 5, 2013. Fisica Quantistica. Monica Sambo. Sommario
 May 5, 2013 Bohr, Born,, Dirac e Pauli accettano in modo incondizionato la nuova fisica Einstein, De, e pur fornendo importanti contributi alla nuova teoria cercano di ottenere una descrizione CAUSALE
May 5, 2013 Bohr, Born,, Dirac e Pauli accettano in modo incondizionato la nuova fisica Einstein, De, e pur fornendo importanti contributi alla nuova teoria cercano di ottenere una descrizione CAUSALE
LA RIVOLUZIONE QUANTISTICA
 LA RIVOLUZIONE QUANTISTICA Franco Prati Università dell Insubria - Como NINDA URUK Il pane dei Sumeri Ricerca scientifica ed epistemologia 5 dicembre 2012 Congresso Internazionale dei Fisici in onore di
LA RIVOLUZIONE QUANTISTICA Franco Prati Università dell Insubria - Como NINDA URUK Il pane dei Sumeri Ricerca scientifica ed epistemologia 5 dicembre 2012 Congresso Internazionale dei Fisici in onore di
CHIMICA: studio della composizione e della struttura della materia e delle sue trasformazioni
 CHIMICA: studio della composizione e della struttura della materia e delle sue trasformazioni composto materia sostanza pura miscela omogenea elemento eterogenea Elementi, Composti e Miscele Miscela eterogenea
CHIMICA: studio della composizione e della struttura della materia e delle sue trasformazioni composto materia sostanza pura miscela omogenea elemento eterogenea Elementi, Composti e Miscele Miscela eterogenea
2bis. I modelli atomici
 2bis. I modelli atomici 2.1 Il modello di Thomson 2.2 Il modello di Rutherford; 2.3 Il dualismo particella-onda; 2.4 Il modello di Bohr 2.5 Il modello a orbitali 2.6 Il riempimento degli orbitali e le
2bis. I modelli atomici 2.1 Il modello di Thomson 2.2 Il modello di Rutherford; 2.3 Il dualismo particella-onda; 2.4 Il modello di Bohr 2.5 Il modello a orbitali 2.6 Il riempimento degli orbitali e le
STRUTTURA ATOMICA E CONFIGURAZIONE ELETTRONICA
 pg 1 STRUTTURA ATOMICA E CONFIGURAZIONE ELETTRONICA Per capire il comportamento degli atomi dobbiamo studiare il comportamento dei suoi elettroni L'atomo e le sue particelle NON sono direttamente visibili
pg 1 STRUTTURA ATOMICA E CONFIGURAZIONE ELETTRONICA Per capire il comportamento degli atomi dobbiamo studiare il comportamento dei suoi elettroni L'atomo e le sue particelle NON sono direttamente visibili
STORIA DELL'ATOMO DA DEMOCRITO A SCHRÖDINGER
 DEMOCRITO STORIA DELL'ATOMO DA DEMOCRITO A SCHRÖDINGER Democrito, IV sec. a.c., deduce l'esistenza di atomi (atomòs = indivisibile) da un processo logico e puramente teorico attraverso il quale comprende
DEMOCRITO STORIA DELL'ATOMO DA DEMOCRITO A SCHRÖDINGER Democrito, IV sec. a.c., deduce l'esistenza di atomi (atomòs = indivisibile) da un processo logico e puramente teorico attraverso il quale comprende
4. Lo spettro discreto: emissione e assorbimento di luce da parte di atomi stato fondamentale stati eccitati
 4. Lo spettro discreto: emissione e assorbimento di luce da parte di atomi Accanto allo spettro continuo che i corpi emettono in ragione del loro stato termico, si osservano spettri discreti che sono caratteristici
4. Lo spettro discreto: emissione e assorbimento di luce da parte di atomi Accanto allo spettro continuo che i corpi emettono in ragione del loro stato termico, si osservano spettri discreti che sono caratteristici
Dai primi modelli alla teoria moderna
 MODELLI ATOMICI Dai primi modelli alla teoria moderna I modelli atomici nacquero, dall'intuizione di alcuni scienziati di fronte all'impossibilità di interpretare in modo semplice i fenomeni complessi.
MODELLI ATOMICI Dai primi modelli alla teoria moderna I modelli atomici nacquero, dall'intuizione di alcuni scienziati di fronte all'impossibilità di interpretare in modo semplice i fenomeni complessi.
PROFILO IN USCITA PER IL PRIM0 ANNO FISICA Sezioni internazionale ad opzione Inglese (L,M,N,O,P,Q)
 PROFILO IN USCITA PER IL PRIM0 ANNO Premessa Come stabilito dal Collegio dei docenti e conformemente con gli obiettivi della attuale sperimentazione, la programmazione seguirà, principalmente, la scansione
PROFILO IN USCITA PER IL PRIM0 ANNO Premessa Come stabilito dal Collegio dei docenti e conformemente con gli obiettivi della attuale sperimentazione, la programmazione seguirà, principalmente, la scansione
Struttura Elettronica degli Atomi
 Prof. A. Martinelli Struttura Elettronica degli Atomi Dipartimento di Farmacia 1 La Natura ondulatoria della luce - La luce visibile è una piccola parte dello spettro delle onde elettromagnetiche. 1 La
Prof. A. Martinelli Struttura Elettronica degli Atomi Dipartimento di Farmacia 1 La Natura ondulatoria della luce - La luce visibile è una piccola parte dello spettro delle onde elettromagnetiche. 1 La
2.1 (p. 37) Bohr descrisse un orbitale atomico come una traiettoria circolare seguita dall elettrone. Un orbitale è una
 Capitolo 2 Risposte alle Domande ed esercizi inclusi nel Capitolo 2.1 (p. 37) Bohr descrisse un orbitale atomico come una traiettoria circolare seguita dall elettrone. Un orbitale è una regione di spazio
Capitolo 2 Risposte alle Domande ed esercizi inclusi nel Capitolo 2.1 (p. 37) Bohr descrisse un orbitale atomico come una traiettoria circolare seguita dall elettrone. Un orbitale è una regione di spazio
Scienziati in Erba Chimica
 Scienziati in Erba Chimica Acqua Oro Zucchero La Chimica ü ü ü ü ü ü ü ü ü ü Cosa studia la chimica? Classificazione della materia Stati della materia Formule chimiche Atomo Tavola periodica degli elementi
Scienziati in Erba Chimica Acqua Oro Zucchero La Chimica ü ü ü ü ü ü ü ü ü ü Cosa studia la chimica? Classificazione della materia Stati della materia Formule chimiche Atomo Tavola periodica degli elementi
IL MODELLO ATOMICO DI BOHR
 IL MODELLO ATOMICO DI BOHR LA LUCE Un valido contributo alla comprensione della struttura dell atomo venne dato dallo studio delle radiazioni luminose emesse dagli atomi opportunamente sollecitati. Lo
IL MODELLO ATOMICO DI BOHR LA LUCE Un valido contributo alla comprensione della struttura dell atomo venne dato dallo studio delle radiazioni luminose emesse dagli atomi opportunamente sollecitati. Lo
Introduzione della Meccanica Quantistica nella Scuola Secondaria Superiore
 Università degli Studi di Ferrara SSIS Indirizzo FIM Classe A049 Ciclo VIII Dissertazione Finale A.A. 2007/2008 Introduzione della Meccanica Quantistica nella Scuola Secondaria Superiore Specializzando
Università degli Studi di Ferrara SSIS Indirizzo FIM Classe A049 Ciclo VIII Dissertazione Finale A.A. 2007/2008 Introduzione della Meccanica Quantistica nella Scuola Secondaria Superiore Specializzando
LE PARTICELLE ELEMENTARI: loro scoperta
 LE PARTICELLE ELEMENTARI: loro scoperta Atomo: composto da particelle elementari più piccole (protoni, neutroni, elettroni) Atomi di elementi diversi contengono le STESSE particelle, ma in numero diverso
LE PARTICELLE ELEMENTARI: loro scoperta Atomo: composto da particelle elementari più piccole (protoni, neutroni, elettroni) Atomi di elementi diversi contengono le STESSE particelle, ma in numero diverso
n(z) = n(0) e m gz/k B T ; (1)
 Corso di Introduzione alla Fisica Quantistica (f) Prova scritta 4 Luglio 008 - (tre ore a disposizione) [sufficienza con punti 8 circa di cui almeno 4 dagli esercizi nn. 3 e/o 4] [i bonus possono essere
Corso di Introduzione alla Fisica Quantistica (f) Prova scritta 4 Luglio 008 - (tre ore a disposizione) [sufficienza con punti 8 circa di cui almeno 4 dagli esercizi nn. 3 e/o 4] [i bonus possono essere
Atomo e particelle atomiche
 Atomo e particelle atomiche La natura elettrica della materia lo strofinio di qualsiasi materiale provoca la comparsa su di esso di una carica elettrica capace di attrarre piccoli oggetti; la carica elettrica
Atomo e particelle atomiche La natura elettrica della materia lo strofinio di qualsiasi materiale provoca la comparsa su di esso di una carica elettrica capace di attrarre piccoli oggetti; la carica elettrica
PROGETTO AMICI DI SCIASCIA. Fisica delle particelle
 PROGETTO AMICI DI SCIASCIA Fisica delle particelle TEMI TRATTATI NELLA PRESENTAZIONE 1. STORIA DELLA FISICA DELLE PARTICELLE 2. COME E FATTO L ATOMO? IPOTESI SULLA STRUTTURA DELL ATOMO 3. LA FISICA DELLE
PROGETTO AMICI DI SCIASCIA Fisica delle particelle TEMI TRATTATI NELLA PRESENTAZIONE 1. STORIA DELLA FISICA DELLE PARTICELLE 2. COME E FATTO L ATOMO? IPOTESI SULLA STRUTTURA DELL ATOMO 3. LA FISICA DELLE
Lezione n. 19. L equazione. di Schrodinger L atomo. di idrogeno Orbitali atomici. 02/03/2008 Antonino Polimeno 1
 Chimica Fisica - Chimica e Tecnologia Farmaceutiche Lezione n. 19 L equazione di Schrodinger L atomo di idrogeno Orbitali atomici 02/03/2008 Antonino Polimeno 1 Dai modelli primitivi alla meccanica quantistica
Chimica Fisica - Chimica e Tecnologia Farmaceutiche Lezione n. 19 L equazione di Schrodinger L atomo di idrogeno Orbitali atomici 02/03/2008 Antonino Polimeno 1 Dai modelli primitivi alla meccanica quantistica
La struttura della materia
 La struttura della materia IL CORPO NERO In fisica, i corpi solidi o liquidi emettono radiazioni elettromagnetiche, a qualsiasi temperatura. Il corpo nero, invece, è un oggetto ideale che assorbe tutta
La struttura della materia IL CORPO NERO In fisica, i corpi solidi o liquidi emettono radiazioni elettromagnetiche, a qualsiasi temperatura. Il corpo nero, invece, è un oggetto ideale che assorbe tutta
Misura del momento magnetico dell elettrone
 FACOLTÀ Università degli Studi di Roma Tre DI SCIENZE MATEMATICHE, FISICHE E NATURALI Corso di Laurea in Fisica Misura del momento magnetico dell elettrone Candidato: Andrea Sciandra Matricola 4480 Relatore:
FACOLTÀ Università degli Studi di Roma Tre DI SCIENZE MATEMATICHE, FISICHE E NATURALI Corso di Laurea in Fisica Misura del momento magnetico dell elettrone Candidato: Andrea Sciandra Matricola 4480 Relatore:
Chimica. La chimica studia composizione, struttura, proprietà e trasformazioni della materia
 Chimica La chimica studia composizione, struttura, proprietà e trasformazioni della materia La materia è costituita da atomi uguali o diversi, uniti fra loro da forze di legame strettamente dipendenti
Chimica La chimica studia composizione, struttura, proprietà e trasformazioni della materia La materia è costituita da atomi uguali o diversi, uniti fra loro da forze di legame strettamente dipendenti
Fenomeni quantistici
 Fenomeni quantistici 1. Radiazione di corpo nero Leggi di Wien e di Stefan-Boltzman Equipartizione dell energia classica Correzione quantistica di Planck 2. Effetto fotoelettrico XIII - 0 Radiazione da
Fenomeni quantistici 1. Radiazione di corpo nero Leggi di Wien e di Stefan-Boltzman Equipartizione dell energia classica Correzione quantistica di Planck 2. Effetto fotoelettrico XIII - 0 Radiazione da
Tabella periodica degli elementi
 Tabella periodica degli elementi Perchè ha questa forma? Ovvero, esiste una regola per l ordinamento dei singoli atomi? Le proprietà dei materiali hanno una relazione con la tabella? L applicazione dei
Tabella periodica degli elementi Perchè ha questa forma? Ovvero, esiste una regola per l ordinamento dei singoli atomi? Le proprietà dei materiali hanno una relazione con la tabella? L applicazione dei
Introduzione ai fenomeni quantistici
 Introduzione ai fenomeni quantistici Tratto da: The Feynman lectures on physics, vol. 3 Marco Bonvini Nicodemo Magnoli Meccanica: Keplero (1608-1619) Galilei (1630) Newton (1687) Termodinamica: Kelvin
Introduzione ai fenomeni quantistici Tratto da: The Feynman lectures on physics, vol. 3 Marco Bonvini Nicodemo Magnoli Meccanica: Keplero (1608-1619) Galilei (1630) Newton (1687) Termodinamica: Kelvin
Tutta la materia è fatta da particelle piccolissime, invisibili ed indivisibili dette ATOMI;
 Tutta la materia è fatta da particelle piccolissime, invisibili ed indivisibili dette ATOMI; ELEMENTO: sostanza formata da un solo tipo di atomi, tutti uguali e con le stesse proprietà chimiche; COMPOSTO:
Tutta la materia è fatta da particelle piccolissime, invisibili ed indivisibili dette ATOMI; ELEMENTO: sostanza formata da un solo tipo di atomi, tutti uguali e con le stesse proprietà chimiche; COMPOSTO:
Spettro elettromagnetico
 Spettro elettromagnetico Sorgenti Finestre Tipo Oggetti rilevabili Raggi γ ev Raggi X Lunghezza d onda E hc = hν = = λ 12. 39 λ( A o ) Visibile Infrarosso icro onde Onde-radio Dimensione degli oggetti
Spettro elettromagnetico Sorgenti Finestre Tipo Oggetti rilevabili Raggi γ ev Raggi X Lunghezza d onda E hc = hν = = λ 12. 39 λ( A o ) Visibile Infrarosso icro onde Onde-radio Dimensione degli oggetti
Quantum Theory. E la natura dell'atomo. M. Orlandelli, A. Peloni
 Quantum Theory E la natura dell'atomo M. Orlandelli, A. Peloni Quantum Mechanics: prime idee (inizio 1900) A. Einstein: Effetto fotoelettrico C. Maxwell Equazioni delle onde elettromagnetiche M. Planck:
Quantum Theory E la natura dell'atomo M. Orlandelli, A. Peloni Quantum Mechanics: prime idee (inizio 1900) A. Einstein: Effetto fotoelettrico C. Maxwell Equazioni delle onde elettromagnetiche M. Planck:
La Struttura degli atomi. ChimicaGenerale_lezione5 1
 La Struttura degli atomi ChimicaGenerale_lezione5 1 Modello atomico di Thomson Massa e carica dell'atomo sono distribuiti in modo uniforme nell'atomo La repulsione reciproca tiene gli elettroni lontani,
La Struttura degli atomi ChimicaGenerale_lezione5 1 Modello atomico di Thomson Massa e carica dell'atomo sono distribuiti in modo uniforme nell'atomo La repulsione reciproca tiene gli elettroni lontani,
Vincenzo Branchina. Rivoluzioni Scientifiche. Fisica Quantistica. Università di Catania Dipartimento di Fisica e Astronomia
 Vincenzo Branchina Rivoluzioni Scientifiche Fisica Quantistica Università di Catania Dipartimento di Fisica e Astronomia Giarre, 5 Marzo 2015 Nuova Meccanica Quantistica: Equazione di Schrodinger (1925)
Vincenzo Branchina Rivoluzioni Scientifiche Fisica Quantistica Università di Catania Dipartimento di Fisica e Astronomia Giarre, 5 Marzo 2015 Nuova Meccanica Quantistica: Equazione di Schrodinger (1925)
L energia assorbita dall atomo durante l urto iniziale è la stessa del fotone che sarebbe emesso nel passaggio inverso, e quindi vale: m
 QUESITI 1 Quesito Nell esperimento di Rutherford, una sottile lamina d oro fu bombardata con particelle alfa (positive) emesse da una sorgente radioattiva. Secondo il modello atomico di Thompson le particelle
QUESITI 1 Quesito Nell esperimento di Rutherford, una sottile lamina d oro fu bombardata con particelle alfa (positive) emesse da una sorgente radioattiva. Secondo il modello atomico di Thompson le particelle
L ATOMO NELLA STORIA.
 L ATOMO NELLA STORIA. L'atomo è la più piccola porzione di materia che può caratterizzare un elemento e che ne possiede le proprietà chimiche, deriva dal greco atomos, indivisibile, e veniva usata dagli
L ATOMO NELLA STORIA. L'atomo è la più piccola porzione di materia che può caratterizzare un elemento e che ne possiede le proprietà chimiche, deriva dal greco atomos, indivisibile, e veniva usata dagli
LA STRUTTURA DELL ATOMO
 Capitolo 4 LA STRUTTURA DELL ATOMO N.B I concetti proposti sulle slide, in linea di massima seguono l ordine e i contenuti del libro, ma!!!! Ci possono essere delle variazioni Prof. Vincenzo Leo - Chimica
Capitolo 4 LA STRUTTURA DELL ATOMO N.B I concetti proposti sulle slide, in linea di massima seguono l ordine e i contenuti del libro, ma!!!! Ci possono essere delle variazioni Prof. Vincenzo Leo - Chimica
LASER. Light Amplification by Stimulated Emission of Radiation. Introduzione. Assorbimento, emissione spontanea, emissione stimolata
 LASER Light Amplification by Stimulated Emission of Radiation Introduzione. Assorbimento, emissione spontanea, emissione stimolata Cenni storici 1900 Max Planck introduce la teoria dei quanti (la versione
LASER Light Amplification by Stimulated Emission of Radiation Introduzione. Assorbimento, emissione spontanea, emissione stimolata Cenni storici 1900 Max Planck introduce la teoria dei quanti (la versione
Un introduzione alla Meccanica Quantistica
 Un introduzione alla Meccanica Quantistica La Teoria che nessuno capisce! Chiunque non resti sconvolto dalla teoria quantistica, sicuramente NON L HA CAPITA N. Bohr Quanto piu` la teoria dei quanti incontra
Un introduzione alla Meccanica Quantistica La Teoria che nessuno capisce! Chiunque non resti sconvolto dalla teoria quantistica, sicuramente NON L HA CAPITA N. Bohr Quanto piu` la teoria dei quanti incontra
p e c = ev Å
 Corso di Introduzione alla Fisica Quantistica (f) Soluzioni Esercizi: Giugno 006 * Quale la lunghezza d onda di de Broglie di un elettrone che ha energia cinetica E 1 = KeV e massa a riposo m 0 = 9.11
Corso di Introduzione alla Fisica Quantistica (f) Soluzioni Esercizi: Giugno 006 * Quale la lunghezza d onda di de Broglie di un elettrone che ha energia cinetica E 1 = KeV e massa a riposo m 0 = 9.11
Dai primi modelli atomici alla teoria moderna
 Dai primi modelli atomici alla teoria moderna 1 Se numerose evidenze sperimentali avevano permesso di trovare l'esistenza delle particelle subatomiche, le loro dimensioni, così infinitamente piccole, non
Dai primi modelli atomici alla teoria moderna 1 Se numerose evidenze sperimentali avevano permesso di trovare l'esistenza delle particelle subatomiche, le loro dimensioni, così infinitamente piccole, non
Struttura atomica della materia
 Struttura atomica della materia 1 FASE fase 3 fase 1 fase 2 FASE: porzione di materia chimicamente e fisicamente omogenea delimitata da superfici di separazione ben definite 2 Classificazione della materia
Struttura atomica della materia 1 FASE fase 3 fase 1 fase 2 FASE: porzione di materia chimicamente e fisicamente omogenea delimitata da superfici di separazione ben definite 2 Classificazione della materia
2. La struttura dell atomo
 2. La struttura dell atomo 2.1 Particelle elementari 2.2 I modelli atomici: storia dell atomo 2.3 Numero atomico e numero di massa; 2.4 Isotopi; 2.5 Elementi e tavola periodica 2.1 Particelle elementari
2. La struttura dell atomo 2.1 Particelle elementari 2.2 I modelli atomici: storia dell atomo 2.3 Numero atomico e numero di massa; 2.4 Isotopi; 2.5 Elementi e tavola periodica 2.1 Particelle elementari
Programma svolto nell a.s
 ISTITUTO DI ISTRUZIONE SUPERIORE VIA SILVESTRI, 301 ROMA Sez. associata: I.T.C.G. "Alberto Ceccherelli" - Via di Bravetta, 383 Materia: Scienze Integrate - CHIMICA Docente: De Rosa Giovanna Classe: I Sez.:
ISTITUTO DI ISTRUZIONE SUPERIORE VIA SILVESTRI, 301 ROMA Sez. associata: I.T.C.G. "Alberto Ceccherelli" - Via di Bravetta, 383 Materia: Scienze Integrate - CHIMICA Docente: De Rosa Giovanna Classe: I Sez.:
FISICA QUANTISTICA LIMITI AL MODELLO ATOMICO DI RUTHERFORD. e - Per spiegare la disposizione degli elettroni nell atomo (STRUTTURA ELETTRONICA)
 LIMITI AL MODELLO ATOMICO DI RUTHERFORD e - + nucleo In base alle leggi della FISICA CLASSICA, una particella carica dotata di un movimento circolare libera energia. Di conseguenza, gli elettroni che,
LIMITI AL MODELLO ATOMICO DI RUTHERFORD e - + nucleo In base alle leggi della FISICA CLASSICA, una particella carica dotata di un movimento circolare libera energia. Di conseguenza, gli elettroni che,
Il bosone di Higgs: che cosa è? Come funziona? E a che cosa serve? Stefano Sandrelli INAF Osservatorio Astronomico di Brera
 Il bosone di Higgs: che cosa è? Come funziona? E a che cosa serve? Stefano Sandrelli INAF Osservatorio Astronomico di Brera Riassunto: che cosa è la luce? Onda o par5cella? Il fotone. Natura ondulatoria
Il bosone di Higgs: che cosa è? Come funziona? E a che cosa serve? Stefano Sandrelli INAF Osservatorio Astronomico di Brera Riassunto: che cosa è la luce? Onda o par5cella? Il fotone. Natura ondulatoria
Radiazione e Materia. Insegnamento di Chimica Generale CCS CHI e MAT. Scuola di Ingegneria Industriale e dell Informazione
 Scuola di Ingegneria Industriale e dell Informazione Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Radiazione e Materia Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio
Scuola di Ingegneria Industriale e dell Informazione Insegnamento di Chimica Generale 083424 - CCS CHI e MAT Radiazione e Materia Prof. Dipartimento CMIC Giulio Natta http://iscamap.chem.polimi.it/citterio
Chimica Generale ed Inorganica
 Chimica Generale ed Inorganica Corso di Laurea in Scienze Biologiche (Canale A-L) Docente: Dr.ssa V. Guglielmotti Email: vguglielmotti@unitus.it Testi consigliati. J. Kotz, P. M. Treichel, J. R. Townsend,
Chimica Generale ed Inorganica Corso di Laurea in Scienze Biologiche (Canale A-L) Docente: Dr.ssa V. Guglielmotti Email: vguglielmotti@unitus.it Testi consigliati. J. Kotz, P. M. Treichel, J. R. Townsend,
Unità didattica 10. Decima unità didattica (Fisica) 1. Corso integrato di Matematica e Fisica per il Corso di Farmacia
 Unità didattica 10 Radioattività... 2 L atomo... 3 Emissione di raggi x... 4 Decadimenti nucleari. 6 Il decadimento alfa.... 7 Il decadimento beta... 8 Il decadimento gamma...... 9 Interazione dei fotoni
Unità didattica 10 Radioattività... 2 L atomo... 3 Emissione di raggi x... 4 Decadimenti nucleari. 6 Il decadimento alfa.... 7 Il decadimento beta... 8 Il decadimento gamma...... 9 Interazione dei fotoni
Lezione simulata: il modello atomico di Bohr
 : il modello atomico di Bohr Emanuele Biolcati Prova orale concorso docenti classe A020 18 agosto 2016 Emanuele Biolcati 1 Sommario Introduzione 1 Introduzione Contesto e finalità Modalità di lezione e
: il modello atomico di Bohr Emanuele Biolcati Prova orale concorso docenti classe A020 18 agosto 2016 Emanuele Biolcati 1 Sommario Introduzione 1 Introduzione Contesto e finalità Modalità di lezione e
Esercizi. 1. Fotoni, elettroni. 2. Struttura della materia. 3. Nuclei, radioattività. 4. Produzione e consumo di energia E-X - 0
 Esercizi 1. Fotoni, elettroni 2. Struttura della materia 3. Nuclei, radioattività 4. Produzione e consumo di energia E-X - 0 Calcolare il flusso di fotoni supposti monocromatici a lunghezza d onda di 450
Esercizi 1. Fotoni, elettroni 2. Struttura della materia 3. Nuclei, radioattività 4. Produzione e consumo di energia E-X - 0 Calcolare il flusso di fotoni supposti monocromatici a lunghezza d onda di 450
Theory Italiano (Italy)
 Q3-1 Large Hadron Collider (10 punti) Prima di iniziare questo problema, leggi le istruzioni generali nella busta a parte. In questo problema è discussa la fisica dell acceleratore di particelle del CERN
Q3-1 Large Hadron Collider (10 punti) Prima di iniziare questo problema, leggi le istruzioni generali nella busta a parte. In questo problema è discussa la fisica dell acceleratore di particelle del CERN
TEORIA QUANTISTICA E STRUTTURA ATOMICA
 TEORIA QUANTISTICA E STRUTTURA ATOMICA Gli argomenti di queste lezioni sono trattati nel Capitolo 7 del testo e nei paragrafi 1, e 3 del Capitolo 8. Non ci sono parti da non considerare. La moderna definizione
TEORIA QUANTISTICA E STRUTTURA ATOMICA Gli argomenti di queste lezioni sono trattati nel Capitolo 7 del testo e nei paragrafi 1, e 3 del Capitolo 8. Non ci sono parti da non considerare. La moderna definizione
ATOMI E MOLECOLE. Tutte le varie forme di materia esistenti sono costituite da sostanze semplici (elementi) e da sostanze composte (composti).
 1 ATOMI E MOLECOLE Tutte le varie forme di materia esistenti sono costituite da sostanze semplici (elementi) e da sostanze composte (composti). Un elemento (es. il mercurio) è una sostanza che non può
1 ATOMI E MOLECOLE Tutte le varie forme di materia esistenti sono costituite da sostanze semplici (elementi) e da sostanze composte (composti). Un elemento (es. il mercurio) è una sostanza che non può
Chimica e Propedeutica Biochimica
 Chimica e Propedeutica Biochimica Beatrice Vallone Linda Savino Dipartimento di Scienze Biochimiche Sapienza - Università di Roma E-mail: beatrice.vallone@uniroma.it CHIMICA: STUDIO DELLA MATERIA: Proprietà
Chimica e Propedeutica Biochimica Beatrice Vallone Linda Savino Dipartimento di Scienze Biochimiche Sapienza - Università di Roma E-mail: beatrice.vallone@uniroma.it CHIMICA: STUDIO DELLA MATERIA: Proprietà
Misura del rapporto carica massa dell elettrone
 Relazione di: Pietro Ghiglio, Tommaso Lorenzon Laboratorio di fisica del Liceo Scientifico L. da Vinci - Gallarate Misura del rapporto carica massa dell elettrone Lezioni di maggio 2015 Lo scopo dell esperienza
Relazione di: Pietro Ghiglio, Tommaso Lorenzon Laboratorio di fisica del Liceo Scientifico L. da Vinci - Gallarate Misura del rapporto carica massa dell elettrone Lezioni di maggio 2015 Lo scopo dell esperienza
Sezione d urto Rutherford Esperimento di Geiger e Marsden
 Sezione d urto Rutherford Esperimento di Geiger e Marsden Il modello di atomo proposto da Thomson consisteva in una sfera di carica Ze positiva delle dimensioni atomiche (10-8 cm) entro la quale erano
Sezione d urto Rutherford Esperimento di Geiger e Marsden Il modello di atomo proposto da Thomson consisteva in una sfera di carica Ze positiva delle dimensioni atomiche (10-8 cm) entro la quale erano
Enrico Silva - diritti riservati - Non è permessa, fra l altro, l inclusione anche parziale in altre opere senza il consenso scritto dell autore
 Particelle della presente identiche. opera. Principio di Pauli. 1 Particelle identiche: sommario Finora: proprietà di particella singola. Volendo ottenere il comportamento di più particelle, è necessario
Particelle della presente identiche. opera. Principio di Pauli. 1 Particelle identiche: sommario Finora: proprietà di particella singola. Volendo ottenere il comportamento di più particelle, è necessario
Natura della luce. Qualsiasi tipo di onda è caratterizzato da:
 Natura della luce James C. Maxwell (1831-79) dimostrò che tutte le proprietà note della luce erano spiegabili attraverso un insieme di equazioni basate sull ipotesi che la luce fosse un onda elettromagnetica
Natura della luce James C. Maxwell (1831-79) dimostrò che tutte le proprietà note della luce erano spiegabili attraverso un insieme di equazioni basate sull ipotesi che la luce fosse un onda elettromagnetica
L esperimento di Rutherford
 L esperimento di Rutherford Questa esperienza, che riproduce il famoso esperimento di Ernest Ruthrford del 1909, ha lo scopo di studiare l interazione tra la radiazione α e la materia e in particolare
L esperimento di Rutherford Questa esperienza, che riproduce il famoso esperimento di Ernest Ruthrford del 1909, ha lo scopo di studiare l interazione tra la radiazione α e la materia e in particolare
ESAME DI STATO DI LICEO SCIENTIFICO - SCIENTIFICO TECNOLOGICO 2010 Corso Sperimentale Progetto Brocca Tema di Fisica
 ESAME DI STATO DI LICEO SCIENTIFICO - SCIENTIFICO TECNOLOGICO 2010 Corso Sperimentale Progetto Brocca Tema di Fisica La prova Il candidato svolga una relazione su uno solo dei seguenti due temi, a sua
ESAME DI STATO DI LICEO SCIENTIFICO - SCIENTIFICO TECNOLOGICO 2010 Corso Sperimentale Progetto Brocca Tema di Fisica La prova Il candidato svolga una relazione su uno solo dei seguenti due temi, a sua
Interazione luce- atomo
 Interazione luce- atomo Descrizione semiclassica L interazione predominante è quella tra il campo elettrico e le cariche ASSORBIMENTO: Elettrone e protone formano un dipolo che viene messo in oscillazione
Interazione luce- atomo Descrizione semiclassica L interazione predominante è quella tra il campo elettrico e le cariche ASSORBIMENTO: Elettrone e protone formano un dipolo che viene messo in oscillazione
Fisica delle Apparecchiature per Radioterapia, lez. III RADIOTERAPIA M. Ruspa 1
 RADIOTERAPIA 14.01.11 M. Ruspa 1 Con il termine RADIOTERAPIA si intende l uso di radiazioni ionizzanti altamente energetiche (fotoni X o gamma, elettroni, protoni) nel trattamento dei tumori. La radiazione
RADIOTERAPIA 14.01.11 M. Ruspa 1 Con il termine RADIOTERAPIA si intende l uso di radiazioni ionizzanti altamente energetiche (fotoni X o gamma, elettroni, protoni) nel trattamento dei tumori. La radiazione
Corso di CHIMICA INORGANICA
 Corso di CHIMICA INORGANICA Lezione Seconda La teoria atomica La massa atomica e il concetto di Isotopi Dentro l atomo, le particelle subatomiche La Tavola Periodica degli Elementi 2 Gli atomi di un certo
Corso di CHIMICA INORGANICA Lezione Seconda La teoria atomica La massa atomica e il concetto di Isotopi Dentro l atomo, le particelle subatomiche La Tavola Periodica degli Elementi 2 Gli atomi di un certo
Il Modello Standard delle particelle
 Il Modello Standard delle particelle Vittorio Del Duca INFN LNF Stages Estivi 12 giugno 2012 Elementi La materia è fatta di elementi con definite proprietà chimiche Atomi Ciascun elemento ha come mattone
Il Modello Standard delle particelle Vittorio Del Duca INFN LNF Stages Estivi 12 giugno 2012 Elementi La materia è fatta di elementi con definite proprietà chimiche Atomi Ciascun elemento ha come mattone
Natura ondulatoria della luce. Natura corpuscolare della luce
 Natura ondulatoria della luce Data 1803 Autore Thomas Young Esperimento Un fascio di luce solare viene fatto passare da un foro e davanti a questo foro vi è un pannello con due fenditure verticali (coperte
Natura ondulatoria della luce Data 1803 Autore Thomas Young Esperimento Un fascio di luce solare viene fatto passare da un foro e davanti a questo foro vi è un pannello con due fenditure verticali (coperte
Interferenze quantistiche
 FAM Interferenze quantistiche Christian Ferrari Liceo di Locarno Cenni storici 1 Anni 1920: messa in evidenza di uno strano comportamento degli oggetti del mondo microscopico. Esperienze con la luce in
FAM Interferenze quantistiche Christian Ferrari Liceo di Locarno Cenni storici 1 Anni 1920: messa in evidenza di uno strano comportamento degli oggetti del mondo microscopico. Esperienze con la luce in
L Universo secondo la Fisica moderna
 Jesi 16 aprile 2005 L Universo secondo la Fisica moderna Cesare Bini Universita La Sapienza Roma Come la Fisica del XX secolo ha affrontato il problema dell origine dell Universo e quali sono i problemi
Jesi 16 aprile 2005 L Universo secondo la Fisica moderna Cesare Bini Universita La Sapienza Roma Come la Fisica del XX secolo ha affrontato il problema dell origine dell Universo e quali sono i problemi
Tutorato di Fisica 2 Anno Accademico 2010/2011
 Matteo Luca Ruggiero DIFIS@Politecnico di Torino Tutorato di Fisica 2 Anno Accademico 2010/2011 () 2 1.1 Una carica q è posta nell origine di un riferimento cartesiano. (1) Determinare le componenti del
Matteo Luca Ruggiero DIFIS@Politecnico di Torino Tutorato di Fisica 2 Anno Accademico 2010/2011 () 2 1.1 Una carica q è posta nell origine di un riferimento cartesiano. (1) Determinare le componenti del
LEZIONE 008 Struttura atomica TITOLO: STRUTTURA ATOMICA
 TITOLO: STRUTTURA ATOMICA 1898 Scoperta dell'elettrone (Thomson) 1900 Scoperta del protone (Goldstein) 1900 Teoria dei quanti di Planck 1904 Modello atomico di Thomson modello sferico 1911 modello atomico
TITOLO: STRUTTURA ATOMICA 1898 Scoperta dell'elettrone (Thomson) 1900 Scoperta del protone (Goldstein) 1900 Teoria dei quanti di Planck 1904 Modello atomico di Thomson modello sferico 1911 modello atomico
L atomo di Rutherford e la scoperta del neutrone
 Alla fine dell Ottocento i fisici, come Marie Curie (premio Nobel per la Fisica nel 1903 e per la Chimica nel 1911), Pierre Curie (premio Nobel per la Fisica nel 1903) e Henri Becquerel (premio Nobel per
Alla fine dell Ottocento i fisici, come Marie Curie (premio Nobel per la Fisica nel 1903 e per la Chimica nel 1911), Pierre Curie (premio Nobel per la Fisica nel 1903) e Henri Becquerel (premio Nobel per
Il modello strutturale dell atomo
 Il modello strutturale dell atomo Gli atomi sono costituiti dal nucleo e dagli elettroni Proprietà dell atomo dipendono dal nucleo (fisica nucleare) e dagli elettroni (chimica). Il nucleo contiene protoni
Il modello strutturale dell atomo Gli atomi sono costituiti dal nucleo e dagli elettroni Proprietà dell atomo dipendono dal nucleo (fisica nucleare) e dagli elettroni (chimica). Il nucleo contiene protoni
Lezione 5: Primi modelli atomici
 Corso di Fisica moderna di base Modulo 1: Elementi di Struttura della Materia ATTENZIONE: LE SEGUENTI PAGINE SONO INTESE COME UNO SCHEMATICO RIASSUNTO DI QUANTO TRATTATO IN AULA, NON PRETENDONO DI ESSERE
Corso di Fisica moderna di base Modulo 1: Elementi di Struttura della Materia ATTENZIONE: LE SEGUENTI PAGINE SONO INTESE COME UNO SCHEMATICO RIASSUNTO DI QUANTO TRATTATO IN AULA, NON PRETENDONO DI ESSERE
1. La forza di Lorentz. Se un fascio catodico è in un campo magnetico:
 Il campo magnetico 1. La forza di Lorentz Se un fascio catodico è in un campo magnetico: La forza di Lorentz Gli elettroni risentono di una forza magnetica anche se non sono in un filo metallico; l'importante
Il campo magnetico 1. La forza di Lorentz Se un fascio catodico è in un campo magnetico: La forza di Lorentz Gli elettroni risentono di una forza magnetica anche se non sono in un filo metallico; l'importante
Sommario della lezione 4. Proprietà periodiche. Massa atomica e massa molecolare. Concetto di mole. Prime esercitazioni
 Sommario della lezione 4 Proprietà periodiche Massa atomica e massa molecolare Concetto di mole Prime esercitazioni Proprietà periodiche Il raggio atomico è definito come la metà della distanza minima
Sommario della lezione 4 Proprietà periodiche Massa atomica e massa molecolare Concetto di mole Prime esercitazioni Proprietà periodiche Il raggio atomico è definito come la metà della distanza minima
FISICA E LABORATORIO
 Programma di FISICA E LABORATORIO Anno Scolastico 2014-2015 Classe V P indirizzo OTTICO Docente Giuseppe CORSINO Programma di FISICA E LABORATORIO Anno Scolastico 2013-2014 Classe V P indirizzo OTTICO
Programma di FISICA E LABORATORIO Anno Scolastico 2014-2015 Classe V P indirizzo OTTICO Docente Giuseppe CORSINO Programma di FISICA E LABORATORIO Anno Scolastico 2013-2014 Classe V P indirizzo OTTICO
La Vita è una Reazione Chimica
 La Vita è una Reazione Chimica Acqua Oro Zucchero La vita è una reazione chimica ü ü ü ü ü ü ü ü ü ü Cosa studia la chimica? Classificazione della materia Stati della materia Formule chimiche Atomo Tavola
La Vita è una Reazione Chimica Acqua Oro Zucchero La vita è una reazione chimica ü ü ü ü ü ü ü ü ü ü Cosa studia la chimica? Classificazione della materia Stati della materia Formule chimiche Atomo Tavola
Cos è. la Chimica? G. Micera Chimica Generale e Inorganica
 Cos è la Chimica? La Chimica descrive la materia, le sue proprietà, le trasformazioni che essa subisce, e le variazioni di energia associate Materia è tutto ciò che ha massa e volume Energia è la capacità
Cos è la Chimica? La Chimica descrive la materia, le sue proprietà, le trasformazioni che essa subisce, e le variazioni di energia associate Materia è tutto ciò che ha massa e volume Energia è la capacità
Da Newton a Planck. La struttura dell atomo. Da Newton a Planck. Da Newton a Planck. Meccanica classica (Newton): insieme
 Da Newton a Planck Meccanica classica (Newton): insieme La struttura dell atomo di leggi che spiegano il mondo fisico fino alla fine del XIX secolo Prof.ssa Silvia Recchia Quantomeccanica (Planck): insieme
Da Newton a Planck Meccanica classica (Newton): insieme La struttura dell atomo di leggi che spiegano il mondo fisico fino alla fine del XIX secolo Prof.ssa Silvia Recchia Quantomeccanica (Planck): insieme
Indice. Elettrostatica in presenza di dielettrici Costante dielettrica Interpretazione microscopica 119. capitolo. capitolo.
 Indice Elettrostatica nel vuoto. Campo elettrico e potenziale 1 1. Azioni elettriche 1 2. Carica elettrica e legge di Coulomb 5 3. Campo elettrico 8 4. Campo elettrostatico generato da sistemi di cariche
Indice Elettrostatica nel vuoto. Campo elettrico e potenziale 1 1. Azioni elettriche 1 2. Carica elettrica e legge di Coulomb 5 3. Campo elettrico 8 4. Campo elettrostatico generato da sistemi di cariche
LA STRUTTURA DELL ATOMO 4.A PRE-REQUISITI 4.B PRE-TEST 4.6 ENERGIE DI IONIZZAZIONE E DISTRIBUZIONE DEGLI ELETTRONI 4.C OBIETTIVI
 LA STRUTTURA DELL ATOMO 4.A PRE-REQUISITI 4.B PRE-TEST 4.C OBIETTIVI 4.1 UNO SGUARDO ALLA STORIA 4.2 L ATOMO DI BOHR (1913) 4.5.2 PRINCIPIO DELLA MASSIMA MOLTEPLICITA (REGOLA DI HUND) 4.5.3 ESERCIZI SVOLTI
LA STRUTTURA DELL ATOMO 4.A PRE-REQUISITI 4.B PRE-TEST 4.C OBIETTIVI 4.1 UNO SGUARDO ALLA STORIA 4.2 L ATOMO DI BOHR (1913) 4.5.2 PRINCIPIO DELLA MASSIMA MOLTEPLICITA (REGOLA DI HUND) 4.5.3 ESERCIZI SVOLTI
L Atomo e le Molecole
 L Atomo e le Molecole L atomo L'atomo, la particella che come un mattone costituisce tutta la materia, non è un corpicciolo semplice. Esso è a sua volta composto da particelle elementari piccolissime:
L Atomo e le Molecole L atomo L'atomo, la particella che come un mattone costituisce tutta la materia, non è un corpicciolo semplice. Esso è a sua volta composto da particelle elementari piccolissime:
Struttura elettronica degli atomi. La teoria dei quanti e la meccanica ondulatoria. La moderna descrizione dell atomo
 Struttura elettronica degli atomi La teoria dei quanti e la meccanica ondulatoria La moderna descrizione dell atomo 1 Generalità delle onde elettromagnetiche λ Ampiezza massima: E max (B max ) Lunghezza
Struttura elettronica degli atomi La teoria dei quanti e la meccanica ondulatoria La moderna descrizione dell atomo 1 Generalità delle onde elettromagnetiche λ Ampiezza massima: E max (B max ) Lunghezza
