La chimica organica è la chimica dei composti contenenti carbonio
|
|
|
- Serafina Franchini
- 6 anni fa
- Visualizzazioni
Transcript
1 Chimica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio I carbonati, l anidride carbonica e i cianuri metallici sono un eccezione in quanto vengono classificati come composti inorganici. Il carbonio è l unico elemento capace di legarsi fortemente con se stesso e formare lunghe catene o anelli e allo stesso tempo capace di legarsi fortemente con elementi non metallici come idrogeno, ossigeno, azoto e con gli alogeni. Per queste sue proprietà questo elemento dà origine a miriadi di composti (sono noti diversi milioni di composti, corrispondenti a circa il 98% di tutte le sostanze chimiche note, e il loro numero continua a crescere)
2 Breve storia della chimica organica Il termine chimica organica deriva dal fatto che una volta con questo termine si definivano i composti che potessero essere sintetizzati da organismi viventi, come ad esempio legno, ossa, vestiti, cibi, medicine, e le sostanze complesse che formano il nostro corpo (in antitesi con la chimica inorganica che era quella basata sui composti sintetizzati artificialmente). Questa teoria fu abbandonata nel 1828 quando il chimico tedesco Friedrich Wohler preparò l urea (componente dell urina quindi materiale chiaramento organico) riscaldando un sale inorganico: il cianato di ammonio. T O N 4 OCN 2 N C Fu quindi evidente che una sostanza organica poteva essere sintetizzata anche in laboratorio oltre che da organismi viventi. Nonostante ciò si ritenne opportuno mantenere la vecchia divisione tra materiali organici ed inorganici N 2
3 Campi di interesse della chimica organica Visto l elevatissimo numero di composti organici esistenti, la chimica organica riveste un ruolo fondamentale in innumerevoli campi. In particolare, la chimica organica svolge un ruolo fondamentale per la comprensione dei sistemi viventi. Come detto in precedenza gli organismi viventi sono composti principalmente da molecole organiche e i meccanismi che permettono a questi organismi di sopravvivere e riprodursi, possono essere scomposti in una serie di semplici reazioni di chimica organica. La chimica organica e stata quindi fondamentale per capire i processi biologici e per sintetizzare farmaci. Un altro importante campo di applicazione della chimica organica è nella sintesi dei materiali polimerici. I polimeri (o materie plastiche) sono infatti delle molecole organiche e i processi di sintesi (polimerizzazione) sono delle reazioni di chimica organica. I composti del carbonio (in particolare quelli ottenuti dal petrolio) svolgono inoltre un ruolo fondamentale nel soddisfare il nostro fabbisogno energetico (riscaldamento, trasporti, illuminazione..)
4 Nomenclatura Chimica organica Nomi tradizionali e nomi IUPAC: In passato si assegnavano i nomi alle molecole organiche in base alla loro origine o a certe proprietà. Per esempio l acido citrico deriva dal fatto che si trova nel frutto del cedro, l acido formico è sintetizzato dalle formiche o la morfina induce il sonno (da Morpheus dio greco del sonno). Visto l enorme numero di composti organici che sono stati successivamente scoperti, è stato necessario creare una nomenclatura sistematica che potesse permettere una facile ed univoca identificazione di ogni molecola organica. Le regole generali di questa nomenclatura sono state codificate dalla International Union of Pure and Applied Chemistry (IUPAC). Per molti composti (in particolare quelli di uso più comune) viene ancora utilizzato anche in campo scientifico il nome tradizionale accanto alla nomencaltura IUPAC.
5 In queste lezioni verranno prima descritti gli idrocarburi alifatici e aromatici e successivamente verranno descritti tutti gli altri composti come derivati di queste molecole più semplici, per ogni classe di composti verranno descritte : la formula generale,(di struttura e struttura semplificata) la nomenclatura, Proprietà (ibridazione C, solubilità, isomerie ) le reazioni principali (preparazione e reazioni) usi in medicina
6 Nomenclatura IUPAC degli Alcani vedi file a parte n 15a Sono elencate di seguito alcune delle regole principali, definite dalla IUPAC (International Union of Pure and Applied Chemistry) per la nomenclatura degli alcani: 1. Si sceglie come struttura base la catena più lunga possibile. 2. Si considera il composto come derivato da questa struttura per sostituzione degli atomi di idrogeno con gruppi alchilici. [Si dicono alchilici quei gruppi che contengono un idrogeno in meno del relativo alcano. Il nome di questi gruppi si ottiene semplicemente sostituendo con -ile il suffisso -ano dell'alcano corrispondente: C 3 -, metile; C 3 -C 2 -, etile; C 3 -C 2 -C 2 -, propile; ecc.] 3. Si numerano gli atomi di carbonio della catena principale cominciando dall'estremità che permette di usare i numeri più bassi per indicare i sostituenti. 4. Se lo stesso gruppo compare più di una volta come catena laterale, si aggiunge il prefisso di-, tri-, tetra-, ecc. 5. Se vi sono gruppi alchilici diversi legati alla catena principale si elencano in ordine di alfabetico (prima gli etili poi i metili, i propili,, ecc.). 6. I nomi IUPAC siscrivono in un unica parola, i numeri sepatrati da virgole mentre numero e lettera da un trattino es. 2,3,5- trimetileptano 7. Se ci sono due ramificazioni la numeraqzione inizia dall estremità più vicina al sostituente che viene per primo in ordine alfabetico
7 Elettrofili e Nucleofili Elettrofilo: Si definisce elettrofilo un atomo, uno ione o una molecola elettron-deficiente (quindi positivo o parzialmente positivo)) che mostra affinità per una coppia elettronica e che perciò cercherà di legarsi ad un nucleofilo Nucleofilo: Si definisce nucleofilo un atomo, ione o molecola che possiede una coppia di elettroni (quindi negativo parzialmentenegativo)che può impegnare nella formazione di un legame chimico per reazione con un elettrofilo
8 Le molecole polarizzate reagiscono con reattivi di carica opposta NUCLEOFILO Y d+ C Se la molecola ha una parziale carica positiva, reagirà con reattivi che hanno elettroni disponibili, i reattivi NUCLEOFILI X ELETTROFILO + R d- O Se la molecola ha una parziale carica negativa, reagirà con reattivi che hanno carica positiva, i reattivi ELETTROFILI
9 Classificazione degli atomi di carbonio È spesso utile classificare un atomo di carbonio di un alcano in base al numero di altri atomi di carbonio a cui è legato. Un atomo di carbonio potrà quindi essere detto: primario, secondario, terziario o quaternario, a seconda che leghi uno, due, tre o quattro altri atomi di carbonio.
10 In chimica organica, si definisce carbocatione uno ione positivo, derivato da una molecola organica, la cui carica risiede su un atomo di carbonio. La carica elettrica positiva rende la particella estremamente reattiva, in grado di legarsi ad anioni o di sottrarre elettroni da altre molecole vicine. I carbocationi alchilici derivano dagli alcani ed hanno una geometria simile a quella dei radicali alchilici: l'atomo di carbonio che reca la carica positiva ha ibridazione sp 2, ha quindi struttura planare, l'orbitale p perpendicolare al piano del carbocatione, non coinvolto
11 Carbocatione modello del carbocatione metile, l'ombreggiatura rappresenta l'orbitale p vuoto nell'ibridazione, è vuoto. Similmente ai radicali, sono detti primari i carbocationi alchilici aventi struttura R- C 2+, secondari quelli aventi struttura R 2 C + e terziari quelli aventi struttura R 3 C +.
12 C 3 -C 2 -C 2 -C + 2 carbocatione primario C 3 -C 2 - C-C 3 carbocatione secondario + + C 3 - C -C 3 carbocatione terziario I C 3 Il carattere primario, secondario o terziario influisce sulla stabilità e sulla reattività carbocationi in misura ancora maggiore a quanto avviene per i corrispondenti radicali. A causa dell'effetto induttivo stabilizzante esercitato dai gruppi R vicini, l'ordine di stabilità dei carbocationi alchilici è + terziario > secondario > primario + stabile - stabile I carbocationi possono essere anche stabilizzati per risonanza, quando sono coniugati a sistemi π quali doppi legami o anelli aromatici. C 2 =C-C 2 +. C 2 -C=C 2 carbocatione allilico C 6 5 -C 2 + carbocatione benzilico
13 Processi Omolitici ed Eterolitici Rottura di un Legame Formazione di un Legame
14 Basicità e Nucleofilicità Base I (-) Cl (-) 2 O C 3 CO 2 (-) RS (-) CN (-) RO (-) N 2 (-) C 3 (-) Acido Coniugato I Cl 3 O (+) C 3 CO 2 RS CN RO N 3 C 4 pk a
15 Nucleophilicity: C 3 CO 2 (-) < Cl (-) < Br (-) < N 3 (-) < C 3 O (-) < CN (-) < I (-) < C 3 S (-)
16 Equilibrio e Velocità di una Reazione aa + bb cc + dd K eq. = [C]c [D] d [A] a [B] b E = 0, K eq. =1 E > 0, K eq. <1 V= cost.e - E /RT. K eq. = e - E/RT E < 0, K eq. >1 Reazione ad un singolo stadio, endotermica Reazione ad un singolo stadio, esotermica Reazione a due stadi, esotermica
17 Idrocarburi Sono i composti organici binari, costituiti solo da Carbonio e Idrogeno Saturi alcani Idrocarburi Alifatici Insaturi alcheni alchini Aromatici Idrocarburi saturi: presentano esclusivamente legami singoli carbonio-carbonio Idrocarburi insaturi: contengono almeno un legame multiplo carbonio-carbonio
18 Idrocarburi saturi: alcani Ogni atomo di carbonio ha ibridazione sp 3 ed è legato a 4 atomi mediante legami s. Insolubili in acqua La famiglia degli alcani costituisce una serie omologa cioè una serie di composti dove ogni membro differisce dal successivo di un termine costante C 2 detto gruppo metilene Formula generale degli alcani: C n 2n+2 (n > 1) Se o < n > 4 = gas 5 < n>18 liquido n> 18 solido n=1 C 4 C 4 metano n=2 C 2 6 C 3 -C 3 etano n=3 C 3 8 C 3 -C 2 -C 3 propano n=4 C 4 10 C 3 -C 2 -C 2 -C 3 butano
19 Alcani: struttura tetraedrica del carbonio Rappresentazione tridimensionale della molecola di C 4. Dalla teoria è prevedibile che la geometria imposta dalle coppie elettroniche attorno all atomo di carbonio centrale del C 4 sia tetraedrica e può essere descritta in termini di un atomo di carbonio che lega quattro atomi di idrogeno con ibridazione sp C Struttura tetraedrica che mostra l angolo di Modello per la rappresentazione legame planare Modello ball and stick Modello space filling
20 Alcani: rotazione intorno al legame s La rotazione lungo l asse carbonio-carbonio non influenza la sovrapposizione dei due orbitali sp 3 che formano il legame carbonio-carbonio e quindi non modifica l energia di legame. Per questo motivo la rotazione intorno all asse C-C è libera.
21 Ricordiamo!! Definizione di isomero Si definiscono isomeri due o più molecole aventi stessa formula molecolare ma differente formula di struttura. Esistono vari tipi di isomeria: Costituzionale o Strutturale: gli atomi di carbonio sono legati tra di loro in maniera differente (per esempio isobutano e normalbutano).(cambia l ordine) Stereoisomeria: gli stereoisomeri presentano gli stessi legami ma differiscono per il modo in cui gli atomi sono orientati nello spazio. Esistonoi due tipi di stereoisomeria :Isomeria Conformazionale e Configurazionale Abbiamo. isomeri conformazionali gli isomeri che possono trasformarsi l uno nell altro senza la rottura di legami (per esempio le diverse conformazioni anti e gauche del n-butano). Isomeria Configurazionale si divide in Si chiamano isomeri geometrici i diastereoisomeri che debbono la loro esistenza alla mancanza di libera rotazione intorno ai doppi legami (isomeria cis/trans nel 2-butene). Si chiamano isomeri ottici ( legata all atomo di C asimmetrico)gli isomeri che non sono sovrapponibili alla loro immagine speculare.( enantiomeri) Per trasformare uno stereoisomero nell altro è necessario rompere e riformare almeno un legame. Si chiamano diastereoisomeri gli stereoisomeri che non sono uno l immagine speculare dell altro
22 Conformazioni degli alcani La barriera di energia per passare da una conformazione all altra è di circa 3kcal/mol e di conseguenza può avvenire con velocità alta già a temperatura ambiente
23 Conformazioni degli alcani Le conformazioni A e B sono dette gauche e presentano un angolo diedro tra gruppi metilici di 60, mentre la conformazione C è detta anti e presenta un angolo di 180. La conformazione anti è più stabile delle gauche di circa 0,9 kcal/mol a causa delle minori interazioni repulsive tra i gruppi metilici.
24 Alcani: isomeri di struttura Per n>3 esistono più isomeri di struttura. Le diverse strutture di queste molecole portano a differenti proprietà chimiche e fisiche Modello ball and sticks Modello space filling n-butano C 3 C 2 C 2 C 3 isobutano C 3 C C 3 C 3 Gli alcani a catena lineare sono chiamati normali (n-). Gli altri sono detti ramificati
25 Nomenclatura degli alcani Gli alcani con n< 4 hanno nomi particolari Per n>4 il nome degli alcani si ottiene aggiungendo il suffisso - ano alla radice greca del numero di atomi di carbonio (pent- per cinque, es- per sei etc.). Per un idrocarburo ramificato la radice del nome è determinata dalla catena più lunga di atomi di carbonio 6 atomi di C esano Quando gli alcani fungono da sostituenti essi vengono denominati sostituendo il suffisso - ano con il suffisso -il. Sono chiamati gruppi alchilici. C 3 C 2 C 2 C 3 C 2 C C 2 C 3 C 3 C 2 C 3 C 2 C 2 C 3 C 3 C C 3 metil etil propil isopropil
26 Nomenclatura degli alcani La posizione dei sostituenti è specificata numerando la catena più lunga in modo essi abbiano il numero più piccolo C C 3 C 2 C C 2 C C 2 C etilesano Quando sono presenti diversi sostituenti vanno elencati in ordine alfabetico usando i prefissi di-, tri-, etc. per indicare la presenza di sostituenti uguali 2 1 Numerazione corretta Numerazione non corretta
27 Cicloalcani Oltre a formare catene, gli atomi di C possono formare degli anelli. I cicloalcani sono anelli formati esclusivamente da gruppi C 2 Formula generale dei cicloalcani: C n 2n (n > 3) C C C Il più semplice è il ciclopropano C 3 6 in cui gli atomi di C formano un triangolo equilatero con angoli di 60 ; gli orbitali ibridi sp 3 non si sovrappongono estesamente e ciò provoca un legame C-C debole ed in tensione e la molecola è molto più reattiva del propano. Analogamente si comporta il ciclobutano (angoli di 90 ). Al contrario il cicloepentano e il cicloesano sono abbastanza stabili perché i loro anelli hanno angoli di legame più vicini all angolo del tetraedro. (TEORIA DELLE TENSIONI DI LEGAME) Reazioni : di addizione fino a n=4 poi sostituzione Il ciclopropano veniva usato in medicina come anestetico generale N.B. è esplosivo!
28 Cicloalcani condensati I più importanti nel nostro organismo derivano dal ciclopentanoperidrofenantrene (es colesterolo)
29 Cicloalcani: nomenclatura La nomenclatura segue le stesse regole adottate per gli alcani. Si premette il prefisso ciclo- e l anello viene numerato in modo da avere i numeri più bassi per i sostituenti. C 2 C C 3 1-etil-3-metilcicloesano
30 La Conformazione del Ciclopropano
31 Cicloesano: strutture a barca e sedia Questi due protoni tendono a respingersi Conformazione a barca Conformazione a sedia Non si hanno interazioni tra protoni e di conseguenza questa è la forma più stabile Gli idrogeni in rosso sono detti equatoriali mentre quelli in blu sono detti assiali
32 Le Principali Conformazioni dell'anello del Cicloesano
33 Nomenclatura dei CicloAlcani Semplici Nome Ciclopropano Ciclobutano Ciclopentano Cicloesano Cicloeptano Cicloalcano Formula Molecolare C 3 6 C 4 8 C 5 10 C 6 12 C 7 14 C n 2n Struttura Condensata (C 2 ) n Struttura Lineare La Nomenclatura dei cicloalcani non sostituiti è molto semplice: basta mettere il prefisso "ciclo"prima del nome dell'alcano con il corrispondente numero di atomi di carbonio
34 Reazioni degli alcani Gli alcani sono poco reattivi ma possono reagire ad alta temperatura Reazione di combustione: Reazione tra l alcano ed ossigeno con formazione di CO 2 e 2 O. Reazione esotermica. C 4 10(g) + 13/2 O 2 4 CO O + cal Reazioni di sostituzione radicalica hn C 4 + Cl 2 C 3 Cl + Cl clorometano hn C 3 Cl + Cl 2 C 2 Cl 2 + Cl diclorometano (clouro di metilene) hn C 2 Cl 2 + Cl 2 CCl 3 + Cl triclorometano (cloroformio) hn CCl 3 + Cl 2 CCl 4 + Cl tetraclorometano La reazione avviene con un meccanismo di SOSTITUZIONE radicalica: Cl 2 hn 2Cl Il Cl è molto reattivo e capace di attaccare il legame C-
35 Alcani - reazioni In particolare la reazione di Combustione: C 3 -C 2 -C O 2 > 3 O=C=O O + calore Due punti importanti riguardanti questa reazione: (1) Poichè tutti i legami covalenti presenti nella molecola di reagente vengono rotti, la quantità di calore svolto dipende dal numero e dalla forza di questi legami. (2) La stechiometria dei reagenti è molto importante. Se è presente una quantità di ossigeno insufficiente, nei prodotti di reazione sarà presente anche monossido di carbonio, un gas altamente tossico. C 3 -C 2 -C O 2 > O=C=O + 2 CO O + calore
36 Meccanismo della SOSTITUZIONE Radicalica degli Alcani
37 First step Meccanismo della Bromurazione Radicalica R Br R C R -Br Second step R Br-Br R C R Br
38 Utilizzi degli alcani USI IN MEDICINA = gli alcani sono poco reattivi e incopatibili con la vita cellulare Da ricordare il ciclopropano come anestetico generale
39 Idrocarburi insaturi: alcheni Gli alcheni sono idrocarburi con un legame doppio C=C dovuto all ibridazione sp 2. Formula generale degli alcheni: C n 2n (n > 2) La nomenclatura è simile a quella degli alcani: Il nome di base dell idrocarburo finisce in -ene Il doppio legame è indicato dall atomo di Carbonio a numerazione più bassa C 2 C C 2 C 3 1-butene 6 3 C C 3 C C C 3 5 C 2 4 C C 2 C C C 3 2-butene 4-metil-cis-2-esene
40 Idrocarburi insaturi: alcheni Orbitali molecolari dell etilene Negli alcheni i carboni dei doppi legami presentano ibridazione sp 2. Il legame s C-C è formato per accoppiamento di due elettroni presenti negli orbitali sp 2 e il legame p per accoppiamento di elettroni p. I due orbitali p sui due atomi di carbonio dell etilene devono essere allineati (paralleli) per poter formare legami p. Questo impedisce la rotazione dei due gruppi C 2 l uno rispetto all altro a temperatura ordinaria, contrariamente agli alcani per i quali è possibile la libera rotazione.
41 Alcheni: isomeria cis/trans Attorno agli atomi di C uniti mediante il doppio legame la rotazione è impedita. Ciò comporta il manifestarsi dell isomeria geometrica. Ad esempio il 2-butene esiste in due isomeri geometrici. Cis 2-butene C 3 C=C C 3 C 3 C 3 C=C Trans 2-butene
42 Idrocarburi insaturi: alchini Gli alcheni sono idrocarburi con un legame triplo carbonio carbonio dovuto all ibridazione sp. Formula generale degli alchini: C n 2n-2 (n > 2) La nomenclatura fa uso del suffisso -ino ed è analoga a quella degli alcheni C 3 C 2 C C C C 2 C 2 C 3 C 3 5-etil-3-eptino Anche gli idrocarburi insaturi possono esistere in strutture cicliche
43 Idrocarburi insaturi: alchini Orbitali molecolari dell acetilene Negli alchini i carboni del triplo legame presentano ibridazione sp. Il legame s C-C è formato per accoppiamento di due elettroni presenti negli orbitali sp e i 2 legami p per accoppiamento di due coppie di elettroni p. Analogamente agli alcheni, anche per gli alchini la rotazione intorno all asse C-C è impedita a temperatura ordinaria.
44 Reazioni di alcheni e alchini Le principali reazioni sono reazioni di addizione elettrofila con rottura di legami π che sono più deboli dei legami s. Gli elettroni π esercitano nel legame un'azione molto minore degli elettroni σ e inoltre si trovano ad una distanza maggiore dal nucleo: sono quindi meno saldamente legati e perciò più disponibili per un reattivo alla ricerca di elettroni. Il doppio legame risulta, in definitiva, una «sorgente di elettroni»; Le più importanti sono: Addizione di 2 Reazioni di idrogenazione Addizione di alogeni Reazioni di alogenazione Pt C 2 C C C 3 C 2 C 3 Pt C 2 C C 2 C + 3 Br C C 2 2 C 2 C 3 Addizione di acqua Reazione di idratazione Br Br Addizione di Acidi Un altra importante reazione degli idrocarburi insaturi è la reazione di polimerizzazione. Tra gli esempi più importanti di polimeri ottenibili da idrocarburi insaturi ci sono il polietilene, il polipropilene, il polibutadiene e il polistirene. n C 2 C 2 cat. C 2 C 2 n
45 Il meccanismo della reazione di addizione elettrofila a: Alcheni simmetrici Alcheni asimmetrici (regola di Markovnikov) Teoria del carbocatione (spiegazione della regola di Markovnikov)
46 MECCANISMO dell Addizione Elettrofila agli alcheni simmetrici C C + + C + 1 o Stadio C + + Br - C C Br 2 o Stadio La reazione di addizione all'etene non richiede particolari commenti: i due atomi di carbonio impegnati nel doppio legame sono infatti perfettamente equivalenti e avremo comunque un unico prodotto. Non è così nel caso di un termine superiore all'etene, qualora i due atomi di carbonio insaturi si trovino in una "condizione elettronica" diversa
47 Orientazione nelle Reazioni di Addizione agli Alcheni: La regola di Markovnikov C C + Cl Cl C C C Cl C 3 C 3 C 3 C Propene 2-Cloropropano 1-Cloropropano non si forma In questi casi, la reazione di addizione segue la regola di Markovnikov Nell'addizione ad un doppio legame carbonio-carbonio, l'addendo positivo (generalmente un protone) si lega al carbonio che ha già il maggior numero di idrogeni legati a sé». La regola di Markovnikov trova giustificazione nella stabilità del carbocatione che compare come intermedio nella reazione di addizione.
48 Razionalizzazione della Regola di Markovnikov No favored Ogni considerazione sulla stabilità deve essere basata sull'intensità della carica del carbocatione: più la carica è intensa, maggiore è l'energia potenziale della molecola, minore la sua stabilità. Poiché il carbocatione secondario porta due gruppi alchilici sul carbonio che ospita la carica positiva, questa sarà più "indebolita" e quindi meno intensa che nel carbocatione primario. Il carbocatione secondario è dunque più stabile ed è quello su cui andrà ad addizionarsi l'addendo negativo (o la base) nella reazione di addizione.
49 L'addizione elettrofila ad un doppio legame carbonio-carbonio implica la formazione del carbocatione intermedio più stabile e cioè dell'ordine maggiore possibile
50 Addizione di acqua Tra le reazioni di addizione al doppio legame, ne ricorderemo una che ha un particolare interesse biochimico: l'addizione di acqua. Gli alcheni sono inerti rispetto all'acqua pura: la dissociazione in 3 O + e O - è infatti troppo piccola (10-7 M) per poter dar luogo a reazioni elettrofile. In ambiente acido, la reazione di addizione invece avviene, con formazione di un alcol, secondo il consueto meccanismo e in accordo con la regola di Markovnikov Con etene si ottiene etanolo (alcol etilico), con propene 2-propanolo Prova a fare la reazione
51 Stato di ossidazione del C (abituarsi a vedere in quale stato di ossidazione è il carbonio) C 4 R C 3 R C 2 C 2 O R C O C=O R C O O C02
52 Formule di risonanza: si ha risonanza quando una molecola può essere rappresentata da due o più strutture ad energia simile che si differenziano solo per la disposizione degli elettroni Idrocarburi aromatici Orbitali molecolari del benzene Regola di uckel i composti aromatici devono avere 4n + 2 elettroni p o Un numero dispari di doppietti Gli elettroni p sono delocalizzati su tutto l anello
53 Idrocarburi aromatici
54 La completa delocalizzazione dei sei elettroni in un unico orbitale contenente sei elettroni è rappresentato graficamente con un anello interno all esagono nei cui vertici sono collocati i sei atomi di carbonio. a b
55 Il benzene risuona fra le due forme limite. Il passaggio dall una forma all altra si verifica per semplice spostamento di cariche elettriche.
56 Nel benzene tutti gli atomi di carbonio hanno ibridazione sp 2 degli orbitali di valenza. I sei orbitali p z paralleli non ibridati di ciascuno dei sei atomi di carbonio contengono un elettrone
57 I 10 carboni del naftalene sono tutti ibridati sp 2 e ciascuno di essi contribuisce con 1 elettrone alla aromaticità dell idrocarburo
58 Regola di uckel per prevedere il comportamento aromatico di composti ciclici e - p = 4n + 2 o un numero dispari di doppietti n = serie dei numeri naturali n e-p
59 Composti aromatici policiclici benzene naftalene antracene fenantrene
60 ciclooctatetraene Esempi di composti non aromatici
61 ETEROCICLICI AROMATICI furano piridina Benzene + Pirrolo tiofene indolo pirrolo imidazolo Pirimidina + Imidazolo purina
62 o-diclorobenzene m-diclorobenzene p-diclorobenzene Idrocarburi aromatici: nomenclatura La nomenclatura dei derivati del benzene è simile a quella usata per i sistemi ciclici saturi. In presenza di più sostituenti la loro posizione è indicata con i numeri Si possono anche usare i prefissi orto- (o-) meta- (m-) para- (p-) Cl Cl Cl Cl sostituenti adiacenti sostituenti distanziati da un atomo di C sostituenti contrapposti Cl 1 2 1,2-diclorobenzene Cl Cl Cl
63 Idrocarburi aromatici: nomenclatura Alcuni derivati del benzene hanno nomi tradizionali. Tra questi i più importanti sono: C 3 C 3 metilbenzene (toluene) 1,4-dimetilbenzene (para-xilene) C 3 Il benzene è la molecola aromatica più semplice; sistemi più complessi possono essere visti come degli anelli benzenici fusi. Queste molecole sono dette composti aromatici ad anelli condensati naftalene antracene fenantrene Quando il benzene funge da sostituente è detto gruppo fenile.
64 Reazioni del benzene Reazioni del benzene Il benzene non dà reazioni di addizione poiché queste lo trasformerebbero in un prodotto meno stabile, distruggendo il sistema aromatico dell'anello. Il prodotto avrebbe cioè un'energia potenziale maggiore del reagente. Per fare un'addizione sul benzene occorre fornire molta energia (condizioni piuttosto drastiche); di conseguenza non è possibile alcun controllo della reazione. Infatti, una volta iniziata l'addizione, il prodotto (diene) si trova ad un livello energetico molto più alto del benzene (è più instabile e molto più reattivo) e poiché trova le condizioni per reagire ancora, si trasforma direttamente in un composto ciclico saturo, che è ad un livello energetico inferiore rispetto al diene (o all'alchene) intermedio. In definitiva, qualsiasi reazione di addizione sul benzene porta alla saturazione di tutti i legami p. Il benzene tende a dare piuttosto reazioni di sostituzione
65 Analogamente agli alcheni, per il fatto di avere una nuvola elettronica p delocalizzata, il benzene si comporta come una base. Le sostituzioni che tenderà a dare saranno quindi di tipo elettrofilo, cioè con reagenti alla ricerca di elettroni Le reazioni di sostituzione tipiche del benzene sono: 1. nitrazione 2. solfonazione 3. alogenazione 4. alchilazione 5. acilazione
66 Il meccanismo di reazione della sostituzione elettrofila è rappresentato di seguito: 1. Il sostituente elettrofilo si avvicina all'anello lateralmente rispetto al piano della molecola. 2. Si ha una azione di richiamo sugli elettroni p del benzene e uno dei legami p si polarizza in modo da consentire 3. l'attacco del sostituente, che sfrutta una coppia di elettroni p per legarsi Si forma un intermedio instabile, detto complesso s, al quale contribuiscono tre differenti forme risonanti (4,5,6). L'atomo che ha subito l'attacco ha cambiato il suo stato di ibridazione da sp 2 a sp 3, per cui esso è escluso dalla "coniugazione" col resto del sistema. Anche se si può ancora parlare di risonanza, non si può più parlare di aromaticità. 7. L'energia di risonanza di questo catione non è elevata come quella del benzene; l'espulsione di un protone può tuttavia riportare il complesso s alle condizioni di aromaticità. 8. Si ottiene così il prodotto sostituito finale.
67 Meccanismo generale di sostituzione elettrofila aromatica addizione elettrofila eliminazione Carbocatione arilico stabilizzato per risonanza
La chimica organica è la chimica dei composti contenenti carbonio
 Chimica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio I carbonati, il biossido di carbonio e i cianuri metallici sono un eccezione in quanto vengono classificati
Chimica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio I carbonati, il biossido di carbonio e i cianuri metallici sono un eccezione in quanto vengono classificati
Chimica Organica. Breve storia della chimica organica
 Chimica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio I carbonati, il biossido di carbonio e i cianuri metallici sono un eccezione in quanto vengono classificati
Chimica Organica Definizione La chimica organica è la chimica dei composti contenenti carbonio I carbonati, il biossido di carbonio e i cianuri metallici sono un eccezione in quanto vengono classificati
CHIMICA ORGANICA CHIMICA DEL CARBONIO
 CHIMICA ORGANICA CHIMICA DEL CARBONIO Fino al 1828 con il termine organico si indicavano le sostanze prodotte dagli organismi viventi, mentre si classificavano come inorganiche tutte le altre Dopo il 1828
CHIMICA ORGANICA CHIMICA DEL CARBONIO Fino al 1828 con il termine organico si indicavano le sostanze prodotte dagli organismi viventi, mentre si classificavano come inorganiche tutte le altre Dopo il 1828
PERCHE STUDIARE LA CHIMICA ORGANICA?
 CIMICA ORGANICA CE COSA E LA CIMICA ORGANICA? La chimica organica è dedicata alla descrizione della struttura, delle proprietà e delle funzioni dei composti del carbonio (C). PERCE STUDIARE LA CIMICA ORGANICA?
CIMICA ORGANICA CE COSA E LA CIMICA ORGANICA? La chimica organica è dedicata alla descrizione della struttura, delle proprietà e delle funzioni dei composti del carbonio (C). PERCE STUDIARE LA CIMICA ORGANICA?
Alcani e cicloalcani. Nomenclatura e nomi comuni Struttura e proprietà Reazioni
 Alcani e cicloalcani Nomenclatura e nomi comuni Struttura e proprietà Reazioni Alcani Gli orbitali atomici hanno forme ben definite. Gli orbitali S sono sferici con gli e - confinati in una regione sferica
Alcani e cicloalcani Nomenclatura e nomi comuni Struttura e proprietà Reazioni Alcani Gli orbitali atomici hanno forme ben definite. Gli orbitali S sono sferici con gli e - confinati in una regione sferica
Teoria degli orbitali. Lo spazio intorno al nucleo in cui è possibile trovare con la massima probabilità gli elettroni viene chiamato orbitale.
 Teoria degli orbitali Lo spazio intorno al nucleo in cui è possibile trovare con la massima probabilità gli elettroni viene chiamato orbitale. orbitale nucleo STPA-Chimica Organica 1 L orbitale 1s Gli
Teoria degli orbitali Lo spazio intorno al nucleo in cui è possibile trovare con la massima probabilità gli elettroni viene chiamato orbitale. orbitale nucleo STPA-Chimica Organica 1 L orbitale 1s Gli
IDROCARBURI I ALCANI ANALISI CONFORMAZIONALE
 IDROCARBURI I ALCANI NOMENCLATURA ANALISI CONFORMAZIONALE REAZIONI GLI IDROCARBURI CONTENGONO SOLO CARBONIO ED IDROGENO VENGONO DISTINTI IN TRE CLASSI 1. SATURI: SOLO LEGAMI SEMPLICI C-C SE SATURI ED ACICLICI:
IDROCARBURI I ALCANI NOMENCLATURA ANALISI CONFORMAZIONALE REAZIONI GLI IDROCARBURI CONTENGONO SOLO CARBONIO ED IDROGENO VENGONO DISTINTI IN TRE CLASSI 1. SATURI: SOLO LEGAMI SEMPLICI C-C SE SATURI ED ACICLICI:
IDROCARBURI. Alcani Alcheni Alchini C-C C=C C C
 IDROCARBURI Alcani Alcheni Alchini C-C C=C C C Nomenclatura Degli idrocarburi saturi (Alcani) CH 4 Metano C 2 H 6 Etano C n H 2n+2 Si dicono alchilici quei gruppi che contengono un idrogeno in meno del
IDROCARBURI Alcani Alcheni Alchini C-C C=C C C Nomenclatura Degli idrocarburi saturi (Alcani) CH 4 Metano C 2 H 6 Etano C n H 2n+2 Si dicono alchilici quei gruppi che contengono un idrogeno in meno del
Alcheni: struttura e reattività
 Alcheni: struttura e reattività Alcheni Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n H 2n Alcheni in biologia ormone delle piante che induce la maturazione dei frutti costituente
Alcheni: struttura e reattività Alcheni Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n H 2n Alcheni in biologia ormone delle piante che induce la maturazione dei frutti costituente
Alchini (C n H 2n-2 ) Alcheni: idrocarburi insaturi con uno o più legami carbonio-carbonio doppi.
 himica rganica Alcheni Idrocarburi ( x y ) Alifatici Aromatici Alcani ( n 2n+2 ) Alcheni ( n 2n ) Alchini ( n 2n-2 ) icloalcani ( n 2n ) Alcheni: idrocarburi insaturi con uno o più legami carbonio-carbonio
himica rganica Alcheni Idrocarburi ( x y ) Alifatici Aromatici Alcani ( n 2n+2 ) Alcheni ( n 2n ) Alchini ( n 2n-2 ) icloalcani ( n 2n ) Alcheni: idrocarburi insaturi con uno o più legami carbonio-carbonio
Chimica Organica. In passato, i composti chimici erano suddivisi in due grandi gruppi,
 Chimica Organica In passato, i composti chimici erano suddivisi in due grandi gruppi, inorganici e organici, in base alla loro origine. La chimica organica diveniva così la chimica dei composti del carbonio.
Chimica Organica In passato, i composti chimici erano suddivisi in due grandi gruppi, inorganici e organici, in base alla loro origine. La chimica organica diveniva così la chimica dei composti del carbonio.
Alcheni: struttura e reattività
 Alcheni: struttura e reattività Alcheni Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n 2n Alcheni in biologia ormone delle piante che induce la maturazione dei frutti costituente
Alcheni: struttura e reattività Alcheni Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n 2n Alcheni in biologia ormone delle piante che induce la maturazione dei frutti costituente
Alcheni: : struttura e reattività. Alcheni. Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n. H 2n. Alcheni in biologia
 Alcheni: : struttura e reattività Alcheni Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n H 2n Alcheni in biologia ormone delle piante che induce la maturazione dei frutti costituente
Alcheni: : struttura e reattività Alcheni Gli alcheni sono detti anche olefine e sono idrocarburi insaturi C n H 2n Alcheni in biologia ormone delle piante che induce la maturazione dei frutti costituente
COMPOSTI AROMATICI. Formula C 6 H 6
 COMPOSTI AROMATICI Gli alcani ed alcheni hanno diversa reattività chimica. Vi è un altra classe di idrocarburi che pur essendo insaturi hanno un comportamento chimico diverso dagli alcheni Sono i composti
COMPOSTI AROMATICI Gli alcani ed alcheni hanno diversa reattività chimica. Vi è un altra classe di idrocarburi che pur essendo insaturi hanno un comportamento chimico diverso dagli alcheni Sono i composti
Classificazione degli idrocarburi
 Classificazione degli idrocarburi ALCANI Alcani: idrocarburi saturi contenenti solo legami semplici carbonio-carbonio (tutti i carboni sono ibridati sp3). Modelli molecolari di etano, propano e butano.
Classificazione degli idrocarburi ALCANI Alcani: idrocarburi saturi contenenti solo legami semplici carbonio-carbonio (tutti i carboni sono ibridati sp3). Modelli molecolari di etano, propano e butano.
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA)
 La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) IL CARBONIO E un non metallo, appartiene al IV gruppo ed al II periodo. Possiede 4 elettroni esterni per
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) IL CARBONIO E un non metallo, appartiene al IV gruppo ed al II periodo. Possiede 4 elettroni esterni per
IBRIDAZIONE DEL CARBONIO NEGLI ALCANI PREMESSA: COSA SONO GLI ORBITALI IBRIDI.
 ALCANI Gli alcani sono composti organici costituiti solamente da carbonio e idrogeno (per questo motivo appartengono alla più ampia classe degli idrocarburi), aventi formula bruta C n H (2n + 2). Gli alcani
ALCANI Gli alcani sono composti organici costituiti solamente da carbonio e idrogeno (per questo motivo appartengono alla più ampia classe degli idrocarburi), aventi formula bruta C n H (2n + 2). Gli alcani
Capitolo 23 Dal carbonio agli idrocarburi
 Capitolo 23 Dal carbonio agli idrocarburi 1. I composti organici 2. Gli idrocarburi saturi: alcani e cicloalcani 3. L isomeria 4. La nomenclatura degli idrocarburi saturi 5. Proprietà fisiche e chimiche
Capitolo 23 Dal carbonio agli idrocarburi 1. I composti organici 2. Gli idrocarburi saturi: alcani e cicloalcani 3. L isomeria 4. La nomenclatura degli idrocarburi saturi 5. Proprietà fisiche e chimiche
Il termine arene viene impiegato per descrivere gli idrocarburi aromatici, in analogia con gli alcheni. prodotto di sostituzione.
 I Il termine aromatico venne riferito inizialmente all odore caratteristico di questa categoria di idrocarburi. Successivamente, tale nome è stato usato per indicare che questi composti sono altamente
I Il termine aromatico venne riferito inizialmente all odore caratteristico di questa categoria di idrocarburi. Successivamente, tale nome è stato usato per indicare che questi composti sono altamente
- il DNA, la molecola che contiene l informazione genetica, - le proteine dei nostro organismo ( proteine dei muscoli, della pelle, gli enzimi),
 La chimica organica è la chimica dei composti del carbonio, che sono i mattoni con cui sono costruiti tutti i corpi viventi della terra. Questi composti comprendono ad esempio - il DNA, la molecola che
La chimica organica è la chimica dei composti del carbonio, che sono i mattoni con cui sono costruiti tutti i corpi viventi della terra. Questi composti comprendono ad esempio - il DNA, la molecola che
CHIMICA ORGANICA. Gli alcheni
 1 2-ALENI IMIA ORGANIA ALENI Formula generale n 2n Desinenza -ene Gli alcheni La prima classe di idrocarburi insaturi è quella degli alcheni, detti anche olefine, che presentano lungo la catena uno o più
1 2-ALENI IMIA ORGANIA ALENI Formula generale n 2n Desinenza -ene Gli alcheni La prima classe di idrocarburi insaturi è quella degli alcheni, detti anche olefine, che presentano lungo la catena uno o più
ALIFATICI AROMATICI (Areni) POLIENI BENZENE e derivati CICLOALCHENI CICLOALCANI ALCHINI
 CIMICA ORGANICA IDROCARBURI Gli idrocarburi sono composti che contengono solo atomi di e C e, a seconda del tipo di legami chimici presenti nella molecola, possono essere suddivisi secondo il seguente
CIMICA ORGANICA IDROCARBURI Gli idrocarburi sono composti che contengono solo atomi di e C e, a seconda del tipo di legami chimici presenti nella molecola, possono essere suddivisi secondo il seguente
Gruppi funzionali Un gruppo funzionale è un atomo o un gruppo di atomi con proprietà chimiche e fisiche tipiche. E
 Gruppi funzionali Gruppi funzionali La reattività chimica di ogni molecola organica, indipendentemente dalle sue dimensioni o dalla sua complessità, è determinata dai gruppi funzionali che essa contiene
Gruppi funzionali Gruppi funzionali La reattività chimica di ogni molecola organica, indipendentemente dalle sue dimensioni o dalla sua complessità, è determinata dai gruppi funzionali che essa contiene
Isomeria Costituzionale. Isomeria Conformazionale
 Isomeria ostituzionale Isomeri ostituzionali: omposti con uguale formula molecolare ma con un diverso ordine con cui sono legati gli atomi tra loro. Isomeria onformazionale onformazione: ciascuna disposizione
Isomeria ostituzionale Isomeri ostituzionali: omposti con uguale formula molecolare ma con un diverso ordine con cui sono legati gli atomi tra loro. Isomeria onformazionale onformazione: ciascuna disposizione
IDROCARBURI: classificazione
 ALCANI 1 IDROCARBURI: classificazione 2 ALCANI Formula bruta: C n H 2n+2 1 C CH 4 2 C C 2 H 6 3 C C 3 H 8 4 C C 4 H 10 3 ALCANI: ibridazione Orbitali s, p e sp 3 z orbitale 2s y x z z z orbitali 2p y x
ALCANI 1 IDROCARBURI: classificazione 2 ALCANI Formula bruta: C n H 2n+2 1 C CH 4 2 C C 2 H 6 3 C C 3 H 8 4 C C 4 H 10 3 ALCANI: ibridazione Orbitali s, p e sp 3 z orbitale 2s y x z z z orbitali 2p y x
Idrocarburi Al A ifatici Ar A oma m tici
 GLI IDROCARBURI Gli idrocarburi sono i più semplici composti del carbonio con l'idrogeno. Sono le molecole di base della chimica organica poiché, oltre ad essere molto numerosi, tutti gli altri composti
GLI IDROCARBURI Gli idrocarburi sono i più semplici composti del carbonio con l'idrogeno. Sono le molecole di base della chimica organica poiché, oltre ad essere molto numerosi, tutti gli altri composti
Introduzione alla Chimica Organica. Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display.
 Introduzione alla Chimica Organica Copyright The McGraw-ill Companies, Inc. Permission required for reproduction or display. 1 Elementi Comuni nei Composti Organici 2 Classificazione degli idrocarburi
Introduzione alla Chimica Organica Copyright The McGraw-ill Companies, Inc. Permission required for reproduction or display. 1 Elementi Comuni nei Composti Organici 2 Classificazione degli idrocarburi
I composti organici. Gli idrocarburi: composti binari, ovvero costituiti solo da due elementi. Carbonio (C) e idrogeno (H)
 I composti organici Gli idrocarburi: composti binari, ovvero costituiti solo da due elementi. Carbonio (C) e idrogeno (H) Gli idrocarburi Gli Alcani Costituiti da uno o più atomi di carbonio legati tra
I composti organici Gli idrocarburi: composti binari, ovvero costituiti solo da due elementi. Carbonio (C) e idrogeno (H) Gli idrocarburi Gli Alcani Costituiti da uno o più atomi di carbonio legati tra
Reazioni Stereospecifiche e Stereoselettive
 Reazioni Stereospecifiche e Stereoselettive La stereospecificità in chimica è la proprietà di una stessa reazione di generare stereoisomeri diversi partendo da stereoisomeri diversi. Si differenzia dalla
Reazioni Stereospecifiche e Stereoselettive La stereospecificità in chimica è la proprietà di una stessa reazione di generare stereoisomeri diversi partendo da stereoisomeri diversi. Si differenzia dalla
Idrocarburi Saturi. Cicloalcani
 Idrocarburi Saturi Cicloalcani Cicloalcani I cicloalcani sono idrocarburi i cui atomi di carbonio sono uniti per formare un anello In natura sono presenti cicloalcani con dimensioni dell anello che vanno
Idrocarburi Saturi Cicloalcani Cicloalcani I cicloalcani sono idrocarburi i cui atomi di carbonio sono uniti per formare un anello In natura sono presenti cicloalcani con dimensioni dell anello che vanno
Reazioni degli alcani
 Reazioni degli alcani I legami degli alcani sono semplici, covalenti e non polari per questo sono composti praticamente inerti.(parum affinis ) Reagiscono solo con ossigeno (ossidoriduzioni) e con gli
Reazioni degli alcani I legami degli alcani sono semplici, covalenti e non polari per questo sono composti praticamente inerti.(parum affinis ) Reagiscono solo con ossigeno (ossidoriduzioni) e con gli
Gli Alcheni. Ibridazione sp 2. I legami chimici degli alcheni
 Gli Alcheni 2p Energia Ibridazione sp 2 sp 2 1s I tre orbitali ibridi sono disposti su un piano secondo una geometria trigonaleplanare con angoli di 120. L'orbitale 2p che non partecipa all'ibridazione
Gli Alcheni 2p Energia Ibridazione sp 2 sp 2 1s I tre orbitali ibridi sono disposti su un piano secondo una geometria trigonaleplanare con angoli di 120. L'orbitale 2p che non partecipa all'ibridazione
LA CHIMICA DEL CARBONIO
 LA CHIMICA DEL CARBONIO E QUELLA PARTE DELLA CHIMICA CHE STUDIA IL CARBONIO E TUTTI I SUOI DERIVATI. I COMPOSTI DEL CARBONIO POSSONO ESSERE NATURALI (PROTEINE, ACIDI NUCLEICI, LIPIDI E CARBOIDRATI) O ESSERE
LA CHIMICA DEL CARBONIO E QUELLA PARTE DELLA CHIMICA CHE STUDIA IL CARBONIO E TUTTI I SUOI DERIVATI. I COMPOSTI DEL CARBONIO POSSONO ESSERE NATURALI (PROTEINE, ACIDI NUCLEICI, LIPIDI E CARBOIDRATI) O ESSERE
REAZIONI DEGLI ALCHENI
 REAZIONI DEGLI ALCHENI La reazione caratteristica degli alcheni è l addizione al C=C Idroalogenazione Idratazione (acido-catalizzata) Alogenazione Ossidrilazione (ossidazione) Idrogenazione (riduzione)
REAZIONI DEGLI ALCHENI La reazione caratteristica degli alcheni è l addizione al C=C Idroalogenazione Idratazione (acido-catalizzata) Alogenazione Ossidrilazione (ossidazione) Idrogenazione (riduzione)
Complementi di Chimica Organica. Composti Aromatici: Benzene C 6 H 6 (1825) (1865) Friedrich August Kekulé
 Composti Aromatici: Benzene C 6 6 (1825) (1865) Friedrich August Kekulé Composti Aromatici: Benzene, energia di coniugazione = -119.5 KJ/mol (-119.2 x 3 = -357.6) = -208.2 KJ/mol -357.6 KJ/mol (-208.2
Composti Aromatici: Benzene C 6 6 (1825) (1865) Friedrich August Kekulé Composti Aromatici: Benzene, energia di coniugazione = -119.5 KJ/mol (-119.2 x 3 = -357.6) = -208.2 KJ/mol -357.6 KJ/mol (-208.2
Alcani. Es. CH 3 CH 2 CH 2 CH 3
 Alcani Gli alcani sono i composti organici più semplici costituiti solo da atomi di e di (Idrocarburi); Sono composti saturi poiché ogni atomo di carbonio è legato al numero massimo possibile (4) di altri
Alcani Gli alcani sono i composti organici più semplici costituiti solo da atomi di e di (Idrocarburi); Sono composti saturi poiché ogni atomo di carbonio è legato al numero massimo possibile (4) di altri
Aromaticità. Addizione elettrofila alcheni
 Aromaticità Le molecole sono aromatiche se sono soddisfatte le seguenti condizioni: La molecola è ciclica La molecola è interamente coniugata La molecola è planare (atomi di carbonio con ibridazione sp
Aromaticità Le molecole sono aromatiche se sono soddisfatte le seguenti condizioni: La molecola è ciclica La molecola è interamente coniugata La molecola è planare (atomi di carbonio con ibridazione sp
Gruppi funzionali. Gruppi funzionali
 Gruppi funzionali Gruppi funzionali La reattività chimica di ogni molecola organica, indipendentemente dalle sue dimensioni o dalla sua complessità, è determinata dai gruppi funzionali che essa contiene
Gruppi funzionali Gruppi funzionali La reattività chimica di ogni molecola organica, indipendentemente dalle sue dimensioni o dalla sua complessità, è determinata dai gruppi funzionali che essa contiene
La chimica organica si occupa dello studio della struttura, delle proprietà e delle reazioni dei composti del carbonio.
 La chimica organica si occupa dello studio della struttura, delle proprietà e delle reazioni dei composti del carbonio. Proteine, zuccheri, lipidi, DNA.. farmaci arta, fibre, plastica s2p2 Z=6 2p 1s 2
La chimica organica si occupa dello studio della struttura, delle proprietà e delle reazioni dei composti del carbonio. Proteine, zuccheri, lipidi, DNA.. farmaci arta, fibre, plastica s2p2 Z=6 2p 1s 2
Modulo di Biochimica 3 CFU (30 ore) Orario delle Lezioni: 1 semestre (settembre-dicembre) Lunedì 14-17
 Corso di laurea in ingegneria Biomedica A.A. 2017/2018 Modulo di Biochimica 3 CFU (30 ore) Orario delle Lezioni: 1 semestre (settembre-dicembre) Lunedì 14-17 Dott.ssa Morena Arba PhD. morena.arba@unica.it
Corso di laurea in ingegneria Biomedica A.A. 2017/2018 Modulo di Biochimica 3 CFU (30 ore) Orario delle Lezioni: 1 semestre (settembre-dicembre) Lunedì 14-17 Dott.ssa Morena Arba PhD. morena.arba@unica.it
CHIMICA ORGANICA. Gli idrocarburi aromatici
 1 D-IDROCARBURI AROMATICI CHIMICA ORGANICA IDROCARBURI AROMATICI Formula generale C n H n Desinenza -benzene Gli idrocarburi aromatici Gli idrocarburi aromatici (areni o alchilbenzeni) sono caratterizzati
1 D-IDROCARBURI AROMATICI CHIMICA ORGANICA IDROCARBURI AROMATICI Formula generale C n H n Desinenza -benzene Gli idrocarburi aromatici Gli idrocarburi aromatici (areni o alchilbenzeni) sono caratterizzati
Alcheni e alchini. idrocarburi. Insaturi C-C doppi/tripli. alcani. Saturi C-C semplici cicloalcani. aromatici
 Alcheni e alchini alcani Saturi C-C semplici cicloalcani idrocarburi Insaturi C-C doppi/tripli aromatici 1 Alcheni e Alchini Alcheni e alchini sono idrocarburi che hanno rispettivamente un doppio legame
Alcheni e alchini alcani Saturi C-C semplici cicloalcani idrocarburi Insaturi C-C doppi/tripli aromatici 1 Alcheni e Alchini Alcheni e alchini sono idrocarburi che hanno rispettivamente un doppio legame
Ammine : caratteristiche strutturali
 Ammine : caratteristiche strutturali Le ammine sono composti formalmente derivanti dall ammoniaca in cui uno o più atomi di idrogeno sono stati sostituiti da gruppi alchilici Come per l ammonica l azoto
Ammine : caratteristiche strutturali Le ammine sono composti formalmente derivanti dall ammoniaca in cui uno o più atomi di idrogeno sono stati sostituiti da gruppi alchilici Come per l ammonica l azoto
Nomenclatura. Gli idrocarburi alifatici
 Gli idrocarburi alifatici Gli idrocarburi sono i composti organici più semplici, sono infatti costituiti solo da carbonio e idrogeno (da cui il nome, appunto, di idro-carburi). Pur essendo relativamente
Gli idrocarburi alifatici Gli idrocarburi sono i composti organici più semplici, sono infatti costituiti solo da carbonio e idrogeno (da cui il nome, appunto, di idro-carburi). Pur essendo relativamente
Formule di risonanza. Chimica Organica II. Come individuarle: Come valutarne l importanza:
 Formule di risonanza Come individuarle: Le formule di risonanza devono rispettare le regole delle strutture di Lewis La posizione dei nuclei deve rimanere fissa (le formule di risonanza vengono scritte
Formule di risonanza Come individuarle: Le formule di risonanza devono rispettare le regole delle strutture di Lewis La posizione dei nuclei deve rimanere fissa (le formule di risonanza vengono scritte
COMPOSTI AROMATICI POLICICLICI
 CHIMICA DEI COMPOSTI AROMATICI POLICICLICI CHIMICA DI PIRROLO, FURANO E TIOFENE CHIMICA DI IMIDAZOLI, OSSAZOLI E TIAZOLI CHIMICA DI ISOSSAZOLI, PIRAZOLI, ISOTIAZOLI LEZIONE 5 COMPOSTI AROMATICI POLICICLICI
CHIMICA DEI COMPOSTI AROMATICI POLICICLICI CHIMICA DI PIRROLO, FURANO E TIOFENE CHIMICA DI IMIDAZOLI, OSSAZOLI E TIAZOLI CHIMICA DI ISOSSAZOLI, PIRAZOLI, ISOTIAZOLI LEZIONE 5 COMPOSTI AROMATICI POLICICLICI
Formule di risonanza. Chimica Organica II. Come individuarle: Come valutarne l importanza:
 Formule di risonanza Come individuarle: Le formule di risonanza devono rispettare le regole delle strutture di Lewis La posizione dei nuclei deve rimanere fissa (le formule di risonanza vengono scritte
Formule di risonanza Come individuarle: Le formule di risonanza devono rispettare le regole delle strutture di Lewis La posizione dei nuclei deve rimanere fissa (le formule di risonanza vengono scritte
Gli idrocarburi sono composti organici, che contengono soltanto atomi di carbonio e di idrogeno. Gli atomi di carbonio (C) sono legati tra loro a
 Gli idrocarburi sono composti organici, che contengono soltanto atomi di carbonio e di idrogeno. Gli atomi di carbonio (C) sono legati tra loro a formare lo scheletro della molecola, mentre gli atomi di
Gli idrocarburi sono composti organici, che contengono soltanto atomi di carbonio e di idrogeno. Gli atomi di carbonio (C) sono legati tra loro a formare lo scheletro della molecola, mentre gli atomi di
Stereochimica di alcani e cicloalcani
 di alcani e cicloalcani Conformazioni, conformeri Due conformazioni dell etano. Le conformazioni sono arrangiamenti diversi di atomi che interconvertono per rotazione attorno al legame C-C. Rappresentazione
di alcani e cicloalcani Conformazioni, conformeri Due conformazioni dell etano. Le conformazioni sono arrangiamenti diversi di atomi che interconvertono per rotazione attorno al legame C-C. Rappresentazione
Alcheni: struttura e proprietà
 Chimica Organica Informazione Scientifica sul Farmaco Alcheni: struttura e proprietà Organic Chemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: struttura degli alcheni nomenclatura proprietà fisiche
Chimica Organica Informazione Scientifica sul Farmaco Alcheni: struttura e proprietà Organic Chemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: struttura degli alcheni nomenclatura proprietà fisiche
Introduzione alla chimica organica. Daniele Dondi
 Introduzione alla chimica organica Daniele Dondi dondi@unipv.it 1 enni sulla nascita della chimica organica Analisi elementari tramite combustione WÖLER (metà 1800) sintetizza l urea KLBE sintetizza l
Introduzione alla chimica organica Daniele Dondi dondi@unipv.it 1 enni sulla nascita della chimica organica Analisi elementari tramite combustione WÖLER (metà 1800) sintetizza l urea KLBE sintetizza l
IDROCARBURI INSATURI: GLI ALCHENI HANNO ALMENO UN DOPPIO LEGAME NELLA STRUTTURA NOMENCLATURA: RADICE COME NEGLI IDROCARBURI, DESINENZA -ENE
 IDRCARBURI INSATURI: GLI ALCENI ANN ALMEN UN DPPI LEGAME NELLA STRUTTURA NMENCLATURA: RADICE CME NEGLI IDRCARBURI, DESINENZA -ENE butano 2-butene o but-2-ene Esempi di nomenclatura degli alcheni Esempi
IDRCARBURI INSATURI: GLI ALCENI ANN ALMEN UN DPPI LEGAME NELLA STRUTTURA NMENCLATURA: RADICE CME NEGLI IDRCARBURI, DESINENZA -ENE butano 2-butene o but-2-ene Esempi di nomenclatura degli alcheni Esempi
Stereochimica di alcani e cicloalcani. Stereochimica. Conformazioni, conformeri
 di alcani e cicloalcani Conformazioni, conformeri Due conformazioni dell etano. I differenti conformeri si interconvertono per rotazione attorno al legame C-C. 1 Rappresentazione a cavalletto e proiezione
di alcani e cicloalcani Conformazioni, conformeri Due conformazioni dell etano. I differenti conformeri si interconvertono per rotazione attorno al legame C-C. 1 Rappresentazione a cavalletto e proiezione
Introduzione alla chimica organica. Daniele Dondi
 Introduzione alla chimica organica Daniele Dondi dondi@unipv.it Il carbonio nelle sue ibridazioni sp 3 sp 2 sp Il carbonio è un elemento fondamentale per la chimica organica. La stabilità del legame -
Introduzione alla chimica organica Daniele Dondi dondi@unipv.it Il carbonio nelle sue ibridazioni sp 3 sp 2 sp Il carbonio è un elemento fondamentale per la chimica organica. La stabilità del legame -
Aromaticità Un composto si definisce aromatico se possiede un anello di elettroni chiuso.
 Aromaticità Un composto si definisce aromatico se possiede un anello di elettroni chiuso. E anche detto aromatico, quando tramite i seguenti criteri soddisfa la regola di ückel: 1. I composti aromatici
Aromaticità Un composto si definisce aromatico se possiede un anello di elettroni chiuso. E anche detto aromatico, quando tramite i seguenti criteri soddisfa la regola di ückel: 1. I composti aromatici
Capitolo 4 Reazioni degli alcheni
 himica Organica Informazione Scientifica sul Farmaco apitolo 4 Reazioni degli alcheni Organic hemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: richiami generali sulle reazioni chimice reattività
himica Organica Informazione Scientifica sul Farmaco apitolo 4 Reazioni degli alcheni Organic hemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: richiami generali sulle reazioni chimice reattività
CHIMICA ORGANICA - CLASSE 3 - RISPOSTE
 CHIMICA ORGANICA - CLASSE 3 - RISPOSTE Prof: Anna Rosa MASTELLARI. Specializzazione di CHIMICA Testo: CHIMICA ORGANICA, BIORGANICA E LABORATORIO ALCANI E CICLOALCANI (Capitolo 2) 1. Assegnare la nomenclatura
CHIMICA ORGANICA - CLASSE 3 - RISPOSTE Prof: Anna Rosa MASTELLARI. Specializzazione di CHIMICA Testo: CHIMICA ORGANICA, BIORGANICA E LABORATORIO ALCANI E CICLOALCANI (Capitolo 2) 1. Assegnare la nomenclatura
ALCHENI: Reazioni del doppio legame
 ALCENI: REATTIVITÀ ALCENI: Reazioni del doppio legame Reazione di addizione Addizioni ioniche Addizioni con meccanismo concertato ADDIZIONI IONICE ADDIZIONE DI ACIDI ALOGENIDRICI ADDIZIONE DI ACQUA ROTTURA
ALCENI: REATTIVITÀ ALCENI: Reazioni del doppio legame Reazione di addizione Addizioni ioniche Addizioni con meccanismo concertato ADDIZIONI IONICE ADDIZIONE DI ACIDI ALOGENIDRICI ADDIZIONE DI ACQUA ROTTURA
Appunti di Chimica Organica Elementi per CdL Ostetricia CHIMICA ORGANICA. Appunti di Lezione. Elementi per il corso di Laurea In Ostetricia
 Appunti di himica Organica Elementi per dl Ostetricia IMIA ORGANIA Appunti di Lezione Elementi per il corso di Laurea In Ostetricia Autore: Roberto Zanrè A.A. 2009/2010 1 Appunti di himica Organica Elementi
Appunti di himica Organica Elementi per dl Ostetricia IMIA ORGANIA Appunti di Lezione Elementi per il corso di Laurea In Ostetricia Autore: Roberto Zanrè A.A. 2009/2010 1 Appunti di himica Organica Elementi
GLI ALCANI. Michele Kodrič
 GLI ALCANI Michee Kodrič DEGLI ALCANI VEDREMO: (CARATTERISTICE (NOMENCLATURA (FORMULAZIONE (COMPOSTI PRINCIPALI (REATTIVITA (OTTENIMENTO (ISOMERIA DI CATENA (GRUPPI ALCILICI 1 CARATTERISTICE DEGLI ALCANI
GLI ALCANI Michee Kodrič DEGLI ALCANI VEDREMO: (CARATTERISTICE (NOMENCLATURA (FORMULAZIONE (COMPOSTI PRINCIPALI (REATTIVITA (OTTENIMENTO (ISOMERIA DI CATENA (GRUPPI ALCILICI 1 CARATTERISTICE DEGLI ALCANI
Idrocarburi Saturi. Reazioni
 Idrocarburi Saturi Reazioni Fonti ed usi Gli alcani lineari, ramificati e ciclici si ottengono principalmente dalla lavorazione (frazionamento, cracking, etc.), del petrolio. Fonti ed usi Gli alcani, soprattutto
Idrocarburi Saturi Reazioni Fonti ed usi Gli alcani lineari, ramificati e ciclici si ottengono principalmente dalla lavorazione (frazionamento, cracking, etc.), del petrolio. Fonti ed usi Gli alcani, soprattutto
BENZENE E DERIVATI. Composto aromatico: termine usato per indicare il benzene ed i suoi derivati C 6 H 6. Arene: Idrocarburo aromatico
 BENZENE E DERIVATI Composto aromatico: termine usato per indicare il benzene ed i suoi derivati C 6 H 6 Arene: Idrocarburo aromatico Gruppo arilico: gruppo sostituente che deriva da un arene per rimozione
BENZENE E DERIVATI Composto aromatico: termine usato per indicare il benzene ed i suoi derivati C 6 H 6 Arene: Idrocarburo aromatico Gruppo arilico: gruppo sostituente che deriva da un arene per rimozione
PIANO DI LAVORO ANNUALE
 PIANO DI LAVORO ANNUALE Classe 3B A.S. 2013-14 Disciplina: Chimica Organica Docente: prof. Laura M. Iannone Ore settimanali: 4 Libro di testo: Percorsi di Chimica Organica, di Paolo De Maria ed. Zanichelli.
PIANO DI LAVORO ANNUALE Classe 3B A.S. 2013-14 Disciplina: Chimica Organica Docente: prof. Laura M. Iannone Ore settimanali: 4 Libro di testo: Percorsi di Chimica Organica, di Paolo De Maria ed. Zanichelli.
Pronti per l Università Liceo Scientifico de Caprariis Atripalda PON F
 Pronti per l Università Liceo Scientifico de Caprariis Atripalda PON F2 2011-14 La chimica del carbonio Il Carbonio Copyright 2008 PresentationFx.com Redistribution Prohibited Image 2008 clix@sxc.hu This
Pronti per l Università Liceo Scientifico de Caprariis Atripalda PON F2 2011-14 La chimica del carbonio Il Carbonio Copyright 2008 PresentationFx.com Redistribution Prohibited Image 2008 clix@sxc.hu This
Chimica Organica. Studio dei composti del CARBONIO
 Chimica Organica Studio dei composti del CARBONIO 1 Contengono C, H e possono contenere N, O, S Carbonio legato covalentemente ad un metallo Tutti gli elementi possibili Composti organici 2 Perché si formano
Chimica Organica Studio dei composti del CARBONIO 1 Contengono C, H e possono contenere N, O, S Carbonio legato covalentemente ad un metallo Tutti gli elementi possibili Composti organici 2 Perché si formano
Cos è la chimica organica
 Cos è la chimica organica La prima definizione di chimica organica si deve al chimico svedese Jacob Berzelius nel 1807: la chimica organica è la scienza che studia i comportamenti chimici e fisici dei
Cos è la chimica organica La prima definizione di chimica organica si deve al chimico svedese Jacob Berzelius nel 1807: la chimica organica è la scienza che studia i comportamenti chimici e fisici dei
Alchini. Suffisso: -ino. d. H 3 CCH 2 CC CH
 Alchini Suffisso: -ino Indicare la posizione del triplo legame con il numero che lo contraddistingue nella catena. La numerazione comincia sempre dall estremità più prossima al triplo legame. 3 3 2 2 2
Alchini Suffisso: -ino Indicare la posizione del triplo legame con il numero che lo contraddistingue nella catena. La numerazione comincia sempre dall estremità più prossima al triplo legame. 3 3 2 2 2
CHIMICA ORGANICA. Gli alchini
 1 C3-ALCHINI CHIMICA ORGANICA ALCHINI Formula generale C n n 2 Desinenza -ino Gli alchini Gli alchini sono caratterizzati dalla presenza di uno o più tripli legami carboniocarbonio e sono anch essi classificati
1 C3-ALCHINI CHIMICA ORGANICA ALCHINI Formula generale C n n 2 Desinenza -ino Gli alchini Gli alchini sono caratterizzati dalla presenza di uno o più tripli legami carboniocarbonio e sono anch essi classificati
Idrocarburi AROMATICI
 Idrocarburi AROMATICI Composti aromatici Gli idrocarburi aromatici costituiscono una particolare classe di composti che contengono 2n 1 doppi legami coniugati in una struttura ciclica, strutturalmente
Idrocarburi AROMATICI Composti aromatici Gli idrocarburi aromatici costituiscono una particolare classe di composti che contengono 2n 1 doppi legami coniugati in una struttura ciclica, strutturalmente
Conformazione degli alcani
 onformazione degli alcani La conformazione di un alcano si riferisce alla disposizione tridimensionale degli atomi che risulta dalla rotazione attorno al legame -. Nonostante in una molecola possano esservi
onformazione degli alcani La conformazione di un alcano si riferisce alla disposizione tridimensionale degli atomi che risulta dalla rotazione attorno al legame -. Nonostante in una molecola possano esservi
Capitolo 10 Composti Aromatici
 himica Organica Informazione Scientifica sul Farmaco apitolo 10 omposti Aromatici Organic hemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: scoperta del benzene struttura elettronica del benzene
himica Organica Informazione Scientifica sul Farmaco apitolo 10 omposti Aromatici Organic hemistry, 5 th Edition L. G. Wade, Jr. In questa lezione: scoperta del benzene struttura elettronica del benzene
I.T.I.S. VOLTA - Perugia A. S. 2011/2012 CLASSE 3 a sez. AC MATERIA: Chimica Organica Bio-Org. delle Fermentazione e Lab.
 I.T.I.S. VOLTA - Perugia A. S. 2011/2012 CLASSE 3 a sez. AC MATERIA: Chimica Organica Bio-Org. delle Fermentazione e Lab. (Esercizi da svolgere durante il periodo estivo) Strumento da utilizzare: libro
I.T.I.S. VOLTA - Perugia A. S. 2011/2012 CLASSE 3 a sez. AC MATERIA: Chimica Organica Bio-Org. delle Fermentazione e Lab. (Esercizi da svolgere durante il periodo estivo) Strumento da utilizzare: libro
Prof.ssa Stacca Prof.ssa Stacca
 La bassa differenza di elettronegatività tra C e H fa sì che i legami presenti negli alcani siano legami covalenti quasi omopolari; di conseguenza gli alcani sono composti apolari. La bassa differenza
La bassa differenza di elettronegatività tra C e H fa sì che i legami presenti negli alcani siano legami covalenti quasi omopolari; di conseguenza gli alcani sono composti apolari. La bassa differenza
Reazioni di Chimica Organica
 Reazioni di Chimica Organica 1. Sostituzione CH 4 + Cl 2 + energia > CH 3 Cl + HCl 2. Addizione C =C + XY C C X Y 3. Eliminazione 4. Riarrangiamento 1 Elettrofili e Nucleofili Reagenti elettrofili: composti
Reazioni di Chimica Organica 1. Sostituzione CH 4 + Cl 2 + energia > CH 3 Cl + HCl 2. Addizione C =C + XY C C X Y 3. Eliminazione 4. Riarrangiamento 1 Elettrofili e Nucleofili Reagenti elettrofili: composti
CORSO DI CHIMICA ORGANICA. Testo consigliato: Chimica Organica H.Hart,D.J.Hart, L.E.Craine Zanichelli
 CORSO DI CIMICA ORGANICA Testo consigliato: Chimica Organica.art,D.J.art, L.E.Craine Zanichelli Nucleo contenente neutroni e protoni 10-2 m Spazio extranucleare contenente elettroni NUMERO ATOMICO: numero
CORSO DI CIMICA ORGANICA Testo consigliato: Chimica Organica.art,D.J.art, L.E.Craine Zanichelli Nucleo contenente neutroni e protoni 10-2 m Spazio extranucleare contenente elettroni NUMERO ATOMICO: numero
CHIMICA II (CHIMICA ORGANICA)
 CHIMICA II (CHIMICA ORGANICA) Prof. Gennaro Piccialli Prof. Aldo Galeone Prof. Giorgia Oliviero Testo Consigliato: gruppo 1 (matricole A-E) gruppo 2 (matricole F-O) gruppo 3 (matricole P-Z) Introduzione
CHIMICA II (CHIMICA ORGANICA) Prof. Gennaro Piccialli Prof. Aldo Galeone Prof. Giorgia Oliviero Testo Consigliato: gruppo 1 (matricole A-E) gruppo 2 (matricole F-O) gruppo 3 (matricole P-Z) Introduzione
La Chimica Organica idrogeno carbonio azoto ossigeno composti covalenti catene di atomi di carbonio strutture covalenti e debolmente polarizzate
 LA IMIA ORGANIA La himica Organica I quattro elementi idrogeno, carbonio, azoto e ossigeno rappresentano più del 95% dei costituenti della materia vivente. I composti organici sono composti covalenti che
LA IMIA ORGANIA La himica Organica I quattro elementi idrogeno, carbonio, azoto e ossigeno rappresentano più del 95% dei costituenti della materia vivente. I composti organici sono composti covalenti che
LA CHIMICA ORGANICA IBRIDAZIONE
 LA CHIMICA ORGANICA Detta anche LA CHIMICA DEL CARBONIO (C) perché Il C gioca un ruolo fondamentale in tutte le molecole organiche (cioè appartenenti o derivanti da esseri viventi). Possiamo spiegarlo
LA CHIMICA ORGANICA Detta anche LA CHIMICA DEL CARBONIO (C) perché Il C gioca un ruolo fondamentale in tutte le molecole organiche (cioè appartenenti o derivanti da esseri viventi). Possiamo spiegarlo
R-X ALOGENURI ALCHILICI. F Cl Br I. Nomenclatura. In genere si indicano con. + - Il legame C-X è polarizzato, ciò rende il carbonio elettrofilo
 ALOGENURI ALCHILICI In genere si indicano con Nomenclatura R-X + - Il legame C-X è polarizzato, ciò rende il carbonio elettrofilo X F Cl Br I 3-Bromo-2-metilpentano 4-Bromo-cicloesene trans-2-clorocicloesanolo
ALOGENURI ALCHILICI In genere si indicano con Nomenclatura R-X + - Il legame C-X è polarizzato, ciò rende il carbonio elettrofilo X F Cl Br I 3-Bromo-2-metilpentano 4-Bromo-cicloesene trans-2-clorocicloesanolo
ALCANI metano. etano. pentano. butano. propano. Idrocarburo: molecola contenente solo carbonio ed idrogeno
 ALCANI Idrocarburo: molecola contenente solo carbonio ed idrogeno Idrocarburo saturo: molecola contenente solo legami semplici carbonio-carbonio Alcano: Idrocarburo saturo contenente solo catene aperte
ALCANI Idrocarburo: molecola contenente solo carbonio ed idrogeno Idrocarburo saturo: molecola contenente solo legami semplici carbonio-carbonio Alcano: Idrocarburo saturo contenente solo catene aperte
1. COS È LA CHIMICA ORGANICA?
 Università degli Studi di Bari Dipartimento di Farmacia Scienze del Farmaco Corso di Laurea in Tecniche Erboristiche A.A. 2013-2014 Chimica Organica Prof. Giuseppe Gerardo Carbonara Finalità. Scopo del
Università degli Studi di Bari Dipartimento di Farmacia Scienze del Farmaco Corso di Laurea in Tecniche Erboristiche A.A. 2013-2014 Chimica Organica Prof. Giuseppe Gerardo Carbonara Finalità. Scopo del
IDROCARBURI ALIFATICI
 CHIMICA ORGANICA (Lezioni in classe prof. Adriano Muschiato) Nel 1828 il chimico tedesco Friedrich Wöhler per la prima volta riesce a sintetizzare da reagenti inorganici l UREA: Nel sud della Germania
CHIMICA ORGANICA (Lezioni in classe prof. Adriano Muschiato) Nel 1828 il chimico tedesco Friedrich Wöhler per la prima volta riesce a sintetizzare da reagenti inorganici l UREA: Nel sud della Germania
Alcoli ed eteri Composti organici che contengono legami singoli C-O
 Alcoli ed eteri Composti organici che contengono legami singoli C-O Chimica Organica CH 3 CH 2 CH 3 CH 2 O CH 2 CH 3 Alcol etilico etanolo Etere etilico dietiletere Fenolo idrossibenzene Nomenclatura degli
Alcoli ed eteri Composti organici che contengono legami singoli C-O Chimica Organica CH 3 CH 2 CH 3 CH 2 O CH 2 CH 3 Alcol etilico etanolo Etere etilico dietiletere Fenolo idrossibenzene Nomenclatura degli
CHIMICA ORGANICA = STUDIO DEI COMPOSTI DEL CARBONIO. energia superiore. energia inferiore. orbitale s
 CIMICA ORGANICA = STUDIO DEI COMPOSTI DEL CARBONIO C elemento del secondo periodo della tavola periodica; numero atomico = 6 configurazione elettronica del C 2p 2s 1s energia superiore energia inferiore
CIMICA ORGANICA = STUDIO DEI COMPOSTI DEL CARBONIO C elemento del secondo periodo della tavola periodica; numero atomico = 6 configurazione elettronica del C 2p 2s 1s energia superiore energia inferiore
STEREOISOMERIA trans-1,4-dimetilcicloesano cis-1,4-dimetilcicloesano
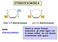 STEREOISOMERIA trans-1,4-dimetilcicloesano cis-1,4-dimetilcicloesano sono stereoisomeri Hanno la stessa formula molecolare, gli atomi legati con lo stesso ordine, ma con diversa orientazione nello spazio
STEREOISOMERIA trans-1,4-dimetilcicloesano cis-1,4-dimetilcicloesano sono stereoisomeri Hanno la stessa formula molecolare, gli atomi legati con lo stesso ordine, ma con diversa orientazione nello spazio
Figura. Benzene e aromaticità
 Figura Benzene e aromaticità Benzene e composti aromatici dal carbone da ciliegie pesche mandorle dal balsamo di Tolu Benzene e composti aromatici ormone steroideo naturale analgesico naturale tranquillante
Figura Benzene e aromaticità Benzene e composti aromatici dal carbone da ciliegie pesche mandorle dal balsamo di Tolu Benzene e composti aromatici ormone steroideo naturale analgesico naturale tranquillante
INTRODUZIONE ALLO STUDIO DELLA CHIMICA ORGANICA
 INTRODUZIONE ALLO STUDIO DELLA CHIMICA ORGANICA ai primi dell 800 Il chimico svedese Jacob Berzelius (1779-1848) indicava le sostanze con il termine organico se ottenute dagli organismi viventi (animali
INTRODUZIONE ALLO STUDIO DELLA CHIMICA ORGANICA ai primi dell 800 Il chimico svedese Jacob Berzelius (1779-1848) indicava le sostanze con il termine organico se ottenute dagli organismi viventi (animali
Composti carbonilici. Chimica Organica II
 Composti carbonilici Il gruppo carbonilico è formato da un carbonio legato tramite un doppio legame ad un ossigeno. Probabilmente è il gruppo funzionale più importante. Le proprietà del gruppo carbonilico
Composti carbonilici Il gruppo carbonilico è formato da un carbonio legato tramite un doppio legame ad un ossigeno. Probabilmente è il gruppo funzionale più importante. Le proprietà del gruppo carbonilico
Nome degli alcheni a catena lineare
 Gli alcheni sono idrocarboni insaturi. insaturi (almeno un doppio legame) idrocarboni (solo e ) n 2n 1-Esene 6 12 opyright 1999, Michael J. Wovkulich. All rights reserved. Nome degli alcheni a catena lineare
Gli alcheni sono idrocarboni insaturi. insaturi (almeno un doppio legame) idrocarboni (solo e ) n 2n 1-Esene 6 12 opyright 1999, Michael J. Wovkulich. All rights reserved. Nome degli alcheni a catena lineare
Capitolo 8 Alcoli e Fenoli
 Chimica Organica Informazione Scientifica sul Farmaco Capitolo 8 Alcoli e Fenoli Organic Chemistry, 5 th Edition L. G. Wade, Jr. Struttura degli Alcoli Alcoli: Il gruppo funzionale è l ossidrile (), legato
Chimica Organica Informazione Scientifica sul Farmaco Capitolo 8 Alcoli e Fenoli Organic Chemistry, 5 th Edition L. G. Wade, Jr. Struttura degli Alcoli Alcoli: Il gruppo funzionale è l ossidrile (), legato
IDROCARBURI AROMATICI
 IDROCARBURI AROMATICI IL BENZENE E una sostanza chimica liquida e incolore dal caratteristico odore aromatico pungente. A temperatura ambiente volatilizza assai facilmente. La maggior parte del benzene
IDROCARBURI AROMATICI IL BENZENE E una sostanza chimica liquida e incolore dal caratteristico odore aromatico pungente. A temperatura ambiente volatilizza assai facilmente. La maggior parte del benzene
Delocalizzazione elettronica e risonanza
 Delocalizzazione elettronica e risonanza E sufficiente? La risonanza è quel fenomeno per cui una molecola può essere rappresentata attraverso diverse strutture che differiscano tra loro solo per una diversa
Delocalizzazione elettronica e risonanza E sufficiente? La risonanza è quel fenomeno per cui una molecola può essere rappresentata attraverso diverse strutture che differiscano tra loro solo per una diversa
Addizioni nucleofile. Addizioni a C=O
 Addizioni nucleofile Addizioni a C= Substrato Un composto che possiede un atomo di carbonio elettron-deficiente legato con un legame π (che si possa rompere facilmente) ad un atomo più elettronegativo
Addizioni nucleofile Addizioni a C= Substrato Un composto che possiede un atomo di carbonio elettron-deficiente legato con un legame π (che si possa rompere facilmente) ad un atomo più elettronegativo
Capitolo 6 Composti Aromatici
 himica Organica Scienze della Terra, dell Ambiente e del Territorio apitolo 6 omposti Aromatici Organic hemistry, 5 th Edition L. G. Wade, Jr. Scoperta del Benzene I composti aromatici sono tra i primi
himica Organica Scienze della Terra, dell Ambiente e del Territorio apitolo 6 omposti Aromatici Organic hemistry, 5 th Edition L. G. Wade, Jr. Scoperta del Benzene I composti aromatici sono tra i primi
REAZIONI E LORO MECCANISMI
 REAZIONI E LORO MECCANISMI Rivisitazione dei concetti di Omolisi, Eterolisi Reagenti Nucleofili e Reagenti Elettrofili Addizione elettrofila Sostituzione nucleofila Eliminazione Reazioni radicaliche Reazioni
REAZIONI E LORO MECCANISMI Rivisitazione dei concetti di Omolisi, Eterolisi Reagenti Nucleofili e Reagenti Elettrofili Addizione elettrofila Sostituzione nucleofila Eliminazione Reazioni radicaliche Reazioni
Alchini. Francesca Anna Scaramuzzo, PhD
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alchini Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate per
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Alchini Francesca Anna Scaramuzzo, PhD Dipartimento di Scienze di Base e Applicate per
TAVOLA PERIODICA DEGLI ELEMENTI
 TAVOLA PERIODIA DEGLI ELEMENTI Idrogeno = 1 legame Ossigeno = 2 legami O Azoto = 3 legami N arbonio = 4 legami Questi sono gli atomi che intervengono maggiormente nelle reazioni che tratteremo nella
TAVOLA PERIODIA DEGLI ELEMENTI Idrogeno = 1 legame Ossigeno = 2 legami O Azoto = 3 legami N arbonio = 4 legami Questi sono gli atomi che intervengono maggiormente nelle reazioni che tratteremo nella
