PALONOSETRON ( )
|
|
|
- Michela Riccio
- 6 anni fa
- Visualizzazioni
Transcript
1 PALONOSETRON ( ) Specialità: Aloxi (Italfarmaco) Forma Farmaceutica: 1flac.no ev Dosaggio: 0.25mg Prezzo: 112,89 Prezzo al pubblico da banca dati Farmadati Marzo 2007 ATC: A04AA05 Categoria terapeutica: Antiemetici e antinausea - antagonisti 5HT3 Classe PTN: H-OSP1 Indicazioni Ministeriali: Prevenzione della nausea e del vomito acuti, associati a chemioterapia oncologica altamente emetogena e prevenzione della nausea e del vomito associati a chemioterapia oncologica moderatamente emetogena. Decisioni della CTR: Farmaco inserito in PTORV con nota (data valutazione: ) Nota: Farmaci ad attività sostanzialmente equivalente; le singole C.T. ne scelgano non più di due sulla base delle indicazioni registrate, della documentazione scientifica disponibile e del costo per DDD o PDD. Commenti: Sulla base dei dati ad oggi disponibili Palonosetron viene considerato sovrapponibile agli altri antiemetici della stessa classe. Considerando che attualmente ha vinto la gara regionale l ondansetron, il farmaco, in analogia agli altri che non hanno vinto la gara, potrà essere richiesto esclusivamente su richiesta motivata. Analisi della letteratura Il preciso meccanismo con cui la chemioterapia antiblastica induce nausea e vomito non è chiaro: sembra probabile che chemioterapici differenti agiscano su siti diversi ed alcuni farmaci agiscano su più siti. Certamente implicati nell insorgenza dell emesi seguente a chemioterapia sono la zona di attivazione chemorecettoriale (CTZ), il tratto gastrointestinale, meccanismi vestibolari, meccanismi corticali, alterazioni del gusto e dell olfatto, unitamente ad alcuni neurotrasmettitori, localizzati nell area postrema del cervello, quali dopamina, serotonina, istamina, noradrenalina, apomorfina, neurotensina, angiotensina II, polipeptide intestinale vasoattivo, gastrina, vasopressina, ed altri. Il tratto gastrointestinale contiene circa l 80% del quantitativo totale di serotonina. Durante la chemioterapia le cellule enterocromaffini che tappezzano il tratto gastrointestinale sono danneggiate e rilasciano serotonina. Questa va a stimolare i neuroni afferenti vagali che attivano il centro del vomito o attivano direttamente la CTZ. Il meccanismo d azione degli antagonisti dei recettori 5-HT3 è sconosciuto, sembra che presentino sia un effetto periferico che un effetto centrale. Gli inibitori dei recettori 5-HT3 bloccano i recettori della serotonina e conseguentemente la cascata neuronale di eventi che portano a nausea e vomito. L obiettivo della trattamento è quello di prevenire completamente la nausea o il vomito da chemioterapia (CINV). La CINV può essere acuta, se si presenta entro le 24 ore dopo l inizio della chemioterapia, ritardata quando persiste per sei-sette giorni dopo la chemioterapia o anticipatoria se i sintomi si manifestano prima della somministrazione dei chemioterapici. Quest ultima compare generalmente quando una precedente chemioterapia ha causato nausea e vomito gravi, ed è considerata una risposta condizionata. I chemioterapici possono essere classificati come altamente, moderatamente o lievemente emetizzanti. Palonosetron è un antagonista selettivo ad elevata affinità per i recettori 5-HT3, il quinto commercializzato in Italia, autorizzato dall EMEA con procedura centralizzata per la prevenzione della nausea e del vomito acuti associati a chemioterapia altamente emetogena e per la prevenzione della nausea e del vomito associati a chemioterapia oncologica moderatamente emetogena. Palonosetron è commercializzato in fiale da 0.25 mg.
2 Rispetto ad altri antagonisti 5-HT3, quali ondansetron o tropisetron, ha dimostrato di avere in vitro un affinità molto più elevata per il recettore. Circa il 50% della dose somministrata ev di palonosetron è metabolizzata nel fegato, ed il 40% della dose di farmaco si ritrova immodificato nelle urine. Palosetron presenta un emivita di eliminazione plasmatica di 40 ore. Sembra che la farmacocinetica non sia influenzata da fattori quali: età, disfunzione epatica o lieve-moderata insufficienza renale, tuttavia l esposizione sistemica totale aumenta del 28% nei pazienti con insufficienza renale severa. L efficacia clinica del farmaco è stata testata in tre studi clinici principali, in uno studio dose-risposta e in uno studio dopo cicli ripetuti di chemioterapia (1). Nello studio dose risposta è stato stabilito che il dosaggio efficace è compreso tra mg. I tre studi principali, di non inferiorità, multicentrici randomizzati in doppio cieco ed a tre bracci, di fase III hanno valutato efficacia e sicurezza di due dosaggi di palonosetron ev vs ondansetron o dolasetron. Nausea e vomito da chemioterapia moderatamente emetizzante Il primo studio (2) ha arruolato 563 pazienti naive e non naive (58% circa) alla chemioterapia, e destinati a ricevere una terapia moderatamente emetogena: ciclofosfamide e doxorubicina i farmaci più utilizzati. I pazienti sono stati randomizzati ad uno dei seguenti trattamenti: palonosetron 0,25 mg, palonosetron 0,75 mg oppure ondansetron 32 mg, in singola dose per via endovenosa, prima del ciclo di chemioterapia. A nessun paziente è stato somministrato un corticosteroide prima del trattamento. Dopo la chemioterapia, a discrezione del clinico, è stato permesso l uso di un farmaco di salvataggio. L end-point principale di efficacia era rappresentato dalla frazione di pazienti che raggiungevano una risposta completa (CR: definita come nessun episodio di vomito e nessun ricorso a farmaci di salvataggio) nelle prime 24 successive alla terapia (fase acuta). Sono stati valutati come end point secondari la frazione di pazienti con una CR durante la fase ritardata e nel periodo complessivo (0-120 ore) seguente alla chemioterapia, la frazione di pazienti con controllo completo (CC: nessun episodio di vomito, nessuna sensazione di nausea severa, nessun ricorso a farmaci di salvataggio) in fase acuta, ritardata, complessiva, il tempo all insuccesso del trattamento (lasso di tempo per il verificarsi del primo episodio emetico o del primo utilizzo di un farmaco di salvataggio). L efficacia è stata valutata sia mediante un analisi intention to treat (ITT) che da un analisi per protocol (PP). I due dosaggi di palonosetron venivano considerati non inferiori al trattamento di confronto se la differenza nel tasso di risposta (CR) non avesse superato il 15% (margine inferiore dell intervallo di confidenza al 97,5%). Secondo l analisi ITT entrambi i dosaggi di palonosetron si sono dimostrati non inferiori ad ondansetron nella CR in fase acuta (81% palonosetron 0.25 mg; 73.5% palonosetron 0.75 mg; 68.6% ondansetron 32 mg). Relativamente agli end-point secondari: entrambe le dosi di palonosetron si sono dimostrate efficaci almeno quanto ondansetron nelle risposte complete durante il periodo di emesi ritardata (giorno 2-5) (74.1%; 64.6%; 55.1%) e complessivamente (0-120 h) (69.3%; 58.7%; 50.3%). Il tempo all insuccesso del trattamento era significativamente più prolungato in seguito alla terapia con palonosetron 0.25 mg rispetto a ondansetron (p<0.001). Nel secondo studio (3) 592 pazienti in terapia con farmaci moderatamente emetogeni (per la maggior parte dei pazienti il ciclo era costituito da antraciclina + ciclofosfamide) sono stati randomizzati a ricevere palonosetron ev in dose singola di 0.25 mg o 0.75 mg oppure dolasetron ev in dose singola di 100 mg. Con un emendamento successivo era permessa la somministrazione, a discrezione del clinico, di una singola dose di 20 mg di desametasone, 15 minuti prima della chemioterapia (5% dei pazienti ne hanno beneficiato). Sono stati inclusi nello studio pazienti naive (67%) e non-naive alla chemioterapia, con esperienza al massimo di nausea di grado moderato. Gli end-point primari e secondari erano gli stessi dello studio precedente. I pazienti sono stati valutati sia mediante una analisi ITT (n=569), sia mediante un analisi PP. Lo studio ha confermato la non inferiorità di entrambi i dosaggi di palonosetron vs. ondansetron nella CR in fase acuta (palonosetron 0,25 mg: 63%, palonosetron 0,75 mg: 57,1%, dolasetron 100 mg: 52,9%). Una quantità maggiore di risposte complete si era verificata anche durante il periodo di emesi ritardata (54% per palonosetron 0.25 mg; 56.6% palonosetron 0.75 mg; 38.7% dolasetron 100 mg). L analisi per sottogruppi ha evidenziato che pazienti non-naive presentano un incremento delle CR nel periodo complessivo (palonosetron 0.25 mg 67.7% vs 60.5%; dolasetron 100 mg 65.2% vs 46.4%) rispetto ai pazienti naive. La scelta di reclutare soggetti che non abbiano avuto esperienza di nausea se non di grado moderato, potrebbe aver selezionato pazienti soggetti ad un rischio inferiore di sviluppare nausea o vomito successivi a chemioterapia. Confrontando i pazienti che hanno ricevuto un corticosteroide rispetto a quelli che invece non l hanno ricevuto si sono osservati risultati in favore dell associazione palonosetron 0.25 mg + desametasone nelle CR (palonosetron 0.25 mg + desametasone 72.7% vs palonosetron 0.25 mg 62.4%; dolasetron 100 mg + desametasone 62.5% vs dolasetron 100 mg 52.5%) (si tenga conto che solo il 5% dei pazienti ha assunto desametasone).
3 Tutti e due gli studi hanno subito significative modifiche al disegno in corso d opera: emendamenti sono stati formulati relativamente ai criteri di eleggibilità, definizione dell end point primario, metodo di randomizzazione, uso di farmaci concomitanti. Inoltre, in entrambi gli studi gli antiserotoninergici non sono stati associati, come avrebbero dovuto, col desametasone nella profilassi dell emesi acuta e non veniva somministrata una profilassi per l emesi ritardata. In aggiunta, molti pazienti erano pretrattati con precedente esperienza di nausea e vomito acuti e ritardati indotti da chemioterapia. Nausea e vomito da chemioterapia altamente emetizzante Uno studio randomizzato, in doppio cieco, pubblicato di recente (4) di non inferiorità condotto su 667 pazienti sottoposti a chemioterapia altamente emetizzante, ha confrontato l efficacia di una singola dose di due diversi dosaggi di palonosetron (0.25 mg e 0.75 mg) vs ondansetron 32 mg prima del ciclo chemioterapico nel prevenire nausea e vomito indotti da chemioterapia altamente emetogena. Gli endpoint principali e secondari erano identici a quelli degli studi precedenti. Per l analisi di efficacia principale è stata utilizzata una coorte ITT di pazienti (n=667). La maggior parte di questi pazienti era naive alla chemioterapia (59%), e circa due terzi dei pazienti avevano ricevuto un pretrattamento con desametasone. Gli agenti chemioterapici più utilizzati sono stati cisplatino (dose mediana 80 mg/m 2 ) e ciclofosfamide. Gli autori dello studio hanno presentato i risultati suddividendo i dati relativi all intera popolazione ITT studiata e quelli relativi alla popolazione ITT che aveva ricevuto il pretrattamento con desametasone. Nella popolazione ITT completa, entrambi i dosaggi di palonosetron sono risultati non inferiori a ondansetron (percentuale di CR: palonosetron 0,75 mg: 59,2%, palonosetron 0,25 mg: 65,5%, ondansetron 32 mg: 57%). Palonosetron ha ottenuto una percentuale numericamente maggiore di CR rispetto ad ondansetron durante le fasi di emesi ritardata (45.5% palonosetron 0.25 mg, 48% palonosetron 0.75 mg, 38.9% ondansetron) e complessiva. Nessuna differenza significativa si e dimostrata tra i gruppi nelle percentuali di CC durante tutti i periodi cumulativi, e nemmeno nel tempo all insuccesso del trattamento. Nel sottogruppo di pazienti che avevano ricevuto anche desametasone (67% circa del totale), molti dei quali naive alla chemioterapia (61.9%) si e osservato un numero più elevato nelle risposte complete, durante la fase acuta, nei bracci palonosetron + desametasone rispetto al braccio ondansetron + desametasone (64.7% palonosetron 0.25 mg; 62.7% palonosetron 0.75 mg; 55.8% ondansetron). Uno studio di supporto citato dall EMEA (1), multicentrico, in aperto, ha valutato la sicurezza a piu lungo termine di palonosetron al dosaggio di 0.75 mg ev per la prevenzione della nausea e del vomito associati a cicli ripetuti di chemioterapia. Sono stati arruolati in questo studio pazienti precedentemente inseriti nei tre studi precedenti, per i quali era previsto almeno un ulteriore ciclo di chemioterapia. Sono stati arruolati 905 pazienti per un totale di 1733 cicli. Lo studio non ha evidenziato problemi particolari di sicurezza. L EMEA evidenzia una serie di carenze metodologiche nel piano clinico del farmaco. I dati relativi all emesi ritardata devono essere esaminati con cautela, innanzitutto perché nei trial sono stati considerati come end-point secondari ed inoltre perché i trattamenti di confronto utilizzati non sono stati somministrati a dosi adeguate per controllare l emesi ritardata. Nei due studi con chemioterapia moderatamente emetogena, inoltre, manca quasi totalmente il trattamento con steroidi, considerati di elezione per la prevenzione di questo tipo di emesi. Un recente update delle Linee guida ASCO (5) per l uso dei farmaci antiemetici in oncologia riporta che tutti gli antagonisti dei recettori 5HT3, ai dosaggi terapeuticamente analoghi, sono da considerarsi equivalenti per il loro profilo di efficacia e di sicurezza e possono essere considerati intercambiabili. Riguardo specificatamente al palonosetron, l Update Committee sottolinea che, sebbene il farmaco abbia riportato alcuni risultati numericamente positivi in alcuni degli end-point secondari dei tre studi registrativi, tutti e tre gli studi avevano un obiettivo di non inferiorità e sono quindi necessari studi prospettici disegnati specificatamente con un obiettivo di superiorità per poter affermare che palonosetron sia preferibile agli altri antagonisti dei recettori 5HT3. Tollerabilità: In genere palonosetron è ben tollerato e gli effetti collaterali rilevati dagli studi sono, per la maggior parte di intensità moderata e non correlati al trattamento. Gli eventi avversi associati a palonosetron sono simili a quelli dei farmaci della stessa classe per natura, frequenza, durata ed intensità. In particolare mal di testa e costipazione sono gli eventi maggiormente osservati. L incidenza di reazioni avverse serie era bassa in tutti gli studi e nessuna sembrava essere correlata al trattamento in studio. Non è stata osservata alcuna differenza rilevante relativamente ai risultati dei test di laboratorio, variazione dei segni vitali ed ECG. Le variazioni dell intervallo QT all elettrocardiogramma non sono risultate differenti da quelle osservate per ondansetron e dolasetron. Conclusioni
4 Palonosetron è un antagonista a lunga emivita selettivo e ad elevata affinità per i recettori 5-HT 3. Il dosaggio efficace è compreso tra 0,25 e 6 mg. E indicato per la prevenzione della nausea e del vomito acuti associati a chemioterapia altamente emetogena e per la prevenzione della nausea e del vomito associati a chemioterapia oncologica moderatamente emetogena. L efficacia clinica del farmaco è stata testata in tre studi clinici principali di non inferiorità in pazienti sottoposti a chemioterapia altamente o moderatamente emetogena (1,2,3,4). In tutti gli studi veniva definita una risposta completa (assenza di emesi e nessuna terapia di supporto a 24 h dalla chemioterapia) ed il controllo completo della sintomatologia, ovvero nessun episodio di emesi, assenza di terapia di supporto e di nausea nelle fasi acuta, ritardata e totale nelle 120 h successive alla terapia. Nei due studi con chemioterapia moderatamente emetogena 563 e 592 pazienti hanno ricevuto in singola dose palonosetron 0,25 o 0,75 mg o ondansetron 32 mg (I studio) o dolasetron 100 mg (II studio) prima della chemioterapia (1,2,3). Nel primo studio non venivano somministrati steroidi, nel secondo a seguito di un emendamento è stata consentita la somministrazione di 20 mg di desametasone 15 minuti prima della chemioterapia; soltanto il 5% dei pazienti ne ha però beneficiato. L efficacia a 24 h è risultata simile in entrambi i casi per palonosetron 0,25 mg vs i trattamenti di confronto; a 120 h palonosetron ha dimostrato un trend di maggiori percentuali di successo. Tutti e due gli studi hanno subito significative modifiche al disegno durante lo svolgimento: emendamenti sono stati formulati relativamente ai criteri di eleggibilità, definizione dell end-point primario, metodo di randomizzazione, uso di farmaci concomitanti. In entrambi gli studi non è stata prevista l associazione, come previsto dalle linee guida, col desametasone nella profilassi dell emesi acuta e non veniva somministrata una profilassi per l emesi ritardata. Uno studio randomizzato, in doppio cieco, su 667 pazienti sottoposti a chemioterapia altamente emetizzante, ha confrontato l efficacia di una singola dose di due diversi dosaggi di palonosetron (0.25 mg e 0.75 mg) vs ondansetron 32 mg prima del ciclo (4). La maggior parte di questi pazienti era naive alla chemioterapia (59%), e circa due terzi dei pazienti avevano ricevuto un pretrattamento dopo 24h, mentre palonosetron è risultato superiore ad ondansetron durante le fasi di emesi ritardata e complessiva. Nel sottogruppo di pazienti che avevano ricevuto anche desametasone si e osservato un numero più elevato di risposte complete, durante la fase acuta, con palonosetron. Palonosetron risulta generalmente ben tollerato. Cefalea e costipazione sono gli eventi maggiormente osservati. Allo stato attuale delle cose risultano necessari studi di superiorità per evidenziare un eventuale ruolo peculiare di questo farmaco rispetto ad altri agenti della stessa classe. I costi della terapia con palonosetron, inoltre, sono superiori rispetto agli altri antagonisti 5HT 3 presenti in PTORV. Bibliografia: 1. Palonosetron (Aloxi ). European Pubblic Assessment Report- Scientific Discussion (accesso del ) 2. Gralla R. et al., Annals of Oncology 2003, 14: Eisenberg P. et al., Cancer 2003, 98: Aapro M.S. et al., Annals of Oncology 2006, Advance Access 14 June 5. American Society of Clinical Oncology Guideline for Antiemetics in Oncology: Update Costi comparativi per emesi acuta da chemioterapia moderatamente o altamente emetogena: Costo del trattamento con palonosetron PRINCIPIO ATTIVO SPECIALITA DOSAGGIO DA SCHEDA TECNICA COSTO DEL TRATTAMENTO ALL OSPEDALE Palonosetron Aloxi 1 fl 0.25 mg in bolo ev prima della chemioterapia (1 fl) 43,21* *Prezzo massimo di cessione al SSN da GU 54 del ex factory IVA esclusa comprensivo dello sconto obbligatorio per le strutture pubbliche del SSN del 36,83% Costo di altri farmaci PRINCIPIO ATTIVO SPECIALITA DOSAGGIO DA SCHEDA TECNICA COSTO DEL TRATTAMENTO ALL OSPEDALE Ondansetron Zofran 1 fl 8 mg 8-32 mg ev lenta 9,56-38,24^ Granisetron Kytril 1 fl 3 mg 3-9 mg ev lenta 14,52 43,56^ Tropisetron Navoban iniett 1 fl 5 mg 5 mg ev lenta 10.08** ^Prezzo 50% del prezzo al pubblico IVA esclusa da listino ditta GSK e Roche aggiornati al 1/3/2007
5 ** Prezzo massimo di cessione al SSN ex factory IVA esclusa comprensivo dello sconto obbligatorio per le strutture pubbliche del SSN del 63,29% da listino ditta Novartis aggiornato al 1/3/2007 Ultima revisione del testo: Aprile 2007
Linee guida 2016 per la terapia antiemetica in oncologia
 Linee guida 2016 per la terapia antiemetica in oncologia Fonte: Multinational Association of Supportive Care in Cancer (MASCC) European Society for Medical Oncology (ESMO) Antiemetic Guideline 2016 Testi
Linee guida 2016 per la terapia antiemetica in oncologia Fonte: Multinational Association of Supportive Care in Cancer (MASCC) European Society for Medical Oncology (ESMO) Antiemetic Guideline 2016 Testi
ETICA E RICERCA per assistere e curare in oncologia
 III CONGRESSO NAZIONALE AIIAO Ancona 29-30-31 maggio 2014 ETICA E RICERCA per assistere e curare in oncologia Buone pratiche assistenziali Nursing ed emesi Buone pratiche assistenziali: Nursing ed emesi
III CONGRESSO NAZIONALE AIIAO Ancona 29-30-31 maggio 2014 ETICA E RICERCA per assistere e curare in oncologia Buone pratiche assistenziali Nursing ed emesi Buone pratiche assistenziali: Nursing ed emesi
Commissione Regionale Farmaco LAPATINIB
 Commissione Regionale Farmaco (D.G.R. 1540/2006 e D.G.R. 490 dell 11 aprile 2011) Documento relativo a: LAPATINIB Settembre 2011 Indicazioni registrate Lapatinib Il lapatinib ha ricevuto la seguente estensione
Commissione Regionale Farmaco (D.G.R. 1540/2006 e D.G.R. 490 dell 11 aprile 2011) Documento relativo a: LAPATINIB Settembre 2011 Indicazioni registrate Lapatinib Il lapatinib ha ricevuto la seguente estensione
Antiemetici: aspetti generali
 Vomito Evento fisico che risulta nell evacuazione forzata dei contenuti gastrici attraverso la bocca Spesso preceduto da nausea (sensazione di disgusto o di vomito incipiente) Puo essere positivo (persino
Vomito Evento fisico che risulta nell evacuazione forzata dei contenuti gastrici attraverso la bocca Spesso preceduto da nausea (sensazione di disgusto o di vomito incipiente) Puo essere positivo (persino
Trattamento dell'emesi in chemioterapia ''Granisetron''
 Università degli Studi di Padova Facoltà di Farmacia Trattamento dell'emesi in chemioterapia ''Granisetron'' di Raniero Impagliatelli Relatore: prof. Francesco Dall'Acqua A. A. 2006-07 1. Prospetto delle
Università degli Studi di Padova Facoltà di Farmacia Trattamento dell'emesi in chemioterapia ''Granisetron'' di Raniero Impagliatelli Relatore: prof. Francesco Dall'Acqua A. A. 2006-07 1. Prospetto delle
Specialità: Mabthera (Roche SpA) Forma farmaceutica: 1fl ev 500mg - Prezzo: euro fl 10ml 100mg - Prezzo: euro
 RITUXIMAB Linfoma non-hodgkin: La terapia di mantenimento per pazienti con linfoma follicolare ricaduto/refrattario che rispondono a terapia di induzione con chemioterapia con o senza Rituximab. (09-01-2007)
RITUXIMAB Linfoma non-hodgkin: La terapia di mantenimento per pazienti con linfoma follicolare ricaduto/refrattario che rispondono a terapia di induzione con chemioterapia con o senza Rituximab. (09-01-2007)
Linee Guida AIOM Terapia Antiemetica
 Linee Guida AIOM 2006 Terapia Antiemetica Aggiornamento: dicembre 2006 Responsabile: Fausto Roila Estensori: Carlo Basurto Silvana Chiara Elisabetta Campora M. Cristina Locatelli I pazienti sottoposti
Linee Guida AIOM 2006 Terapia Antiemetica Aggiornamento: dicembre 2006 Responsabile: Fausto Roila Estensori: Carlo Basurto Silvana Chiara Elisabetta Campora M. Cristina Locatelli I pazienti sottoposti
Farmaci biologici nel trattamento della psoriasi: differenze nei criteri di valutazione tra USA e UE.
 Farmaci biologici nel trattamento della psoriasi: differenze nei criteri di valutazione tra USA e UE. Renato Bertini Malgarini, Giuseppe Pimpinella, Luca Pani 10 dicembre 2012- Istituto Superiore di Sanità
Farmaci biologici nel trattamento della psoriasi: differenze nei criteri di valutazione tra USA e UE. Renato Bertini Malgarini, Giuseppe Pimpinella, Luca Pani 10 dicembre 2012- Istituto Superiore di Sanità
CAPIRE E CURARE L EMESI
 CAPIRE E CURARE L EMESI dott.ssa Claudia Corbo U.O. Oncologia Ospedale Sacro Cuore di Gesù Fatebenefratelli - Benevento Benevento 9 giugno 2011 Nel paziente neoplastico l emesi può essere: determinata
CAPIRE E CURARE L EMESI dott.ssa Claudia Corbo U.O. Oncologia Ospedale Sacro Cuore di Gesù Fatebenefratelli - Benevento Benevento 9 giugno 2011 Nel paziente neoplastico l emesi può essere: determinata
Lezione 2 Come leggere l articolo scientifico
 Analisi critica della letteratura scientifica Lezione 2 Come leggere l articolo scientifico Struttura dell articolo Introduzione Metodi Risultati e Discussione Perché è stato fatto? Come è stato condotto?
Analisi critica della letteratura scientifica Lezione 2 Come leggere l articolo scientifico Struttura dell articolo Introduzione Metodi Risultati e Discussione Perché è stato fatto? Come è stato condotto?
Studio SENIORS Trial sull effetto di nebivololo su mortalità e ospedalizzazioni per malattie cardiovascolari in pazienti anziani con insufficienza
 Trial sull effetto di nebivololo su mortalità e ospedalizzazioni per malattie cardiovascolari in pazienti anziani con insufficienza cardiaca (1) Introduzione (1) Età media dei pazienti con insufficienza
Trial sull effetto di nebivololo su mortalità e ospedalizzazioni per malattie cardiovascolari in pazienti anziani con insufficienza cardiaca (1) Introduzione (1) Età media dei pazienti con insufficienza
Documento PTR n. 119 relativo a:
 Direzione Generale Sanità e Politiche Sociali Commissione Regionale del Farmaco (D.G.R. 1540/2006, 2129/2010 e 490/2011) Documento PTR n. 119 relativo a: MEDICINALI ORIGINATOR E BIOSIMILARI DELL ERITROPOIETINA
Direzione Generale Sanità e Politiche Sociali Commissione Regionale del Farmaco (D.G.R. 1540/2006, 2129/2010 e 490/2011) Documento PTR n. 119 relativo a: MEDICINALI ORIGINATOR E BIOSIMILARI DELL ERITROPOIETINA
RIVISTA: lnt Journal of lmpotence Research (2006) 18, MJ. Dresser, D. Desai, S. Gidwani, AD. Seftel, NB. Modi O B I E T T I V I
 I D E N T I F I C A T I V O A R T I C O L O TITOLO: Dapoxetine, a novel treatment for premature ejaculation, does not have pharmacokinetic interactions with phosphodiesterase-5 inhibitors Dapoxetina, nuovo
I D E N T I F I C A T I V O A R T I C O L O TITOLO: Dapoxetine, a novel treatment for premature ejaculation, does not have pharmacokinetic interactions with phosphodiesterase-5 inhibitors Dapoxetina, nuovo
PROTOCOLLO PER IL CONTROLLO DELLA NAUSEA E DEL VOMITO DA TERAPIA ONCOLOGICA PRESSO L A.S.P. DI ENNA
 Pagina 1 di 9 PROTOCOLLO PER IL CONTROLLO DELLA NAUSEA E DEL VOMITO DA TERAPIA ONCOLOGICA PRESSO L A.S.P. DI ENNA Nome/Funzione Data Firma Redazione Dott.ssa Giuseppa Cinzia Di Martino Responsabile UFA
Pagina 1 di 9 PROTOCOLLO PER IL CONTROLLO DELLA NAUSEA E DEL VOMITO DA TERAPIA ONCOLOGICA PRESSO L A.S.P. DI ENNA Nome/Funzione Data Firma Redazione Dott.ssa Giuseppa Cinzia Di Martino Responsabile UFA
Antiemetici: aspetti generali
 Emesi Evento fisico che risulta nell evacuazione forzata dei contenuti gastrici attraverso la bocca Puo essere auto-indotta (bulimia) o involontaria (associata ad es. a influenza, gravidanza, chinetosi,
Emesi Evento fisico che risulta nell evacuazione forzata dei contenuti gastrici attraverso la bocca Puo essere auto-indotta (bulimia) o involontaria (associata ad es. a influenza, gravidanza, chinetosi,
DOCUMENTO DI CONFRONTO DEI COSTI TRA PRINCIPI ATTIVI APPARTENENTI A CATEGORIE TERAPEUTICHE AD ELEVATO IMPATTO DI SPESA TERRITORIALE
 1/12 DOCUMENTO DI CONFRONTO DEI COSTI TRA PRINCIPI ATTIVI APPARTENENTI A CATEGORIE TERAPEUTICHE AD ELEVATO IMPATTO DI SPESA TERRITORIALE PREMESSA Nel 2014 la spesa farmaceutica territoriale della Regione
1/12 DOCUMENTO DI CONFRONTO DEI COSTI TRA PRINCIPI ATTIVI APPARTENENTI A CATEGORIE TERAPEUTICHE AD ELEVATO IMPATTO DI SPESA TERRITORIALE PREMESSA Nel 2014 la spesa farmaceutica territoriale della Regione
Prima dei 15 anni il dosaggio di paracetamolo dipende dal peso del bambino e deve essere compreso tra i 10 e i 15 mg/kg/dose; l intervallo tra una
 1 2 Prima dei 15 anni il dosaggio di paracetamolo dipende dal peso del bambino e deve essere compreso tra i 10 e i 15 mg/kg/dose; l intervallo tra una dose e l altra deve essere sempre almeno di 4 ore.
1 2 Prima dei 15 anni il dosaggio di paracetamolo dipende dal peso del bambino e deve essere compreso tra i 10 e i 15 mg/kg/dose; l intervallo tra una dose e l altra deve essere sempre almeno di 4 ore.
Antiemetici: aspetti generali
 Emesi Evento fisico che risulta nell evacuazione forzata dei contenuti gastrici attraverso la bocca Puo essere auto-indotta (bulimia) o involontaria (associata ad es. a influenza, gravidanza, chinetosi,
Emesi Evento fisico che risulta nell evacuazione forzata dei contenuti gastrici attraverso la bocca Puo essere auto-indotta (bulimia) o involontaria (associata ad es. a influenza, gravidanza, chinetosi,
la ricerca infermieristica
 Dall esperienza un metodo: la ricerca infermieristica C. Forni CPSE responsabile Centro Ricerca Servizio Assistenza Istituti Ortopedici Rizzoli Bologna Un esperienza. Istituto Ortopedico Rizzoli Bologna
Dall esperienza un metodo: la ricerca infermieristica C. Forni CPSE responsabile Centro Ricerca Servizio Assistenza Istituti Ortopedici Rizzoli Bologna Un esperienza. Istituto Ortopedico Rizzoli Bologna
PROSPETTIVE DI RICERCA INDIPENDENTE E DI RISULTATO. Fausto Roila Oncologia Medica, Perugia
 PROSPETTIVE DI RICERCA INDIPENDENTE E DI RISULTATO Fausto Roila Oncologia Medica, Perugia LA NECESSITA DI UNA RICERCA INDIPENDENTE L industria promuove studi di sviluppo del farmaco per registrarlo (talora
PROSPETTIVE DI RICERCA INDIPENDENTE E DI RISULTATO Fausto Roila Oncologia Medica, Perugia LA NECESSITA DI UNA RICERCA INDIPENDENTE L industria promuove studi di sviluppo del farmaco per registrarlo (talora
Maria Antonietta Lepore Indagini sperimentali sui nuovi anticoagulanti orali. Meccanismo di azione e interazioni farmacologiche
 A06 Maria Antonietta Lepore Indagini sperimentali sui nuovi anticoagulanti orali Meccanismo di azione e interazioni farmacologiche Copyright MMXV Aracne editrice int.le S.r.l. www.aracneeditrice.it info@aracneeditrice.it
A06 Maria Antonietta Lepore Indagini sperimentali sui nuovi anticoagulanti orali Meccanismo di azione e interazioni farmacologiche Copyright MMXV Aracne editrice int.le S.r.l. www.aracneeditrice.it info@aracneeditrice.it
ALLEGATO III RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO, ETICHETTATURA E FOGLIO ILLUSTRATIVO
 ALLEGATO III RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO, ETICHETTATURA E FOGLIO ILLUSTRATIVO 17 18 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Kytril e denominazioni
ALLEGATO III RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO, ETICHETTATURA E FOGLIO ILLUSTRATIVO 17 18 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Kytril e denominazioni
Scheda di valutazione
 Farmaci antiemetici antiserotoninergici Scheda di valutazione Individuazione della sovrapponibilità clinica negli usi prevalenti e delle eventuali indicazioni esclusive Rapporto tecnico a cura del gruppo
Farmaci antiemetici antiserotoninergici Scheda di valutazione Individuazione della sovrapponibilità clinica negli usi prevalenti e delle eventuali indicazioni esclusive Rapporto tecnico a cura del gruppo
RITUXIMAB in associazione a metotressato è indicato per il trattamento dell artrite reumatoide attiva di grado severo in pazienti adulti.
 RITUXIMAB in associazione a metotressato è indicato per il trattamento dell artrite reumatoide attiva di grado severo in pazienti adulti. (28-02-2007) Specialità: Mabthera (Roche SpA) Forma farmaceutica:
RITUXIMAB in associazione a metotressato è indicato per il trattamento dell artrite reumatoide attiva di grado severo in pazienti adulti. (28-02-2007) Specialità: Mabthera (Roche SpA) Forma farmaceutica:
GAZZETTA UFFICIALE DELLA REPUBBLICA ITALIANA Serie generale n. 115
 AGENZIA ITALIANA DEL FARMACO DETERMINAZIONE 9 Maggio 2007 Modifica degli stampati dei medicinali contenenti farmaci antinfiammatori non steroidei (FANS) non selettivi per uso sistemico - ATC M01A. omissis
AGENZIA ITALIANA DEL FARMACO DETERMINAZIONE 9 Maggio 2007 Modifica degli stampati dei medicinali contenenti farmaci antinfiammatori non steroidei (FANS) non selettivi per uso sistemico - ATC M01A. omissis
Gruppo di lavoro per l appropriatezza prescrittiva ospedale/territorio Documento finale - giugno 2014
 Gruppo di lavoro per l appropriatezza prescrittiva ospedale/territorio Documento finale - giugno 2014 Prescrizione di farmaci Classe C10AA (inibitori della HMG CoA reduttasi) L indicazione regionale è
Gruppo di lavoro per l appropriatezza prescrittiva ospedale/territorio Documento finale - giugno 2014 Prescrizione di farmaci Classe C10AA (inibitori della HMG CoA reduttasi) L indicazione regionale è
MINI-REPORT - Tafluprost
 MINI-REPORT - Tafluprost PRINCIPIO ATTIVO: Tafluprost NOME COMMERCIALE: Saflutan (Merck Sharp & Dohme) FORMULAZIONE: collirio monodose- 30 fl 15 mcg/ml 0,3-priva di conservante (unico in commercio in Italia)
MINI-REPORT - Tafluprost PRINCIPIO ATTIVO: Tafluprost NOME COMMERCIALE: Saflutan (Merck Sharp & Dohme) FORMULAZIONE: collirio monodose- 30 fl 15 mcg/ml 0,3-priva di conservante (unico in commercio in Italia)
SCHEDA DI VALUTAZIONE PER L INSERIMENTO DI FARMACI NON PRESENTI NEL PTR
 RICHIESTA DI INSERIMENTO IN PTR DI DEFERASIROX ATC V03AC03 (EXJADE ) Presentata da : Dott. Carlo Floris, componente della Commissione PTR Commissione Prontuario terapeutico provinciale ASl n 6 Per le seguenti
RICHIESTA DI INSERIMENTO IN PTR DI DEFERASIROX ATC V03AC03 (EXJADE ) Presentata da : Dott. Carlo Floris, componente della Commissione PTR Commissione Prontuario terapeutico provinciale ASl n 6 Per le seguenti
Università degli studi di Genova Facoltà di Medicina e Chirurgia Corso di Laurea in Medicina e Chirurgia
 Università degli studi di Genova Facoltà di Medicina e Chirurgia Corso di Laurea in Medicina e Chirurgia Relatori: Chiar.ma Prof.ssa Antonietta Piana Chiar.mo Dott. Andrea Stimamiglio Candidata: Oliveri
Università degli studi di Genova Facoltà di Medicina e Chirurgia Corso di Laurea in Medicina e Chirurgia Relatori: Chiar.ma Prof.ssa Antonietta Piana Chiar.mo Dott. Andrea Stimamiglio Candidata: Oliveri
EMR Merck KGaA, Darmstadt, Germania. Fase clinica IIIb
 1/7 Sinossi Titolo della Numero della NEXT NSCLC ErbituX Trial Sperimentazione in aperto, randomizzata, multinazionale, di fase IIIb, di valutazione dell attività e della sicurezza di cetuximab come terapia
1/7 Sinossi Titolo della Numero della NEXT NSCLC ErbituX Trial Sperimentazione in aperto, randomizzata, multinazionale, di fase IIIb, di valutazione dell attività e della sicurezza di cetuximab come terapia
Ciascuna compressa rivestita con film contiene 2 mg di granisetron (in forma di cloridrato).
 1. DENOMINAZIONE DEL MEDICINALE Kytril compresse rivestite con film da 1 mg Kytril compresse rivestite con film da 2 mg 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 2.1 Descrizione generale 2.2 Composizione
1. DENOMINAZIONE DEL MEDICINALE Kytril compresse rivestite con film da 1 mg Kytril compresse rivestite con film da 2 mg 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA 2.1 Descrizione generale 2.2 Composizione
SCHEDA DI VALUTAZIONE PER L INSERIMENTO DI FARMACI NON PRESENTI NEL PTR ERLOTINIB
 RICHIESTA DI INSERIMENTO IN PTR DI ATC L01XE03 (TARCEVA ) Presentata da Componente Commissione Prontuario Terapeutico Regionale In data 13 Dicembre 2006 Per le seguenti motivazioni (sintesi): Tarceva non
RICHIESTA DI INSERIMENTO IN PTR DI ATC L01XE03 (TARCEVA ) Presentata da Componente Commissione Prontuario Terapeutico Regionale In data 13 Dicembre 2006 Per le seguenti motivazioni (sintesi): Tarceva non
RISPERIDONE formulazione im ( )
 RISPERIDONE formulazione im (18-10-2006) Specialità: Risperdal (Janssen Cilag) Forma farmaceutica: 1 fl 25 mg Prezzo: 165,69 1 fl 37,5 mg 213,80 1 fl 50 mg 267,24 Prezzo da banca dati Farmadati settembre
RISPERIDONE formulazione im (18-10-2006) Specialità: Risperdal (Janssen Cilag) Forma farmaceutica: 1 fl 25 mg Prezzo: 165,69 1 fl 37,5 mg 213,80 1 fl 50 mg 267,24 Prezzo da banca dati Farmadati settembre
Approccio Terapeutico all iperglicemia a digiuno e postprandiale. Irene Brandolin S.C. Medicina Interna E.O. Ospedali Galliera Savona, 23 Marzo 2013
 Approccio Terapeutico all iperglicemia a digiuno e postprandiale Irene Brandolin S.C. Medicina Interna E.O. Ospedali Galliera Savona, 23 Marzo 2013 La triade glicemica nella gestione del diabete Glicemia
Approccio Terapeutico all iperglicemia a digiuno e postprandiale Irene Brandolin S.C. Medicina Interna E.O. Ospedali Galliera Savona, 23 Marzo 2013 La triade glicemica nella gestione del diabete Glicemia
Bergamo, 06 Giugno Dr.ssa Chiricosta
 Progetto INFOLOGIC : Interazioni farmacologiche evitabili tra i farmaci prescritti in regime di SSN ai pazienti in politerapia, affetti da patologie croniche Bergamo, 06 Giugno 2014 - Dr.ssa Chiricosta
Progetto INFOLOGIC : Interazioni farmacologiche evitabili tra i farmaci prescritti in regime di SSN ai pazienti in politerapia, affetti da patologie croniche Bergamo, 06 Giugno 2014 - Dr.ssa Chiricosta
INFORMATI VACCINATI PROTETTI VACCINO EPATITE Β
 EPATITE B SEI SICURO DI USARE MISURE DI PREVENZIONE ADEGUATE PER PROTEGGERTI DALL EPATITE B? INFORMATI VACCINATI PROTETTI VACCINO EPATITE Β RICORDA CHE: L epatite B causa un infiammazione acuta del fegato,
EPATITE B SEI SICURO DI USARE MISURE DI PREVENZIONE ADEGUATE PER PROTEGGERTI DALL EPATITE B? INFORMATI VACCINATI PROTETTI VACCINO EPATITE Β RICORDA CHE: L epatite B causa un infiammazione acuta del fegato,
L aggiornamento pubblicato nel marzo del 2007 è stato integrato con la pubblicazione della prima lista di farmaci essenziali ad uso pediatrico
 Nel 1977, l Organizzazione Mondiale della Sanità (OMS) pubblica il primo report sui farmaci essenziali. Indicato con l acronimo WHO TRS 615, il report tecnico costituisce la prima lista di farmaci essenziali
Nel 1977, l Organizzazione Mondiale della Sanità (OMS) pubblica il primo report sui farmaci essenziali. Indicato con l acronimo WHO TRS 615, il report tecnico costituisce la prima lista di farmaci essenziali
AULA ROSSA STUDI CLINICI IN CORSO
 Terza Giornata Fiorentina dedicata ai pazienti con malattie mieloproliferative croniche AULA ROSSA STUDI CLINICI IN CORSO Che cosa è uno studio clinico e a cosa serve? Si definisce sperimentazione clinica,
Terza Giornata Fiorentina dedicata ai pazienti con malattie mieloproliferative croniche AULA ROSSA STUDI CLINICI IN CORSO Che cosa è uno studio clinico e a cosa serve? Si definisce sperimentazione clinica,
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA)
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Comunicazione diretta agli operatori sanitari relativa a reazioni avverse gravi conseguenti
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Comunicazione diretta agli operatori sanitari relativa a reazioni avverse gravi conseguenti
Colchicina nella prevenzione degli eventi cardiovascolari
 Revisione Cochrane 2016 Colchicina nella prevenzione degli eventi cardiovascolari Hemkens LG, Ewald H, Gloy VL, et al. Colchicine for prevention of cardiovascular events. Cochrane Database Syst Rev 2016;1:CD011047.
Revisione Cochrane 2016 Colchicina nella prevenzione degli eventi cardiovascolari Hemkens LG, Ewald H, Gloy VL, et al. Colchicine for prevention of cardiovascular events. Cochrane Database Syst Rev 2016;1:CD011047.
BEVACIZUMAB - AVASTIN
 giunta regionale Allegato B al Decreto n. 139 del 3 giugno 2015 pag. 1/8 Regione del Veneto Area Sanità e Sociale RACCOMANDAZIONI EVIDENCE BASED BEVACIZUMAB - AVASTIN Indicazione in esame: Bevacizumab
giunta regionale Allegato B al Decreto n. 139 del 3 giugno 2015 pag. 1/8 Regione del Veneto Area Sanità e Sociale RACCOMANDAZIONI EVIDENCE BASED BEVACIZUMAB - AVASTIN Indicazione in esame: Bevacizumab
Quali sono le novità nella terapia ormonale sostitutiva nell insufficienza delle ghiandole surrenaliche?
 ANDREA GIUSTINA Direttore Cattedra Endocrinologia Università degli Studi di Brescia Quali sono le novità nella terapia ormonale sostitutiva nell insufficienza delle ghiandole surrenaliche? Come da determinazione
ANDREA GIUSTINA Direttore Cattedra Endocrinologia Università degli Studi di Brescia Quali sono le novità nella terapia ormonale sostitutiva nell insufficienza delle ghiandole surrenaliche? Come da determinazione
SIEDP JOURNAL CLUB DIABETE. Maggio 2012
 SIEDP JOURNAL CLUB DIABETE Maggio 2012 Commento su: Insulin degludec, an ultra-longacting basal insulin, versus insulin glargine in basalbolus treatment with mealtime insulin aspart in type 1 diabetes
SIEDP JOURNAL CLUB DIABETE Maggio 2012 Commento su: Insulin degludec, an ultra-longacting basal insulin, versus insulin glargine in basalbolus treatment with mealtime insulin aspart in type 1 diabetes
L INDUZIONE MEDICA CONSISTE
 1 IN OSTETRICIA, L INDUZIONE MEDICA CONSISTE NELL UTILIZZO DI OSSITOCINA O DI PROSTAGLANDINE. GLI SVANTAGGI DEL TRAVAGLIO INDOTTO FARMACOLOGICAMENTE CONSISTONO IN: CONTRAZIONI DOLOROSE E TROPPO INTENSE
1 IN OSTETRICIA, L INDUZIONE MEDICA CONSISTE NELL UTILIZZO DI OSSITOCINA O DI PROSTAGLANDINE. GLI SVANTAGGI DEL TRAVAGLIO INDOTTO FARMACOLOGICAMENTE CONSISTONO IN: CONTRAZIONI DOLOROSE E TROPPO INTENSE
Gli Antagonisti degli oppiodi. Dr. S. Di Santo
 Gli Antagonisti degli oppiodi Dr. S. Di Santo Definizione - Un farmaco è detto antagonista quando, legandosi ad un recettore non lo attiva ma lo "blocca". - L'antagonista tende ad impedire all agonista
Gli Antagonisti degli oppiodi Dr. S. Di Santo Definizione - Un farmaco è detto antagonista quando, legandosi ad un recettore non lo attiva ma lo "blocca". - L'antagonista tende ad impedire all agonista
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA)
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA) Agosto 2012 Comunicazione diretta agli operatori sanitari sull associazione tra
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA) Agosto 2012 Comunicazione diretta agli operatori sanitari sull associazione tra
Allegato III. Modifiche ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo
 Allegato III Modifiche ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo Nota: Queste modifiche ai paragrafi pertinenti del Riassunto delle Caratteristiche
Allegato III Modifiche ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo Nota: Queste modifiche ai paragrafi pertinenti del Riassunto delle Caratteristiche
NERIDRONATO SODICO (12-09-2007)
 NERIDRONATO SODICO (12-09-2007) Specialità: Nerixia (Abiogen SpA) Forma Farmaceutica: 2fl inf.ev Dosaggio: 100 mg Prezzo: 89.00 1fl iniet. 25mg Prezzo: 14.65 Prezzo al pubblico da banca dati Farmadati
NERIDRONATO SODICO (12-09-2007) Specialità: Nerixia (Abiogen SpA) Forma Farmaceutica: 2fl inf.ev Dosaggio: 100 mg Prezzo: 89.00 1fl iniet. 25mg Prezzo: 14.65 Prezzo al pubblico da banca dati Farmadati
QUALI NOVITA NELLE RECENTI LINEE GUIDA DELLA INSUFFICIENZA CARDIACA?
 QUALI NOVITA NELLE RECENTI LINEE GUIDA DELLA INSUFFICIENZA CARDIACA? Dott. Cesare Albanese si dichiara assenza di conflitto di interessi LE PRINCIPALI NOVITA RISPETTO ALLE LINEE GUIDA ESC DEL 2012 (I)
QUALI NOVITA NELLE RECENTI LINEE GUIDA DELLA INSUFFICIENZA CARDIACA? Dott. Cesare Albanese si dichiara assenza di conflitto di interessi LE PRINCIPALI NOVITA RISPETTO ALLE LINEE GUIDA ESC DEL 2012 (I)
RICERCA E SVILUPPO DI NUOVI FARMACI
 RICERCA E SVILUPPO DI NUOVI FARMACI In passato le scoperte dei farmaci erano occasionali. Si trattava di sostanze di derivazione vegetale o animale STRATEGIE DI RICERCA: Quali sono i fattori che influenzano
RICERCA E SVILUPPO DI NUOVI FARMACI In passato le scoperte dei farmaci erano occasionali. Si trattava di sostanze di derivazione vegetale o animale STRATEGIE DI RICERCA: Quali sono i fattori che influenzano
MODULO PER LA RICHIESTA DI INSERIMENTO IN PRONTUARIO ASL AL
 Sede legale: Viale Giolitti,2 15033 Casale Monferrato (AL) Partita IVA/Codice Fiscale n. 02190140067 Alla Segreteria Scientifica della COMMISSIONE TERAPEUTICA AZIENDALE Presidente Dr.ssa Elide AZZAN Te.
Sede legale: Viale Giolitti,2 15033 Casale Monferrato (AL) Partita IVA/Codice Fiscale n. 02190140067 Alla Segreteria Scientifica della COMMISSIONE TERAPEUTICA AZIENDALE Presidente Dr.ssa Elide AZZAN Te.
Studio INFERMIERISTICO,
 Studio INFERMIERISTICO, osservazionale multicentrico di raccolta dati su nausea e vomito di Pazienti sottoposti a trattamento chemioterapico con farmaci altamente e moderatamente emetizzanti. Elenco persone
Studio INFERMIERISTICO, osservazionale multicentrico di raccolta dati su nausea e vomito di Pazienti sottoposti a trattamento chemioterapico con farmaci altamente e moderatamente emetizzanti. Elenco persone
SCHEDA DI VALUTAZIONE PER L INSERIMENTO DI FARMACI NON PRESENTI NEL PTR
 RICHIESTA DI INSERIMENTO IN PTR DI SILDENAFIL G04BE03 (REVATIO ) Presentata da Commissione Terapeutica Provinciale Sassari In data novembre 2008 Per le seguenti motivazioni (sintesi) Trattamento di pazienti
RICHIESTA DI INSERIMENTO IN PTR DI SILDENAFIL G04BE03 (REVATIO ) Presentata da Commissione Terapeutica Provinciale Sassari In data novembre 2008 Per le seguenti motivazioni (sintesi) Trattamento di pazienti
nella prevenzione della nausea e del vomito precoci e tardivi A cura del Gruppo Regionale Farmaci Oncologici (GReFO)
 Raccomandazioni evidence-based Aprepitant nella prevenzione della nausea e del vomito precoci e tardivi A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n.15 Settembre 2011
Raccomandazioni evidence-based Aprepitant nella prevenzione della nausea e del vomito precoci e tardivi A cura del Gruppo Regionale Farmaci Oncologici (GReFO) Raccomandazione d uso n.15 Settembre 2011
INTERAZIONI FARMACOLOGICHE
 INTERAZIONI FARMACOLOGICHE Università degli studi di Cagliari Facoltà di Medicina e Chirurgia Dipartimento di Neuroscienze B. B. Brodie Sezione Farmacologia Clinica Prof.ssa Maria Del Zompo INTERAZIONI
INTERAZIONI FARMACOLOGICHE Università degli studi di Cagliari Facoltà di Medicina e Chirurgia Dipartimento di Neuroscienze B. B. Brodie Sezione Farmacologia Clinica Prof.ssa Maria Del Zompo INTERAZIONI
PERUGIA INTERNATIONAL CANCER CONFERENCE VII
 PERUGIA INTERNATIONAL CANCER CONFERENCE VII MULTINATIONAL ASSOCIATION OF SUPPORTIVE CARE IN CANCER CONSENSUS CONFERENCE SULLA TERAPIA ANTIEMETICA PERUGIA, 29-31 marzo, 2004 Ultimo aggiornamento: 1 settembre
PERUGIA INTERNATIONAL CANCER CONFERENCE VII MULTINATIONAL ASSOCIATION OF SUPPORTIVE CARE IN CANCER CONSENSUS CONFERENCE SULLA TERAPIA ANTIEMETICA PERUGIA, 29-31 marzo, 2004 Ultimo aggiornamento: 1 settembre
Presentazione dei dati
 Presentazione dei dati Per ogni principio attivo, per il quale è stato possibile reperire informazioni riguardanti il passaggio nel latte materno, è stata creata una scheda monografica con informazioni
Presentazione dei dati Per ogni principio attivo, per il quale è stato possibile reperire informazioni riguardanti il passaggio nel latte materno, è stata creata una scheda monografica con informazioni
LA GESTIONE E LA PRESA IN CARICO DELLE REAZIONI ALLERGICHE ALESSIA ZARDINI INFERMIERA U.O. ONCOLOGIA OSPEDALE S. CUORE DON CALABRIA NEGRAR
 LA GESTIONE E LA PRESA IN CARICO DELLE REAZIONI ALLERGICHE ALESSIA ZARDINI INFERMIERA U.O. ONCOLOGIA OSPEDALE S. CUORE DON CALABRIA NEGRAR LINEE GUIDA NCCN Le reazioni allergiche vengono classificate in:
LA GESTIONE E LA PRESA IN CARICO DELLE REAZIONI ALLERGICHE ALESSIA ZARDINI INFERMIERA U.O. ONCOLOGIA OSPEDALE S. CUORE DON CALABRIA NEGRAR LINEE GUIDA NCCN Le reazioni allergiche vengono classificate in:
SCHEDA DI VALUTAZIONE PER L INSERIMENTO DI FARMACI NON PRESENTI NEL PTR DAPTOMICINA
 RICHIESTA DI INSERIMENTO IN PTR DI ATC J01XX09 (CUBICIN ) Presentata da : Commissione Prontuario terapeutico provinciale Cagliari In data novembre 2007 Per le seguenti motivazioni : La daptomicina possiede
RICHIESTA DI INSERIMENTO IN PTR DI ATC J01XX09 (CUBICIN ) Presentata da : Commissione Prontuario terapeutico provinciale Cagliari In data novembre 2007 Per le seguenti motivazioni : La daptomicina possiede
Università del Piemonte Orientale. Corso di Laurea in Medicina e Chirurgia. Corso di Statistica Medica. I modelli di studio
 Università del Piemonte Orientale Corso di Laurea in Medicina e Chirurgia Corso di Statistica Medica I modelli di studio Corso di laurea in medicina e chirurgia - Statistica Medica Disegno dello studio
Università del Piemonte Orientale Corso di Laurea in Medicina e Chirurgia Corso di Statistica Medica I modelli di studio Corso di laurea in medicina e chirurgia - Statistica Medica Disegno dello studio
Capitolo 3.2. La valutazione economica dei Nuovi Anticoagulanti Orali (NOACs) nella prevenzione di ictus in pazienti con fibrillazione atriale (SPAF)
 La valutazione economica dei Nuovi Anticoagulanti Orali (NOACs) nella prevenzione di ictus in pazienti con fibrillazione atriale (SPAF) Analisi di Budget Impact a livello nazionale e regionale 159 Analisi
La valutazione economica dei Nuovi Anticoagulanti Orali (NOACs) nella prevenzione di ictus in pazienti con fibrillazione atriale (SPAF) Analisi di Budget Impact a livello nazionale e regionale 159 Analisi
SINOSSI DELLO STUDO TITOLO DELLO STUDIO
 SINOSSI DELLO STUDO TITOLO DELLO STUDIO Studio clinico randomizzato e controllato, in aperto, per comparare l efficacia analgesica di percorsi terapeutici effettuati con ossicodone, fentanyl e buprenorfina
SINOSSI DELLO STUDO TITOLO DELLO STUDIO Studio clinico randomizzato e controllato, in aperto, per comparare l efficacia analgesica di percorsi terapeutici effettuati con ossicodone, fentanyl e buprenorfina
Evidenze cliniche: punto d incontro fra ricercatore e clinico. 09/05/2004 Dr. Giovanni Filocamo Dipartimento di Neuroscienze - Aimef 1
 Evidenze cliniche: punto d incontro fra 09/05/2004 Dr. Giovanni Filocamo Dipartimento di Neuroscienze - Aimef 1 Obiettivi del ricercatore Valutare: 1.La storia naturale della malattia e la gravità della
Evidenze cliniche: punto d incontro fra 09/05/2004 Dr. Giovanni Filocamo Dipartimento di Neuroscienze - Aimef 1 Obiettivi del ricercatore Valutare: 1.La storia naturale della malattia e la gravità della
PEGINTERFERONE ( )
 PEGINTERFERONE (12-11-2003) Specialità: Pegasys ; PegIntron PEGINTERFERONE ALFA-2a Specialità: Pegasys (Roche) Forma farmaceutica: soluz. iniett.1 sir.preriempita + ago 135 mcg in 0.5ml - Prezzo: euro
PEGINTERFERONE (12-11-2003) Specialità: Pegasys ; PegIntron PEGINTERFERONE ALFA-2a Specialità: Pegasys (Roche) Forma farmaceutica: soluz. iniett.1 sir.preriempita + ago 135 mcg in 0.5ml - Prezzo: euro
Riabilitazione dopo sindrome coronarica acuta
 Riabilitazione dopo sindrome coronarica acuta INTRODUZIONE Le malattie cardiovascolari sono la causa principale di morte e disabilità in tutti i paesi del mondo occidentale,inclusa l Italial Le malattie
Riabilitazione dopo sindrome coronarica acuta INTRODUZIONE Le malattie cardiovascolari sono la causa principale di morte e disabilità in tutti i paesi del mondo occidentale,inclusa l Italial Le malattie
TRATTAMENTO DELLA DIPENDENZA E DEI DISTURBI CORRELATI AGLI OPPIOIDI
 Dipartimento delle Dipendenze TRATTAMENTO DELLA DIPENDENZA E DEI DISTURBI CORRELATI AGLI OPPIOIDI Ambiti di Intervento Trattamenti in fase acuta Intossicazione Acuta Sindrome di Astinenza Trattamenti in
Dipartimento delle Dipendenze TRATTAMENTO DELLA DIPENDENZA E DEI DISTURBI CORRELATI AGLI OPPIOIDI Ambiti di Intervento Trattamenti in fase acuta Intossicazione Acuta Sindrome di Astinenza Trattamenti in
Gli antipsicotici atipici ( nuovi ) Clinica Psichiatrica Cantonale Mendrisio, 10 aprile 2000 G. M. Zanini
 Gli antipsicotici atipici ( nuovi ) Clinica Psichiatrica Cantonale Mendrisio, 10 aprile 2000 G. M. Zanini Quali sono? Clozapina (Leponex) Risperidone (Risperdal) Olanzapina (Zyprexa) Sertindolo (Serdolect)
Gli antipsicotici atipici ( nuovi ) Clinica Psichiatrica Cantonale Mendrisio, 10 aprile 2000 G. M. Zanini Quali sono? Clozapina (Leponex) Risperidone (Risperdal) Olanzapina (Zyprexa) Sertindolo (Serdolect)
Sinossi Protocollo Sperimentale GOIM 21002
 1 Sinossi Protocollo Sperimentale GOIM 21002 STUDIO MULTICENTRICO DI FASE II SULL UTILIZZO DI NANOPARTICLE ALBUMIN- BOUND PACLITAXEL (ABX) IN ASSOCIAZIONE A CAPECITABINA NEL TRATTAMENTO DI PRIMA LINEA
1 Sinossi Protocollo Sperimentale GOIM 21002 STUDIO MULTICENTRICO DI FASE II SULL UTILIZZO DI NANOPARTICLE ALBUMIN- BOUND PACLITAXEL (ABX) IN ASSOCIAZIONE A CAPECITABINA NEL TRATTAMENTO DI PRIMA LINEA
AIFA Agenzia Italiana del Farmaco Natalizumab (Tysabri)
 AIFA - Natalizumab (Tysabri) 18/02/2010 (Livello 2) AIFA Agenzia Italiana del Farmaco Natalizumab (Tysabri) Nota Informativa Importante Del 18 Febbraio 2010 file:///c /documenti/notys120.htm [18/02/2010
AIFA - Natalizumab (Tysabri) 18/02/2010 (Livello 2) AIFA Agenzia Italiana del Farmaco Natalizumab (Tysabri) Nota Informativa Importante Del 18 Febbraio 2010 file:///c /documenti/notys120.htm [18/02/2010
I medici non devono più prescrivere medicinali contenenti calcitonina in forma di spray nasale per il trattamento dell'osteoporosi.
 20 Luglio 2012 EMA/CHMP/483874/2012 L Agenzia Europea del Medicinali raccomanda la limitazione dell uso a lungo termine di medicinali a base di calcitonina Ritiro della formulazione intranasale per il
20 Luglio 2012 EMA/CHMP/483874/2012 L Agenzia Europea del Medicinali raccomanda la limitazione dell uso a lungo termine di medicinali a base di calcitonina Ritiro della formulazione intranasale per il
Emicrania. Una delle forme più comuni di cefalea che si manifesta in modo localizzato da un solo lato della testa e, raramente compare bilateralmente.
 Emicrania Una delle forme più comuni di cefalea che si manifesta in modo localizzato da un solo lato della testa e, raramente compare bilateralmente. L attacco emicranico si manifesta come dolore pulsante
Emicrania Una delle forme più comuni di cefalea che si manifesta in modo localizzato da un solo lato della testa e, raramente compare bilateralmente. L attacco emicranico si manifesta come dolore pulsante
ERLOTINIB (Tarceva) POTENZIALI EFFETTI COLLATERALI
 ERLOTINIB (Tarceva) POTENZIALI EFFETTI COLLATERALI Le informazioni contenute in questo modello sono fornite in collaborazione con la Associazione Italiana Malati di Cancro, parenti ed amici ; per maggiori
ERLOTINIB (Tarceva) POTENZIALI EFFETTI COLLATERALI Le informazioni contenute in questo modello sono fornite in collaborazione con la Associazione Italiana Malati di Cancro, parenti ed amici ; per maggiori
Sintesi generale della valutazione scientifica dei medicinali contenenti nimesulide (formulazioni sistemiche) (cfr. allegato I)
 Allegato II Conclusioni scientifiche e motivi della modifica del riassunto delle caratteristiche del prodotto, dell etichettatura e del foglio illustrativo presentati dall EMA 41 Conclusioni scientifiche
Allegato II Conclusioni scientifiche e motivi della modifica del riassunto delle caratteristiche del prodotto, dell etichettatura e del foglio illustrativo presentati dall EMA 41 Conclusioni scientifiche
Trattamento Sistemico dell Artrite Reumatoide nell Adulto con particolare riferimento ai farmaci biologici
 Trattamento Sistemico dell Artrite Reumatoide nell Adulto con particolare riferimento ai farmaci biologici Gruppo Multidisciplinare sui Farmaci Biologici in Reumatologia Regione Emilia Romagna C. Salvarani,
Trattamento Sistemico dell Artrite Reumatoide nell Adulto con particolare riferimento ai farmaci biologici Gruppo Multidisciplinare sui Farmaci Biologici in Reumatologia Regione Emilia Romagna C. Salvarani,
DEFERIPRONE ( )
 DEFERIPRONE (12-09-2007) Specialità: Ferriprox (Chiesi Farmaceutici SpA) Forma Farmaceutica: 100 cpr Dosaggio: 500 mg Prezzo: 262.33 Prezzo al pubblico da banca dati Farmadati Settembre 2007 ATC: V03AC02
DEFERIPRONE (12-09-2007) Specialità: Ferriprox (Chiesi Farmaceutici SpA) Forma Farmaceutica: 100 cpr Dosaggio: 500 mg Prezzo: 262.33 Prezzo al pubblico da banca dati Farmadati Settembre 2007 ATC: V03AC02
frequente caratterizzato da fastidio/dolore addominale e alterazioni dell alvo (costipazione e/o diarrea). Questa sindrome si manifesta con un elevata
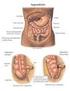 RIASSUNTO I Introduzione La sindrome dell intestino irritabile (IBS) è un disturbo funzionale molto frequente caratterizzato da fastidio/dolore addominale e alterazioni dell alvo (costipazione e/o diarrea).
RIASSUNTO I Introduzione La sindrome dell intestino irritabile (IBS) è un disturbo funzionale molto frequente caratterizzato da fastidio/dolore addominale e alterazioni dell alvo (costipazione e/o diarrea).
ANAFILASSI reazione allergica grave, a rapida insorgenza, che può causare la morte.
 REPORT OSSERVATORIO ALLERGOLOGICO REGIONALE ANAFILASSI reazione allergica grave, a rapida insorgenza, che può causare la morte. La diagnosi è clinica, basata su caratteristiche cliniche e di probabilità
REPORT OSSERVATORIO ALLERGOLOGICO REGIONALE ANAFILASSI reazione allergica grave, a rapida insorgenza, che può causare la morte. La diagnosi è clinica, basata su caratteristiche cliniche e di probabilità
AIFA - Agenzia Italiana del Farmaco
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITÀ REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Luglio 2013 Restrizione della popolazione target e limitazione della durata del trattamento
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITÀ REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Luglio 2013 Restrizione della popolazione target e limitazione della durata del trattamento
Dùtor, a mè gnù la prospera! Operetta (non proprio comica) in due atti
 Operetta (non proprio comica) in due atti ATTO PRIMO 1. il quesito ATTO SECONDO 5. il quesito ATTO PRIMO 4. la risposta Il caso clinico ATTO PRIMO 2. il PICO ATTO SECONDO 6. la risposta ATTO PRIMO 3. la
Operetta (non proprio comica) in due atti ATTO PRIMO 1. il quesito ATTO SECONDO 5. il quesito ATTO PRIMO 4. la risposta Il caso clinico ATTO PRIMO 2. il PICO ATTO SECONDO 6. la risposta ATTO PRIMO 3. la
SCHEDA FARMACO Decitabina (Dacogen)
 Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta SCHEDA FARMACO Decitabina (Dacogen) Dacogen 50 mg polvere per concentrato per soluzione
Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta SCHEDA FARMACO Decitabina (Dacogen) Dacogen 50 mg polvere per concentrato per soluzione
ARIPIPRAZOLO soluzione iniettabile ( )
 ARIPIPRAZOLO soluzione iniettabile (09-09-2008) Specialità: Abilify(Brisol-Myers Squibb srl) Forma farmaceutica: flaconcini 1.3 ml, 7.5mg/ml - Prezzo: euro 5.02 ATC: N05AX12 Categoria terapeutica: Antipsicotici
ARIPIPRAZOLO soluzione iniettabile (09-09-2008) Specialità: Abilify(Brisol-Myers Squibb srl) Forma farmaceutica: flaconcini 1.3 ml, 7.5mg/ml - Prezzo: euro 5.02 ATC: N05AX12 Categoria terapeutica: Antipsicotici
SCHEDA FARMACO. Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta
 Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta Cabazitaxel (JEVTANA) SCHEDA FARMACO 60 mg - concentrato e solvente per soluzione per
Principio attivo (nome commerciale) Forma farmaceutica e dosaggio, posologia, prezzo, regime di rimborsabilità, ditta Cabazitaxel (JEVTANA) SCHEDA FARMACO 60 mg - concentrato e solvente per soluzione per
Effetti degli NSAIDs sulla pressione arteriosa
 Effetti degli NSAIDs sulla pressione arteriosa Le malattie cardiovascolari sono le cause più comuni di morte nel mondo e la valutazione dell ipertensione è uno dei parametri più importanti da valutare.
Effetti degli NSAIDs sulla pressione arteriosa Le malattie cardiovascolari sono le cause più comuni di morte nel mondo e la valutazione dell ipertensione è uno dei parametri più importanti da valutare.
SCHEDA DI VALUTAZIONE PER L INSERIMENTO DI FARMACI NON PRESENTI NEL PTR
 RICHIESTA DI INSERIMENTO IN PTR DI SORAFENIB L01XE05 (Nexavar ) Presentata da Commissione Terapeutica Provinciale di Sassari In data gennaio 2009 Per le seguenti motivazioni: Sorafenib modifica lo standard
RICHIESTA DI INSERIMENTO IN PTR DI SORAFENIB L01XE05 (Nexavar ) Presentata da Commissione Terapeutica Provinciale di Sassari In data gennaio 2009 Per le seguenti motivazioni: Sorafenib modifica lo standard
Produttività, capacità di attrarre risorse e trasferibilità
 Produttività, capacità di attrarre Trials clinici Anno 2008 Studio Gisas: aripiprazolo, olanzapina e aloperidolo nel trattamento a lungo termine della schizofrenia Lo studio si propone di valutare l utilità
Produttività, capacità di attrarre Trials clinici Anno 2008 Studio Gisas: aripiprazolo, olanzapina e aloperidolo nel trattamento a lungo termine della schizofrenia Lo studio si propone di valutare l utilità
Ruolo dell Infermiere nella gestione di un Trial clinico
 Ricerca clinica Studi di fase I, II, III 3 Ruolo dell Infermiere nella gestione di un Trial clinico Processo Approvazione Attivazione Susanna Bassi Infermiera di ricerca, Ematologia Dh Ospedale di Circolo
Ricerca clinica Studi di fase I, II, III 3 Ruolo dell Infermiere nella gestione di un Trial clinico Processo Approvazione Attivazione Susanna Bassi Infermiera di ricerca, Ematologia Dh Ospedale di Circolo
ANALISI DEI SEGNALI SULLE REAZIONI DA VACCINI SORVEGLIANZA SULLE REAZIONI AVVERSE DA VACCINO. Chiara Biagi. Bologna, 4 dicembre 2012
 ANALISI DEI SEGNALI SULLE REAZIONI DA VACCINI Chiara Biagi SORVEGLIANZA SULLE REAZIONI AVVERSE DA VACCINO Bologna, 4 dicembre 2012 Alma Mater Studiorum Università di Bologna Dipartimento di Scienze Mediche
ANALISI DEI SEGNALI SULLE REAZIONI DA VACCINI Chiara Biagi SORVEGLIANZA SULLE REAZIONI AVVERSE DA VACCINO Bologna, 4 dicembre 2012 Alma Mater Studiorum Università di Bologna Dipartimento di Scienze Mediche
CHEMIOPROFILASSI PRIMARIA
 CHEMIOPROFILASSI PRIMARIA Somministrazione di chemioterapici o antibiotici a persone recentemente esposte a un rischio di contagio con lo scopo di bloccare lo sviluppo del processo infettivo. CHEMIOPROFILASSI
CHEMIOPROFILASSI PRIMARIA Somministrazione di chemioterapici o antibiotici a persone recentemente esposte a un rischio di contagio con lo scopo di bloccare lo sviluppo del processo infettivo. CHEMIOPROFILASSI
ALLEGATOA alla Dgr n del 03 novembre 2014 pag. 1/5
 giunta regionale 9^ legislatura ALLEGATOA alla Dgr n. 2056 del 03 novembre 2014 pag. 1/5 PRESCRIZIONE DI PRODOTTI IMMUNOTERAPICI PROVVISTI DI AIC INDICATI NEL TRATTAMENTO DELLA RINITE ALLERGICA NELLA REGIONE
giunta regionale 9^ legislatura ALLEGATOA alla Dgr n. 2056 del 03 novembre 2014 pag. 1/5 PRESCRIZIONE DI PRODOTTI IMMUNOTERAPICI PROVVISTI DI AIC INDICATI NEL TRATTAMENTO DELLA RINITE ALLERGICA NELLA REGIONE
Quali dati sono stati presentati sugli agonisti del GLP-1
 Quali dati sono stati presentati sugli agonisti del GLP-1 I responder a una dose di 3 mg di liraglutide con perdita di peso precoce hanno ottenuto una perdita di peso maggiore e la regressione alla normoglicemia
Quali dati sono stati presentati sugli agonisti del GLP-1 I responder a una dose di 3 mg di liraglutide con perdita di peso precoce hanno ottenuto una perdita di peso maggiore e la regressione alla normoglicemia
Il farmaco generico, ormai ridefinito farmaco equivalente, è considerato essenzialmente simile al medicinale già in commercio (farmaco originatore)
 1 Il farmaco generico, ormai ridefinito farmaco equivalente, è considerato essenzialmente simile al medicinale già in commercio (farmaco originatore) dal punto di vista qualitativo e quantitativo ma con
1 Il farmaco generico, ormai ridefinito farmaco equivalente, è considerato essenzialmente simile al medicinale già in commercio (farmaco originatore) dal punto di vista qualitativo e quantitativo ma con
AGOPUNTURA CINESE TRADIZIONALE COME SUPPORTIVE CARE IN CORSO DI CHEMIOTERAPIA ANTIBLASTICA SISTEMICA
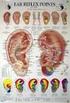 AGOPUNTURA CINESE TRADIZIONALE COME SUPPORTIVE CARE IN CORSO DI CHEMIOTERAPIA ANTIBLASTICA SISTEMICA Dott.ssa Benedetta Benedetti Tutor Scuola Tao U.O. Medicina Oncologica Direttore Dr. F. Artioli U.O.
AGOPUNTURA CINESE TRADIZIONALE COME SUPPORTIVE CARE IN CORSO DI CHEMIOTERAPIA ANTIBLASTICA SISTEMICA Dott.ssa Benedetta Benedetti Tutor Scuola Tao U.O. Medicina Oncologica Direttore Dr. F. Artioli U.O.
Commissione Regionale Farmaco VELAGLUCERASI ALFA
 Commissione Regionale Farmaco (D.G.R. 1540/2006, 2129/2010 e 490/2011) Doc. PTR n.147 relativo a: VELAGLUCERASI ALFA Novembre 2011 Indicazioni registrate Velaglucerasi alfa Velaglucerasi alfa (VEL) è indicato
Commissione Regionale Farmaco (D.G.R. 1540/2006, 2129/2010 e 490/2011) Doc. PTR n.147 relativo a: VELAGLUCERASI ALFA Novembre 2011 Indicazioni registrate Velaglucerasi alfa Velaglucerasi alfa (VEL) è indicato
Utilizzo degli anticoagulanti orali non vitamina K dipendenti (Nuovi. Antiacoagulanti Orali-NAO) nella malattia tromboembolica venosa
 Utilizzo degli anticoagulanti orali non vitamina K dipendenti (Nuovi Antiacoagulanti Orali-NAO) nella malattia tromboembolica venosa C.Mazzone, G.Sola Nei mesi scorsi al rivaroxaban (Xarelto) si sono successivamente
Utilizzo degli anticoagulanti orali non vitamina K dipendenti (Nuovi Antiacoagulanti Orali-NAO) nella malattia tromboembolica venosa C.Mazzone, G.Sola Nei mesi scorsi al rivaroxaban (Xarelto) si sono successivamente
Commissione Regionale Farmaco (D.G.R. 1540/2006 e D.G.R. 2330/2008) Documento relativo a: LIRAGLUTIDE
 Commissione Regionale Farmaco (D.G.R. 1540/2006 e D.G.R. 2330/2008) Documento relativo a: LIRAGLUTIDE Settembre 2010 1 Indicazioni registrate Liraglutide La liraglutide è indicata per il trattamento di
Commissione Regionale Farmaco (D.G.R. 1540/2006 e D.G.R. 2330/2008) Documento relativo a: LIRAGLUTIDE Settembre 2010 1 Indicazioni registrate Liraglutide La liraglutide è indicata per il trattamento di
DETERMINAZIONE 17 dicembre 2008
 DETERMINAZIONE 17 dicembre 2008 Regime di rimborsabilita' e prezzo di vendita del medicinale «Eucreas» (vildagliptin + metformina cloridrato), autorizzata con procedura centralizzata europea dalla Commissione
DETERMINAZIONE 17 dicembre 2008 Regime di rimborsabilita' e prezzo di vendita del medicinale «Eucreas» (vildagliptin + metformina cloridrato), autorizzata con procedura centralizzata europea dalla Commissione
Dott. Francesco Fiorica
 Dottorato di ricerca XXII ciclo Università degli Studi di Catania: Approccio Oncologico Multimodale in età geriatrica FATTIBILITA ED EFFICACIA DI UN TRATTAMENTO DI RADIOTERAPIA IN PAZIENTI ANZIANI CON
Dottorato di ricerca XXII ciclo Università degli Studi di Catania: Approccio Oncologico Multimodale in età geriatrica FATTIBILITA ED EFFICACIA DI UN TRATTAMENTO DI RADIOTERAPIA IN PAZIENTI ANZIANI CON
STUDI CLINICI IN CORSO nella MIELOFIBROSI
 Quinta Giornata Fiorentina dedicata ai pazienti con malattie mieloproliferative croniche Sabato 9 Maggio 2015 STUDI CLINICI IN CORSO nella MIELOFIBROSI Paola Guglielmelli Laboratorio Congiunto MMPC, AOU
Quinta Giornata Fiorentina dedicata ai pazienti con malattie mieloproliferative croniche Sabato 9 Maggio 2015 STUDI CLINICI IN CORSO nella MIELOFIBROSI Paola Guglielmelli Laboratorio Congiunto MMPC, AOU
CHEMIOTERAPIA ADIUVANTE NEL NSCLC IN FASE INIZIALE: SÌ, MA SENZA TRASCURARE LA QUALITÀ DI VITA
 CHEMIOTERAPIA ADIUVANTE NEL NSCLC IN FASE INIZIALE: SÌ, MA SENZA TRASCURARE LA QUALITÀ DI VITA In pazienti con carcinoma polmonare NSCLC in fase iniziale operabile, la chemioterapia adiuvante, aggiunta
CHEMIOTERAPIA ADIUVANTE NEL NSCLC IN FASE INIZIALE: SÌ, MA SENZA TRASCURARE LA QUALITÀ DI VITA In pazienti con carcinoma polmonare NSCLC in fase iniziale operabile, la chemioterapia adiuvante, aggiunta
SCHEDA DI VALUTAZIONE PER L INSERIMENTO DI FARMACI NON PRESENTI NEL PTR
 RICHIESTA DI INSERIMENTO IN PTR DI BECLOMETASONE DIPROPIONATO E FORMOTEROLO FUMARATO ATC R03AK07 (FOSTER ) Presentata da Commissione Terapeutica provinciale Sassari In data novembre 2008 Per le seguenti
RICHIESTA DI INSERIMENTO IN PTR DI BECLOMETASONE DIPROPIONATO E FORMOTEROLO FUMARATO ATC R03AK07 (FOSTER ) Presentata da Commissione Terapeutica provinciale Sassari In data novembre 2008 Per le seguenti
