Corso di. Proteomica e bioinformatica. modulo: Biochimica delle proteine
|
|
|
- Gaetano Carbone
- 6 anni fa
- Visualizzazioni
Transcript
1 Corso di Proteomica e bioinformatica modulo: Biochimica delle proteine Dott. Stefano Toppo Dipartimento di Chimica Biologica (Vallisneri piano terra stanza 85) Viale G. Colombo, Padova. Tel.: Fax.: stefano.toppo@unipd.it Home-page:
2 Sito web delle lezioni, orari e comunicazioni di varia natura e di interesse generale del corso Si accede tramite login e password cliccando sull anno accademico di riferimento del corso: L anno è Login: corso08 Password: bioc2008
3 Pietre miliari Le proteine supportano ogni reazione che avviene in un sistema biologico Le proteine compongono il 50% del peso secco della cellula; sono presenti in percentuali molto maggiori a quelle delle altre macromolecole cellulari Ca Johannes Mulder e Jakob Berzelius ( C, N, O, H in gelatina, albumina,...). Proteus... -> proteine Almeno 40 Premi Nobel per la Chimica o per Biologia e Medicina sono stati assegnati in relazione a studi su proteine
4 Funzioni delle proteine: Riconoscimento Catalisi Switch Funzionali Struttura
5 Alcune Funzioni delle Proteine Enzimi/catalizzatori Proteine contrattili o strutturali Proteine di trasporto Effettori Proteine di difesa Proteine per il trasporto elettronico Recettori Repressori Chaperoni Proteine di deposito TRIPSINA ACTINA Hb INSULINA Ab Cyt OXID CD4 Jun GroEl FERRITINA
6
7
8 La struttura delle proteine e descritta da quattro livelli di organizzazione Struttura Primaria- la sequenza di aminoacidi Struttura Secondaria - strutture locali stabilizzate da legami H che coinvolgono lo scheletro peptidico (cioe i gruppi carbonilici e aminici) e che si estendono in una dimensione Struttura Terziaria - Descrive i ripiegamenti che permettono alle proteine di assumere una struttura tridimensionale. Stabilizzata da tutti i tipi di interazioni deboli che coinvolgono le catene laterali degli aminoacidi. I ponti disolfuro, se presenti, hanno un ruolo nella stabilizzazione di questa struttura. Struttura Quaternaria - organizzazione in subunita
9
10 Il codice genetico
11 Il codice genetico Ala/A GCU, GCC, GCA, GCG Leu/L UUA, UUG, CUU, CUC, CUA, CUG Arg/R CGU, CGC, CGA, CGG, AGA, AGG Lys/K AAA, AAG Asn/N AAU, AAC Met/M AUG Asp/D GAU, GAC Phe/F UUU, UUC Cys/C UGU, UGC Pro/P CCU, CCC, CCA, CCG Gln/Q CAA, CAG Ser/S UCU, UCC, UCA, UCG, AGU, AGC Glu/E GAA, GAG Thr/T ACU, ACC, ACA, ACG Gly/G GGU, GGC, GGA, GGG Trp/W UGG His/H CAU, CAC Tyr/Y UAU, UAC Ile/I AUU, AUC, AUA Val/V GUU, GUC, GUA, GUG START AUG STOP UAG, UGA, UAA Start/stop codons 1. The most common start codon is AUG, which codes for methionine, so most amino acid chains start with methionine. 2. The three stop codons have been given names: UAG is amber, UGA is opal (sometimes also called umber), and UAA is ochre. "Amber" was named by discoverers Richard Epstein and Charles Steinberg after their friend Harris Bernstein, whose last name means "amber" in German. The other two stop codons were named 'ochre" and "opal" in order to keep the "color names" theme.
12 Il codice genetico Ala/A GCU, GCC, GCA, GCG Leu/L UUA, UUG, CUU, CUC, CUA, CUG Arg/R CGU, CGC, CGA, CGG, AGA, AGG Lys/K AAA, AAG Asn/N AAU, AAC Met/M AUG Asp/D GAU, GAC Phe/F UUU, UUC Cys/C UGU, UGC Pro/P CCU, CCC, CCA, CCG Gln/Q CAA, CAG Ser/S UCU, UCC, UCA, UCG, AGU, AGC Glu/E GAA, GAG Thr/T ACU, ACC, ACA, ACG Gly/G GGU, GGC, GGA, GGG Trp/W UGG His/H CAU, CAC Tyr/Y UAU, UAC Ile/I AUU, AUC, AUA Val/V GUU, GUC, GUA, GUG START AUG STOP UAG, UGA, UAA 1. Un codone è detto quattro volte degenere se qualsiasi nucleotide nella sua terza posizione codifica lo stesso amminoacido (ad esempio, UCA, UCC, UCG e UCU, tutti corrispondenti alla serina); 2. è detto due volte degenere se solo due delle quattro basi nella sua terza posizione codificano lo stesso amminoacido (ad esempio AAA ed AAG, corrispondenti alla lisina). Nei codoni due volte degeneri, i nucleotidi equivalenti nella terza posizione sono sempre o due purine (A / G) o due pirimidine (C / U).
13 Il codice genetico Ala/A GCU, GCC, GCA, GCG Leu/L UUA, UUG, CUU, CUC, CUA, CUG Arg/R CGU, CGC, CGA, CGG, AGA, AGG Lys/K AAA, AAG Asn/N AAU, AAC Met/M AUG Asp/D GAU, GAC Phe/F UUU, UUC Cys/C UGU, UGC Pro/P CCU, CCC, CCA, CCG Gln/Q CAA, CAG Ser/S UCU, UCC, UCA, UCG, AGU, AGC Glu/E GAA, GAG Thr/T ACU, ACC, ACA, ACG Gly/G GGU, GGC, GGA, GGG Trp/W UGG His/H CAU, CAC Tyr/Y UAU, UAC Ile/I AUU, AUC, AUA Val/V GUU, GUC, GUA, GUG START AUG STOP UAG, UGA, UAA 1. La ridondanza rende il codice genetico meno vulnerabile alle mutazioni causali. Un codone quattro volte ridondante può subire qualsiasi mutazione alla sua terza posizione ed un codone due volte ridondante può subire una delle tre possibili mutazioni alla sua terza posizione senza che l'amminoacido da esso espresso - e quindi la struttura della proteina in cui l'amminoacido verrà inserito - cambi. Inoltre, dato che le mutazioni per transizione (da una purina all'altra o da una pirimidina all'altra) sono più probabili delle mutazioni per transversione (da purina a pirimidina o viceversa), l'equivalenza tra purine o tra pirimidine nei codoni due volte degeneri aggiunge un'ulteriore resistenza.
14 Il codice genetico Ala/A GCU, GCC, GCA, GCG Leu/L UUA, UUG, CUU, CUC, CUA, CUG Arg/R CGU, CGC, CGA, CGG, AGA, AGG Lys/K AAA, AAG Asn/N AAU, AAC Met/M AUG Asp/D GAU, GAC Phe/F UUU, UUC Cys/C UGU, UGC Pro/P CCU, CCC, CCA, CCG Gln/Q CAA, CAG Ser/S UCU, UCC, UCA, UCG, AGU, AGC Glu/E GAA, GAG Thr/T ACU, ACC, ACA, ACG Gly/G GGU, GGC, GGA, GGG Trp/W UGG His/H CAU, CAC Tyr/Y UAU, UAC Ile/I AUU, AUC, AUA Val/V GUU, GUC, GUA, GUG START AUG STOP UAG, UGA, UAA Diverse variazioni al codice genetico standard sono state trovate nei mitocondri. Anche i protozoi ciliati presentano qualche modifica: in loro (come anche in alcune specie di alga verde) UAG e, spesso, UAA codificano la glutammina e UGA codifica la cisteina. In alcune specie di lievito CUG codifica la serina. codici genetici A dispetto di queste variazioni, i codici genetici usati da tutte le forme di vita della Terra sono molto simili. Dato che i codici genetici possibili e potenzialmente adatti alla vita sono molti, la teoria dell'evoluzione fa pensare che questo codice genetico sia andato a definirsi molto presto nella storia della vita su questo pianeta. Le pressioni che poi possono aver portato all'evoluzione di codici genetici non canonici sono state sicuramente secondarie, in particolare si pensa legate a fenomeni di resistenza al trasferimento genico o all'attacco virale.
15 Il codice genetico Ala/A GCU, GCC, GCA, GCG Leu/L UUA, UUG, CUU, CUC, CUA, CUG Arg/R CGU, CGC, CGA, CGG, AGA, AGG Lys/K AAA, AAG Asn/N AAU, AAC Met/M AUG Asp/D GAU, GAC Phe/F UUU, UUC Cys/C UGU, UGC Pro/P CCU, CCC, CCA, CCG Gln/Q CAA, CAG Ser/S UCU, UCC, UCA, UCG, AGU, AGC Glu/E GAA, GAG Thr/T ACU, ACC, ACA, ACG Gly/G GGU, GGC, GGA, GGG Trp/W UGG His/H CAU, CAC Tyr/Y UAU, UAC Ile/I AUU, AUC, AUA Val/V GUU, GUC, GUA, GUG START AUG STOP UAG, UGA, UAA Codon Usage Different organisms often show particular preferences for one of the several codons that encode the same amino acid. How these preferences arise is a much debated area of molecular evolution. It is generally acknowledged that codon preferences reflect a balance between mutational biases and natural selection for translational optimization. Optimal codons in fast-growing microorganisms, like Escherichia coli or Saccharomyces cerevisiae (baker's yeast), reflect the composition of their respective genomic trna pool. It is thought that optimal codons help to achieve faster translation rates and high accuracy. As a result of these factors, translational selection is expected to be stronger in highly expressed genes, as is indeed the case for the above-mentioned organisms. In other organisms that do not show high growing rates or that present small genomes, codon usage optimization is normally absent, and codon preferences are determined by the characteristic mutational biases seen in that particular genome. Examples of this are Homo sapiens (human) and Helicobacter pylori. Organisms that show an intermediate level of codon usage optimization include Drosophila melanogaster (fruit fly), Caenorhabditis eleganss (nematode worm) or Arabidopsis thaliana (wall cress).
16 Peso molecolare vs. Mr Mr e la massa molecolare relativa a 1/12 della massa dell isotopo 12C (che vale esattamente 12 u.m.a.). Mr e un rapporto, e quindi ADIMENSIONALE. 1 Da equivale alla massa di 1 g / N (6.022 x ). Spesso si usa il Da per indicare il peso molecolare, che quindi rappresenta la massa, espressa in g, di una mole di proteina. Il peso molecolare ha dimensoni di g/mole. Dal punto di vista pratico Mr e peso molecolare vengono usati indifferentemente.
17 Ka, pka e ph La costante di dissociazione acida è un valore che rappresenta, ad una data temperatura, il grado di dissociazione di un acido. Maggiore è la costante, maggiore è la tendenza dell'acido a dissociarsi, maggiore è la sua "forza". Data la reazione di dissociazione di un generico acido HA la costante di dissociazione acida corrispondente viene calcolata come in cui le parentesi quadre indicano la concentrazione molare della specie racchiusa tra esse. I valori delle costanti di dissociazione riportati in letteratura sono convenzionalmente quelli misurati a 20 C; spesso non vengono riportati i valori delle costanti, bensì i corrispondenti pk a, definiti come Per soluzioni sufficientemente diluite di acidi deboli, per i quali la concentrazione della specie indissociata [HA] può essere ragionevolmente approssimata con il valore della concentrazione nominale dell'acido, il ph è legato alla costante di dissociazione secondo l equazione di Henderson Hasselbach: ph = pka + log([a-]/[ha])
18
19
20 Valori di pk a delle catene laterali R dissociabili degli aminoacidi Serina, Ser, S: pk ar = 13 Treonina, Thr, T: pk ar = 13 Arginina, Arg, R: pk ar = 12.5 Lisina, Lys, K: pk ar = 10.5 Tirosina, Tyr, Y: pk ar = 10.1 Cisteina, Cys, C: pk ar = 8.3 Selenocysteina, Secys, U: pk ar = 7.5 Istidina, His, H: pk ar = 6.0 Acido Aspartico, Asp, D: pk ar = 3.9 Acido Glutammico, Glu, E: pk ar = 4.1
21
22
23
24
25
26 Optical activity (quantified by the rotation of the plane of polarized light as it passes through a substance) was measured long before the three dimensional structure of molecules could be determined by methods such as X-ray Crystallography (back to the very earliest work of Pasteur in the 1840s. Pasteur was studying the properties of salts of tartaric acid products of grape fermentation). The experimental assignment of optical activity was then symbolized with the letter "d" or the "+" sign (for dextrotatory, right handed or clockwise rotation of the plane of polarized light when viewed toward the light source) and "l" or "-" (for levorotatory, left hand or counterclockwise rotation). Later the "D" and "L" symbols were associated with absolute configuration based on the arbitrary, but as it turned out, correct assignment of the absolute configuration of the dextrotatory and levorotatory forms of glyceraldehyde. In this symbolism, absolute configuration is based on chemical synthesis starting with glyceraldehyde (Fischer and Rosanoff) and optical activity is specified using the "+" and "-" notation. There is no correspondence between the D,L system and the real rotation of the plane of polarized light optical activity (right + or left -) (see L-cysteine).
27 A second absolute configuration notation using the symbols R (from rectus, latin for right) and S (from sinister, latin for left) was developed by Cahn, Ingold & Prelog. In this approach, the substituents on an assymetric carbon (eg. a tetrahedral carbon with four different substituents) are prioritized by decreasing atomic number. Configuration is assigned by "looking" down the bond to the lowest priority substituent and assigning R to the configuration where the remaining subtituents are arranged clockwise in decreasing priority. S is then assigned to the molecular form where the substituents are arranged counterclockwise. Some other rules for assigning R/S configuration (double bonds account for twice the atomic number of the components): Group Priorities: SH > OH > NH 2 > COOH > CHO > CH 2 OH > C 6 H 5 > CH 3 > H Larger groups are ranked at their points of divergence, i.e. a CH 2 CH 2 SH is greater than a CH 2 CH 2 OH
28 Both threonine and isoleucine have a second assymetric carbon center at carbon position 3 along their chains. The absolute configuration of the normal protein component, L-threonine, is 2S,3R. The mirror image compound (the enantiomer) is D-threonine (2R,3S). The diastereomer with 2S, 3S configuration is called L-allo-threonine (D-allo-threonine is then 2R, 3R). For isoleucine, the configuration of normal L-isoleucine is 2S, 3S.
29 PERCHE L ISOLEUCINA E IN CONFORMAZIONE 2s,3s? COSA INDICANO I NUMERI 2 E 3? acido 2(S)-ammino-3(S)-metilpentanoico (nome IUPAC) È un acido con 5 Carboni e numerazione che parte dal C del C=O. In posizione 2 troviamo il C-alfa chirale (configurazione S) e in 3 troviamo il secondo C chirale (configurazione S)
30
31 Gli aminoacidi sono le unita strutturali che costituiscono le proteine Centrale alla struttura degli aminoacidi e il carbonio α che e legato covalentemente sia al carbonio aminico che carbossilico La catena laterale (R) da ad ogni aminoacido la sua identita In soluzione neutra il gruppo carbossilico esiste come COO - e il gruppo aminico come NH 3+. E quindi uno zwitterione Gli aminoacidi sono molecole chirali
32 Stereochimica degli aminoacidi Tutti gli aminoacidi eccetto la glicina sono chirali Gli L-aminoacidi predominano in natura La nomenclatura D,L- e basata sulla D- e L- gliceraldeide Il sistema di nomenclatura R,S e migliore, dato che gli aminoacidi isoleucina e treonina (che hanno due centri chirali) possono venir classificati in maniera non ambigua
33 Aminoacidi nutrizionalmente essenziali e non Nurizionalmente essenziali Arginina Istidina Isoleucina Leucina Lisina Metionina Fenilalanina Treonina Triptofano Valina Nurizionalmente non essenziali Alanina Asparagina Aspartato Cisteina Glutammato Glutammina Glicina Prolina Selenocisteina Serina Tirosina Non tutti gli aminoacidi possono essere sintetizzati dall uomo questi si configurano come nutrizionalmente essenziali
34 Le proteine sono polimeri non ramificati di aminoacidi la formazione del legame peptidico porta ad eliminazione di H 2 O. Lo scheletro di una proteina consiste della sequenza ripetuta -N-Cα-C-
35 Il legame peptidico e solitamente rappresentato come un legame singolo tra il carbonio carbonilico e l azoto amidico Ha parziale (40%) carattere di doppio legame L atomo di N e parzialmente positivo; l atomo di O parzialmente negativo Si trova solitamente nella conformazione trans dell O carbonilico e dell H amidico E lungo circa nm - e quindi piu corto di un tipico legame singolo (0.145 nm per un legame C-N) ma piu lungo di un doppio legame
36 Il parziale carattere di doppio legame del legame peptidico Le interazioni di risonanza fra C, O e N che partecipano al gruppo peptidico possono essere rappresentate come due estremi, ma il legame peptidico e descritto al meglio come un ibrido di risonanza tra le due forme estreme E prevista rotazione tra C-N gli atomi C e N sono ibridizzati sp2 e gli atomi C e O partecipano ad un legame p greco, lasciando all N una coppia di elettroni negli orbitali 2p Non e prevista rotazione tra C-N la coppia solitaria e sull O e C-N partecipano ad un legame p greco
37 Conseguenze della risonanza del legame peptidico La risonanza del legame peptidico ha tre conseguenze importanti: 1. Restringe le possibilita di rotazione attorno al legame peptidico sicche e possibile solo la rotazione tra Cα-CO e Cα Ν 2. I sei atomi che compongono i gruppi del legame peptidico tendono ad essere coplanari formando il piano amidico 3. Il legame peptidico e piu corto di un legame singolo e piu lungo di un legame doppio e la sua energia è di 88 kj/mol circa
38
39
40
41
42
43
44
45 Idrofobici e idrofilici
46
47
Biologia Molecolare. CDLM in CTF La riparazione del DNA
 Biologia Molecolare CDLM in CTF 2010-2011 La riparazione del DNA I tipi di mutazione e le conseguenze Le classi di danno al DNA Meccanismi di riparazione La necessità di codificare l informazione L informazione
Biologia Molecolare CDLM in CTF 2010-2011 La riparazione del DNA I tipi di mutazione e le conseguenze Le classi di danno al DNA Meccanismi di riparazione La necessità di codificare l informazione L informazione
Alcune domande di carattere evolutivo
 Alcune domande di carattere evolutivo 1. Perché tutti gli organismi viventi (a parte le solite, rare, eccezioni usano lo stesso insieme di 20 aminoacidi? Interrelazioni tra organismi 2. Perché gli amino
Alcune domande di carattere evolutivo 1. Perché tutti gli organismi viventi (a parte le solite, rare, eccezioni usano lo stesso insieme di 20 aminoacidi? Interrelazioni tra organismi 2. Perché gli amino
POLITECNICO DI BARI Corso di Laurea Magistrale in Ingegneria Elettronica BIOINFORMATICA DNA COMPUTING Docente Prof. Giuseppe Mastronardi
 POLITECNICO DI BARI Corso di Laurea Magistrale in Ingegneria Elettronica BIOINFORMATICA DNA COMPUTING Docente Prof. Giuseppe Mastronardi Sommario Introduzione Cenni di biologia Modello di Adleman Modello
POLITECNICO DI BARI Corso di Laurea Magistrale in Ingegneria Elettronica BIOINFORMATICA DNA COMPUTING Docente Prof. Giuseppe Mastronardi Sommario Introduzione Cenni di biologia Modello di Adleman Modello
Produzione di proteine eterologhe. Cosa occorre per l espressione l livello di una proteina nella cellula? Trascrizione/traduzione/stabilità
 Cosa occorre per l espressione l ad alto livello di una proteina nella cellula? Trascrizione/traduzione/stabilità Promotore forte (trascrizione) Presenza di segnali per il riconoscimento dell mrna da parte
Cosa occorre per l espressione l ad alto livello di una proteina nella cellula? Trascrizione/traduzione/stabilità Promotore forte (trascrizione) Presenza di segnali per il riconoscimento dell mrna da parte
LE AUGURO BUON LAVORO!
 Nome:. Cognome:...... Pt./137 Nota ESAME DI SCIENZE SPERIMENTALI: BIOLOGIA Indicazioni: 1. Risponda sempre negli spazi indicati; non separi né scriva sul retro dei fogli. 2. Scriva, o, laddove richiesto,
Nome:. Cognome:...... Pt./137 Nota ESAME DI SCIENZE SPERIMENTALI: BIOLOGIA Indicazioni: 1. Risponda sempre negli spazi indicati; non separi né scriva sul retro dei fogli. 2. Scriva, o, laddove richiesto,
La sintesi delle proteine
 La sintesi delle proteine Struttura del trna In che modo l informazione contenuta sotto forma di sequenze nucleotidiche nel DNA e nell RNA si traduce nella sequenza amminoacidica delle proteine? Esperimenti
La sintesi delle proteine Struttura del trna In che modo l informazione contenuta sotto forma di sequenze nucleotidiche nel DNA e nell RNA si traduce nella sequenza amminoacidica delle proteine? Esperimenti
07/01/2015. I promotori inducibili sono un metodo di espressione dotato di estrema flessibilità
 I promotori inducibili sono un metodo di espressione dotato di estrema flessibilità Sistemi altamente utilizzati: plac e derivati, T7RNA pol, promotore pbad Promotori attivati da particolari condizioni
I promotori inducibili sono un metodo di espressione dotato di estrema flessibilità Sistemi altamente utilizzati: plac e derivati, T7RNA pol, promotore pbad Promotori attivati da particolari condizioni
esperto prof. Ciro Formica
 esperto prof. Ciro Formica Immagini e testi tratti dai website di: genome.wellcome.ac.uk, dnaftb.org, unipv.it, unimi.it, wikipedia.it, unibs.it, unisi.it, unina.it, uniroma2.it, nih.gov, zanichelli.it,
esperto prof. Ciro Formica Immagini e testi tratti dai website di: genome.wellcome.ac.uk, dnaftb.org, unipv.it, unimi.it, wikipedia.it, unibs.it, unisi.it, unina.it, uniroma2.it, nih.gov, zanichelli.it,
LE AUGURO BUON LAVORO!
 Nome:. Cognome:...... ESAME DI SCIENZE SPERIMENTALI: BIOLOGIA Pt./129 Indicazioni: 1. Non separi i fogli. 2. Scriva, o, laddove richiesto, indichi in modo chiaro, preciso e ben leggibile. Risposte di difficile
Nome:. Cognome:...... ESAME DI SCIENZE SPERIMENTALI: BIOLOGIA Pt./129 Indicazioni: 1. Non separi i fogli. 2. Scriva, o, laddove richiesto, indichi in modo chiaro, preciso e ben leggibile. Risposte di difficile
07/01/2015. Induzione di un promotore: un modo di superare problemi di tossicità. Plac, il promotore inducibile per eccellenza
 Induzione di un promotore: un modo di superare problemi di tossicità Induzione Crescita non inibita Crescita rallentata Crescita bloccata e/o lisi cellulare Crescita di un ceppo che esprime una proteina
Induzione di un promotore: un modo di superare problemi di tossicità Induzione Crescita non inibita Crescita rallentata Crescita bloccata e/o lisi cellulare Crescita di un ceppo che esprime una proteina
Prof. Giorgio Sartor. Sintesi proteica. Trasmissione dell informazione
 rof. Giorgio Sartor Sintesi proteica Copyright 2001-2013 by Giorgio Sartor. All rights reserved. B15 -Versione 1.0 nov2013 Trasmissione dell informazione L informazione è contenuta nel DA ed è trasferita
rof. Giorgio Sartor Sintesi proteica Copyright 2001-2013 by Giorgio Sartor. All rights reserved. B15 -Versione 1.0 nov2013 Trasmissione dell informazione L informazione è contenuta nel DA ed è trasferita
Amminoacidi. Struttura base di un a-amminoacido
 Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
condizioni particolari di crescita (es. assenza di ossigeno) Alcune proteine (o loro prodotti) vengono ottenuti in condizioni di anaerobiosi
 I promotori inducibili consentono una grande flessibilità nella scelta di vettori d espressioned La scelta di vettori d espressione d dipende principalmente da: RESA Tossicità delle proteine eterologhe
I promotori inducibili consentono una grande flessibilità nella scelta di vettori d espressioned La scelta di vettori d espressione d dipende principalmente da: RESA Tossicità delle proteine eterologhe
Prof. Fulvio Ursini Dipartimento di Chimica Biologica (Vallisneri IV piano Nord) Viale G. Colombo, Padova. Tel.
 Prof. Fulvio Ursini Dipartimento di Chimica Biologica (Vallisneri IV piano Nord) Viale G. Colombo, 3-35121 Padova. Tel.:+39-049-8276104 Fax.:+39-049-8073310 E-mail: fulvio.ursini@unipd.it Funzioni delle
Prof. Fulvio Ursini Dipartimento di Chimica Biologica (Vallisneri IV piano Nord) Viale G. Colombo, 3-35121 Padova. Tel.:+39-049-8276104 Fax.:+39-049-8073310 E-mail: fulvio.ursini@unipd.it Funzioni delle
Struttura degli amminoacidi
 AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
AMINOACIDI Struttura. Funzione. Classificazione. Proprietà
 AMINOACIDI Struttura Funzione Classificazione Proprietà 1 STRUTTURA Composti caratterizzati dalla presenza di un gruppo aminico (NH 2 ) e di un gruppo acido (COOH) legati al medesimo carbonio (C). In soluzione
AMINOACIDI Struttura Funzione Classificazione Proprietà 1 STRUTTURA Composti caratterizzati dalla presenza di un gruppo aminico (NH 2 ) e di un gruppo acido (COOH) legati al medesimo carbonio (C). In soluzione
all codons are used in protein synthesis 20 amino acids 3 termination (stop) codons: UAA, UAG, UGA
 Il Codice Genetico The genetic code consists of 64 triplet codons (A, G, C, U) 4 3 = 64 all codons are used in protein synthesis 20 amino acids 3 termination (stop) codons: UAA, UAG, UGA AUG (methionine)
Il Codice Genetico The genetic code consists of 64 triplet codons (A, G, C, U) 4 3 = 64 all codons are used in protein synthesis 20 amino acids 3 termination (stop) codons: UAA, UAG, UGA AUG (methionine)
Proteine strutturali Sostegno meccanico Cheratina: costituisce i capelli Collagene: costituisce le cartilagini Proteine di immagazzinamento
 Tipo Funzione Esempi Enzimi Accelerano le reazioni chimiche Saccarasi: posiziona il saccarosio in modo che possa essere scisso nelle due unità di glucosio e fruttosio che lo formano Ormoni Messaggeri chimici
Tipo Funzione Esempi Enzimi Accelerano le reazioni chimiche Saccarasi: posiziona il saccarosio in modo che possa essere scisso nelle due unità di glucosio e fruttosio che lo formano Ormoni Messaggeri chimici
Struttura delle Proteine
 Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
L mrna ED IL CODICE GENETICO
 L mrna ED IL CODICE GENETICO LA SEQ. NUCLEOTIDICA DI UN GENE, PER MEZZO DELL mrna, E TRADOTTA NELLA SEQ. AMINOACIDICA DI UN PEPTIDE SEGUENDO REGOLE NOTE COME CODICE GENETICO. LA SUCCESSIONE CONSECUTIVA
L mrna ED IL CODICE GENETICO LA SEQ. NUCLEOTIDICA DI UN GENE, PER MEZZO DELL mrna, E TRADOTTA NELLA SEQ. AMINOACIDICA DI UN PEPTIDE SEGUENDO REGOLE NOTE COME CODICE GENETICO. LA SUCCESSIONE CONSECUTIVA
La struttura delle proteine e e descritta da quattro livelli di organizzazione
 La struttura delle proteine e e descritta da quattro livelli di organizzazione Struttura Primaria- - la sequenza di aminoacidi Struttura Secondaria - strutture locali stabilizzate da legami H che coinvolgono
La struttura delle proteine e e descritta da quattro livelli di organizzazione Struttura Primaria- - la sequenza di aminoacidi Struttura Secondaria - strutture locali stabilizzate da legami H che coinvolgono
all codons are used in protein synthesis 20 amino acids 3 termination (stop) codons: UAA, UAG, UGA
 The genetic code consists of 64 triplet codons (A, G, C, U) 4 3 = 64 all codons are used in protein synthesis 20 amino acids 3 termination (stop) codons: UAA, UAG, UGA AUG (methionine) is the start codon
The genetic code consists of 64 triplet codons (A, G, C, U) 4 3 = 64 all codons are used in protein synthesis 20 amino acids 3 termination (stop) codons: UAA, UAG, UGA AUG (methionine) is the start codon
MACROMOLECOLE. Polimeri (lipidi a parte)
 MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH. ) ed un gruppo carbossilico ( COOH) nella stessa molecola
 Amminoacidi (1) Presentano un gruppo amminico ( NH 2 ) ed un gruppo carbossilico ( COOH) nella stessa molecola CH 3 NH 2 C H α * COOH Acido 2-ammino propanoico (acido α-ammino propionico) 1 Amminoacidi
Amminoacidi (1) Presentano un gruppo amminico ( NH 2 ) ed un gruppo carbossilico ( COOH) nella stessa molecola CH 3 NH 2 C H α * COOH Acido 2-ammino propanoico (acido α-ammino propionico) 1 Amminoacidi
Amminoacidi. Struttura base di un a-amminoacido
 Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Il Codice Genetico. La decodifica della sequenza nucleotidica in. sequenza aminoacidica
 Il Codice Genetico La decodifica della sequenza nucleotidica in sequenza aminoacidica La sequenza del mrna viene letta a gruppi di 3 nucleotidi, senza interruzioni e senza sovrapposizioni; 4 3 = 64 ---------64
Il Codice Genetico La decodifica della sequenza nucleotidica in sequenza aminoacidica La sequenza del mrna viene letta a gruppi di 3 nucleotidi, senza interruzioni e senza sovrapposizioni; 4 3 = 64 ---------64
Sintesi e degradazione delle proteine
 Prof. Giorgio Sartor Sintesi e degradazione delle proteine Copyright 2001-2012 by Giorgio Sartor. All rights reserved. B15 - Versione 1.4.2 may 2012 Trasmissione dell informazione L informazione è contenuta
Prof. Giorgio Sartor Sintesi e degradazione delle proteine Copyright 2001-2012 by Giorgio Sartor. All rights reserved. B15 - Versione 1.4.2 may 2012 Trasmissione dell informazione L informazione è contenuta
sono le unità monomeriche che costituiscono le proteine hanno tutti una struttura comune
 AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
Sintesi e degradazione delle proteine
 Prof. Giorgio Sartor Sintesi e degradazione delle proteine Copyright 2001- by Giorgio Sartor. All rights reserved. B15 - Versione 1.4.1 may Trasmissione dell informazione L informazione è contenuta nel
Prof. Giorgio Sartor Sintesi e degradazione delle proteine Copyright 2001- by Giorgio Sartor. All rights reserved. B15 - Versione 1.4.1 may Trasmissione dell informazione L informazione è contenuta nel
Il flusso dell informazione genica Le proteine natura ed informazione Il codice genetico La traduzione (sintesi proteica) Cenni sul folding delle
 Il flusso dell informazione genica Le proteine natura ed informazione Il codice genetico La traduzione (sintesi proteica) Cenni sul folding delle proteine Genotipo e fenotipo Mutazioni e polimorfismi Il
Il flusso dell informazione genica Le proteine natura ed informazione Il codice genetico La traduzione (sintesi proteica) Cenni sul folding delle proteine Genotipo e fenotipo Mutazioni e polimorfismi Il
LE PROTEINE: POLIMERI COSTITUITI DA 20 TIPI DI MONOMERI, I 20 AMINOACIDI
 LE PROTEINE: POLIMERI OSTITUITI DA 20 TIPI DI MONOMERI, I 20 AMINOAIDI OGNI PROTEINA PUO ESSERE FORMATA DA MOLTE DEINE O ENTINAIA DI AMINOAIDI E SI LEGANO A FORMARE UNA ATENA NON RAMIFIATA La catena di
LE PROTEINE: POLIMERI OSTITUITI DA 20 TIPI DI MONOMERI, I 20 AMINOAIDI OGNI PROTEINA PUO ESSERE FORMATA DA MOLTE DEINE O ENTINAIA DI AMINOAIDI E SI LEGANO A FORMARE UNA ATENA NON RAMIFIATA La catena di
CHIMICA BIOLOGICA. Seconda Università degli Studi di Napoli. DiSTABiF. Antimo Di Maro. Lezione 3. Corso di Laurea in Scienze Biologiche
 Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Antimo Di Maro Anno Accademico 2016-2017 Lezione 3 GLI AMMINOACIDI PROTEICI Le
Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Antimo Di Maro Anno Accademico 2016-2017 Lezione 3 GLI AMMINOACIDI PROTEICI Le
α-amminoacidi O α O α R CH C O - NH 3 forma ionizzata sale interno (zwitterione) OH NH 2 forma non ionizzata (non esistente in realtà)
 Amminoacidi 2 forma non ionizzata (non esistente in realtà) 3 forma ionizzata sale interno (zwitterione) In soluzione acquosa c'è equilibrio tra tre forme 3 forma cationica p molto acidi 3 forma zwitterionica
Amminoacidi 2 forma non ionizzata (non esistente in realtà) 3 forma ionizzata sale interno (zwitterione) In soluzione acquosa c'è equilibrio tra tre forme 3 forma cationica p molto acidi 3 forma zwitterionica
TRADUZIONE. 2. Transfer (legato agli aminoacidi) 3. Ribosomale (associato a proteine nei ribosomi)
 enhancer promotore regione trascritta TATA trascrizione 5 3 splicing mrna 5 3 traduzione Proteina NH2 COOH Funzione biologica TRADUZIONE I tre ruoli svolti dall RNA: 1. Messaggero 2. Transfer (legato agli
enhancer promotore regione trascritta TATA trascrizione 5 3 splicing mrna 5 3 traduzione Proteina NH2 COOH Funzione biologica TRADUZIONE I tre ruoli svolti dall RNA: 1. Messaggero 2. Transfer (legato agli
Dal gene alla proteina
 Dal gene alla proteina Il collegamento tra geni e proteine La trascrizione e la traduzione sono i due principali processi che legano il gene alla proteina: uno sguardo panoramico Le informazioni genetiche
Dal gene alla proteina Il collegamento tra geni e proteine La trascrizione e la traduzione sono i due principali processi che legano il gene alla proteina: uno sguardo panoramico Le informazioni genetiche
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH
 Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( OO) nella stessa molecola 3 N 2 α * OO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-himica Organica 1 Amminoacidi
Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( OO) nella stessa molecola 3 N 2 α * OO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-himica Organica 1 Amminoacidi
C1. Il codone di inizio parte dal quinto nucleotide. La sequenza aminoacidica sarà Met Gly Asn Lys Pro Gly Gln STOP.
 Soluzioni ai problemi del Capitolo 13 Domande concettuali C1. Il codone di inizio parte dal quinto nucleotide. La sequenza aminoacidica sarà Met Gly Asn Lys Pro Gly Gln STOP. C2. Quando si dice che il
Soluzioni ai problemi del Capitolo 13 Domande concettuali C1. Il codone di inizio parte dal quinto nucleotide. La sequenza aminoacidica sarà Met Gly Asn Lys Pro Gly Gln STOP. C2. Quando si dice che il
Seminario di Bioinformatica AA
 Seminario di Bioinformatica AA 2007-2008 Broccolo Daniele Marcon Lorenzo Vandoni Riccardo {broccolo, marcon, vandoni}@cli.di.unipi.it Sommario /1 Pattern matching: cos è e perché Algoritmi per il pattern
Seminario di Bioinformatica AA 2007-2008 Broccolo Daniele Marcon Lorenzo Vandoni Riccardo {broccolo, marcon, vandoni}@cli.di.unipi.it Sommario /1 Pattern matching: cos è e perché Algoritmi per il pattern
L mrna ED IL CODICE GENETICO
 L mrna ED IL CODICE GENETICO LA SEQ. NUCLEOTIDICA DI UN GENE, PER MEZZO DELL mrna, E TRADOTTA NELLA SEQ. AMINOACIDICA DI UN PEPTIDE SEGUENDO REGOLE NOTE COME CODICE GENETICO. LA SUCCESSIONE CONSECUTIVA
L mrna ED IL CODICE GENETICO LA SEQ. NUCLEOTIDICA DI UN GENE, PER MEZZO DELL mrna, E TRADOTTA NELLA SEQ. AMINOACIDICA DI UN PEPTIDE SEGUENDO REGOLE NOTE COME CODICE GENETICO. LA SUCCESSIONE CONSECUTIVA
Proteine: struttura e funzione
 Proteine: struttura e funzione Prof.ssa Flavia Frabetti PROTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (C, H, O,
Proteine: struttura e funzione Prof.ssa Flavia Frabetti PROTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (C, H, O,
amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente
 Gli amminoacidi naturali sono α-amminoacidi : il gruppo amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente formula generale: gruppo funzionale carbossilico
Gli amminoacidi naturali sono α-amminoacidi : il gruppo amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente formula generale: gruppo funzionale carbossilico
La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa.
 La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa. Le cellule contengono 4 famiglie principali di piccole molecole organiche: Amminoacidi
La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa. Le cellule contengono 4 famiglie principali di piccole molecole organiche: Amminoacidi
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
INTERAZIONE TRA mrna, trna e RIBOSOMI
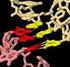 INTERAZIONE TRA mrna, trna e RIBOSOMI mrna: porta l'informazione della sequenza degli aminoacidi di una determinata proteina. trna: ogni trna è specifico per il trasporto di un determinato aminoacido Ribosoma:
INTERAZIONE TRA mrna, trna e RIBOSOMI mrna: porta l'informazione della sequenza degli aminoacidi di una determinata proteina. trna: ogni trna è specifico per il trasporto di un determinato aminoacido Ribosoma:
scaricato da I peptidi risultano dall unione di due o più aminoacidi mediante un legame COVALENTE
 Legame peptidico I peptidi risultano dall unione di due o più aminoacidi mediante un legame COVALENTE tra il gruppo amminico di un aminoacido ed il gruppo carbossilico di un altro. 1 Catene contenenti
Legame peptidico I peptidi risultano dall unione di due o più aminoacidi mediante un legame COVALENTE tra il gruppo amminico di un aminoacido ed il gruppo carbossilico di un altro. 1 Catene contenenti
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH
 Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( COO) nella stessa molecola C 3 N 2 C α * COO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-Chimica Organica
Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( COO) nella stessa molecola C 3 N 2 C α * COO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-Chimica Organica
Percorsi di chimica organica - Soluzioni degli esercizi del testo
 ercorsi di chimica organica - Soluzioni degli esercizi del testo AITL 14 1. Il prefisso α negli α-amminoacidi sta ad indicare che il gruppo amminico, - 2, si trova sul carbonio alfa (carbonio legato al
ercorsi di chimica organica - Soluzioni degli esercizi del testo AITL 14 1. Il prefisso α negli α-amminoacidi sta ad indicare che il gruppo amminico, - 2, si trova sul carbonio alfa (carbonio legato al
Allineamento dei 2 RNA
 La traduzione 2 codone Allineamento dei 2 RNA anticodone Studi Molecolari hanno dimostrato che: 3 residui nucleotidici del mrna sono necessari per codificare ciascun amminoacido Il linguaggio contenuto
La traduzione 2 codone Allineamento dei 2 RNA anticodone Studi Molecolari hanno dimostrato che: 3 residui nucleotidici del mrna sono necessari per codificare ciascun amminoacido Il linguaggio contenuto
Državni izpitni center BIOLOGIA. Prova d'esame 2. Giovedì, 28 agosto 2008 / 120 minuti
 Codice del candidato: Državni izpitni center *M08242112I* SESSIONE AUTUNNALE BIOLOGIA Prova d'esame 2 Giovedì, 28 agosto 2008 / 120 minuti Al candidato sono consentiti l'uso della penna stilografica o
Codice del candidato: Državni izpitni center *M08242112I* SESSIONE AUTUNNALE BIOLOGIA Prova d'esame 2 Giovedì, 28 agosto 2008 / 120 minuti Al candidato sono consentiti l'uso della penna stilografica o
Trascrizione e maturazione degli RNA
 Trascrizione e maturazione degli RNA L RNA è sisntetizzato a partire dal DNA nel processo della trascrizione L RNA veicola l informazione genica contenuta nel DNA (nucleo) in modo che possa esprimersi
Trascrizione e maturazione degli RNA L RNA è sisntetizzato a partire dal DNA nel processo della trascrizione L RNA veicola l informazione genica contenuta nel DNA (nucleo) in modo che possa esprimersi
PROTIDI: LE PROTEINE E GLI AMMINOACIDI
 PROTIDI: LE PROTEINE E GLI AMMINOACIDI GLI AMMINOACIDI Struttura generica di un amminoacido. R rappresenta un gruppo laterale specifico di ogni amminoacido. In chimica, gli amminoacidi (impropriamente
PROTIDI: LE PROTEINE E GLI AMMINOACIDI GLI AMMINOACIDI Struttura generica di un amminoacido. R rappresenta un gruppo laterale specifico di ogni amminoacido. In chimica, gli amminoacidi (impropriamente
Traduzione: dal RNA messaggero alle proteine Sintesi proteica
 Traduzione: dal RNA messaggero alle proteine Sintesi proteica D. L. Nelson, M. M. Cox, I PRINCIPI DI BIOCHIMICA DI LEHNINGER 4/E, Zanichelli Editore S.p.A. Copyright 2006 La traduzione Necessita di: (Codice)
Traduzione: dal RNA messaggero alle proteine Sintesi proteica D. L. Nelson, M. M. Cox, I PRINCIPI DI BIOCHIMICA DI LEHNINGER 4/E, Zanichelli Editore S.p.A. Copyright 2006 La traduzione Necessita di: (Codice)
Caratteristiche generali
 AMMINOACIDI Gli amminoacidi sono le unità costruttive (building blocks) delle proteine. Come dice il termine, gli amminoacidi naturali sono costituiti da un gruppo amminico (-NH 2 ) e da un gruppo carbossilico
AMMINOACIDI Gli amminoacidi sono le unità costruttive (building blocks) delle proteine. Come dice il termine, gli amminoacidi naturali sono costituiti da un gruppo amminico (-NH 2 ) e da un gruppo carbossilico
Vittoria Patti MACROMOLECOLE BIOLOGICHE. 4. proteine
 Vittoria Patti MACROMOLECOLE BIOLOGICHE 4. proteine 1 Funzioni principali delle proteine funzione cosa significa esempi ENZIMATICA STRUTTURALE TRASPORTO MOVIMENTO DIFESA IMMUNITARIA ORMONALE catalizzare
Vittoria Patti MACROMOLECOLE BIOLOGICHE 4. proteine 1 Funzioni principali delle proteine funzione cosa significa esempi ENZIMATICA STRUTTURALE TRASPORTO MOVIMENTO DIFESA IMMUNITARIA ORMONALE catalizzare
Definizione Composti quaternari: C H O N S P Fe Mg I
 PROTIDI Definizione Composti quaternari: C H O N S P Fe Mg I ORIGINE cellulare ogni cellula sintetizza le sue prote CARATTERISTICHE insolubili in acqua sensibili a variazioni di ph coagulano in presenza
PROTIDI Definizione Composti quaternari: C H O N S P Fe Mg I ORIGINE cellulare ogni cellula sintetizza le sue prote CARATTERISTICHE insolubili in acqua sensibili a variazioni di ph coagulano in presenza
SUBUNITA MAGGIORE = 60S (rrna 28S, 5.8S e 5S + 45 proteine) SUBUNITA MAGGIORE = 50S (rrna 23S e 5S + 34 proteine)
 TRADUZIONE I RIBOSOMI I Ribosomi hanno un diametro di circa 15-30 nm, sono costituiti da proteine ed rrna e sia nei Procarioti che negli Eucarioti, sono costituiti da una subunità maggiore e da una subunità
TRADUZIONE I RIBOSOMI I Ribosomi hanno un diametro di circa 15-30 nm, sono costituiti da proteine ed rrna e sia nei Procarioti che negli Eucarioti, sono costituiti da una subunità maggiore e da una subunità
AMMINOACIDI amminoacidi residuo amminoacidico Zwitterioni STEREOISOMERIA enantiomeri
 AMMINOACIDI Le proteine sono la macromolecola più abbondante nelle cellule e svolgono la maggior parte delle funzioni cellulari. Le proteine sono polimeri di amminoacidi (monomeri), in cui ogni residuo
AMMINOACIDI Le proteine sono la macromolecola più abbondante nelle cellule e svolgono la maggior parte delle funzioni cellulari. Le proteine sono polimeri di amminoacidi (monomeri), in cui ogni residuo
BIOMOLECOLE (PROTEINE)
 BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
Università Telematica Pegaso. Indice
 LE PROTEINE PROF.SSA AUSILIA ELCE Indice 1 INTRODUZIONE -------------------------------------------------------------------------------------------------------------- 3 2 TRASCRIZIONE--------------------------------------------------------------------------------------------------------------
LE PROTEINE PROF.SSA AUSILIA ELCE Indice 1 INTRODUZIONE -------------------------------------------------------------------------------------------------------------- 3 2 TRASCRIZIONE--------------------------------------------------------------------------------------------------------------
Lezione 1. Le molecole di base che costituiscono la vita
 Lezione 1 Le molecole di base che costituiscono la vita Le molecole dell ereditarietà 5 3 L informazione ereditaria di tutti gli organismi viventi, con l eccezione di alcuni virus, è a carico della molecola
Lezione 1 Le molecole di base che costituiscono la vita Le molecole dell ereditarietà 5 3 L informazione ereditaria di tutti gli organismi viventi, con l eccezione di alcuni virus, è a carico della molecola
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA. Angela Chambery Lezione 4
 Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 4 Scoperta degli amminoacidi: gli amminoacidi essenziali Gli amminoacidi essenziali sono quegli amminoacidi che un
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 4 Scoperta degli amminoacidi: gli amminoacidi essenziali Gli amminoacidi essenziali sono quegli amminoacidi che un
Le proteine. Polimeri composto da 20 diversi aminoacidi
 Le proteine Polimeri composto da 20 diversi aminoacidi (D. Voet, J.G. Voet, Biochemistry, 3 ed., John Wiley & Sons, 2004) PROTEINE come ATTUATORI nella cellula Trasporto elettronico Trasporto di ioni e
Le proteine Polimeri composto da 20 diversi aminoacidi (D. Voet, J.G. Voet, Biochemistry, 3 ed., John Wiley & Sons, 2004) PROTEINE come ATTUATORI nella cellula Trasporto elettronico Trasporto di ioni e
Biochimica. studio della vita a livello molecolare
 Biochimica studio della vita a livello molecolare studio della composizione molecolare dei sistemi viventi studio delle reazioni chimiche cui vanno incontro i sistemi viventi ALCUNI QUESITI DELLA BIOCHIMICA
Biochimica studio della vita a livello molecolare studio della composizione molecolare dei sistemi viventi studio delle reazioni chimiche cui vanno incontro i sistemi viventi ALCUNI QUESITI DELLA BIOCHIMICA
moli OH - /mole amminoacido
 ) ) Di seguito è riportata la curva di titolazione di un amminoacido. Osservando il grafico: a) stabilire il valore dei pka dell aminoacido b) calcolare il valore del pi e individuarlo sul grafico. c)
) ) Di seguito è riportata la curva di titolazione di un amminoacido. Osservando il grafico: a) stabilire il valore dei pka dell aminoacido b) calcolare il valore del pi e individuarlo sul grafico. c)
DNA E PROTEINE IL DNA E RACCHIUSO NEL NUCLEO, MENTRE LA SINTESI PROTEICA SI SVOLGE NEL CITOPLASMA: COME VIENE TRASPORTATA L INFORMAZIONE?
 DNA E PROTEINE NUMEROSI DATI SUGGERISCONO CHE IL DNA SVOLGA IL SUO RUOLO GENETICO CONTROLLANDO LA SINTESI DELLE PROTEINE, IN PARTICOLARE DETERMINANDONE LA SEQUENZA IN AMINOACIDI E NECESSARIO RISPONDERE
DNA E PROTEINE NUMEROSI DATI SUGGERISCONO CHE IL DNA SVOLGA IL SUO RUOLO GENETICO CONTROLLANDO LA SINTESI DELLE PROTEINE, IN PARTICOLARE DETERMINANDONE LA SEQUENZA IN AMINOACIDI E NECESSARIO RISPONDERE
LE PROTEINE. SONO Polimeri formati dall unione di AMMINOACIDI (AA) Rende diversi i 20 AA l uno dall altro UN ATOMO DI C AL CENTRO
 LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
Codice Genetico (segue) 04/11/2015. «Wobble base pairs» (appaiamento tentennante di basi) CODICE GENETICO
 «Wobble base pairs» (appaiamento tentennante di basi) CODICE GENETICO http://www.atdbio.com/img/articles/rna wobble base pairs large.png CODICE GENETICO Codice mediante il quale la sequenza nucleotidica
«Wobble base pairs» (appaiamento tentennante di basi) CODICE GENETICO http://www.atdbio.com/img/articles/rna wobble base pairs large.png CODICE GENETICO Codice mediante il quale la sequenza nucleotidica
INTRODUZIONE ALLA PROTEINE BCP 1-2
 INTRODUZIONE ALLA BIOCHIMICA DELLE PROTEINE BCP 1-2 Pietre miliari Lehninger 1973 Biochemistry Proteine ricombinanti Protein engineering Cristallografia, NMR, EM, MS, spettroscopie... Computing Bioinformaticai
INTRODUZIONE ALLA BIOCHIMICA DELLE PROTEINE BCP 1-2 Pietre miliari Lehninger 1973 Biochemistry Proteine ricombinanti Protein engineering Cristallografia, NMR, EM, MS, spettroscopie... Computing Bioinformaticai
Proprietà comuni. Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici
 Gli aminoacidi Proprietà comuni Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici paragonabili Il gruppo α-aminico è un acido più forte (o una base più debole
Gli aminoacidi Proprietà comuni Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici paragonabili Il gruppo α-aminico è un acido più forte (o una base più debole
Lezione 6. Lo string matching
 Lezione 6 Lo string matching String matching Date due stringhe (sequenze di caratteri) vogliamo stabilire se sono uguali Nel caso dello string matching, due stringhe sono uguali se... sono uguali ( DNA
Lezione 6 Lo string matching String matching Date due stringhe (sequenze di caratteri) vogliamo stabilire se sono uguali Nel caso dello string matching, due stringhe sono uguali se... sono uguali ( DNA
Codice Genetico (segue)
 CODICE GENETICO Nucleotidi, acidi nucleici CODICE GENETICO Codice mediante il quale la sequenza nucleotidica di una molecola di DNA o di RNA specifica la sequenza amminoacidica di un polipeptide. Consiste
CODICE GENETICO Nucleotidi, acidi nucleici CODICE GENETICO Codice mediante il quale la sequenza nucleotidica di una molecola di DNA o di RNA specifica la sequenza amminoacidica di un polipeptide. Consiste
Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi. Possono assumere forme diverse a seconda della funzione
 Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi Hanno elevato PM Possono assumere forme diverse a seconda della funzione svolgono molteplici funzioni Tra le proteine
Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi Hanno elevato PM Possono assumere forme diverse a seconda della funzione svolgono molteplici funzioni Tra le proteine
Lezione 2. costituiscono la vita
 Lezione 2 Le molecole di base che costituiscono la vita Graur Gau and Li: Capitolo o 1 Graur lectures 5 6 7 5 3 Le molecole dell ereditarietà L informazione i ereditaria i di tutti ttigli organismi iviventi,
Lezione 2 Le molecole di base che costituiscono la vita Graur Gau and Li: Capitolo o 1 Graur lectures 5 6 7 5 3 Le molecole dell ereditarietà L informazione i ereditaria i di tutti ttigli organismi iviventi,
Lezione 2. Le molecole di base che costituiscono la vita
 Lezione 2 Le molecole di base che costituiscono la vita Graur and Li: Capitolo 1 5 3 Le molecole dell ereditarietà L informazione ereditaria di tutti gli organismi viventi, con l eccezione di alcuni virus,
Lezione 2 Le molecole di base che costituiscono la vita Graur and Li: Capitolo 1 5 3 Le molecole dell ereditarietà L informazione ereditaria di tutti gli organismi viventi, con l eccezione di alcuni virus,
COMPOSTI AZOTATI. derivanti dall ammoniaca AMMINE. desinenza -INA AMMIDE
 COMPOSTI AZOTATI derivanti dall ammoniaca AMMINE desinenza -INA AMMIDE ANCORA AMMIDI RISONANZA A M M I D I Il legame ammidico ha parziale carattere di doppio legame per la seguente risonanza: Ammidi H
COMPOSTI AZOTATI derivanti dall ammoniaca AMMINE desinenza -INA AMMIDE ANCORA AMMIDI RISONANZA A M M I D I Il legame ammidico ha parziale carattere di doppio legame per la seguente risonanza: Ammidi H
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE Vengono chiamate amminoacidi quelle molecole organiche in cui sono contemporaneamente presenti sia un gruppo acido carbossilico -COOH che un gruppo amminico -NH2. Le proteine, a
AMMINOACIDI E PROTEINE Vengono chiamate amminoacidi quelle molecole organiche in cui sono contemporaneamente presenti sia un gruppo acido carbossilico -COOH che un gruppo amminico -NH2. Le proteine, a
20/12/ tipi di amino acidi: parecchie combinazioni
 20 tipi di amino acidi: parecchie combinazioni Le proteine sono polimeri di amino acidi 1 SEMPLICI : costituite solo da amino acidi PROTEINE CONIUGATE Apoproteina = parte proteica Gruppo prostetico = parte
20 tipi di amino acidi: parecchie combinazioni Le proteine sono polimeri di amino acidi 1 SEMPLICI : costituite solo da amino acidi PROTEINE CONIUGATE Apoproteina = parte proteica Gruppo prostetico = parte
I gruppi R differenziano i 20 amminoacidi standard. Tratto da D. Voet, G. Voet e C.W. Pratt Fondamenti di biochimica
 Gli aminoacidi NOMENCLATURA Aminoacido Abbr. tre lettere Abbr. una lettera Aminoacido Abbr. tre lettere Abbr. una lettera Alanina ALA A Lisina LYS K Arginina ARG R Metionina MET M Asparagina ASN N Fenilalanina
Gli aminoacidi NOMENCLATURA Aminoacido Abbr. tre lettere Abbr. una lettera Aminoacido Abbr. tre lettere Abbr. una lettera Alanina ALA A Lisina LYS K Arginina ARG R Metionina MET M Asparagina ASN N Fenilalanina
La spettroscopia infrarossa
 La spettroscopia infrarossa I legami covalenti delle molecole vibrano continuamente Spettrometria di massa e spettroscopia infrarossa Uno spettro infrarosso si ottiene investendo e facendo attraversare
La spettroscopia infrarossa I legami covalenti delle molecole vibrano continuamente Spettrometria di massa e spettroscopia infrarossa Uno spettro infrarosso si ottiene investendo e facendo attraversare
Trascrizione e maturazione degli RNA
 Trascrizione e maturazione degli RNA Trascrizione e traduzione: espressione dell informazione genica L RNA veicola l informazione genica contenuta nel DNA (nucleo) in modo che possa esprimersi per dare
Trascrizione e maturazione degli RNA Trascrizione e traduzione: espressione dell informazione genica L RNA veicola l informazione genica contenuta nel DNA (nucleo) in modo che possa esprimersi per dare
E. Giordano 16/09/2010
 GRUPPO NAZIONALE DI BIOINGEGNERIA XXIX Scuola Annuale BIOLOGIA SINTETICA Bressanone 13-17 settembre 2010 1/41 COSTITUENTI MOLECOLARI DELLO CHASSIS CELLULARE Emanuele GIORDANO II Facoltà di Ingegneria Dipartimento
GRUPPO NAZIONALE DI BIOINGEGNERIA XXIX Scuola Annuale BIOLOGIA SINTETICA Bressanone 13-17 settembre 2010 1/41 COSTITUENTI MOLECOLARI DELLO CHASSIS CELLULARE Emanuele GIORDANO II Facoltà di Ingegneria Dipartimento
lezione Prof. Spina miliardi di anni fa l universo comparve sotto forma di eruzioni
 Biochimica Matricole dispari 1 1^ lezione Prof. Spina LA BIOCHIMICA 15 20 miliardi di anni fa l universo comparve sotto forma di eruzioni d l f d inimmaginabili di particele subatomiche ricche di energia
Biochimica Matricole dispari 1 1^ lezione Prof. Spina LA BIOCHIMICA 15 20 miliardi di anni fa l universo comparve sotto forma di eruzioni d l f d inimmaginabili di particele subatomiche ricche di energia
Struttura degli Amminoacidi
 Amminoacidi Struttura degli Amminoacidi Amminoacido (o α-amminoacido): molecola che possiede un gruppo amminico primario (-NH 2 ) come sostituente dell atomo di carbonio α, e un gruppo carbossilico acido
Amminoacidi Struttura degli Amminoacidi Amminoacido (o α-amminoacido): molecola che possiede un gruppo amminico primario (-NH 2 ) come sostituente dell atomo di carbonio α, e un gruppo carbossilico acido
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE Vengono chiamate amminoacidi quelle molecole organiche in cui sono contemporaneamente presenti sia un gruppo acido carbossilico -COO che un gruppo amminico -N2. Una molecola appartenente
AMMINOACIDI E PROTEINE Vengono chiamate amminoacidi quelle molecole organiche in cui sono contemporaneamente presenti sia un gruppo acido carbossilico -COO che un gruppo amminico -N2. Una molecola appartenente
Composti organici. I composti organici. Atomi e molecole di carbonio. Atomi e molecole di carbonio. Gruppi funzionali. Isomeri
 I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
Codice Genetico (segue) 29/10/2014 CODICE GENETICO
 CODICE GENETICO Codice mediante il quale la sequenza nucleotidica di una molecola di DNA o di RNA specifica la sequenza amminoacidica di un polipeptide. CODICE GENETICO Consiste di codoni a tre nucleotidi
CODICE GENETICO Codice mediante il quale la sequenza nucleotidica di una molecola di DNA o di RNA specifica la sequenza amminoacidica di un polipeptide. CODICE GENETICO Consiste di codoni a tre nucleotidi
Sequenze nucleotidiche del DNA definite loci costituiscono i geni. Ogni gene codifica per una specifica proteina
 sintesi proteica La sintesi proteica è il processo che porta alla formazione delle proteine da sequenze del DN definite geni. Si tratta di un processo a più fasi Nelle sue linee fondamentali questo processo
sintesi proteica La sintesi proteica è il processo che porta alla formazione delle proteine da sequenze del DN definite geni. Si tratta di un processo a più fasi Nelle sue linee fondamentali questo processo
scaricato da www.sunhope.it Proteine semplici costituite dai soli amminoacidi
 Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
LE MACROMOLECOLE BIOLOGICHE Le cellule contengono 4 famiglie principali di molecole organiche:
 LEZIONE n 1 LE MACROMOLECOLE BIOLOGICHE Le cellule contengono 4 famiglie principali di molecole organiche: macromolecole Macromolecole macromolecole I componenti chimici di una cellula -Le macromolecole
LEZIONE n 1 LE MACROMOLECOLE BIOLOGICHE Le cellule contengono 4 famiglie principali di molecole organiche: macromolecole Macromolecole macromolecole I componenti chimici di una cellula -Le macromolecole
Gli amminoacidi ( 20) hanno proprietà strutturali comuni
 Quando nel XIX secolo gli scienziati rivolsero per la prima volta la loro attenzione alla nutrizione, in breve tempo scoprirono che i prodotti naturali contenenti azoto erano essenziali per la nutrizione
Quando nel XIX secolo gli scienziati rivolsero per la prima volta la loro attenzione alla nutrizione, in breve tempo scoprirono che i prodotti naturali contenenti azoto erano essenziali per la nutrizione
a) un movimento contro gradiente di concentrazione che utilizza fonti primarie di energia
 1. Quale considerazione sulla struttura primaria di una proteina è vera? a) è caratteristica delle proteine insolubili b) i ponti S-S la stabilizzano c) i ponti H la stabilizzano d) la proteina assume
1. Quale considerazione sulla struttura primaria di una proteina è vera? a) è caratteristica delle proteine insolubili b) i ponti S-S la stabilizzano c) i ponti H la stabilizzano d) la proteina assume
Alcol + alcol etere R-OH + R -OH R-O-R + H 2 O Aldeide + alcol emiacetale R-CHO + R -OH R-CHOH-O-R Acido + Acido anidride R-COOH + R -COOH
 Nomenclatura AMIDI Alcol + alcol etere R-OH + R -OH R-O-R + H 2 O Aldeide + alcol emiacetale R-CHO + R -OH R-CHOH-O-R Acido + Acido anidride R-COOH + R -COOH R-CO-O-CO-R + H 2 O Alcol + Acido estere R-COOH
Nomenclatura AMIDI Alcol + alcol etere R-OH + R -OH R-O-R + H 2 O Aldeide + alcol emiacetale R-CHO + R -OH R-CHOH-O-R Acido + Acido anidride R-COOH + R -COOH R-CO-O-CO-R + H 2 O Alcol + Acido estere R-COOH
CONTENUTI DELLA LEZIONE:
 Stereochimica CONTENUTI DELLA LEZIONE: 1. La Chiralità: Molecole chirali e achirali 2. Identificare uno stereocentro 3. Enantiomeri 4. Regole per assegnare la configurazione R,S 5. Diastereoisomeri 6.
Stereochimica CONTENUTI DELLA LEZIONE: 1. La Chiralità: Molecole chirali e achirali 2. Identificare uno stereocentro 3. Enantiomeri 4. Regole per assegnare la configurazione R,S 5. Diastereoisomeri 6.
STRUTTURA E FUNZIONE DELLE PROTEINE
 STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
Formula generale di un amminoacido
 Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
Biochimica. studio della vita a livello molecolare
 Biochimica studio della vita a livello molecolare studio della composizione molecolare dei sistemi viventi studio delle reazioni chimiche cui vanno incontro i sistemi viventi ALCUNI QUESITI DELLA BIOCHIMICA
Biochimica studio della vita a livello molecolare studio della composizione molecolare dei sistemi viventi studio delle reazioni chimiche cui vanno incontro i sistemi viventi ALCUNI QUESITI DELLA BIOCHIMICA
Struttura secondaria
 Struttura secondaria Struttura localmente ordinata Polimeri lineari ad unità monomeriche asimmetriche elica j = 0,1,2,..., N N = numero di residui z j = h z j + z 0 x j = r cos (j2p h z /P + d 0 ) y j
Struttura secondaria Struttura localmente ordinata Polimeri lineari ad unità monomeriche asimmetriche elica j = 0,1,2,..., N N = numero di residui z j = h z j + z 0 x j = r cos (j2p h z /P + d 0 ) y j
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA. Angela Chambery Lezione 5
 Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 5 Il legame peptidico Concetti chiave: In un polipeptide gli amminoacidi sono uniti dai legami peptidici. Il legame
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 5 Il legame peptidico Concetti chiave: In un polipeptide gli amminoacidi sono uniti dai legami peptidici. Il legame
9) Scrivere un disaccaride formato dal β-d-galattosio e dall α-d-n-acetil-glucosammina legati da un legame glicosidico β(1-4).
 CARBOIDRATI - AMMINOACIDI - PROTEINE 1) Scrivere la proiezione di Fisher del D-ribosio e del D-glucosio. La lettera D a cosa si riferisce? Disegnare inoltre il disaccaride ottenuto dalla condensazione
CARBOIDRATI - AMMINOACIDI - PROTEINE 1) Scrivere la proiezione di Fisher del D-ribosio e del D-glucosio. La lettera D a cosa si riferisce? Disegnare inoltre il disaccaride ottenuto dalla condensazione
Le macromolecole dei tessuti - 1
 Le macromolecole dei tessuti - 1 Che cosa sono le proteine? Sono macromolecole complesse ad alta informazione Sono costituite da una o più catene polipeptidiche Ogni catena peptidica è composta da centinaia
Le macromolecole dei tessuti - 1 Che cosa sono le proteine? Sono macromolecole complesse ad alta informazione Sono costituite da una o più catene polipeptidiche Ogni catena peptidica è composta da centinaia
